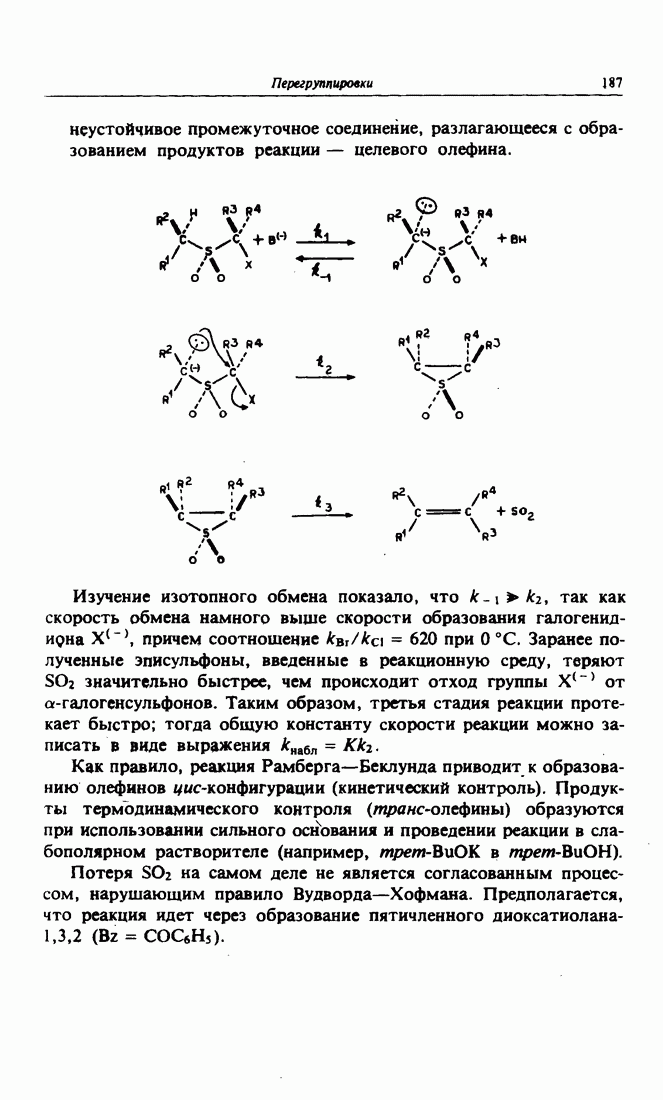
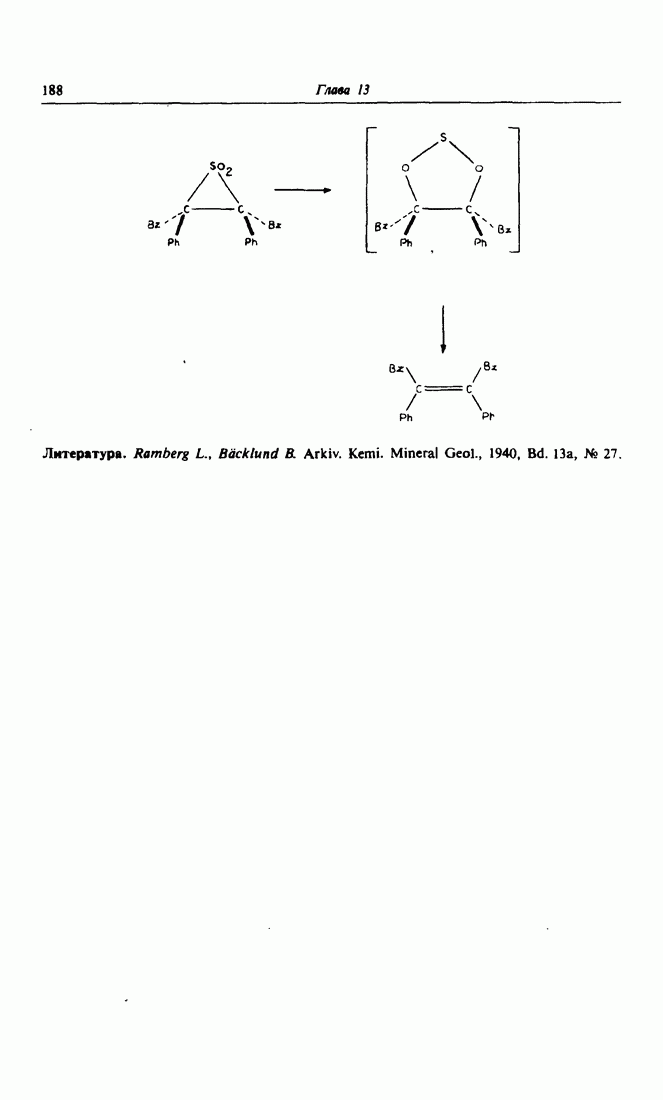
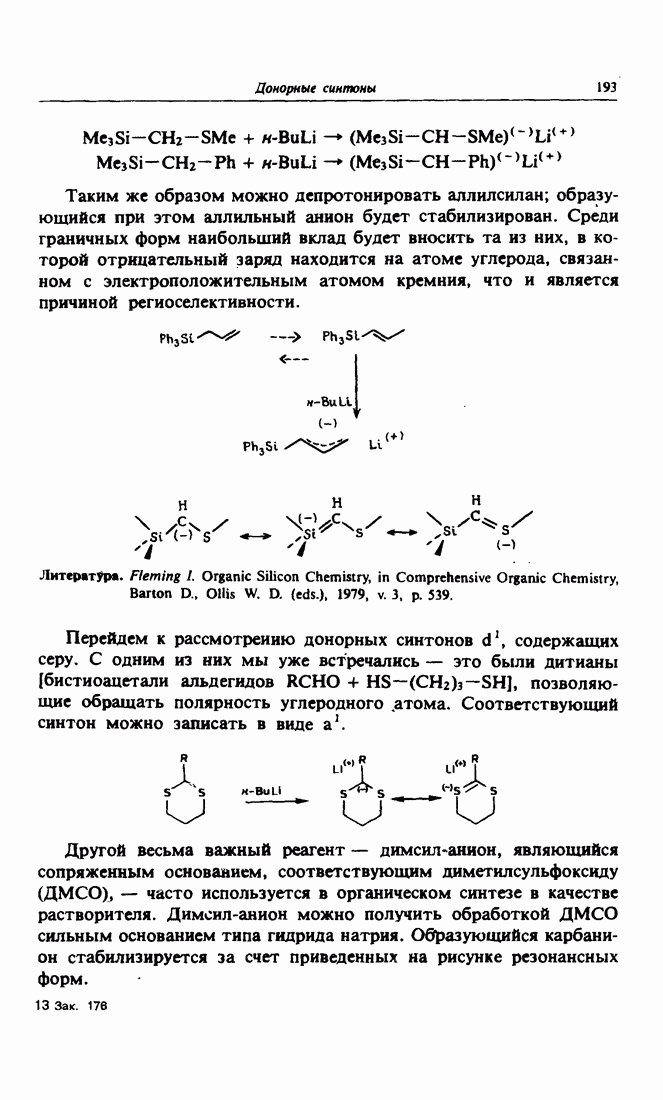
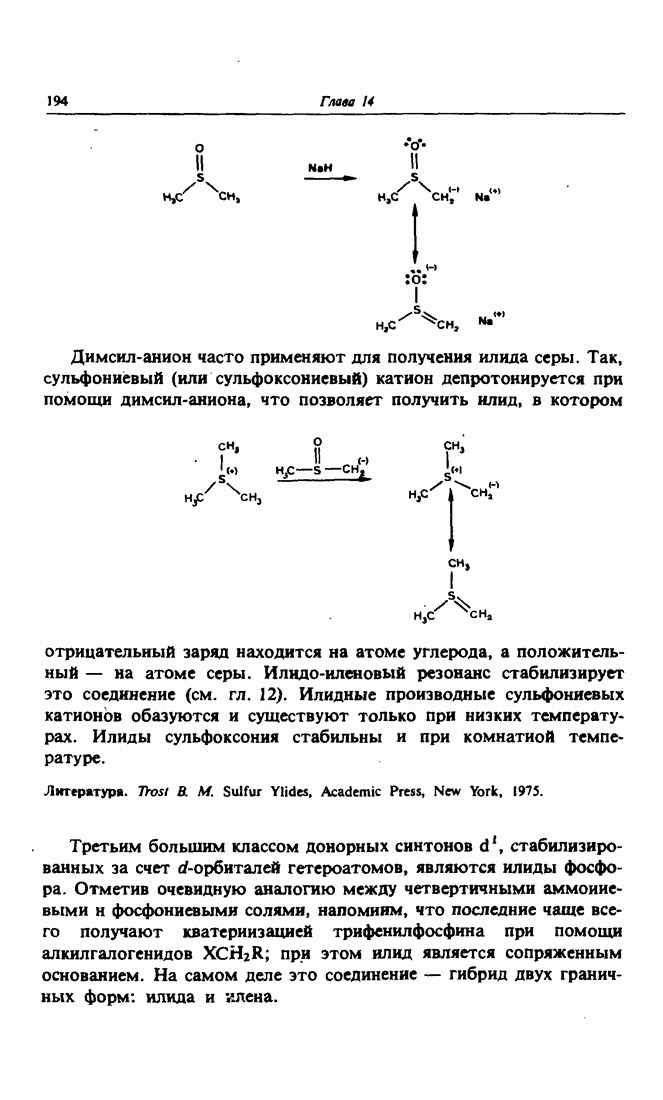
| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
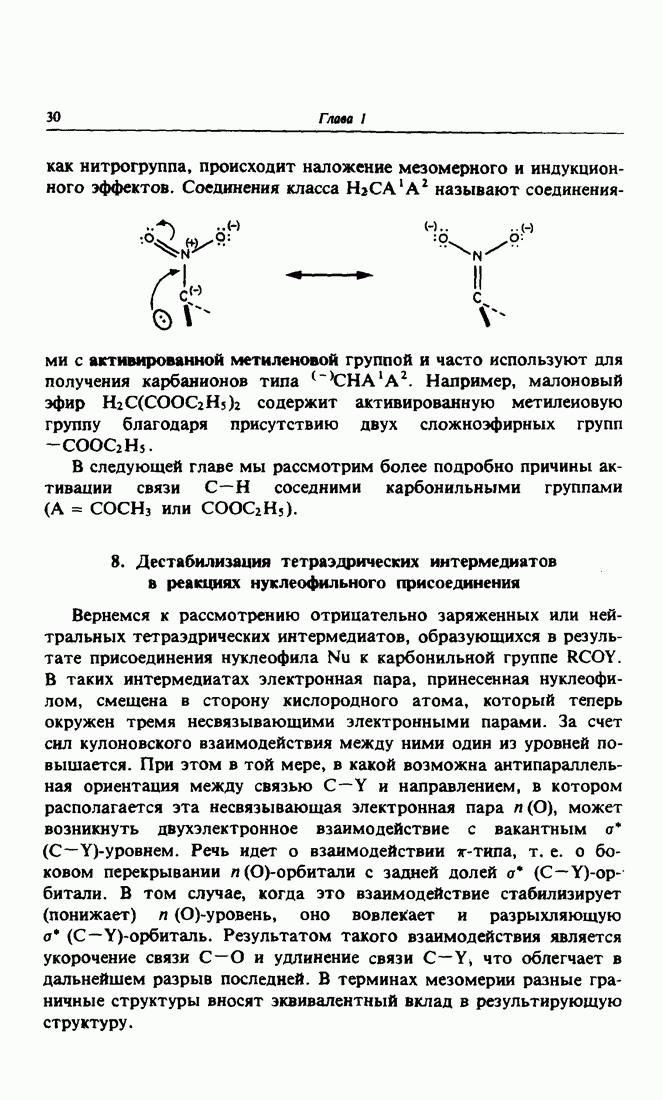
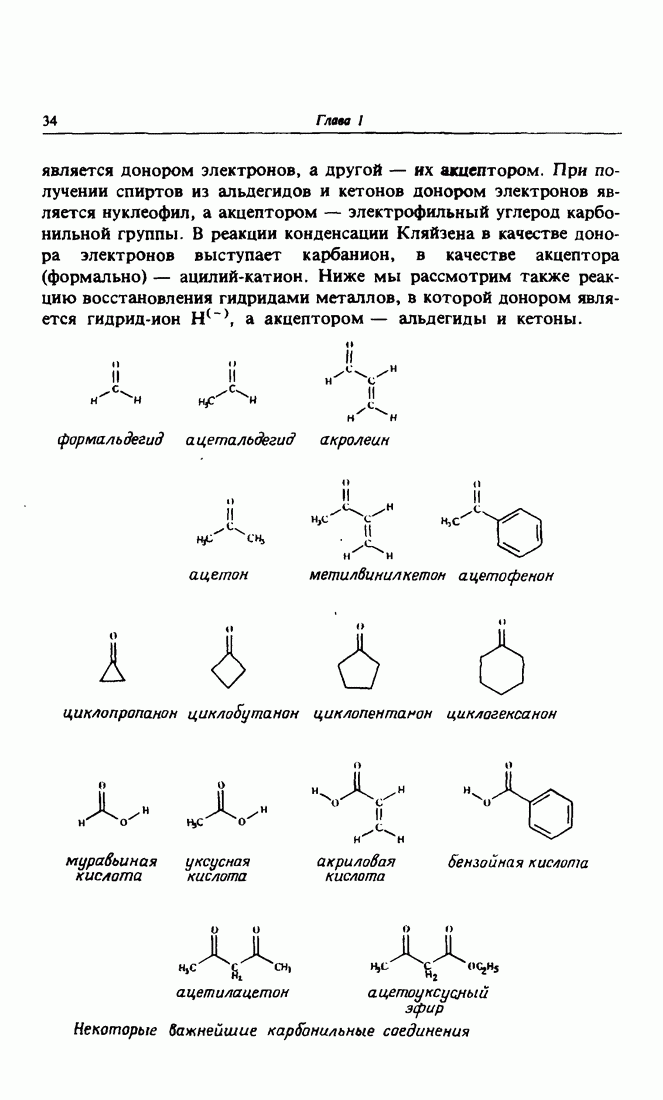
10. Восстановление гидридами металлов
Как уже отмечалось выше, для получения самого простого нуклеофила — гидрид-иона  исходными соединениями служат гидриды металлов, например
исходными соединениями служат гидриды металлов, например  или
или  При взаимодействии гидрид-иона с карбонильной группой происходит обмен катиона металла на протон с образованием спирта — первичного, если в качестве субстрата использовали альдегид, и вторичного, если был взят кетон.
При взаимодействии гидрид-иона с карбонильной группой происходит обмен катиона металла на протон с образованием спирта — первичного, если в качестве субстрата использовали альдегид, и вторичного, если был взят кетон.

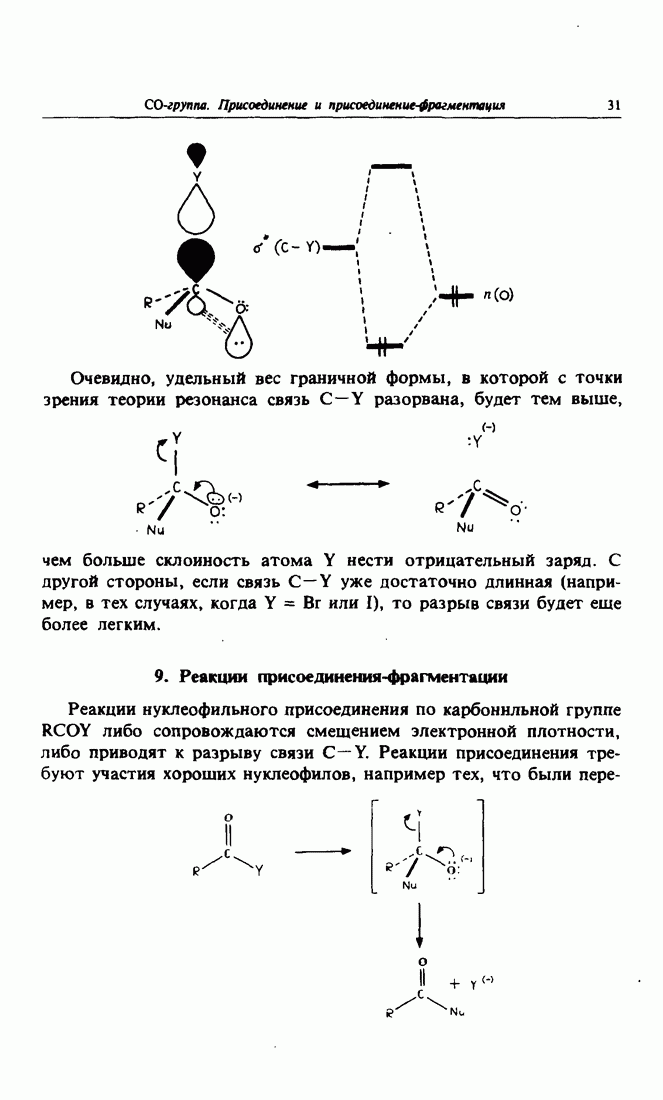
Анализ приведенных выше кинетических данных показывает,  существует вполне определенная зависимость между активностью соединения и его структурой. Так, например, альдегиды гораздо более реакционноспособны, чем кетоны, что является достаточно
существует вполне определенная зависимость между активностью соединения и его структурой. Так, например, альдегиды гораздо более реакционноспособны, чем кетоны, что является достаточно

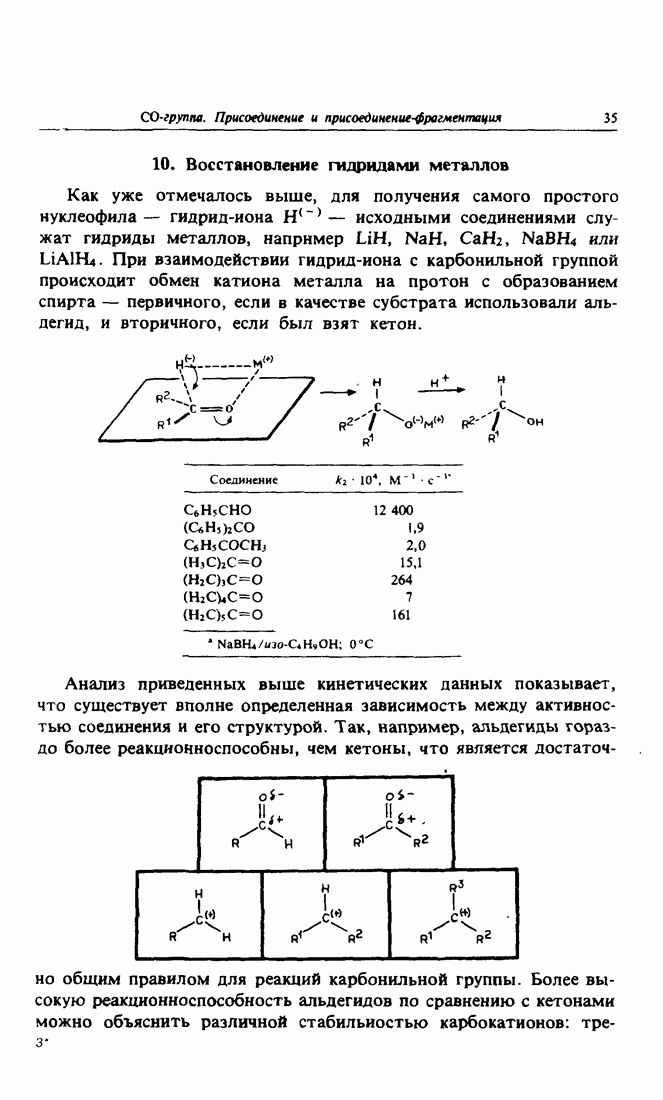
общим правилом для реакций карбонильной группы. Более высокую реакционноспособность альдегидов по сравнению с кетонами можно объяснить различной стабильностью карбокатионов:
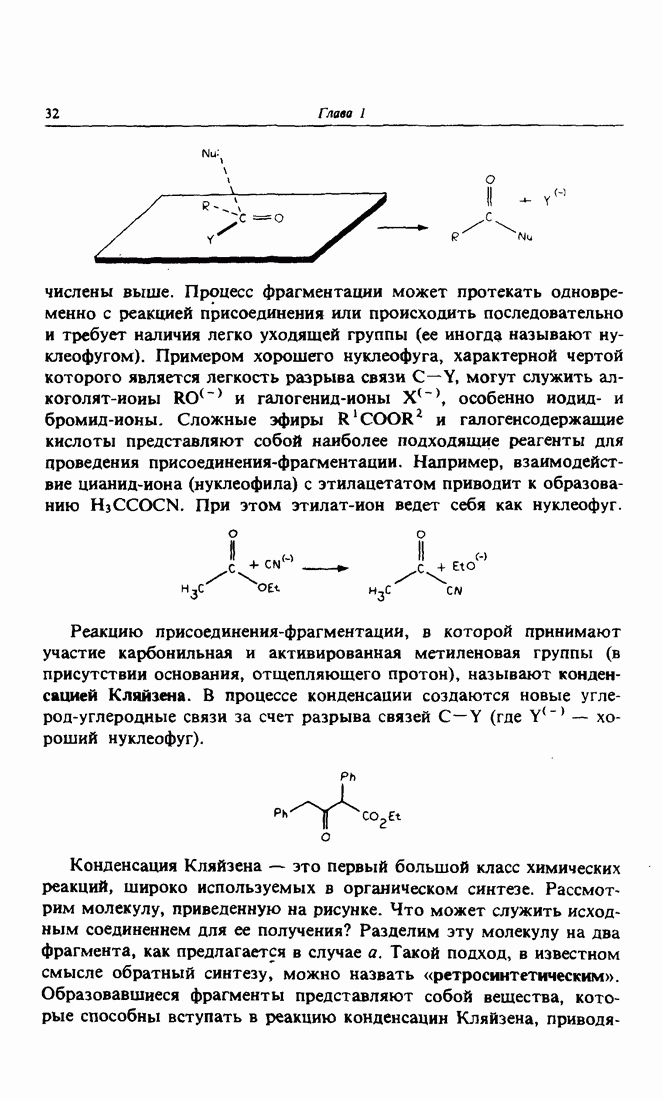
третичные карбокатионы более устойчивы, чем вторичные, которые в свою очередь устойчивее первичных. Известно, что реакционно-способность обратно пропорциональна стабильности, следовательно (в той мере, в которой правомерно проводить аналогию между карбокатионом и углеродом карбонильной группы, несущим частичный положительный заряд), логично было бы ожидать, что альдегиды будут вести себя как более сильные электрофилы по сравнению с кетонамн (образующиеся в этом случае карбокатионы более стабильны благодаря наличию сверхсопряжения связей  групп
групп  с вакантной
с вакантной  -орбиталью атома углерода, несущего
-орбиталью атома углерода, несущего

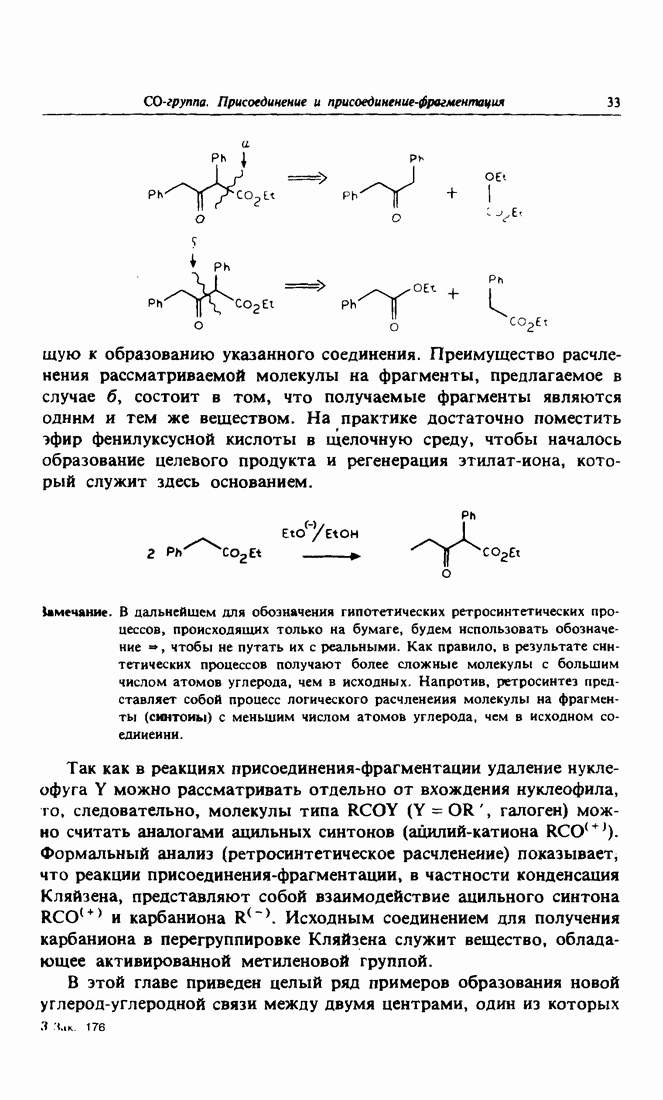
частичный положительный заряд). Бензофенон  и ацетофенон
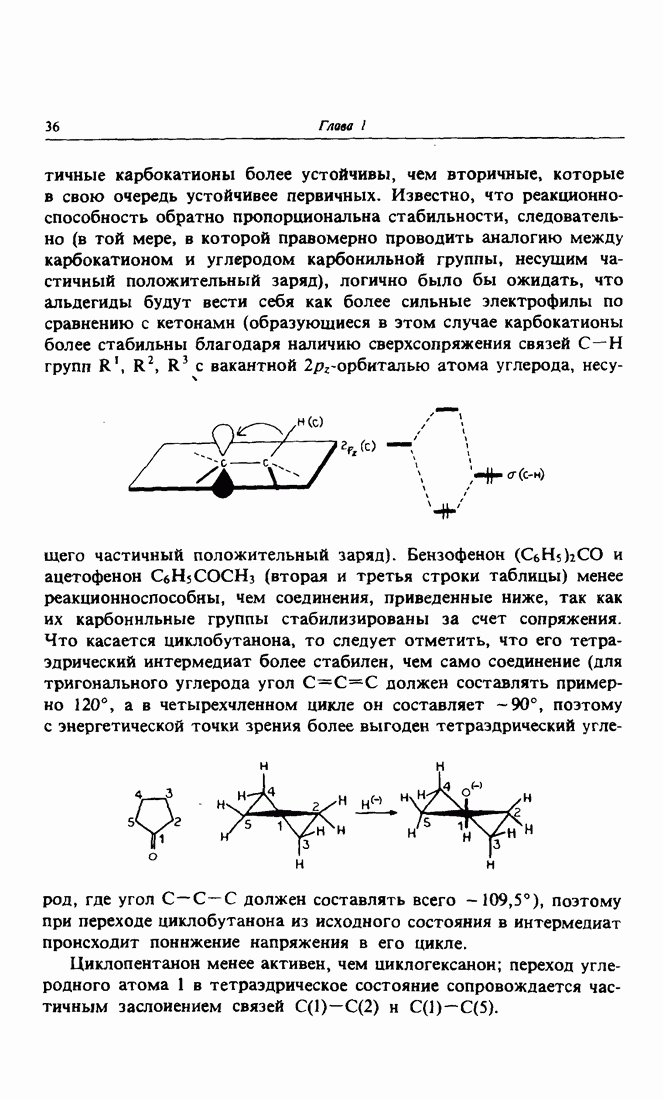
и ацетофенон  (вторая и третья строки таблицы) менее реакционноспособны, чем соединения, приведенные ниже, так как их карбонильные группы стабилизированы за счет сопряжения. Что касается циклобутанона, то следует отметить, что его тетраэдрический интермедиат более стабилен, чем само соединение (для тригонального углерода угол
(вторая и третья строки таблицы) менее реакционноспособны, чем соединения, приведенные ниже, так как их карбонильные группы стабилизированы за счет сопряжения. Что касается циклобутанона, то следует отметить, что его тетраэдрический интермедиат более стабилен, чем само соединение (для тригонального углерода угол  должен составлять примерно 120°, а в четырехчленном цикле он составляет -90°, поэтому с энергетической точки зрения более выгоден тетраэдрический углерод,
должен составлять примерно 120°, а в четырехчленном цикле он составляет -90°, поэтому с энергетической точки зрения более выгоден тетраэдрический углерод,

где угол  должен составлять всего -109,5°), поэтому при переходе циклобутанона из исходного состояния в интермедиат происходит понижение напряжения в его цикле.
должен составлять всего -109,5°), поэтому при переходе циклобутанона из исходного состояния в интермедиат происходит понижение напряжения в его цикле.
Циклопентанон менее активен, чем циклогексанон; переход углеродного атома 1 в тетраэдрическое состояние сопровождается частичным заслонением связей 
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ РЕДАКТОРА
- ВВЕДЕНИЕ
- 1. Орбитальный и зарядовый контроль
- 2. Жесткие и мягкие кислоты и основания
- 3. Термохимические данные и их применение
- Глава 1. КАРБОНИЛЬНАЯ ГРУППА. РЕАКЦИИ ПРИСОЕДИНЕНИЯ И ПРИСОЕДИНЕНИЯ-ФРАГМЕНТАЦИИ
- 1. Карбонильная группа. Простое орбитальное описание
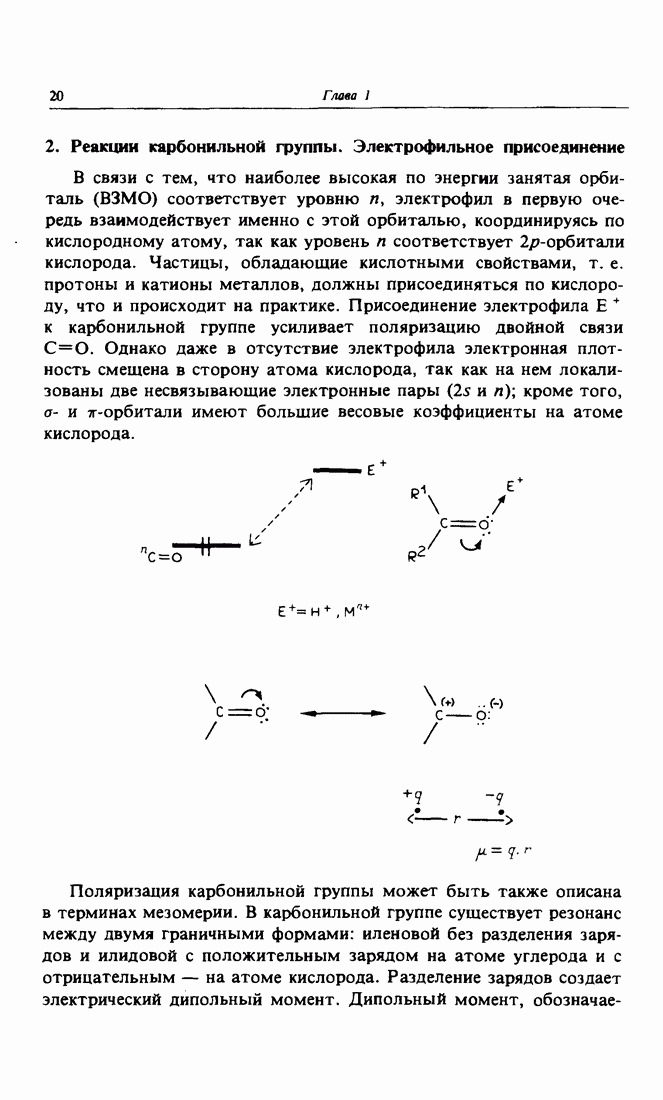
- 2. Реакции карбонильной группы. Электрофильное присоединение
- 3. Основность и нуклеофильность
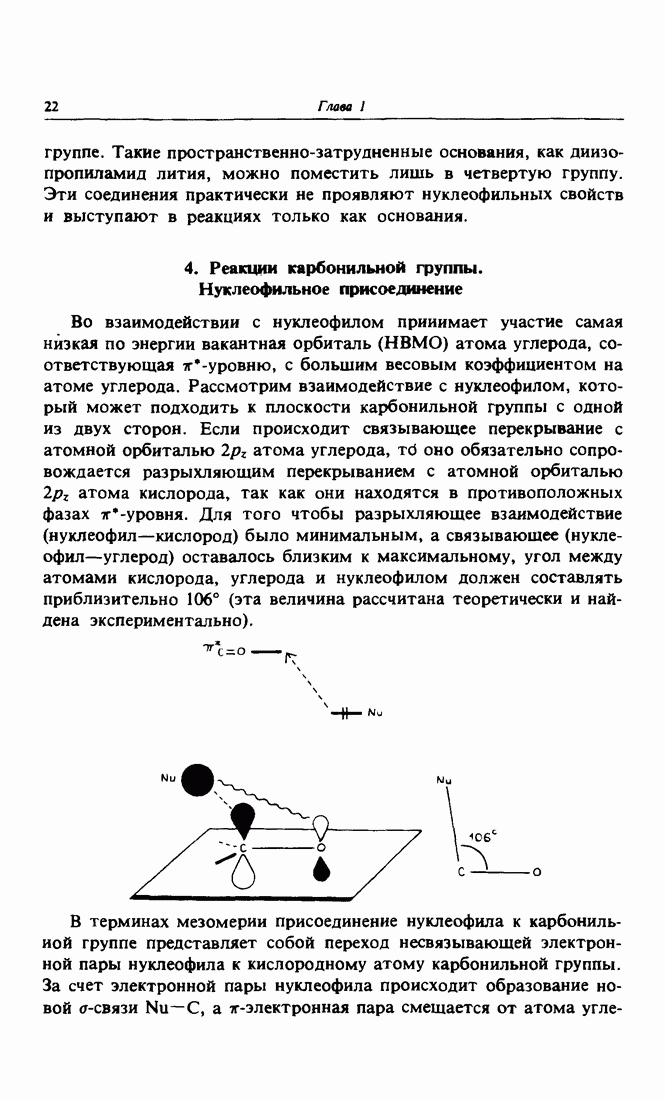
- 4 Реакции карбонильной группы. Нуклеофильное присоединение
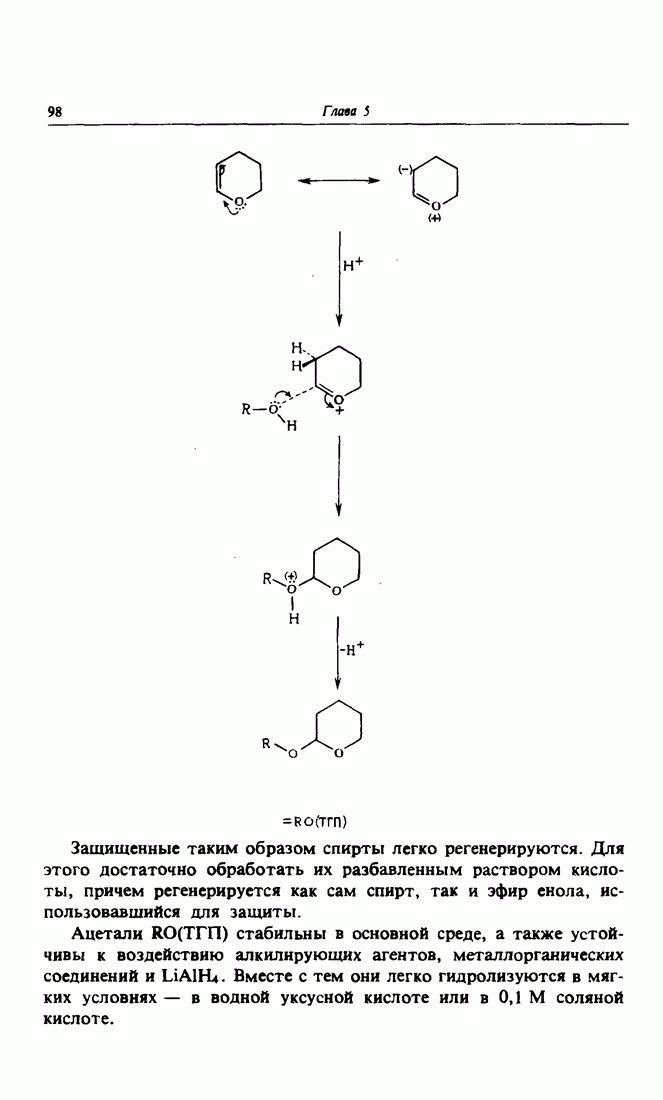
- 5. Защита и регенерация
- 6. Получение различных металлоорганических производных
- 7. Активированная метиленовая группа
- 8. Дестабилизация тетраэдрических интермедиатов в реакциях нуклеофильного присоединения
- 9. Реакции присоединения-фрагментации
- 10. Восстановление гидридами металлов
- 11. Описание конфигурации асимметрического атома углерода
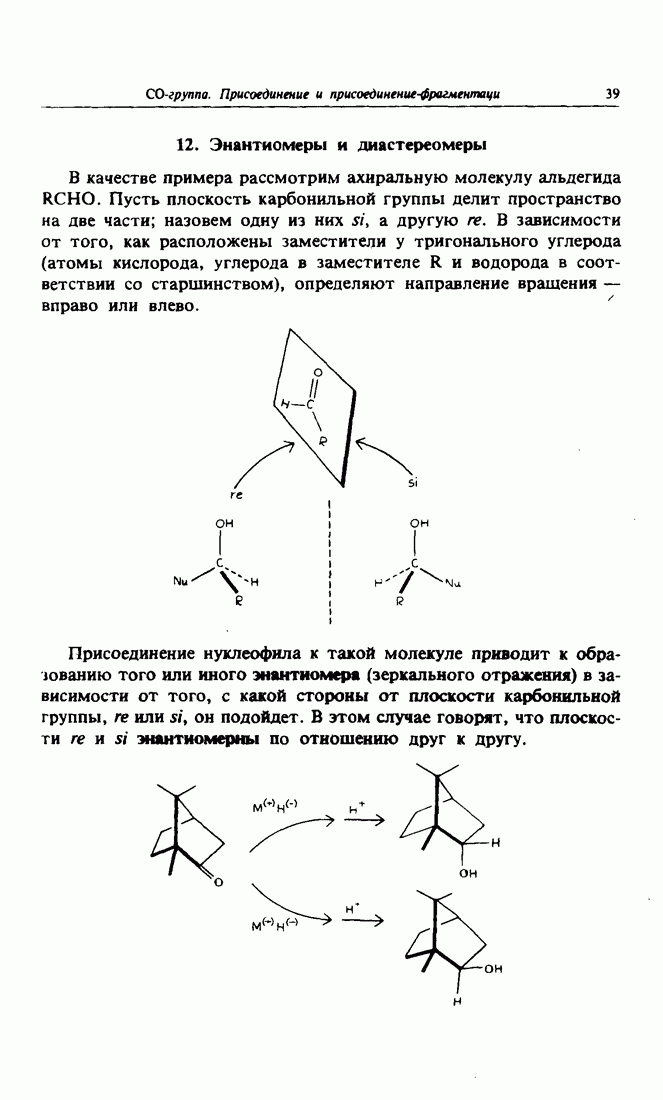
- 12. Энантиомеры и диастереомеры
- 13. Асимметрическая 1,2-индукция
- Глава 2. КАРБОНИЛЬНАЯ ГРУППА. ЕНОЛИЗАЦИЯ. КОНДЕНСАЦИЯ ПО МИХАЭЛЮ
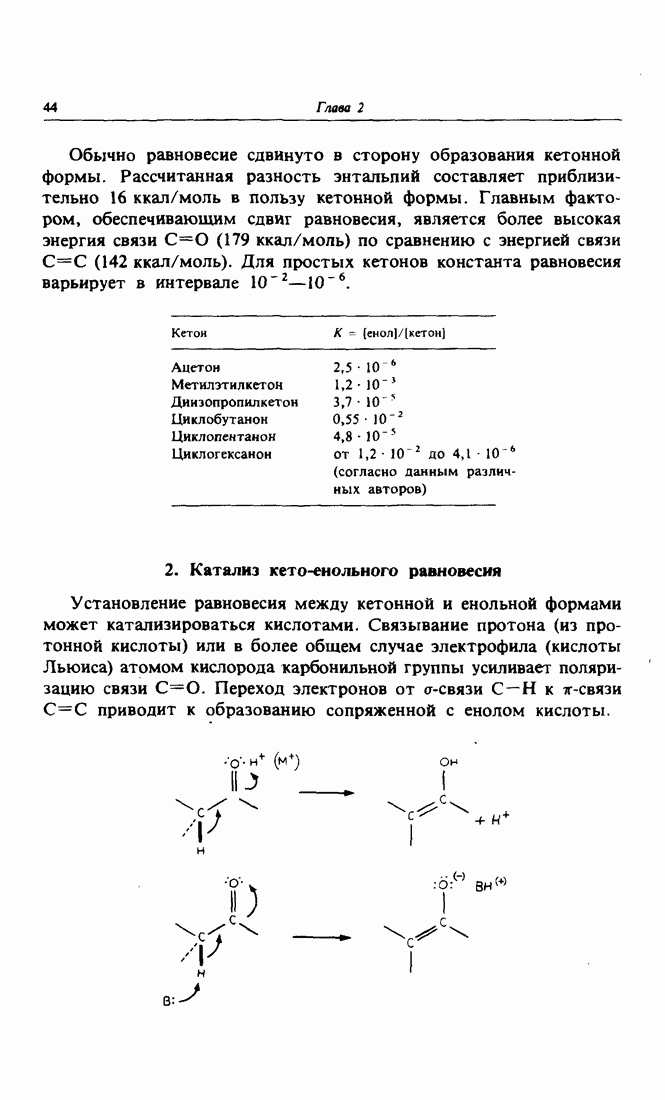
- 1. Кето-енольное равновесие
- 2. Катализ кето-енольного равновесия
- 3. Стереохимия и реакция енолнэации
- 4. Причины ослабления связи Ca-H в кетонах
- 5. Еноляты и их получение
- 6. Эфиры енолов
- 7. Конфигурация енолов и эфиров енолов
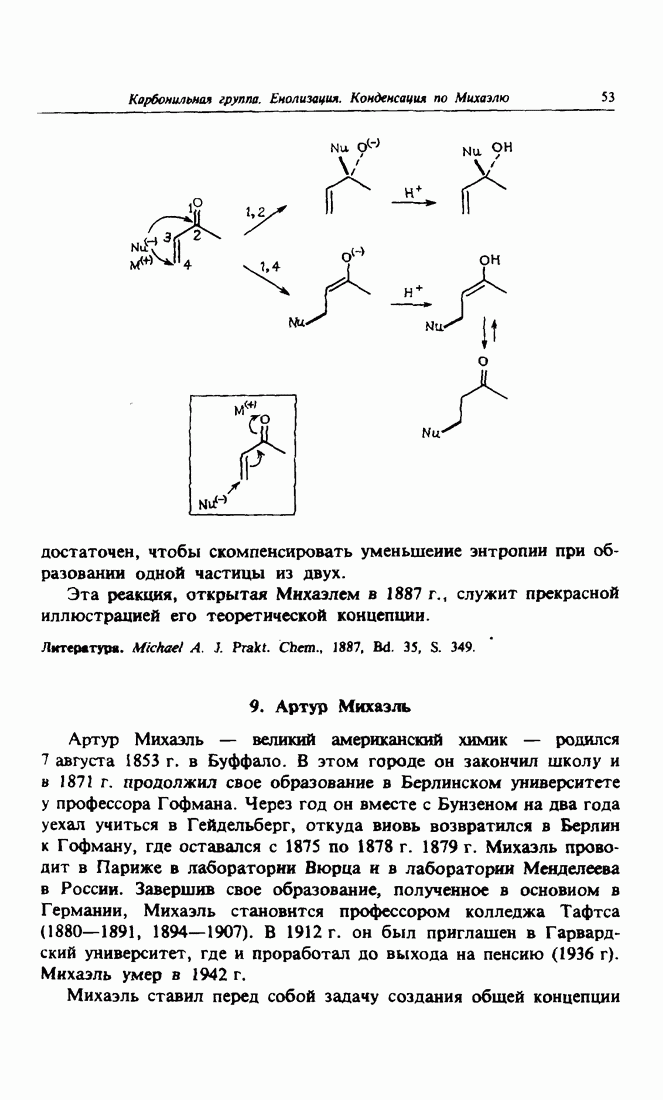
- 8. Реакция Михаэля
- 9. Артур Михаэль
- 10. Региоселективность в реакции Михаэля
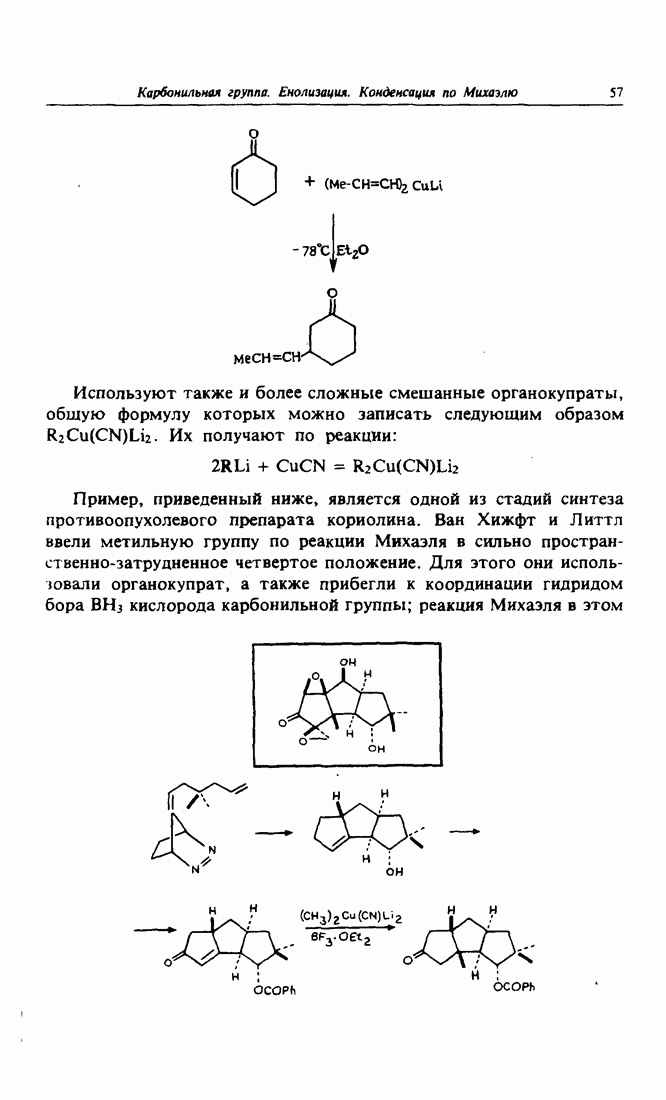
- 11. Применение органокулратов
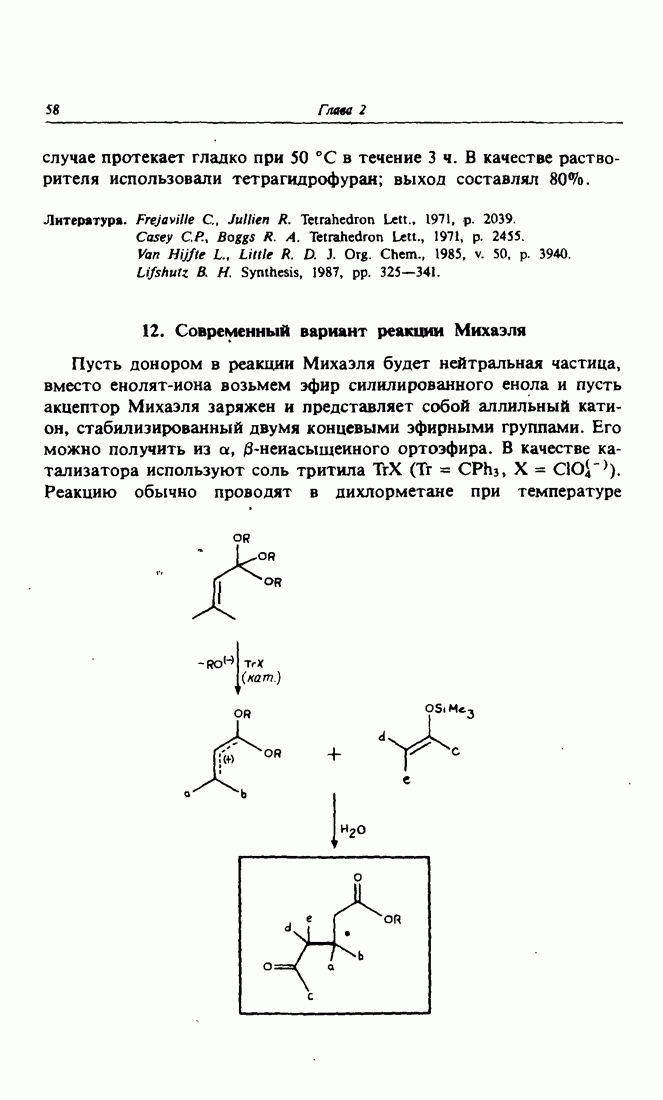
- 12. Современный вариант реакции Михаэля
- 13. Сопряжение или отсутствие сопряжения?
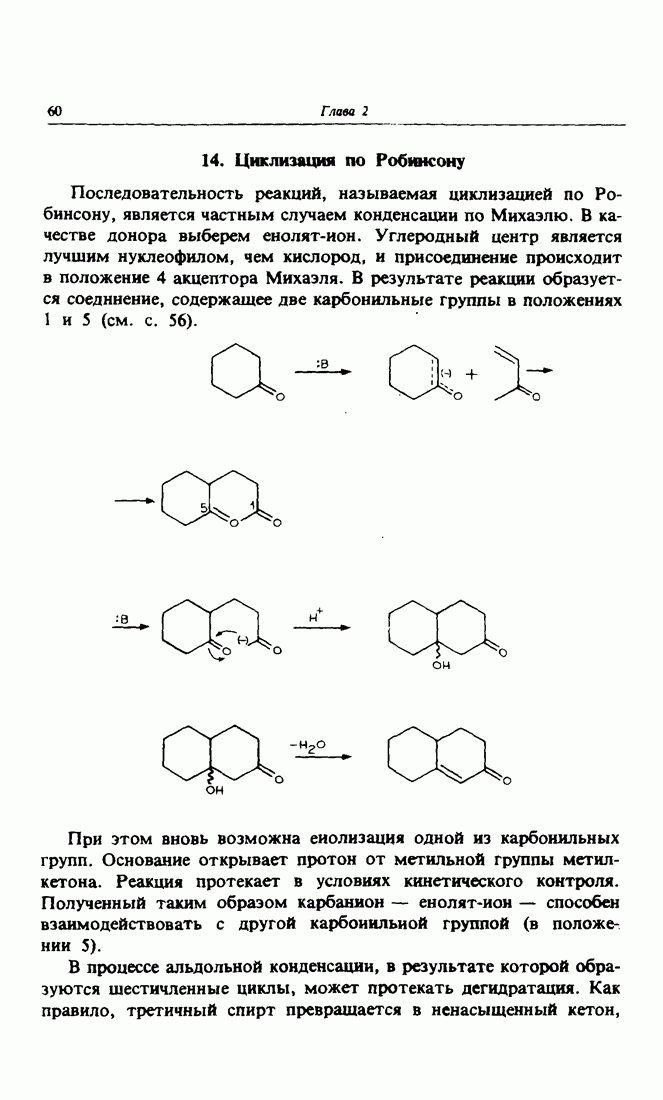
- 14. Циклизация по Робинсону
- 15. Сэр Роберт Робинсон
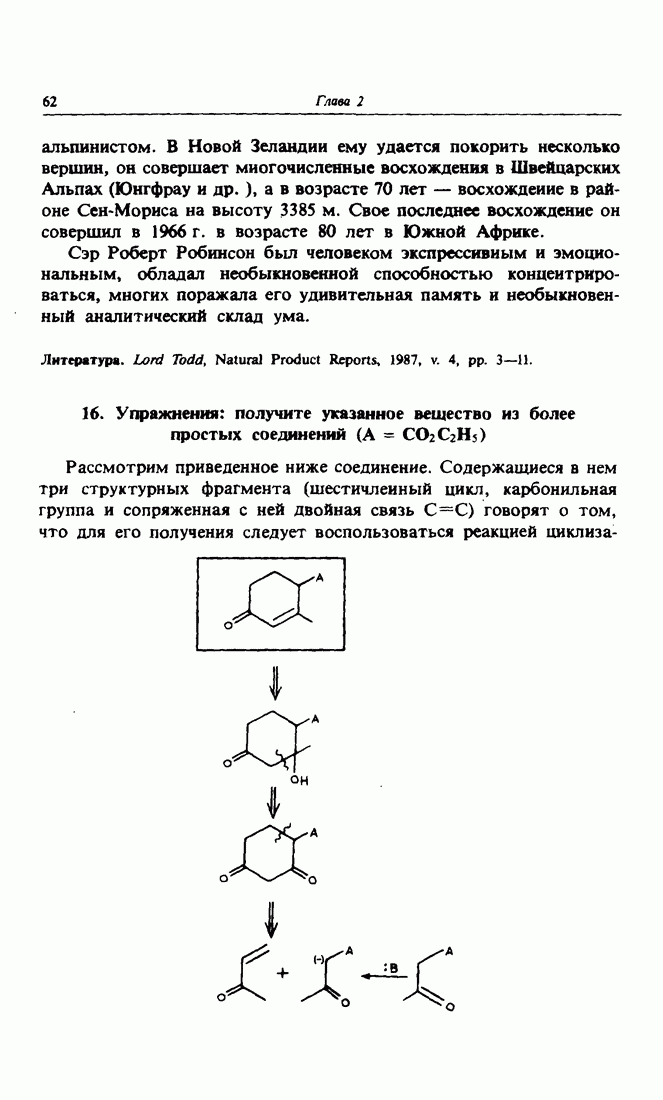
- 16. Упражнения: получите указанное вещество из более простых соединений (A=CO2C2H5)
- Глава 3. КАРБОНИЛЬНАЯ ГРУППА. АЛЬДОЛЬНАЯ КОНДЕНСАЦИЯ
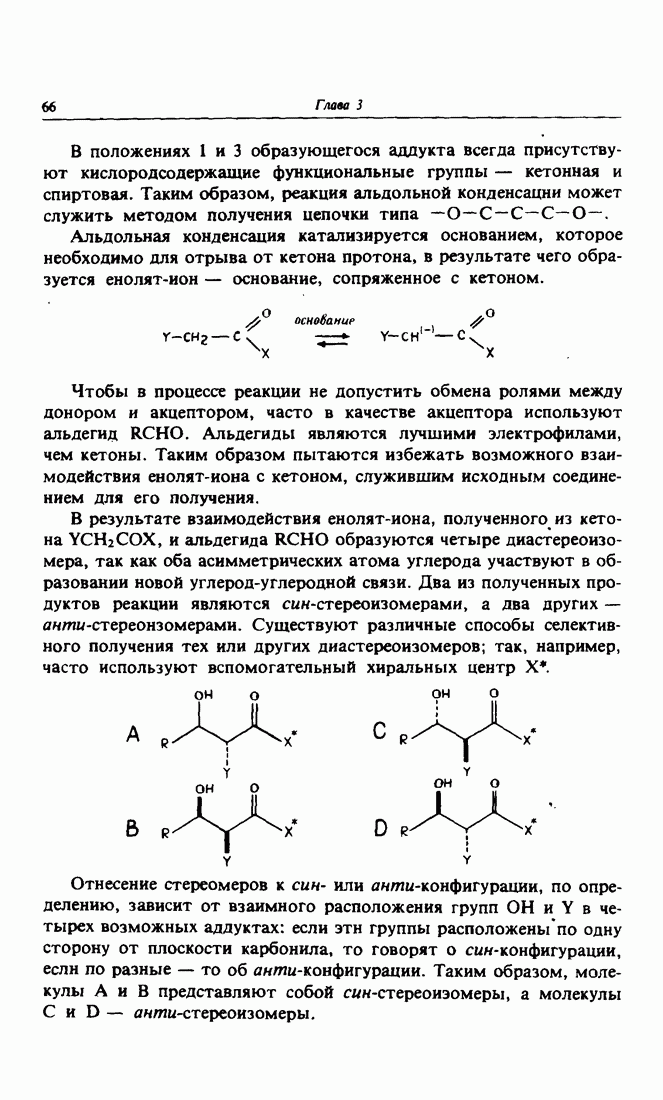
- 2. Устойчивость продуктов альдольиой конденсации
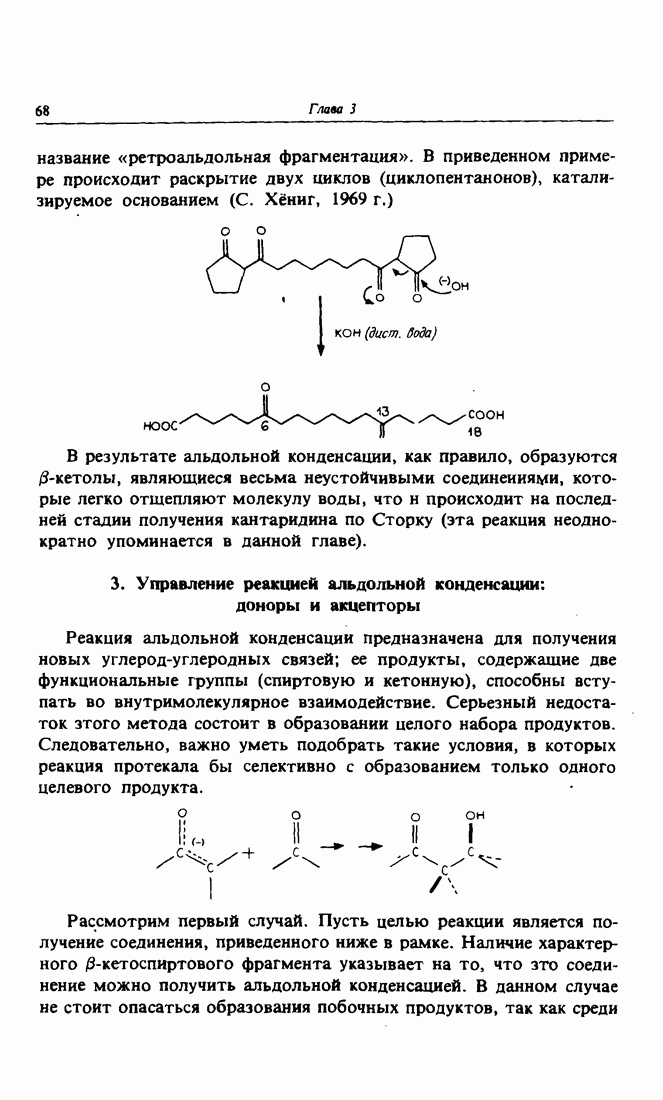
- 3. Управление реакцией альдольной конденсации: доноры и акцепторы
- 4. Управление реакцией альдольной конденсации: син- и анти-диастереомеры
- 5. Стереоселективные реакции альдольной конденсации
- Глава 4. НЕКОТОРЫЕ РЕШЕНИЯ ПРОБЛЕМЫ СЕЛЕКТИВНОСТИ (ХИМИЧЕСКАЯ, РЕГИО- И СТЕРЕОСЕЛЕКТИВНОСТЬ)
- 2. Региоселективность при образовании енолятов
- 3. Селективное получение Е- и Z-енолятов
- 4. Двойной принцип стереоселективности
- 5. Энантиоселективная реакция Михаэля
- 6. Региоселективность в реакциях алкилирования кетонов. Использование енаминов
- 7. Получение хирального центра путем алкилирования енаминов
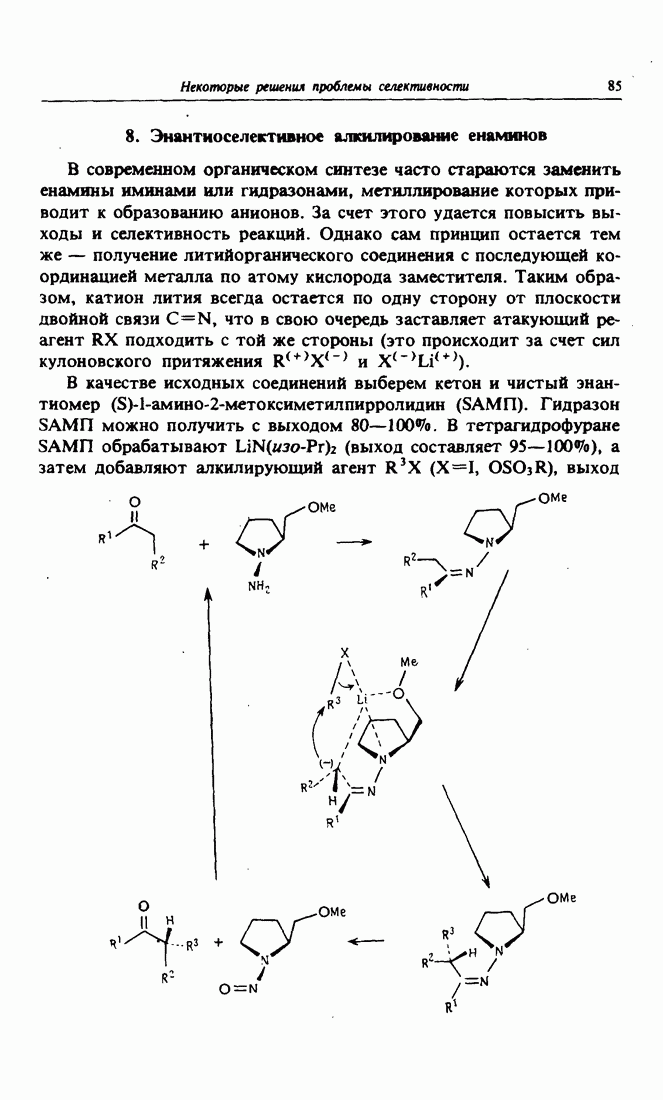
- 8. Энантиоселективное алкилирование енаминов
- 9. Перенос хиральности
- 10. Соотношение между реакционноспособностью и селективностью
- 11. Стереоэлектронный эффект
- 12. Конформации переходного состояния «кресло» и «ванна»
- Глава 5. ЗАЩИТА И РЕГЕНЕРАЦИЯ ФУНКЦИОНАЛЬНЫХ ГРУПП. СПИРТОВАЯ И КАРБОНИЛЬНАЯ ГРУППЫ. ОБРАЩЕНИЕ ПОЛЯРНОСТИ
- 1. Защита карбонильной группы ацетальной
- 2. Защита спиртов. Диметил-трет-бутилсилиловые эфиры
- 3. Защита спиртовых групп при помощи эфиров енолов
- 4. Обращение полярности
- 5. Э. Дж. Кори
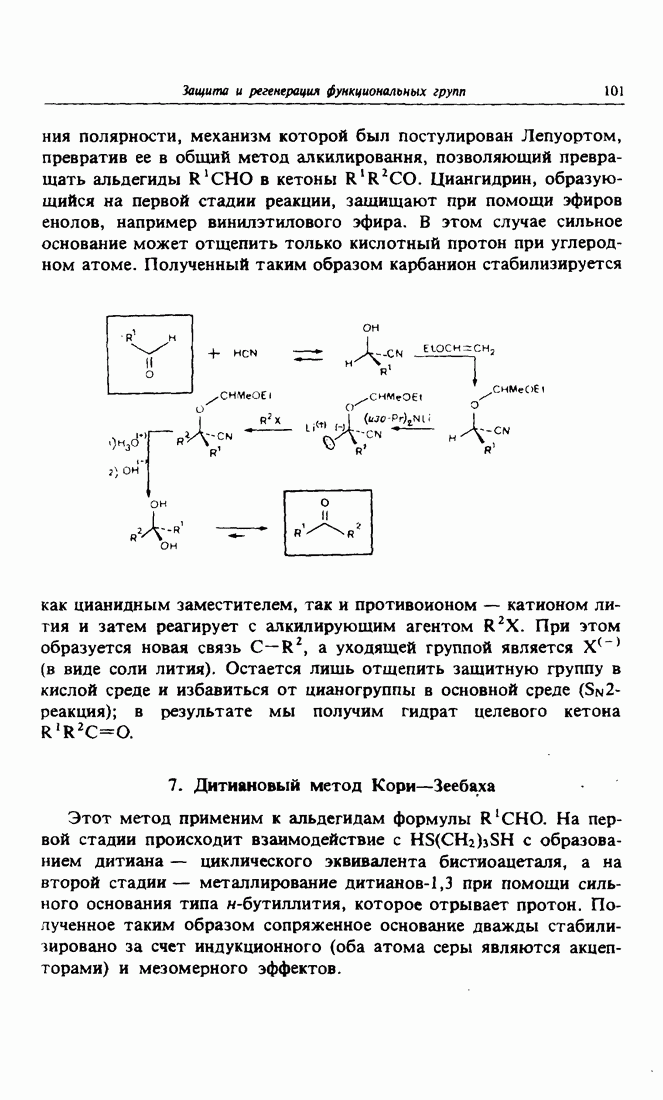
- 6. Инверсия полярности по методу Лепуорта — Шторка
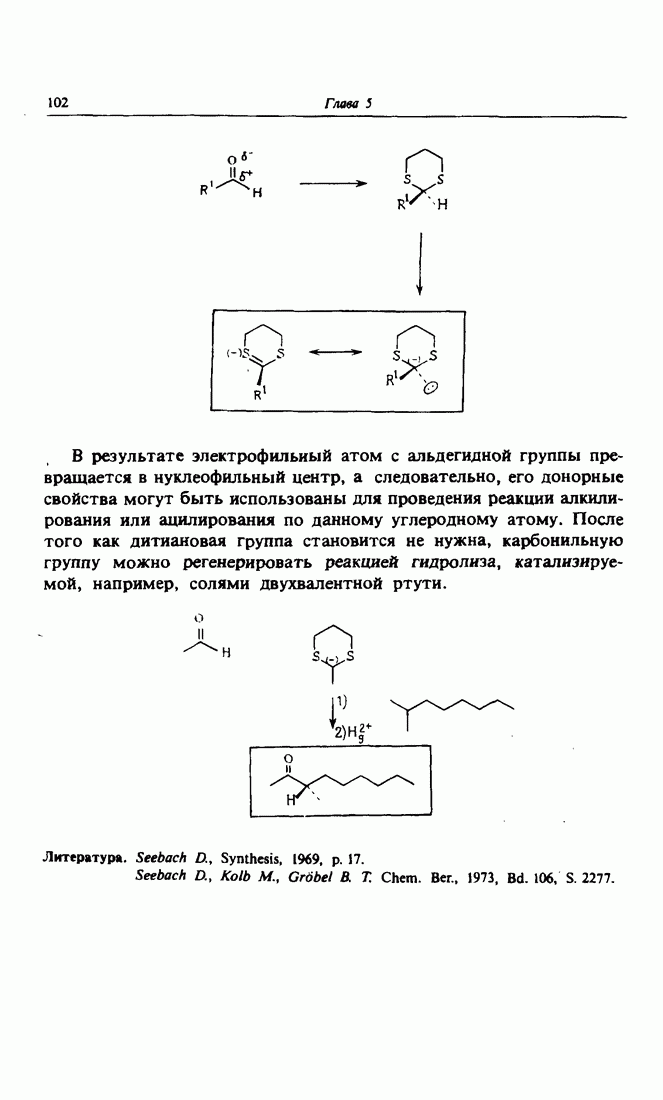
- 7. Дитиановый метод Кори-Зеебаха
- Главе 6. АКТИВАЦИЯ
- 2. Стабилизация конечного состояния
- 3. Дестабилизация начального состояния
- 4. Стабилизация переходного состояния
- Главв 7. ПОСТРОЕНИЕ ЦИКЛОВ
- 2. Региоселективность
- 3. Реакция Дильса — Альдера в условиях обращенного электронного соответствия
- 4. Стереоселективность в реакциях Дильса — Альдера
- 5. Напряжение в циклах
- 6. Построение циклобутанов (метод 1) Термическая димеризация
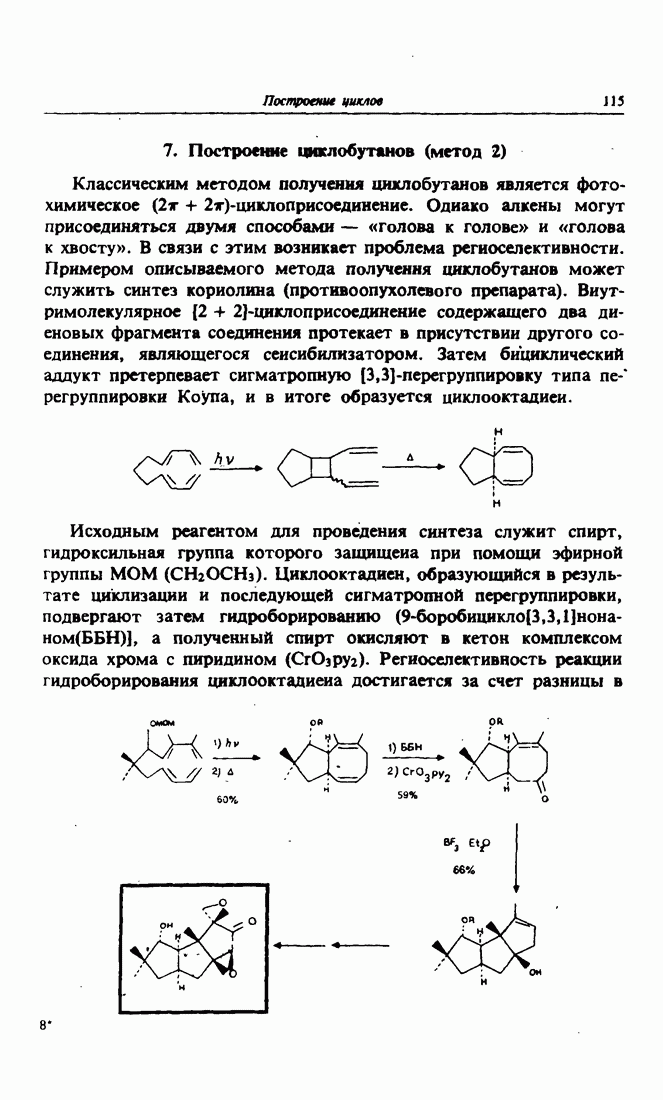
- 7. Построение циклобутанов (метод 2)
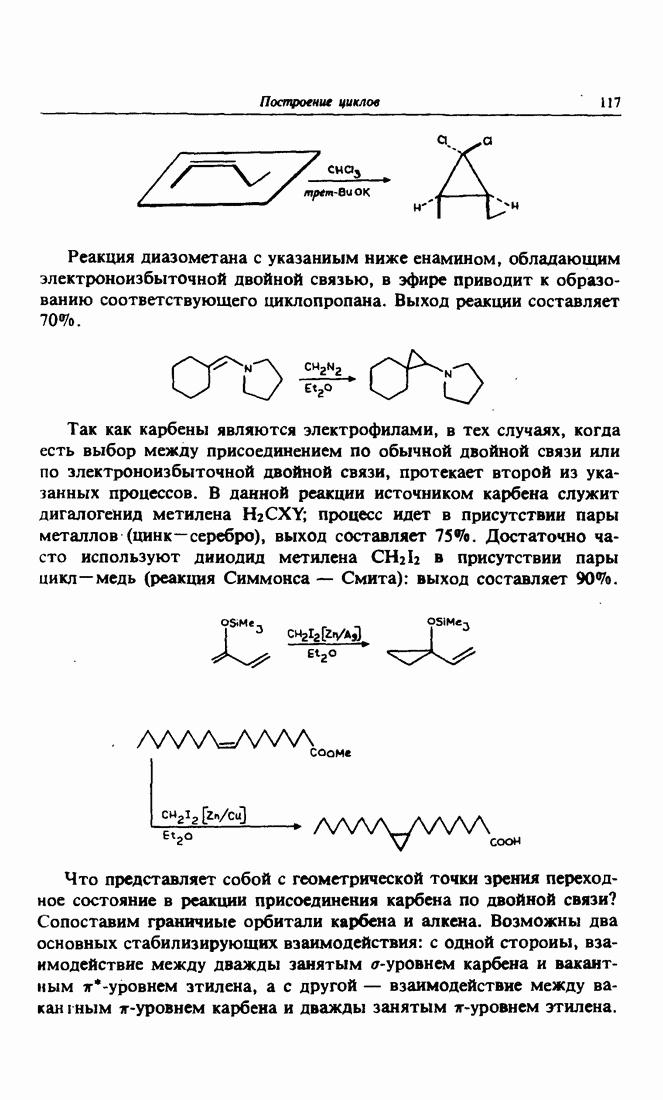
- 8. Синтез циклопропанов. Присоединение карбенов к алкенам
- Глааа 8. ВВЕДЕНИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП. РЕАКЦИИ ЗАМЕЩЕНИЯ
- 2. Соотношение структура — реакционноспособность
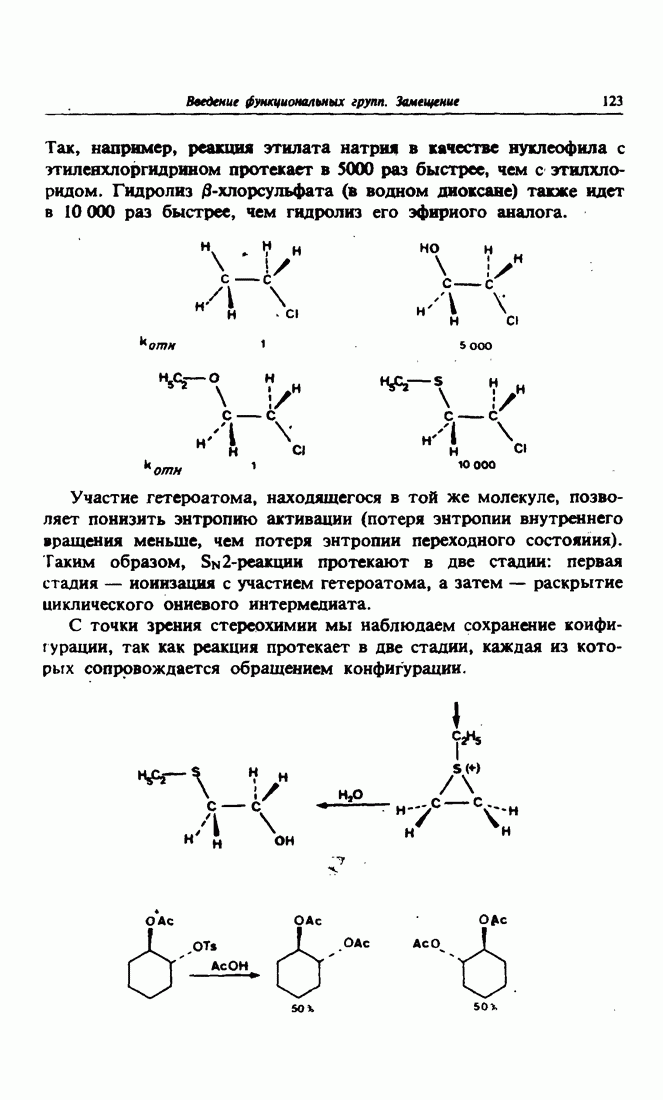
- 3. Участие соседней группы в Sn2-реакциях
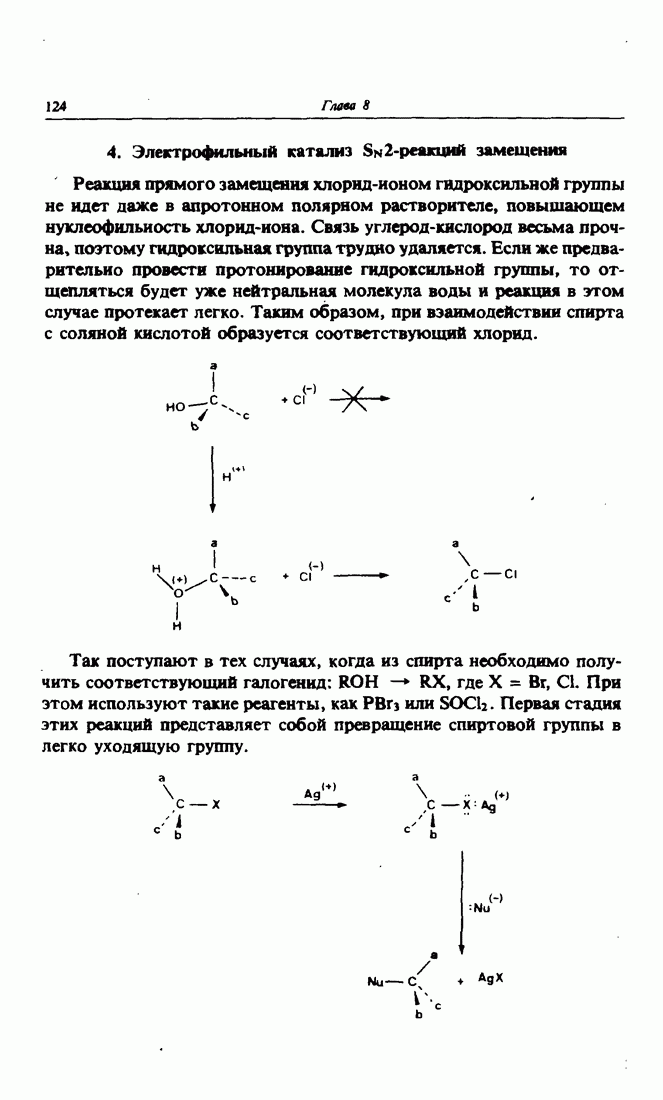
- 4. Электрофильный катализ Sn2-реакций замещения
- 5. Региоселеггивность в реакциях алкилирования
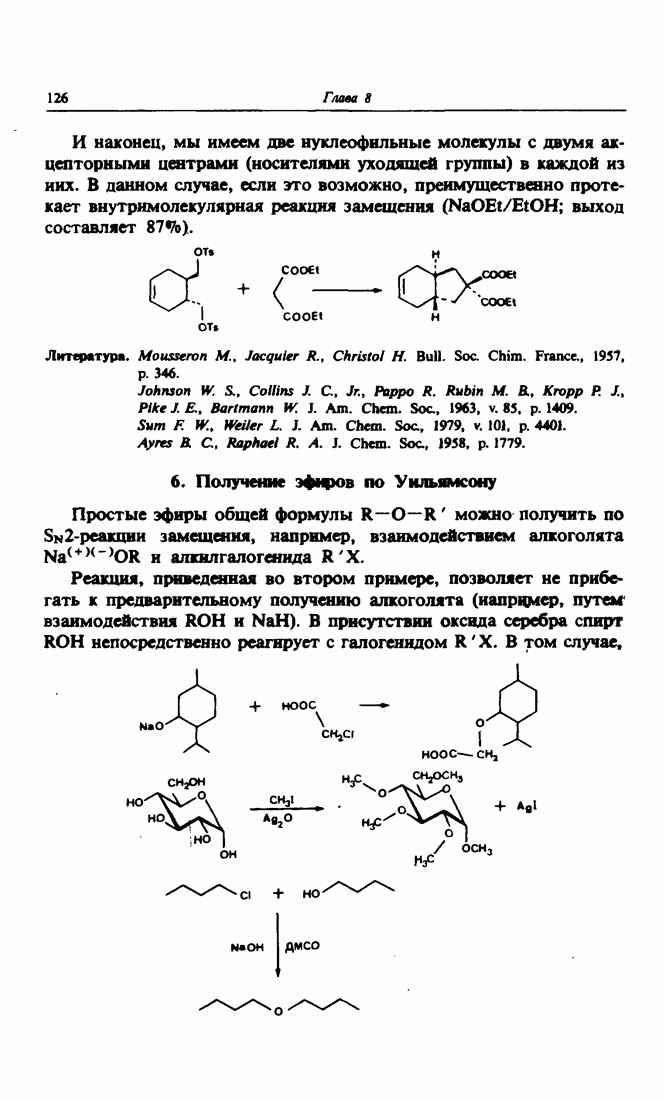
- 6. Получение эфиров по Уильямсону
- 7. К вопросу об обозначениях
- Глава 9. ВВЕДЕНИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП. РЕАКЦИИ ВОССТАНОВЛЕНИЯ
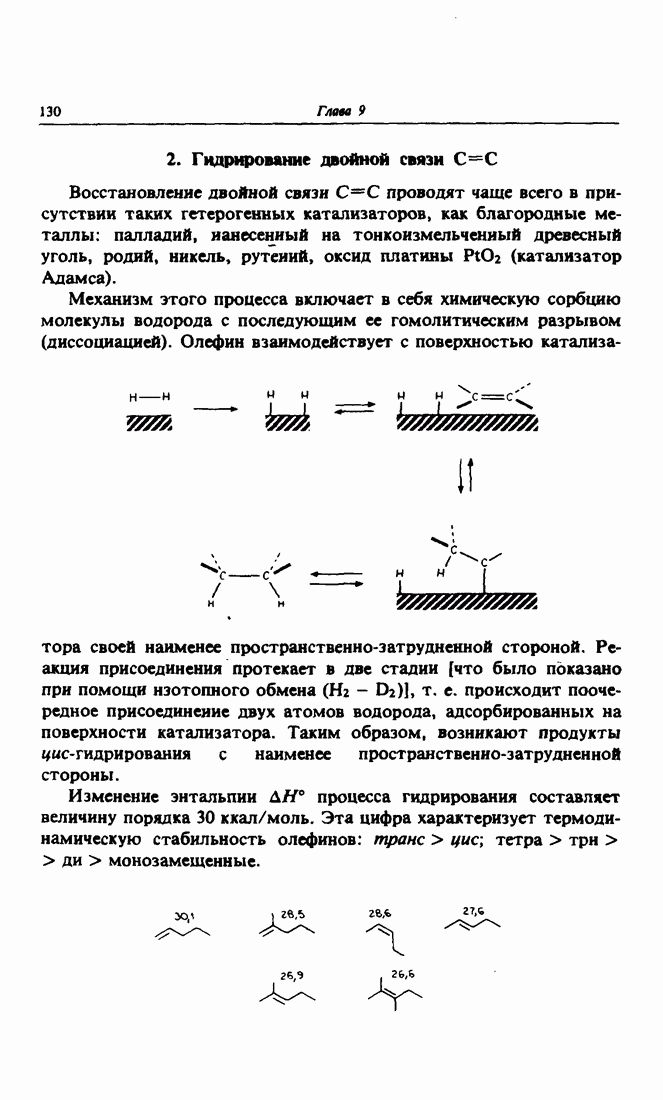
- 2. Гидрирование двойной связи С=С
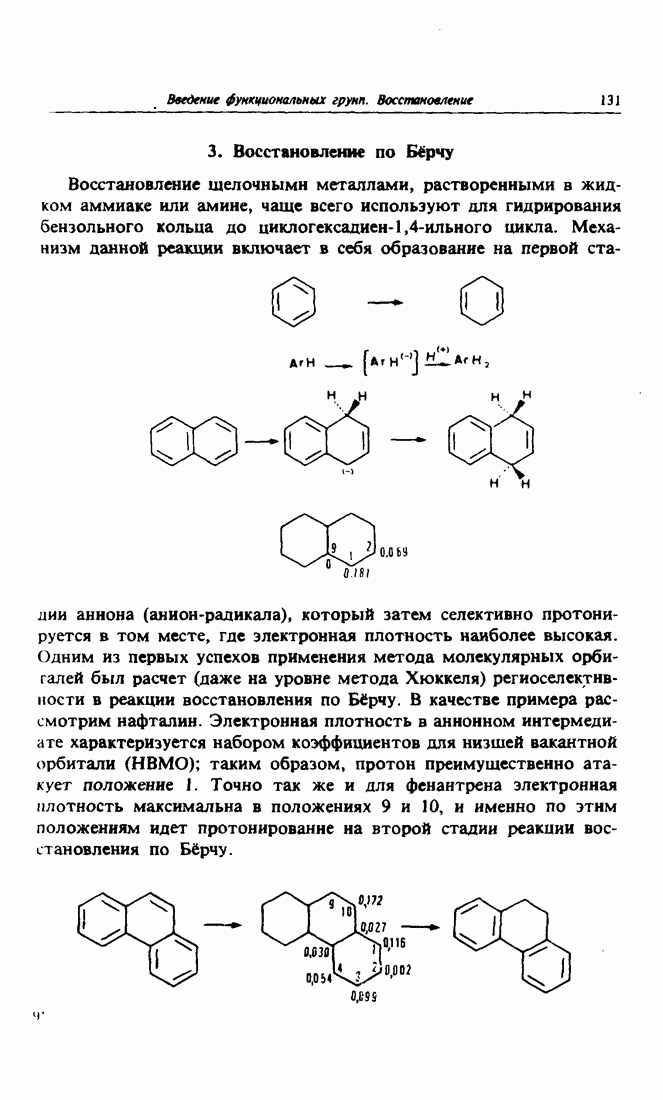
- 3. Восстановление по Бёрчу
- 4. Восстановление карбонильной группы
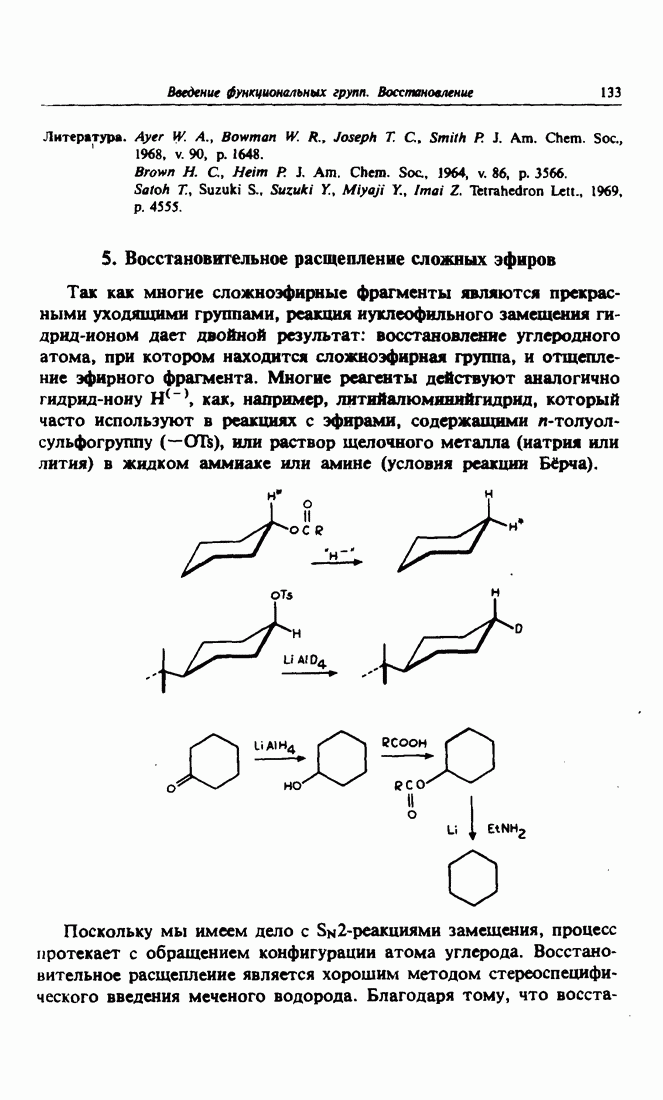
- 5. Восстановительное расщепление сложных эфиров
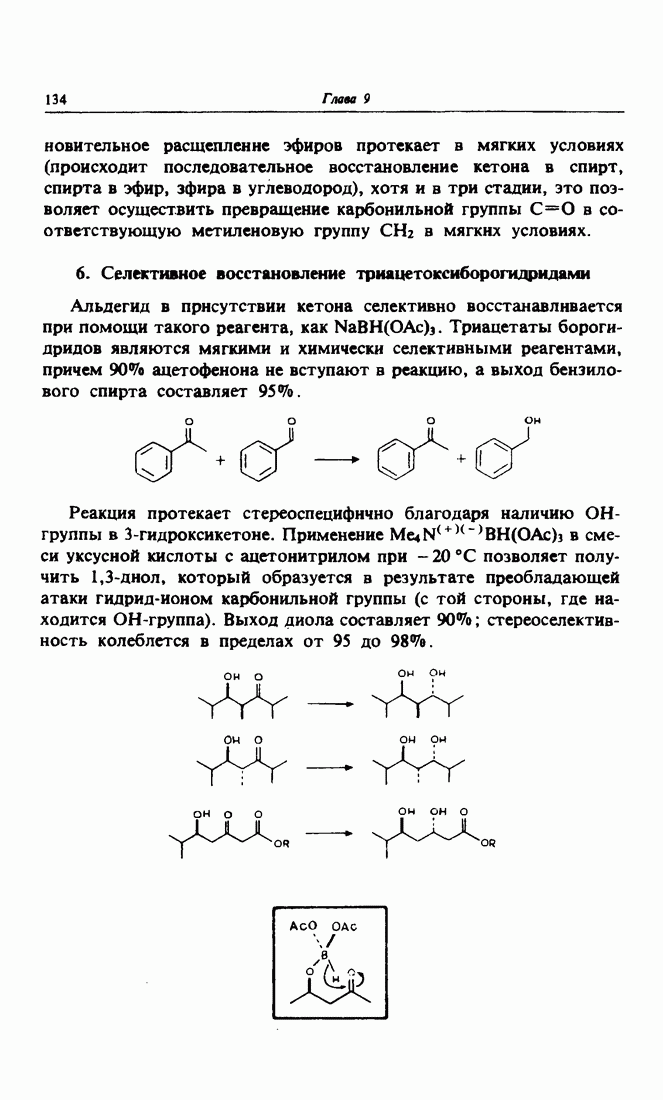
- 6. Селективное восстановление триацетоксиборогидридами
- Глава 10. ВВЕДЕНИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП. РЕАКЦИИ ОКИСЛЕНИЯ
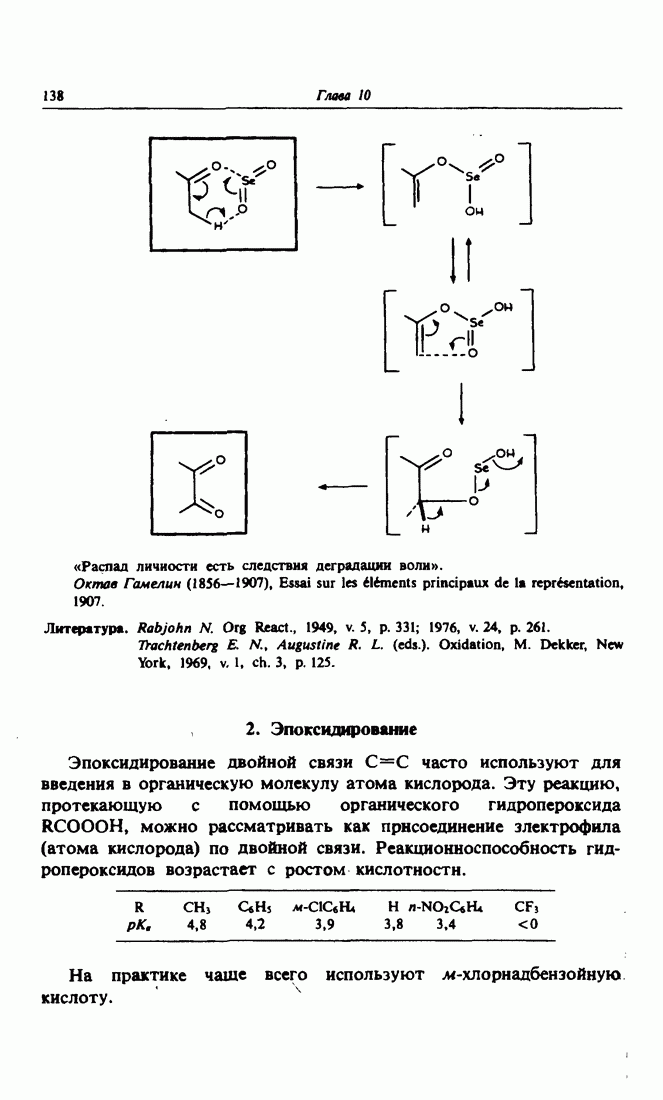
- 2. Эпоксидирование
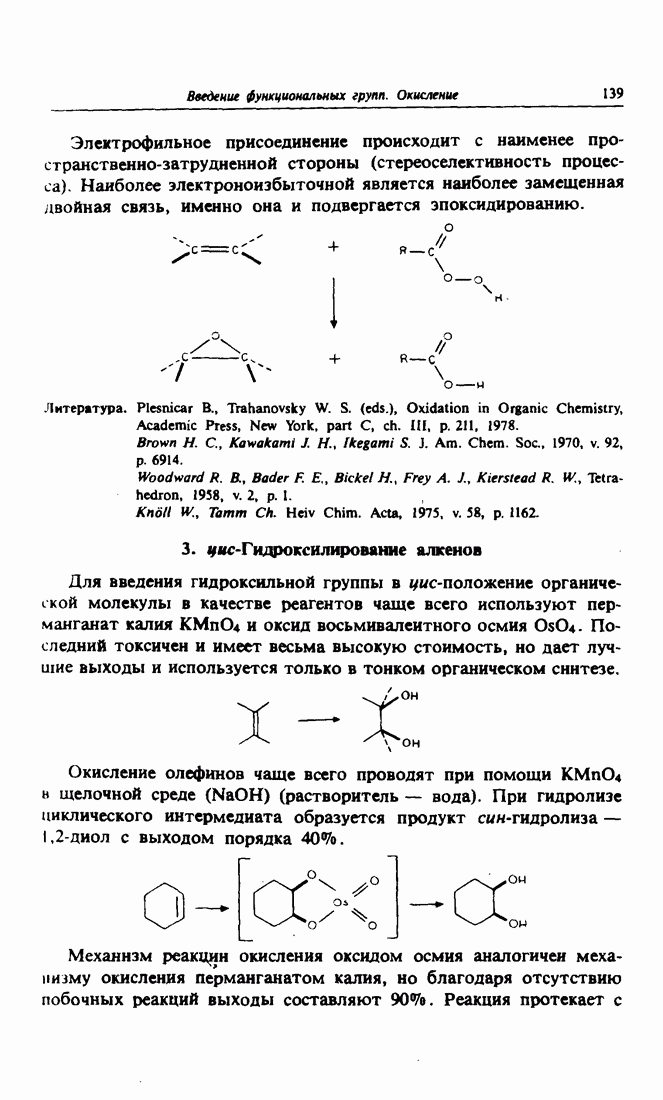
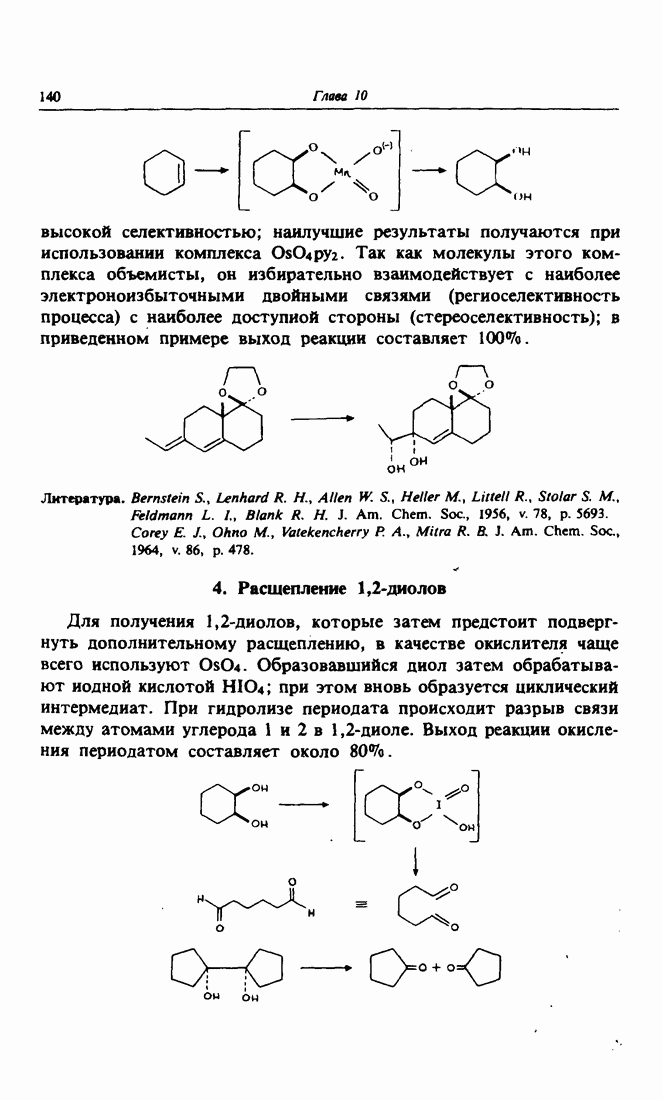
- 3. цис-Гидроксилирование алкенов
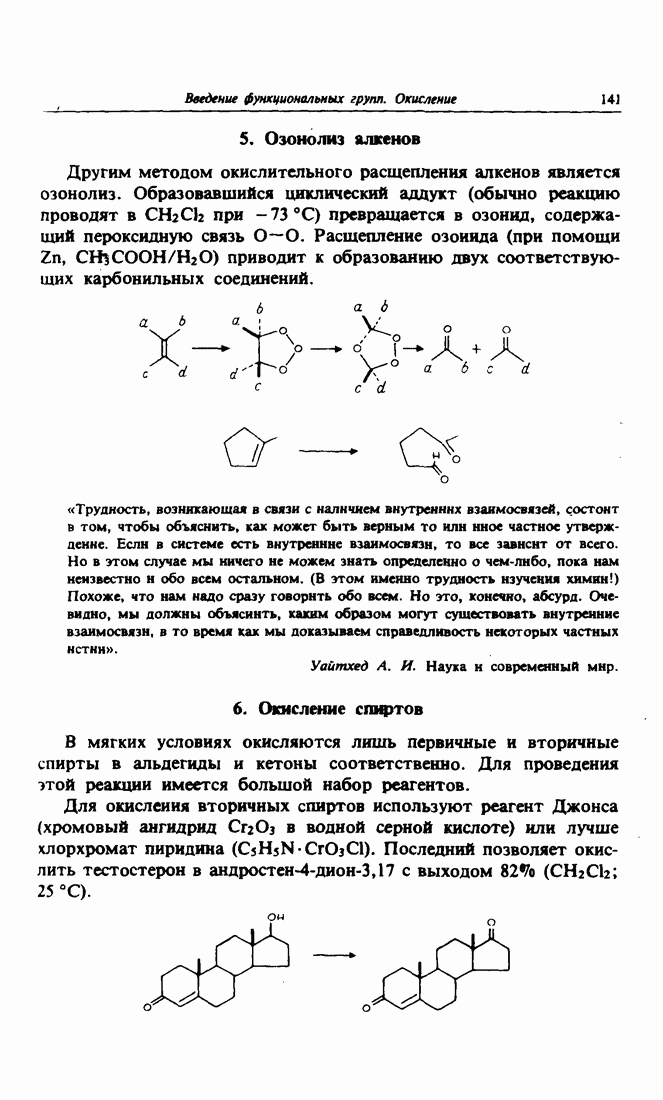
- 4. Расщепление 1,2-диолов
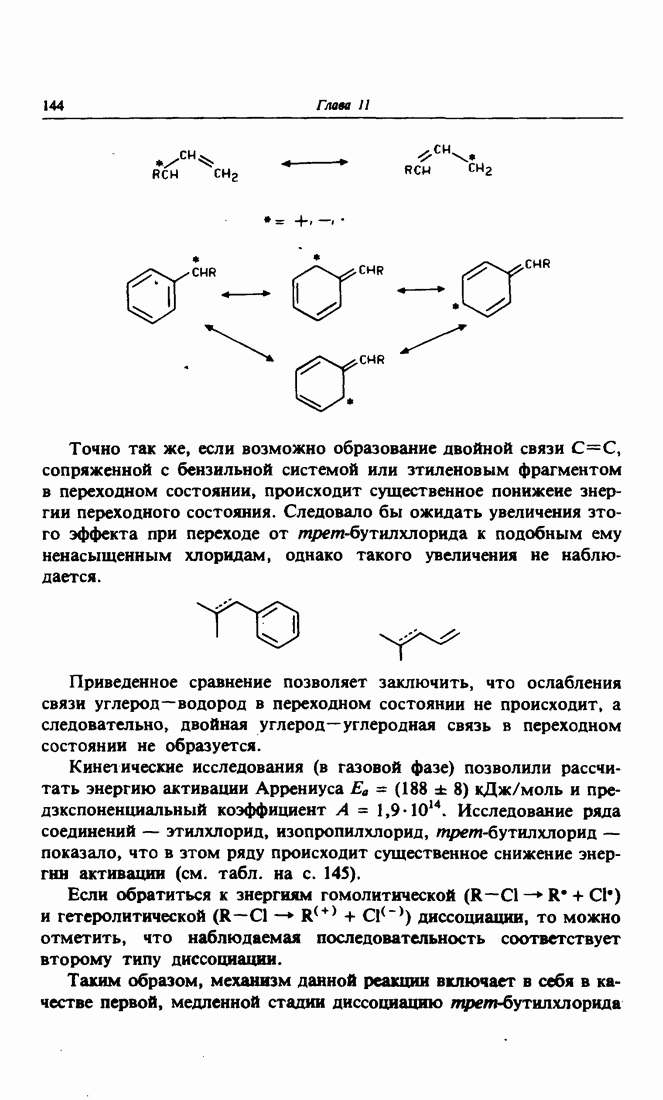
- 5. Озонолиз алкенов
- 6. Окисление спиртов
- Главе 11. РЕАКЦИИ ПРИСОЕДИНЕНИЯ И ЭЛИМИНИРОВАНИЯ
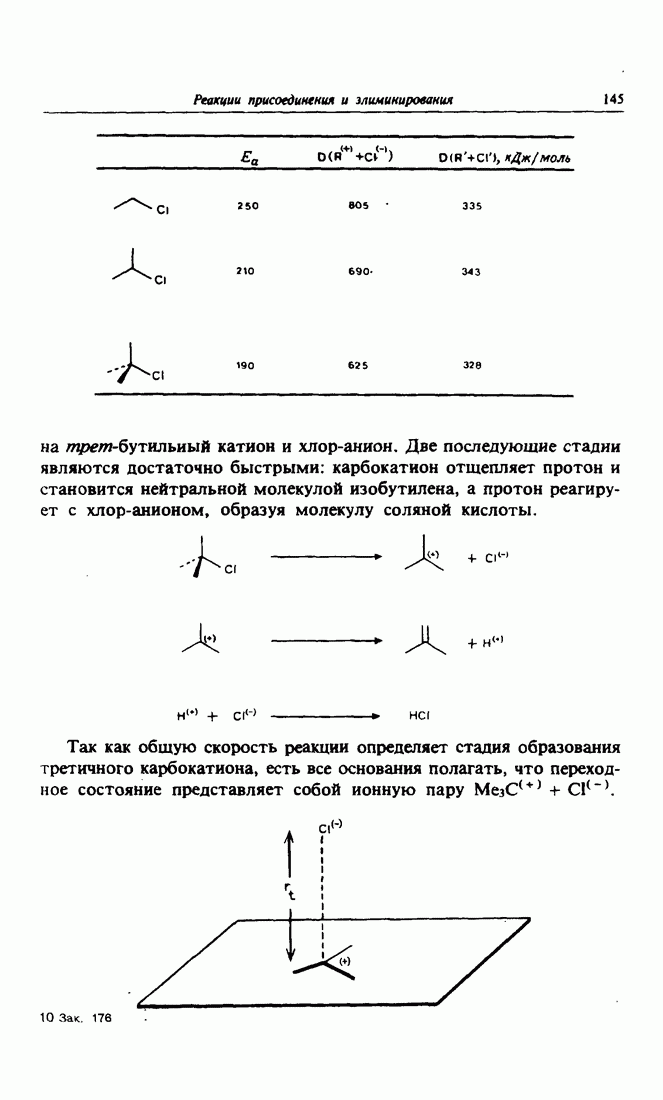
- 2. Классически механизм реакции электрофильного присоединения. Правило Марковникова
- 3. Основные электрофильные агенты
- 3.3. Присоединение гипохлоритов и гипобромитов
- 3.4. Оксимеркурирование
- 3.5. Гидроборирование
- 3.6. Окситаллирование
- 4. Стереохимия реакции присоединения по двойной связи С=С
- 5. Конкуренция нуклеофила и растворителя в реакции электрофильного присоединения
- 6. Присоединение к напряженным олефинам: цис-присоединение
- 7. Стереохимия реакций бимолекулярного элиминирования
- 8. Виды b-элиминирования
- Главв 12. ПЕРЕГРУППИРОВКИ ФУНКЦИОНАЛЬНЫХ ГРУПП. ПРЕВРАЩЕНИЕ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ В ОЛЕФИНЫ ПО РЕАКЦИИ ВИТТИГА
- 2. Реакция Дарзана
- 3. Дарзан — один из великих политехников
- 4. Обобщение и модернизация метода
- 5. Стереоселективность реакции Кори — Чайковского
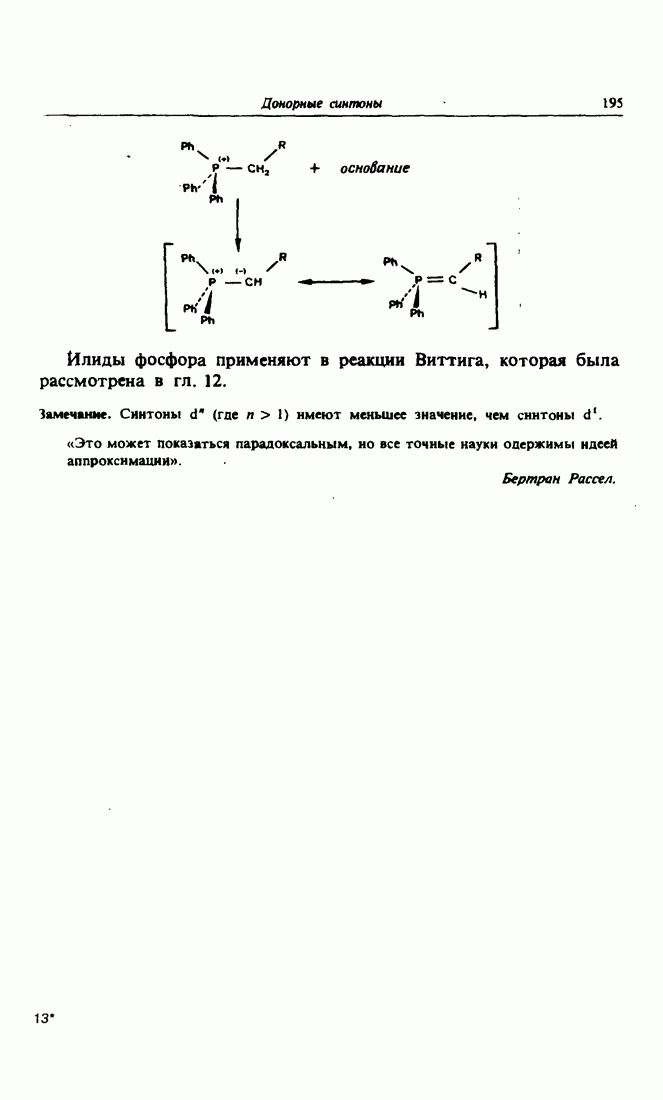
- 6. Реакция Виттига
- 7. Георг Виттиг
- 8. Причины образования различных продуктов в реакциях Виттига и Кори — Чайковского
- 9. Разновидность реакции Виттига: олефинирование по Петерсону
- Главе 13. ПЕРЕГРУППИРОВКИ
- 2. 1,2-Переход в карбокатионах
- 3. Перегруппировка Бекмана
- 4. Перегруппировка Курциуса
- 5. Перегруппировка Байера — Виллигера
- 6. Реакция Рамберга-Беклунда
- Глава 14. ДОНОРНЫЕ СИНТОНЫ
- 2. Алкильные донорные синтоны
- 3. Донорные синтоны d1 с гетероатомами, обладающими d-орбиталью
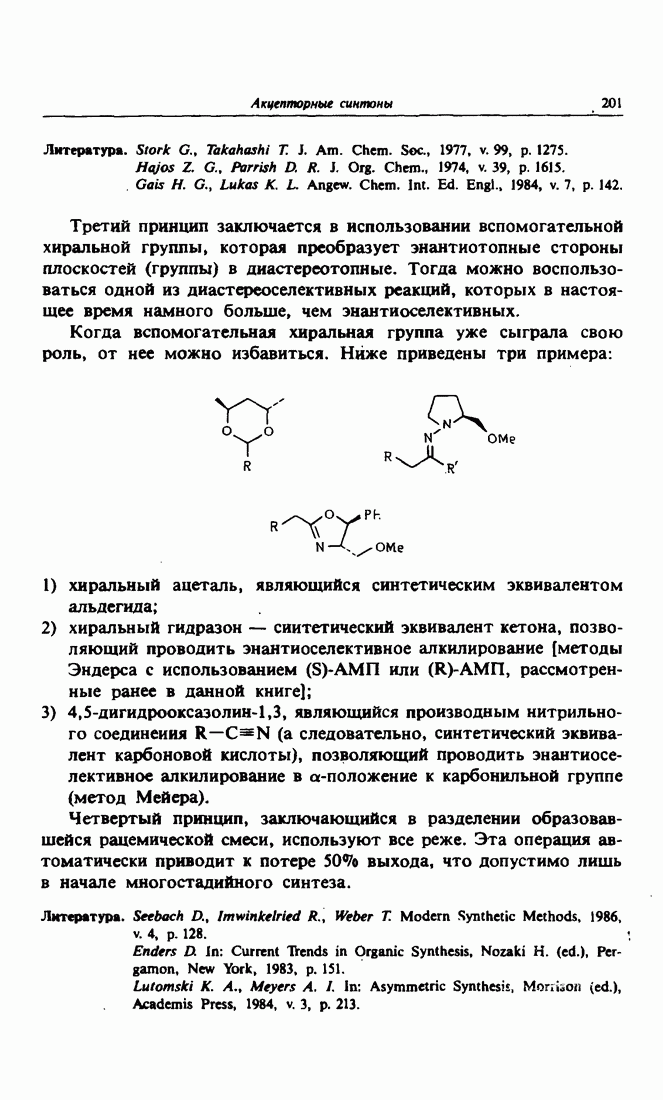
- Глава 15. АКЦЕПТОРНЫЕ СИНТОНЫ
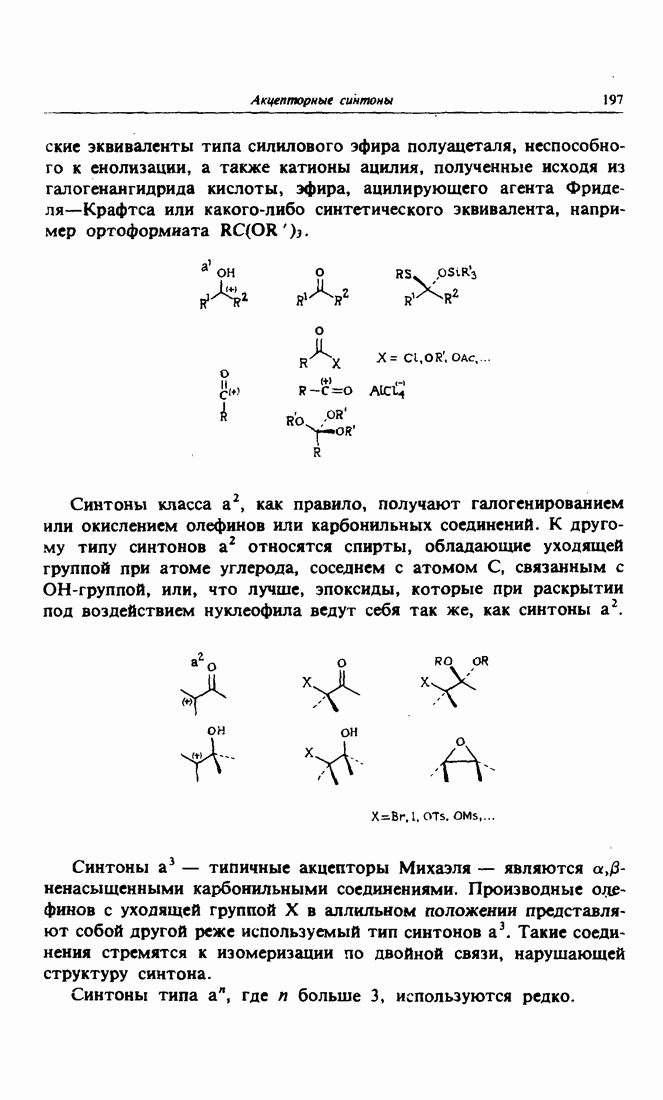
- 1. Синтоны-акцепторы
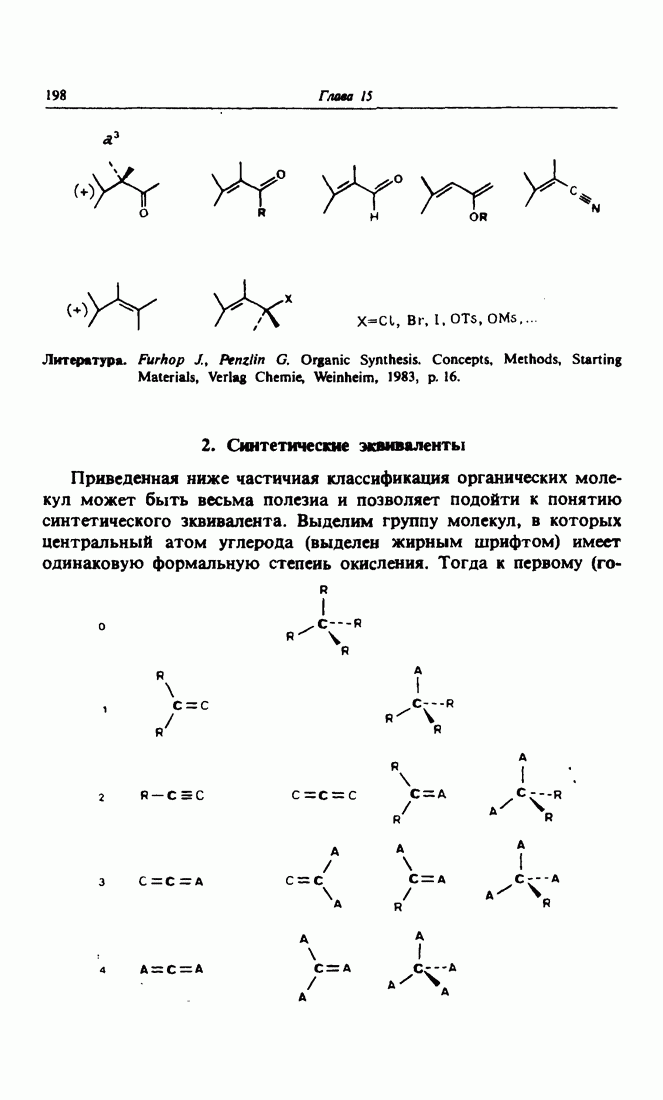
- 2. Синтетические эквиваленты
- 3. Контролируемое образование новых связей
- 4. Расчленение молекулы на фрагменты
- 5. Двойное расчленение молекулы
- 6. Изменение реакционноспособности в результате обращения полярности
- Глава 16. РЕТРОСИНТЕТИЧЕСКИЙ АНАЛИЗ
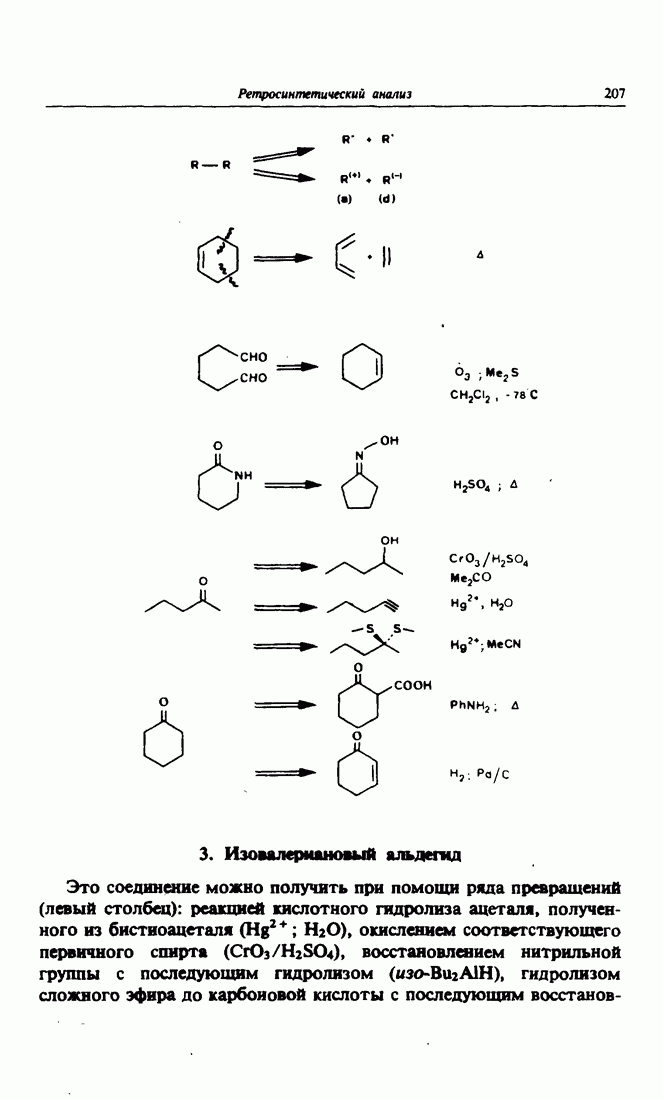
- 2. Цепь превращений
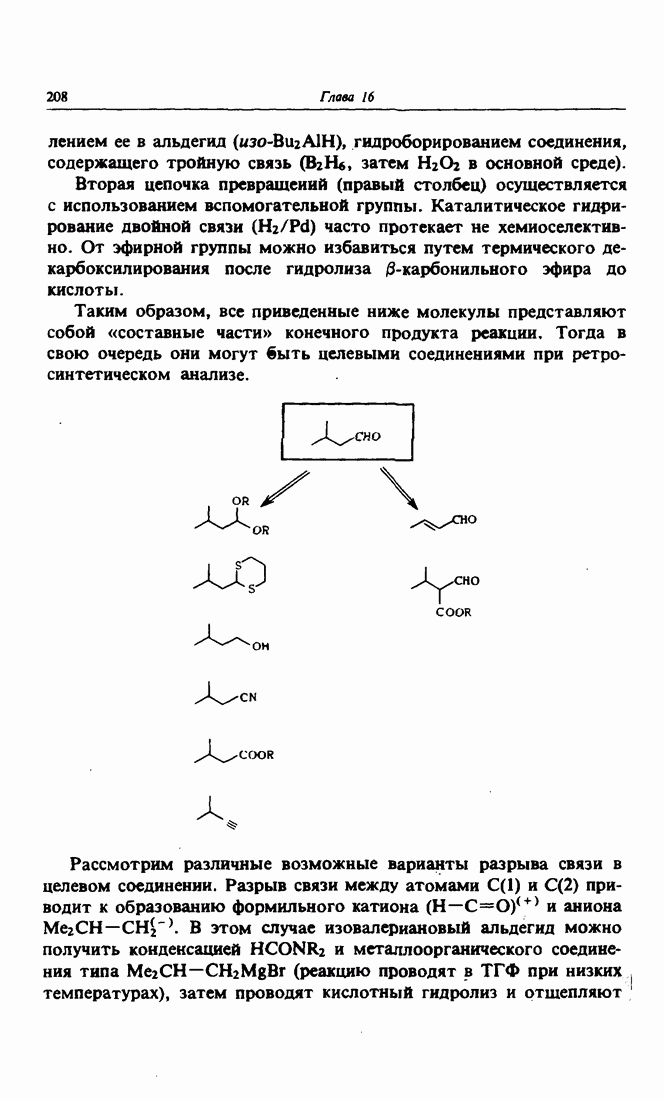
- 3. Изовалериановый альдегид
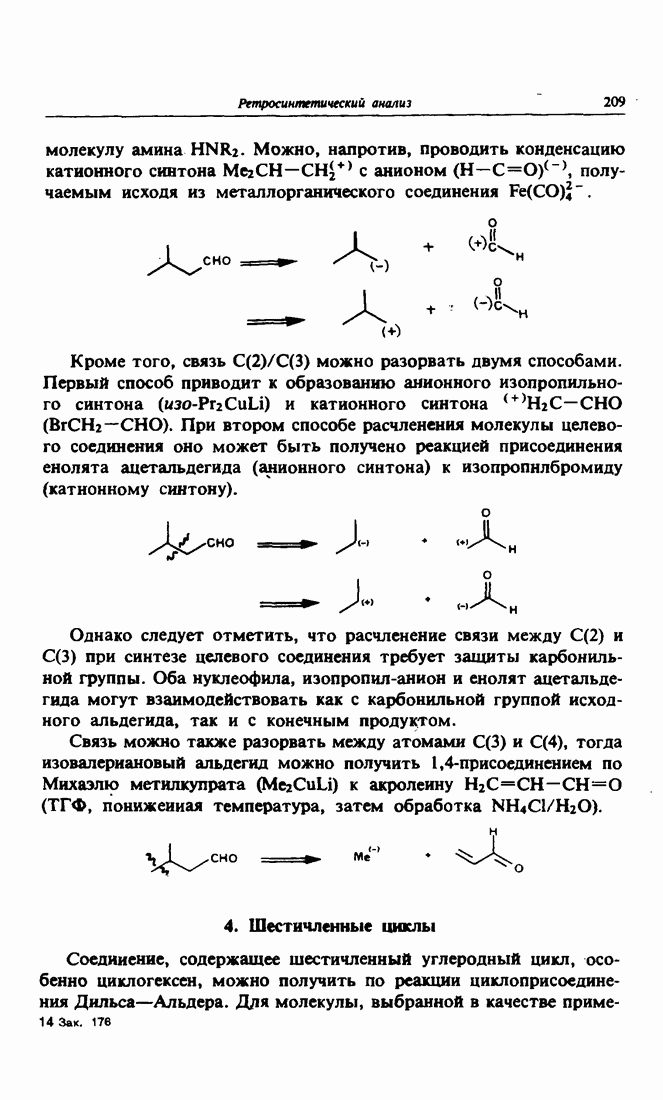
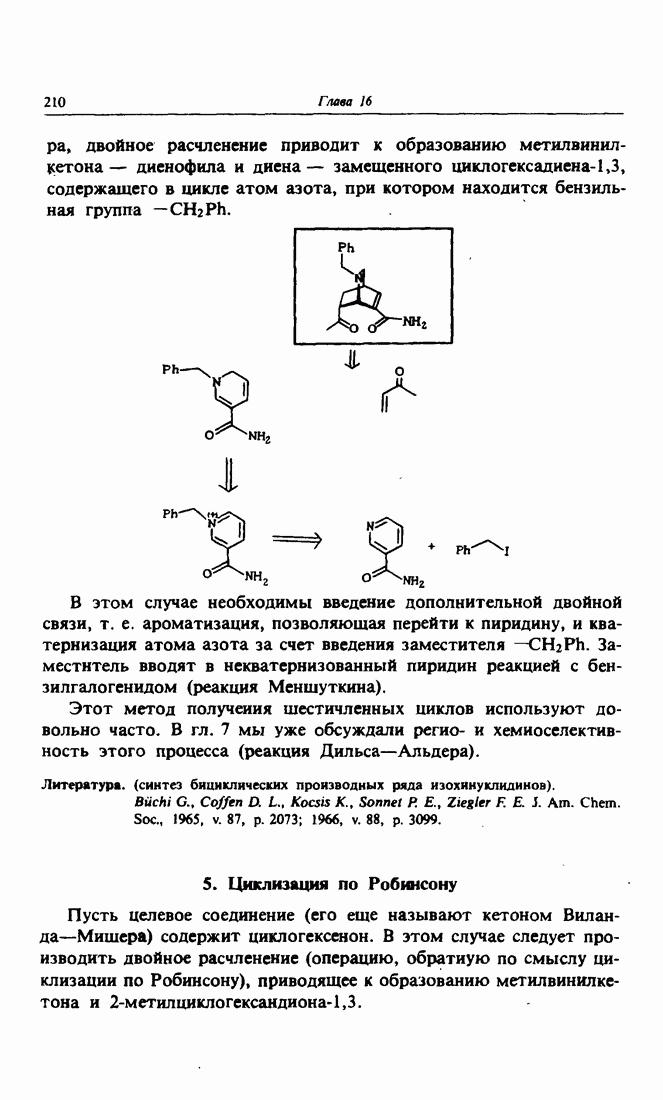
- 4. Шестичленные циклы
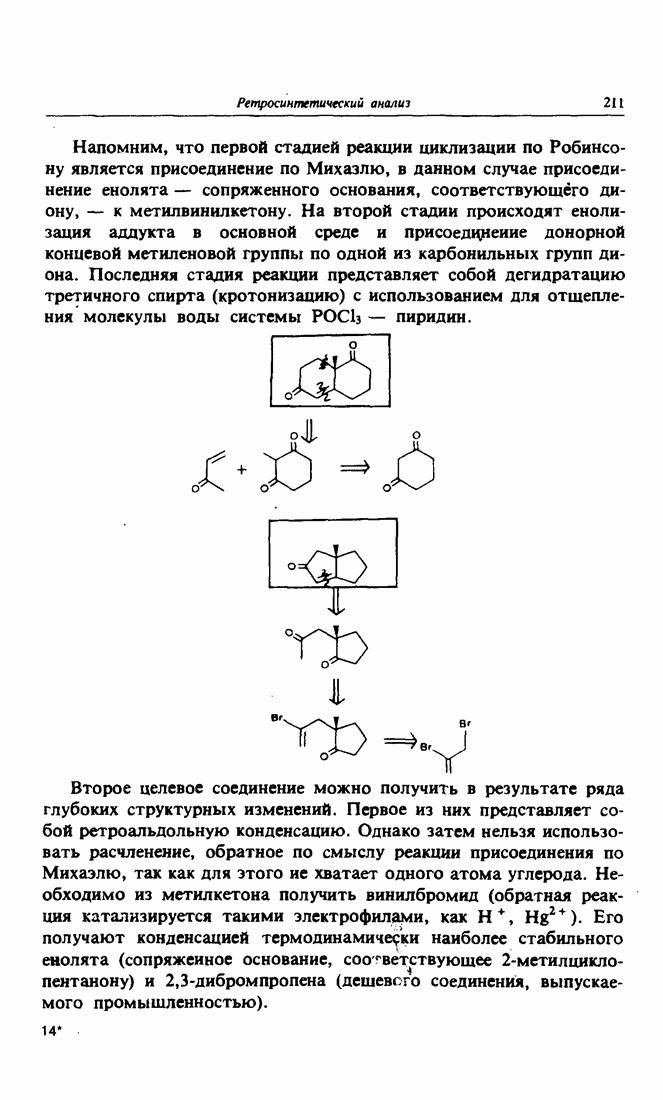
- 5. Циклизация по Робинсону
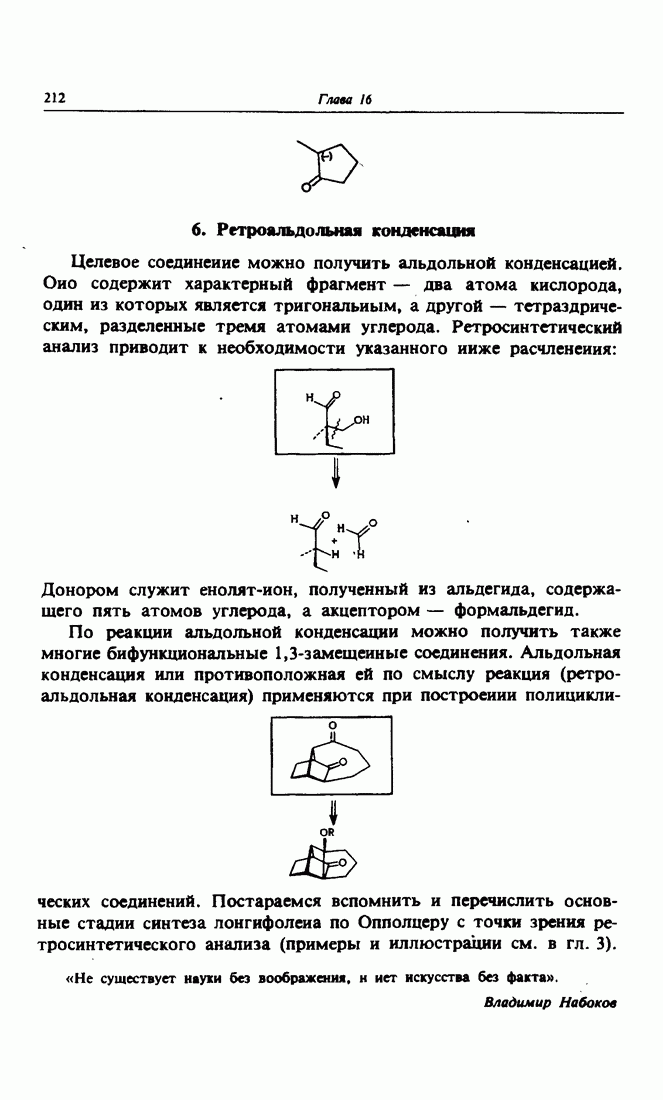
- 6. Ретроальдольная конденсация
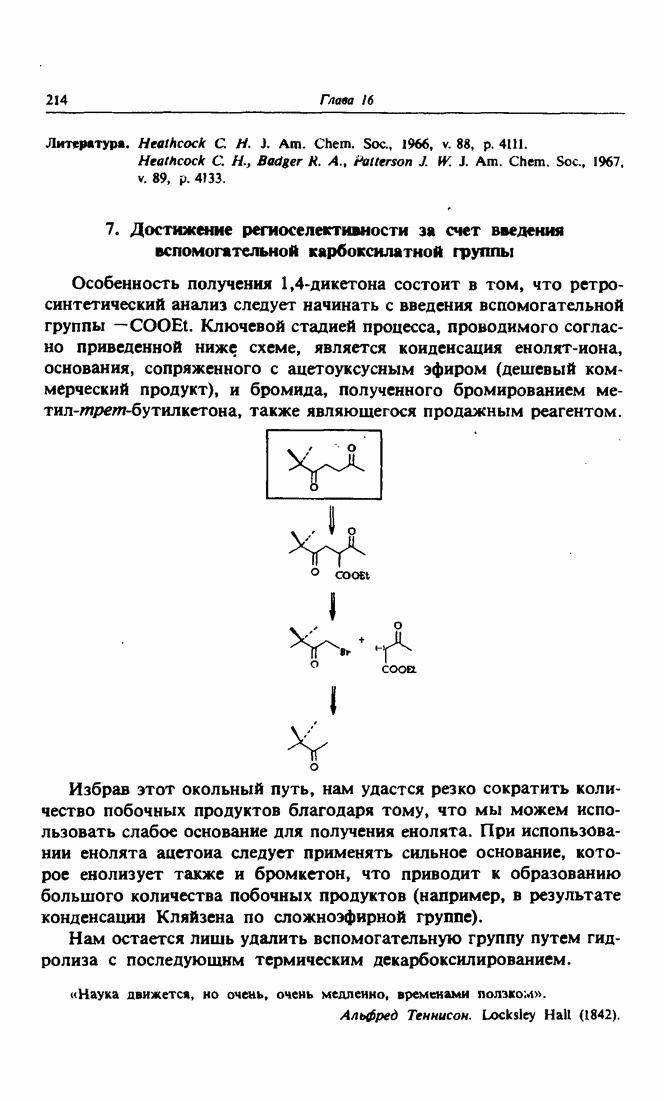
- 7. Достижение региоселективности за счет введения вспомогательной карбоксилатной группы
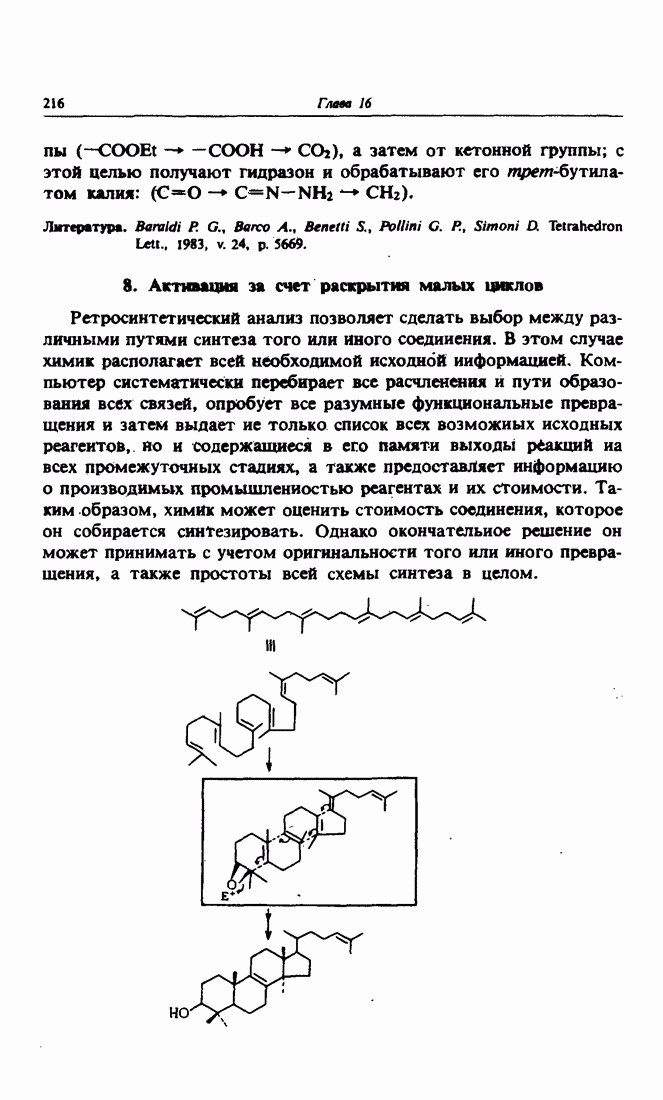
- 8. Активация за счет раскрытия малых циклов
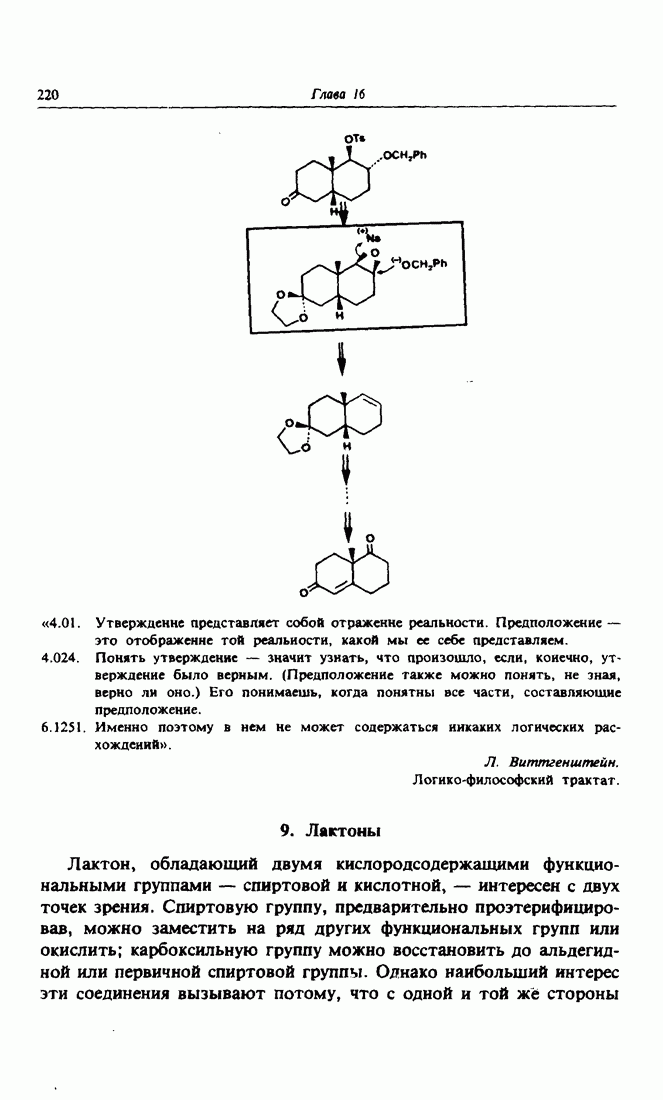
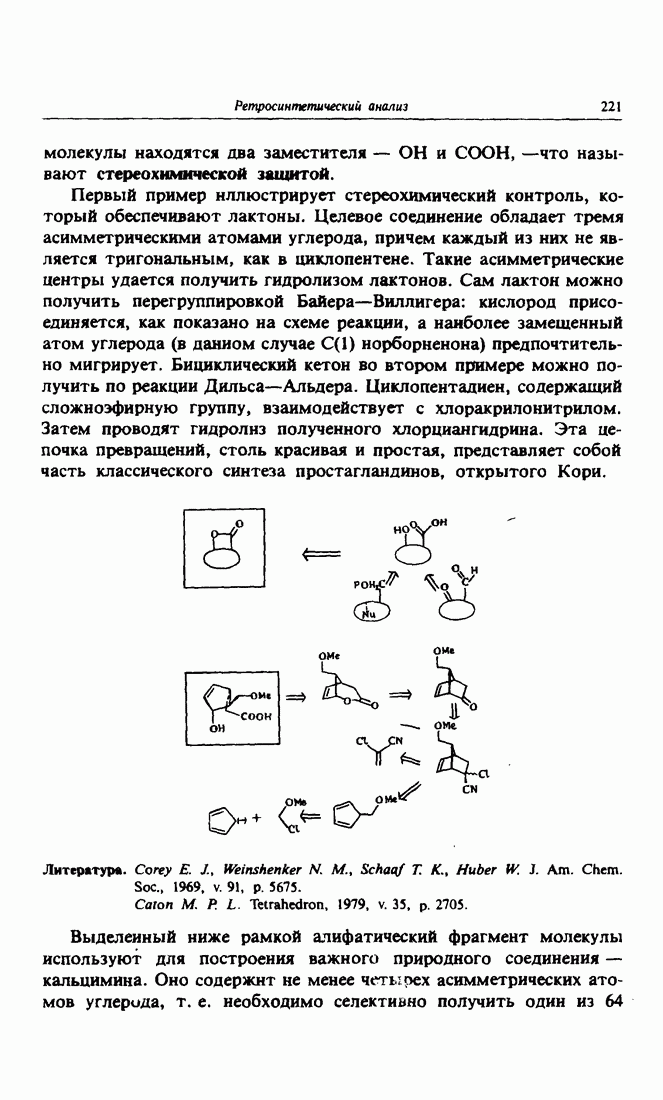
- 9. Лактоны
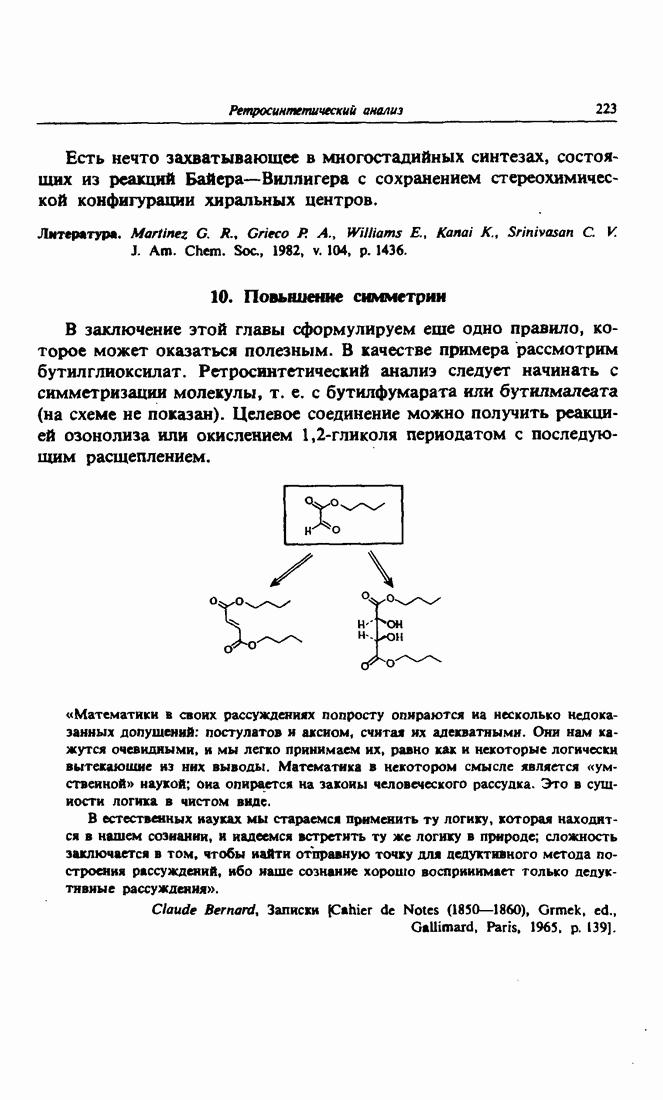
- 10. Повышение симметрии
- ПОСЛЕСЛОВИЕ