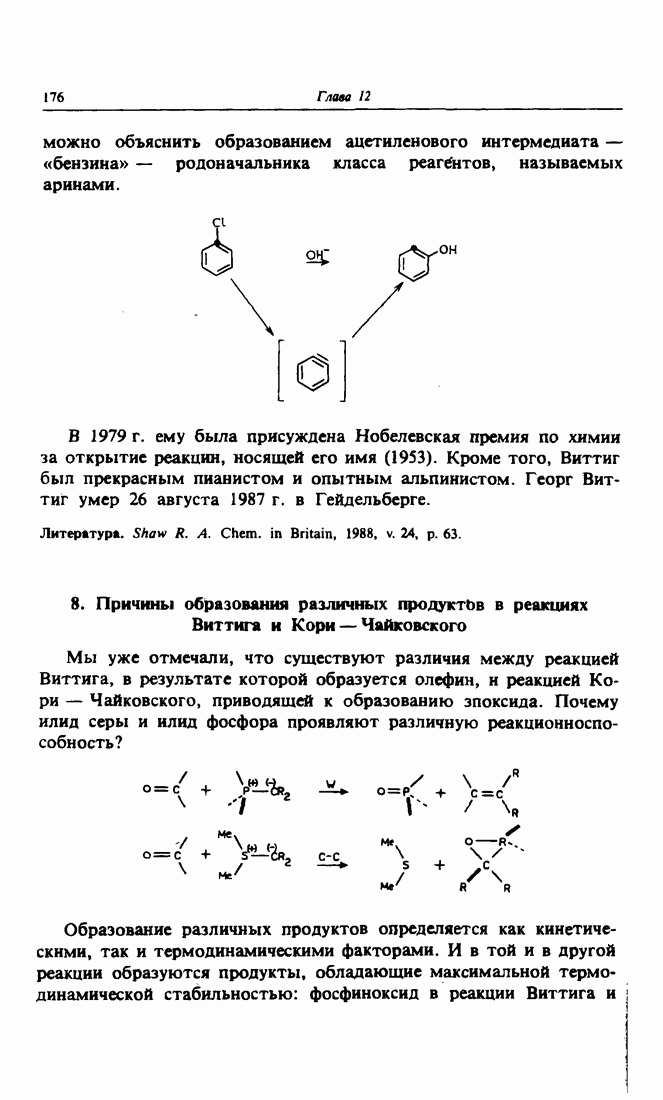
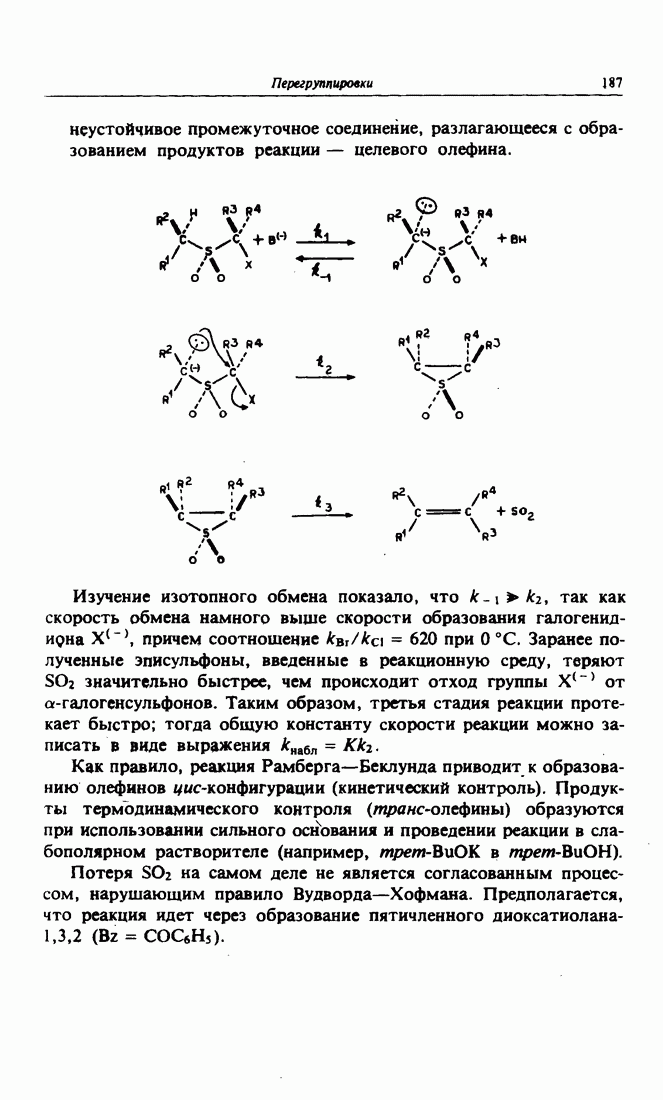
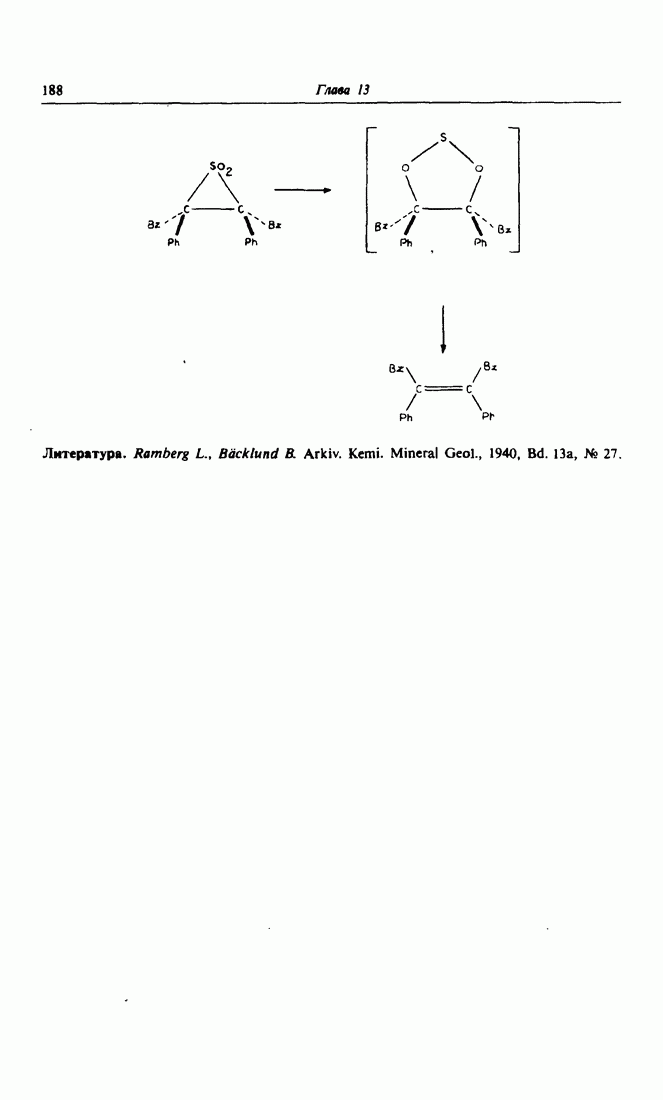
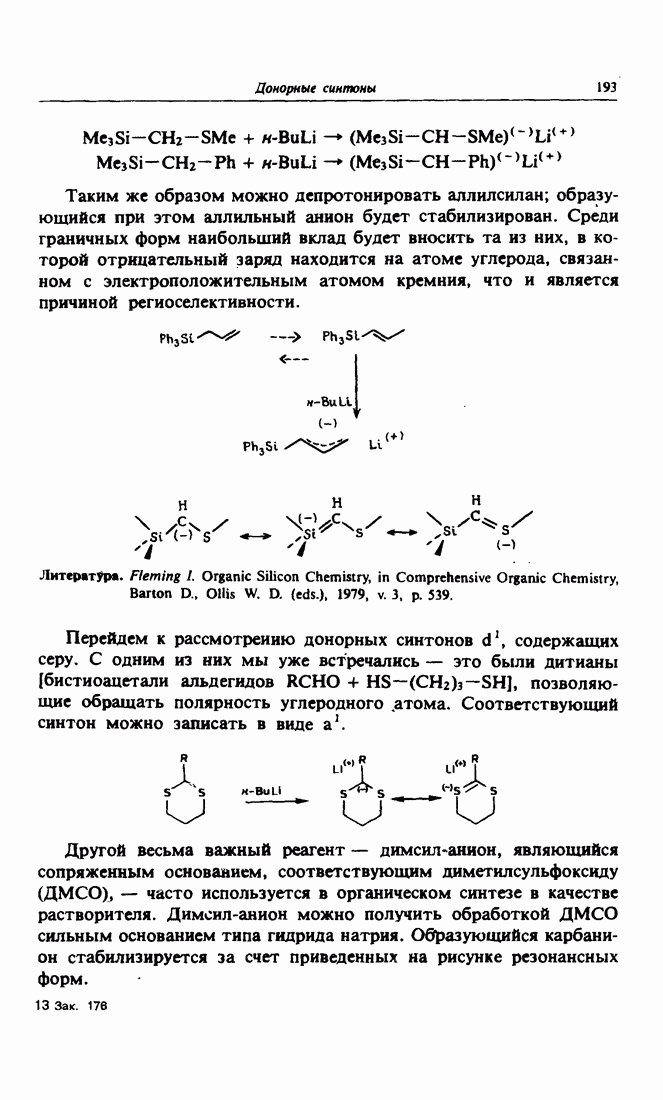
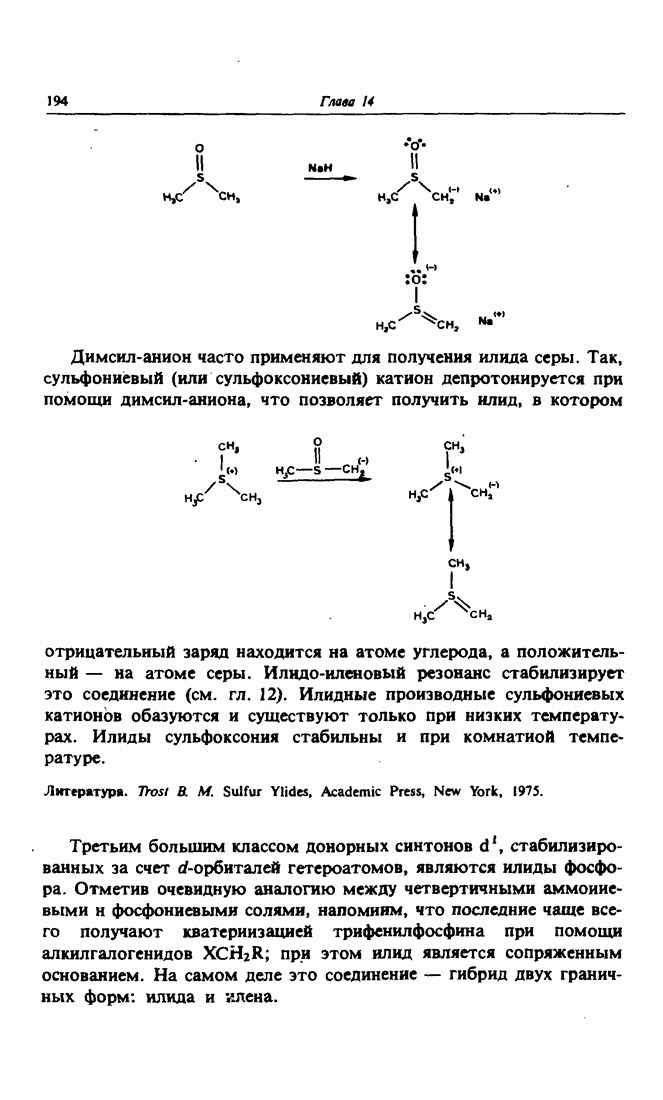
| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
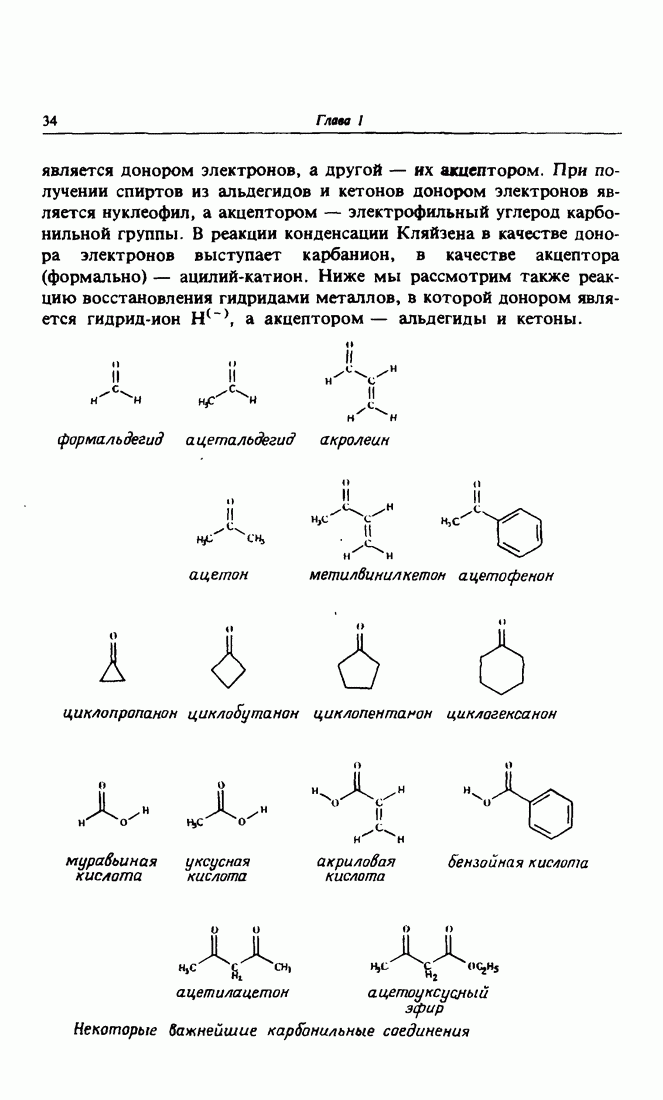
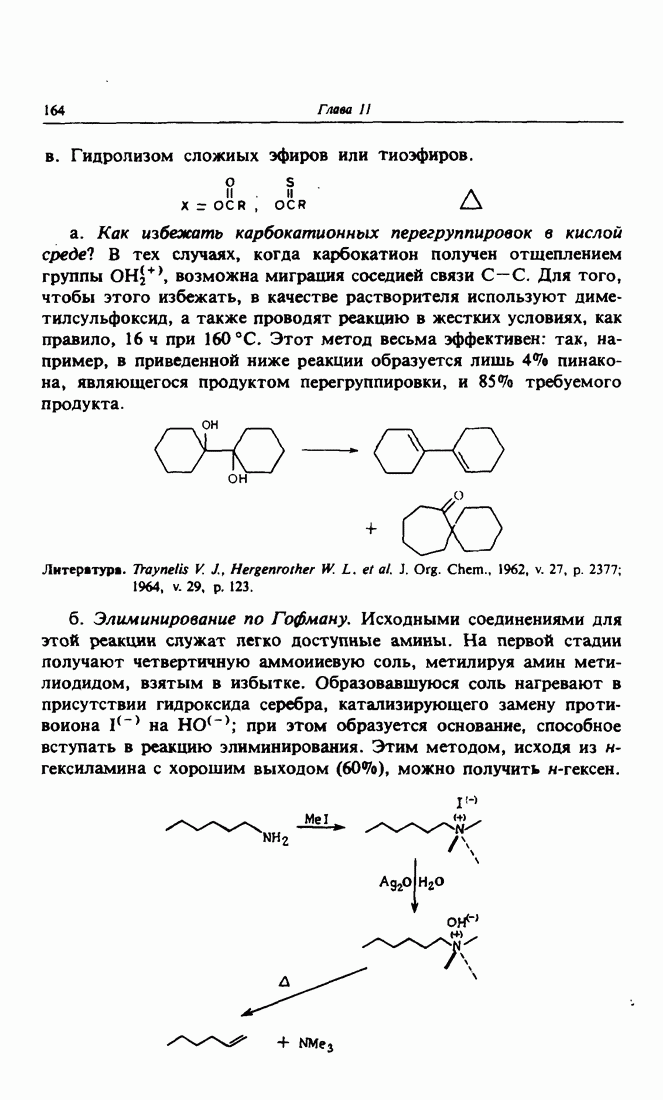
Глава 3. КАРБОНИЛЬНАЯ ГРУППА. АЛЬДОЛЬНАЯ КОНДЕНСАЦИЯ
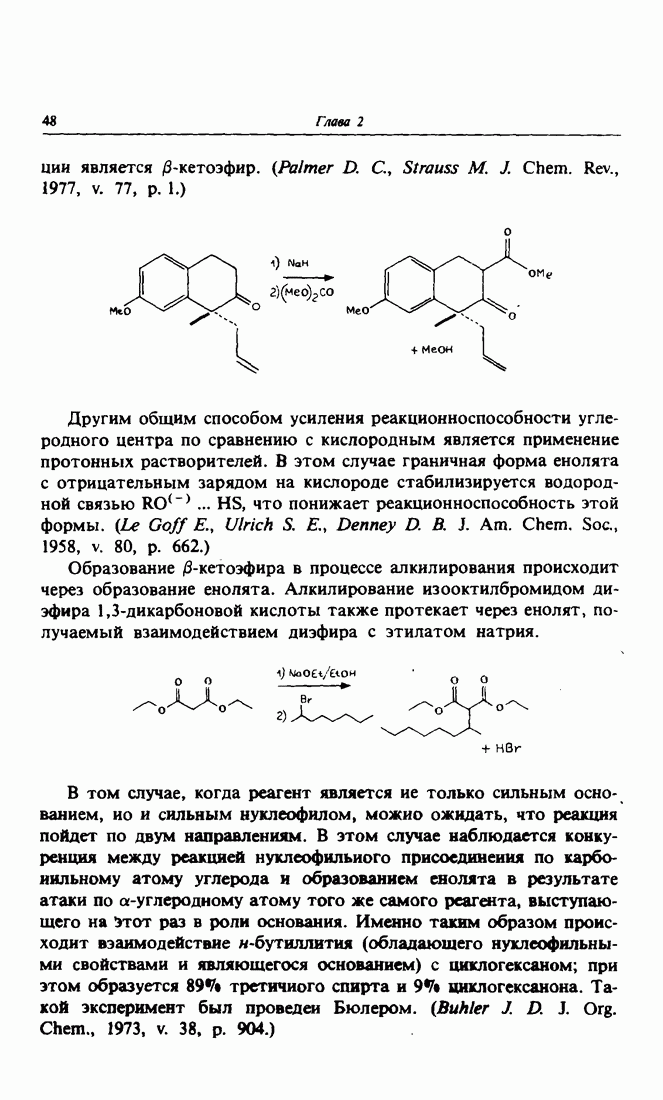
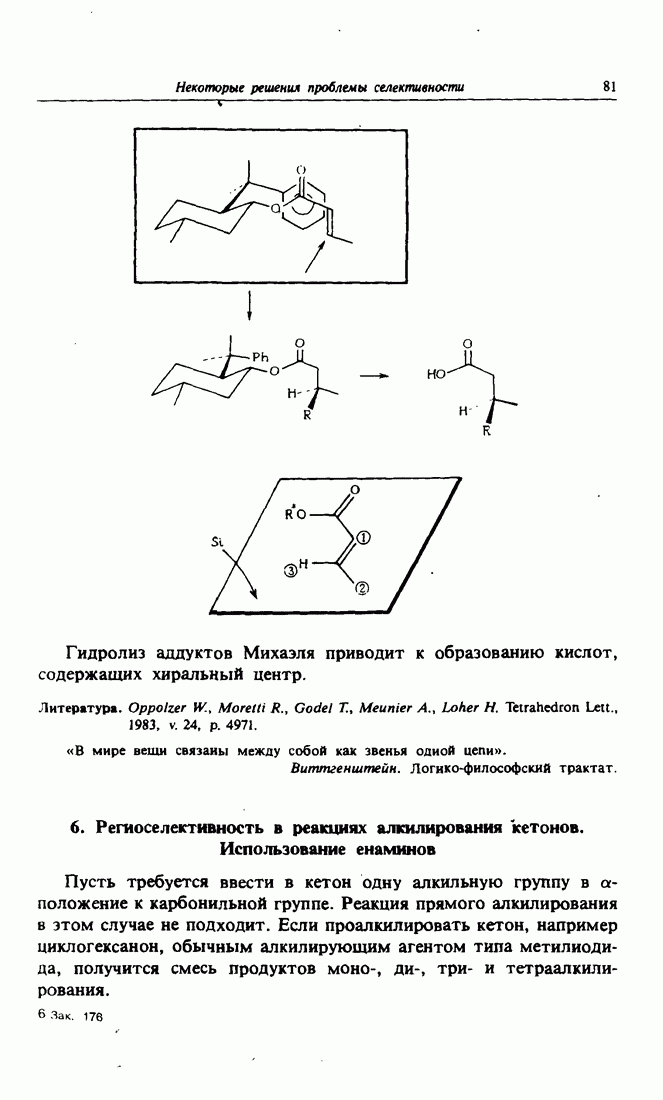
Реакция присоединения енолят-иона в качестве донора к электро-фильному атому углерода карбонильной группы, представляющему собой акцептор, называется альдольной конденсацией. Это третий тип реакций, позволяющих получать новые углерод-углеродные связи. Основное достоинство этого метода состоит в простоте его осуществления, так как для получения енолята карбонильное соединение достаточно обработать основанием, а главный недостаток — в его невысокой селективности: так, например, енолят может реагировать с карбонильным соединением, из которого он был получен.
В данной главе основное внимание уделяется методам контроля за реакцией альдольной конденсации, позволяющим проводить ее селективно.
1. Альдольная конденсация
В альдольной конденсации, как и во многих других реакциях, новая углерод-углеродная связь образуется в результате взаимодействия  и акцептора электронов. Донором является отрицательно заряженный атом углерода енолят-иона, акцептором — несущий частичный положительный заряд атом углерода карбонильной группы.
и акцептора электронов. Донором является отрицательно заряженный атом углерода енолят-иона, акцептором — несущий частичный положительный заряд атом углерода карбонильной группы.

В положениях 1 и 3 образующегося аддукта всегда присутствуют кислородсодержащие функциональные группы — кетонная и спиртовая. Таким образом, реакция альдольной конденсации может служить методом получения цепочки типа 
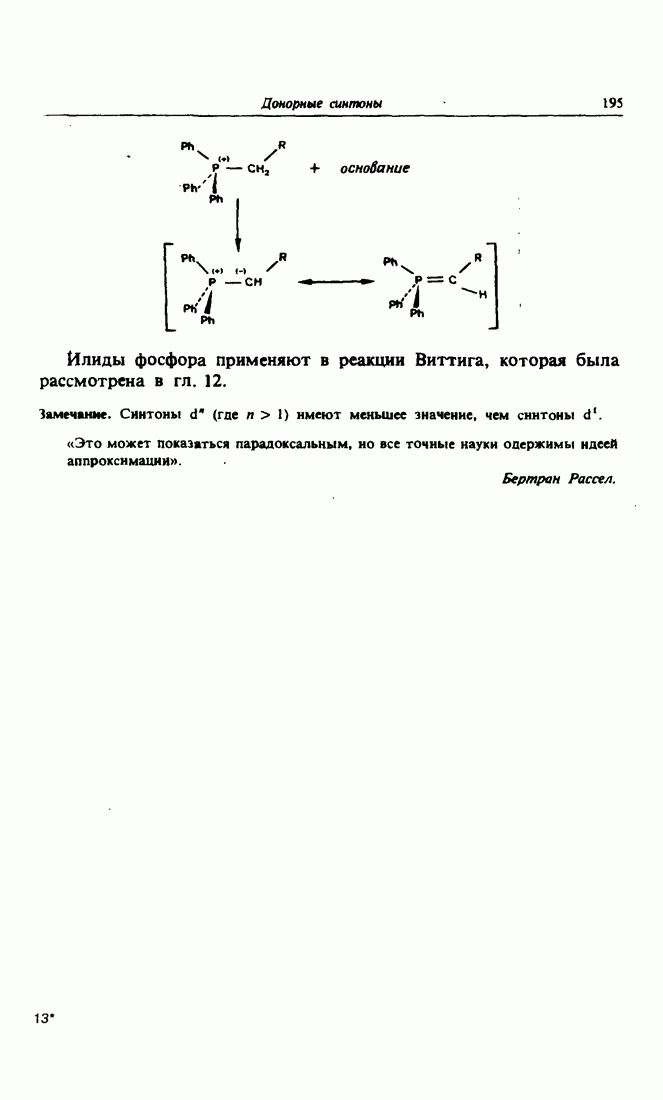
Альдольная конденсация катализируется основанием, которое необходимо для отрыва от кетона протона, в результате чего образуется енолят-ион — основание, сопряженное с кетоном.

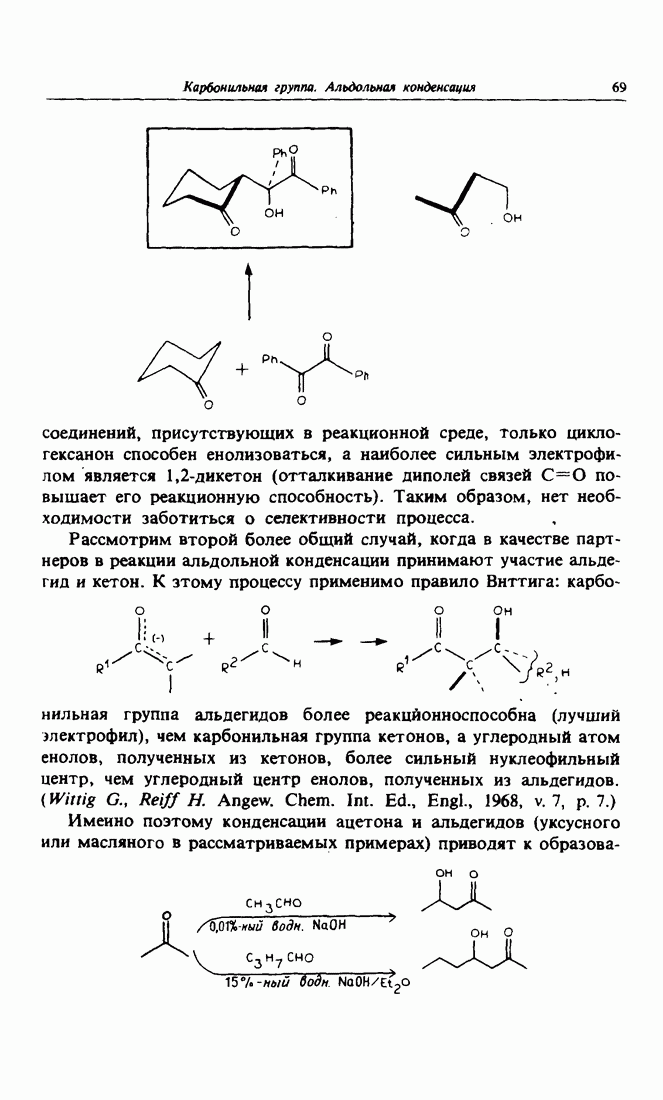
Чтобы в процессе реакции не допустить обмена ролями между донором и акцептором, часто в качестве акцептора используют альдегид  Альдегиды являются лучшими электрофилами, чем кетоны. Таким образом пытаются избежать возможного взаимодействия енолят-иона с кетоном, служившим исходным соединением для его получения.
Альдегиды являются лучшими электрофилами, чем кетоны. Таким образом пытаются избежать возможного взаимодействия енолят-иона с кетоном, служившим исходным соединением для его получения.
В результате взаимодействия енолят-иона, полученного из кетона  и альдегида RCHO образуются четыре диастереоизомера, так как оба асимметрических атома углерода участвуют в образовании новой углерод-углеродной связи. Два из полученных продуктов реакции являются син-стереоизомерами, а два других —
и альдегида RCHO образуются четыре диастереоизомера, так как оба асимметрических атома углерода участвуют в образовании новой углерод-углеродной связи. Два из полученных продуктов реакции являются син-стереоизомерами, а два других —  -стереоизомерами. Существуют различные способы селективного получения тех или других диастереоизомеров; так, например, часто используют вспомогательный хиральных центр
-стереоизомерами. Существуют различные способы селективного получения тех или других диастереоизомеров; так, например, часто используют вспомогательный хиральных центр 

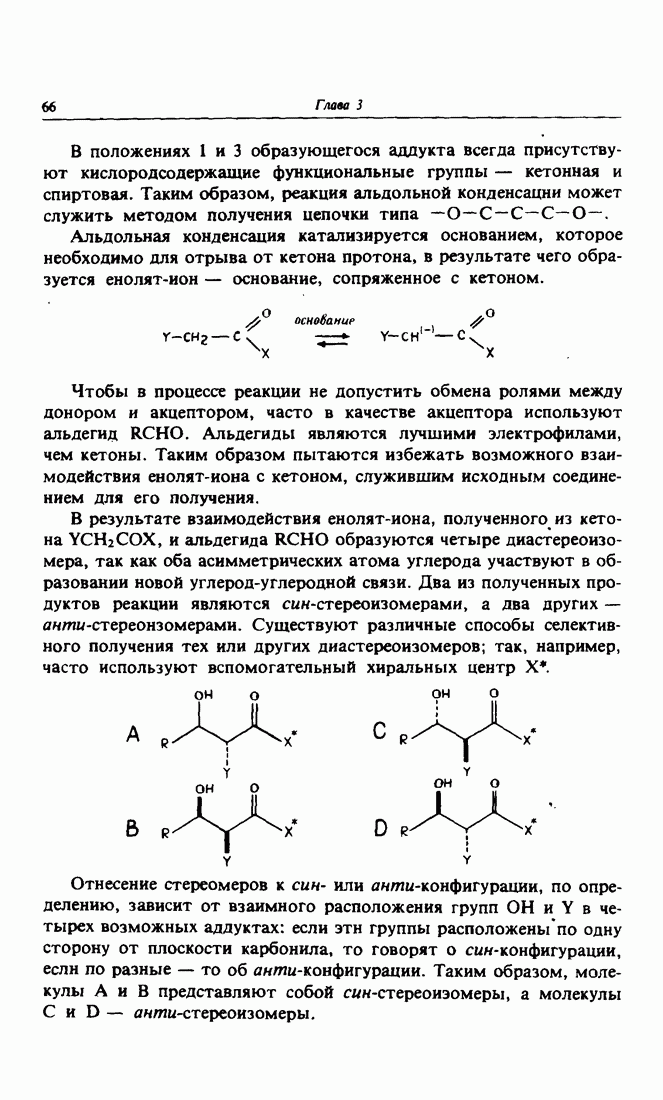
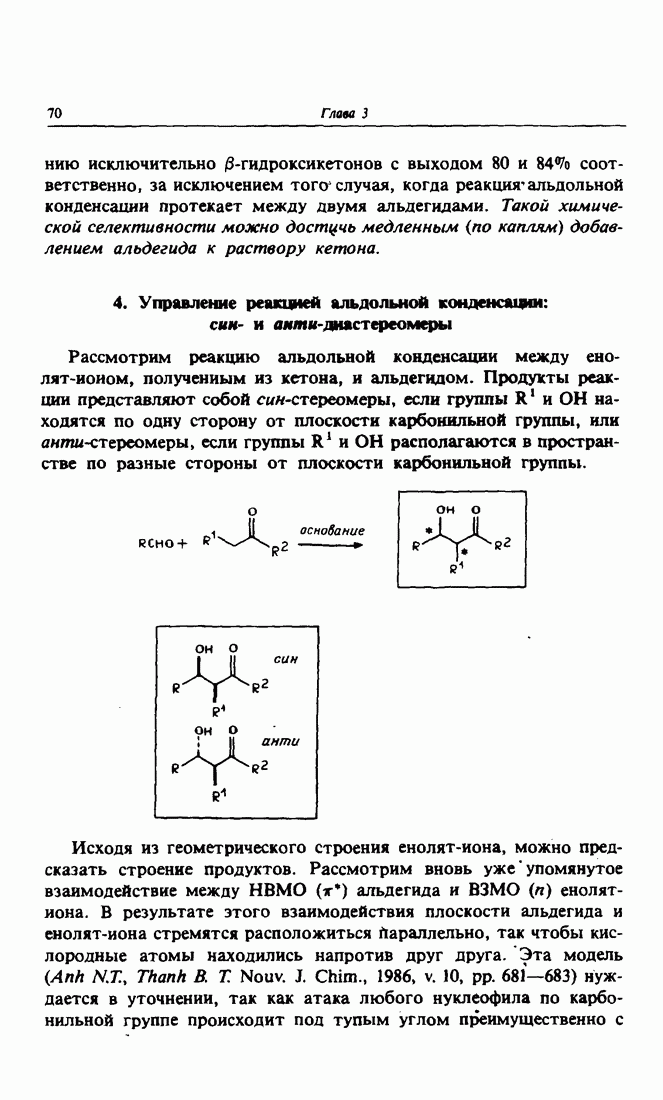
Отнесение стереомеров к син- или анти-конфигурации, по определению, зависит от взаимного расположения групп  и
и  в четырех возможных аддуктах: если этн группы расположеныпо одну сторону от плоскости карбонила, то говорят о син-конфигурации, если по разные — то об анти-конфигурации. Таким образом, молекулы
в четырех возможных аддуктах: если этн группы расположеныпо одну сторону от плоскости карбонила, то говорят о син-конфигурации, если по разные — то об анти-конфигурации. Таким образом, молекулы  представляют собой син-стереоиэомеры, а молекулы
представляют собой син-стереоиэомеры, а молекулы  анти-стереоизомеры.
анти-стереоизомеры.
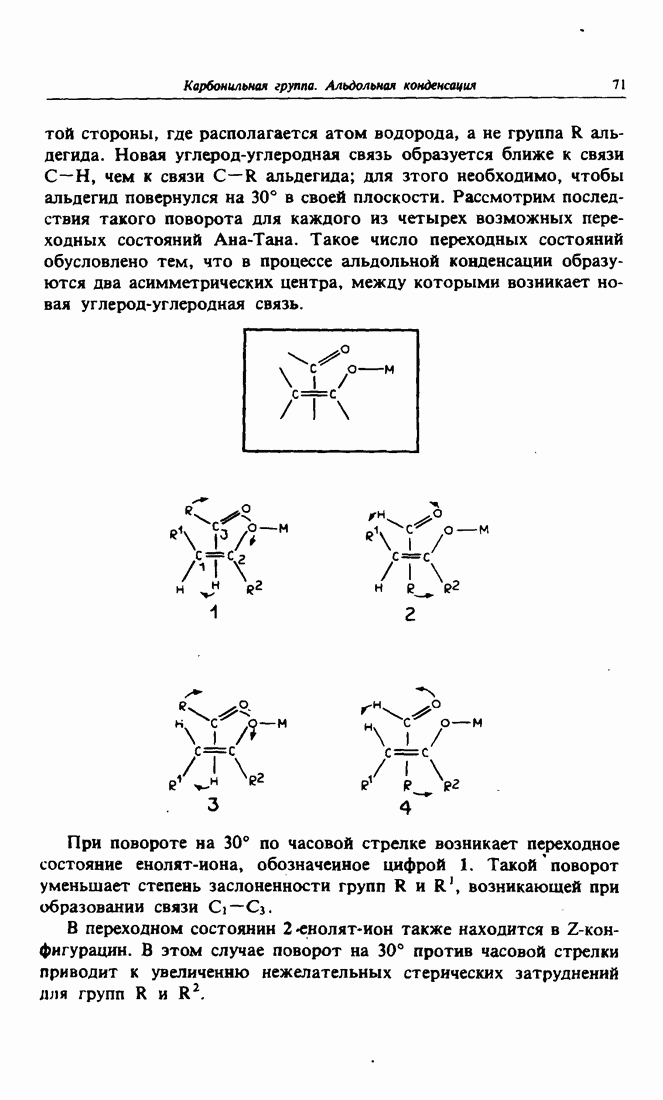
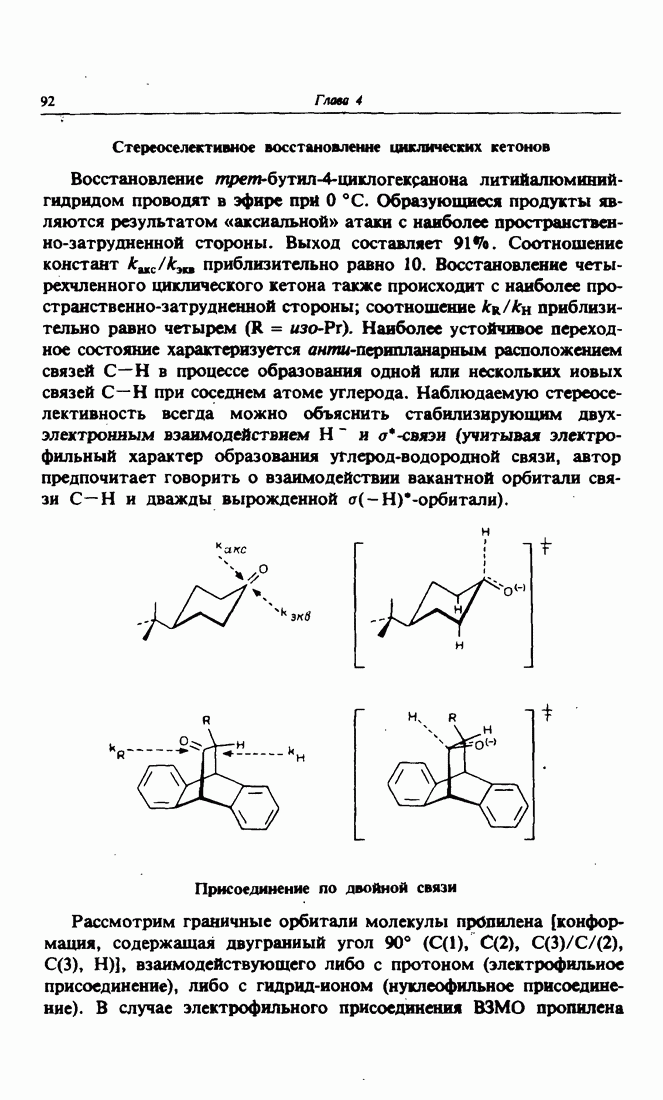
Реакцию альдольиой конденсации можно представить как взаимодействие граничных орбиталей: высшей заполненной молекулярной орбитали енолята и низшей вакантной орбитали альдегида.

Связь образуется в результате перекрывания орбиталей углерода карбонильной группы и двух углеродных атомов енолят-иона, что кажется несколько неожиданным из-за существования между ними электростатического отталкивания, однако присутствие катиона металла — противоиона используемого основания — компенсирует это отталкивание. Кроме того, происходит связывающее перекрывание  -орбиталей двух атомов кислорода. Что касается
-орбиталей двух атомов кислорода. Что касается  -орбитали связи
-орбитали связи  принимающей участие во взаимодействии, то ее весовой коэффициент весьма велик на углероде и достаточно мал на кислороде. Разрыхляющая
принимающей участие во взаимодействии, то ее весовой коэффициент весьма велик на углероде и достаточно мал на кислороде. Разрыхляющая  -орбиталь (енолят-иона) имеет большой весовой коэффициент в противоположной фазе на конечных атомах, а на центральном углеродном атоме этот коэффициент мал.
-орбиталь (енолят-иона) имеет большой весовой коэффициент в противоположной фазе на конечных атомах, а на центральном углеродном атоме этот коэффициент мал.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ РЕДАКТОРА
- ВВЕДЕНИЕ
- 1. Орбитальный и зарядовый контроль
- 2. Жесткие и мягкие кислоты и основания
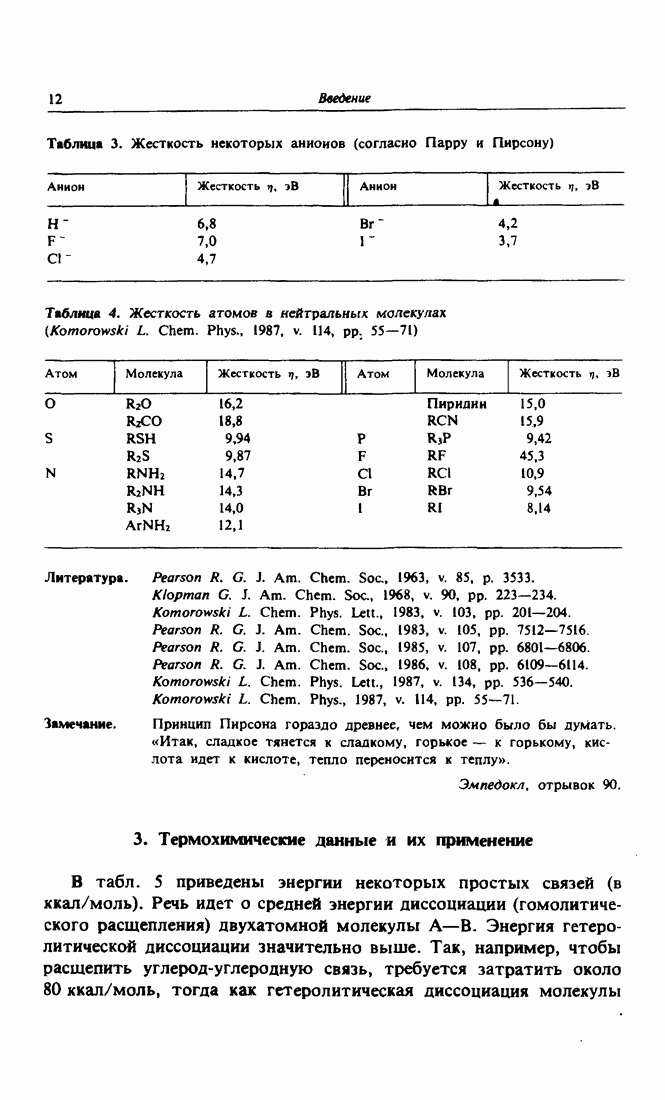
- 3. Термохимические данные и их применение
- Глава 1. КАРБОНИЛЬНАЯ ГРУППА. РЕАКЦИИ ПРИСОЕДИНЕНИЯ И ПРИСОЕДИНЕНИЯ-ФРАГМЕНТАЦИИ
- 1. Карбонильная группа. Простое орбитальное описание
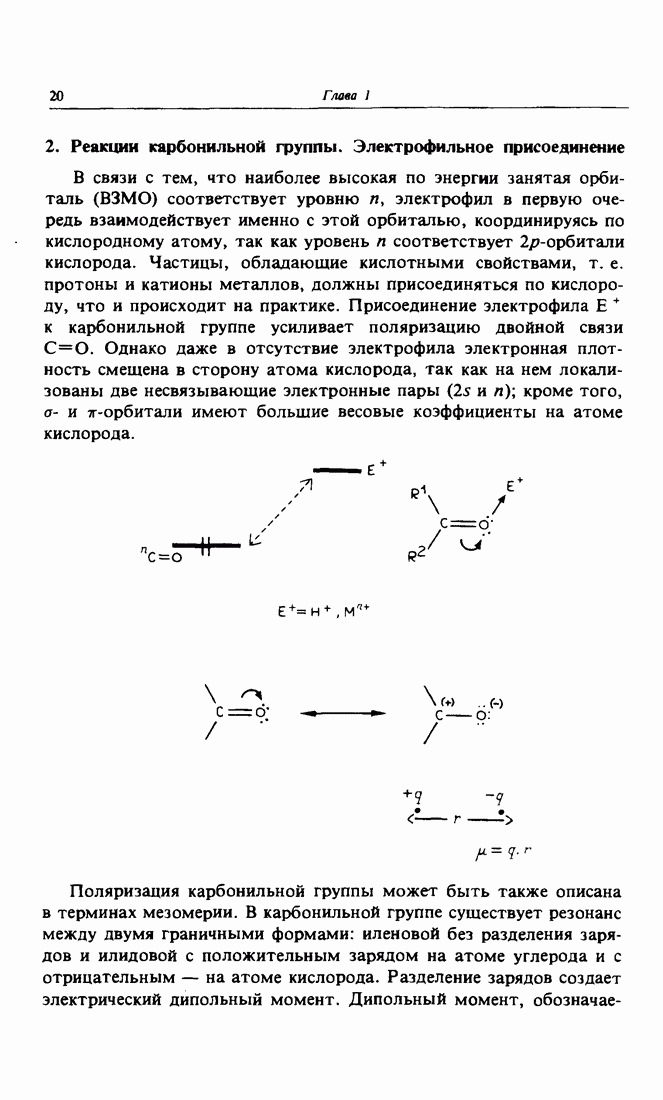
- 2. Реакции карбонильной группы. Электрофильное присоединение
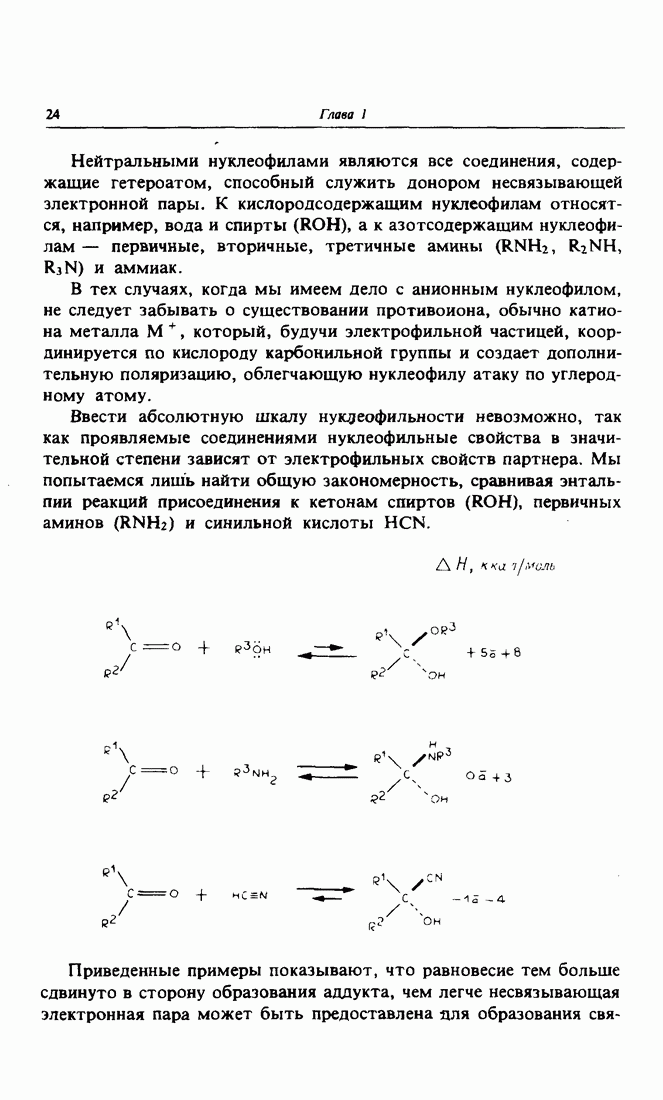
- 3. Основность и нуклеофильность
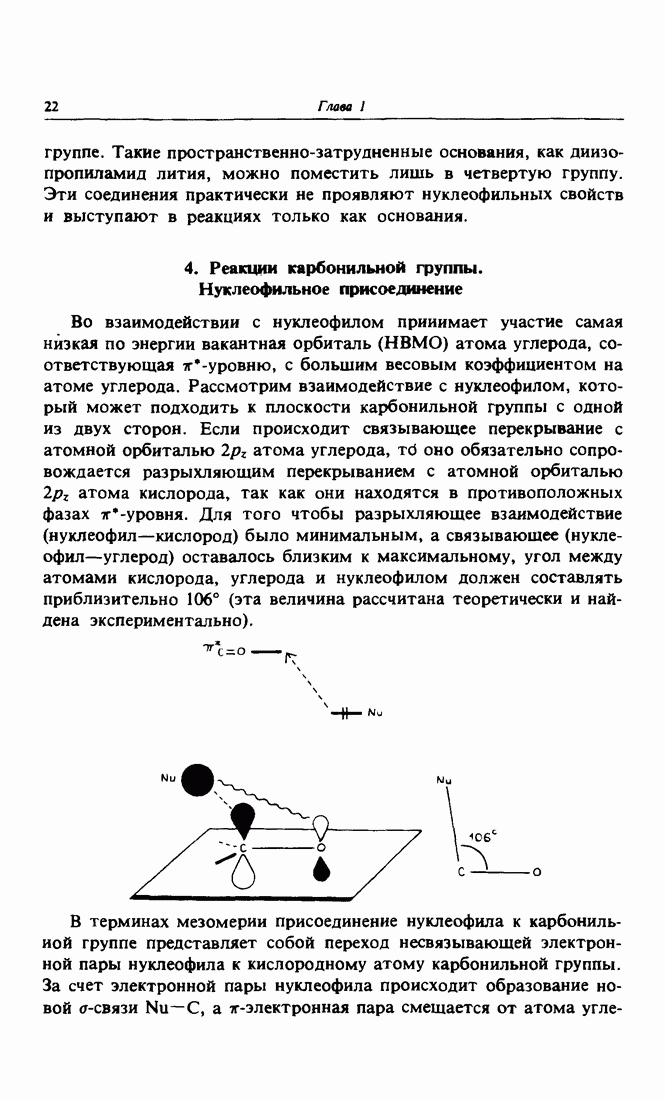
- 4 Реакции карбонильной группы. Нуклеофильное присоединение
- 5. Защита и регенерация
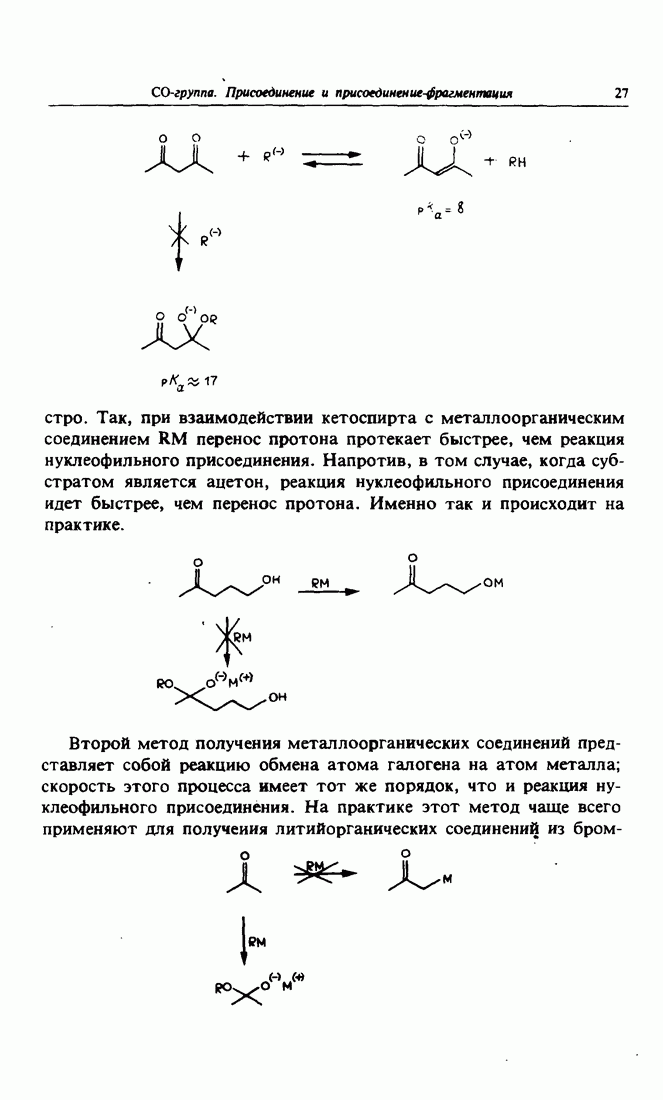
- 6. Получение различных металлоорганических производных
- 7. Активированная метиленовая группа
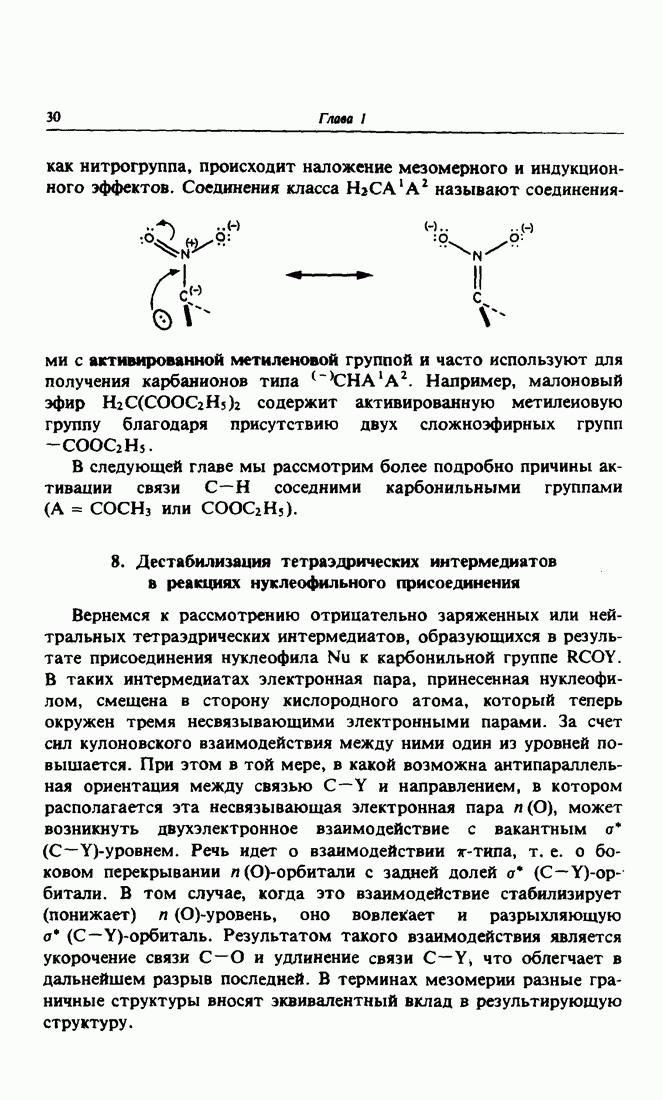
- 8. Дестабилизация тетраэдрических интермедиатов в реакциях нуклеофильного присоединения
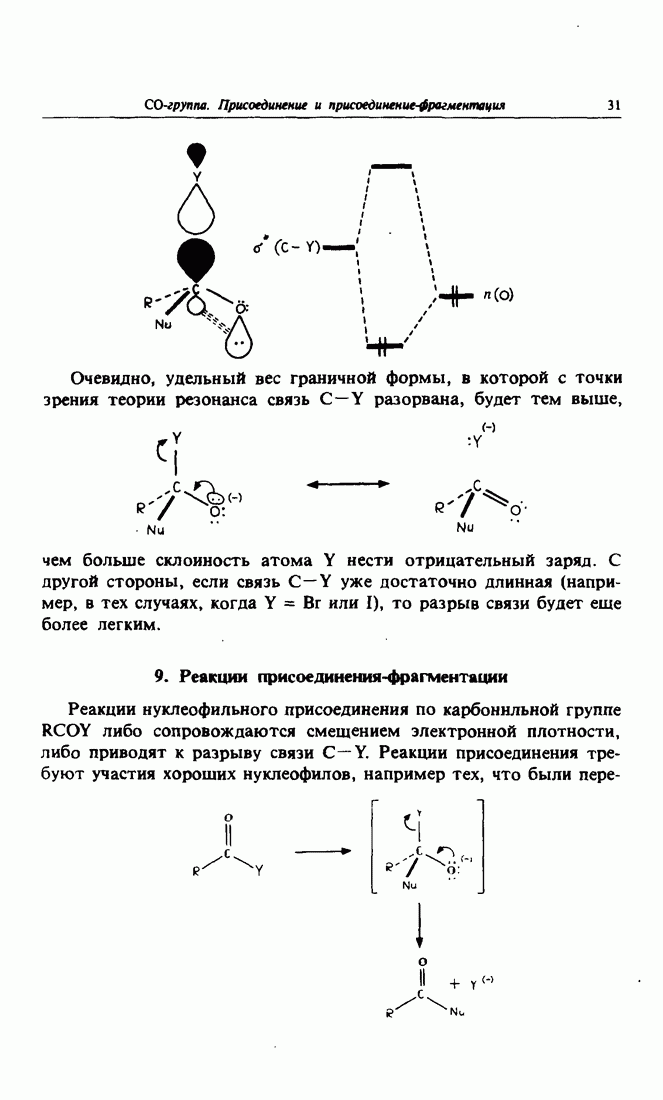
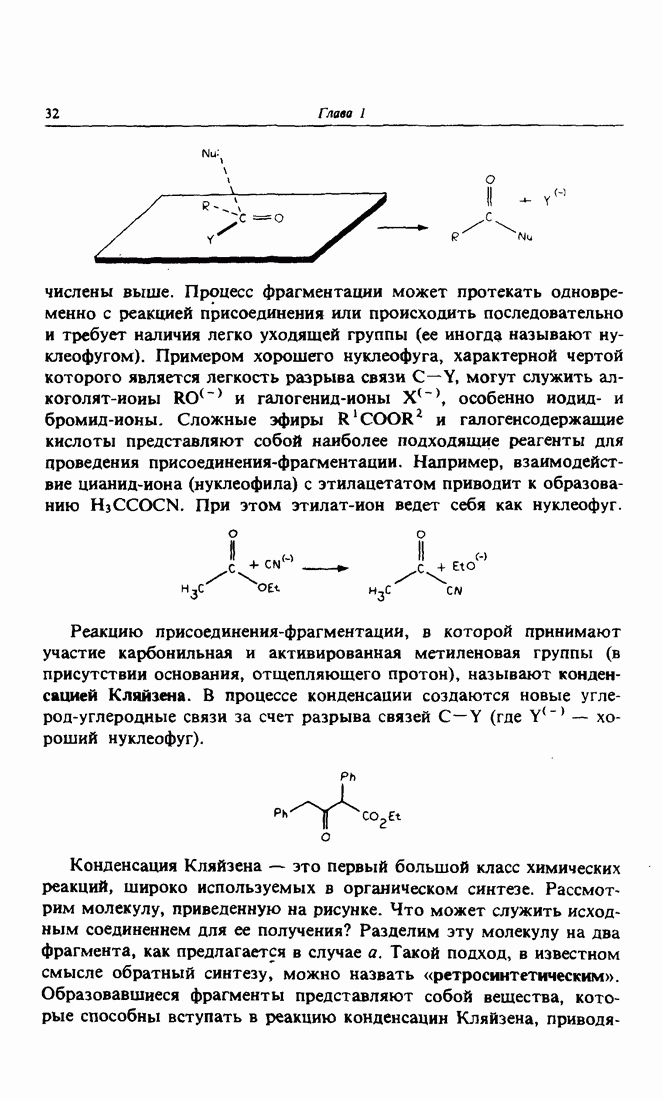
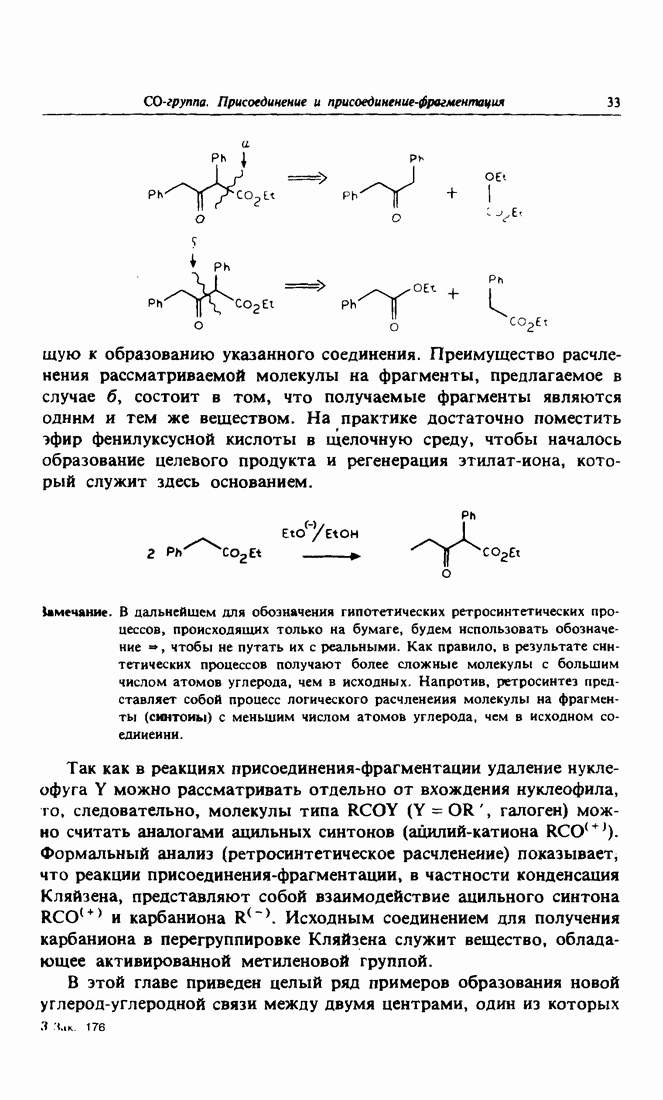
- 9. Реакции присоединения-фрагментации
- 10. Восстановление гидридами металлов
- 11. Описание конфигурации асимметрического атома углерода
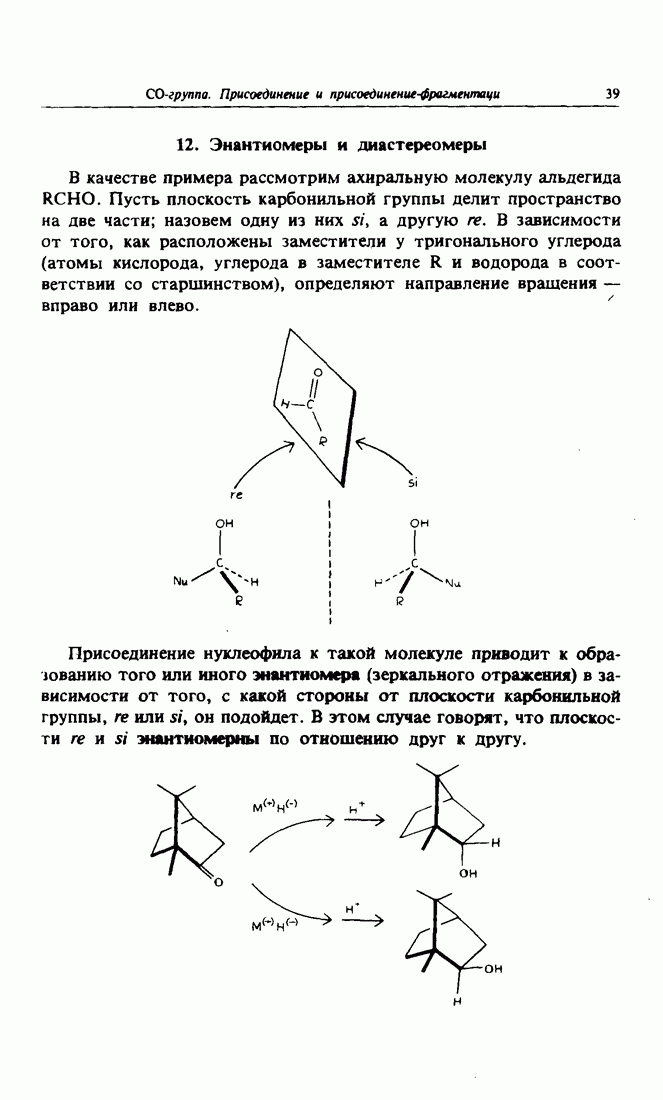
- 12. Энантиомеры и диастереомеры
- 13. Асимметрическая 1,2-индукция
- Глава 2. КАРБОНИЛЬНАЯ ГРУППА. ЕНОЛИЗАЦИЯ. КОНДЕНСАЦИЯ ПО МИХАЭЛЮ
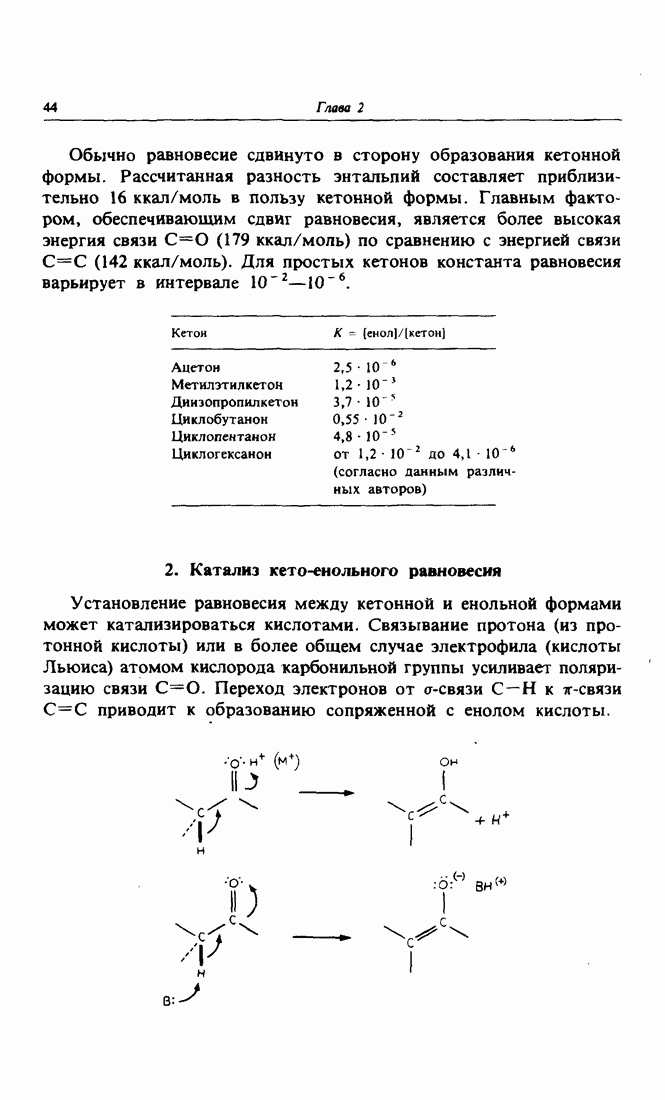
- 1. Кето-енольное равновесие
- 2. Катализ кето-енольного равновесия
- 3. Стереохимия и реакция енолнэации
- 4. Причины ослабления связи Ca-H в кетонах
- 5. Еноляты и их получение
- 6. Эфиры енолов
- 7. Конфигурация енолов и эфиров енолов
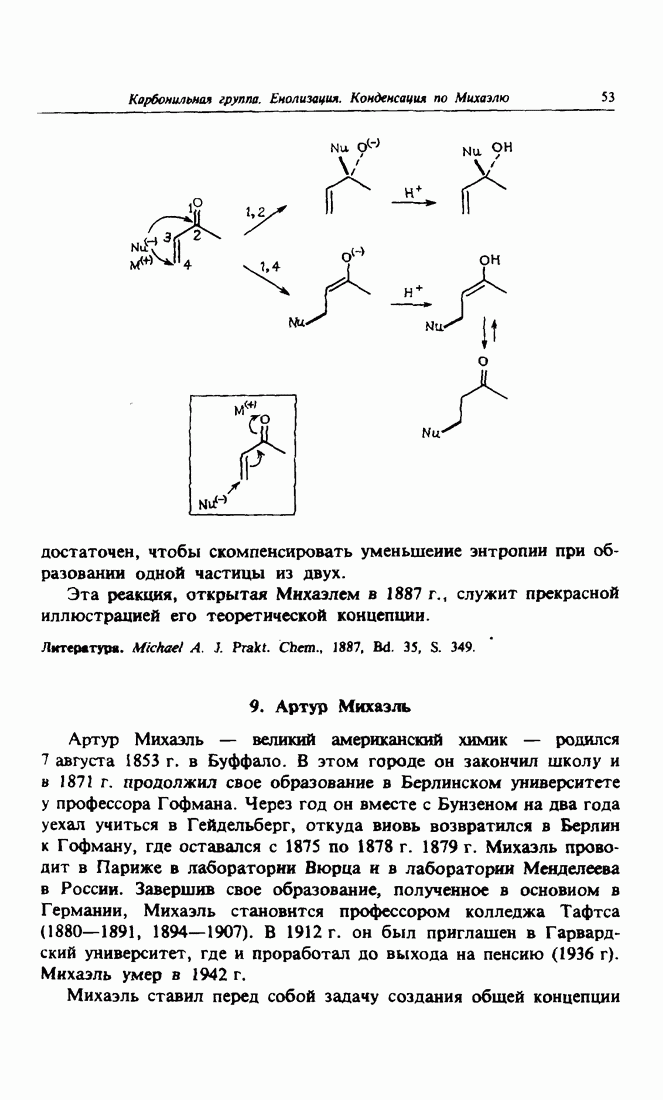
- 8. Реакция Михаэля
- 9. Артур Михаэль
- 10. Региоселективность в реакции Михаэля
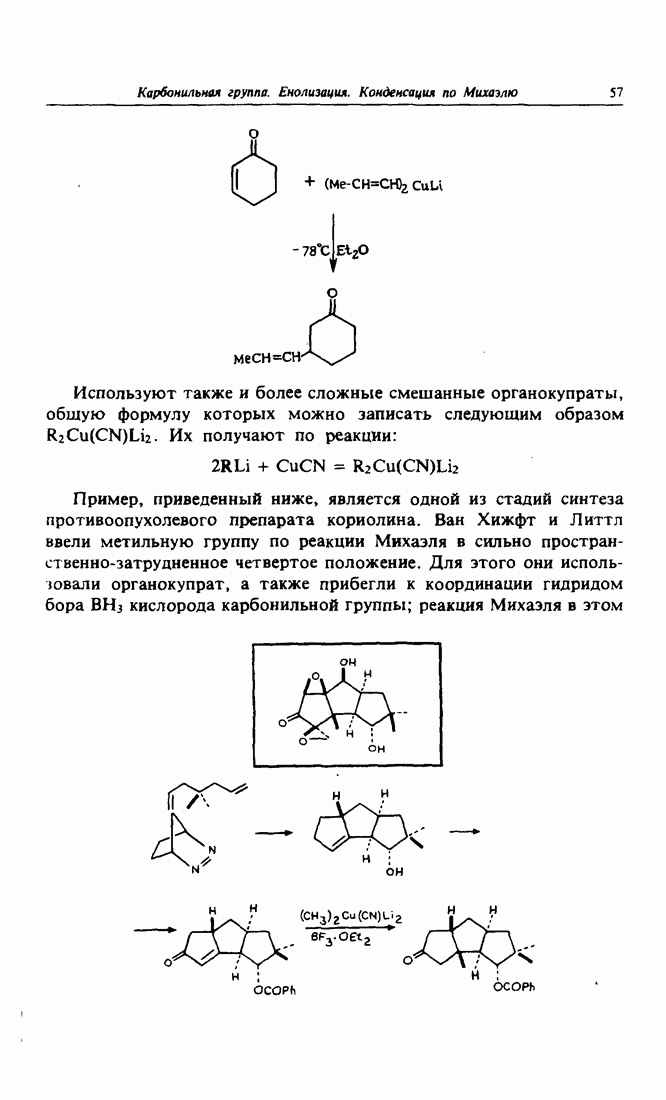
- 11. Применение органокулратов
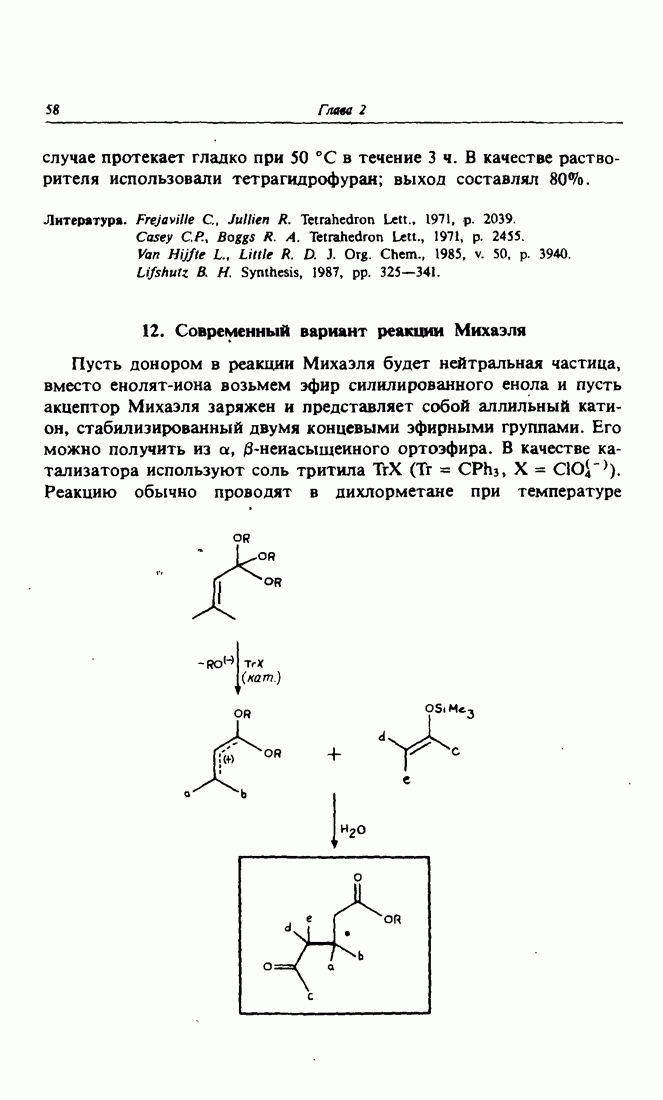
- 12. Современный вариант реакции Михаэля
- 13. Сопряжение или отсутствие сопряжения?
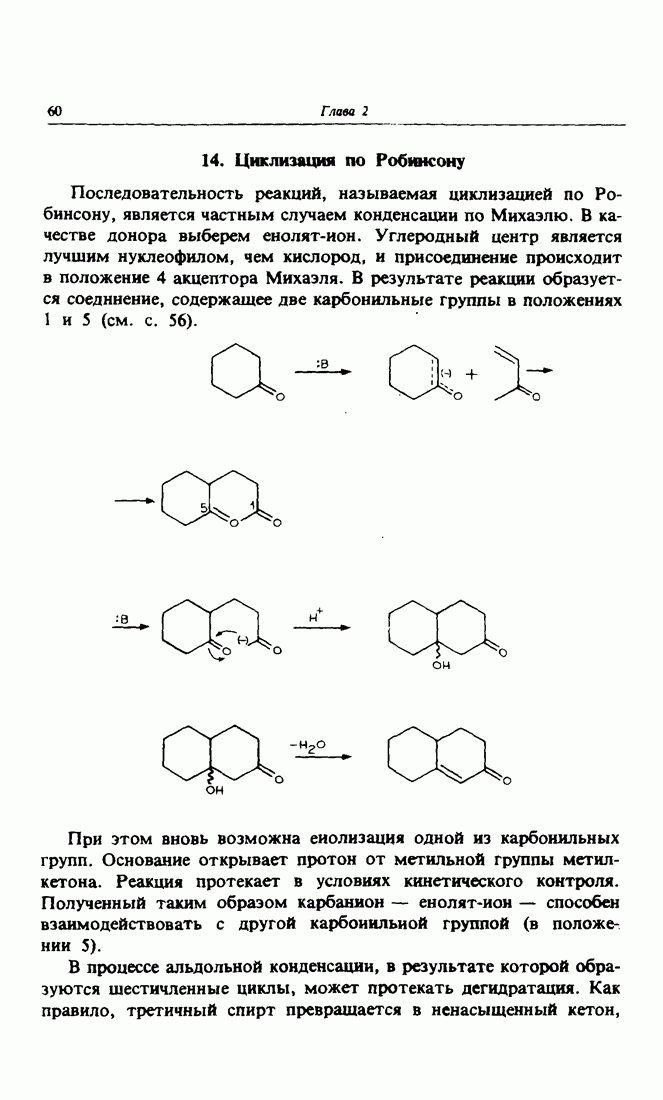
- 14. Циклизация по Робинсону
- 15. Сэр Роберт Робинсон
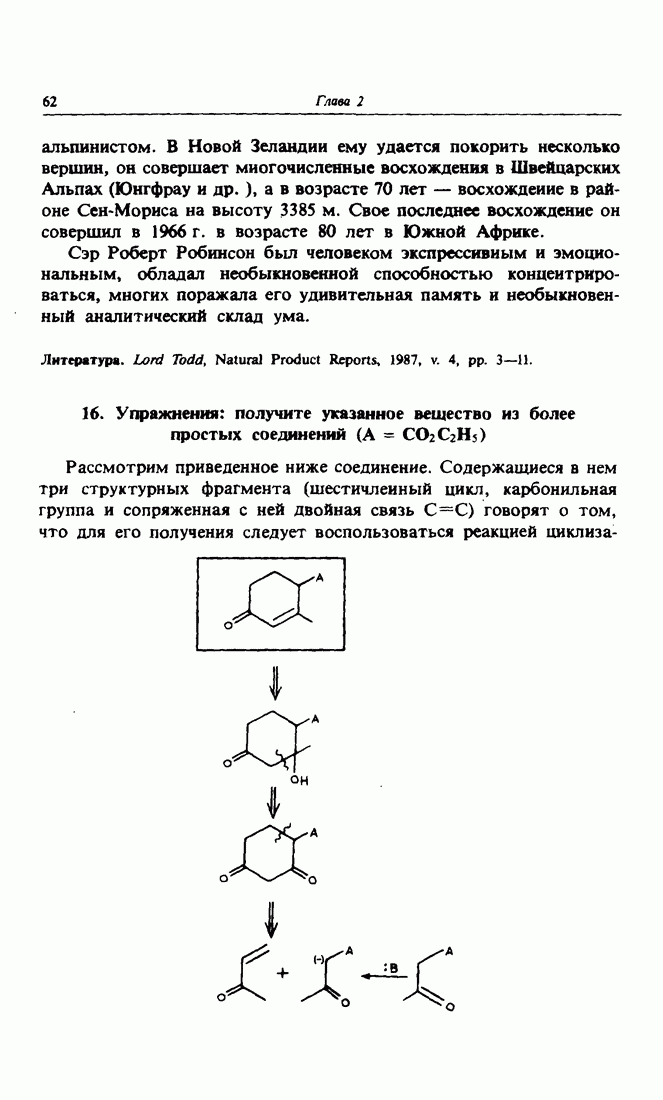
- 16. Упражнения: получите указанное вещество из более простых соединений (A=CO2C2H5)
- Глава 3. КАРБОНИЛЬНАЯ ГРУППА. АЛЬДОЛЬНАЯ КОНДЕНСАЦИЯ
- 2. Устойчивость продуктов альдольиой конденсации
- 3. Управление реакцией альдольной конденсации: доноры и акцепторы
- 4. Управление реакцией альдольной конденсации: син- и анти-диастереомеры
- 5. Стереоселективные реакции альдольной конденсации
- Глава 4. НЕКОТОРЫЕ РЕШЕНИЯ ПРОБЛЕМЫ СЕЛЕКТИВНОСТИ (ХИМИЧЕСКАЯ, РЕГИО- И СТЕРЕОСЕЛЕКТИВНОСТЬ)
- 2. Региоселективность при образовании енолятов
- 3. Селективное получение Е- и Z-енолятов
- 4. Двойной принцип стереоселективности
- 5. Энантиоселективная реакция Михаэля
- 6. Региоселективность в реакциях алкилирования кетонов. Использование енаминов
- 7. Получение хирального центра путем алкилирования енаминов
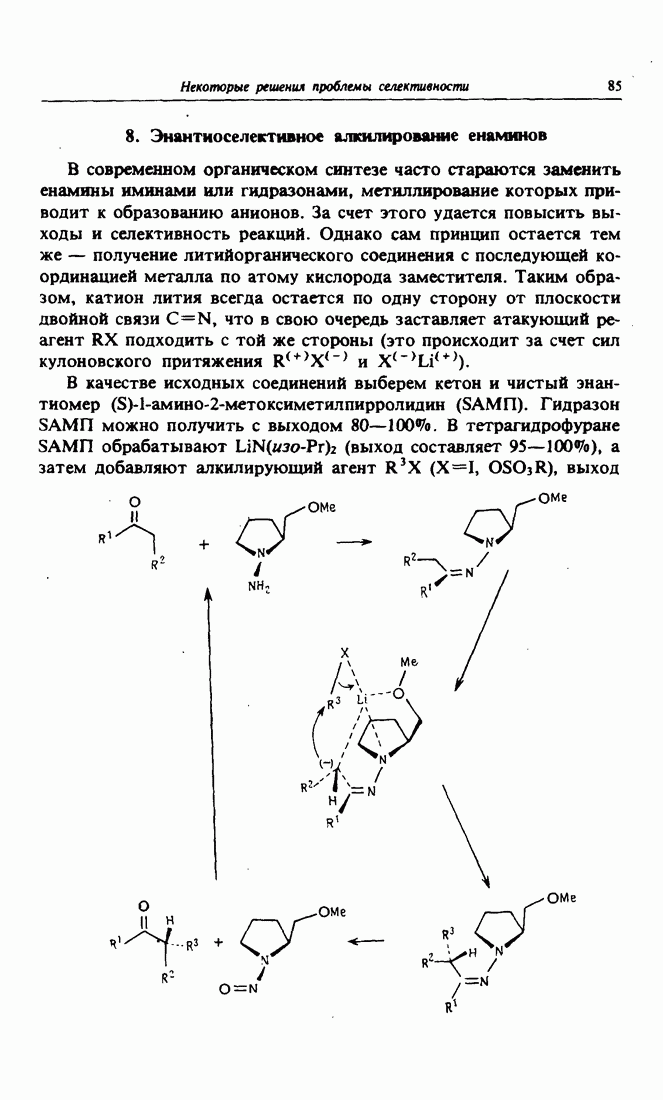
- 8. Энантиоселективное алкилирование енаминов
- 9. Перенос хиральности
- 10. Соотношение между реакционноспособностью и селективностью
- 11. Стереоэлектронный эффект
- 12. Конформации переходного состояния «кресло» и «ванна»
- Глава 5. ЗАЩИТА И РЕГЕНЕРАЦИЯ ФУНКЦИОНАЛЬНЫХ ГРУПП. СПИРТОВАЯ И КАРБОНИЛЬНАЯ ГРУППЫ. ОБРАЩЕНИЕ ПОЛЯРНОСТИ
- 1. Защита карбонильной группы ацетальной
- 2. Защита спиртов. Диметил-трет-бутилсилиловые эфиры
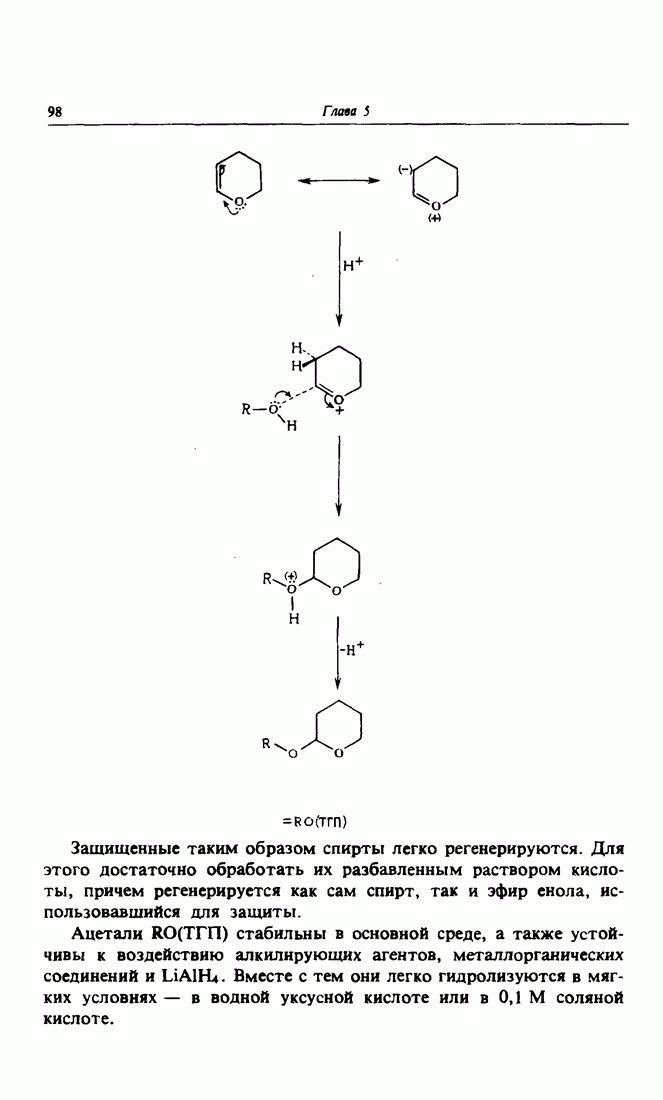
- 3. Защита спиртовых групп при помощи эфиров енолов
- 4. Обращение полярности
- 5. Э. Дж. Кори
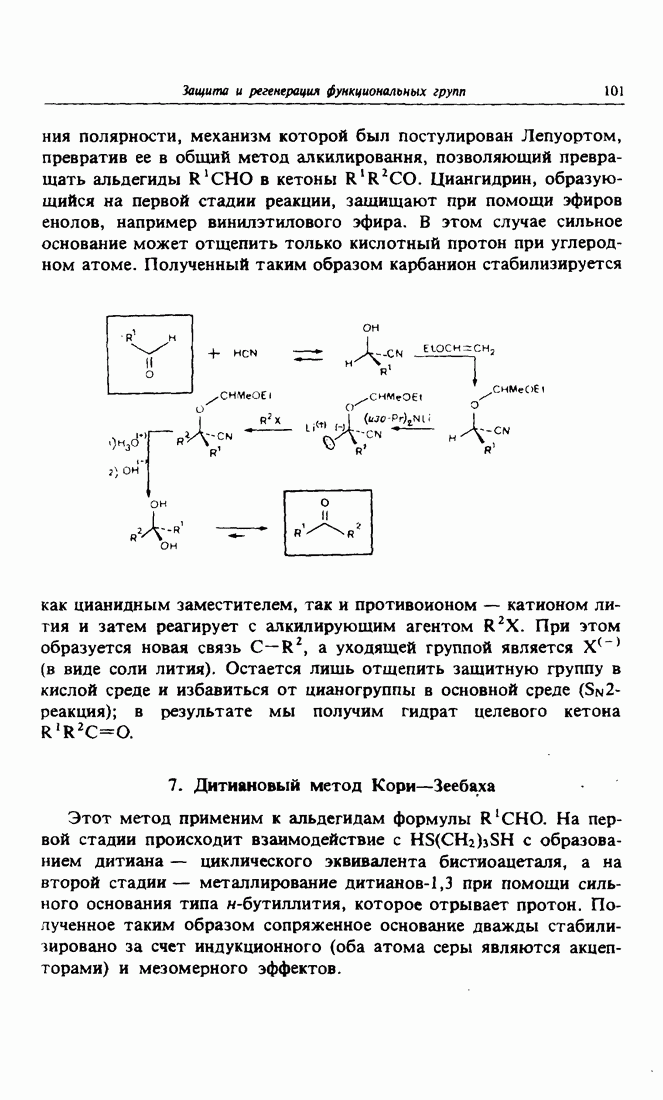
- 6. Инверсия полярности по методу Лепуорта — Шторка
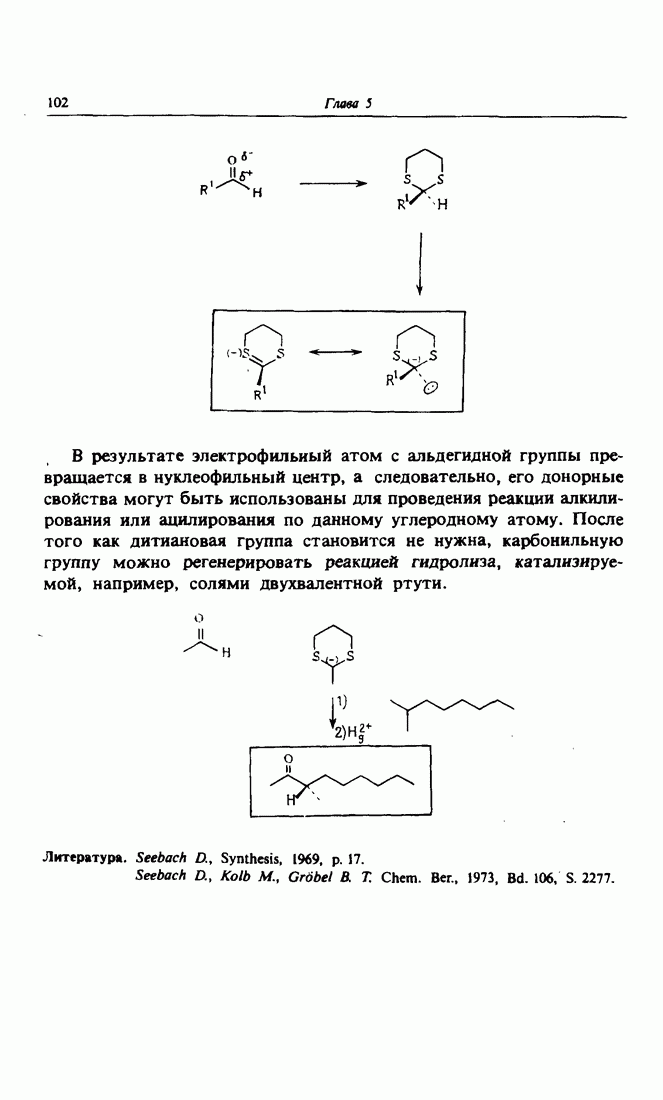
- 7. Дитиановый метод Кори-Зеебаха
- Главе 6. АКТИВАЦИЯ
- 2. Стабилизация конечного состояния
- 3. Дестабилизация начального состояния
- 4. Стабилизация переходного состояния
- Главв 7. ПОСТРОЕНИЕ ЦИКЛОВ
- 2. Региоселективность
- 3. Реакция Дильса — Альдера в условиях обращенного электронного соответствия
- 4. Стереоселективность в реакциях Дильса — Альдера
- 5. Напряжение в циклах
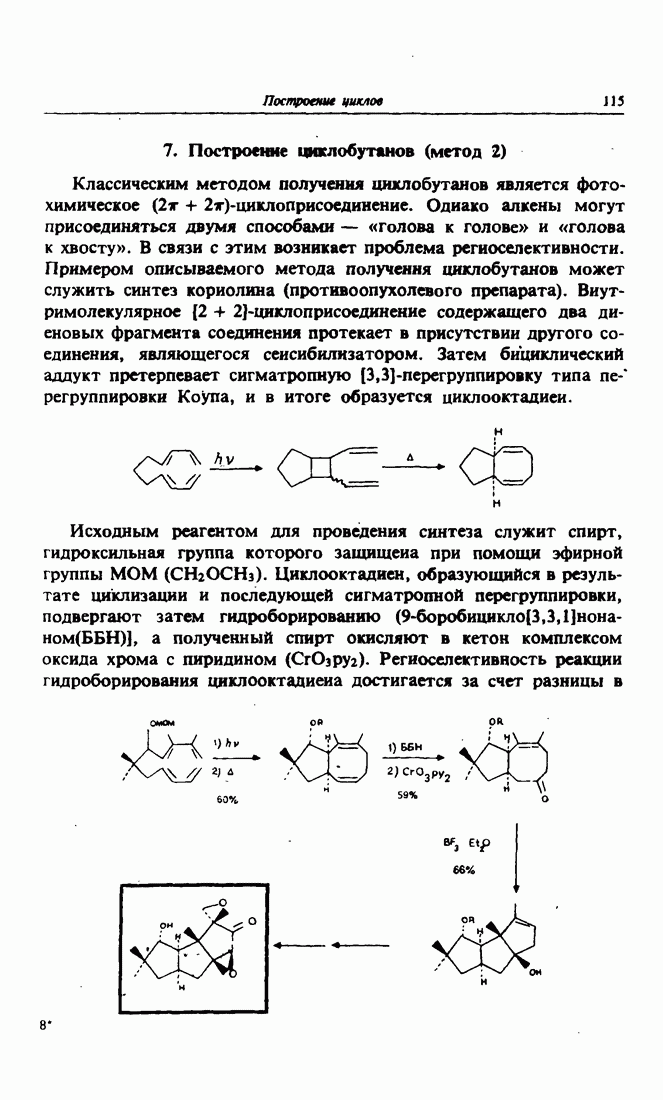
- 6. Построение циклобутанов (метод 1) Термическая димеризация
- 7. Построение циклобутанов (метод 2)
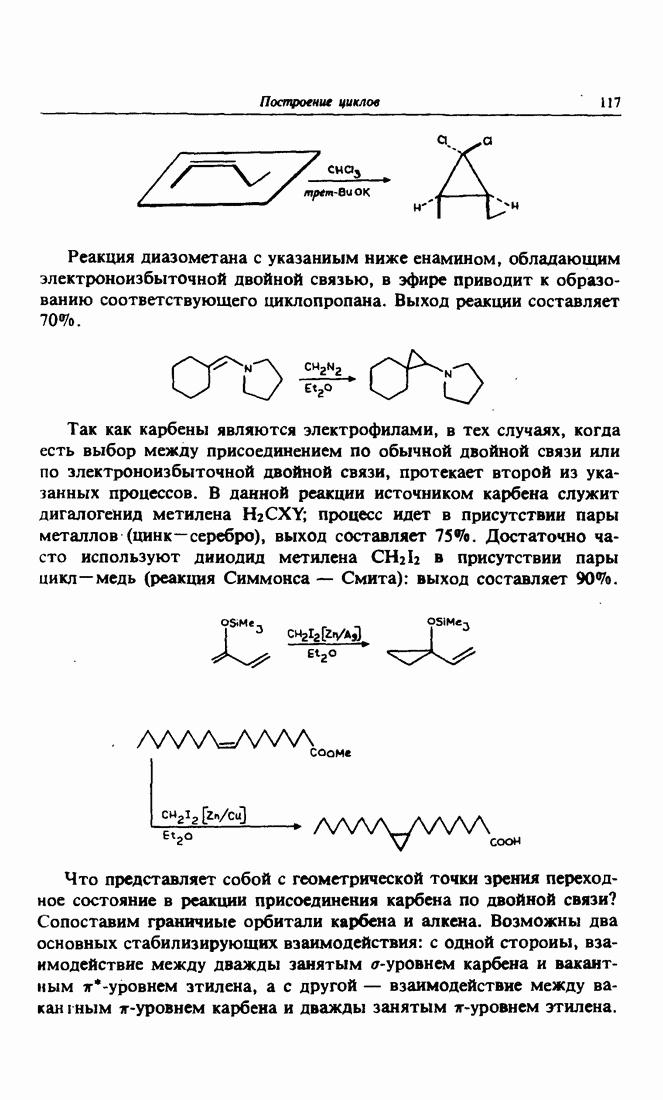
- 8. Синтез циклопропанов. Присоединение карбенов к алкенам
- Глааа 8. ВВЕДЕНИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП. РЕАКЦИИ ЗАМЕЩЕНИЯ
- 2. Соотношение структура — реакционноспособность
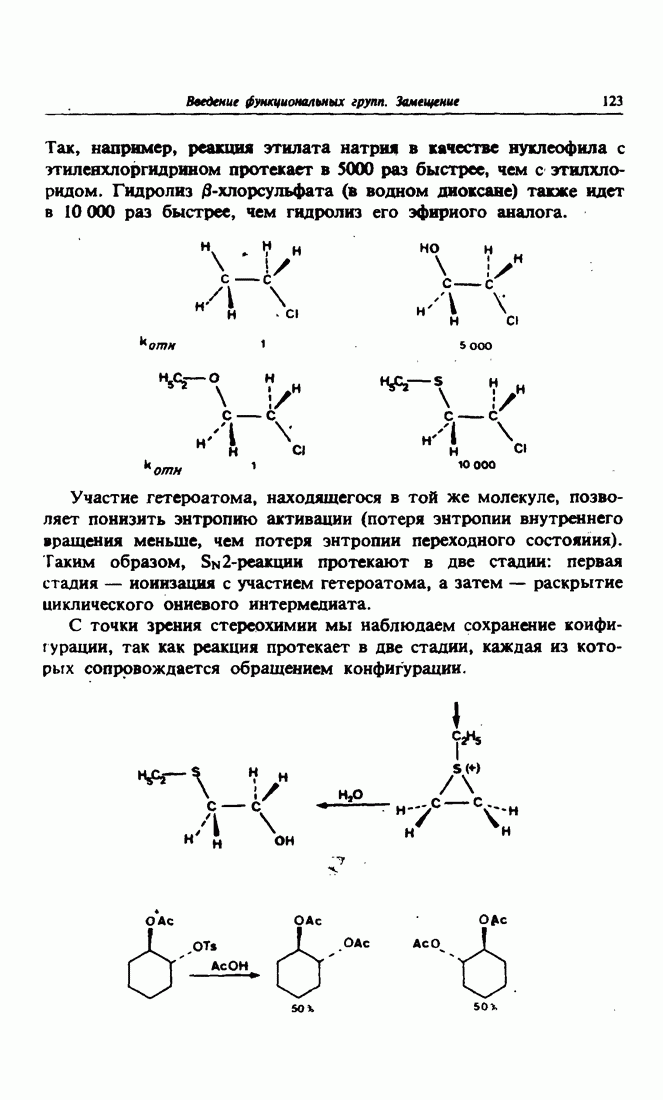
- 3. Участие соседней группы в Sn2-реакциях
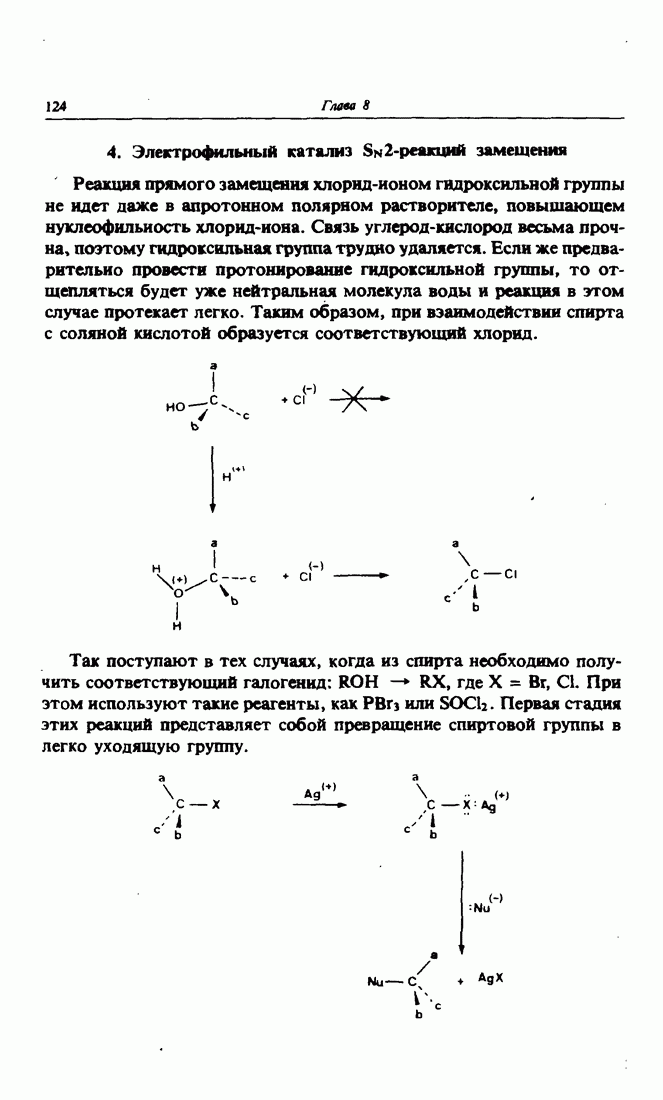
- 4. Электрофильный катализ Sn2-реакций замещения
- 5. Региоселеггивность в реакциях алкилирования
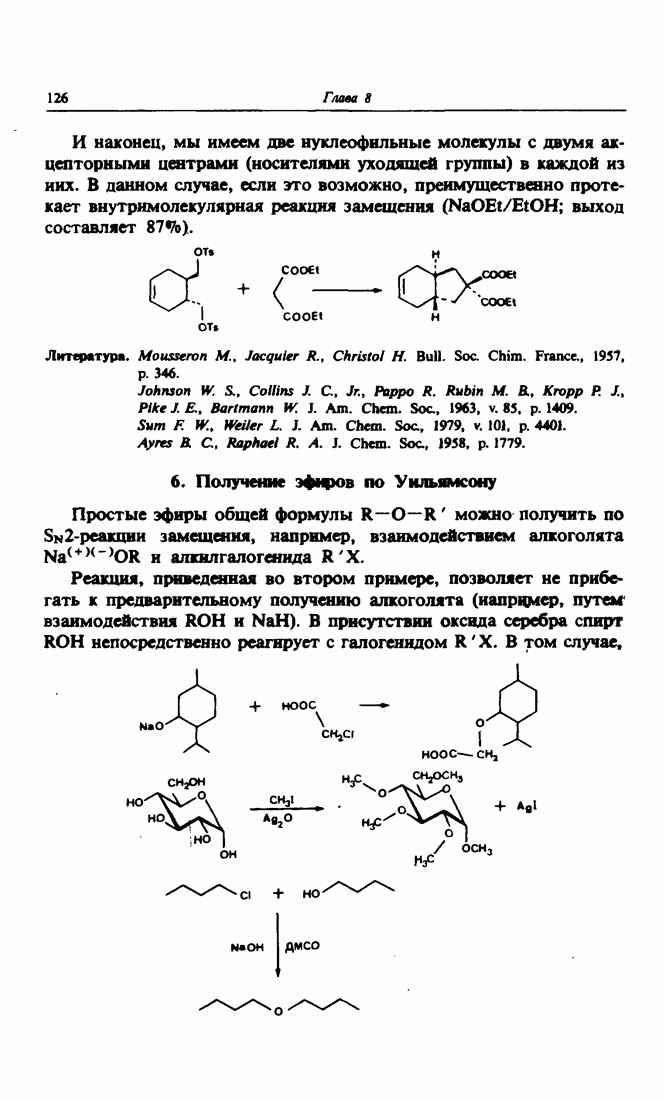
- 6. Получение эфиров по Уильямсону
- 7. К вопросу об обозначениях
- Глава 9. ВВЕДЕНИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП. РЕАКЦИИ ВОССТАНОВЛЕНИЯ
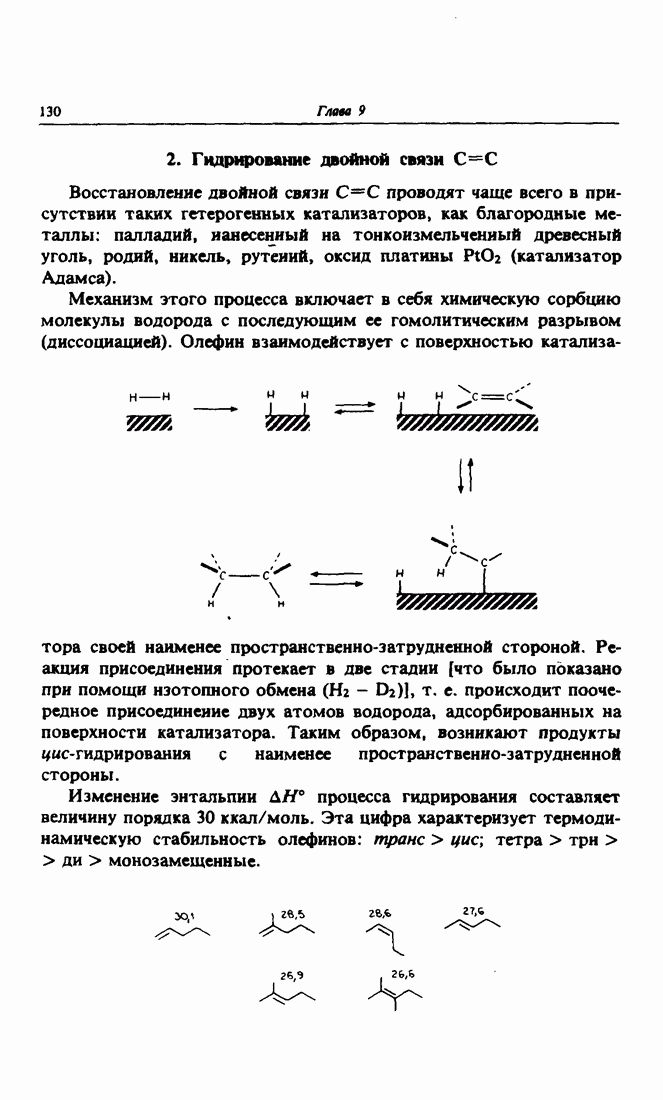
- 2. Гидрирование двойной связи С=С
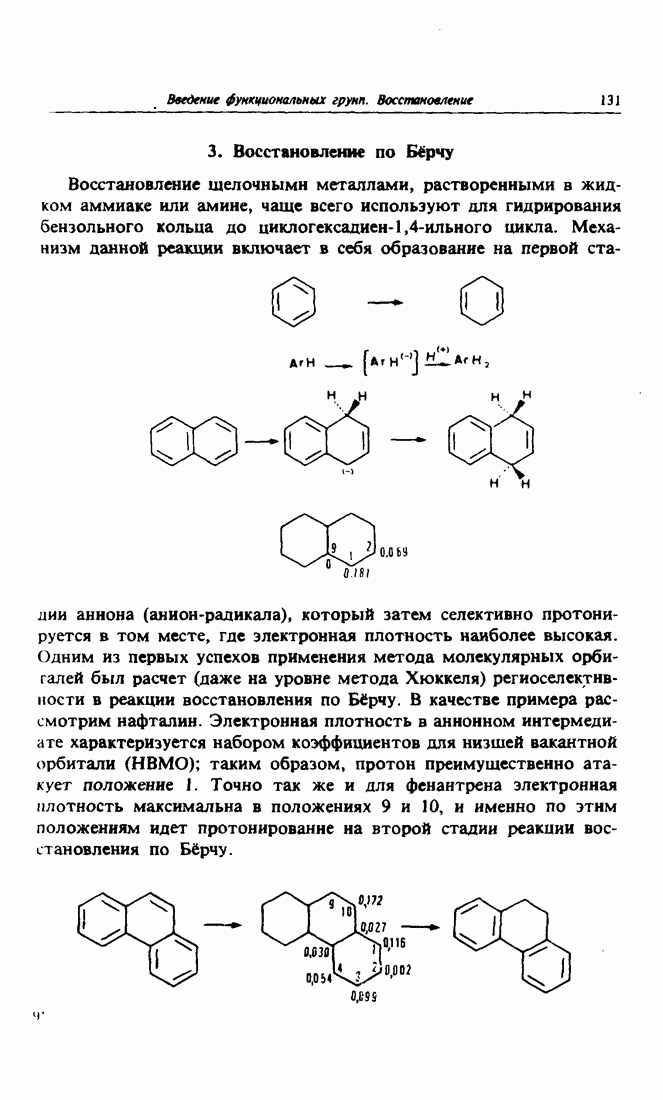
- 3. Восстановление по Бёрчу
- 4. Восстановление карбонильной группы
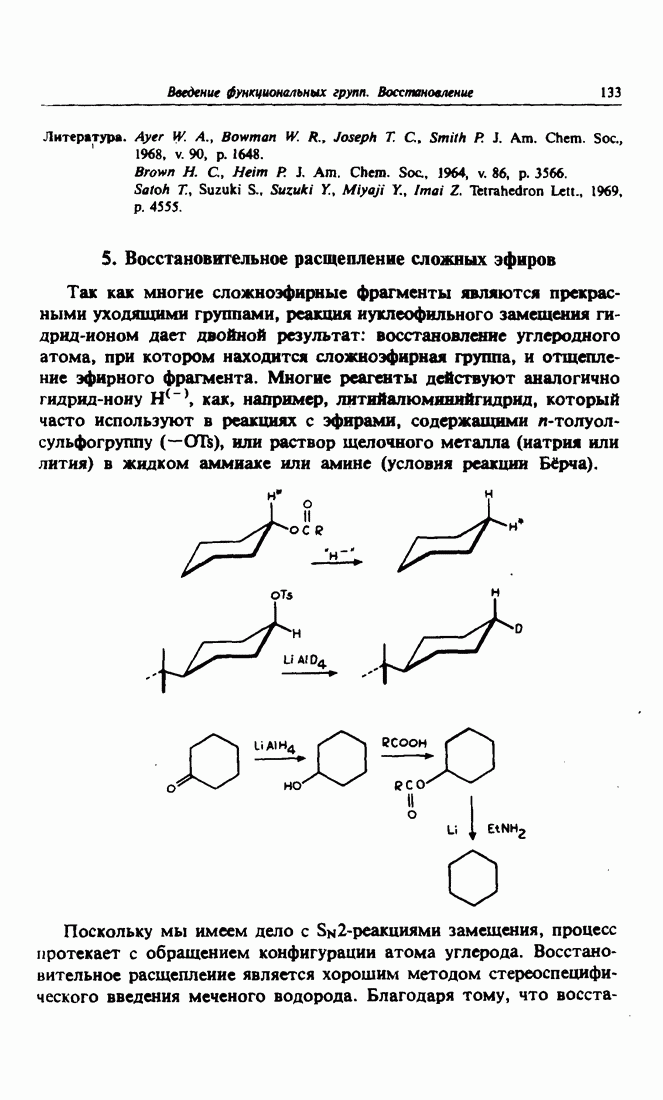
- 5. Восстановительное расщепление сложных эфиров
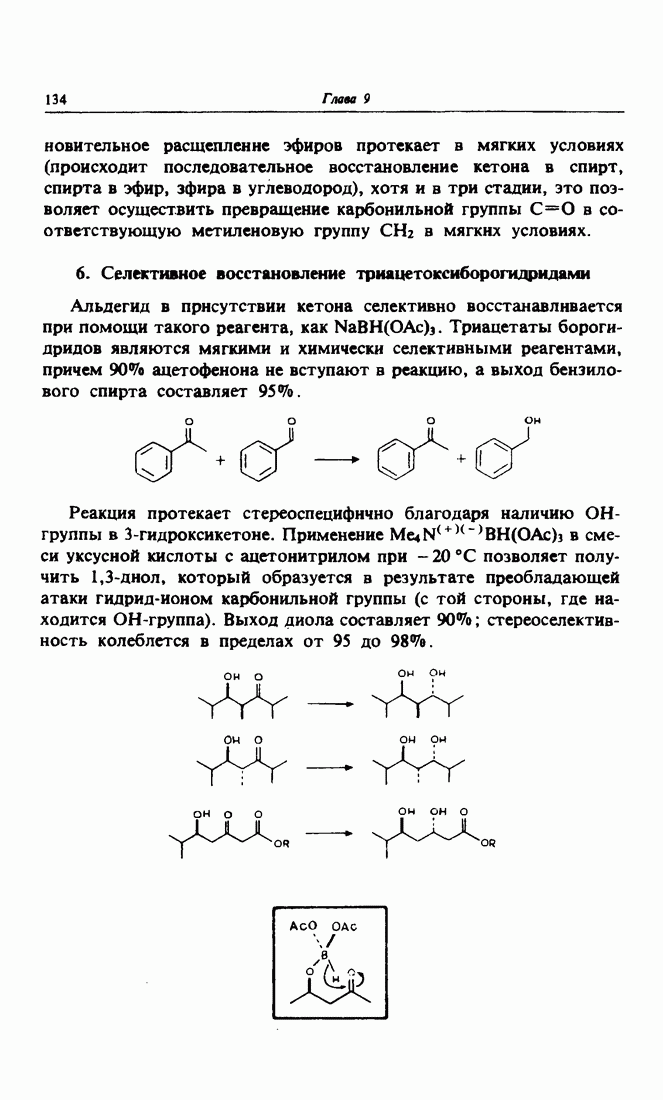
- 6. Селективное восстановление триацетоксиборогидридами
- Глава 10. ВВЕДЕНИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП. РЕАКЦИИ ОКИСЛЕНИЯ
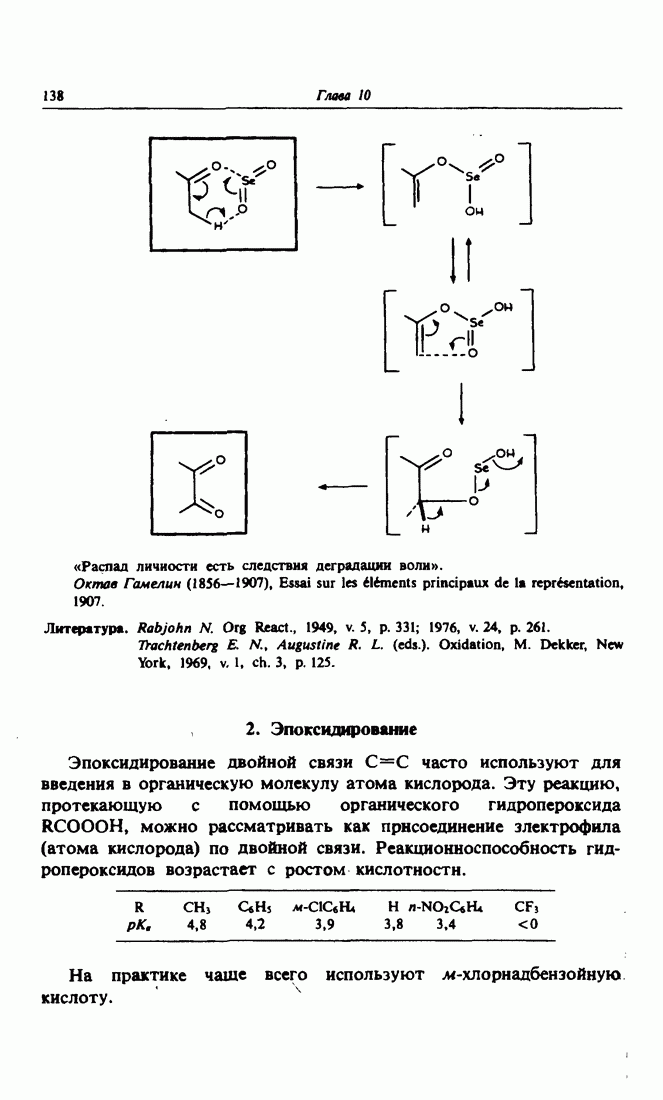
- 2. Эпоксидирование
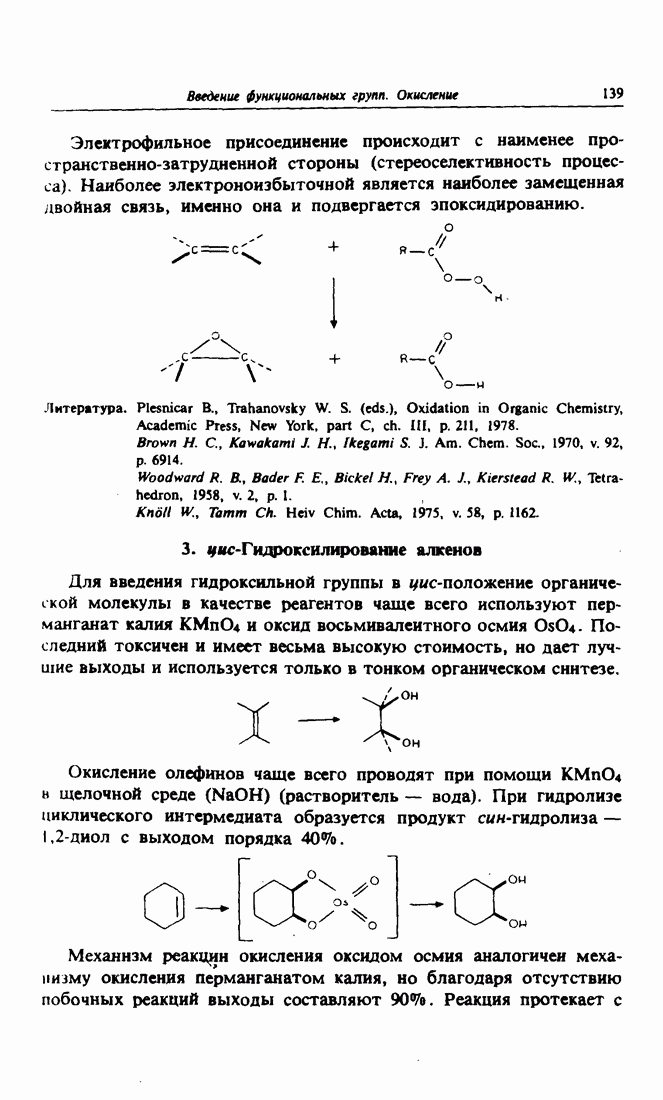
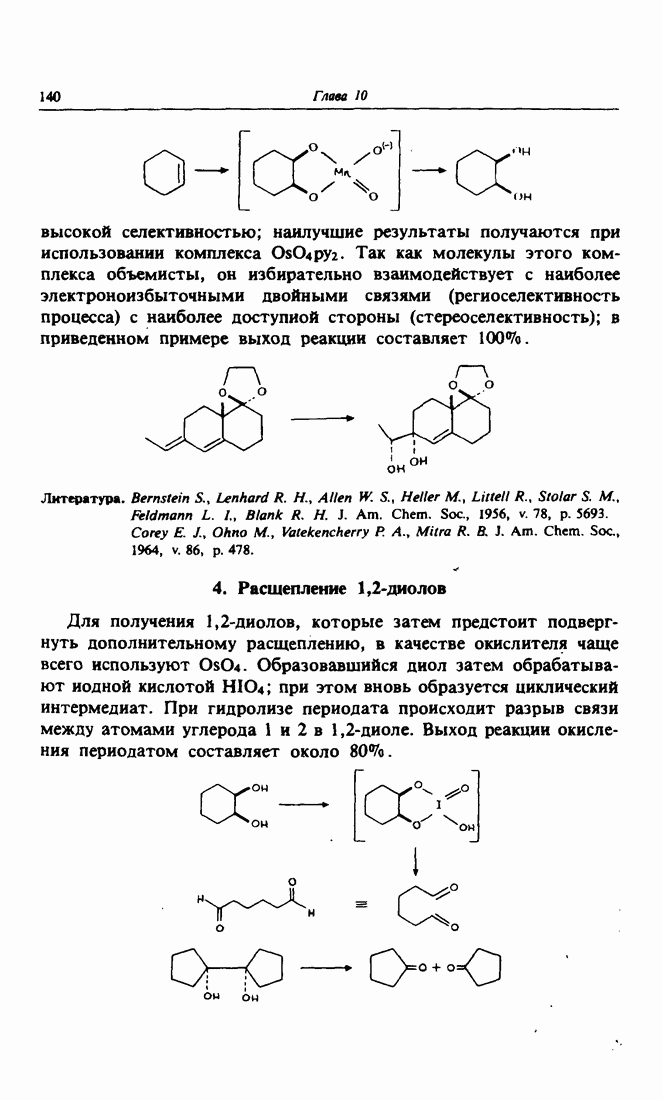
- 3. цис-Гидроксилирование алкенов
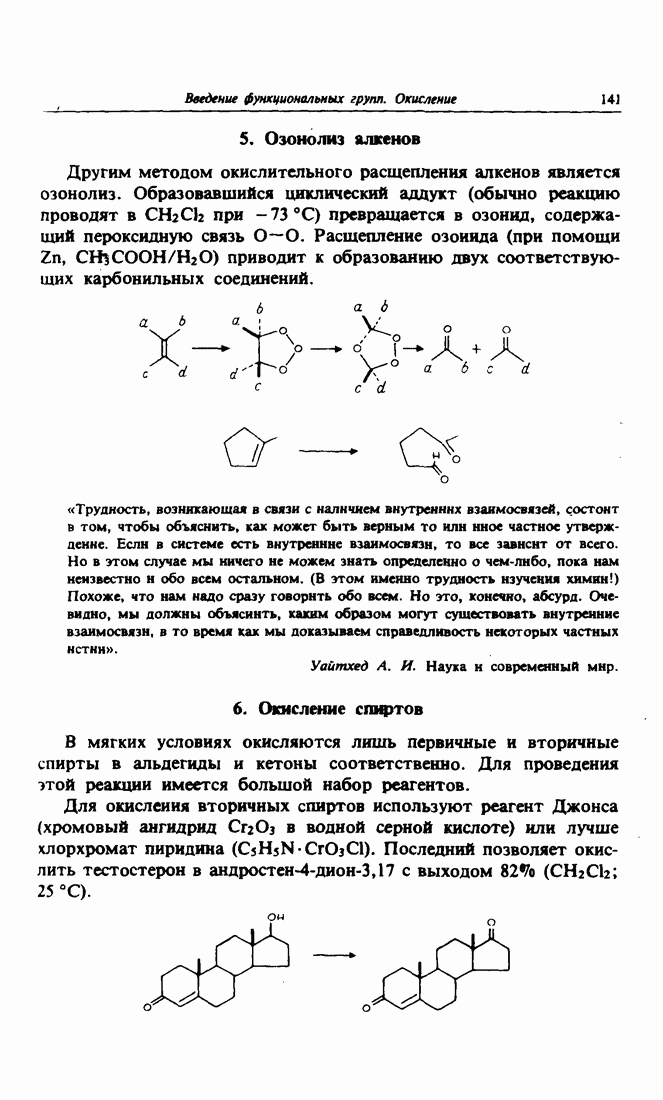
- 4. Расщепление 1,2-диолов
- 5. Озонолиз алкенов
- 6. Окисление спиртов
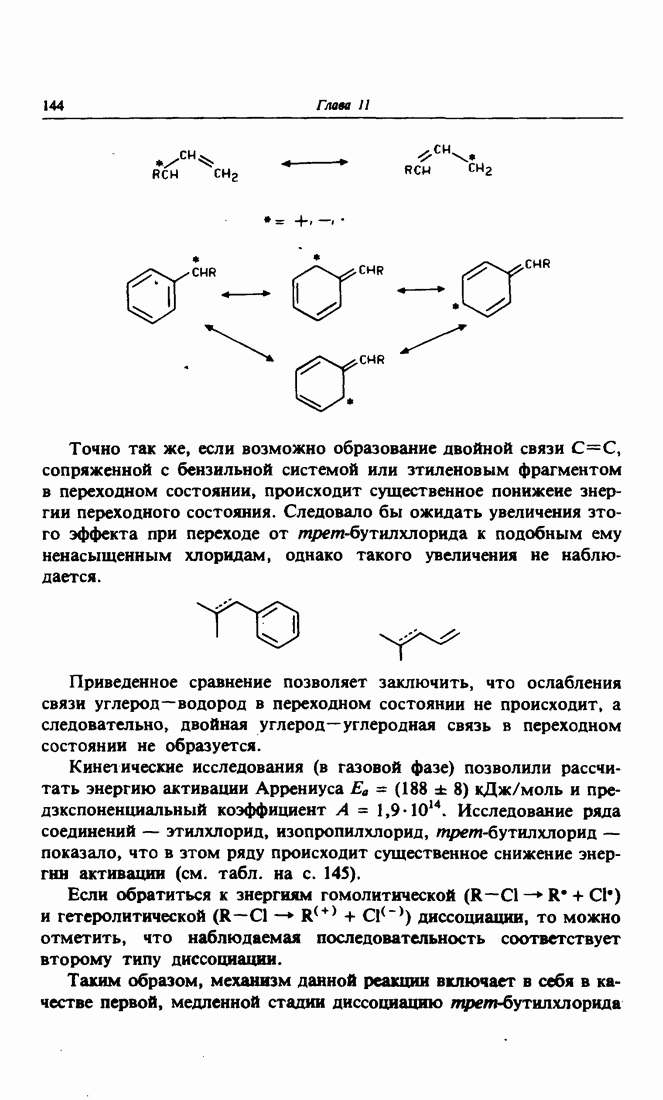
- Главе 11. РЕАКЦИИ ПРИСОЕДИНЕНИЯ И ЭЛИМИНИРОВАНИЯ
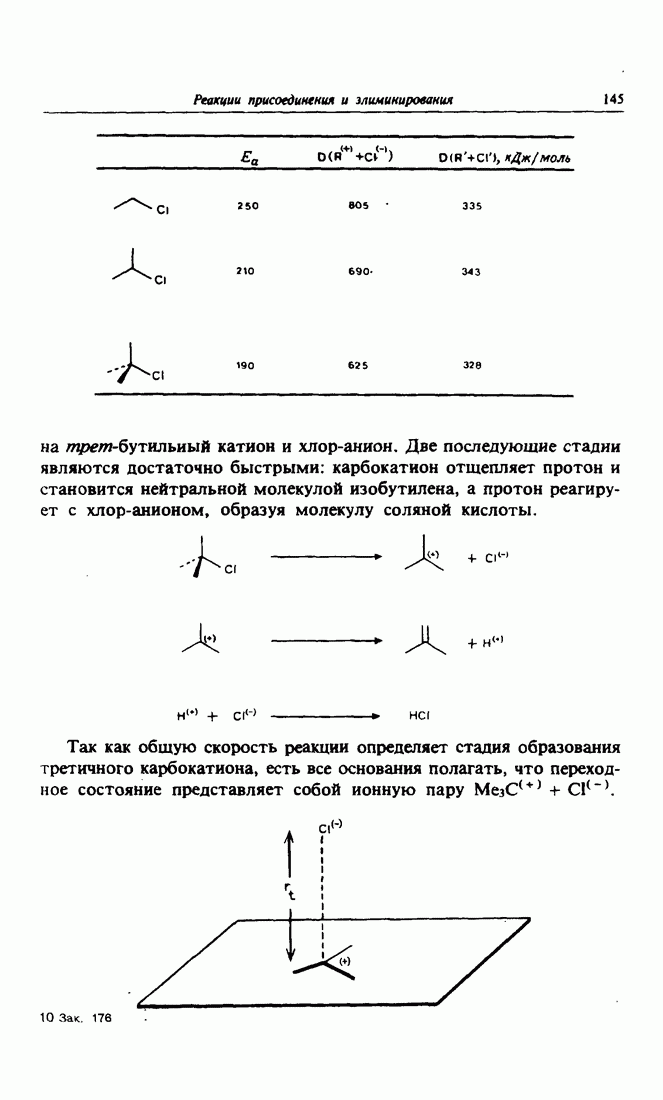
- 2. Классически механизм реакции электрофильного присоединения. Правило Марковникова
- 3. Основные электрофильные агенты
- 3.3. Присоединение гипохлоритов и гипобромитов
- 3.4. Оксимеркурирование
- 3.5. Гидроборирование
- 3.6. Окситаллирование
- 4. Стереохимия реакции присоединения по двойной связи С=С
- 5. Конкуренция нуклеофила и растворителя в реакции электрофильного присоединения
- 6. Присоединение к напряженным олефинам: цис-присоединение
- 7. Стереохимия реакций бимолекулярного элиминирования
- 8. Виды b-элиминирования
- Главв 12. ПЕРЕГРУППИРОВКИ ФУНКЦИОНАЛЬНЫХ ГРУПП. ПРЕВРАЩЕНИЕ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ В ОЛЕФИНЫ ПО РЕАКЦИИ ВИТТИГА
- 2. Реакция Дарзана
- 3. Дарзан — один из великих политехников
- 4. Обобщение и модернизация метода
- 5. Стереоселективность реакции Кори — Чайковского
- 6. Реакция Виттига
- 7. Георг Виттиг
- 8. Причины образования различных продуктов в реакциях Виттига и Кори — Чайковского
- 9. Разновидность реакции Виттига: олефинирование по Петерсону
- Главе 13. ПЕРЕГРУППИРОВКИ
- 2. 1,2-Переход в карбокатионах
- 3. Перегруппировка Бекмана
- 4. Перегруппировка Курциуса
- 5. Перегруппировка Байера — Виллигера
- 6. Реакция Рамберга-Беклунда
- Глава 14. ДОНОРНЫЕ СИНТОНЫ
- 2. Алкильные донорные синтоны
- 3. Донорные синтоны d1 с гетероатомами, обладающими d-орбиталью
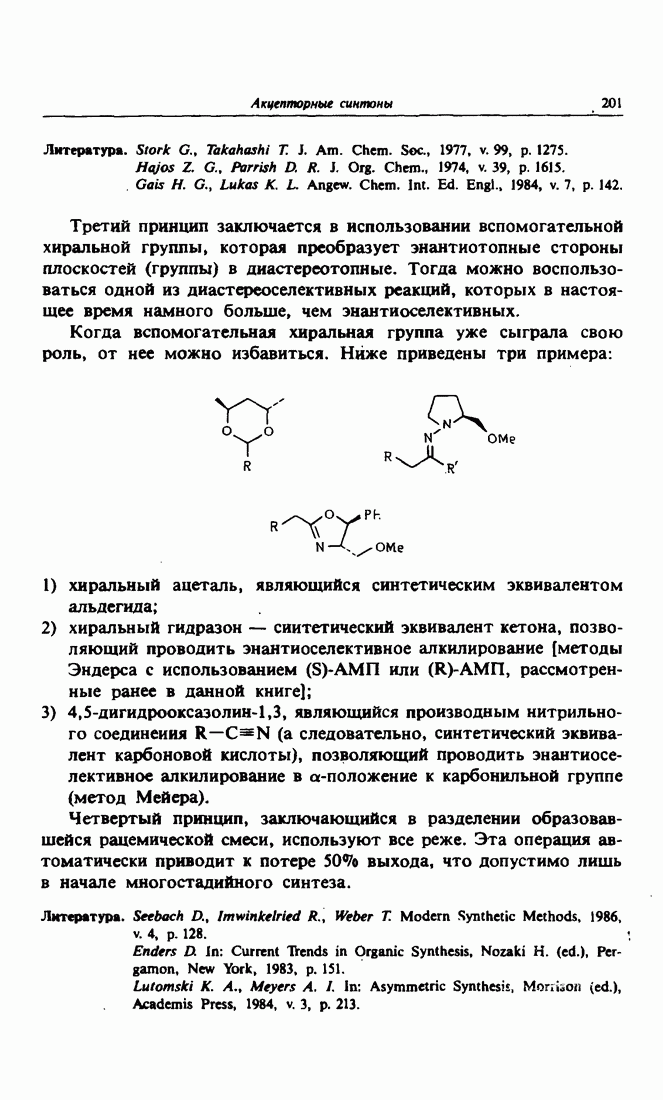
- Глава 15. АКЦЕПТОРНЫЕ СИНТОНЫ
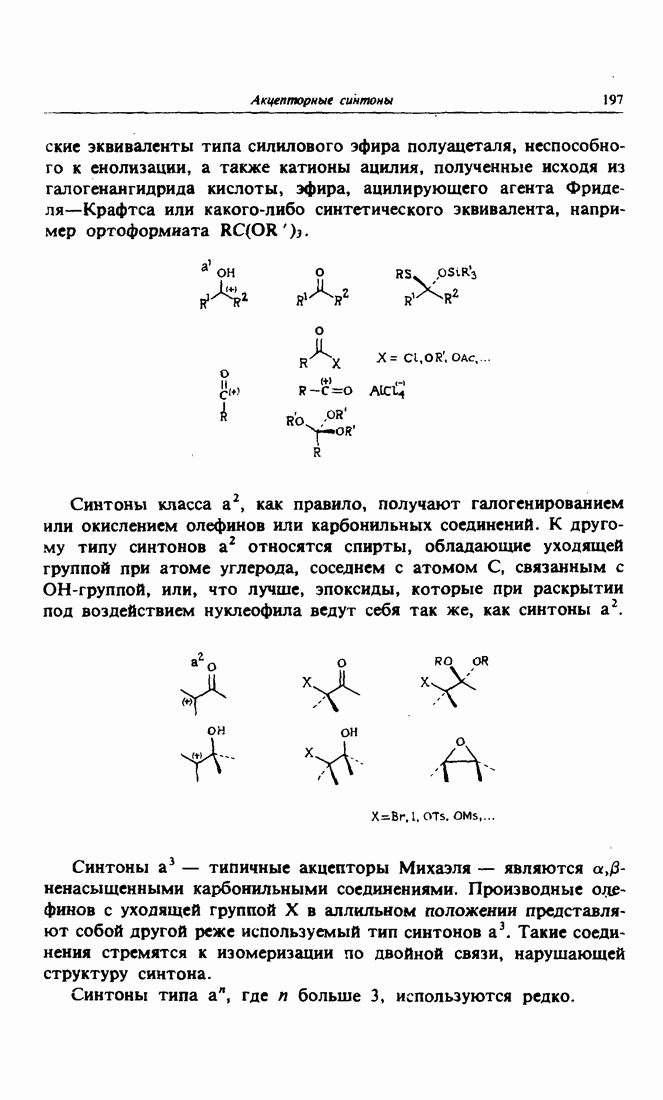
- 1. Синтоны-акцепторы
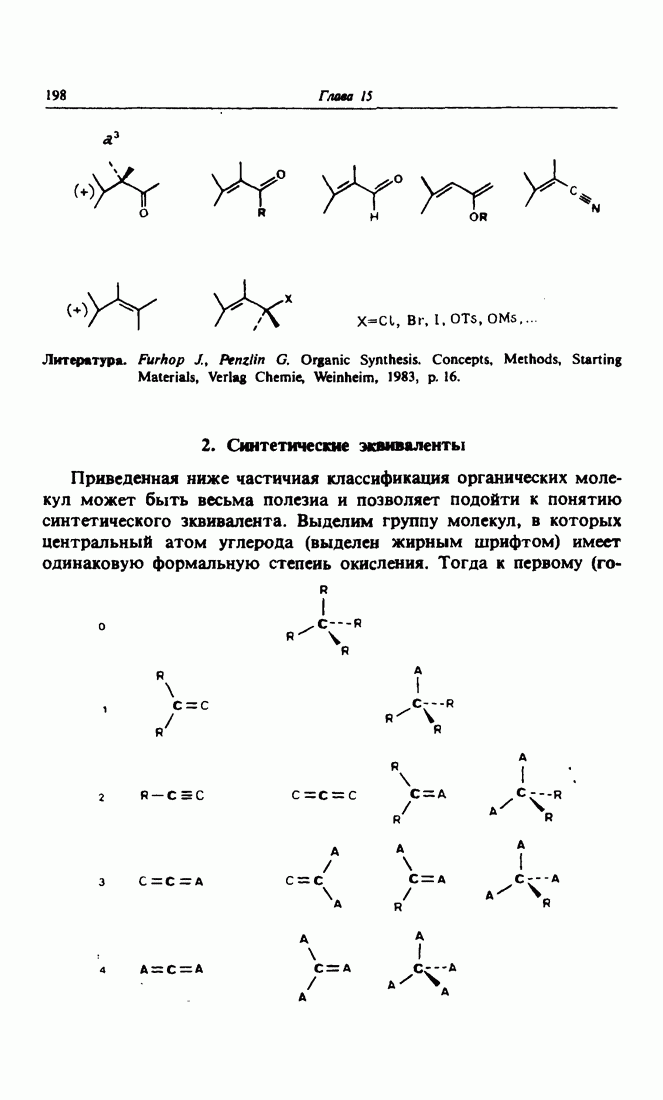
- 2. Синтетические эквиваленты
- 3. Контролируемое образование новых связей
- 4. Расчленение молекулы на фрагменты
- 5. Двойное расчленение молекулы
- 6. Изменение реакционноспособности в результате обращения полярности
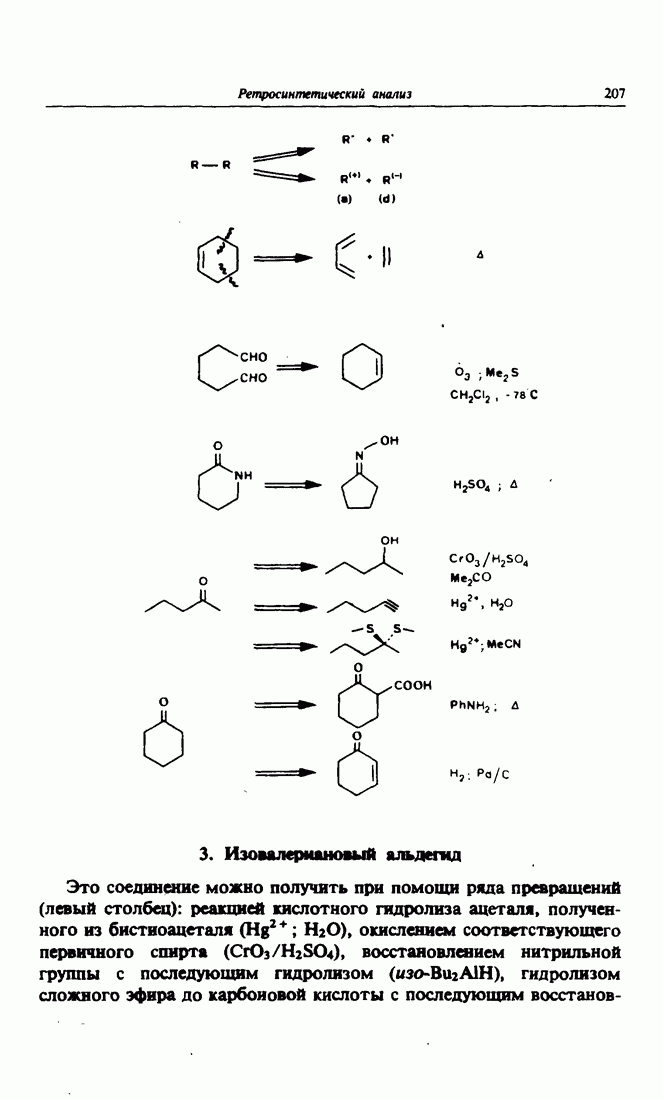
- Глава 16. РЕТРОСИНТЕТИЧЕСКИЙ АНАЛИЗ
- 2. Цепь превращений
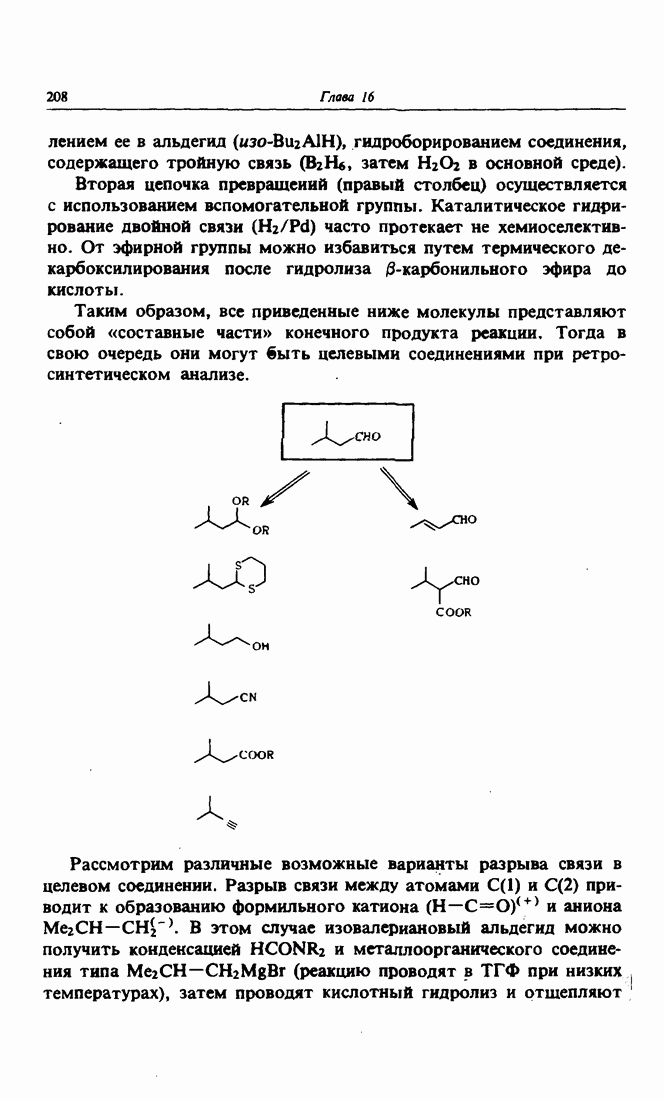
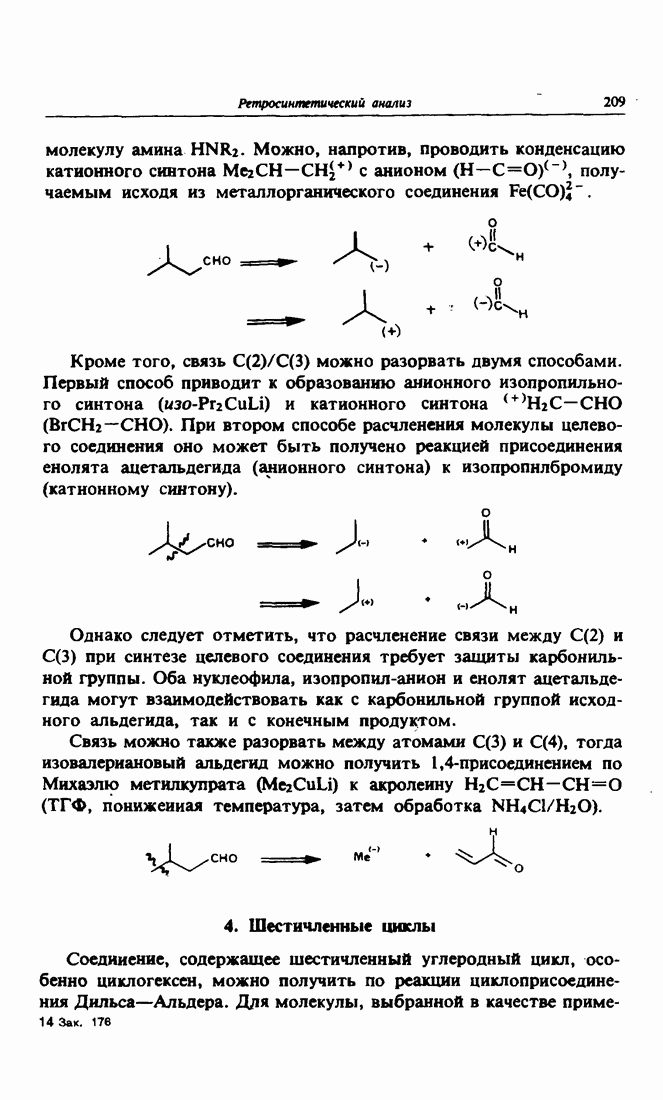
- 3. Изовалериановый альдегид
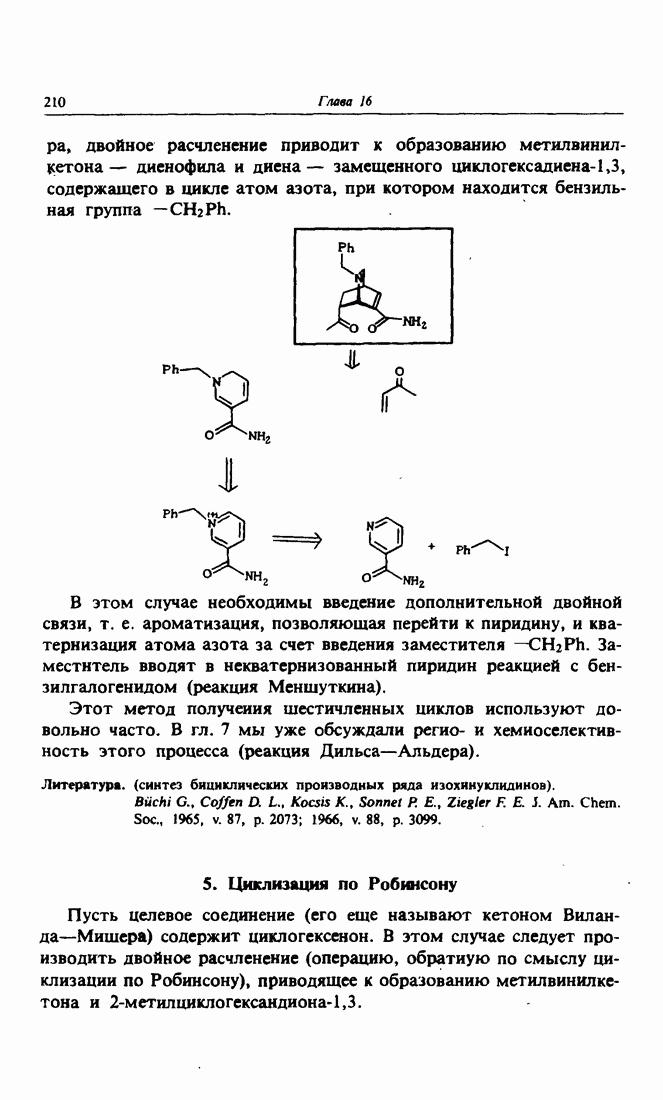
- 4. Шестичленные циклы
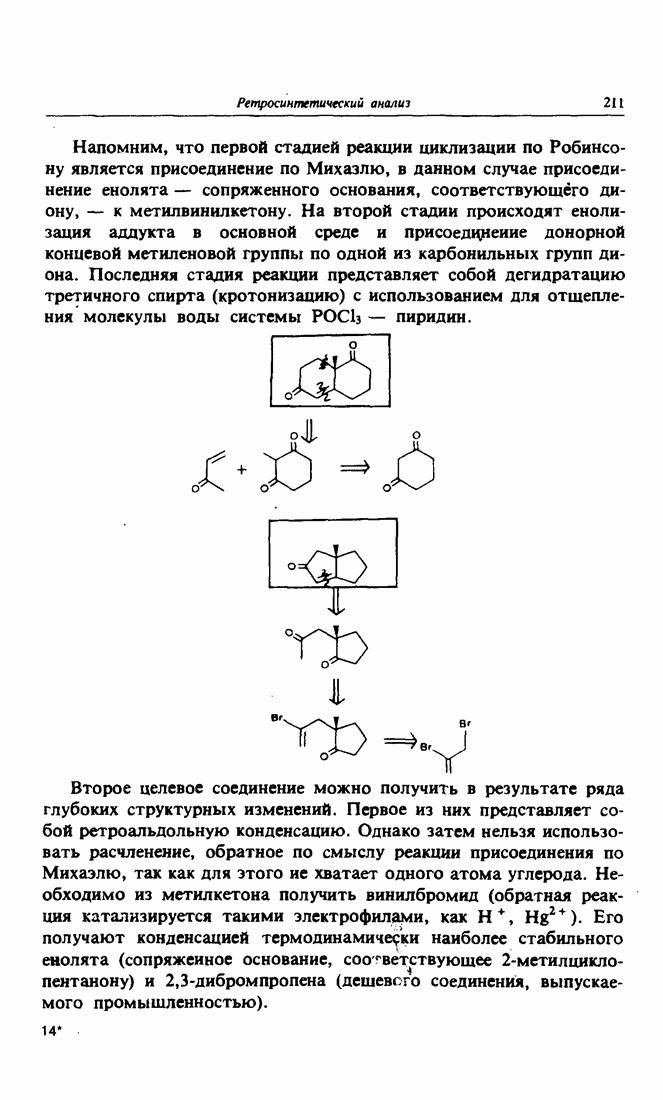
- 5. Циклизация по Робинсону
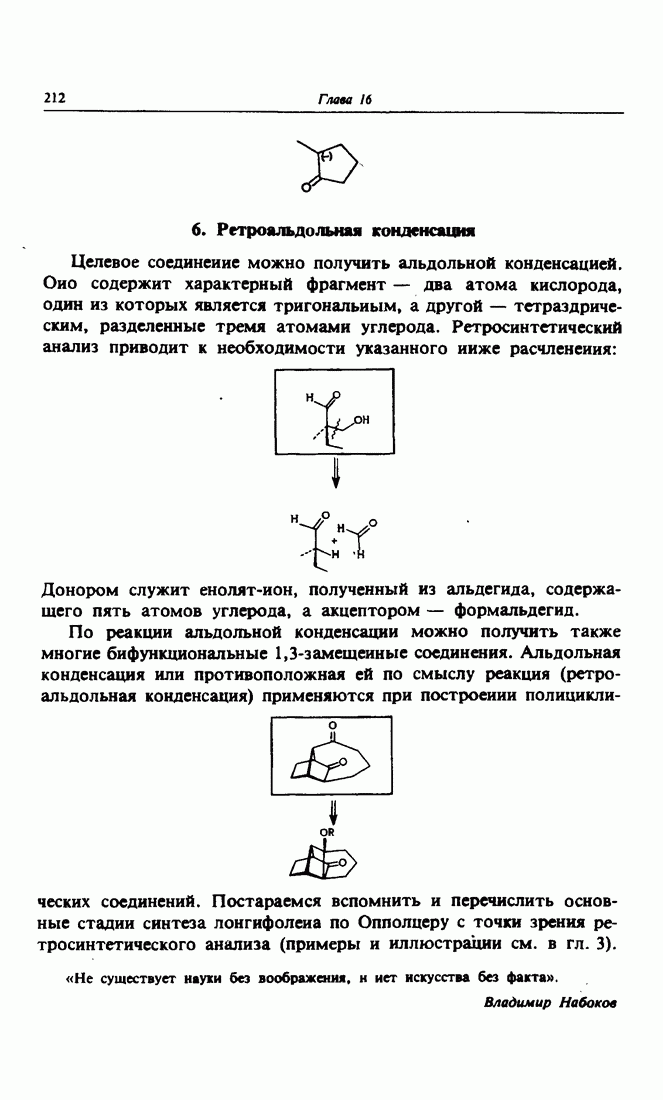
- 6. Ретроальдольная конденсация
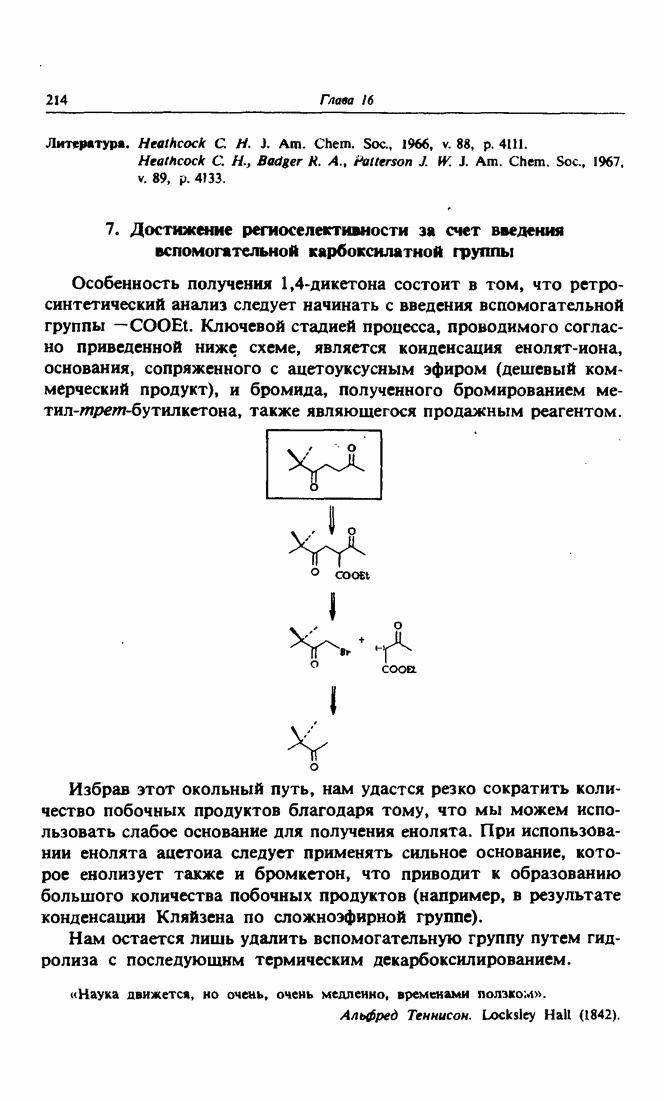
- 7. Достижение региоселективности за счет введения вспомогательной карбоксилатной группы
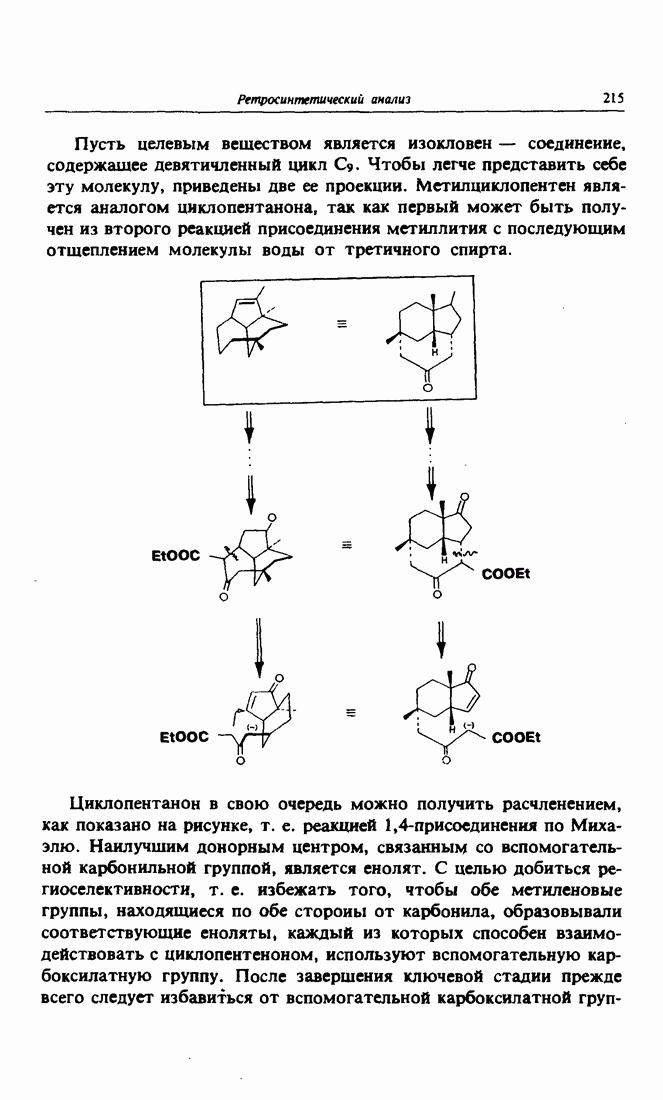
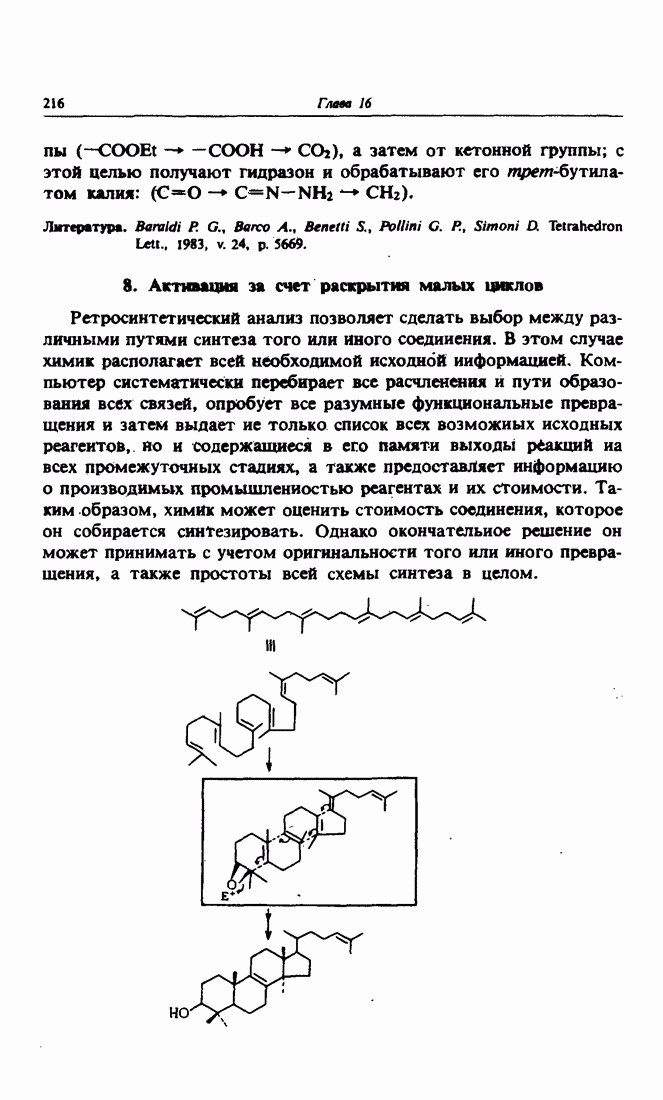
- 8. Активация за счет раскрытия малых циклов
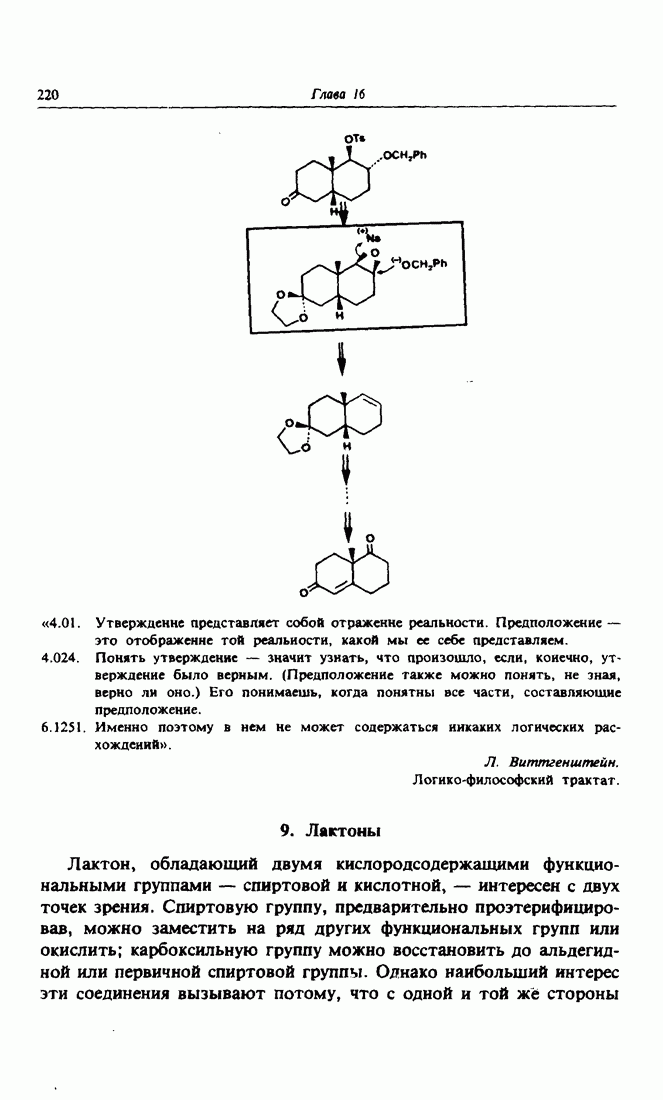
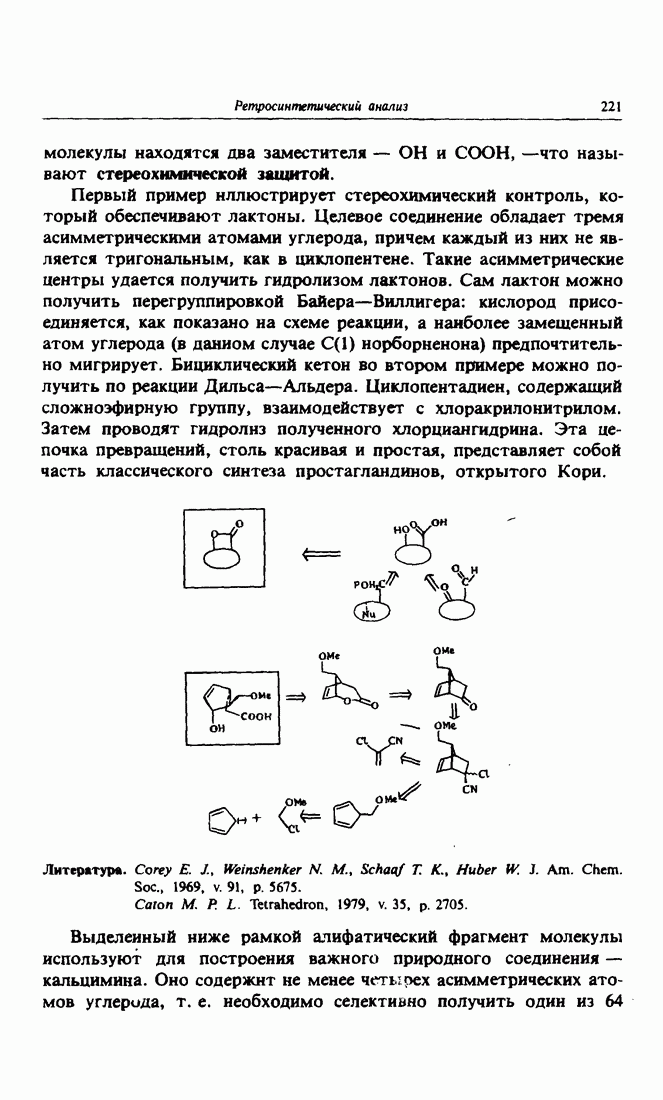
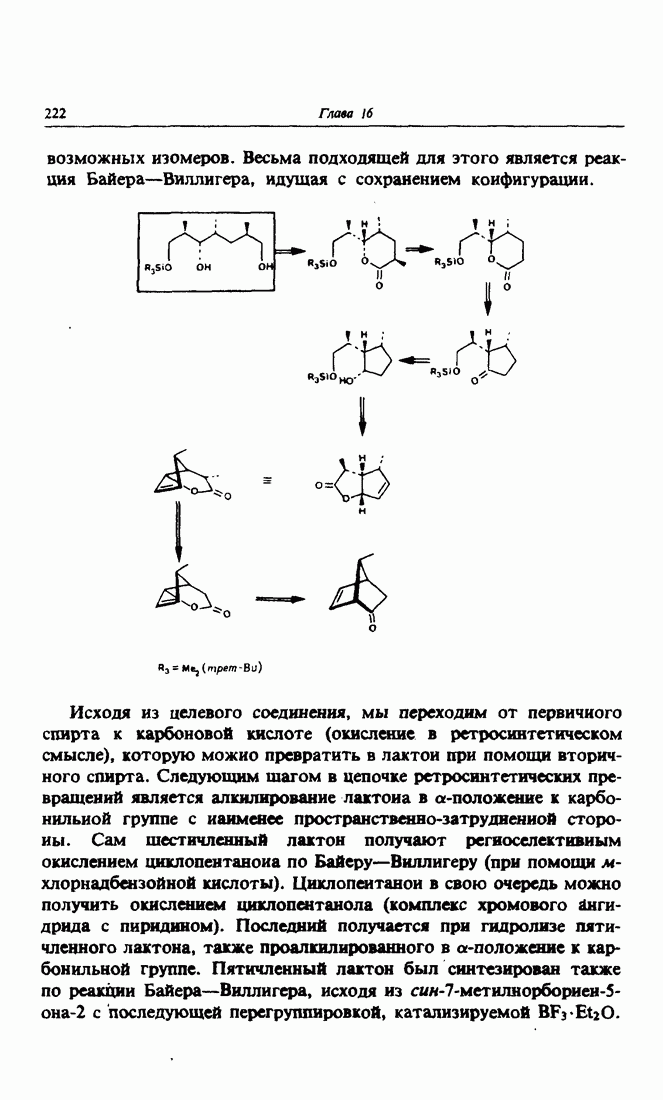
- 9. Лактоны
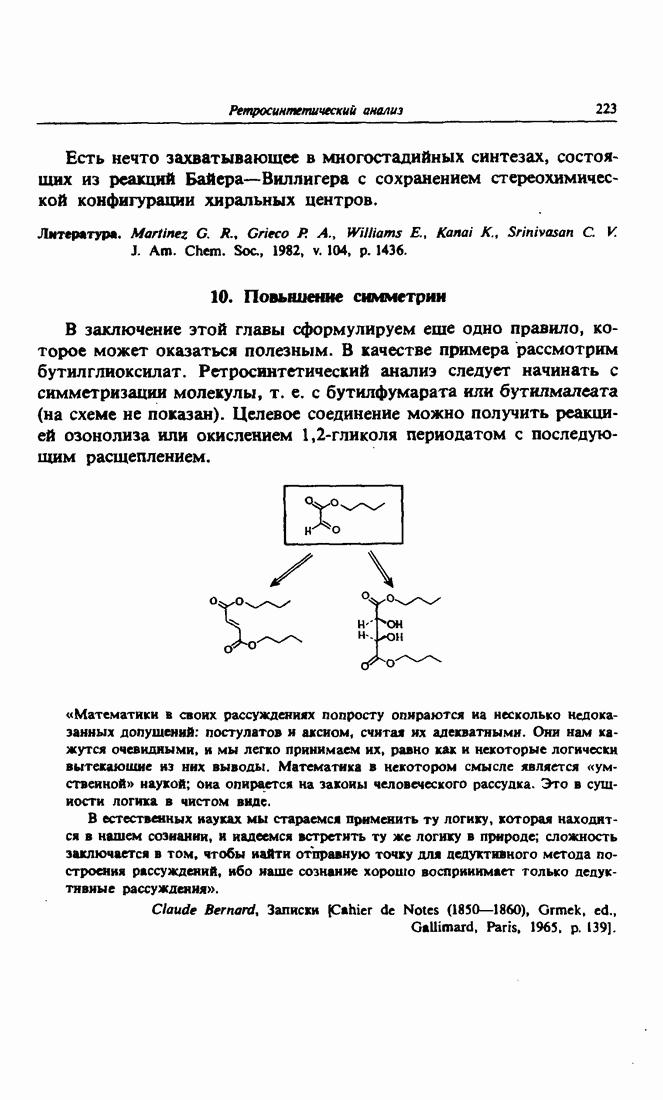
- 10. Повышение симметрии
- ПОСЛЕСЛОВИЕ