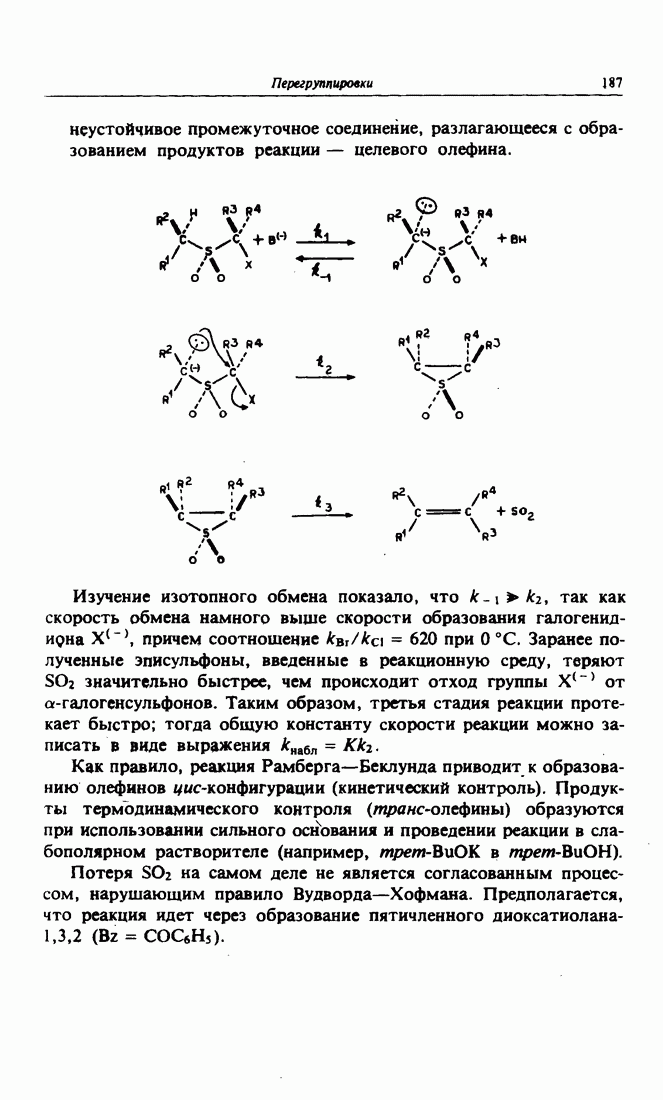
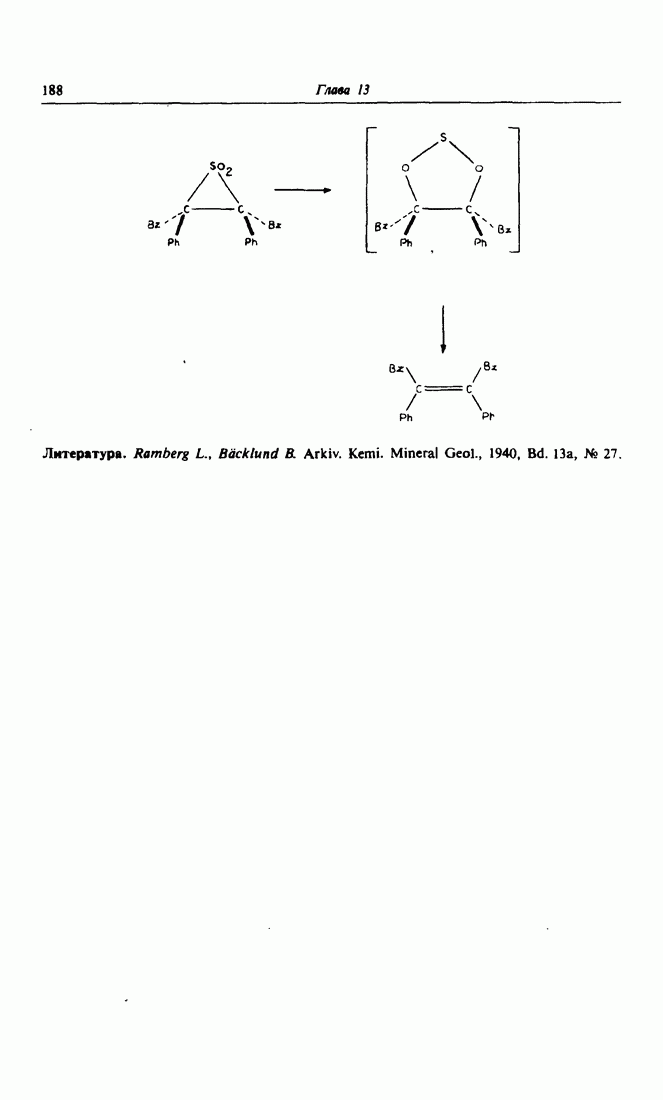
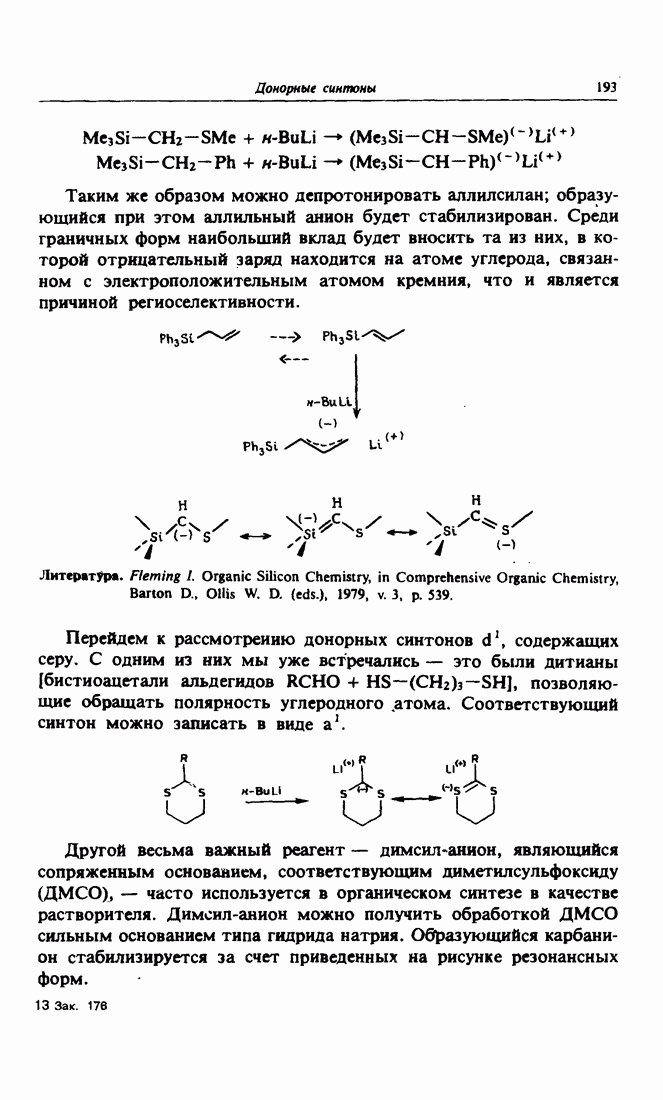
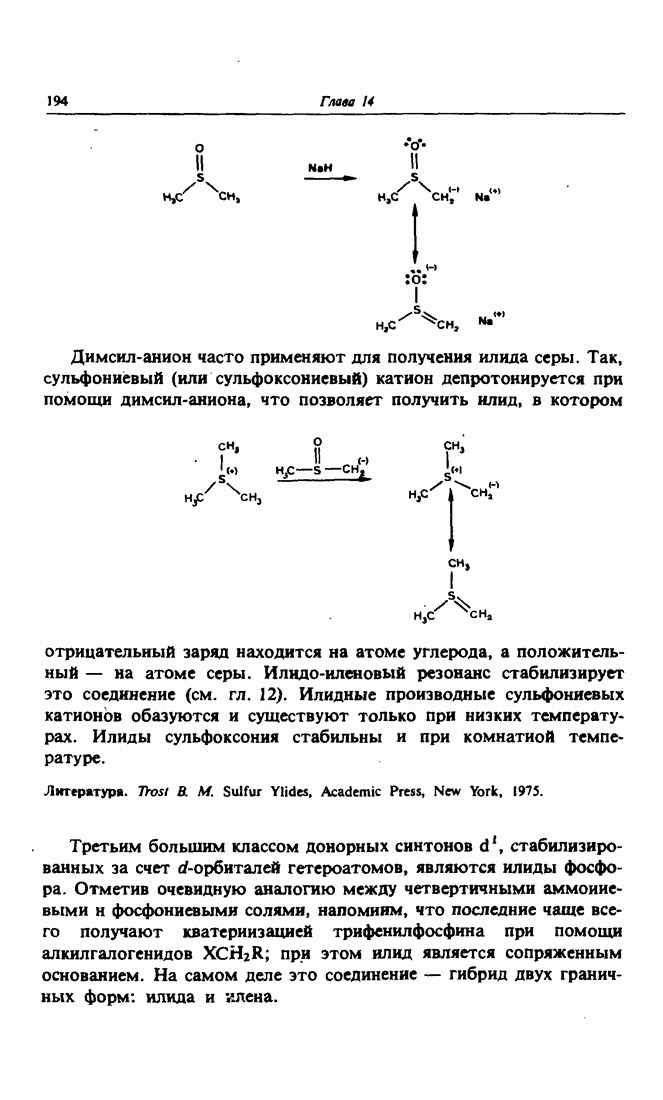
| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
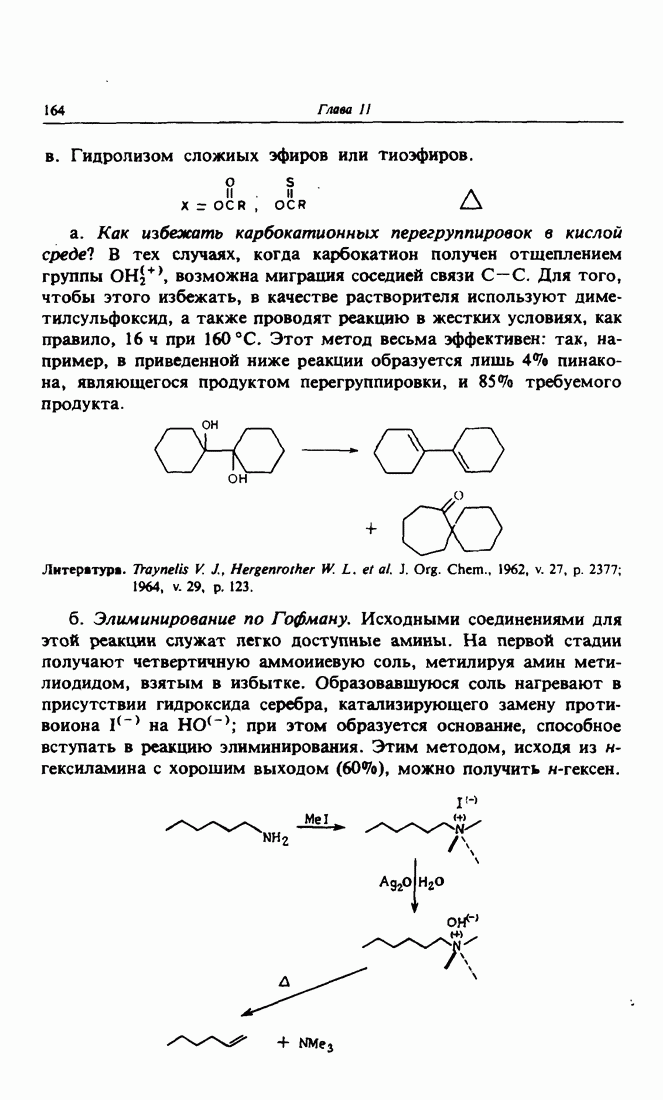
Глава 2. КАРБОНИЛЬНАЯ ГРУППА. ЕНОЛИЗАЦИЯ. КОНДЕНСАЦИЯ ПО МИХАЭЛЮ
Связь  при углеродном атоме, находящемся в
при углеродном атоме, находящемся в  -положеиии к карбонильной группе, характеризуется сравнительно высокой кислотностью. Процесс енолизации может катализироваться как кислотами, так и основаниями. Существенная особенность карбонильной группы заключается в возможности простого получения енолят-иона. Енолы и эфиры енолов (их устойчивые производные) являются интермедиатами в важнейших реакциях, обусловленных высокой реакционноспособностью двойной связи и нуклеофильностью углеродного атома.
-положеиии к карбонильной группе, характеризуется сравнительно высокой кислотностью. Процесс енолизации может катализироваться как кислотами, так и основаниями. Существенная особенность карбонильной группы заключается в возможности простого получения енолят-иона. Енолы и эфиры енолов (их устойчивые производные) являются интермедиатами в важнейших реакциях, обусловленных высокой реакционноспособностью двойной связи и нуклеофильностью углеродного атома.
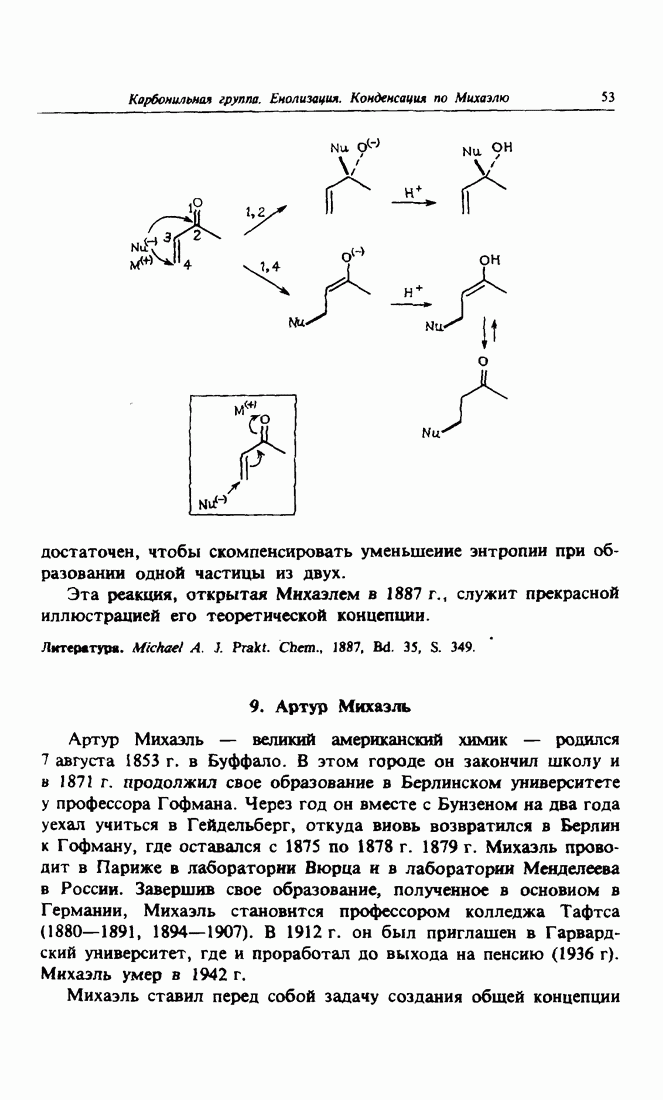
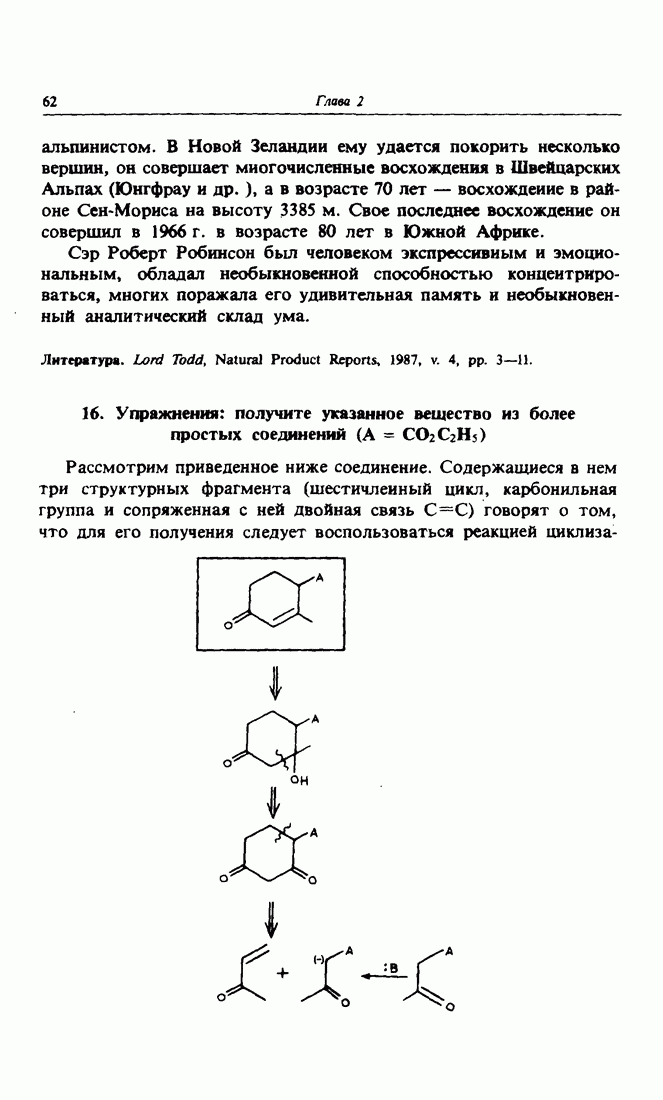
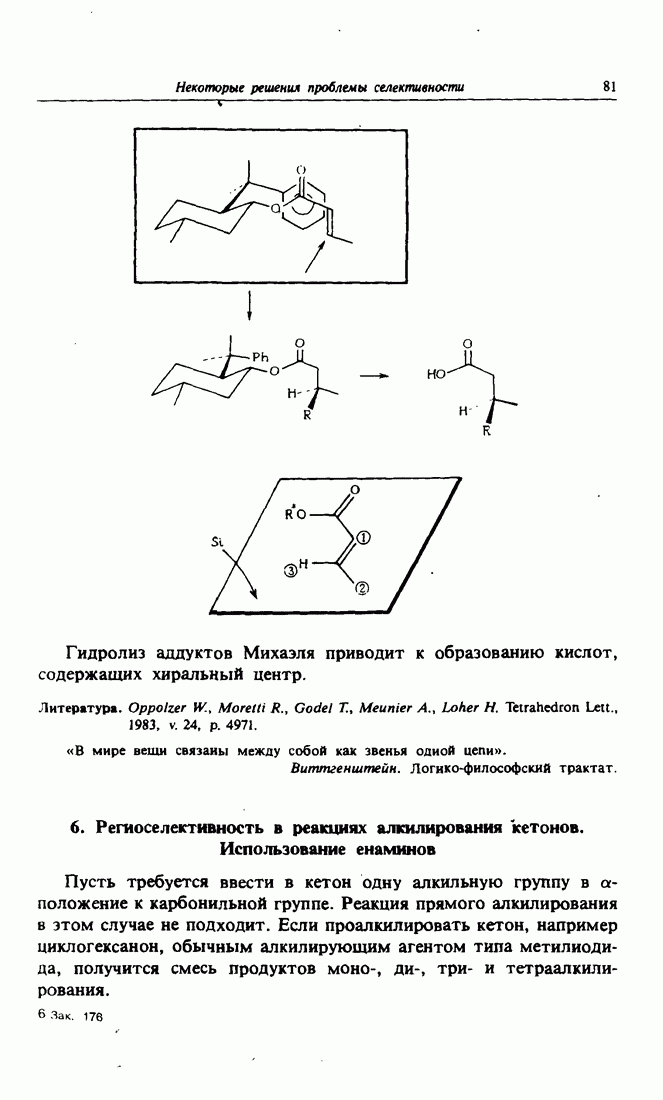
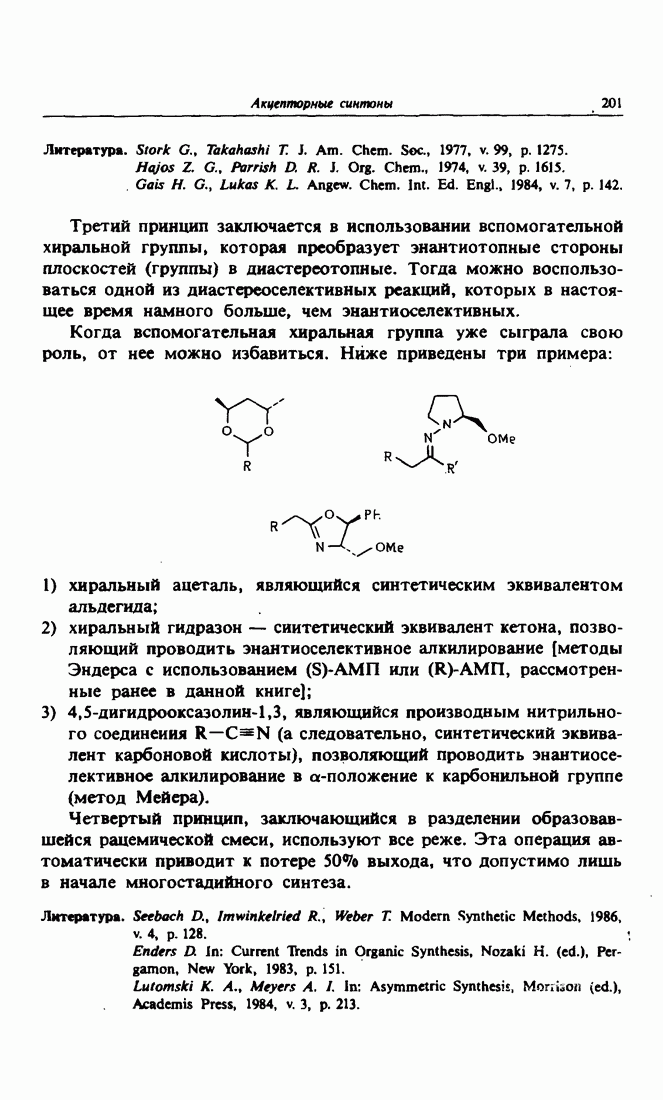
Соединение, содержащее сопряженную с двойной связью карбонильную группу, принято называть акцептором Михаэля. Реакция Михаэля открывает второй путь получения углерод-углеродной связи, рассматриваемый в данном курсе. Эта реакция представляет собой присоединение нуклеофила как донора электронов к акцептору Михаэля. Вместе с нуклеофильным присоединением по карбонильной группе реакция Михаэля является первой стадией циклизации по Робинсону — замечательного метода получения средних и особенно шестичлениых циклов.
1. Кето-енольное равновесие
Таутомерия (превращение кетоиной формы в енольиую) представляет собой переход одного из протонов при  -углеродном атоме к атому кислорода карбонильной группы с одновременным переносом электронной пары.
-углеродном атоме к атому кислорода карбонильной группы с одновременным переносом электронной пары.

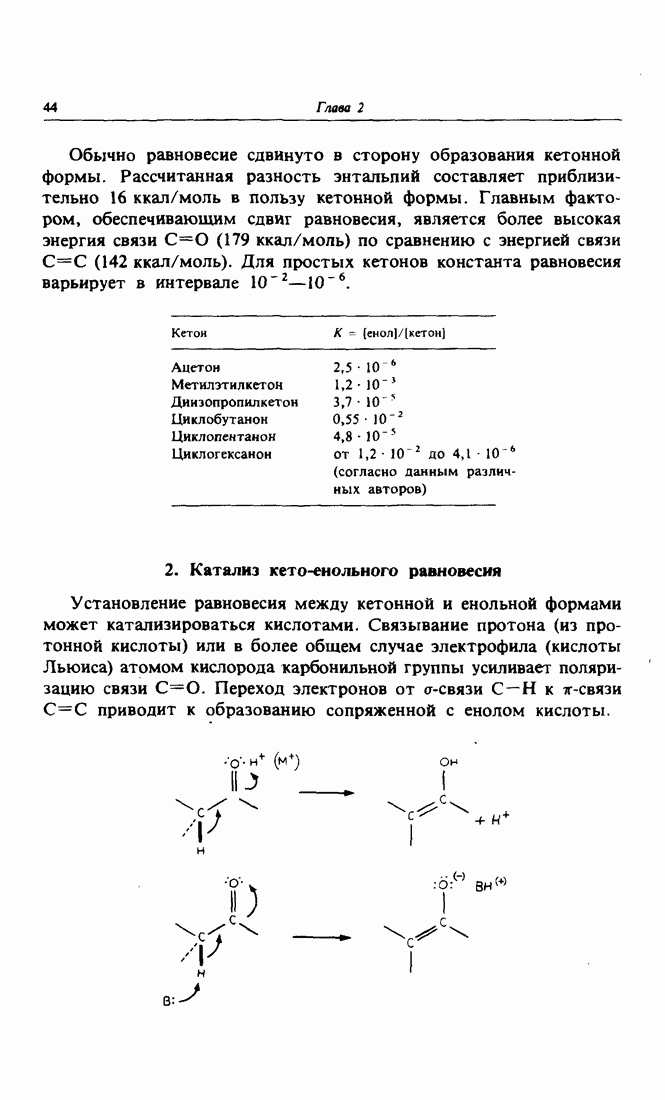
Обычно равновесие сдвинуто в сторону образования кетонной формы. Рассчитанная разность энтальпий составляет приблизительно 16 ккал/моль в пользу кетонной формы. Главным фактором, обеспечивающим сдвиг равновесия, является более высокая энергия связи  (179 ккал/моль) по сравнению с энергией связи
(179 ккал/моль) по сравнению с энергией связи  ккал/моль). Для простых кетонов константа равновесия варьирует в интервале
ккал/моль). Для простых кетонов константа равновесия варьирует в интервале 
(см. скан)
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ РЕДАКТОРА
- ВВЕДЕНИЕ
- 1. Орбитальный и зарядовый контроль
- 2. Жесткие и мягкие кислоты и основания
- 3. Термохимические данные и их применение
- Глава 1. КАРБОНИЛЬНАЯ ГРУППА. РЕАКЦИИ ПРИСОЕДИНЕНИЯ И ПРИСОЕДИНЕНИЯ-ФРАГМЕНТАЦИИ
- 1. Карбонильная группа. Простое орбитальное описание
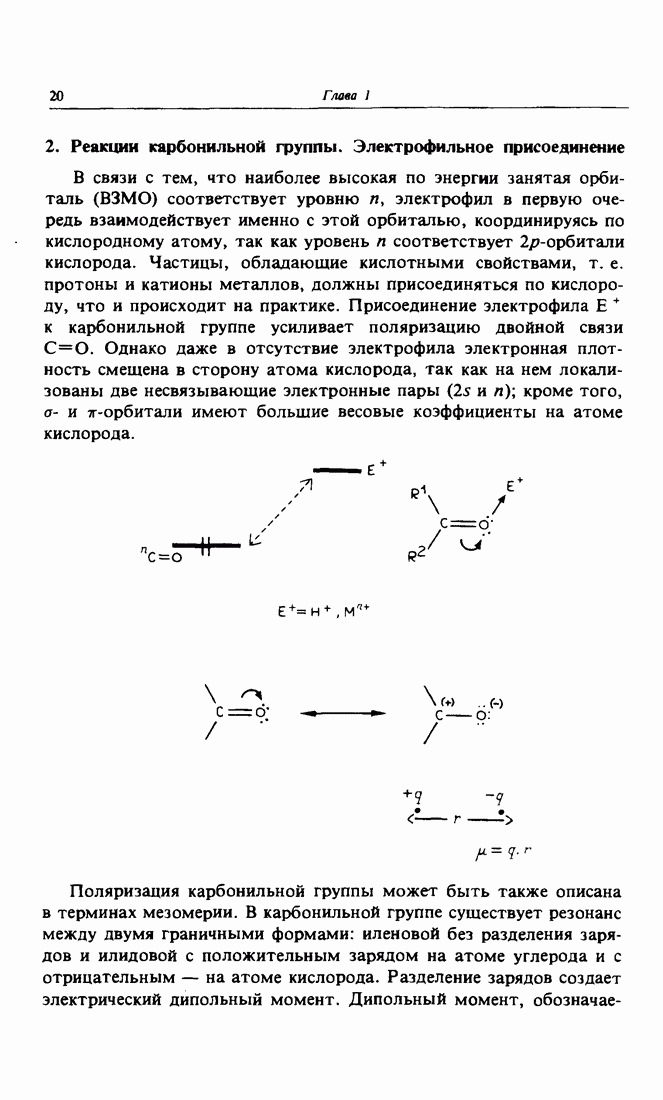
- 2. Реакции карбонильной группы. Электрофильное присоединение
- 3. Основность и нуклеофильность
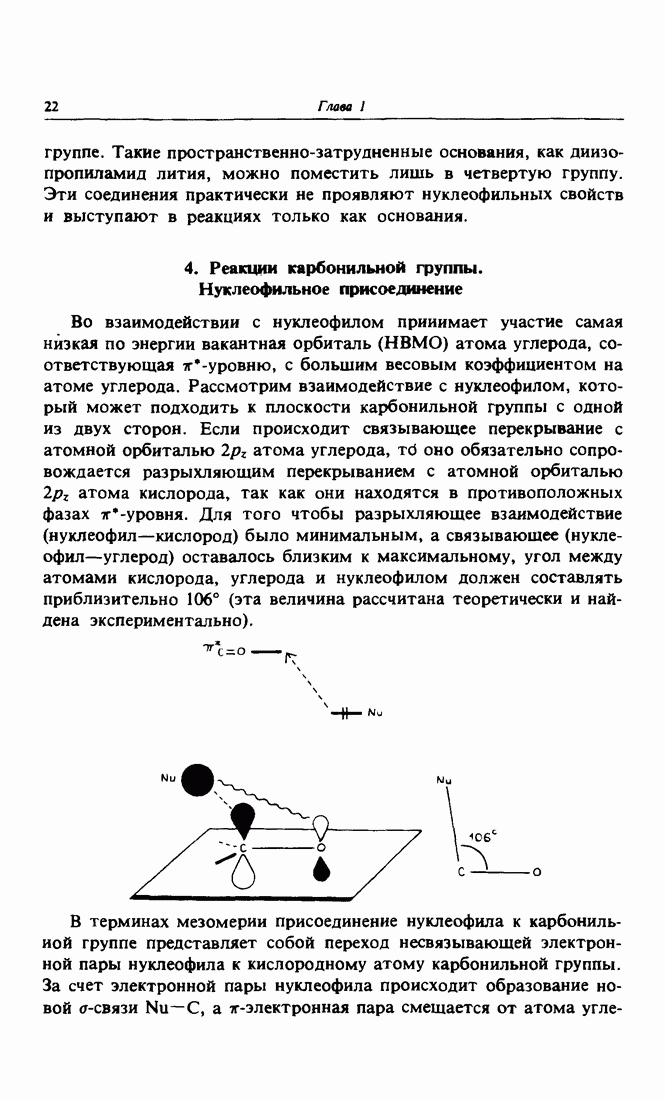
- 4 Реакции карбонильной группы. Нуклеофильное присоединение
- 5. Защита и регенерация
- 6. Получение различных металлоорганических производных
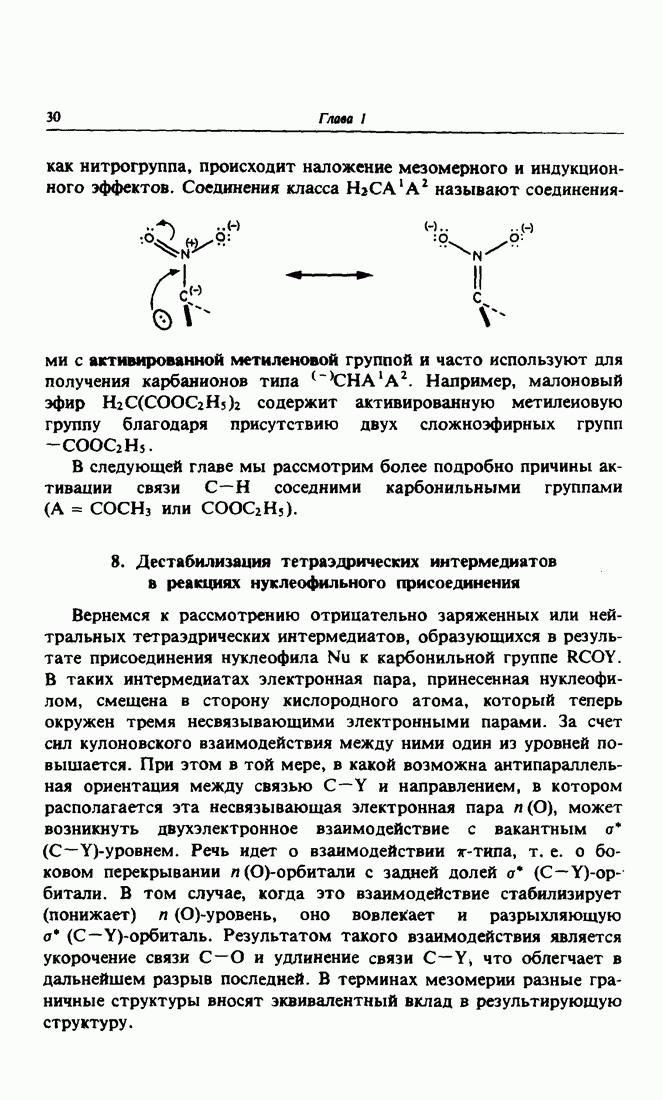
- 7. Активированная метиленовая группа
- 8. Дестабилизация тетраэдрических интермедиатов в реакциях нуклеофильного присоединения
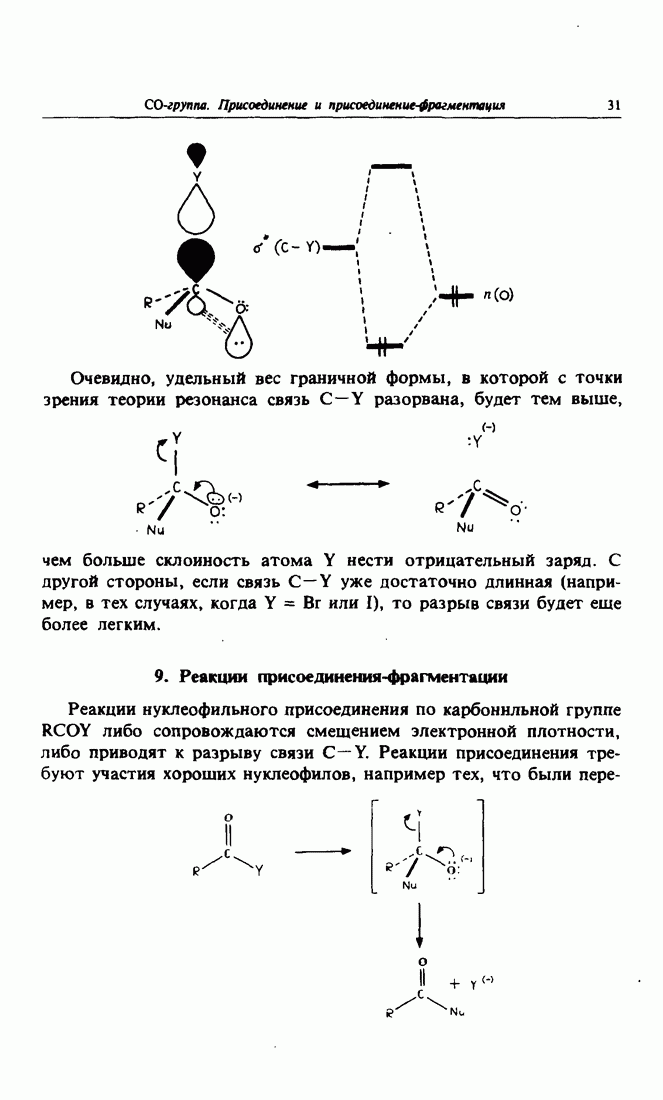
- 9. Реакции присоединения-фрагментации
- 10. Восстановление гидридами металлов
- 11. Описание конфигурации асимметрического атома углерода
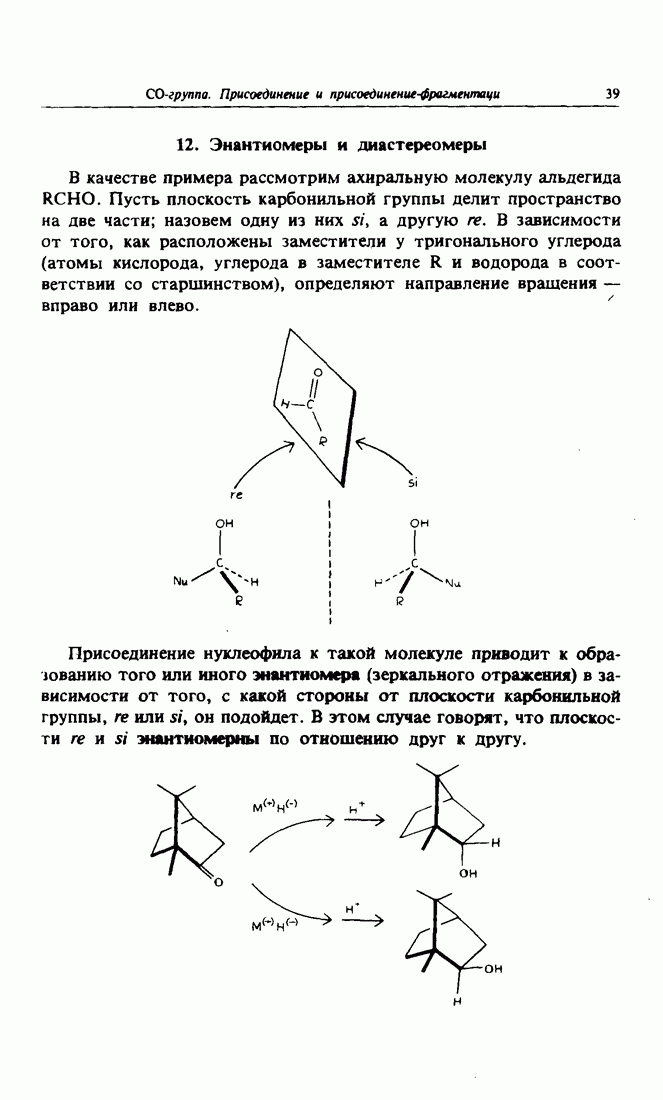
- 12. Энантиомеры и диастереомеры
- 13. Асимметрическая 1,2-индукция
- Глава 2. КАРБОНИЛЬНАЯ ГРУППА. ЕНОЛИЗАЦИЯ. КОНДЕНСАЦИЯ ПО МИХАЭЛЮ
- 1. Кето-енольное равновесие
- 2. Катализ кето-енольного равновесия
- 3. Стереохимия и реакция енолнэации
- 4. Причины ослабления связи Ca-H в кетонах
- 5. Еноляты и их получение
- 6. Эфиры енолов
- 7. Конфигурация енолов и эфиров енолов
- 8. Реакция Михаэля
- 9. Артур Михаэль
- 10. Региоселективность в реакции Михаэля
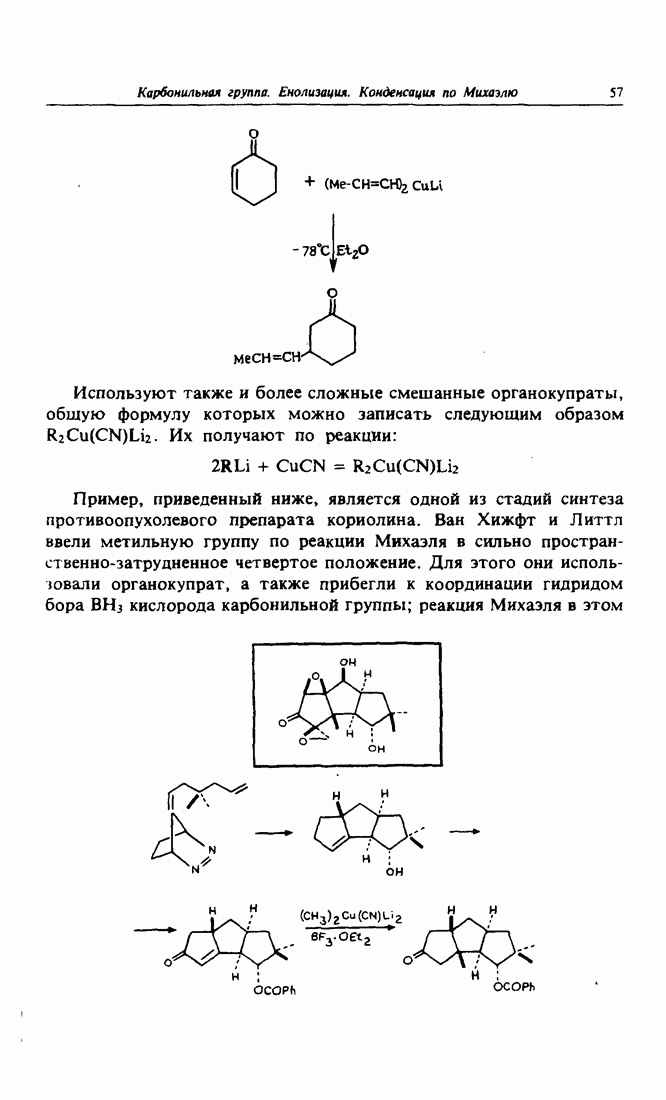
- 11. Применение органокулратов
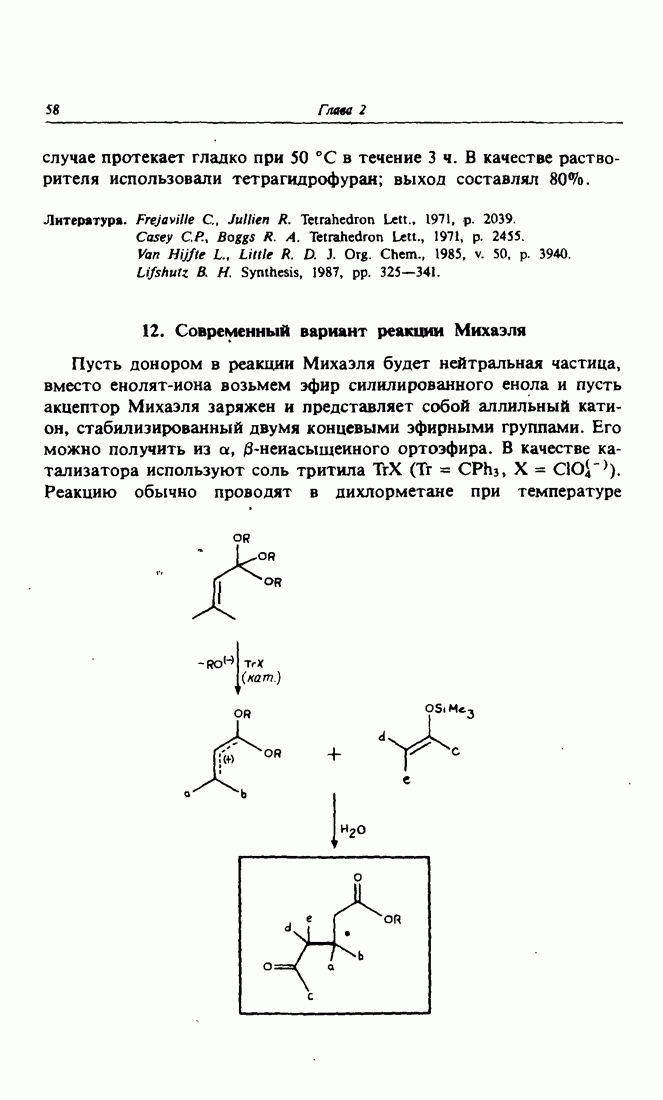
- 12. Современный вариант реакции Михаэля
- 13. Сопряжение или отсутствие сопряжения?
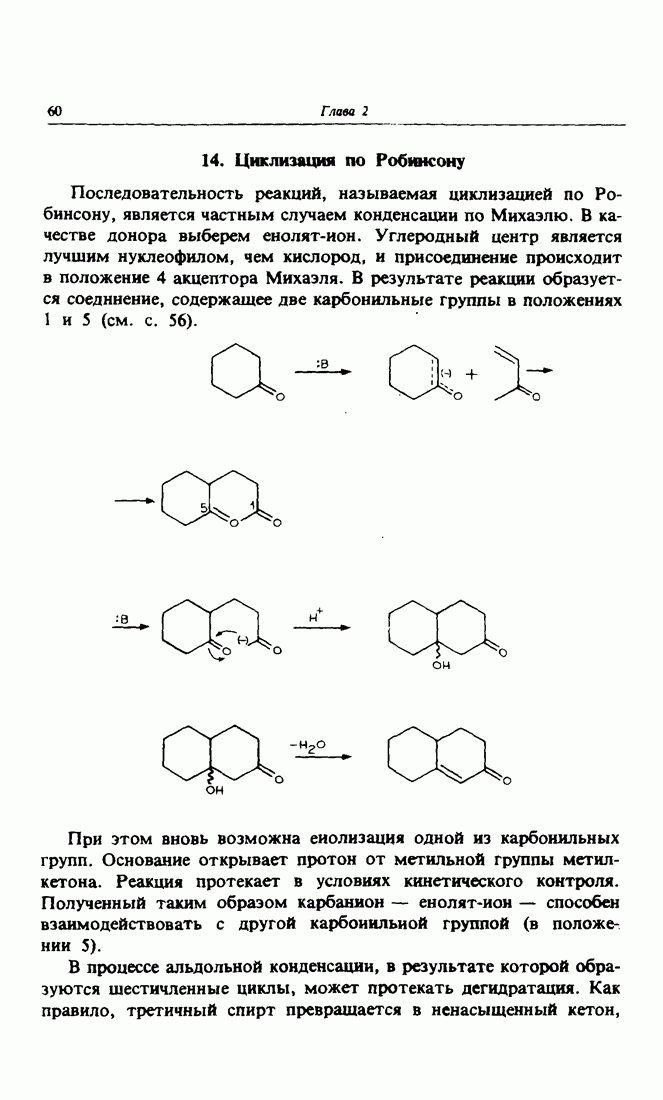
- 14. Циклизация по Робинсону
- 15. Сэр Роберт Робинсон
- 16. Упражнения: получите указанное вещество из более простых соединений (A=CO2C2H5)
- Глава 3. КАРБОНИЛЬНАЯ ГРУППА. АЛЬДОЛЬНАЯ КОНДЕНСАЦИЯ
- 2. Устойчивость продуктов альдольиой конденсации
- 3. Управление реакцией альдольной конденсации: доноры и акцепторы
- 4. Управление реакцией альдольной конденсации: син- и анти-диастереомеры
- 5. Стереоселективные реакции альдольной конденсации
- Глава 4. НЕКОТОРЫЕ РЕШЕНИЯ ПРОБЛЕМЫ СЕЛЕКТИВНОСТИ (ХИМИЧЕСКАЯ, РЕГИО- И СТЕРЕОСЕЛЕКТИВНОСТЬ)
- 2. Региоселективность при образовании енолятов
- 3. Селективное получение Е- и Z-енолятов
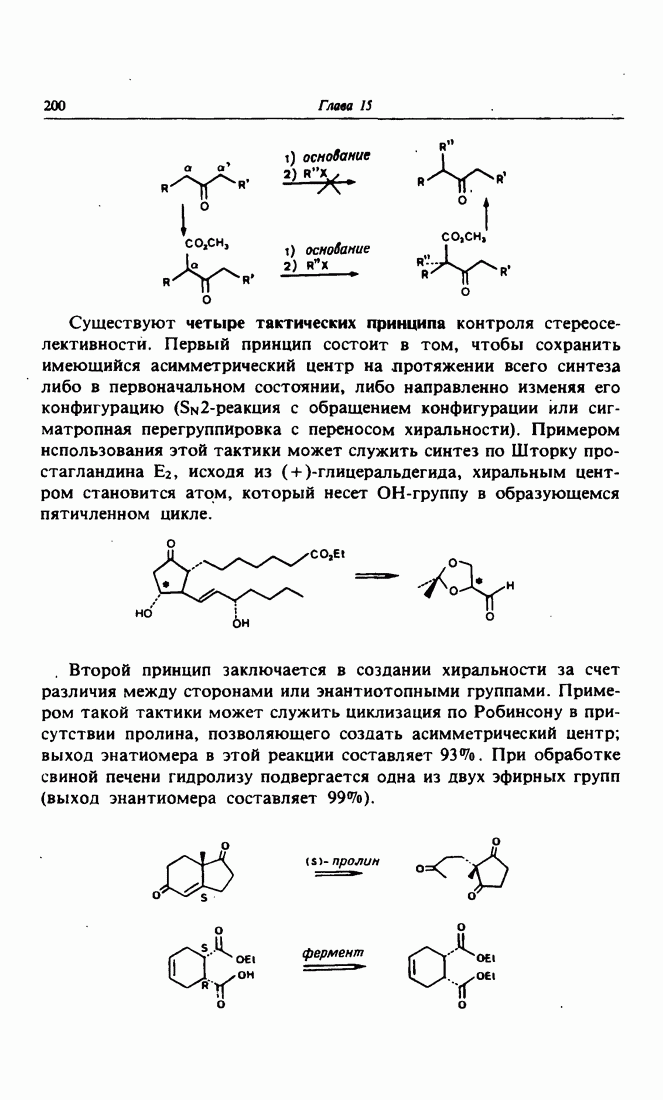
- 4. Двойной принцип стереоселективности
- 5. Энантиоселективная реакция Михаэля
- 6. Региоселективность в реакциях алкилирования кетонов. Использование енаминов
- 7. Получение хирального центра путем алкилирования енаминов
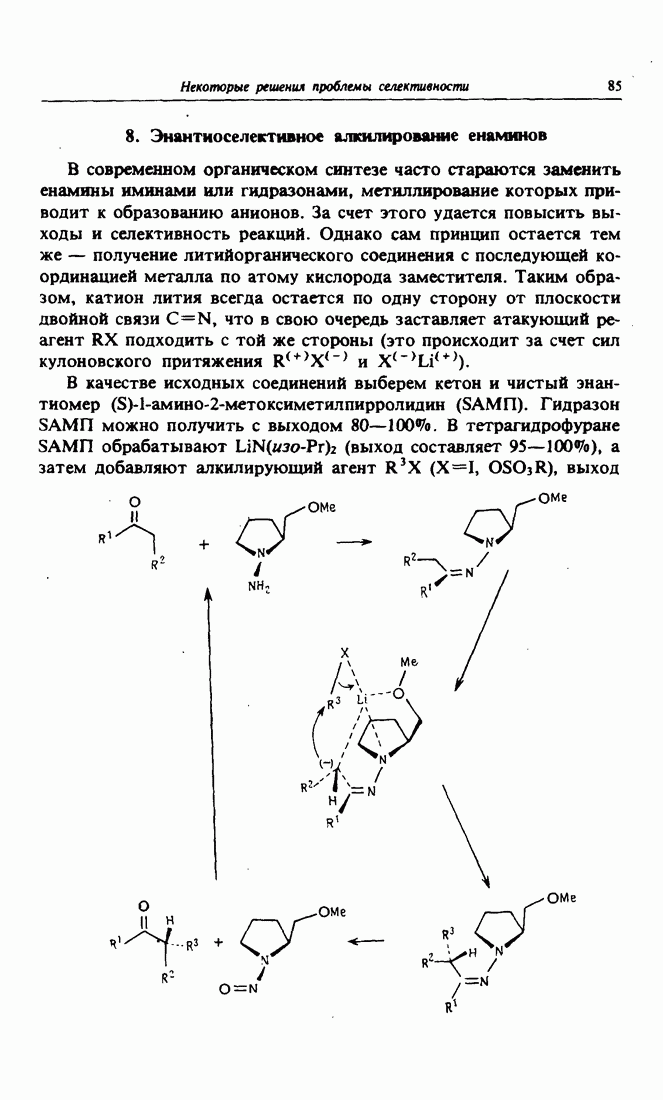
- 8. Энантиоселективное алкилирование енаминов
- 9. Перенос хиральности
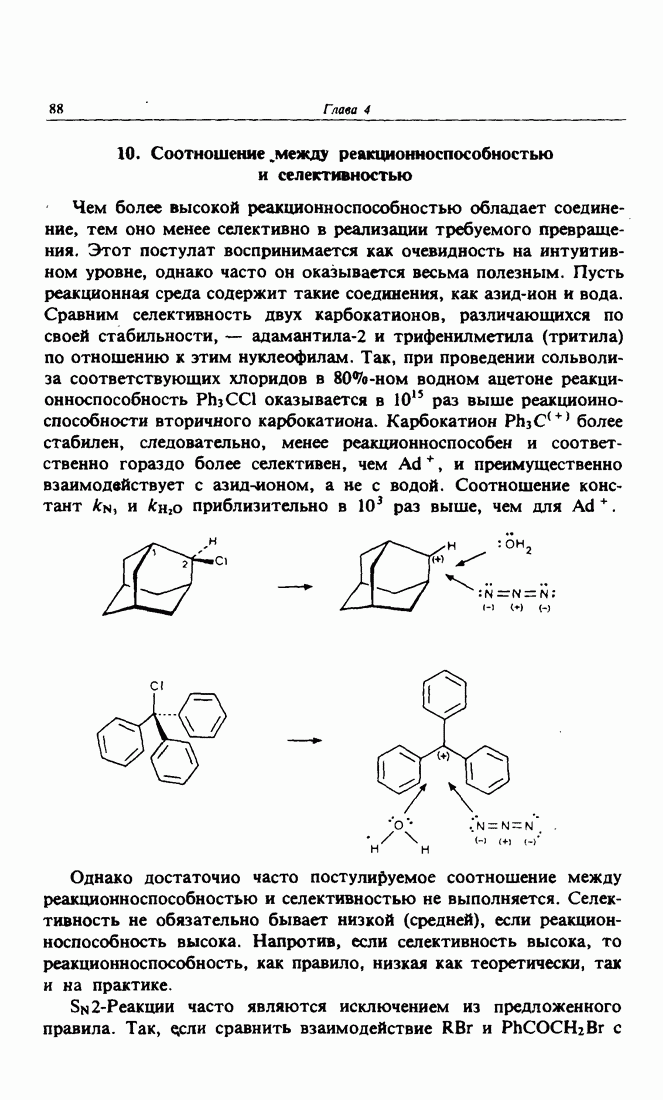
- 10. Соотношение между реакционноспособностью и селективностью
- 11. Стереоэлектронный эффект
- 12. Конформации переходного состояния «кресло» и «ванна»
- Глава 5. ЗАЩИТА И РЕГЕНЕРАЦИЯ ФУНКЦИОНАЛЬНЫХ ГРУПП. СПИРТОВАЯ И КАРБОНИЛЬНАЯ ГРУППЫ. ОБРАЩЕНИЕ ПОЛЯРНОСТИ
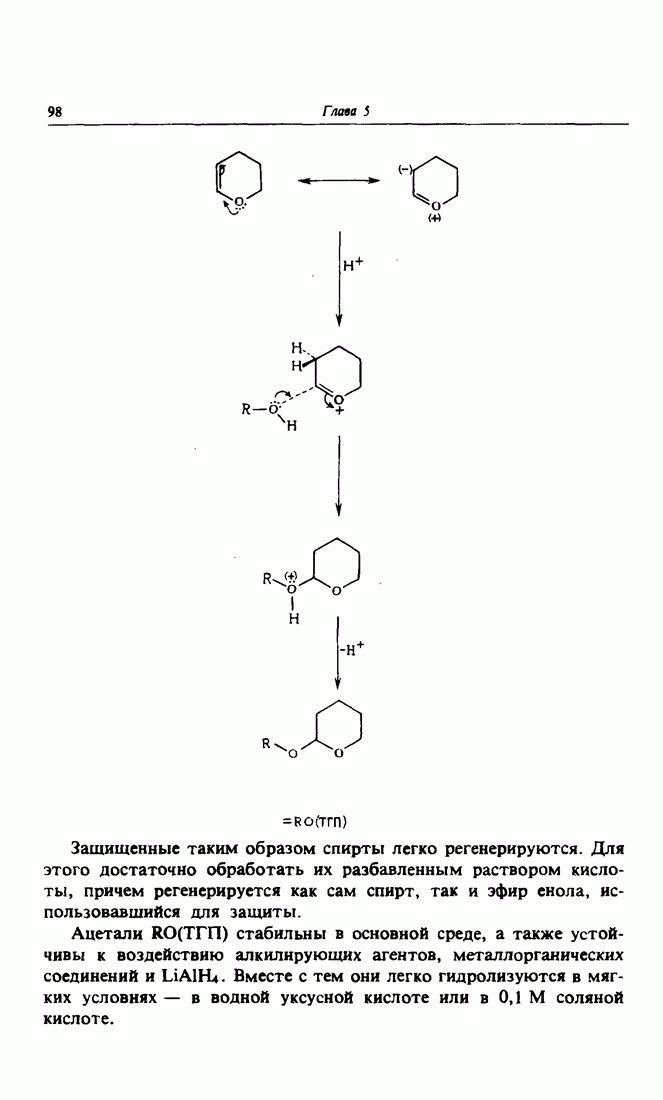
- 1. Защита карбонильной группы ацетальной
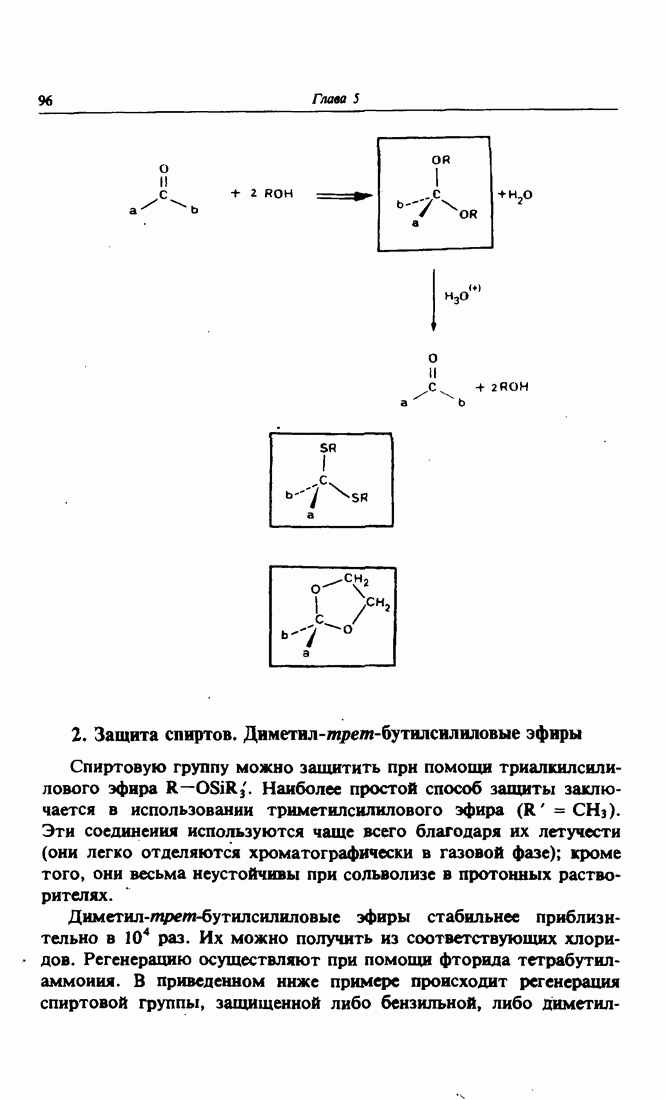
- 2. Защита спиртов. Диметил-трет-бутилсилиловые эфиры
- 3. Защита спиртовых групп при помощи эфиров енолов
- 4. Обращение полярности
- 5. Э. Дж. Кори
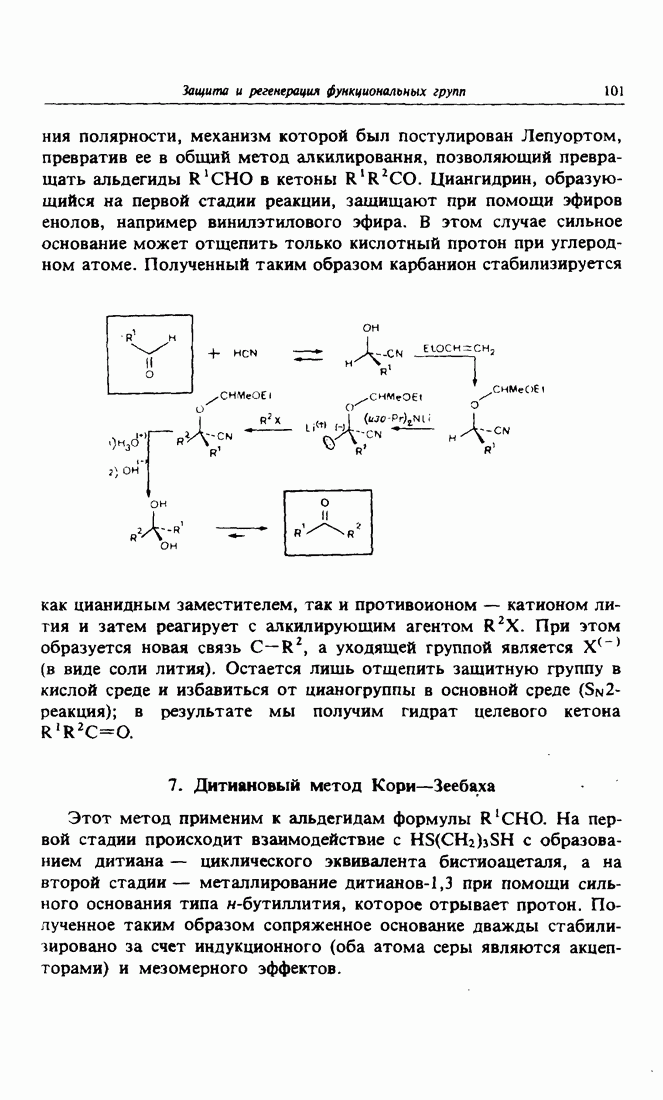
- 6. Инверсия полярности по методу Лепуорта — Шторка
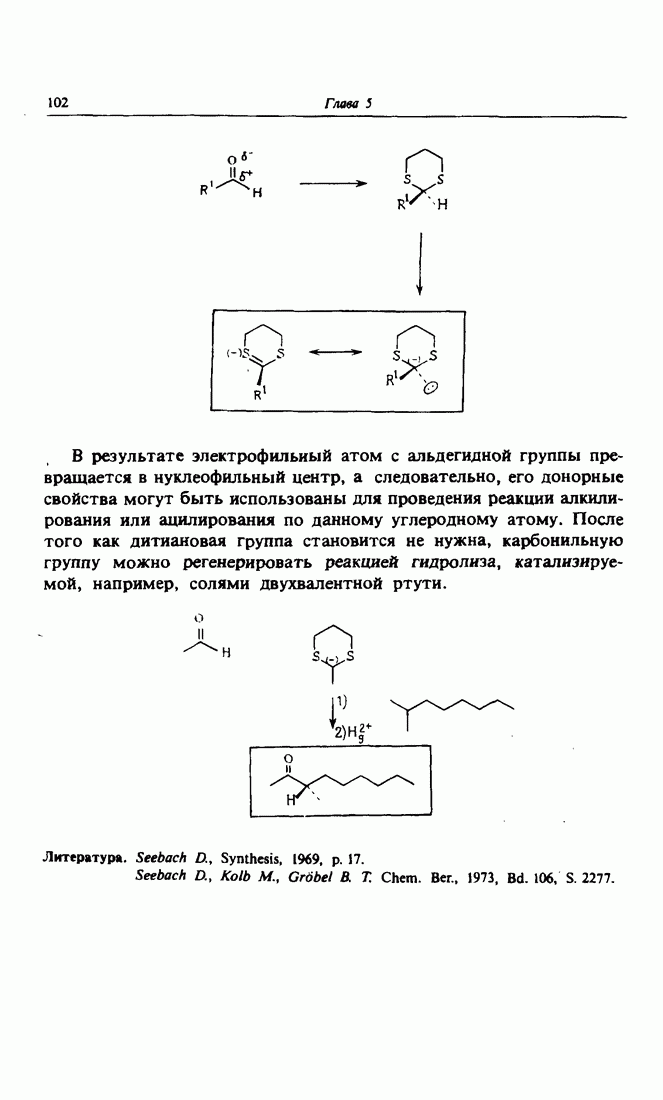
- 7. Дитиановый метод Кори-Зеебаха
- Главе 6. АКТИВАЦИЯ
- 2. Стабилизация конечного состояния
- 3. Дестабилизация начального состояния
- 4. Стабилизация переходного состояния
- Главв 7. ПОСТРОЕНИЕ ЦИКЛОВ
- 2. Региоселективность
- 3. Реакция Дильса — Альдера в условиях обращенного электронного соответствия
- 4. Стереоселективность в реакциях Дильса — Альдера
- 5. Напряжение в циклах
- 6. Построение циклобутанов (метод 1) Термическая димеризация
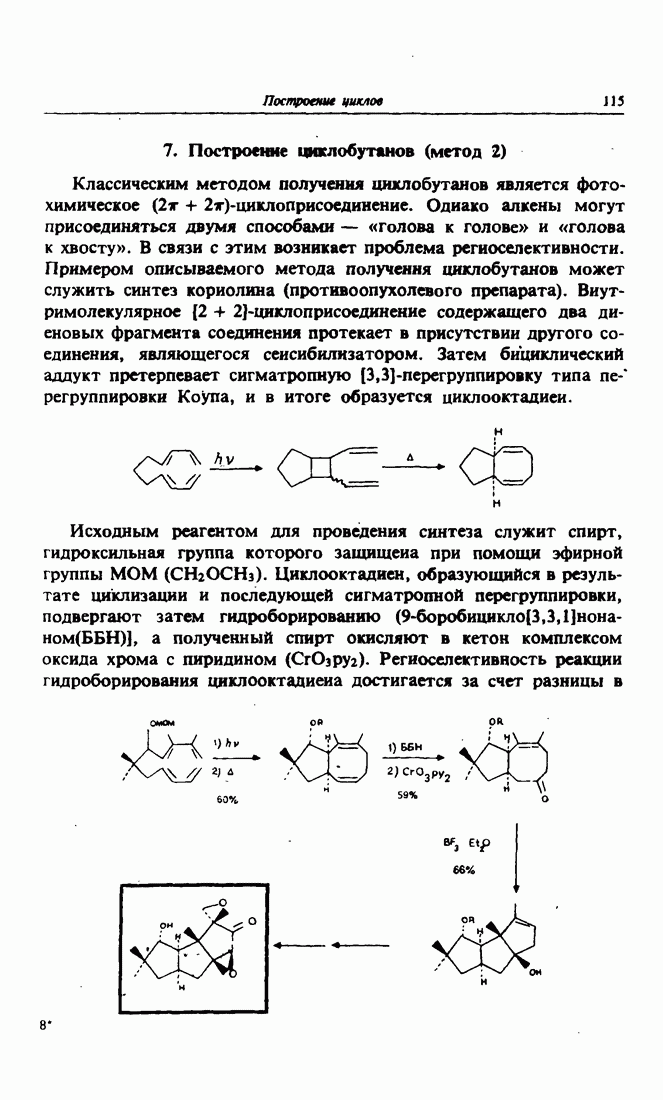
- 7. Построение циклобутанов (метод 2)
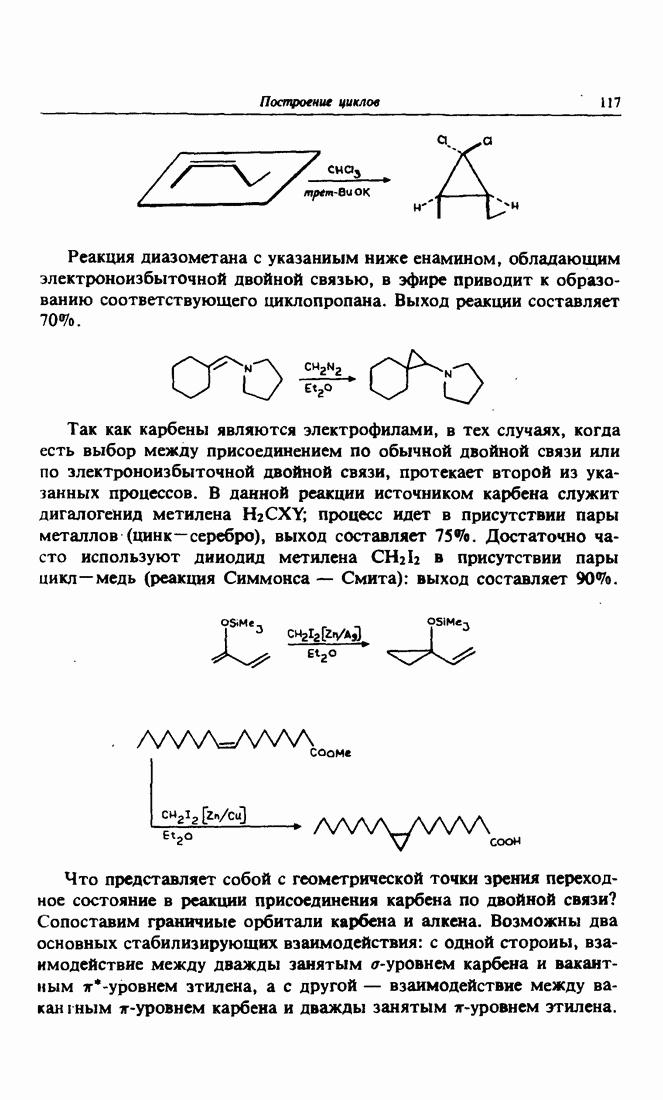
- 8. Синтез циклопропанов. Присоединение карбенов к алкенам
- Глааа 8. ВВЕДЕНИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП. РЕАКЦИИ ЗАМЕЩЕНИЯ
- 2. Соотношение структура — реакционноспособность
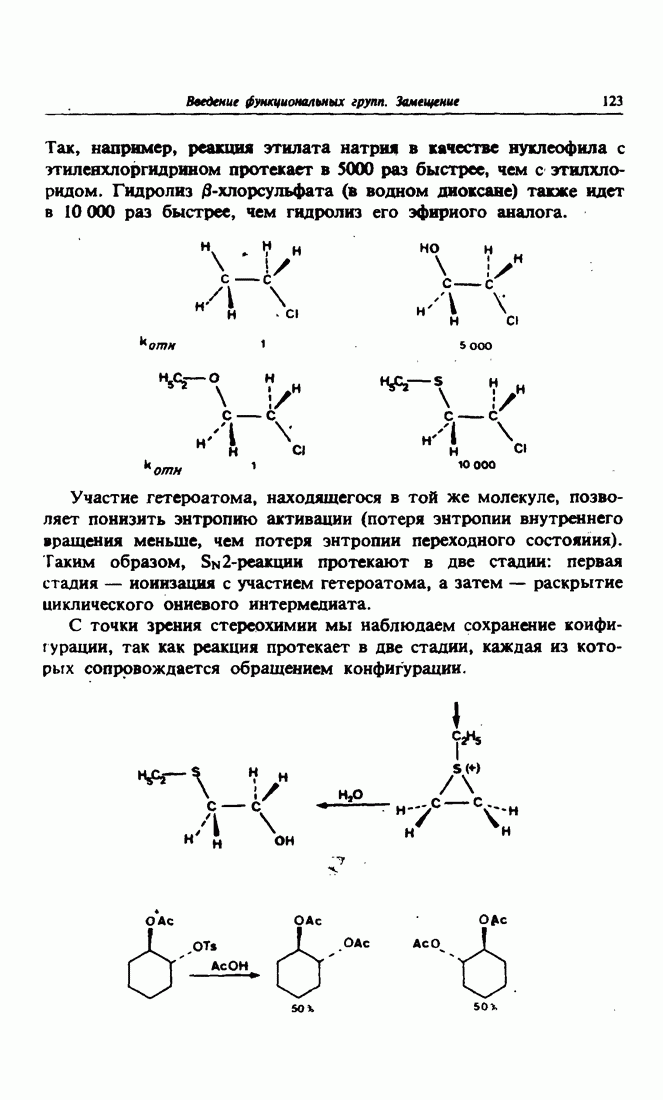
- 3. Участие соседней группы в Sn2-реакциях
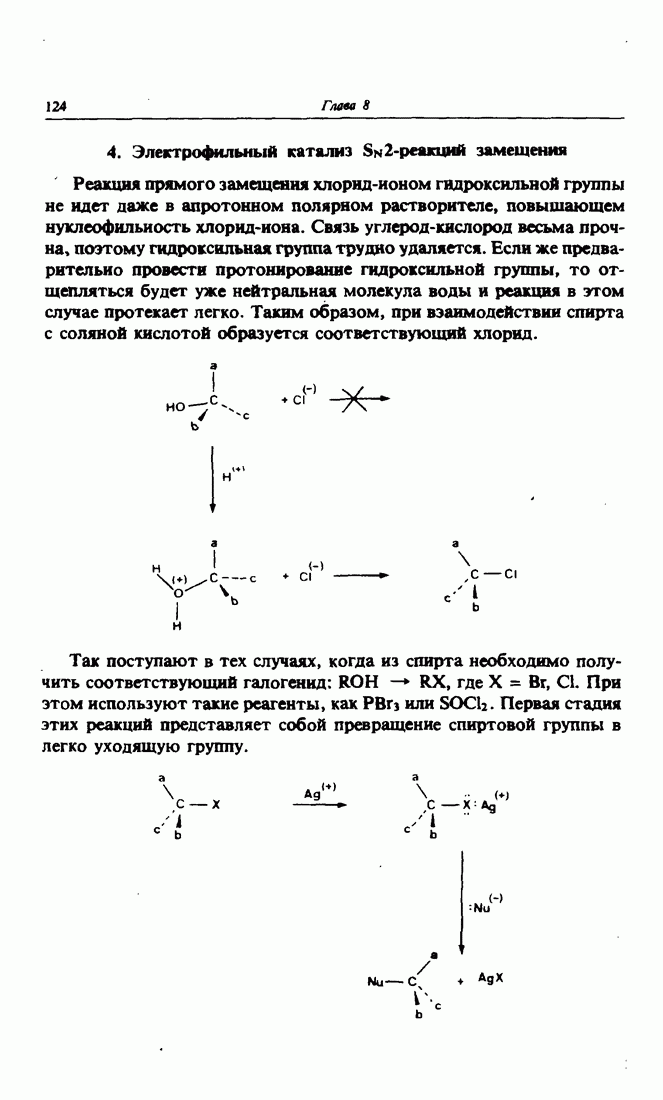
- 4. Электрофильный катализ Sn2-реакций замещения
- 5. Региоселеггивность в реакциях алкилирования
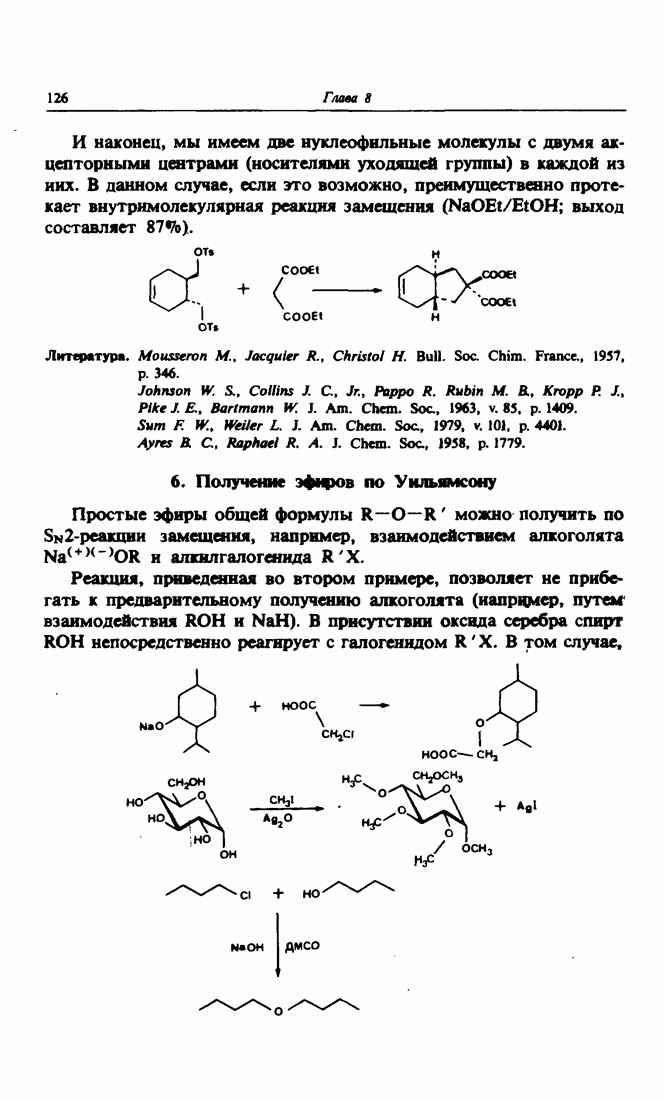
- 6. Получение эфиров по Уильямсону
- 7. К вопросу об обозначениях
- Глава 9. ВВЕДЕНИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП. РЕАКЦИИ ВОССТАНОВЛЕНИЯ
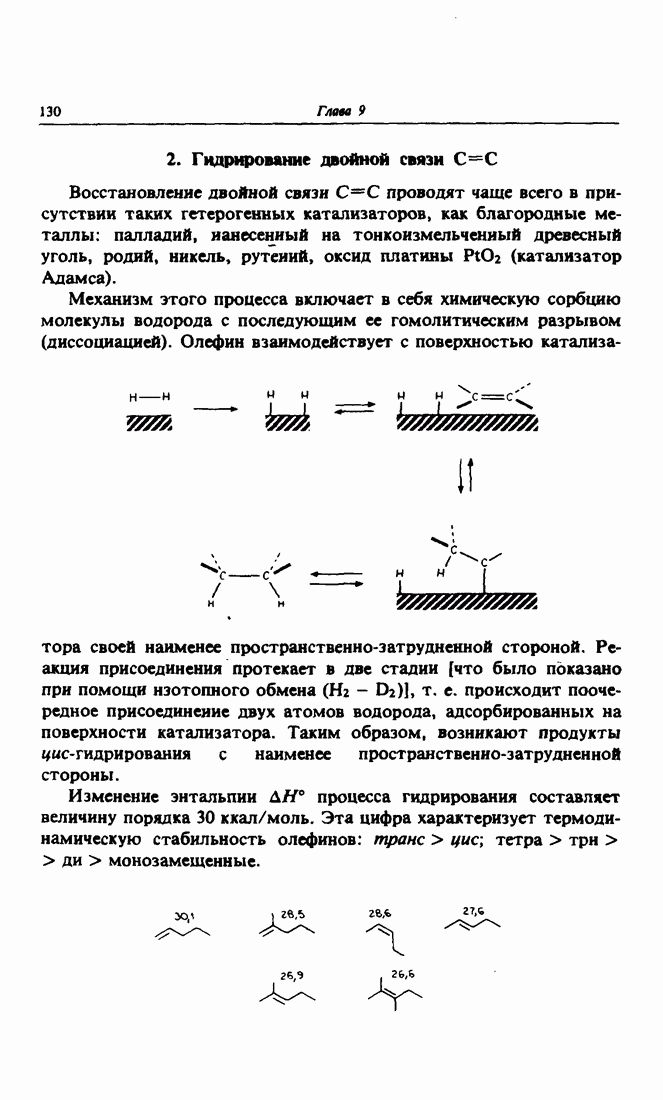
- 2. Гидрирование двойной связи С=С
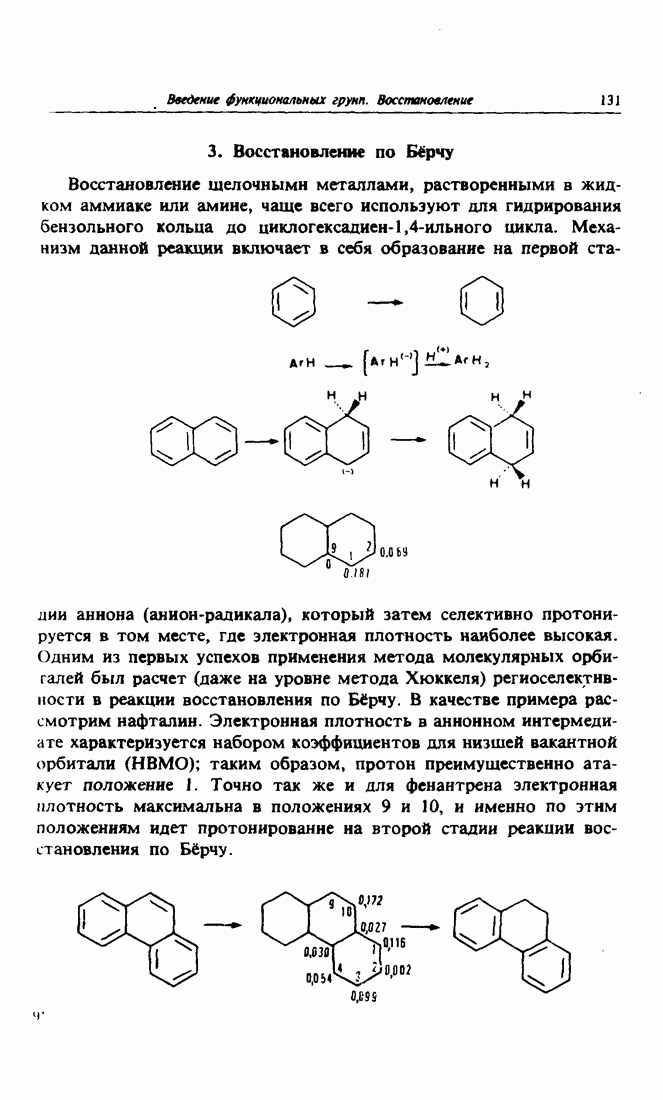
- 3. Восстановление по Бёрчу
- 4. Восстановление карбонильной группы
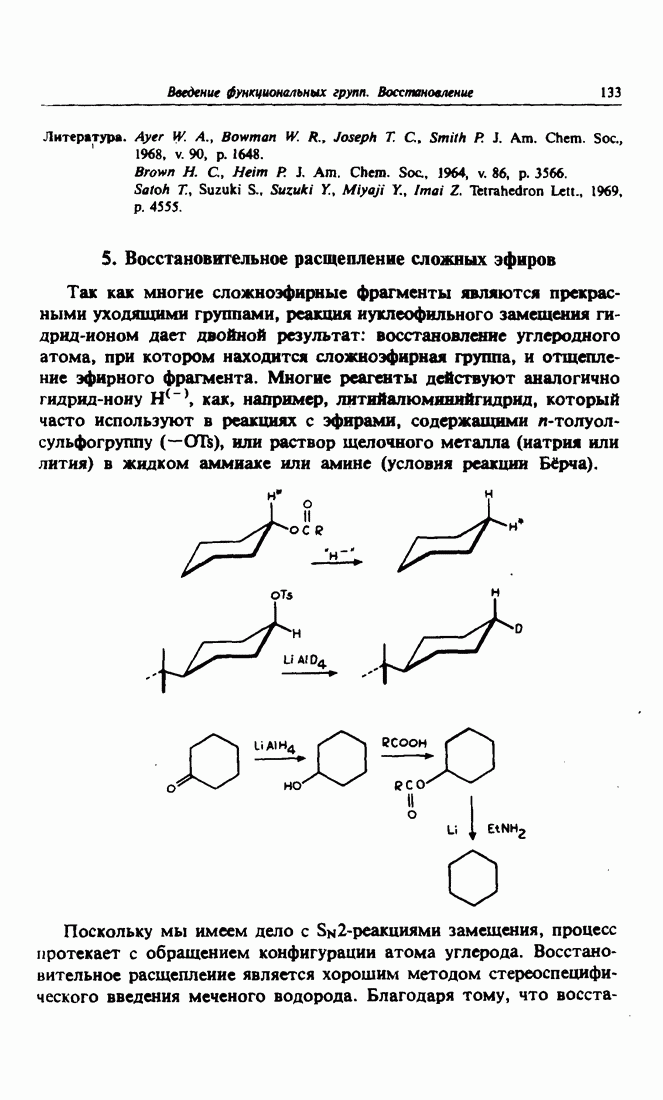
- 5. Восстановительное расщепление сложных эфиров
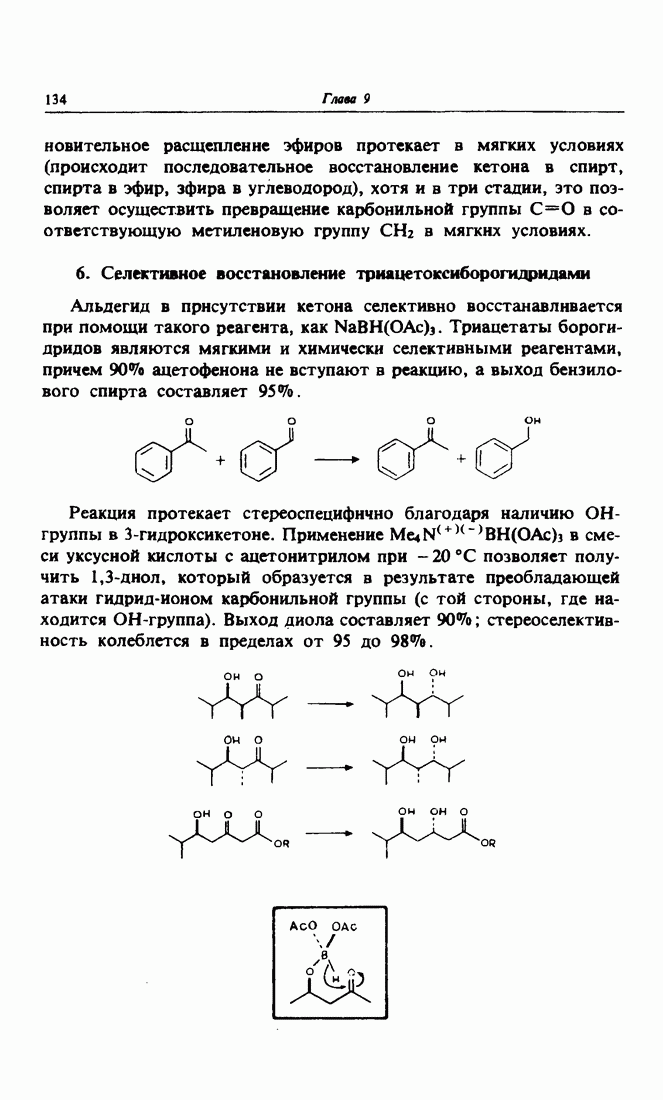
- 6. Селективное восстановление триацетоксиборогидридами
- Глава 10. ВВЕДЕНИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП. РЕАКЦИИ ОКИСЛЕНИЯ
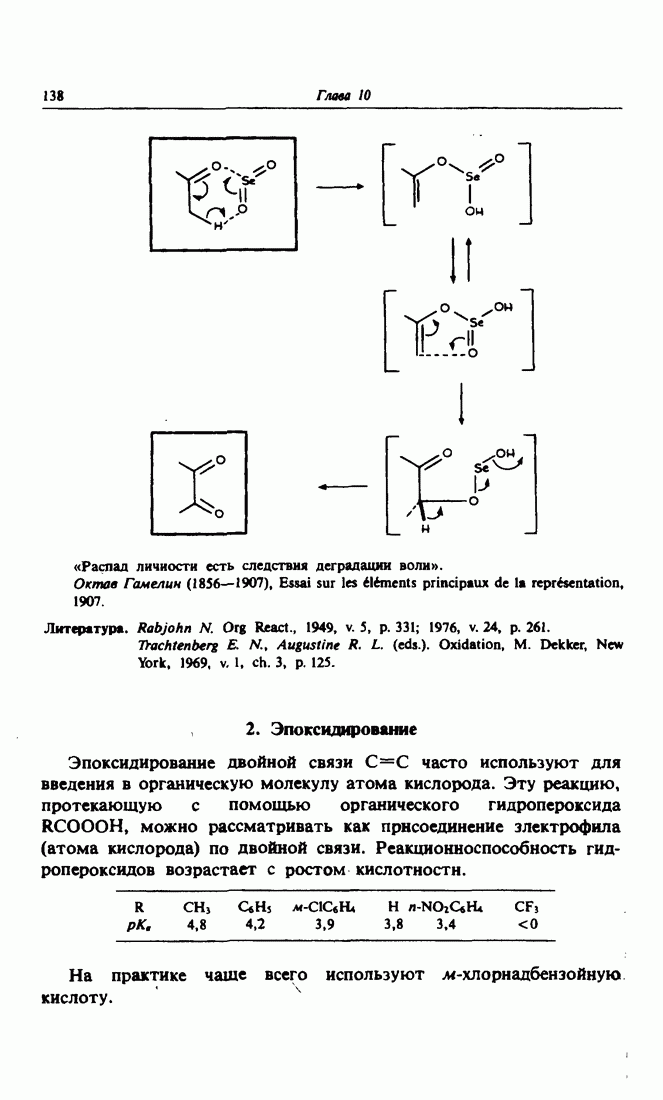
- 2. Эпоксидирование
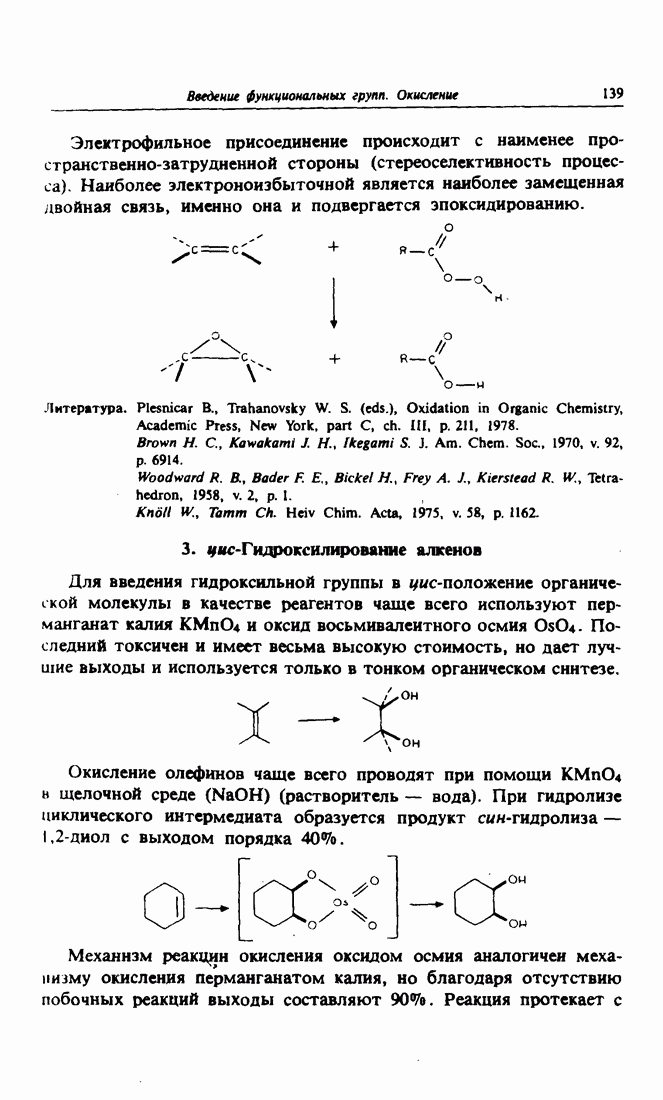
- 3. цис-Гидроксилирование алкенов
- 4. Расщепление 1,2-диолов
- 5. Озонолиз алкенов
- 6. Окисление спиртов
- Главе 11. РЕАКЦИИ ПРИСОЕДИНЕНИЯ И ЭЛИМИНИРОВАНИЯ
- 2. Классически механизм реакции электрофильного присоединения. Правило Марковникова
- 3. Основные электрофильные агенты
- 3.3. Присоединение гипохлоритов и гипобромитов
- 3.4. Оксимеркурирование
- 3.5. Гидроборирование
- 3.6. Окситаллирование
- 4. Стереохимия реакции присоединения по двойной связи С=С
- 5. Конкуренция нуклеофила и растворителя в реакции электрофильного присоединения
- 6. Присоединение к напряженным олефинам: цис-присоединение
- 7. Стереохимия реакций бимолекулярного элиминирования
- 8. Виды b-элиминирования
- Главв 12. ПЕРЕГРУППИРОВКИ ФУНКЦИОНАЛЬНЫХ ГРУПП. ПРЕВРАЩЕНИЕ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ В ОЛЕФИНЫ ПО РЕАКЦИИ ВИТТИГА
- 2. Реакция Дарзана
- 3. Дарзан — один из великих политехников
- 4. Обобщение и модернизация метода
- 5. Стереоселективность реакции Кори — Чайковского
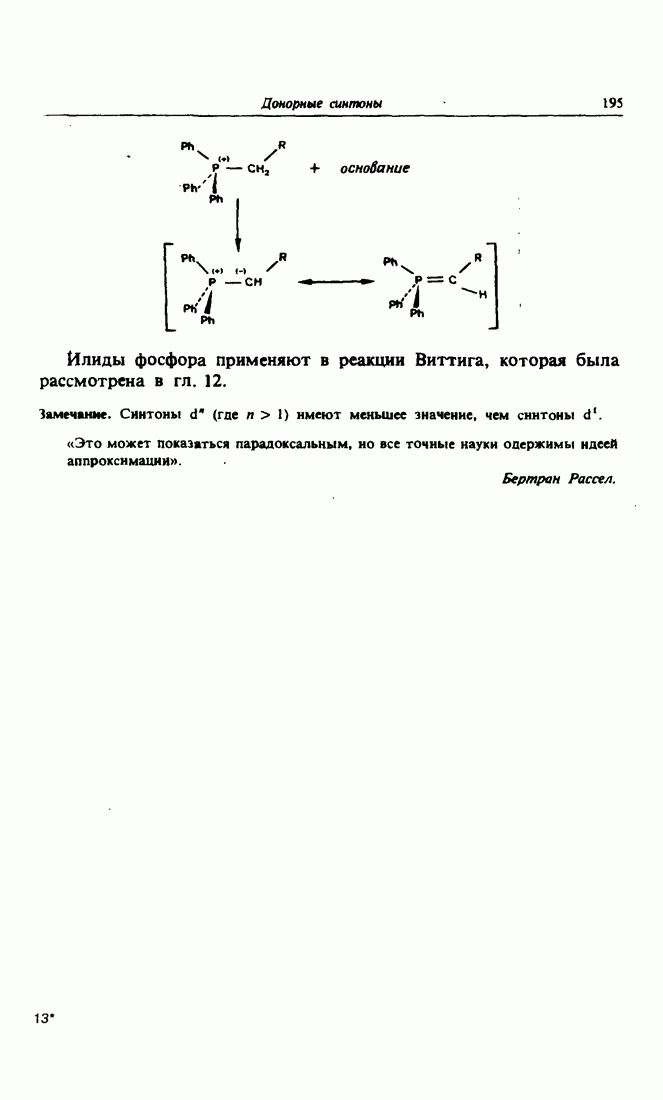
- 6. Реакция Виттига
- 7. Георг Виттиг
- 8. Причины образования различных продуктов в реакциях Виттига и Кори — Чайковского
- 9. Разновидность реакции Виттига: олефинирование по Петерсону
- Главе 13. ПЕРЕГРУППИРОВКИ
- 2. 1,2-Переход в карбокатионах
- 3. Перегруппировка Бекмана
- 4. Перегруппировка Курциуса
- 5. Перегруппировка Байера — Виллигера
- 6. Реакция Рамберга-Беклунда
- Глава 14. ДОНОРНЫЕ СИНТОНЫ
- 2. Алкильные донорные синтоны
- 3. Донорные синтоны d1 с гетероатомами, обладающими d-орбиталью
- Глава 15. АКЦЕПТОРНЫЕ СИНТОНЫ
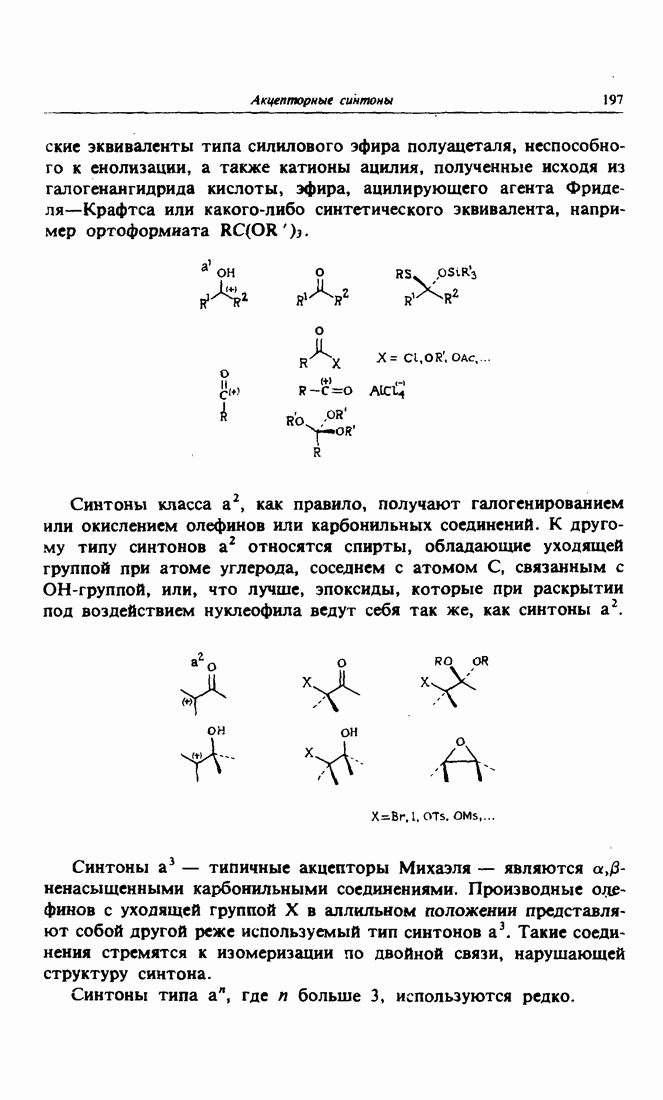
- 1. Синтоны-акцепторы
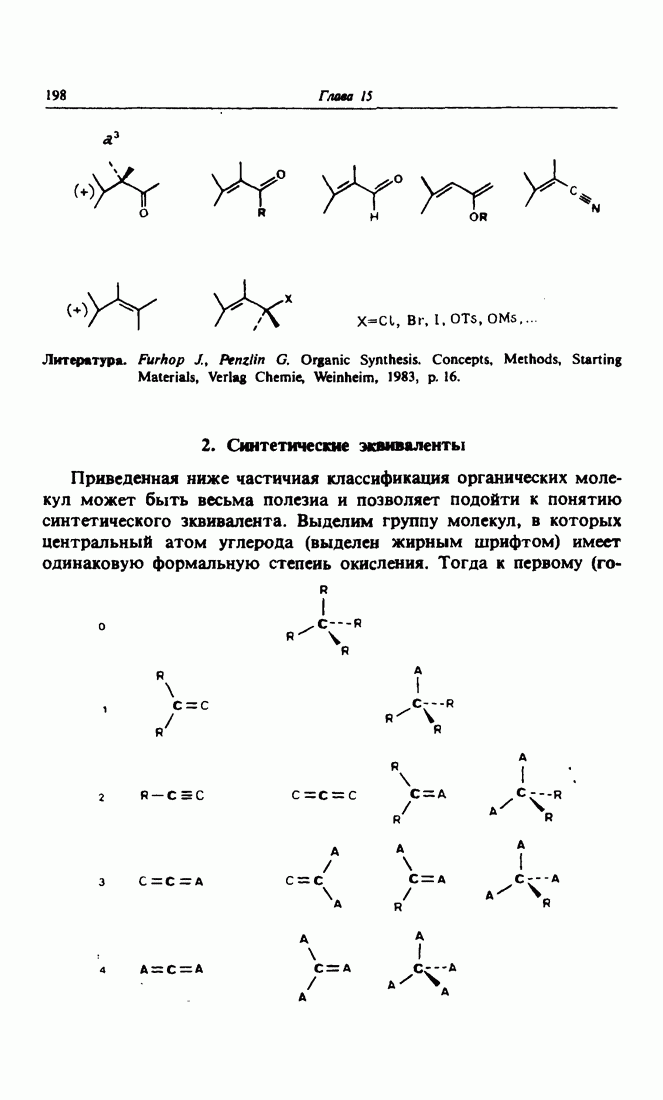
- 2. Синтетические эквиваленты
- 3. Контролируемое образование новых связей
- 4. Расчленение молекулы на фрагменты
- 5. Двойное расчленение молекулы
- 6. Изменение реакционноспособности в результате обращения полярности
- Глава 16. РЕТРОСИНТЕТИЧЕСКИЙ АНАЛИЗ
- 2. Цепь превращений
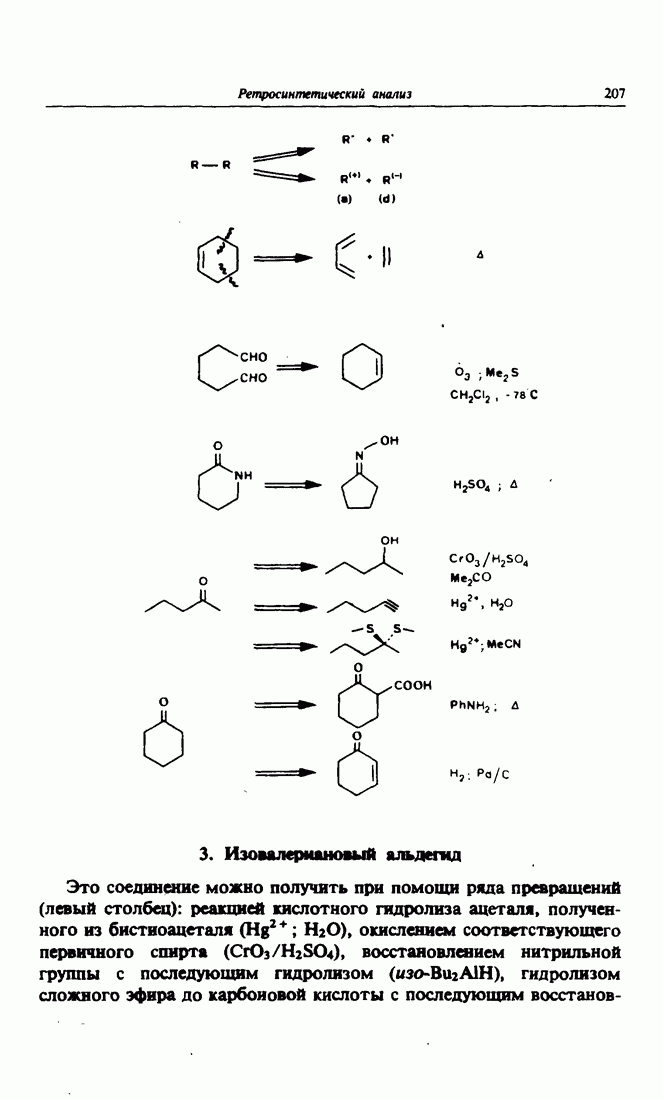
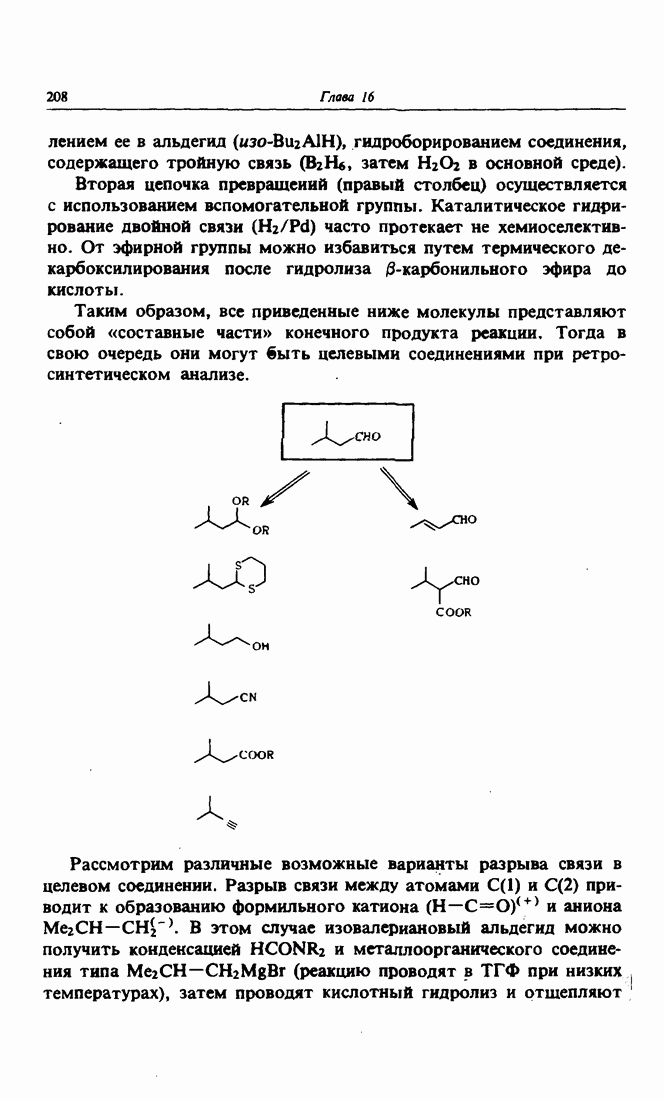
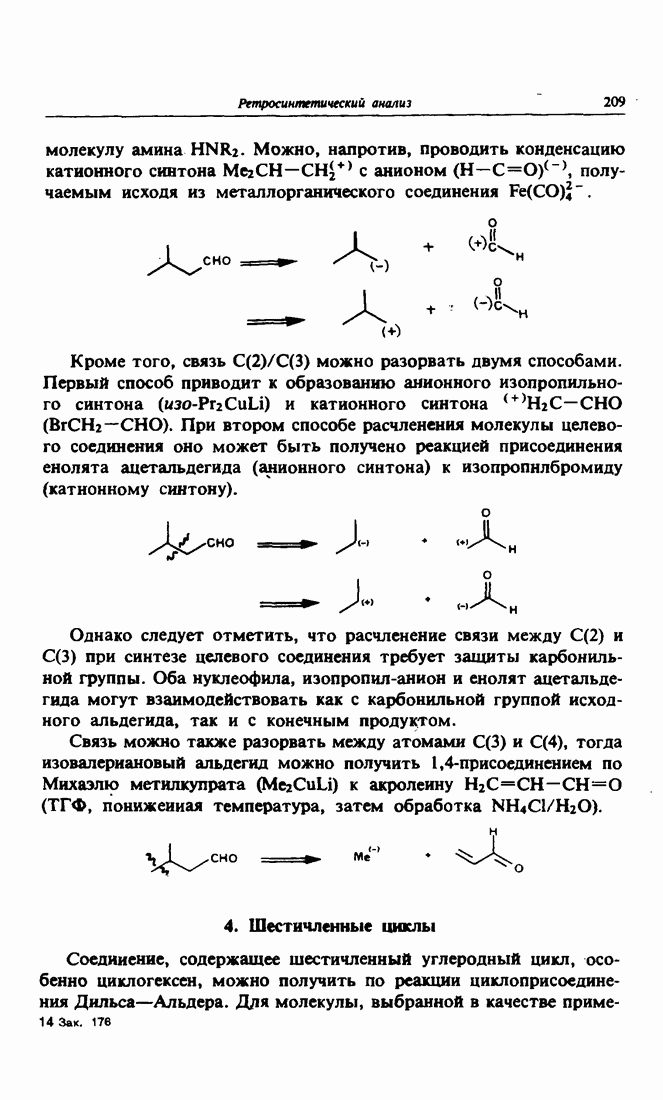
- 3. Изовалериановый альдегид
- 4. Шестичленные циклы
- 5. Циклизация по Робинсону
- 6. Ретроальдольная конденсация
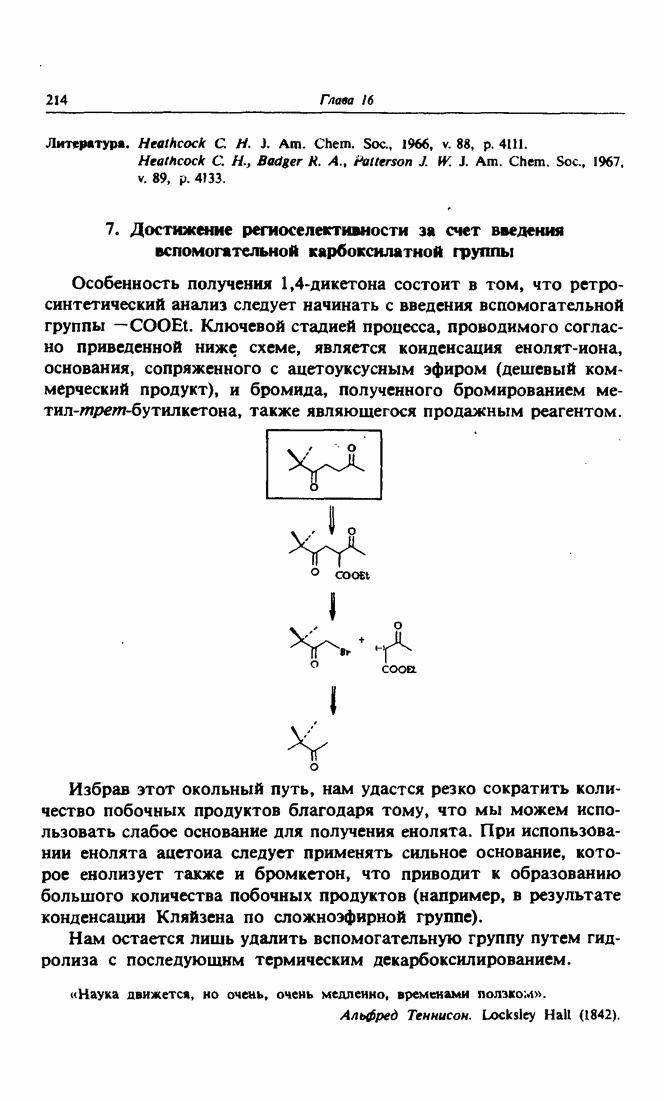
- 7. Достижение региоселективности за счет введения вспомогательной карбоксилатной группы
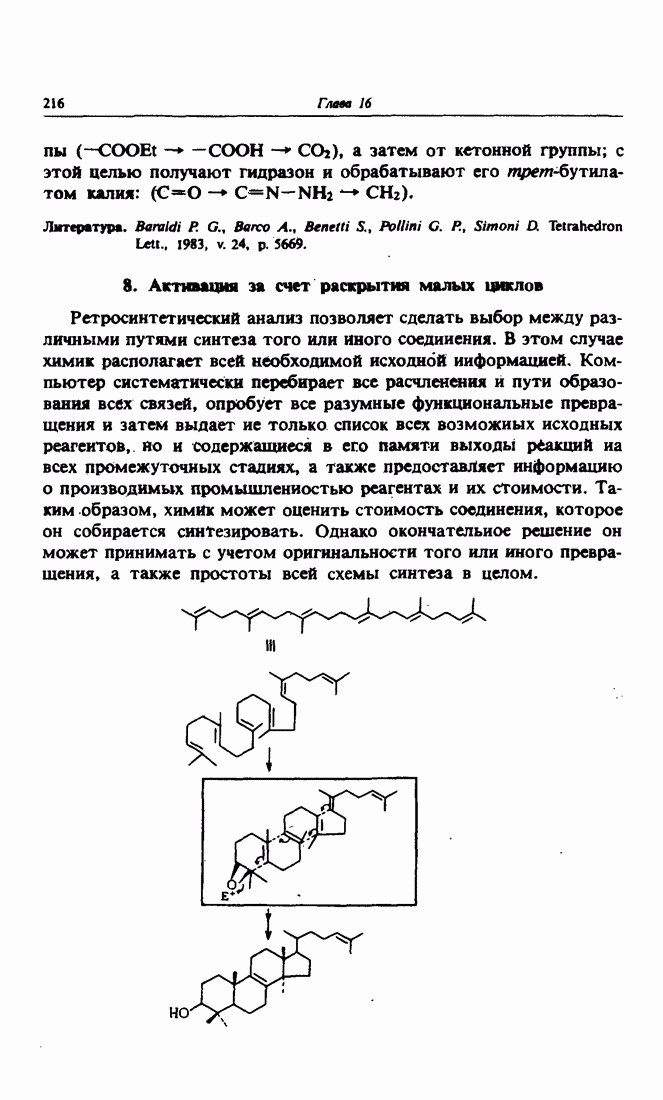
- 8. Активация за счет раскрытия малых циклов
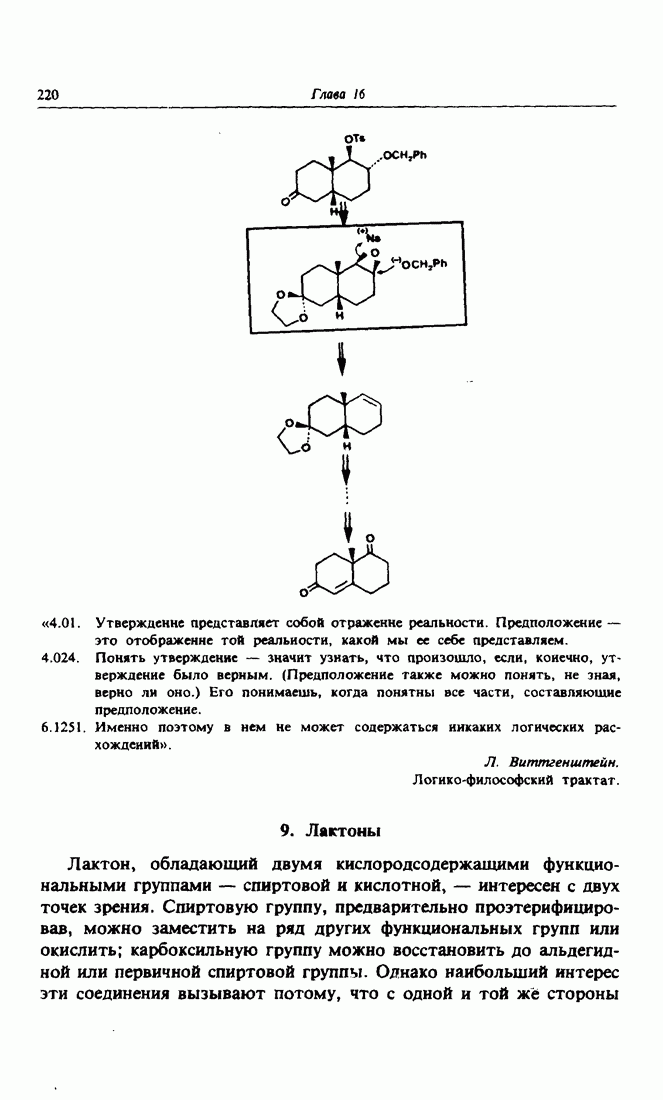
- 9. Лактоны
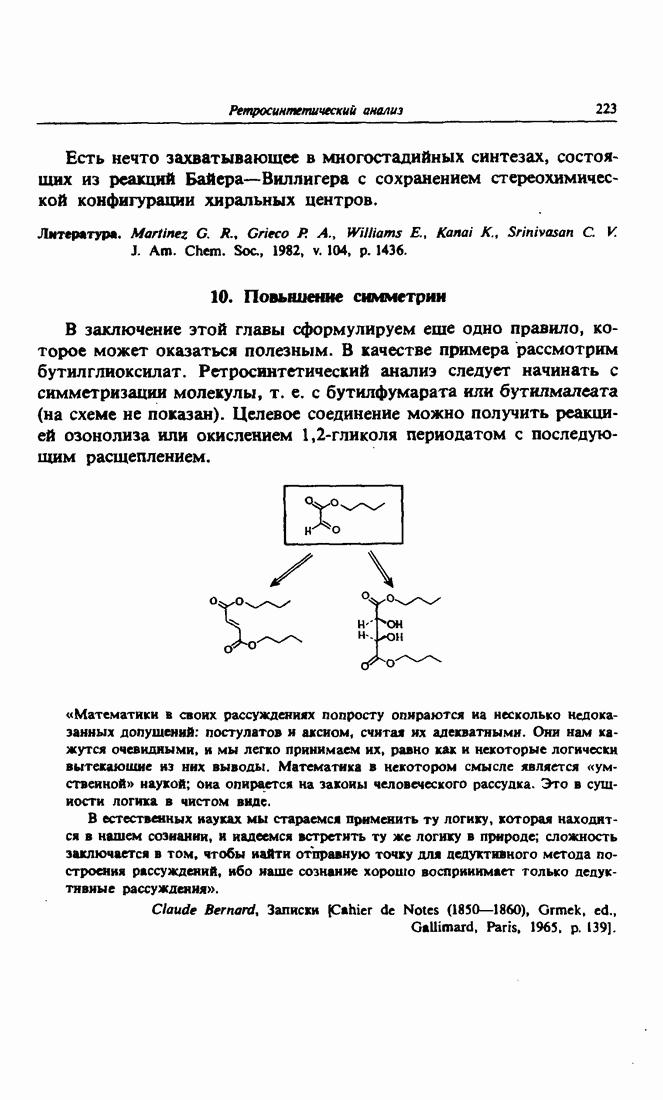
- 10. Повышение симметрии
- ПОСЛЕСЛОВИЕ