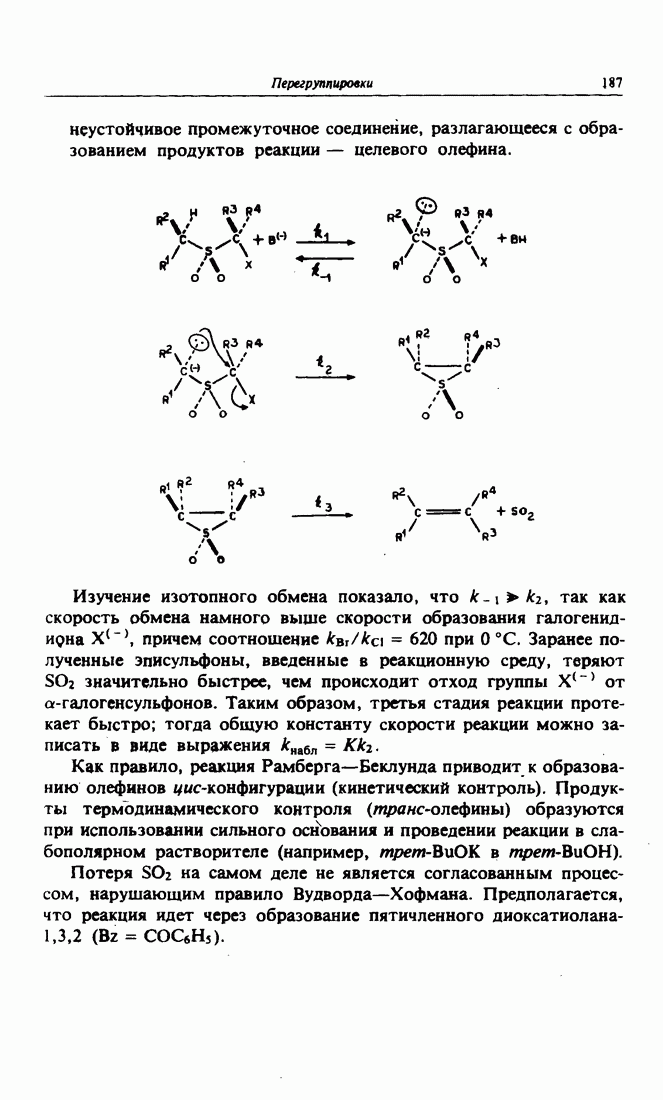
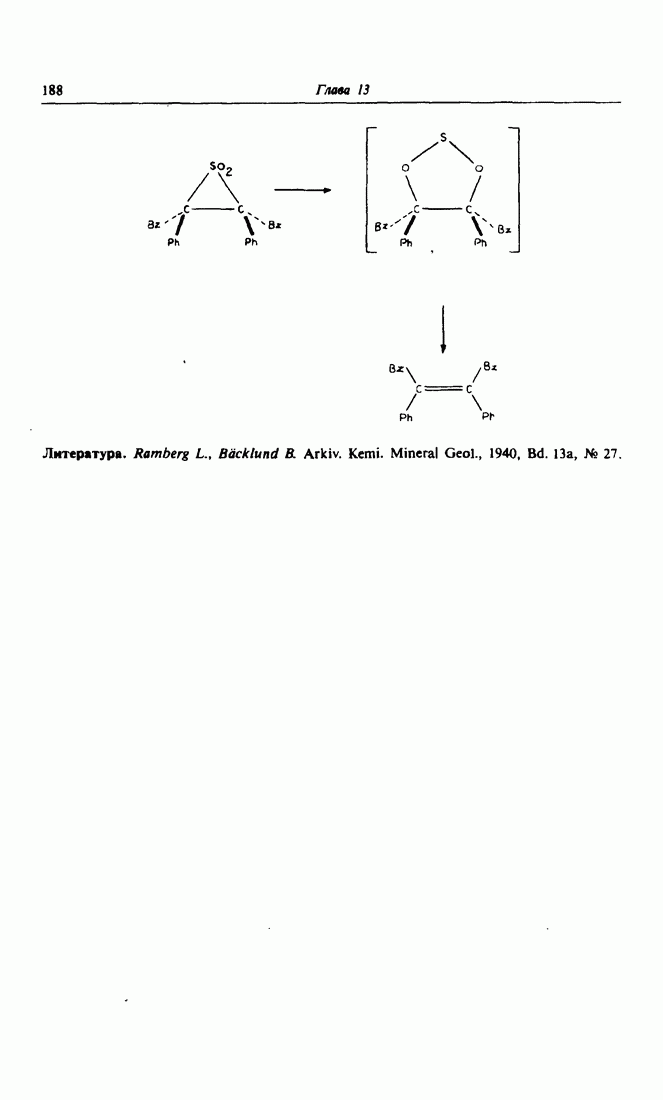
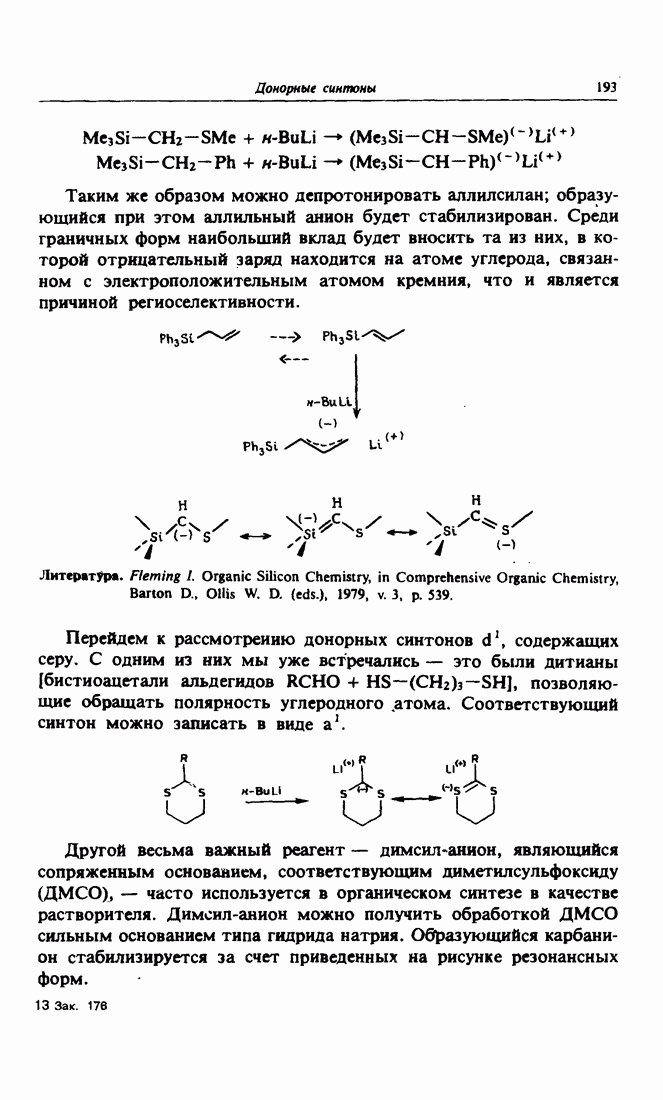
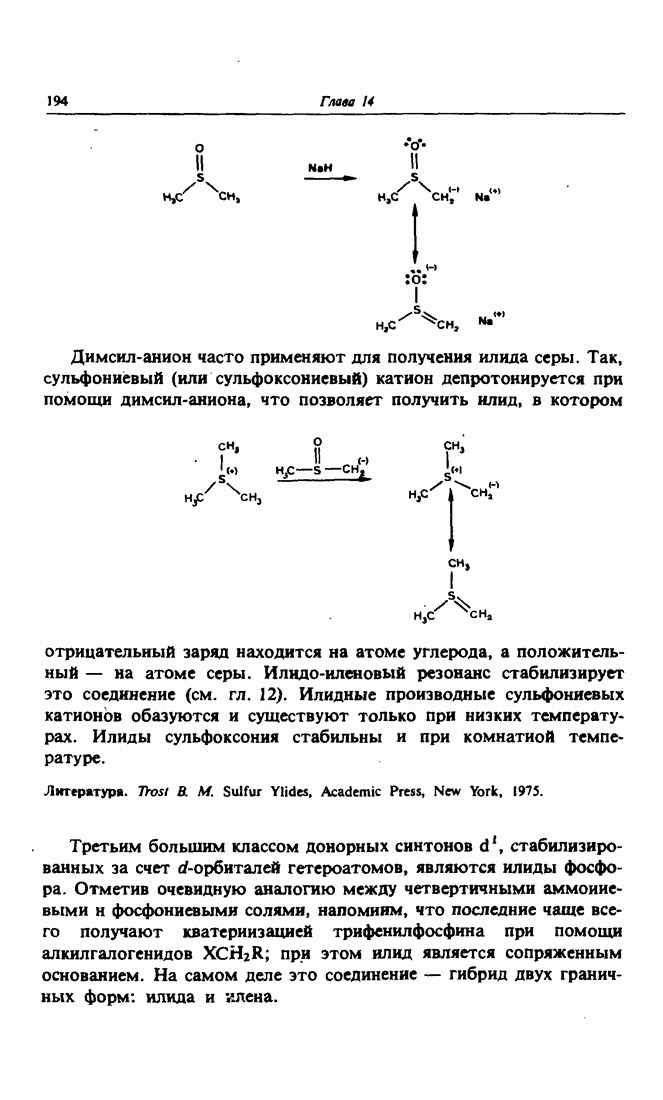
| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
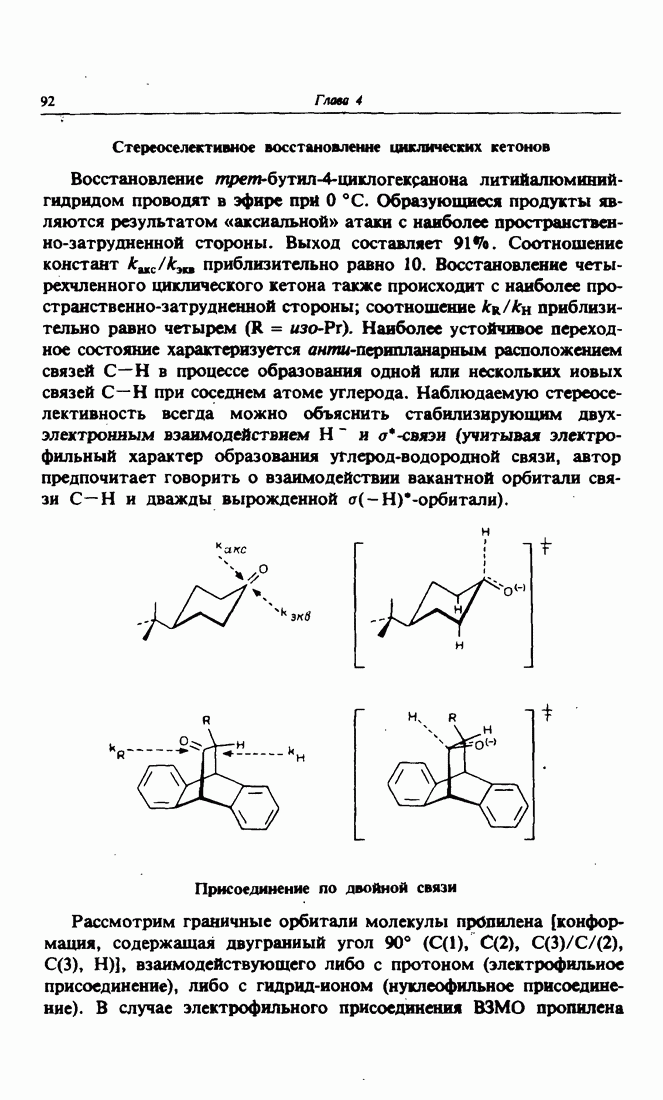
2. 1,2-Переход в карбокатионах
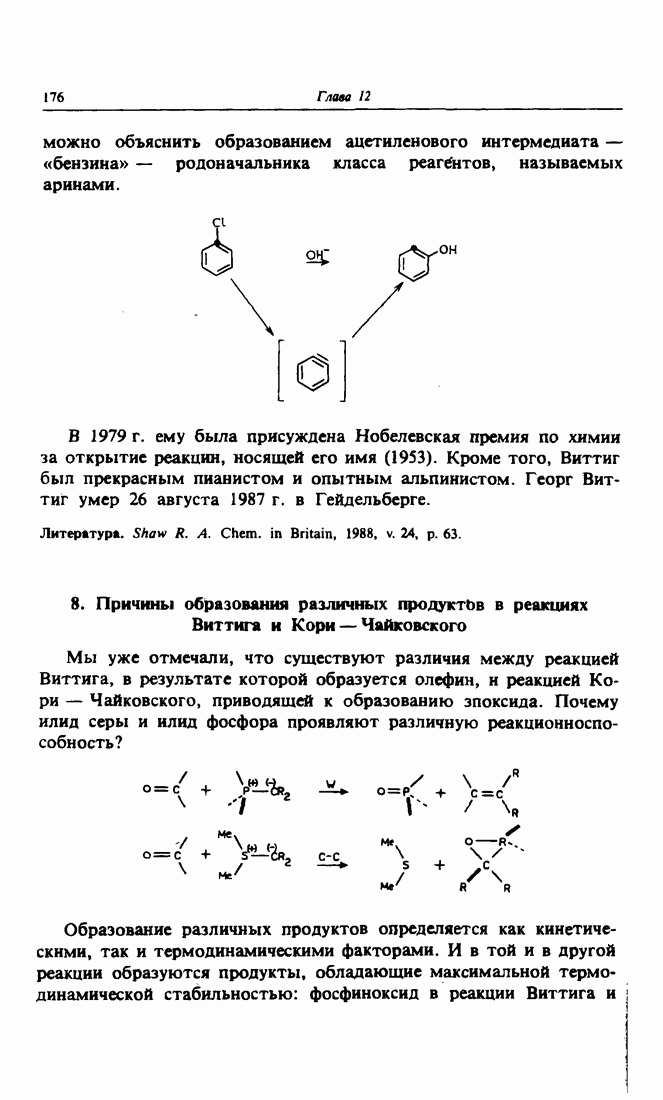
Причина многих перегруппировок — дефицит электронной плотности, в результате которого происходит миграция соседней группы с целью ее компенсации. Примером подобного изменения структуры может служить 1,2-переход в карбокатионах
Вагнера-Меервейна. В результате гетеролитического разрыва связи  где
где  уходящая группа, атом углерода
уходящая группа, атом углерода  приобретает положительный заряд. В результате происходит согласованное или двухстадийкое перемещение
приобретает положительный заряд. В результате происходит согласованное или двухстадийкое перемещение  -связи
-связи  при атоме углерода
при атоме углерода  к атому углерода
к атому углерода  водород, алкильная или арильная группа).
водород, алкильная или арильная группа).

Тогда положительный заряд переходит на атом углерода  при этом происходит отщепление протона или присоединение нуклеофила
при этом происходит отщепление протона или присоединение нуклеофила  в результате чего карбокатион становится нейтральной молекулой. Было отмечено, что, как правило, мигрирующая связь
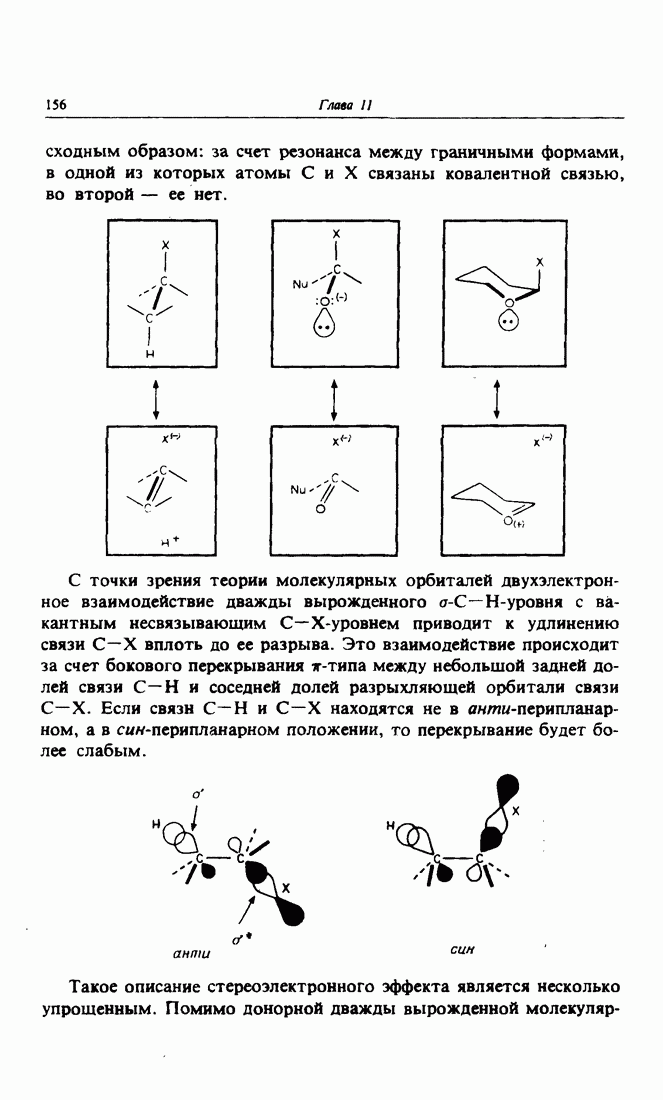
в результате чего карбокатион становится нейтральной молекулой. Было отмечено, что, как правило, мигрирующая связь  находится в анти-перипланарном положении по отношению к связи
находится в анти-перипланарном положении по отношению к связи  и уходящей группе. Так как реакция чаще всего протекает не синхронно, а в две стадии, геометрические требования менее строги: достаточно того, чтобы связь
и уходящей группе. Так как реакция чаще всего протекает не синхронно, а в две стадии, геометрические требования менее строги: достаточно того, чтобы связь  была копланарна с осью
была копланарна с осью  вакантной
вакантной  -орбитали атома
-орбитали атома  что соответствует принципу максимального перекрывания дважды вырожденного и
что соответствует принципу максимального перекрывания дважды вырожденного и  -вакантного уровней.
-вакантного уровней.

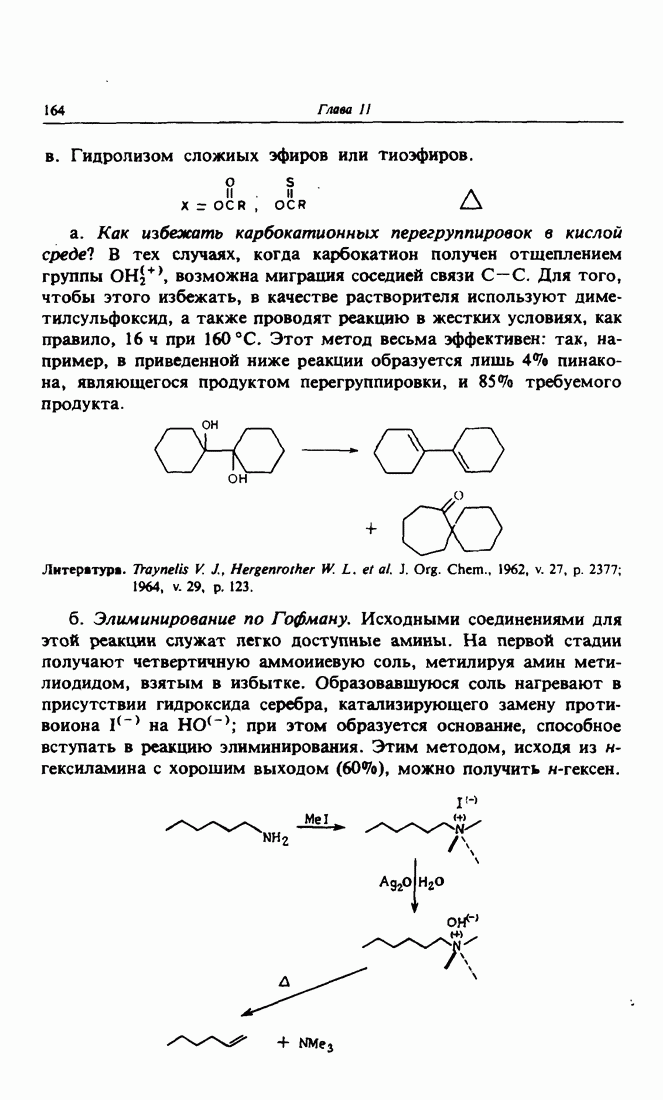
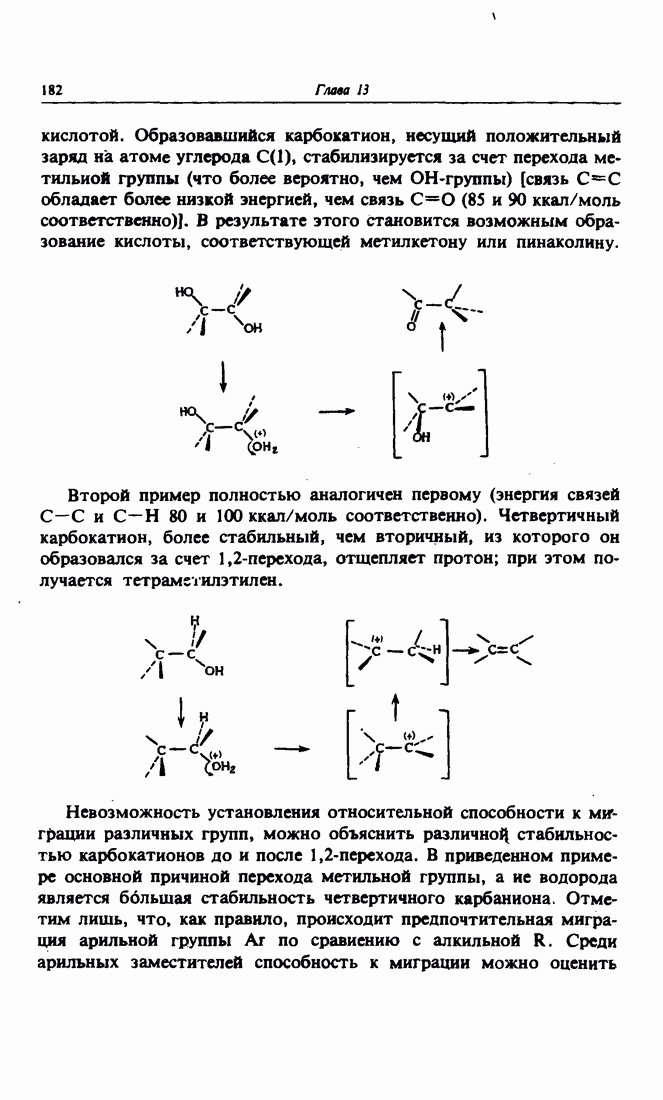
Типичным примером 1,2-перехода в карбокатионах является пинаколиновая перегруппировка. Изображенный на рисунке гликоль или пинакон (содержит четыре метильные группы) протонируется
кислотой. Образовавшийся карбокатион, несущий положительный заряд на атоме углерода  стабилизируется за счет перехода метальной группы (что более вероятно, чем ОН-группы) [связь
стабилизируется за счет перехода метальной группы (что более вероятно, чем ОН-группы) [связь  обладает более низкой энергией, чем связь
обладает более низкой энергией, чем связь  и 90 ккал/моль соответственно)]. В результате этого становится возможным образование кислоты, соответствующей метилкетону или пинаколину.
и 90 ккал/моль соответственно)]. В результате этого становится возможным образование кислоты, соответствующей метилкетону или пинаколину.

Второй пример полностью аналогичен первому (энергия связей  и
и  и 100 ккал/моль соответственно). Четвертичный карбокатион, более стабильный, чем вторичный, из которого он образовался за счет 1,2-перехода, отщепляет протон; при этом получается тетраметилэтилен.
и 100 ккал/моль соответственно). Четвертичный карбокатион, более стабильный, чем вторичный, из которого он образовался за счет 1,2-перехода, отщепляет протон; при этом получается тетраметилэтилен.

Невозможность установления относительной способности к миграции различных групп, можно объяснить различно стабильностью карбокатионов до и после 1,2-перехода. В приведенном примере основной причиной перехода метильной группы, а не водорода является большая стабильность четвертичного карбаниона. Отметим лишь, что, как правило, происходит предпочтительная миграция арильной группы  по сравнению с алкильной
по сравнению с алкильной  Среди арильных заместителей способность к миграции можно оценить
Среди арильных заместителей способность к миграции можно оценить
следующим образом:

Литература.
(см. скан)
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ РЕДАКТОРА
- ВВЕДЕНИЕ
- 1. Орбитальный и зарядовый контроль
- 2. Жесткие и мягкие кислоты и основания
- 3. Термохимические данные и их применение
- Глава 1. КАРБОНИЛЬНАЯ ГРУППА. РЕАКЦИИ ПРИСОЕДИНЕНИЯ И ПРИСОЕДИНЕНИЯ-ФРАГМЕНТАЦИИ
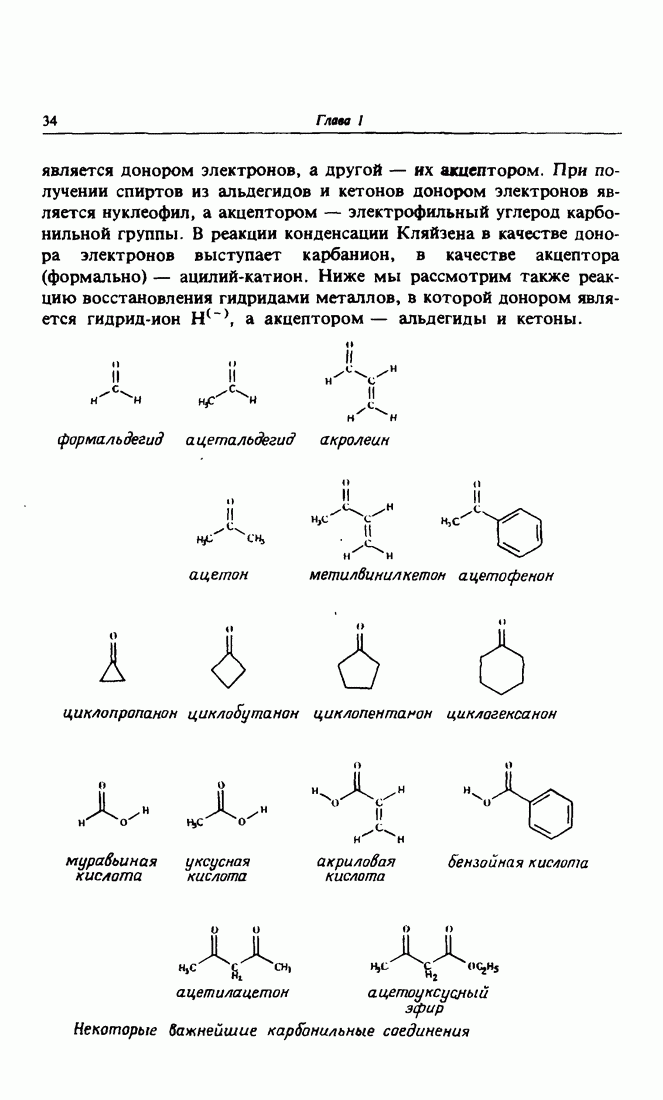
- 1. Карбонильная группа. Простое орбитальное описание
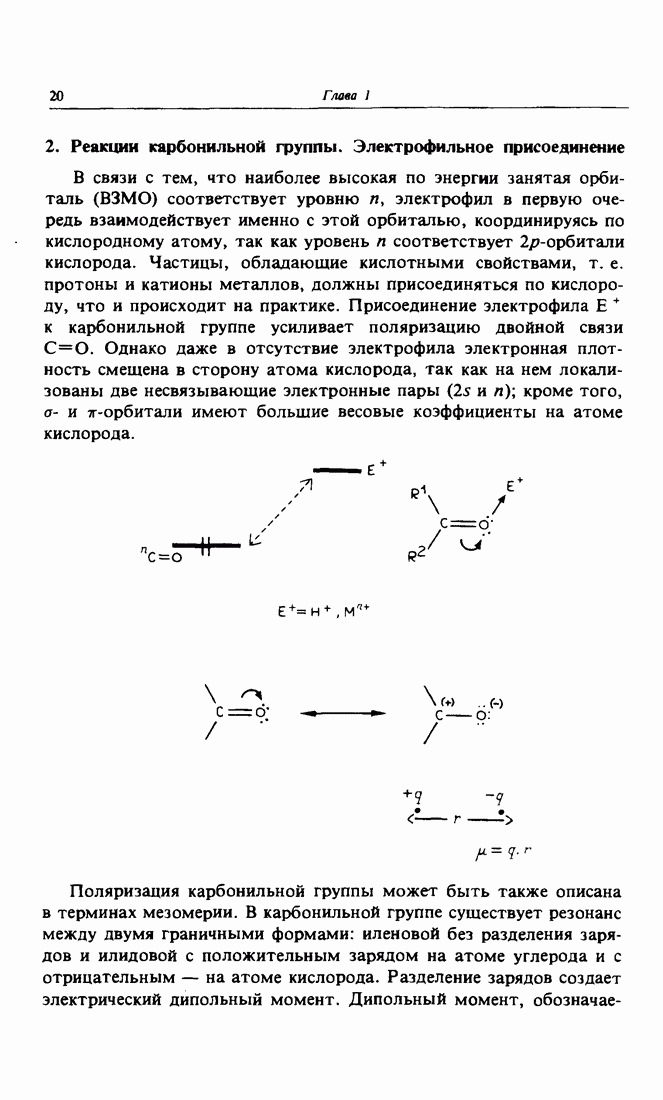
- 2. Реакции карбонильной группы. Электрофильное присоединение
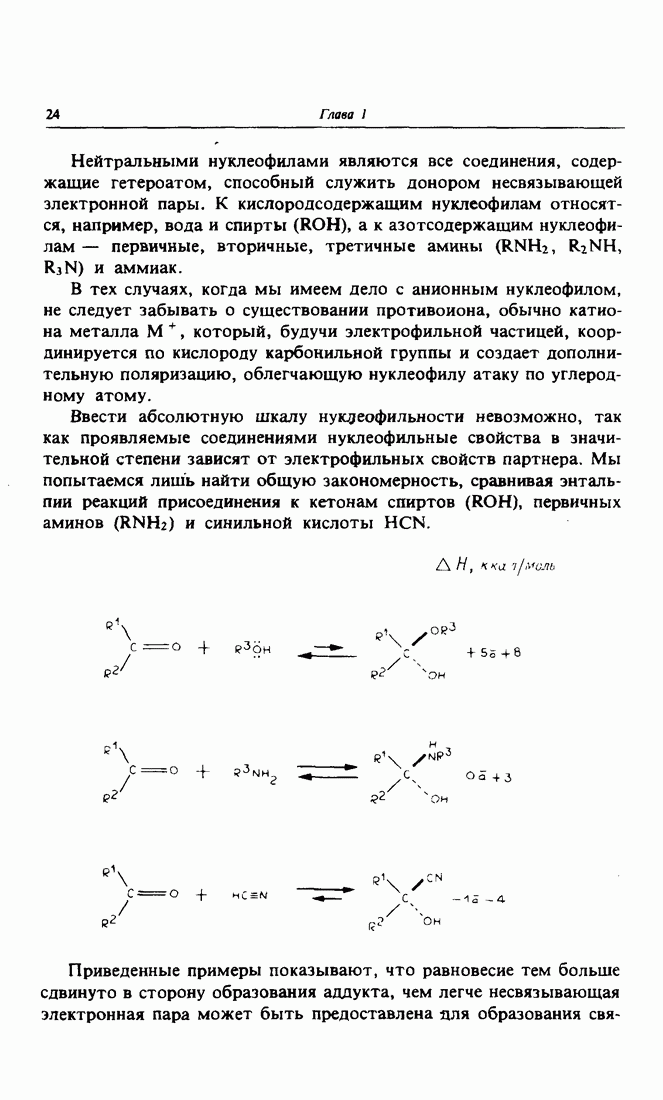
- 3. Основность и нуклеофильность
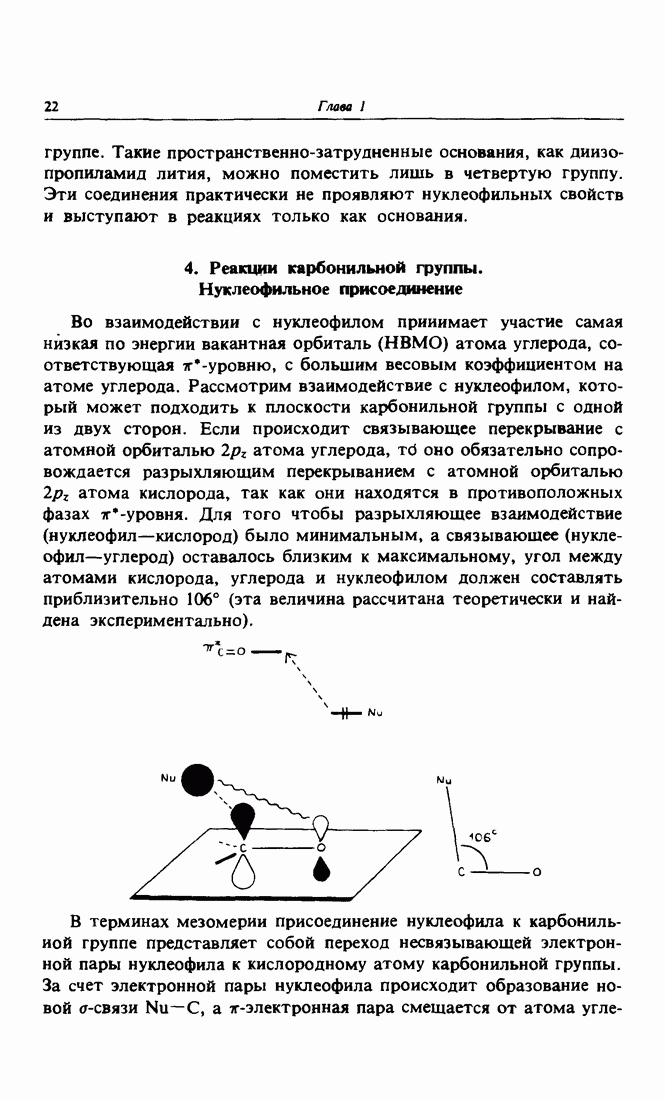
- 4 Реакции карбонильной группы. Нуклеофильное присоединение
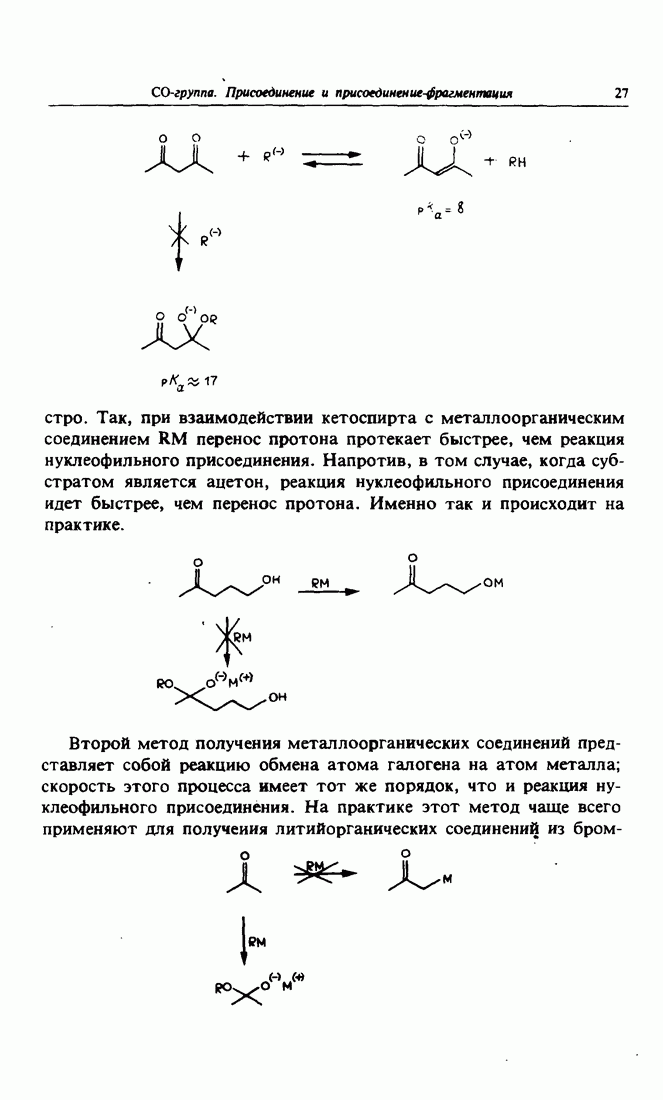
- 5. Защита и регенерация
- 6. Получение различных металлоорганических производных
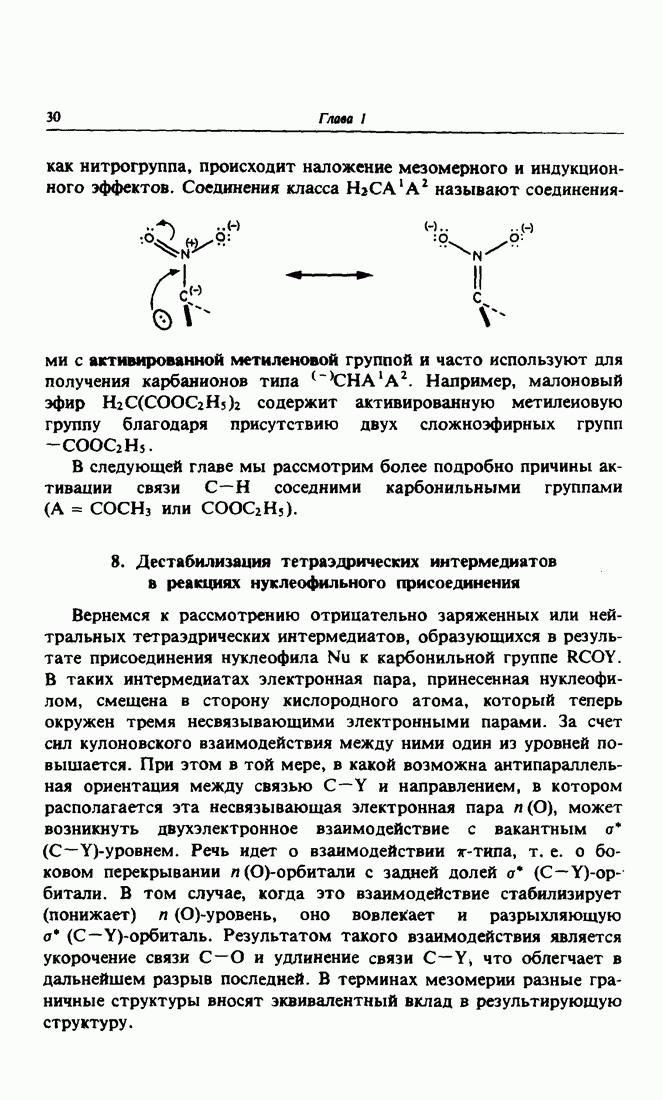
- 7. Активированная метиленовая группа
- 8. Дестабилизация тетраэдрических интермедиатов в реакциях нуклеофильного присоединения
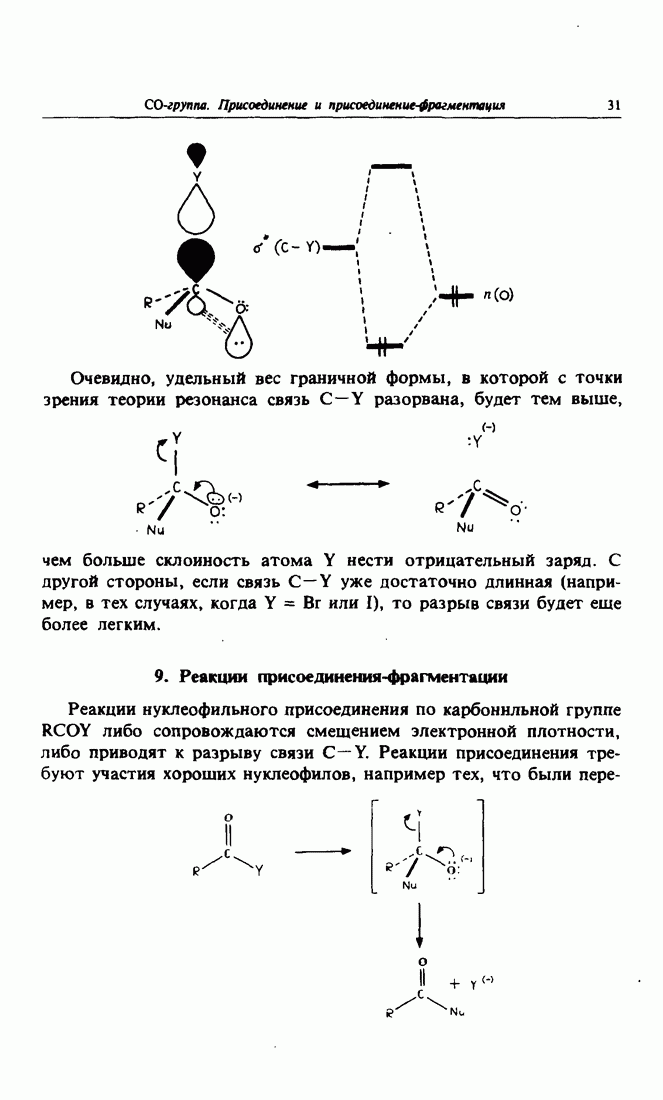
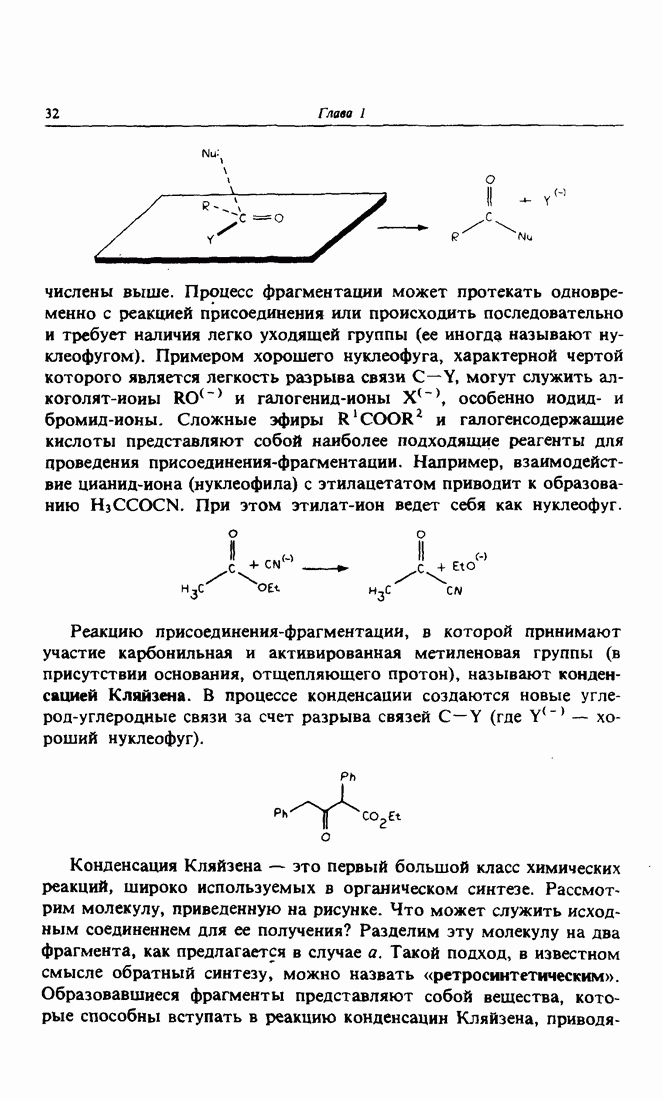
- 9. Реакции присоединения-фрагментации
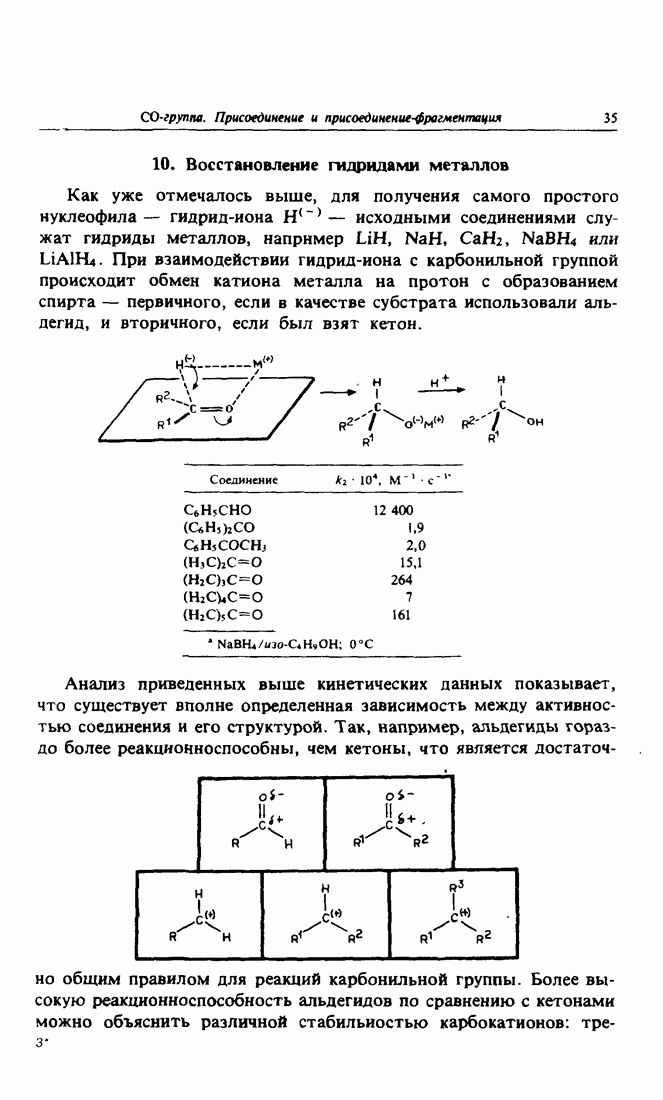
- 10. Восстановление гидридами металлов
- 11. Описание конфигурации асимметрического атома углерода
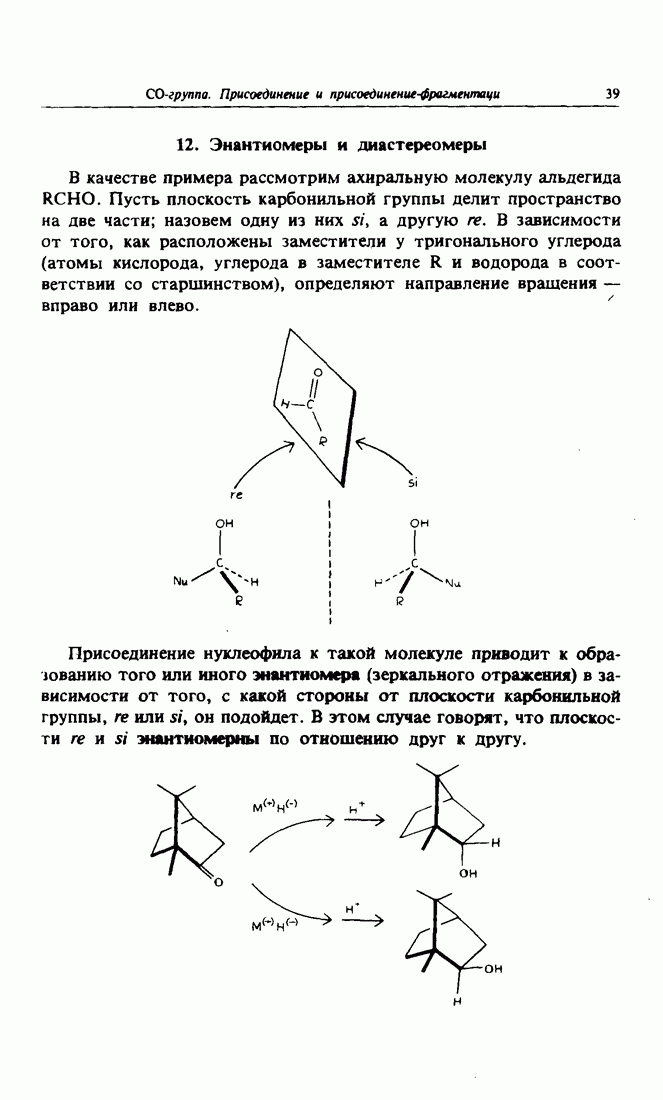
- 12. Энантиомеры и диастереомеры
- 13. Асимметрическая 1,2-индукция
- Глава 2. КАРБОНИЛЬНАЯ ГРУППА. ЕНОЛИЗАЦИЯ. КОНДЕНСАЦИЯ ПО МИХАЭЛЮ
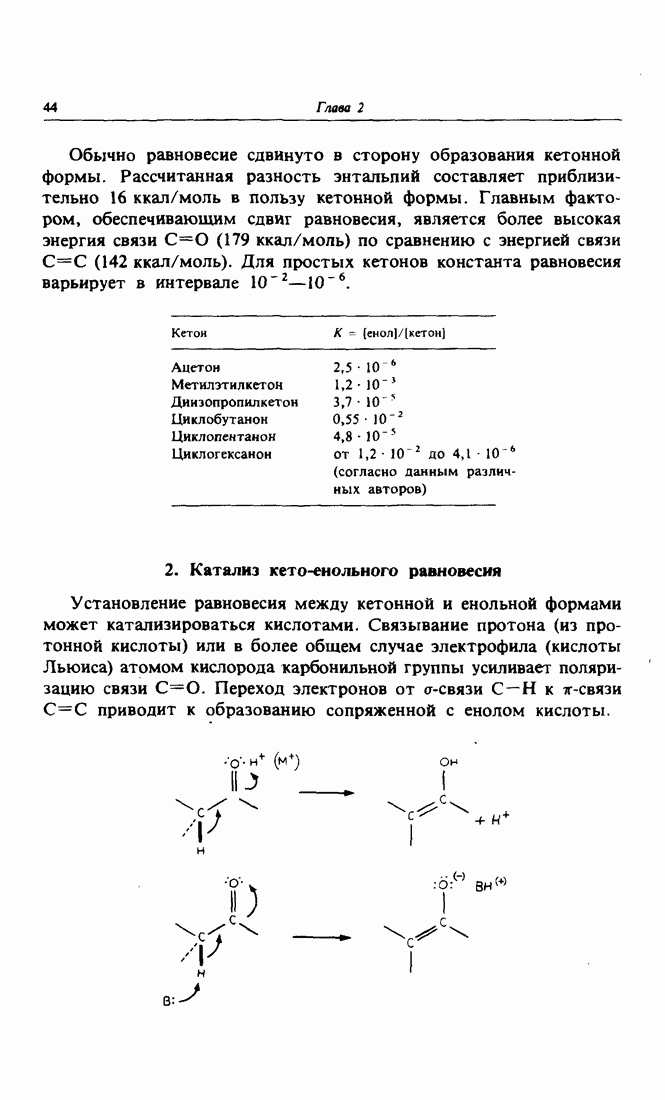
- 1. Кето-енольное равновесие
- 2. Катализ кето-енольного равновесия
- 3. Стереохимия и реакция енолнэации
- 4. Причины ослабления связи Ca-H в кетонах
- 5. Еноляты и их получение
- 6. Эфиры енолов
- 7. Конфигурация енолов и эфиров енолов
- 8. Реакция Михаэля
- 9. Артур Михаэль
- 10. Региоселективность в реакции Михаэля
- 11. Применение органокулратов
- 12. Современный вариант реакции Михаэля
- 13. Сопряжение или отсутствие сопряжения?
- 14. Циклизация по Робинсону
- 15. Сэр Роберт Робинсон
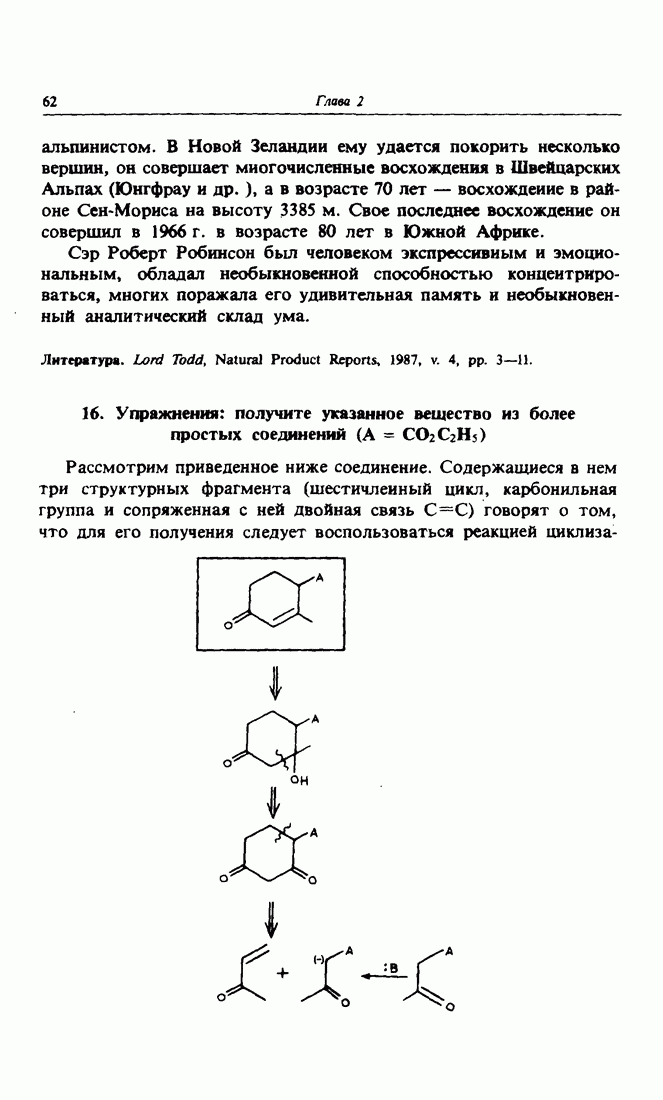
- 16. Упражнения: получите указанное вещество из более простых соединений (A=CO2C2H5)
- Глава 3. КАРБОНИЛЬНАЯ ГРУППА. АЛЬДОЛЬНАЯ КОНДЕНСАЦИЯ
- 2. Устойчивость продуктов альдольиой конденсации
- 3. Управление реакцией альдольной конденсации: доноры и акцепторы
- 4. Управление реакцией альдольной конденсации: син- и анти-диастереомеры
- 5. Стереоселективные реакции альдольной конденсации
- Глава 4. НЕКОТОРЫЕ РЕШЕНИЯ ПРОБЛЕМЫ СЕЛЕКТИВНОСТИ (ХИМИЧЕСКАЯ, РЕГИО- И СТЕРЕОСЕЛЕКТИВНОСТЬ)
- 2. Региоселективность при образовании енолятов
- 3. Селективное получение Е- и Z-енолятов
- 4. Двойной принцип стереоселективности
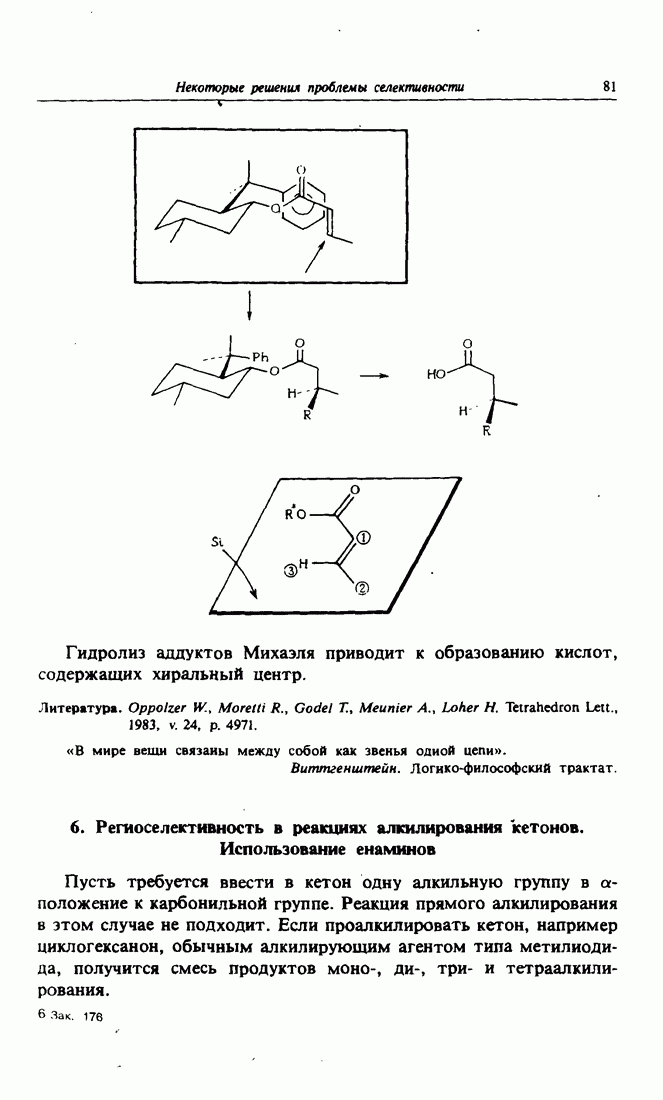
- 5. Энантиоселективная реакция Михаэля
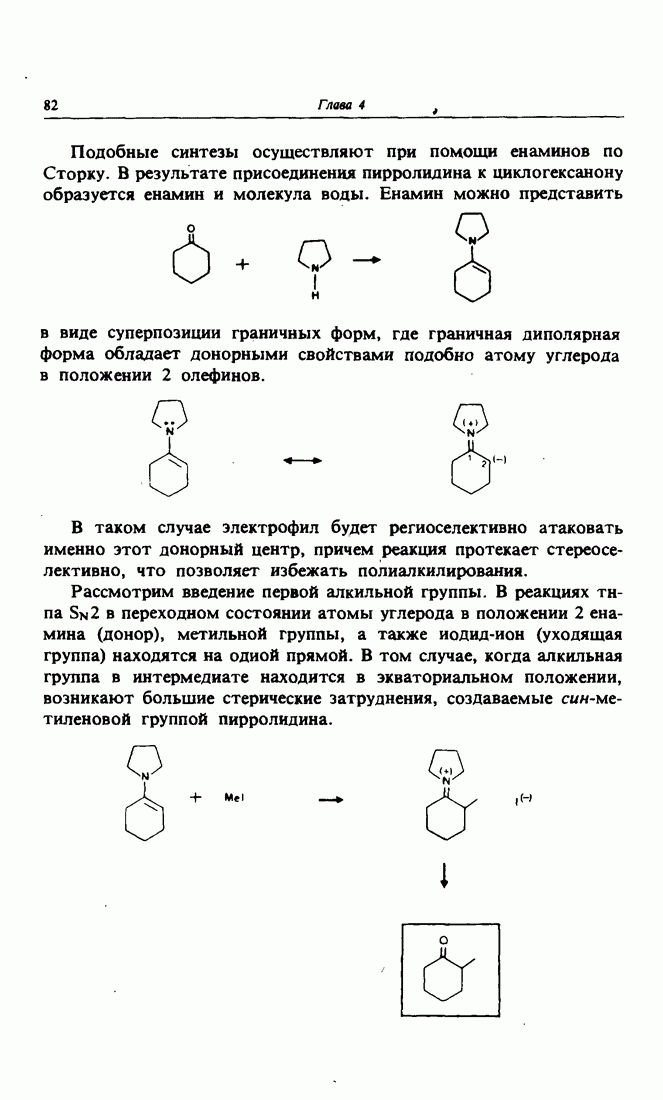
- 6. Региоселективность в реакциях алкилирования кетонов. Использование енаминов
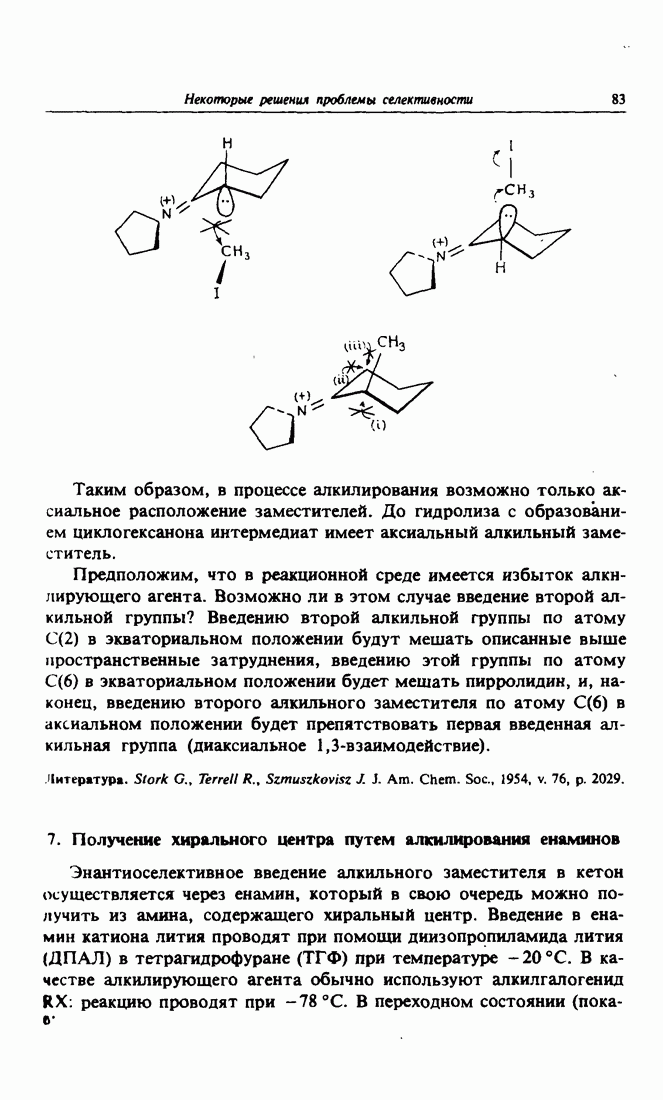
- 7. Получение хирального центра путем алкилирования енаминов
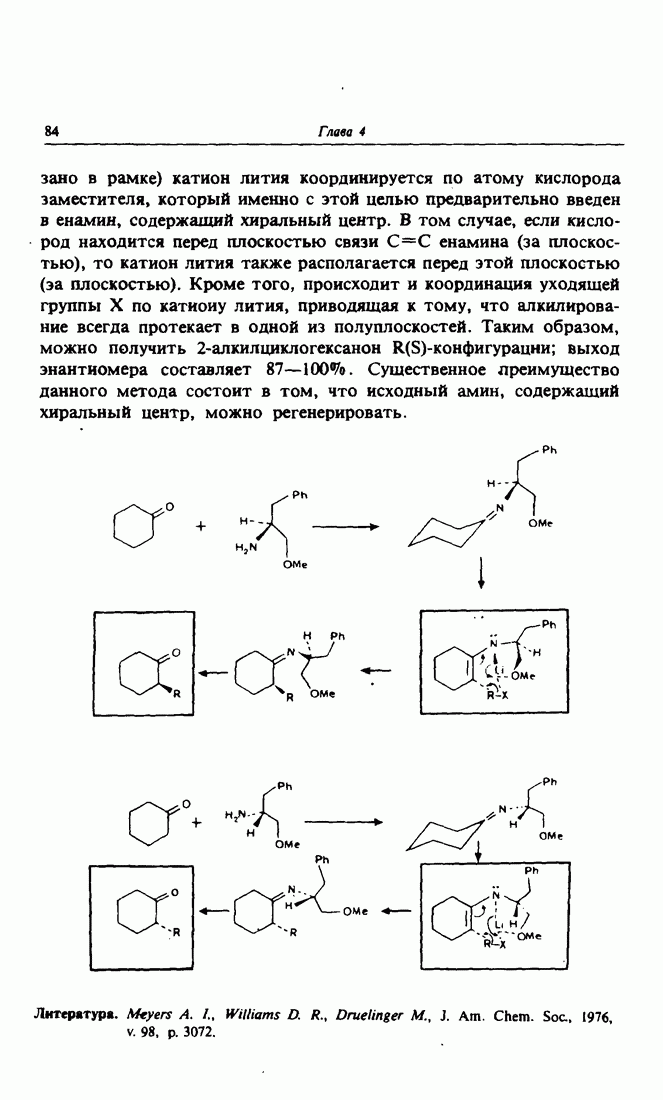
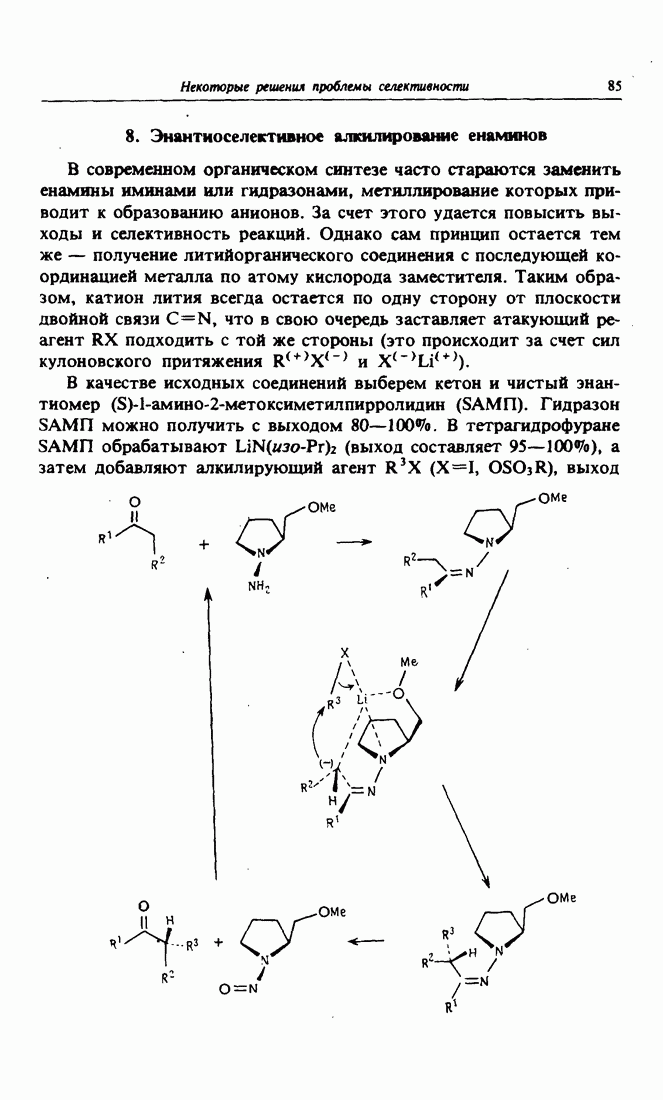
- 8. Энантиоселективное алкилирование енаминов
- 9. Перенос хиральности
- 10. Соотношение между реакционноспособностью и селективностью
- 11. Стереоэлектронный эффект
- 12. Конформации переходного состояния «кресло» и «ванна»
- Глава 5. ЗАЩИТА И РЕГЕНЕРАЦИЯ ФУНКЦИОНАЛЬНЫХ ГРУПП. СПИРТОВАЯ И КАРБОНИЛЬНАЯ ГРУППЫ. ОБРАЩЕНИЕ ПОЛЯРНОСТИ
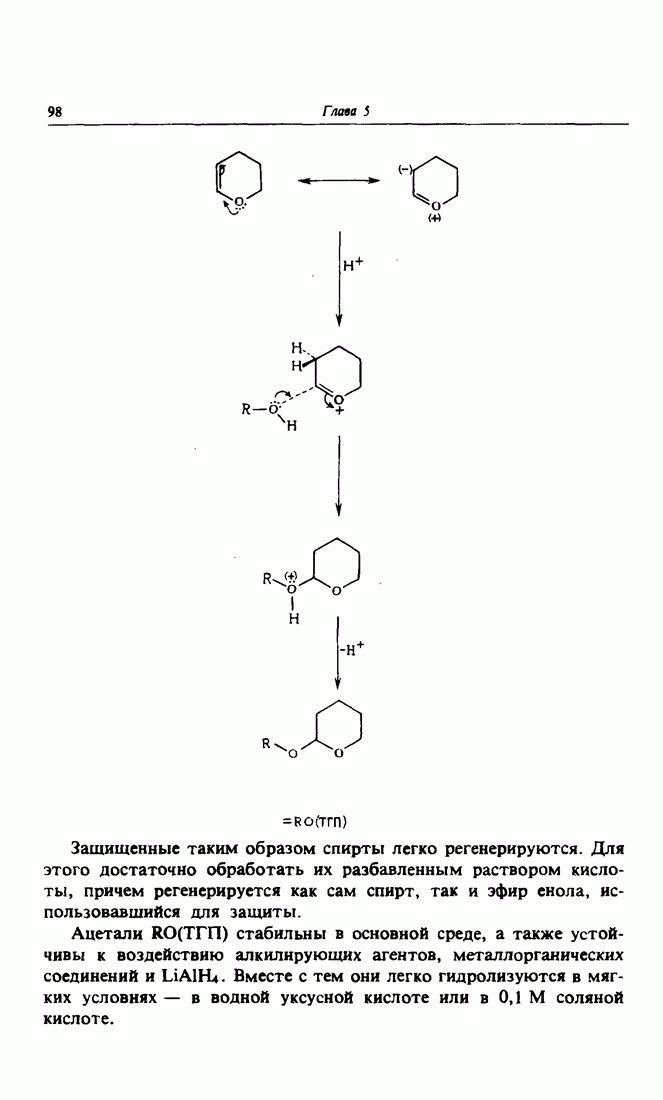
- 1. Защита карбонильной группы ацетальной
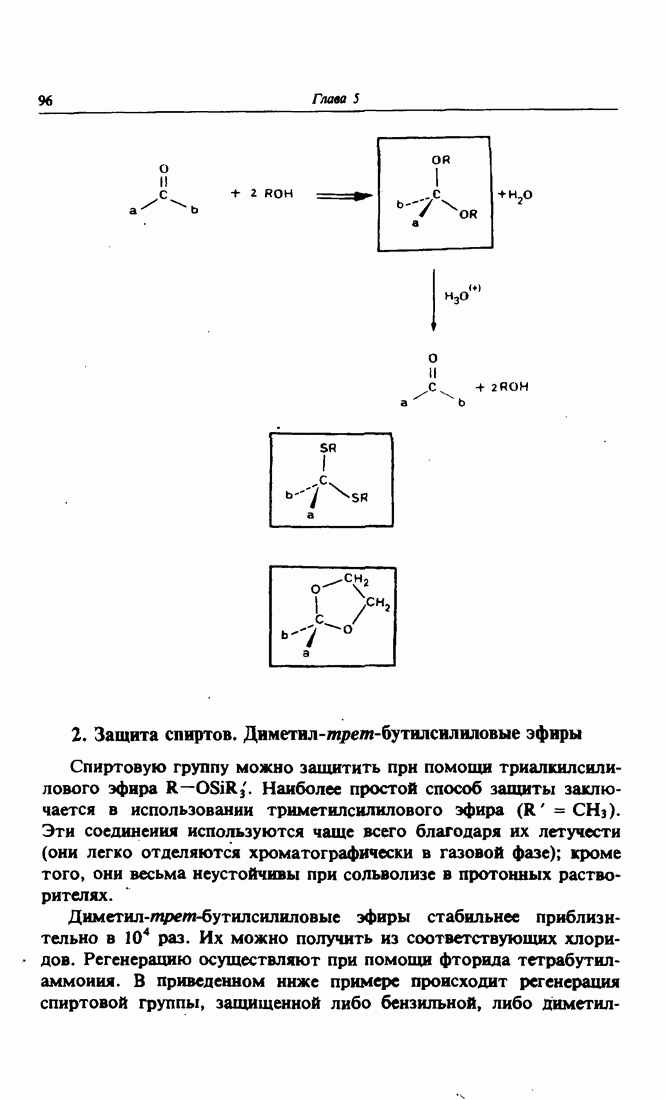
- 2. Защита спиртов. Диметил-трет-бутилсилиловые эфиры
- 3. Защита спиртовых групп при помощи эфиров енолов
- 4. Обращение полярности
- 5. Э. Дж. Кори
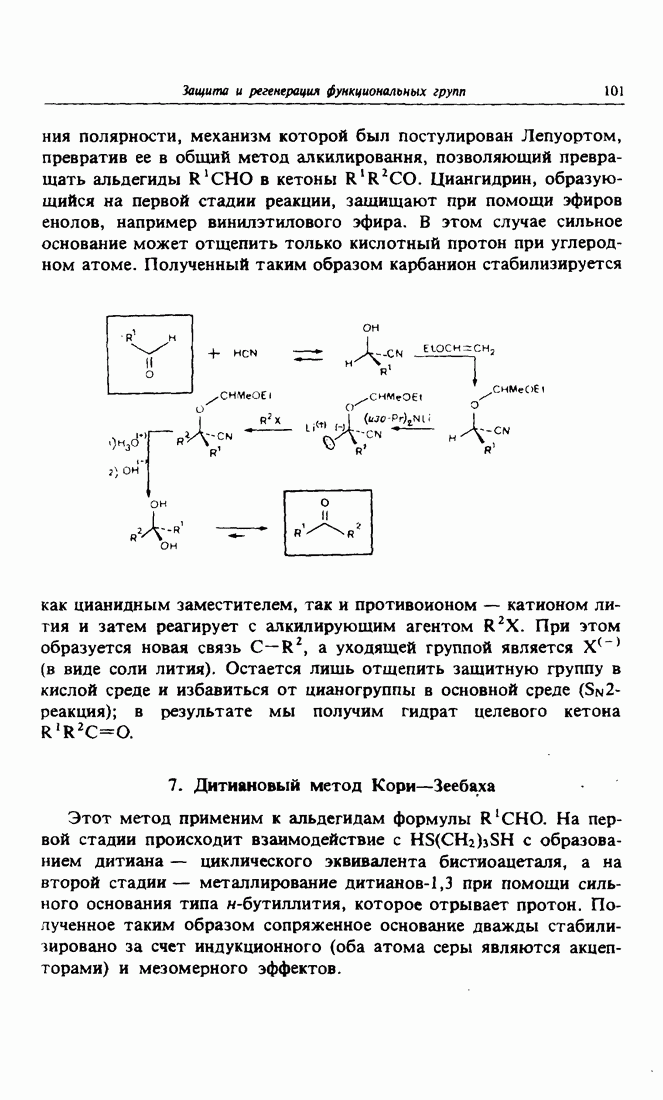
- 6. Инверсия полярности по методу Лепуорта — Шторка
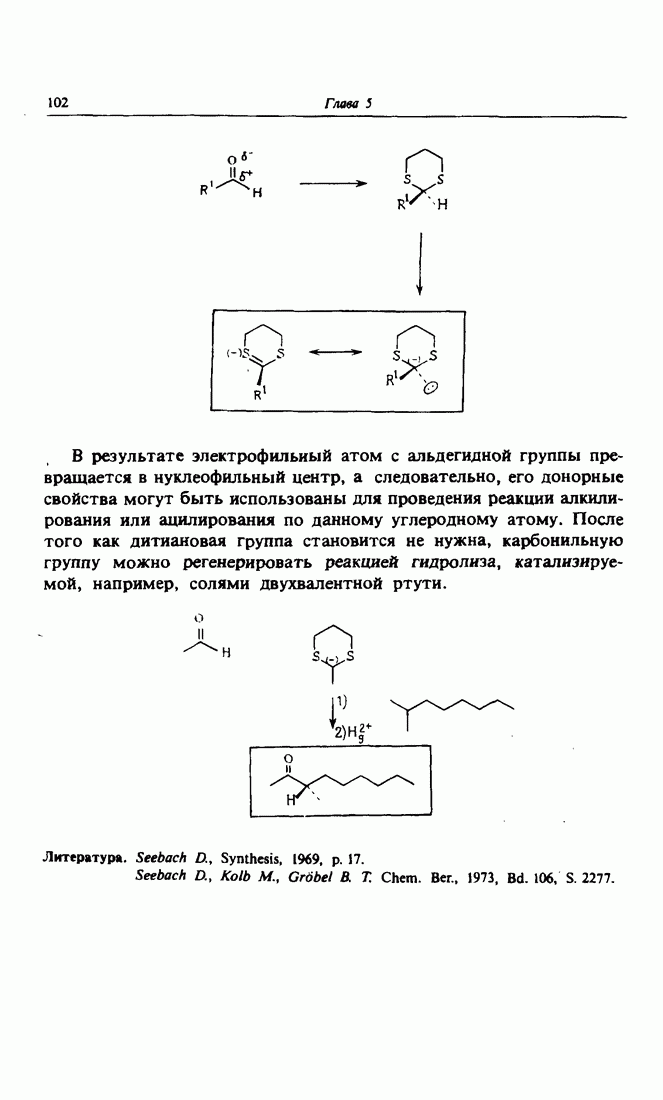
- 7. Дитиановый метод Кори-Зеебаха
- Главе 6. АКТИВАЦИЯ
- 2. Стабилизация конечного состояния
- 3. Дестабилизация начального состояния
- 4. Стабилизация переходного состояния
- Главв 7. ПОСТРОЕНИЕ ЦИКЛОВ
- 2. Региоселективность
- 3. Реакция Дильса — Альдера в условиях обращенного электронного соответствия
- 4. Стереоселективность в реакциях Дильса — Альдера
- 5. Напряжение в циклах
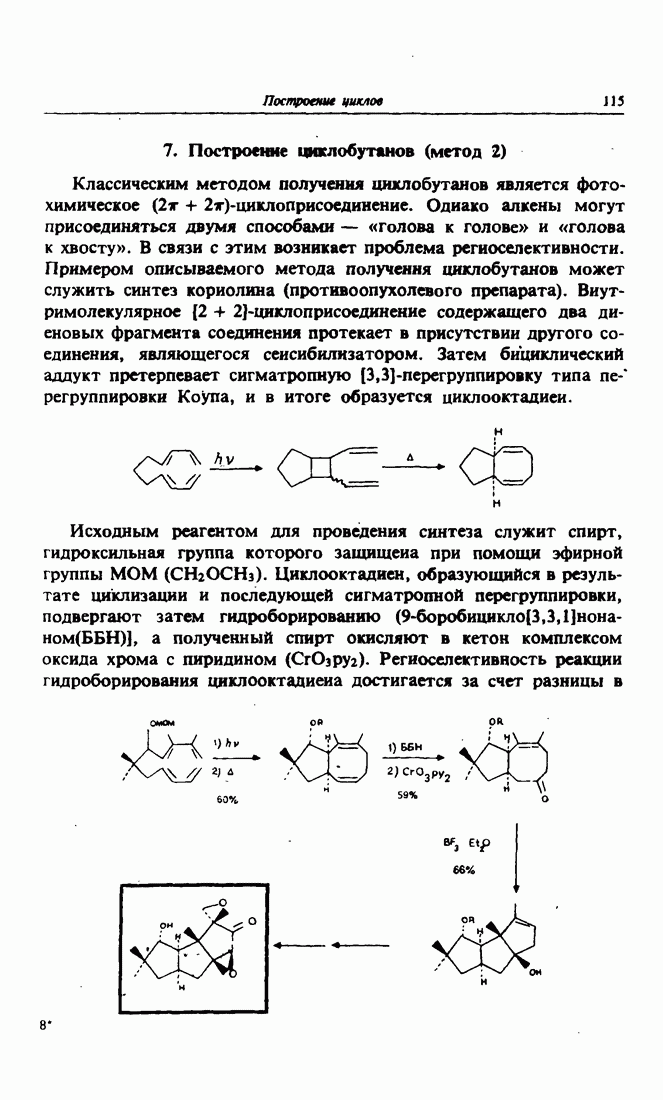
- 6. Построение циклобутанов (метод 1) Термическая димеризация
- 7. Построение циклобутанов (метод 2)
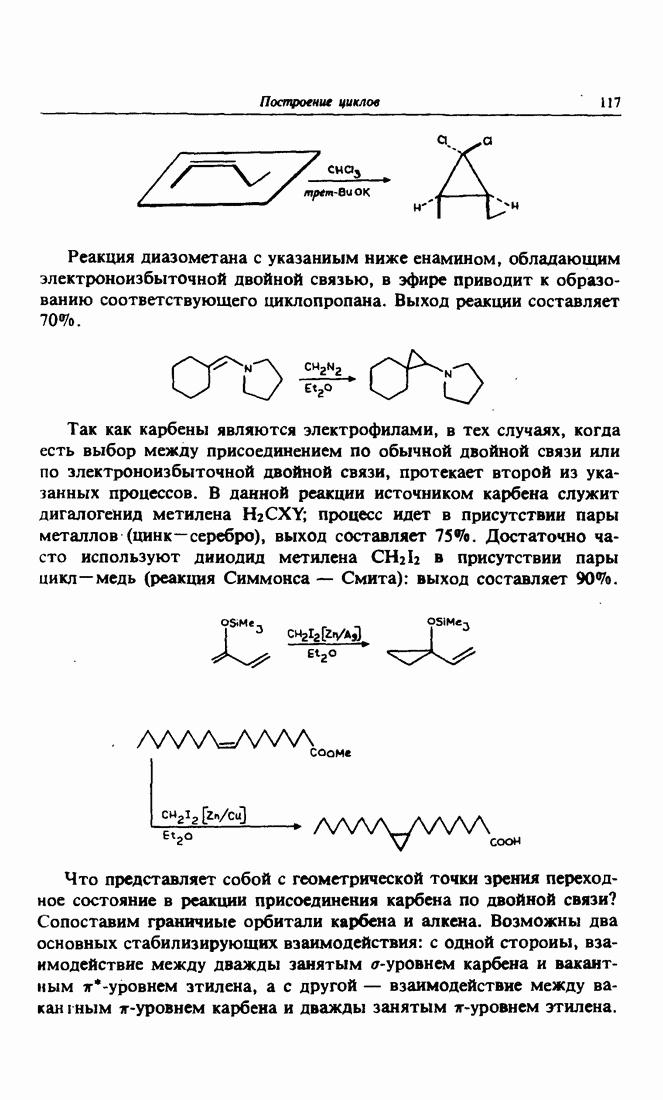
- 8. Синтез циклопропанов. Присоединение карбенов к алкенам
- Глааа 8. ВВЕДЕНИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП. РЕАКЦИИ ЗАМЕЩЕНИЯ
- 2. Соотношение структура — реакционноспособность
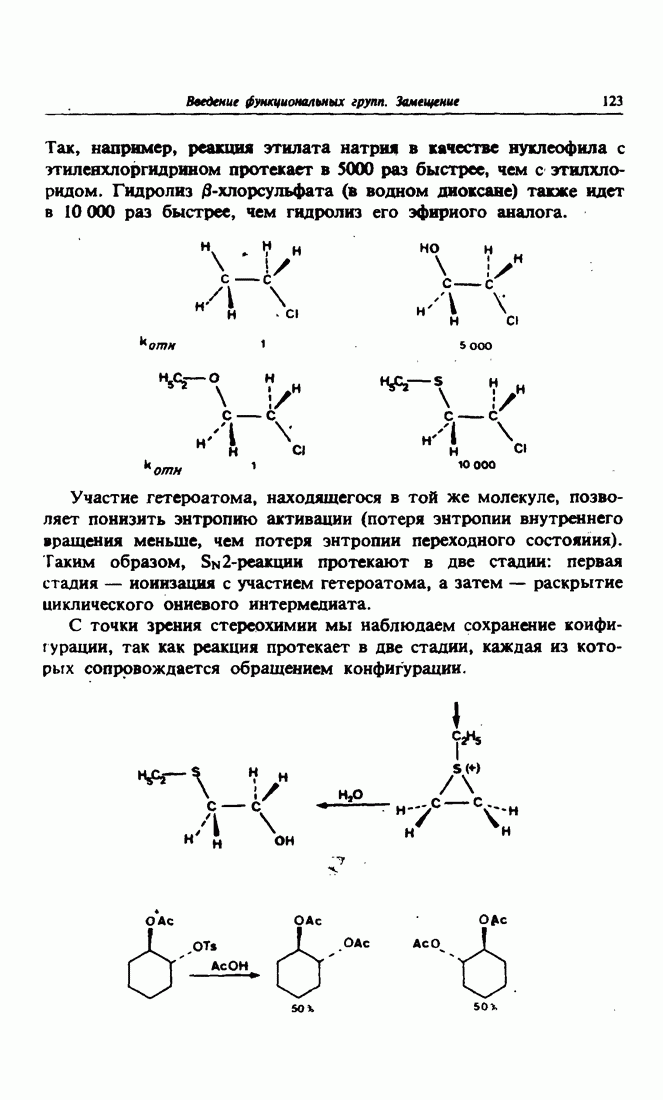
- 3. Участие соседней группы в Sn2-реакциях
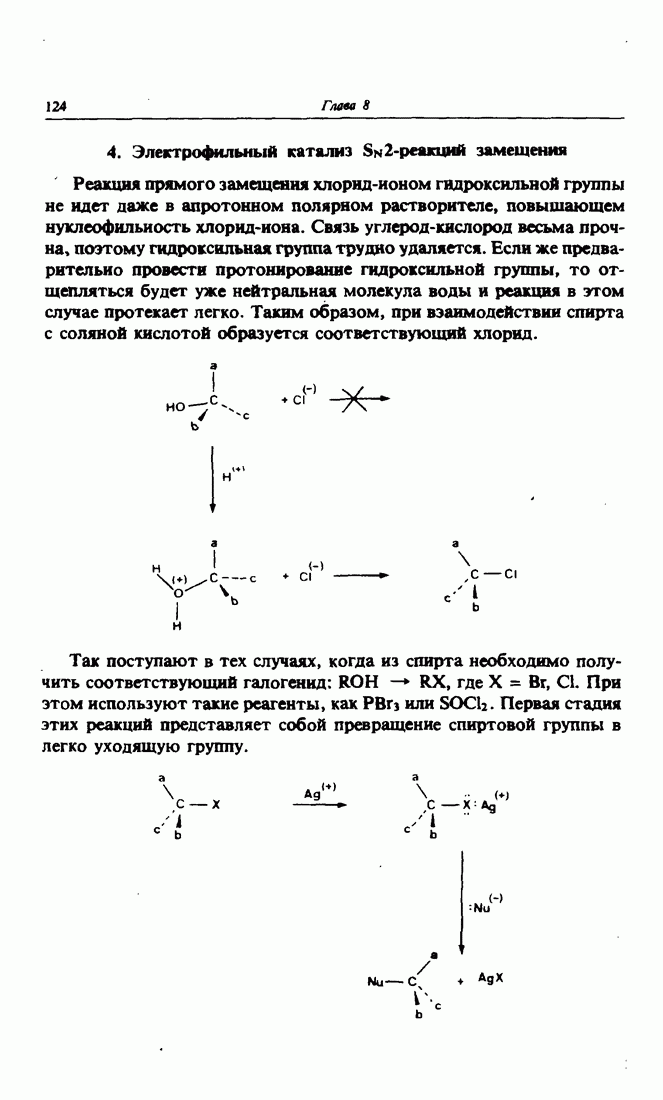
- 4. Электрофильный катализ Sn2-реакций замещения
- 5. Региоселеггивность в реакциях алкилирования
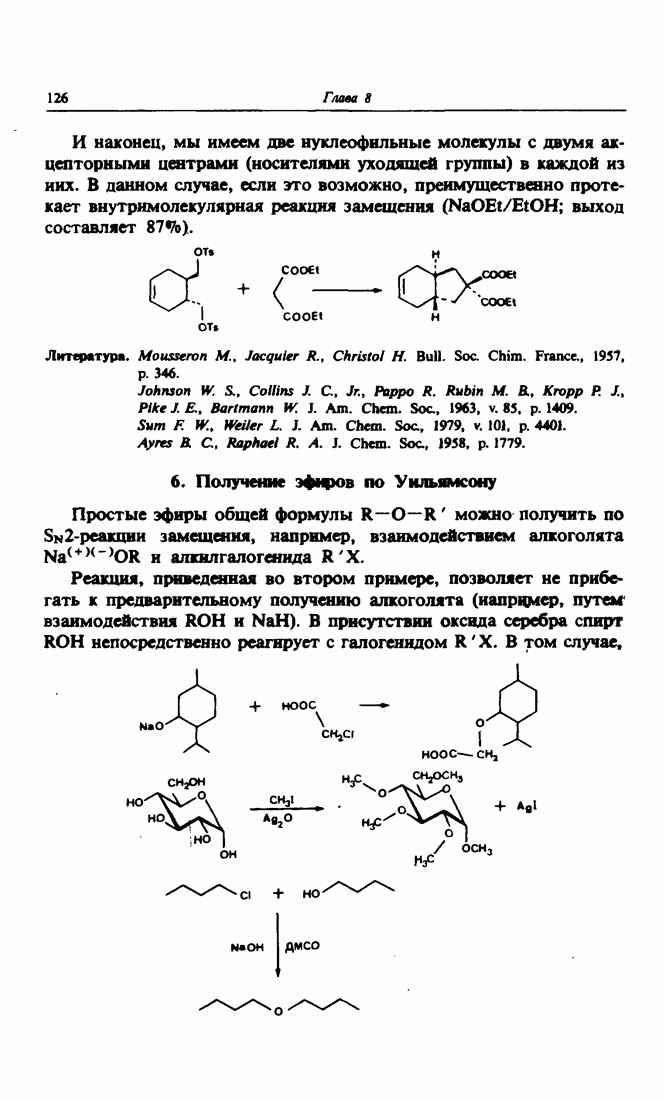
- 6. Получение эфиров по Уильямсону
- 7. К вопросу об обозначениях
- Глава 9. ВВЕДЕНИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП. РЕАКЦИИ ВОССТАНОВЛЕНИЯ
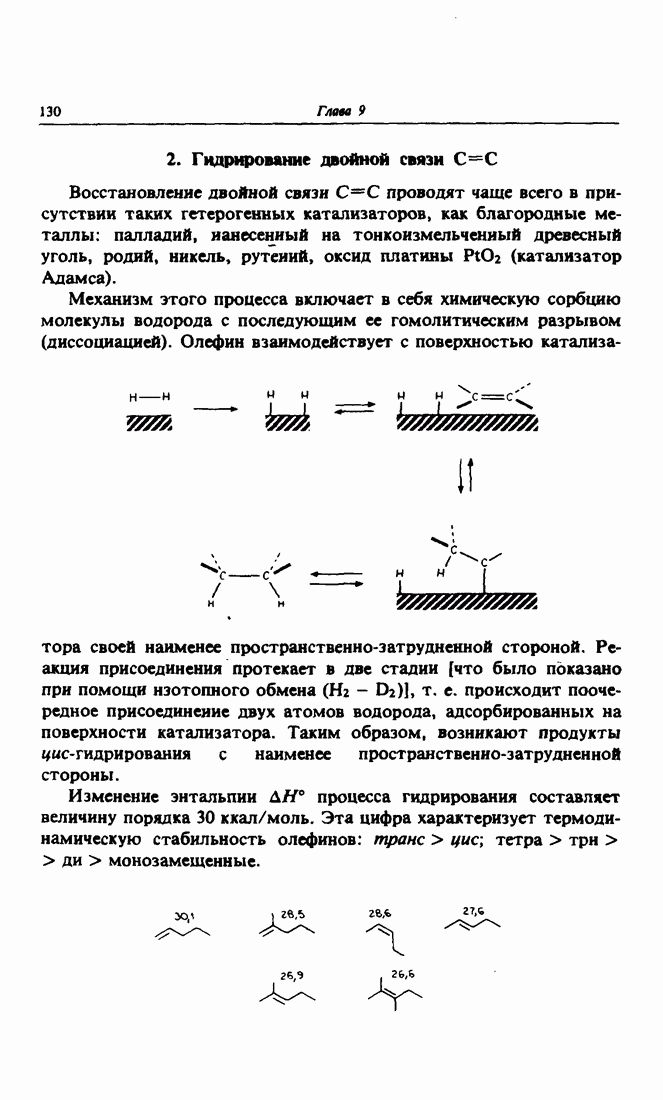
- 2. Гидрирование двойной связи С=С
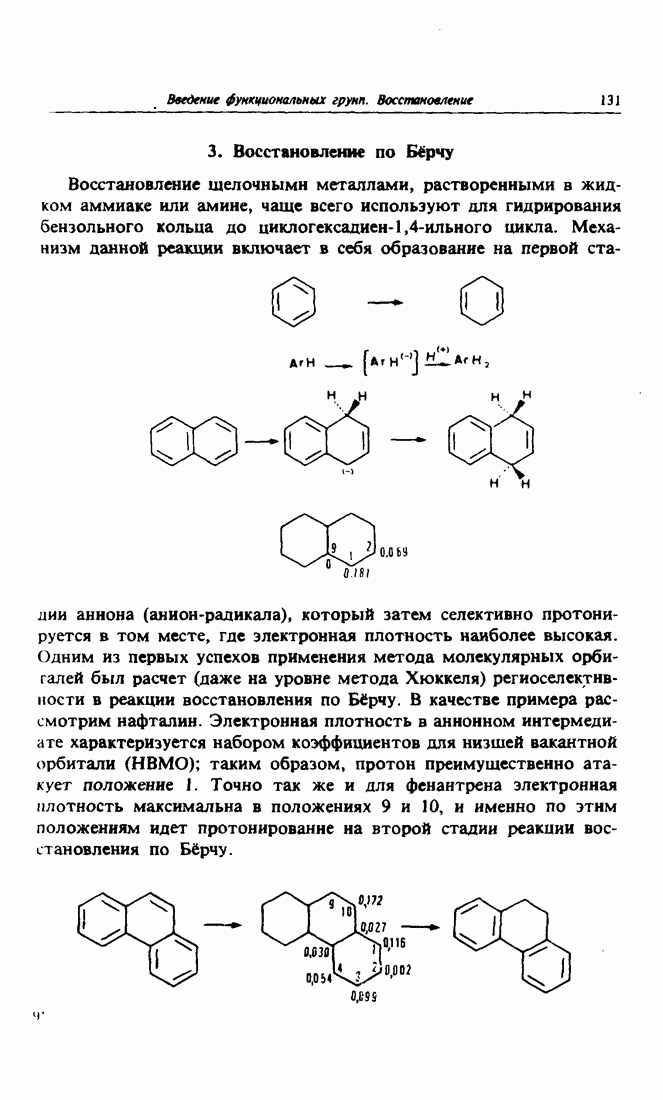
- 3. Восстановление по Бёрчу
- 4. Восстановление карбонильной группы
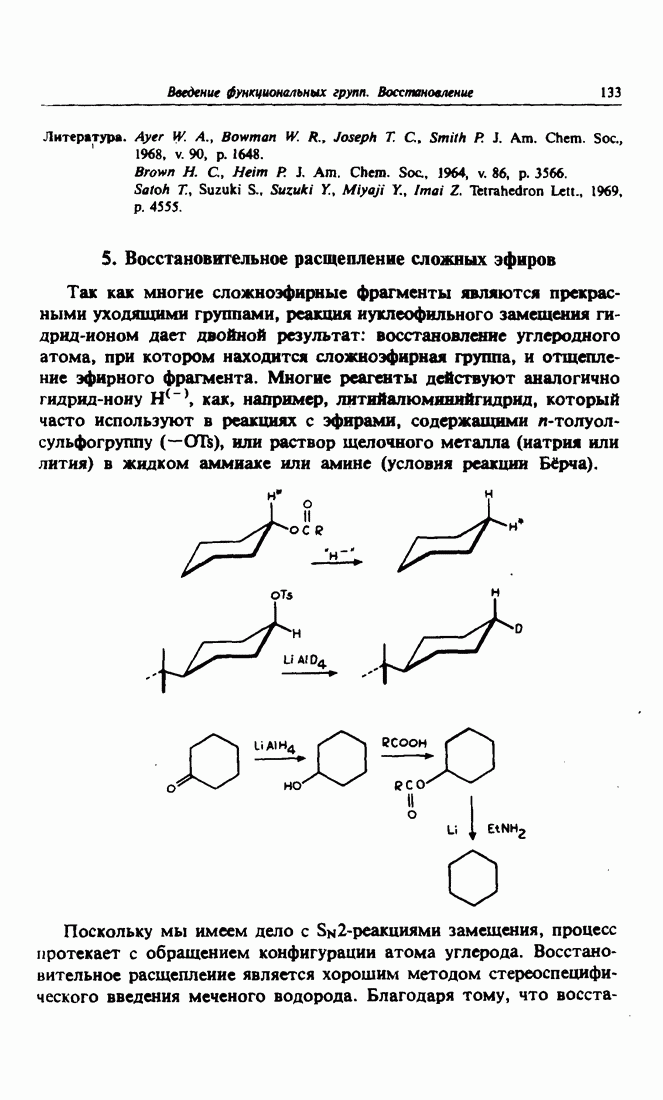
- 5. Восстановительное расщепление сложных эфиров
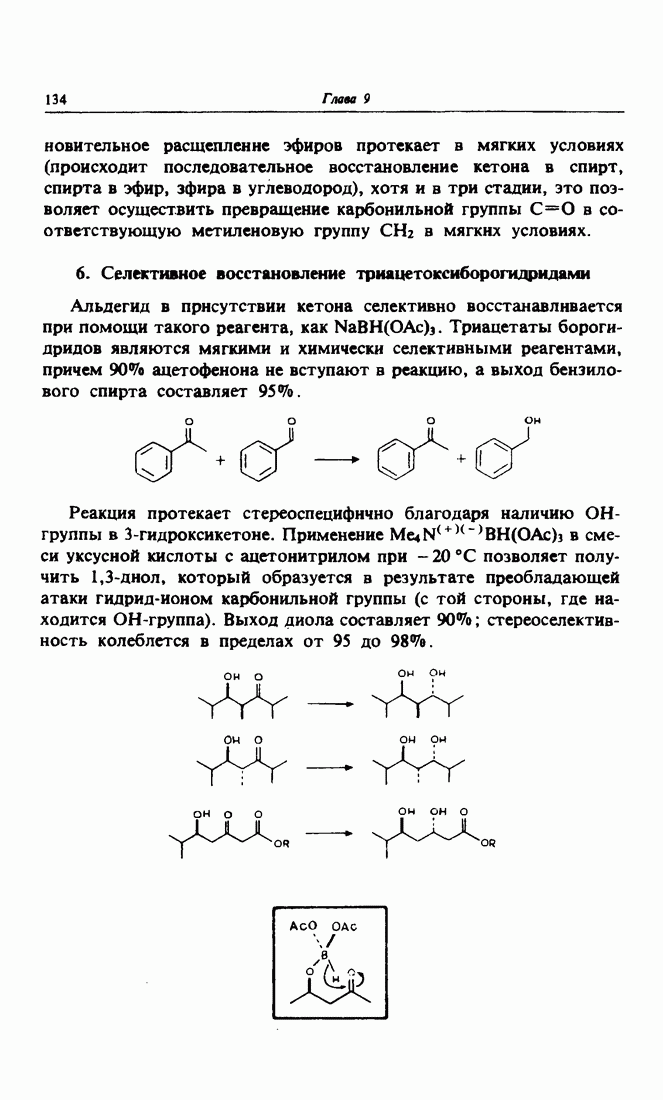
- 6. Селективное восстановление триацетоксиборогидридами
- Глава 10. ВВЕДЕНИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП. РЕАКЦИИ ОКИСЛЕНИЯ
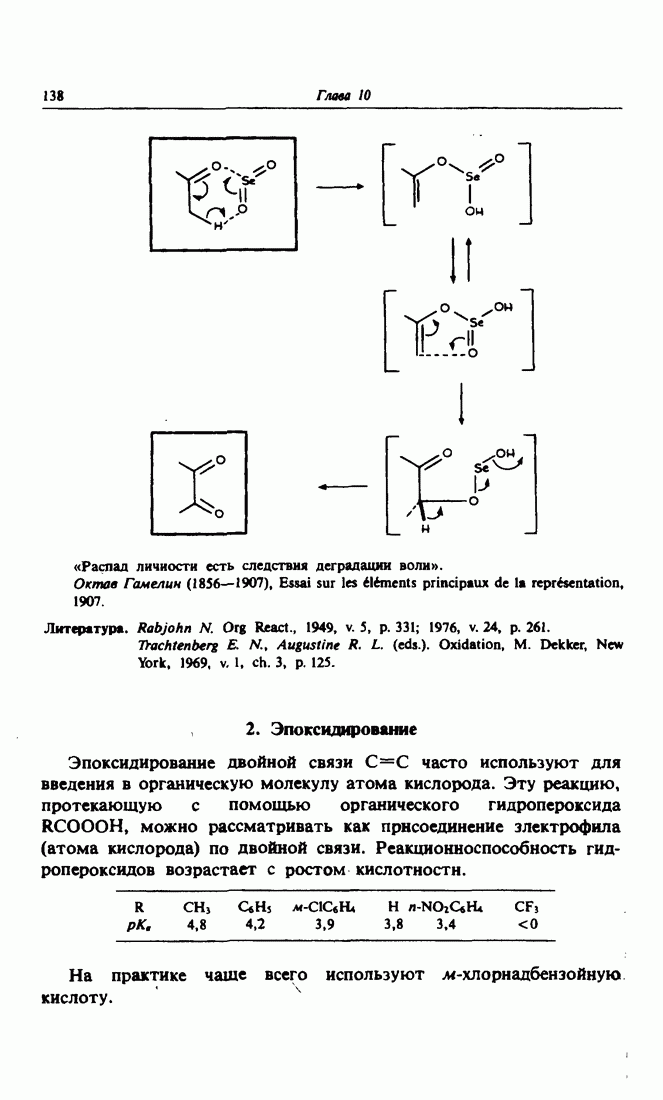
- 2. Эпоксидирование
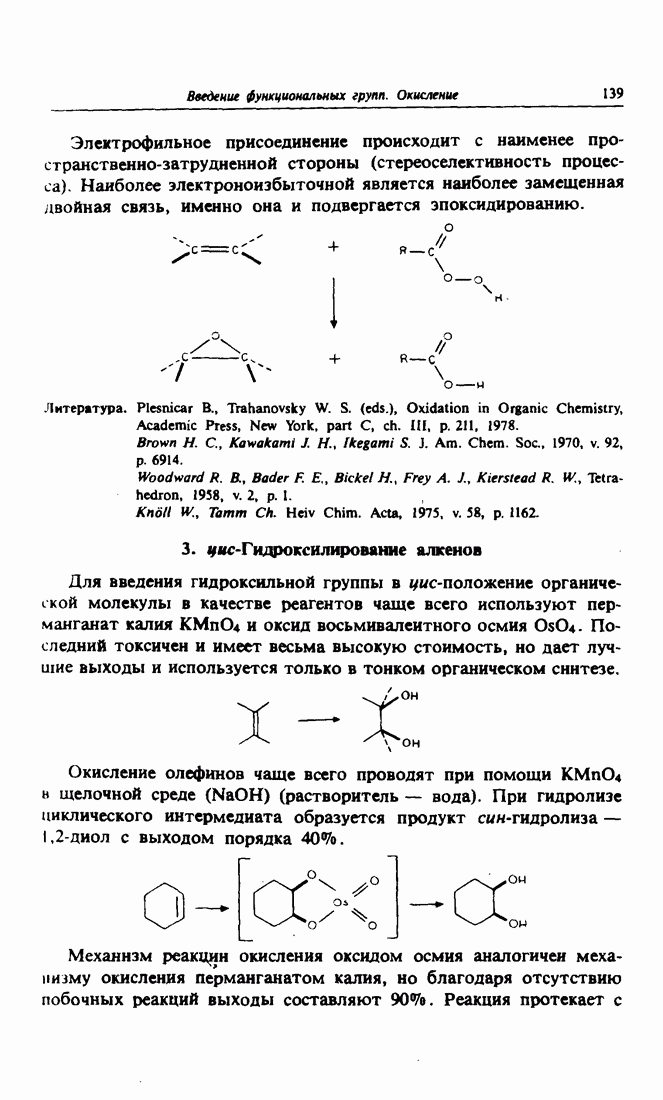
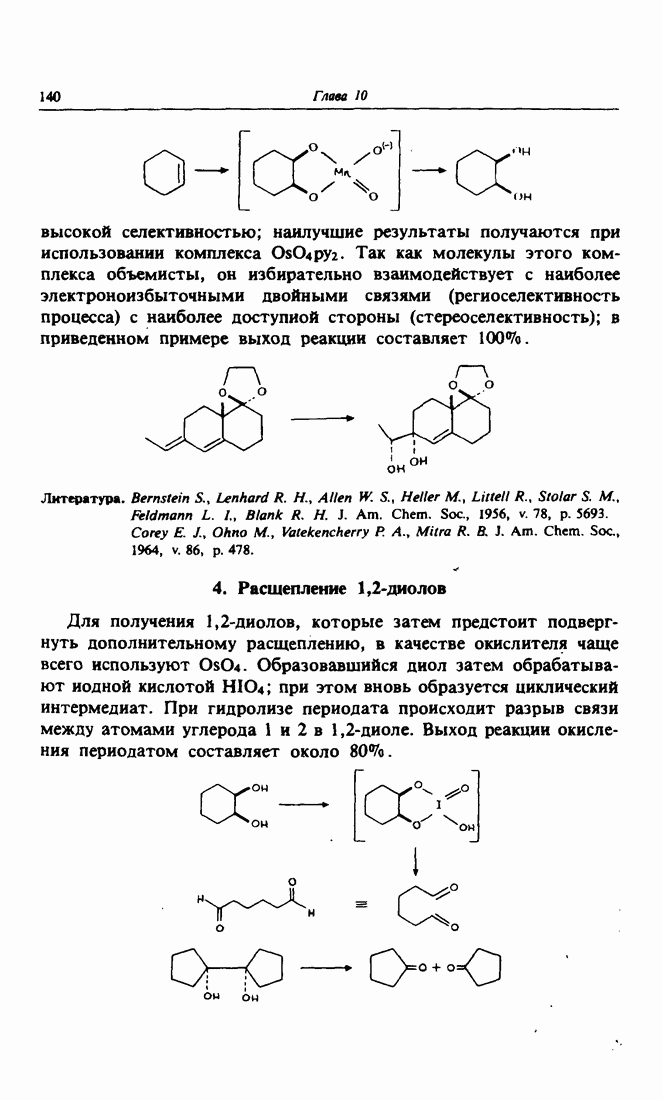
- 3. цис-Гидроксилирование алкенов
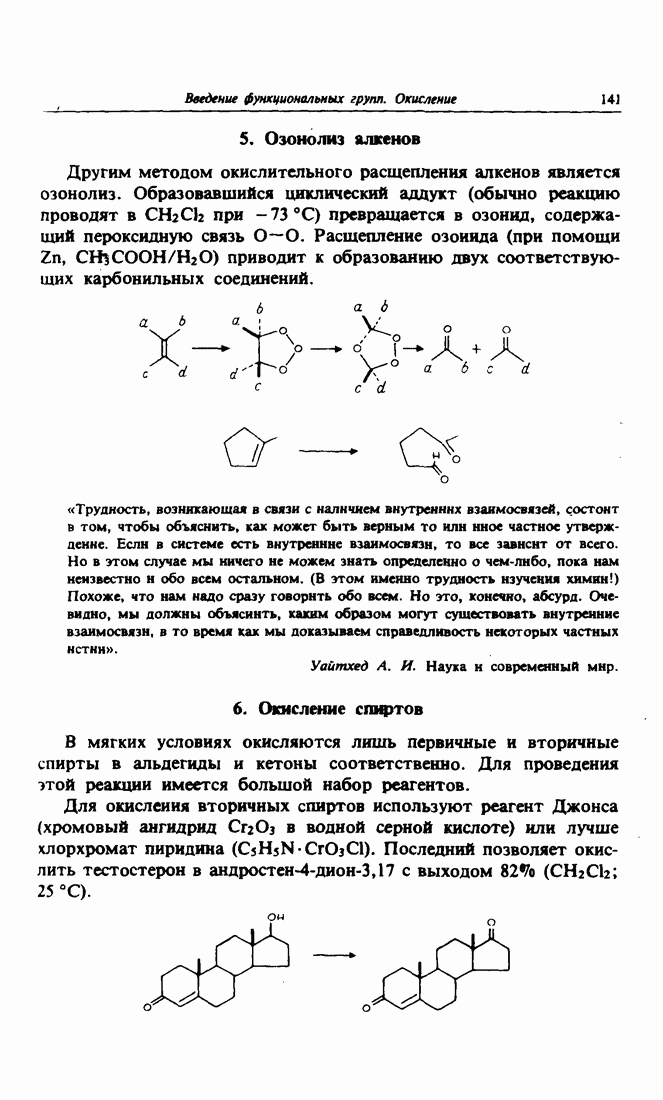
- 4. Расщепление 1,2-диолов
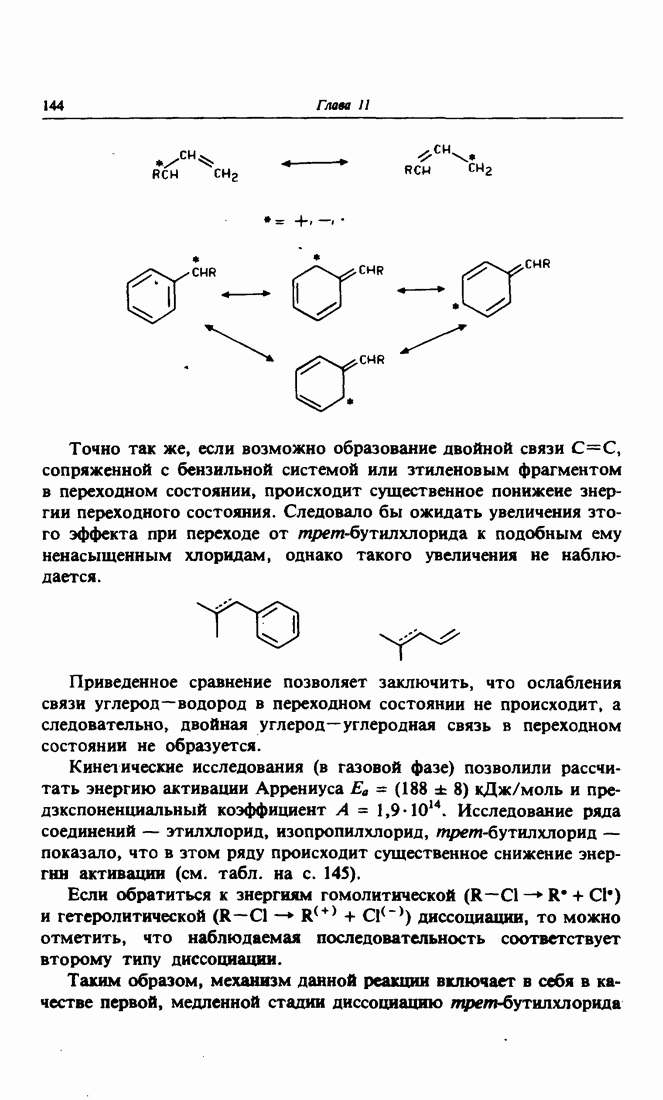
- 5. Озонолиз алкенов
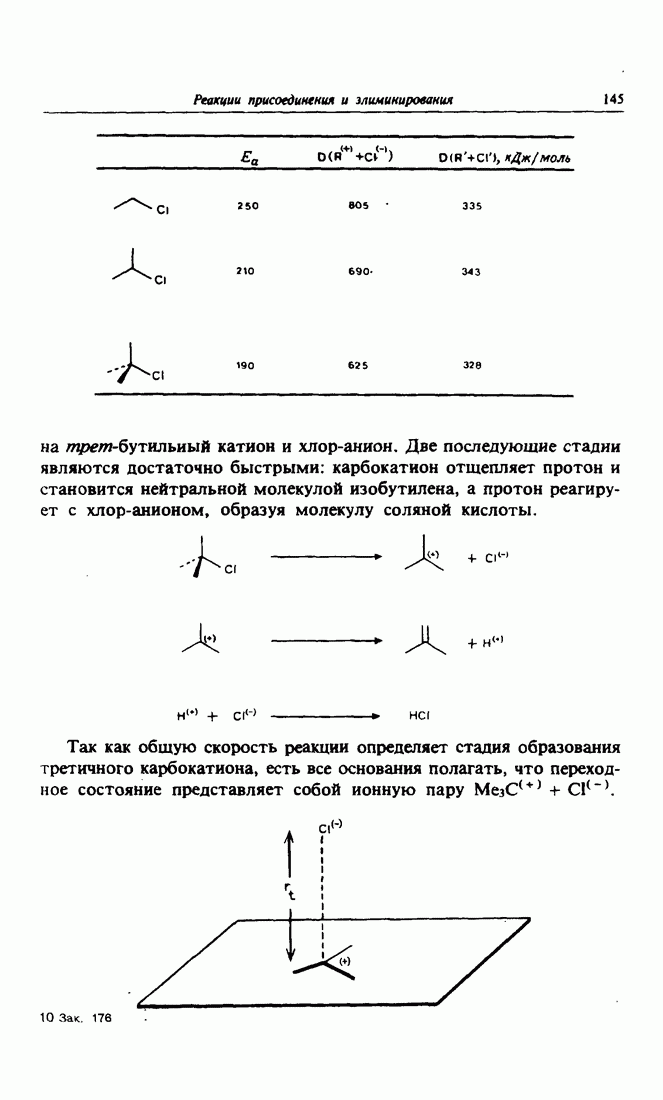
- 6. Окисление спиртов
- Главе 11. РЕАКЦИИ ПРИСОЕДИНЕНИЯ И ЭЛИМИНИРОВАНИЯ
- 2. Классически механизм реакции электрофильного присоединения. Правило Марковникова
- 3. Основные электрофильные агенты
- 3.3. Присоединение гипохлоритов и гипобромитов
- 3.4. Оксимеркурирование
- 3.5. Гидроборирование
- 3.6. Окситаллирование
- 4. Стереохимия реакции присоединения по двойной связи С=С
- 5. Конкуренция нуклеофила и растворителя в реакции электрофильного присоединения
- 6. Присоединение к напряженным олефинам: цис-присоединение
- 7. Стереохимия реакций бимолекулярного элиминирования
- 8. Виды b-элиминирования
- Главв 12. ПЕРЕГРУППИРОВКИ ФУНКЦИОНАЛЬНЫХ ГРУПП. ПРЕВРАЩЕНИЕ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ В ОЛЕФИНЫ ПО РЕАКЦИИ ВИТТИГА
- 2. Реакция Дарзана
- 3. Дарзан — один из великих политехников
- 4. Обобщение и модернизация метода
- 5. Стереоселективность реакции Кори — Чайковского
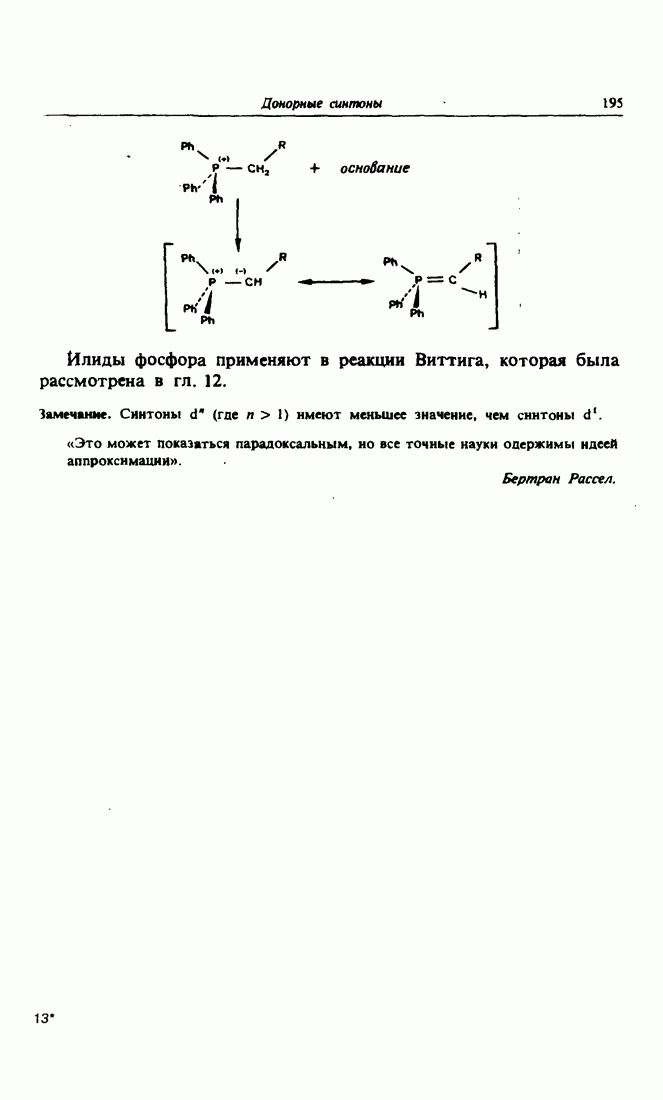
- 6. Реакция Виттига
- 7. Георг Виттиг
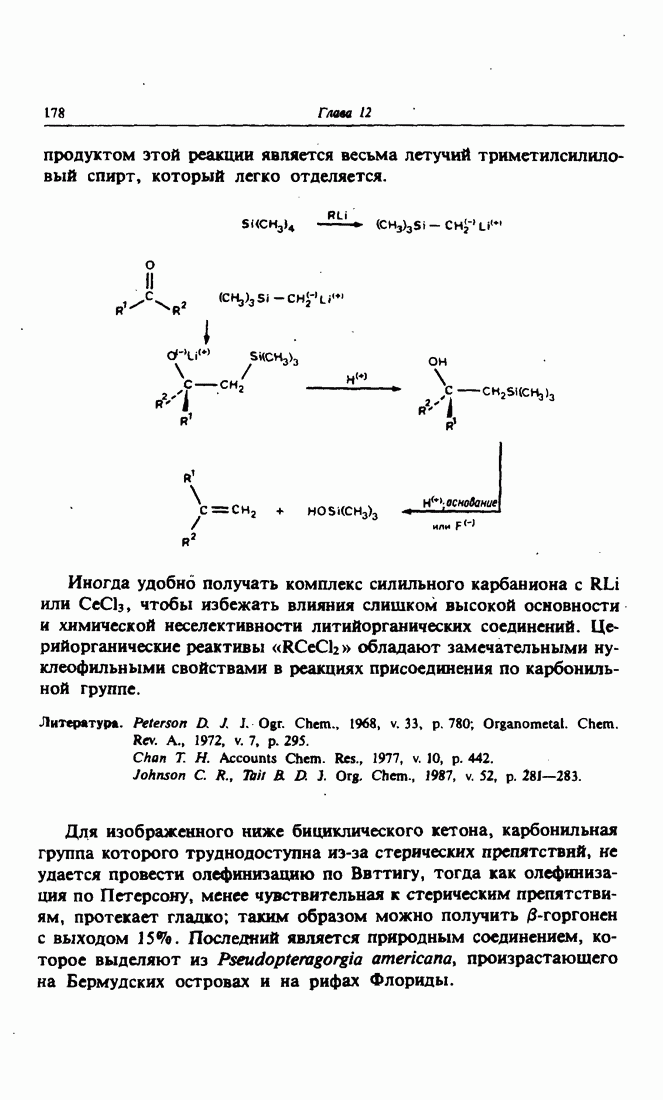
- 8. Причины образования различных продуктов в реакциях Виттига и Кори — Чайковского
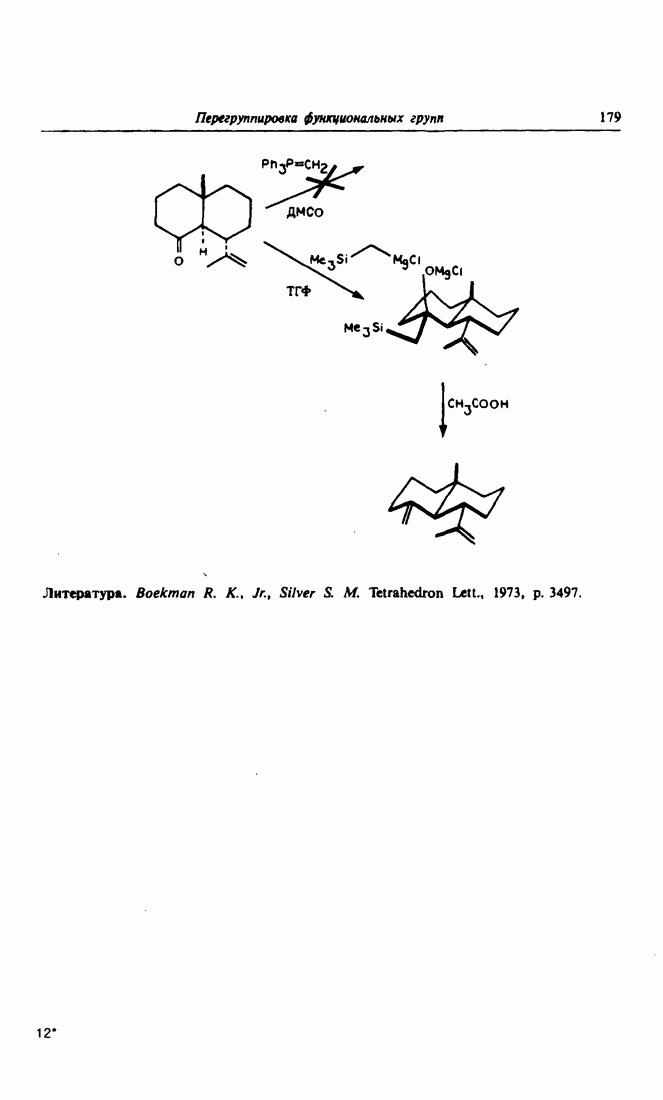
- 9. Разновидность реакции Виттига: олефинирование по Петерсону
- Главе 13. ПЕРЕГРУППИРОВКИ
- 2. 1,2-Переход в карбокатионах
- 3. Перегруппировка Бекмана
- 4. Перегруппировка Курциуса
- 5. Перегруппировка Байера — Виллигера
- 6. Реакция Рамберга-Беклунда
- Глава 14. ДОНОРНЫЕ СИНТОНЫ
- 2. Алкильные донорные синтоны
- 3. Донорные синтоны d1 с гетероатомами, обладающими d-орбиталью
- Глава 15. АКЦЕПТОРНЫЕ СИНТОНЫ
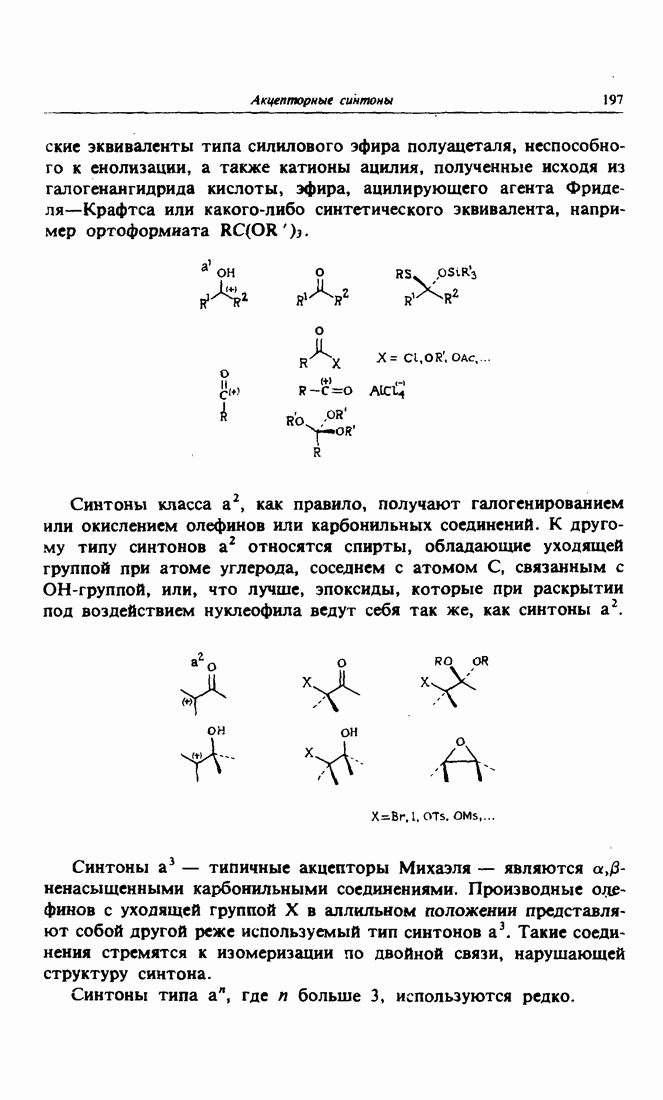
- 1. Синтоны-акцепторы
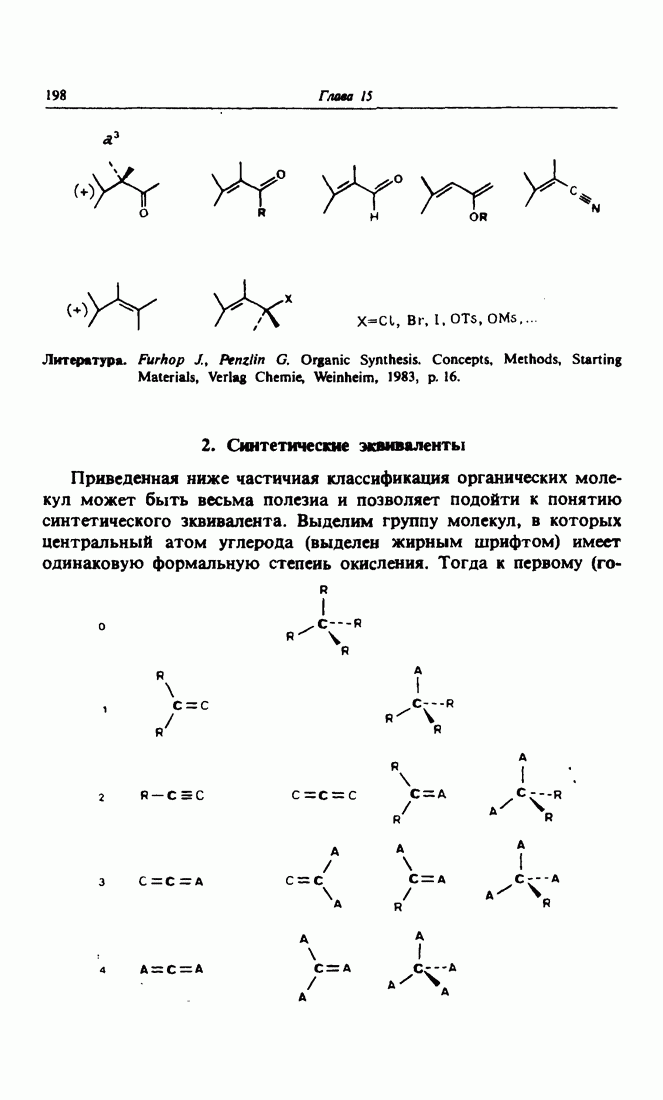
- 2. Синтетические эквиваленты
- 3. Контролируемое образование новых связей
- 4. Расчленение молекулы на фрагменты
- 5. Двойное расчленение молекулы
- 6. Изменение реакционноспособности в результате обращения полярности
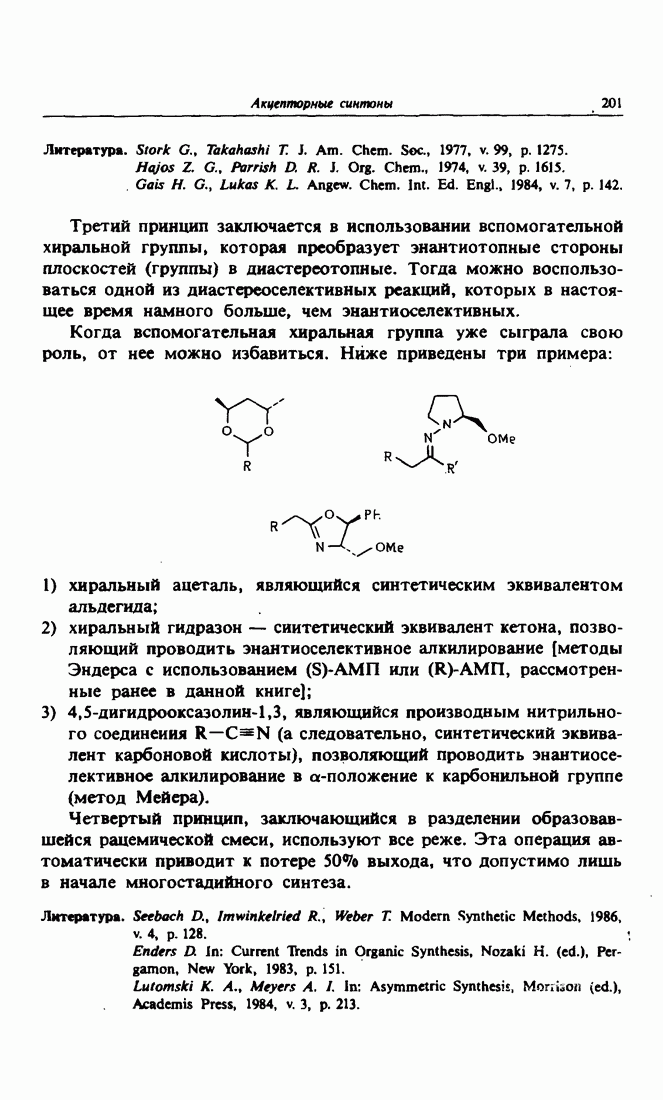
- Глава 16. РЕТРОСИНТЕТИЧЕСКИЙ АНАЛИЗ
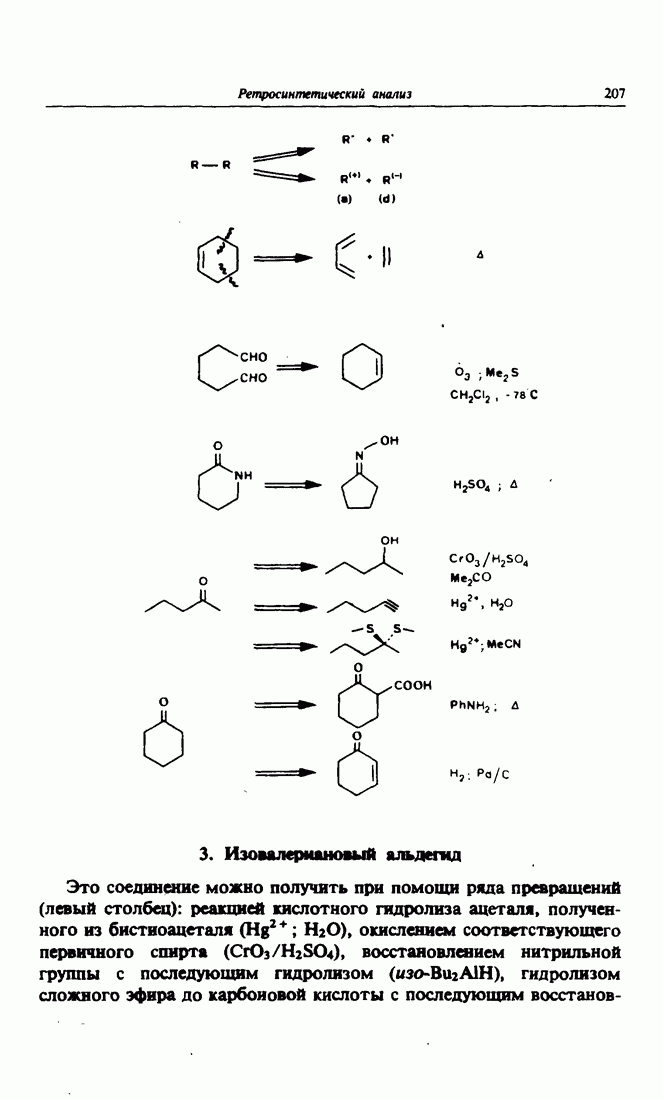
- 2. Цепь превращений
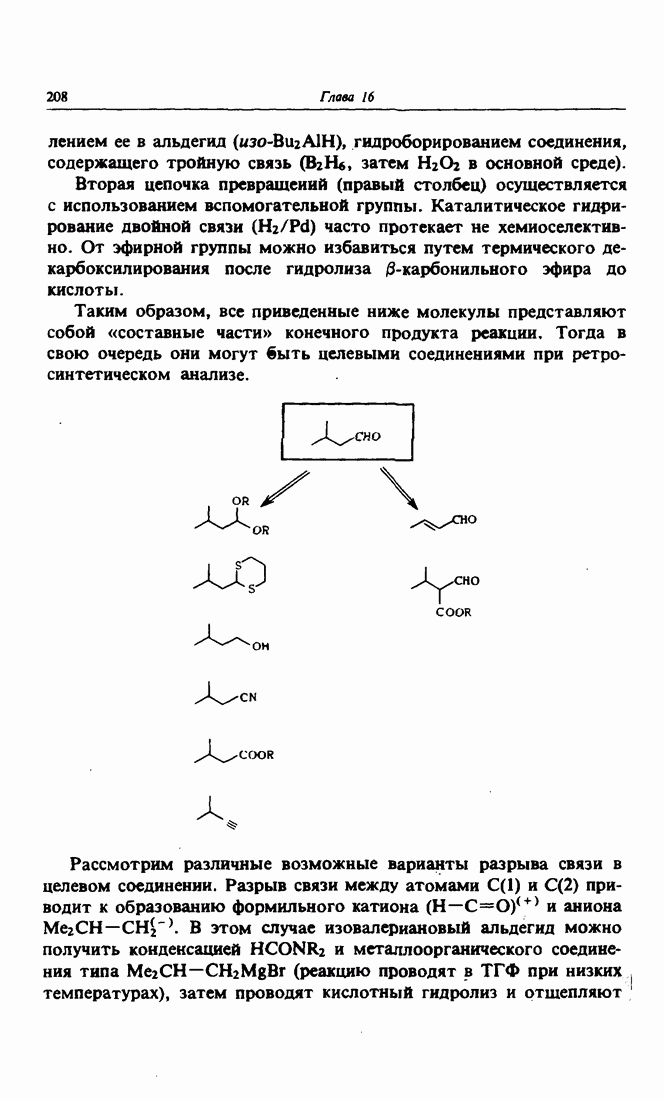
- 3. Изовалериановый альдегид
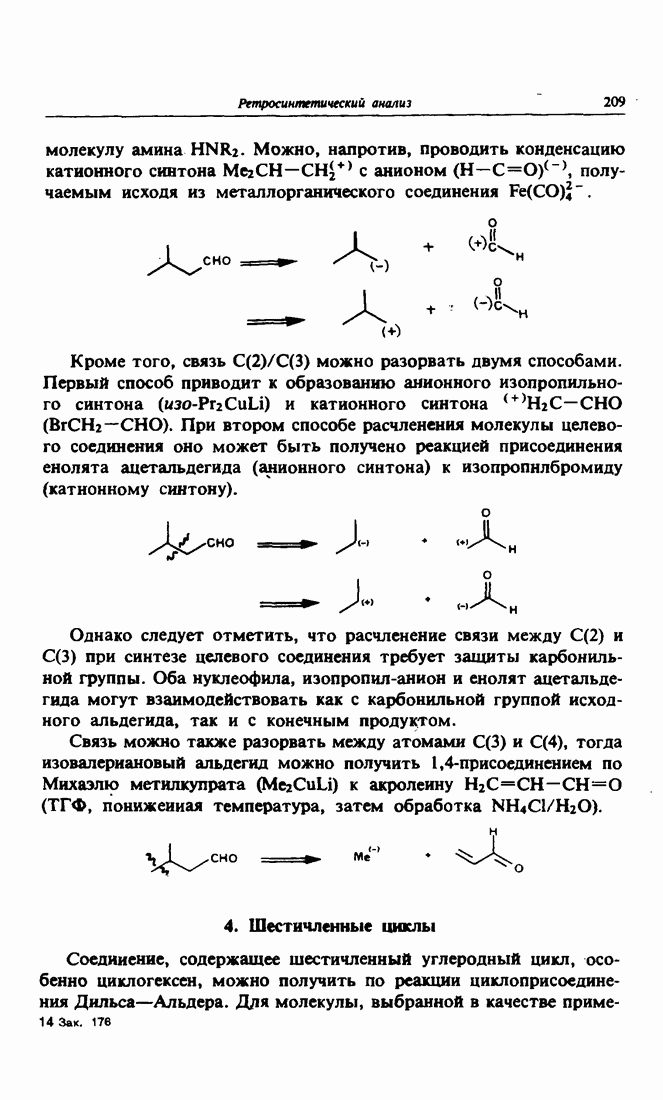
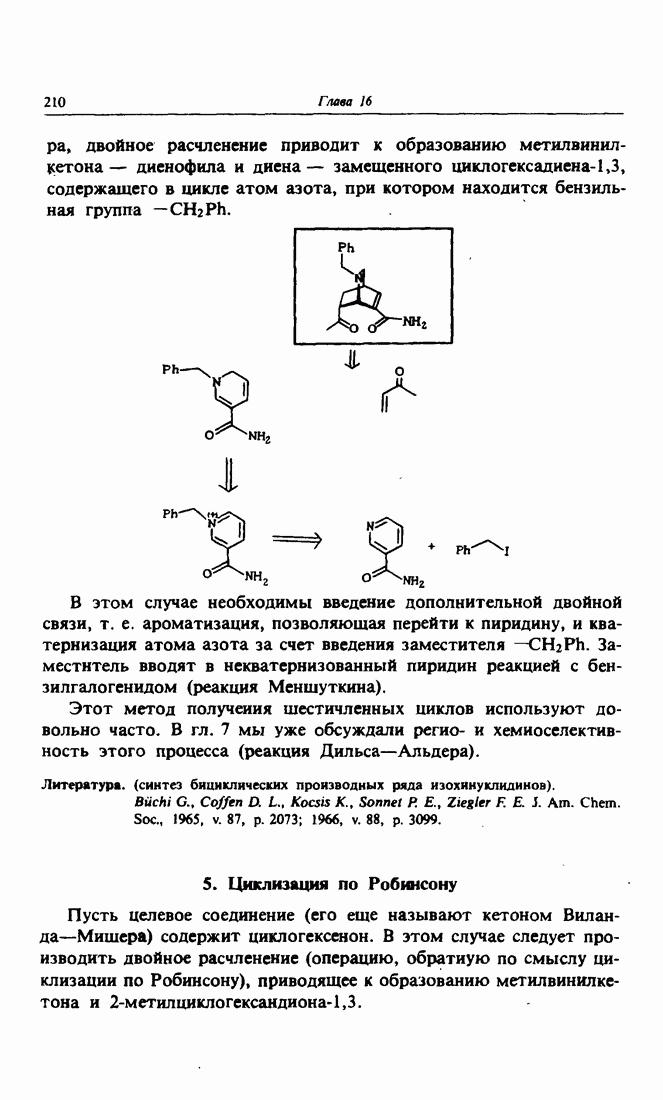
- 4. Шестичленные циклы
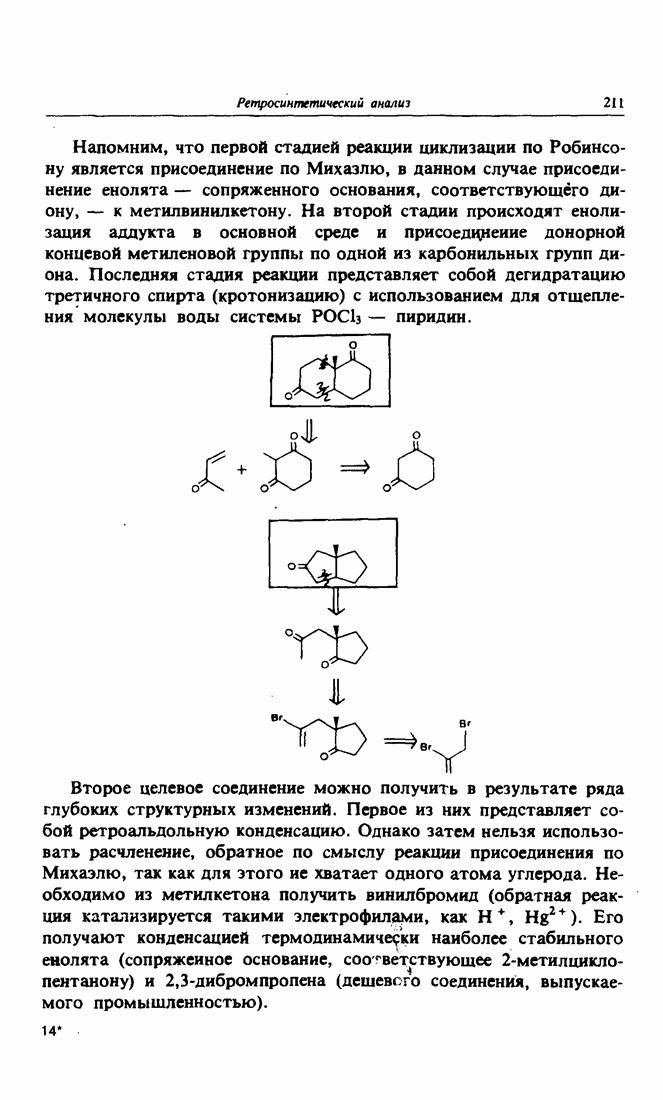
- 5. Циклизация по Робинсону
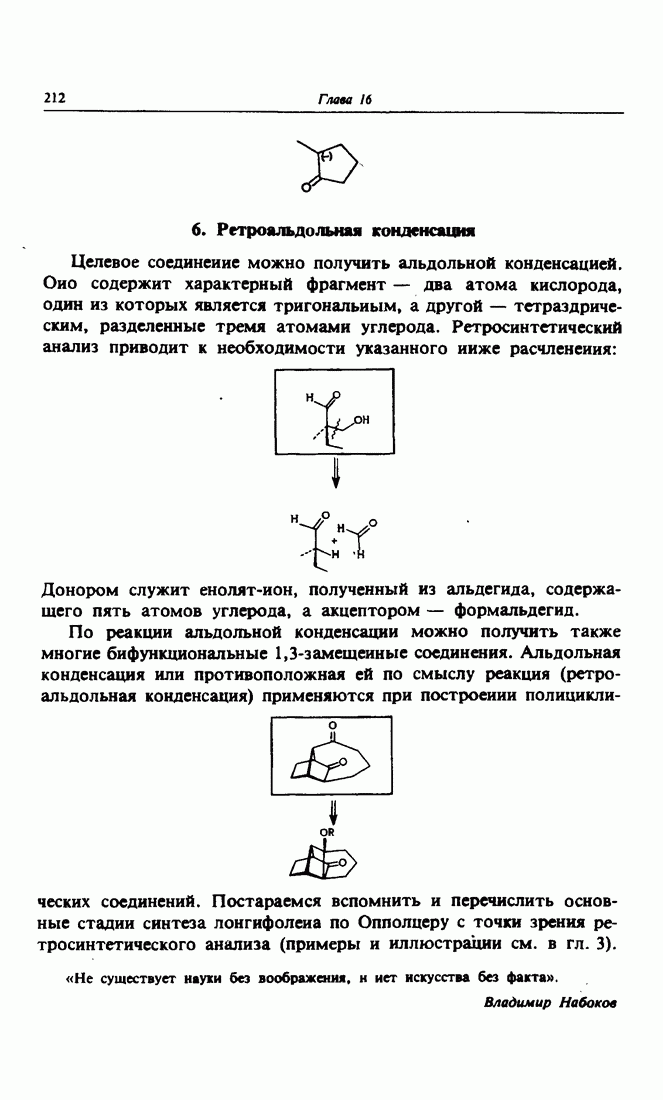
- 6. Ретроальдольная конденсация
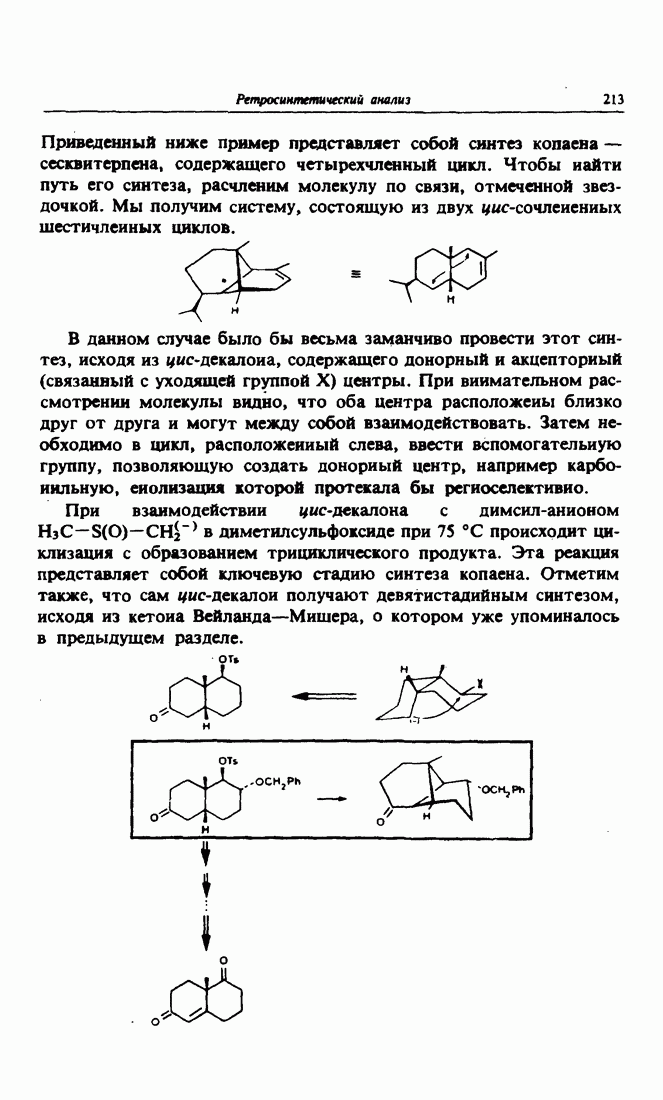
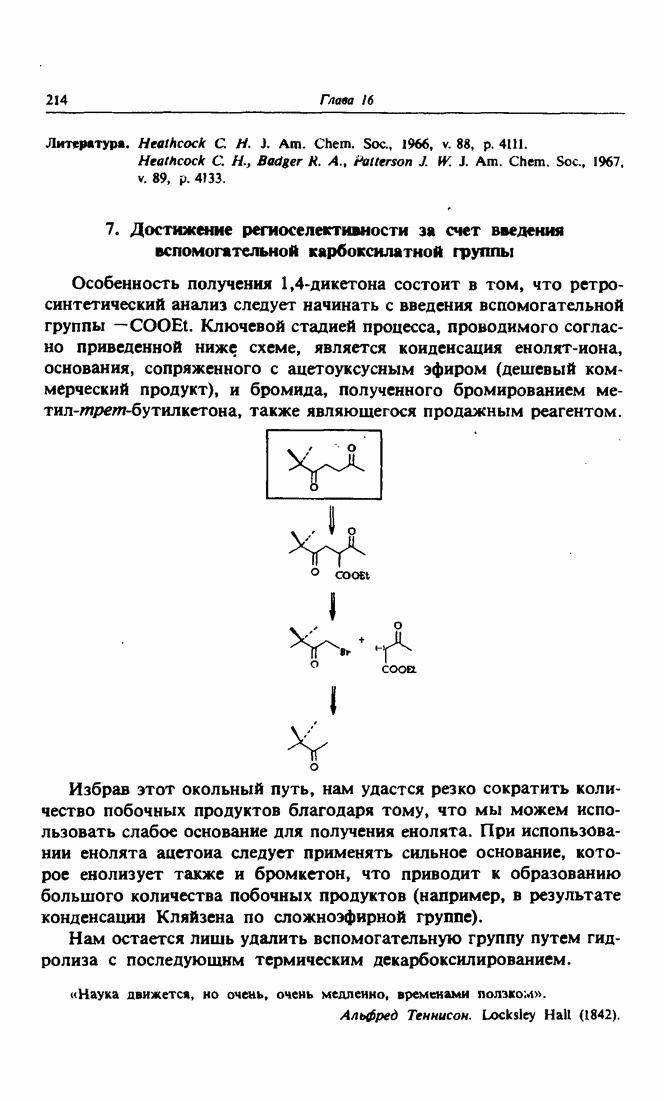
- 7. Достижение региоселективности за счет введения вспомогательной карбоксилатной группы
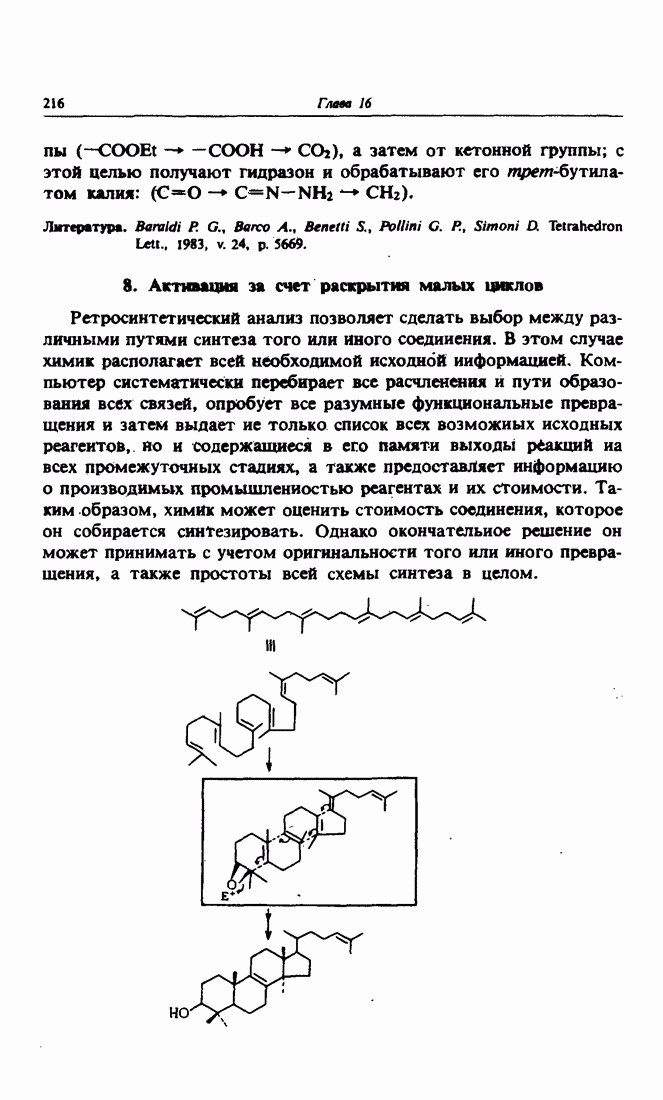
- 8. Активация за счет раскрытия малых циклов
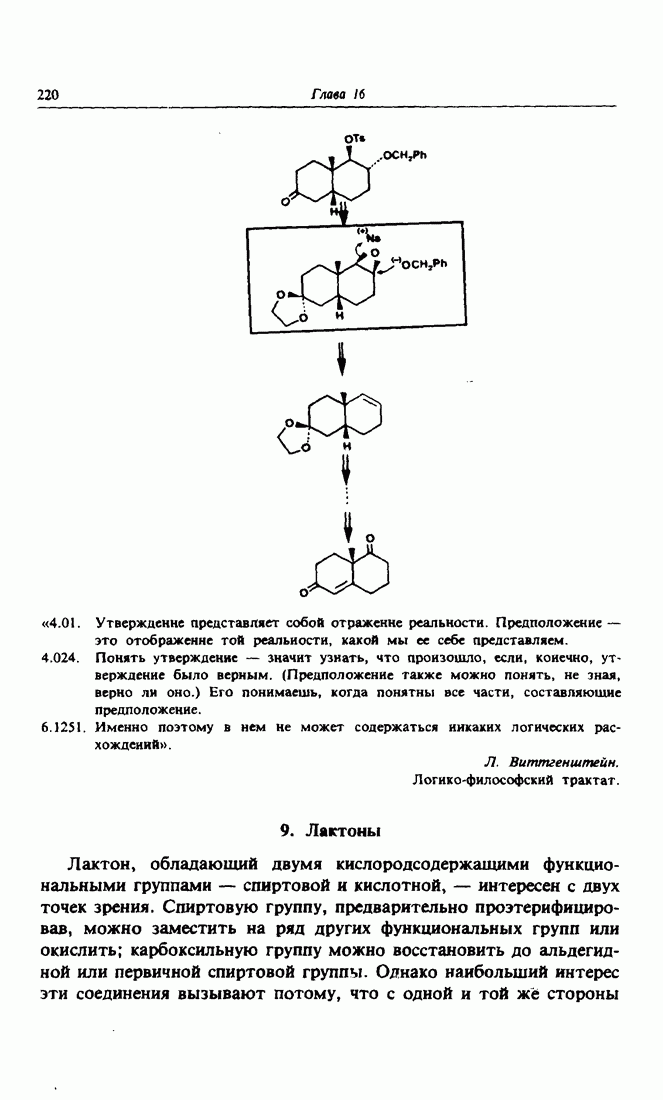
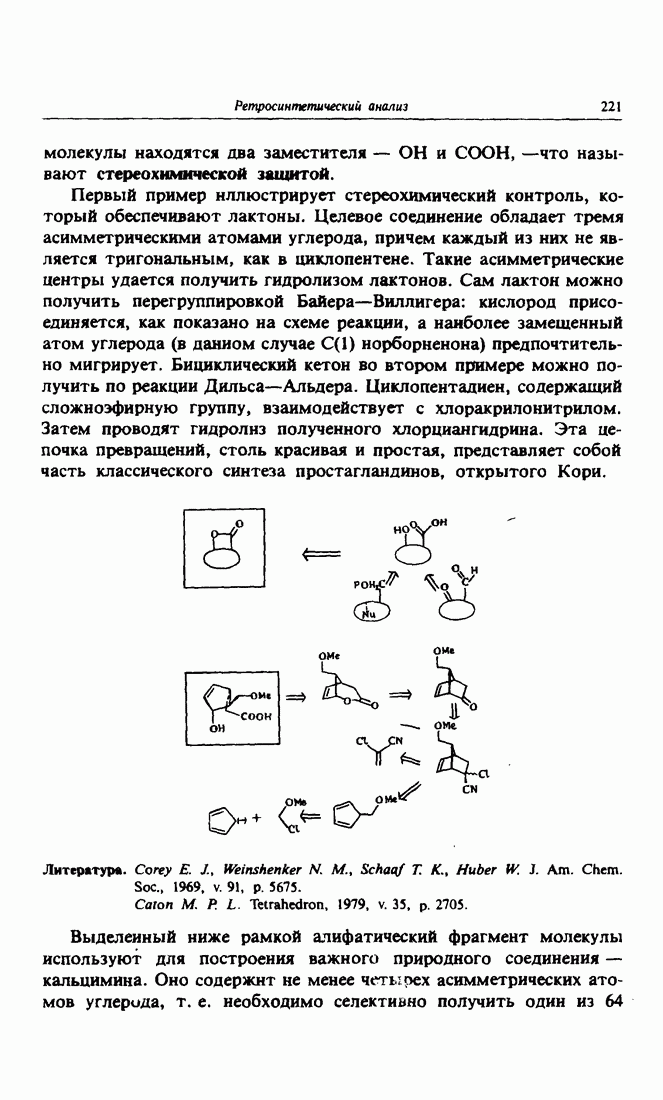
- 9. Лактоны
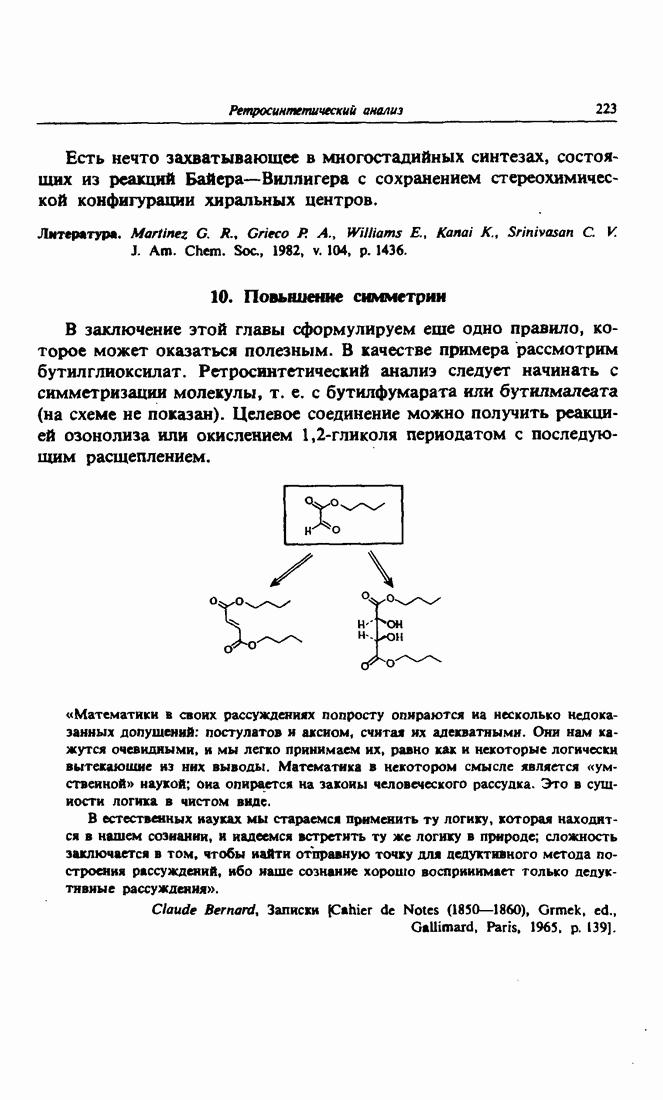
- 10. Повышение симметрии
- ПОСЛЕСЛОВИЕ