| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
Глава 16. РЕТРОСИНТЕТИЧЕСКИЙ АНАЛИЗ
1. Симметризующий ретросинтез
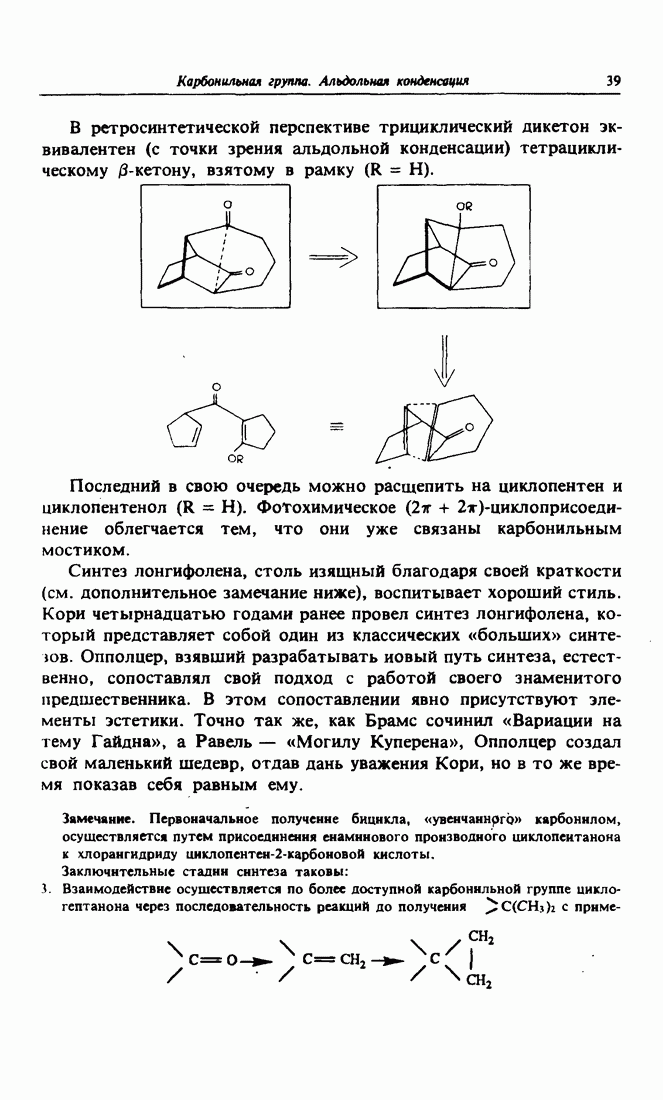
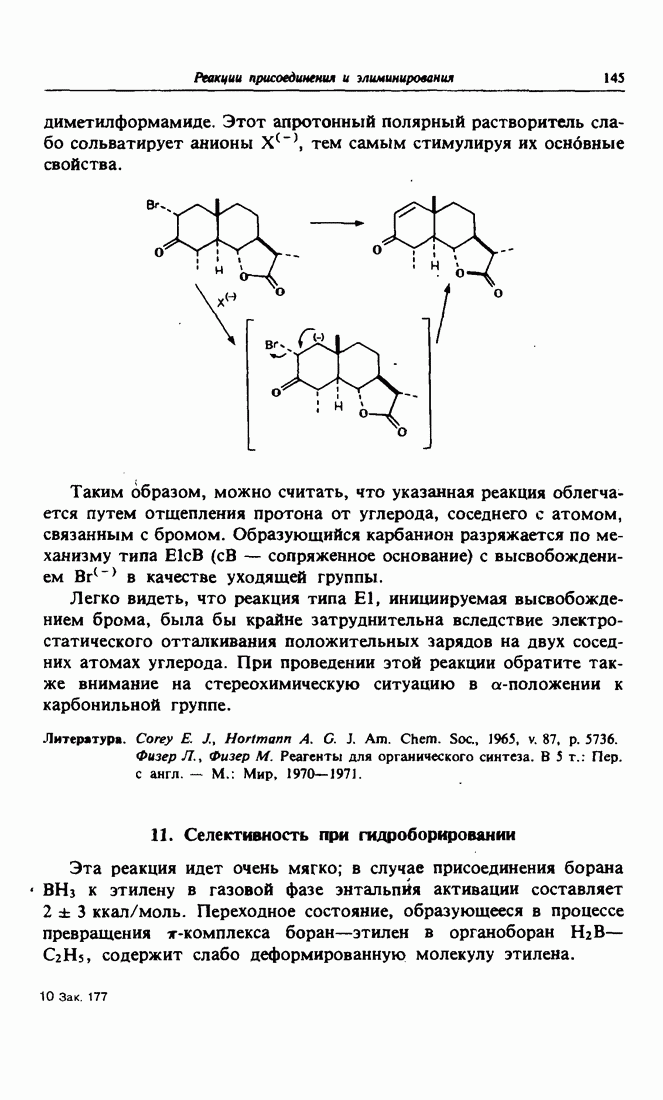
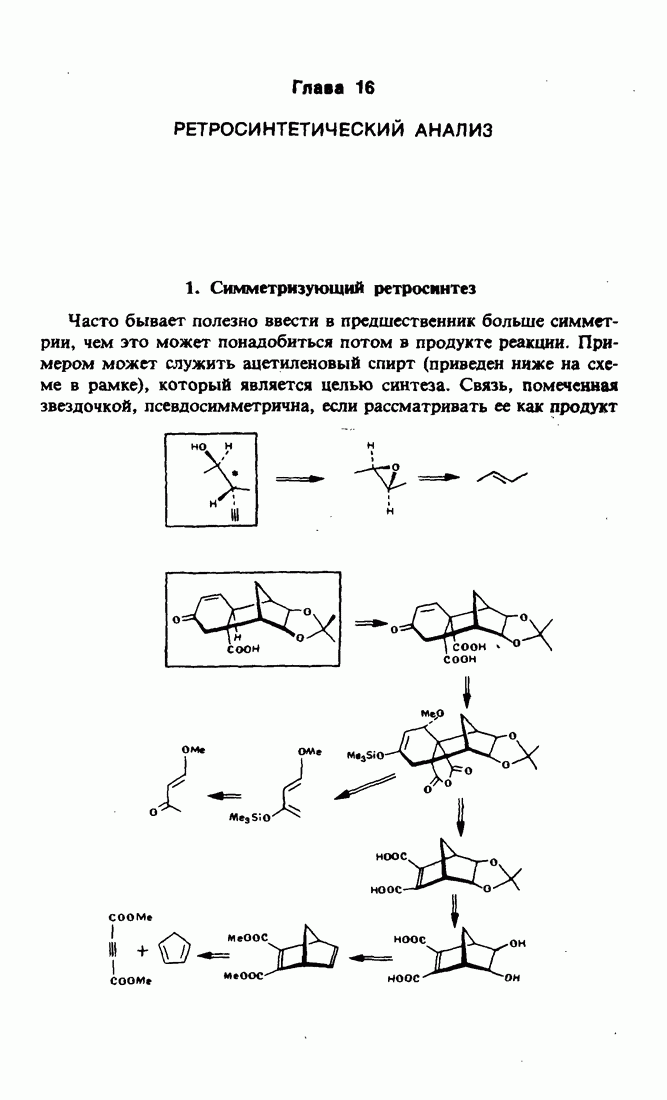
Часто бывает полезно ввести в предшественник больше симметрии, чем это может понадобиться потом в продукте реакции. Примером может служить ацетиленовый спирт (приведен ниже на схеме в рамке), который является целью синтеза. Связь, помеченная звездочкой, псевдосимметрична, если рассматривать ее как продукт
(см. скан)
дисимметрического присоединения по двойной этиленовой связи. Отсюда возникает мысль начать с бутена, точнее с транс-бутена-2, поскольку мы хотим получить эритро-спирт. Структура промежуточного эпоксида определяется процессом активации, которому он подвергается. Достаточно обработать этот эпоксид ацетиленидом, чтобы получить желаемый спирт.
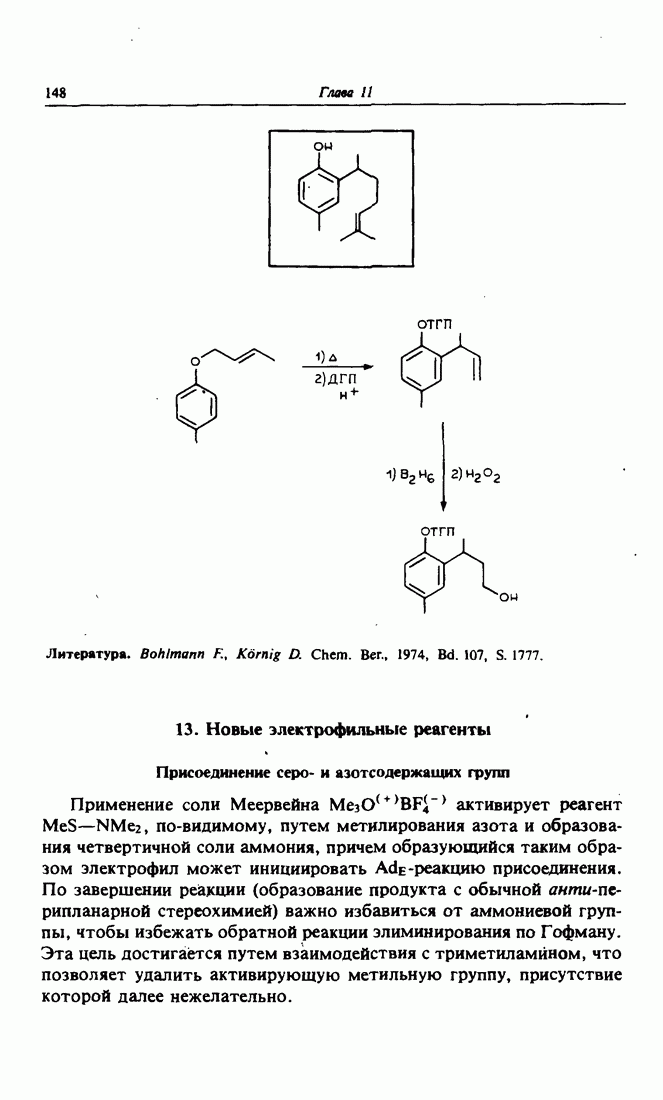
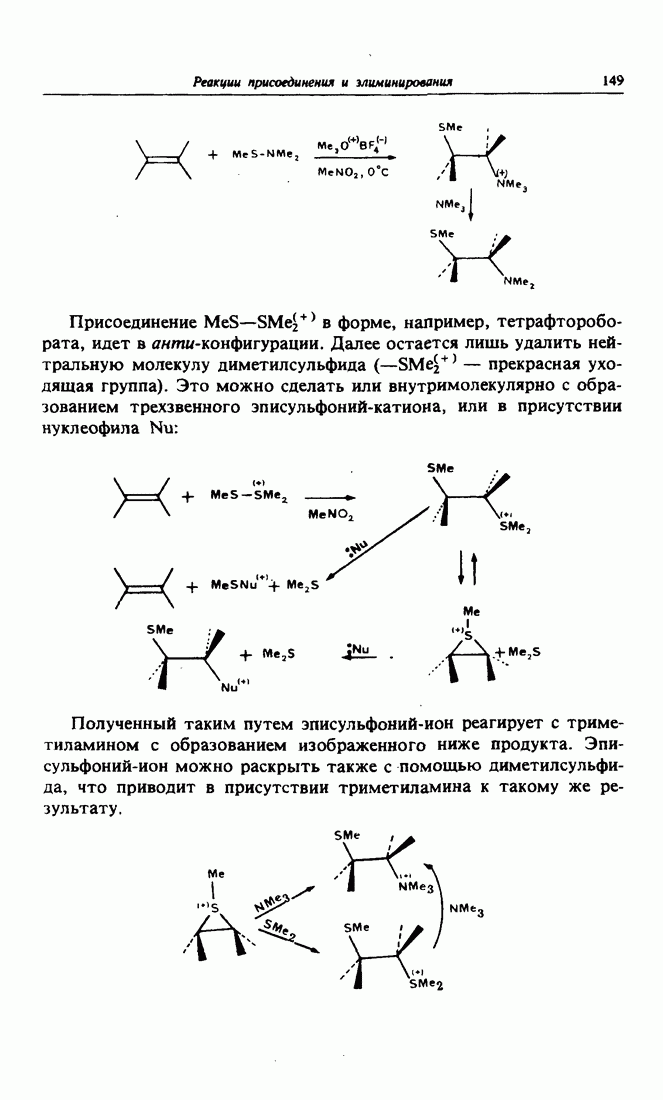
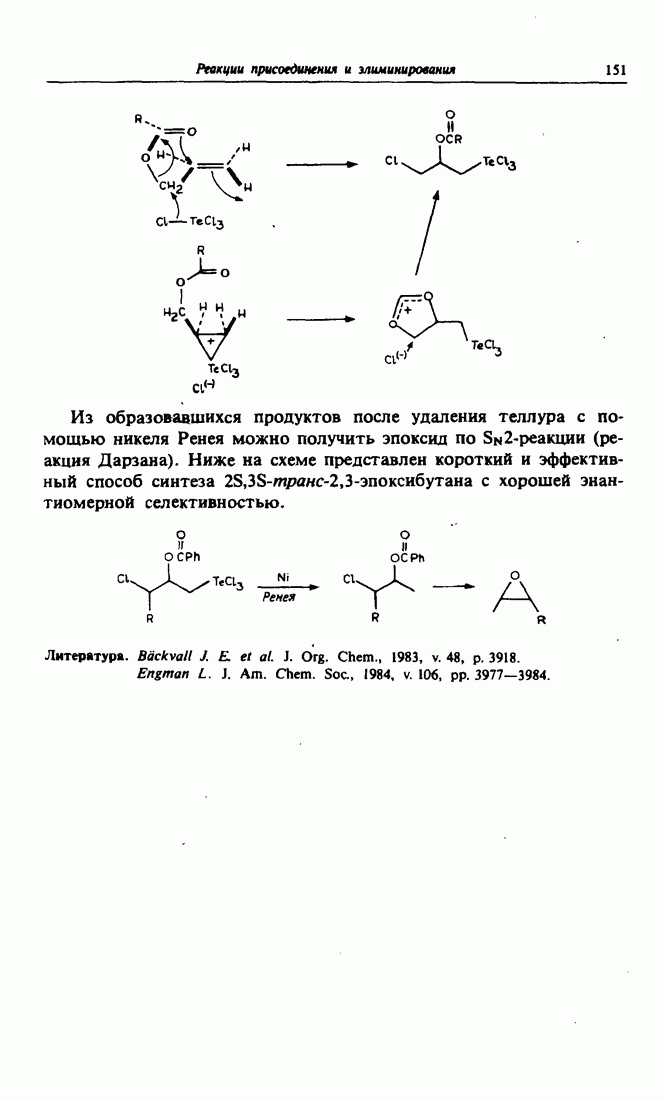
Другой пример позаимствован из синтеза Данишевского. Первая весьма важная стадия этого ретросинтеза состоит в симметризации путем введения второй карбоксильной группы.Ее несложно потом удалить, поскольку она находится в винилоговом положении (через промежуточную двойную связь  -положении к карбоксильной группе). Следовательно, декарбоксилирование при нагревании должно идти гладко. Дикарбоновая кислота одновременно представляет собой еще и циклогексенон. Циклогексен можно получить по реакции Дильса-Альдера. Далее с целью сдвига двойной связи вводят подходящую кислородсодержащую группу в положение, в котором она оказалась бы в результате такого циклоприсоединения. Это диктует, какие надо выбрать днен и диенофил в реакции Дильса-Альдера, чтобы удовлетворить обычным требованиям орбитального соответствия. Таким образом, приходим к необходимости использовать в качестве предшественника диена метилметоксивннилкетон, являющийся коммерчески доступным реактивом. Что касается диенофил а, то выбираем аддукт первой реакции Дильса-Альдера между циклопентадиеном и метиловым эфиром ацетилендикарбоновой кислоты с промежуточным региоселективным образованием 1,2-гликоля.
-положении к карбоксильной группе). Следовательно, декарбоксилирование при нагревании должно идти гладко. Дикарбоновая кислота одновременно представляет собой еще и циклогексенон. Циклогексен можно получить по реакции Дильса-Альдера. Далее с целью сдвига двойной связи вводят подходящую кислородсодержащую группу в положение, в котором она оказалась бы в результате такого циклоприсоединения. Это диктует, какие надо выбрать днен и диенофил в реакции Дильса-Альдера, чтобы удовлетворить обычным требованиям орбитального соответствия. Таким образом, приходим к необходимости использовать в качестве предшественника диена метилметоксивннилкетон, являющийся коммерчески доступным реактивом. Что касается диенофил а, то выбираем аддукт первой реакции Дильса-Альдера между циклопентадиеном и метиловым эфиром ацетилендикарбоновой кислоты с промежуточным региоселективным образованием 1,2-гликоля.
Литература.
(см. скан)
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- Глава 1. КАРБОНИЛЬНАЯ ГРУППА. РЕАКЦИИ ПРИСОЕДИНЕНИЯ И ПРИСОЕДИНЕНИЯ—ФРАГМЕНТАЦИИ
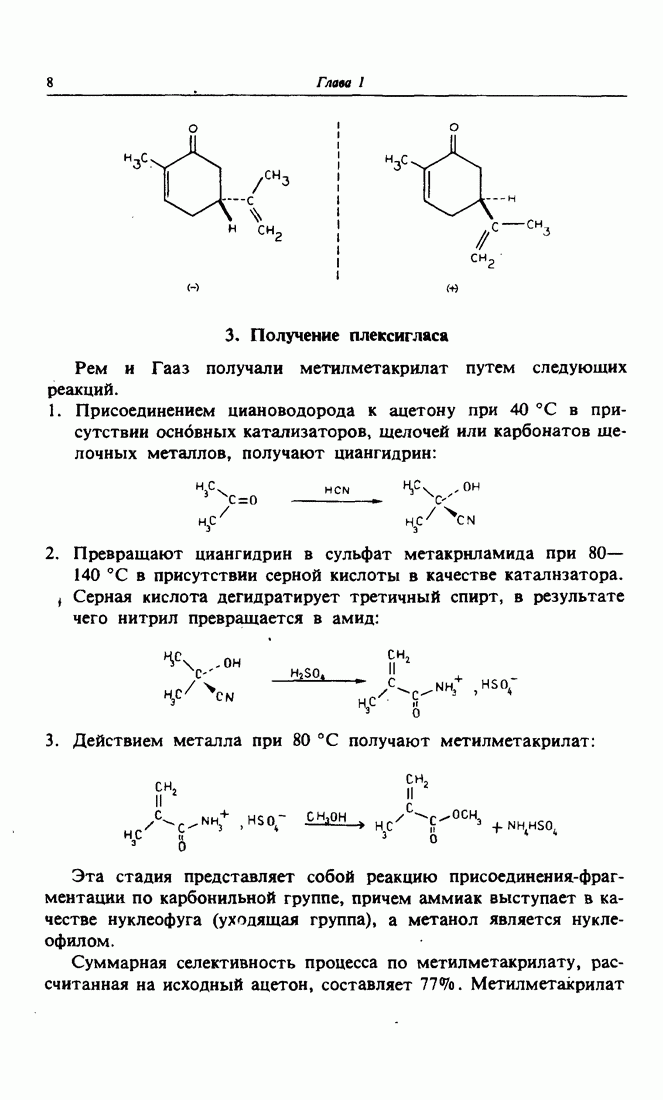
- 3. Получение плексигласа
- 4. Доступность и селективность
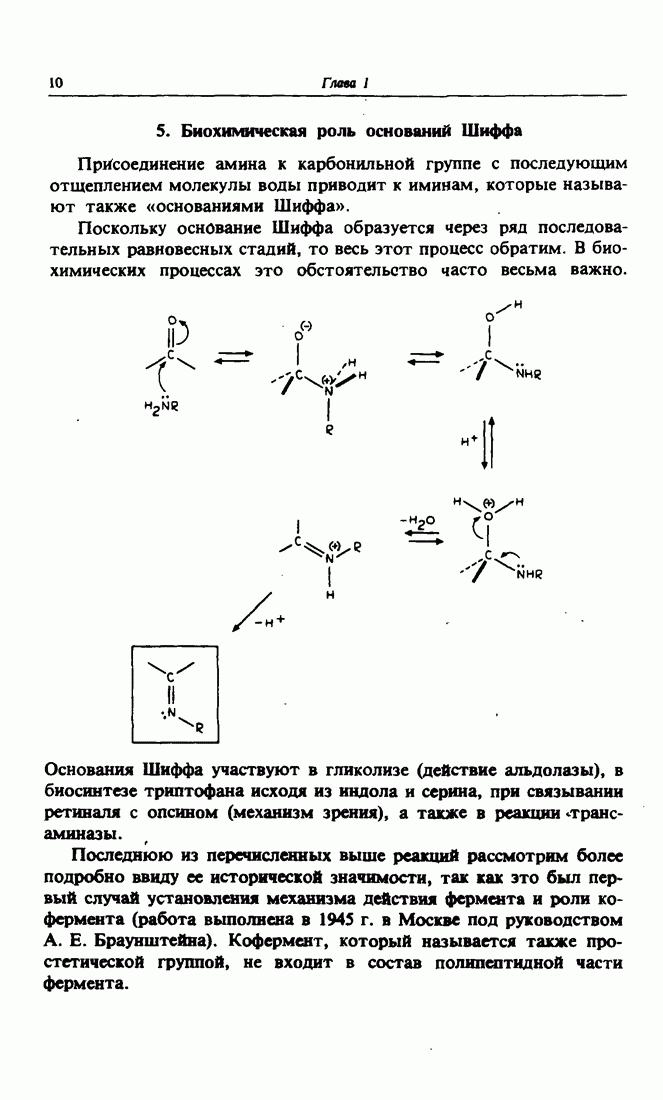
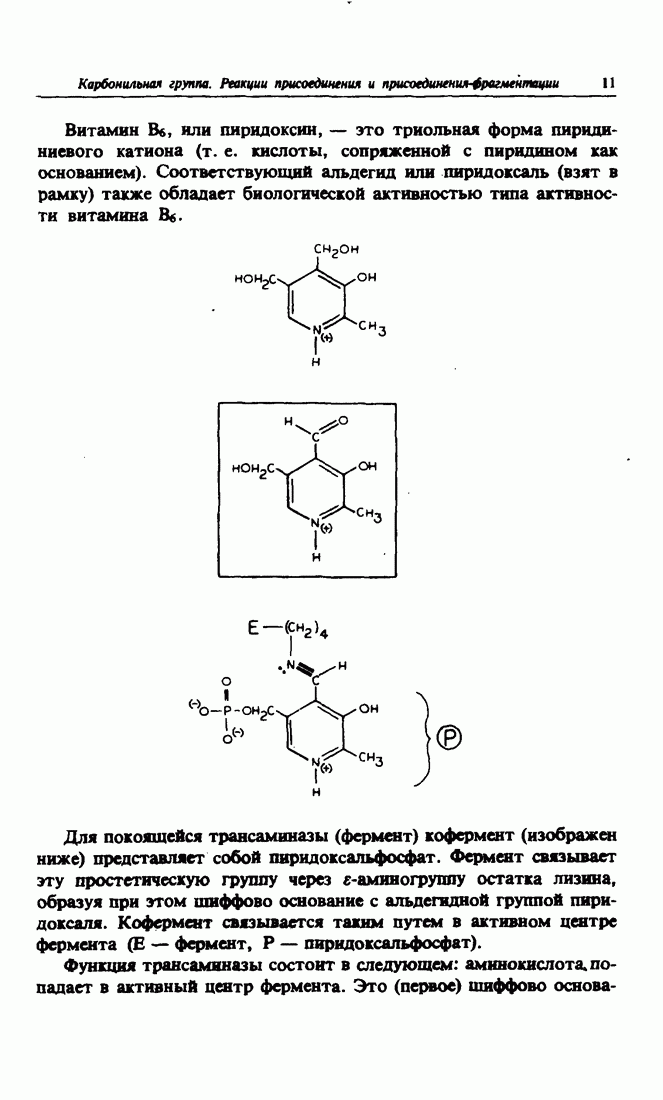
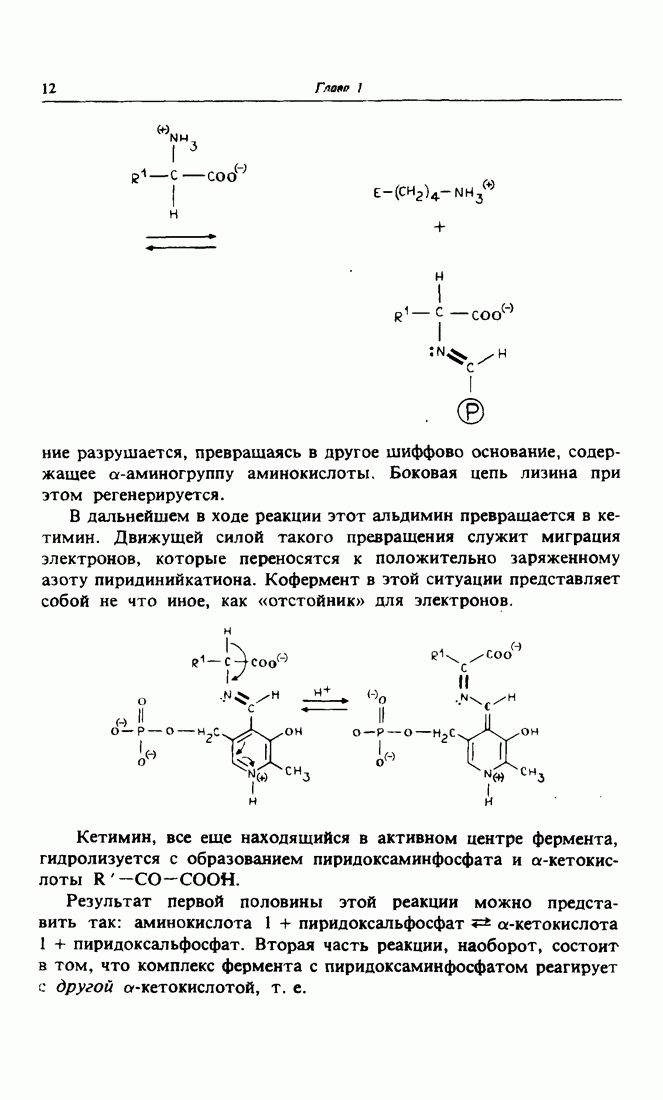
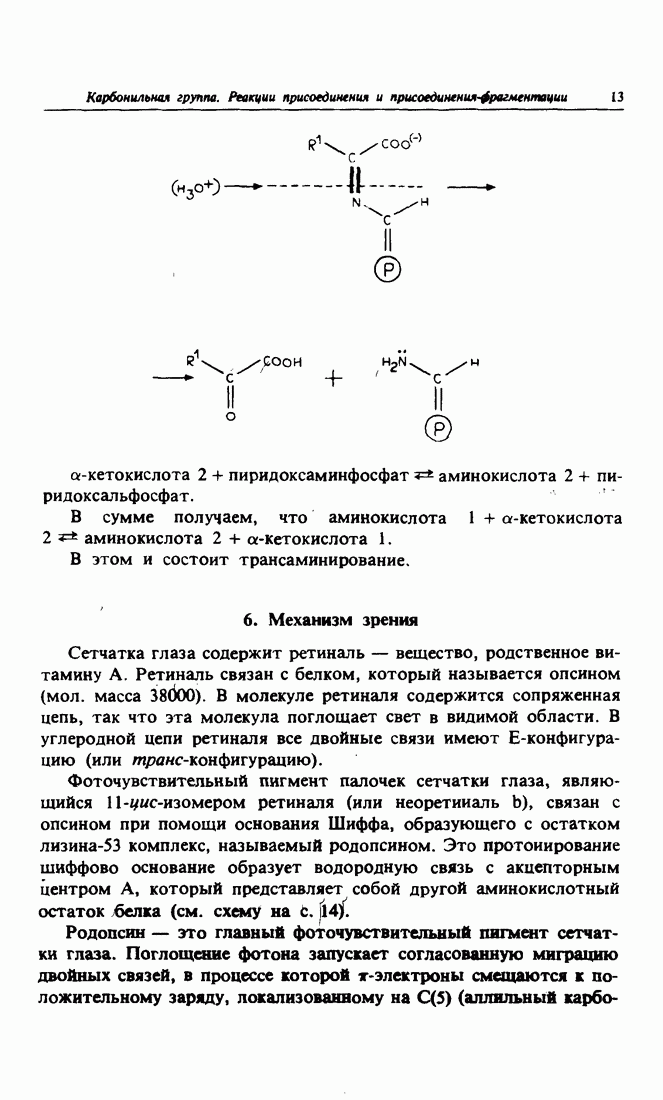
- 5. Биохимическая роль оснований Шиффа
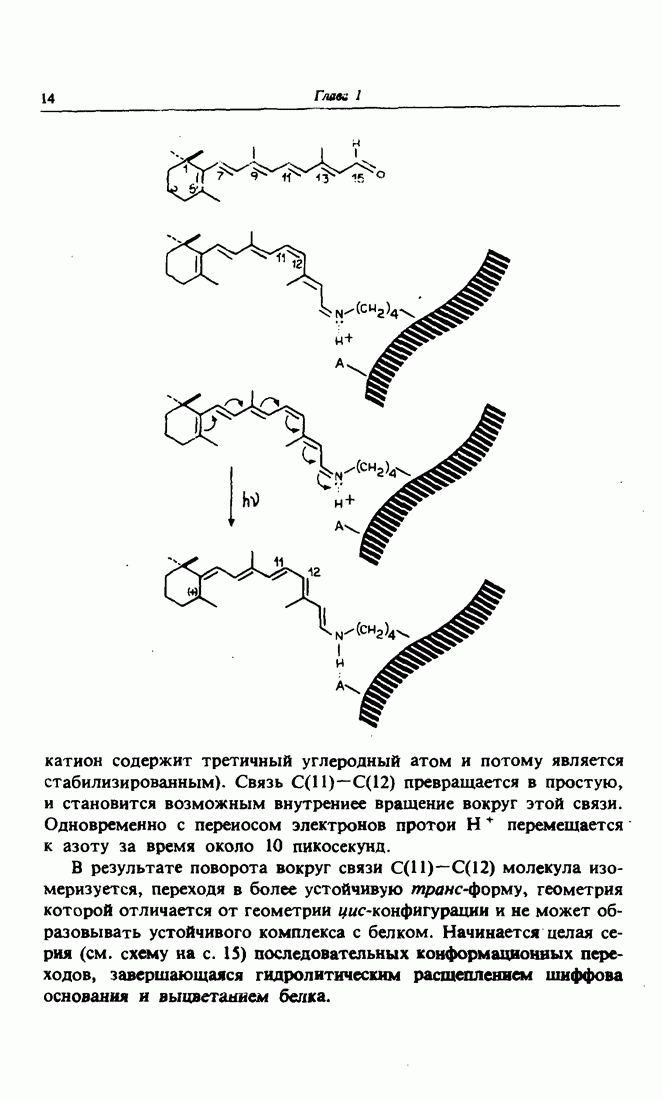
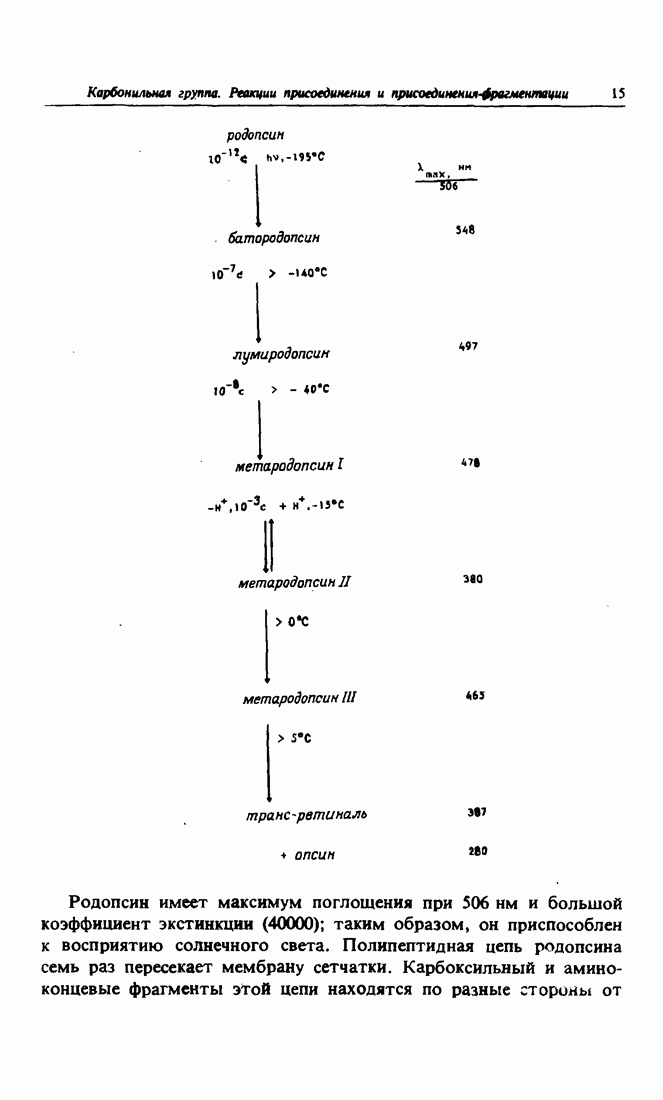
- 6. Механизм зрения
- 7. Цветное зрение
- 8. Новый способ маскировки
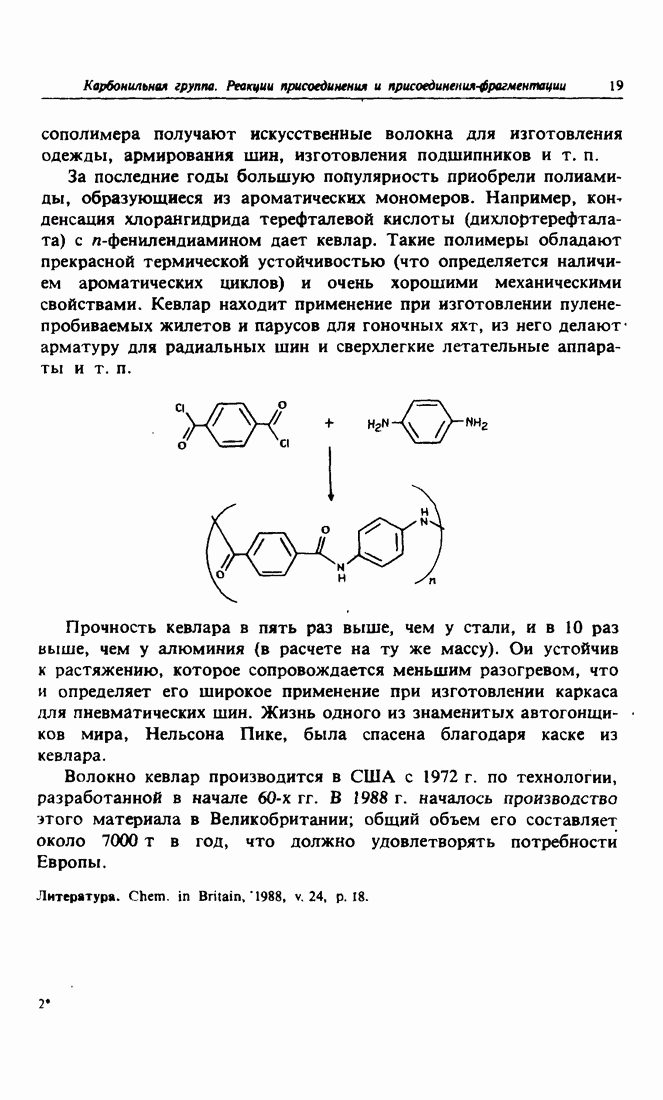
- 9. Полиамиды
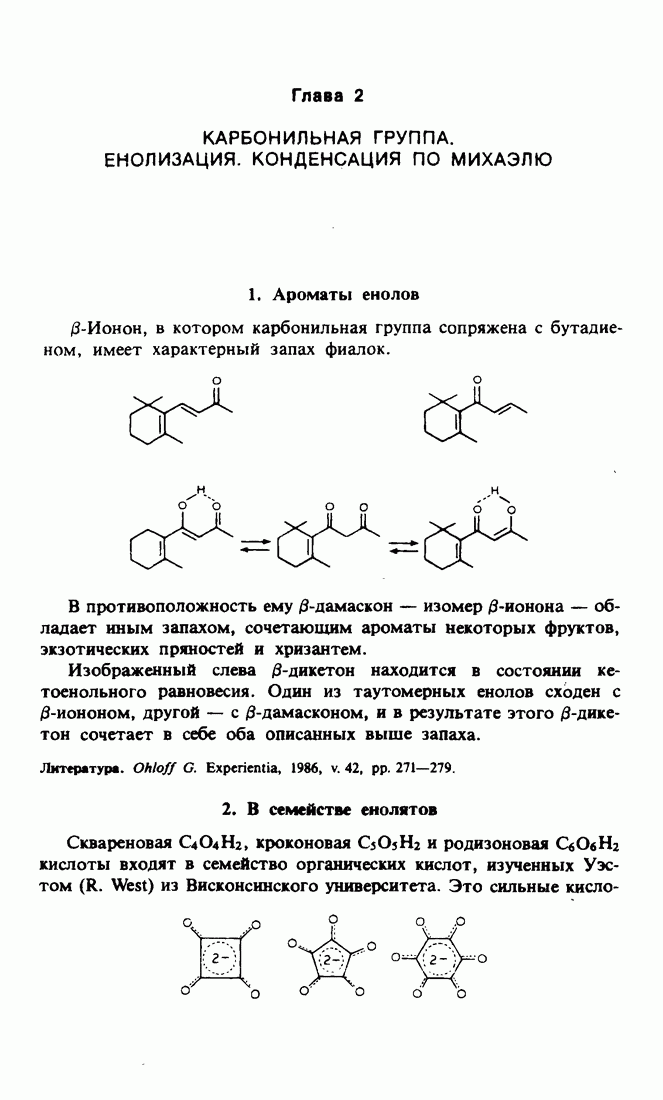
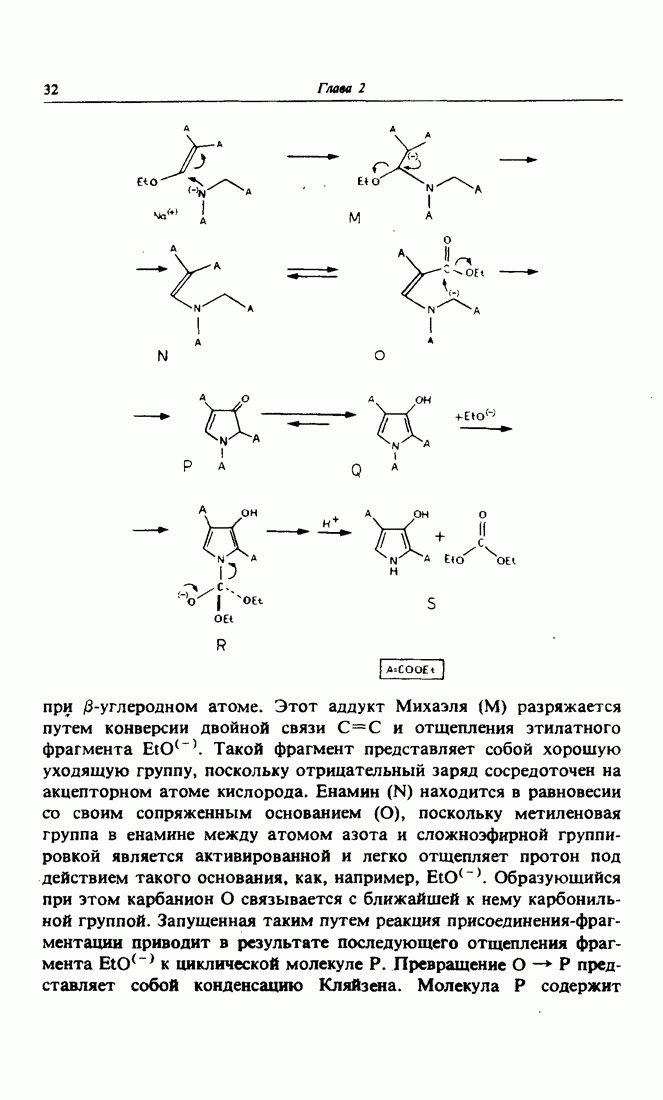
- Глава 2. КАРБОНИЛЬНАЯ ГРУППА. ЕНОЛИЗАЦИЯ. КОНДЕНСАЦИЯ ПО МИХАЭЛЮ
- 2. В семействе енолятов
- 3. Химические продукты, имеющие важные применения в промышленности. Формальдегид
- 4. Бакелит
- 5. Природное соединение, содержащее карбонильную группу и a,b-ненасыщенную связь
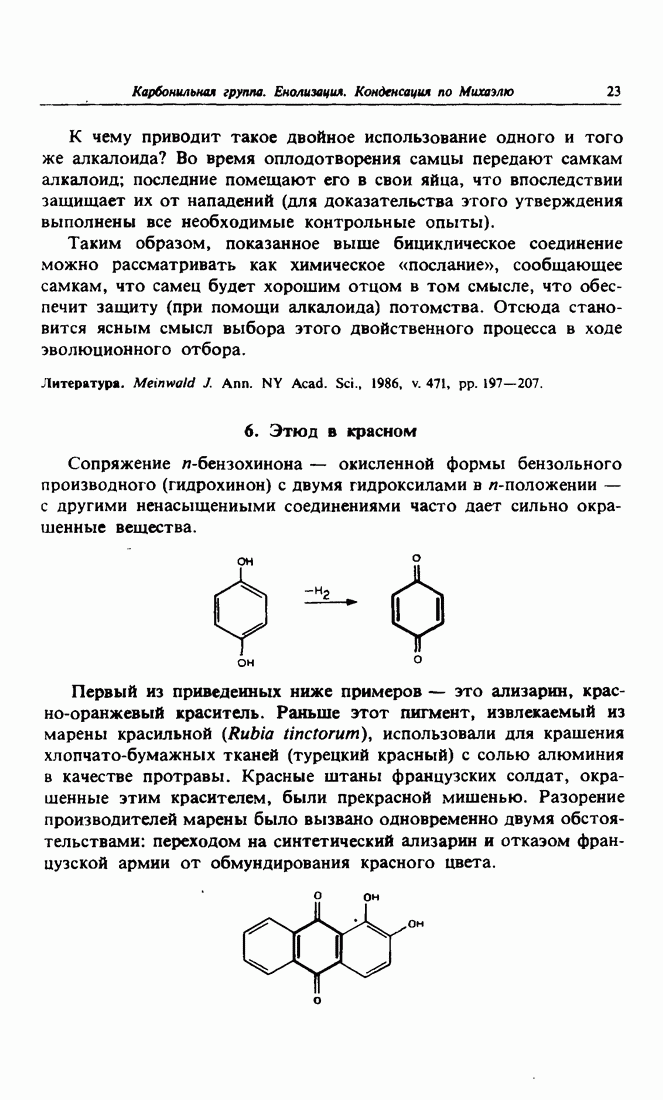
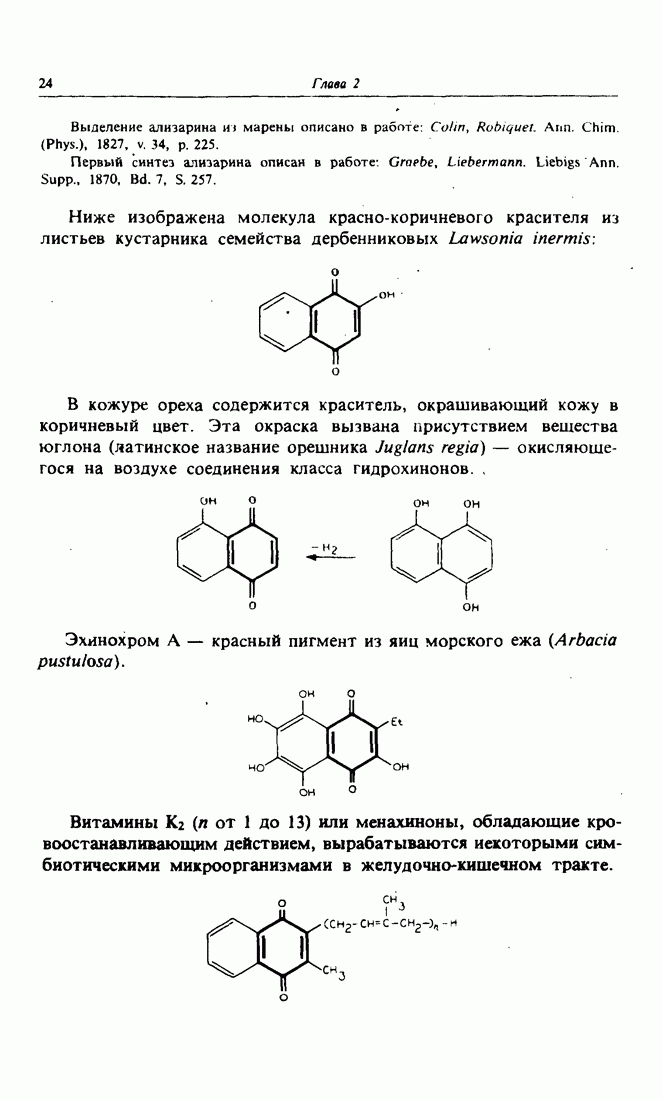
- 6. Этюд в красном
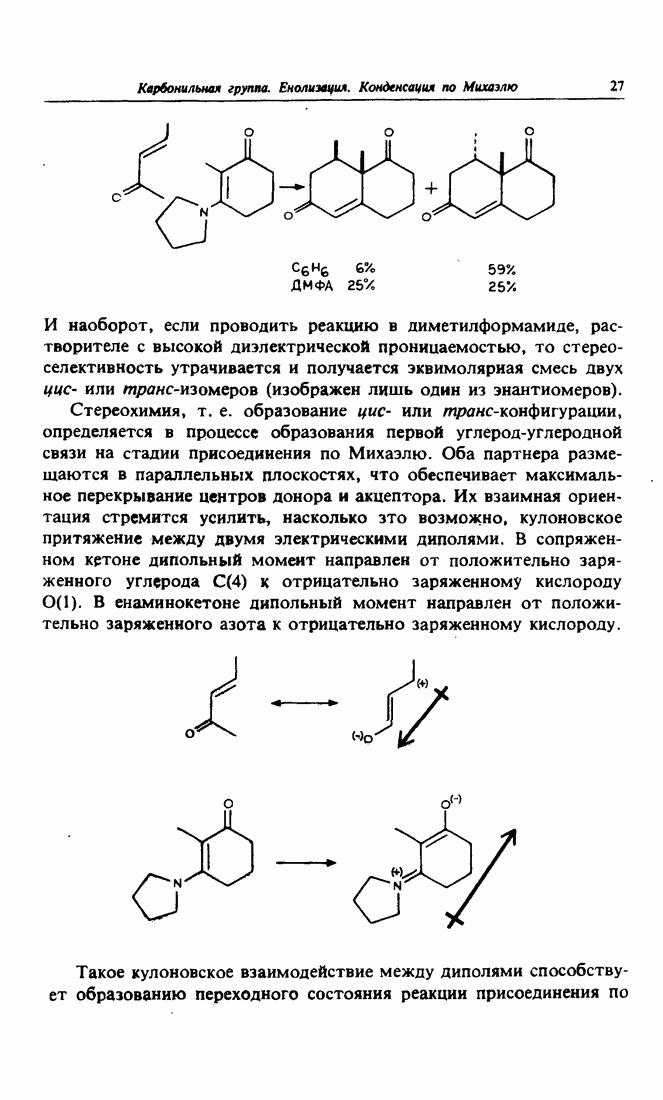
- 7. Использование реакции Михаэля в синтезе стероидов
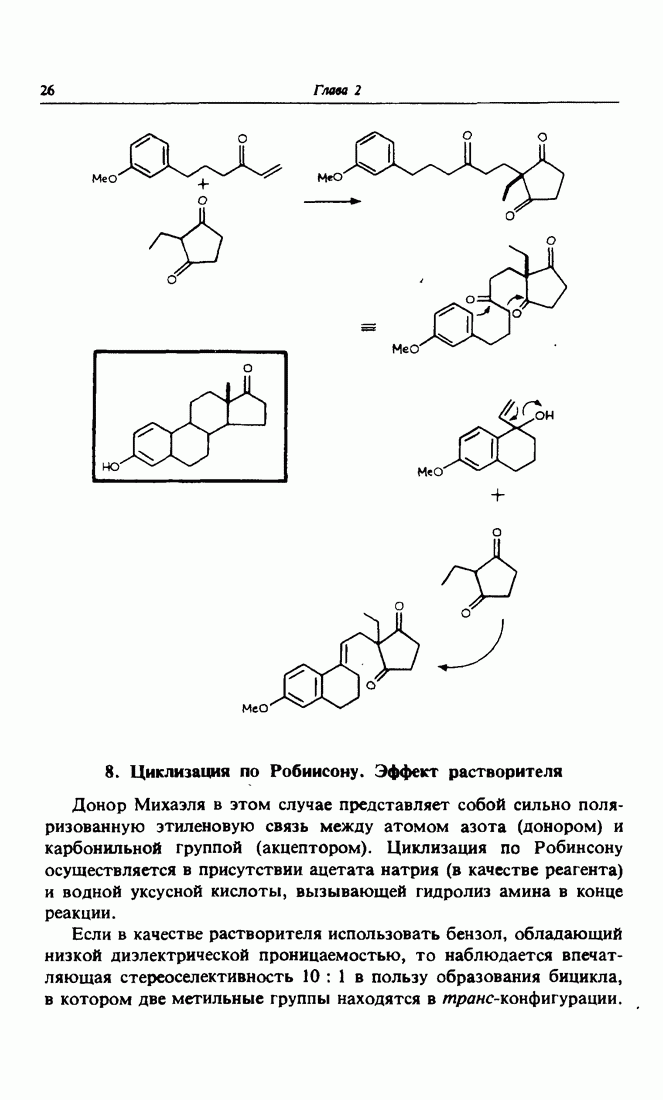
- 8. Циклизация по Робинсону. Эффект растворителя
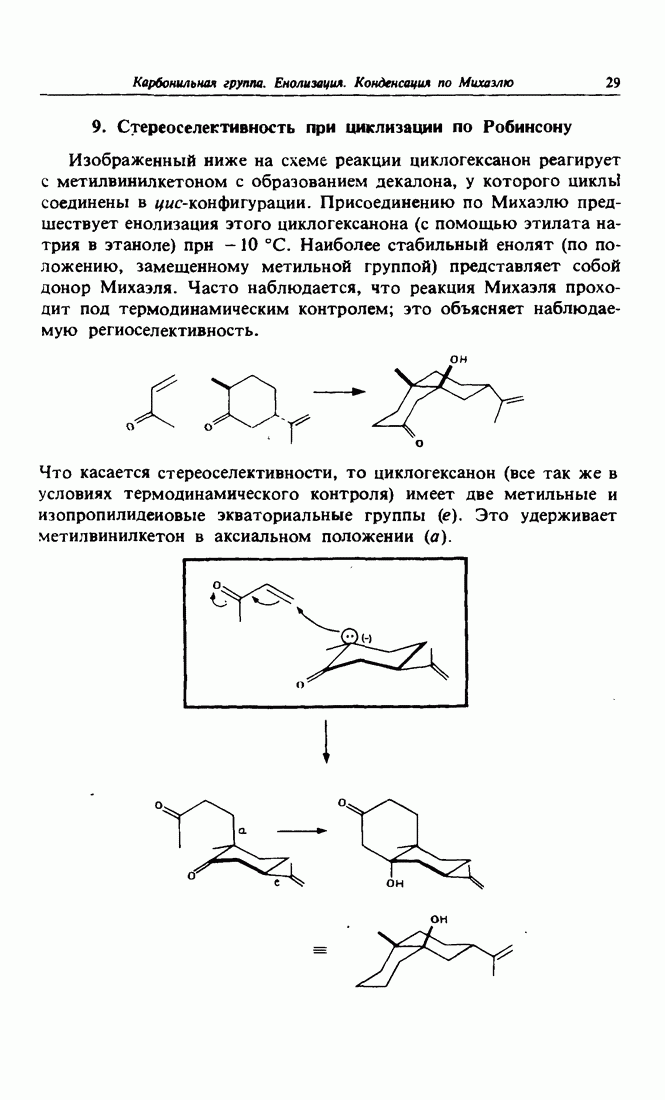
- 9. Стереоселективность при циклизации по Робинсону
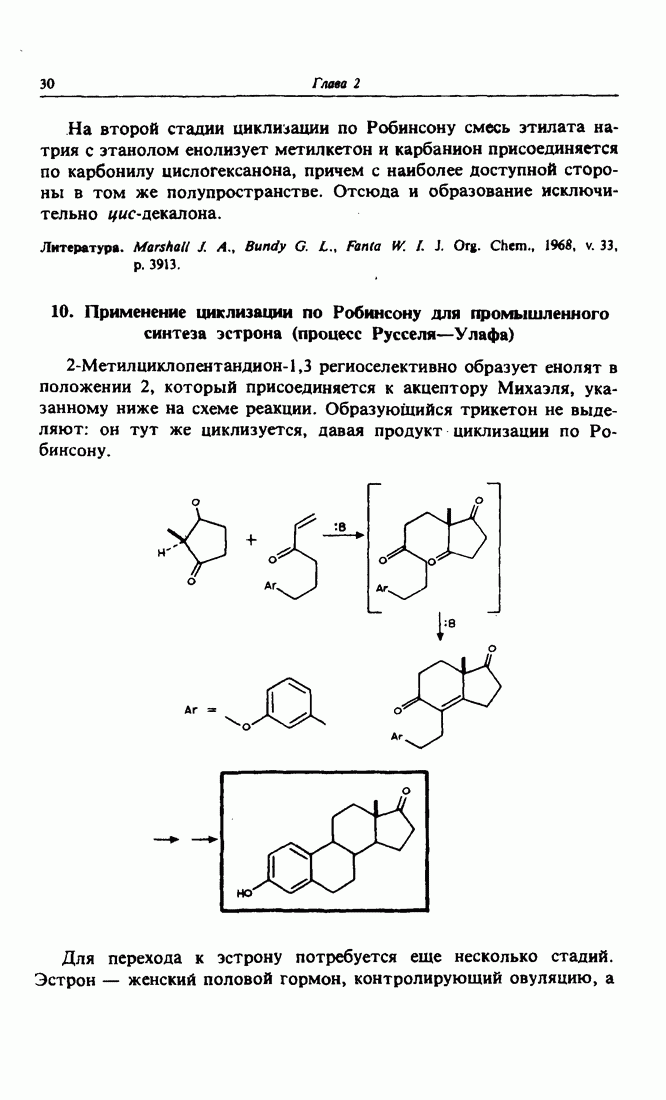
- 10. Применение циклизации по Робинсону для промышленного синтеза эстрона (процесс Русселя-Улафа)
- 11. Следы крови на церковных облатках
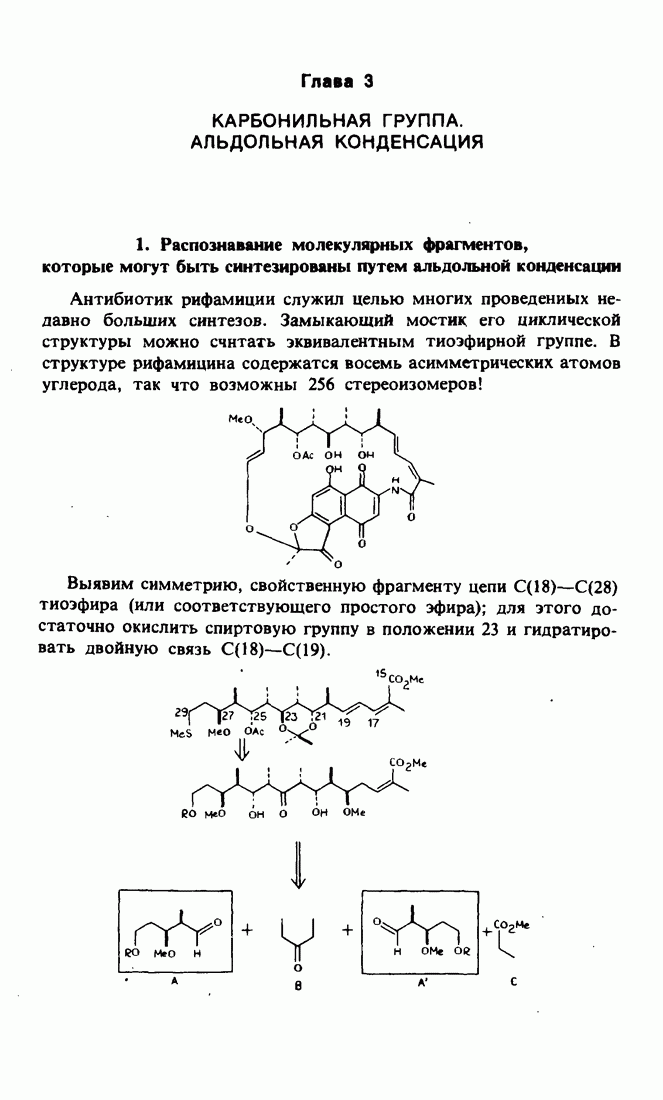
- Глава 3. КАРБОНИЛЬНАЯ ГРУППА. АЛЬДОЛЬНАЯ КОНДЕНСАЦИЯ
- 2. «Музыкальное родство» альдольной конденсации
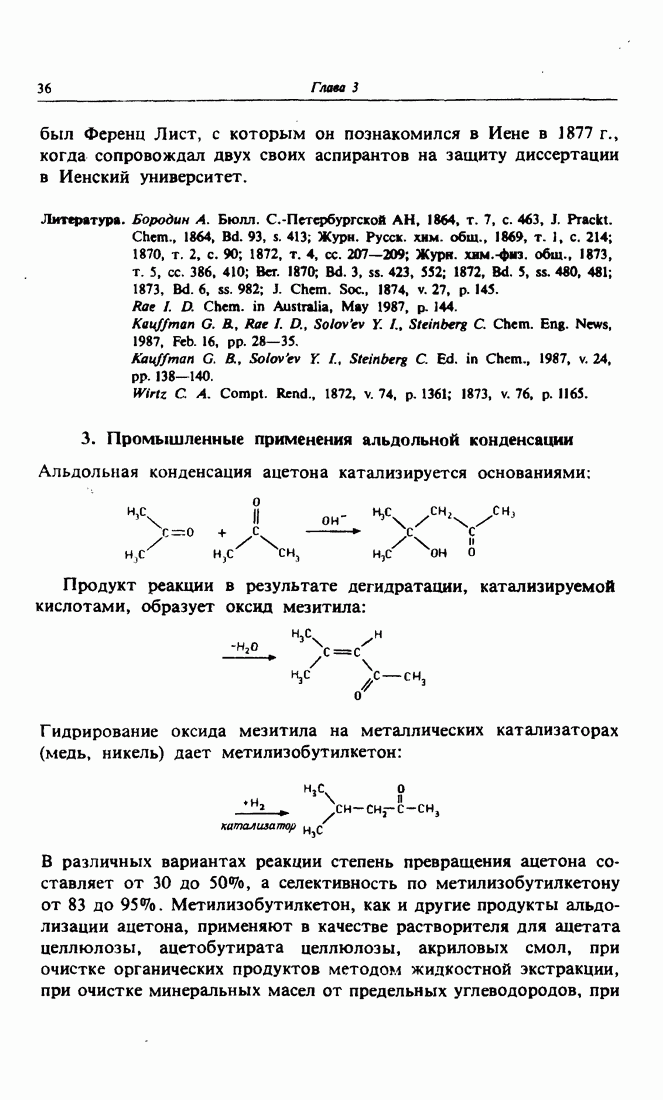
- 3. Промышленные применения альдольной конденсации
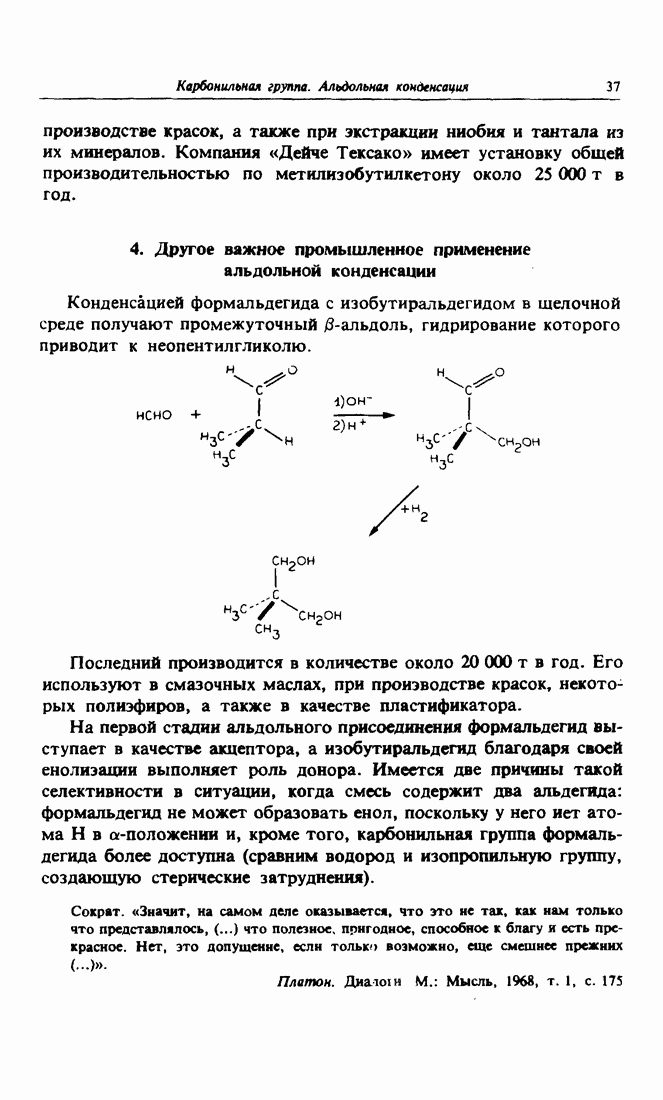
- 4. Другое важное промышленное применение альдольной конденсации
- 5. Альдольная конденсация и «большие» органические синтезы
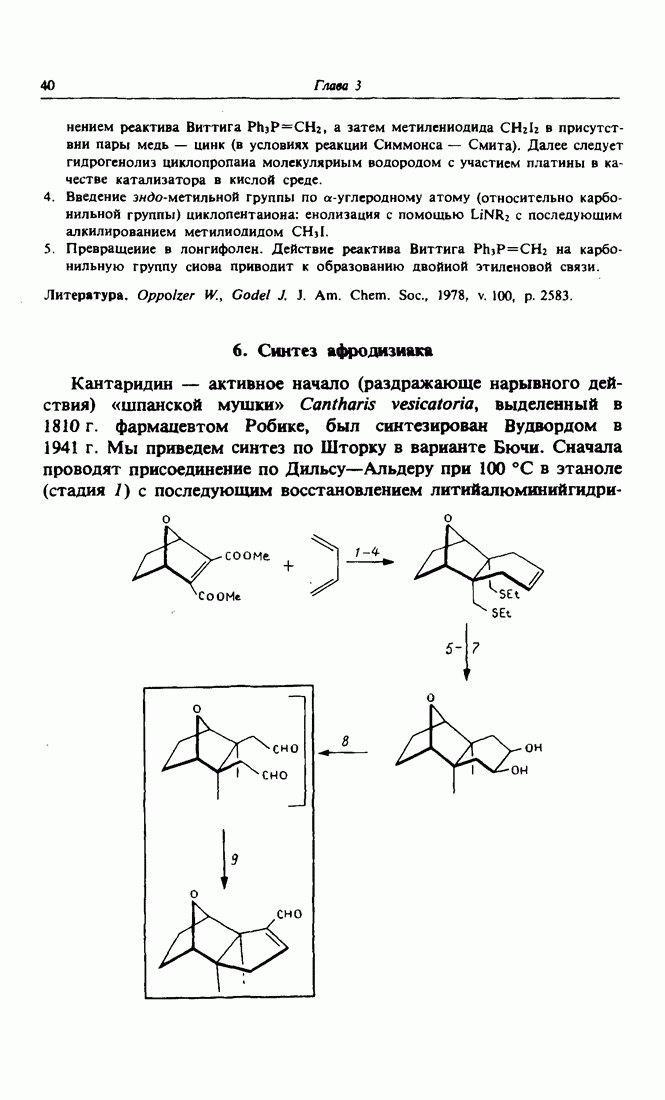
- 6. Синтез афродизиака
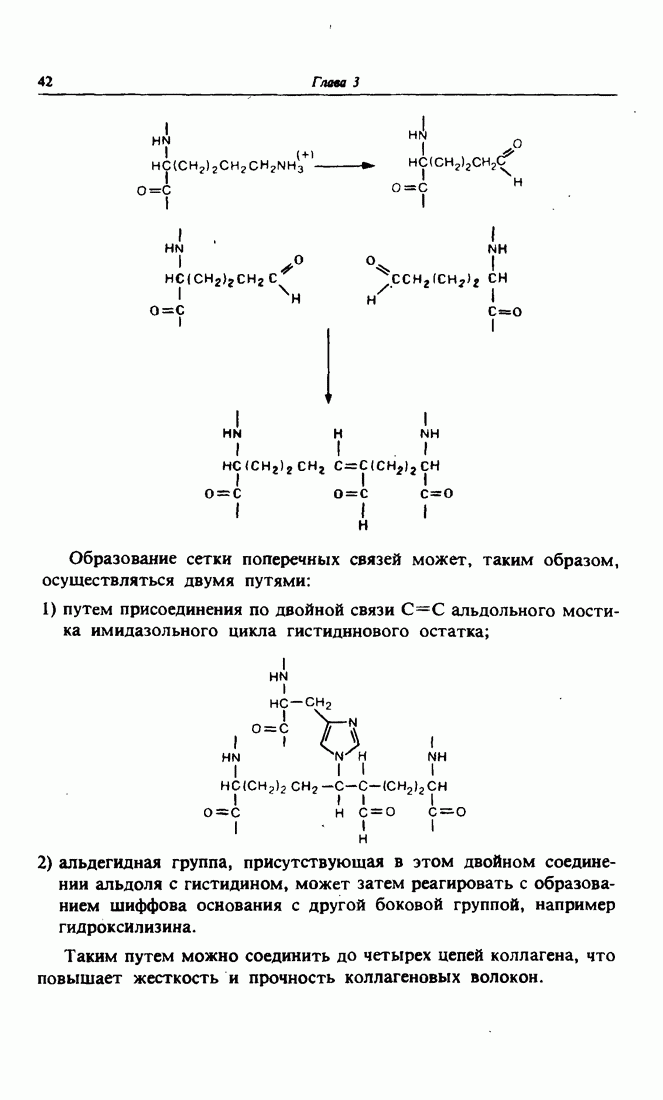
- 7. Альдольная конденсация и механическая прочность сухожилий
- 8. Важные химические продукты. Винилацетат
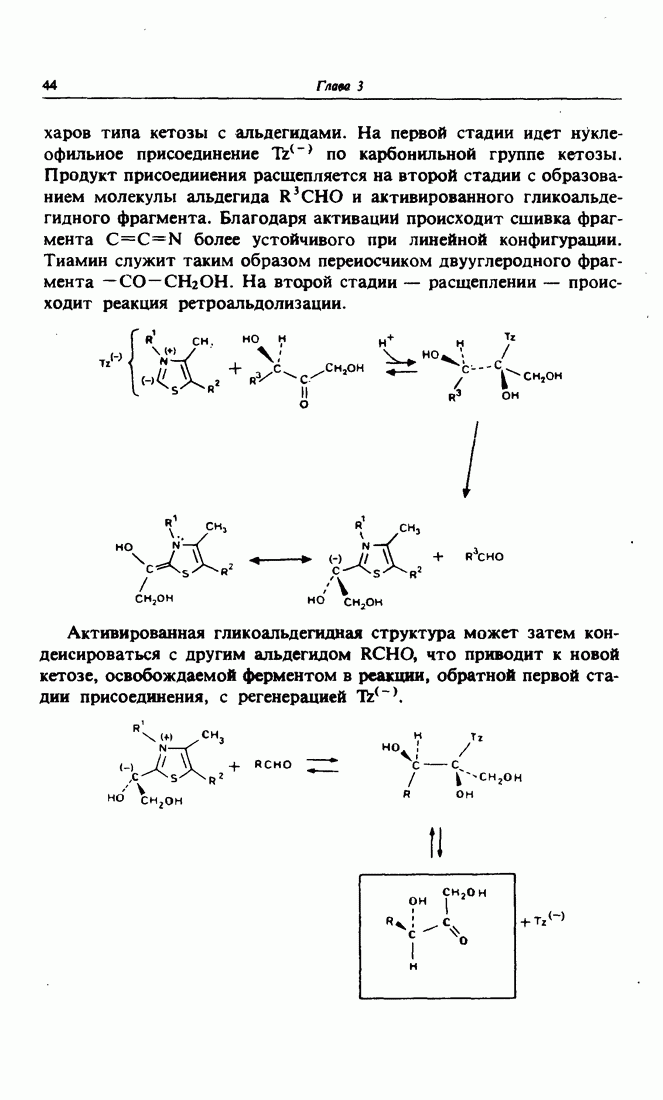
- 9. Недостаток тиамина и синдром Корсакова
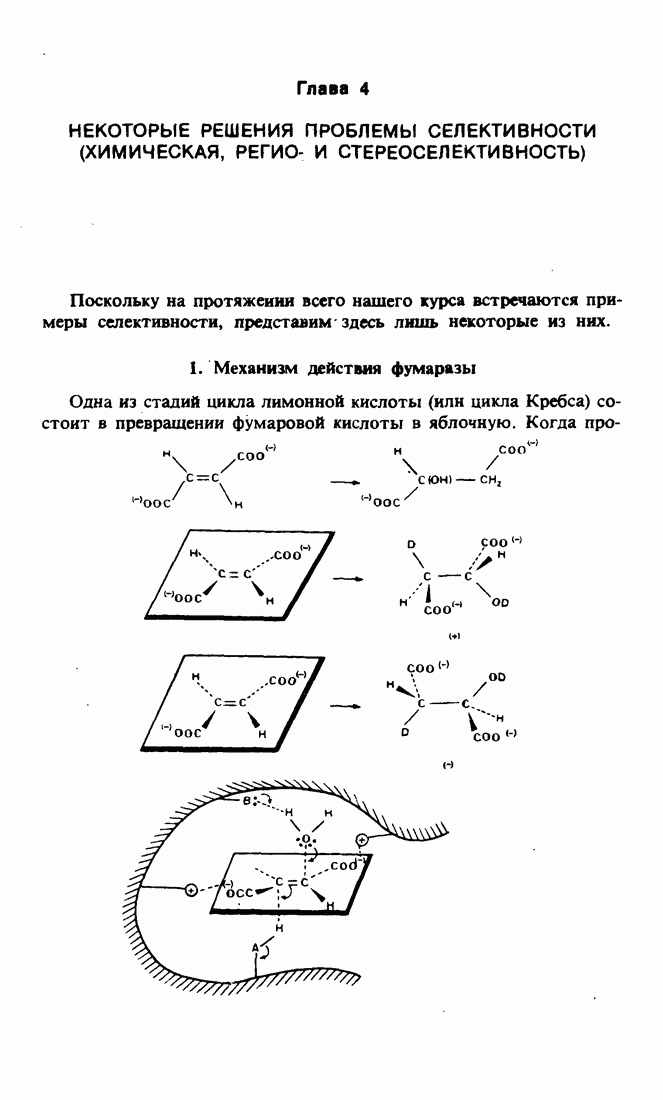
- Глава 4. НЕКОТОРЫЕ РЕШЕНИЯ ПРОБЛЕМЫ СЕЛЕКТИВНОСТИ (ХИМИЧЕСКАЯ, РЕГИО- И СТЕРЕОСЕЛЕКТИВНОСТЬ)
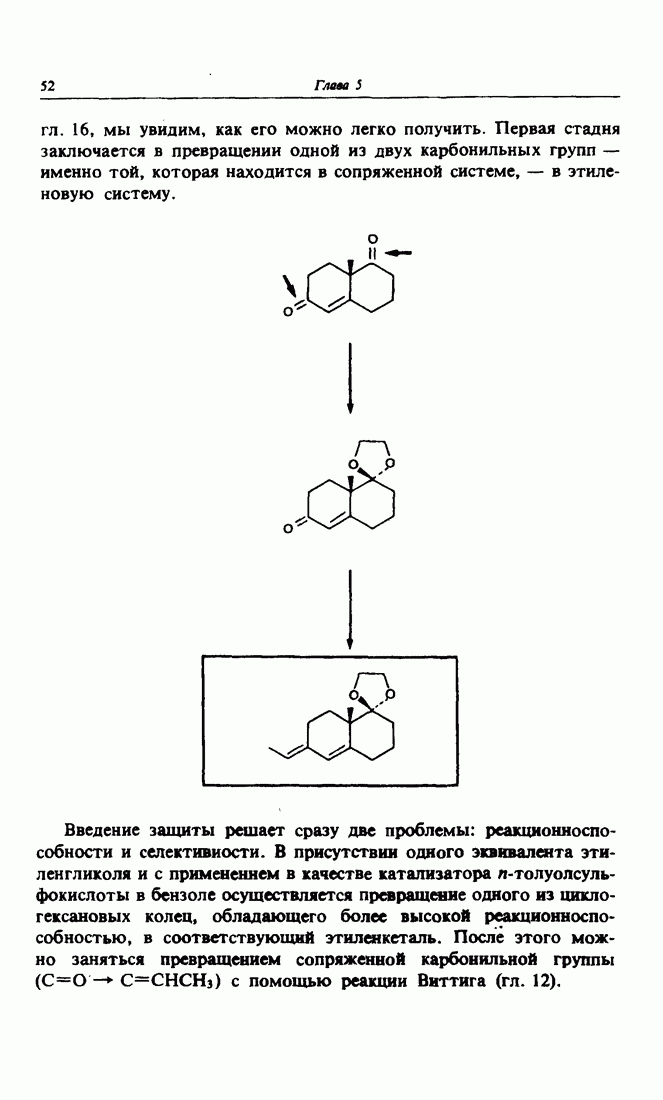
- Глава 5. ЗАЩИТА И РЕГЕНЕРАЦИЯ ФУНКЦИОНАЛЬНЫХ ГРУПП. СПИРТОВАЯ И КАРБОНИЛЬНАЯ ГРУППЫ, ОБРАЩЕНИЕ ПОЛЯРНОСТИ
- 1. Нуклеофильное замещение в молекуле с реакционноспособной карбонильной группой
- 2. Начало синтеза лонгифолена по Кори
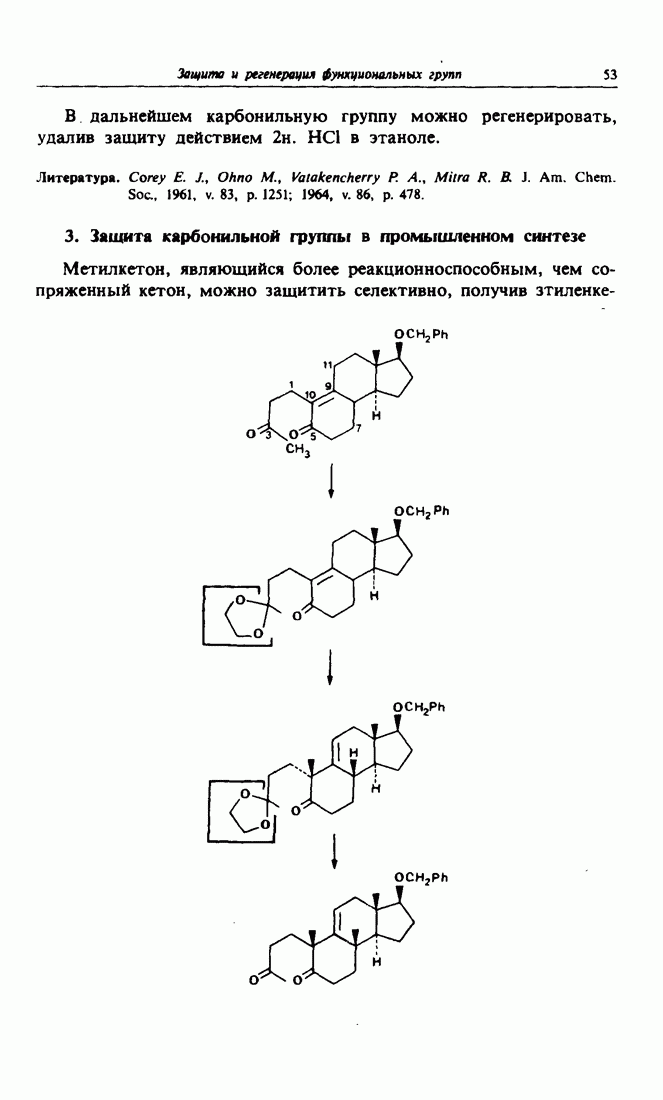
- 3. Защита карбонильной группы в промышленном синтезе
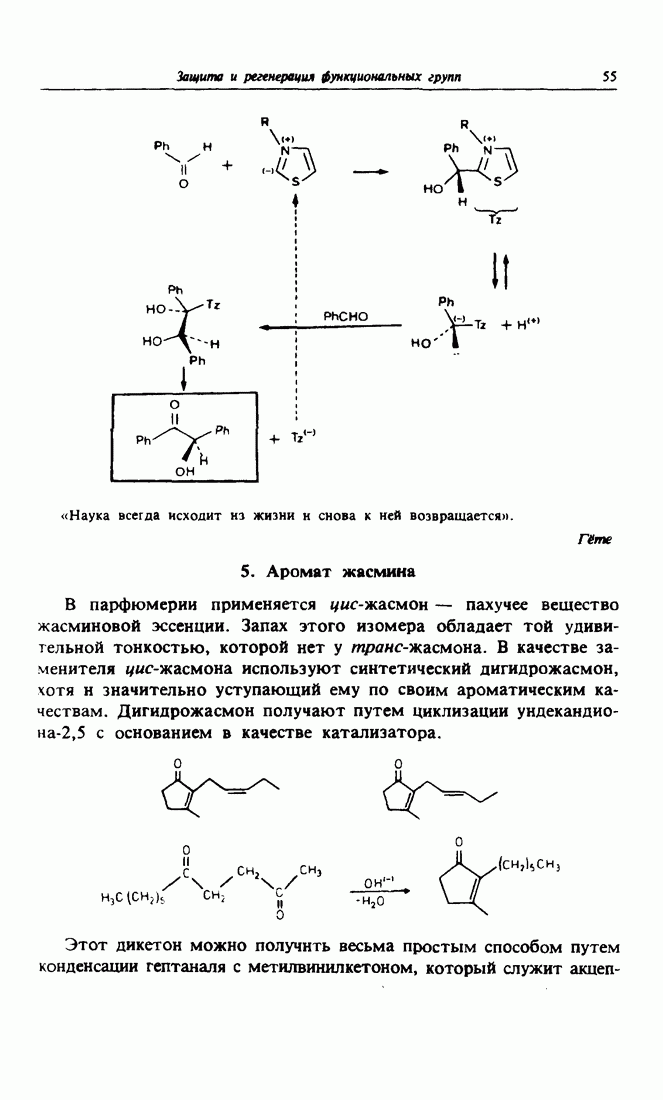
- 4. Механизм ферментативного образования ацетоина
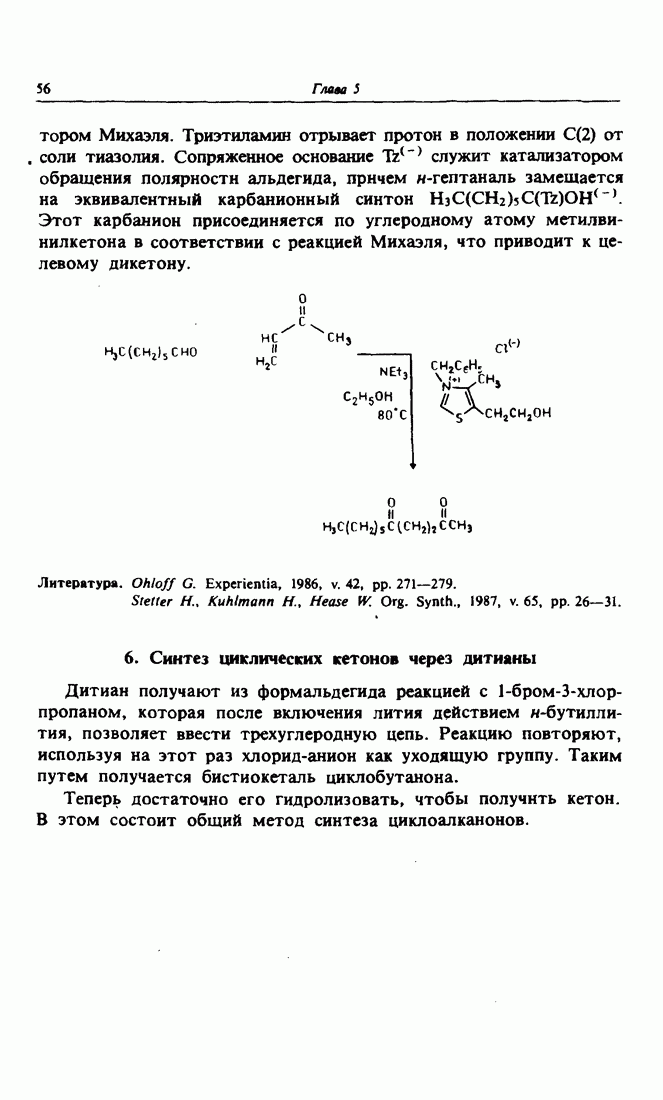
- 5. Аромат жасмина
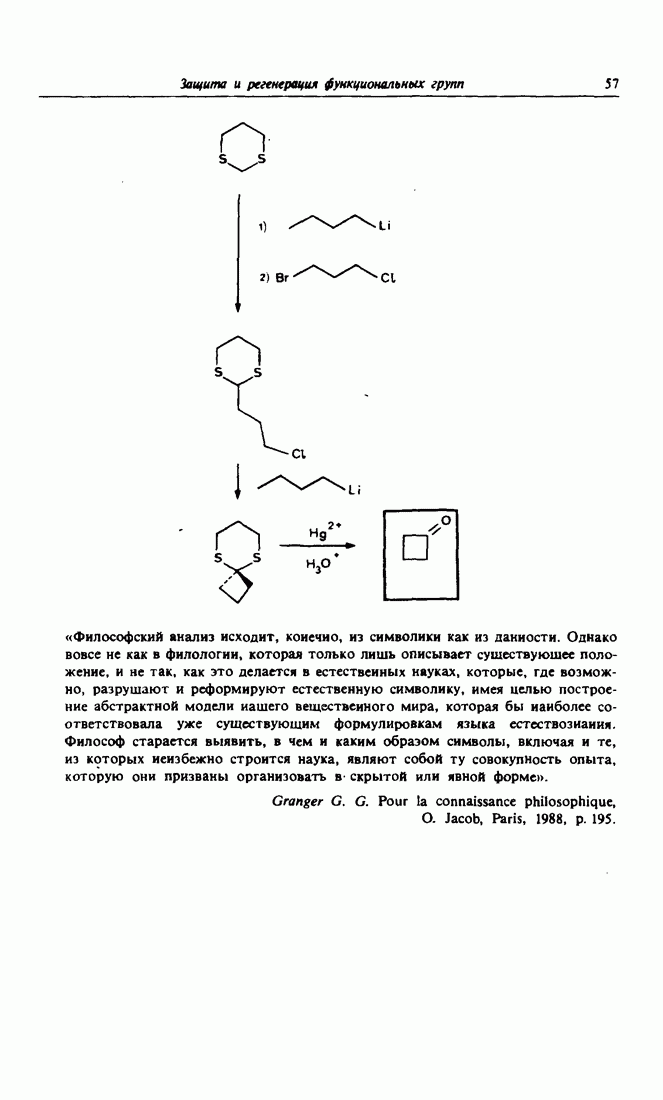
- 6. Синтез циклических кетонов через дитианы
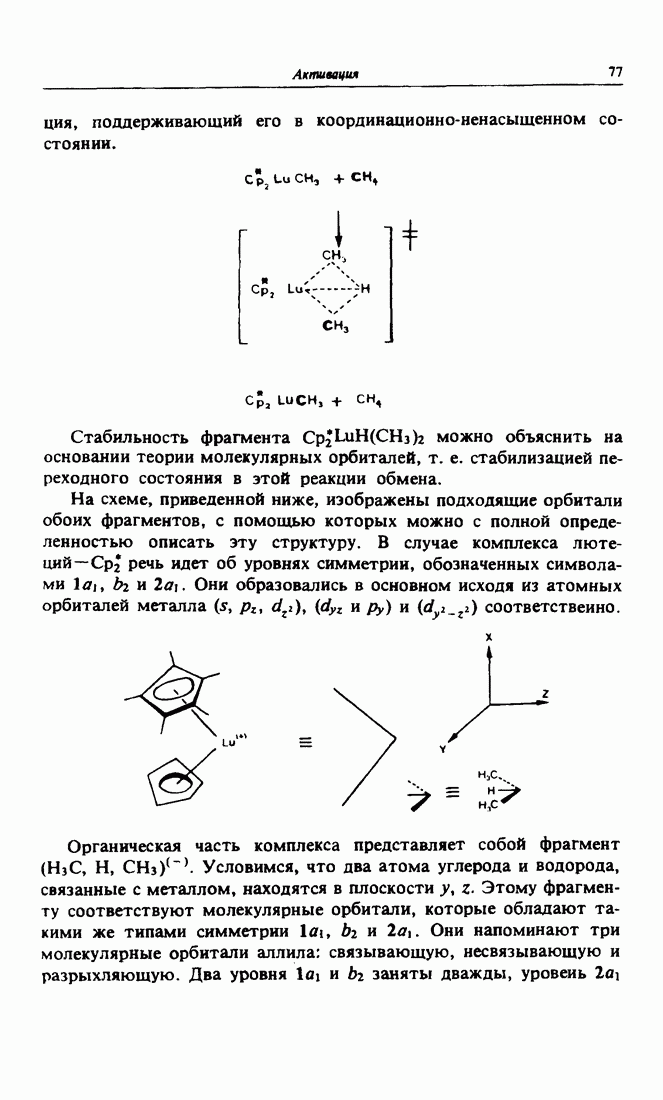
- Глава 6. АКТИВАЦИЯ
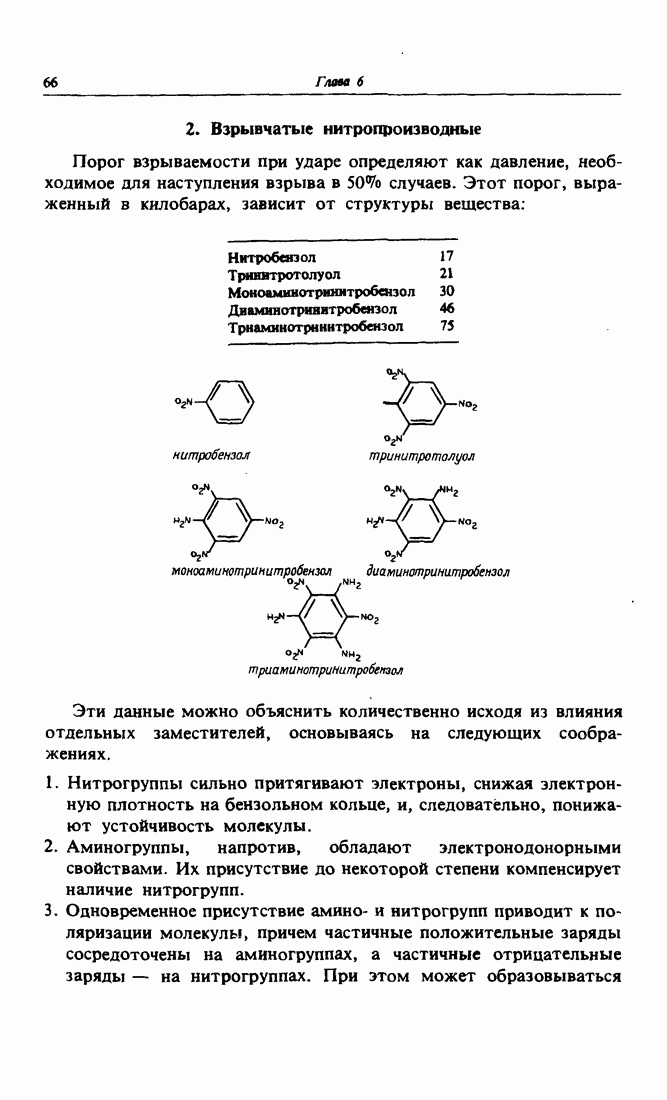
- 2. Взрывчатые нитропроизводные
- 3. Дестабилизация исходного состояния. Катализ путем фазового переноса
- 4. Биолюминесценция или средства общения в мире безмолвия
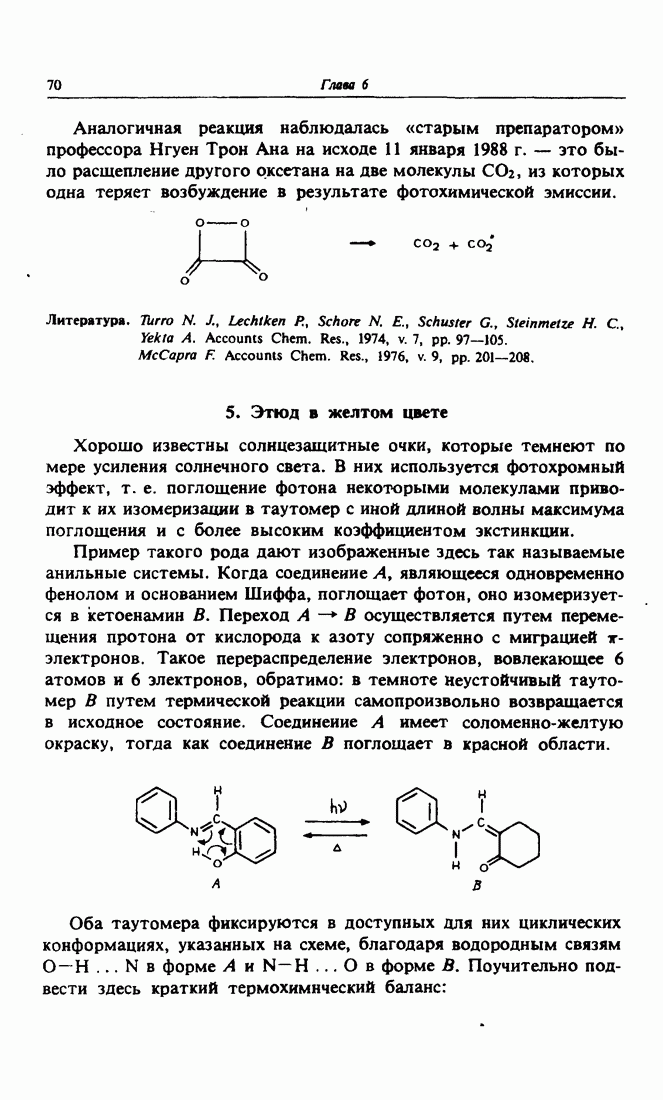
- 5. Этюд в желтом цвете
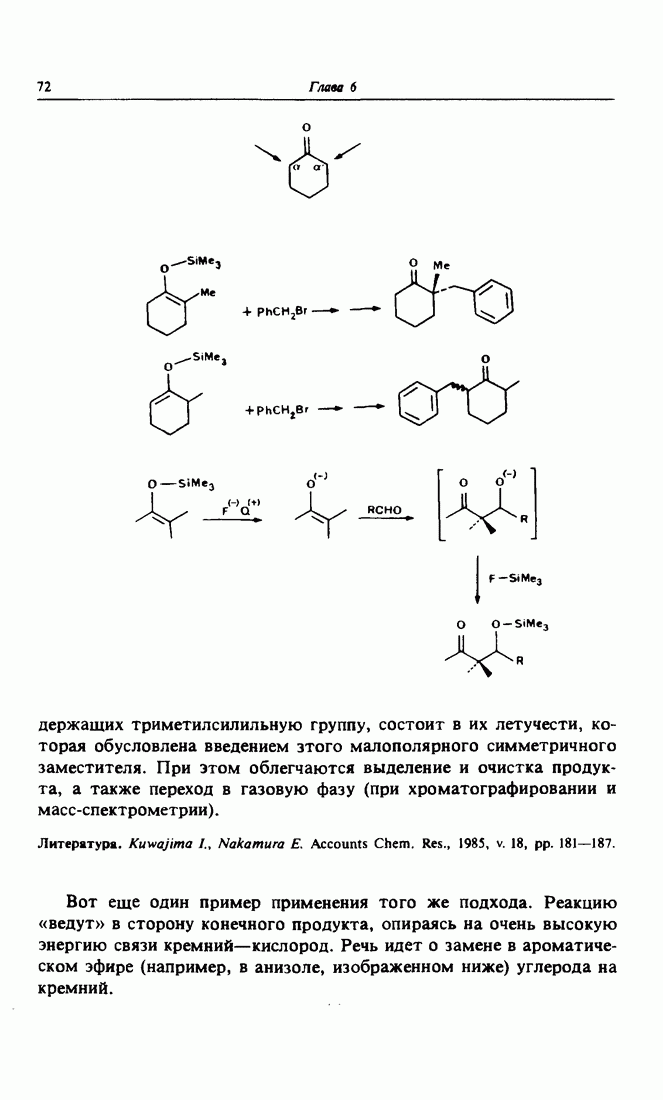
- 6. Стабилизация конечного состояния. Силилированные эфиры фенолов
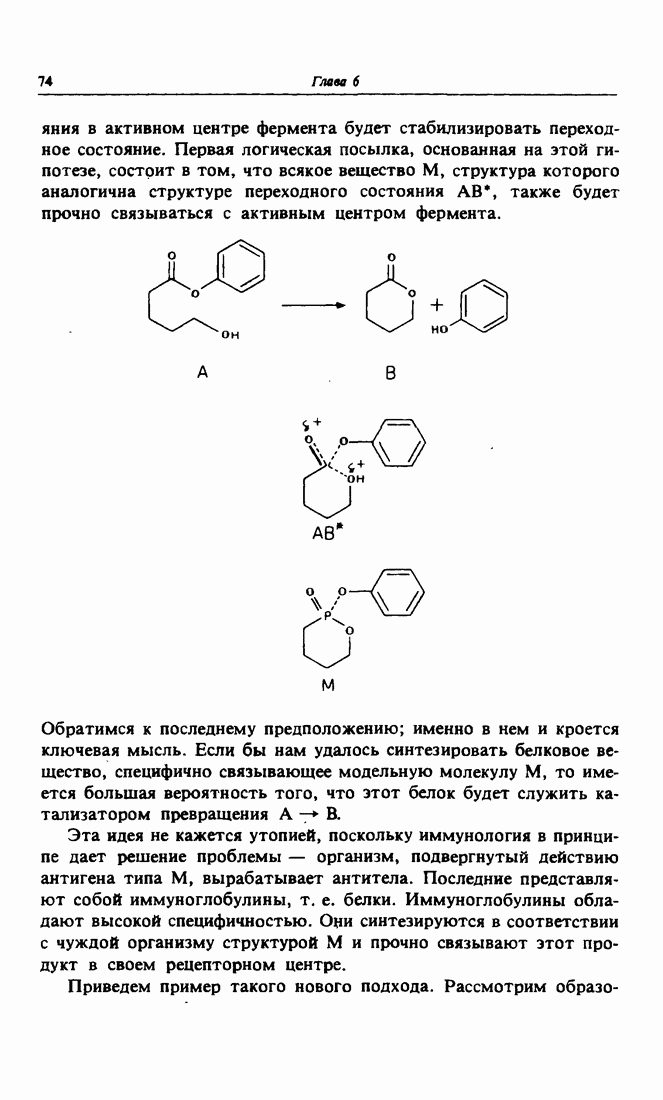
- 7. Биокаталиэ органических реакций
- 8. Активация насыщенных углеводородов
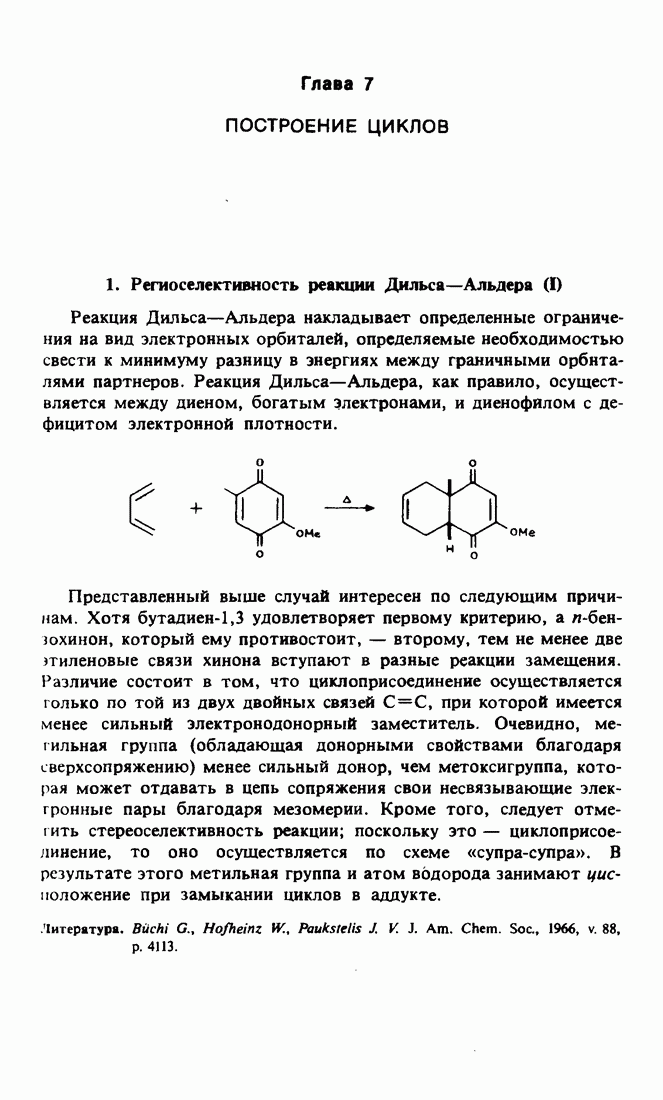
- Глава 7. ПОСТРОЕНИЕ ЦИКЛОВ
- 1. Региоселективность реакции Дильса-Альдера (I)
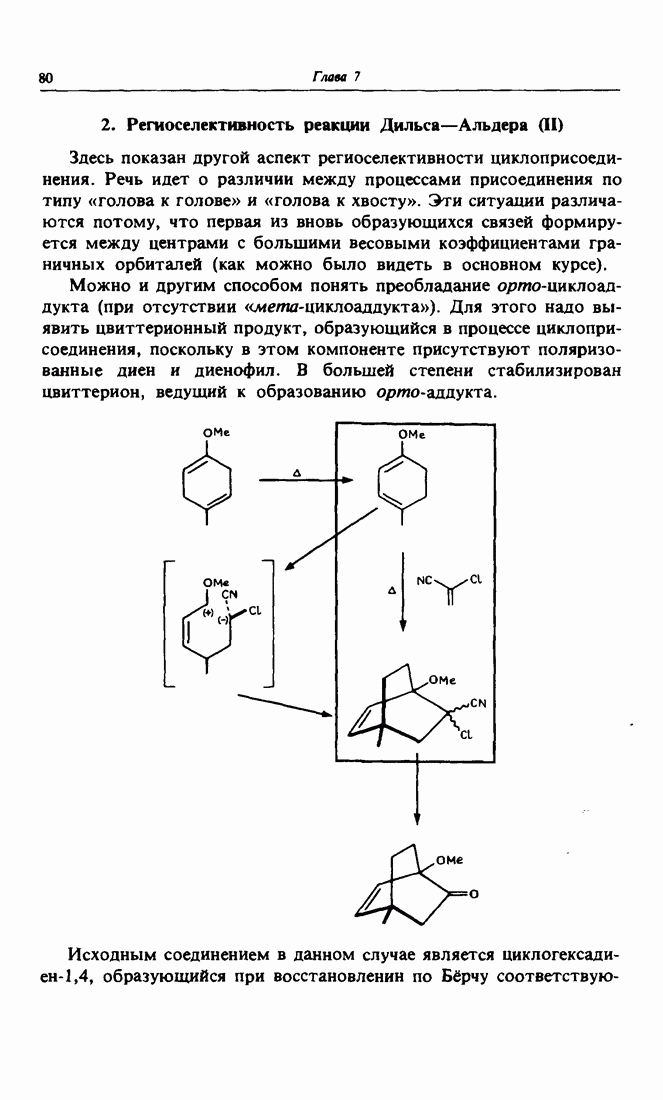
- 2. Региоселективность реакции Дильса-Альдера (II)
- 3. Диенофилы, активированные благодаря напряжению в цикле
- 4. Синтез Дильса-Альдера с раскрытием цикла в аддукте
- 5. Синтетическое значение двух последовательных реакций Дильса-Альдера
- 6. Стадия синтеза морфина
- 7. Другие применения реакции Дильса-Альдера в больших синтезах
- 8. Стереохимический контроль реакции Дильса-Альдера
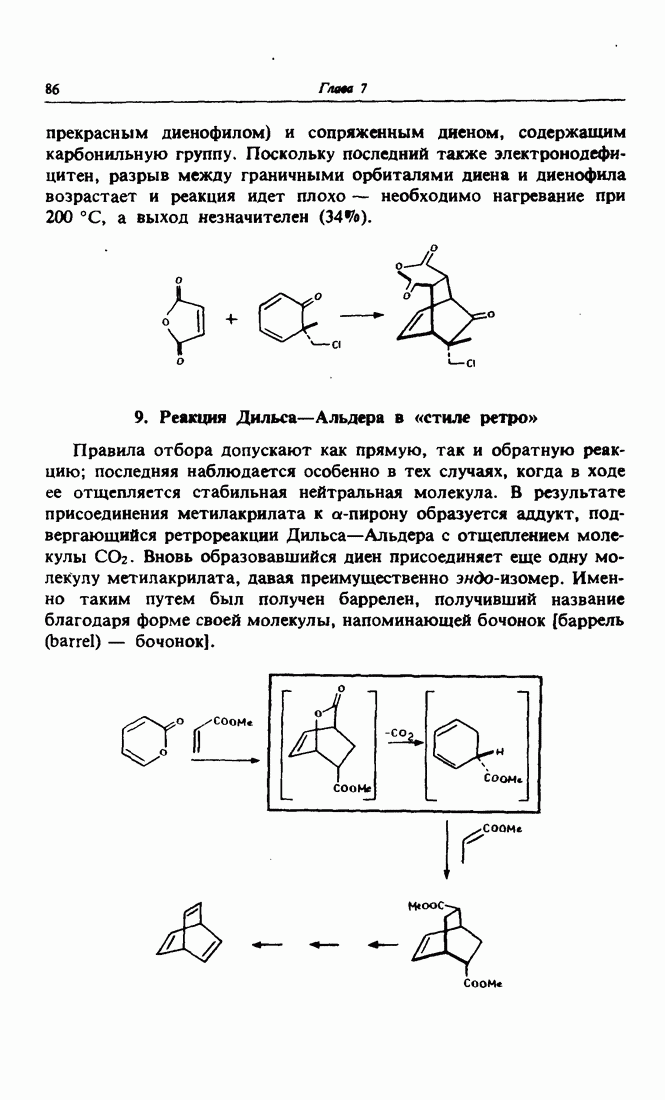
- 9. Реакция Дильса-Альдера в «стиле ретро»
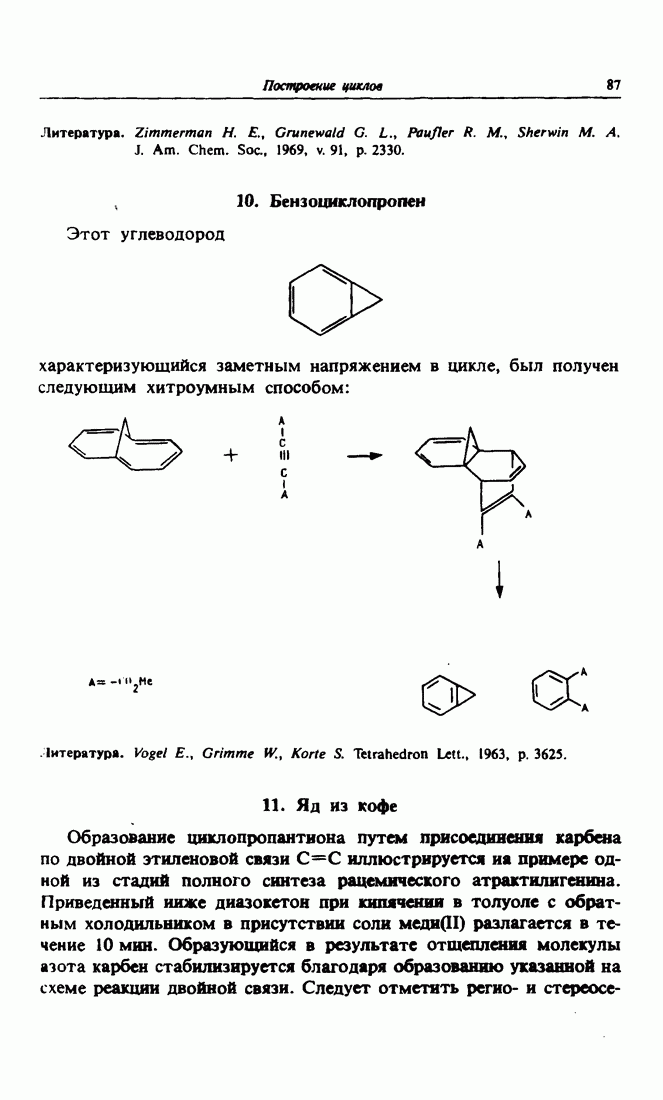
- 10. Бензоциклопропен
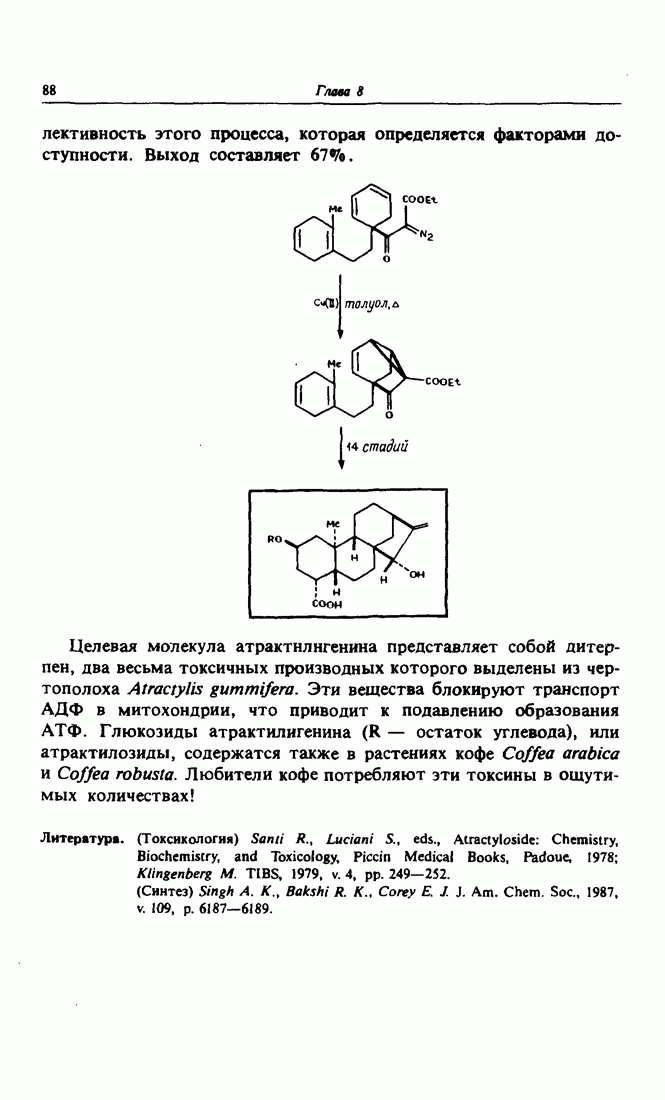
- 11. Яд из кофе
- Глава 8. ВВЕДЕНИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП. РЕАКЦИИ ЗАМЕЩЕНИЯ
- 1. Удлинение углеродной цепи
- 2. Начало синтеза яда
- 3. Активация карбонильной группы путем замещения
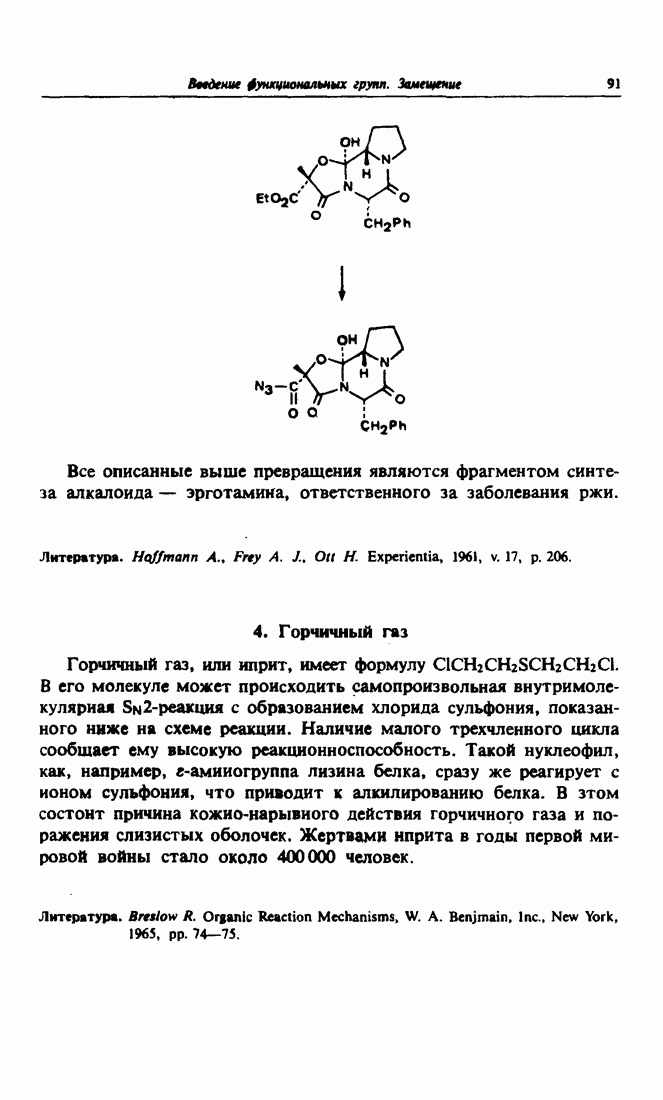
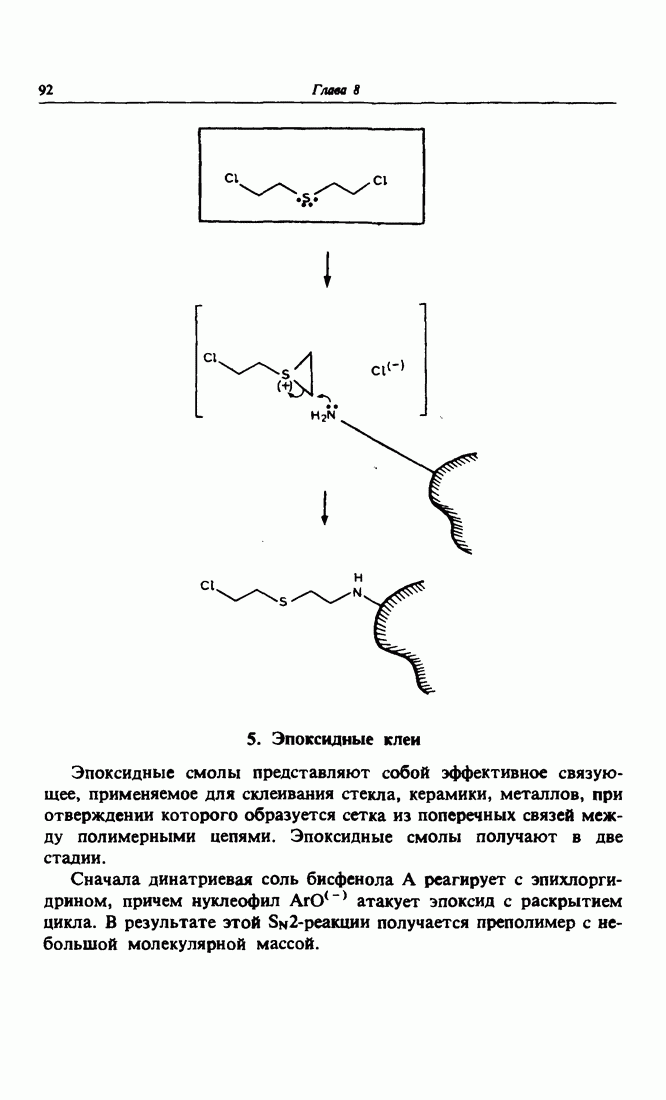
- 4. Горчичный газ
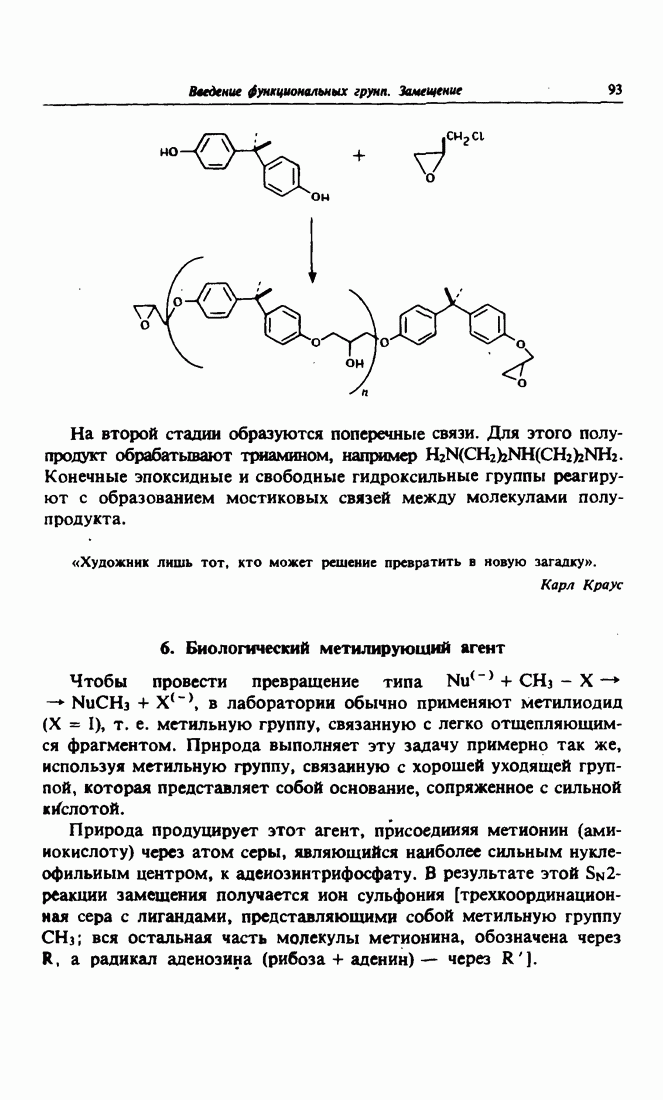
- 5. Эпоксидные клеи
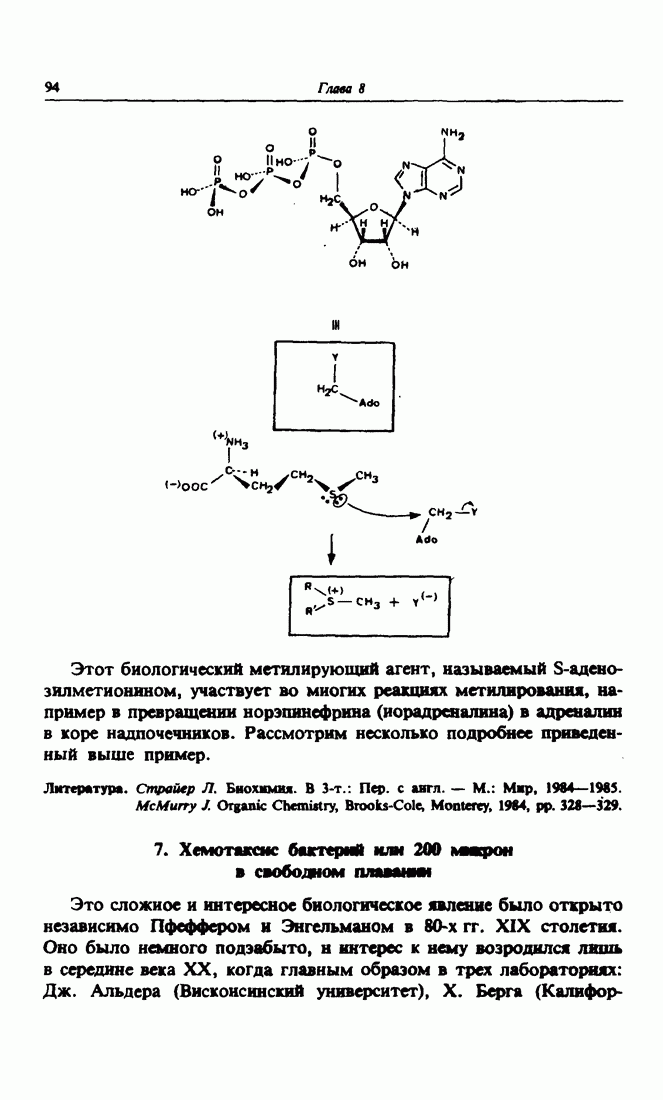
- 6. Биологический метилирующий агент
- 7. Хемотаксис бактерий или 200 мирон в свободном плавании
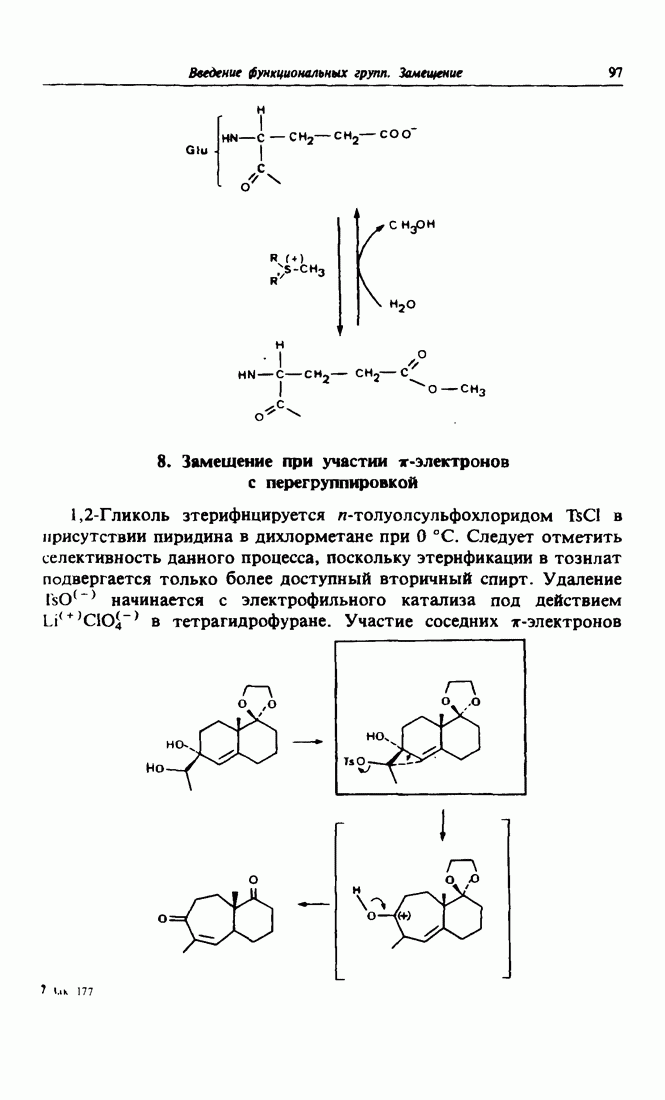
- 8. Замещение при участии «пи»-электронов с перегруппировкой
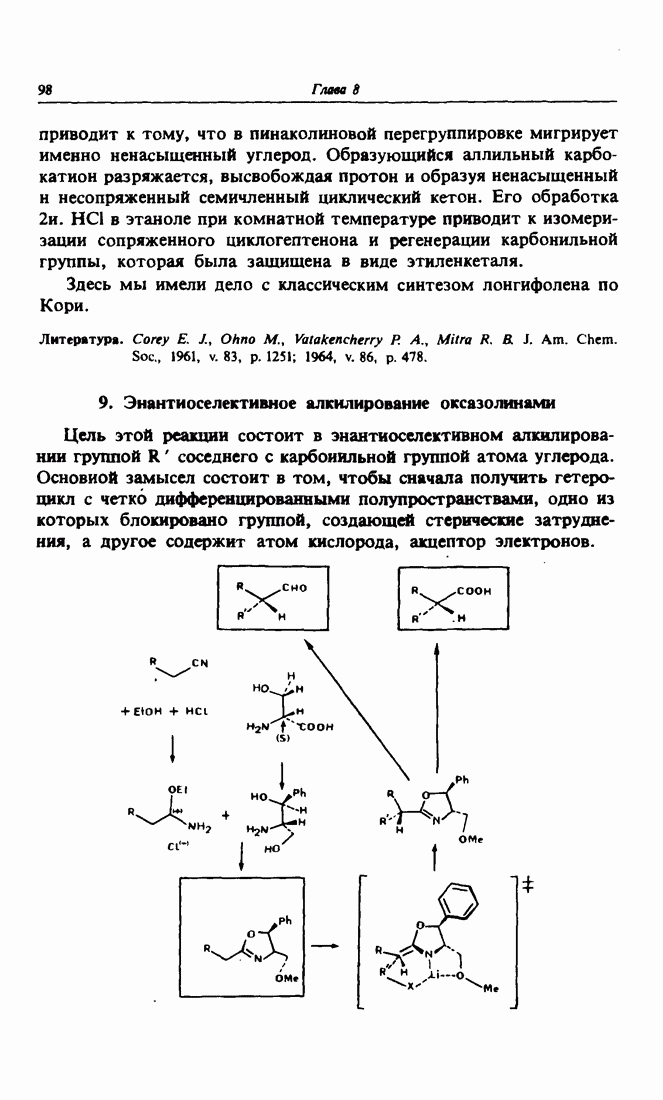
- 9. Энантиоселективное алкилирование оксазолинами
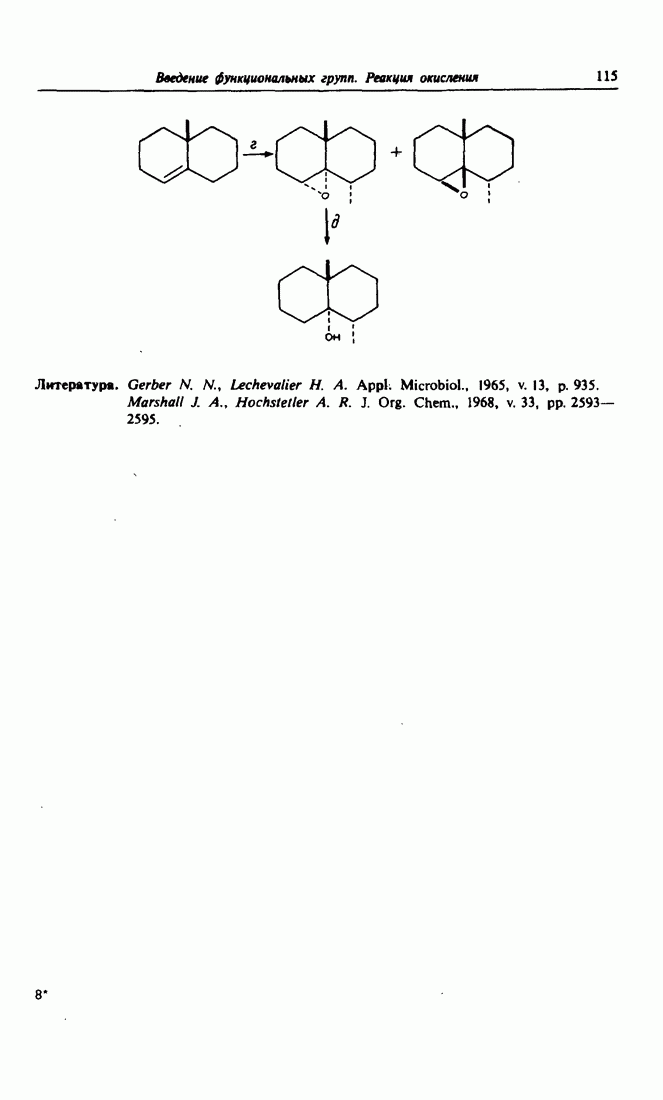
- Глава 9. ВВЕДЕНИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП. РЕАКЦИИ ОКИСЛЕНИЯ
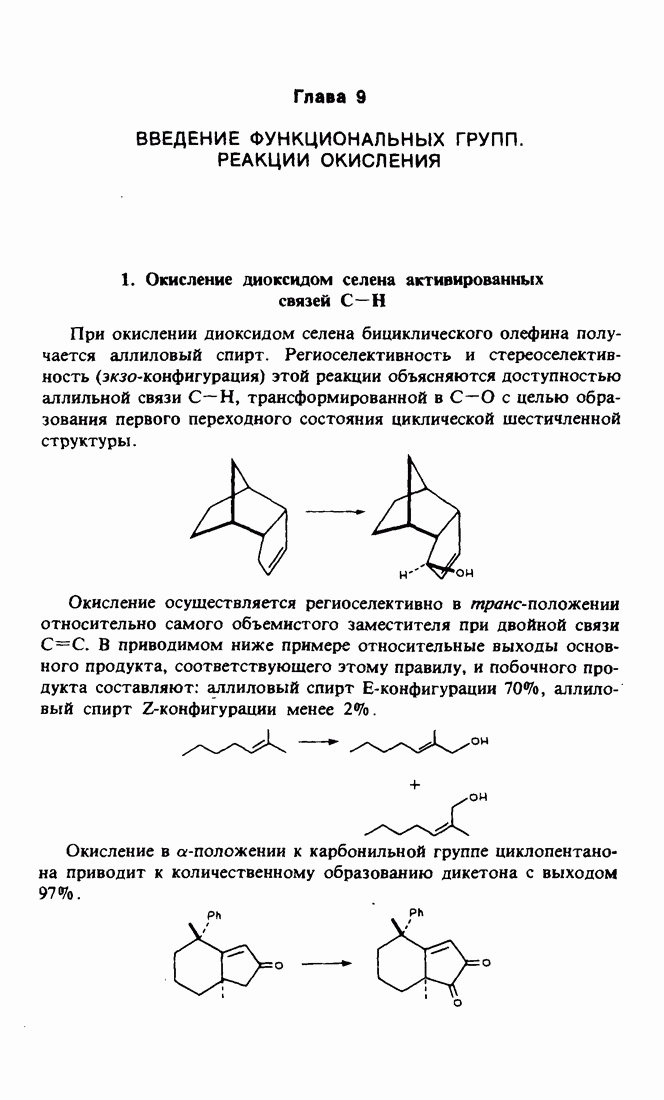
- 1. Окисление диоксидом селена активированных связей C-H
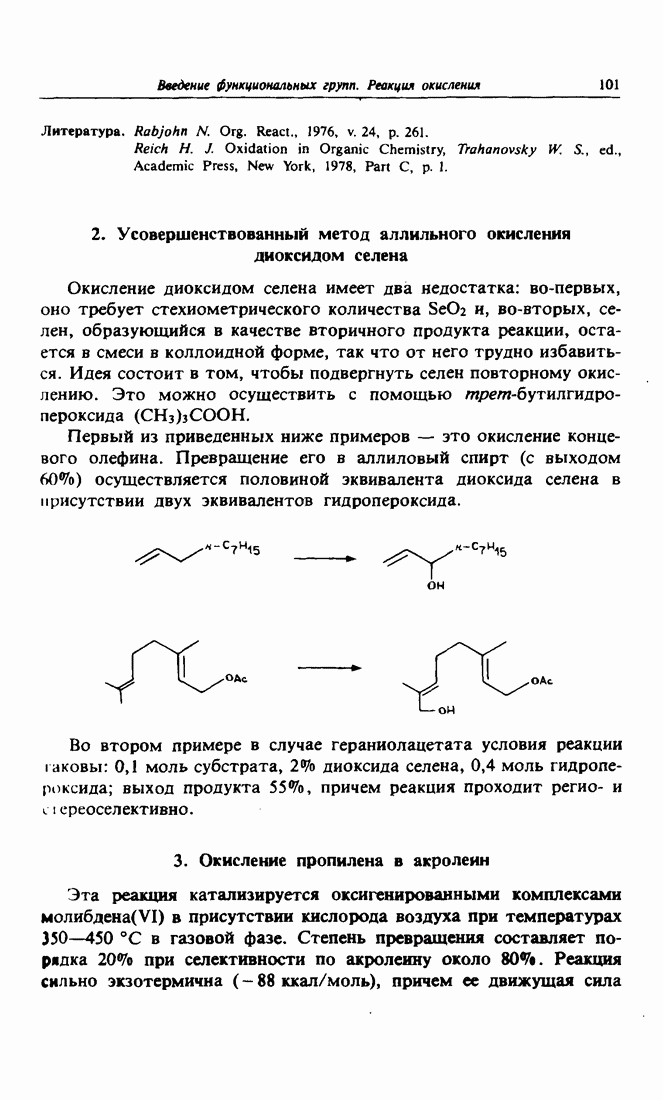
- 2. Усовершенствованный метод аллильного окисления диоксидом селена
- 3. Окисление пропилена в акролеин
- 4. Окисление этилена в этиленоксид
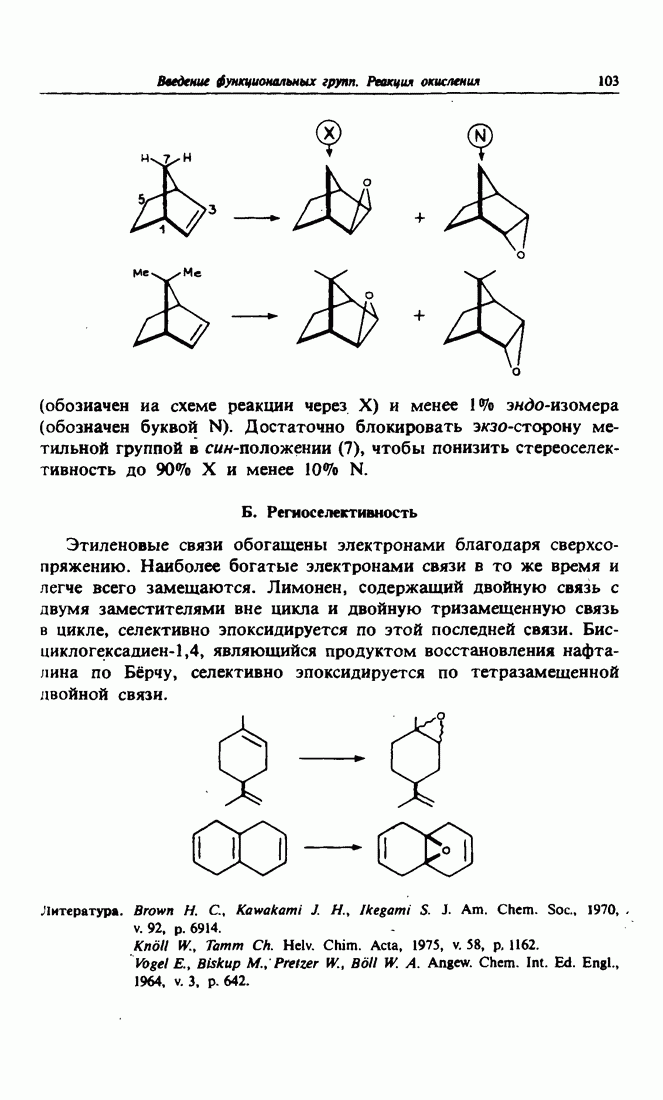
- 5. Селективность при эпоксидировании
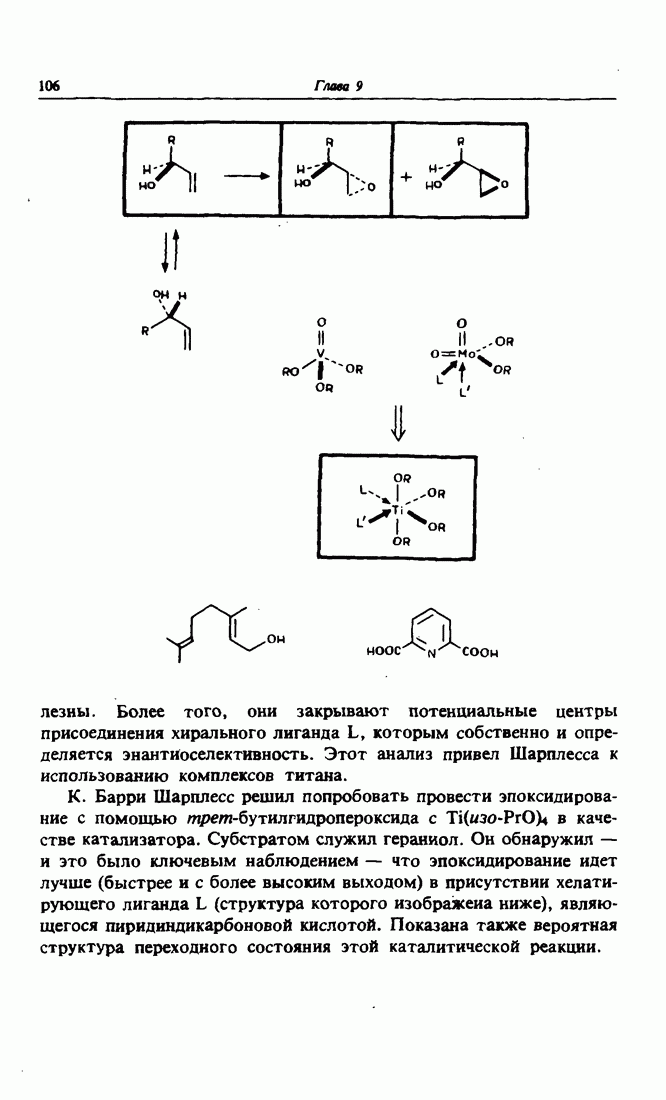
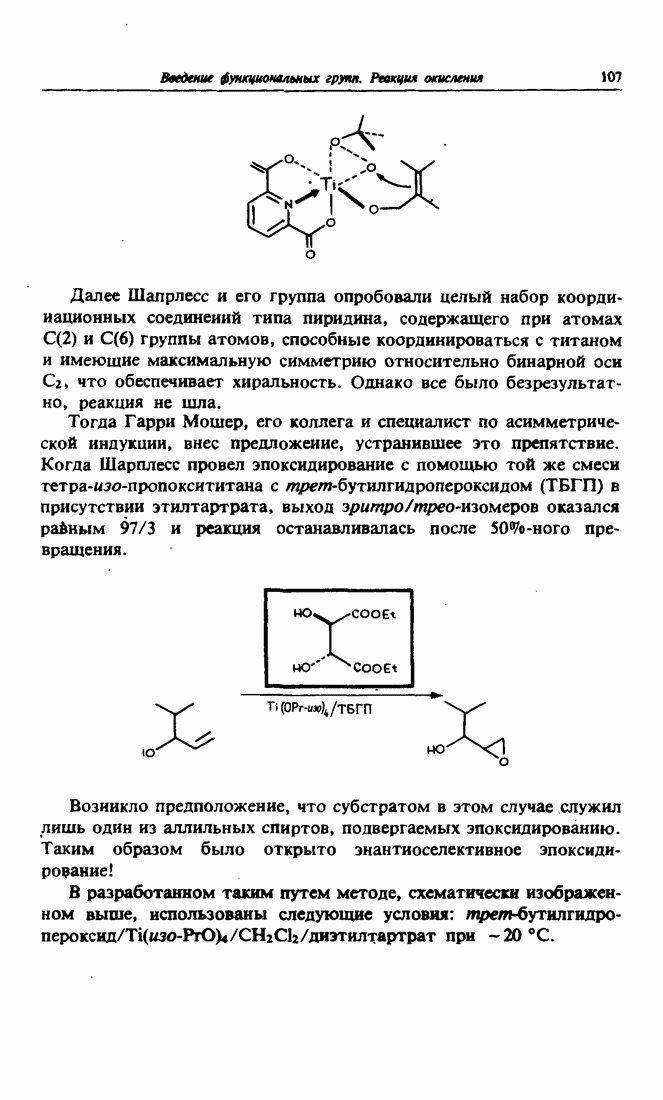
- 6. Энантиоселективное эпоксндирование по Шарплессу
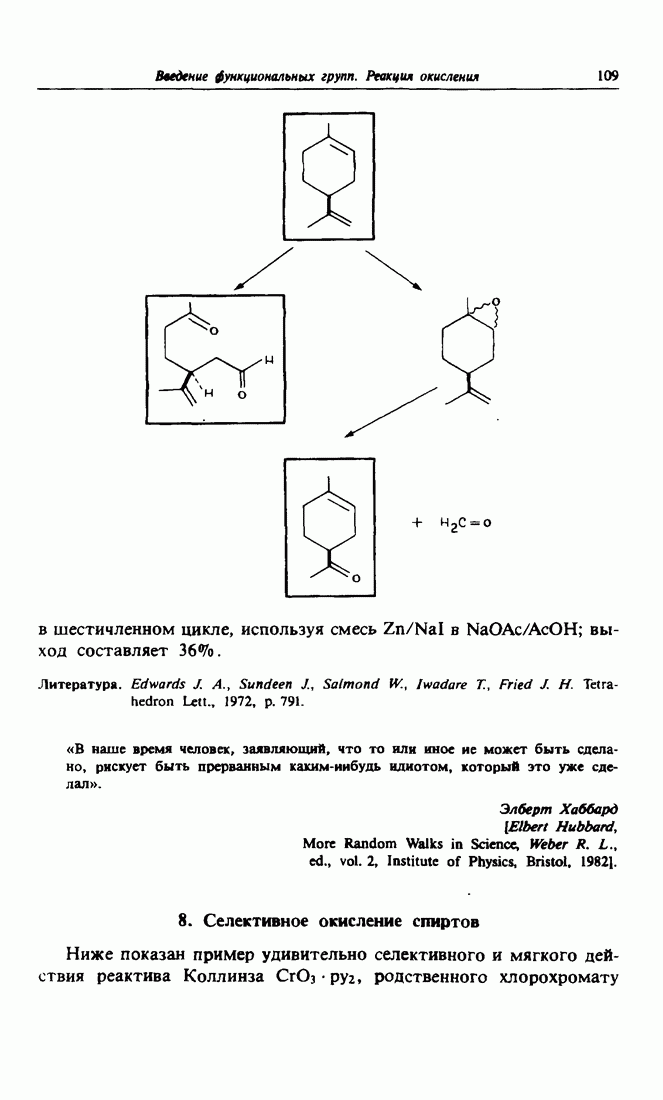
- 7. Селективность оэонолиэа
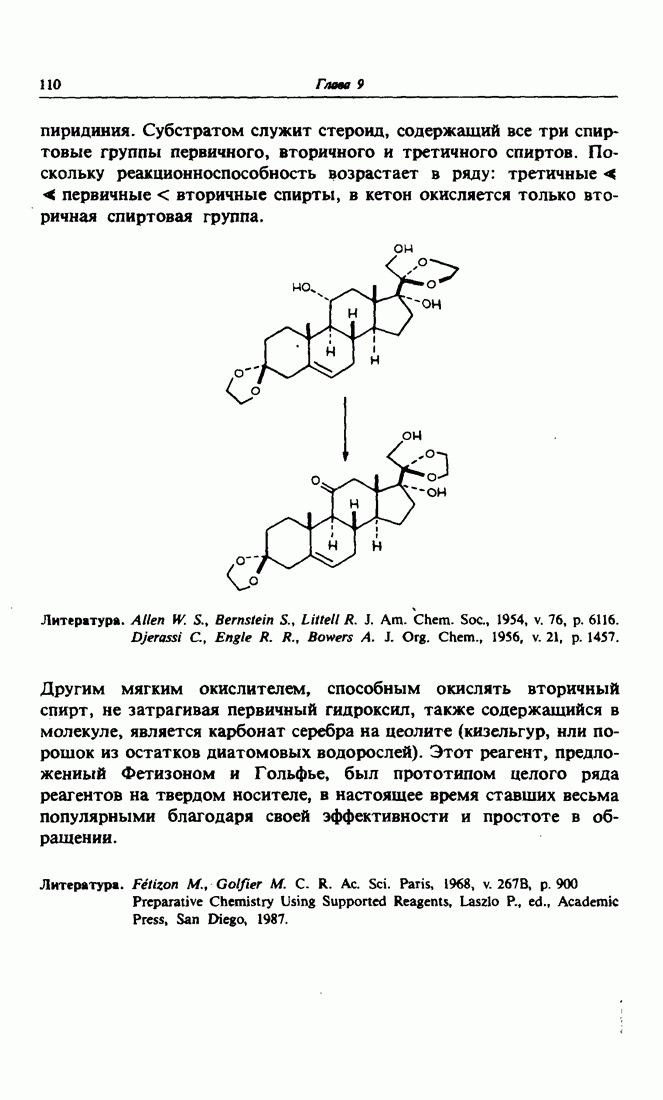
- 8. Селективное окисление спиртов
- 9. Биологическое окисление спиртов
- 10. И фермент может встретиться с затруднениями
- 11. Образование уксусного альдегида путем окисления этилена
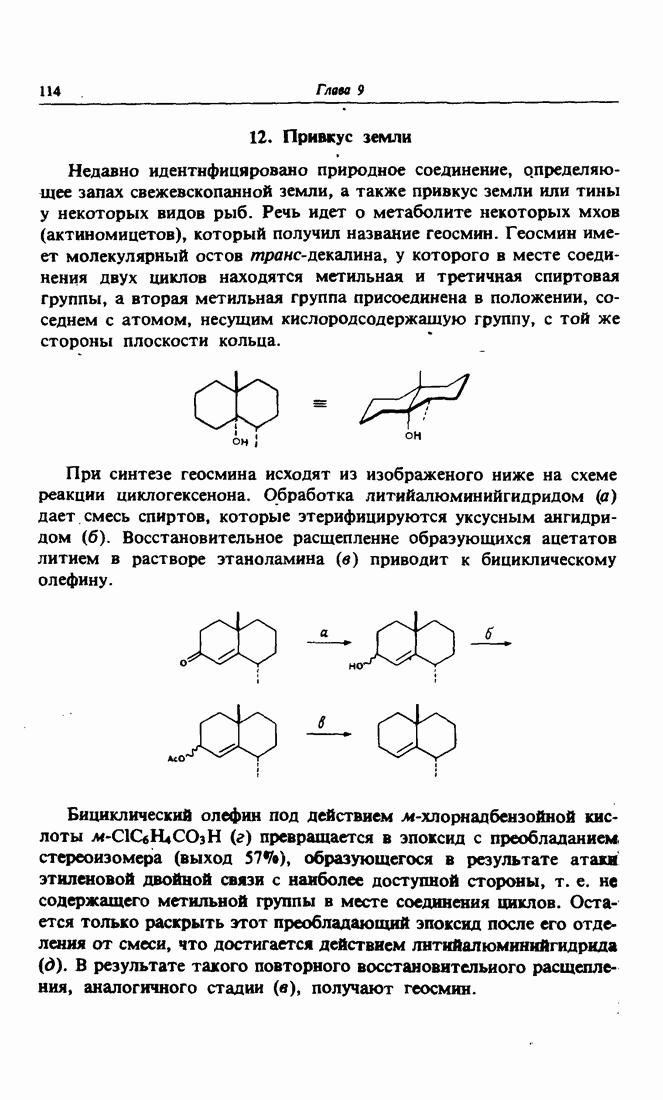
- 12. Привкус земли
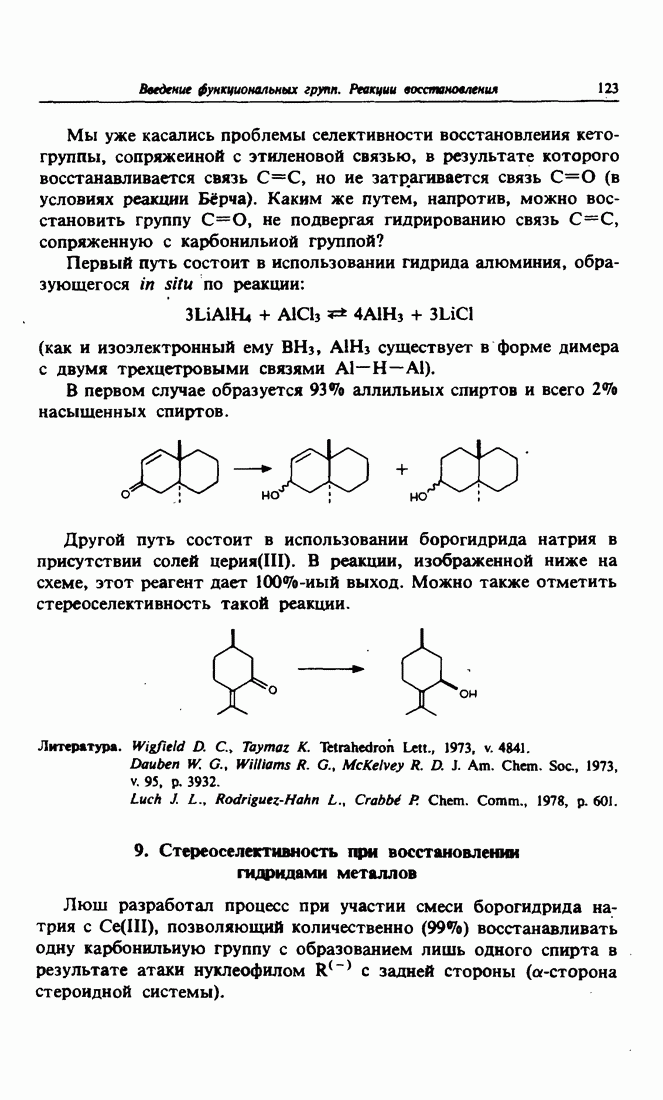
- Глава 10. ВВЕДЕНИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП. РЕАКЦИИ ВОССТАНОВЛЕНИЯ
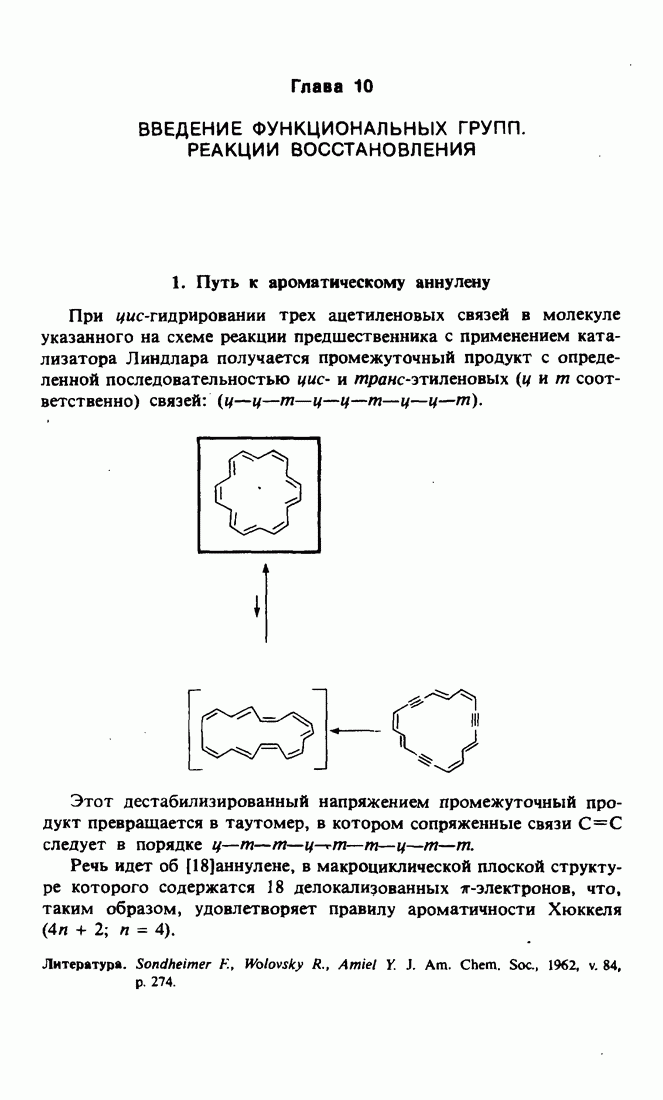
- 1. Путь к ароматическому аннулену
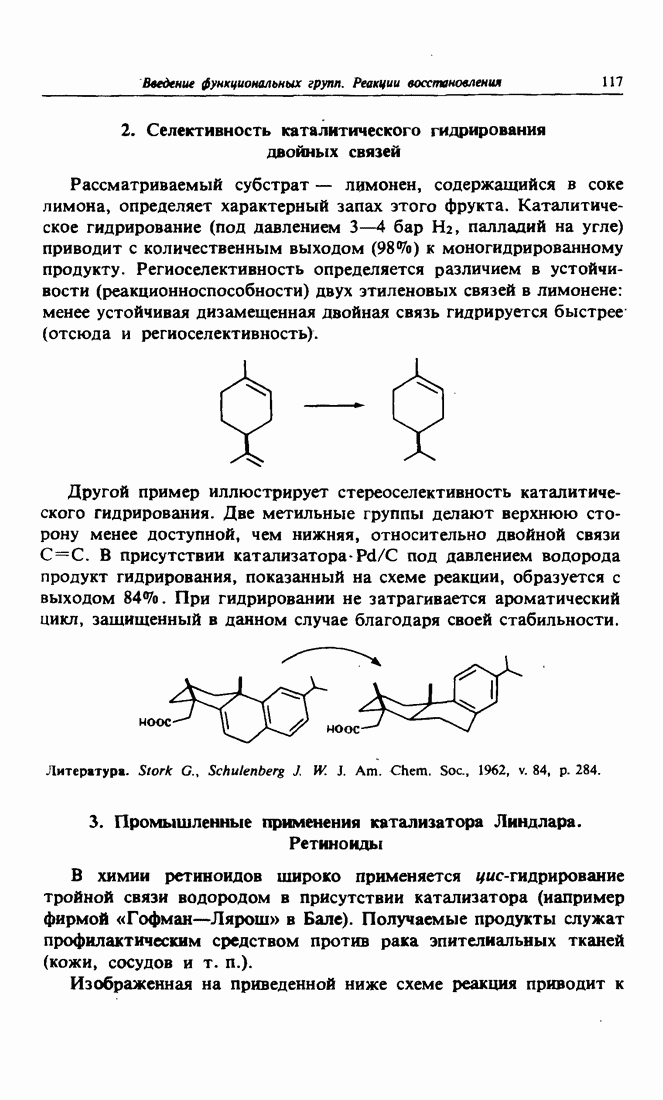
- 2. Селективность каталитического гидрирования двойных связей
- 3. Промышленные применения катализатора Линдлара. Ретиноиды
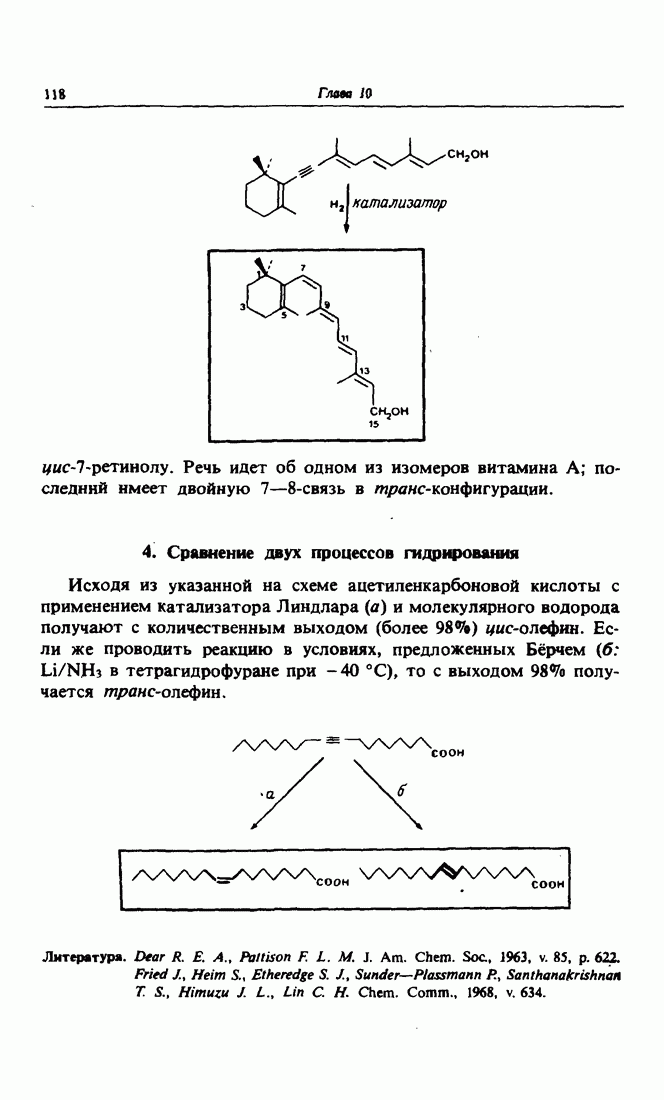
- 4. Сравнение двух процессов гидрирования
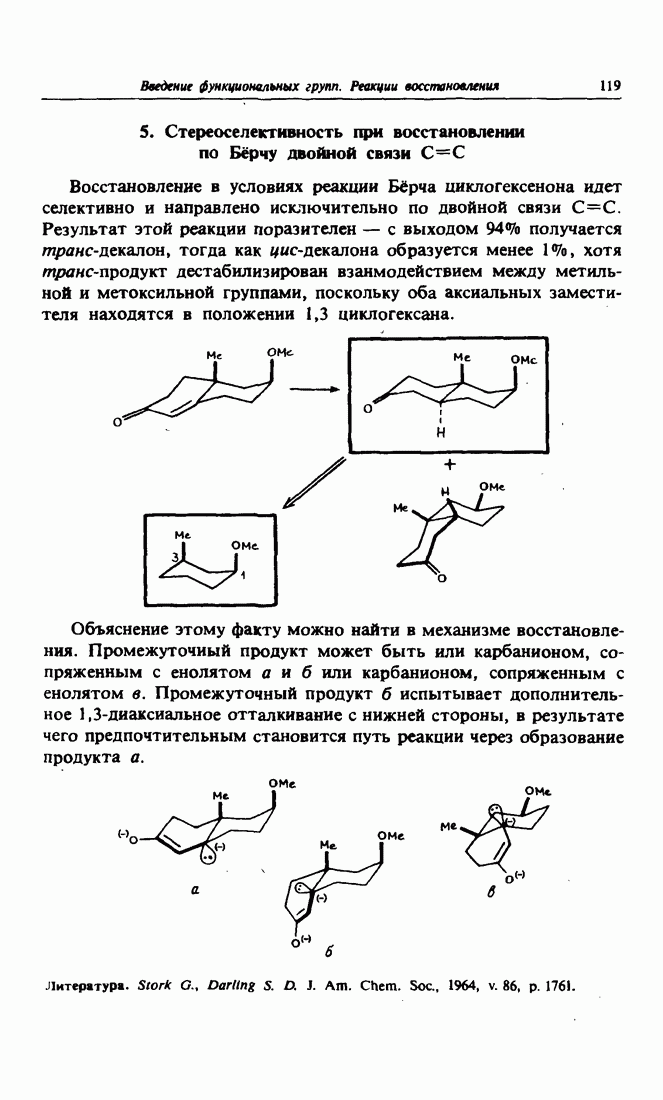
- 5. Стереоселективность при восстановлении по Бёрчу двойной связи С=С
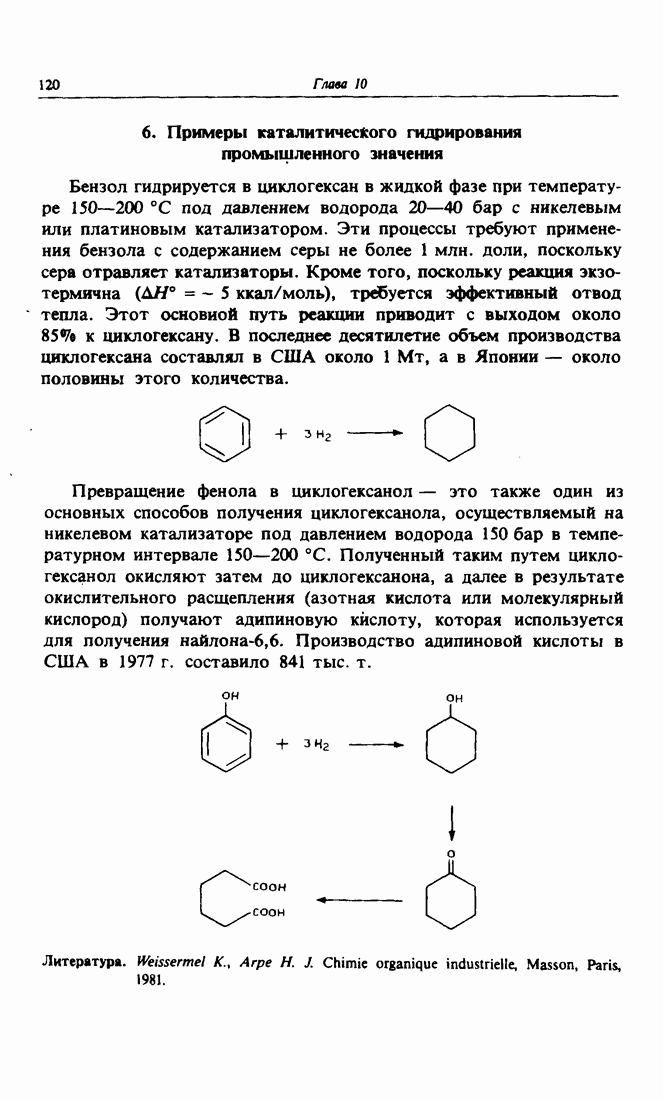
- 6. Примеры каталитического гидрирования промышленного значения
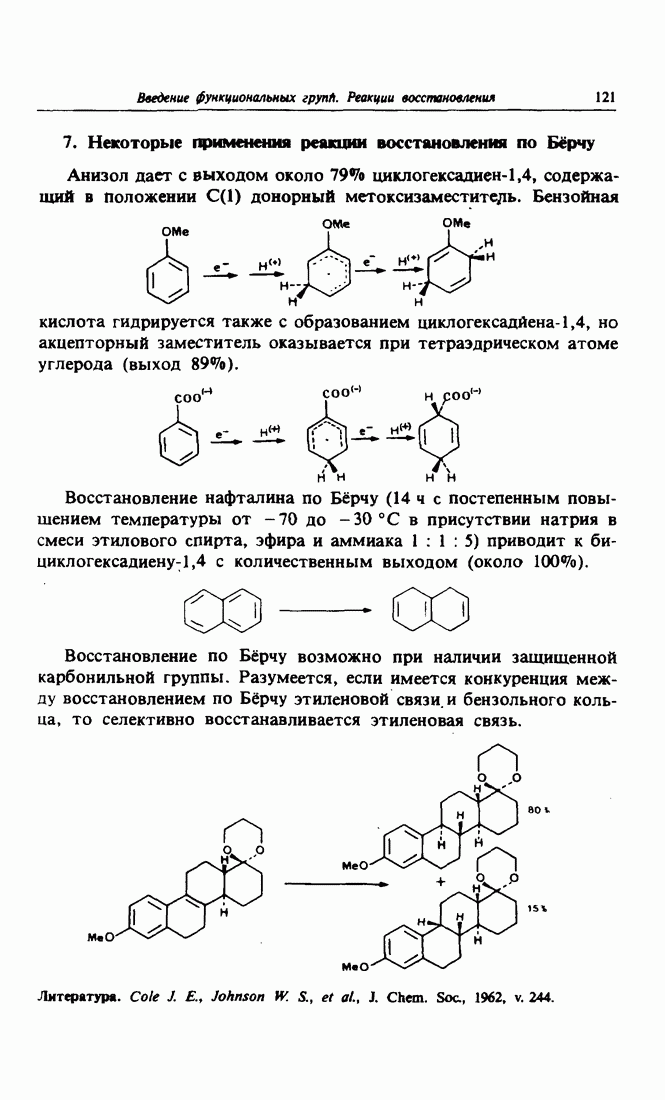
- 7. Некоторые применения реакции восстановления по Бёрчу
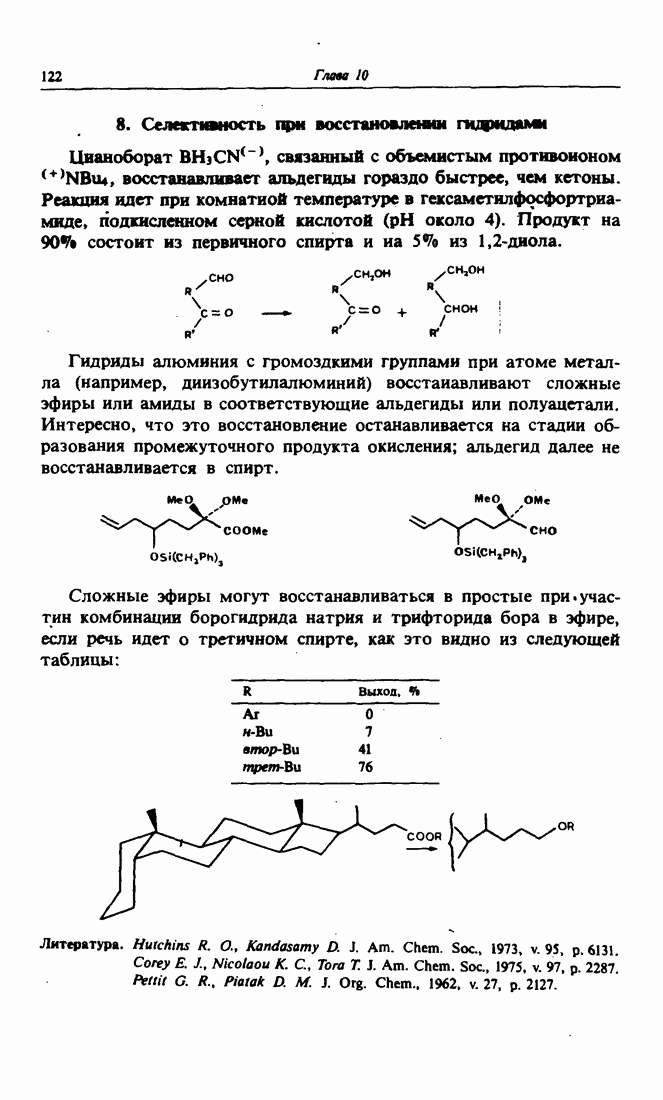
- 8. Селективность при восстановлении гидридами
- 9. Стереоселективность при восстановлении гидридами металлов
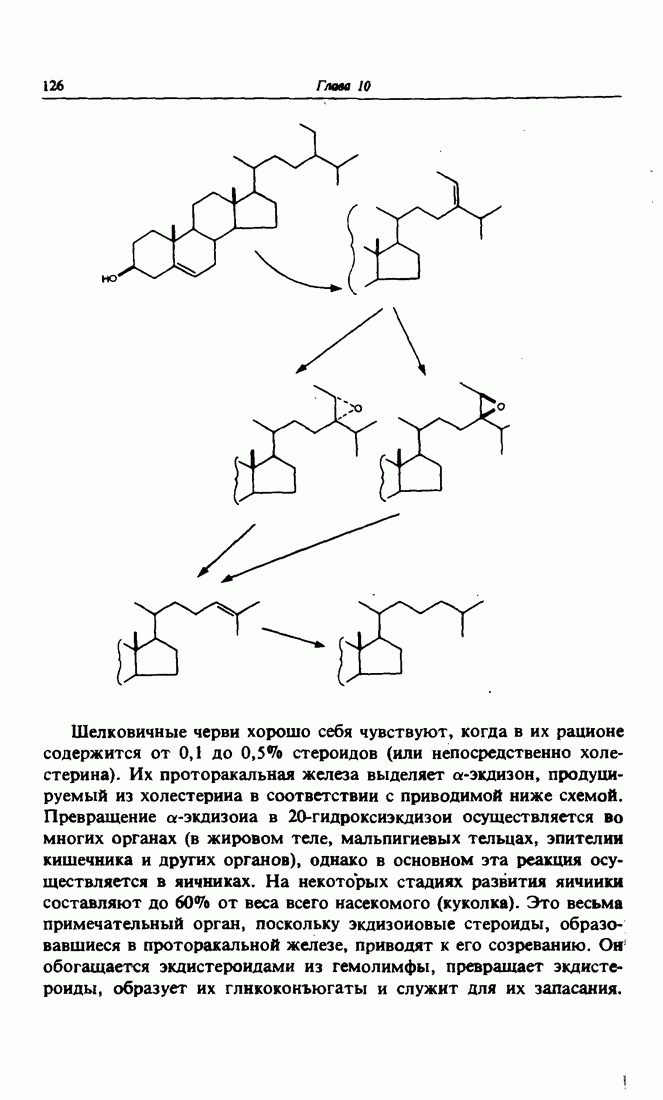
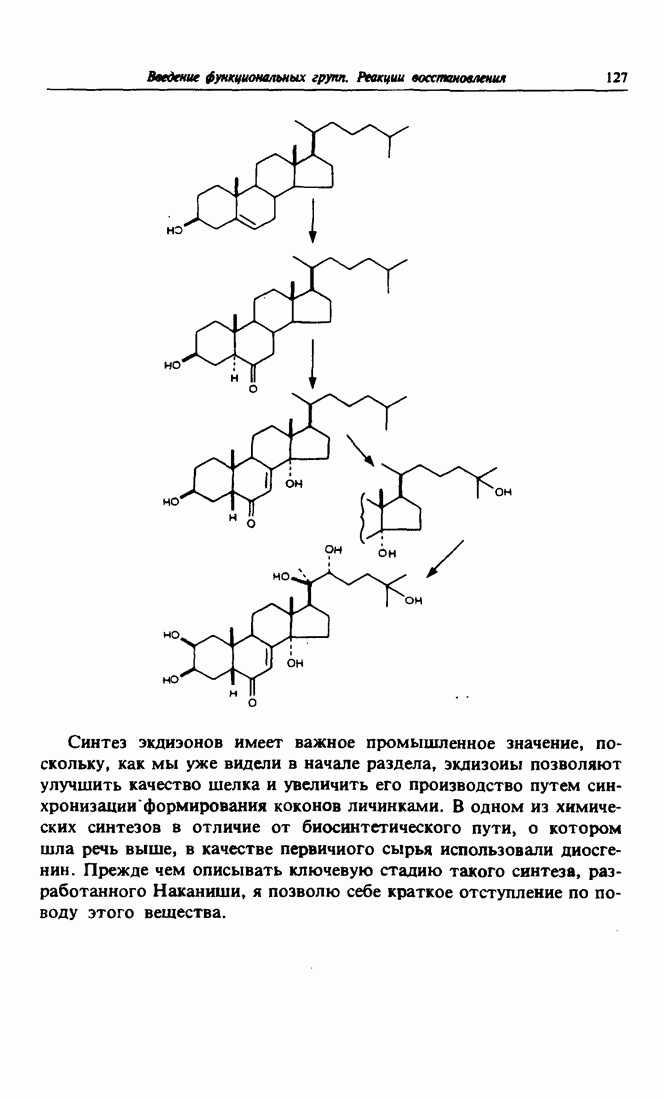
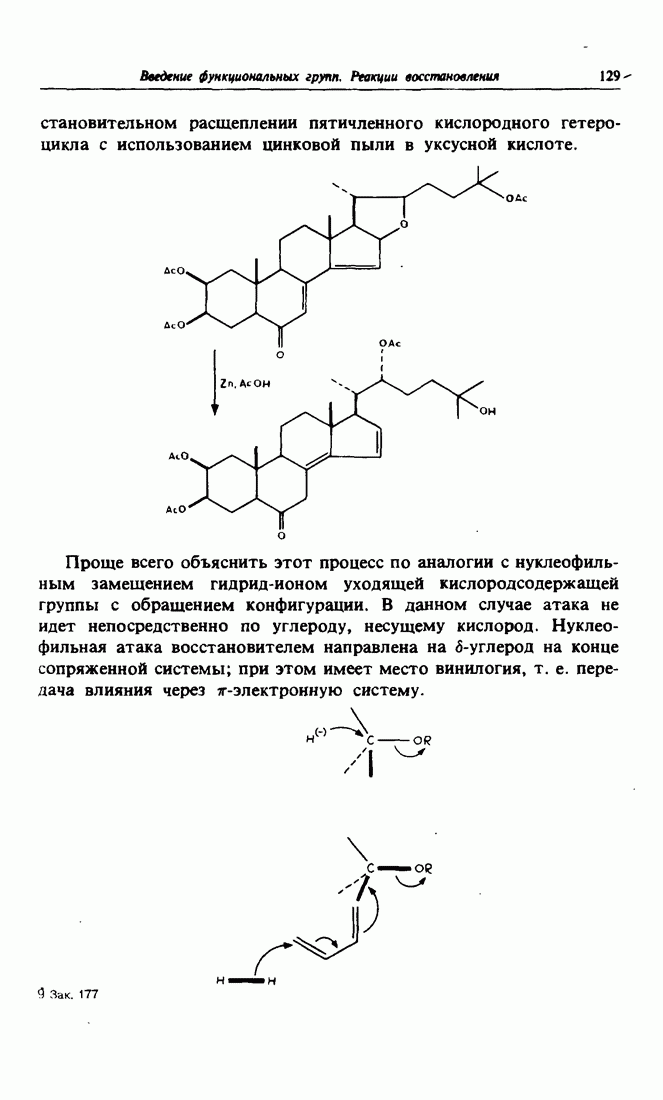
- 10. Как повысить продуктивность шелковичных червей
- Глава 11. РЕАКЦИИ ПРИСОЕДИНЕНИЯ И ЭЛИМИНИРОВАНИЯ
- 1. Полиэтилен
- 2. Некоторые промышленные реакции присоединения к этилену
- 3. Рынок пластмасс
- 4. Старение вин
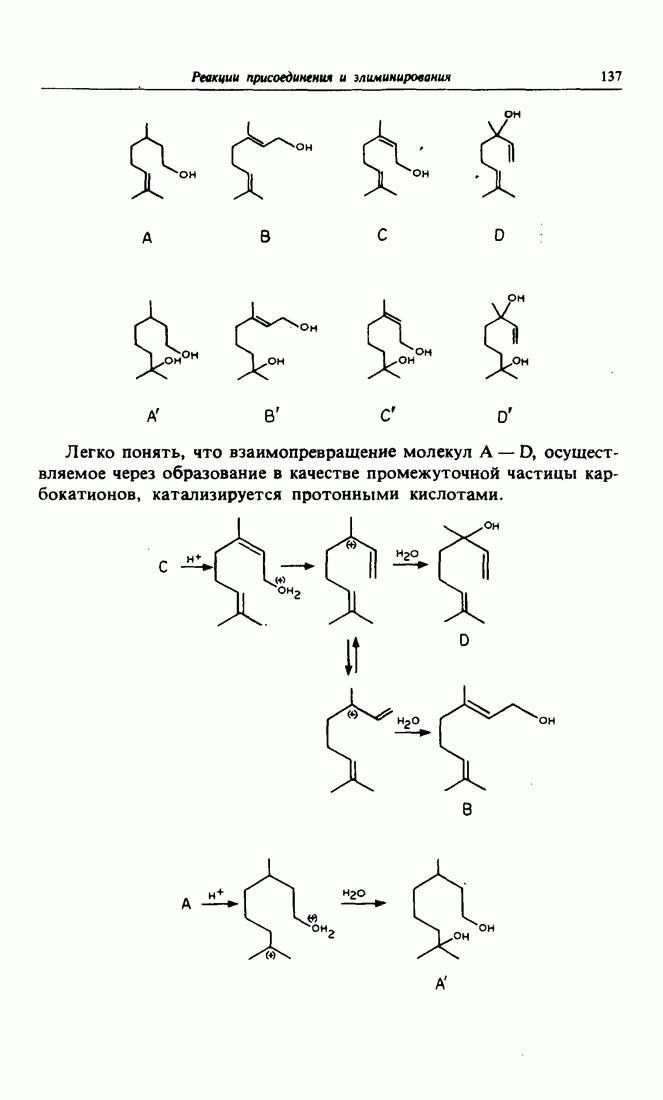
- 5. Запах роз
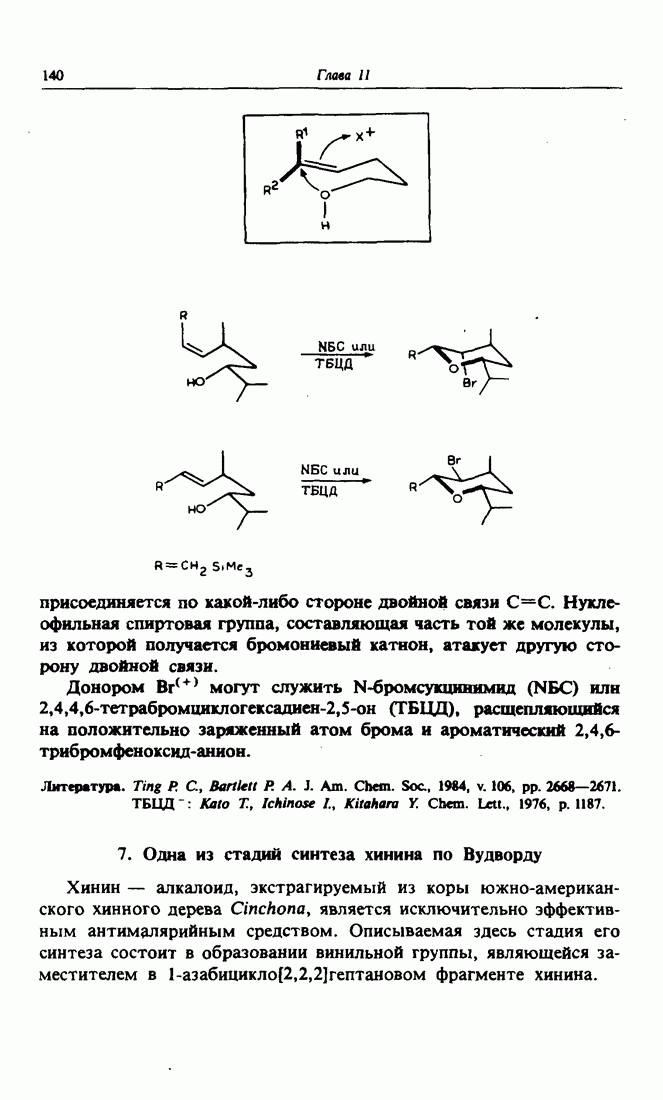
- 6. Применение в синтезе галогенгидринов
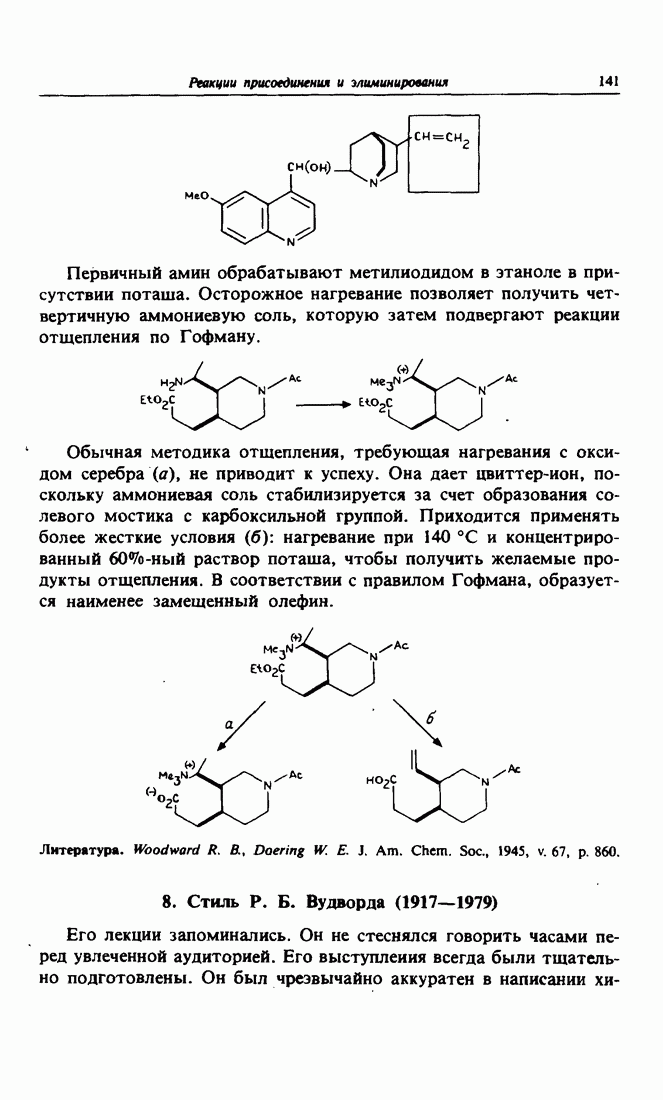
- 7. Одна из стадий синтеза хинина по Вудворду
- 8. Стиль P. Б. Вудворда (1917—1979)
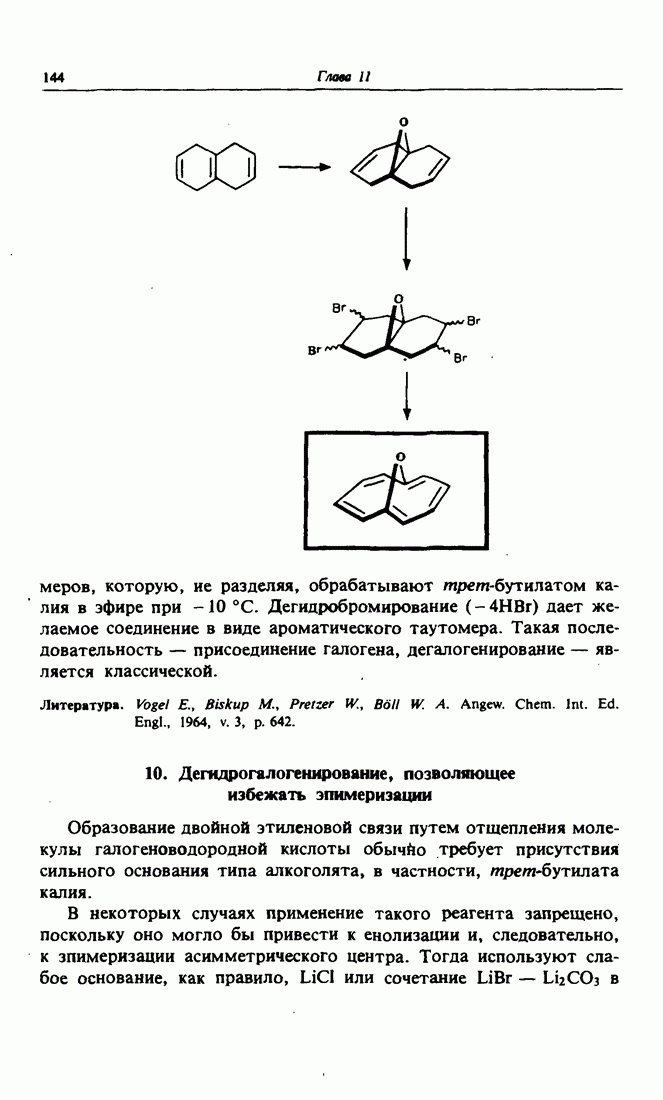
- 9. Галогенирование с последующим дегидрогалогенированием
- 10. Дегидрогалогенирование, позволяющее избежать эпимеризации
- 11. Селективность при гидроборировании
- 12. Начало синтеза эльвирола
- 13. Новые электрофильные реагенты
- Глава 12. ПЕРЕГРУППИРОВКИ ФУНКЦИОНАЛЬНЫХ ГРУПП. ПРЕВРАЩЕНИЕ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ В ОЛЕФИНЫ ПО РЕАКЦИИ ВИТТИГА
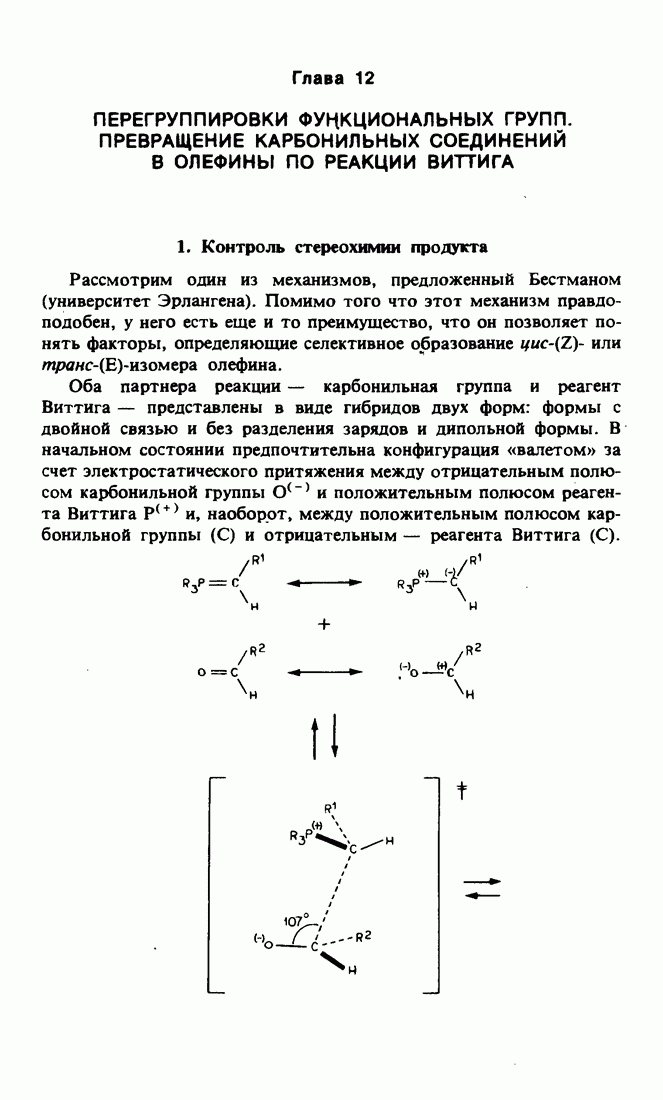
- 1. Контроль стереохимии продукта
- 2. Вариант реакции Виттига в отсутствие енолизации
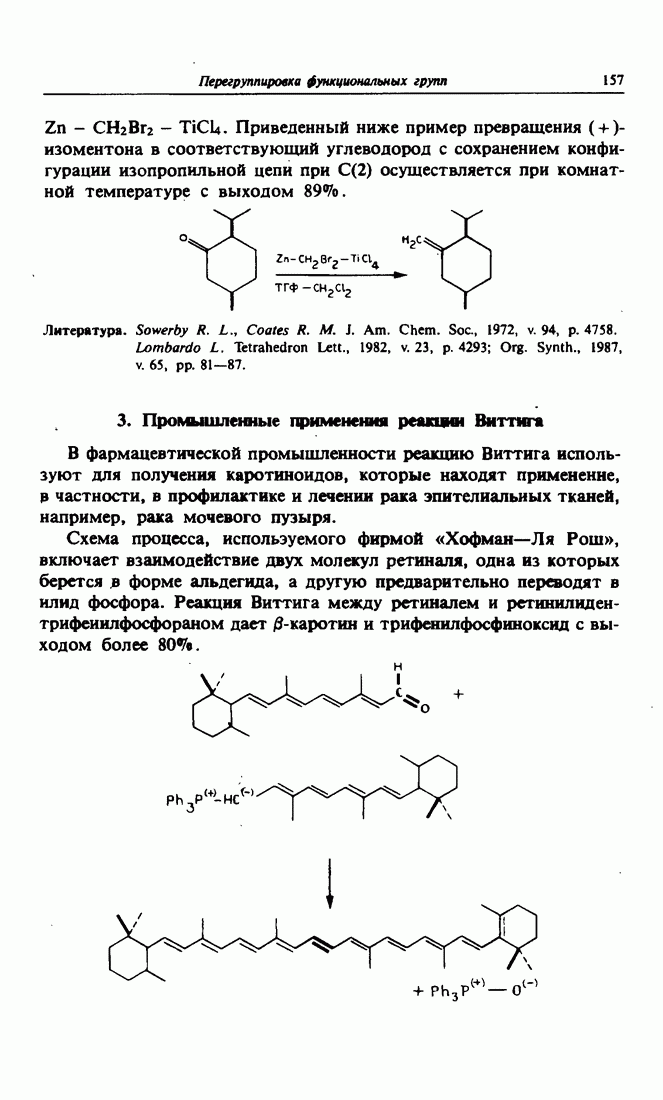
- 3. Промышленные применения реакши Виттига
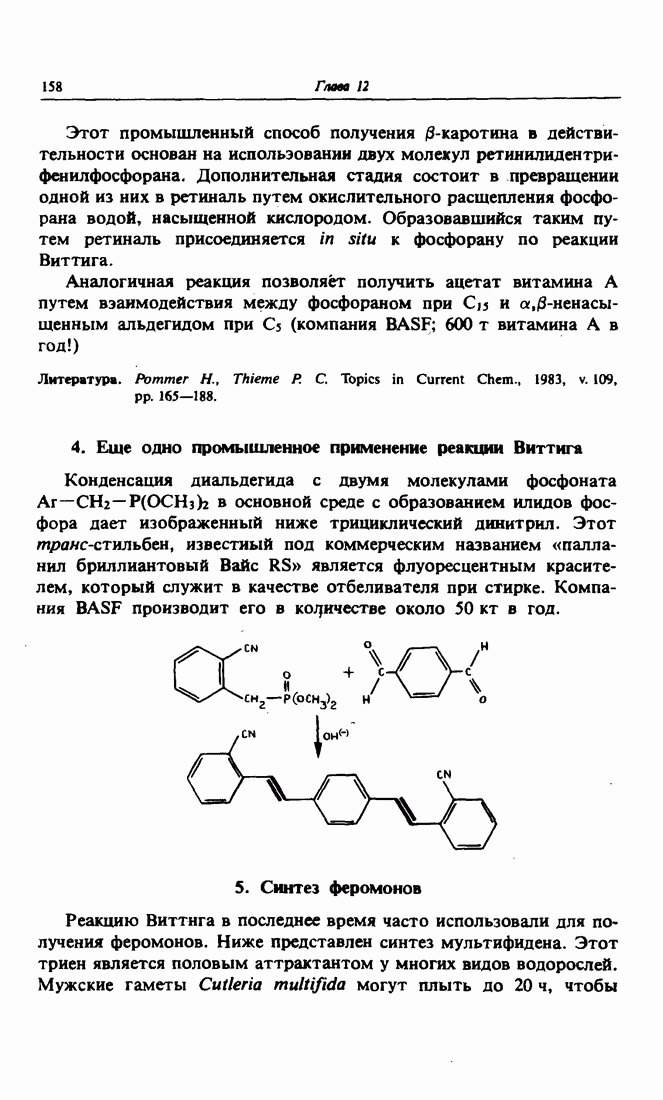
- 4. Еще одно промышленное применение реакции Виттига
- 5. Синтез феромонов
- 6. Другой синтез феромона по реакции Виттига
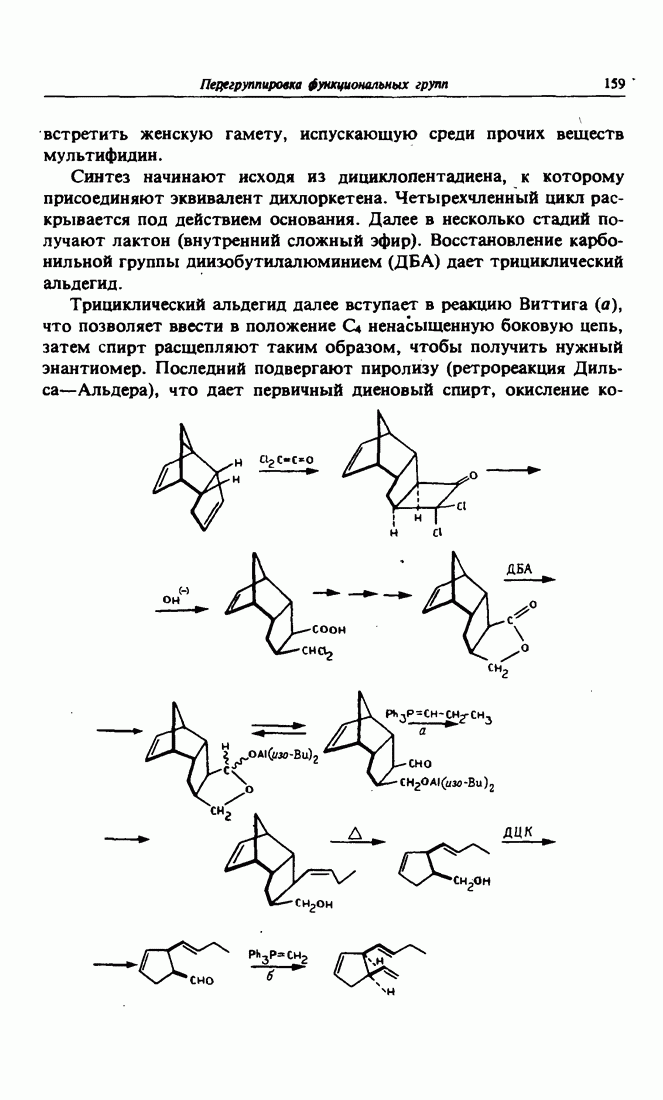
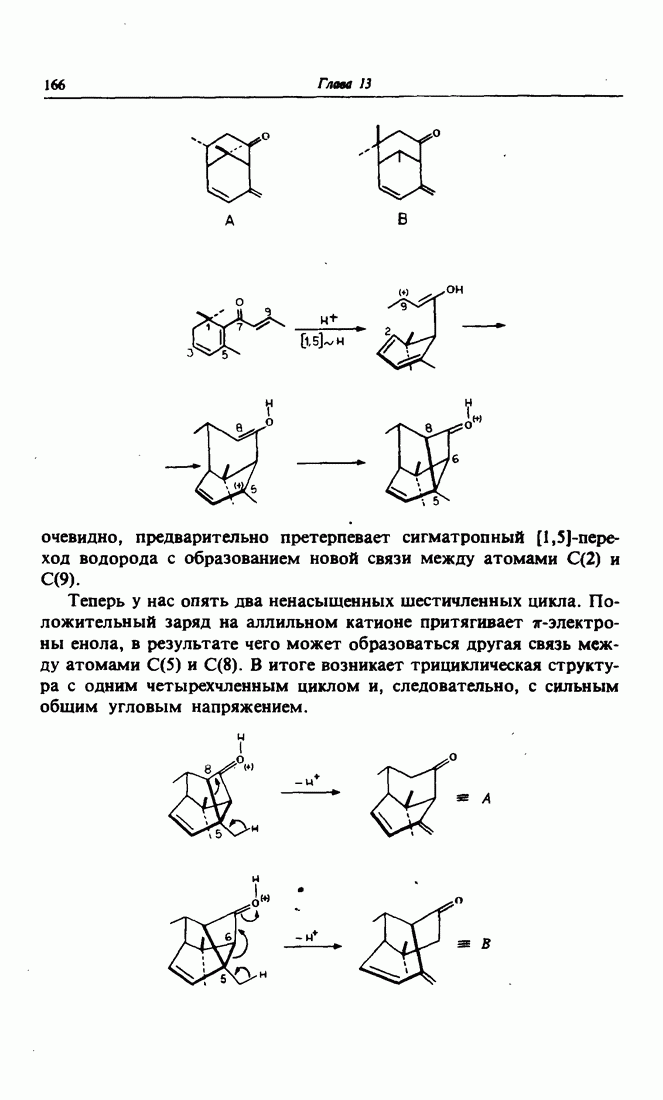
- Глава 13. ПЕРЕГРУППИРОВКИ
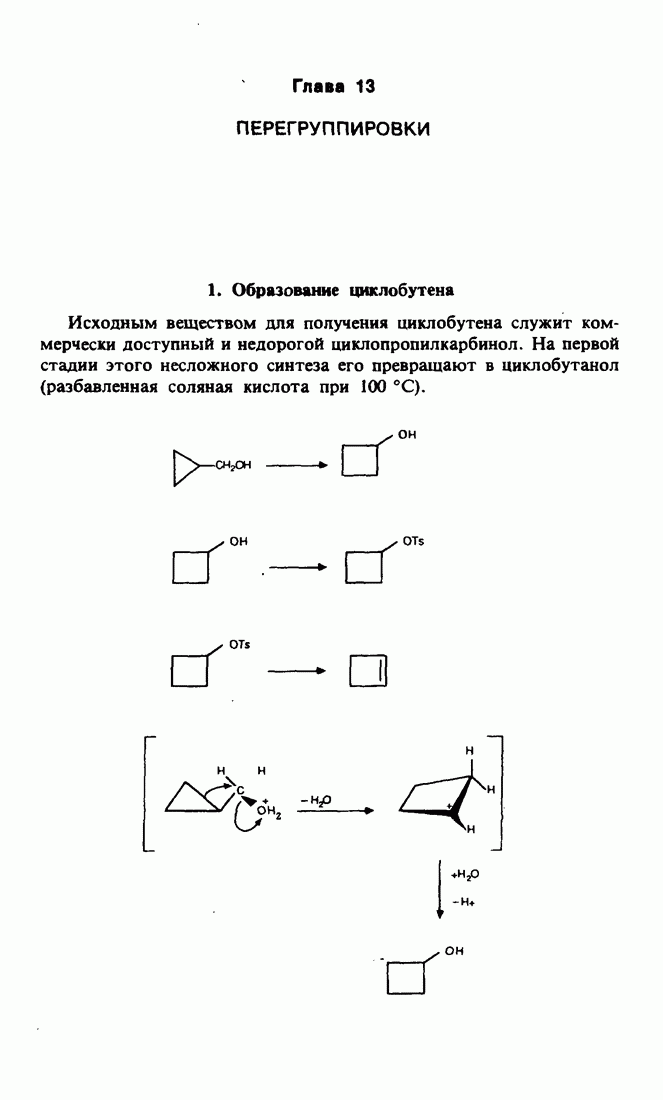
- 1. Образование циклобутена
- 2. 1,2-Миграция
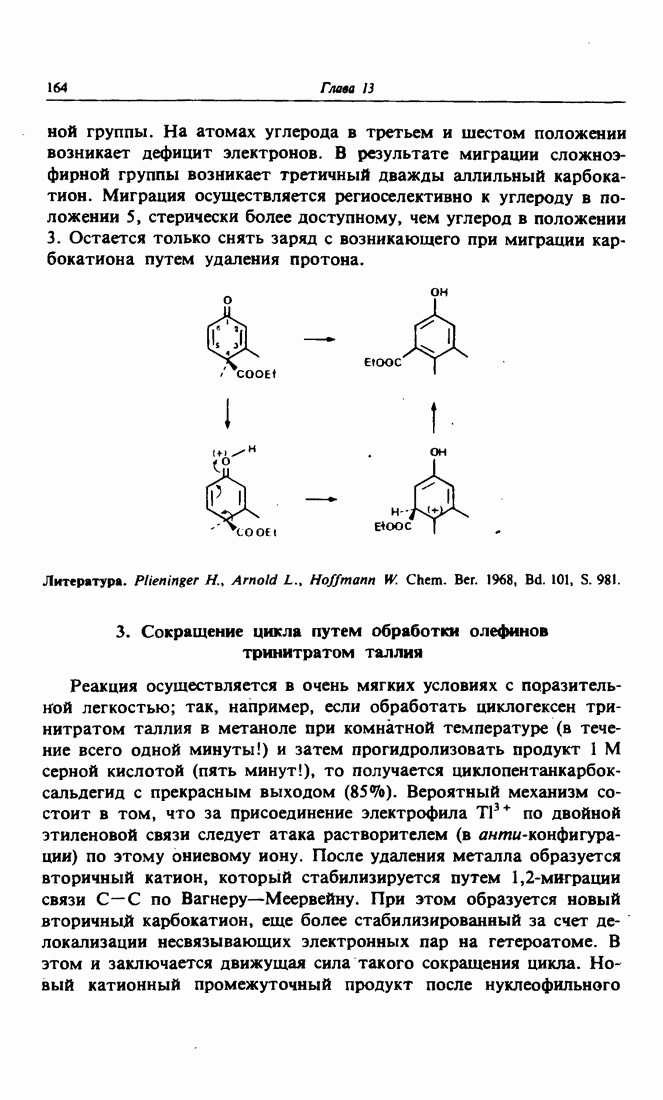
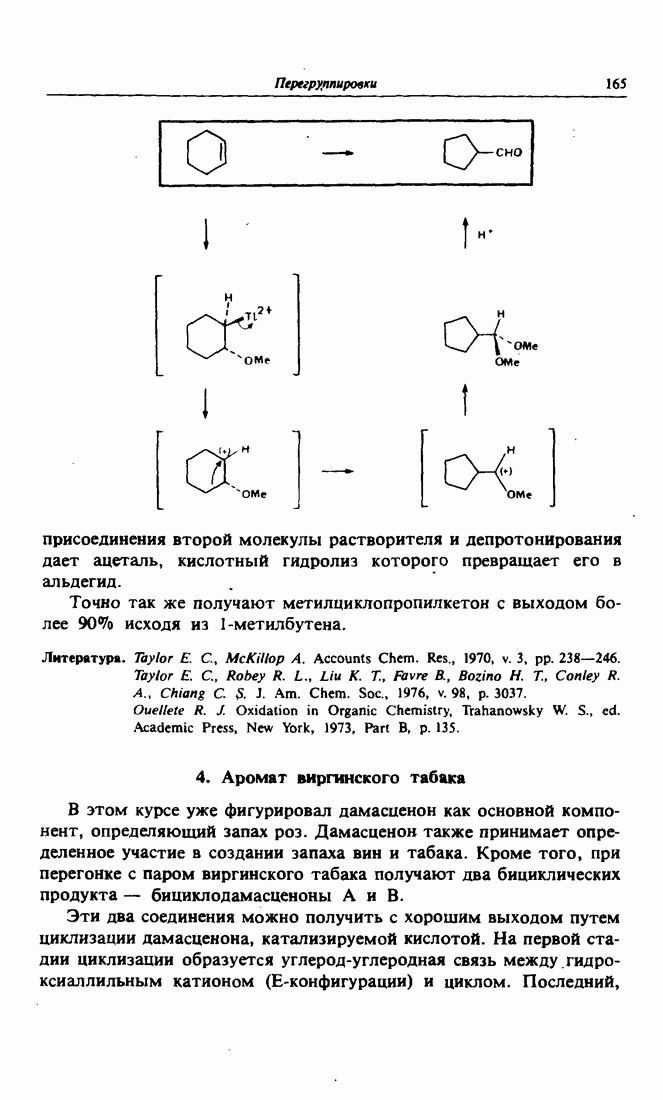
- 3. Сокращение цикла путем обработки олефинов тринитратом таллия
- 4. Аромат виргинского табака
- 5. Маленькие лягушки, которые важнее быка, или для чего служит перегруппировка Бекмана
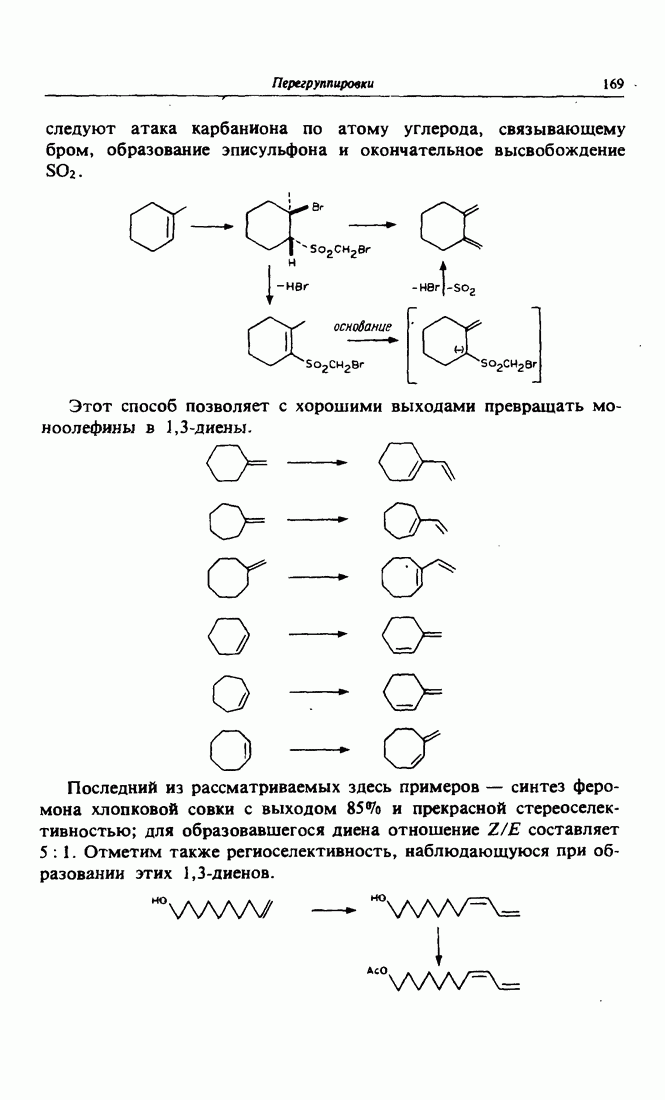
- 6. Некоторые применения реакции Рамберга-Беклунда
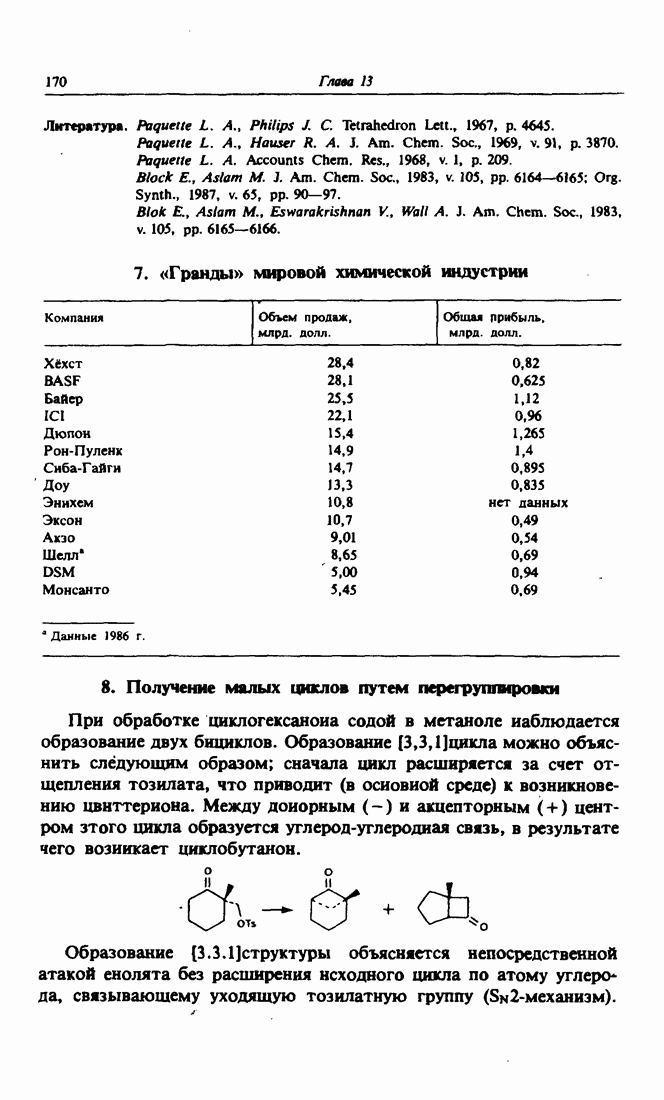
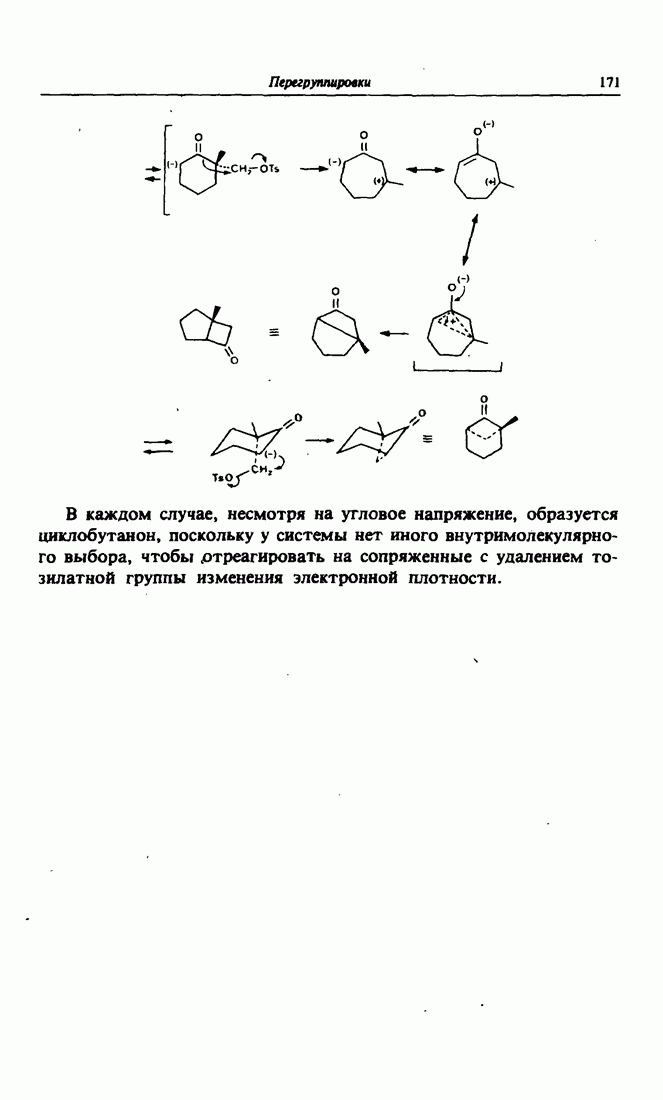
- 8. Получение малых циклов путем перегруппировки
- Главе 14. ДОНОРНЫЕ СИНТОНЫ
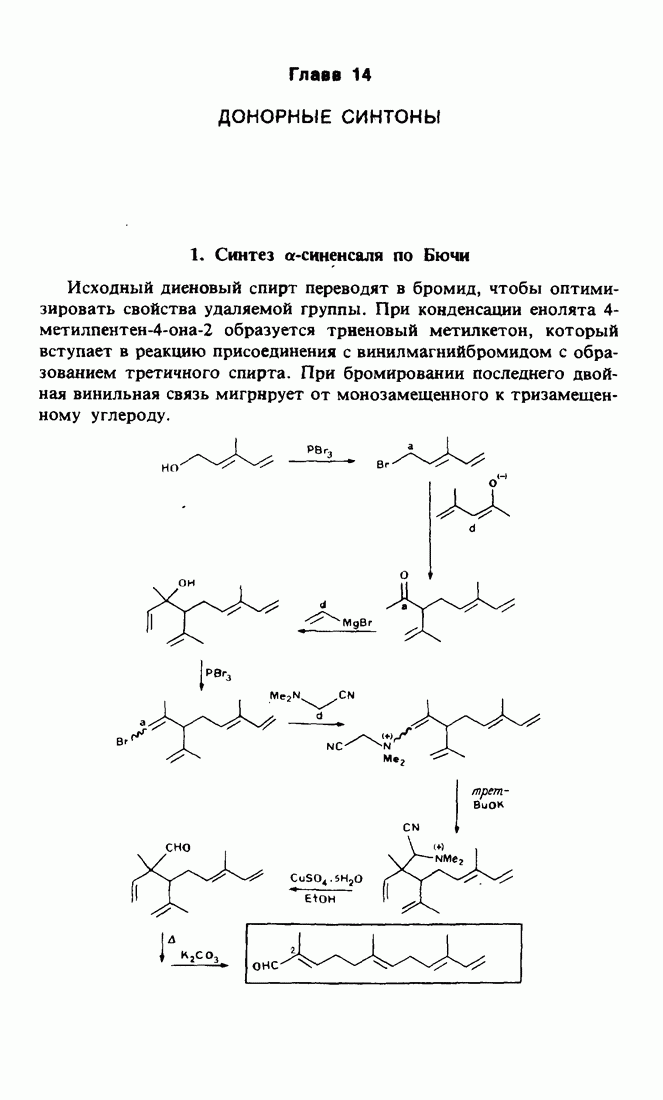
- 1. Синтез а-синенсаля по Бючи
- 2. Начало синтеза кофестола по Кори
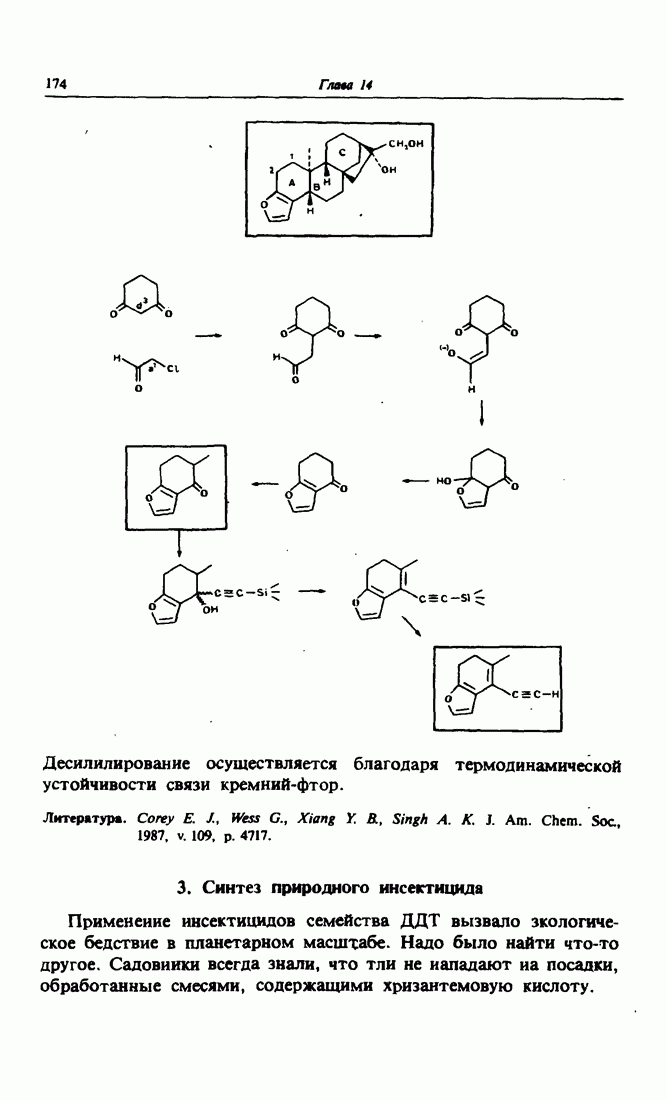
- 3. Синтез природного инсектицида
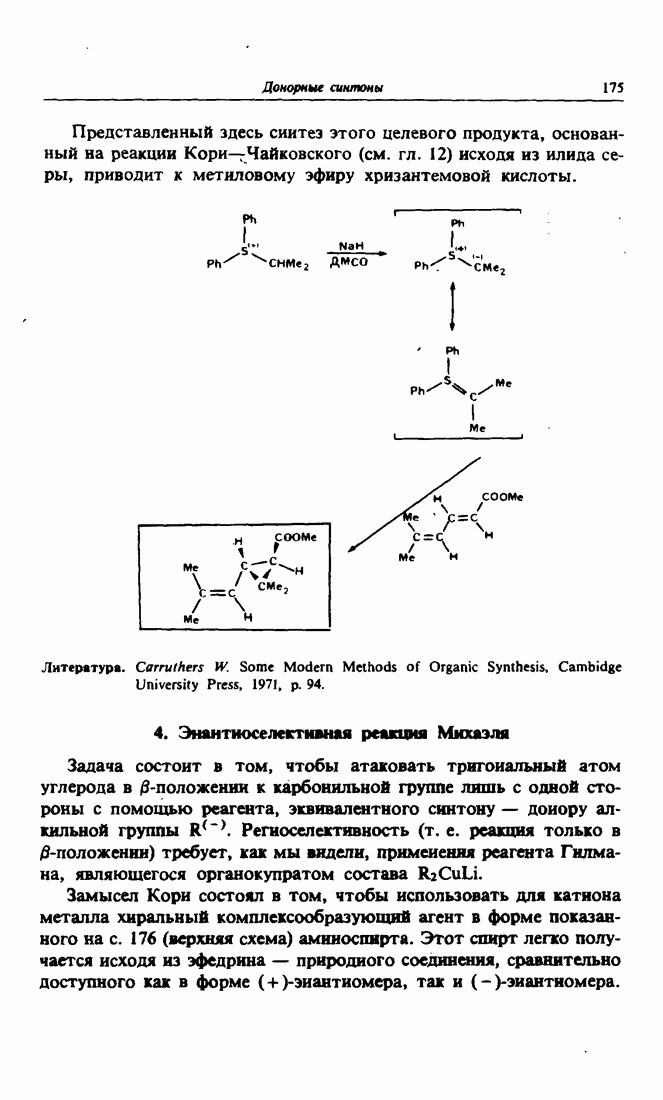
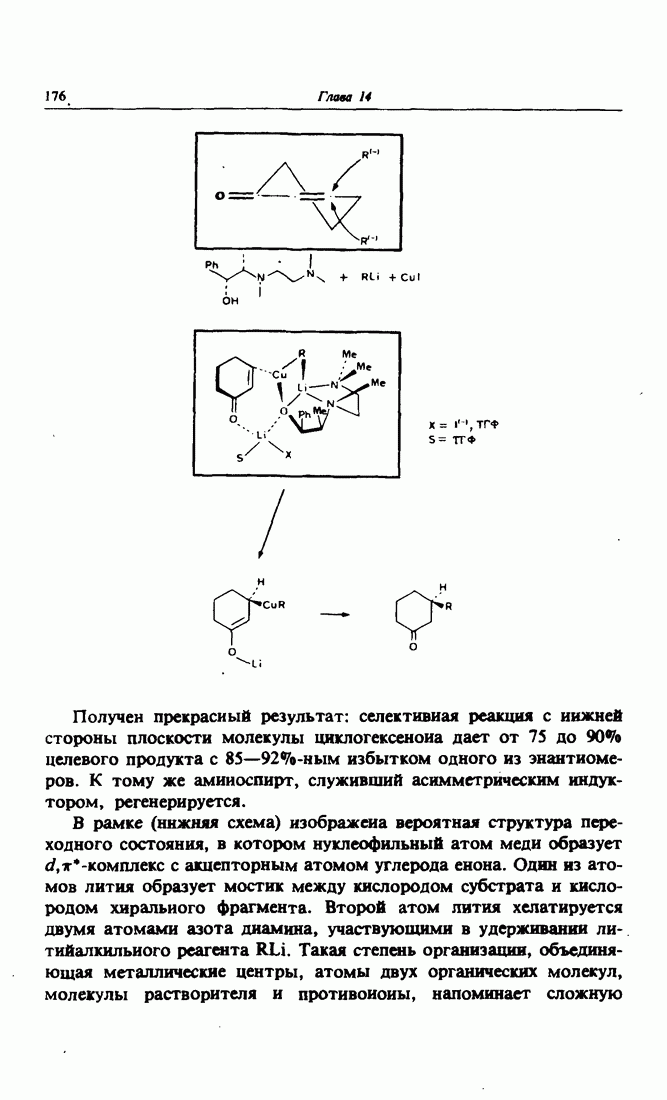
- 4. Энантиоселективная реакция Михаэля
- 5. Хитрые осы
- 6. Химия на основе C1-соединений
- Глава 15. АКЦЕПТОРНЫЕ СИНТОНЫ
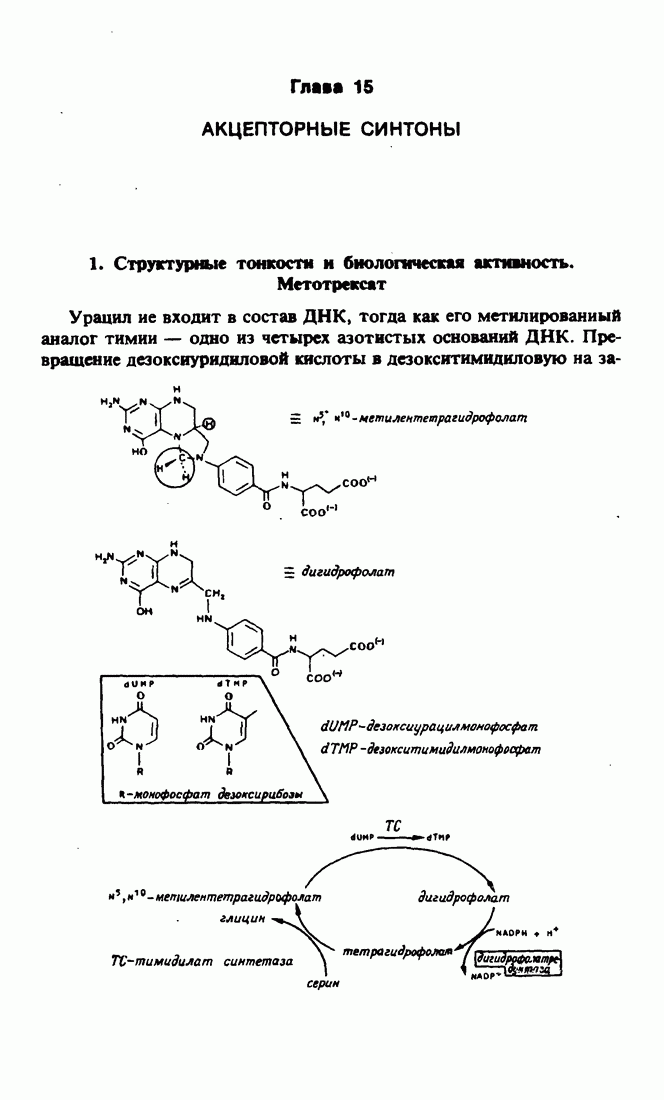
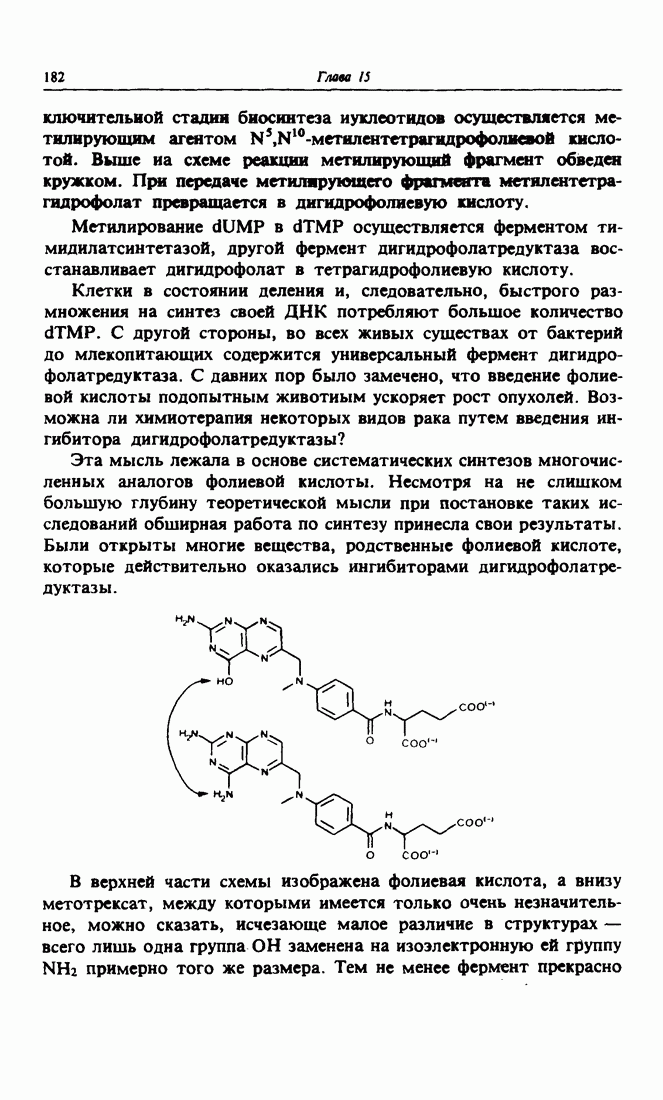
- 1. Структурные тонкости и биологическая активность. Метотрегсат
- 2. Функциональные вариации на структурную тему
- 3. Производство ароматических и вкусовых добавок
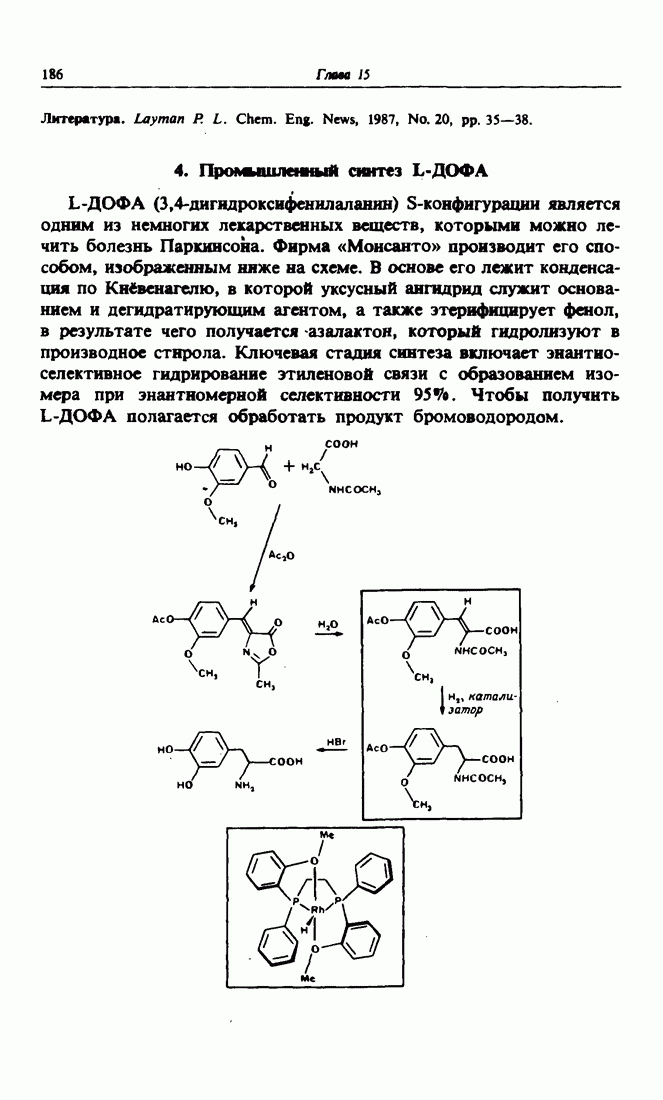
- 4. Проашшлетый синтез L-ДОФА
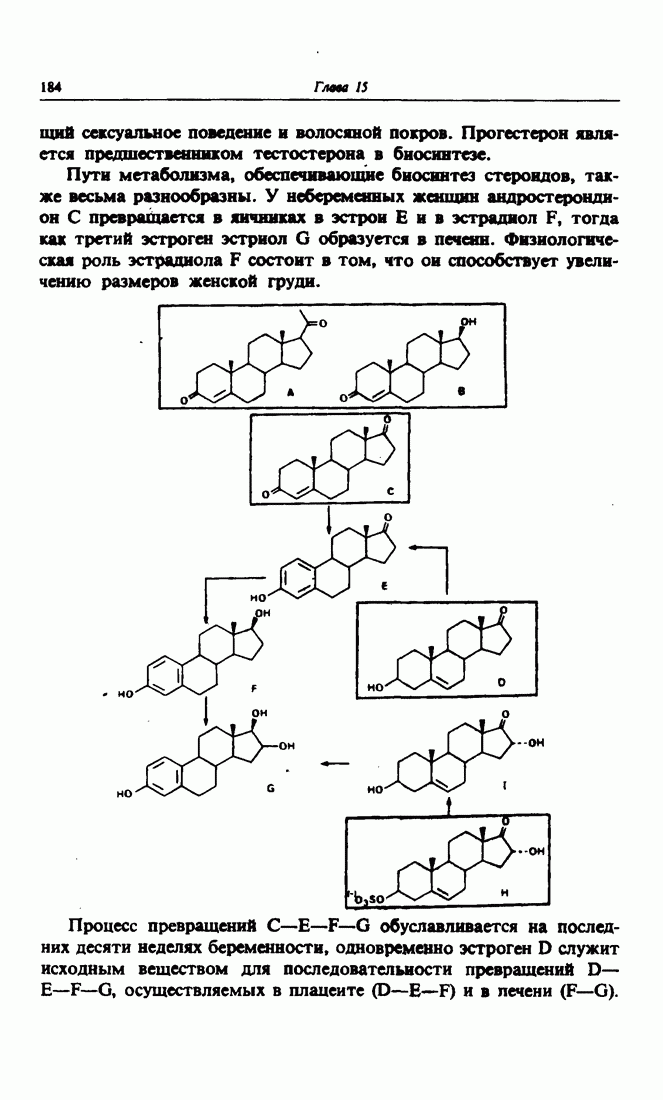
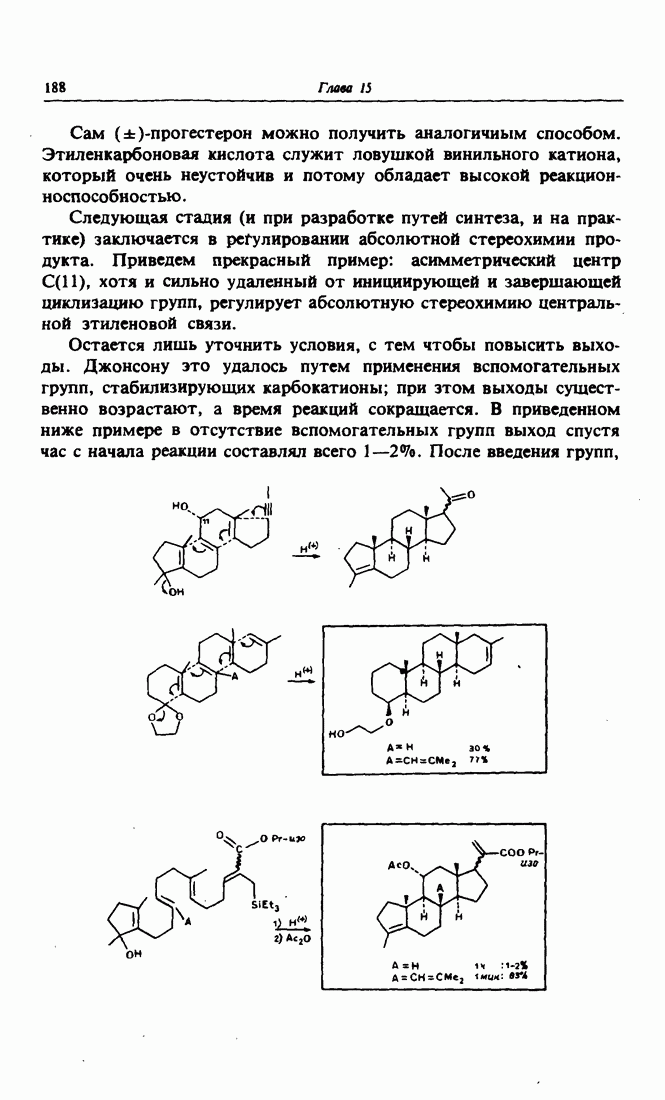
- 5. Биомиметический синтез стероидов
- Глава 16. РЕТРОСИНТЕТИЧЕСКИЙ АНАЛИЗ
- 1. Симметризующий ретросинтез
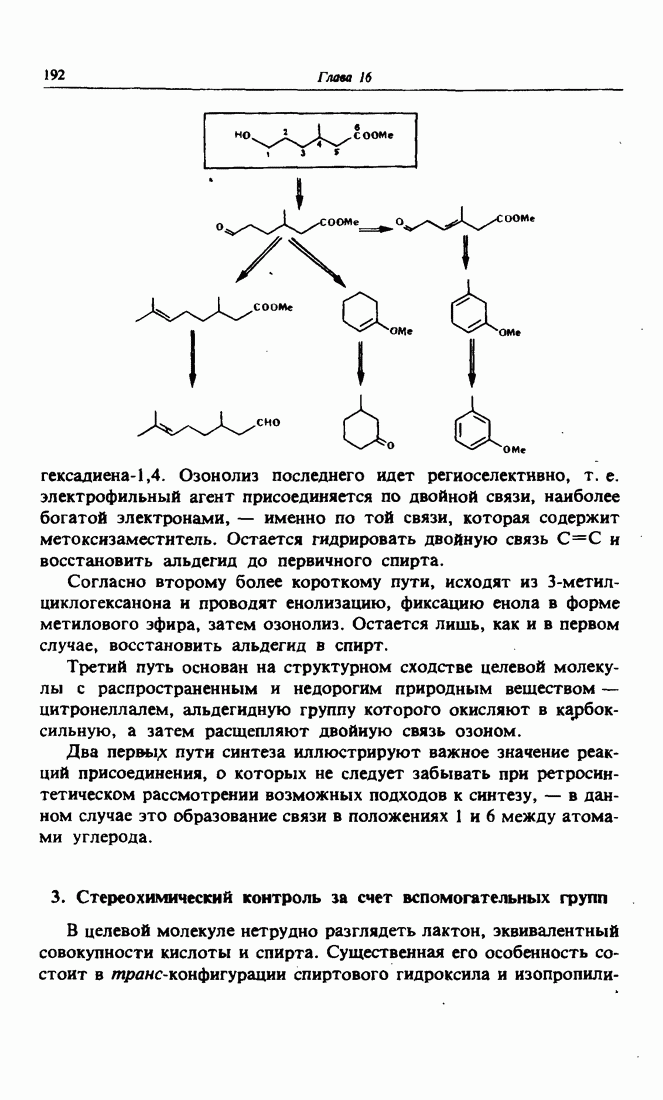
- 2. Реакции присоединения в ретросинтетическом анализе
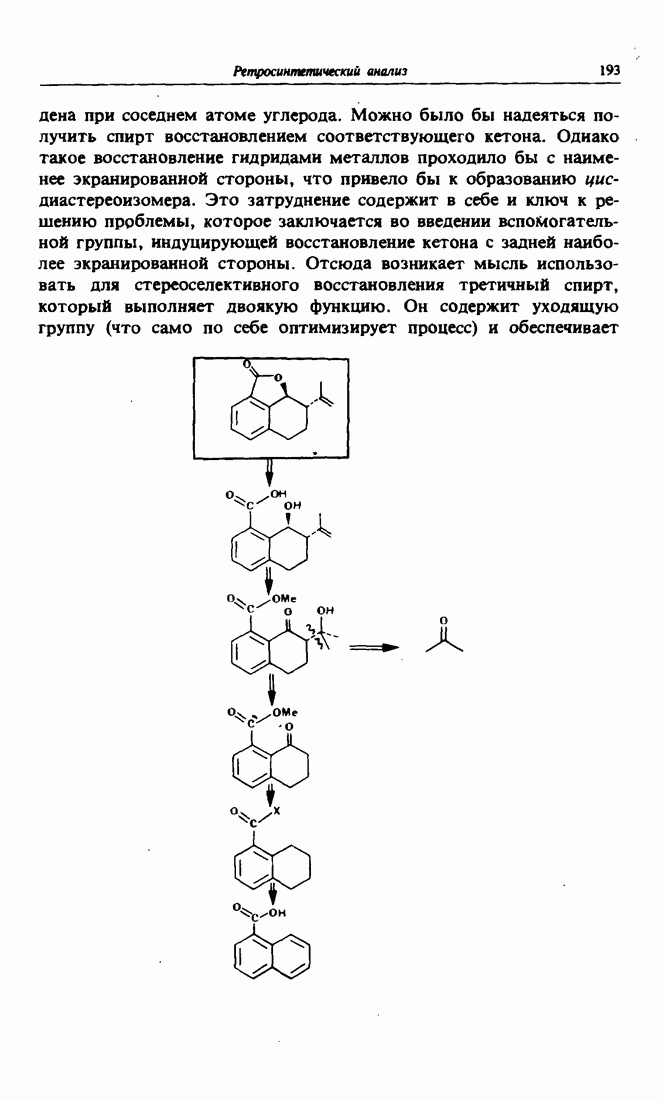
- 3. Стереохимическнй контроль за счет вспомогательных групп
- 4. Окислительный ретросинтез
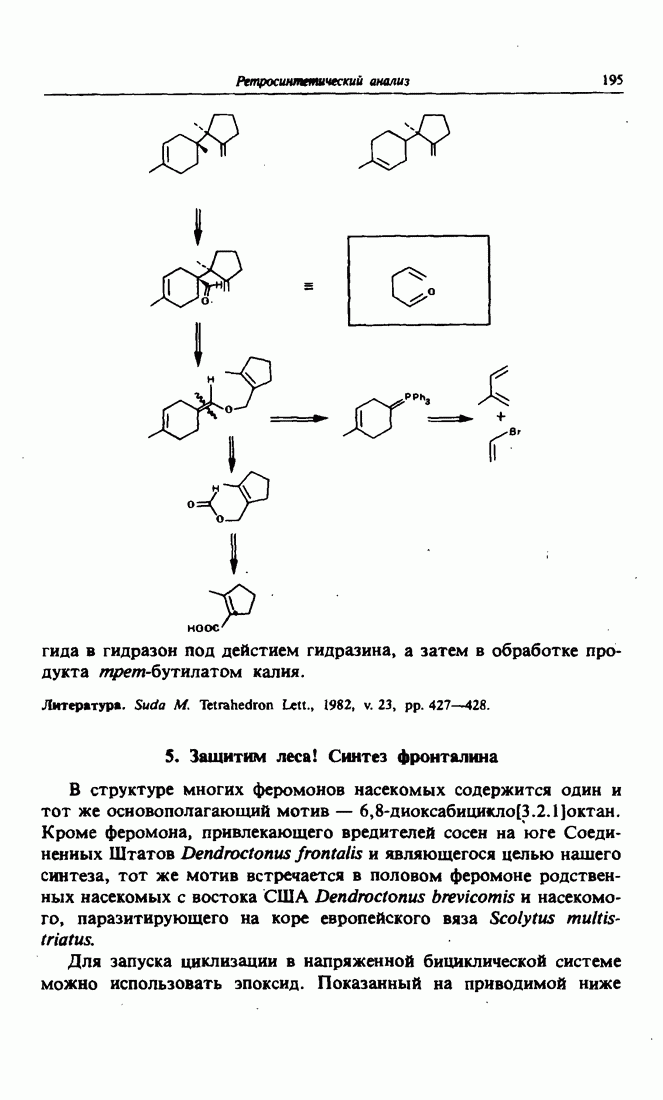
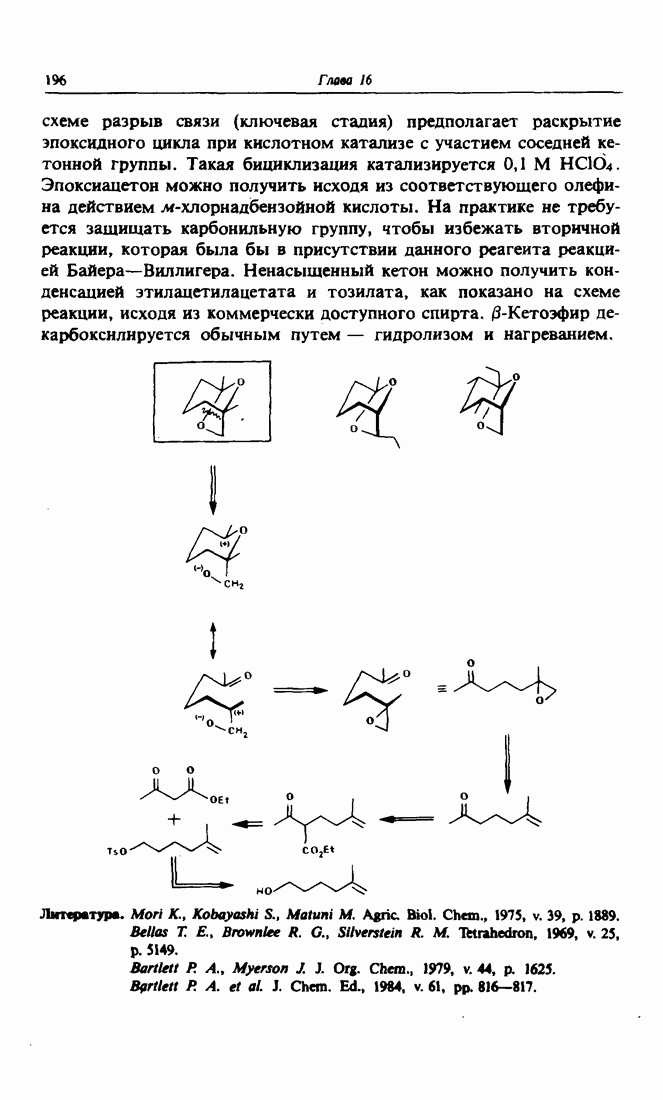
- 5. Защитим леса! Синтез фронталина