| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
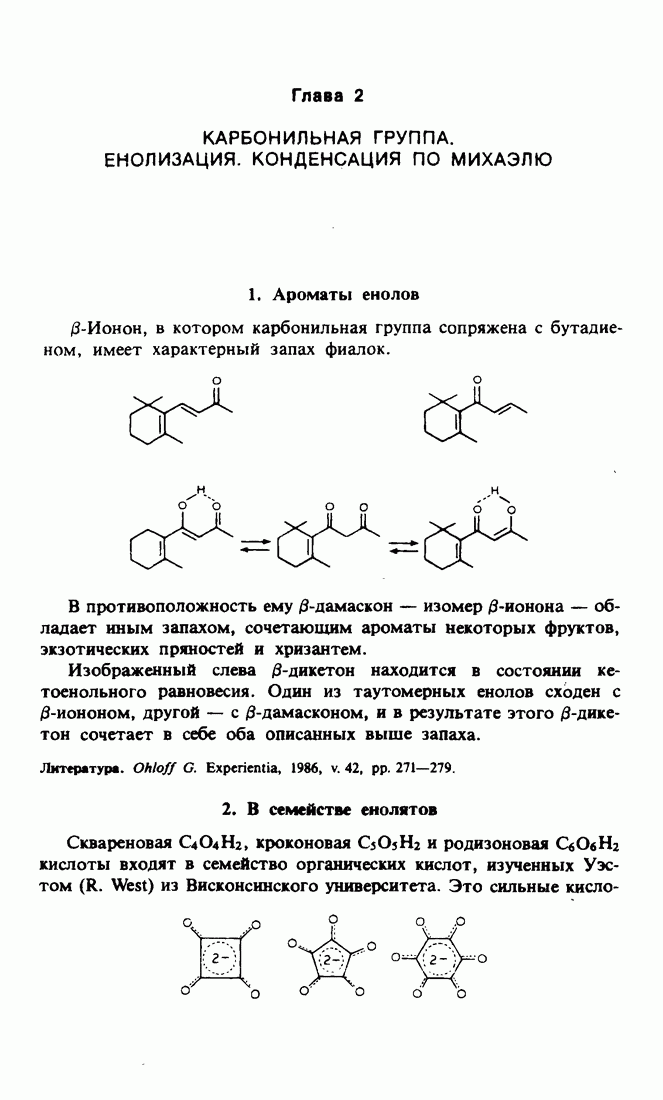
4. Окислительный ретросинтез
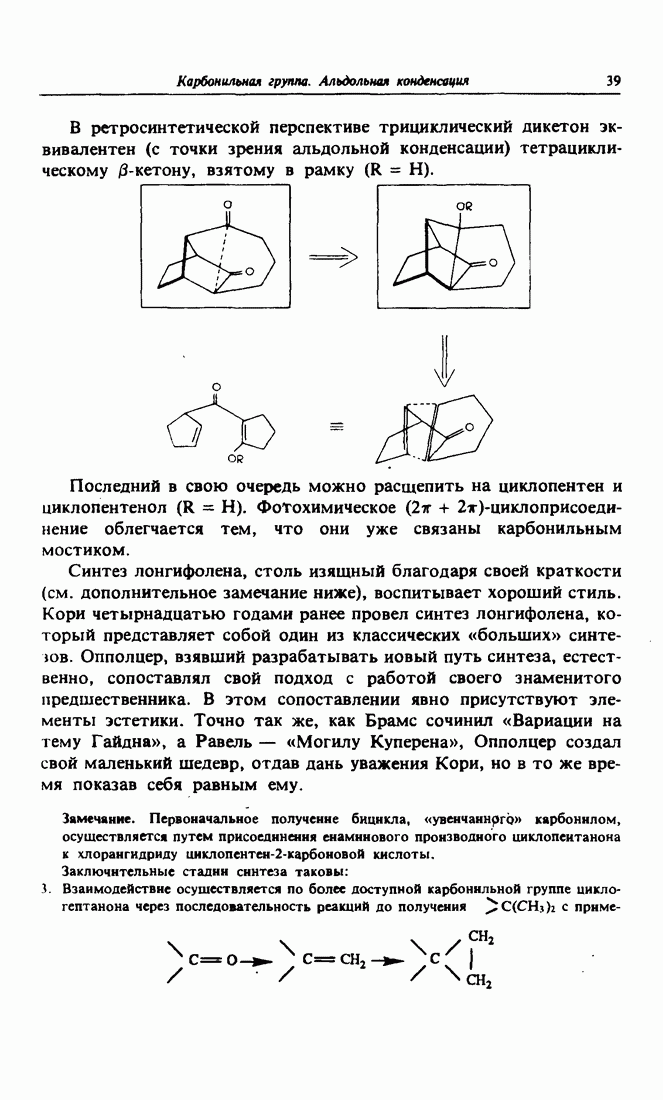
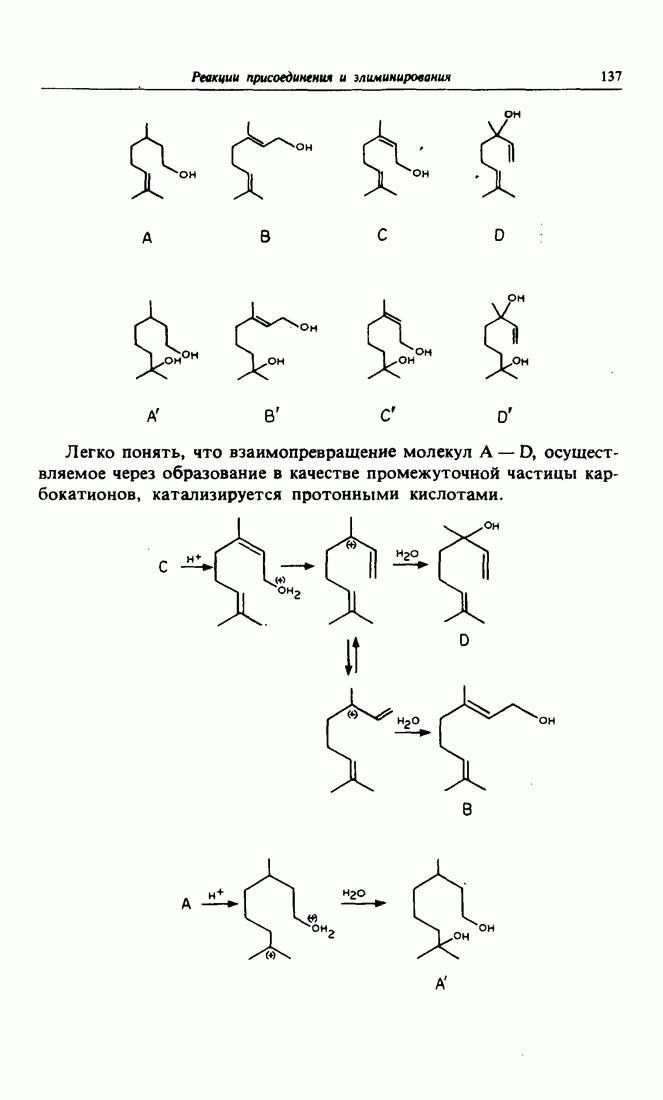
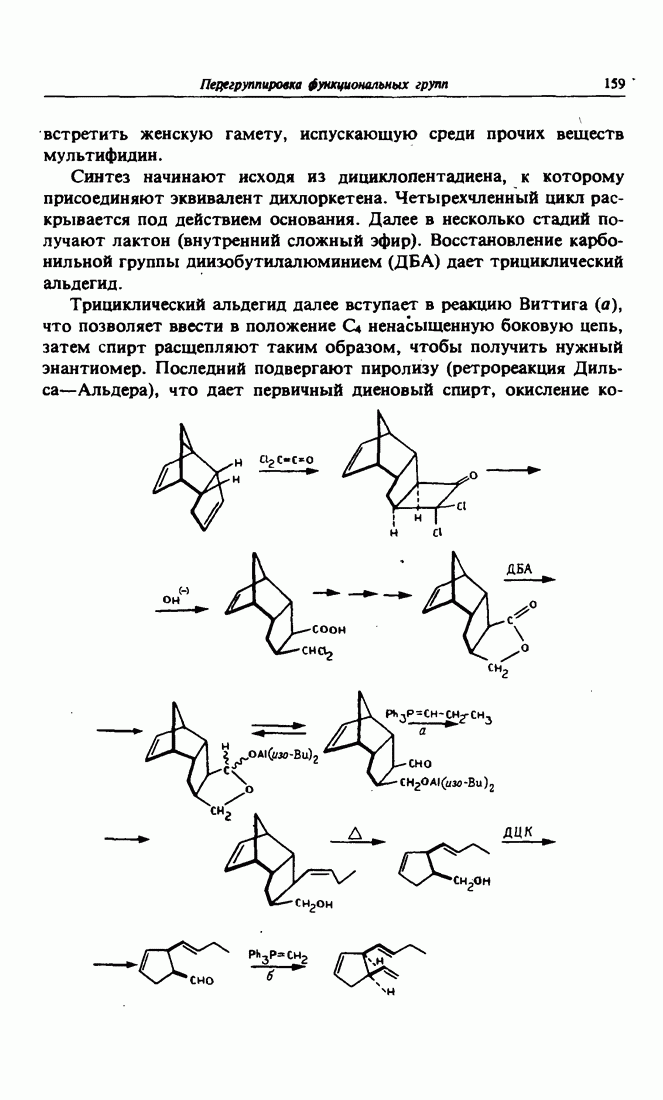
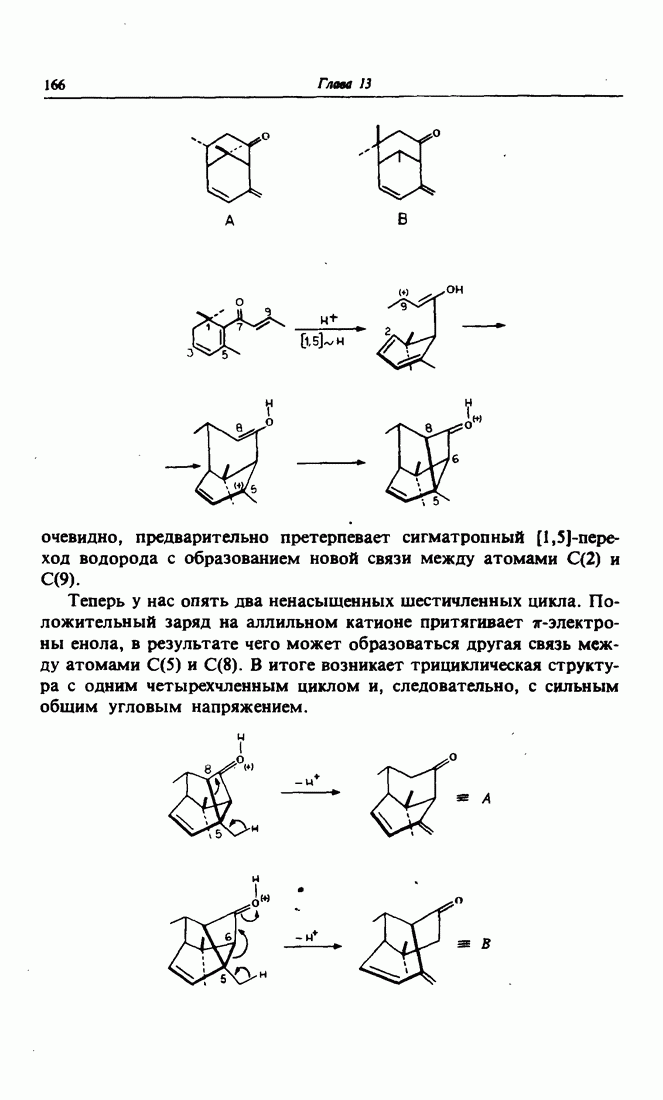
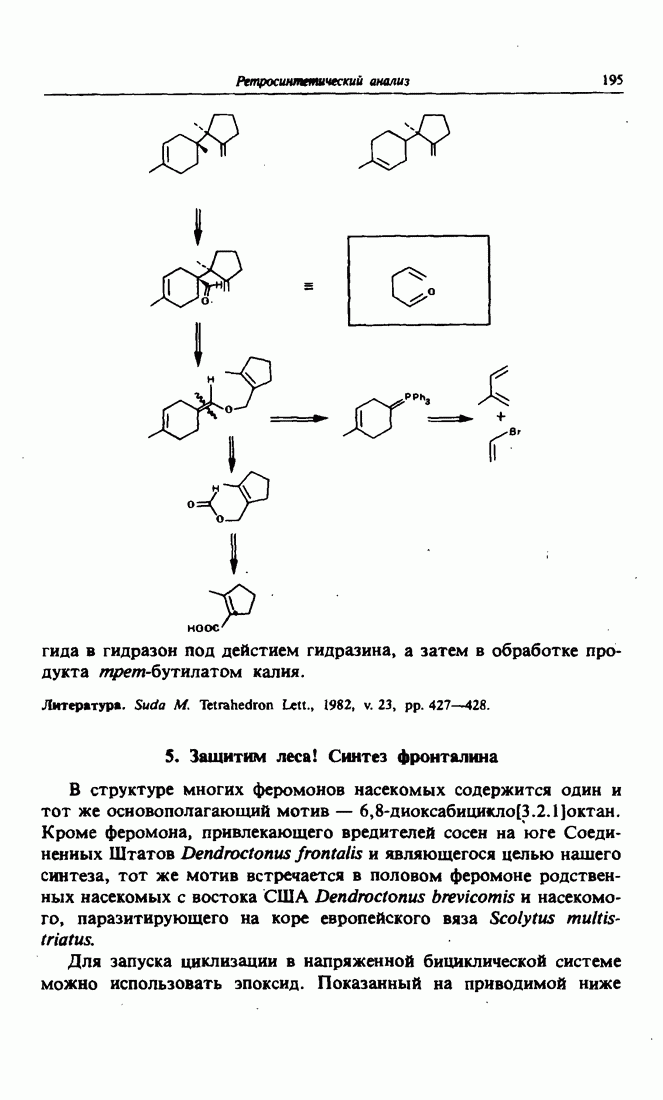
Будучи углеводородами, хотя и ненасыщенными, сесквитерпены растительного происхождения, называемые «бацанен» и «триходиен» не очень подходят в качестве целевых продуктов при ретросинтетических рассуждениях. Следуя завету Дантона («Смелость, смелость и еще раз смелость!»), имело бы смысл заменить одну из метильных групп при четвертичном атоме углерода на альдегидную группу  Какую же именно? Очевидно, ту, которая открывает путь к двум ненасыщенным связям
Какую же именно? Очевидно, ту, которая открывает путь к двум ненасыщенным связям  разделенным двумя тетраэдрическими атомами углерода, поскольку это основополагающий мотив для сигматропной [3.3]перегруппировки, в данном случае перегруппировки Кляйзена. Это приводит к виниловому и аллиловому эфирам в качестве субстратов для перегруппировок Кляйзена. Их можно получить путем указанного на схеме разрыва, а в «обратном», синтетическом смысле — по реакции Виттига. Партнеры для реакции Виттига получаются в свою очередь до реакции Дильса-Альдера, с одной стороны, для образования илида фосфора исходя из соответствующего бромида, а с другой — исходя из 2-метилцикпопентен-1-карбоновой кислоты, которую придется восстановить в первичный спирт литийалюминийгидридом с тем, чтобы этот спирт затем прореагировал с муравьиной кислотой
разделенным двумя тетраэдрическими атомами углерода, поскольку это основополагающий мотив для сигматропной [3.3]перегруппировки, в данном случае перегруппировки Кляйзена. Это приводит к виниловому и аллиловому эфирам в качестве субстратов для перегруппировок Кляйзена. Их можно получить путем указанного на схеме разрыва, а в «обратном», синтетическом смысле — по реакции Виттига. Партнеры для реакции Виттига получаются в свою очередь до реакции Дильса-Альдера, с одной стороны, для образования илида фосфора исходя из соответствующего бромида, а с другой — исходя из 2-метилцикпопентен-1-карбоновой кислоты, которую придется восстановить в первичный спирт литийалюминийгидридом с тем, чтобы этот спирт затем прореагировал с муравьиной кислотой 
Далее для завершения синтеза остается только восстановить альдегид  в метилзамещенное производное
в метилзамещенное производное  Один из способов проведения этого процесса заключается в переводе
Один из способов проведения этого процесса заключается в переводе
(см. скан)
альдегида в гидразон под дейстием гидразина, а затем в обработке продукта  -бутилатом калия.
-бутилатом калия.
Литература.
(см. скан)
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- Глава 1. КАРБОНИЛЬНАЯ ГРУППА. РЕАКЦИИ ПРИСОЕДИНЕНИЯ И ПРИСОЕДИНЕНИЯ—ФРАГМЕНТАЦИИ
- 3. Получение плексигласа
- 4. Доступность и селективность
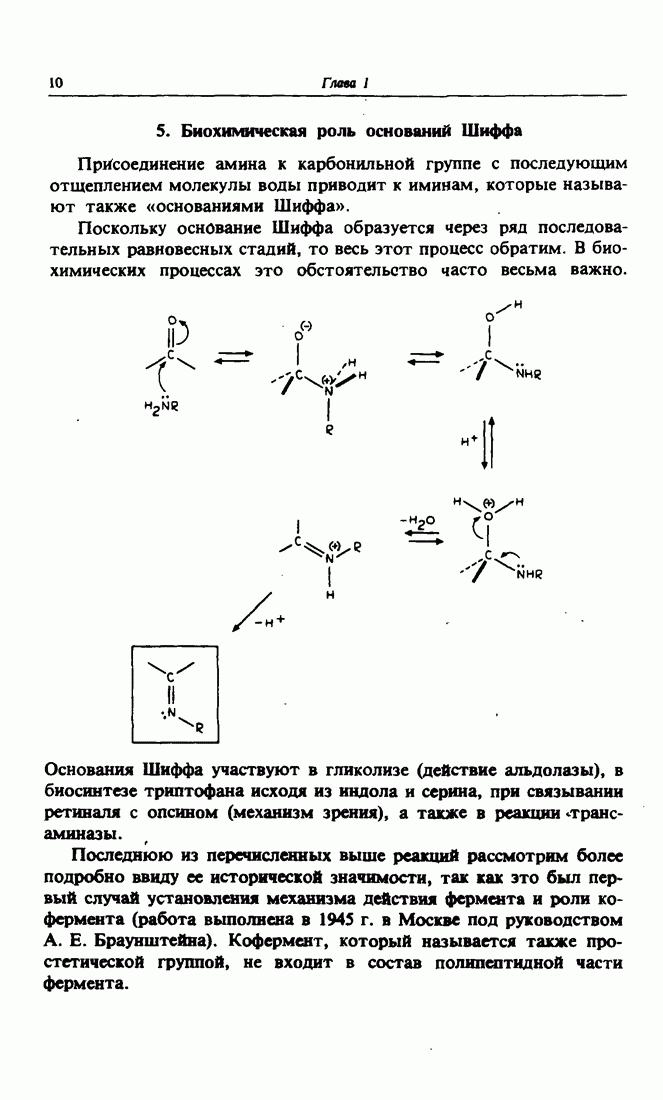
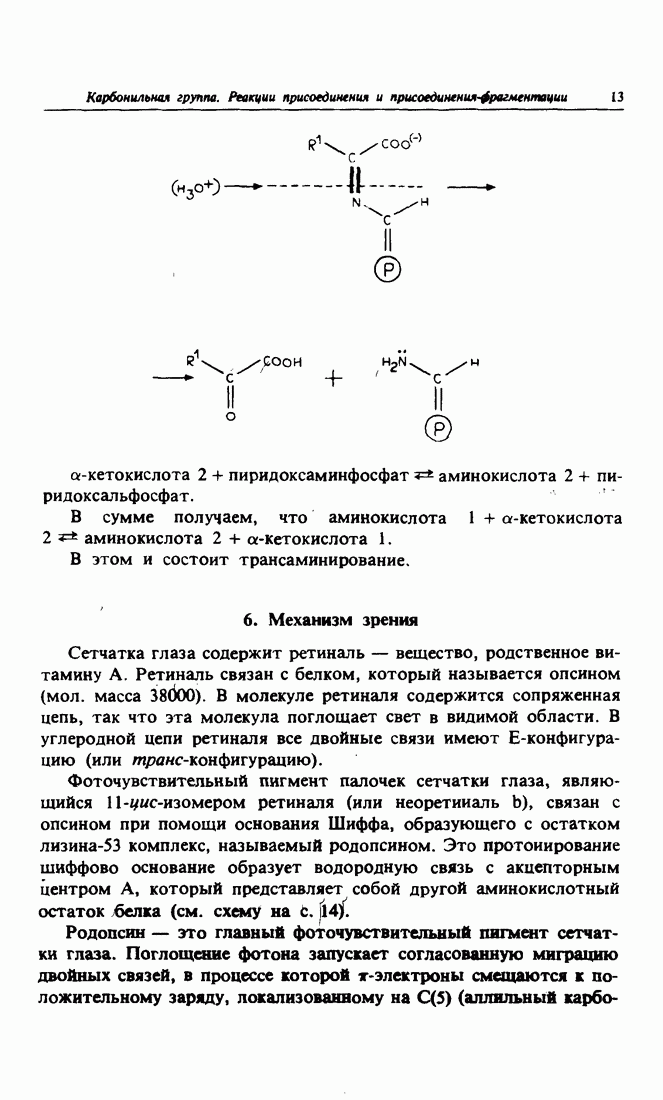
- 5. Биохимическая роль оснований Шиффа
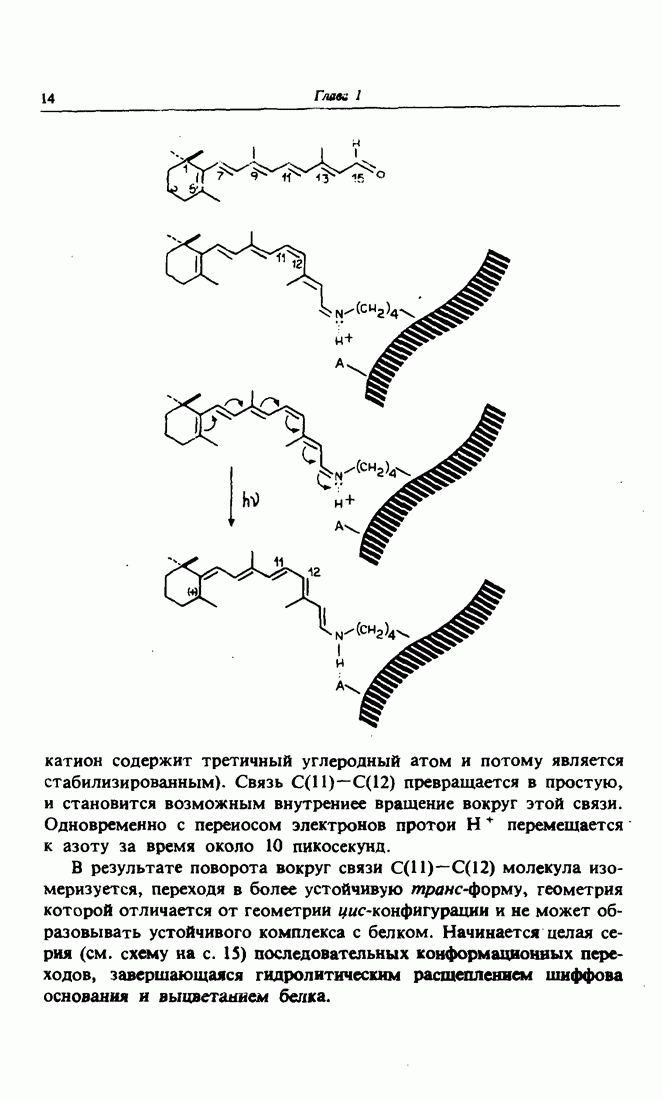
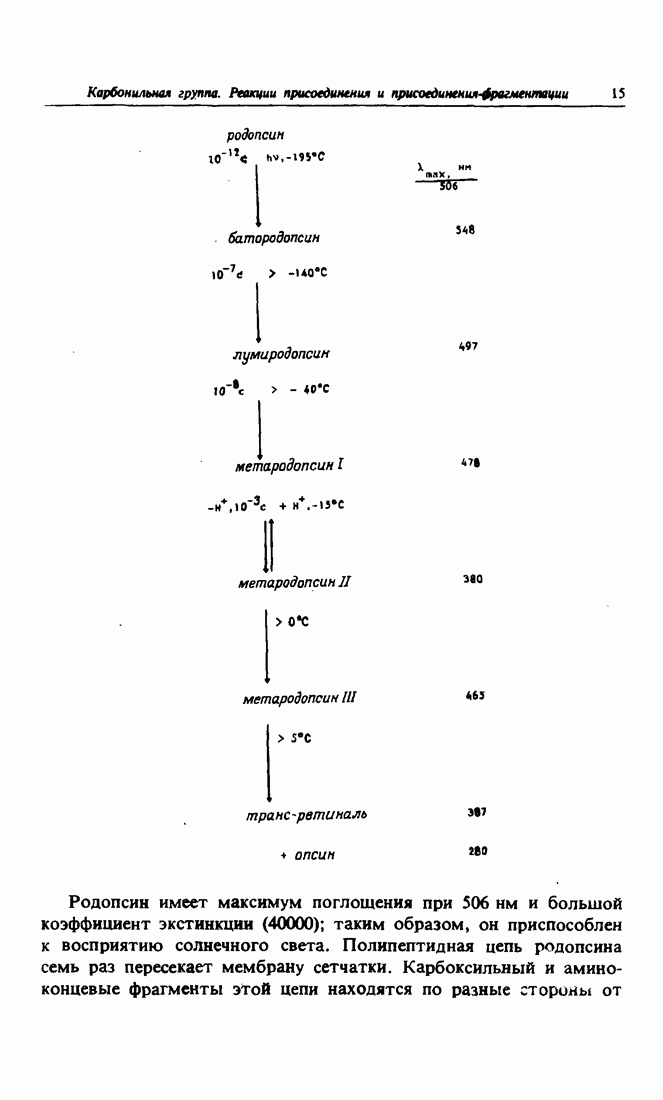
- 6. Механизм зрения
- 7. Цветное зрение
- 8. Новый способ маскировки
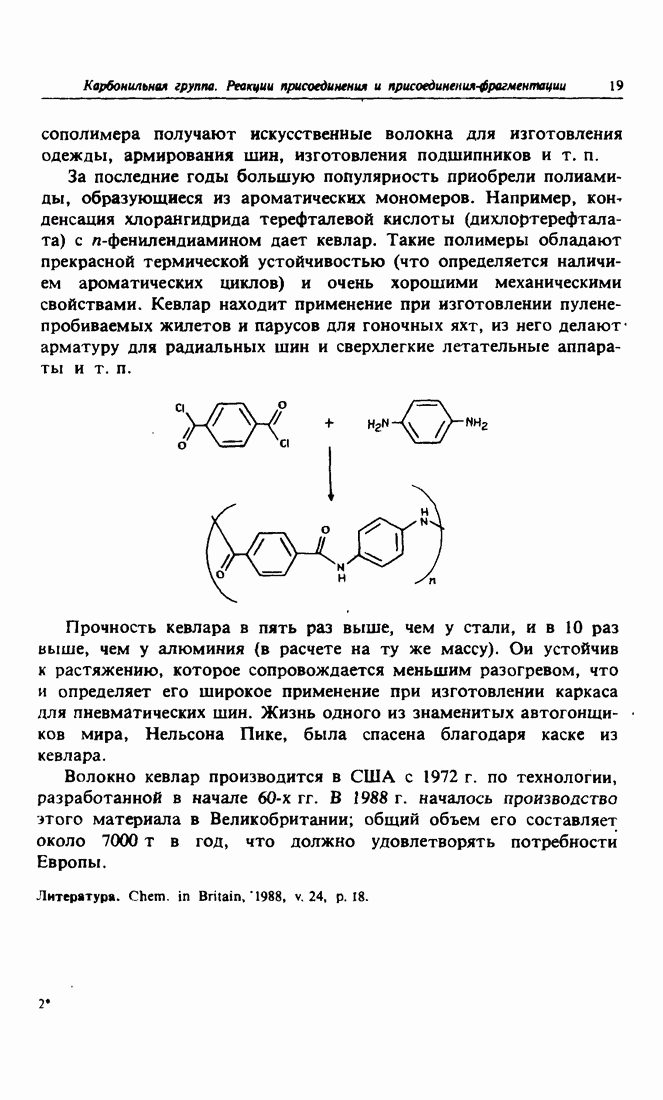
- 9. Полиамиды
- Глава 2. КАРБОНИЛЬНАЯ ГРУППА. ЕНОЛИЗАЦИЯ. КОНДЕНСАЦИЯ ПО МИХАЭЛЮ
- 2. В семействе енолятов
- 3. Химические продукты, имеющие важные применения в промышленности. Формальдегид
- 4. Бакелит
- 5. Природное соединение, содержащее карбонильную группу и a,b-ненасыщенную связь
- 6. Этюд в красном
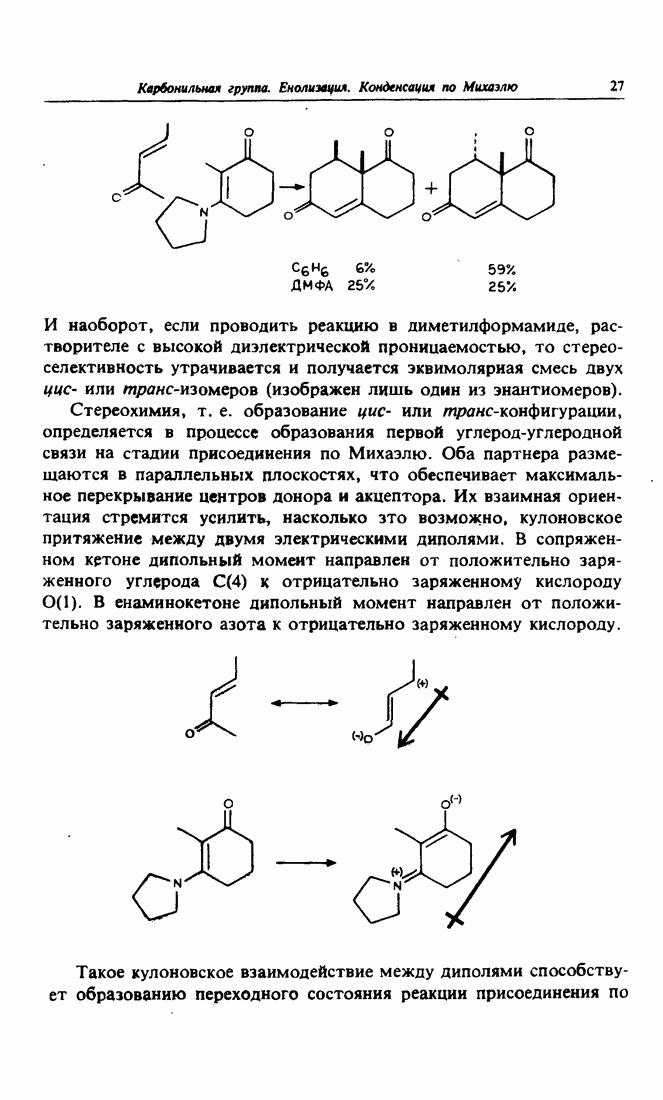
- 7. Использование реакции Михаэля в синтезе стероидов
- 8. Циклизация по Робинсону. Эффект растворителя
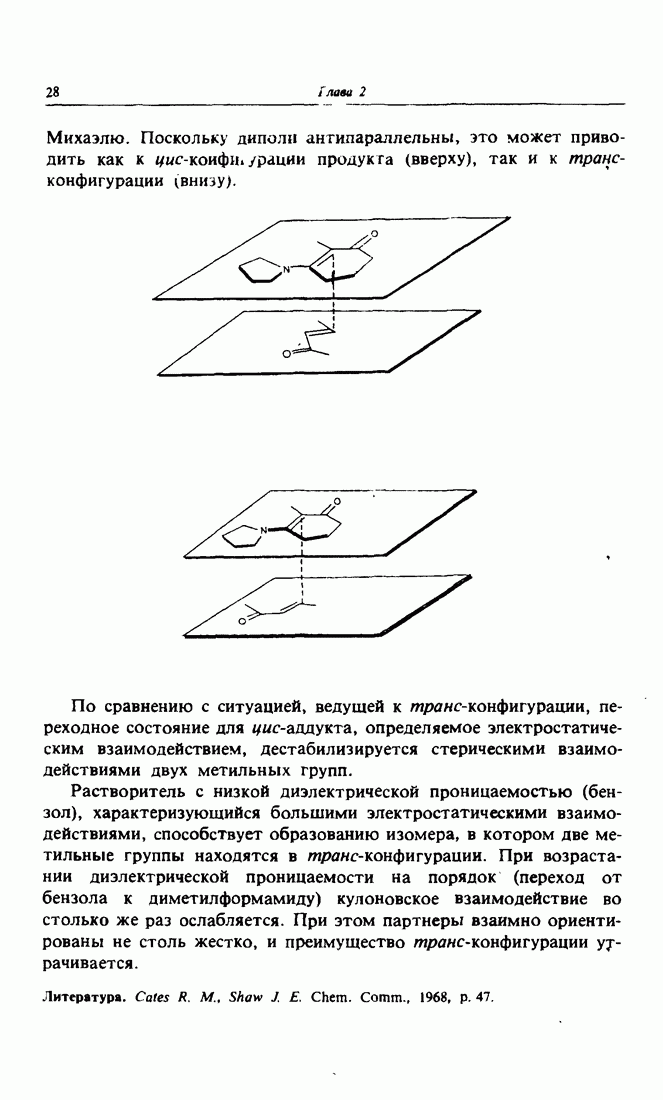
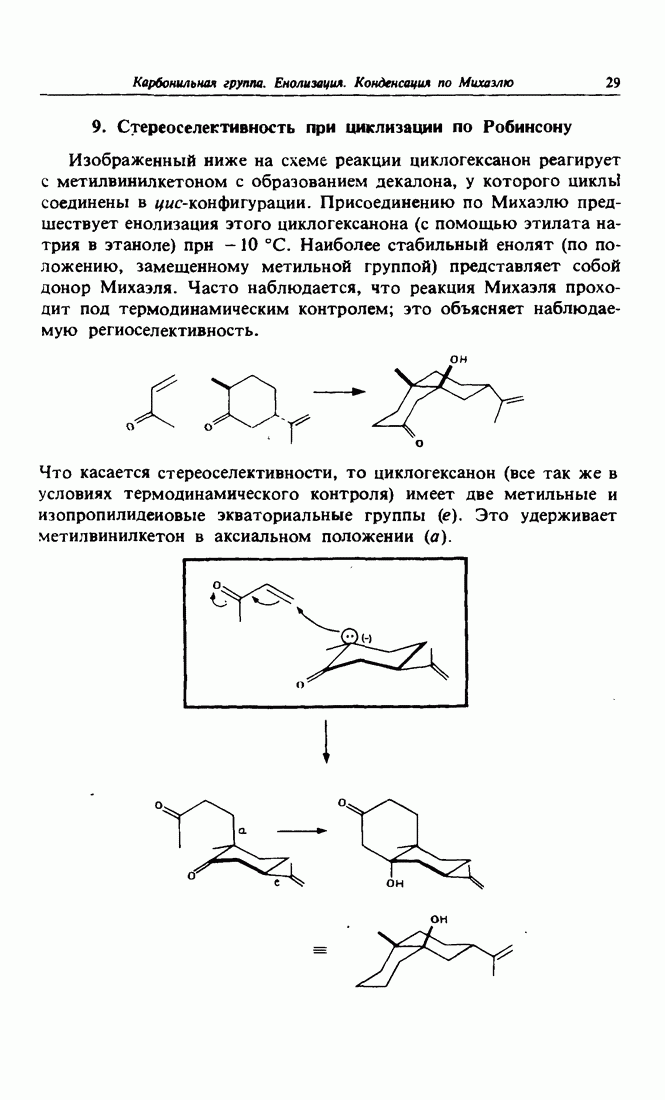
- 9. Стереоселективность при циклизации по Робинсону
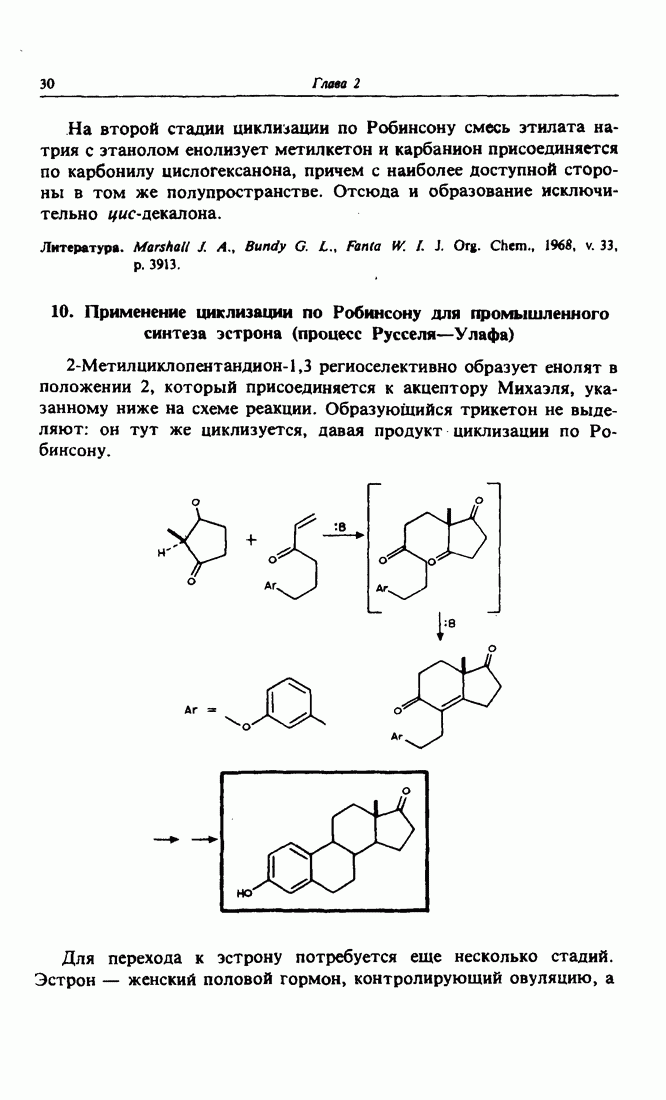
- 10. Применение циклизации по Робинсону для промышленного синтеза эстрона (процесс Русселя-Улафа)
- 11. Следы крови на церковных облатках
- Глава 3. КАРБОНИЛЬНАЯ ГРУППА. АЛЬДОЛЬНАЯ КОНДЕНСАЦИЯ
- 2. «Музыкальное родство» альдольной конденсации
- 3. Промышленные применения альдольной конденсации
- 4. Другое важное промышленное применение альдольной конденсации
- 5. Альдольная конденсация и «большие» органические синтезы
- 6. Синтез афродизиака
- 7. Альдольная конденсация и механическая прочность сухожилий
- 8. Важные химические продукты. Винилацетат
- 9. Недостаток тиамина и синдром Корсакова
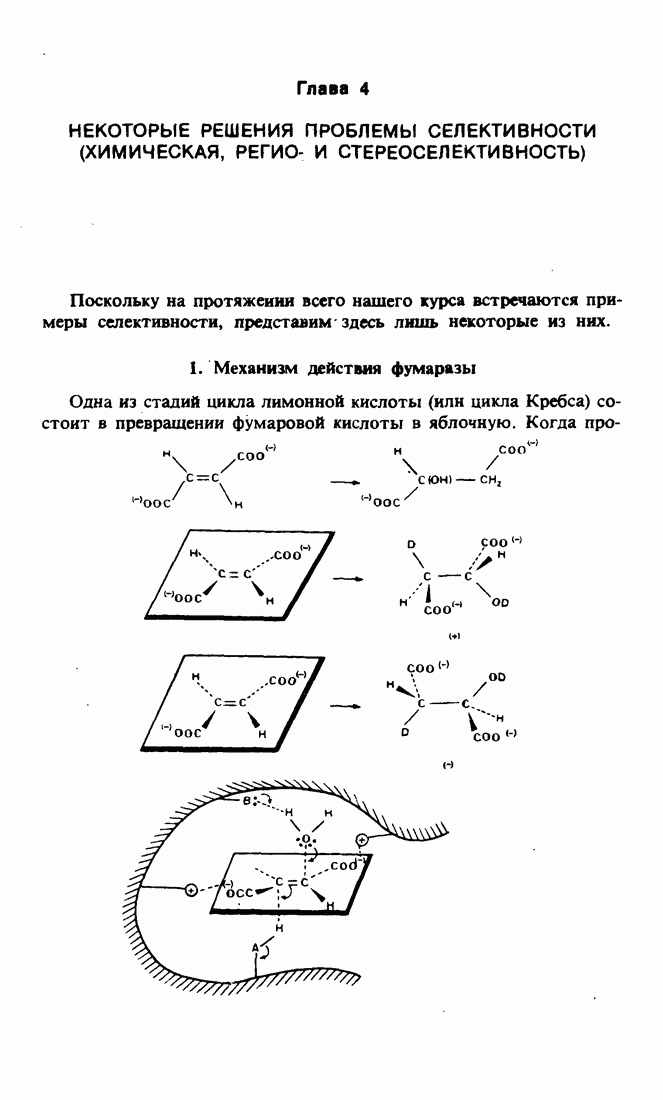
- Глава 4. НЕКОТОРЫЕ РЕШЕНИЯ ПРОБЛЕМЫ СЕЛЕКТИВНОСТИ (ХИМИЧЕСКАЯ, РЕГИО- И СТЕРЕОСЕЛЕКТИВНОСТЬ)
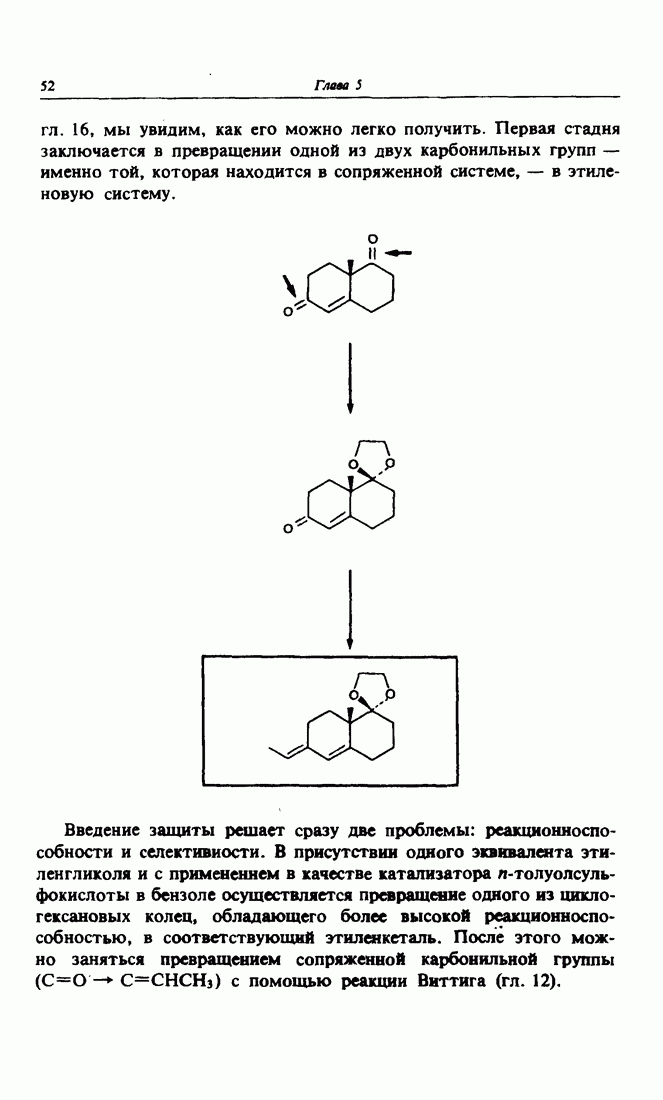
- Глава 5. ЗАЩИТА И РЕГЕНЕРАЦИЯ ФУНКЦИОНАЛЬНЫХ ГРУПП. СПИРТОВАЯ И КАРБОНИЛЬНАЯ ГРУППЫ, ОБРАЩЕНИЕ ПОЛЯРНОСТИ
- 1. Нуклеофильное замещение в молекуле с реакционноспособной карбонильной группой
- 2. Начало синтеза лонгифолена по Кори
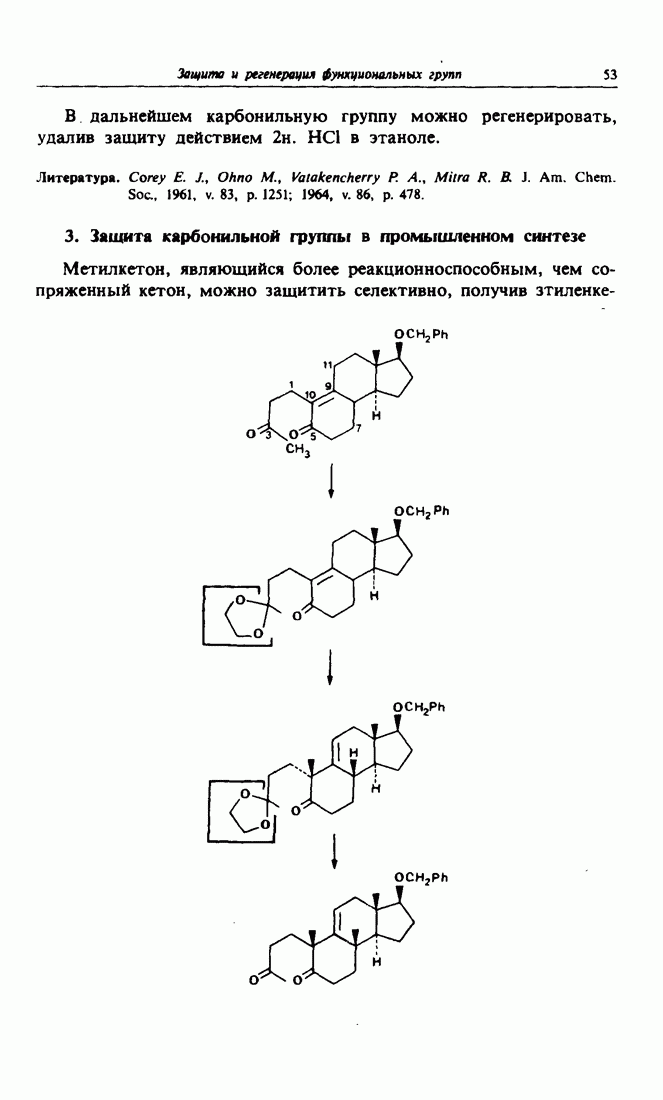
- 3. Защита карбонильной группы в промышленном синтезе
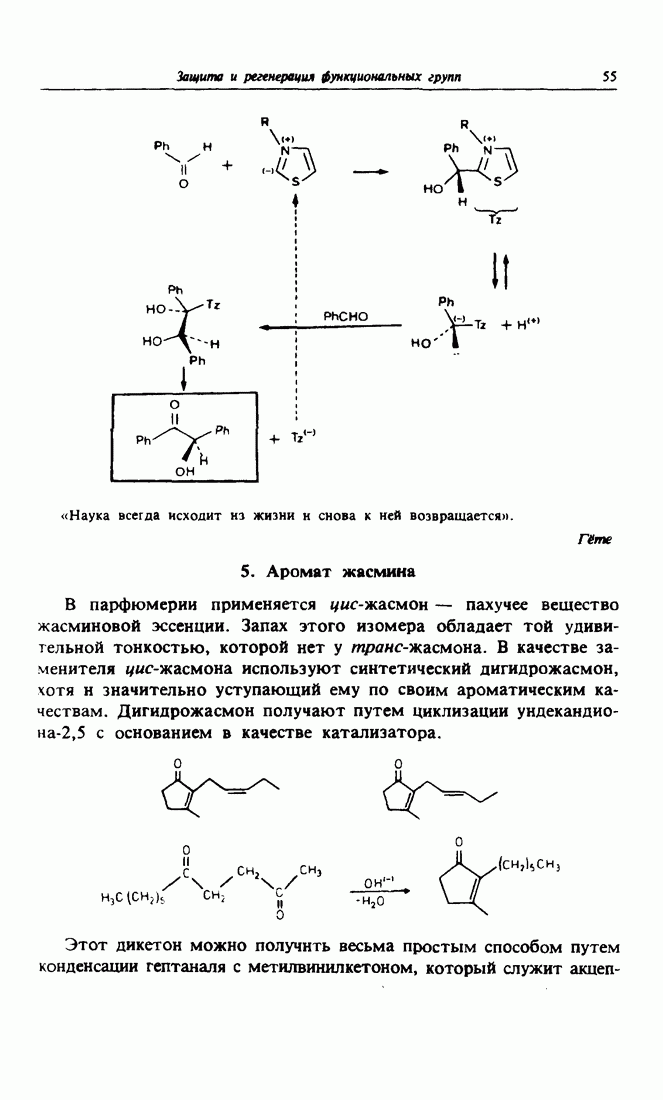
- 4. Механизм ферментативного образования ацетоина
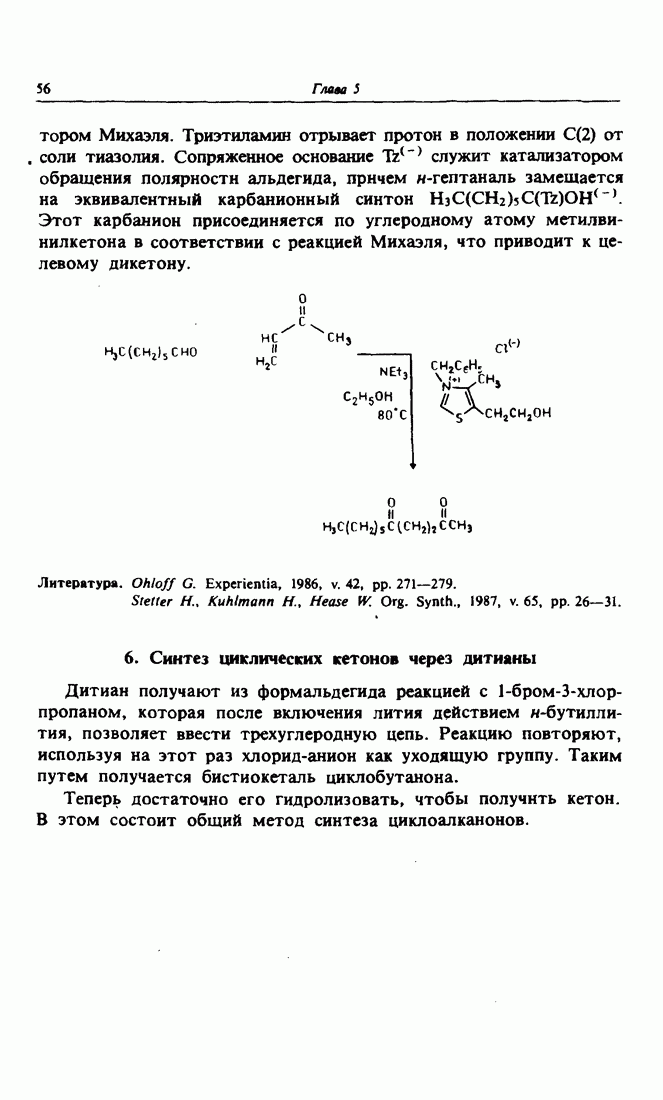
- 5. Аромат жасмина
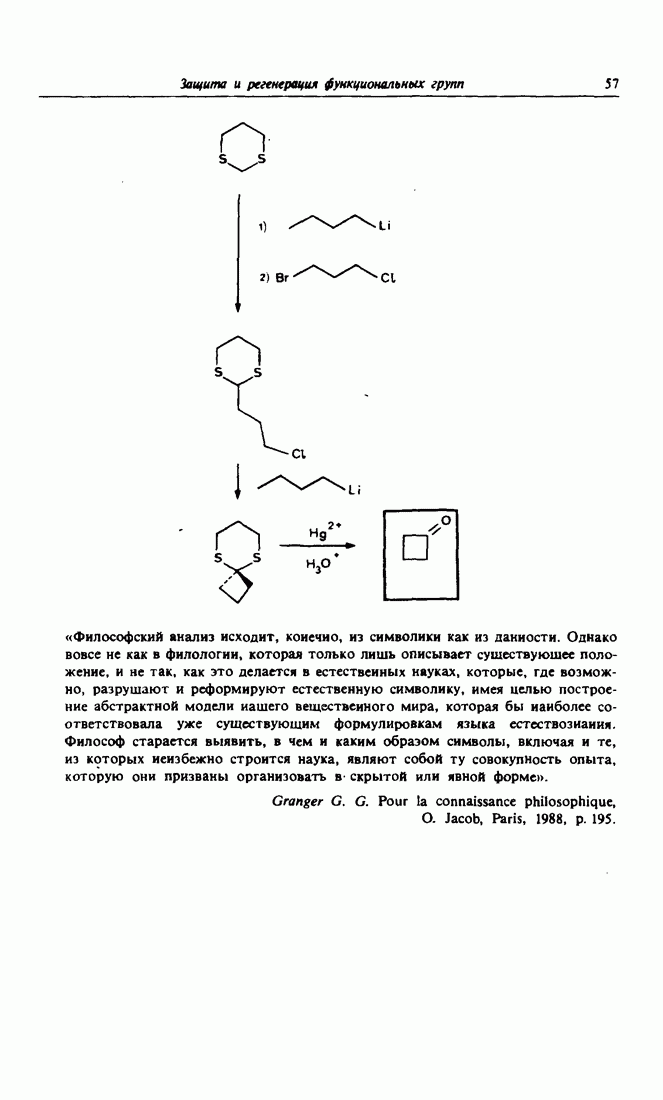
- 6. Синтез циклических кетонов через дитианы
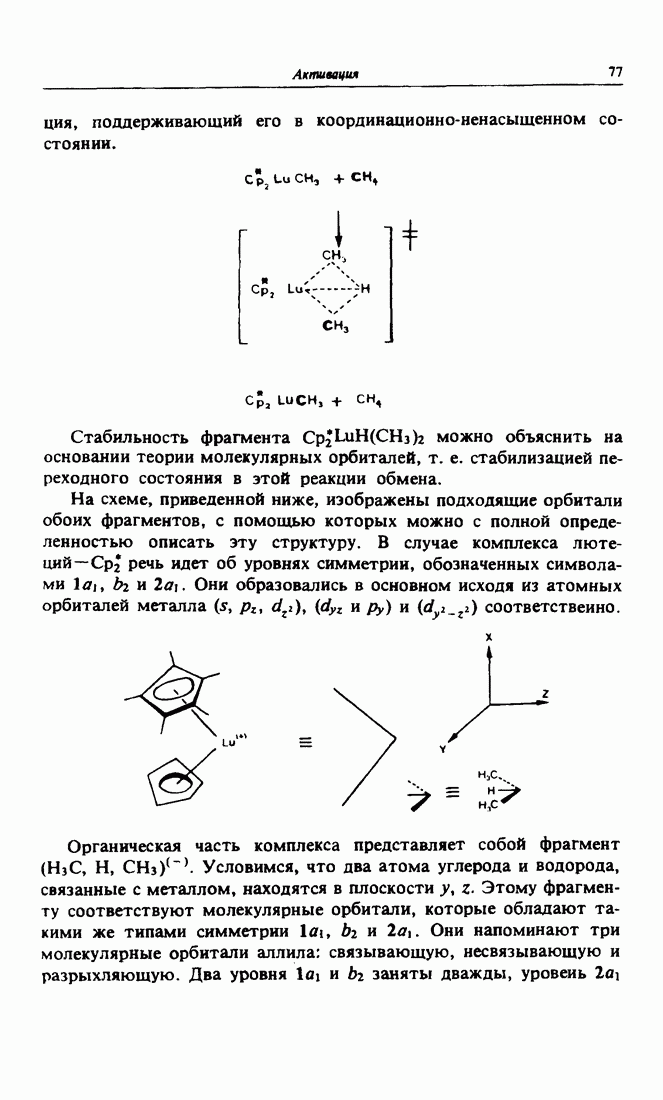
- Глава 6. АКТИВАЦИЯ
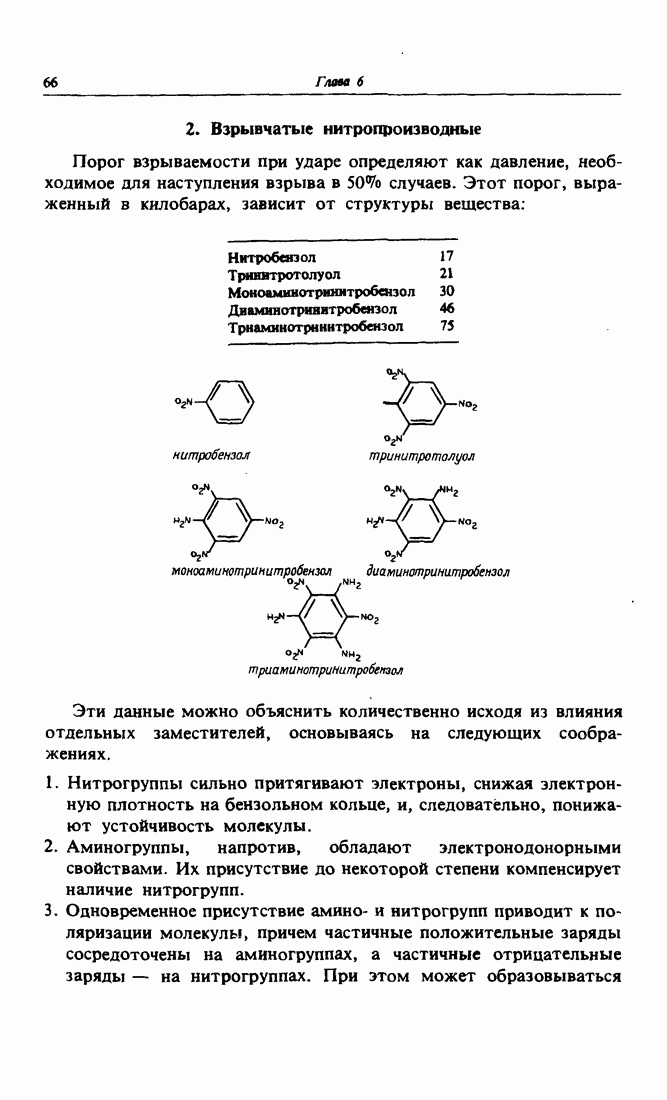
- 2. Взрывчатые нитропроизводные
- 3. Дестабилизация исходного состояния. Катализ путем фазового переноса
- 4. Биолюминесценция или средства общения в мире безмолвия
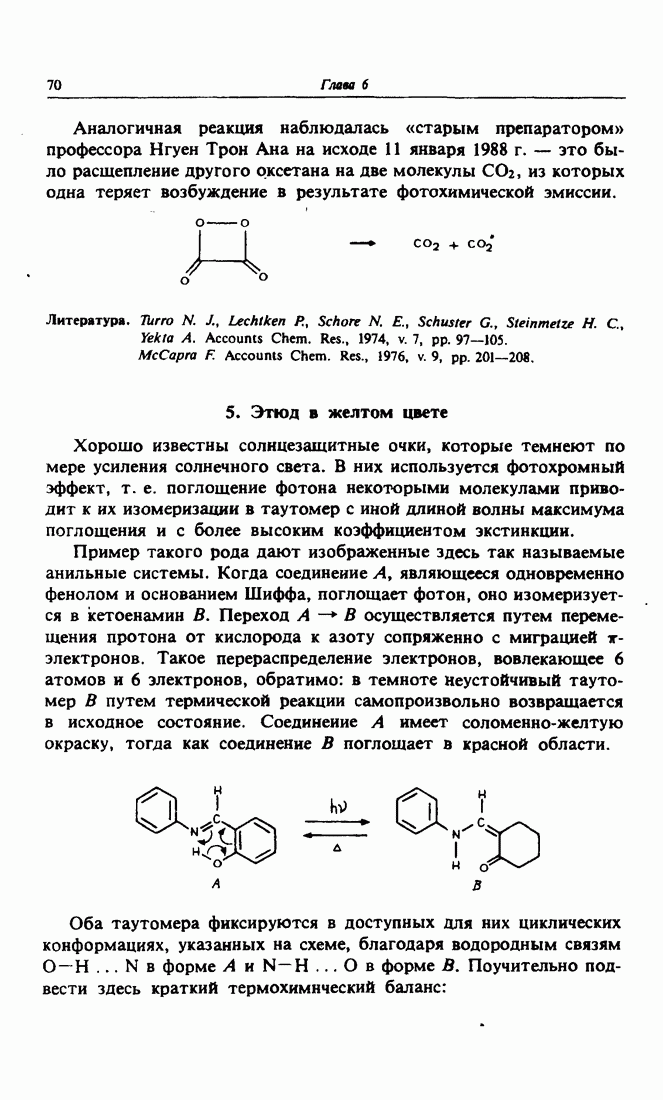
- 5. Этюд в желтом цвете
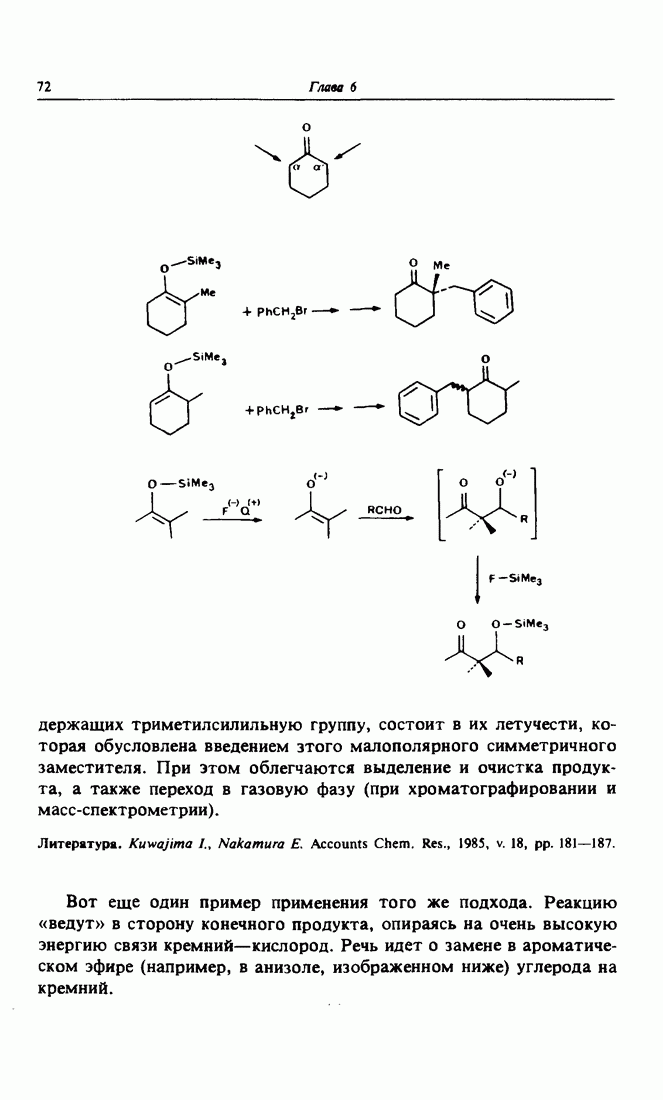
- 6. Стабилизация конечного состояния. Силилированные эфиры фенолов
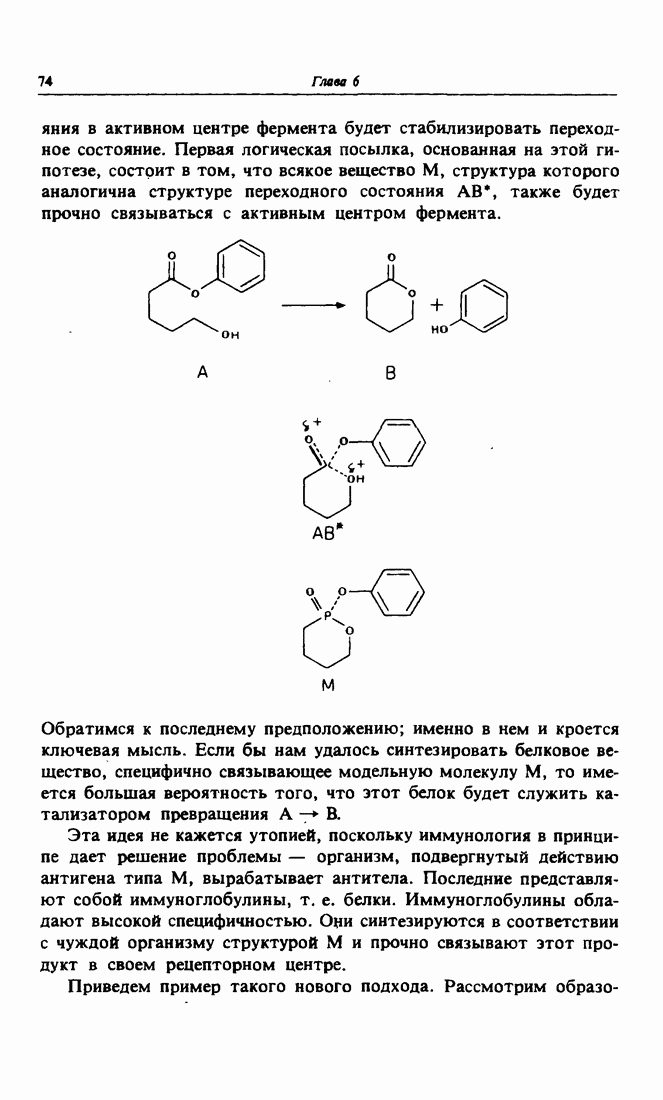
- 7. Биокаталиэ органических реакций
- 8. Активация насыщенных углеводородов
- Глава 7. ПОСТРОЕНИЕ ЦИКЛОВ
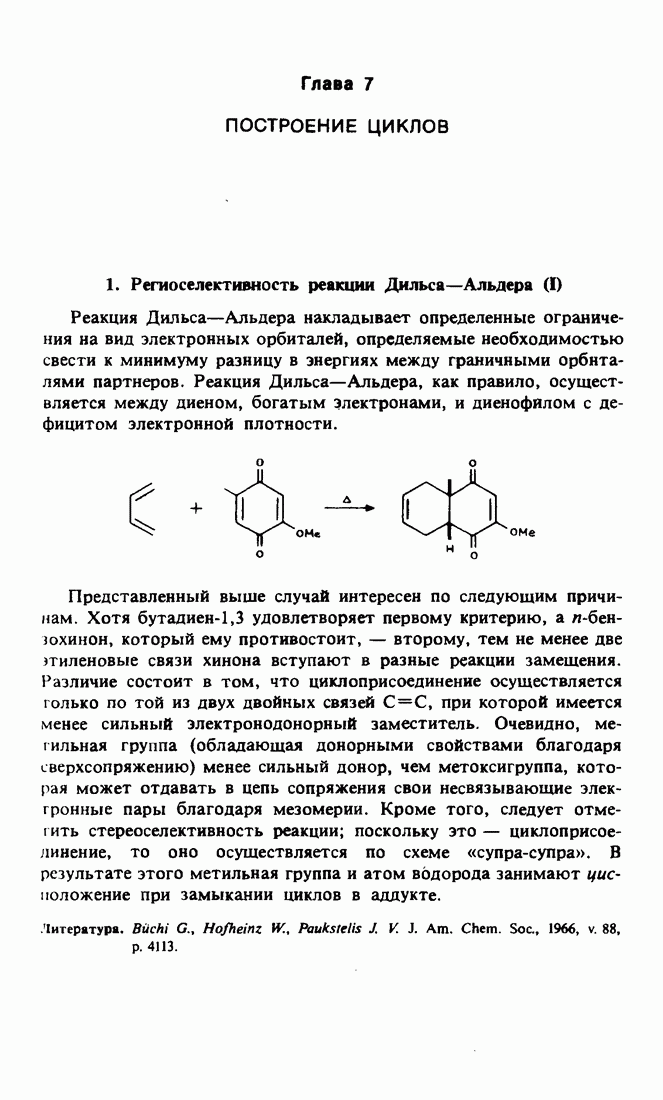
- 1. Региоселективность реакции Дильса-Альдера (I)
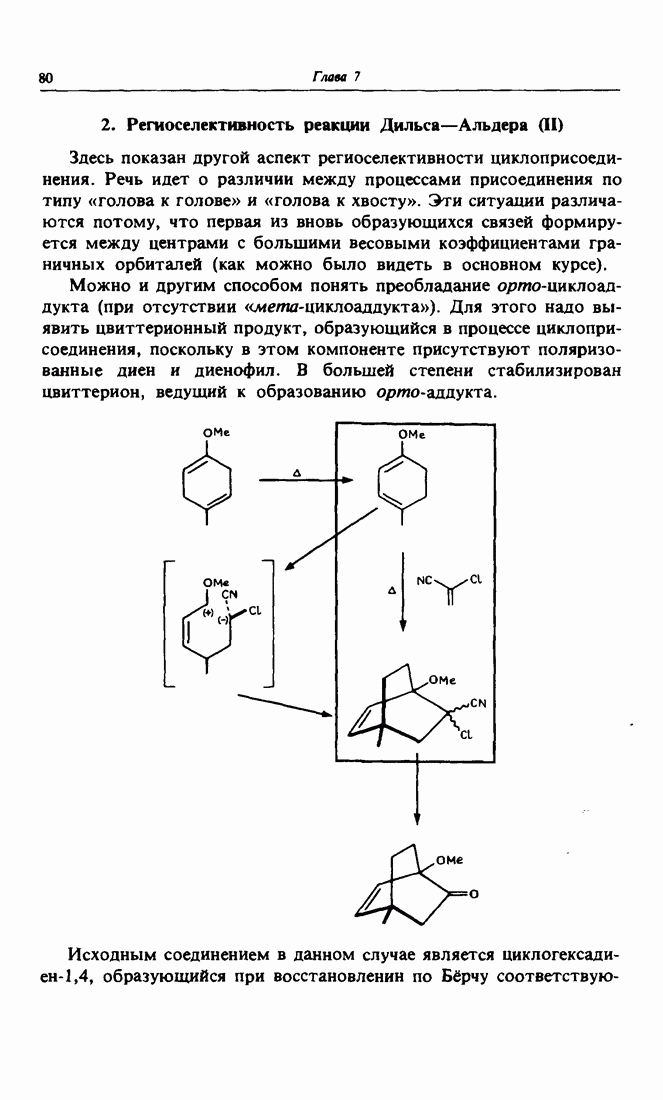
- 2. Региоселективность реакции Дильса-Альдера (II)
- 3. Диенофилы, активированные благодаря напряжению в цикле
- 4. Синтез Дильса-Альдера с раскрытием цикла в аддукте
- 5. Синтетическое значение двух последовательных реакций Дильса-Альдера
- 6. Стадия синтеза морфина
- 7. Другие применения реакции Дильса-Альдера в больших синтезах
- 8. Стереохимический контроль реакции Дильса-Альдера
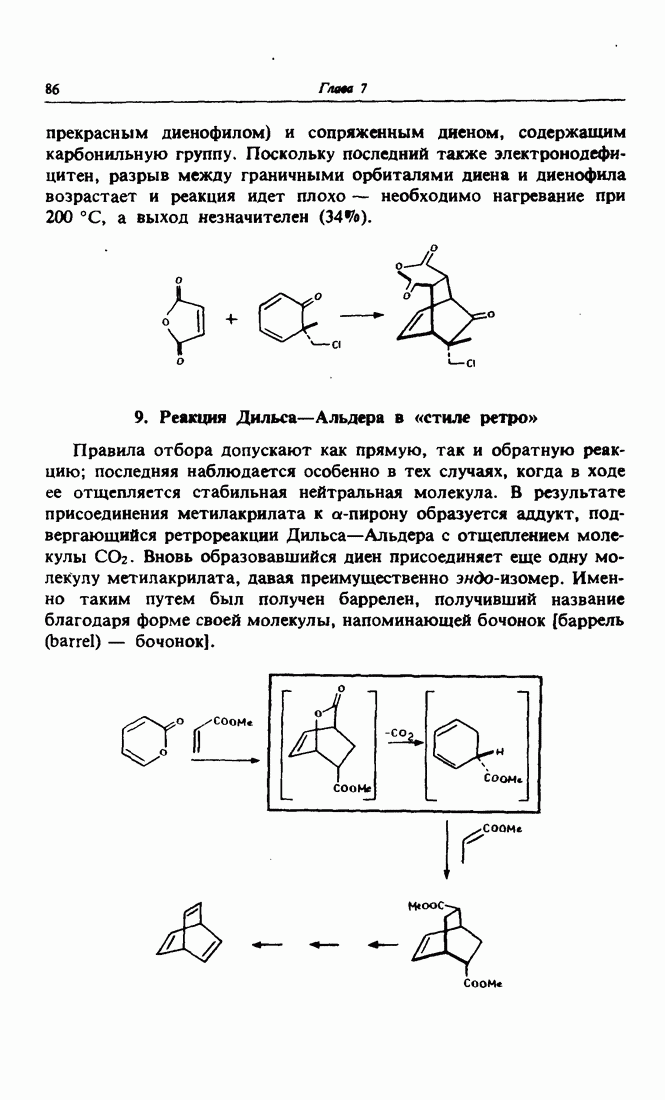
- 9. Реакция Дильса-Альдера в «стиле ретро»
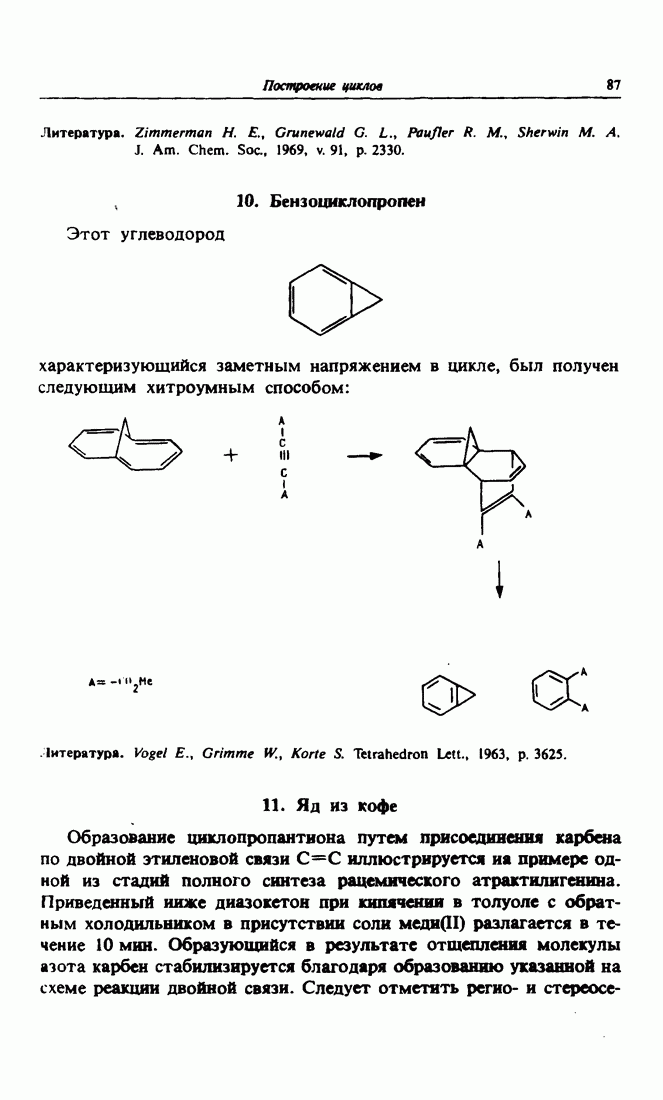
- 10. Бензоциклопропен
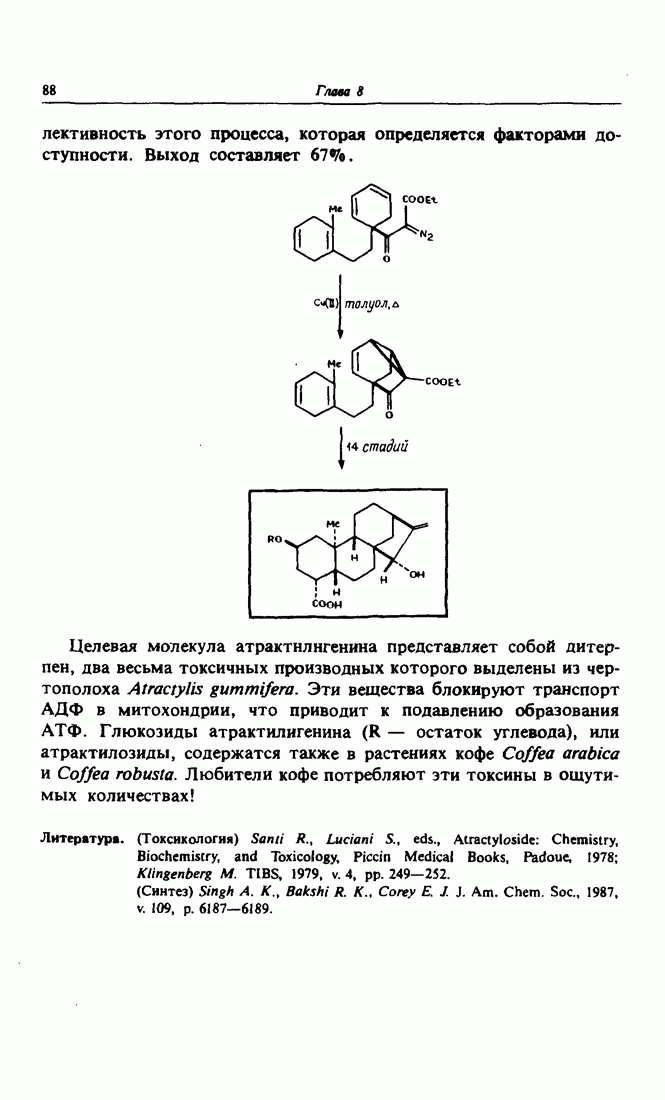
- 11. Яд из кофе
- Глава 8. ВВЕДЕНИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП. РЕАКЦИИ ЗАМЕЩЕНИЯ
- 1. Удлинение углеродной цепи
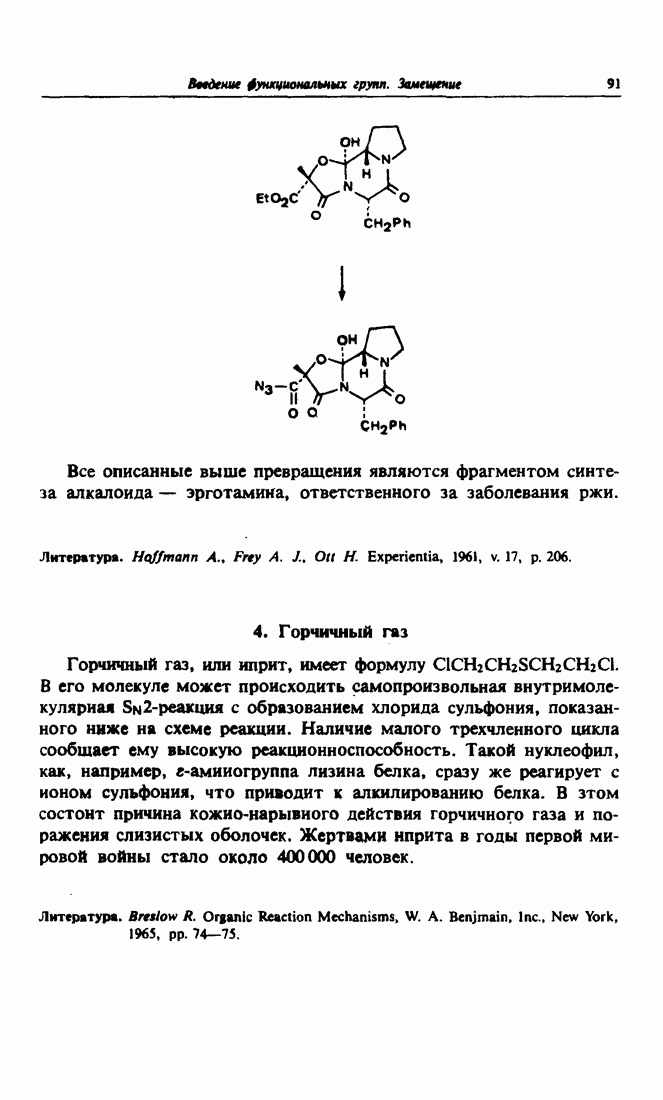
- 2. Начало синтеза яда
- 3. Активация карбонильной группы путем замещения
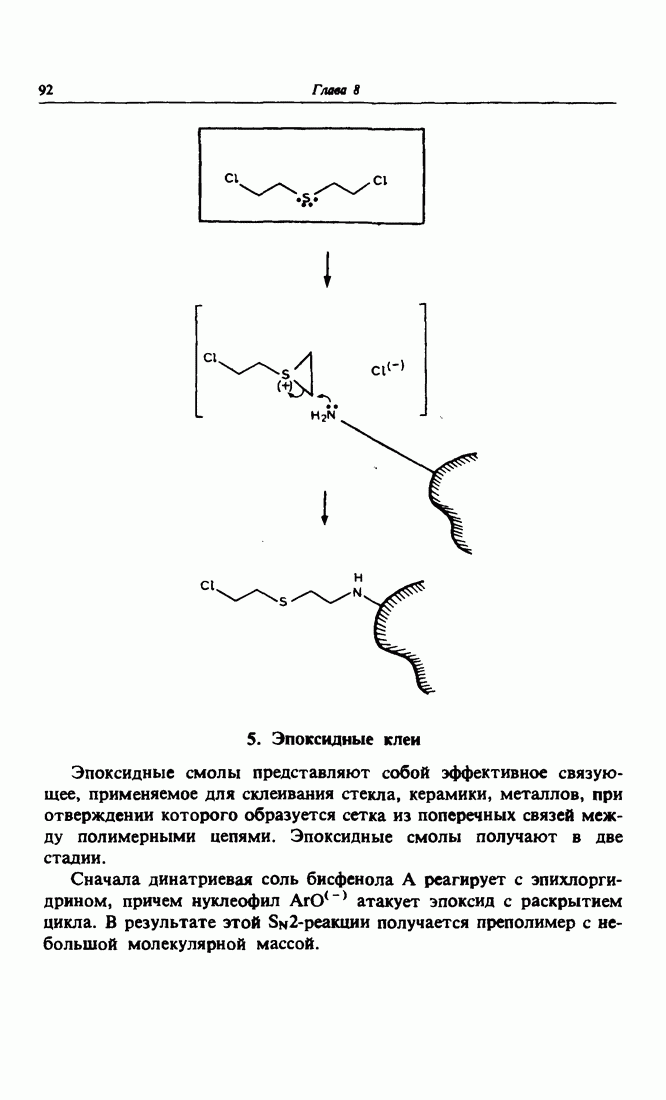
- 4. Горчичный газ
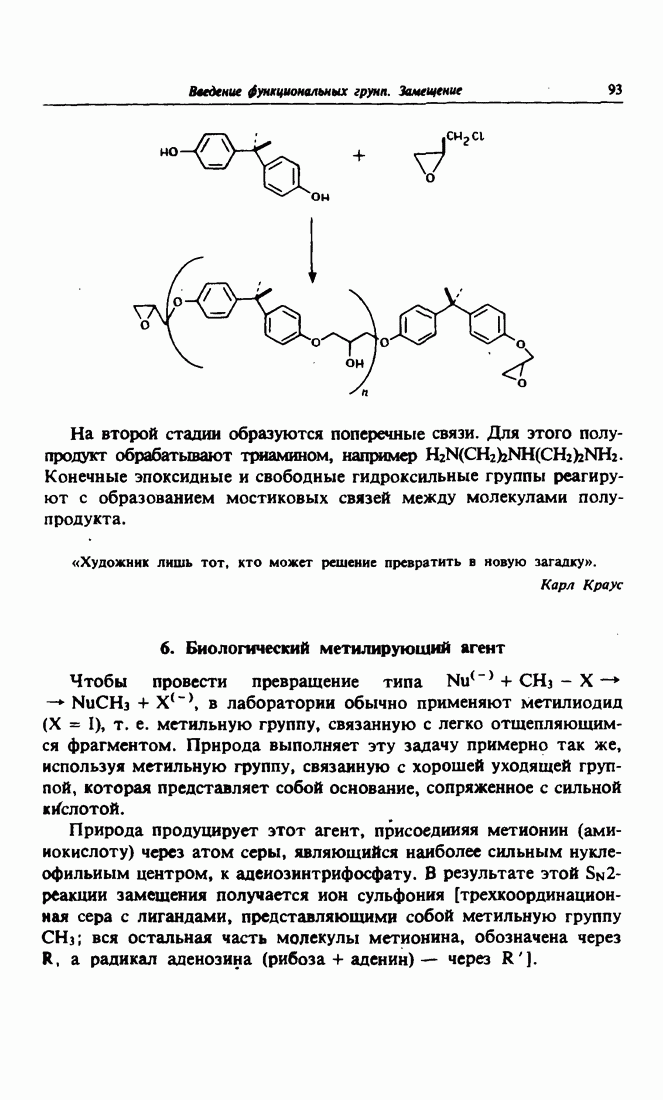
- 5. Эпоксидные клеи
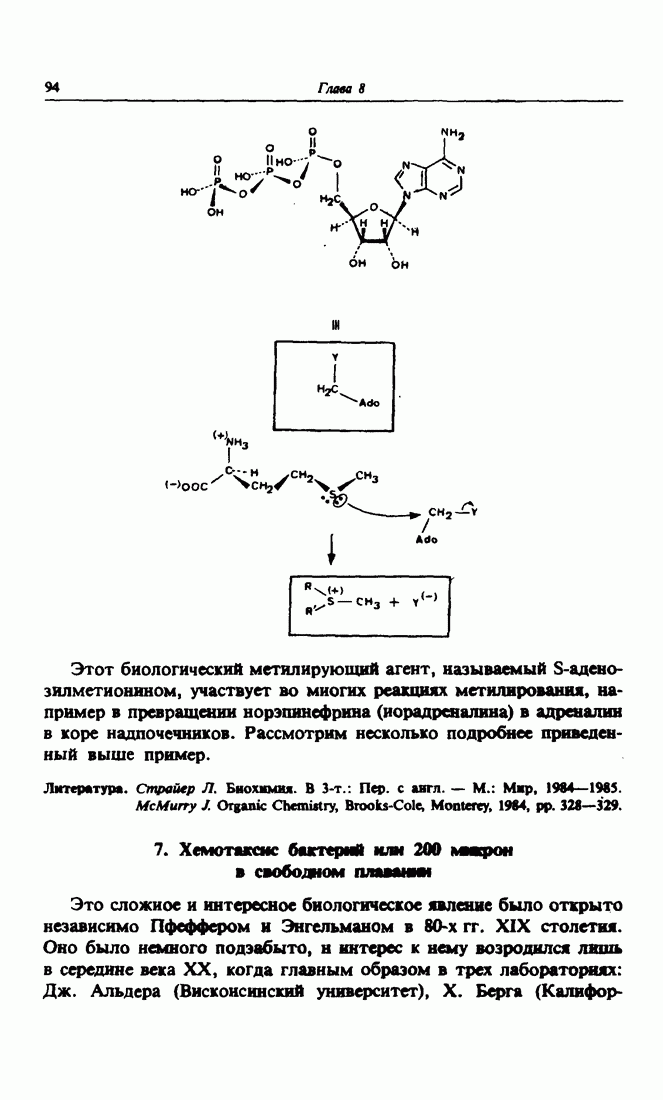
- 6. Биологический метилирующий агент
- 7. Хемотаксис бактерий или 200 мирон в свободном плавании
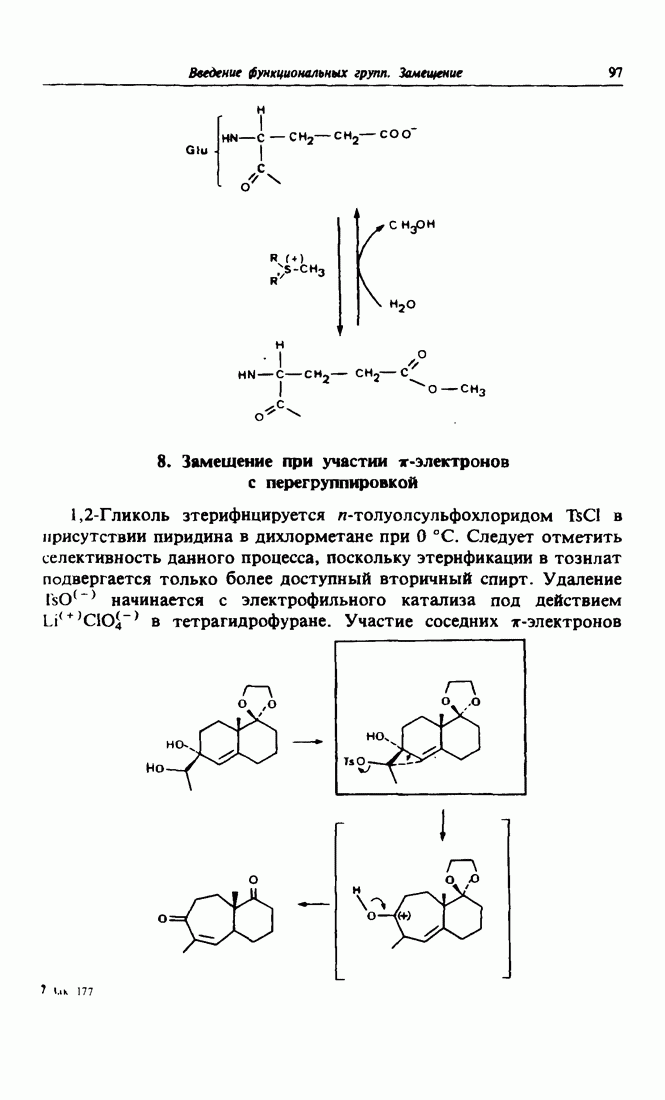
- 8. Замещение при участии «пи»-электронов с перегруппировкой
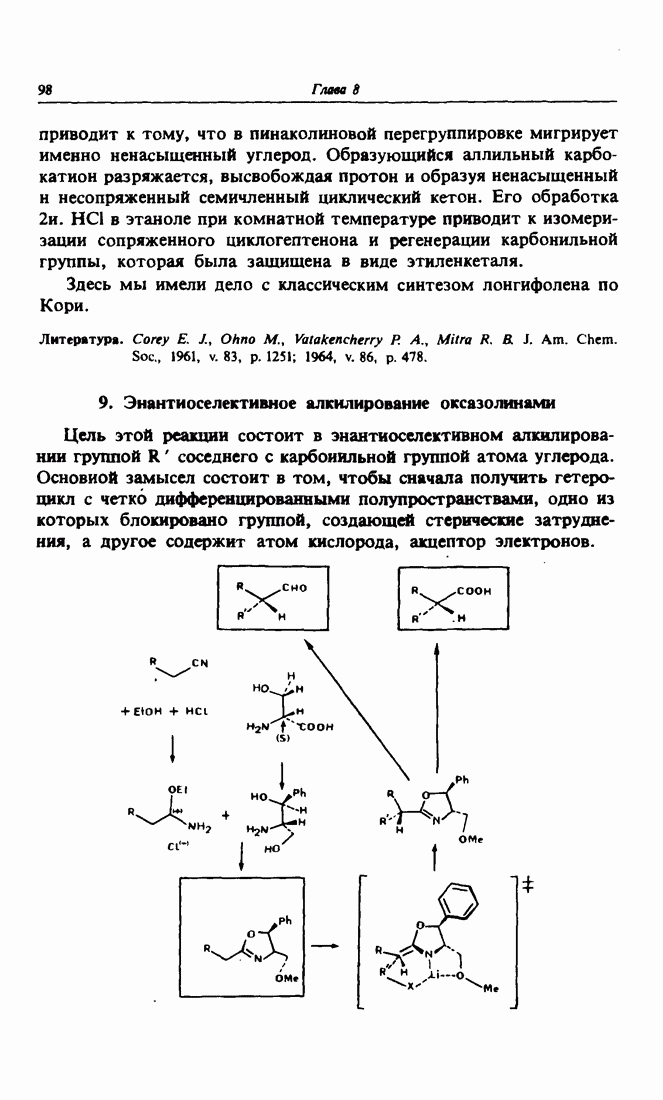
- 9. Энантиоселективное алкилирование оксазолинами
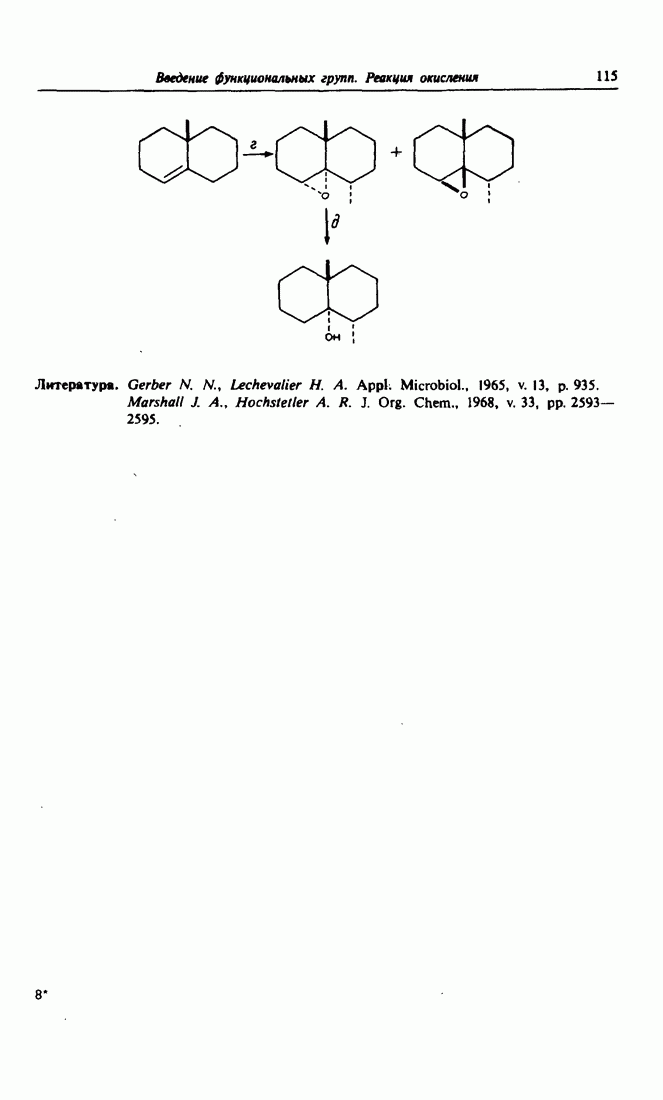
- Глава 9. ВВЕДЕНИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП. РЕАКЦИИ ОКИСЛЕНИЯ
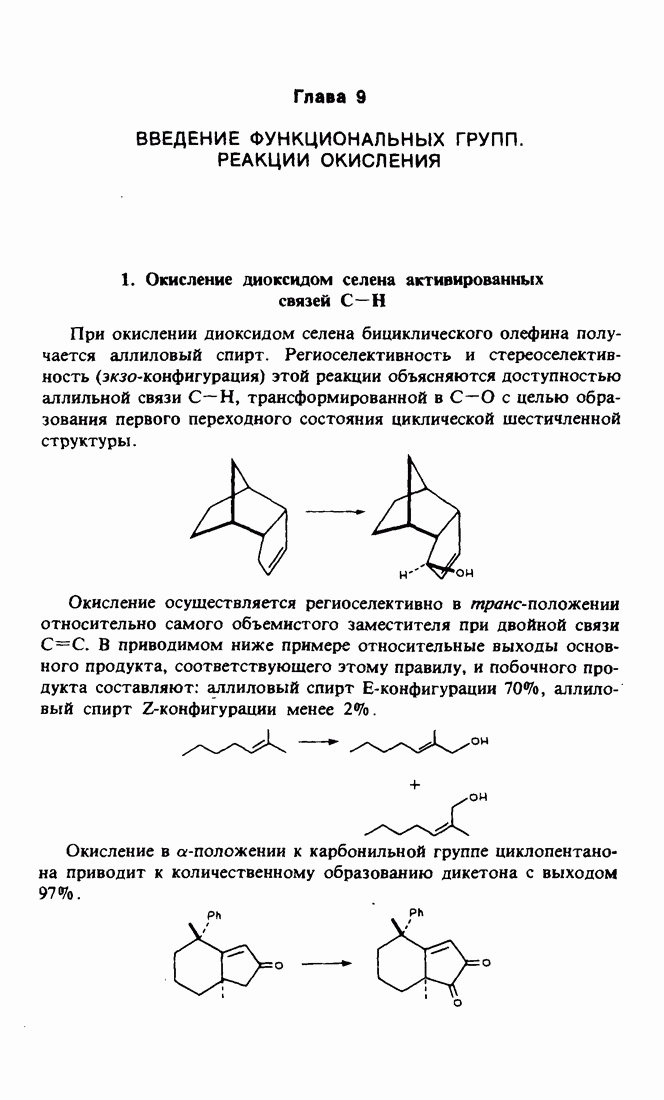
- 1. Окисление диоксидом селена активированных связей C-H
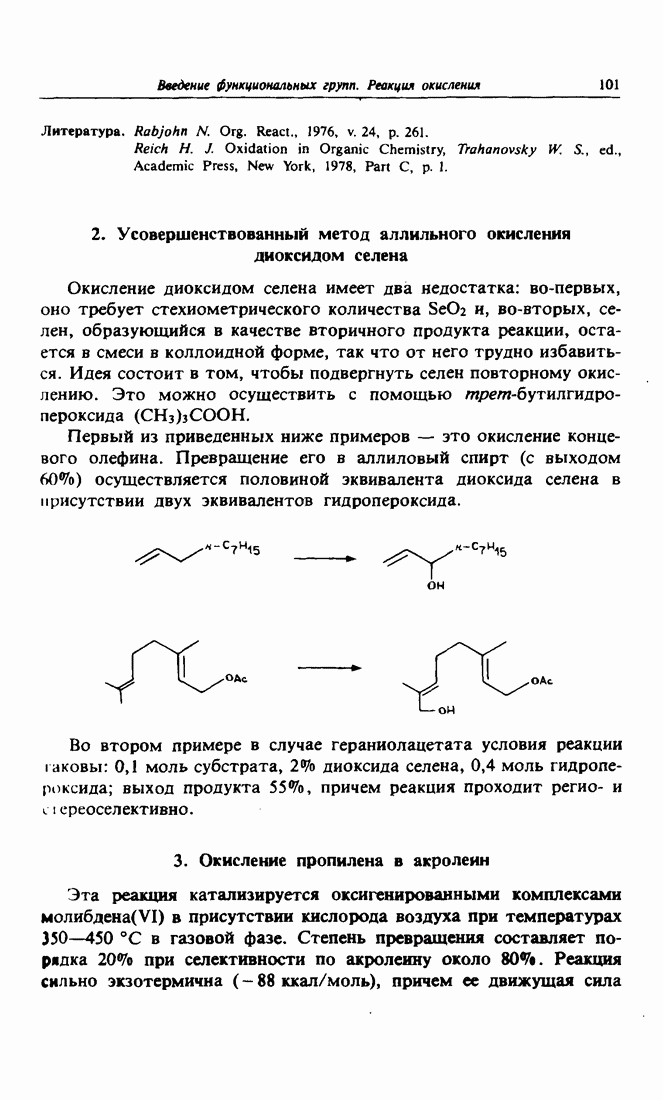
- 2. Усовершенствованный метод аллильного окисления диоксидом селена
- 3. Окисление пропилена в акролеин
- 4. Окисление этилена в этиленоксид
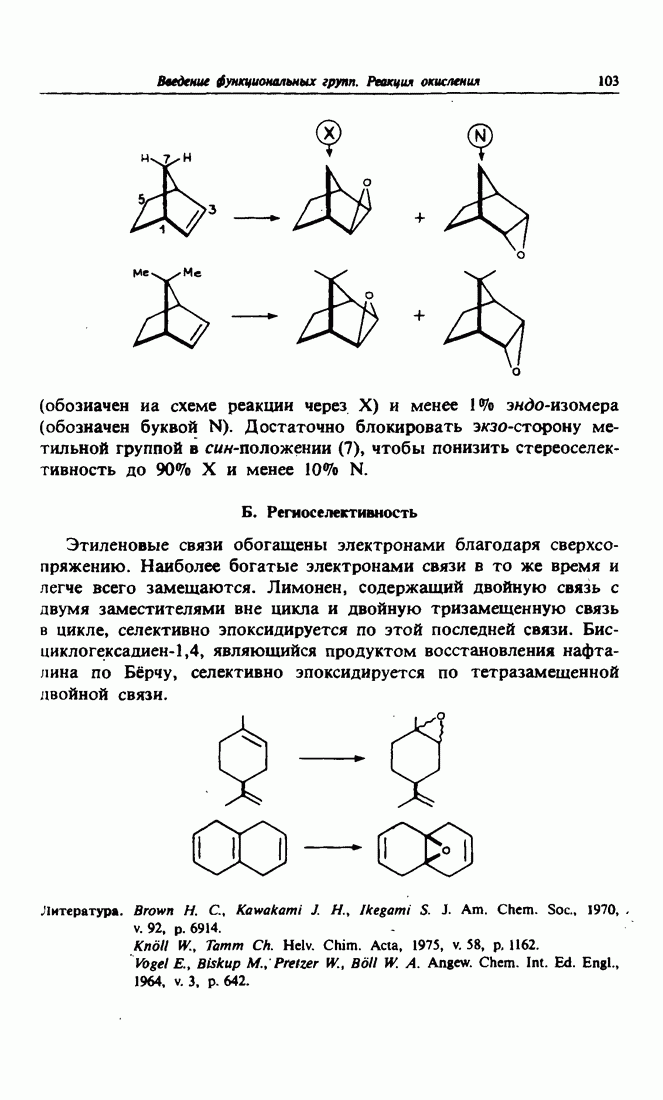
- 5. Селективность при эпоксидировании
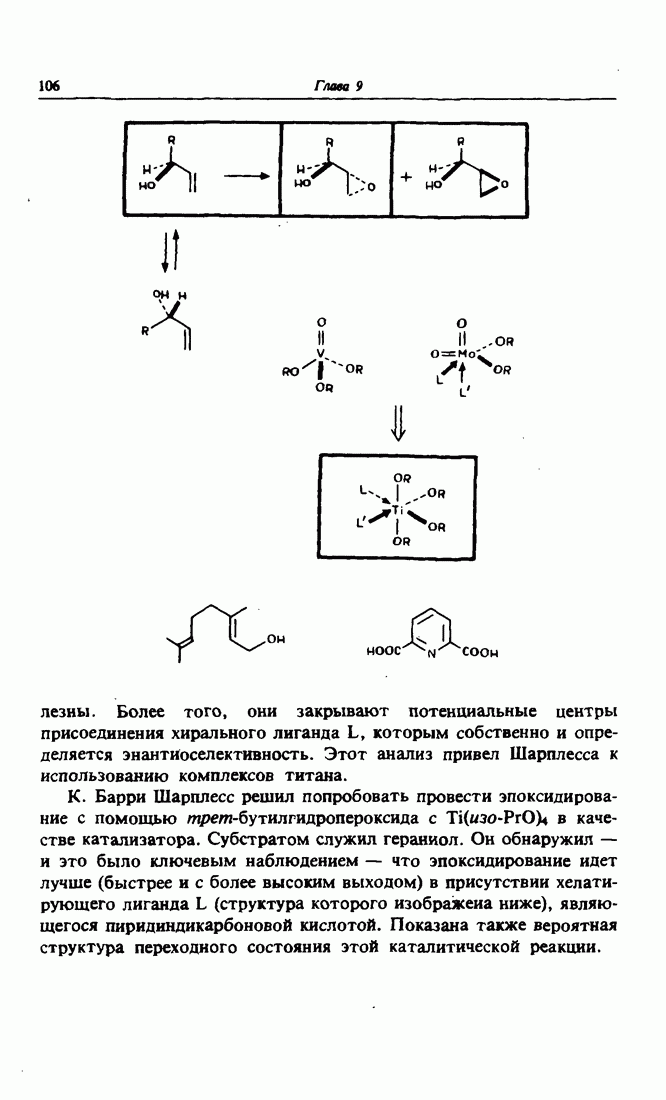
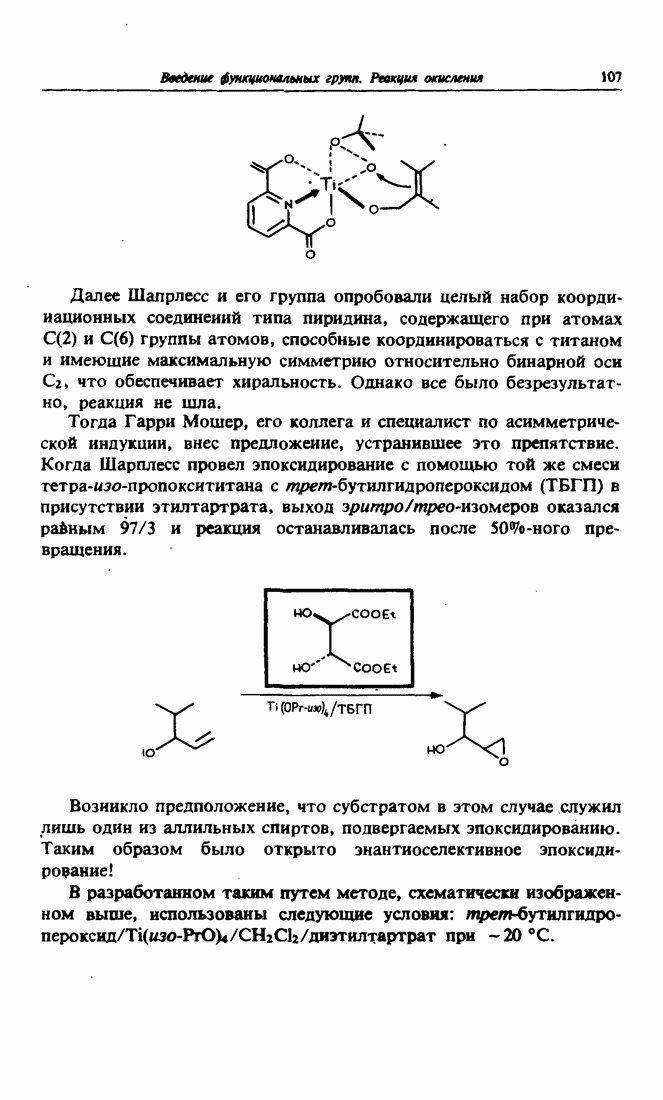
- 6. Энантиоселективное эпоксндирование по Шарплессу
- 7. Селективность оэонолиэа
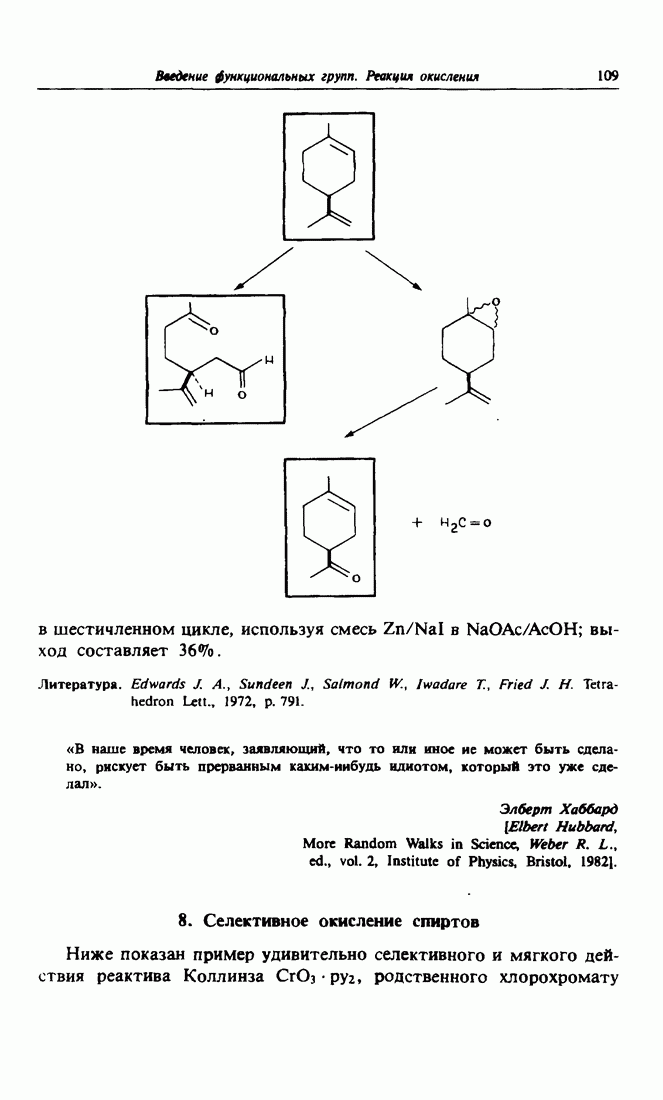
- 8. Селективное окисление спиртов
- 9. Биологическое окисление спиртов
- 10. И фермент может встретиться с затруднениями
- 11. Образование уксусного альдегида путем окисления этилена
- 12. Привкус земли
- Глава 10. ВВЕДЕНИЕ ФУНКЦИОНАЛЬНЫХ ГРУПП. РЕАКЦИИ ВОССТАНОВЛЕНИЯ
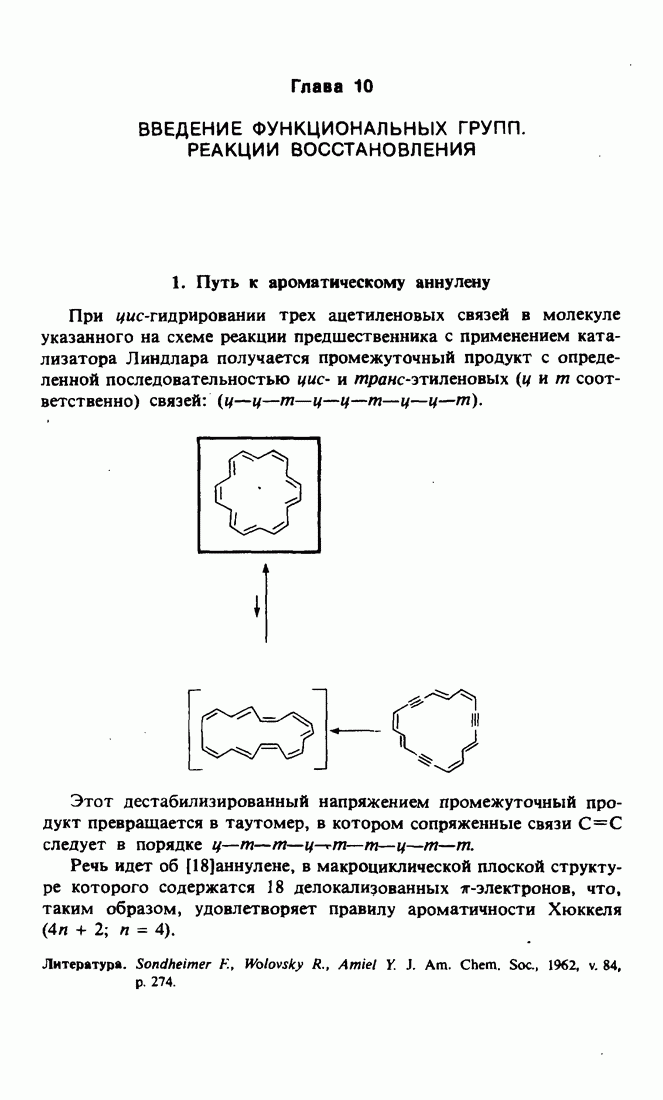
- 1. Путь к ароматическому аннулену
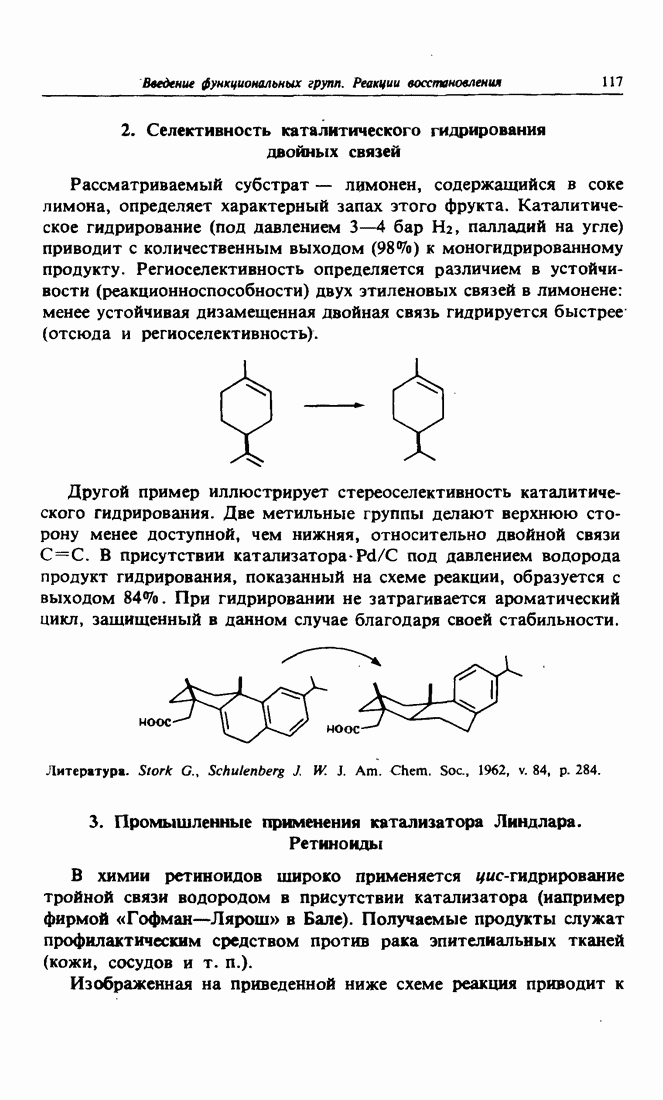
- 2. Селективность каталитического гидрирования двойных связей
- 3. Промышленные применения катализатора Линдлара. Ретиноиды
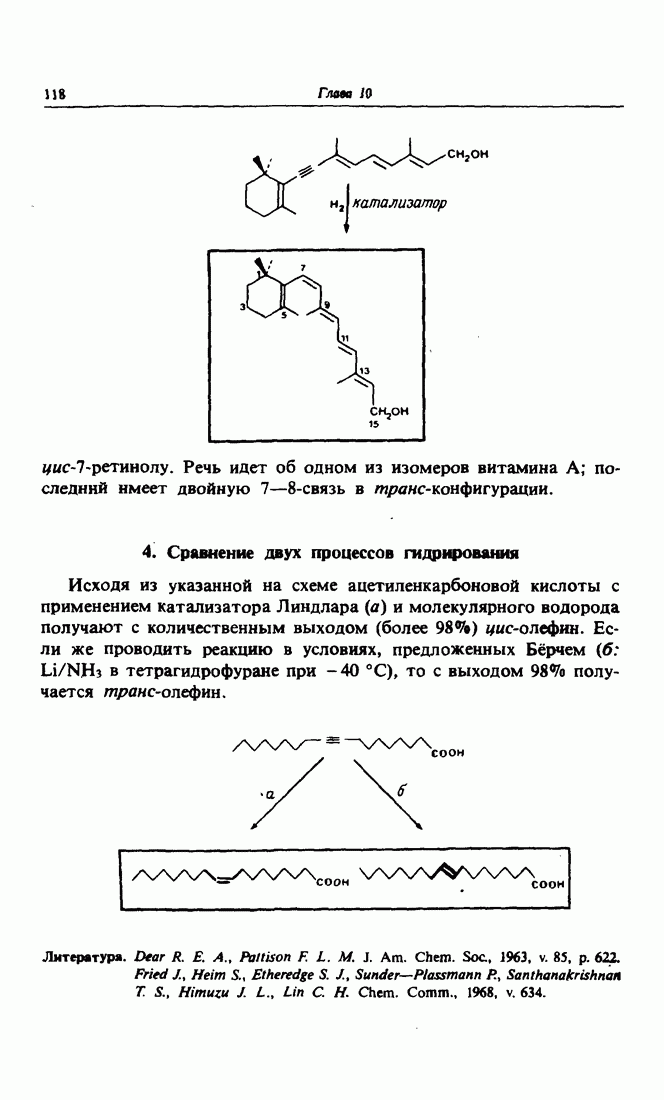
- 4. Сравнение двух процессов гидрирования
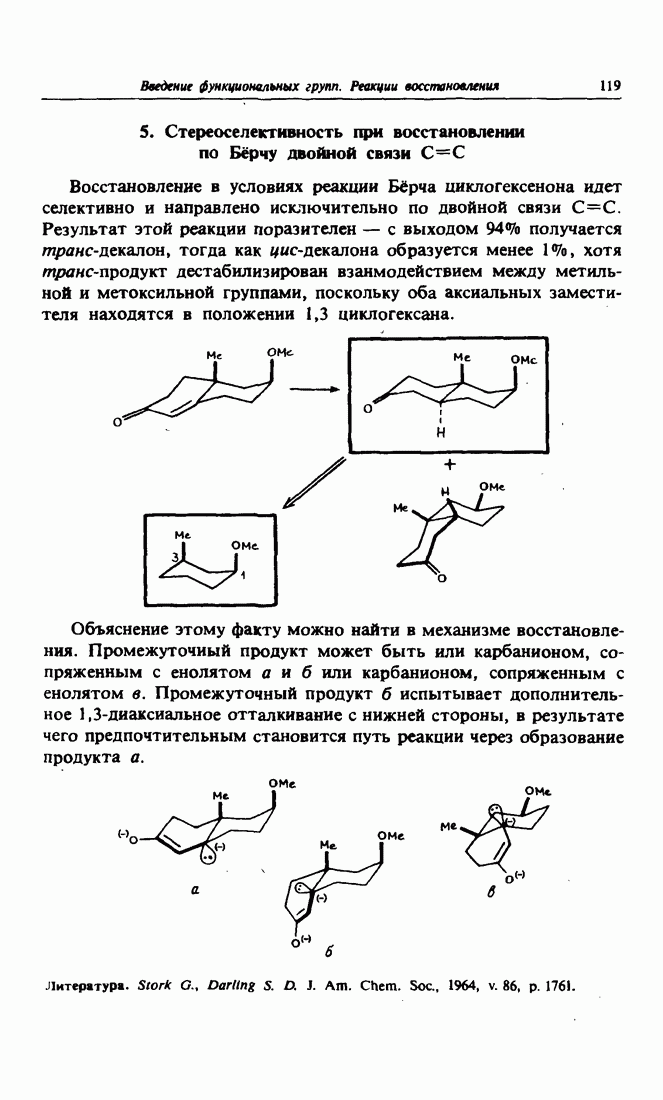
- 5. Стереоселективность при восстановлении по Бёрчу двойной связи С=С
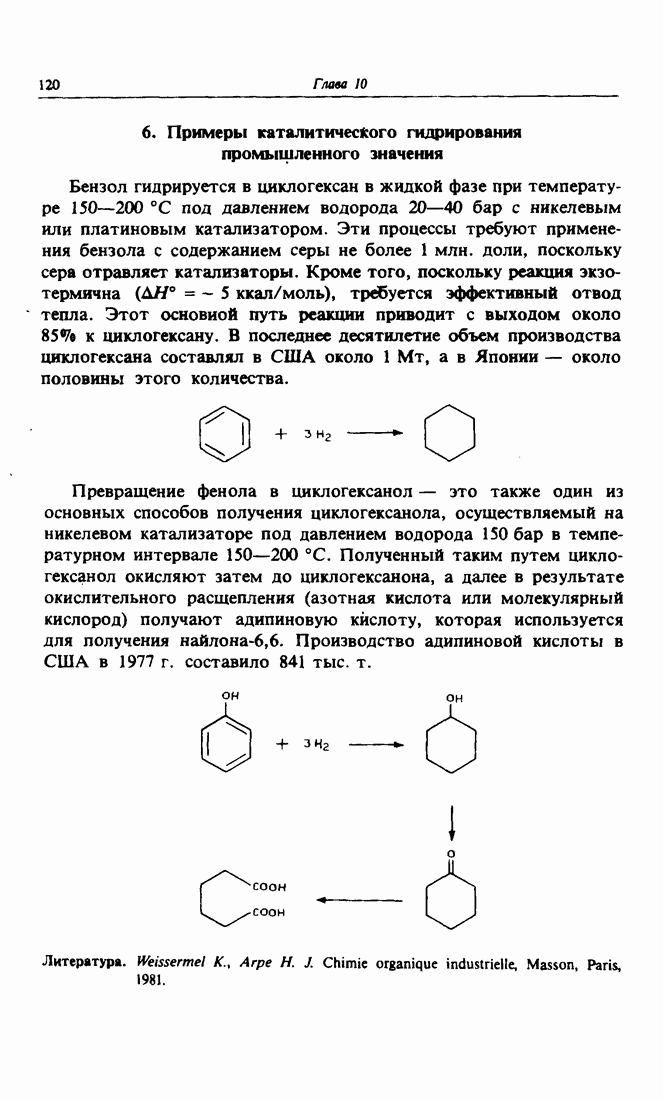
- 6. Примеры каталитического гидрирования промышленного значения
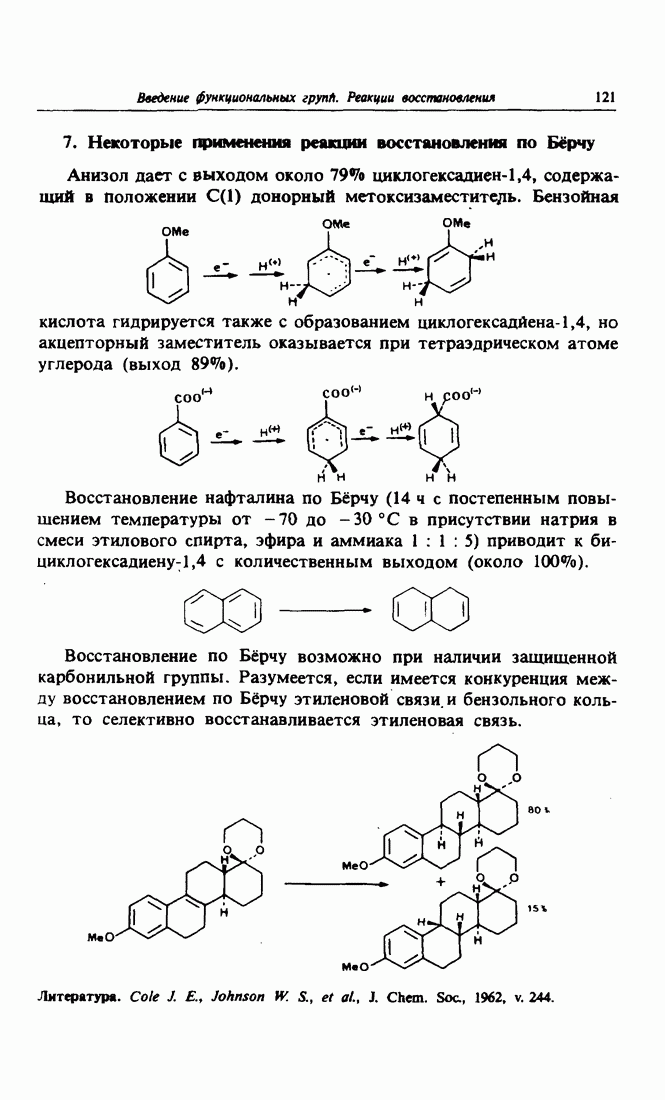
- 7. Некоторые применения реакции восстановления по Бёрчу
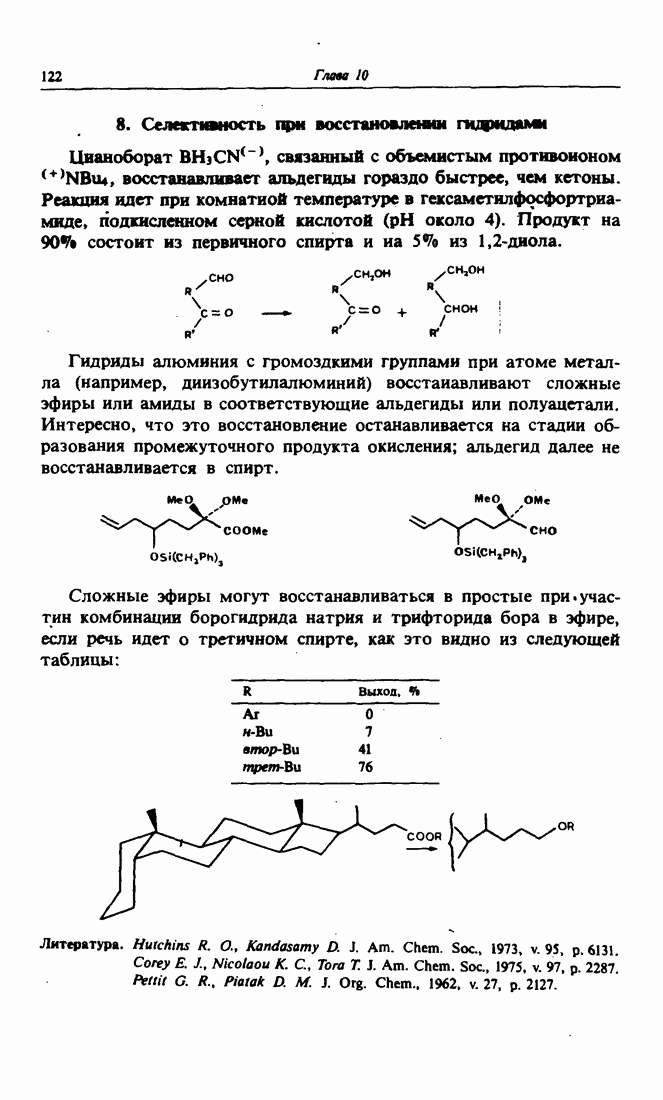
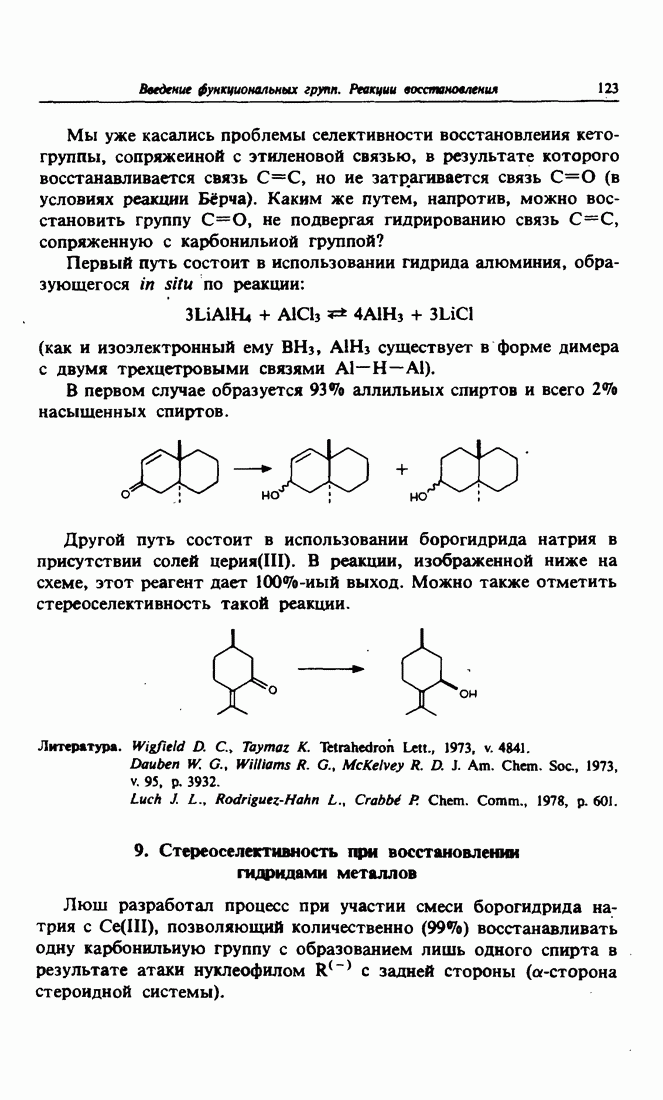
- 8. Селективность при восстановлении гидридами
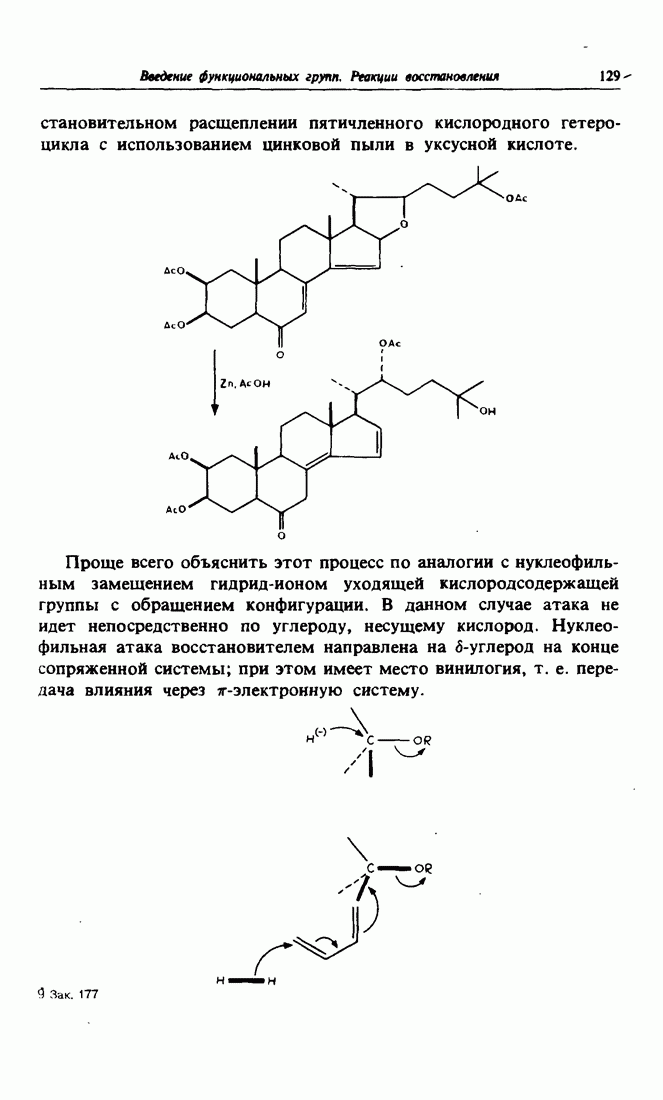
- 9. Стереоселективность при восстановлении гидридами металлов
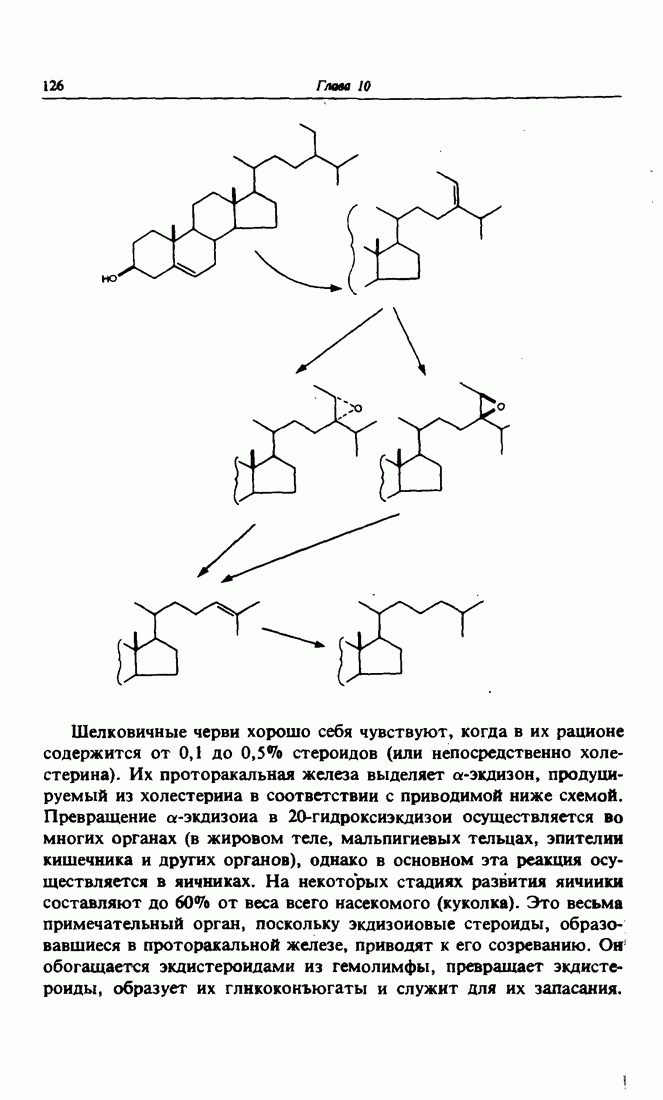
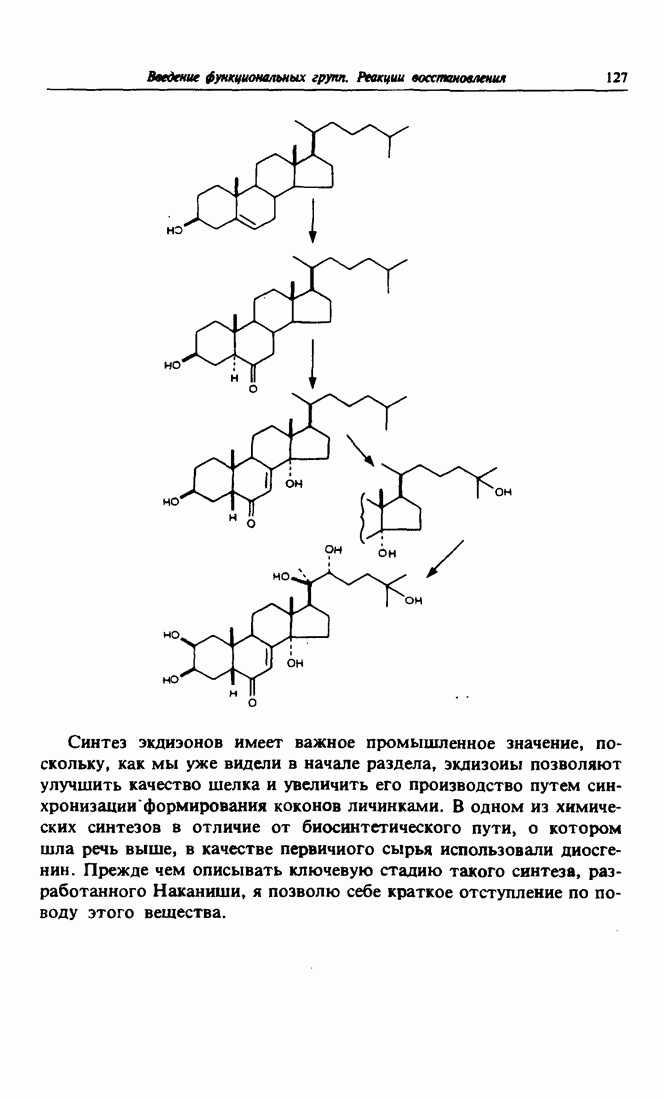
- 10. Как повысить продуктивность шелковичных червей
- Глава 11. РЕАКЦИИ ПРИСОЕДИНЕНИЯ И ЭЛИМИНИРОВАНИЯ
- 1. Полиэтилен
- 2. Некоторые промышленные реакции присоединения к этилену
- 3. Рынок пластмасс
- 4. Старение вин
- 5. Запах роз
- 6. Применение в синтезе галогенгидринов
- 7. Одна из стадий синтеза хинина по Вудворду
- 8. Стиль P. Б. Вудворда (1917—1979)
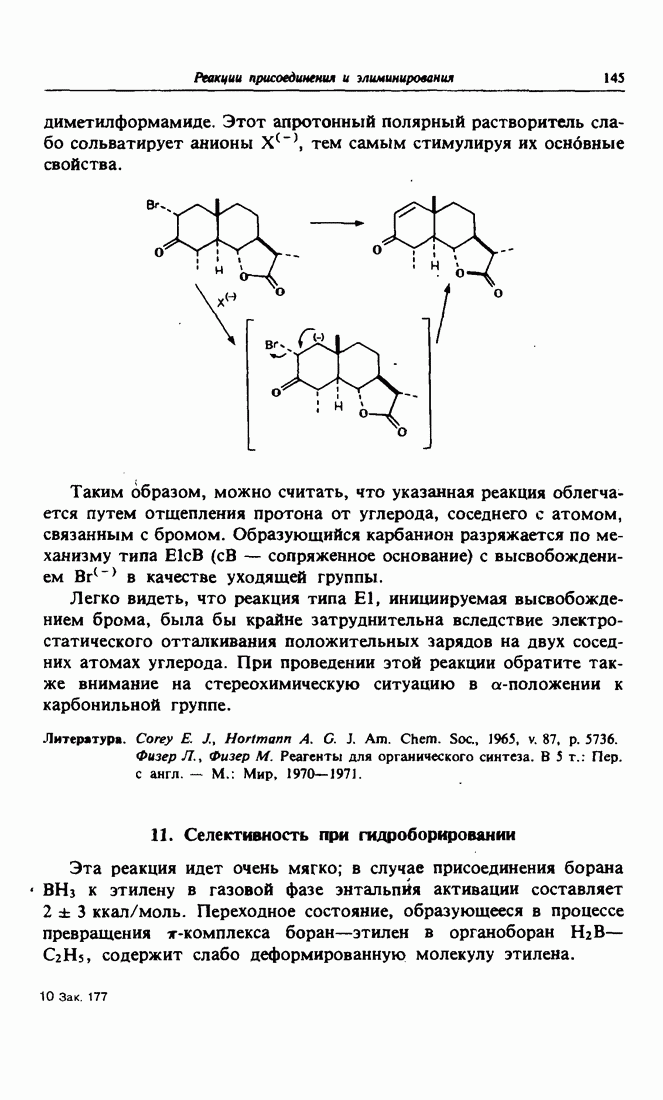
- 9. Галогенирование с последующим дегидрогалогенированием
- 10. Дегидрогалогенирование, позволяющее избежать эпимеризации
- 11. Селективность при гидроборировании
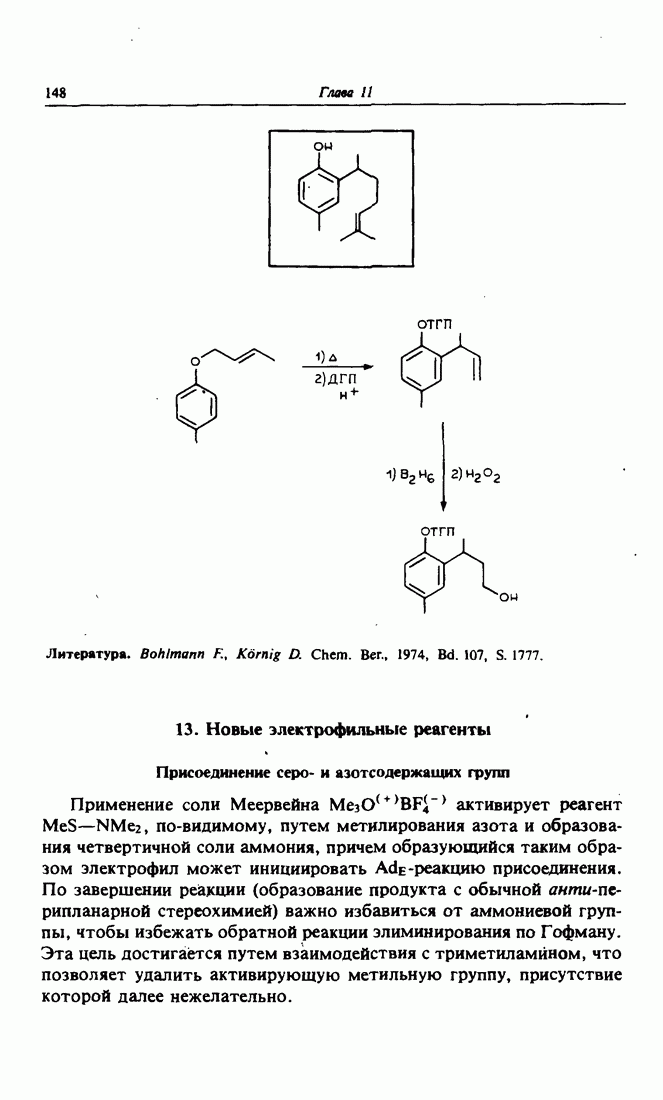
- 12. Начало синтеза эльвирола
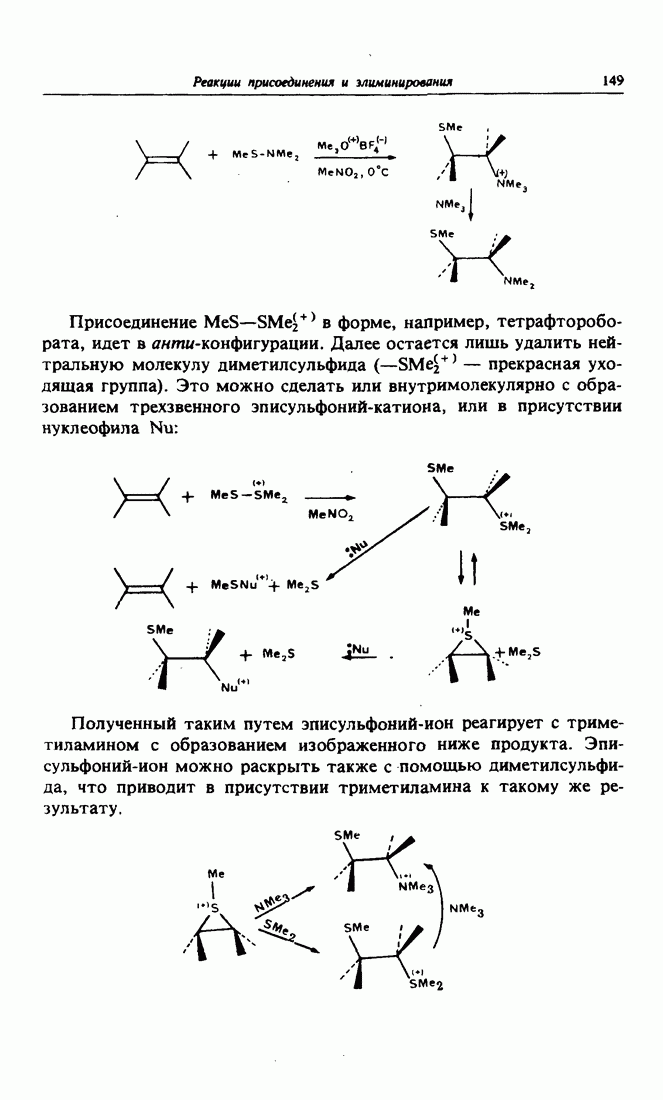
- 13. Новые электрофильные реагенты
- Глава 12. ПЕРЕГРУППИРОВКИ ФУНКЦИОНАЛЬНЫХ ГРУПП. ПРЕВРАЩЕНИЕ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ В ОЛЕФИНЫ ПО РЕАКЦИИ ВИТТИГА
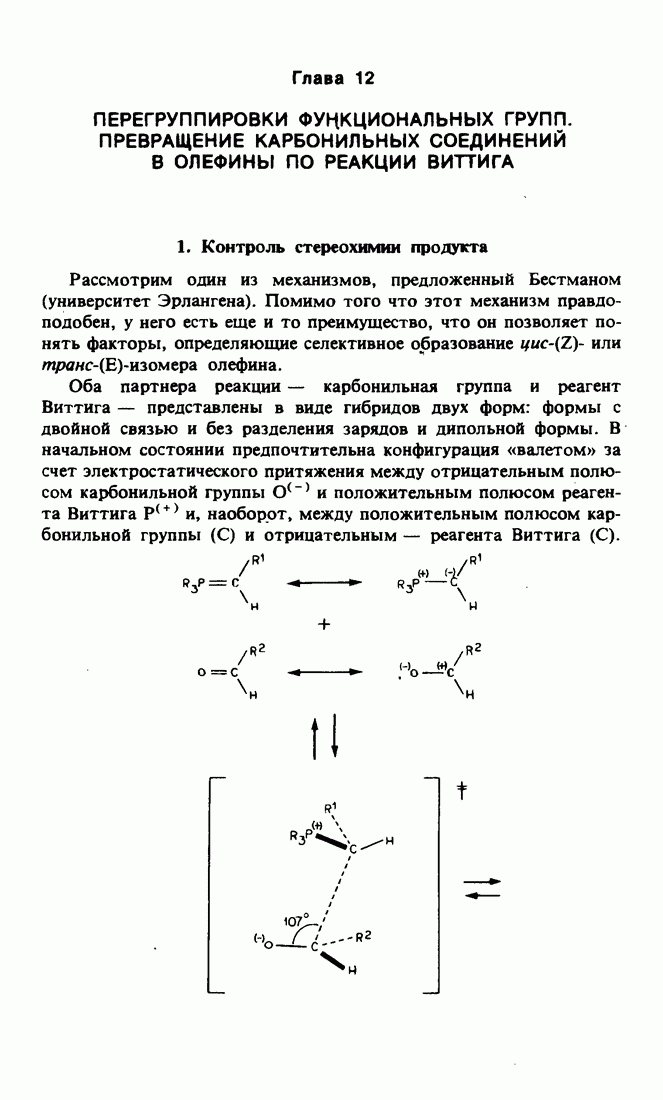
- 1. Контроль стереохимии продукта
- 2. Вариант реакции Виттига в отсутствие енолизации
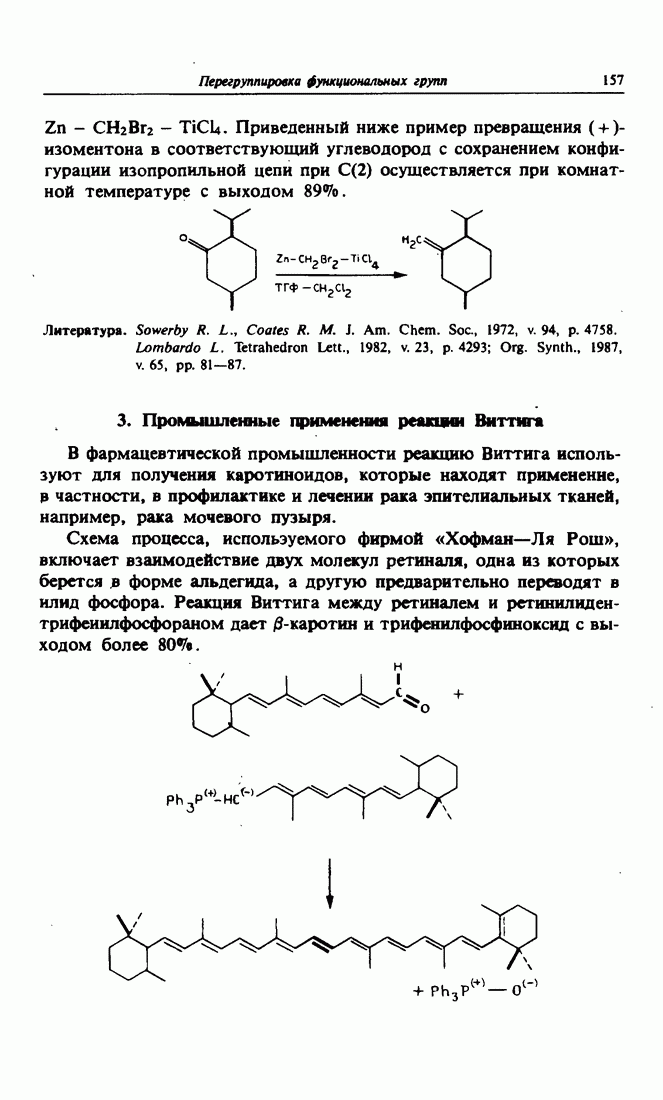
- 3. Промышленные применения реакши Виттига
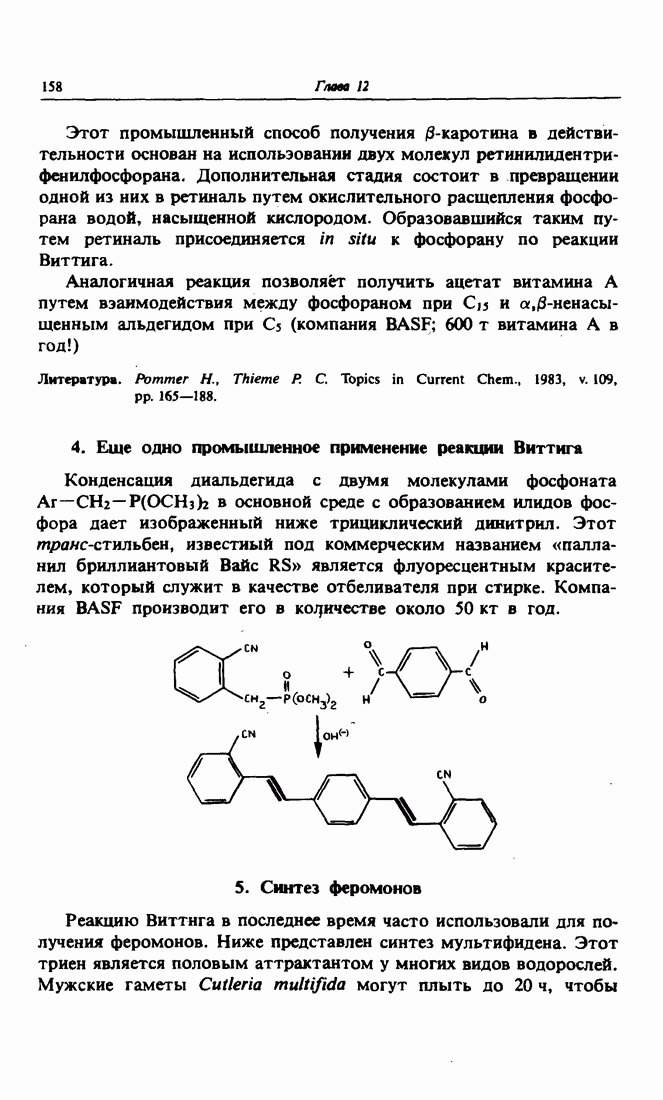
- 4. Еще одно промышленное применение реакции Виттига
- 5. Синтез феромонов
- 6. Другой синтез феромона по реакции Виттига
- Глава 13. ПЕРЕГРУППИРОВКИ
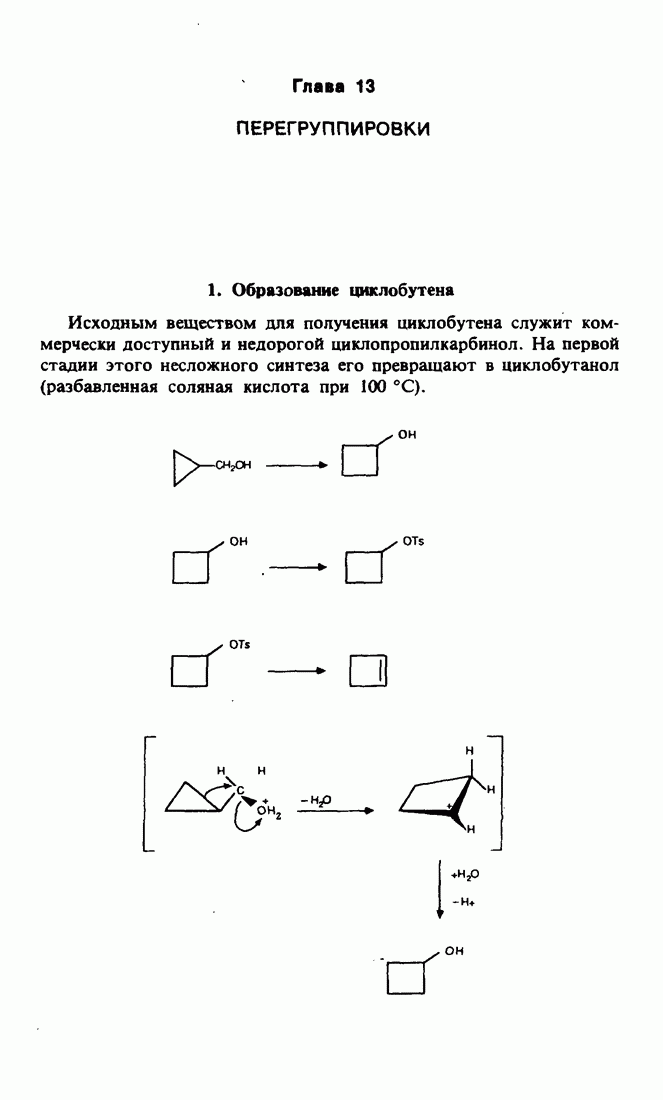
- 1. Образование циклобутена
- 2. 1,2-Миграция
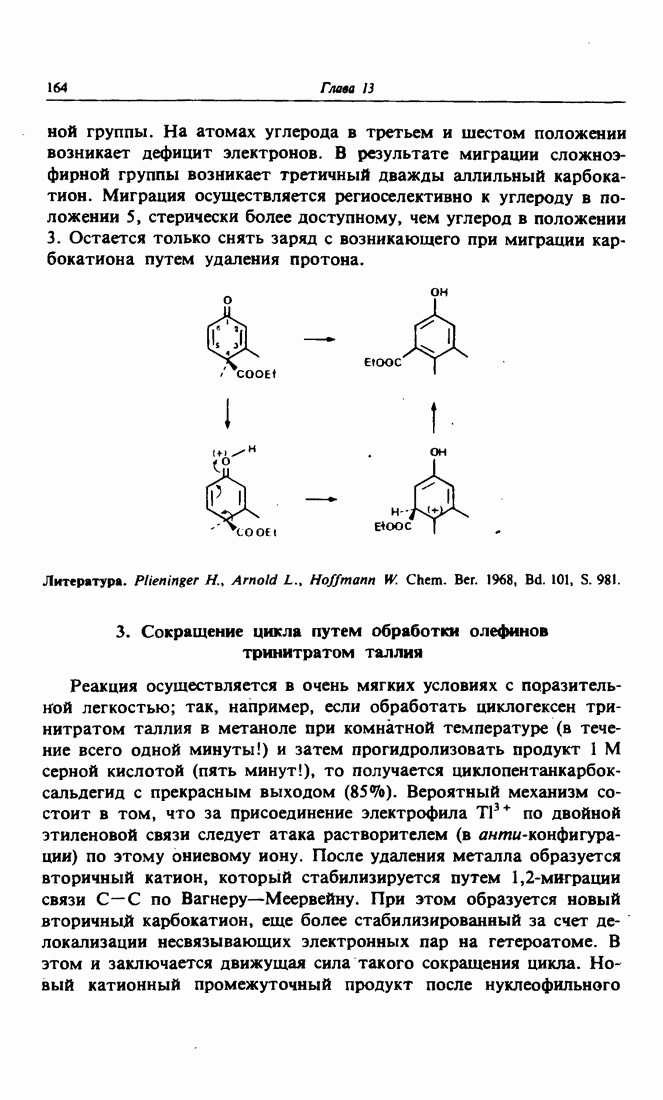
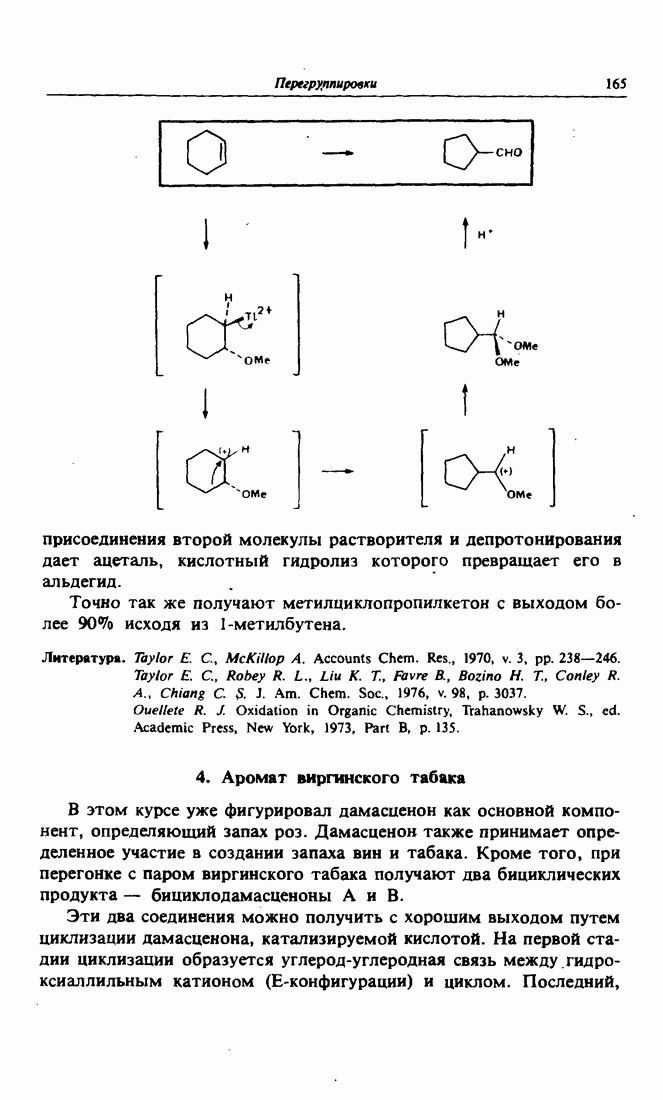
- 3. Сокращение цикла путем обработки олефинов тринитратом таллия
- 4. Аромат виргинского табака
- 5. Маленькие лягушки, которые важнее быка, или для чего служит перегруппировка Бекмана
- 6. Некоторые применения реакции Рамберга-Беклунда
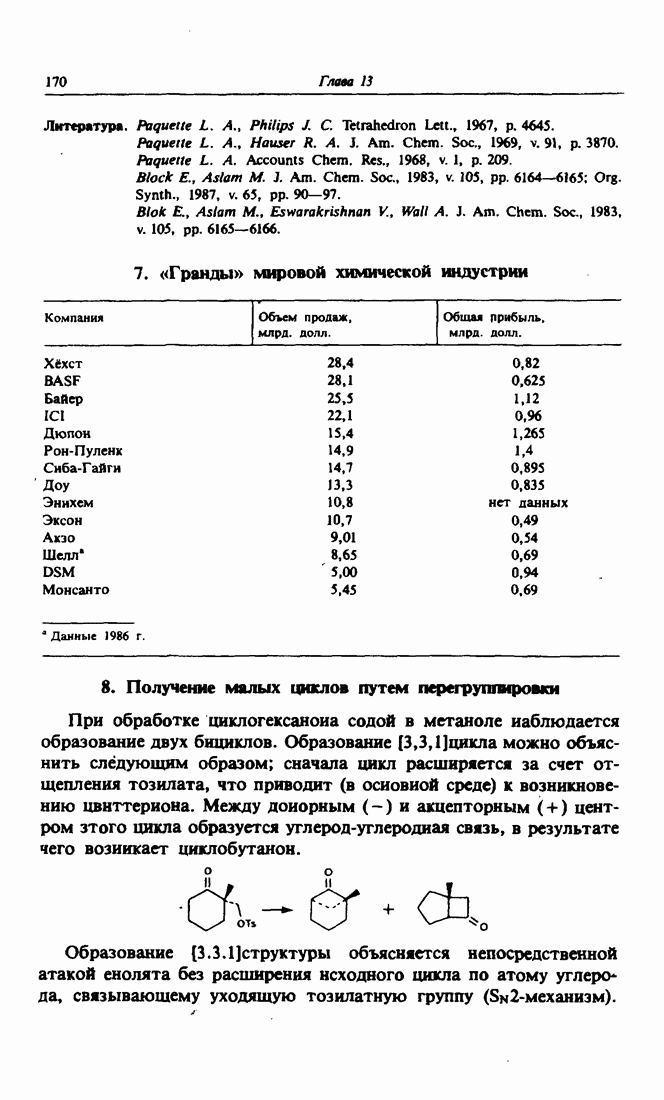
- 8. Получение малых циклов путем перегруппировки
- Главе 14. ДОНОРНЫЕ СИНТОНЫ
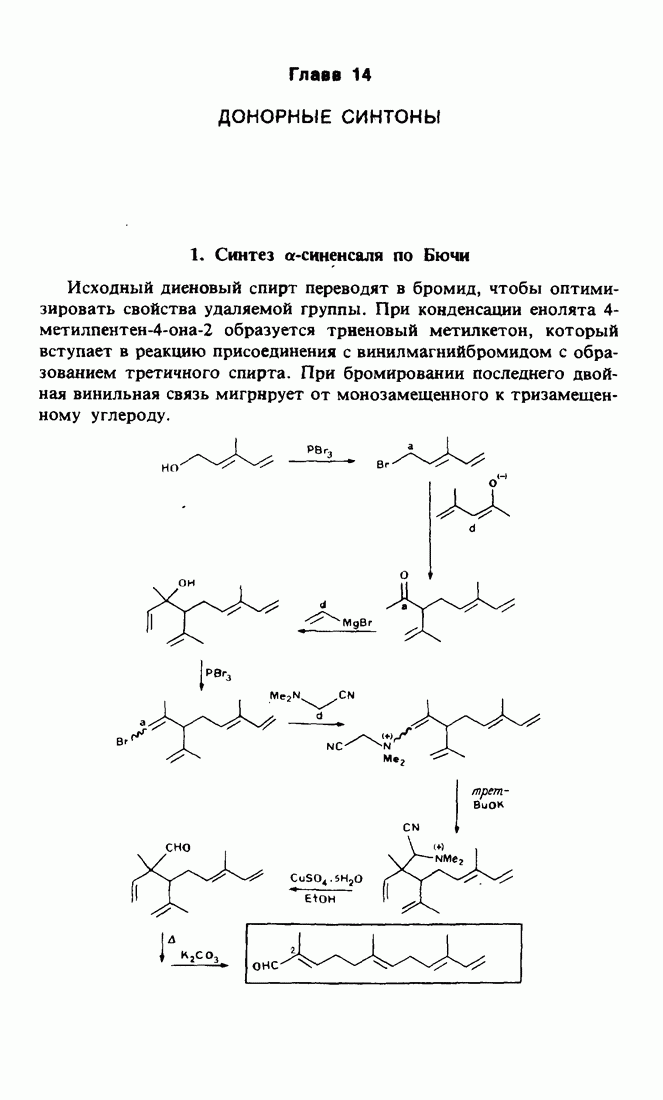
- 1. Синтез а-синенсаля по Бючи
- 2. Начало синтеза кофестола по Кори
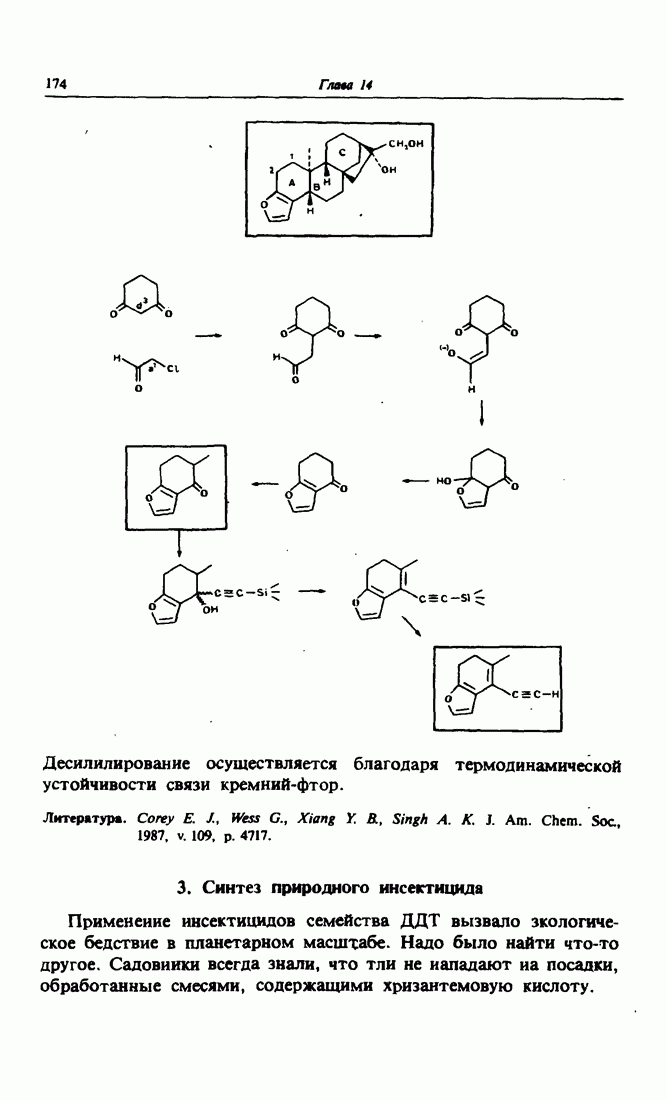
- 3. Синтез природного инсектицида
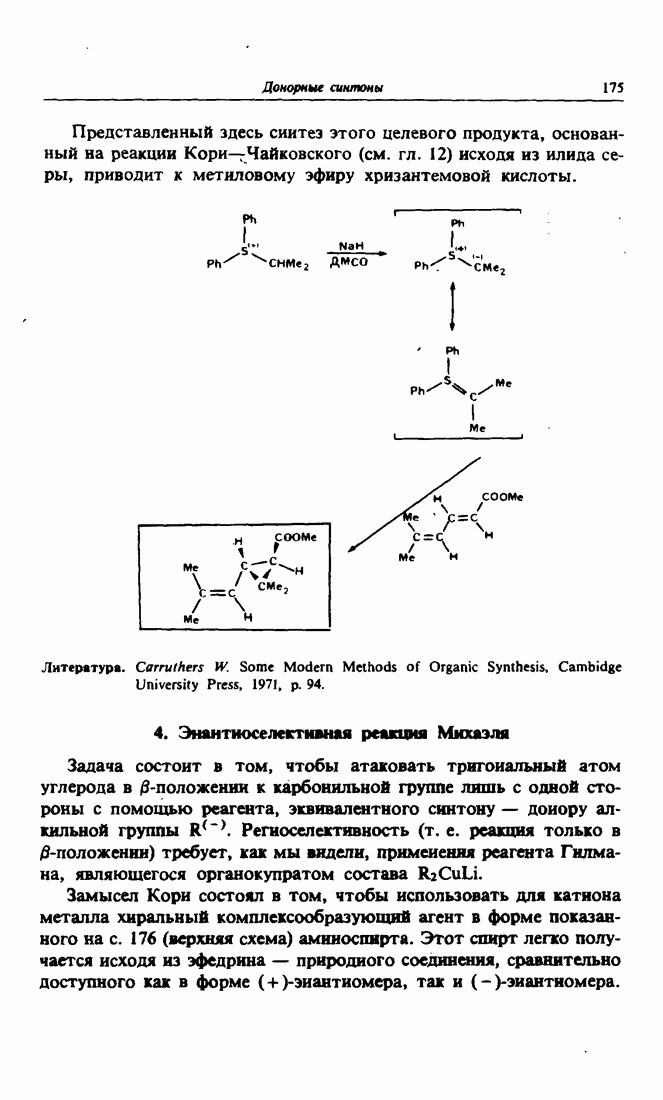
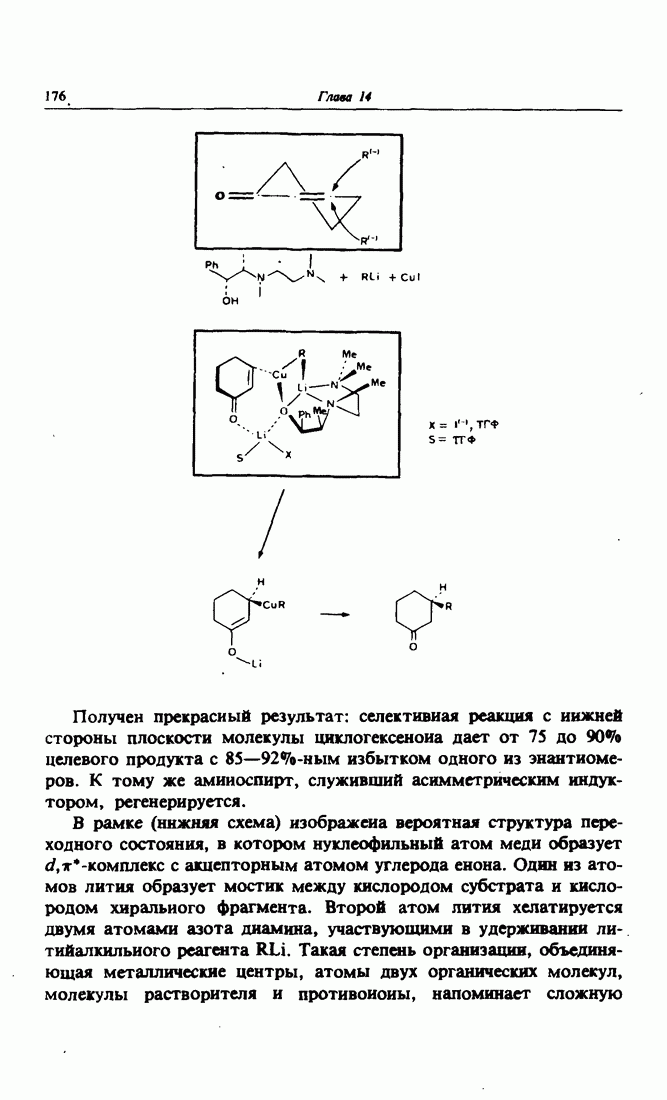
- 4. Энантиоселективная реакция Михаэля
- 5. Хитрые осы
- 6. Химия на основе C1-соединений
- Глава 15. АКЦЕПТОРНЫЕ СИНТОНЫ
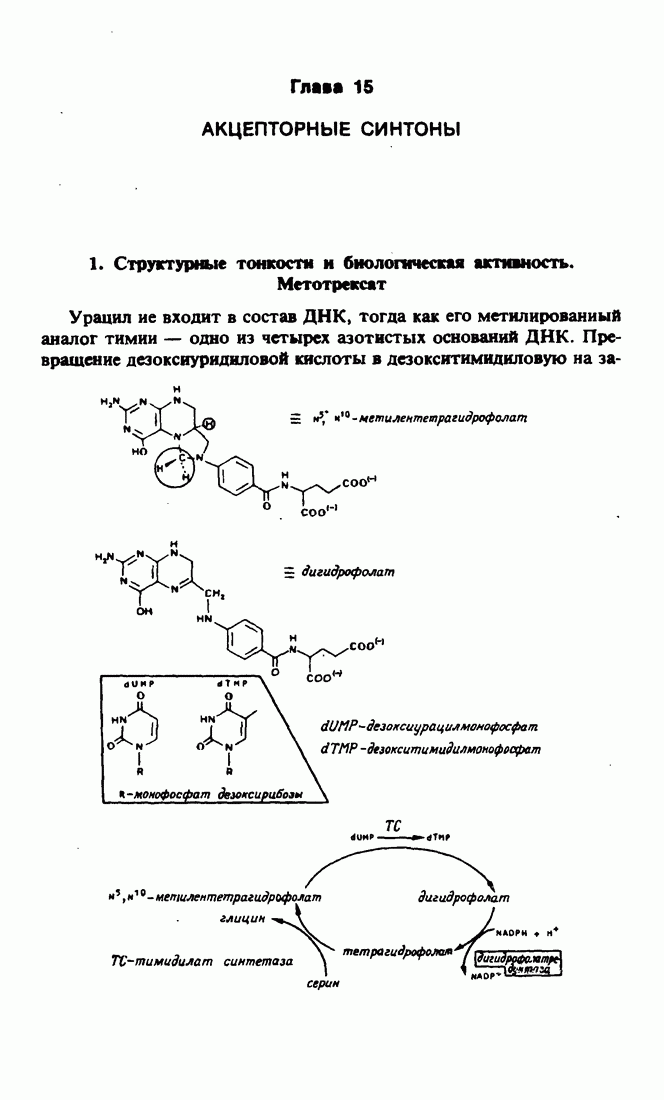
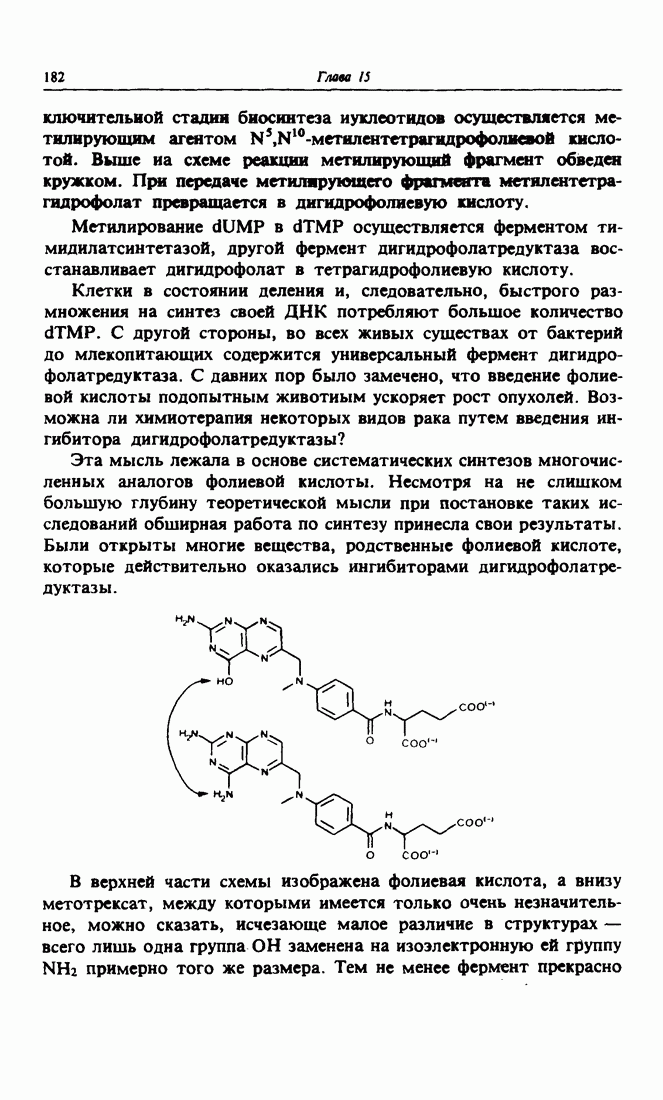
- 1. Структурные тонкости и биологическая активность. Метотрегсат
- 2. Функциональные вариации на структурную тему
- 3. Производство ароматических и вкусовых добавок
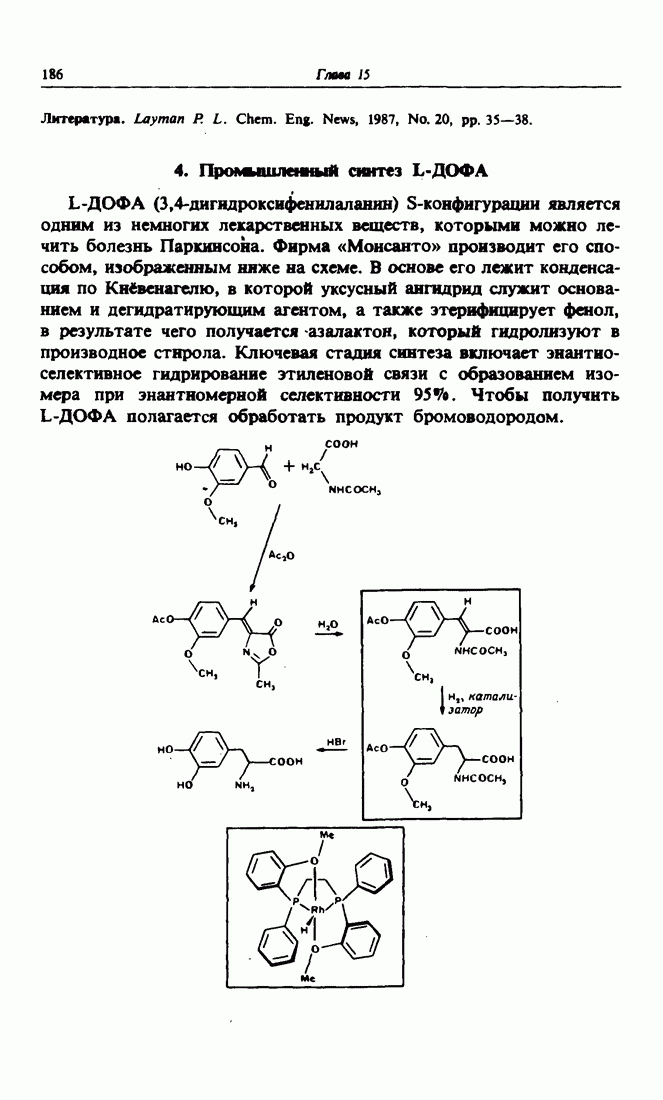
- 4. Проашшлетый синтез L-ДОФА
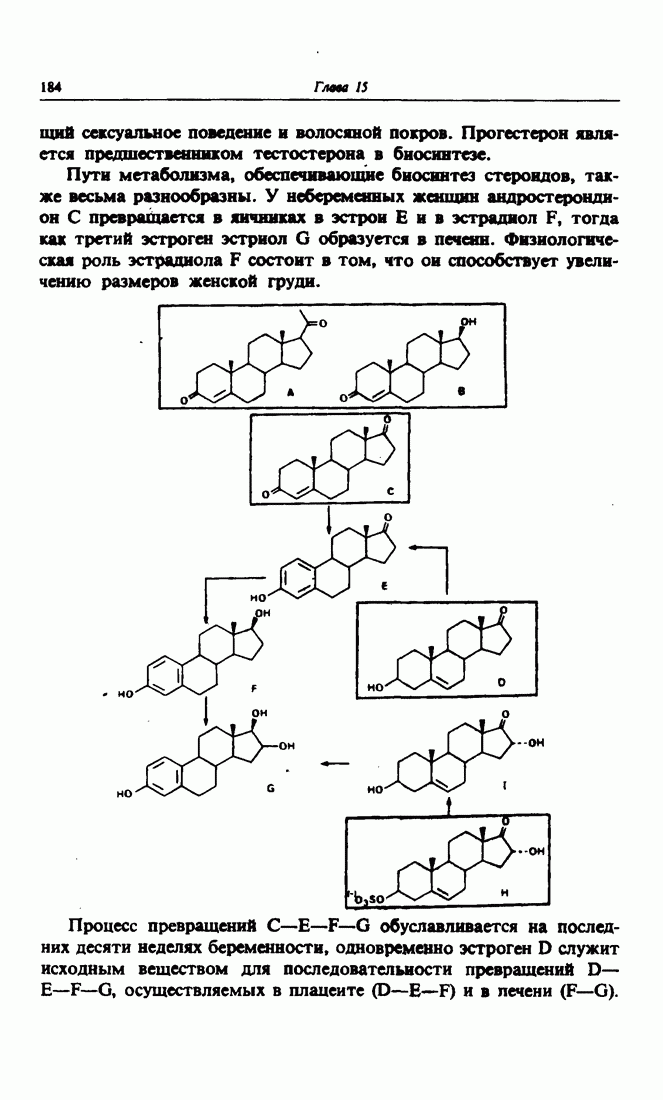
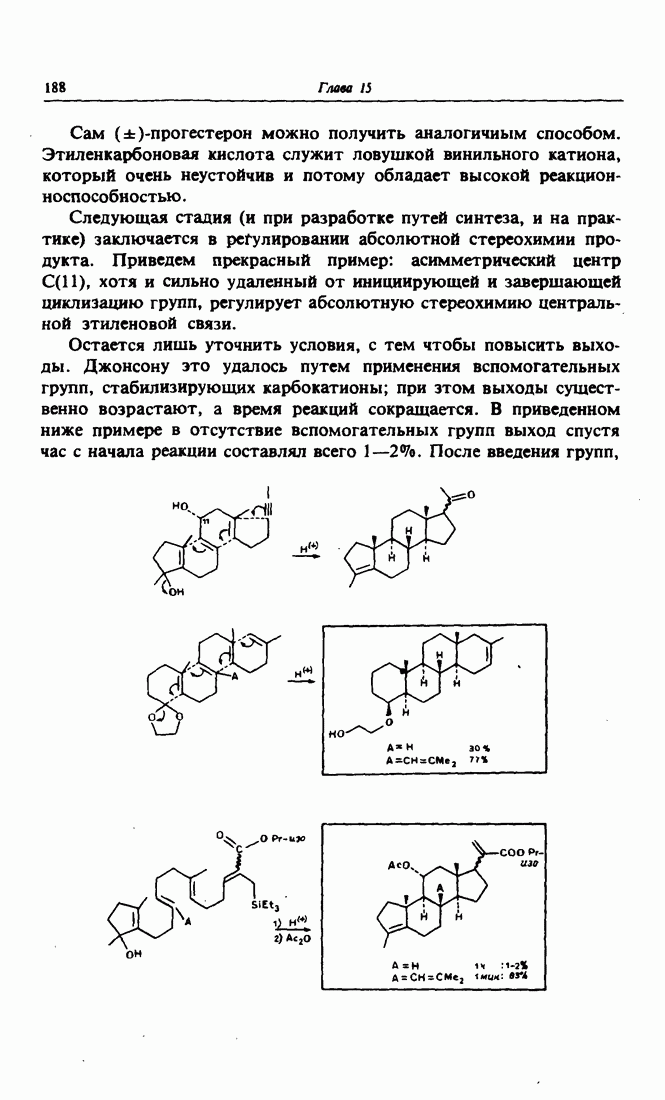
- 5. Биомиметический синтез стероидов
- Глава 16. РЕТРОСИНТЕТИЧЕСКИЙ АНАЛИЗ
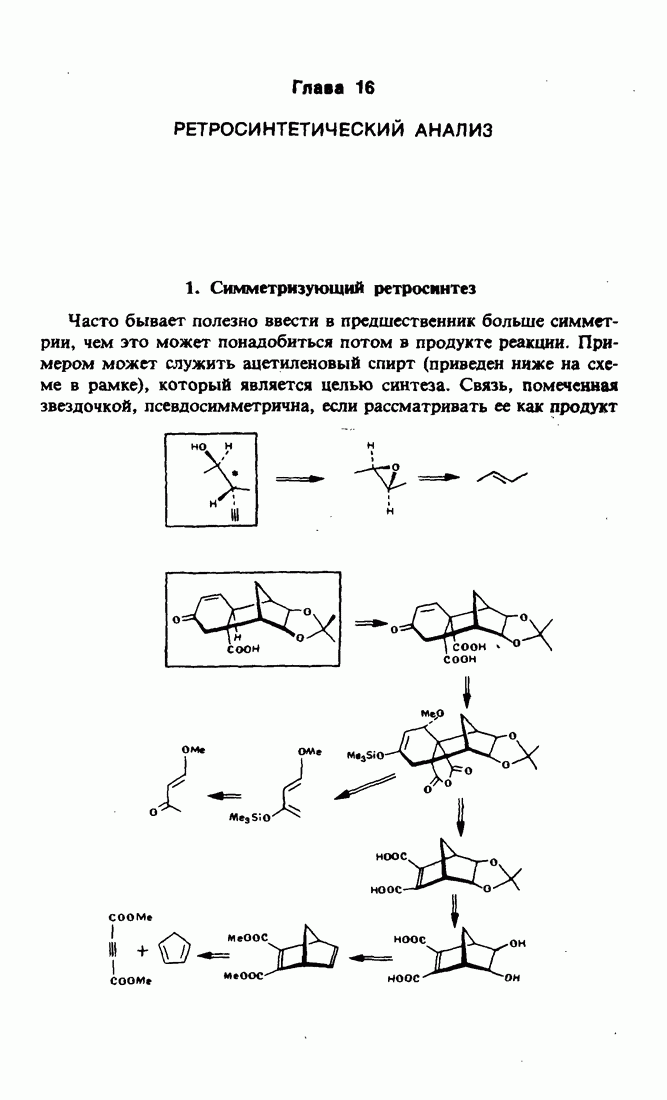
- 1. Симметризующий ретросинтез
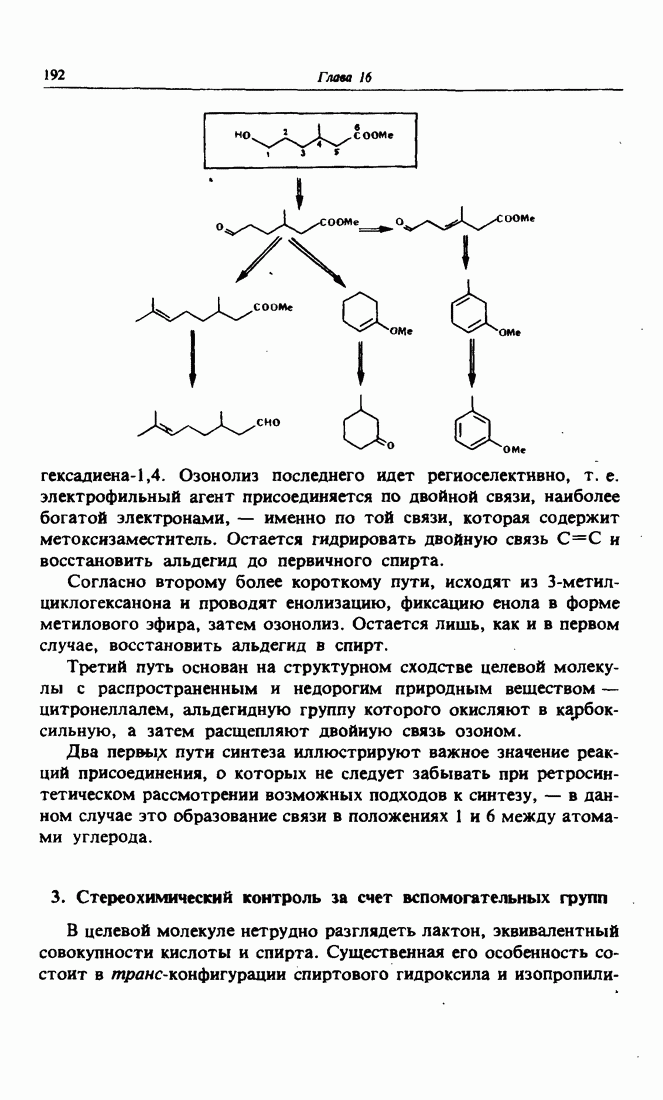
- 2. Реакции присоединения в ретросинтетическом анализе
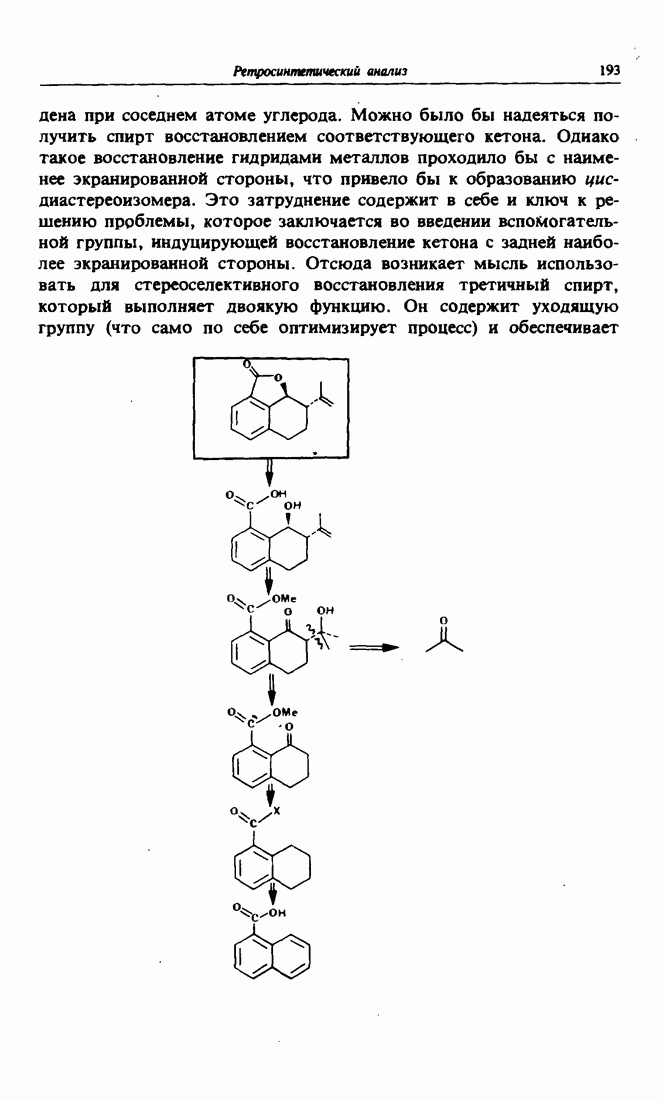
- 3. Стереохимическнй контроль за счет вспомогательных групп
- 4. Окислительный ретросинтез
- 5. Защитим леса! Синтез фронталина