| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
3. Реакционная способность соединений алифатического ряда
3.1. Алканы (насыщенные углеводороды)

Атом углерода в алканах пребывает в первом валентном состоянии  -гибридизация). Если представить, что атом углерода находится в центре правильного тетраэдра, то его связи будут направлены к вершинам последнего, образуя углы
-гибридизация). Если представить, что атом углерода находится в центре правильного тетраэдра, то его связи будут направлены к вершинам последнего, образуя углы  (см. рис, 4). Тетраэдрическая конфигурация четырехвалентного атома углерода в алканах впервые была представлена Я. Вант-Гоффом и Ле-Белем (1871 г.). Поскольку вокруг ординарной связи
(см. рис, 4). Тетраэдрическая конфигурация четырехвалентного атома углерода в алканах впервые была представлена Я. Вант-Гоффом и Ле-Белем (1871 г.). Поскольку вокруг ординарной связи  возможно вращение, для алканов, начиная с этана, характерно существование множества поворотных изомеров (конформеров), отличающихся взаимным расположением атомов или групп атомов, связанных с атомами углерода. Состояние молекулы, характеризующееся определенным расположением атомов водорода или их заместителей вокруг двух атомов углерода, связанных
возможно вращение, для алканов, начиная с этана, характерно существование множества поворотных изомеров (конформеров), отличающихся взаимным расположением атомов или групп атомов, связанных с атомами углерода. Состояние молекулы, характеризующееся определенным расположением атомов водорода или их заместителей вокруг двух атомов углерода, связанных  -связью, называется конформацией.
-связью, называется конформацией.
Расположение атомов или групп атомов друг против друга невыгодно с энергетической точки зрения, так как они испытывают взаимное отталкивание, Из множества конформацнй можно выделить несколько структур, характеризующихся минимумом или максимумом энергии. Так, конформеры молекулы бутана можно представить следующим образом (рис. 15; луч зрения наблюдателя направлен вдоль связи 
Таким образом, углеродные цепи имеют не линейный характер, как это принято формально изображать, а вид ломаных кривых, причем при достаточном удлинении наблюдается тенденция к их закручиванию.

Рис. 15. Изображение кои форме ров бутана с помощью проекционных формул Ньюмена (наблюдение вдоль связи  вокруг которой совершается вращение): а - трансондная, или заторможенная, конформация (наиболееввыгодная) б - частично заслоненная; в — скошенная (гош форма) г - полностью заслоненная, или эклиптическая (наименее иыгодиая),
вокруг которой совершается вращение): а - трансондная, или заторможенная, конформация (наиболееввыгодная) б - частично заслоненная; в — скошенная (гош форма) г - полностью заслоненная, или эклиптическая (наименее иыгодиая),
Энергия взаимного перехода конформеров невелика (4,2 — 20 кДж/моль). Тем не менее в каждый момент большая часть молекул пребывает в более выгодных формах 
Адкзяы отличаютгя сравнительно низкой реакционной способностью ввиду отсутствия в них кратных связей и гетероатомов, вызывающих поляризацию связен.
Реакции алканов протекают в жестких условиях (температура, облучение, катализаторы) преимущественно по радикальным механизмам. Гетеролитические превращения алканы претерпевают лишь в присутствии катализаторов" (алюмосиликатов,  д.) и добавок, способных генерировать карбониевые ионы (спиртов, олефинов), Карбкатион способен атаковать алкан, вырывая гидрид-анион
д.) и добавок, способных генерировать карбониевые ионы (спиртов, олефинов), Карбкатион способен атаковать алкан, вырывая гидрид-анион 

Гомолитнческне реакции протекают в присутствии реагентов — источников сравнительно стабильных радикалов:  кислорода, представляющего собой бирадикал
кислорода, представляющего собой бирадикал  д.
д.
Пути образования радикалов:
1. Термолиз. При температуре выше  алканы расщепляются преимущественно гомолитически.
алканы расщепляются преимущественно гомолитически.
2. Фотолиз. Расщепление. под действием УФ-света.
3. Радиол из. Расщепление под воздействием высокоэнергетического излучения (например,  -лучей).
-лучей).
4. Окислительно-восстановительные реакции нерекисных реагентов и соединении металлов с переменной валентностью.
Энергия гомолитического разрыва связей тем меньше, чем стабильнее образующиеся радикалы (табл. 2).
Несмотря на то что энергия диссоциации связи  довольно высока, стабильные радикалы
довольно высока, стабильные радикалы  расщепляют ее, поскольку при этом выделяется энергия за счет образования более прочных связей:
расщепляют ее, поскольку при этом выделяется энергия за счет образования более прочных связей:

Таблица 2. (см. скан) Энергия гемолитической диссоциации связей при 
Радикальный механизм реализуется, если все стадии процесса экзотермичны.
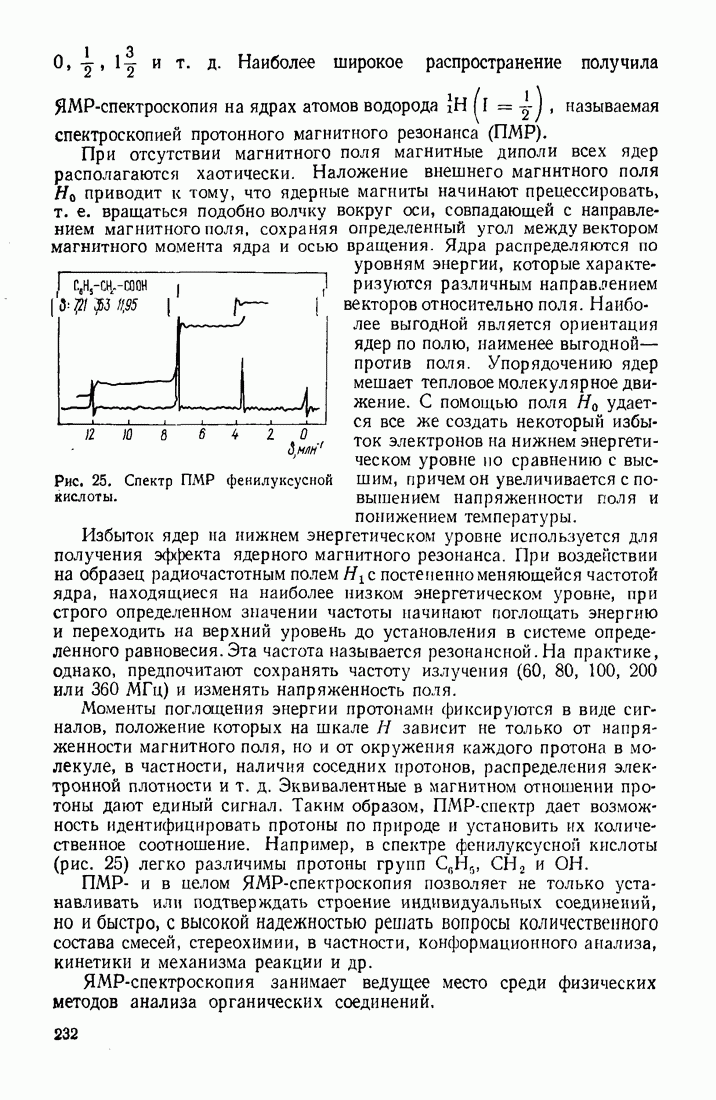
Наиболее характерные реакции алканов относятся к типам электрофильного замещения  расщепления (6) и окисления (7,8).
расщепления (6) и окисления (7,8).
1. Галогенирование:

По реакционной способности галогены можно расположить в ряд:  алканы — в следующий ряд: третичный
алканы — в следующий ряд: третичный  вторичный
вторичный  первичный.
первичный.
Механизм реакции:

Устойчивость алкильного радикала повышается с увеличением его разветвленности, так как группы обладающие  -эффектом, стабилизируют неспаренный электрон.
-эффектом, стабилизируют неспаренный электрон.
2. Внедрение метиленовой группы. В качестве электрофильной частицы, характеризующейся высокой реакционной способностью, выступает метилен (карбен)  имеющий два различных спиновых состояния:
имеющий два различных спиновых состояния:

Источники образования карбена и его производных:

Прямое внедрение метилена:

Для триплетного метилена свойственно последовательное внедрение;

3. Нитрование:

При нитровании по Коновалову используют разбавленную азотную кислоту (при 140 °С). Процесс отличается высокой избирательностью. Легче всего замещается атом водорода у третичного атома углерода, наиболее трудно — у первичного.
Механизм реакции — радикальный.
4. Сульфирование:

5. Сульфохлорирование:

6. Пиролиз (крекинг). При нагревании углеводородов до 250— 800 °С (чаще всего в присутствии катализатора) образуются алканы и алкены с более низкой молекулярной массой.
При использовании катализатора (например, алюмосиликатов) реакция идет через образование карбониевых ионов и приводит к получению более разветвленных углеводородов.
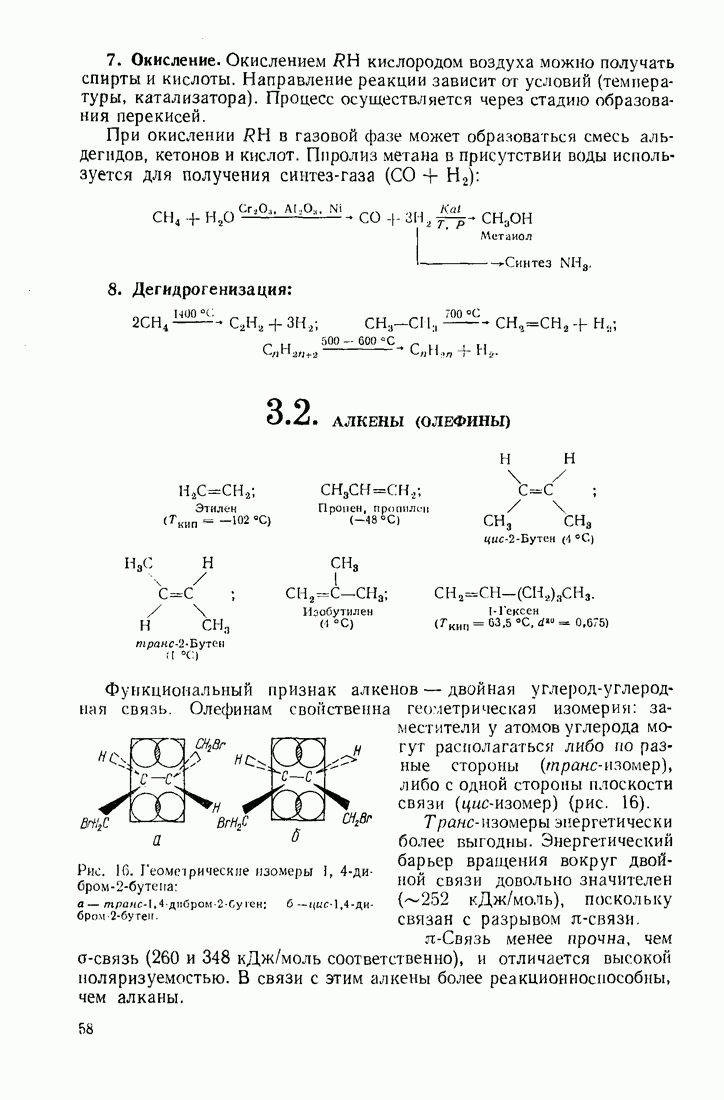
7. Окисление. Окислением  кислородом воздуха можно получать спирты и кислоты. Направление реакции зависит от условий (температуры, катализатора). Процесс осуществляется через стадию образования перекисей.
кислородом воздуха можно получать спирты и кислоты. Направление реакции зависит от условий (температуры, катализатора). Процесс осуществляется через стадию образования перекисей.
При окислении  в газовой фазе может образоваться смесь альдегидов, кетонов и кислот. Пиролиз метана в присутствии воды используется для получения синтез-газа
в газовой фазе может образоваться смесь альдегидов, кетонов и кислот. Пиролиз метана в присутствии воды используется для получения синтез-газа 

8. Дегидрогенизация:

| << Предыдущий параграф | Следующий параграф >> |
- Предисловие
- 1. Введение
- 1.1. Предмет органической химии
- 1.2. Основные этапы развития органической химии
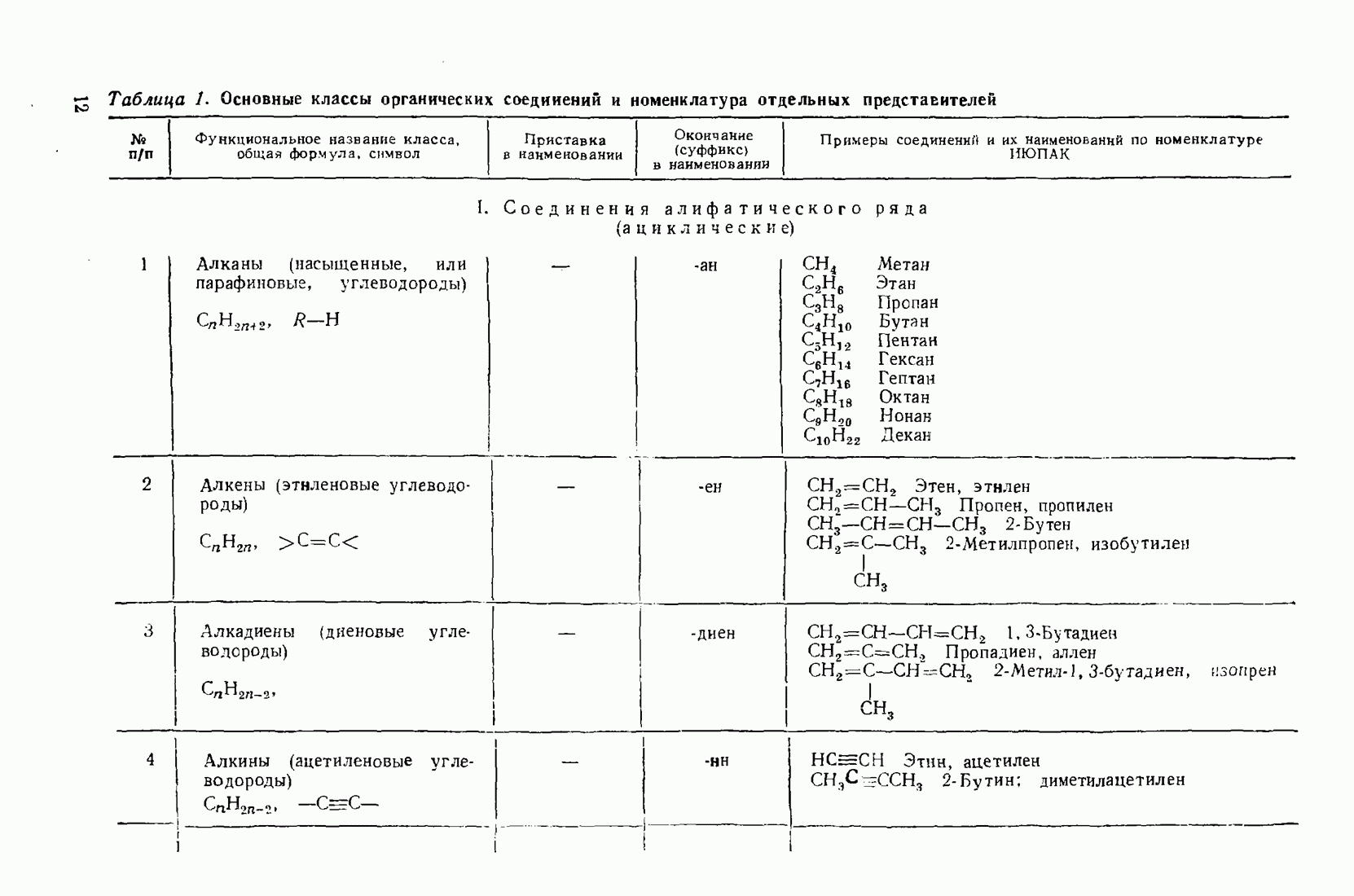
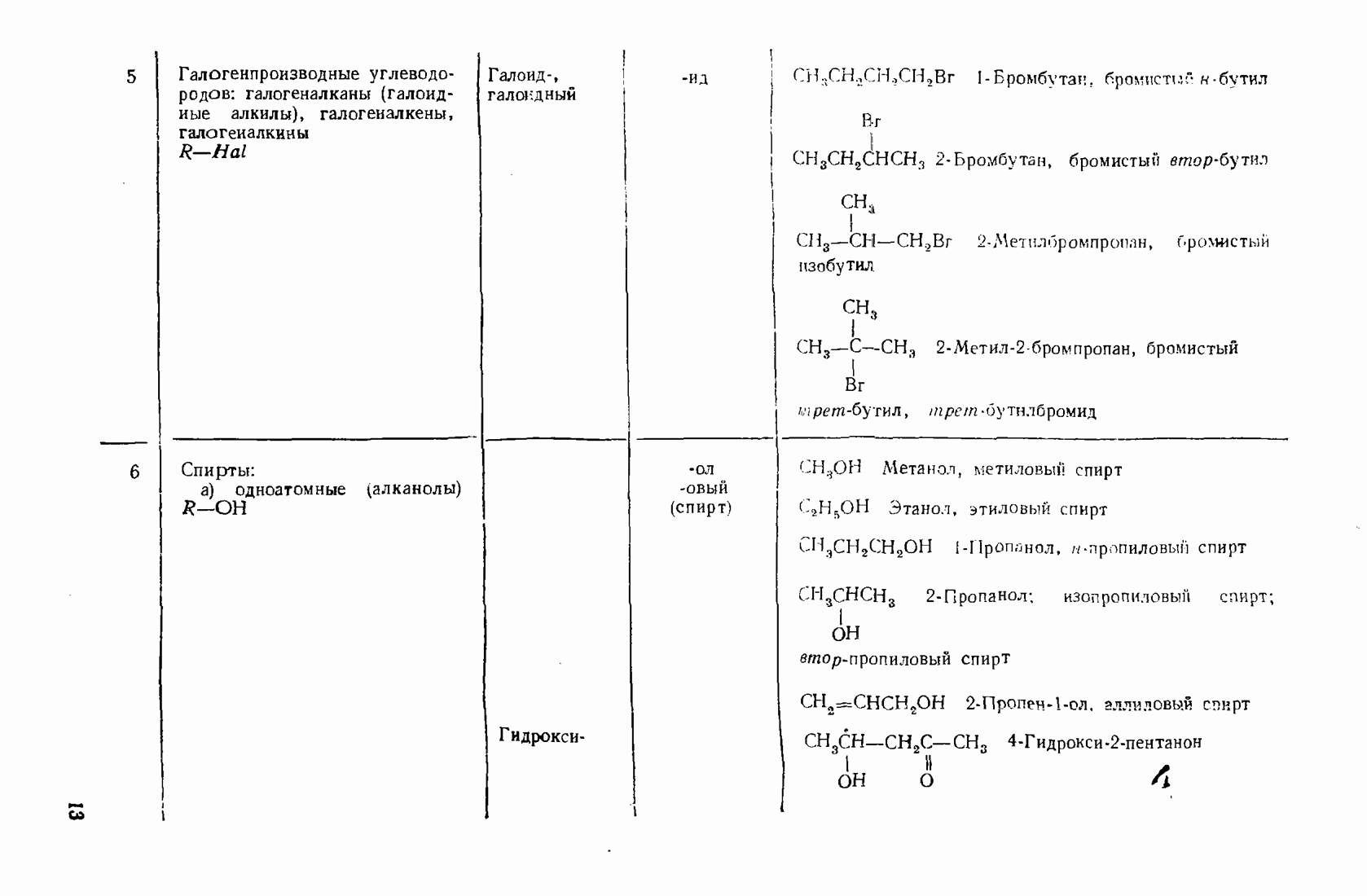
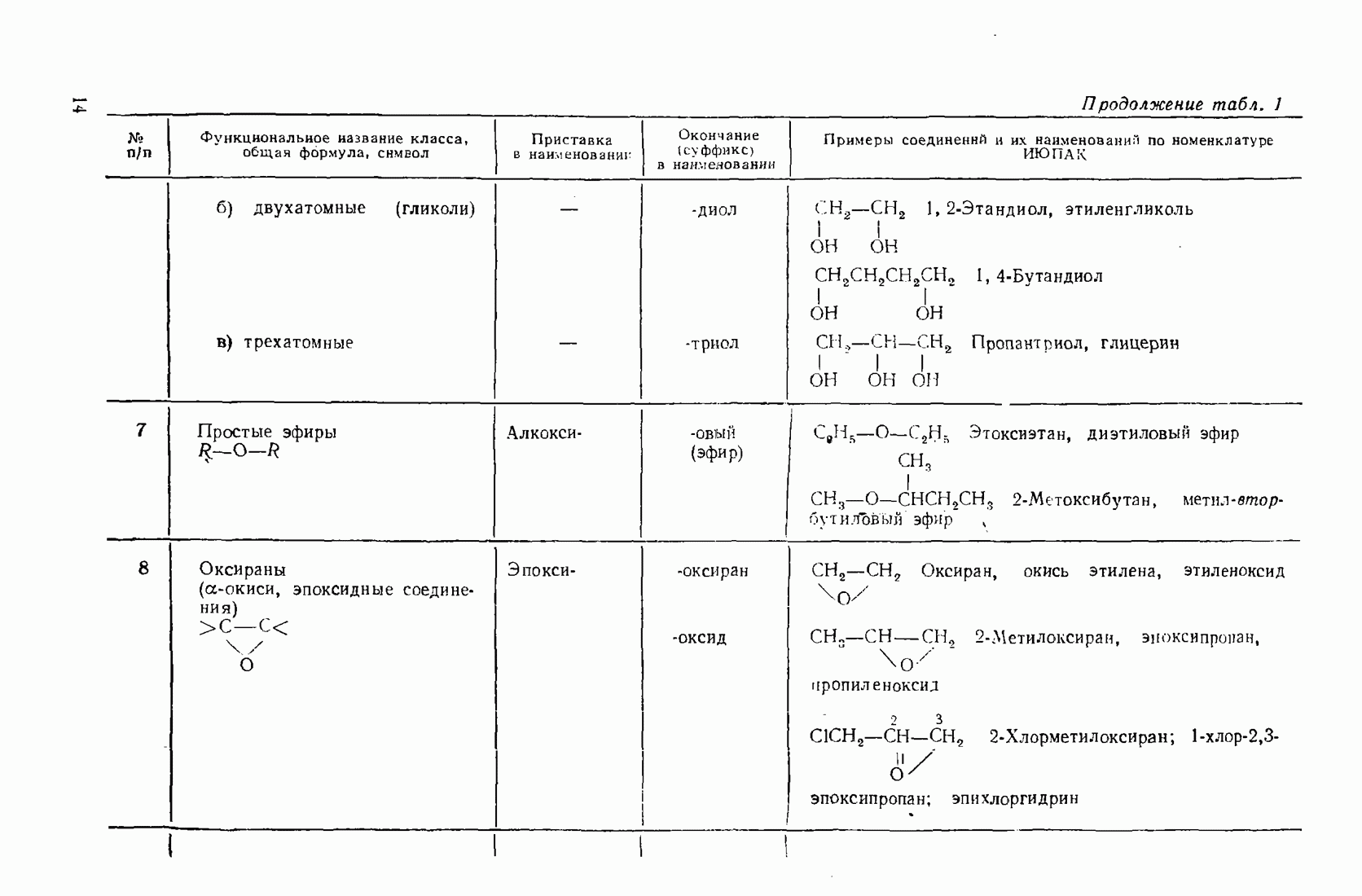
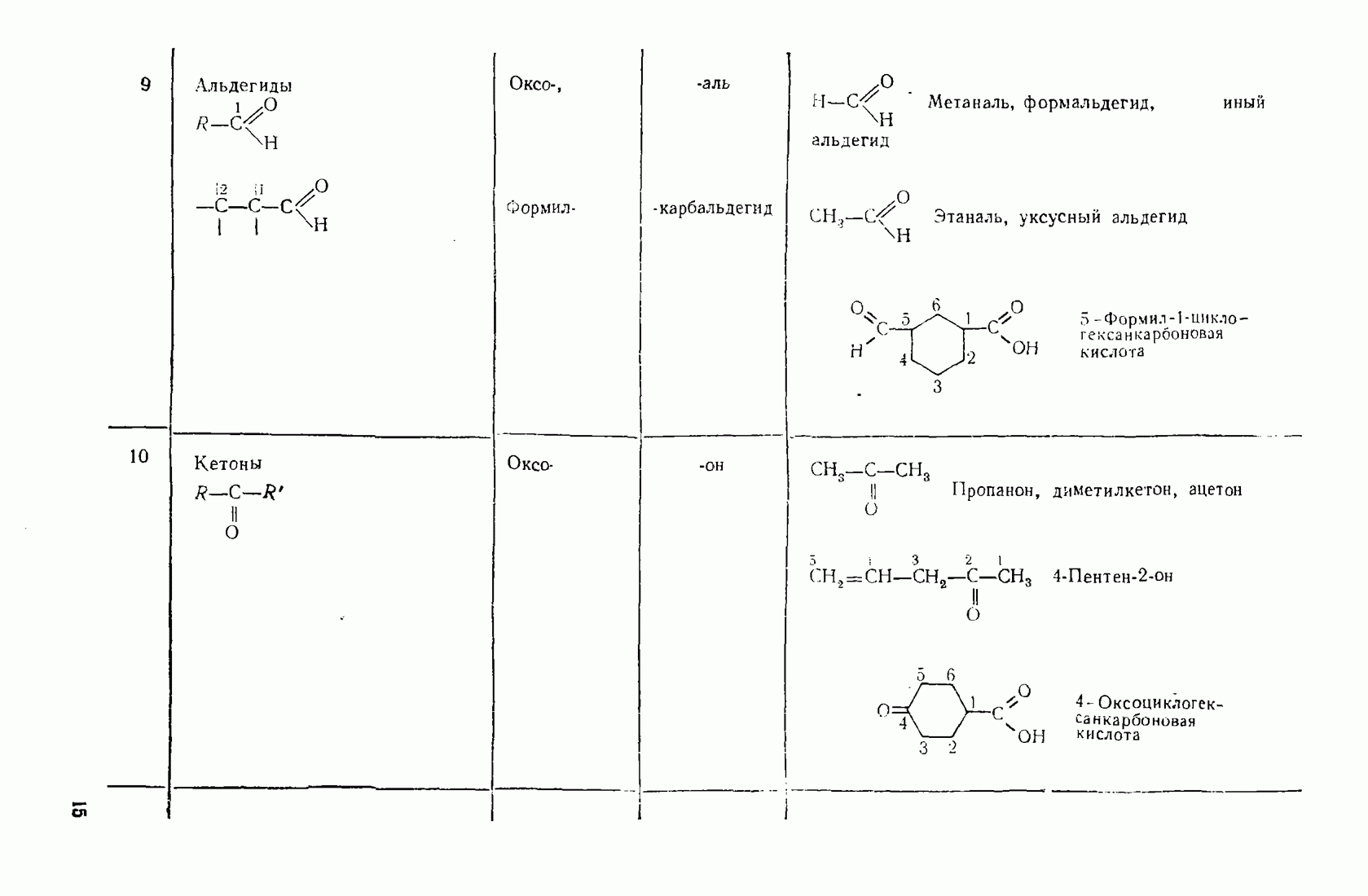
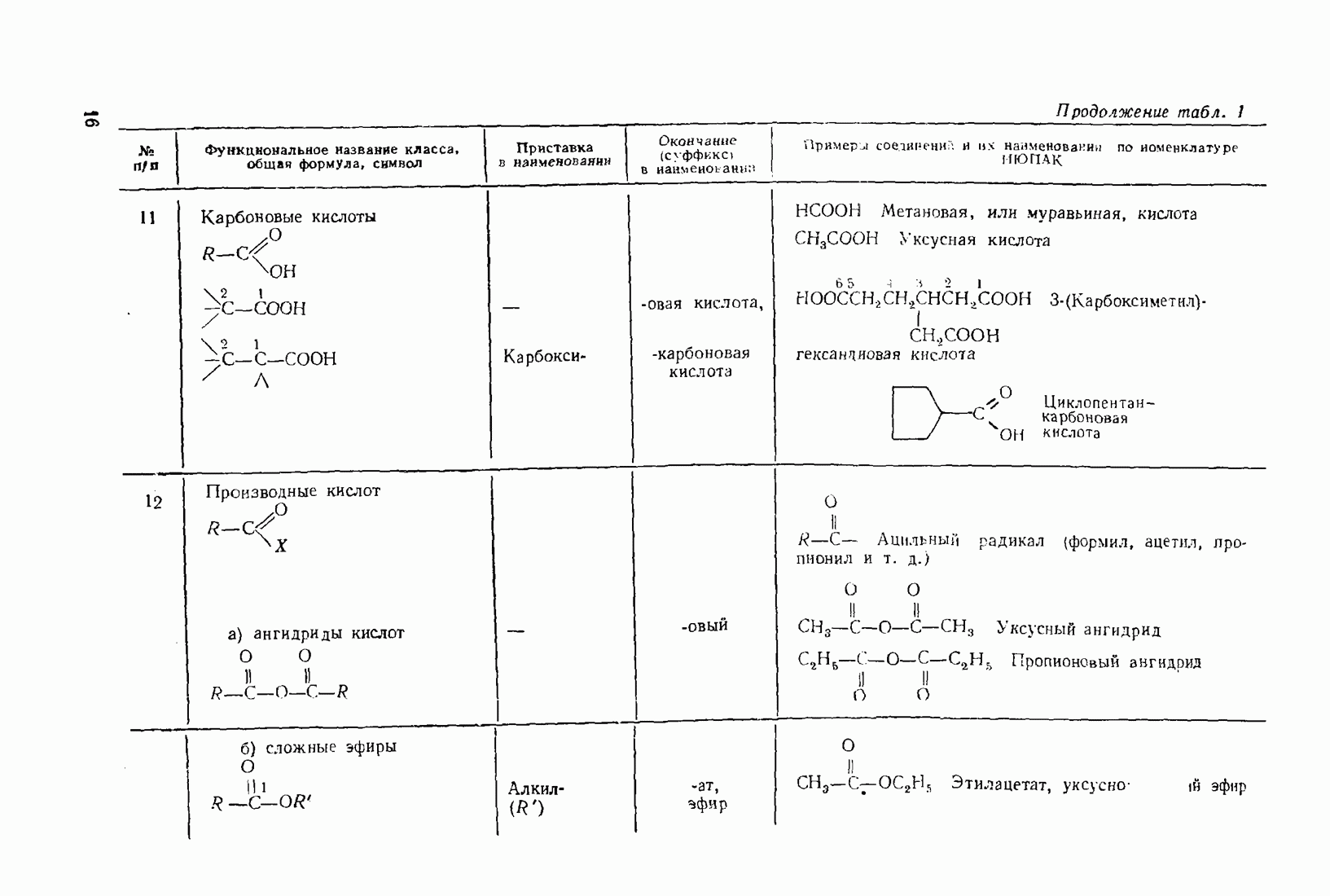
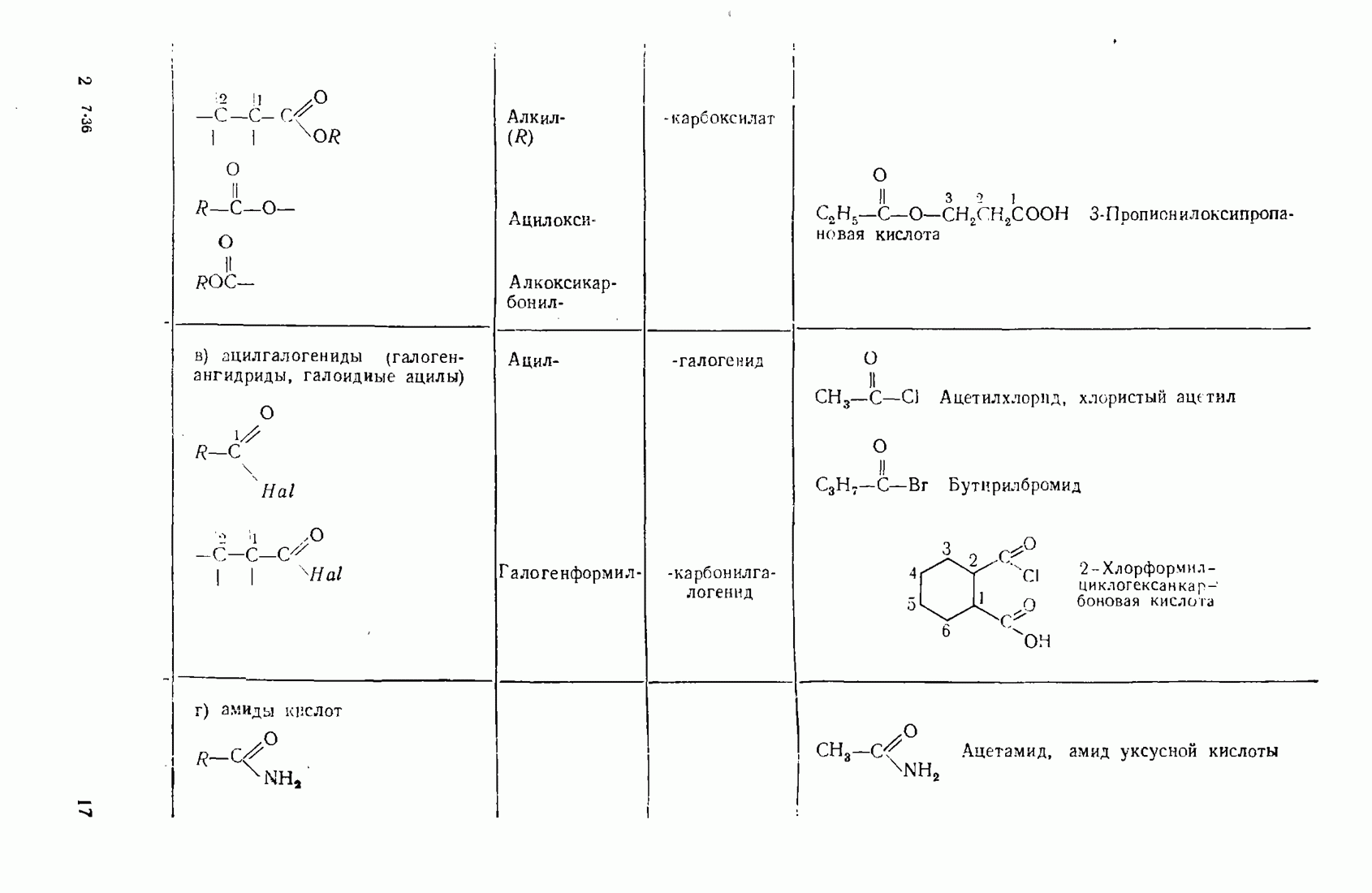
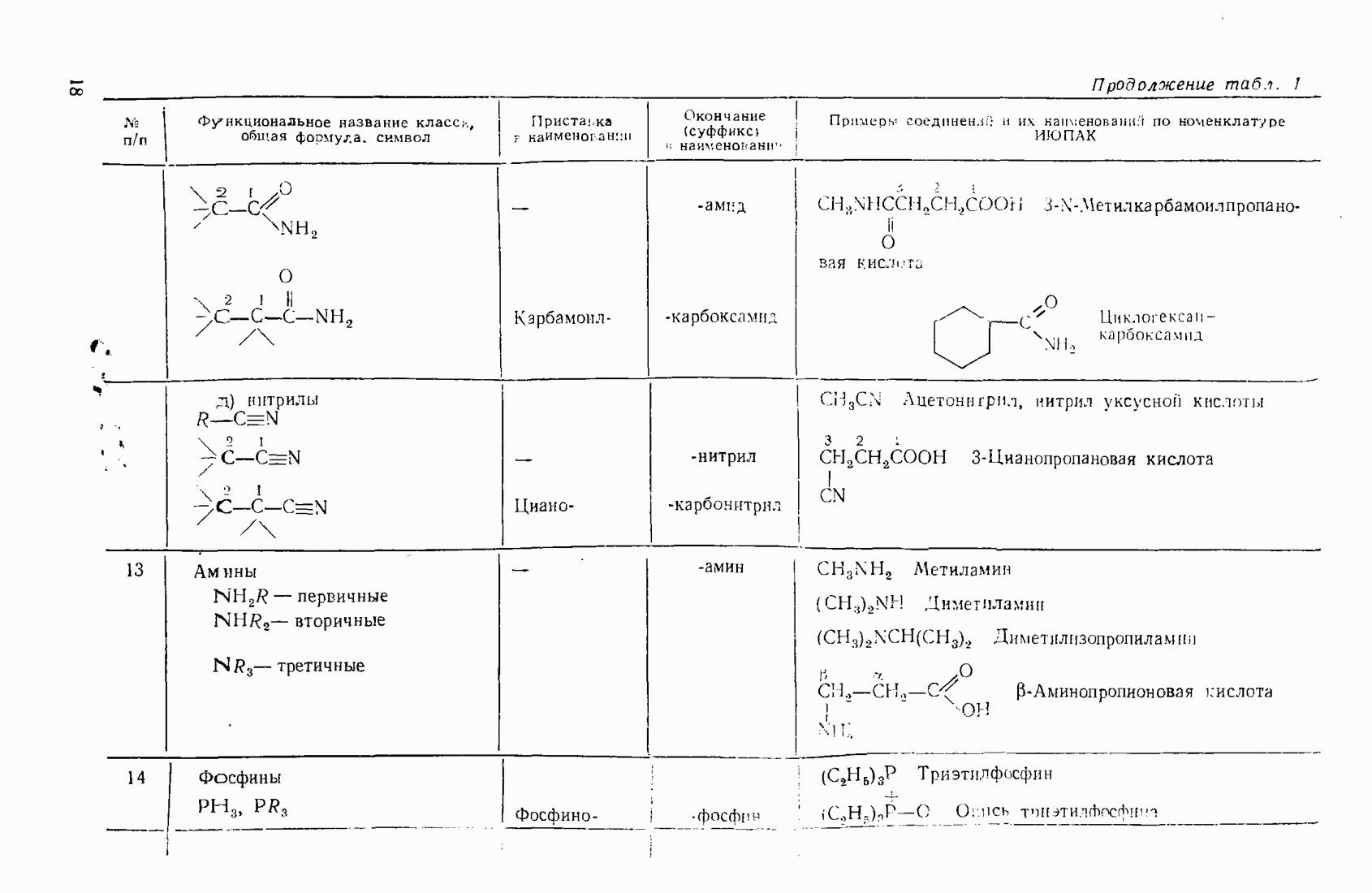
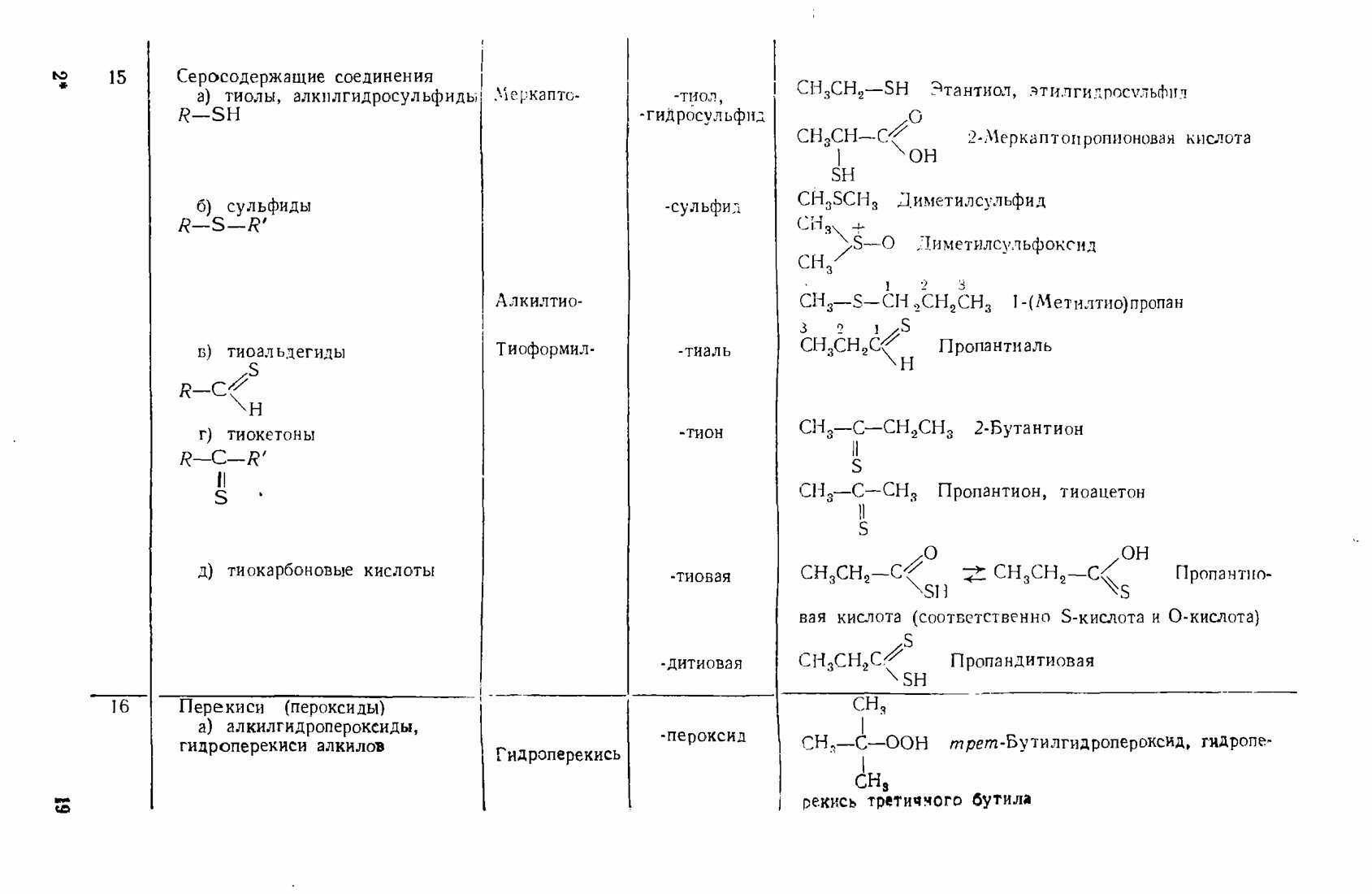
- 1.3. Классификация и номенклатура органических соединений
- 2 Общие теоретические положения органической химии
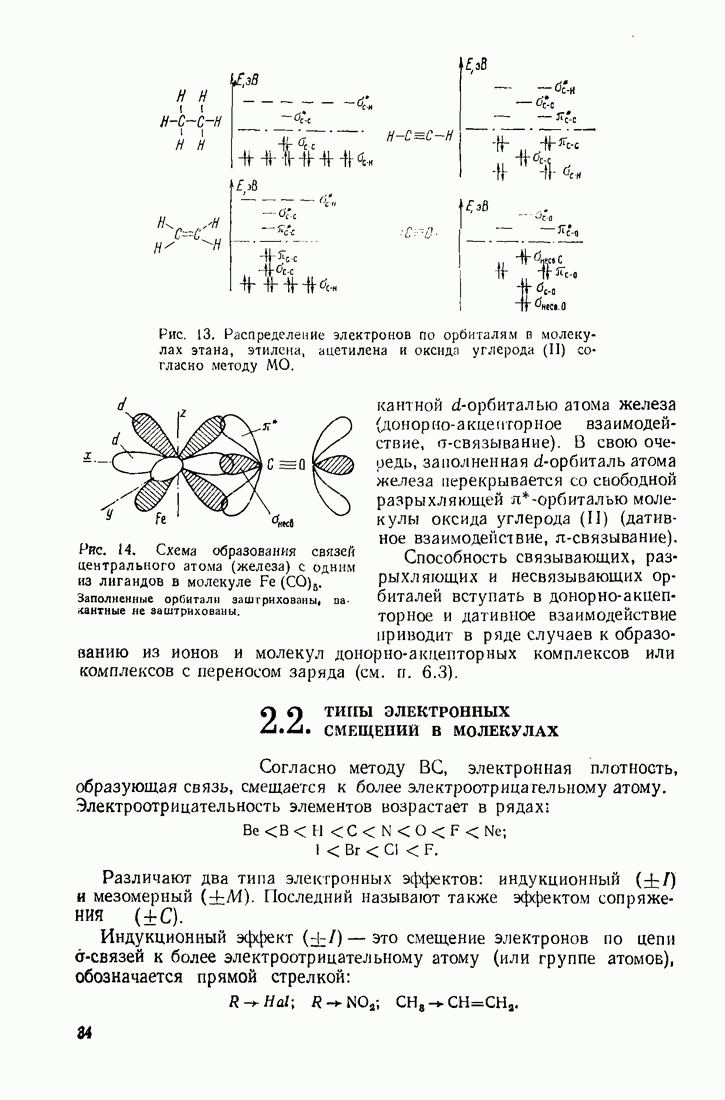
- 2.1. Природа химической связи
- 2.1.1. Типы химических связей
- 2.1.2. Молекулярные орбитали
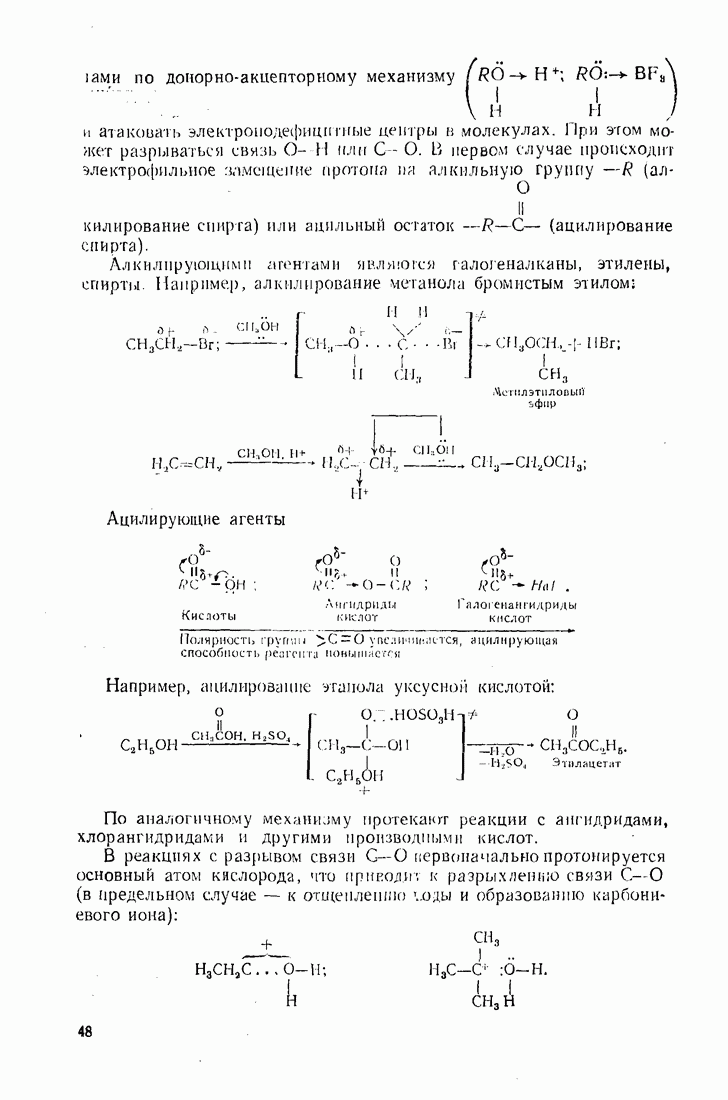
- 2.2. ТИПЫ ЭЛЕКТРОННЫХ СМЕЩЕНИЙ В МОЛЕКУЛАХ
- 2.3. ОБЩИЕ ПРЕДСТАВЛЕНИЯ ОБ ОРГАНИЧЕСКОЙ РЕАКЦИИ
- 2.4. КЛАССИФИКАЦИЯ РЕАГЕНТОВ И РЕАКЦИЙ
- 2.5. КРАТКАЯ ХАРАКТЕРИСТИКА РЕАКЦИОННОЙ СПОСОБНОСТИ НЕКОТОРЫХ СОЕДИНЕНИЙ АЛИФАТИЧЕСКОГО РЯДА
- 2.5.1. Алканы (парафины)
- 2.5.2. Непредельные углеводороды
- 2.5.3. Галогеналканы (галоидные алкилы R-Hal)
- 2.5.4. Спирты (R0Н)
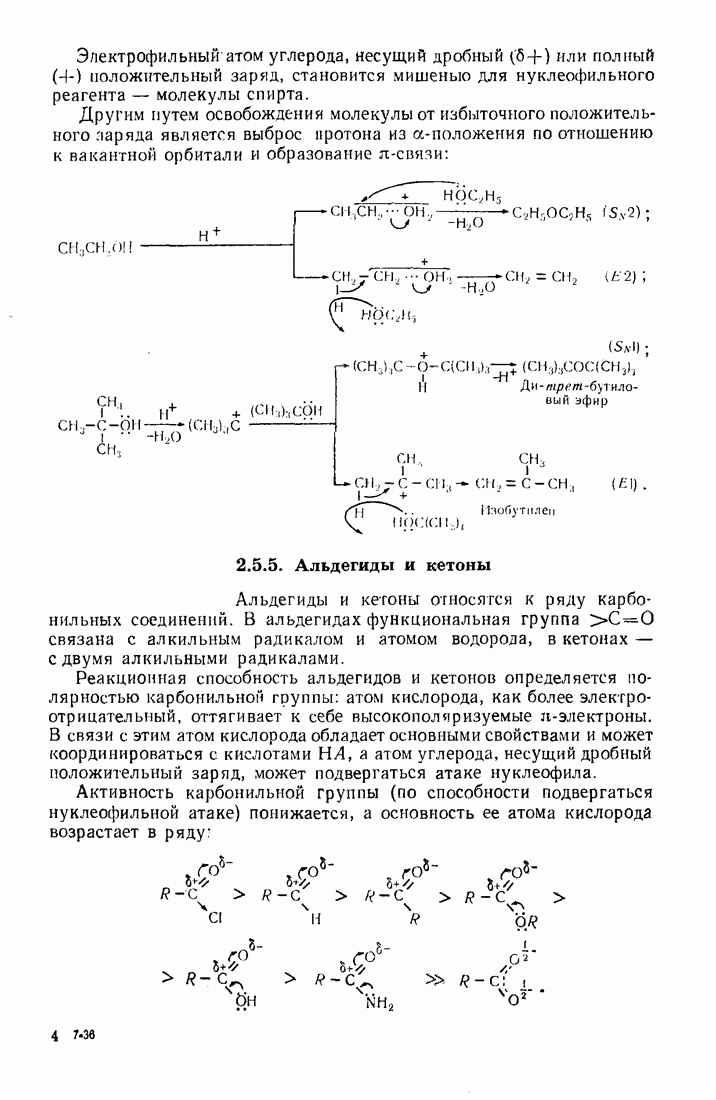
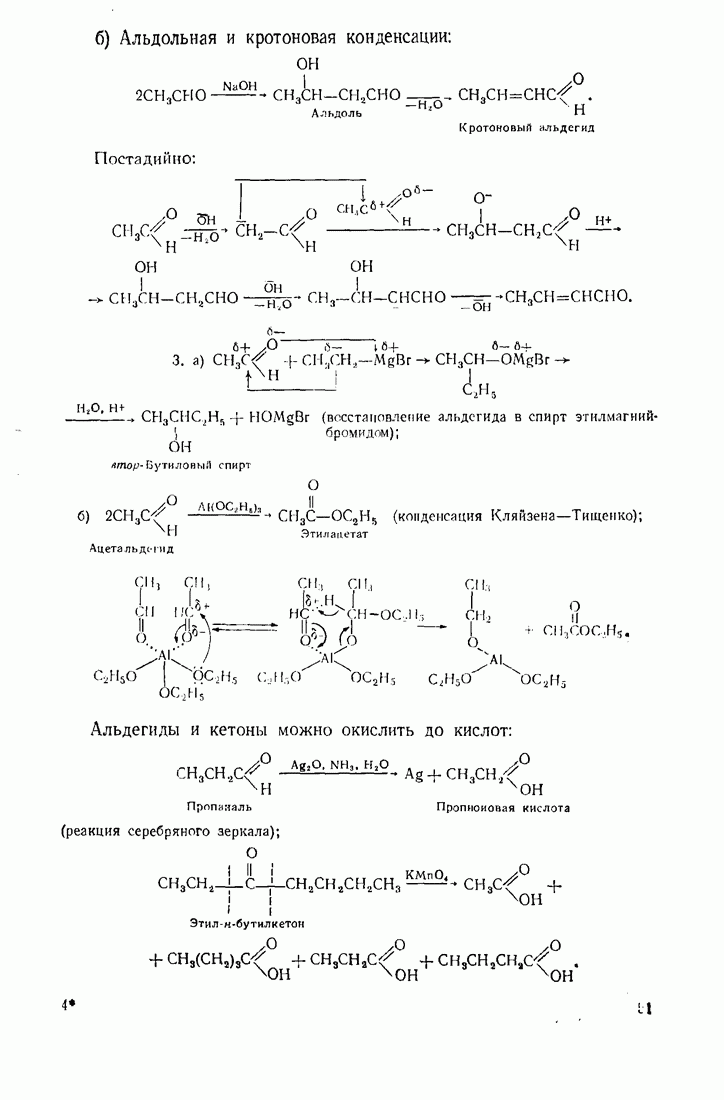
- 2.5.5. Альдегиды и кетоны
- 2.5.6. Карбоновые кислоты (R-СООН) и их производные (R-СО-X)
- 2.5.7. Амины (NH2R, NHR2, NR3)
- 3. Реакционная способность соединений алифатического ряда
- 3.1. Алканы (насыщенные углеводороды)
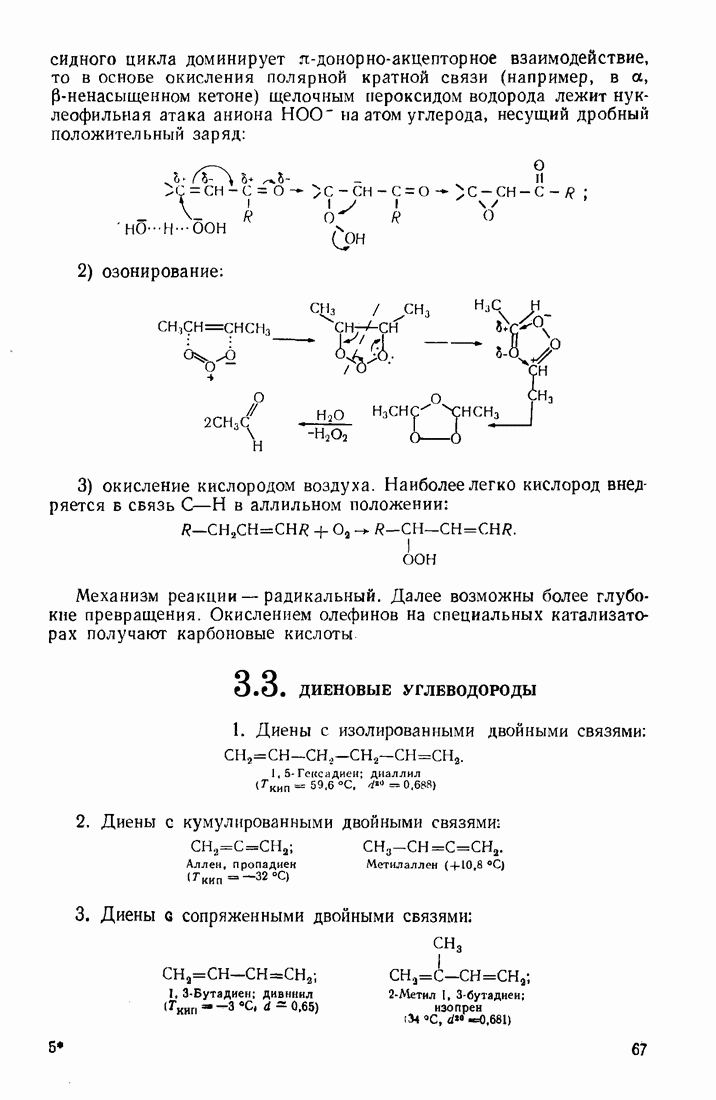
- 3.2. АЛКЕНЫ (ОЛЕФИНЫ)
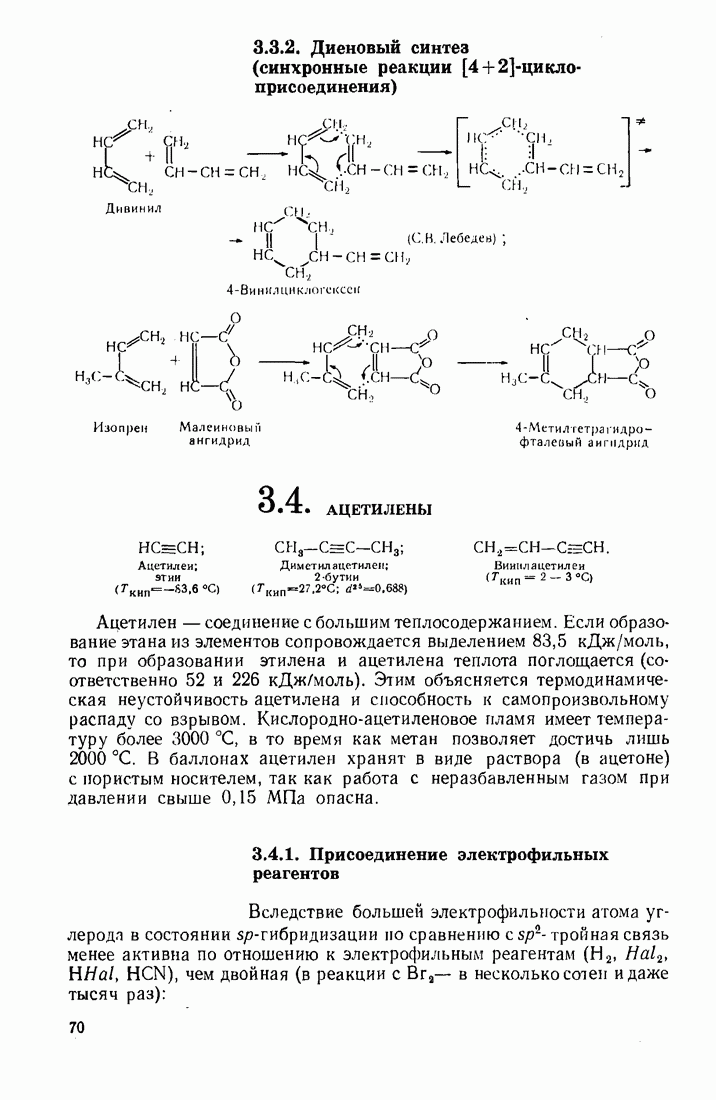
- 3.3. ДИЕНОВЫЕ УГЛЕВОДОРОДЫ
- 3.4. АЦЕТИЛЕНЫ
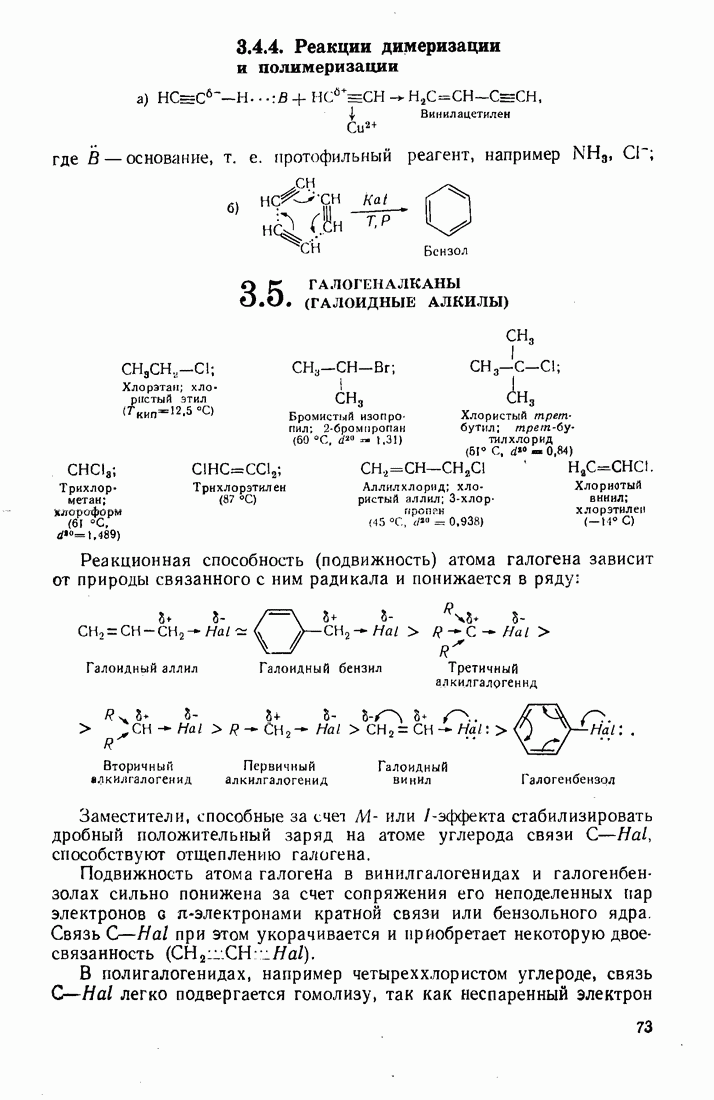
- 3.5. ГАЛОГЕНАЛКАНЫ (ГАЛОИДНЫЕ АЛКИЛЫ)
- 3.6. СПИРТЫ
- 3.7. ПРОСТЫЕ ЭФИРЫ (R-O-R)
- 3.8. ОКСИРАНЫ (ЭПОКСИДНЫЕ СОЕДИНЕНИЯ, a-ОКИСИ)
- 3.9. АЛЬДЕГИДЫ И КЕТОНЫ
- 3.10. КАРБОНОВЫЕ КИСЛОТЫ
- 3.11. НЕКОТОРЫЕ ПРОИЗВОДНЫЕ КИСЛОТ
- 3.12. АМИНЫ
- 3.13. ФОСФОРОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- 3.14. СЕРООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- 3.15. ОРГАНИЧЕСКИЕ ПЕРЕКИСИ (ПЕРОКСИДНЫЕ СОЕДИНЕНИЯ)
- 3.16. ПРОИЗВОДНЫЕ УГОЛЬНОЙ КИСЛОТЫ
- 3.17. ГЕТЕРОАНАЛОГИ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ
- 3.18. АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- 3.18.2. Пространственное расположение и напряженность циклов
- 3.18.3. Особенности химических свойств алициклических соединений
- 4. Полифункциональные производные алифатического ряда
- 4.1. ДВУХОСНОВНЫЕ КАРБОНОВЫЕ КИСЛОТЫ
- 4.2. НЕПРЕДЕЛЬНЫЕ КИСЛОТЫ
- 4.3. ОКСОКИСЛОТЫ (АЛЬДЕГИДО- И КЕТОКИСЛОТЫ)
- 4.4. ОКСИКИСЛОТЫ. ПОНЯТИЕ ОБ ОПТИЧЕСКОЙ ИЗОМЕРИИ
- 4.5. УГЛЕВОДЫ
- 4.5.2. Стереохимия моносахаридов
- 4.5.3. Дисахариды
- 4.5.4. Полисахариды
- 4.5.5. Нахождение в природе и пути превращения углеводов
- 4.6. АМИНОКИСЛОТЫ
- 5. Методы синтеза органических юединений алифатическою рада
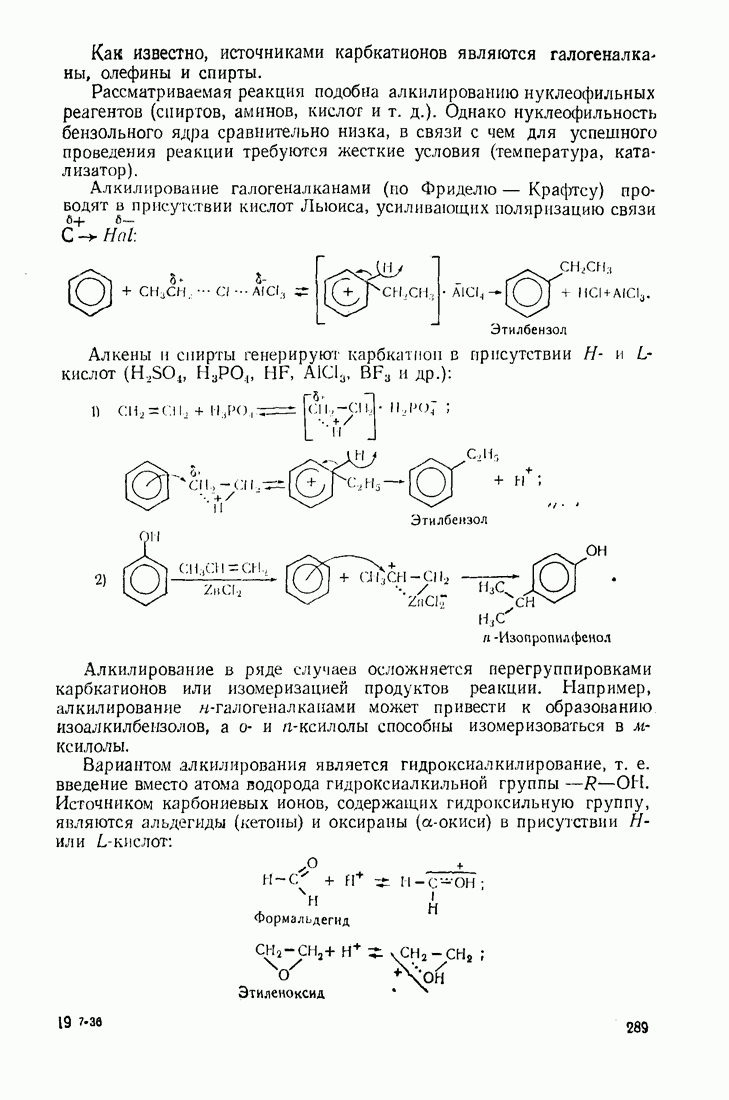
- 5.1. АЛКИЛИРОВАНИЕ
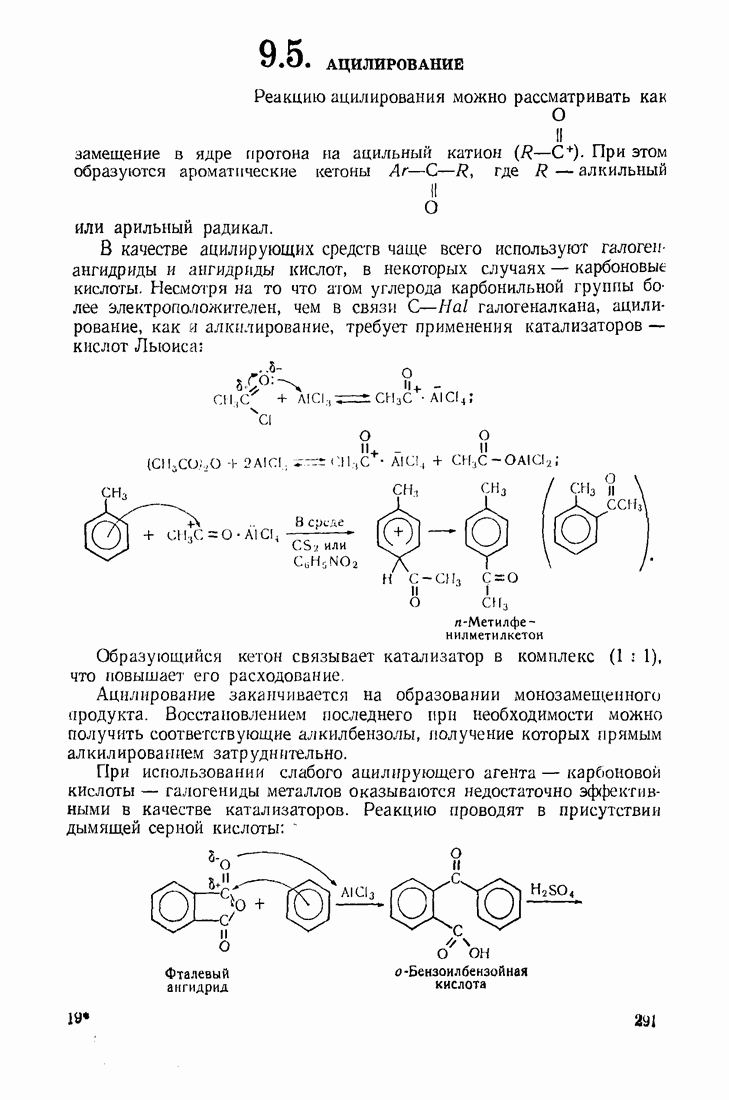
- 5.2. АЦИЛИРОВАНИЕ
- 5.3. ГАЛОГЕНИРОВАНИЕ
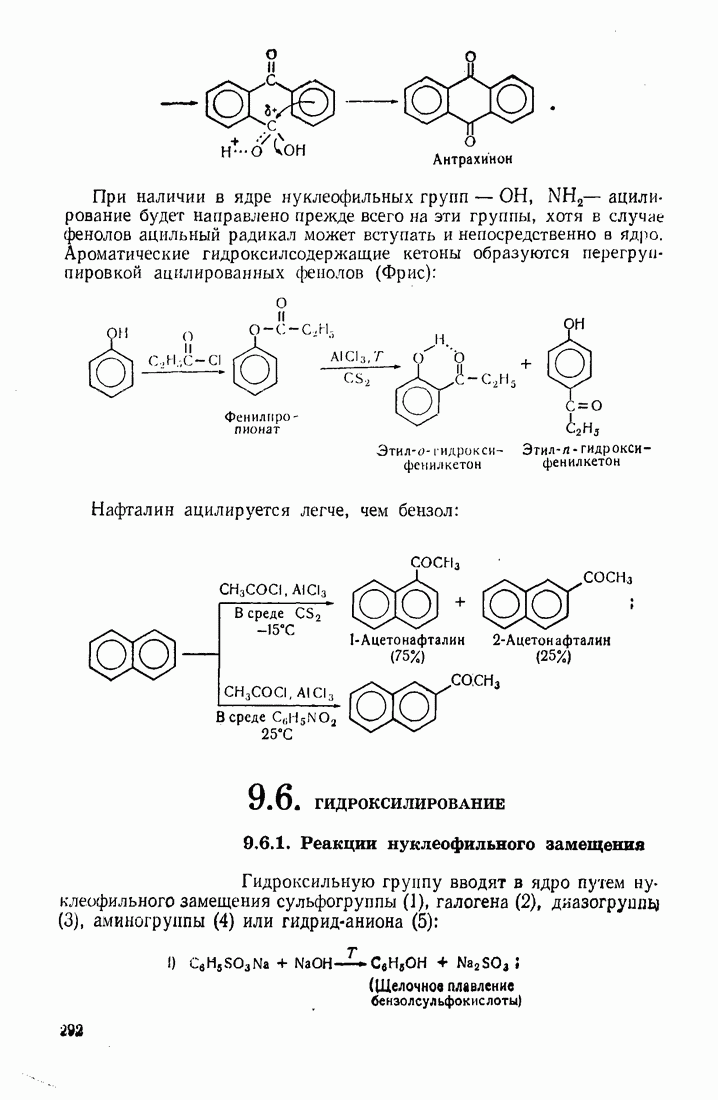
- 5.4. ГИДРОКСИЛИРОВАНИЕ
- 5.5. КАРБОНИЛИРОВАНИЕ (ВВЕДЕНИЕ КАРБОНИЛЬНОЙ ГРУППЫ)
- 5.6. КАРБОКСИЛИРОВАНИЕ
- 5.7. ЭПОКСИДИРОВАНИЕ (ОКСИРАНИРОВАИИЕ)
- 5.8. АМИНИРОВАНИЕ
- 5.9. ОКИСЛЕНИЕ
- 5.10. ВОССТАНОВЛЕНИЕ
- 5.11. АЛКАНЫ
- 5.12 АЛКЕНЫ
- 5.13. ДИЕНОВЫЕ УГЛЕВОДОРОДЫ (1,3-ДИЕНЫ)
- 5.14. АЦЕТИЛЕНЫ
- 5.15 АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- 5.16. ГАЛОГЕН АЛКАНЫ
- 5.17. СПИРТЫ
- 5.18. АЛЬДЕГИДЫ И КЕТОНЫ
- 5.19. КАРБОНОВЫЕ КИСЛОТЫ
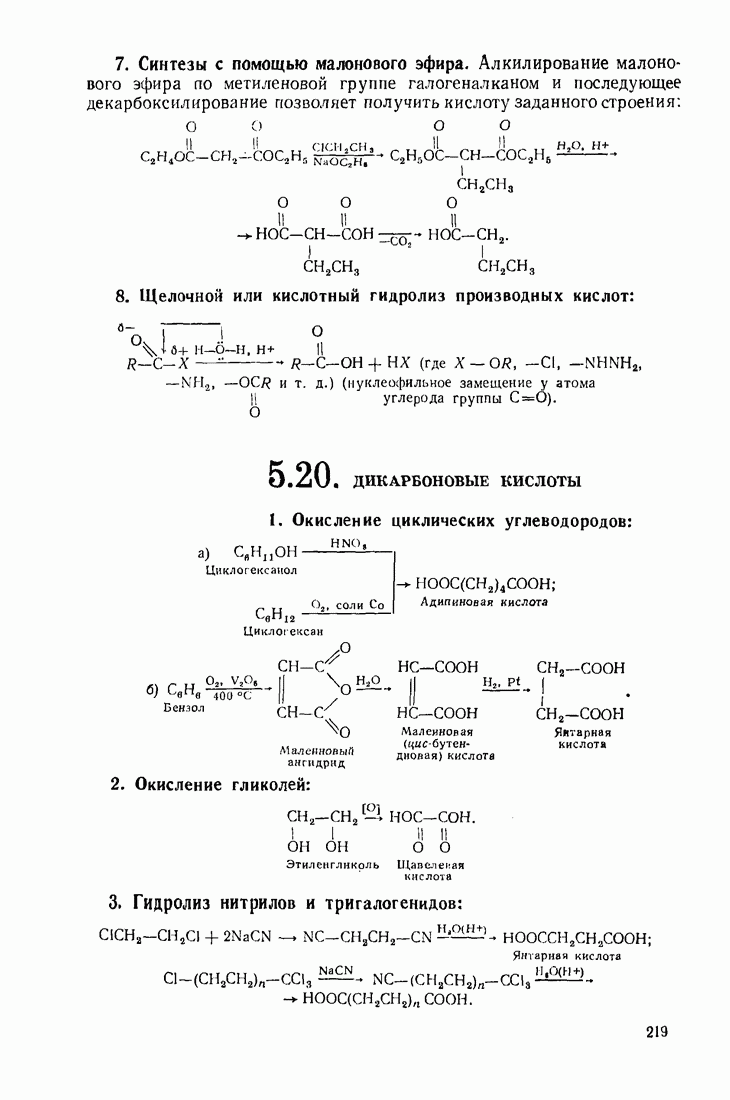
- 5.20. ДИКАРБОНОВЫЕ КИСЛОТЫ
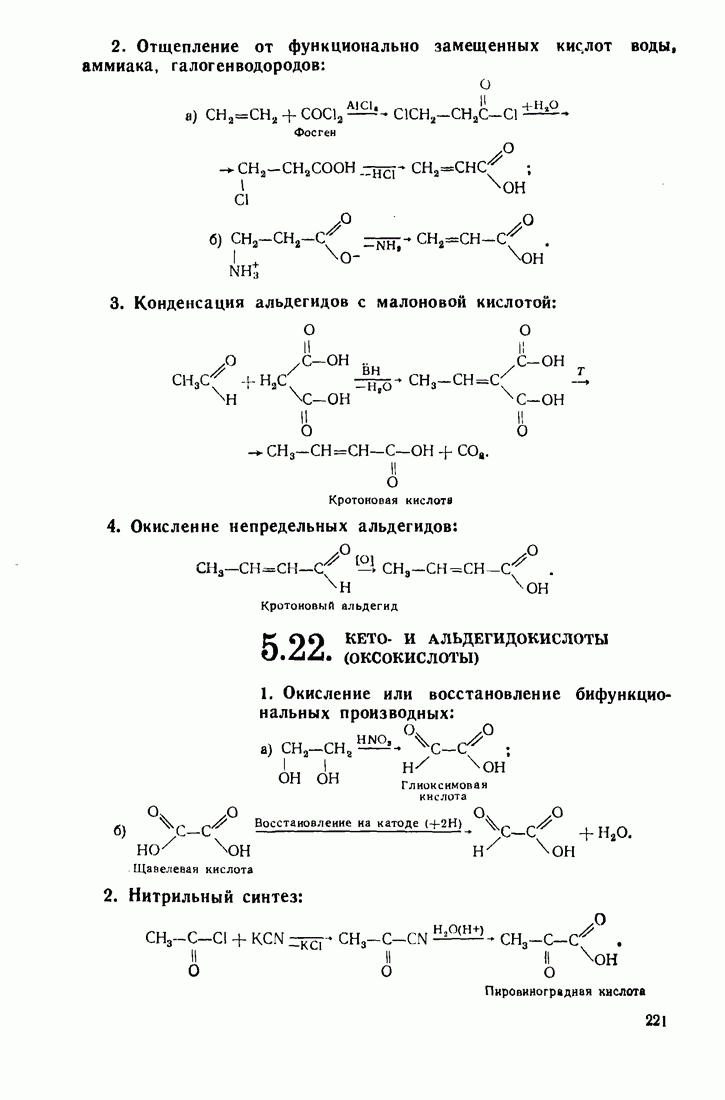
- 5.21. НЕПРЕДЕЛЬНЫЕ КИСЛОТЫ
- 5.22. КЕТО- И АЛЬДЕГИДОКИСЛОТЫ (ОКСОКИСЛОТЫ)
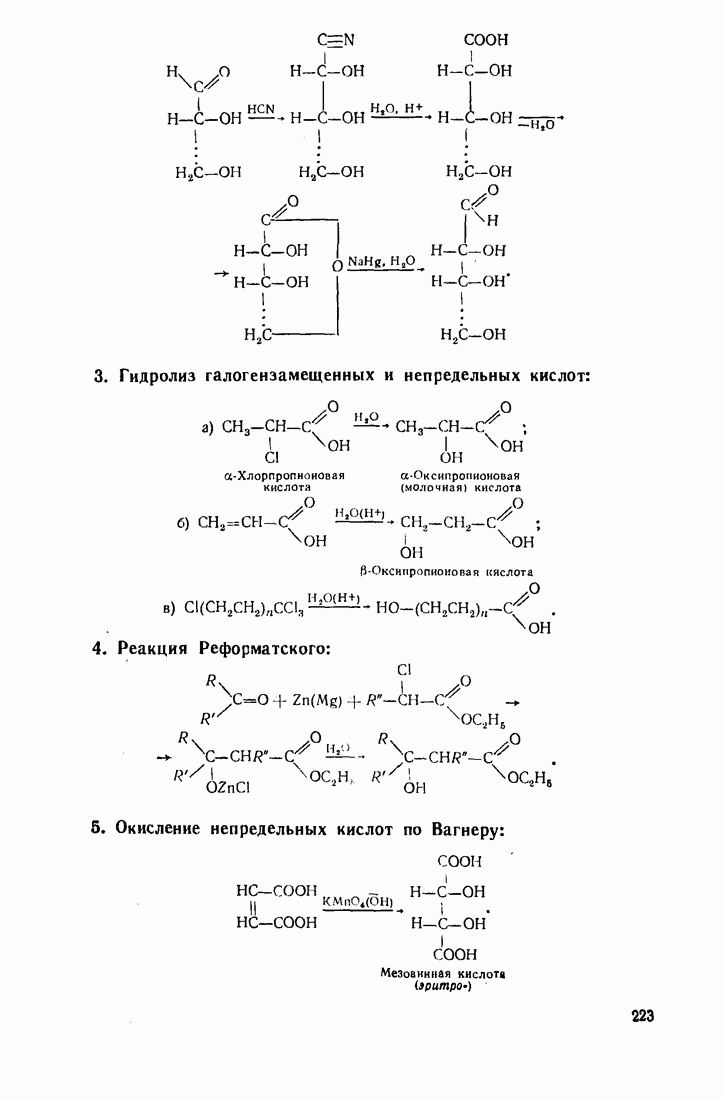
- 5.23. ОКСИКИСЛОТЫ
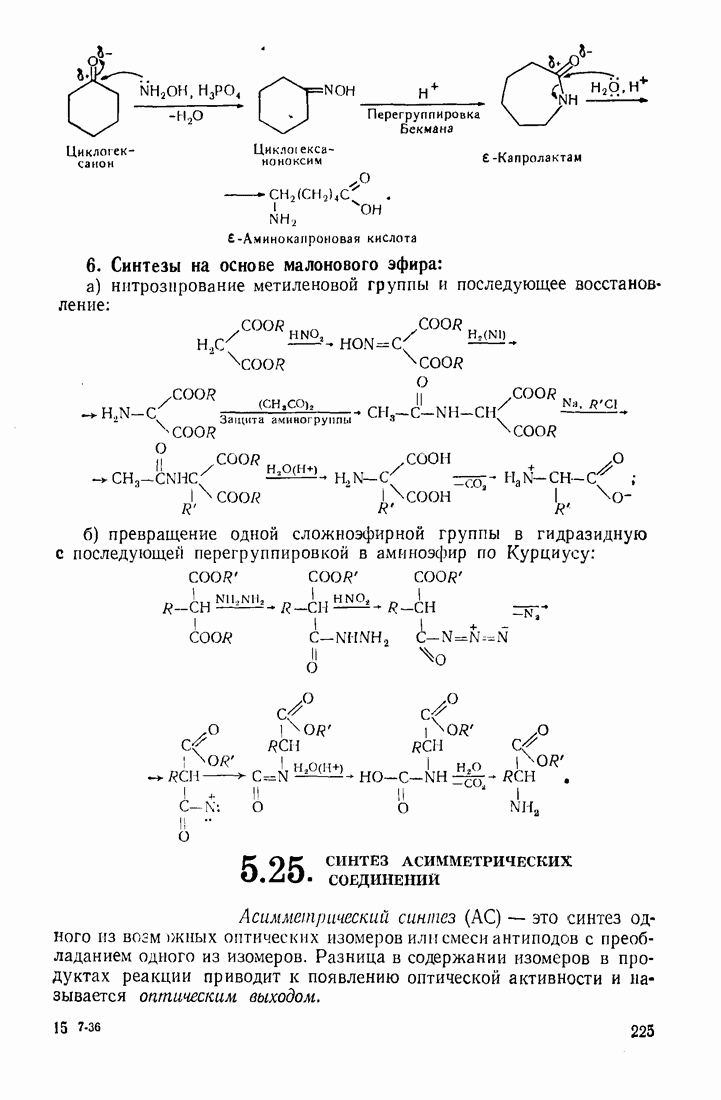
- 5.24. АМИНОКИСЛОТЫ
- 5.25 СИНТЕЗ АСИММЕТРИЧЕСКИХ СОЕДИНЕНИЙ
- 6. Некоторые понятия физической органической химии
- 6.1. СВЯЗЬ СОСТАВА И СТРОЕНИЯ СОЕДИНЕНИЙ С ФИЗИЧЕСКИМИ СВОЙСТВАМИ
- 6.2. ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 6.3. КИСЛОТЫ И ОСНОВАНИЯ В ОРГАНИЧЕСКОЙ ХИМИИ
- 6.4. ОРГАНИЧЕСКИЕ РАСТВОРИТЕЛИ И ИХ ВЛИЯНИЕ НА СКОРОСТЬ И МЕХАНИЗМ РЕАКЦИЙ
- 6.5. КАТАЛИЗ ОРГАНИЧЕСКИХ РЕАКЦИЙ
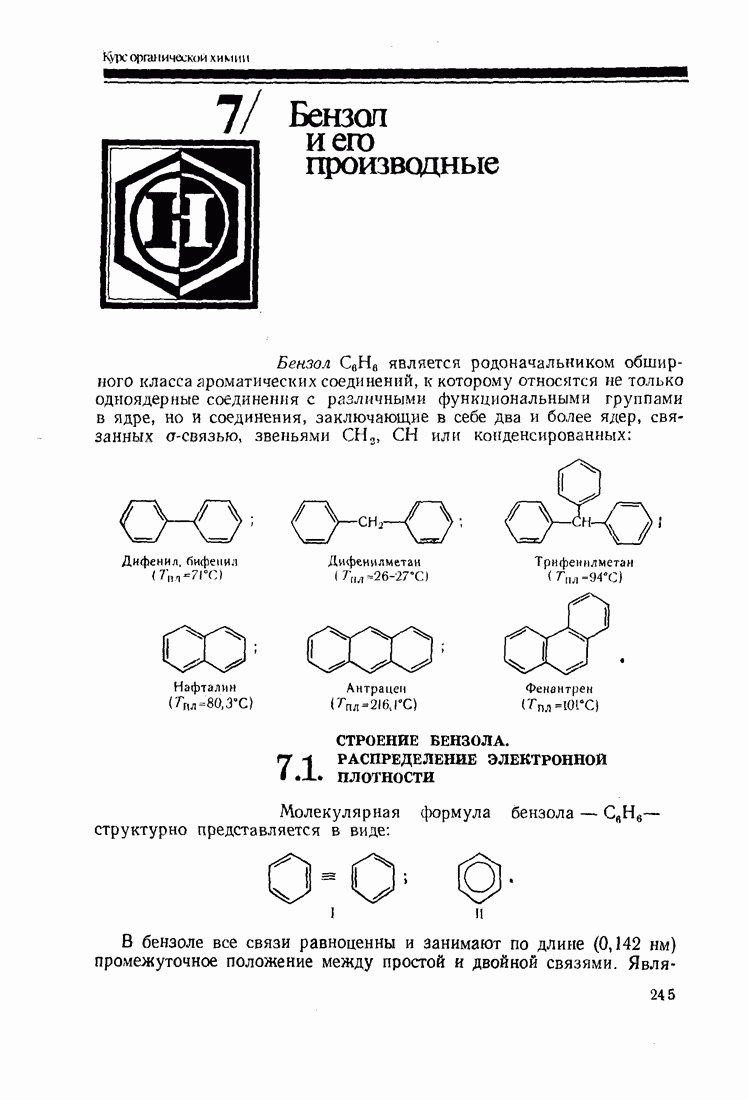
- 7. Бензол и его производные
- 7.1. СТРОЕНИЕ БЕНЗОЛА. РАСПРЕДЕЛЕНИЕ ЭЛЕКТРОННОЙ ПЛОТНОСТИ
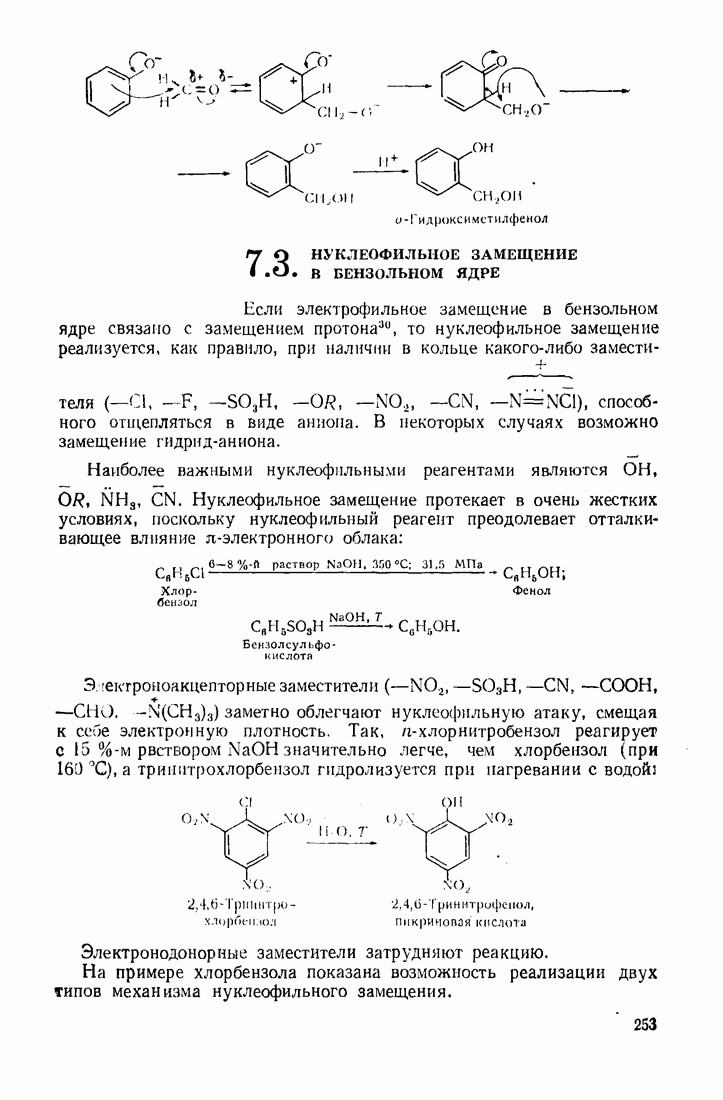
- 7.2. ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ В БЕНЗОЛЬНОМ ЯДРЕ
- 7.3. НУКЛЕОФИЛЬНОЕ ЗАМЕЩЕНИЕ В БЕНЗОЛЬНОМ ЯДРЕ
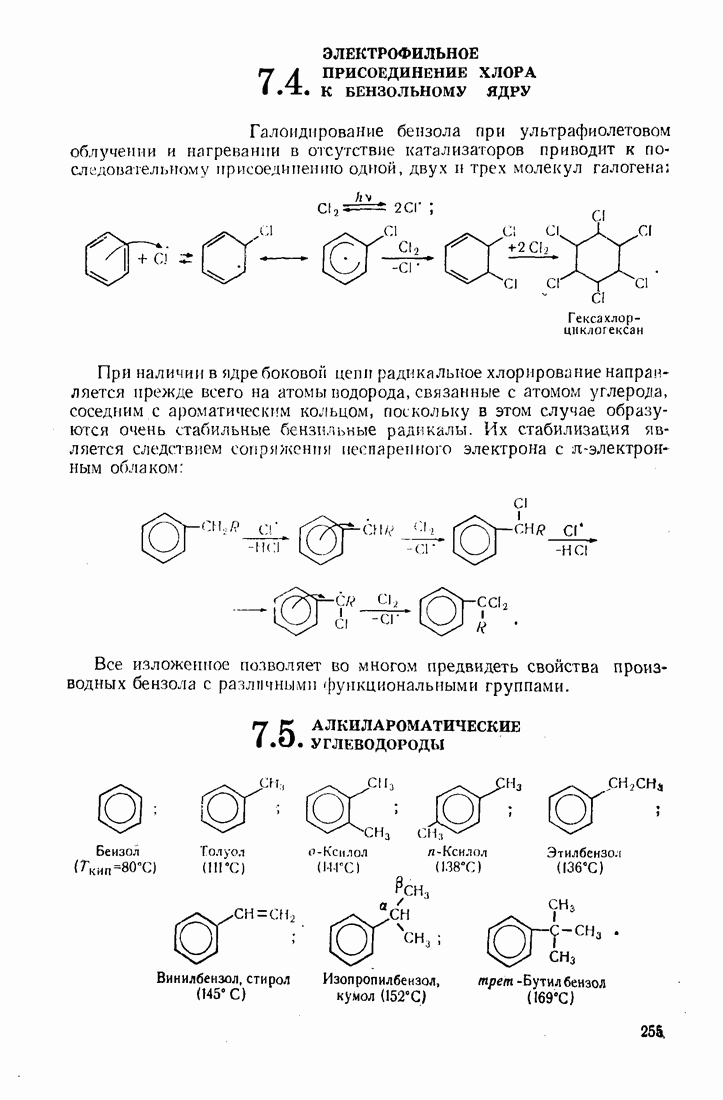
- 7.4. ЭЛЕКТРОФИЛЬНОЕ ПРИСОЕДИНЕНИЕ ХЛОРА К БЕНЗОЛЬНОМУ ЯДРУ
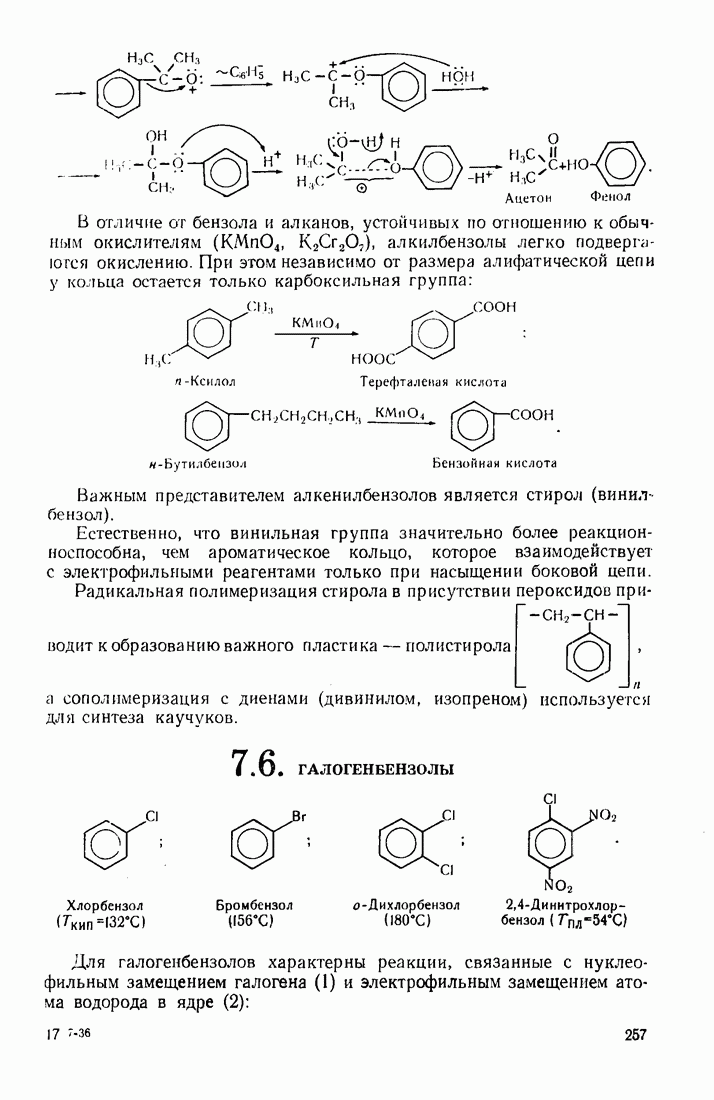
- 7.5. АЛКИЛАРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ
- 7.6. ГАЛОГЕНБЕНЗОЛЫ
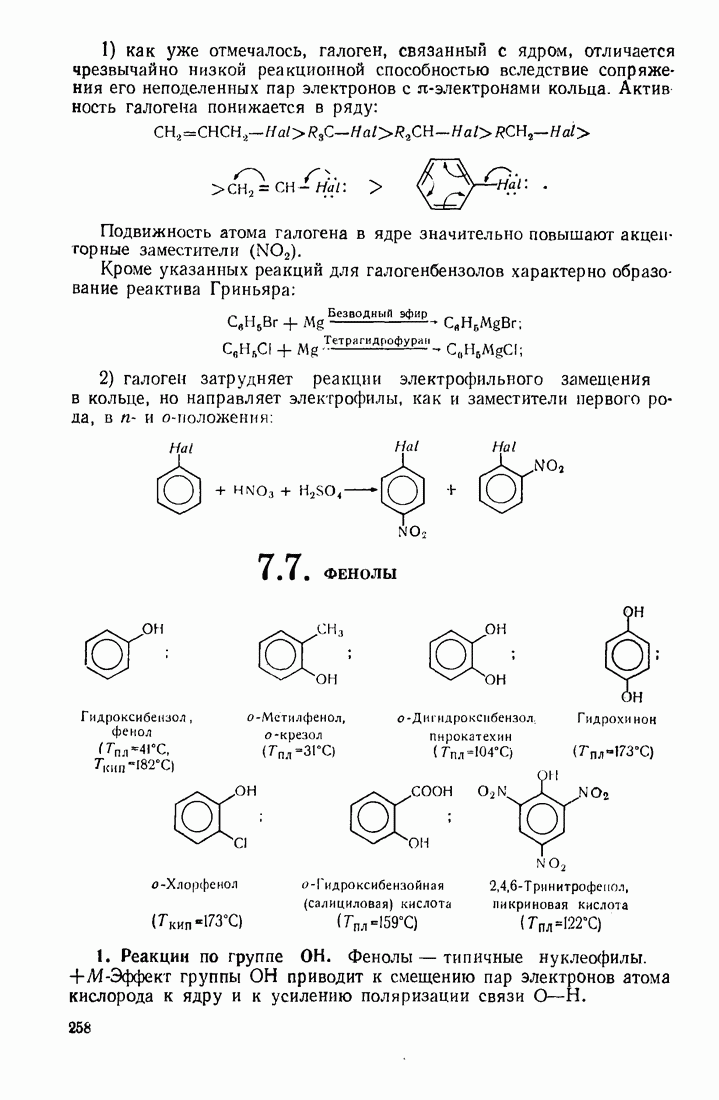
- 7.7. ФЕНОЛЫ
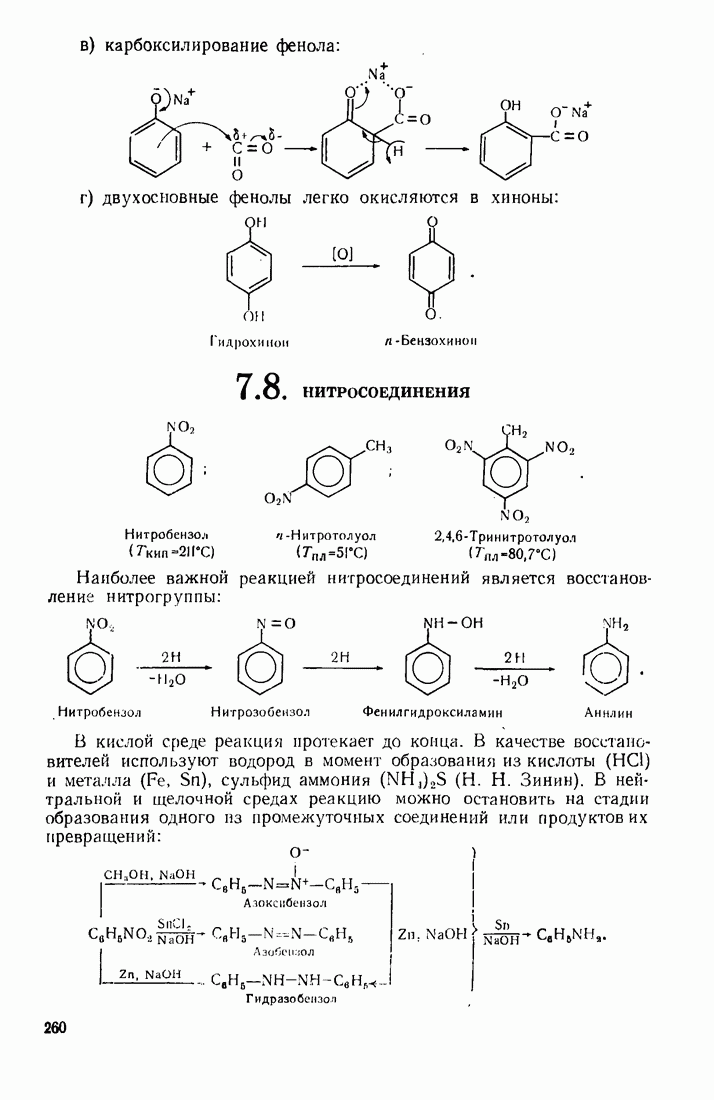
- 7.8. НИТРОСОЕД ИНЕНИЯ
- 7.9. АРОМАТИЧЕСКИЕ АМИНЫ
- 7.10. ДИАЗОСОЕДИНЕНИЯ
- 7.11. АЗОСОЕДИНЕНИЯ
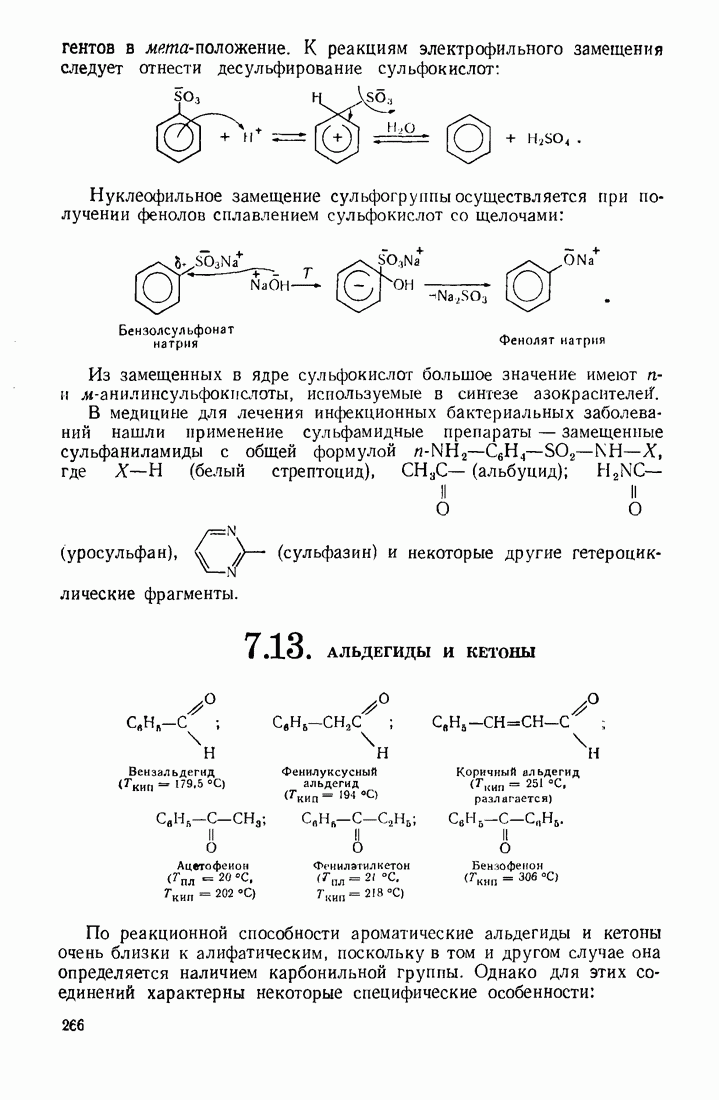
- 7.12. СУЛЬФОКИСЛОТЫ
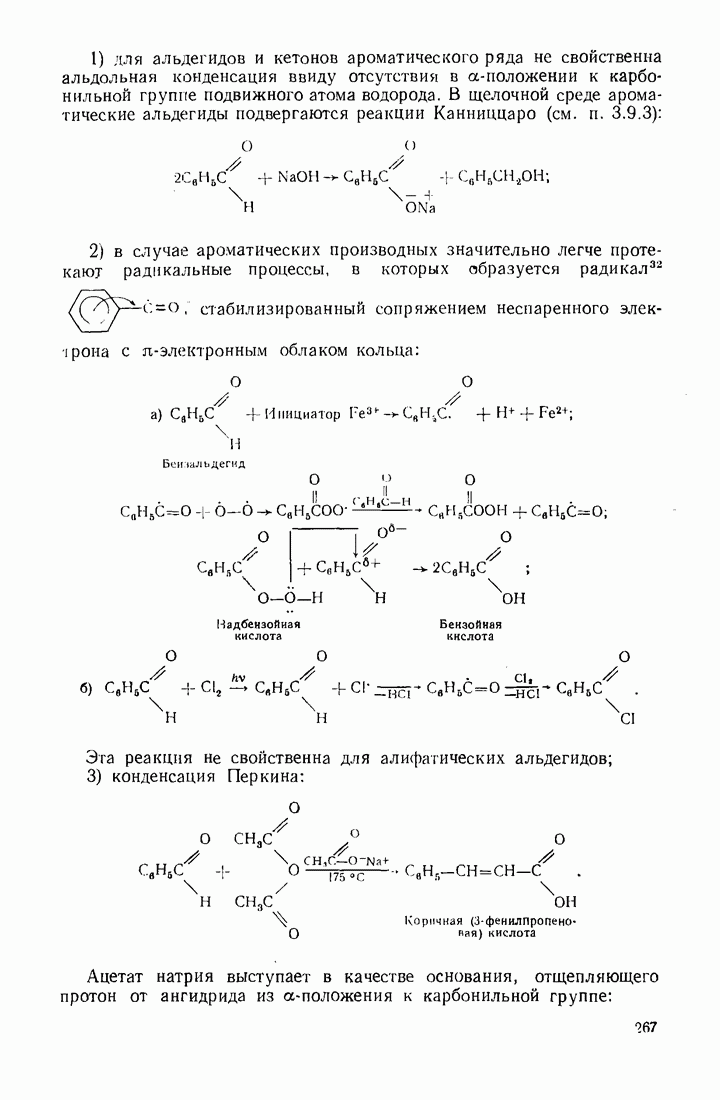
- 7.13. АЛЬДЕГИДЫ И КЕТОНЫ
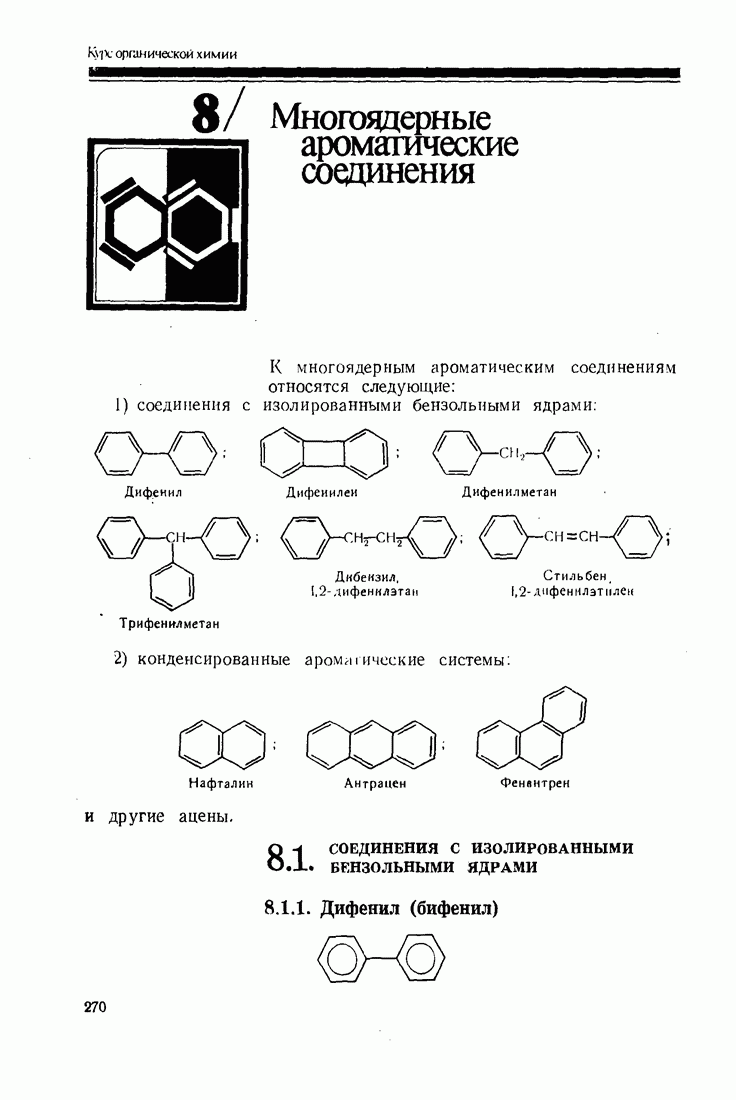
- 8. Многоядерные ароматические соединения
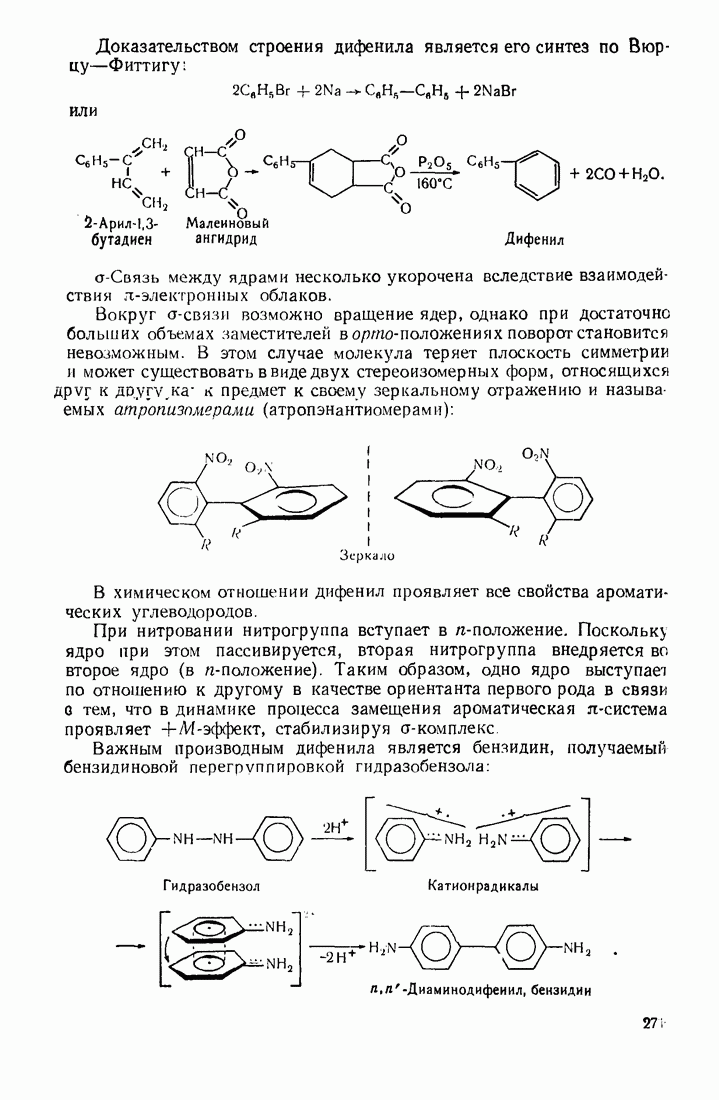
- 8.1. СОЕДИНЕНИЯ С ИЗОЛИРОВАННЫМИ БЕНЗОЛЬНЫМИ ЯДРАМИ
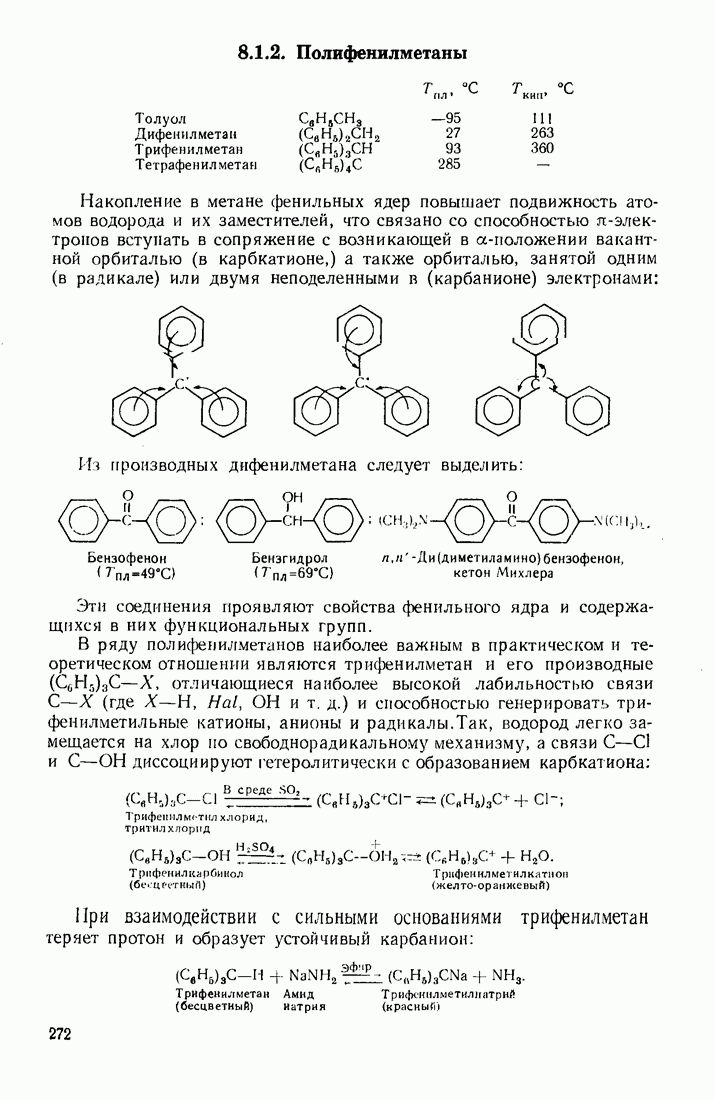
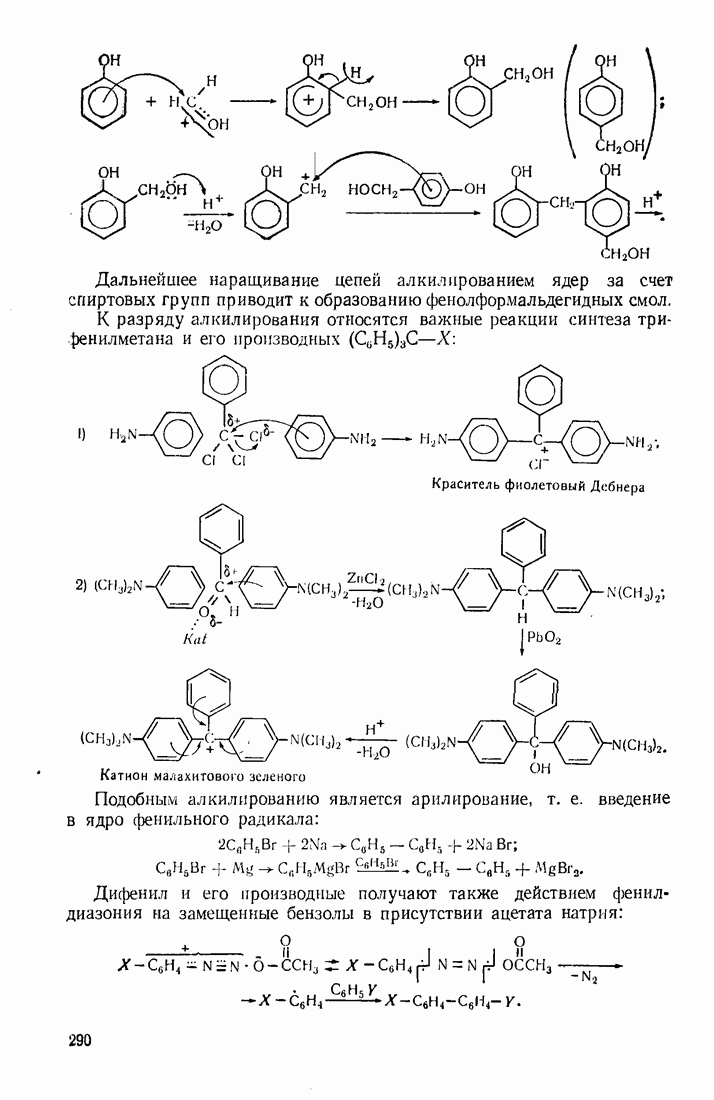
- 8.1.2. Полифенилметаны
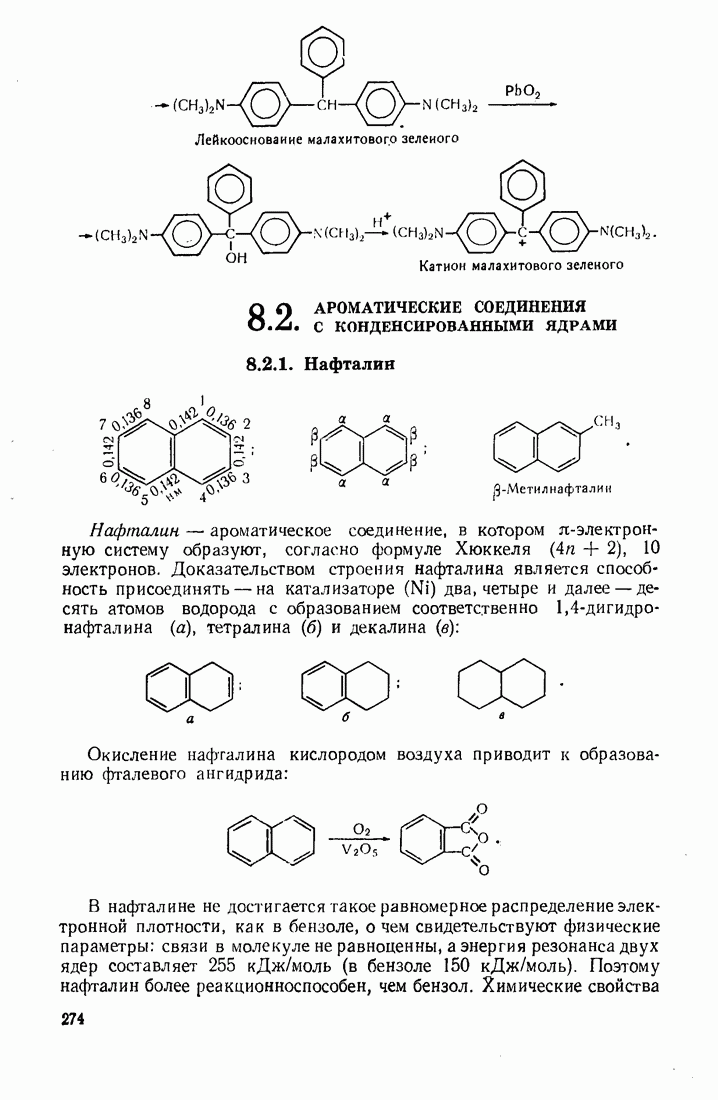
- 8.2. АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ С КОНДЕНСИРОВАННЫМИ ЯДРАМИ
- 8.2.2. Антрацен
- 8.2.3. Фенантрен
- 9. Методы синтеза в ряду ароматических соединений
- 9.1. ГАЛОГЕНИРОВАНИЕ
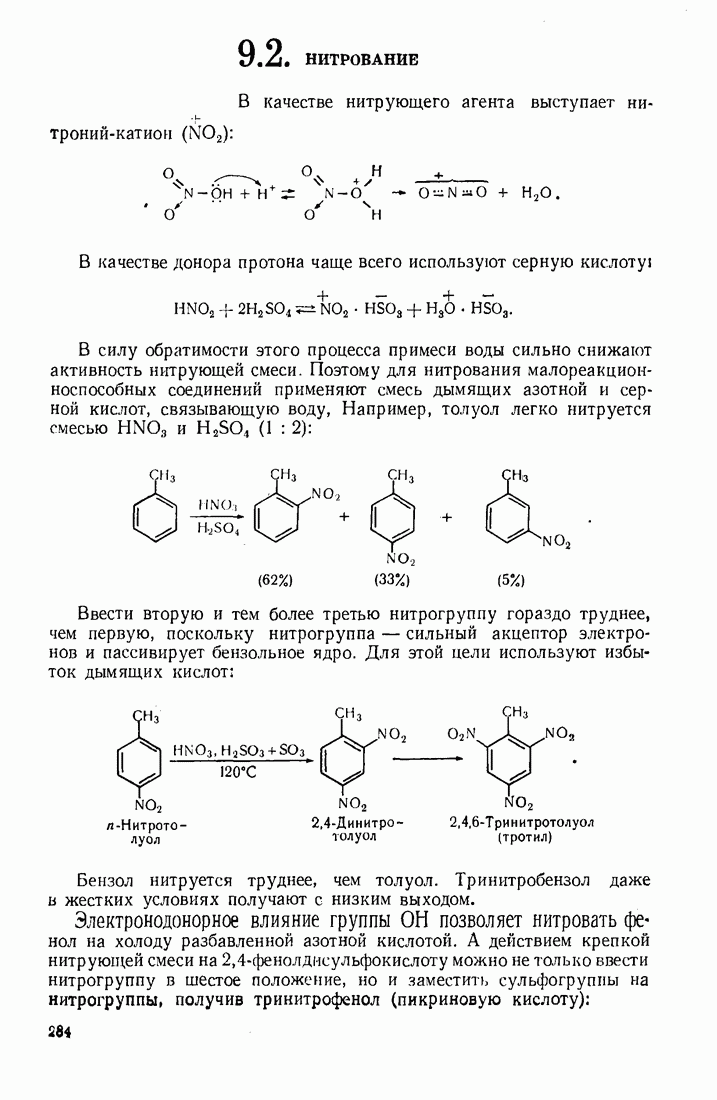
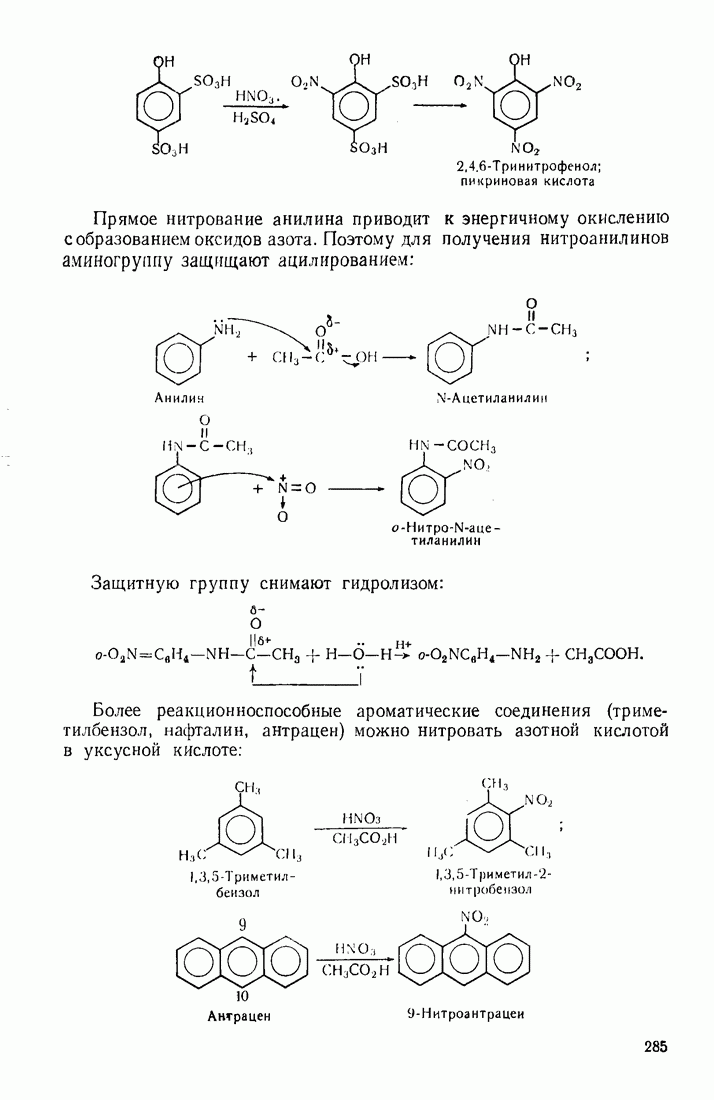
- 9.2. НИТРОВАНИЕ
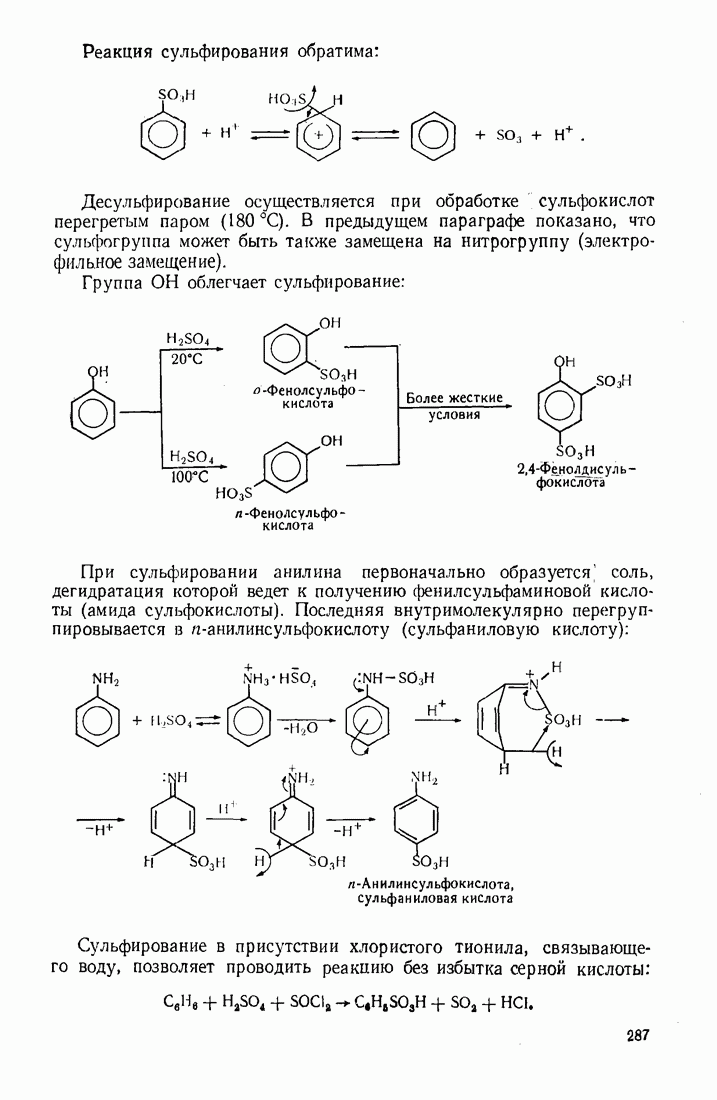
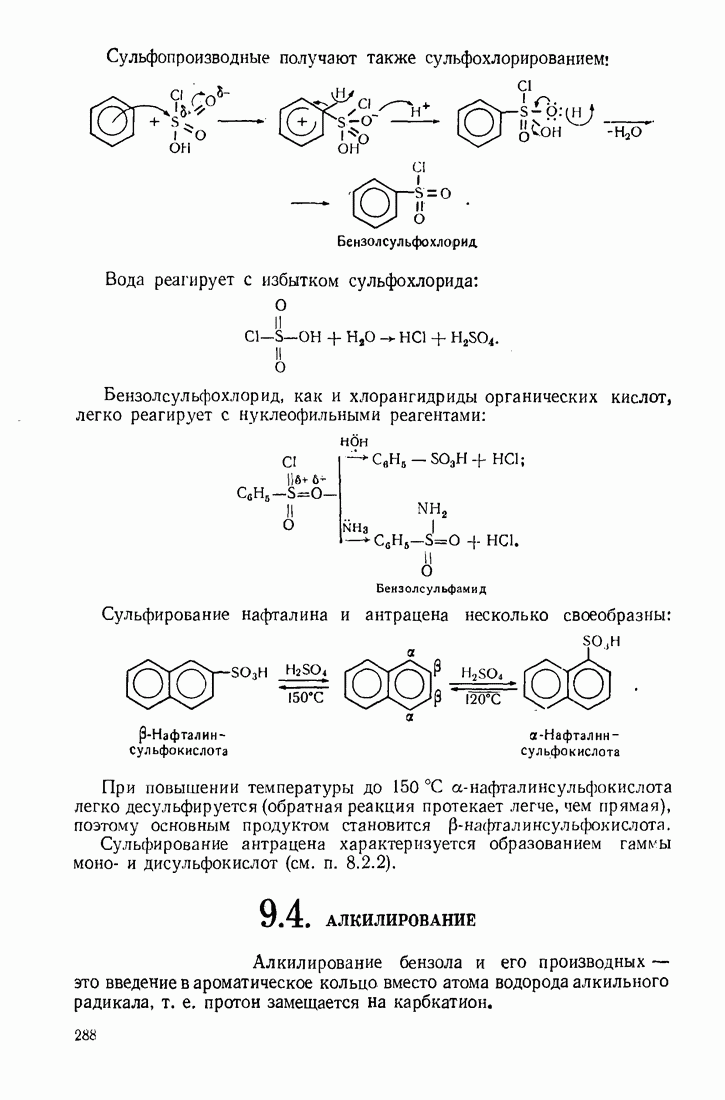
- 9.3. СУЛЬФИРОВАНИЕ
- 9.4. АЛКИЛИРОВАНИЕ
- 9.5. АЦИЛИРОВАНИЕ
- 9.6. ГИДРОКСИЛИРОВАНИЕ
- 9.7. АМИНИРОВАНИЕ
- 9.8. НИТРОЗИРОВАНИЕ
- 9.9. КАРБОНИЛИРОВАНИЕ
- 9.10. КАРБОКСИЛИРОВАНИЕ
- 9.11. ОКИСЛЕНИЕ
- 9.12. ВОССТАНОВЛЕНИЕ
- 10. Гетероциклические соединения
- 10.2. ОБЩАЯ ХАРАКТЕРИСТИКА СТРОЕНИЯ И РЕАКЦИОННОЙ СПОСОБНОСТИ
- 10.3. ПЯТИ- И ШЕСТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С ОДНИМ ГЕТЕРОАТОМОМ
- 10.4. ГЕТЕРОЦИКЛЫ С НЕСКОЛЬКИМИ ГЕТЕРОАТОМАМИ
- 10.5. МЕТОДЫ СИНТЕЗА ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ
- 10.6. П0НЯТИЕ О ПРИРОДНЫХ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЯХ
- 11. Зпементоорганические соединения
- 11.2. ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ НЕКОТОРЫХ НЕМЕТАЛЛОВ
- 11.3. МЕГАЛЛООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- 11.4. ОРГАНИЧЕСКИЕ ПРОИЗВОДНЫЕ ПЕРЕХОДНЫХ МЕТАЛЛОВ
- 12. Сырье и основные направления развития промышленности органического синтеза
- 12.1.1. Нефть и сопутствующий природный газ
- 12.1.2. Углехимическое сырье
- 12.1.3. Лесохимическое и сельскохозяйственное сырье
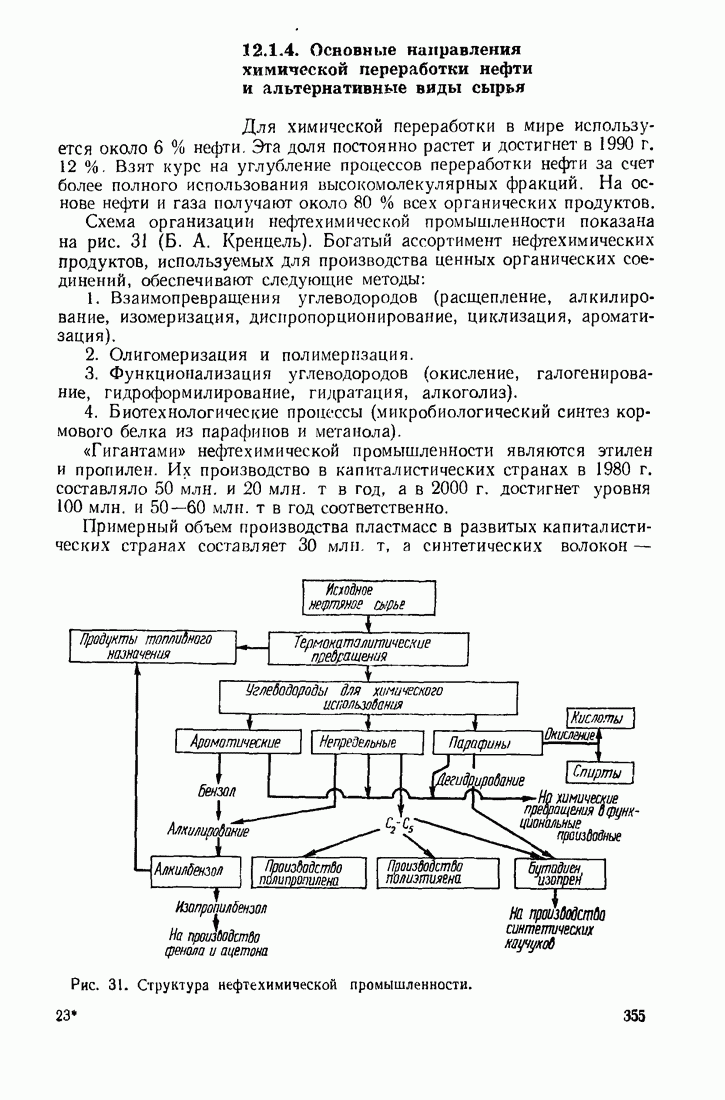
- 12.1.4. Основные направления химической переработки нефти и альтернативные виды сырья
- 12.2. ПУТИ ИСПОЛЬЗОВАНИЯ УГЛЕВОДОРОДОВ И ИХ ПРОИЗВОДНЫХ
- 12.3. РАЗВИТИЕ ХИМИЧЕСКОЙ ПРОМЫШЛЕННОСТИ В СССР В ДВЕНАДЦАТОЙ ПЯТИЛЕТКЕ