| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
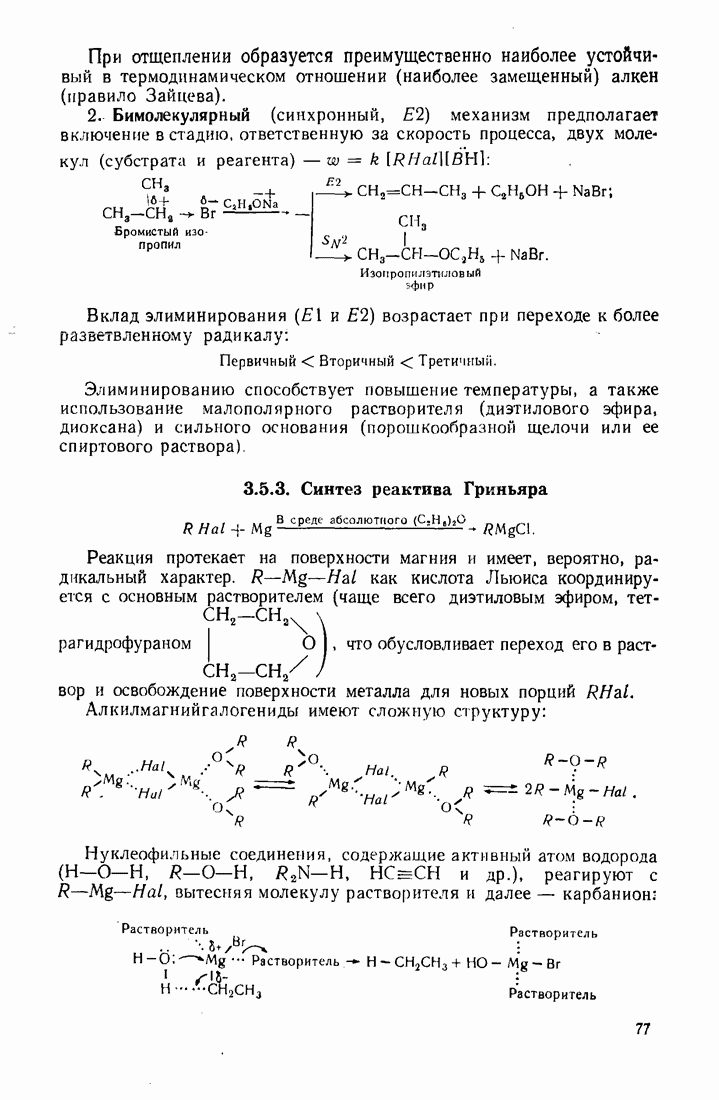
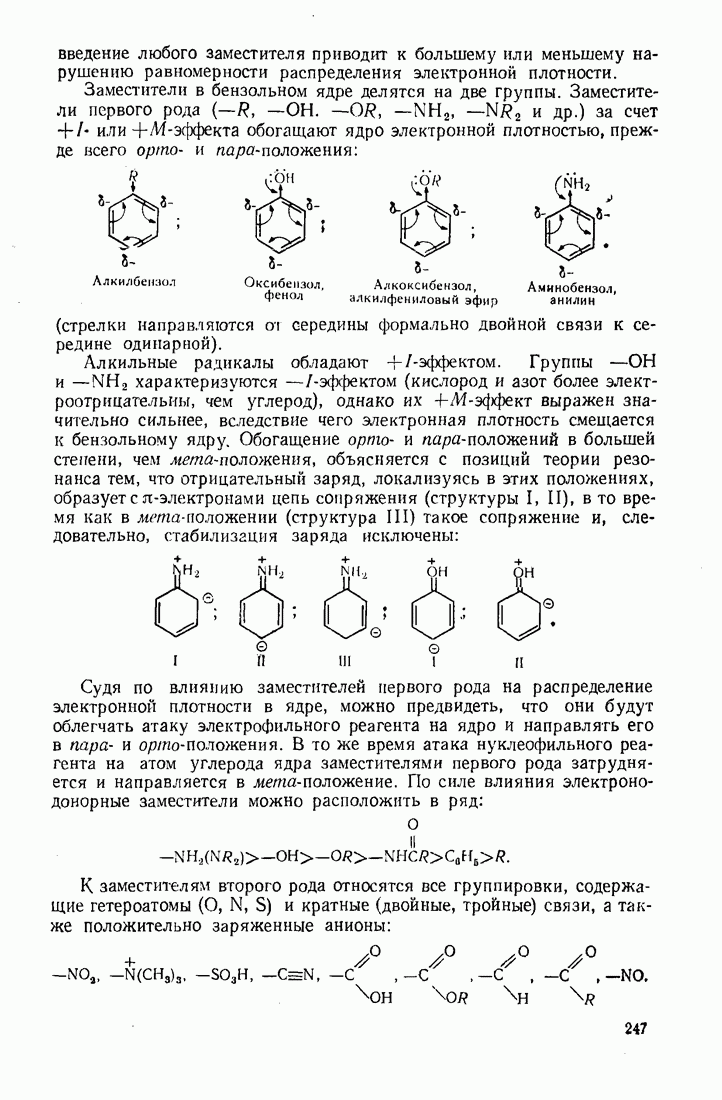
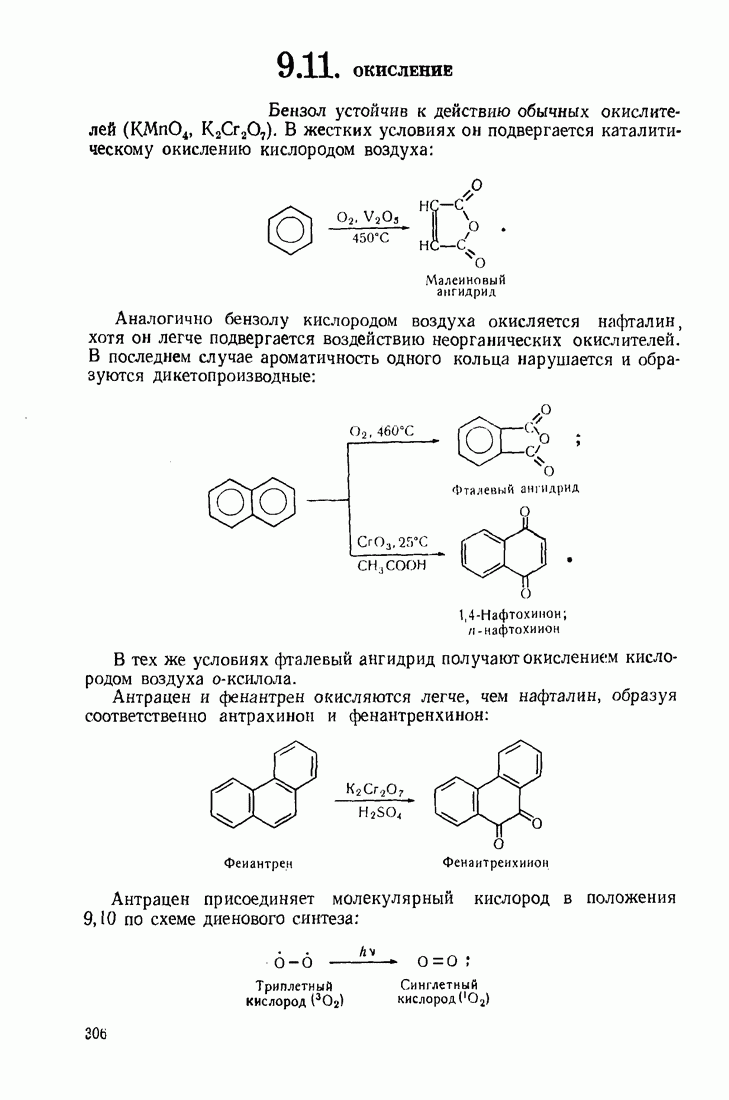
7.2. ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ В БЕНЗОЛЬНОМ ЯДРЕ
Общий механизм:

Электрофильный реагент, обладающий вакантной орбиталью, атакует  -электронное облако, образуя
-электронное облако, образуя  -комплекс. При этом система сопряжения в ядре не нарушается. Далее электрофил принимает пару электронов (из шести) и образует с одним из атомов углерода ядра ковалентную связь (
-комплекс. При этом система сопряжения в ядре не нарушается. Далее электрофил принимает пару электронов (из шести) и образует с одним из атомов углерода ядра ковалентную связь ( -комплекс). В
-комплекс). В  -комплексе один атом углерода пребывает
-комплексе один атом углерода пребывает
в состоянии  -гибридизации, а второй (формально лишившийся
-гибридизации, а второй (формально лишившийся  -связи) приобретает вакантную орбиталь
-связи) приобретает вакантную орбиталь  Сопряжение последней с оставшимися четырьмя
Сопряжение последней с оставшимися четырьмя  -электронами приводит к делокализации и, следовательно, стабилизации положительного заряда. Образовавшийся таким образом циклогексадиенильный катион отщепляет протон (от атома углерода в
-электронами приводит к делокализации и, следовательно, стабилизации положительного заряда. Образовавшийся таким образом циклогексадиенильный катион отщепляет протон (от атома углерода в  -состояиим) и снова превращается в устойчивую ароматическую систему.
-состояиим) и снова превращается в устойчивую ароматическую систему.
Рассматриваемая реакция бензольного ядра в своей начальной стадии напоминает реакцию электрофильного присоединения к кратным связям. На второй стадии вместо присоединения аниона происходит отщепление протона, благодаря чему восстанавливается особэ выгодное в энергетичешлом отношении ароматическое кольцо.
К электрофильным реагентам, способным атаковать бензольное ядро, относятся следующие соединения:
1. Галогены  точнее, положительный конец диполя молекулы. Молекула галогена поляризуется под влиянием субстрата (бензола), растворителя и т. д. Однако эффективно реакция протекает лишь в присутствии катализаторов — кислот Льюиса
точнее, положительный конец диполя молекулы. Молекула галогена поляризуется под влиянием субстрата (бензола), растворителя и т. д. Однако эффективно реакция протекает лишь в присутствии катализаторов — кислот Льюиса  и др.), усиливающих эту поляризацию:
и др.), усиливающих эту поляризацию:
(см. скан)
2. Нитроний-катион  образующийся в смеси азотной и серной кислот (нитрующей смеси):
образующийся в смеси азотной и серной кислот (нитрующей смеси):

или

Серная кислота более сильная, чем азотная, и служит донором протона. Вторым ее назначением в реакции является связывание образующейся воды:

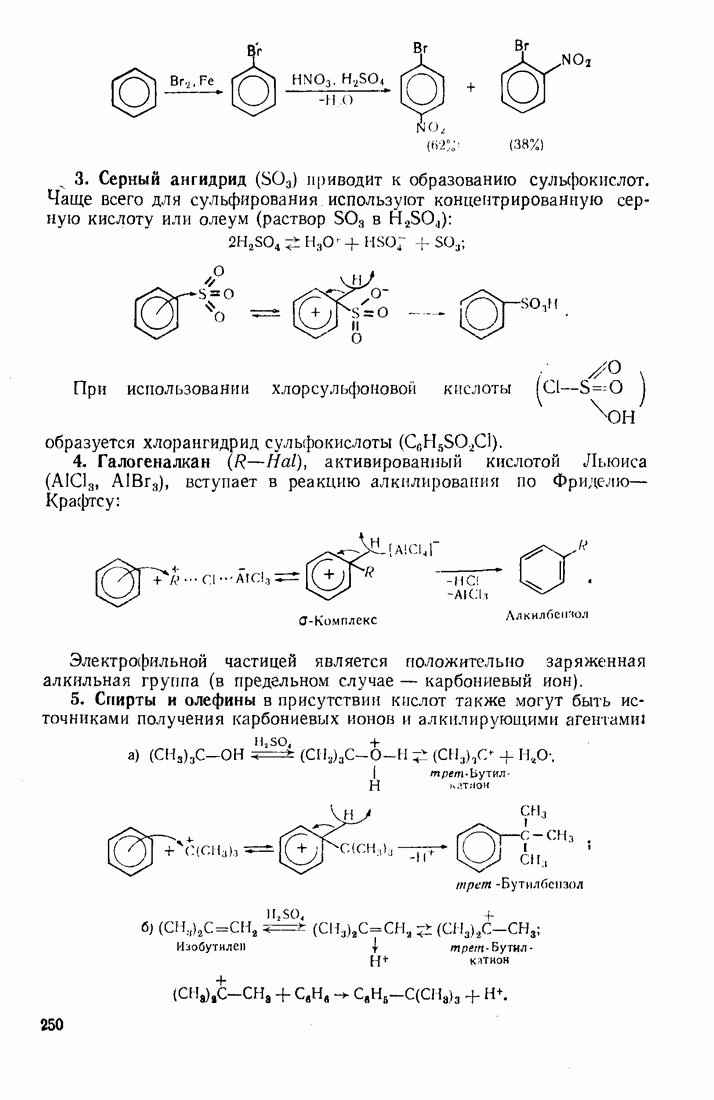
3. Серный ангидрид  приводит к образованию сульфокислот. Чаще всего для сульфирования используют концентрированную серную кислоту или олеум (раствор
приводит к образованию сульфокислот. Чаще всего для сульфирования используют концентрированную серную кислоту или олеум (раствор 

При использовании хлорсульфоновой кислоты 

образуется хлорангидрид сульфокислоты 
4. Галогеналкан  активированный кислотой Льюиса
активированный кислотой Льюиса  вступает в реакцию алкилирования по Фридслю—Крафтсу:
вступает в реакцию алкилирования по Фридслю—Крафтсу:
Электрофильной частицей является положительно заряженная алкильная группа (в предельном случае — карбониевый ион).
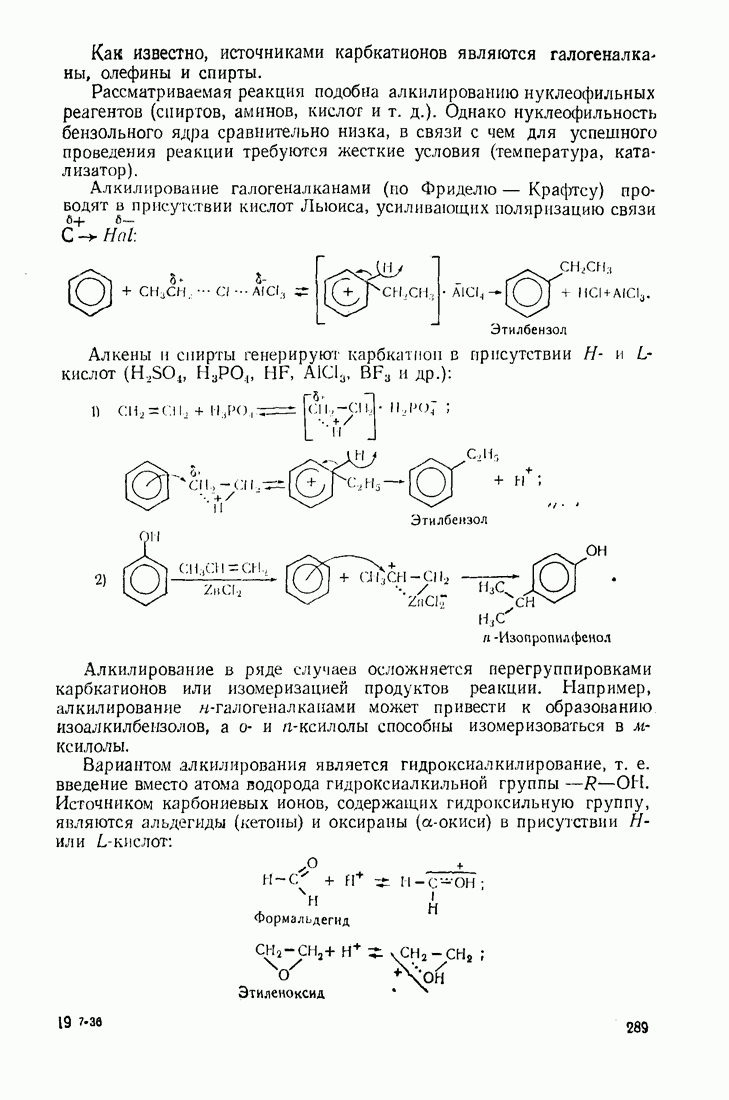
5. Спирты и олефины в присутствии кислот также могут быть источниками получения карбониевых ионов и алкилирующими агентами
(см. скан)
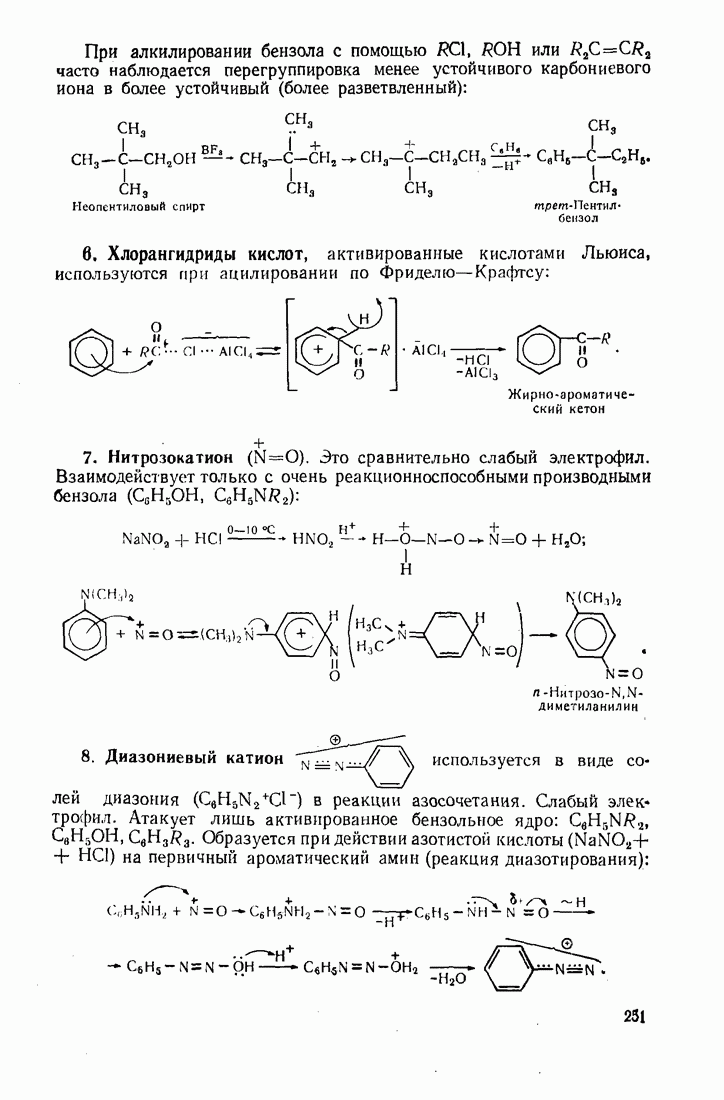
При алкилировании бензола с помощью  или
или  часто наблюдается перегруппировка менее устойчивого карбониевого иона в более устойчивый (более разветвленный):
часто наблюдается перегруппировка менее устойчивого карбониевого иона в более устойчивый (более разветвленный):

6. Хлорангидриды кислот, активированные кислотами Льюиса, используются при ацилировании по Фриделю-Крафтсу:

7. Нитрозокатион  Это сравнительно слабый электрофил. Взаимодействует только с очень peaкционноспособными производными бензола
Это сравнительно слабый электрофил. Взаимодействует только с очень peaкционноспособными производными бензола 

8. Диазониевый катион  используется в виде солей диазония
используется в виде солей диазония  в реакции азосочетания. Слабый электрофил. Атакует лишь активированное бензольное ядро:
в реакции азосочетания. Слабый электрофил. Атакует лишь активированное бензольное ядро:  Образуется при действии азотистой кислоты
Образуется при действии азотистой кислоты  на первичный ароматический амин (реакция диазотирования):
на первичный ароматический амин (реакция диазотирования):

Катион спарен с анионом (например,  ):
):
(см. скан)
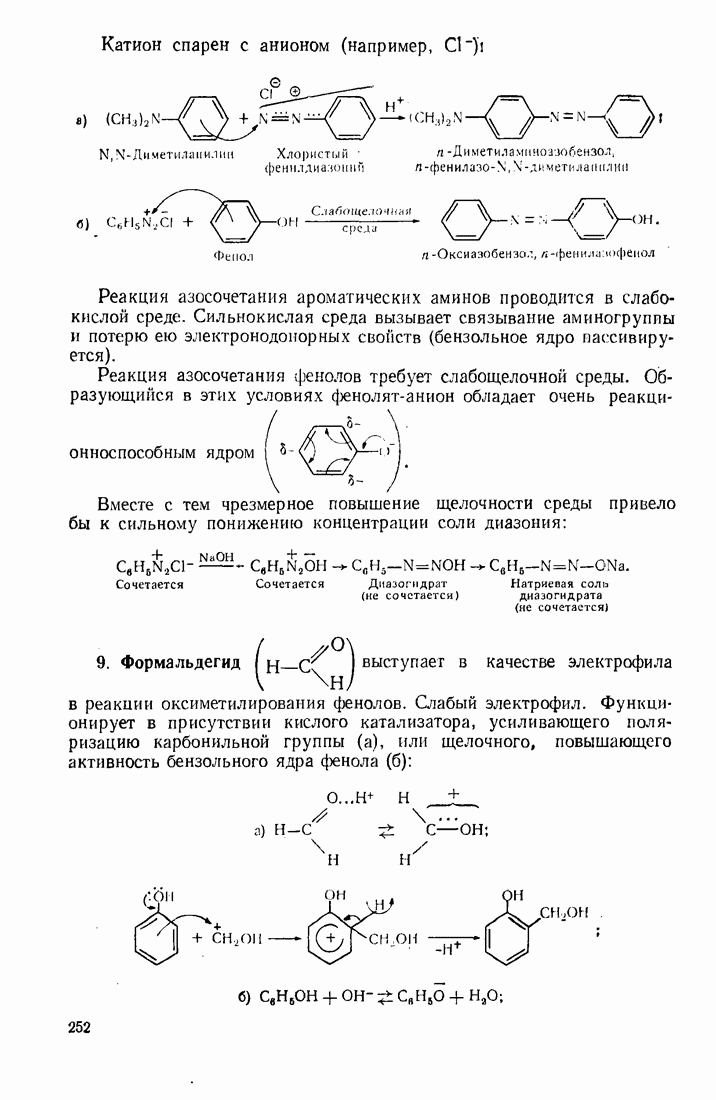
Реакция азосочетания ароматических аминов проводится в слабокислой среде. Сильнокислая среда вызывает связывание аминогруппы и потерю ею электронодонорных свойств (бензольное ядро пассивируется).
Реакция азосочетания фенолов требует слабощелочной среды. Образующийся в этих условиях фенолят-анион обладает очень реакционноспособным ядром 
Вместе с тем чрезмерное повышение щелочности среды привело бы к сильному понижению концентрации соли диазония:

Сочетается Сочетается Диазогидрат Натриевая 
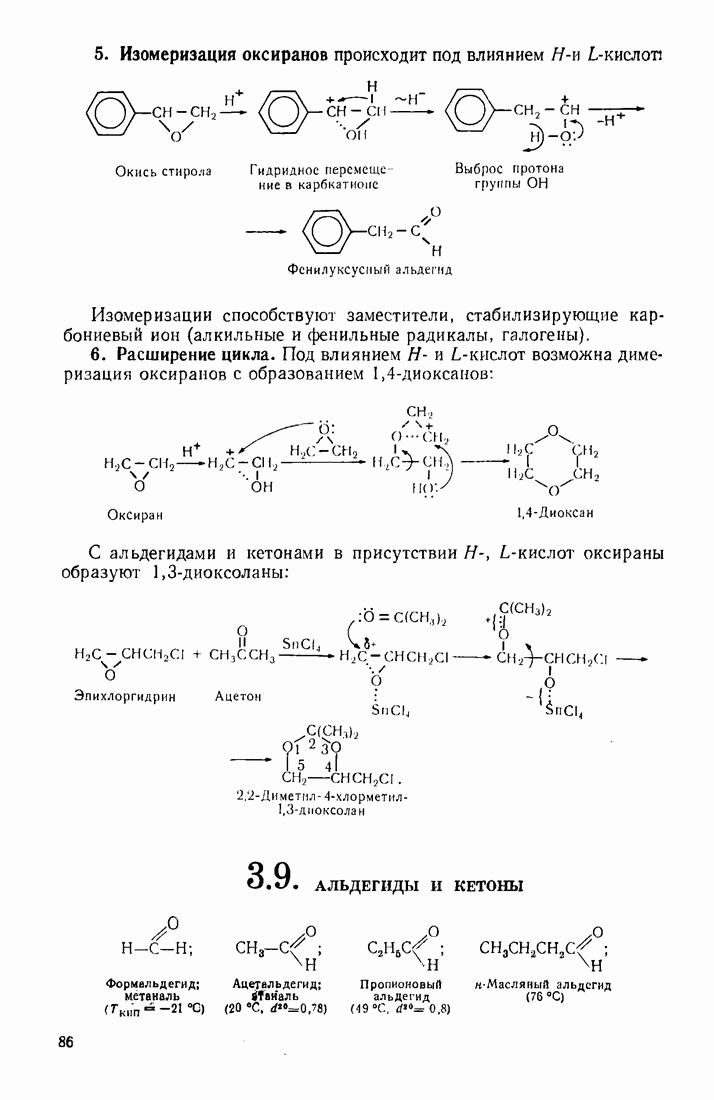
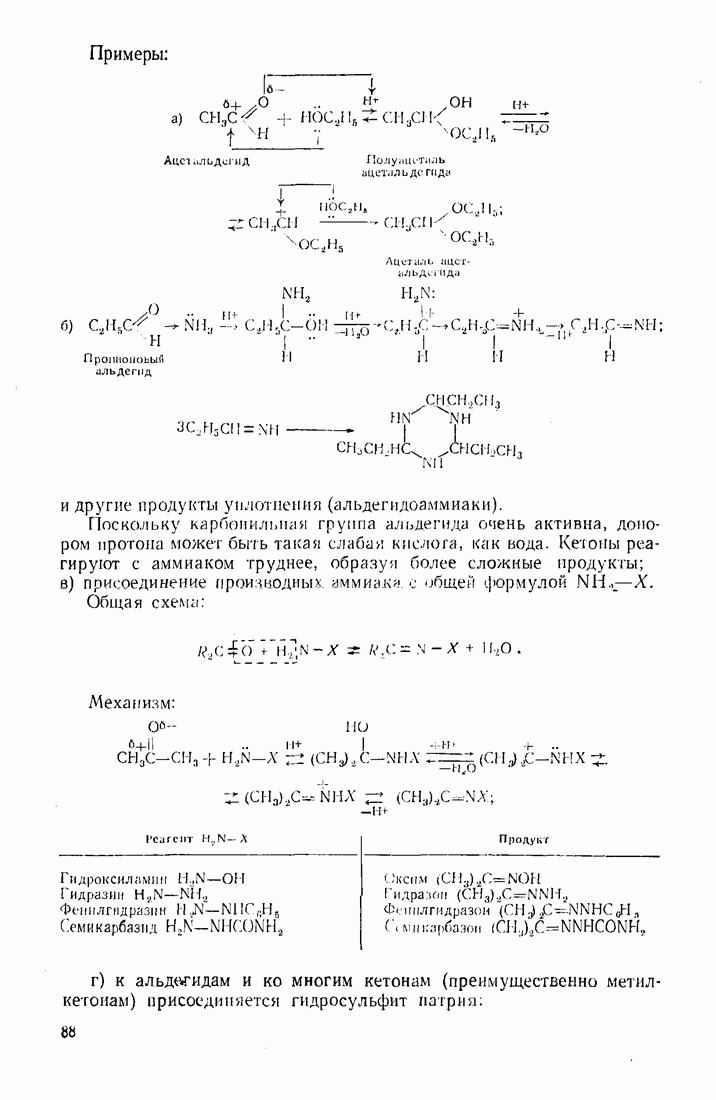
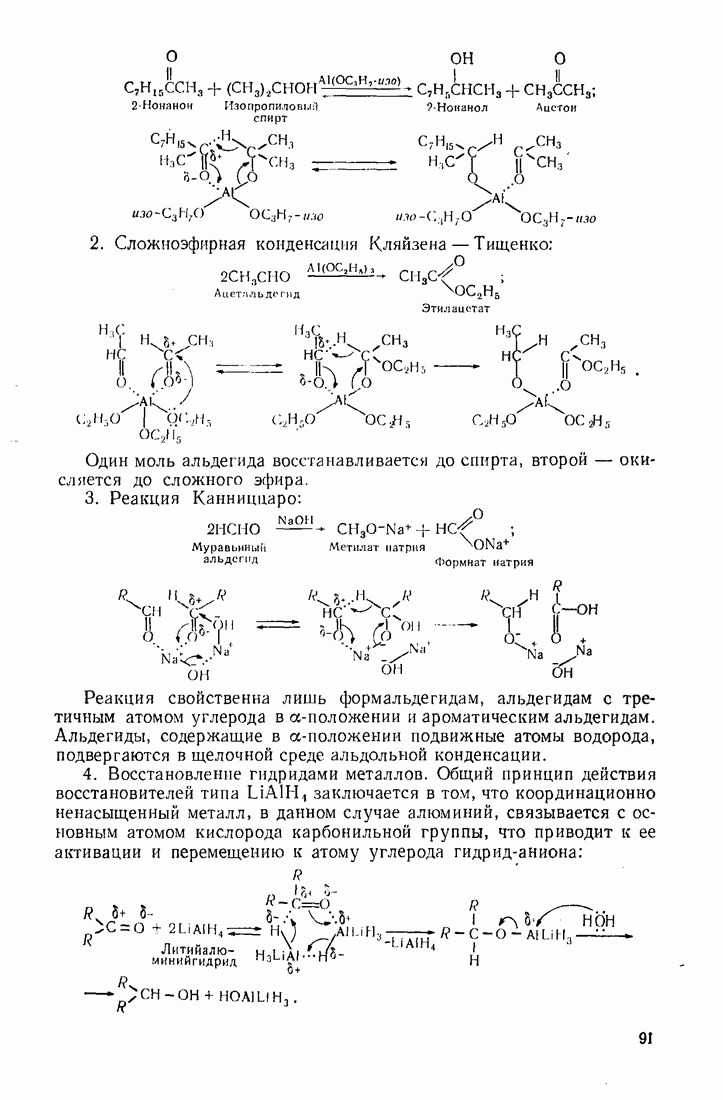
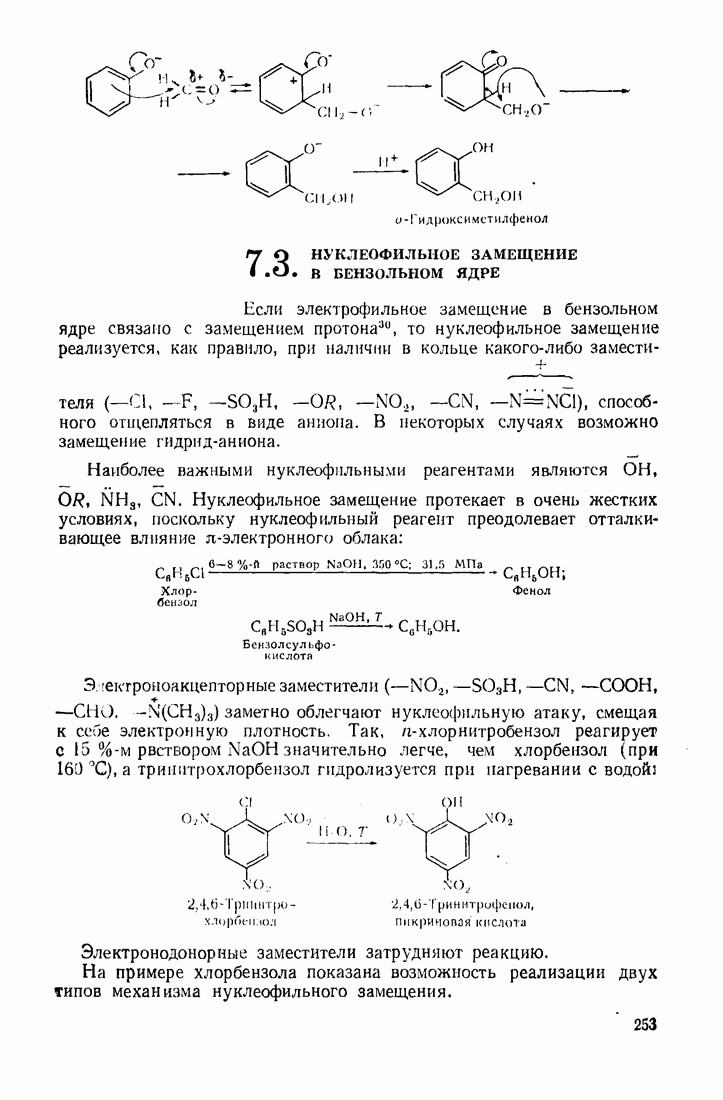
9. Формальдегид  выступает в качестве электрофила в реакции оксиметилирования фенолов. Слабый электрофил. Функционирует в присутствии кислого катализатора, усиливающего поляризацию карбонильной группы (а), или щелочного, повышающего активность бензольного ядра фенола
выступает в качестве электрофила в реакции оксиметилирования фенолов. Слабый электрофил. Функционирует в присутствии кислого катализатора, усиливающего поляризацию карбонильной группы (а), или щелочного, повышающего активность бензольного ядра фенола 
(см. скан)

| << Предыдущий параграф | Следующий параграф >> |
- Предисловие
- 1. Введение
- 1.1. Предмет органической химии
- 1.2. Основные этапы развития органической химии
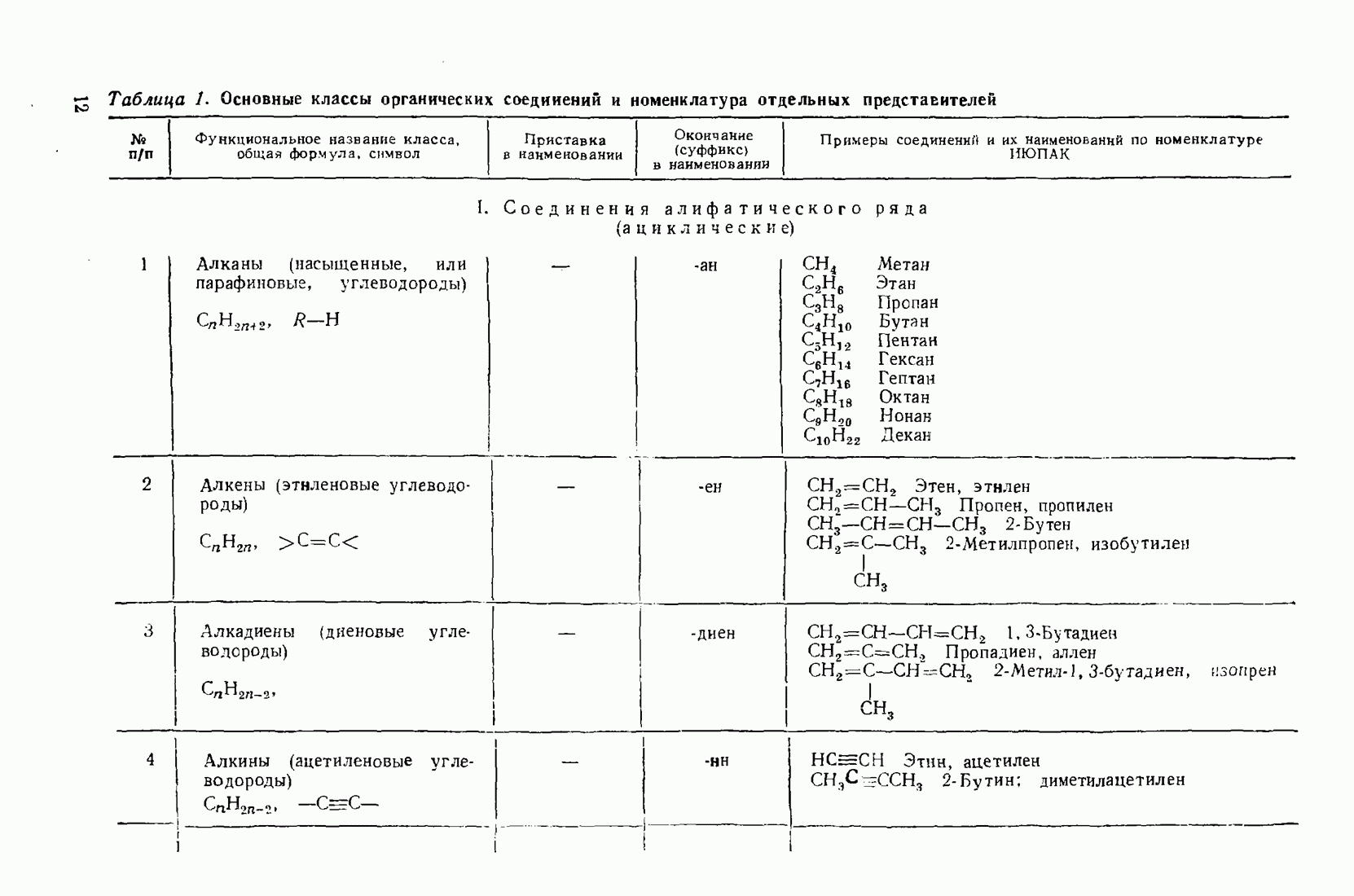
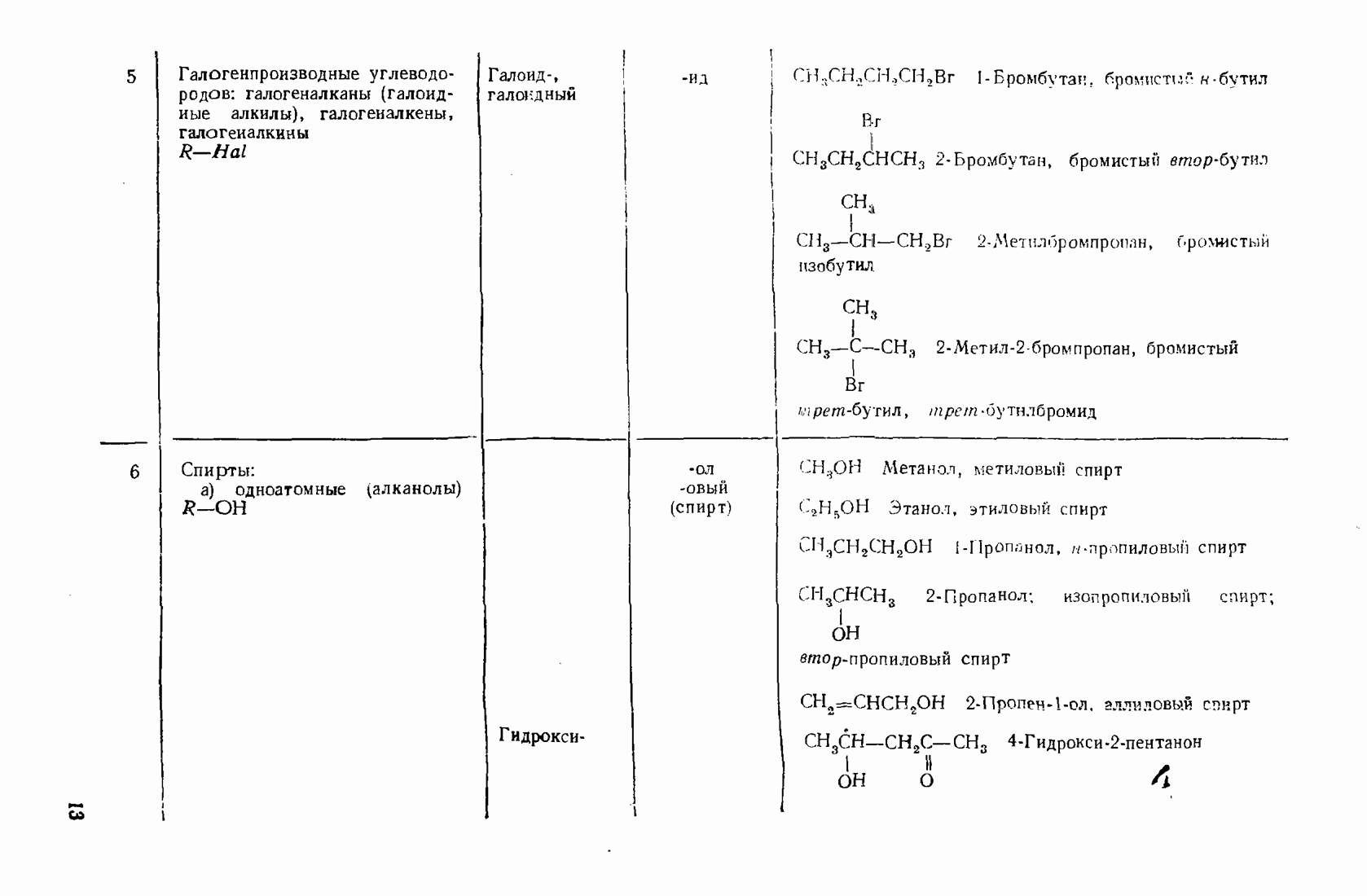
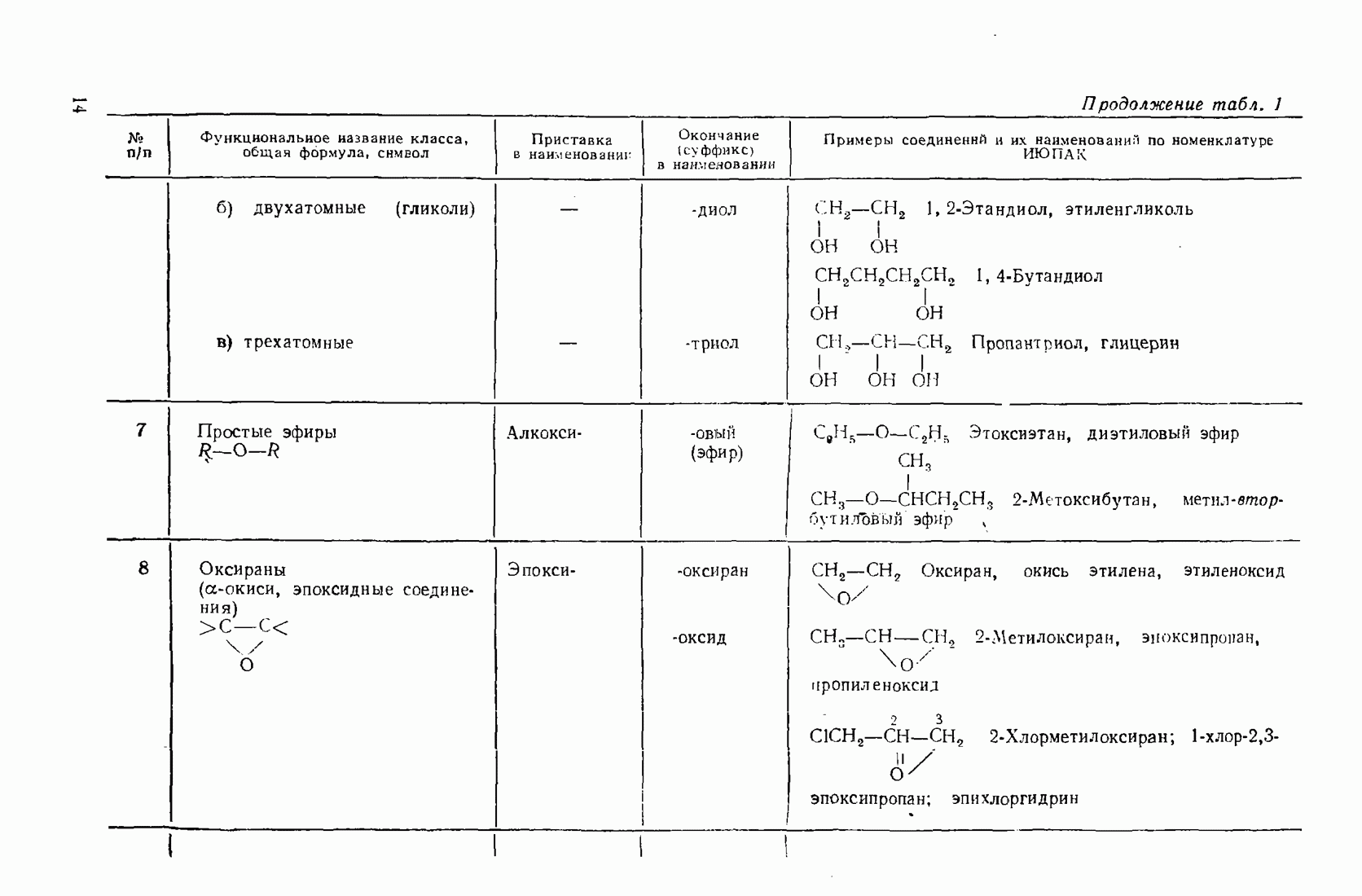
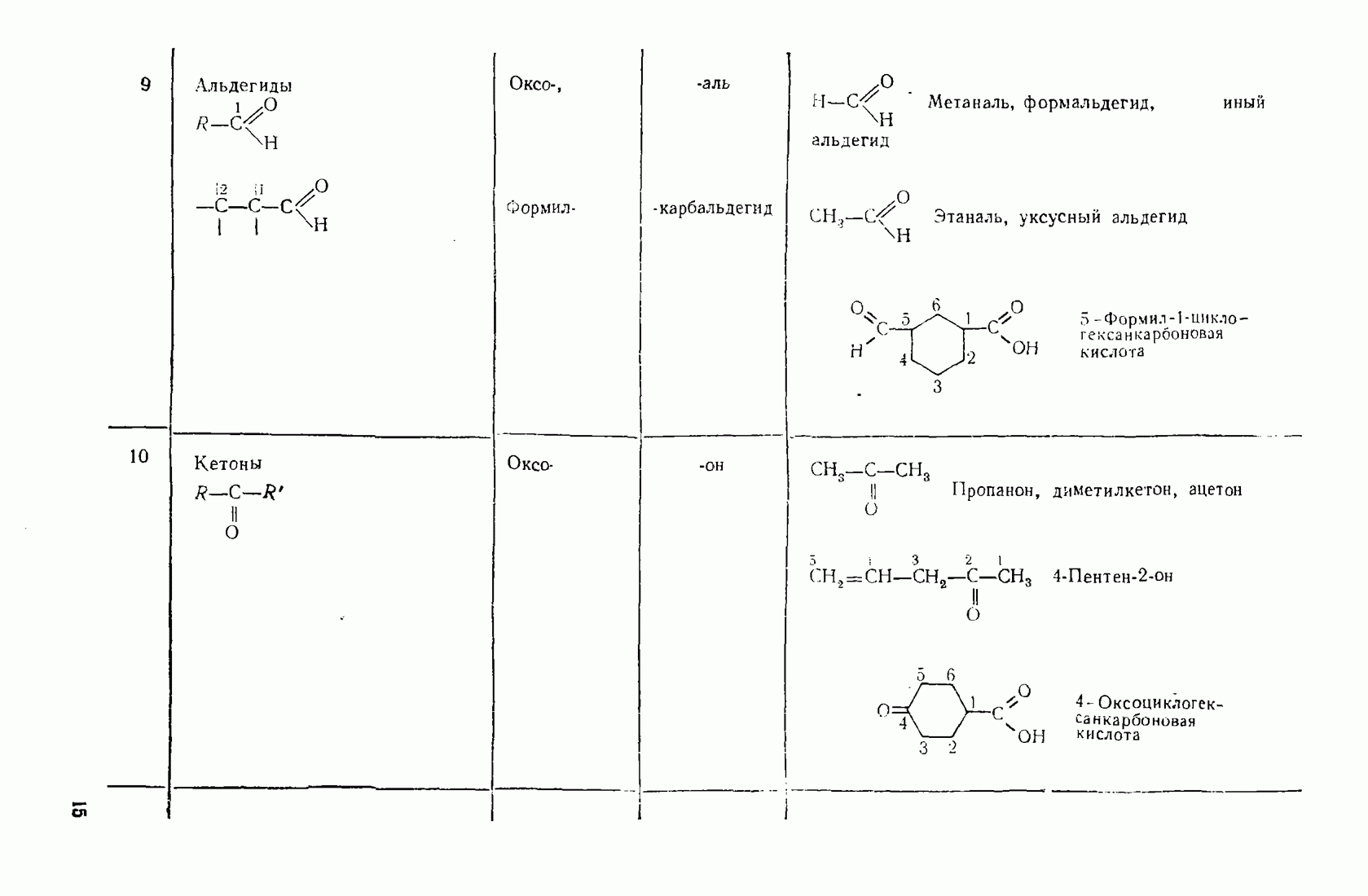
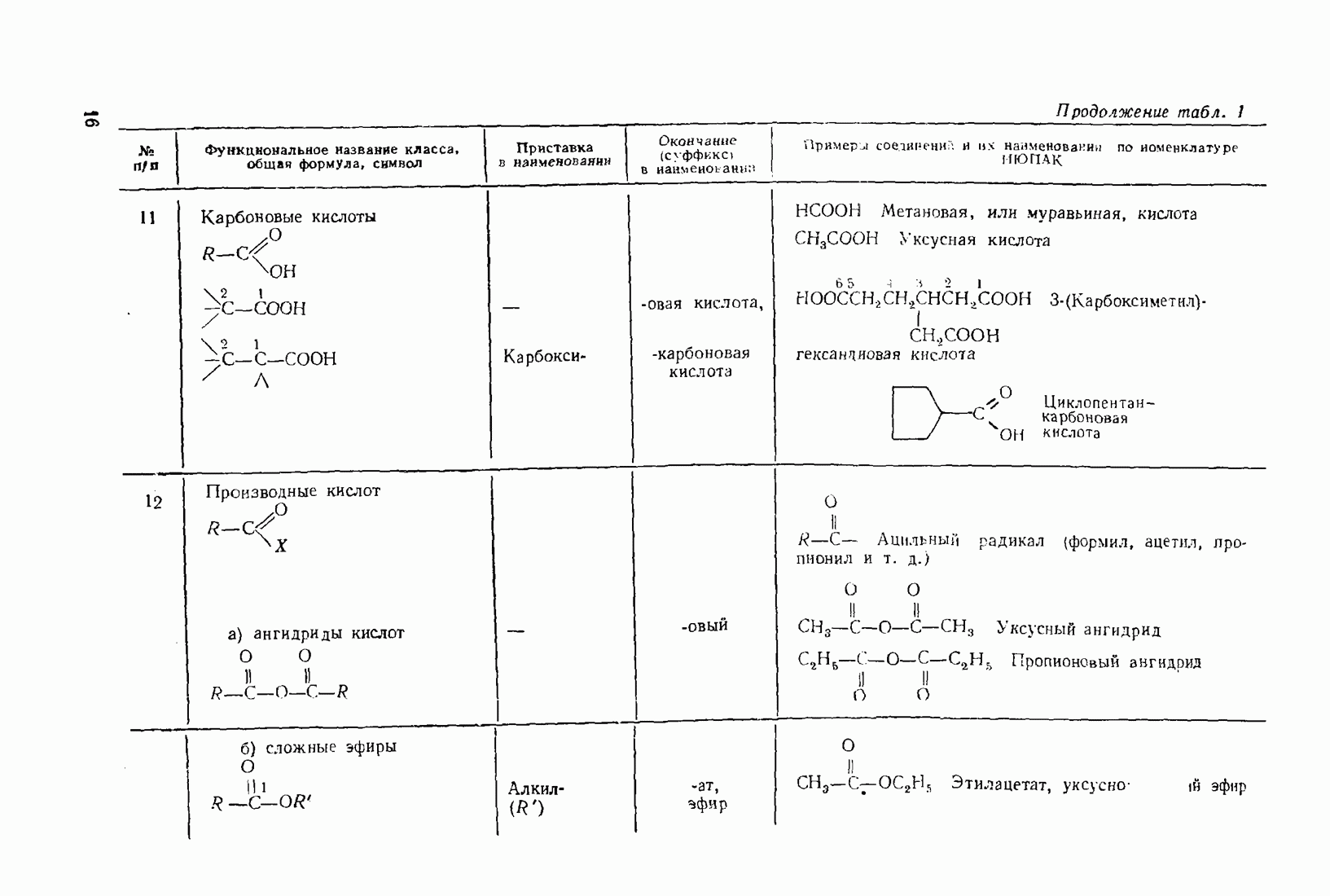
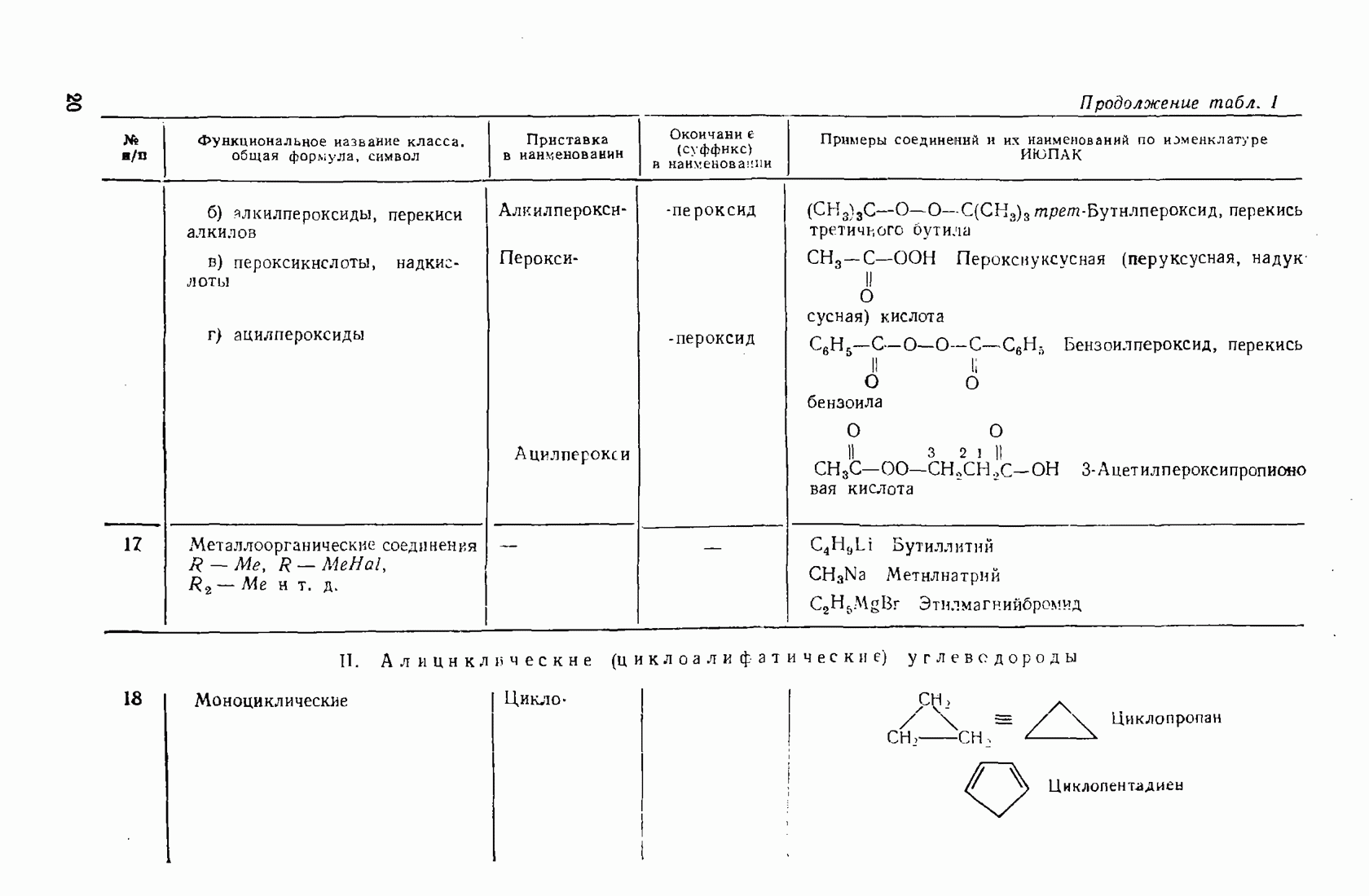
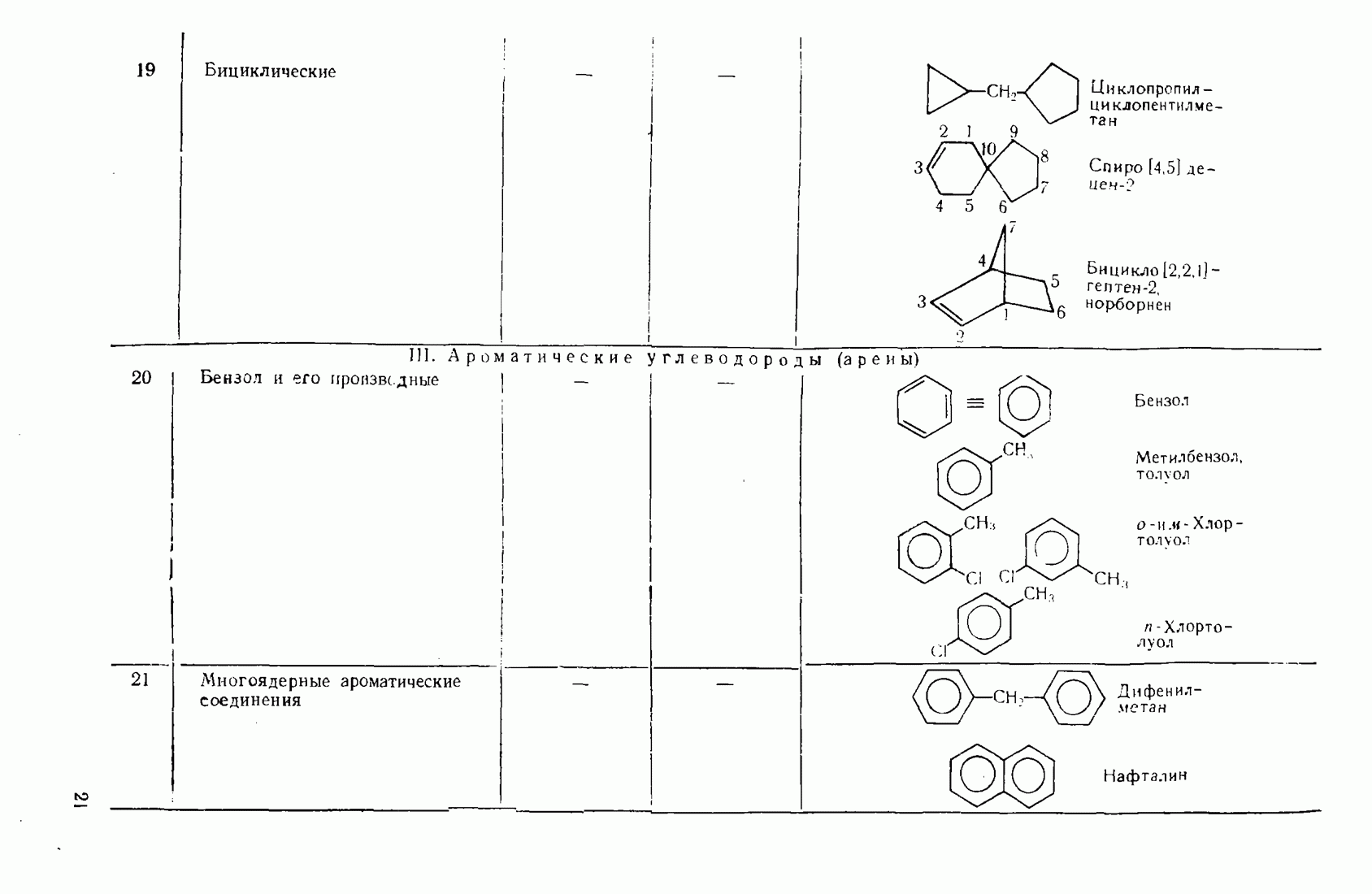
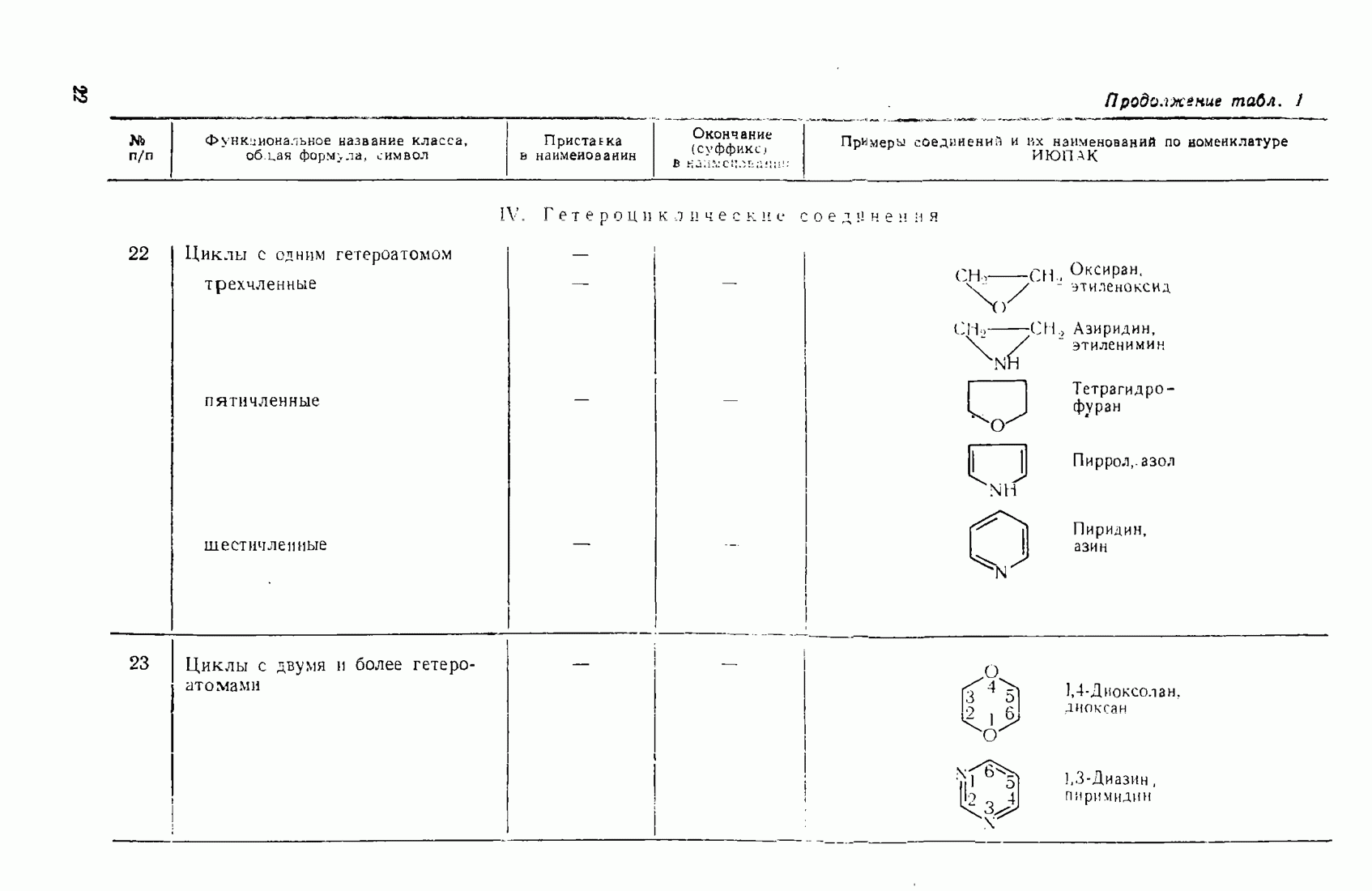
- 1.3. Классификация и номенклатура органических соединений
- 2 Общие теоретические положения органической химии
- 2.1. Природа химической связи
- 2.1.1. Типы химических связей
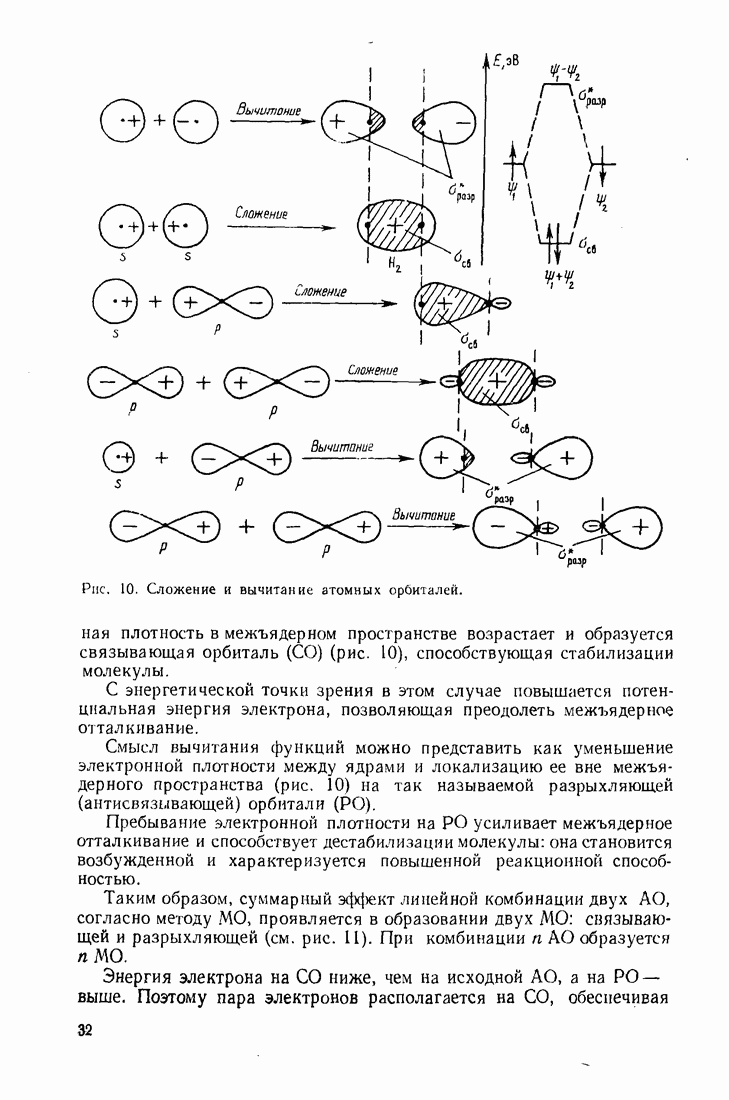
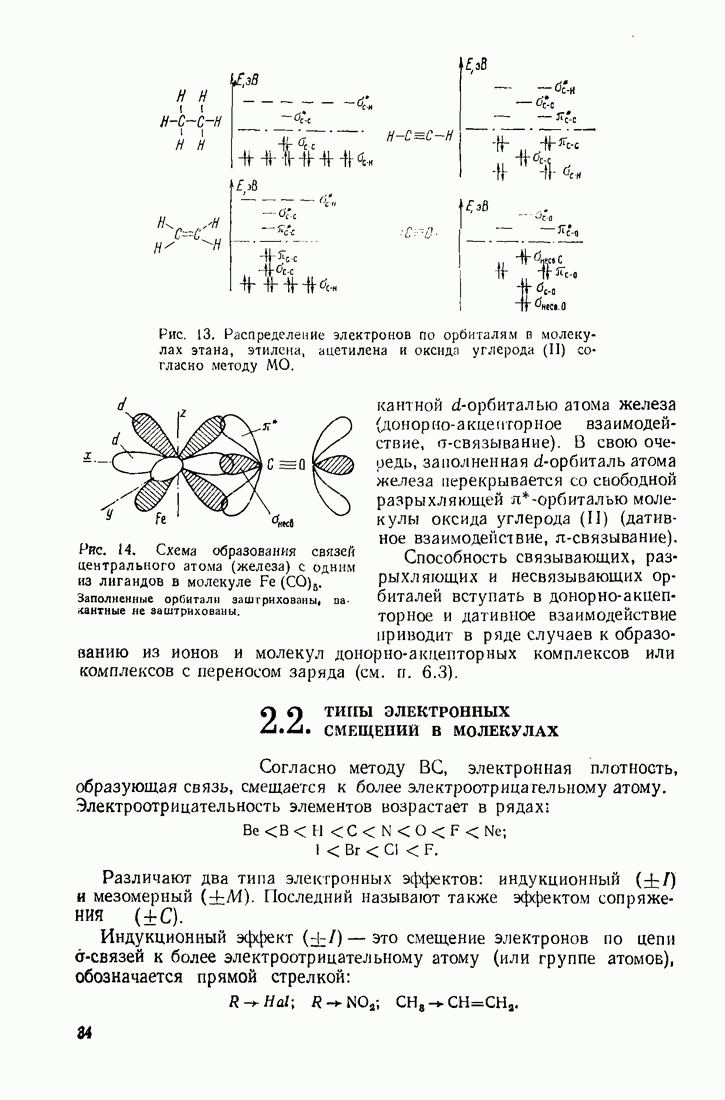
- 2.1.2. Молекулярные орбитали
- 2.2. ТИПЫ ЭЛЕКТРОННЫХ СМЕЩЕНИЙ В МОЛЕКУЛАХ
- 2.3. ОБЩИЕ ПРЕДСТАВЛЕНИЯ ОБ ОРГАНИЧЕСКОЙ РЕАКЦИИ
- 2.4. КЛАССИФИКАЦИЯ РЕАГЕНТОВ И РЕАКЦИЙ
- 2.5. КРАТКАЯ ХАРАКТЕРИСТИКА РЕАКЦИОННОЙ СПОСОБНОСТИ НЕКОТОРЫХ СОЕДИНЕНИЙ АЛИФАТИЧЕСКОГО РЯДА
- 2.5.1. Алканы (парафины)
- 2.5.2. Непредельные углеводороды
- 2.5.3. Галогеналканы (галоидные алкилы R-Hal)
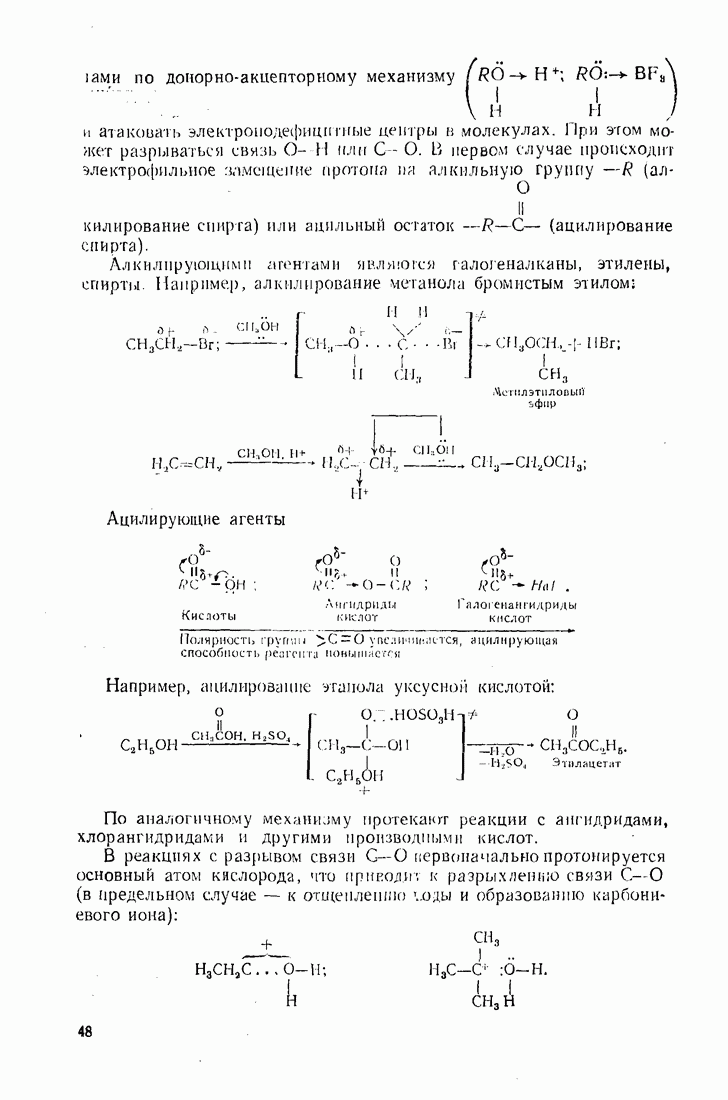
- 2.5.4. Спирты (R0Н)
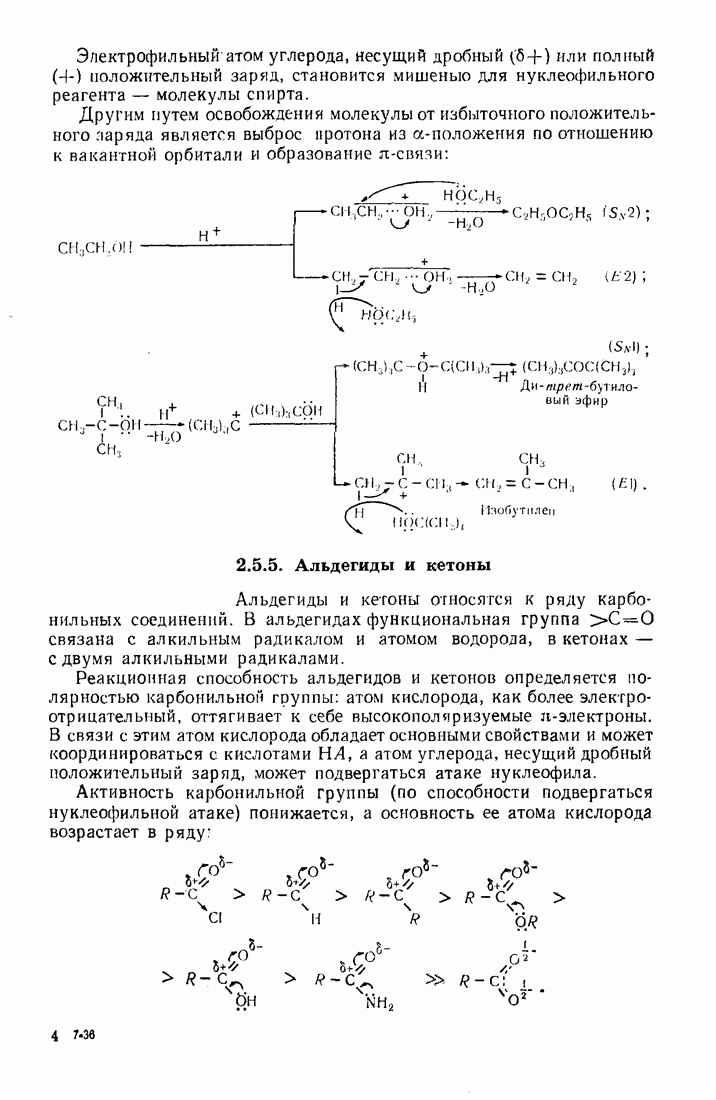
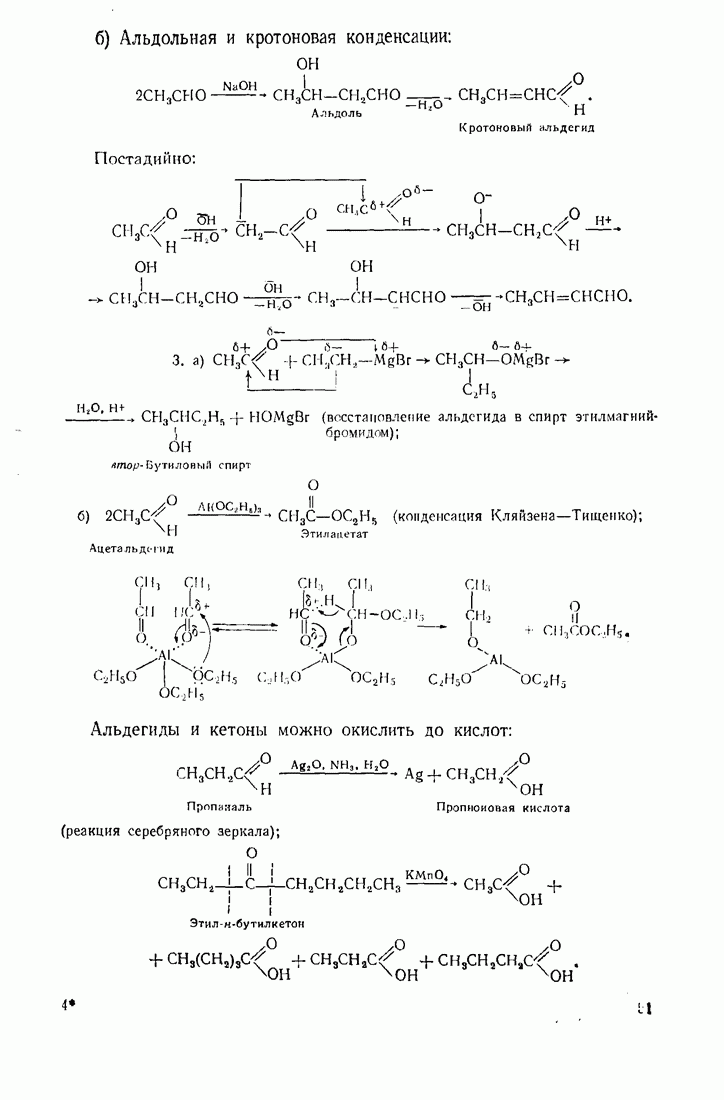
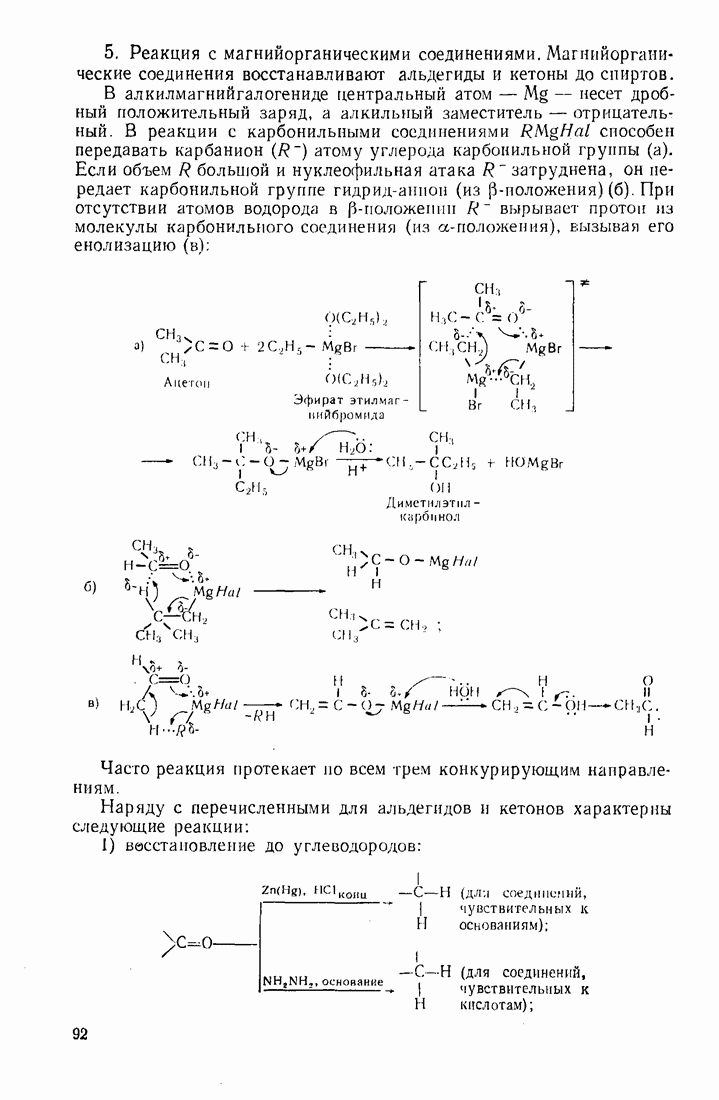
- 2.5.5. Альдегиды и кетоны
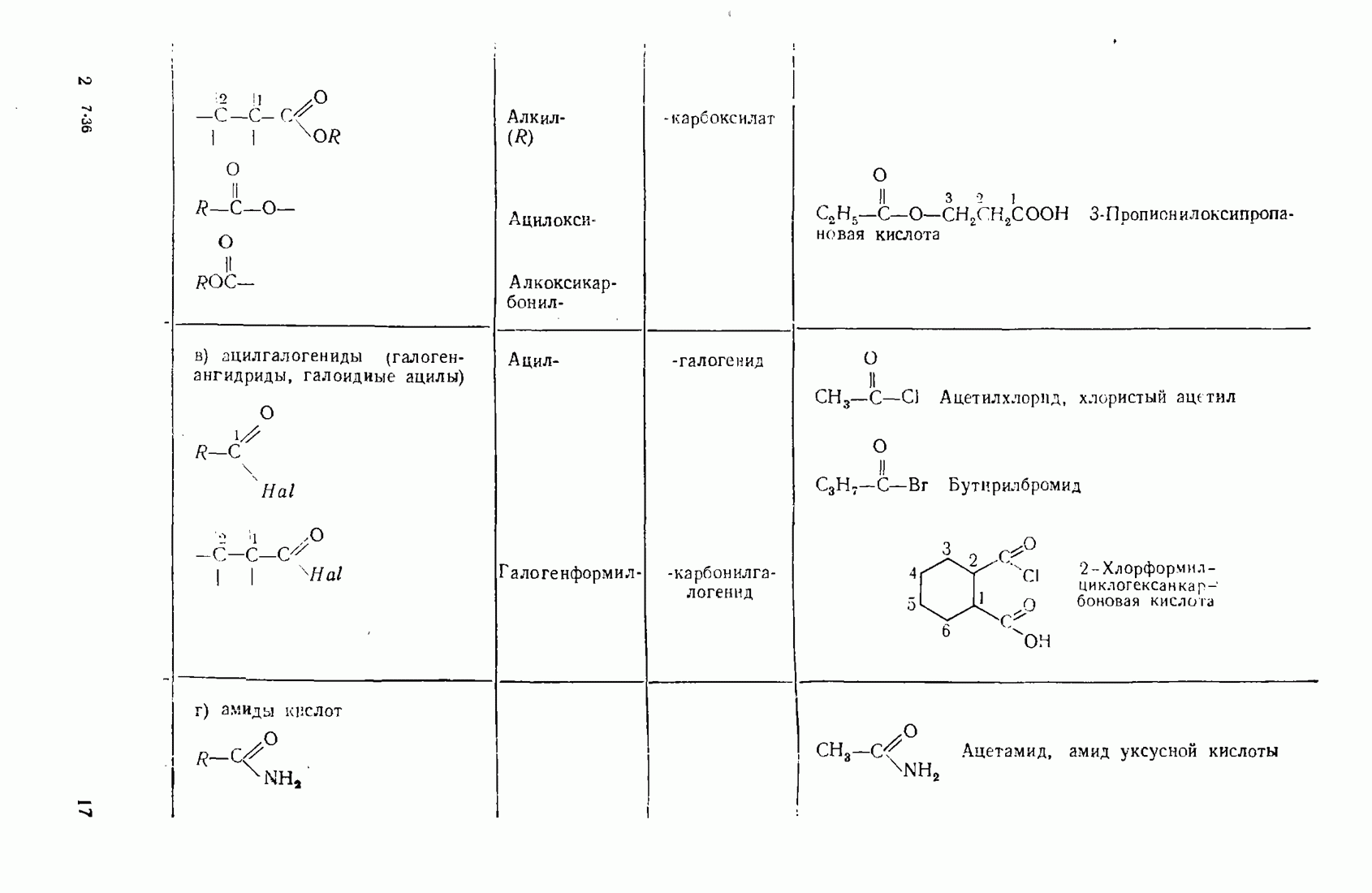
- 2.5.6. Карбоновые кислоты (R-СООН) и их производные (R-СО-X)
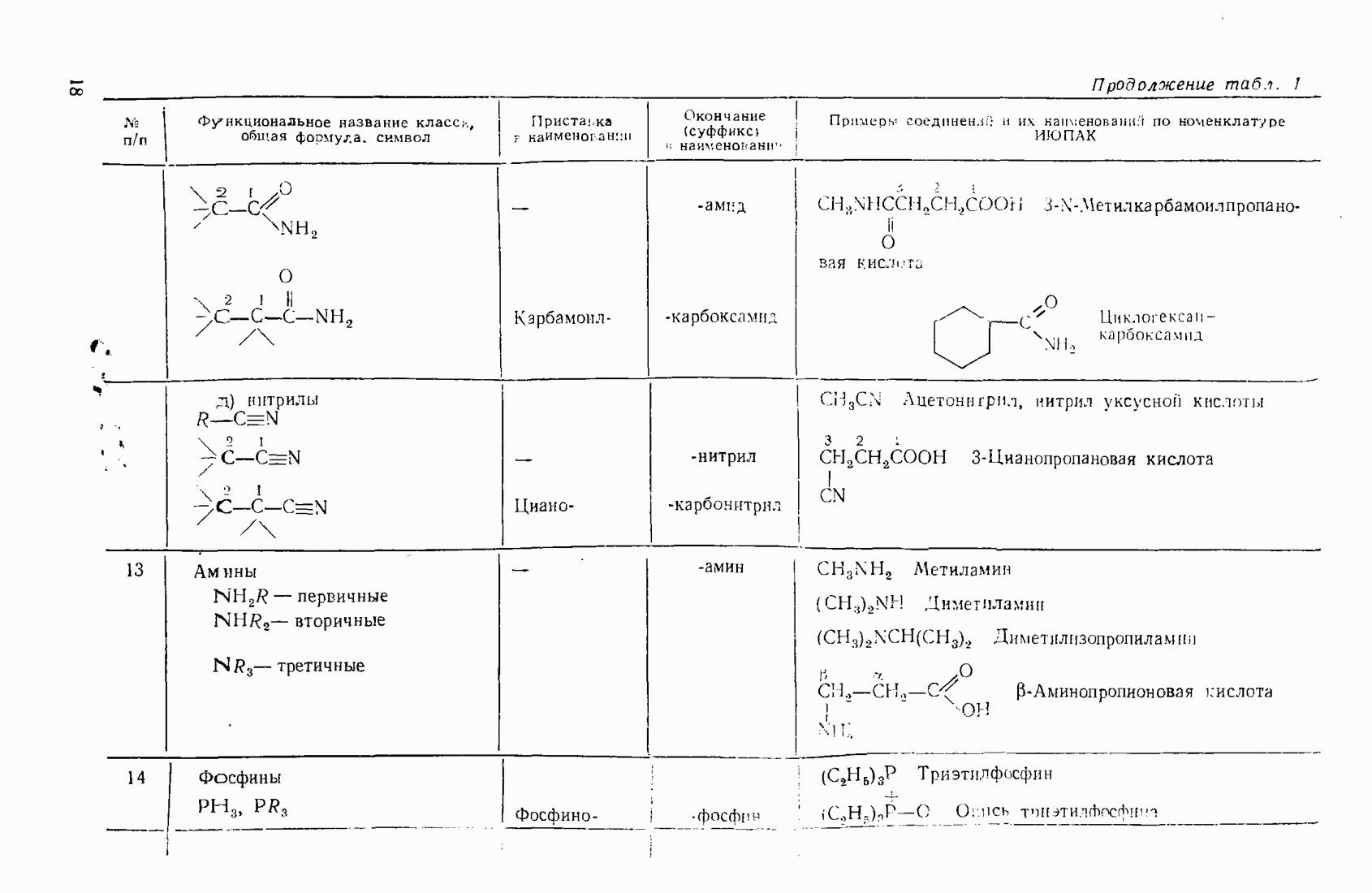
- 2.5.7. Амины (NH2R, NHR2, NR3)
- 3. Реакционная способность соединений алифатического ряда
- 3.1. Алканы (насыщенные углеводороды)
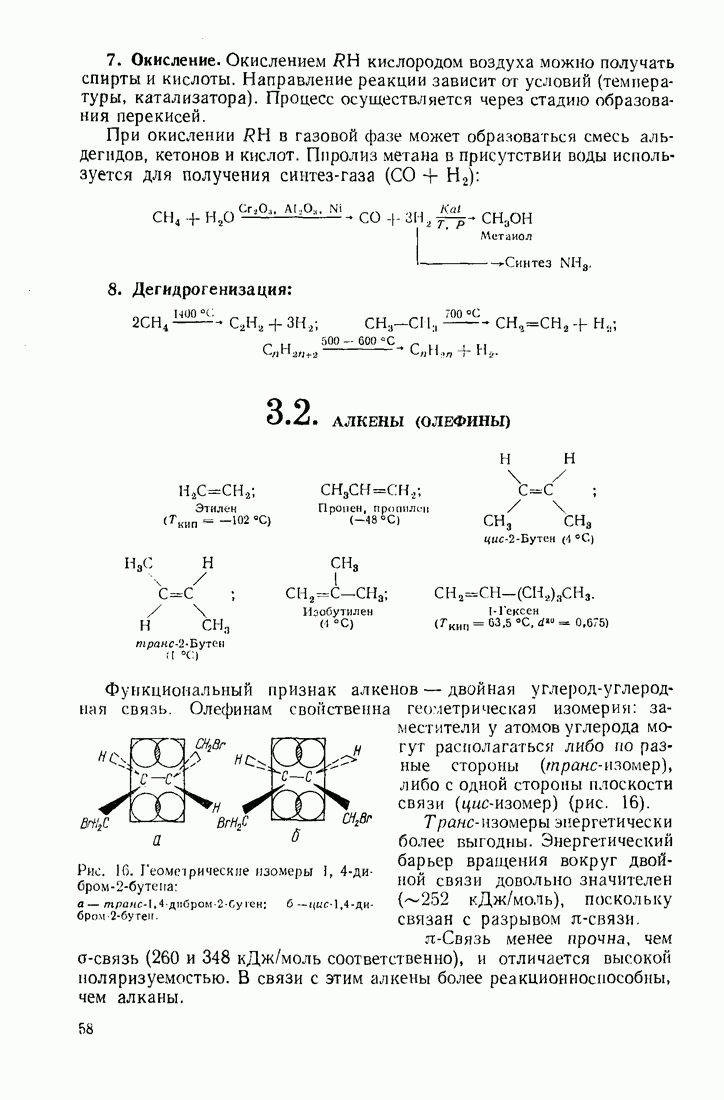
- 3.2. АЛКЕНЫ (ОЛЕФИНЫ)
- 3.3. ДИЕНОВЫЕ УГЛЕВОДОРОДЫ
- 3.4. АЦЕТИЛЕНЫ
- 3.5. ГАЛОГЕНАЛКАНЫ (ГАЛОИДНЫЕ АЛКИЛЫ)
- 3.6. СПИРТЫ
- 3.7. ПРОСТЫЕ ЭФИРЫ (R-O-R)
- 3.8. ОКСИРАНЫ (ЭПОКСИДНЫЕ СОЕДИНЕНИЯ, a-ОКИСИ)
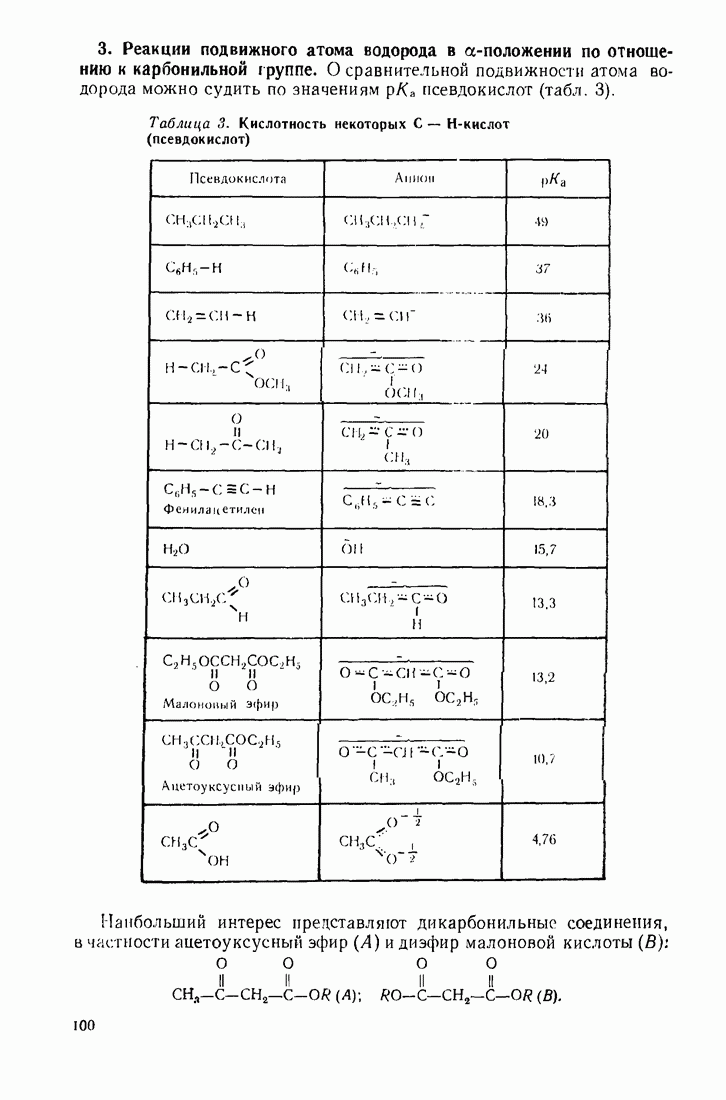
- 3.9. АЛЬДЕГИДЫ И КЕТОНЫ
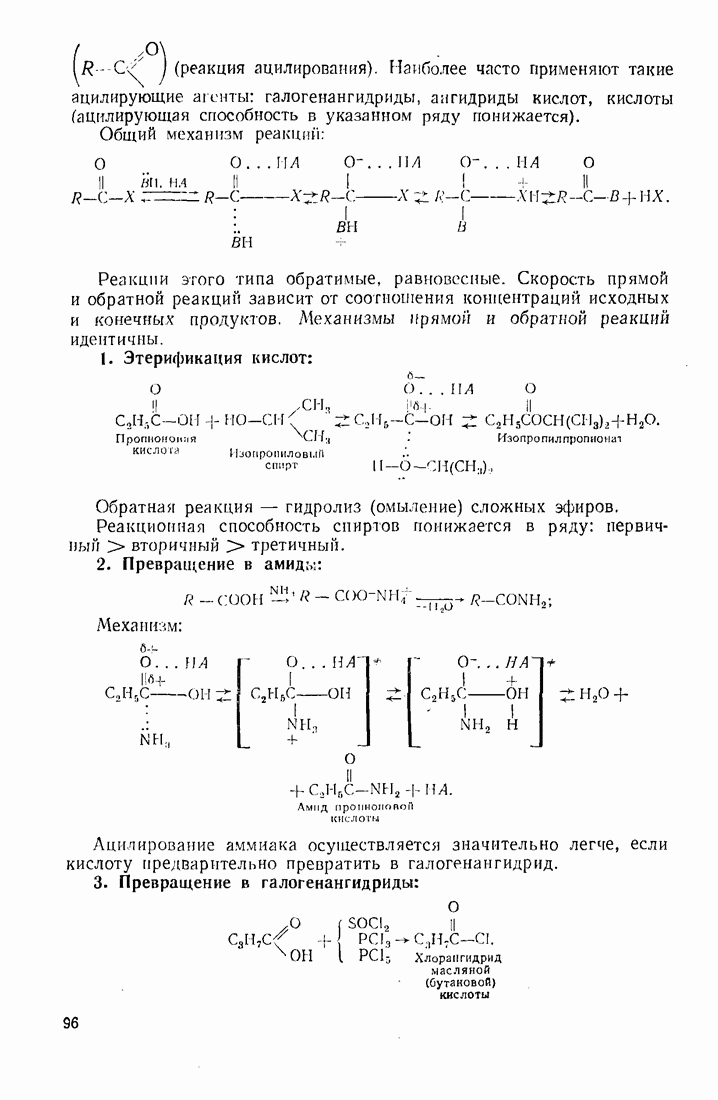
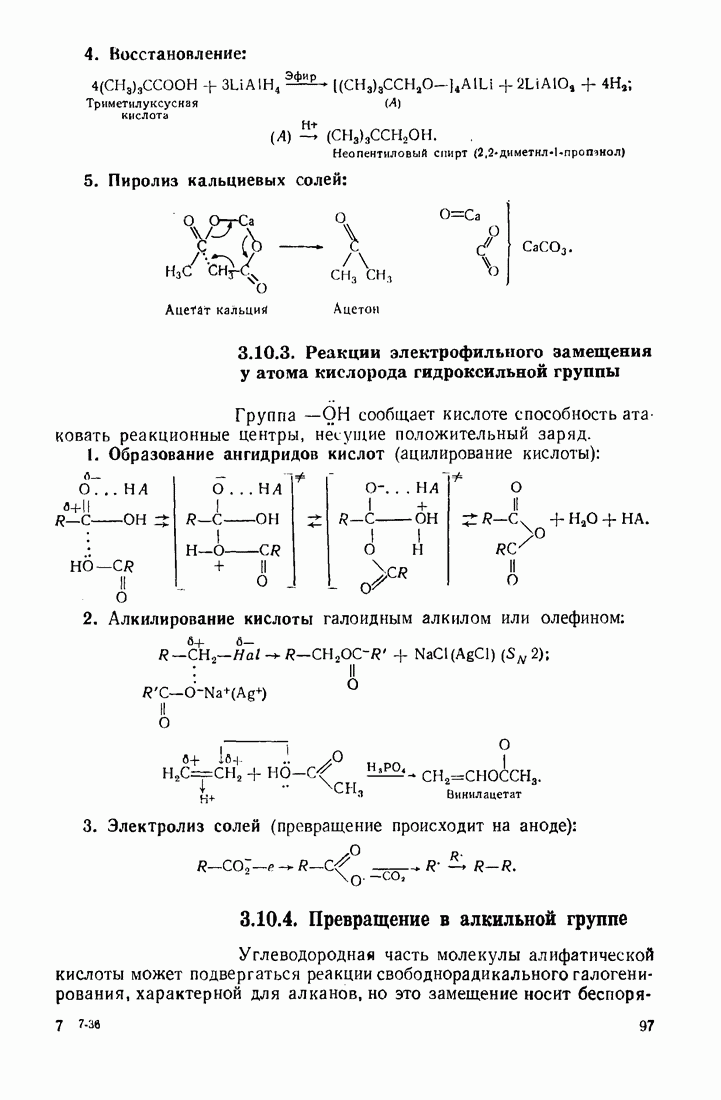
- 3.10. КАРБОНОВЫЕ КИСЛОТЫ
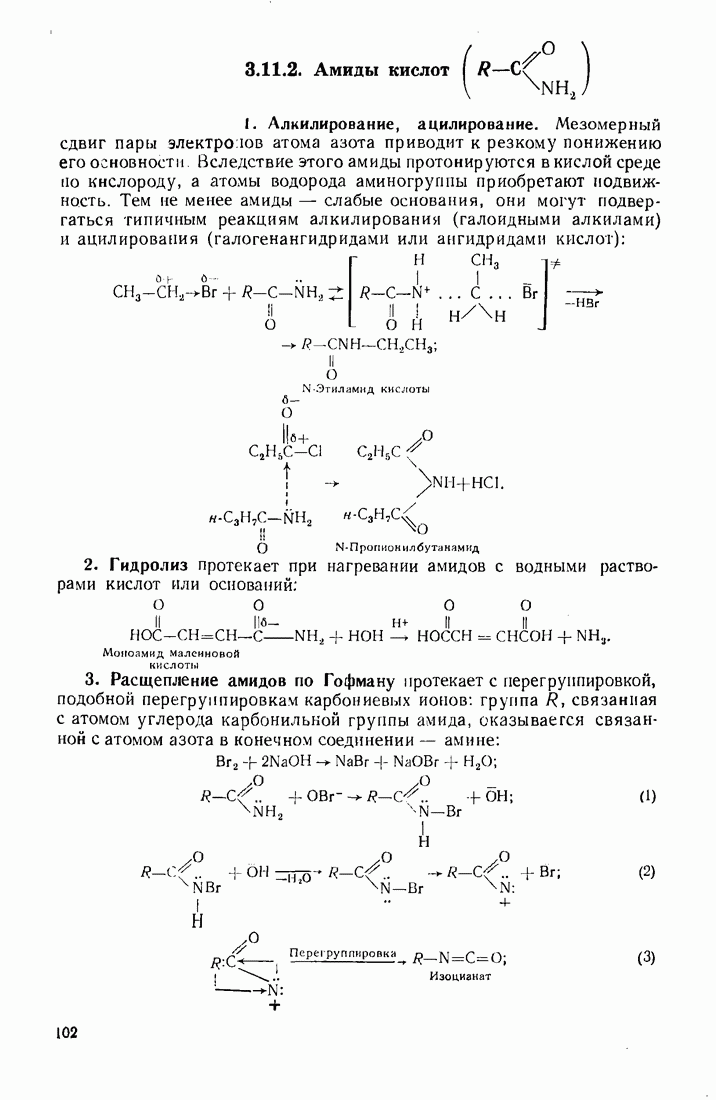
- 3.11. НЕКОТОРЫЕ ПРОИЗВОДНЫЕ КИСЛОТ
- 3.12. АМИНЫ
- 3.13. ФОСФОРОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
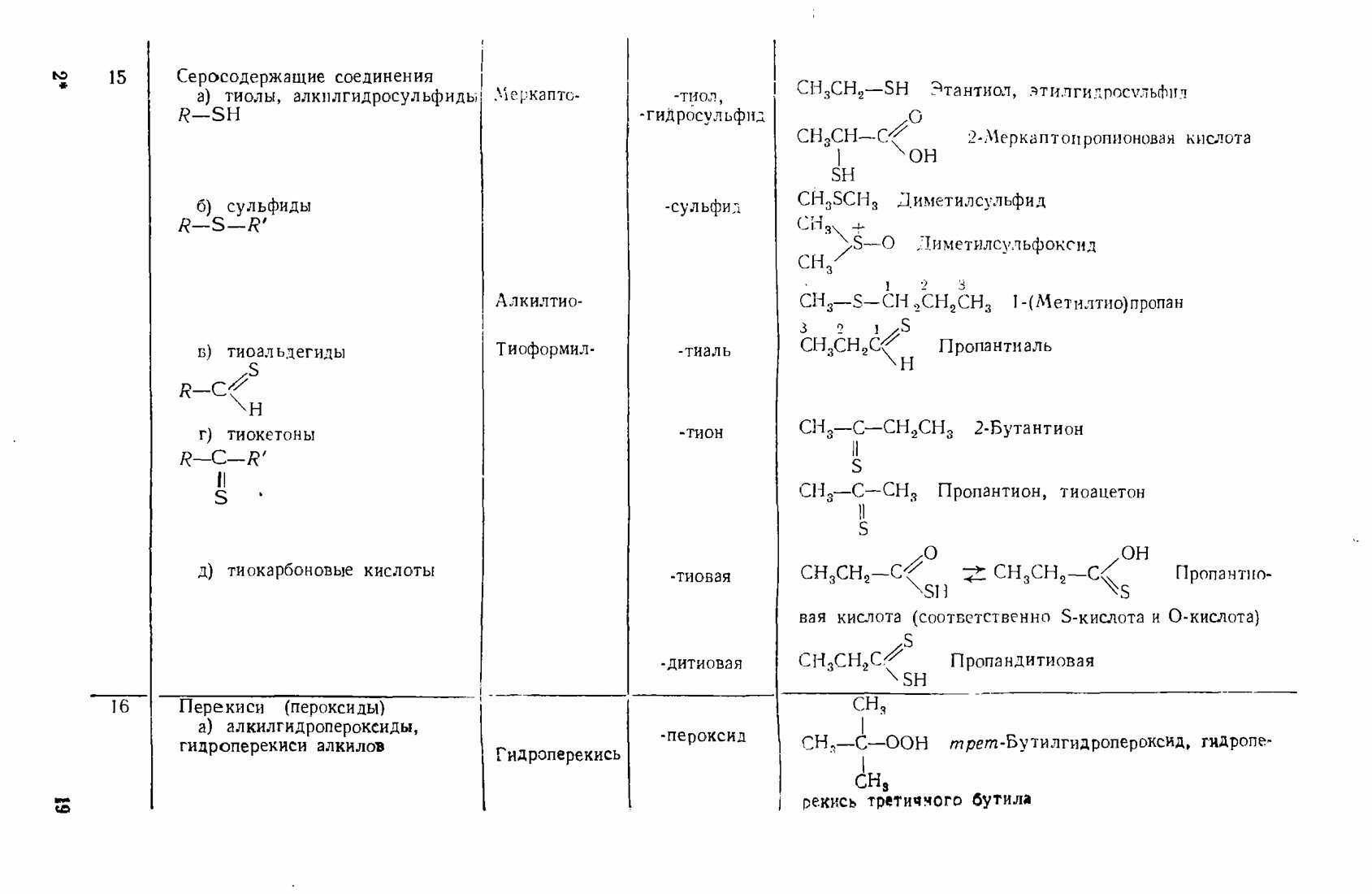
- 3.14. СЕРООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- 3.15. ОРГАНИЧЕСКИЕ ПЕРЕКИСИ (ПЕРОКСИДНЫЕ СОЕДИНЕНИЯ)
- 3.16. ПРОИЗВОДНЫЕ УГОЛЬНОЙ КИСЛОТЫ
- 3.17. ГЕТЕРОАНАЛОГИ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ
- 3.18. АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- 3.18.2. Пространственное расположение и напряженность циклов
- 3.18.3. Особенности химических свойств алициклических соединений
- 4. Полифункциональные производные алифатического ряда
- 4.1. ДВУХОСНОВНЫЕ КАРБОНОВЫЕ КИСЛОТЫ
- 4.2. НЕПРЕДЕЛЬНЫЕ КИСЛОТЫ
- 4.3. ОКСОКИСЛОТЫ (АЛЬДЕГИДО- И КЕТОКИСЛОТЫ)
- 4.4. ОКСИКИСЛОТЫ. ПОНЯТИЕ ОБ ОПТИЧЕСКОЙ ИЗОМЕРИИ
- 4.5. УГЛЕВОДЫ
- 4.5.2. Стереохимия моносахаридов
- 4.5.3. Дисахариды
- 4.5.4. Полисахариды
- 4.5.5. Нахождение в природе и пути превращения углеводов
- 4.6. АМИНОКИСЛОТЫ
- 5. Методы синтеза органических юединений алифатическою рада
- 5.1. АЛКИЛИРОВАНИЕ
- 5.2. АЦИЛИРОВАНИЕ
- 5.3. ГАЛОГЕНИРОВАНИЕ
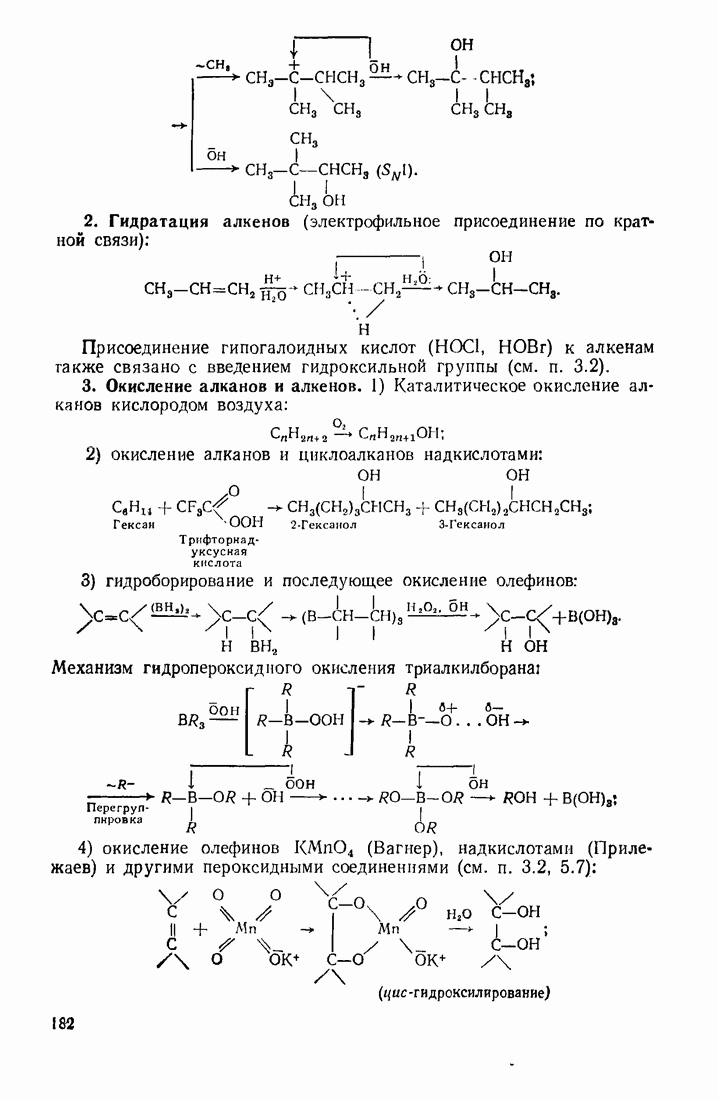
- 5.4. ГИДРОКСИЛИРОВАНИЕ
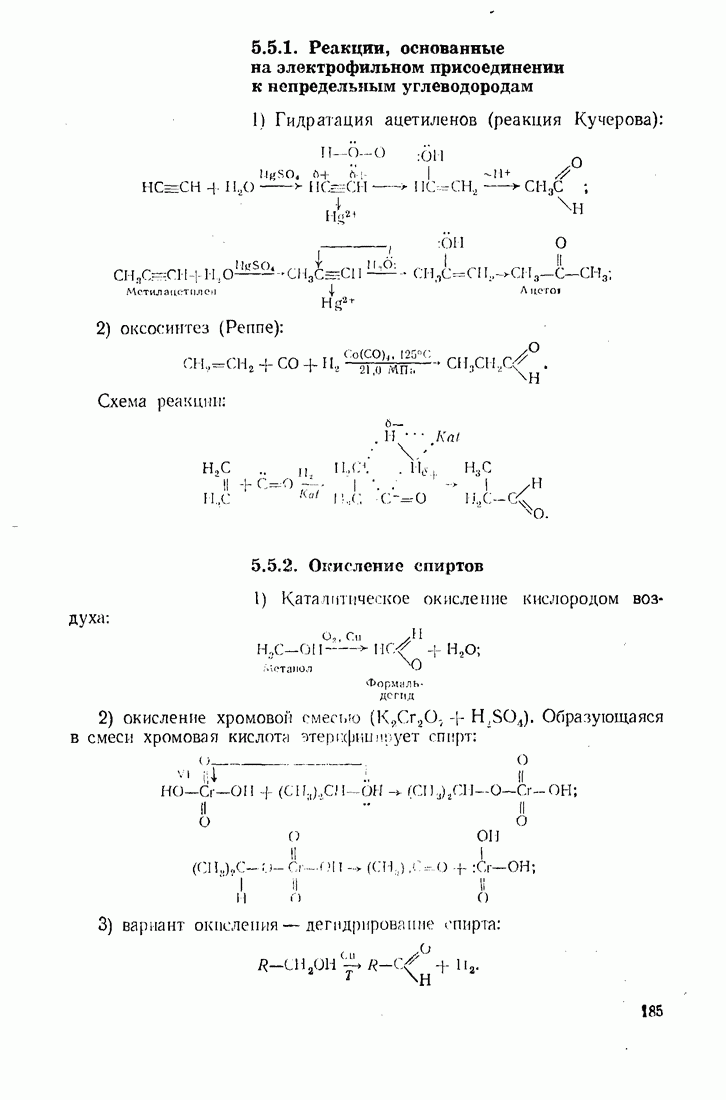
- 5.5. КАРБОНИЛИРОВАНИЕ (ВВЕДЕНИЕ КАРБОНИЛЬНОЙ ГРУППЫ)
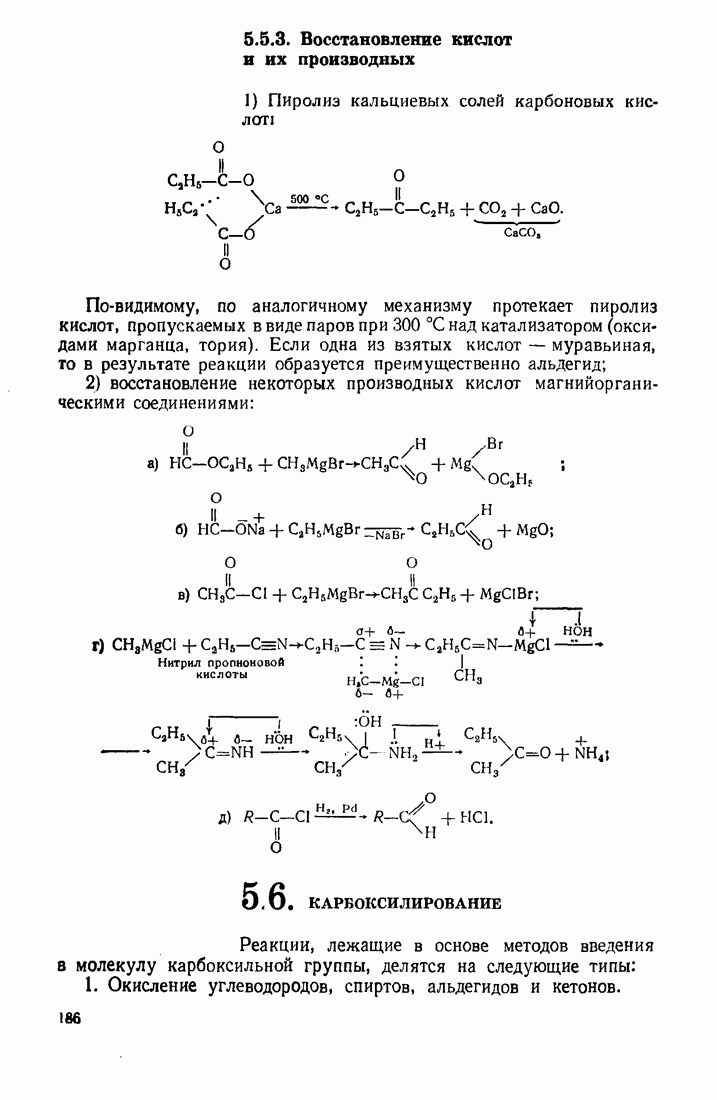
- 5.6. КАРБОКСИЛИРОВАНИЕ
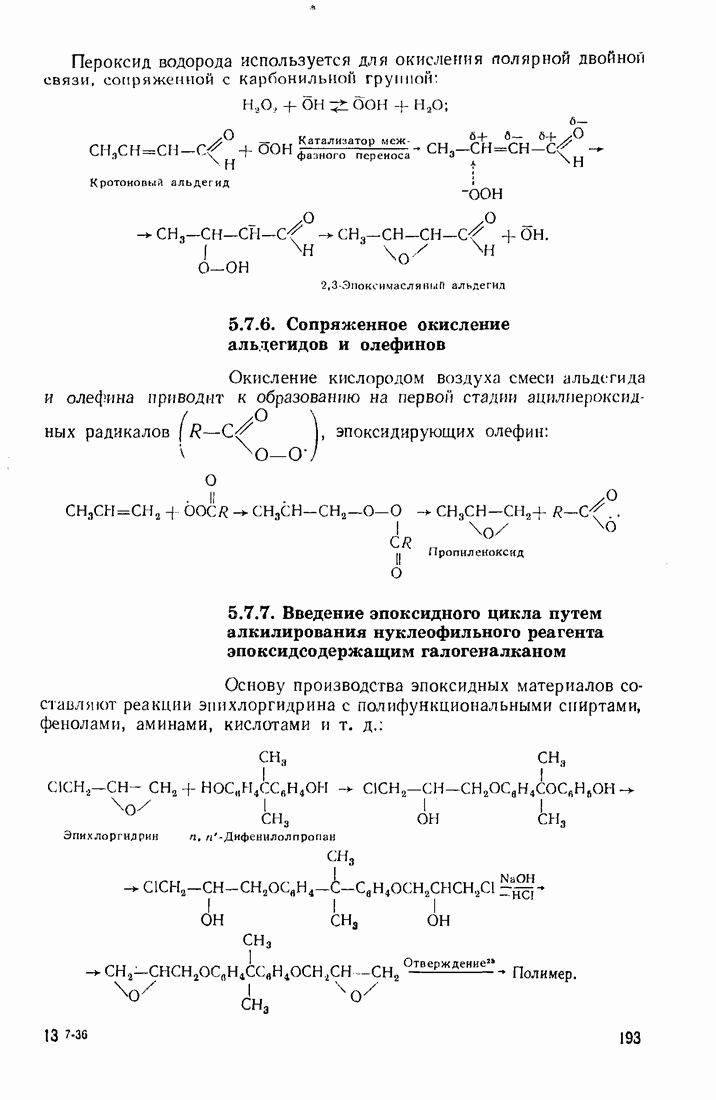
- 5.7. ЭПОКСИДИРОВАНИЕ (ОКСИРАНИРОВАИИЕ)
- 5.8. АМИНИРОВАНИЕ
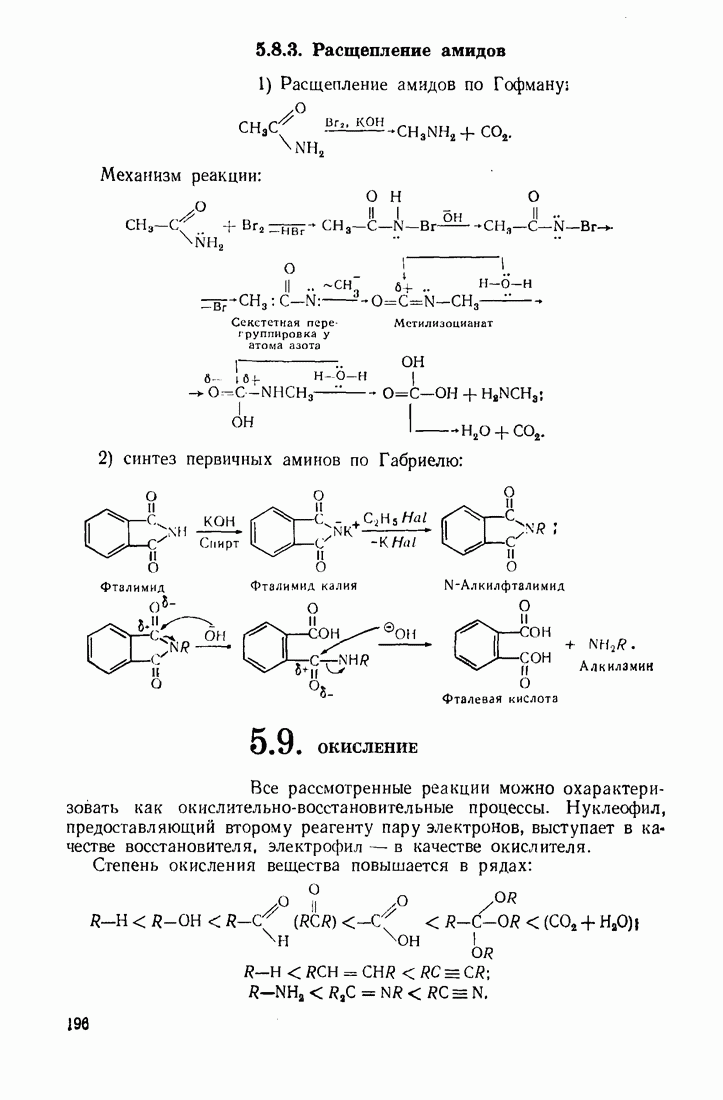
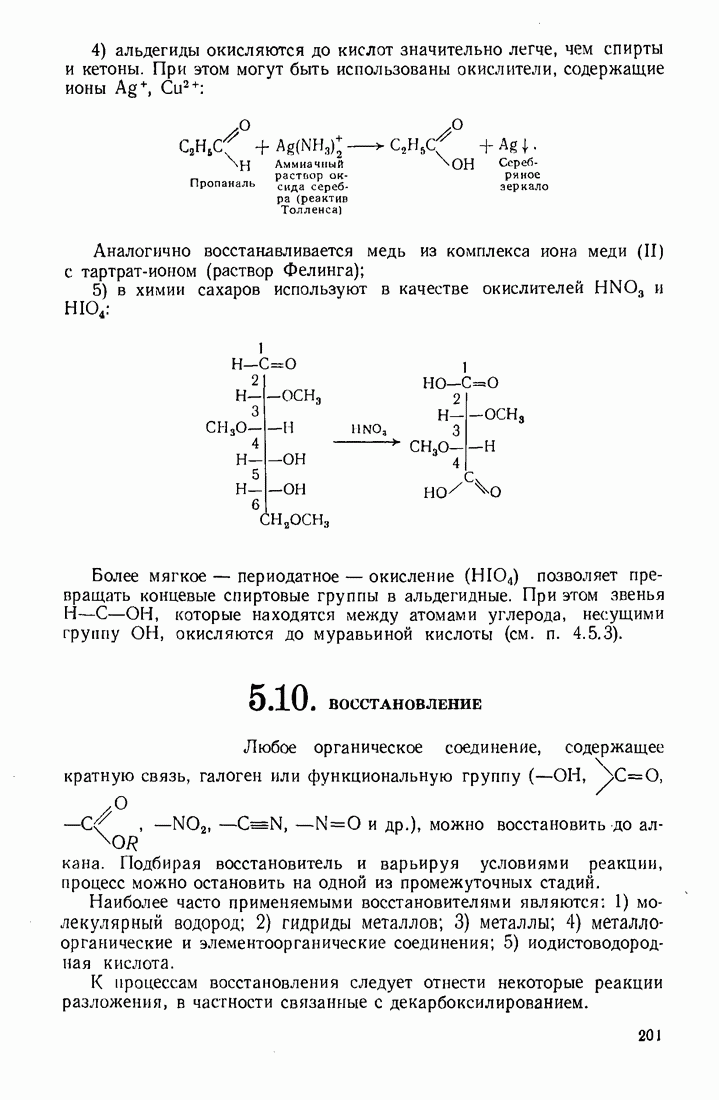
- 5.9. ОКИСЛЕНИЕ
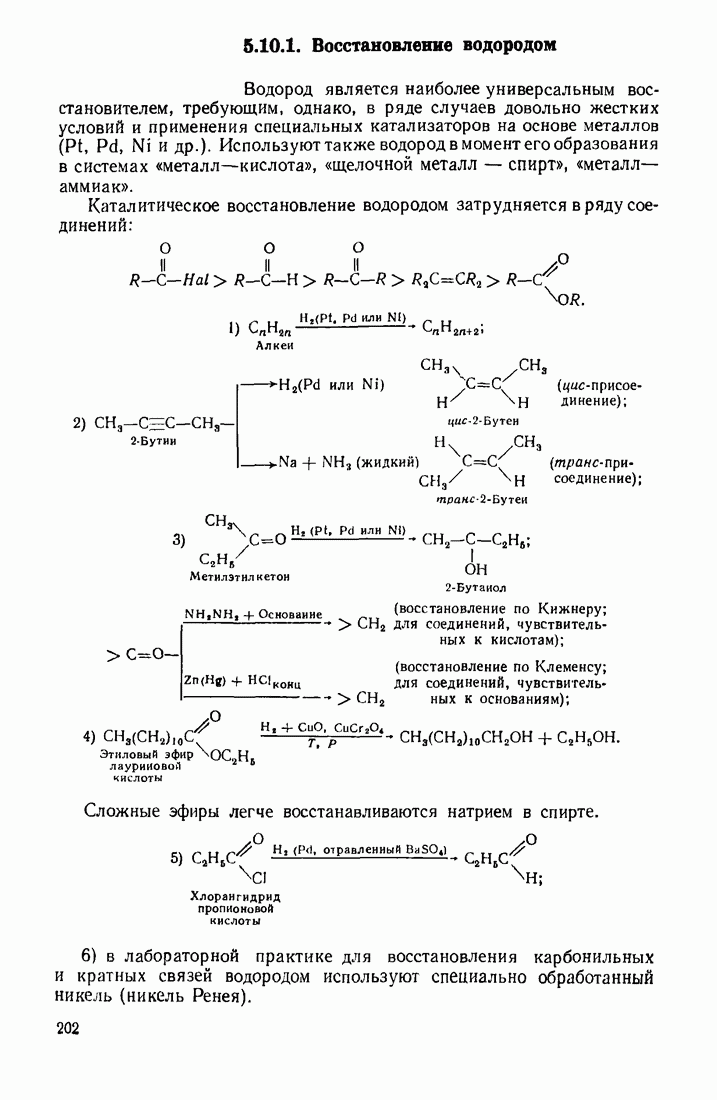
- 5.10. ВОССТАНОВЛЕНИЕ
- 5.11. АЛКАНЫ
- 5.12 АЛКЕНЫ
- 5.13. ДИЕНОВЫЕ УГЛЕВОДОРОДЫ (1,3-ДИЕНЫ)
- 5.14. АЦЕТИЛЕНЫ
- 5.15 АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- 5.16. ГАЛОГЕН АЛКАНЫ
- 5.17. СПИРТЫ
- 5.18. АЛЬДЕГИДЫ И КЕТОНЫ
- 5.19. КАРБОНОВЫЕ КИСЛОТЫ
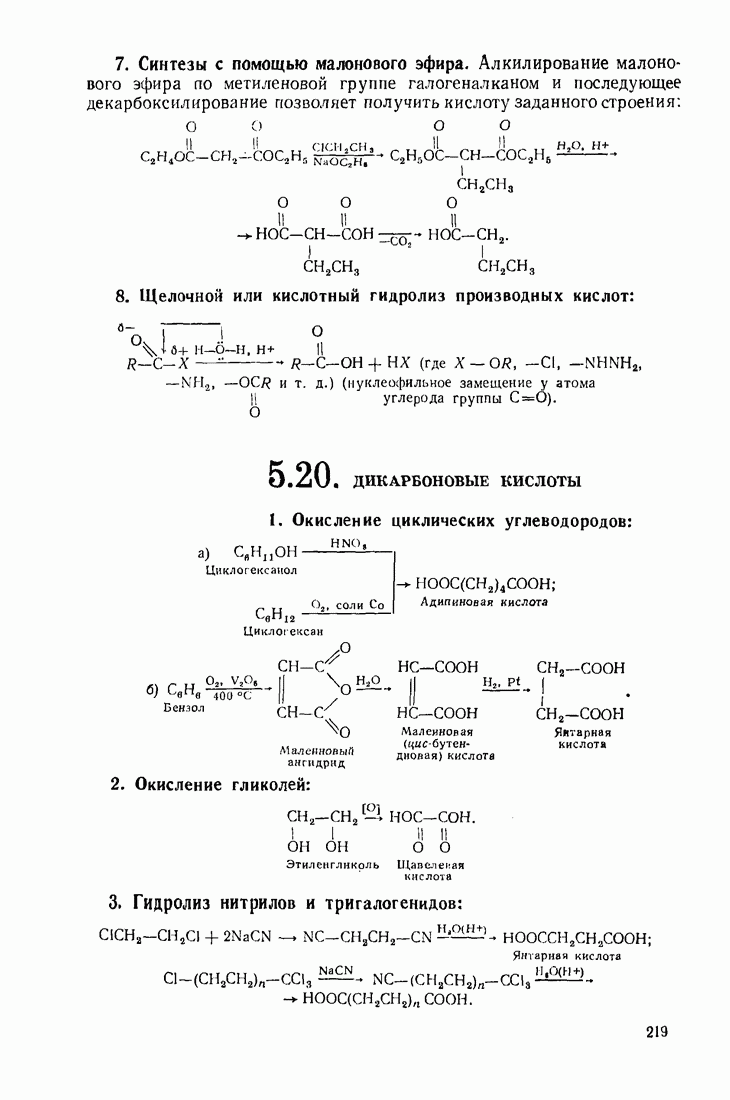
- 5.20. ДИКАРБОНОВЫЕ КИСЛОТЫ
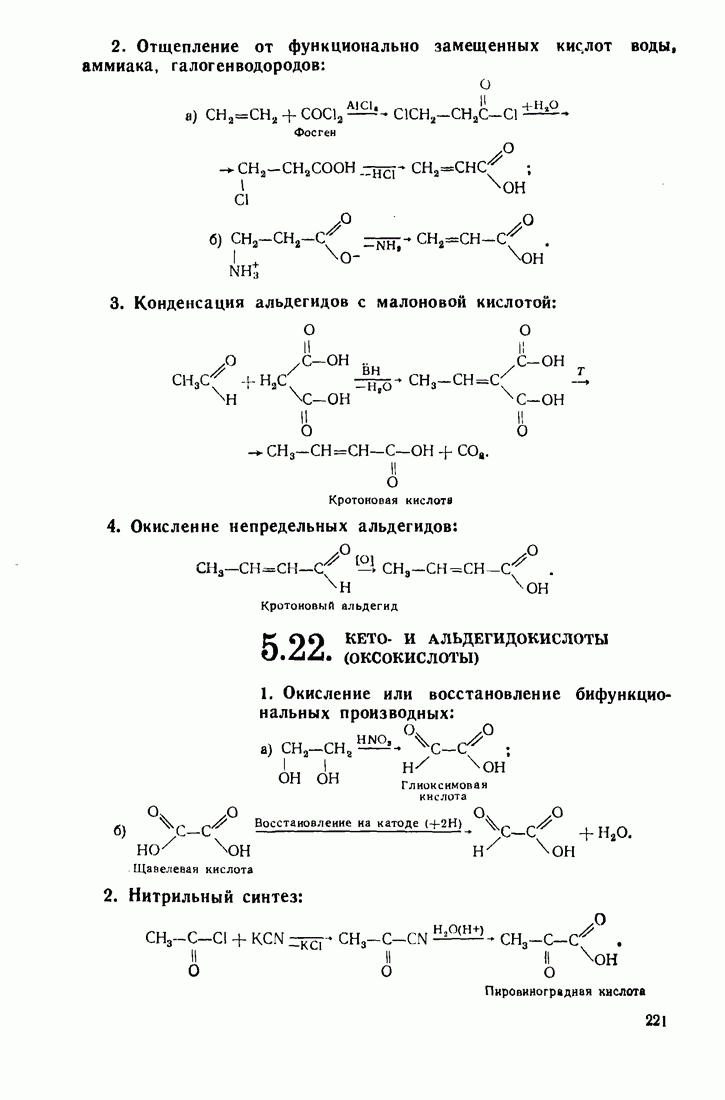
- 5.21. НЕПРЕДЕЛЬНЫЕ КИСЛОТЫ
- 5.22. КЕТО- И АЛЬДЕГИДОКИСЛОТЫ (ОКСОКИСЛОТЫ)
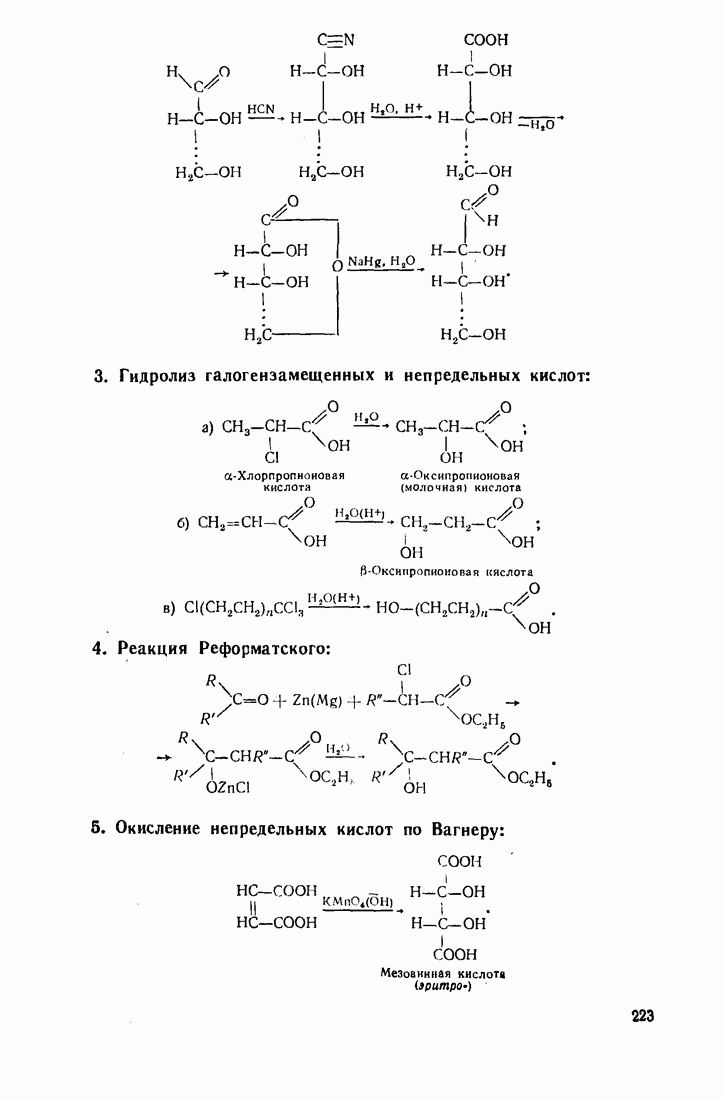
- 5.23. ОКСИКИСЛОТЫ
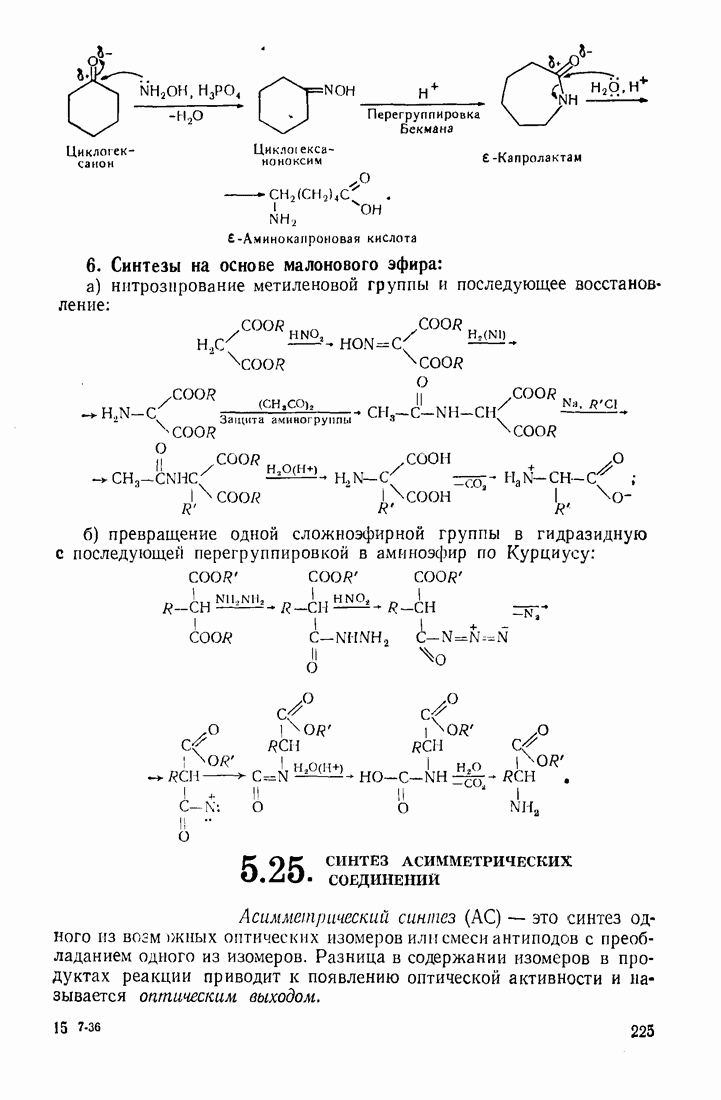
- 5.24. АМИНОКИСЛОТЫ
- 5.25 СИНТЕЗ АСИММЕТРИЧЕСКИХ СОЕДИНЕНИЙ
- 6. Некоторые понятия физической органической химии
- 6.1. СВЯЗЬ СОСТАВА И СТРОЕНИЯ СОЕДИНЕНИЙ С ФИЗИЧЕСКИМИ СВОЙСТВАМИ
- 6.2. ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 6.3. КИСЛОТЫ И ОСНОВАНИЯ В ОРГАНИЧЕСКОЙ ХИМИИ
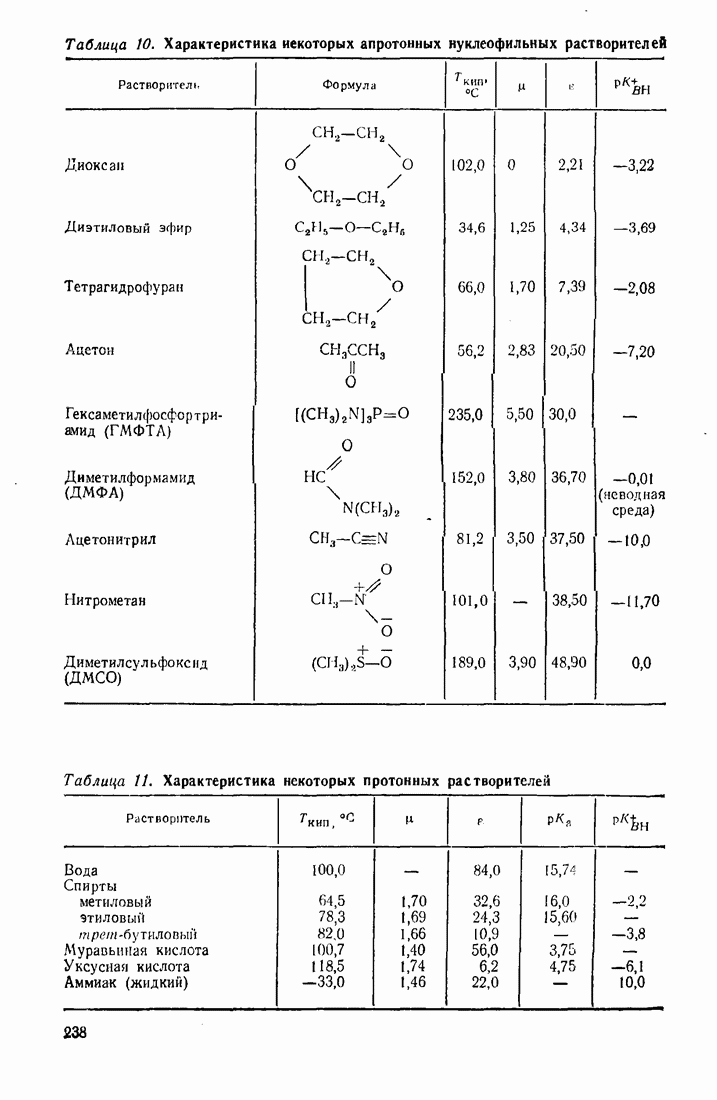
- 6.4. ОРГАНИЧЕСКИЕ РАСТВОРИТЕЛИ И ИХ ВЛИЯНИЕ НА СКОРОСТЬ И МЕХАНИЗМ РЕАКЦИЙ
- 6.5. КАТАЛИЗ ОРГАНИЧЕСКИХ РЕАКЦИЙ
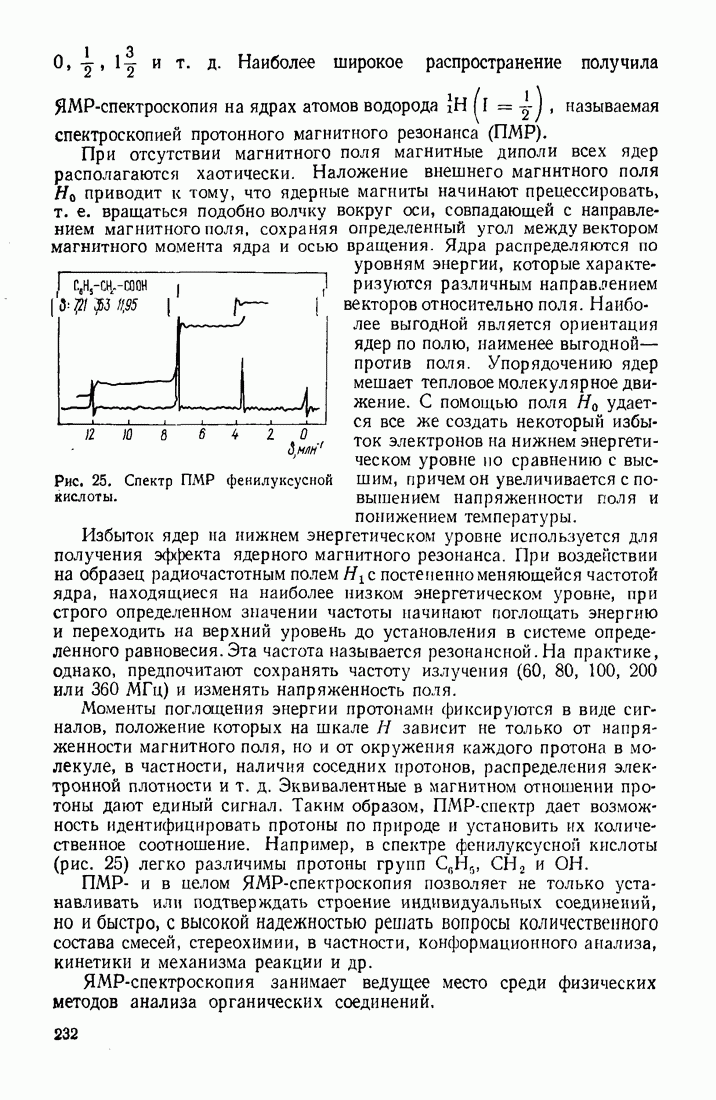
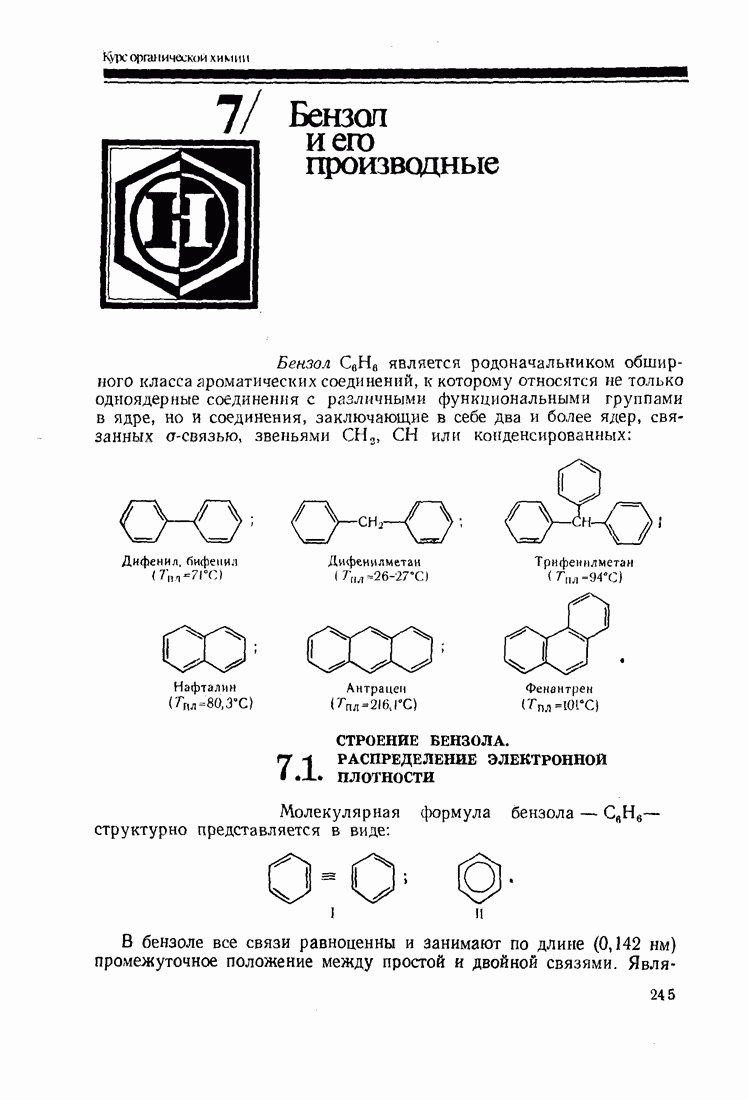
- 7. Бензол и его производные
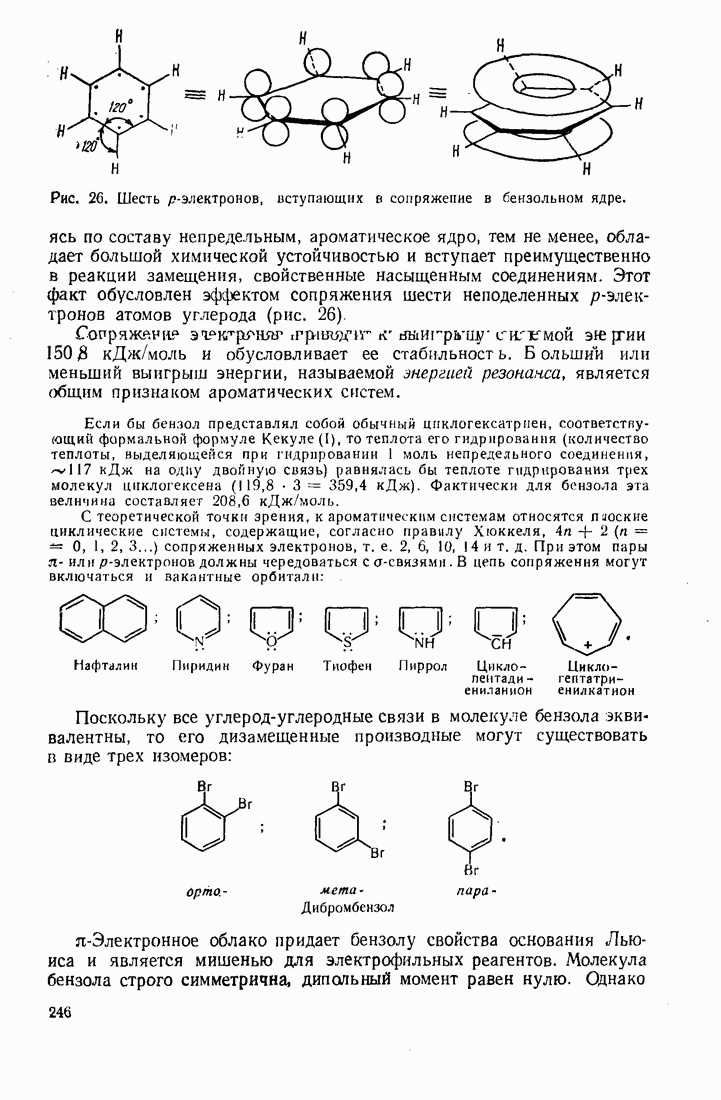
- 7.1. СТРОЕНИЕ БЕНЗОЛА. РАСПРЕДЕЛЕНИЕ ЭЛЕКТРОННОЙ ПЛОТНОСТИ
- 7.2. ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ В БЕНЗОЛЬНОМ ЯДРЕ
- 7.3. НУКЛЕОФИЛЬНОЕ ЗАМЕЩЕНИЕ В БЕНЗОЛЬНОМ ЯДРЕ
- 7.4. ЭЛЕКТРОФИЛЬНОЕ ПРИСОЕДИНЕНИЕ ХЛОРА К БЕНЗОЛЬНОМУ ЯДРУ
- 7.5. АЛКИЛАРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ
- 7.6. ГАЛОГЕНБЕНЗОЛЫ
- 7.7. ФЕНОЛЫ
- 7.8. НИТРОСОЕД ИНЕНИЯ
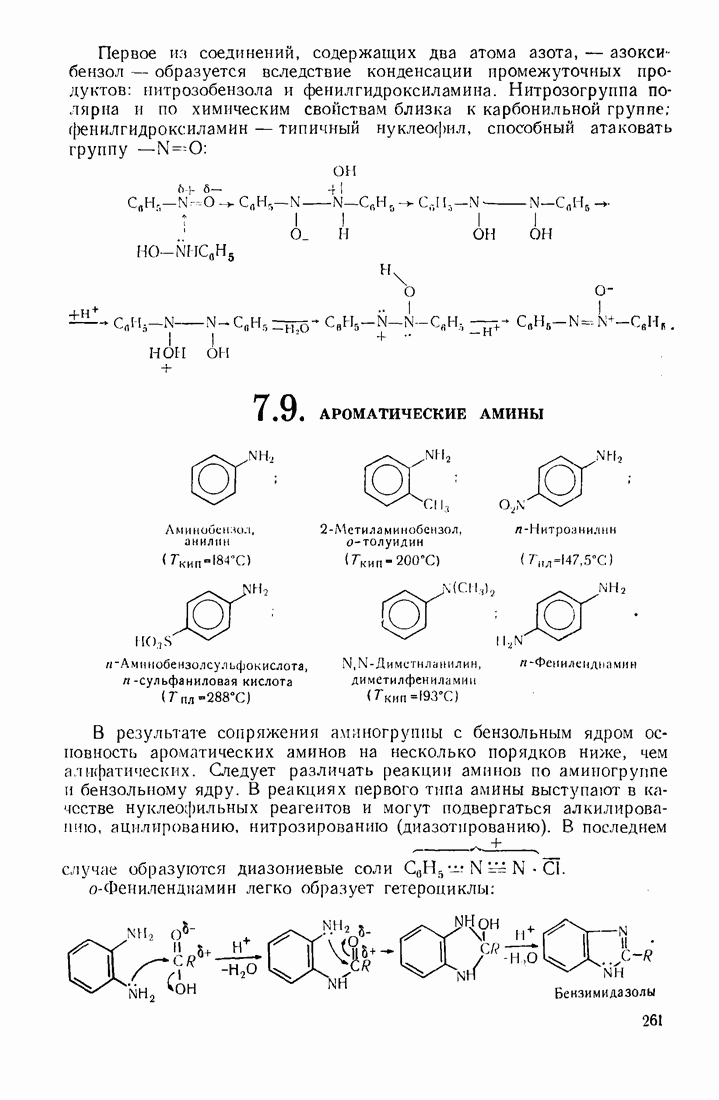
- 7.9. АРОМАТИЧЕСКИЕ АМИНЫ
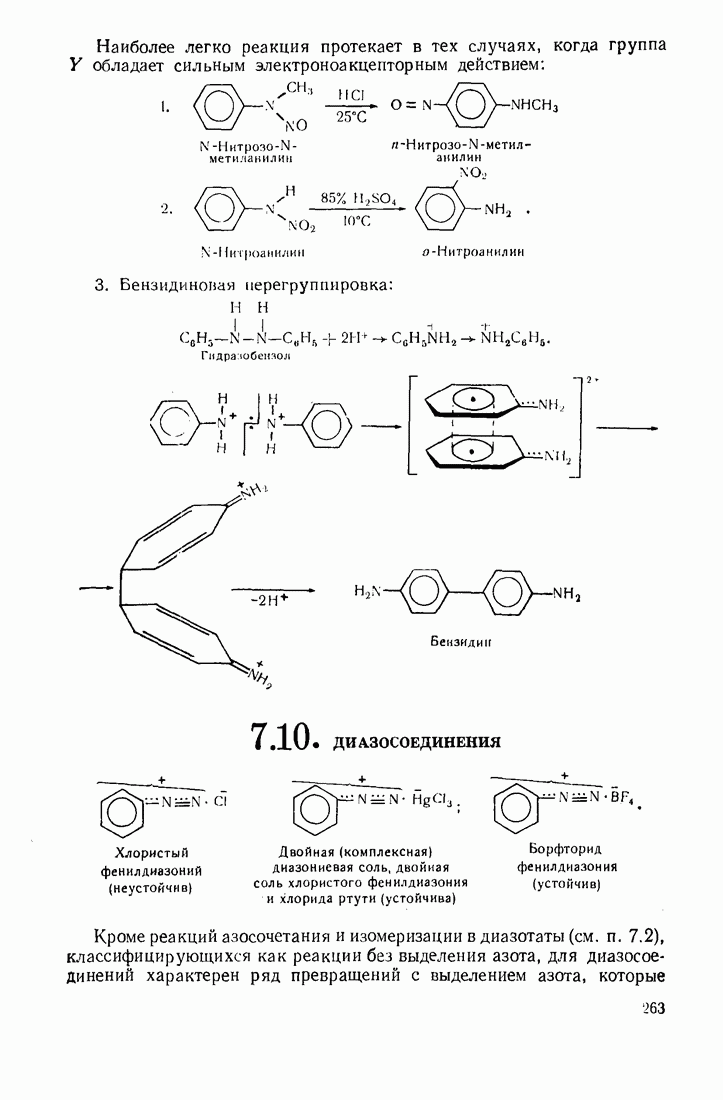
- 7.10. ДИАЗОСОЕДИНЕНИЯ
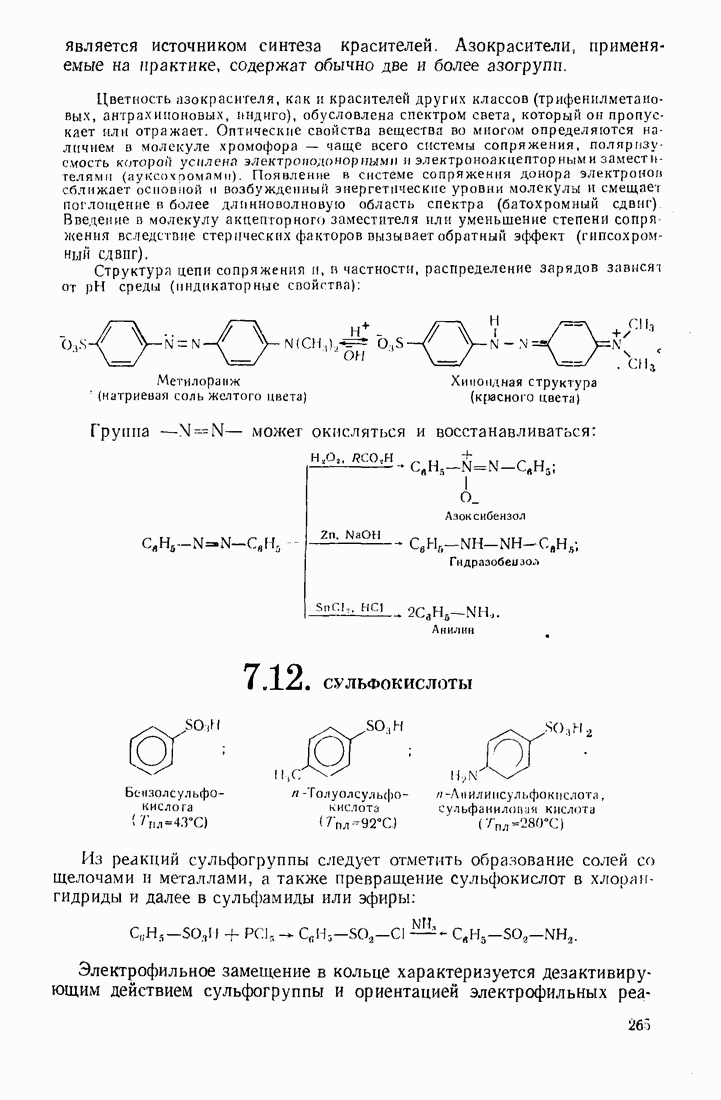
- 7.11. АЗОСОЕДИНЕНИЯ
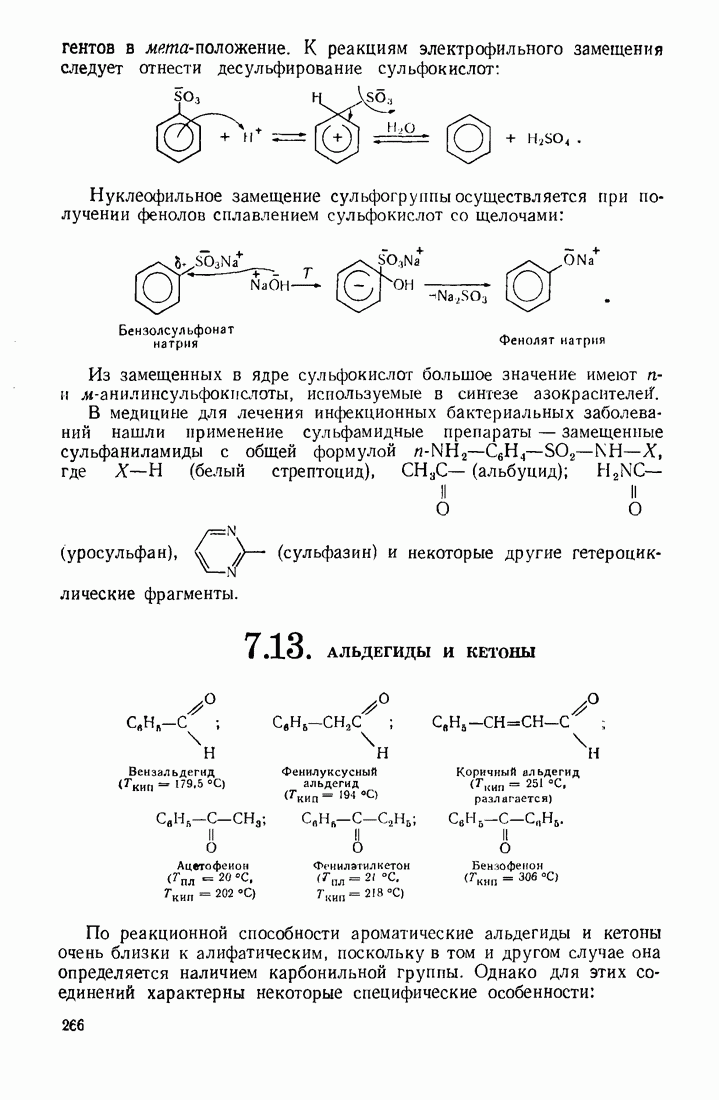
- 7.12. СУЛЬФОКИСЛОТЫ
- 7.13. АЛЬДЕГИДЫ И КЕТОНЫ
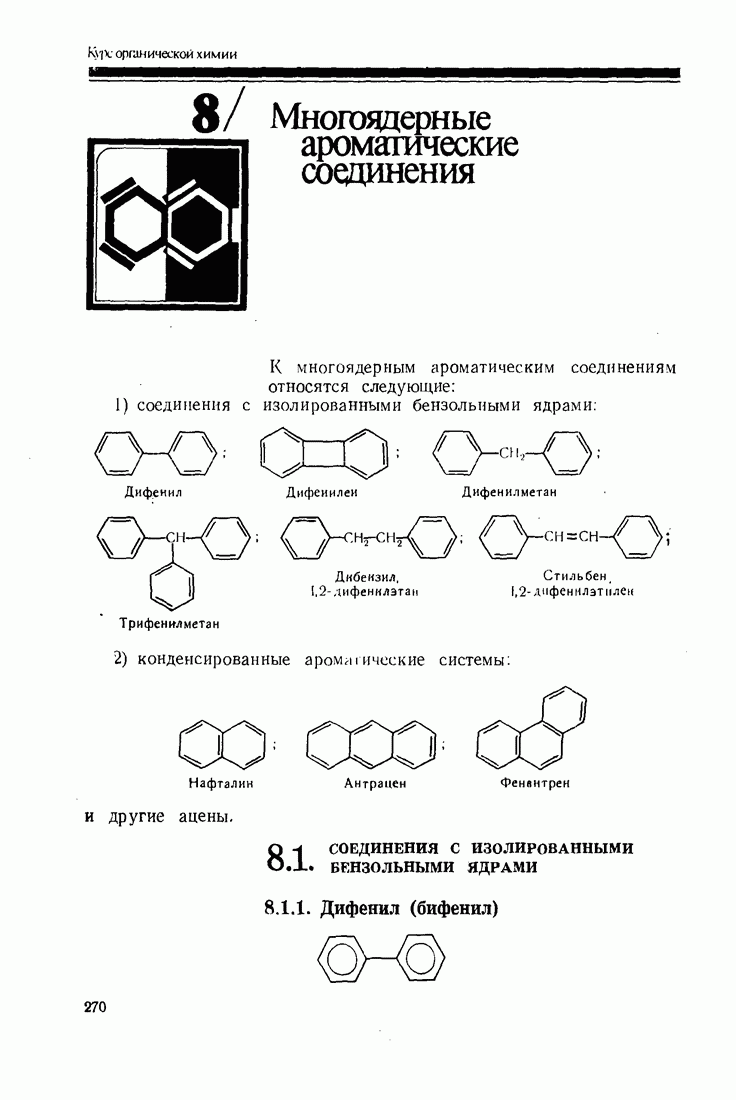
- 8. Многоядерные ароматические соединения
- 8.1. СОЕДИНЕНИЯ С ИЗОЛИРОВАННЫМИ БЕНЗОЛЬНЫМИ ЯДРАМИ
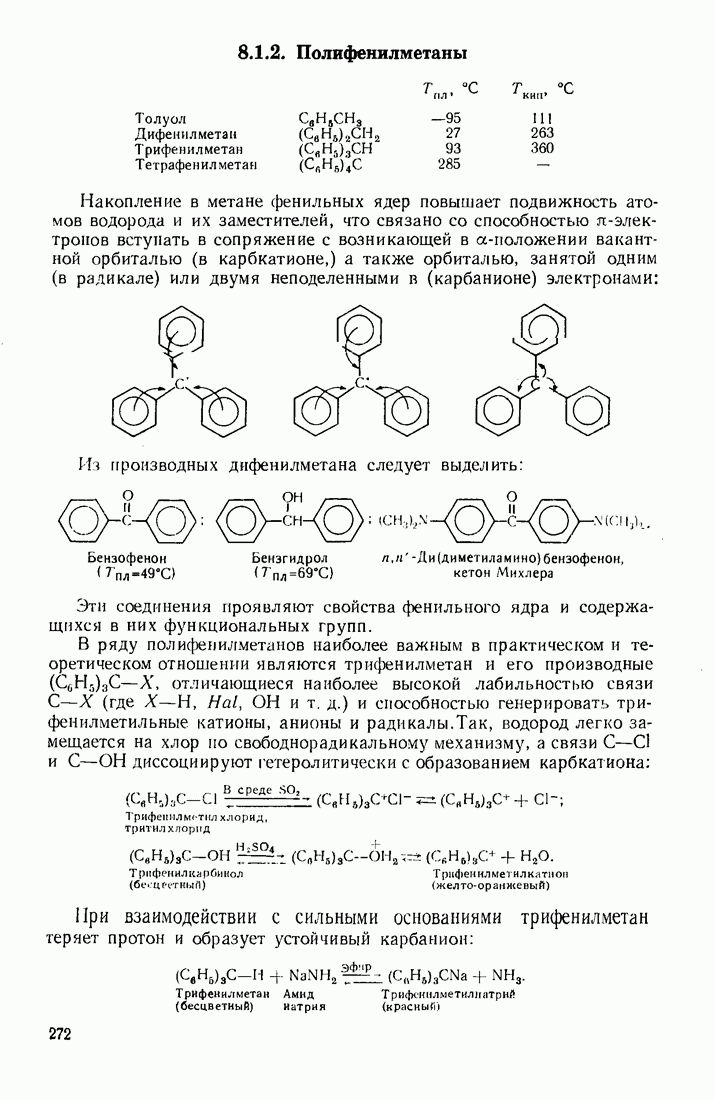
- 8.1.2. Полифенилметаны
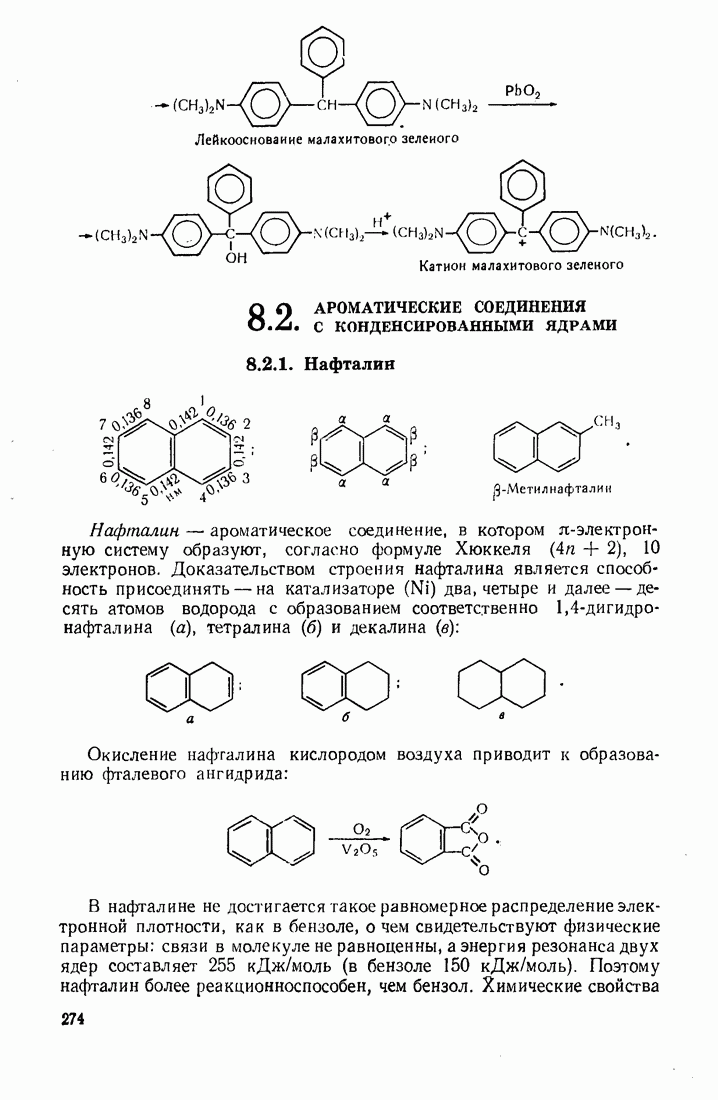
- 8.2. АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ С КОНДЕНСИРОВАННЫМИ ЯДРАМИ
- 8.2.2. Антрацен
- 8.2.3. Фенантрен
- 9. Методы синтеза в ряду ароматических соединений
- 9.1. ГАЛОГЕНИРОВАНИЕ
- 9.2. НИТРОВАНИЕ
- 9.3. СУЛЬФИРОВАНИЕ
- 9.4. АЛКИЛИРОВАНИЕ
- 9.5. АЦИЛИРОВАНИЕ
- 9.6. ГИДРОКСИЛИРОВАНИЕ
- 9.7. АМИНИРОВАНИЕ
- 9.8. НИТРОЗИРОВАНИЕ
- 9.9. КАРБОНИЛИРОВАНИЕ
- 9.10. КАРБОКСИЛИРОВАНИЕ
- 9.11. ОКИСЛЕНИЕ
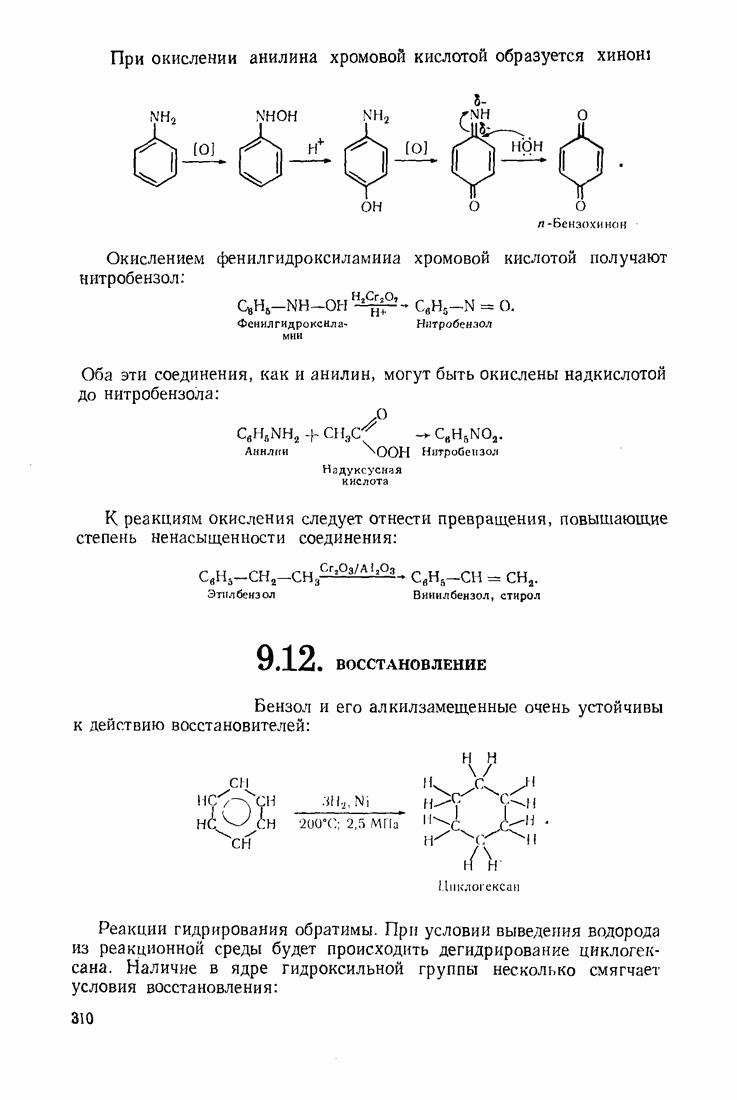
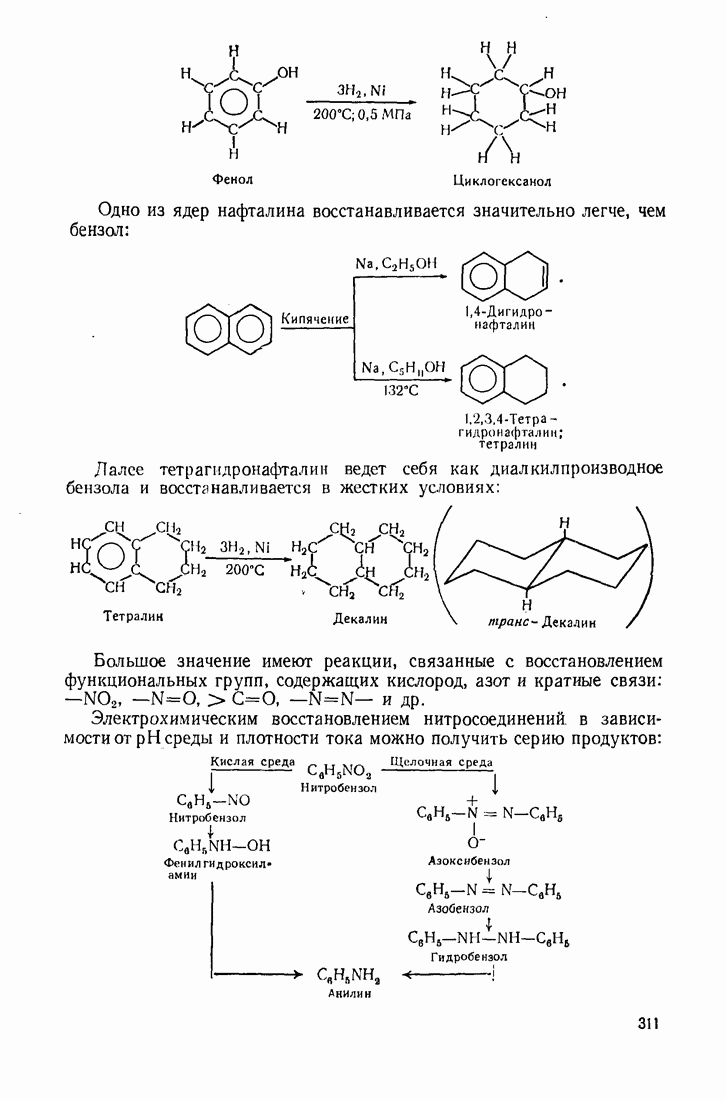
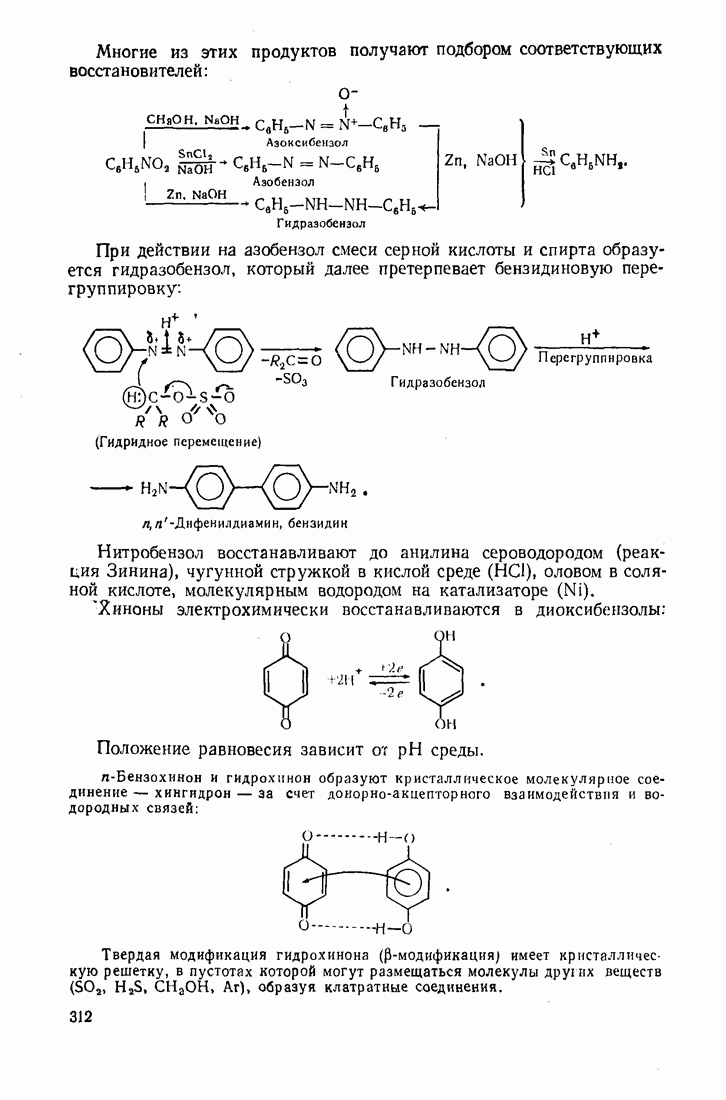
- 9.12. ВОССТАНОВЛЕНИЕ
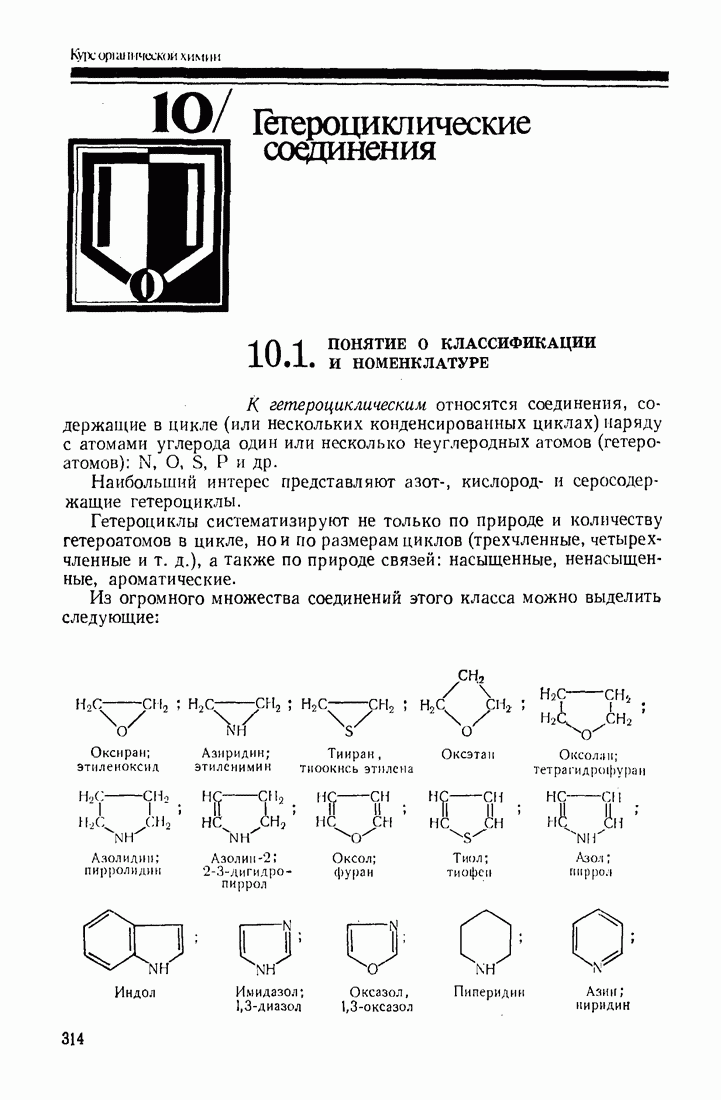
- 10. Гетероциклические соединения
- 10.2. ОБЩАЯ ХАРАКТЕРИСТИКА СТРОЕНИЯ И РЕАКЦИОННОЙ СПОСОБНОСТИ
- 10.3. ПЯТИ- И ШЕСТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С ОДНИМ ГЕТЕРОАТОМОМ
- 10.4. ГЕТЕРОЦИКЛЫ С НЕСКОЛЬКИМИ ГЕТЕРОАТОМАМИ
- 10.5. МЕТОДЫ СИНТЕЗА ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ
- 10.6. П0НЯТИЕ О ПРИРОДНЫХ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЯХ
- 11. Зпементоорганические соединения
- 11.2. ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ НЕКОТОРЫХ НЕМЕТАЛЛОВ
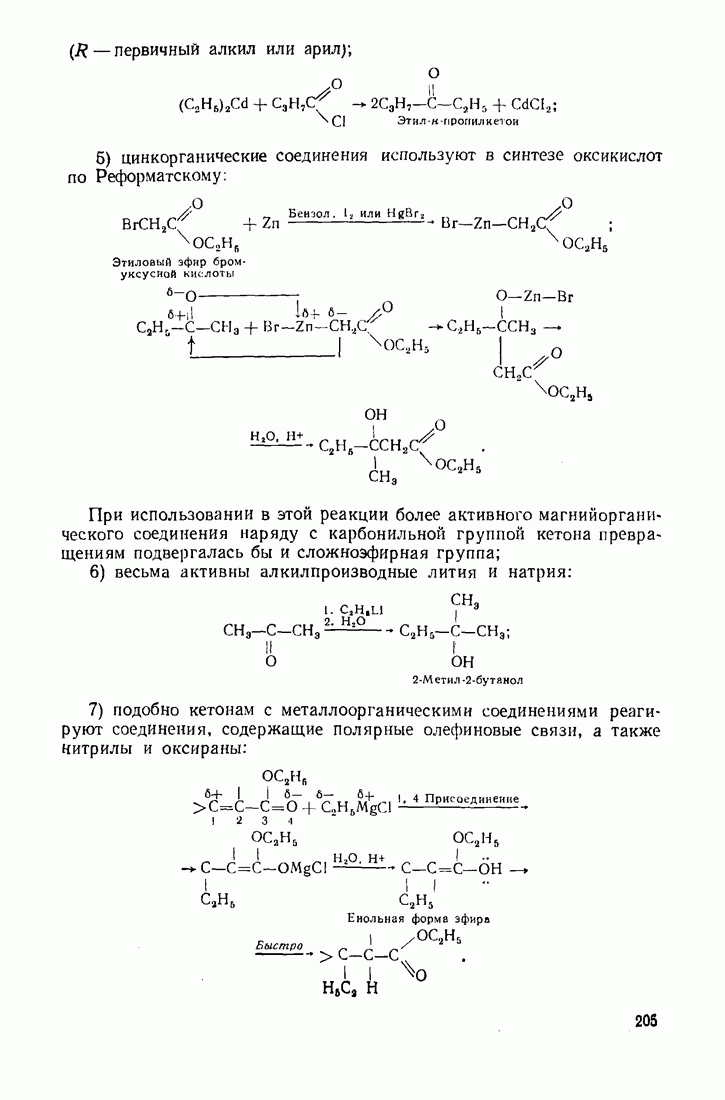
- 11.3. МЕГАЛЛООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- 11.4. ОРГАНИЧЕСКИЕ ПРОИЗВОДНЫЕ ПЕРЕХОДНЫХ МЕТАЛЛОВ
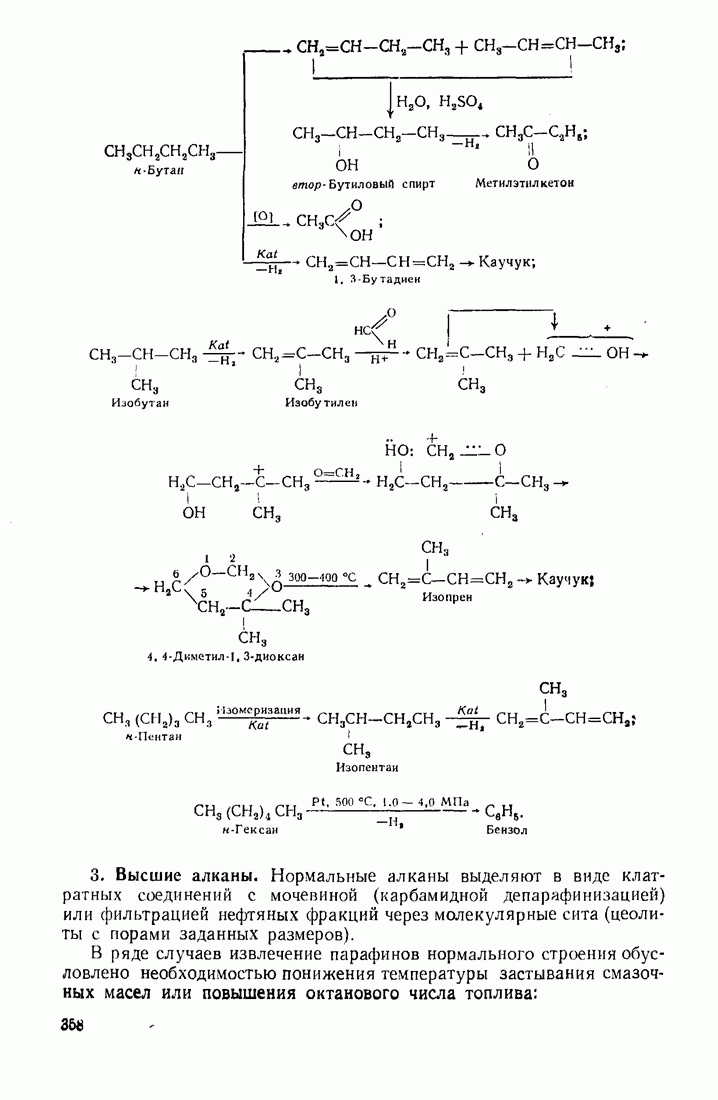
- 12. Сырье и основные направления развития промышленности органического синтеза
- 12.1.1. Нефть и сопутствующий природный газ
- 12.1.2. Углехимическое сырье
- 12.1.3. Лесохимическое и сельскохозяйственное сырье
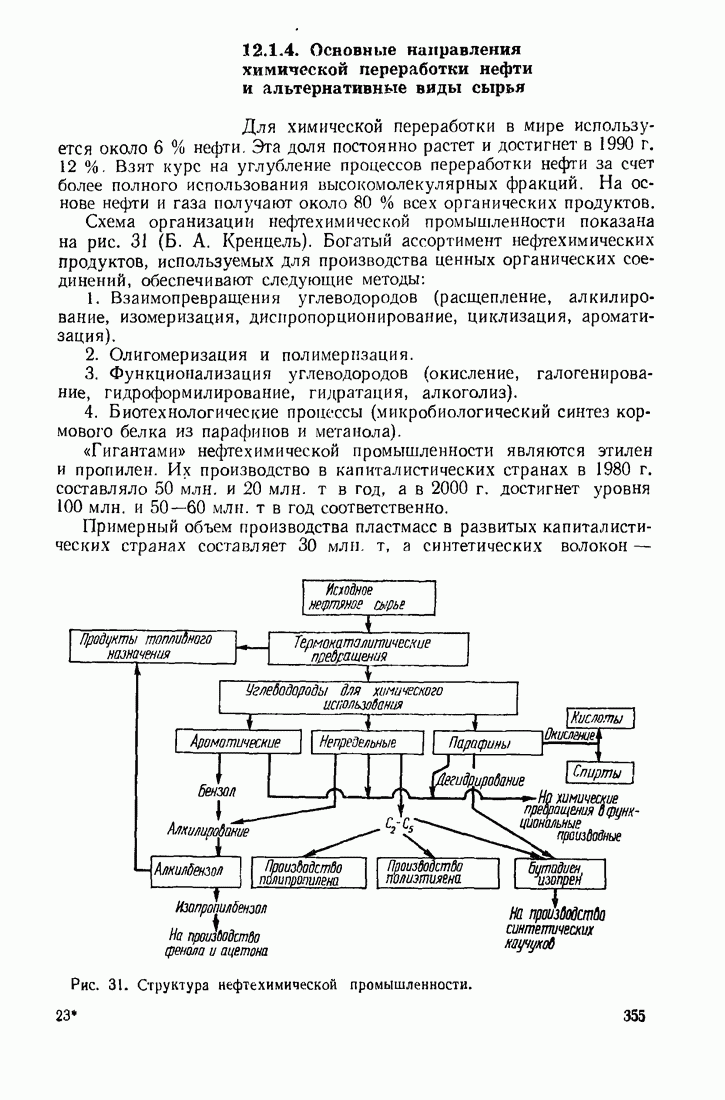
- 12.1.4. Основные направления химической переработки нефти и альтернативные виды сырья
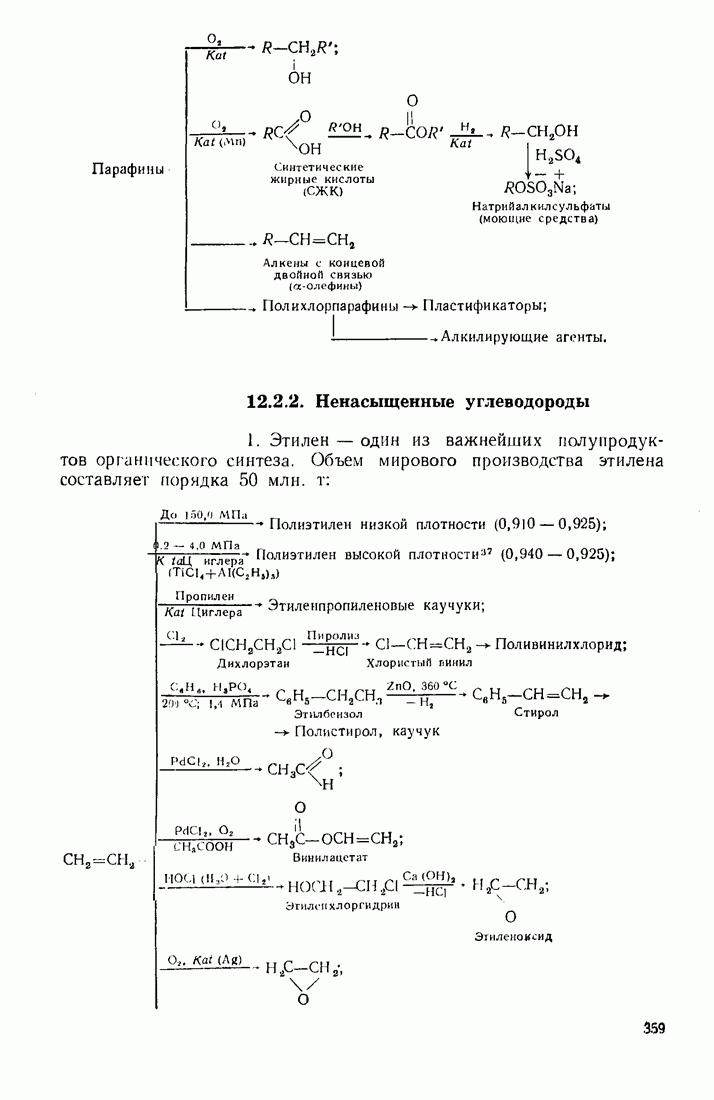
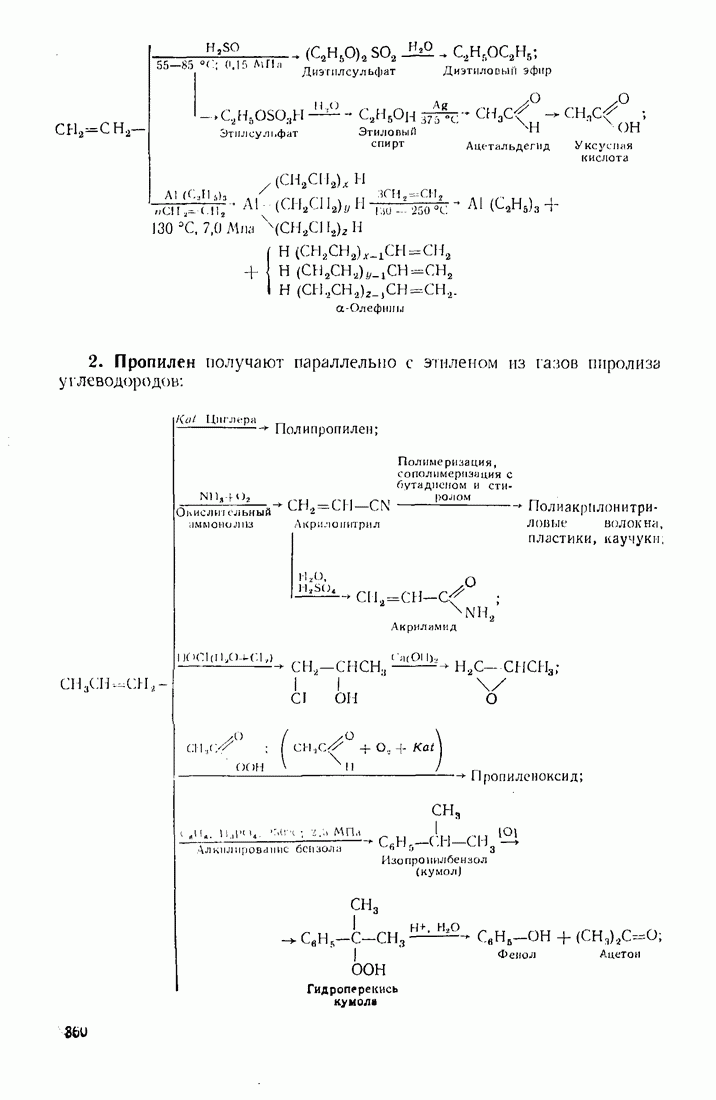
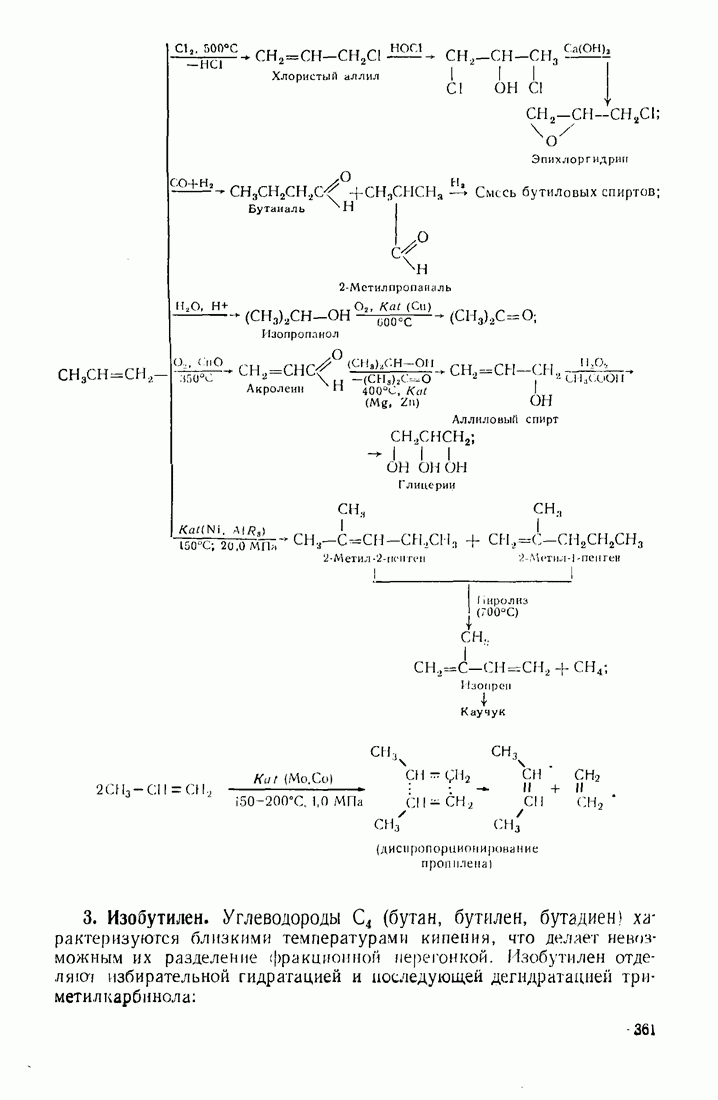
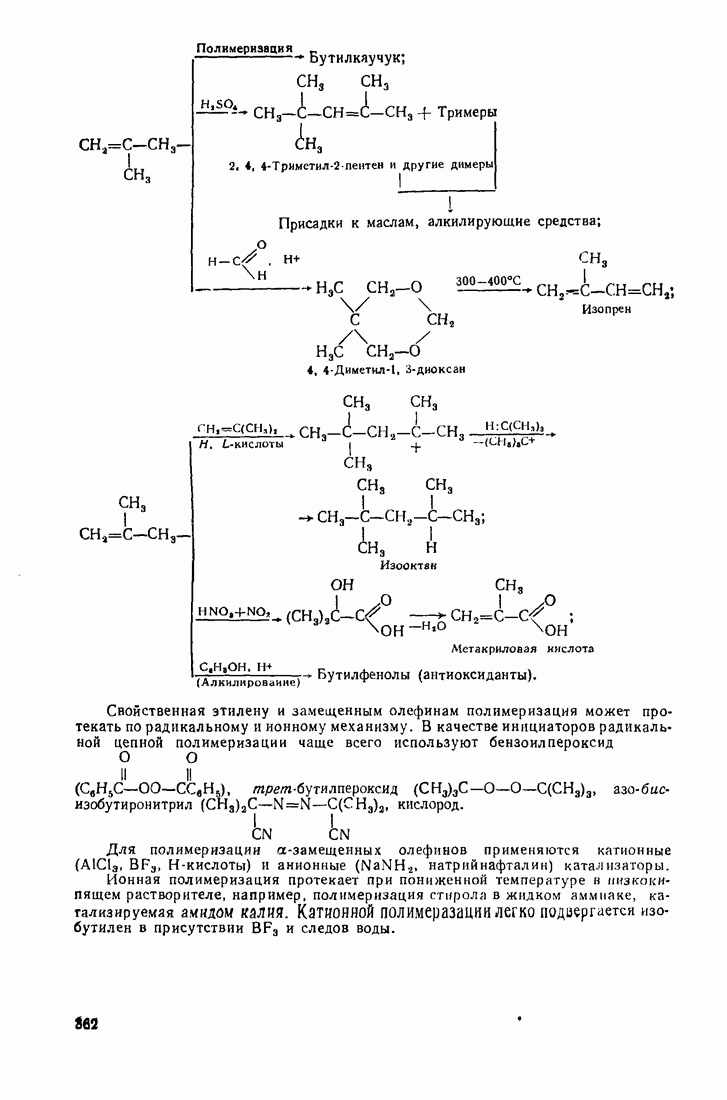
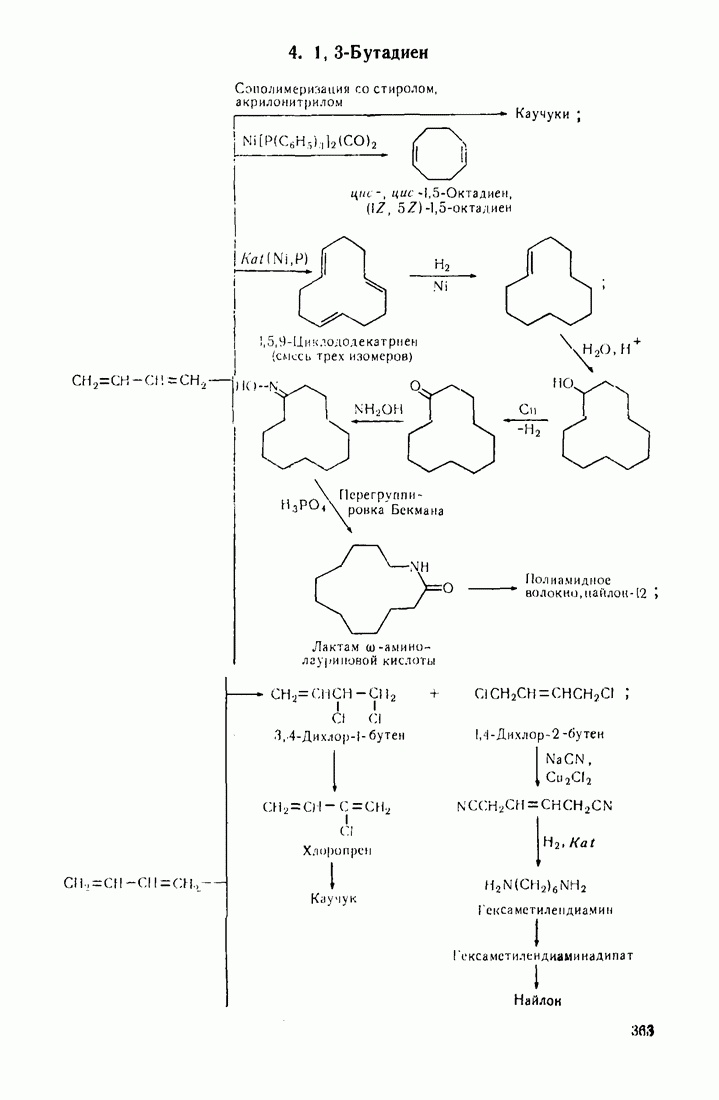
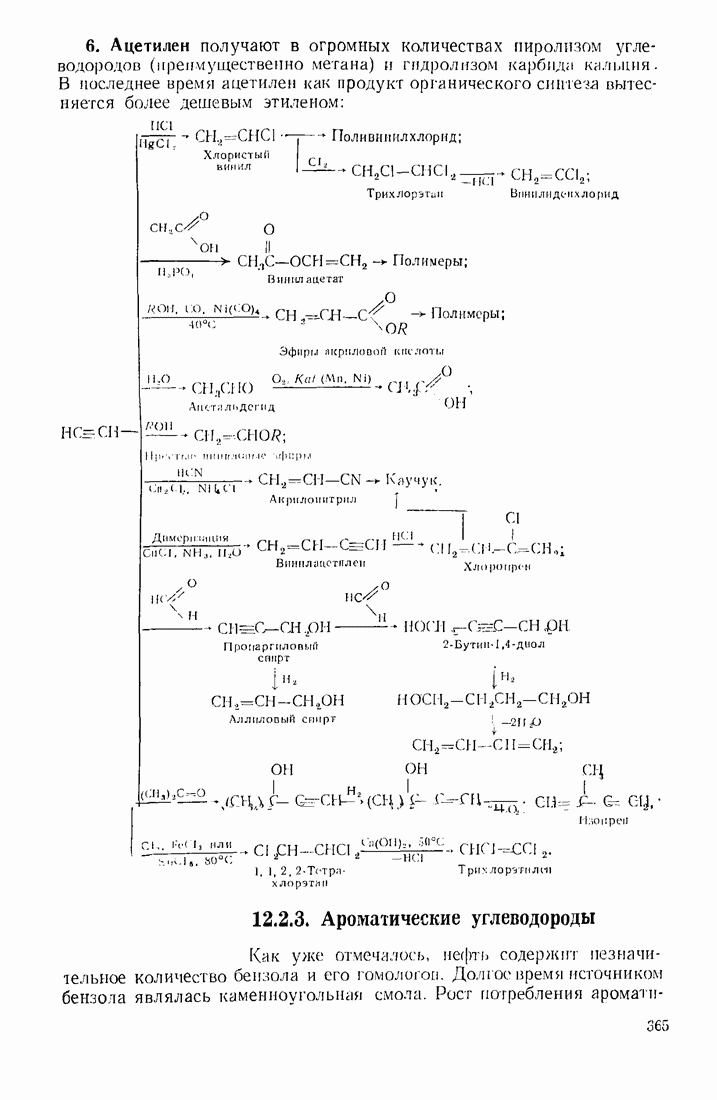
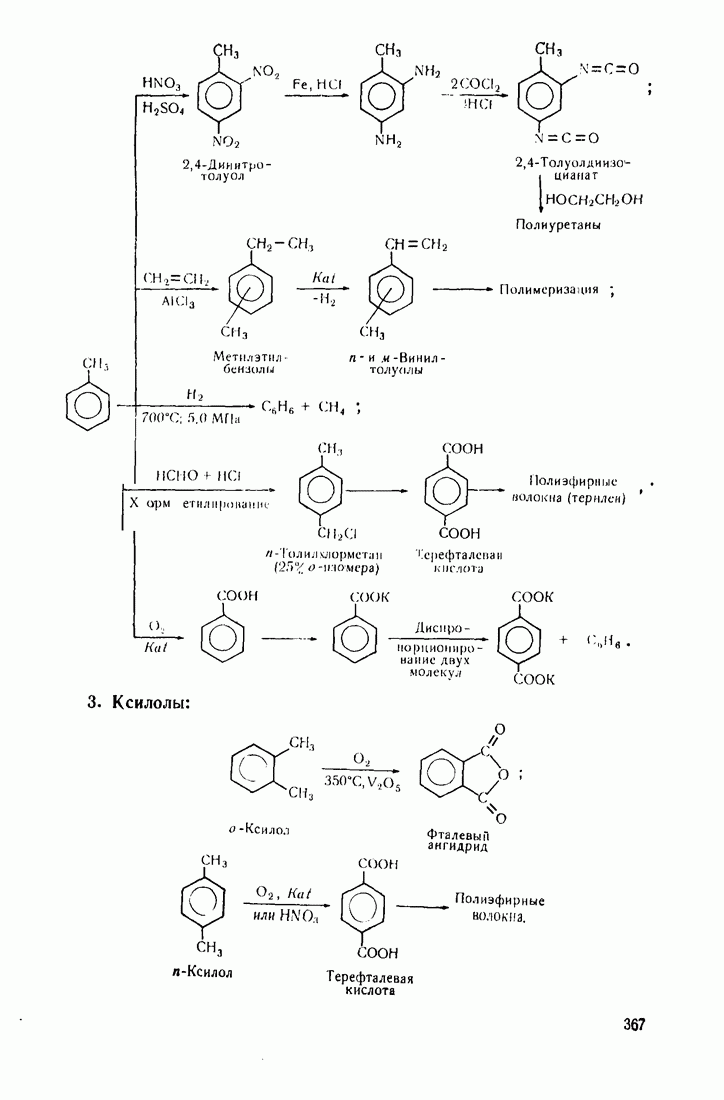
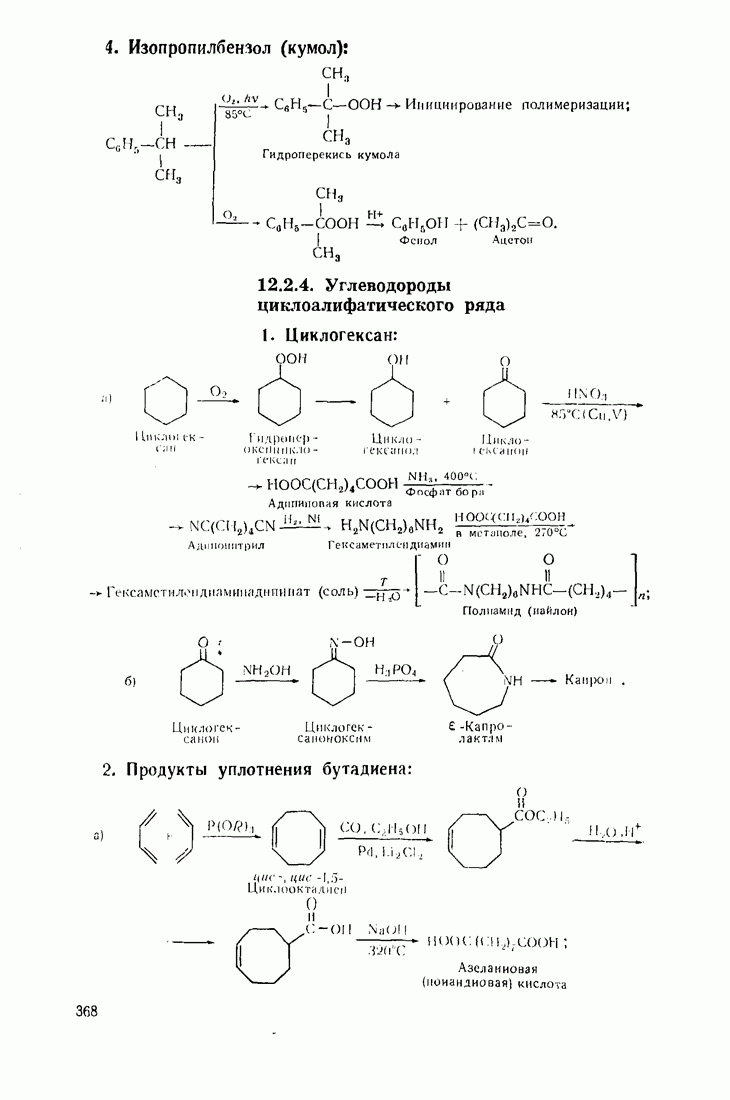
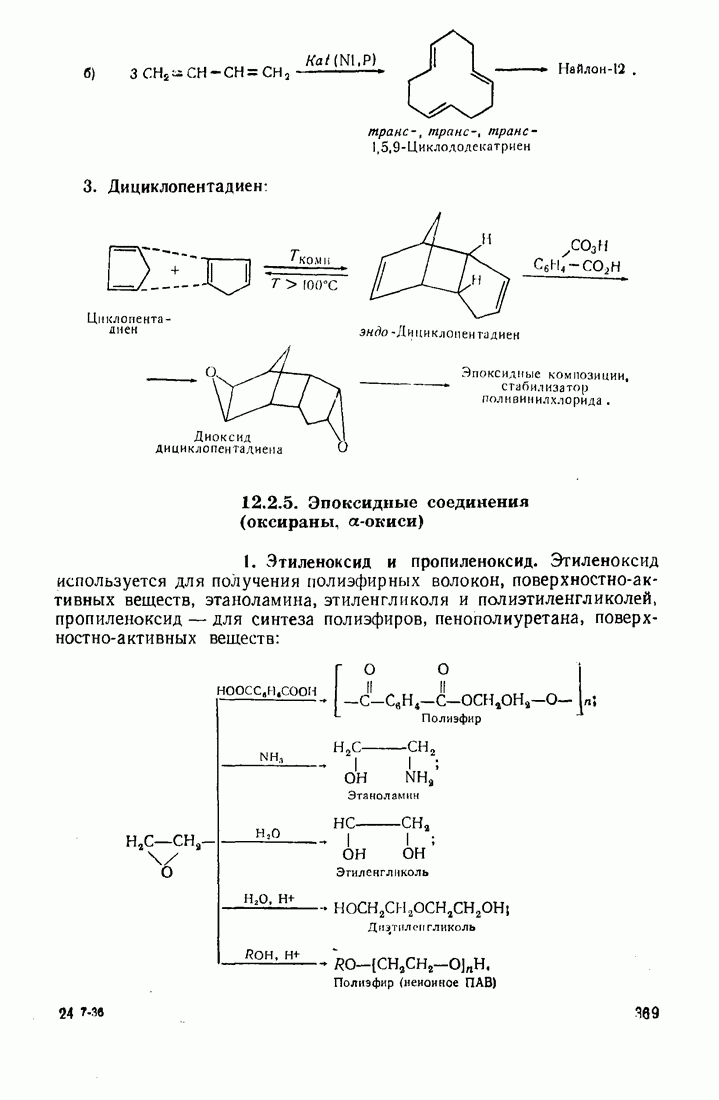
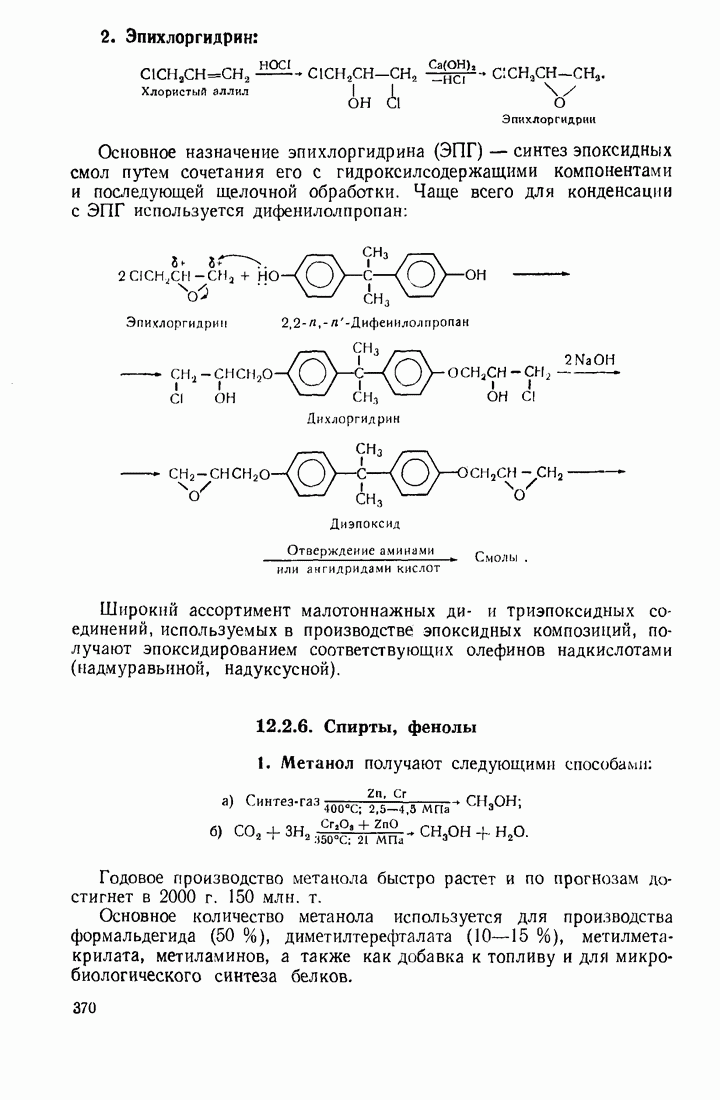
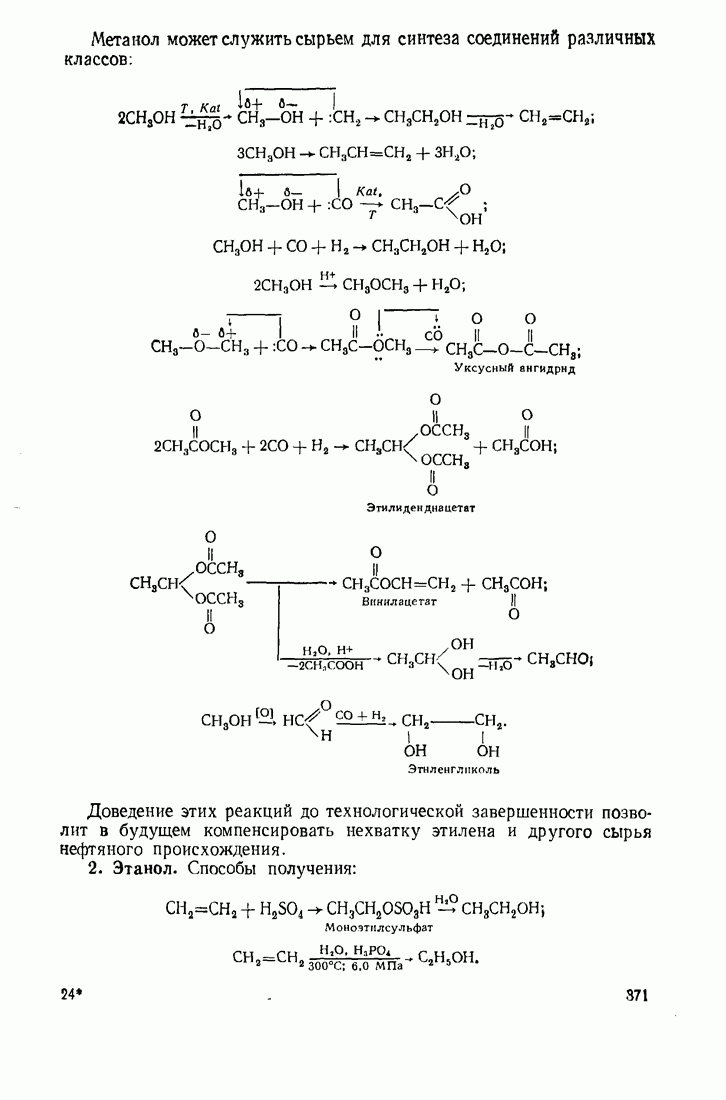
- 12.2. ПУТИ ИСПОЛЬЗОВАНИЯ УГЛЕВОДОРОДОВ И ИХ ПРОИЗВОДНЫХ
- 12.3. РАЗВИТИЕ ХИМИЧЕСКОЙ ПРОМЫШЛЕННОСТИ В СССР В ДВЕНАДЦАТОЙ ПЯТИЛЕТКЕ