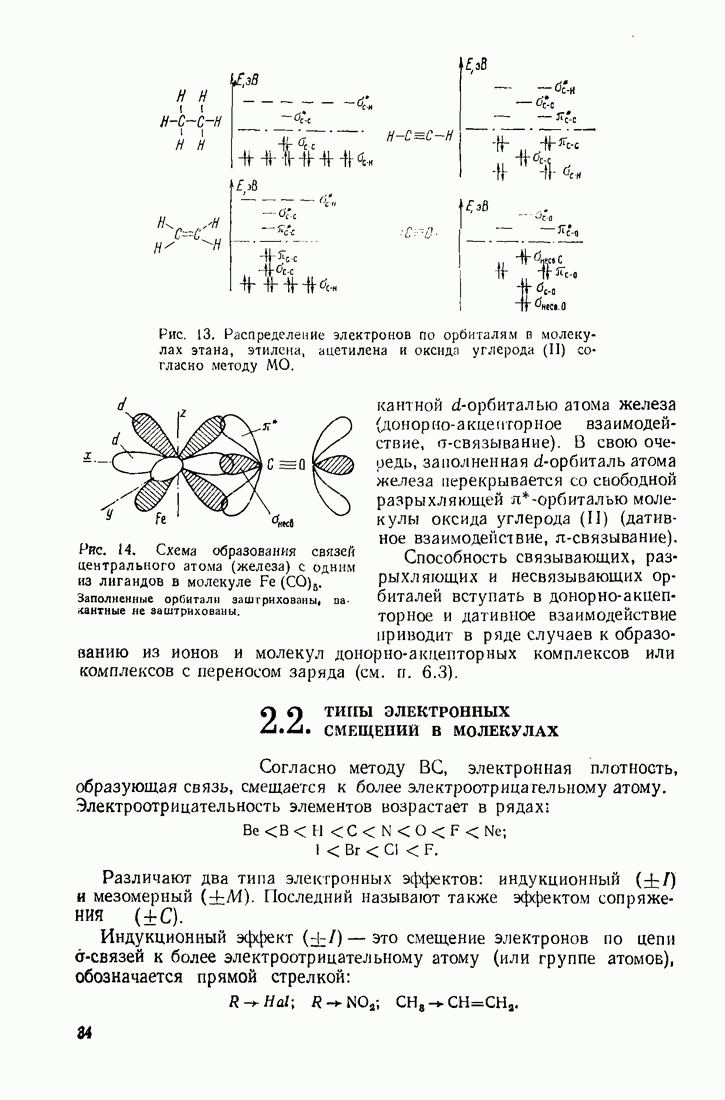
| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
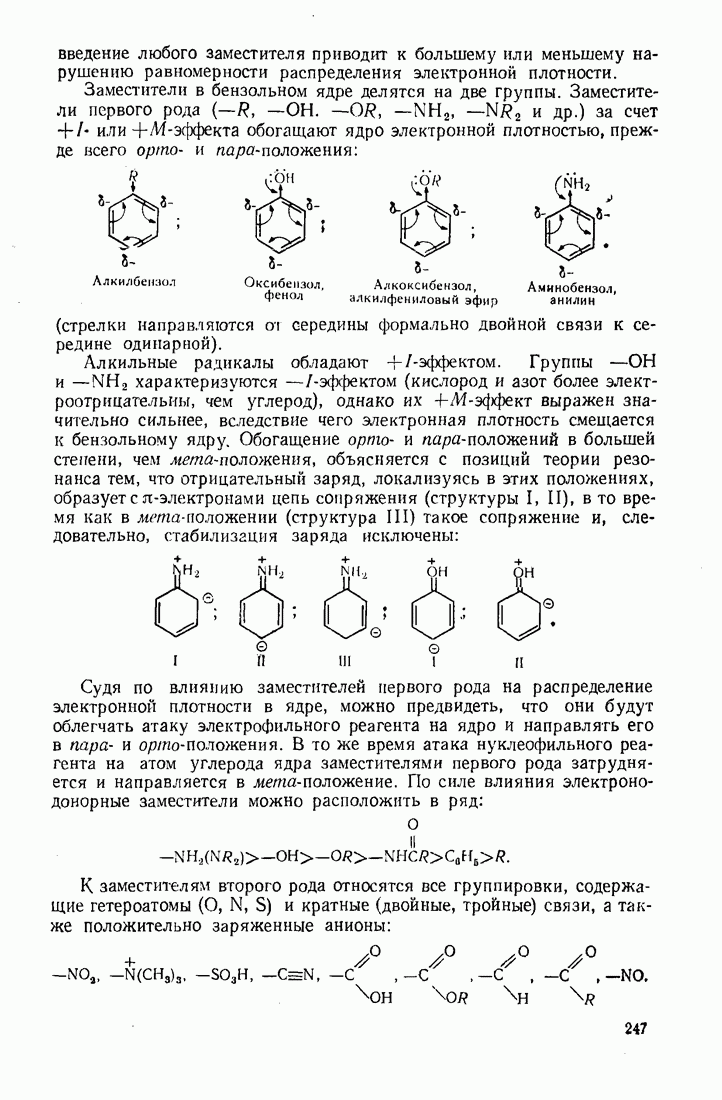
3.13. ФОСФОРОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
Фосфор — элемент пятой группы периодической системы Д. И. Менделеева и во многом является аналогом азота (рис. 17).
Отличительной особенностью фосфора является то, что его валентные электроны находятся на более высоком энергетическом уровне, причем высшие занятые орбитали (ВЗО) и низшие вакантные орбитали  достаточно близки по энергии для осуществления перехода одного электрона на З-орбиталь. В этом случае в образовании связей участвует пять орбиталей
достаточно близки по энергии для осуществления перехода одного электрона на З-орбиталь. В этом случае в образовании связей участвует пять орбиталей  Более того, электрон извне может занимать шестую орбиталь атома фосфора, вследствие чего последний становится шестиковалентным
Более того, электрон извне может занимать шестую орбиталь атома фосфора, вследствие чего последний становится шестиковалентным  Максимальная ковалентность азота, как известно, равна четырем
Максимальная ковалентность азота, как известно, равна четырем 
Соединения пятиковалентного фосфора имеют форму тригональной бипирамиды, хотя не исключена форма и четырехгранной пирамиды (рис. 18).
Фосфор в отличие от азота не образует стабильных ненасыщенных соединений типа нитро-, нитрозо-, азо-, диазосоединений.
Азот образует сравнительно стабильные окисленные формы  для фосфора более характерны соответствующие гидратированные формы:
для фосфора более характерны соответствующие гидратированные формы:

Кратные связи  в соединениях фосфора следует рассматривать как занимающие промежуточное положение между семи-
в соединениях фосфора следует рассматривать как занимающие промежуточное положение между семи-

Рис. 17. Электронное строение атомов азота  и фосфора (б).
и фосфора (б).

Рис. 18. Геометрия соединении пятивалентного фосфора.
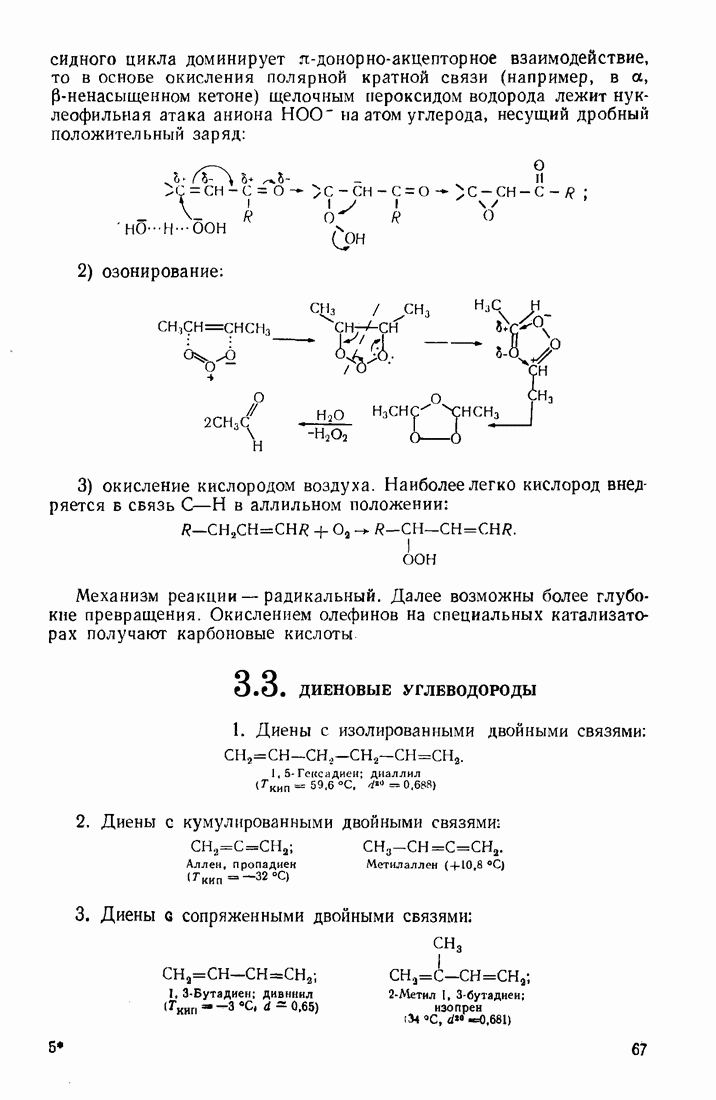
полярной и  -связью типа
-связью типа  (участие
(участие  -Орбитали в боковом перекрывании неэффективно):
-Орбитали в боковом перекрывании неэффективно):

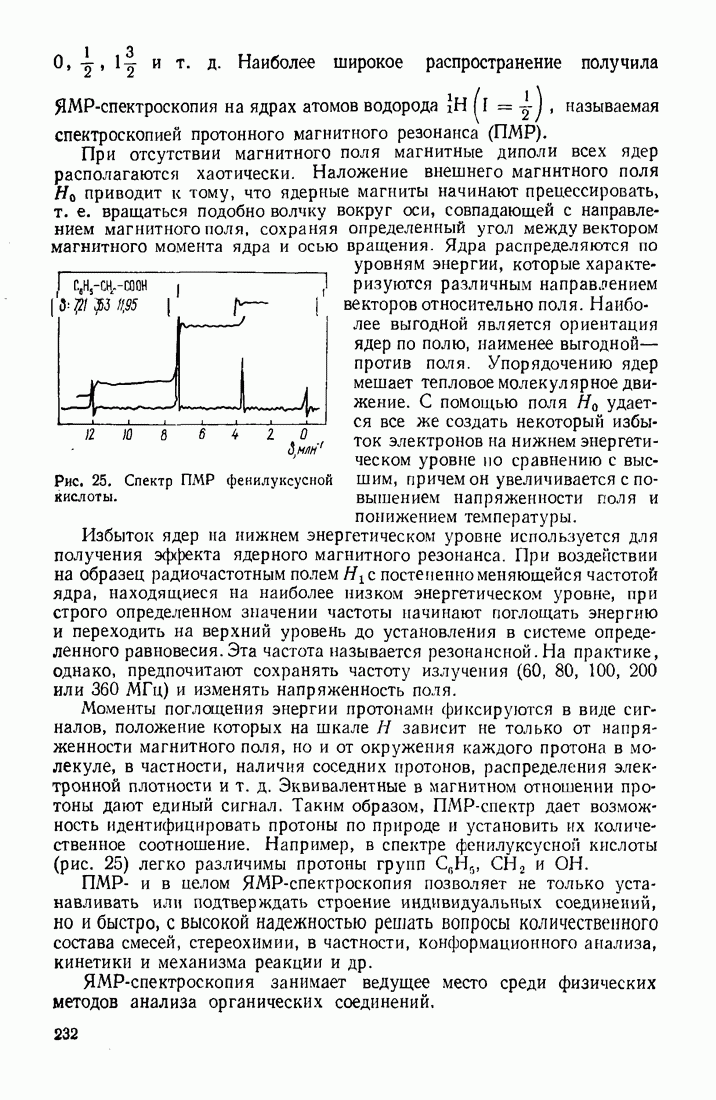
Об этом свидетельствует анализ длин связей и дипольных моментов соединений.
Валентные электроны атома фосфора располагаются дальше от ядра, чем в атоме азота, и поэтому более лабильны. Энергия связей  и
и  заметно ниже, чем соответственно
заметно ниже, чем соответственно  и
и  (табл. 4). Связь
(табл. 4). Связь  легко окисляется на воздухе. В то же время фосфор образует более прочные связи с сильными акцепторами электронов (кислородом, галогенами).
легко окисляется на воздухе. В то же время фосфор образует более прочные связи с сильными акцепторами электронов (кислородом, галогенами).
Таблица 4. (см. скан) Энергия связей фосфора и азота
Наиболее характерными являются соединения трех- и пятивалентного фосфора.
Родоначальником производных трехвалентного фосфора является фосфин  (аналог NH3). Алкилфосфины
(аналог NH3). Алкилфосфины  аналоги аминов, а соли фосфония
аналоги аминов, а соли фосфония  и др.) — подобны четвертичным аммониевым солям.
и др.) — подобны четвертичным аммониевым солям.
Продукты замещения атомов водорода в фосфииах на группу  относятся к кислотам:
относятся к кислотам:

Характерно, однако, что группа  чрезвычайно неустойчива и перегруппировывается в структуру пятивалентного фосфора:
чрезвычайно неустойчива и перегруппировывается в структуру пятивалентного фосфора: 
Продукты замещения группы  на галоген можно рассматривать как галогенангидриды соответствующих кислот:
на галоген можно рассматривать как галогенангидриды соответствующих кислот:

Соединения трехвалентного фосфора часто проявляют нуклеофильные свойства за счет неподеленной пары электронов и легко переходят в соединения пятивалентного фосфора. Так, гидриды фосфора самовоспламеняются на воздухе:

Важное место в химии фосфора занимает реакция Арбузова!

В молекуле треххлористого фосфора подвижность свободной пары электронов, естественно, понижена, поэтому его алкилирование требует применения электрофильного катализатора — кислоты Льюиса:

В то же время атом фосфора, связанный с акцепторами электронов — галогенами, становится электронодефицитным и может быть подвержен нуклеофильной атаке  Например, связь
Например, связь  легко гидролизуется и восстанавливается магний-органическими соединениями:
легко гидролизуется и восстанавливается магний-органическими соединениями:

Соединения пятивалентного фосфора более устойчивы, чем трехвалентного, и могут рассматриваться как производные ряда:

Соединения, содержащие связи  и
и  классифицируются как галогенангидриды, эфиры и амиды соответствующих кислот. Наиболее типичными реакциями соединений этого ряда являются реакции нуклеофильного замещения у атома фосфора:
классифицируются как галогенангидриды, эфиры и амиды соответствующих кислот. Наиболее типичными реакциями соединений этого ряда являются реакции нуклеофильного замещения у атома фосфора:

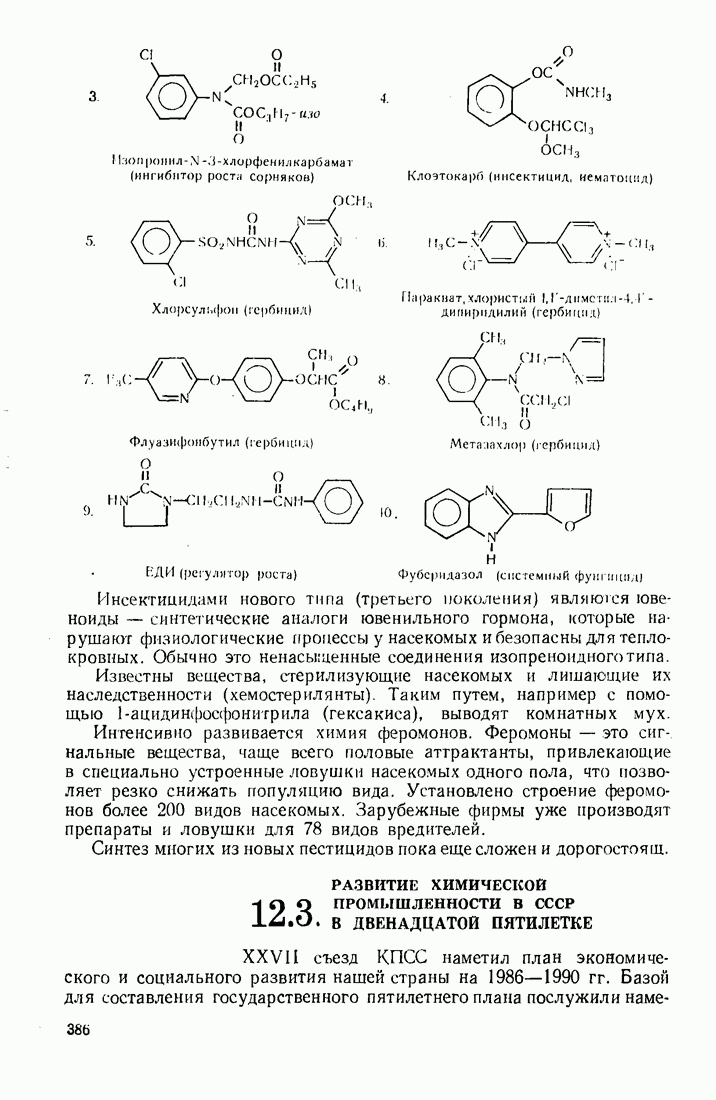
Производные фосфоновых, фосфиновых, фосфорной кислот и их серосодержащих аналогов (тиофосфоновых и тиофосфиновых кислот) применяются в качестве инсектицидов (средств борьбы с вредителями сельского хозяйства):

а также как противоопухолевые препараты.
К типу фосфорорганических производных со смешанными функциями галогенангидридов, эфиров или амидов относятся сильнейшие боевые отравляющие вещества  нервно-паралитического действия (табун, зарин, зоман,
нервно-паралитического действия (табун, зарин, зоман,  -газы):
-газы):

Гидролиз этих  в кислой, а лучше — в щелочной среде приводит к образованию малотоксичных или нетоксичных продуктов.
в кислой, а лучше — в щелочной среде приводит к образованию малотоксичных или нетоксичных продуктов.
Соединения, содержащие пятиковалентный фосфор, — алкилиденфосфораны могут выступать в качестве нуклеофильных реагентов в реакциях с альдегидами и кетонами (реакция Виттига):

Реакция Виттига — один из путей введения в молекулу двойной связи.
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие
- 1. Введение
- 1.1. Предмет органической химии
- 1.2. Основные этапы развития органической химии
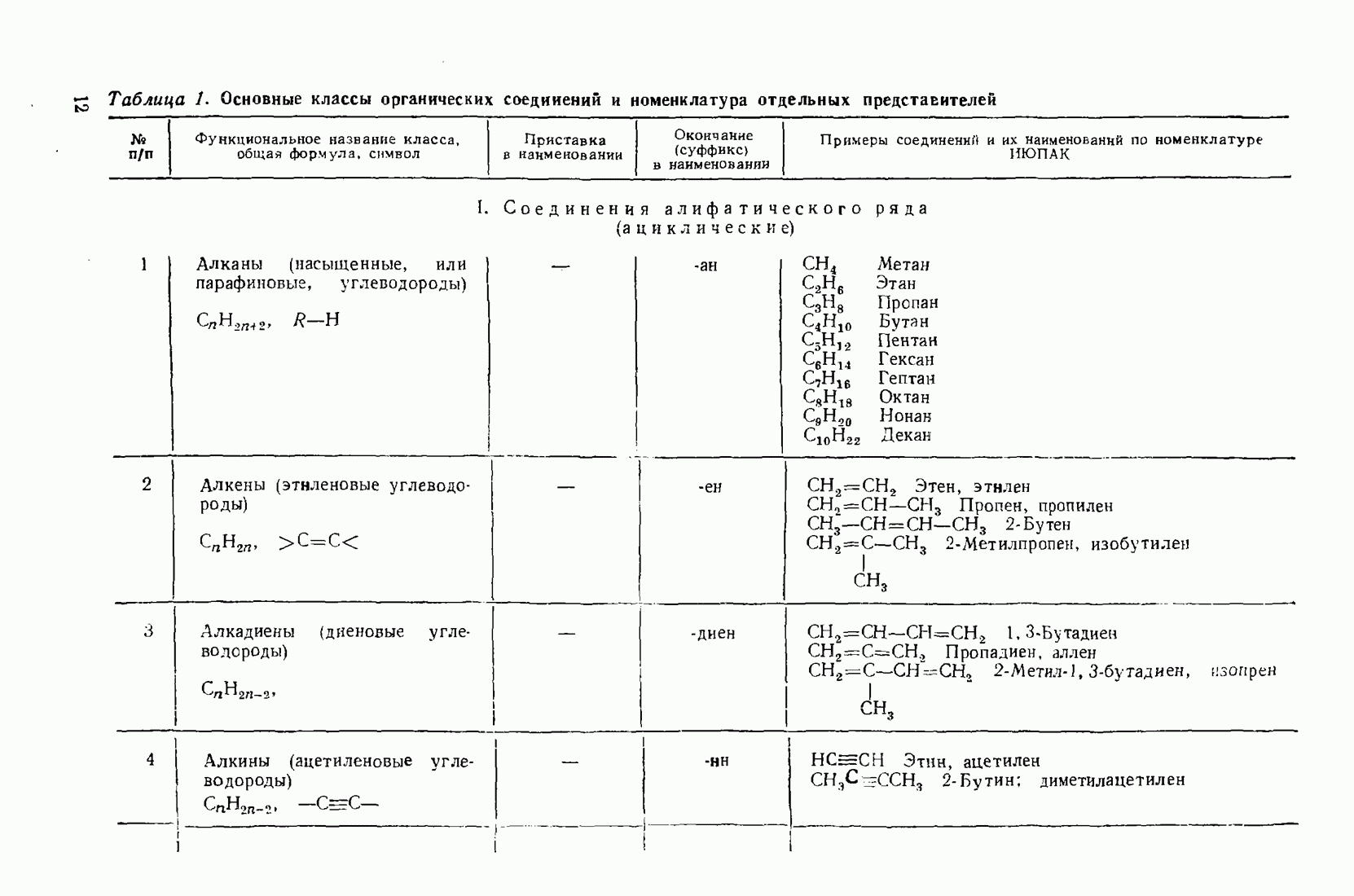
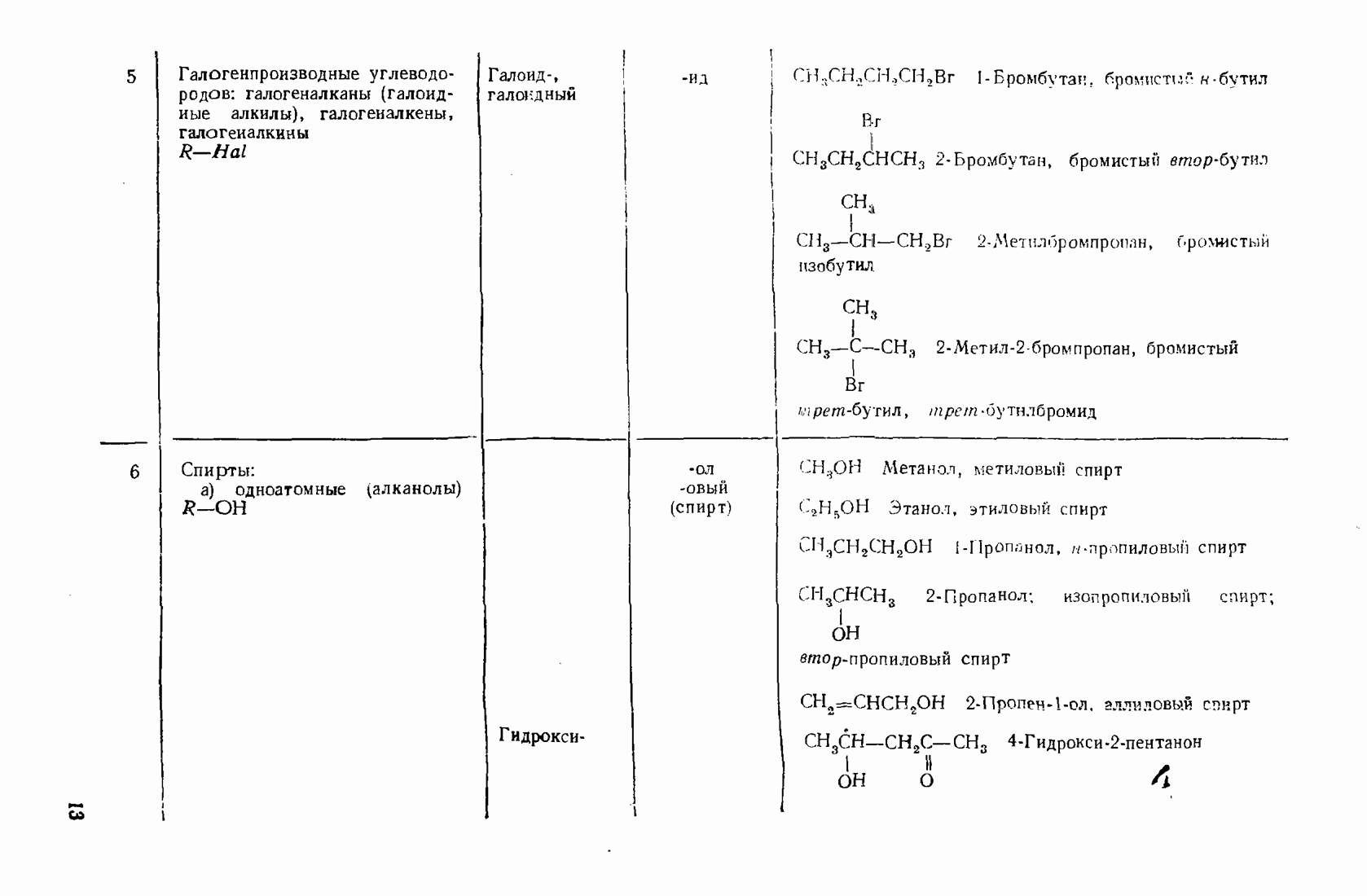
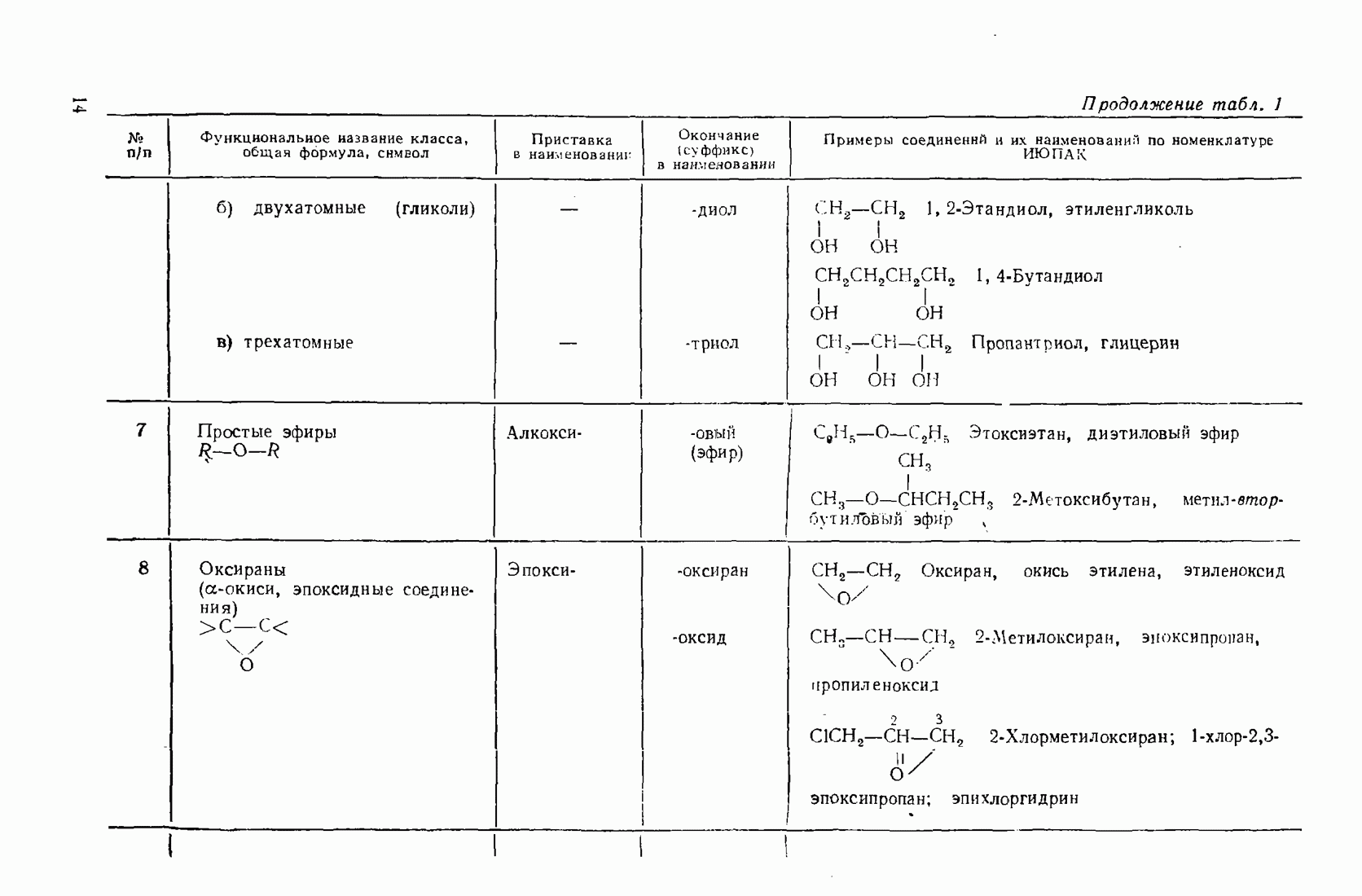
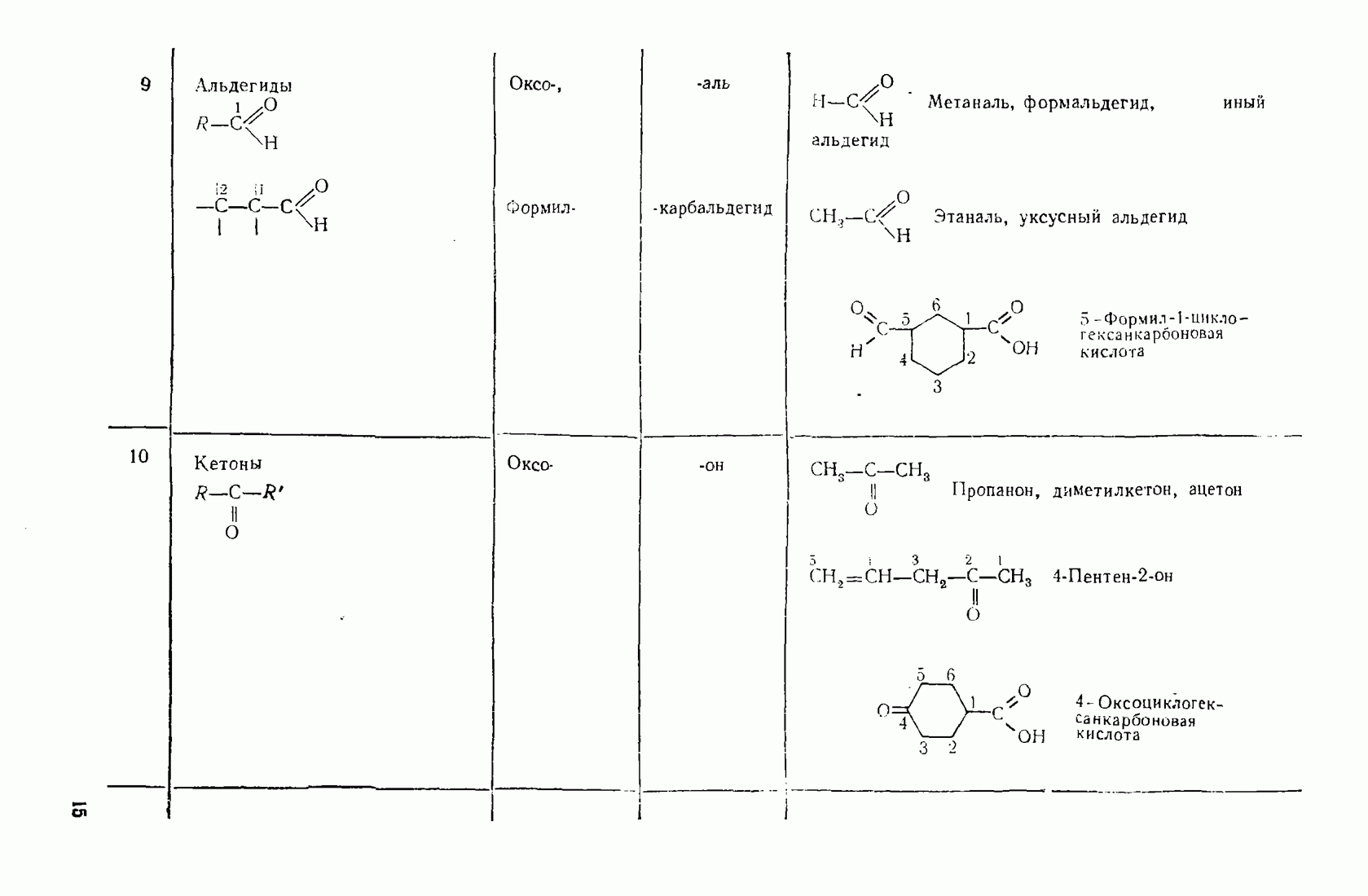
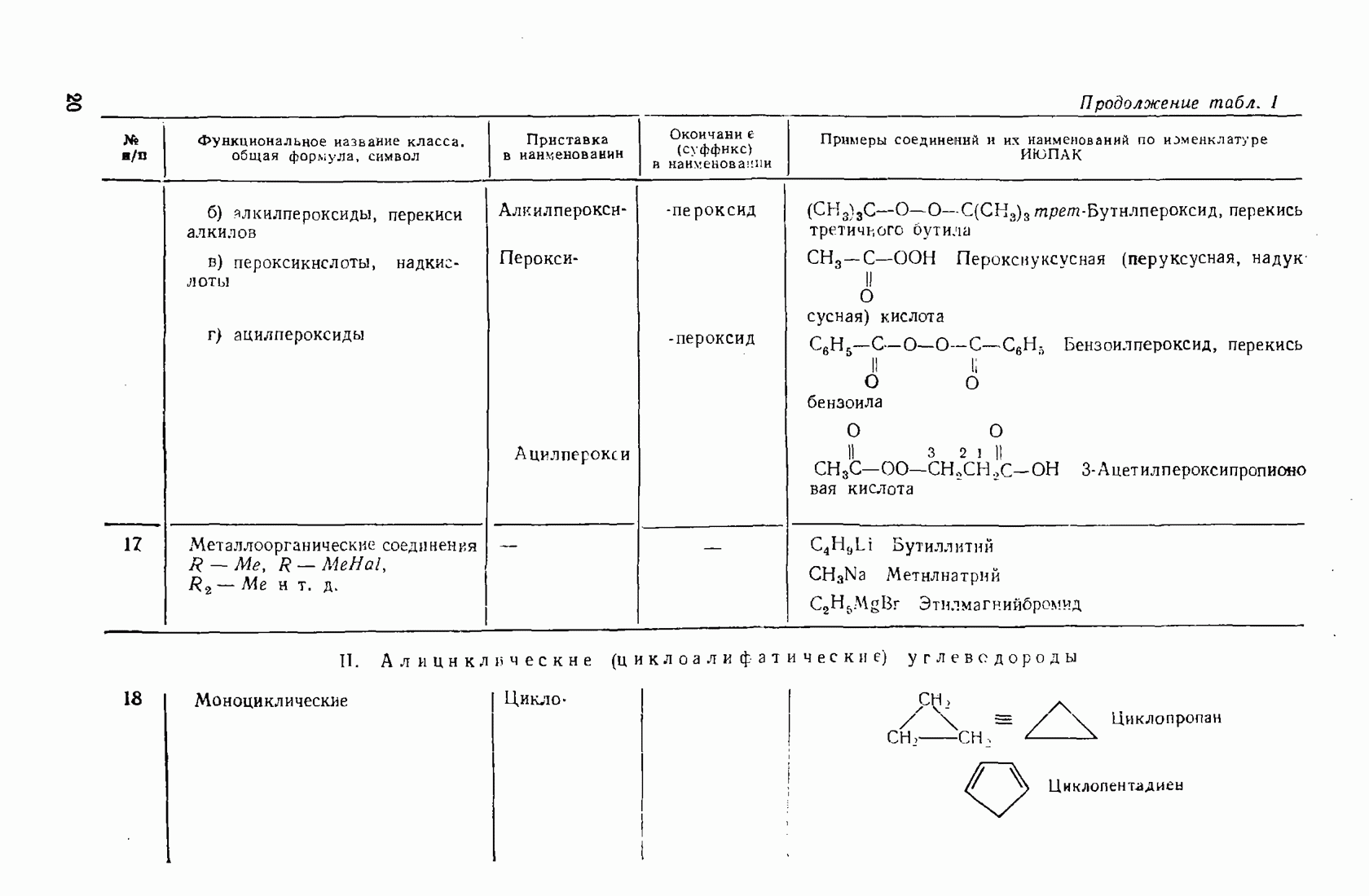
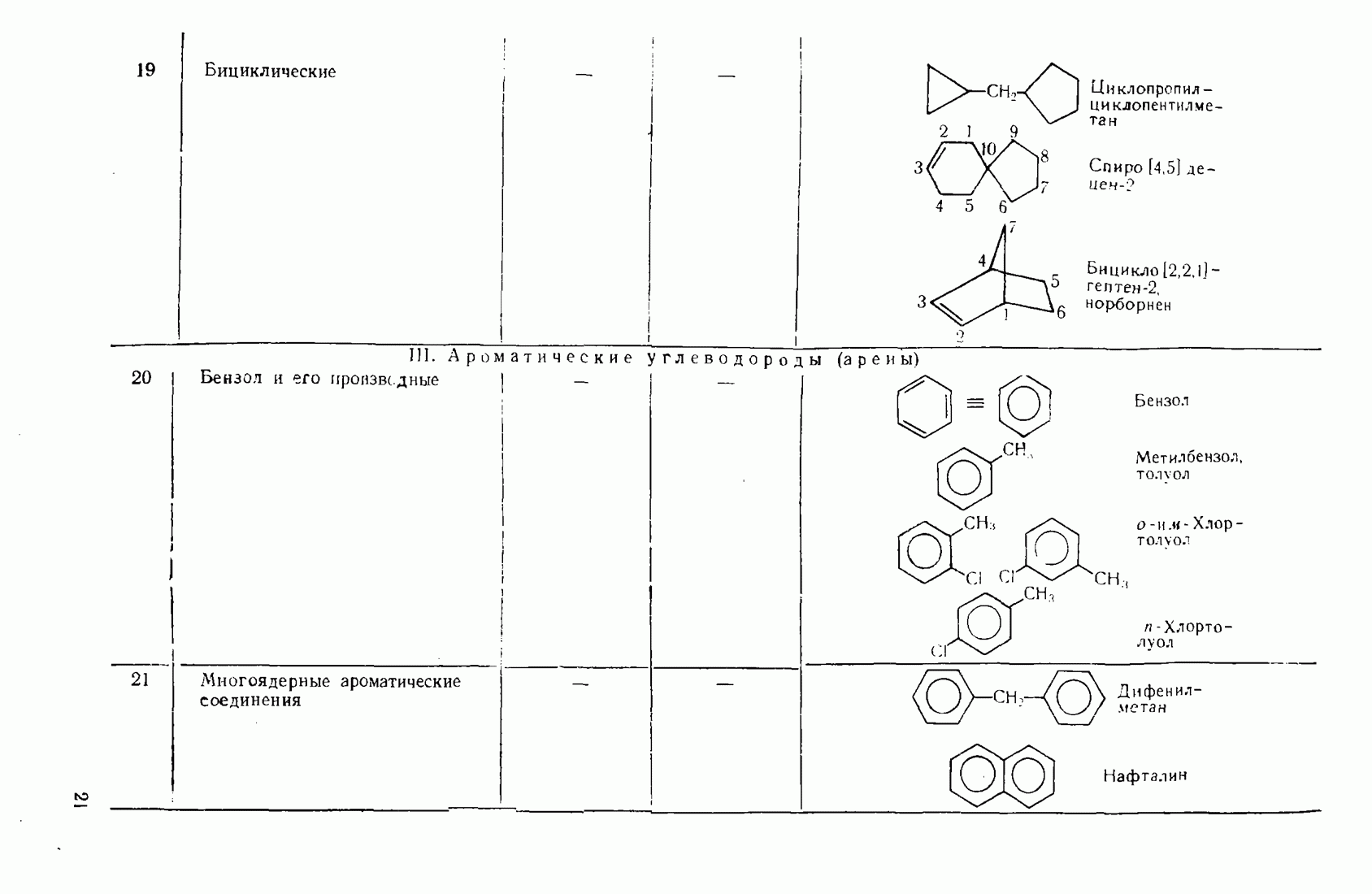
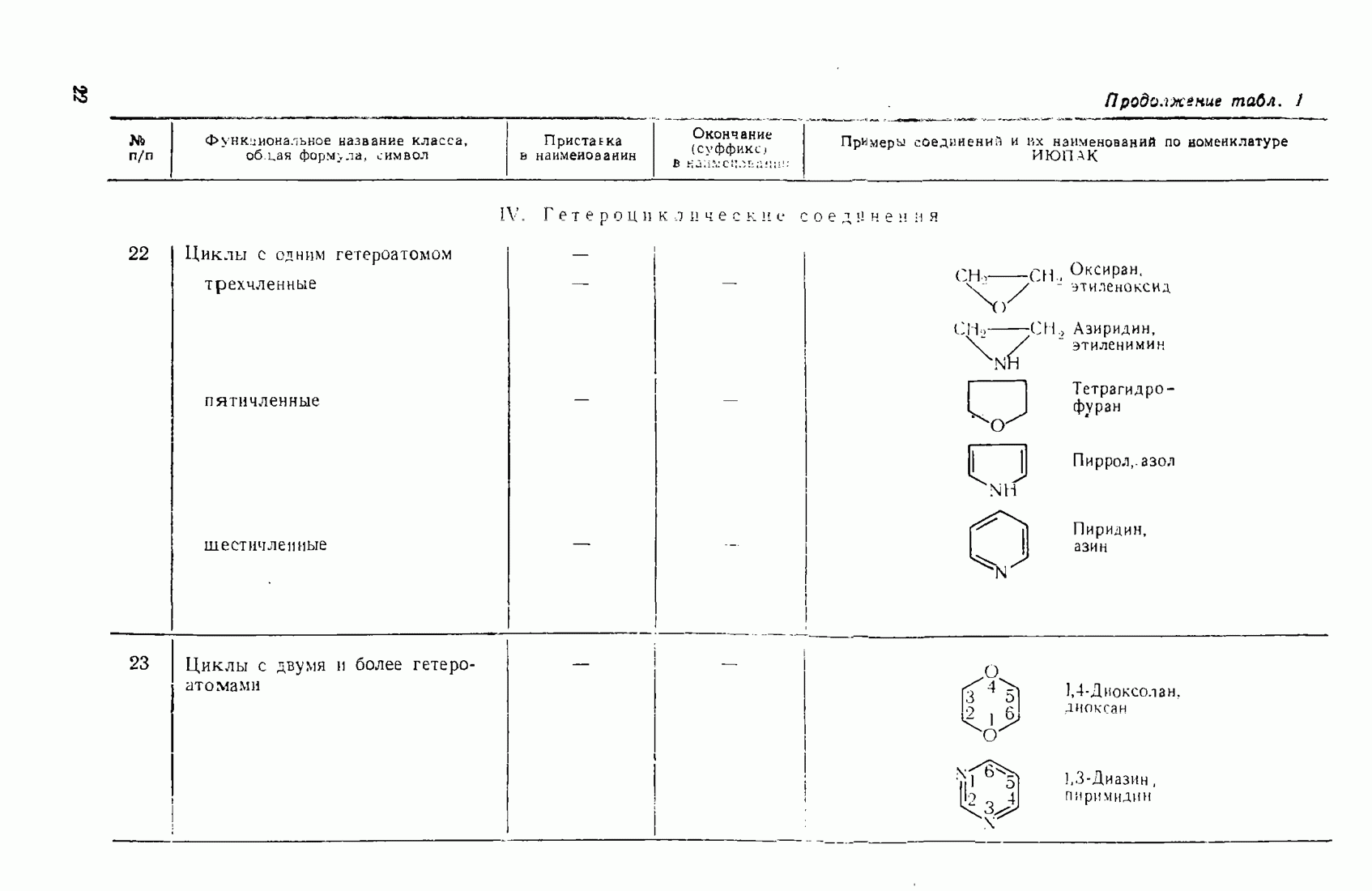
- 1.3. Классификация и номенклатура органических соединений
- 2 Общие теоретические положения органической химии
- 2.1. Природа химической связи
- 2.1.1. Типы химических связей
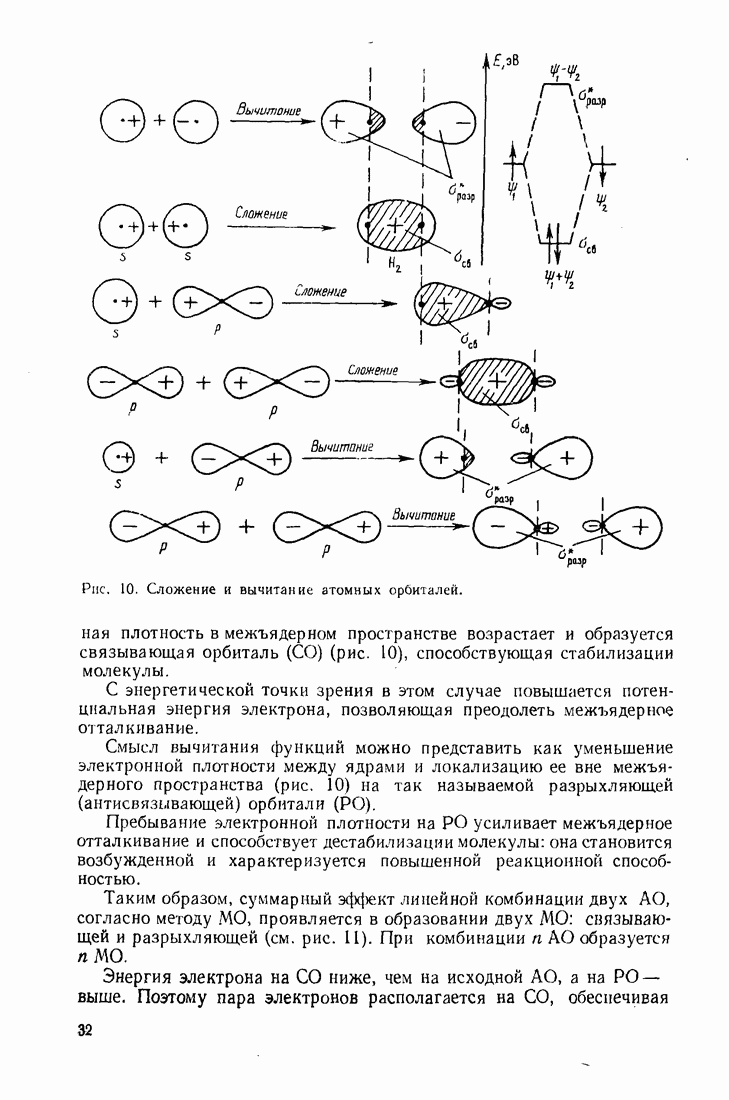
- 2.1.2. Молекулярные орбитали
- 2.2. ТИПЫ ЭЛЕКТРОННЫХ СМЕЩЕНИЙ В МОЛЕКУЛАХ
- 2.3. ОБЩИЕ ПРЕДСТАВЛЕНИЯ ОБ ОРГАНИЧЕСКОЙ РЕАКЦИИ
- 2.4. КЛАССИФИКАЦИЯ РЕАГЕНТОВ И РЕАКЦИЙ
- 2.5. КРАТКАЯ ХАРАКТЕРИСТИКА РЕАКЦИОННОЙ СПОСОБНОСТИ НЕКОТОРЫХ СОЕДИНЕНИЙ АЛИФАТИЧЕСКОГО РЯДА
- 2.5.1. Алканы (парафины)
- 2.5.2. Непредельные углеводороды
- 2.5.3. Галогеналканы (галоидные алкилы R-Hal)
- 2.5.4. Спирты (R0Н)
- 2.5.5. Альдегиды и кетоны
- 2.5.6. Карбоновые кислоты (R-СООН) и их производные (R-СО-X)
- 2.5.7. Амины (NH2R, NHR2, NR3)
- 3. Реакционная способность соединений алифатического ряда
- 3.1. Алканы (насыщенные углеводороды)
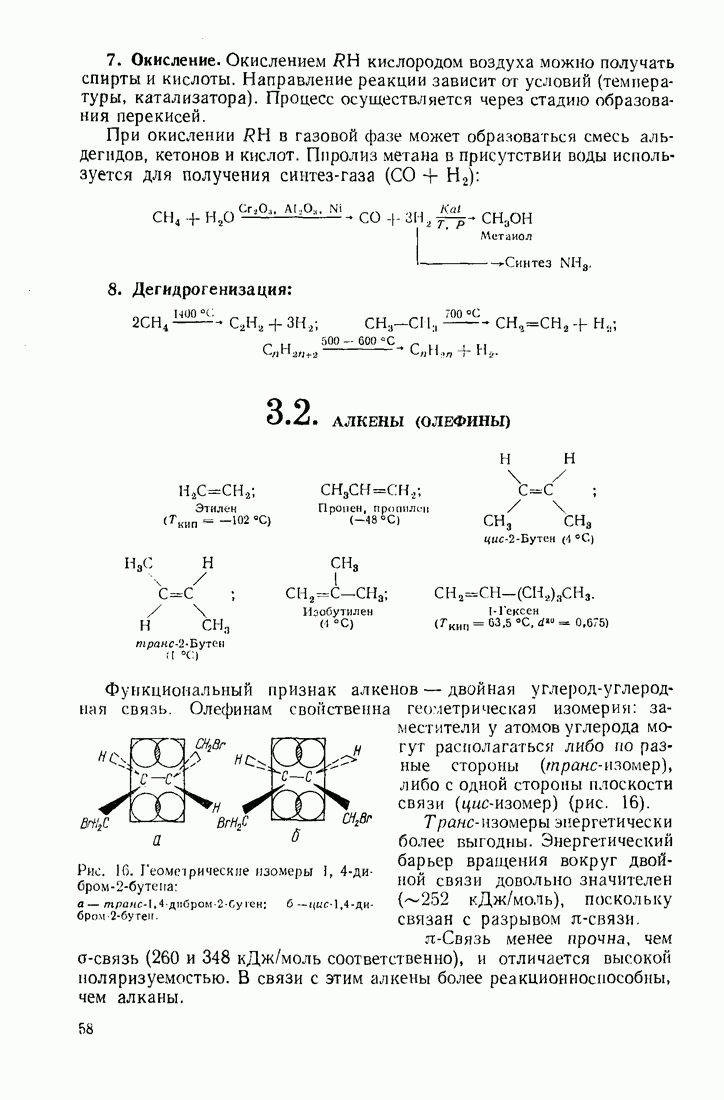
- 3.2. АЛКЕНЫ (ОЛЕФИНЫ)
- 3.3. ДИЕНОВЫЕ УГЛЕВОДОРОДЫ
- 3.4. АЦЕТИЛЕНЫ
- 3.5. ГАЛОГЕНАЛКАНЫ (ГАЛОИДНЫЕ АЛКИЛЫ)
- 3.6. СПИРТЫ
- 3.7. ПРОСТЫЕ ЭФИРЫ (R-O-R)
- 3.8. ОКСИРАНЫ (ЭПОКСИДНЫЕ СОЕДИНЕНИЯ, a-ОКИСИ)
- 3.9. АЛЬДЕГИДЫ И КЕТОНЫ
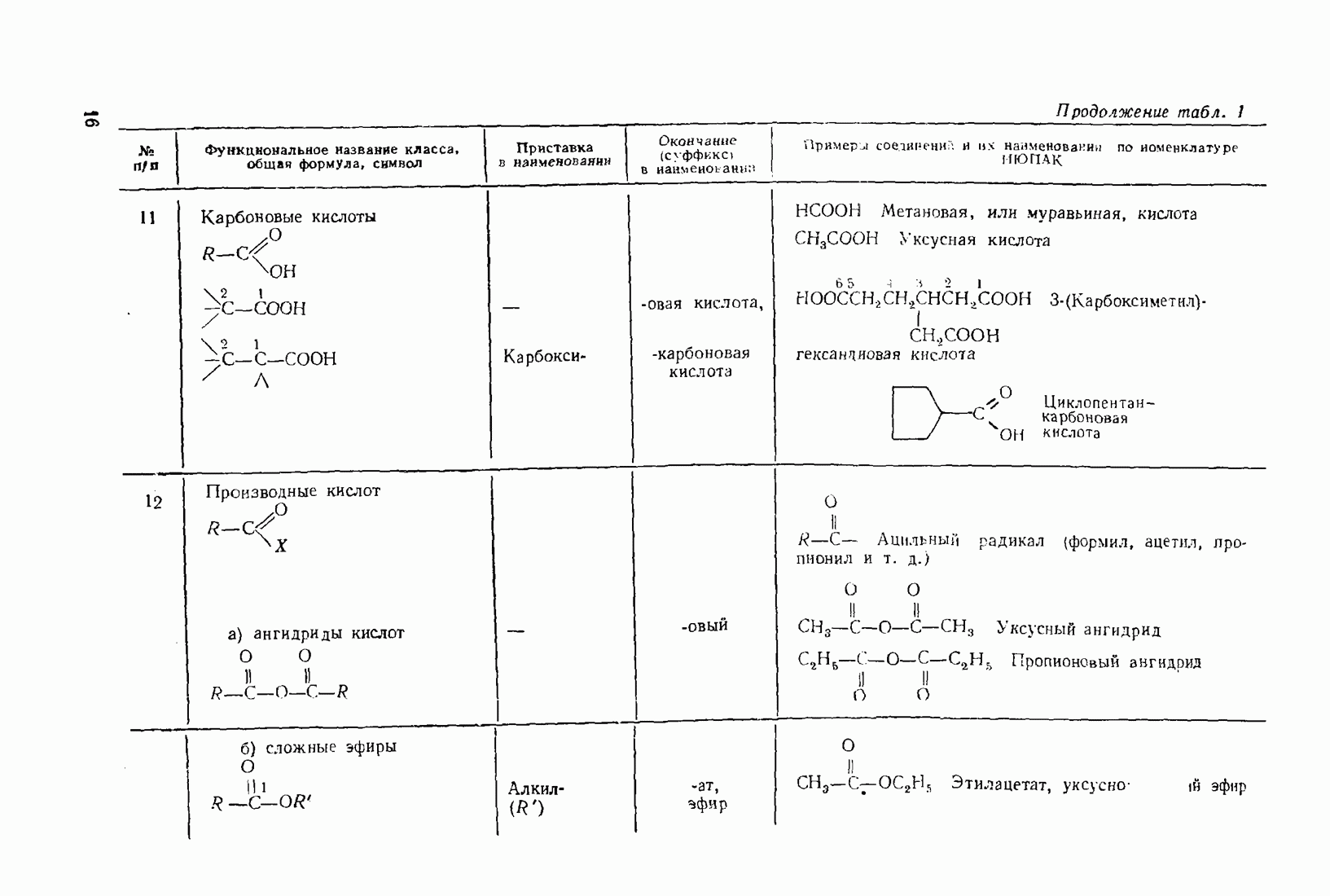
- 3.10. КАРБОНОВЫЕ КИСЛОТЫ
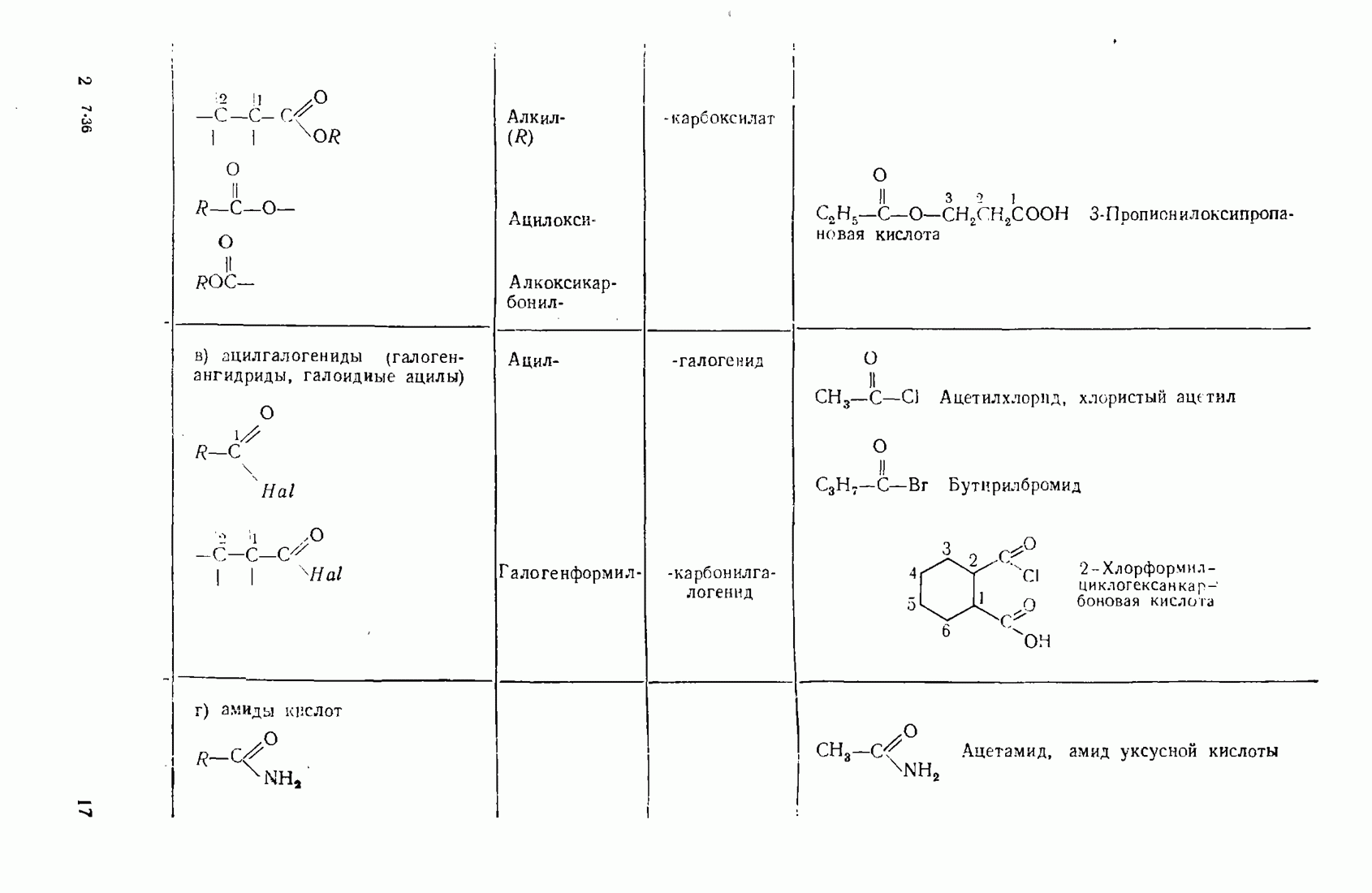
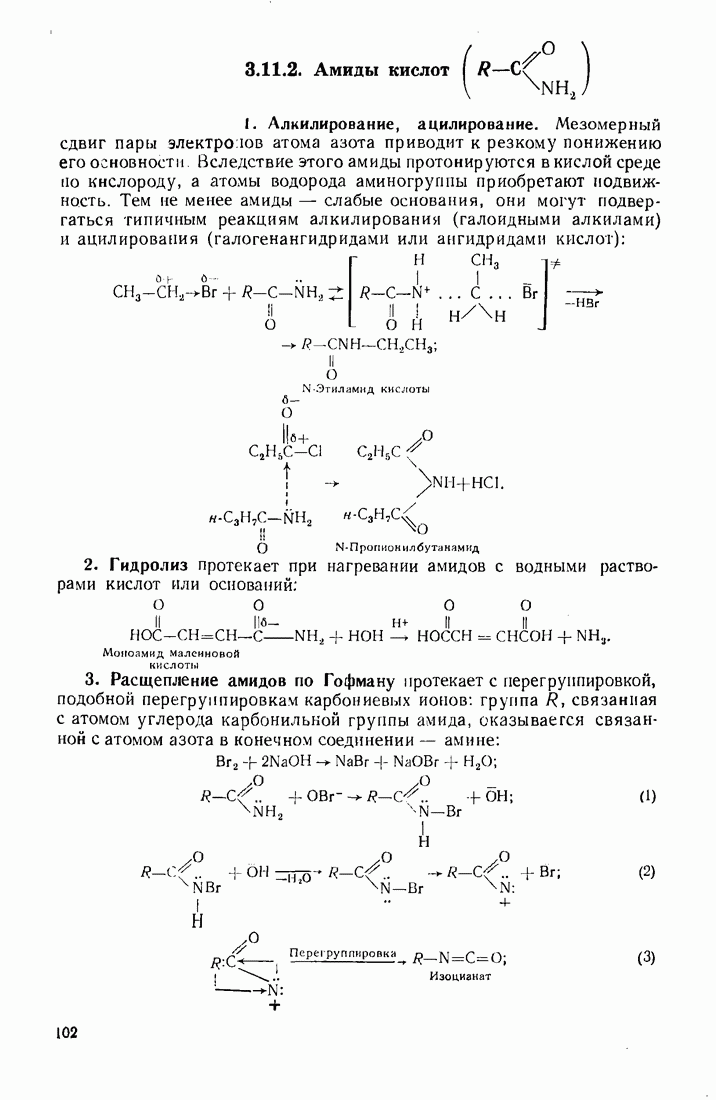
- 3.11. НЕКОТОРЫЕ ПРОИЗВОДНЫЕ КИСЛОТ
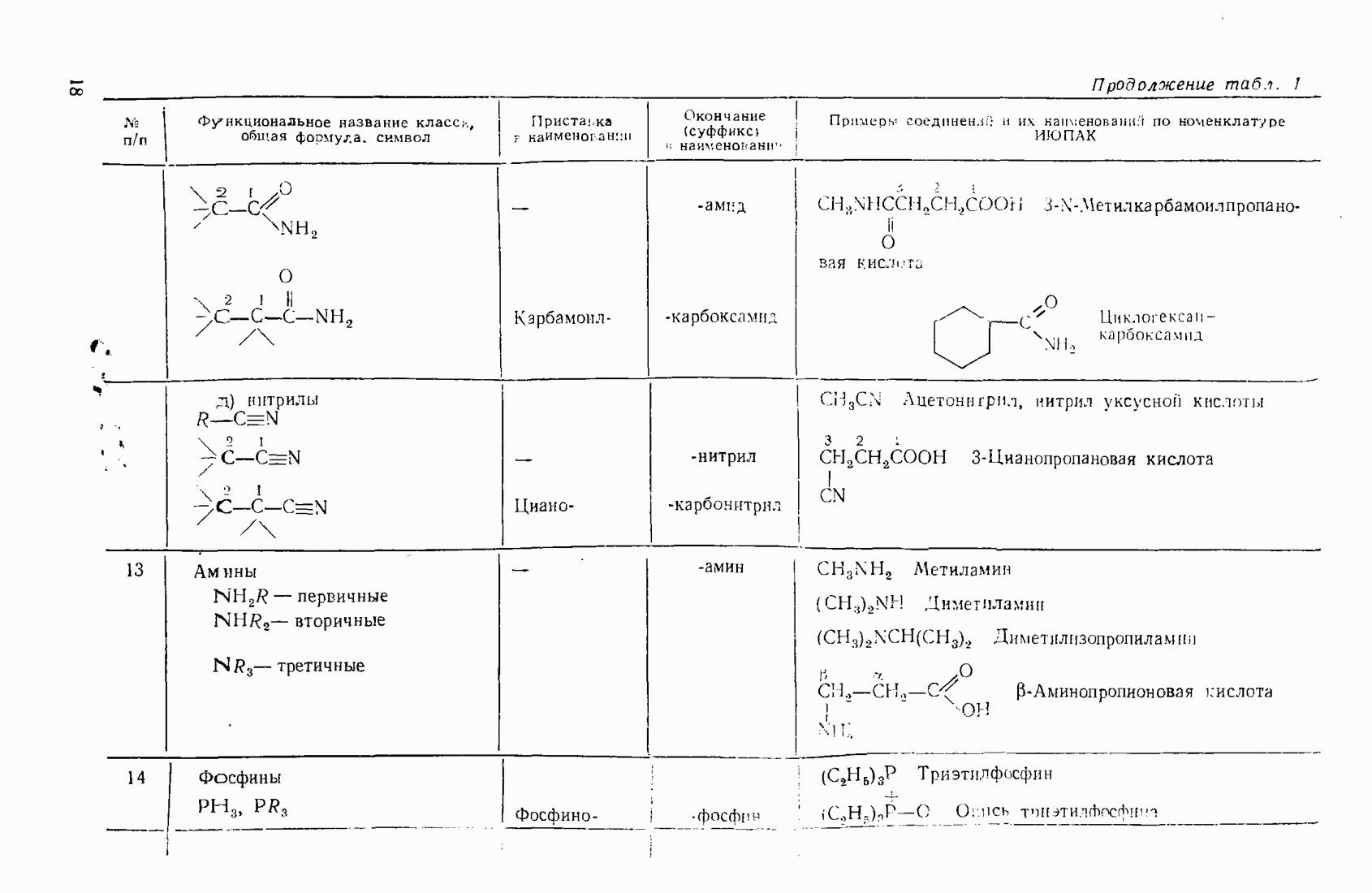
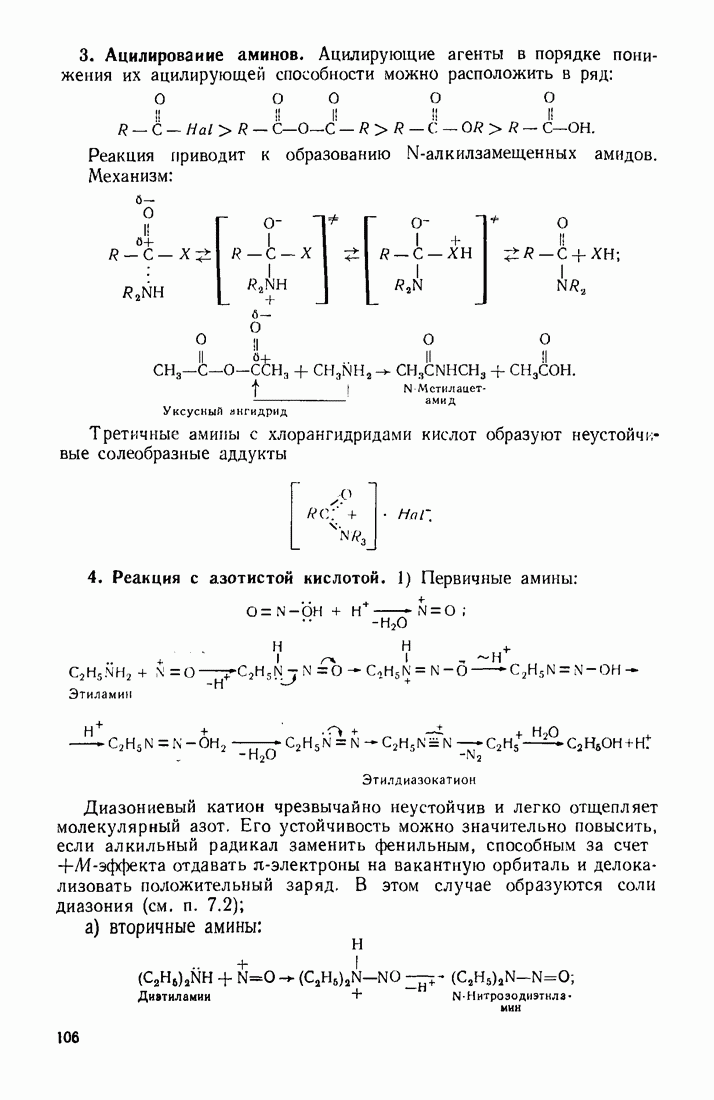
- 3.12. АМИНЫ
- 3.13. ФОСФОРОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
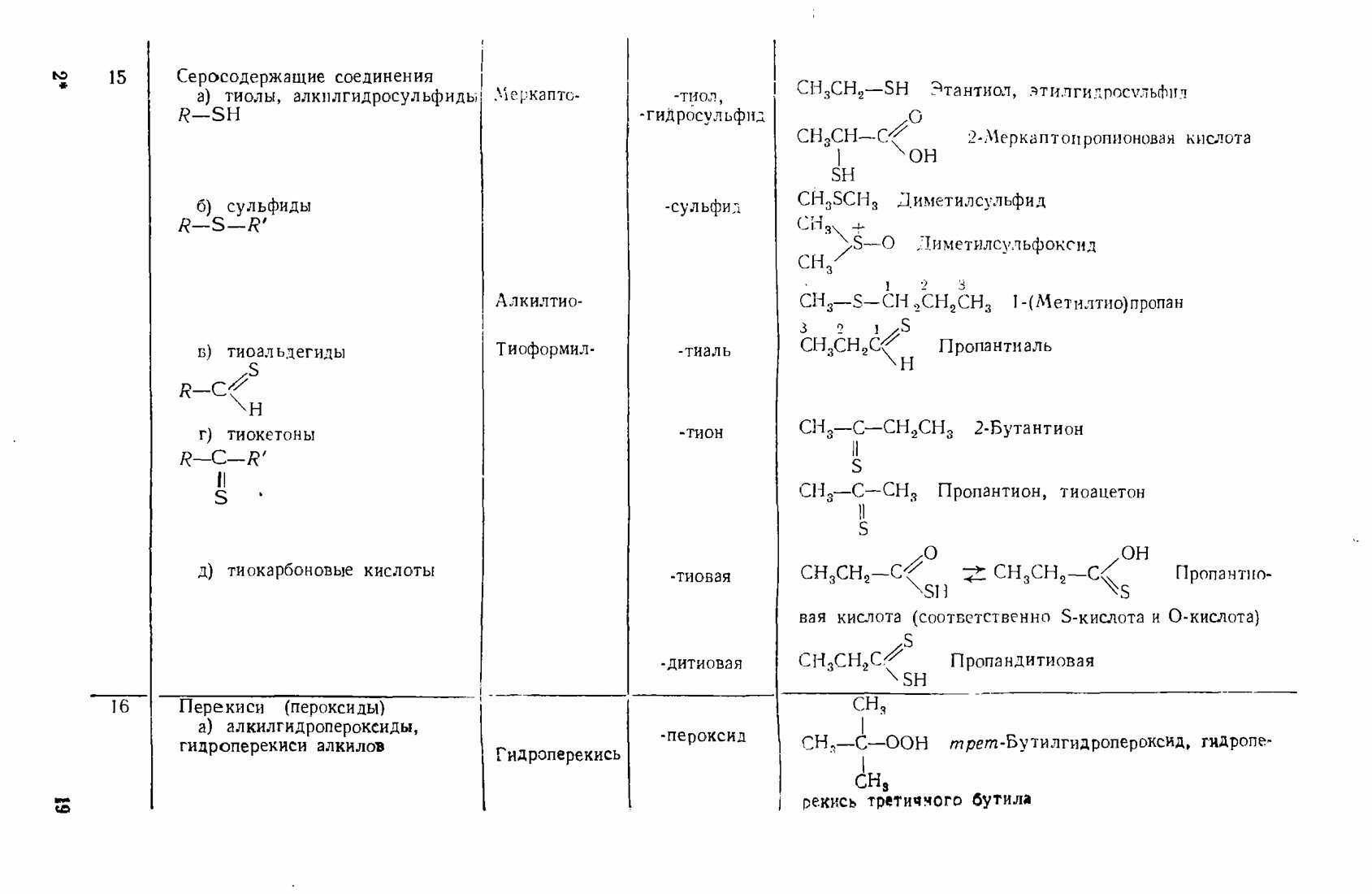
- 3.14. СЕРООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
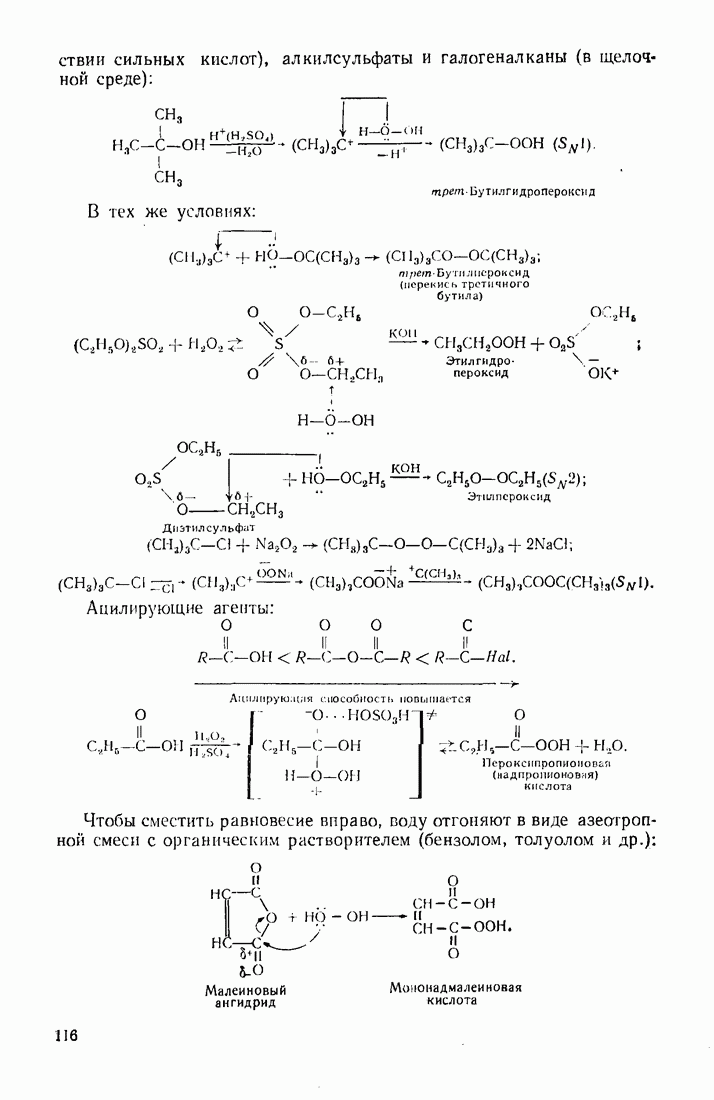
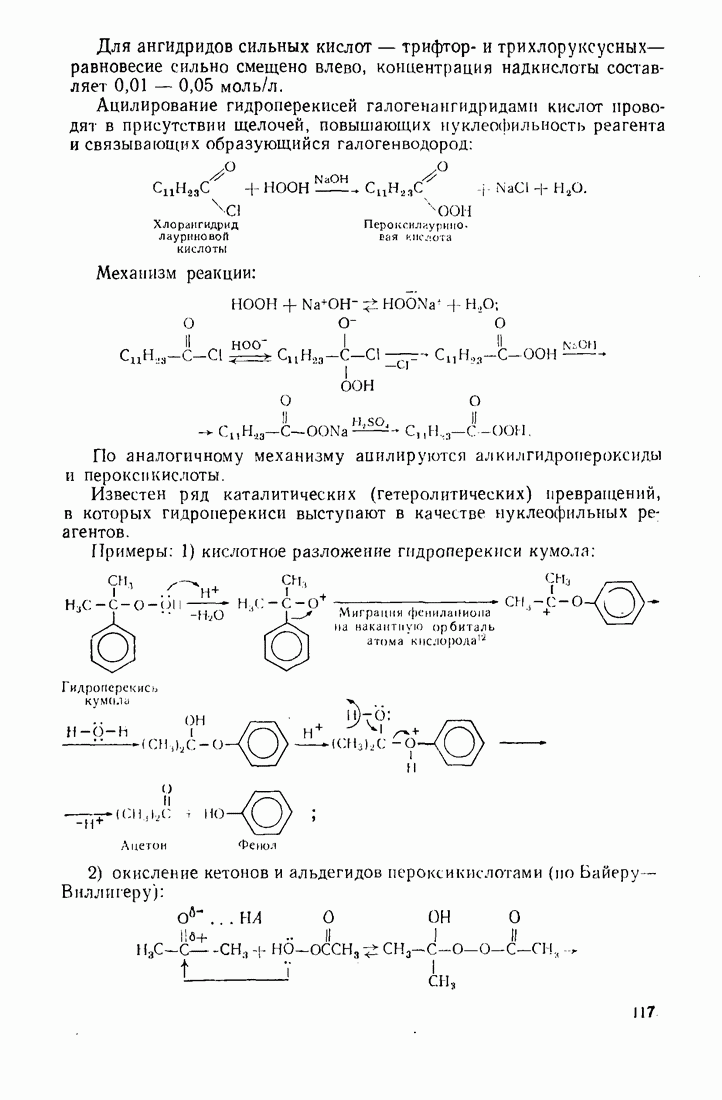
- 3.15. ОРГАНИЧЕСКИЕ ПЕРЕКИСИ (ПЕРОКСИДНЫЕ СОЕДИНЕНИЯ)
- 3.16. ПРОИЗВОДНЫЕ УГОЛЬНОЙ КИСЛОТЫ
- 3.17. ГЕТЕРОАНАЛОГИ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ
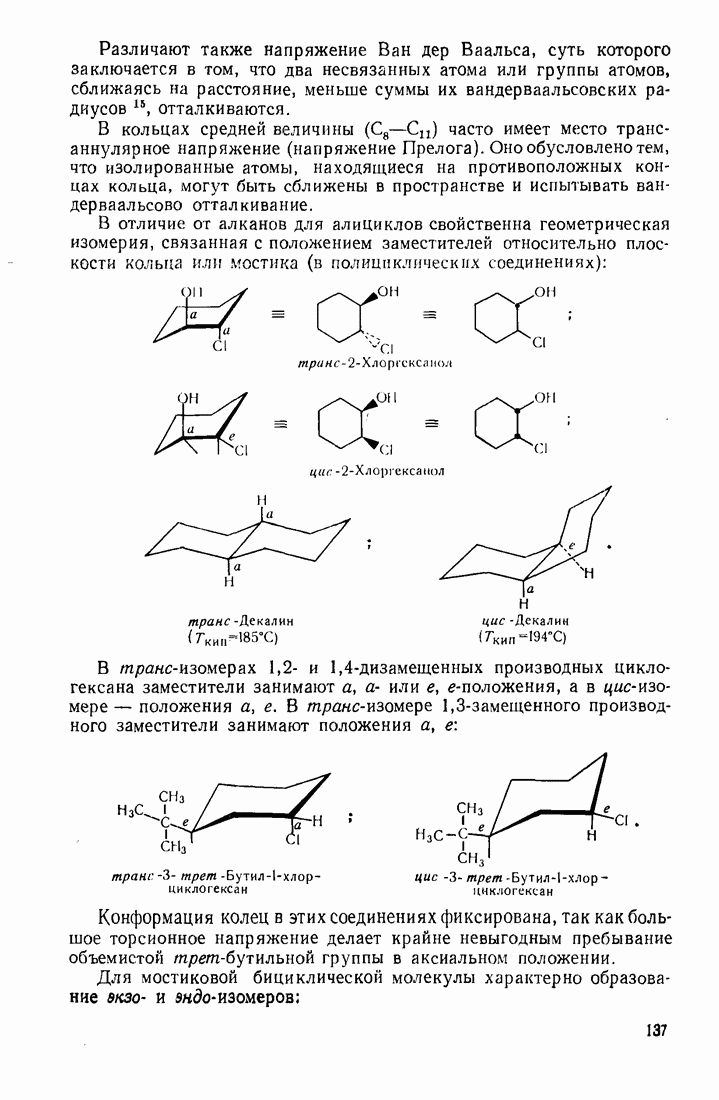
- 3.18. АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- 3.18.2. Пространственное расположение и напряженность циклов
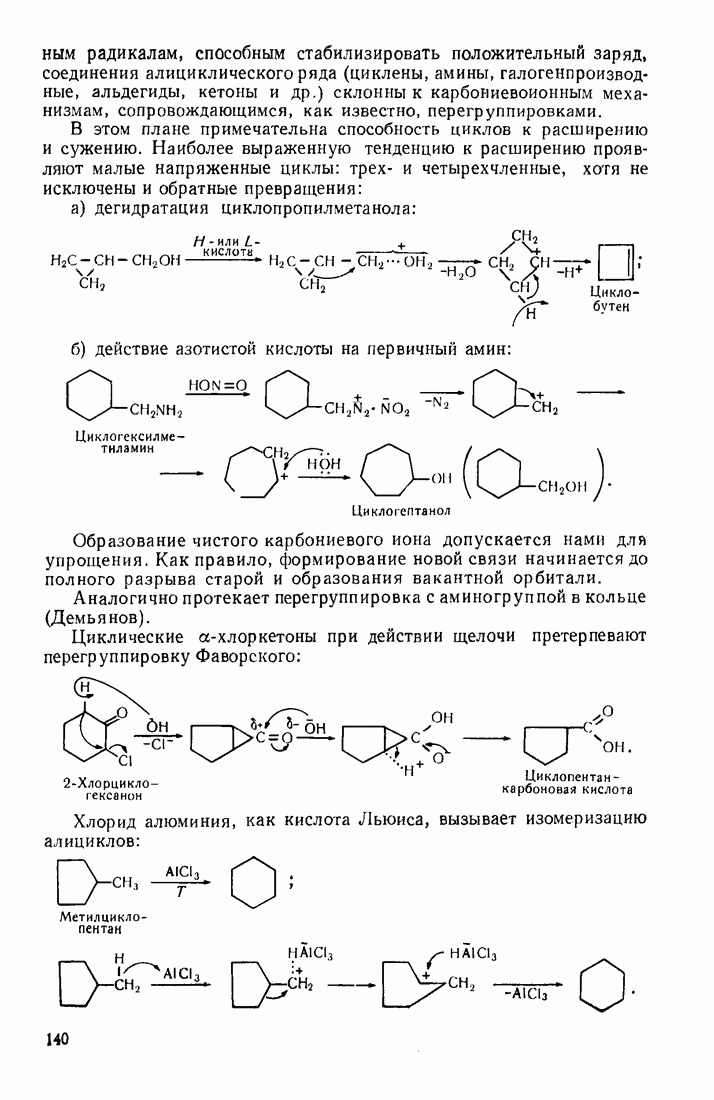
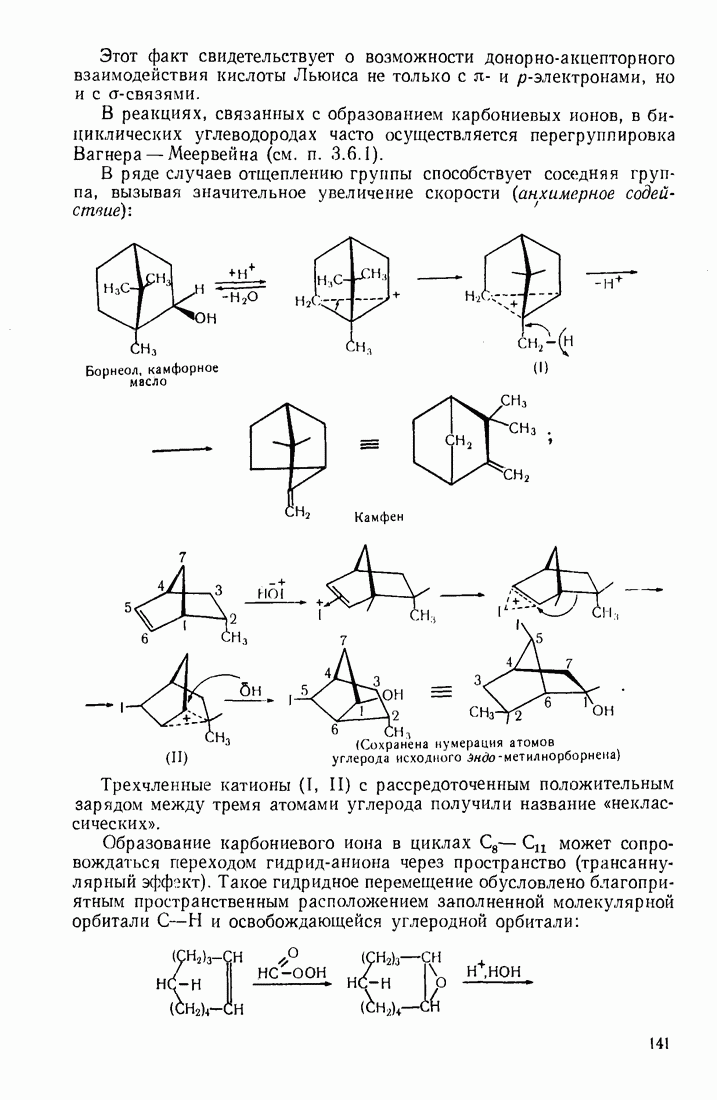
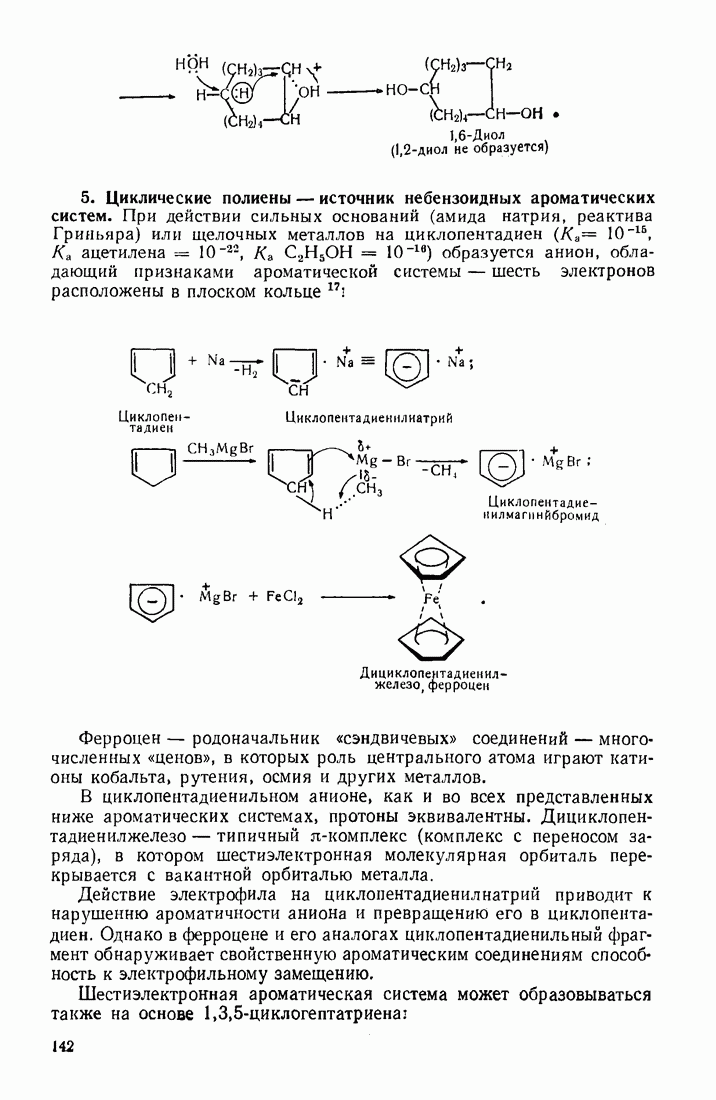
- 3.18.3. Особенности химических свойств алициклических соединений
- 4. Полифункциональные производные алифатического ряда
- 4.1. ДВУХОСНОВНЫЕ КАРБОНОВЫЕ КИСЛОТЫ
- 4.2. НЕПРЕДЕЛЬНЫЕ КИСЛОТЫ
- 4.3. ОКСОКИСЛОТЫ (АЛЬДЕГИДО- И КЕТОКИСЛОТЫ)
- 4.4. ОКСИКИСЛОТЫ. ПОНЯТИЕ ОБ ОПТИЧЕСКОЙ ИЗОМЕРИИ
- 4.5. УГЛЕВОДЫ
- 4.5.2. Стереохимия моносахаридов
- 4.5.3. Дисахариды
- 4.5.4. Полисахариды
- 4.5.5. Нахождение в природе и пути превращения углеводов
- 4.6. АМИНОКИСЛОТЫ
- 5. Методы синтеза органических юединений алифатическою рада
- 5.1. АЛКИЛИРОВАНИЕ
- 5.2. АЦИЛИРОВАНИЕ
- 5.3. ГАЛОГЕНИРОВАНИЕ
- 5.4. ГИДРОКСИЛИРОВАНИЕ
- 5.5. КАРБОНИЛИРОВАНИЕ (ВВЕДЕНИЕ КАРБОНИЛЬНОЙ ГРУППЫ)
- 5.6. КАРБОКСИЛИРОВАНИЕ
- 5.7. ЭПОКСИДИРОВАНИЕ (ОКСИРАНИРОВАИИЕ)
- 5.8. АМИНИРОВАНИЕ
- 5.9. ОКИСЛЕНИЕ
- 5.10. ВОССТАНОВЛЕНИЕ
- 5.11. АЛКАНЫ
- 5.12 АЛКЕНЫ
- 5.13. ДИЕНОВЫЕ УГЛЕВОДОРОДЫ (1,3-ДИЕНЫ)
- 5.14. АЦЕТИЛЕНЫ
- 5.15 АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- 5.16. ГАЛОГЕН АЛКАНЫ
- 5.17. СПИРТЫ
- 5.18. АЛЬДЕГИДЫ И КЕТОНЫ
- 5.19. КАРБОНОВЫЕ КИСЛОТЫ
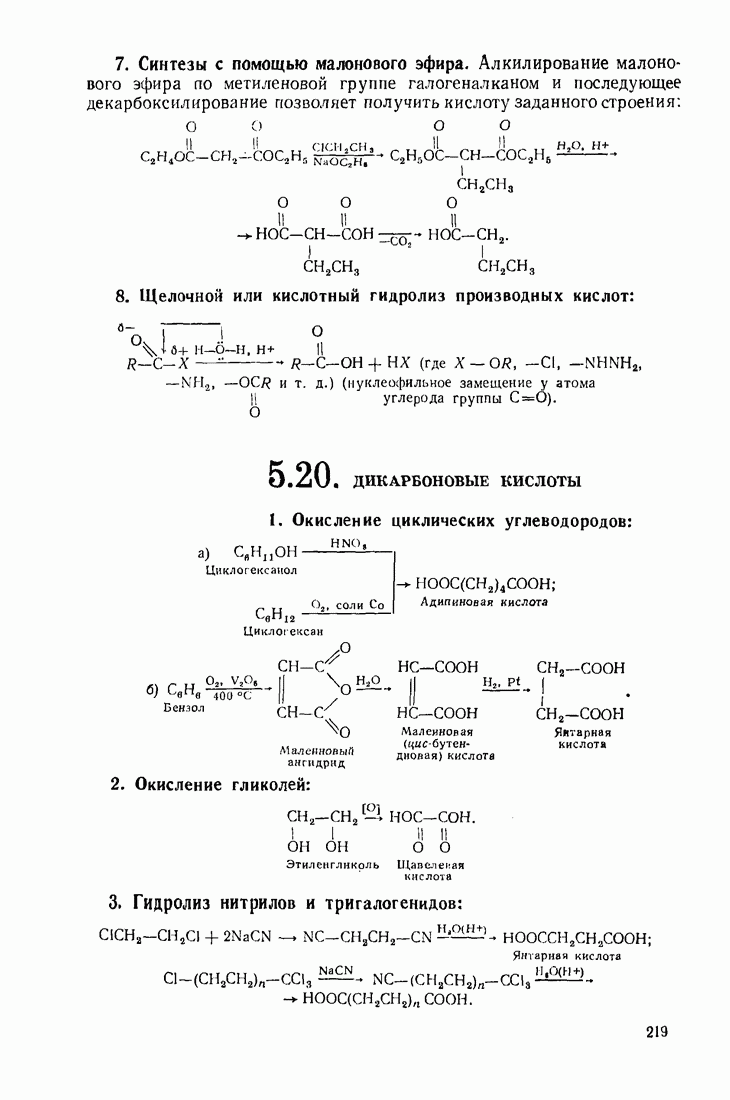
- 5.20. ДИКАРБОНОВЫЕ КИСЛОТЫ
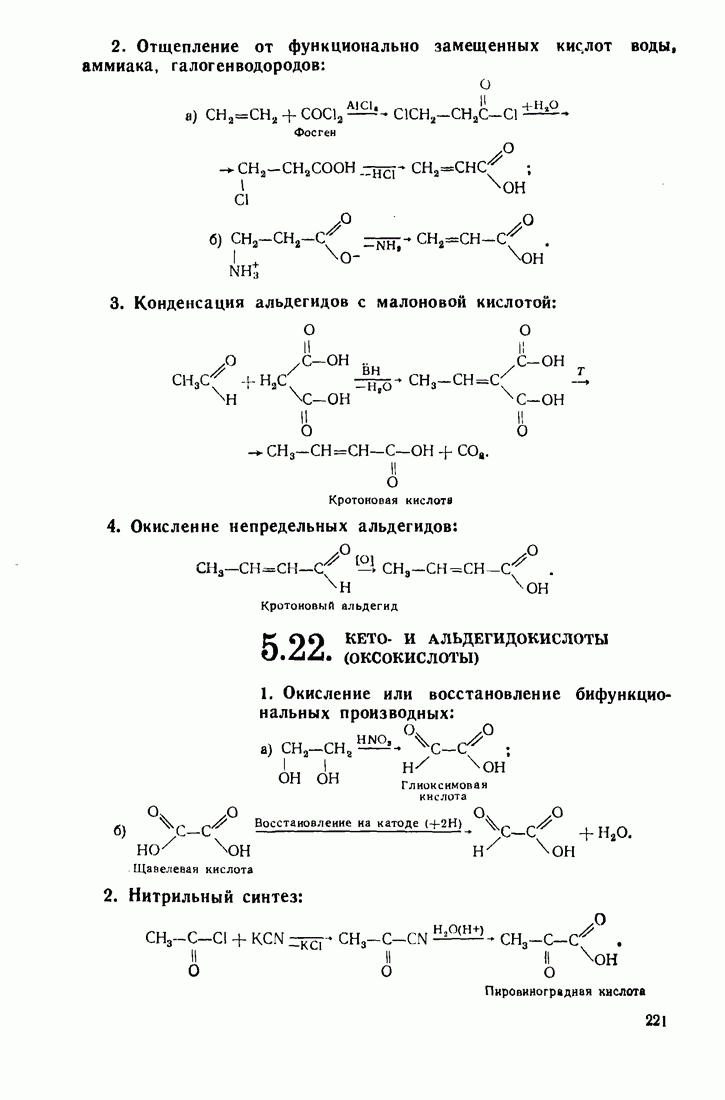
- 5.21. НЕПРЕДЕЛЬНЫЕ КИСЛОТЫ
- 5.22. КЕТО- И АЛЬДЕГИДОКИСЛОТЫ (ОКСОКИСЛОТЫ)
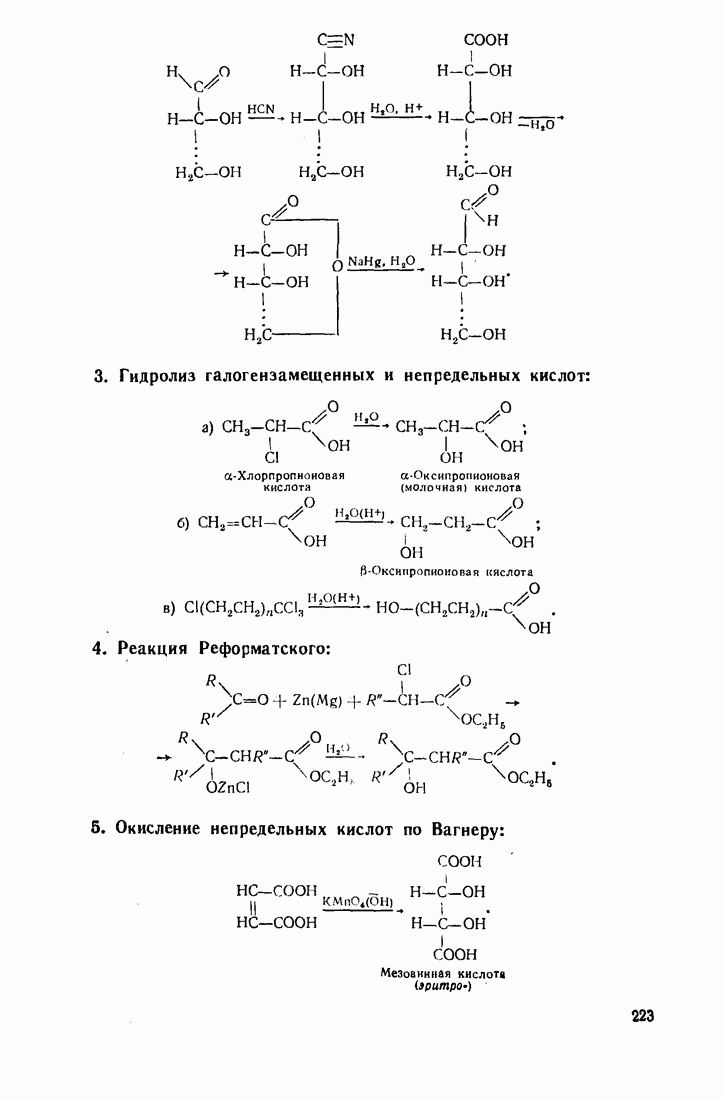
- 5.23. ОКСИКИСЛОТЫ
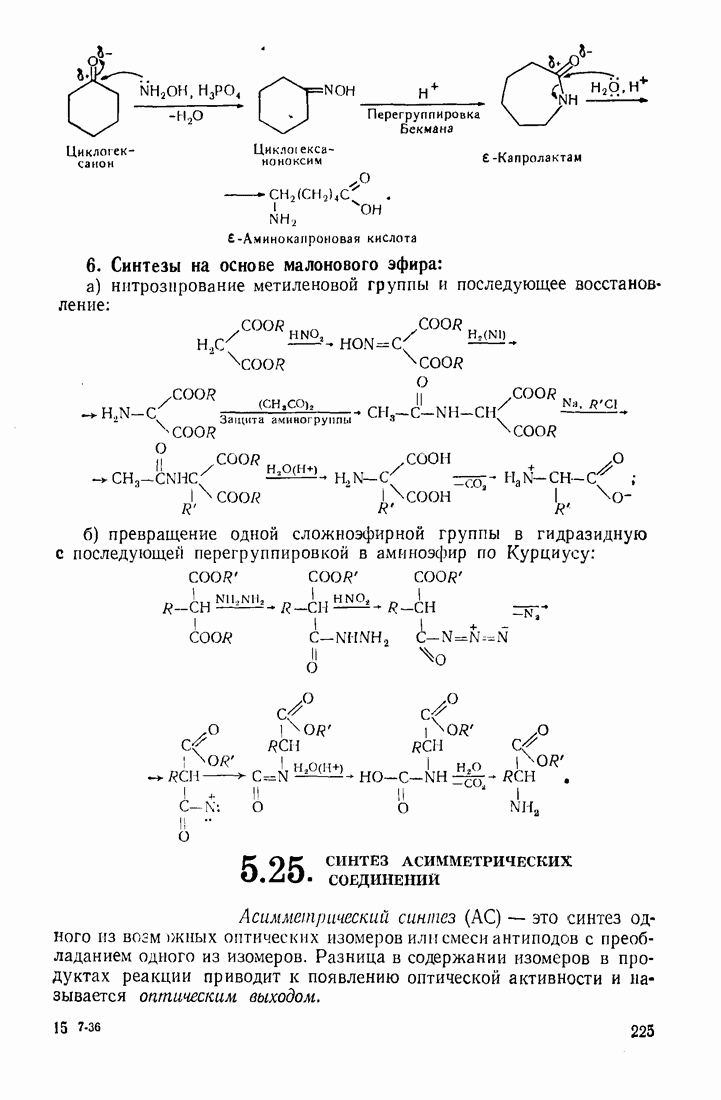
- 5.24. АМИНОКИСЛОТЫ
- 5.25 СИНТЕЗ АСИММЕТРИЧЕСКИХ СОЕДИНЕНИЙ
- 6. Некоторые понятия физической органической химии
- 6.1. СВЯЗЬ СОСТАВА И СТРОЕНИЯ СОЕДИНЕНИЙ С ФИЗИЧЕСКИМИ СВОЙСТВАМИ
- 6.2. ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 6.3. КИСЛОТЫ И ОСНОВАНИЯ В ОРГАНИЧЕСКОЙ ХИМИИ
- 6.4. ОРГАНИЧЕСКИЕ РАСТВОРИТЕЛИ И ИХ ВЛИЯНИЕ НА СКОРОСТЬ И МЕХАНИЗМ РЕАКЦИЙ
- 6.5. КАТАЛИЗ ОРГАНИЧЕСКИХ РЕАКЦИЙ
- 7. Бензол и его производные
- 7.1. СТРОЕНИЕ БЕНЗОЛА. РАСПРЕДЕЛЕНИЕ ЭЛЕКТРОННОЙ ПЛОТНОСТИ
- 7.2. ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ В БЕНЗОЛЬНОМ ЯДРЕ
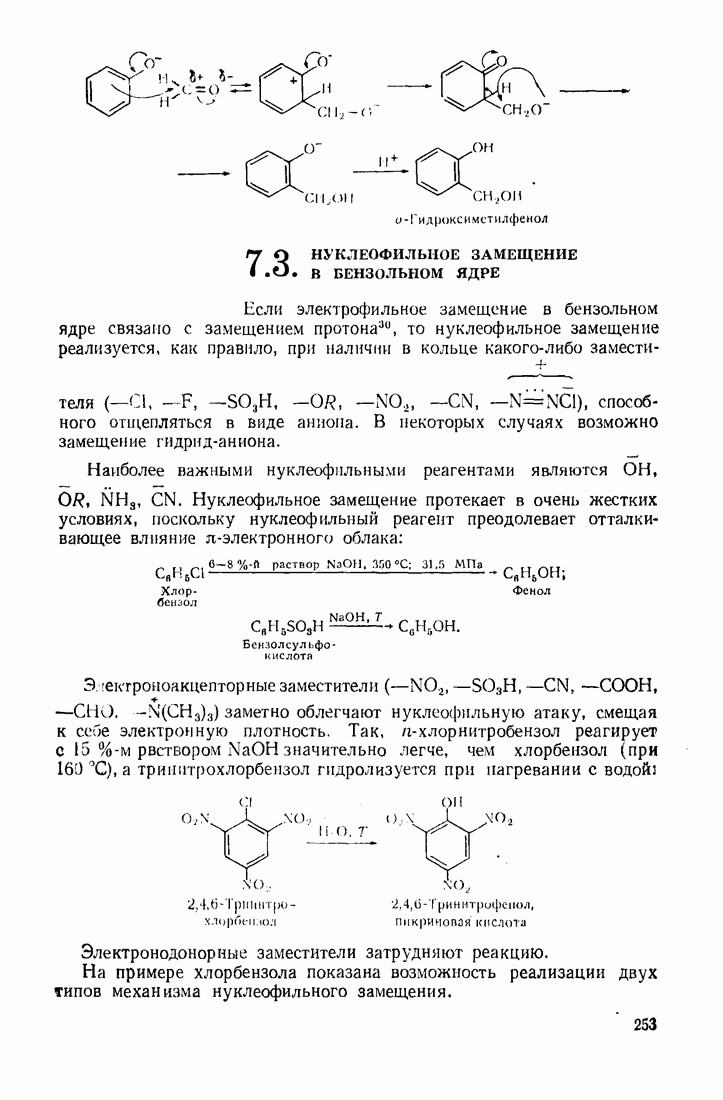
- 7.3. НУКЛЕОФИЛЬНОЕ ЗАМЕЩЕНИЕ В БЕНЗОЛЬНОМ ЯДРЕ
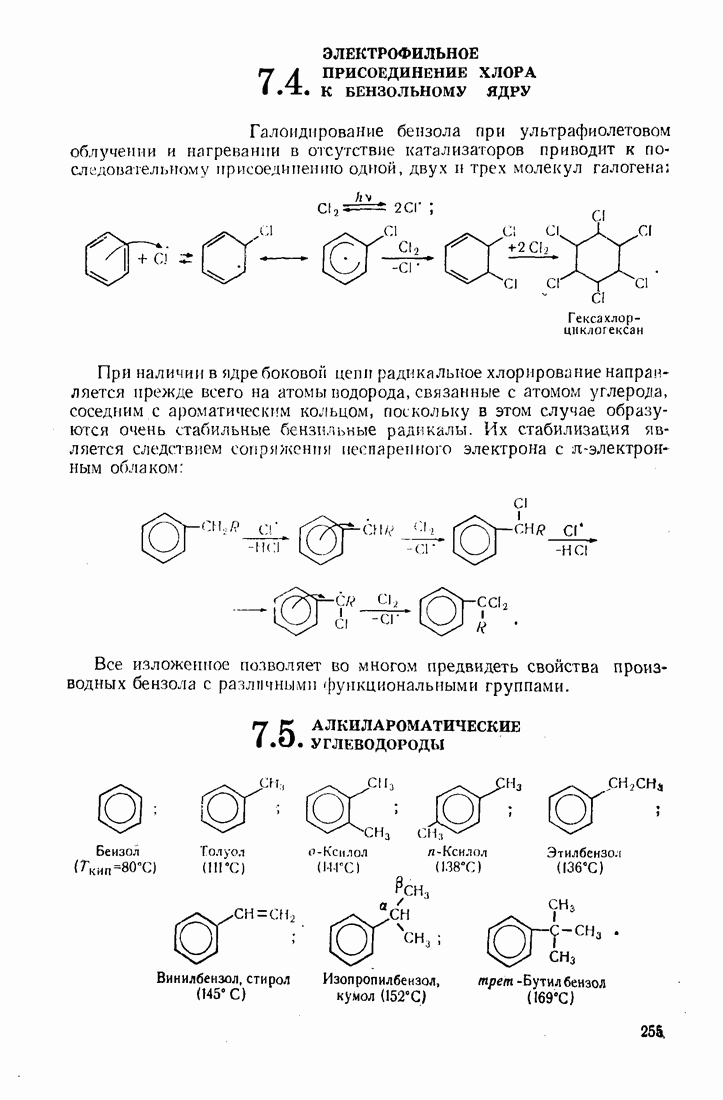
- 7.4. ЭЛЕКТРОФИЛЬНОЕ ПРИСОЕДИНЕНИЕ ХЛОРА К БЕНЗОЛЬНОМУ ЯДРУ
- 7.5. АЛКИЛАРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ
- 7.6. ГАЛОГЕНБЕНЗОЛЫ
- 7.7. ФЕНОЛЫ
- 7.8. НИТРОСОЕД ИНЕНИЯ
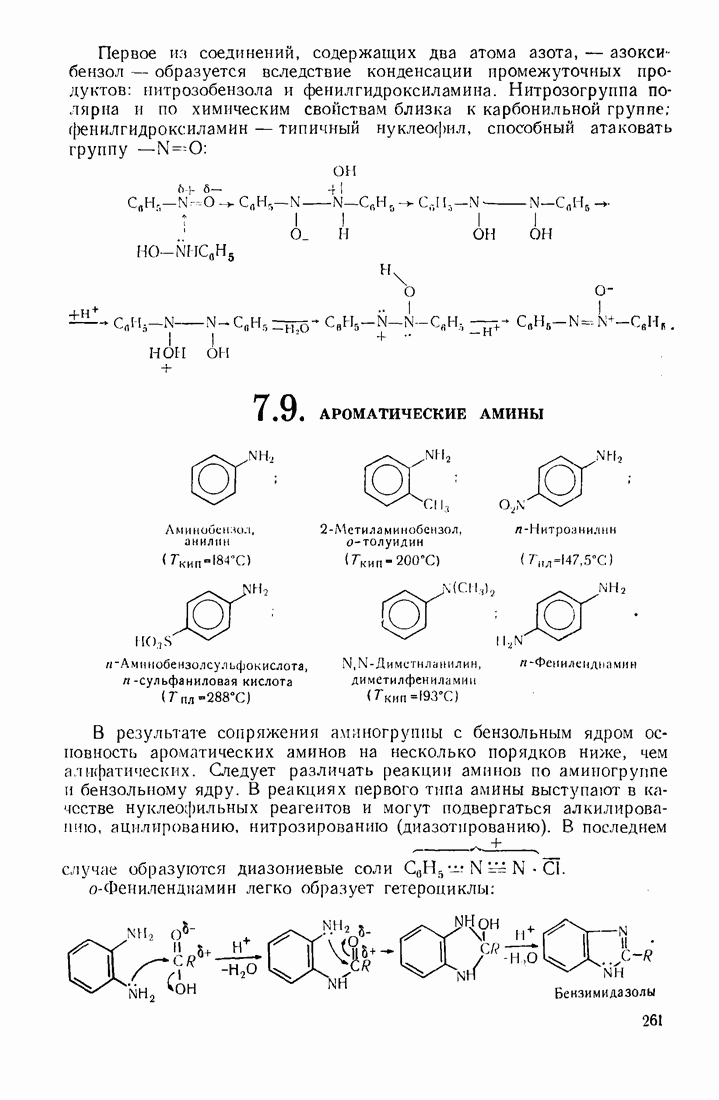
- 7.9. АРОМАТИЧЕСКИЕ АМИНЫ
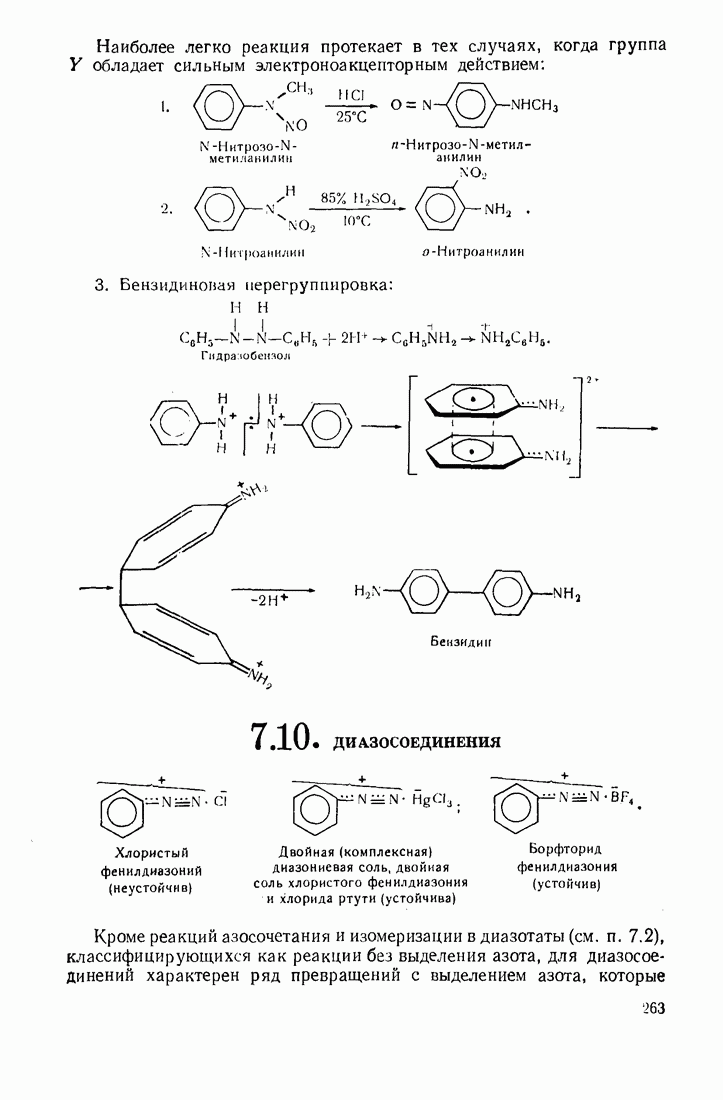
- 7.10. ДИАЗОСОЕДИНЕНИЯ
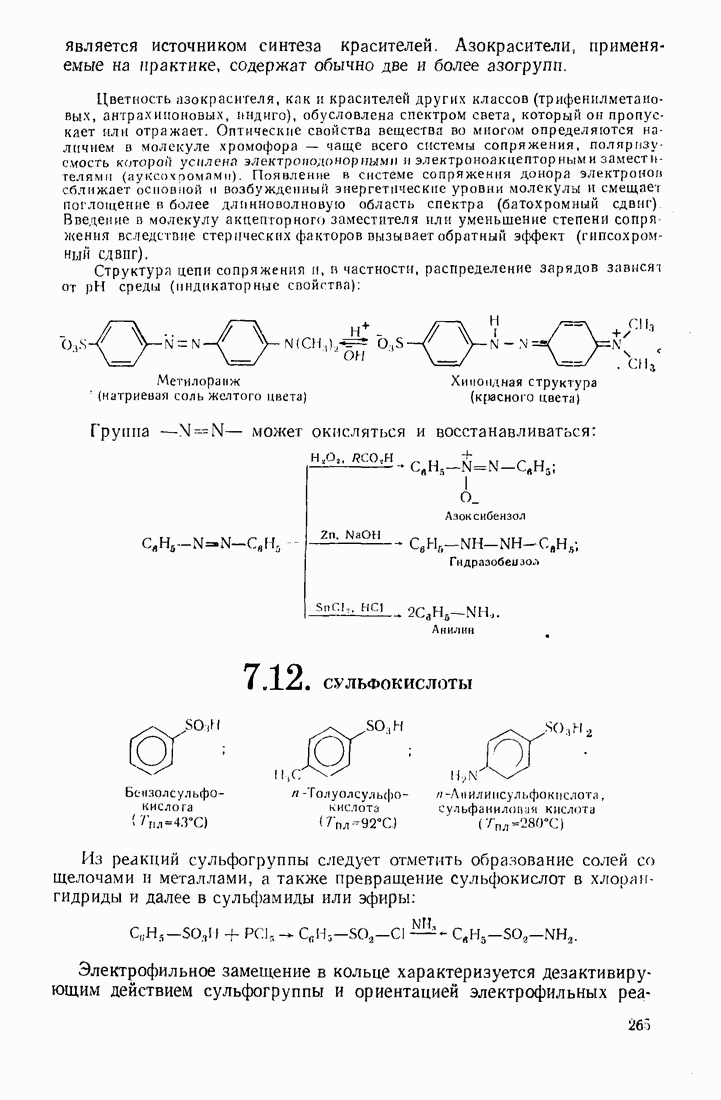
- 7.11. АЗОСОЕДИНЕНИЯ
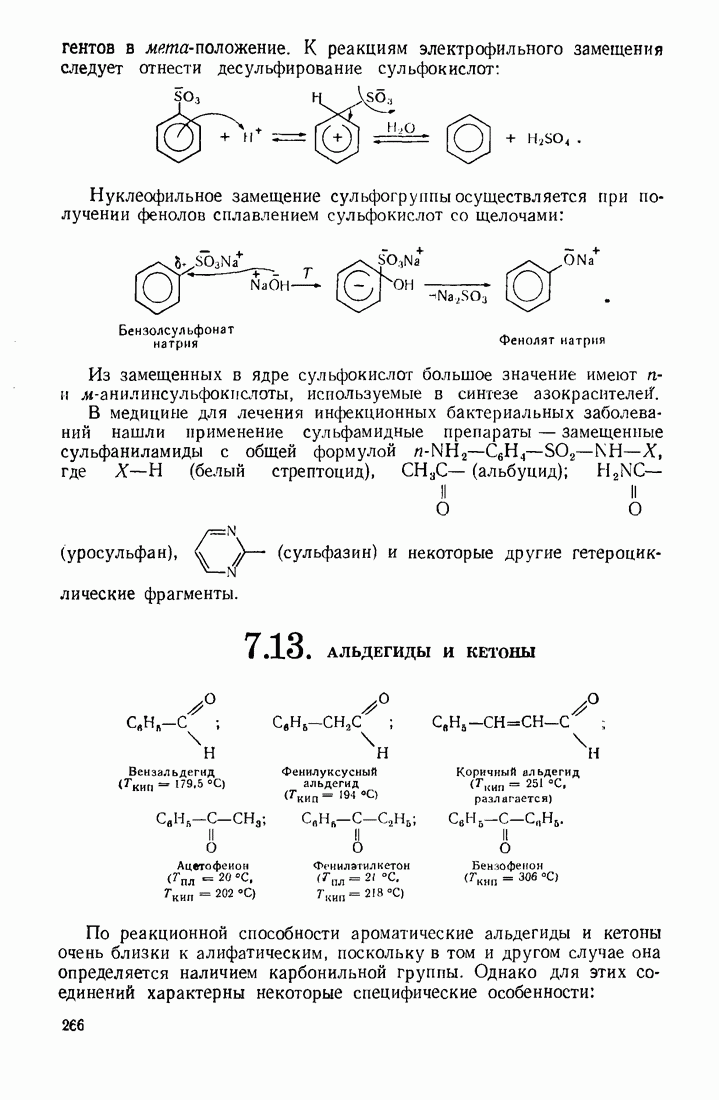
- 7.12. СУЛЬФОКИСЛОТЫ
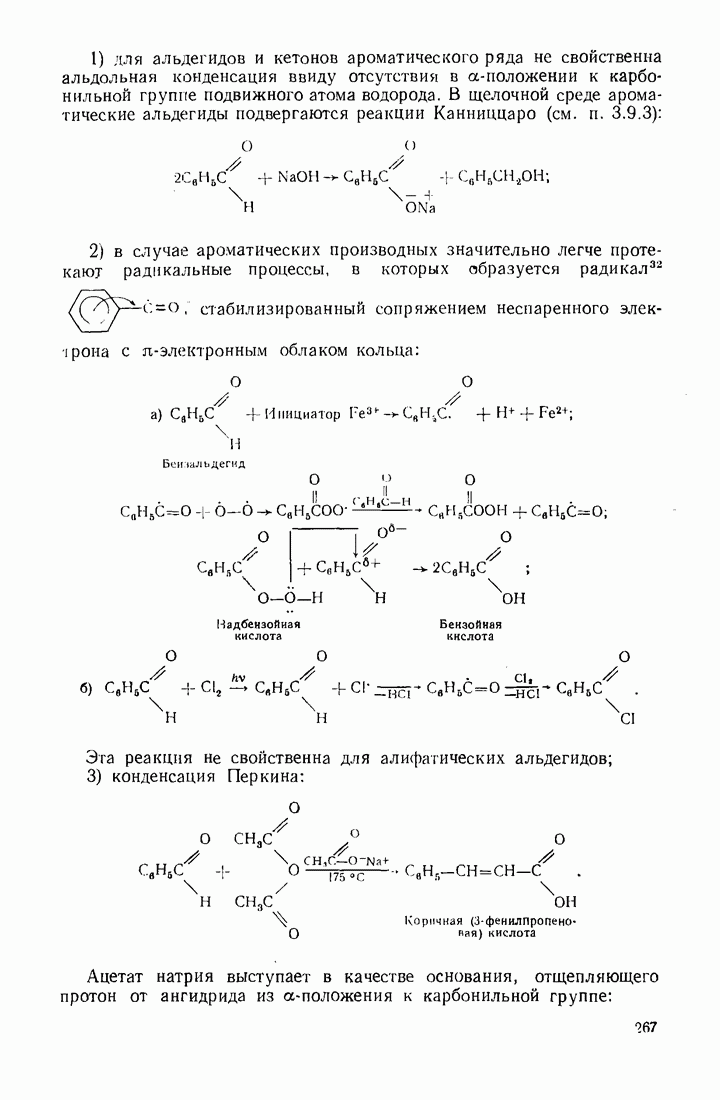
- 7.13. АЛЬДЕГИДЫ И КЕТОНЫ
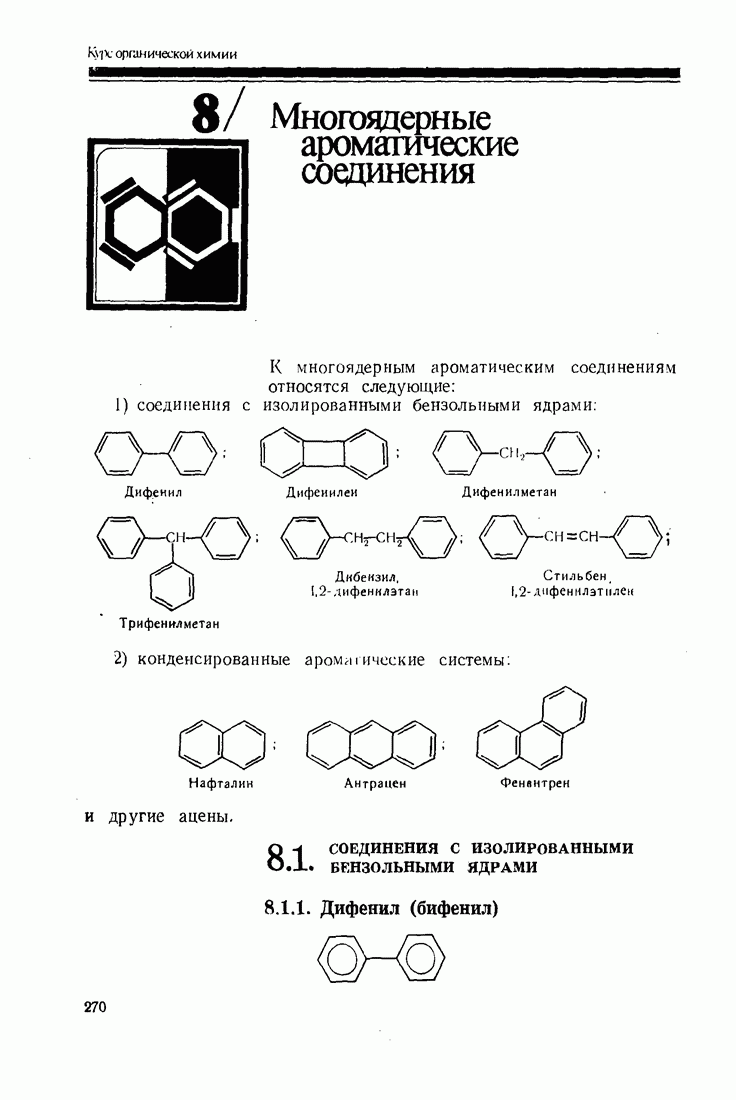
- 8. Многоядерные ароматические соединения
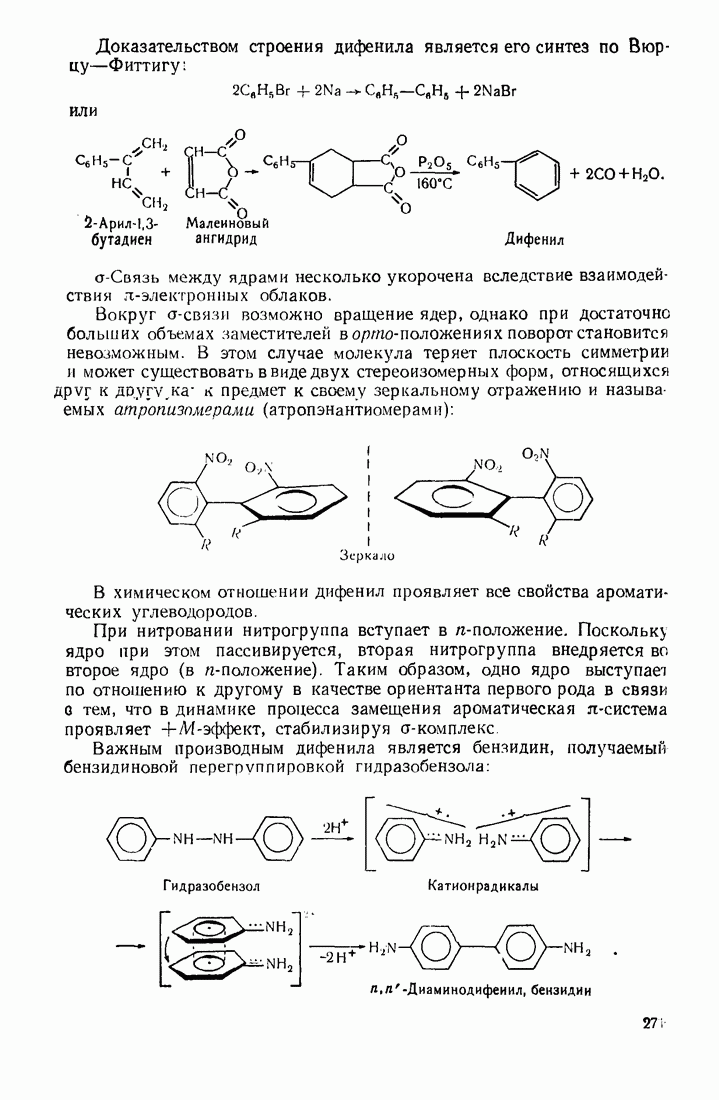
- 8.1. СОЕДИНЕНИЯ С ИЗОЛИРОВАННЫМИ БЕНЗОЛЬНЫМИ ЯДРАМИ
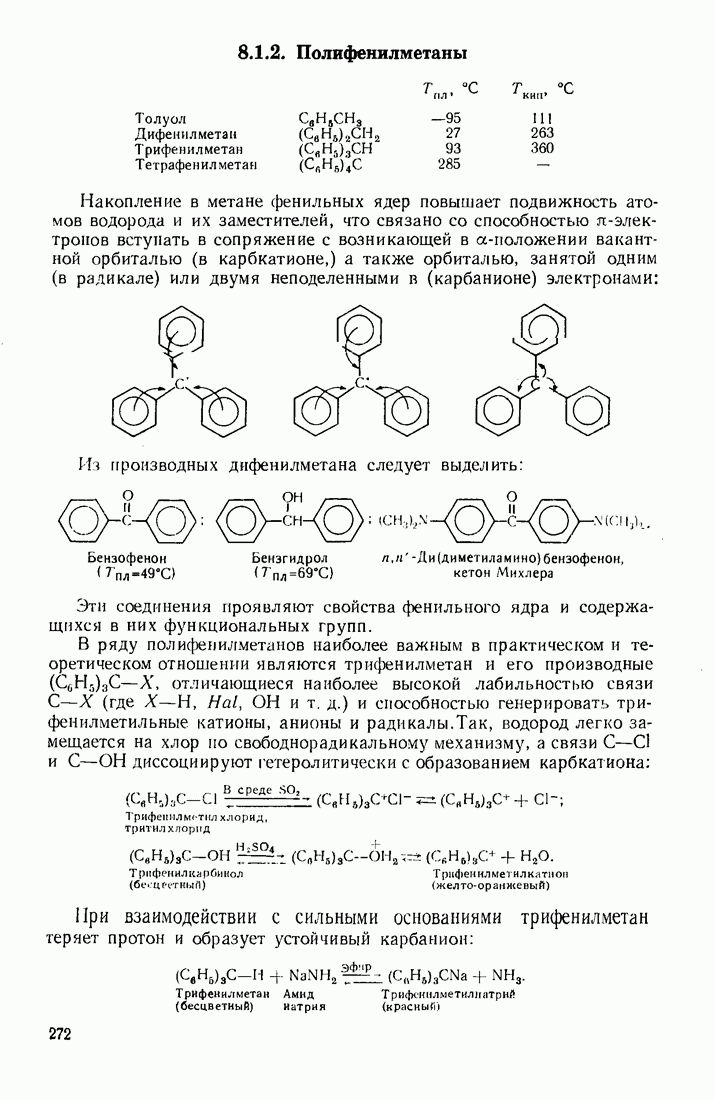
- 8.1.2. Полифенилметаны
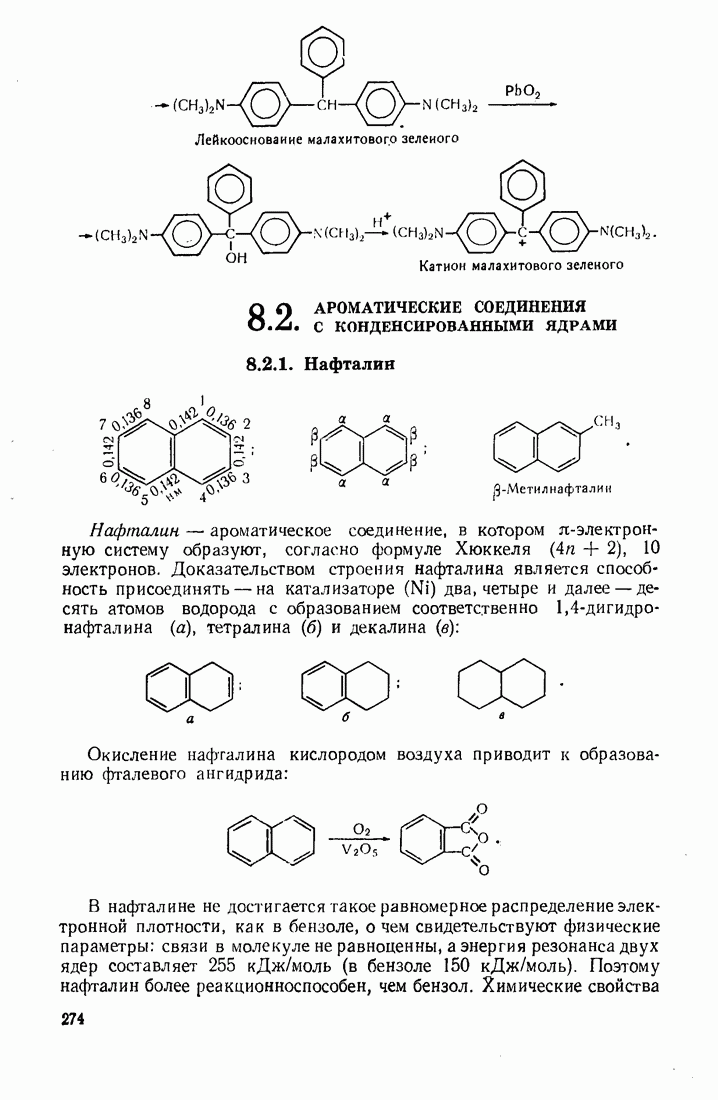
- 8.2. АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ С КОНДЕНСИРОВАННЫМИ ЯДРАМИ
- 8.2.2. Антрацен
- 8.2.3. Фенантрен
- 9. Методы синтеза в ряду ароматических соединений
- 9.1. ГАЛОГЕНИРОВАНИЕ
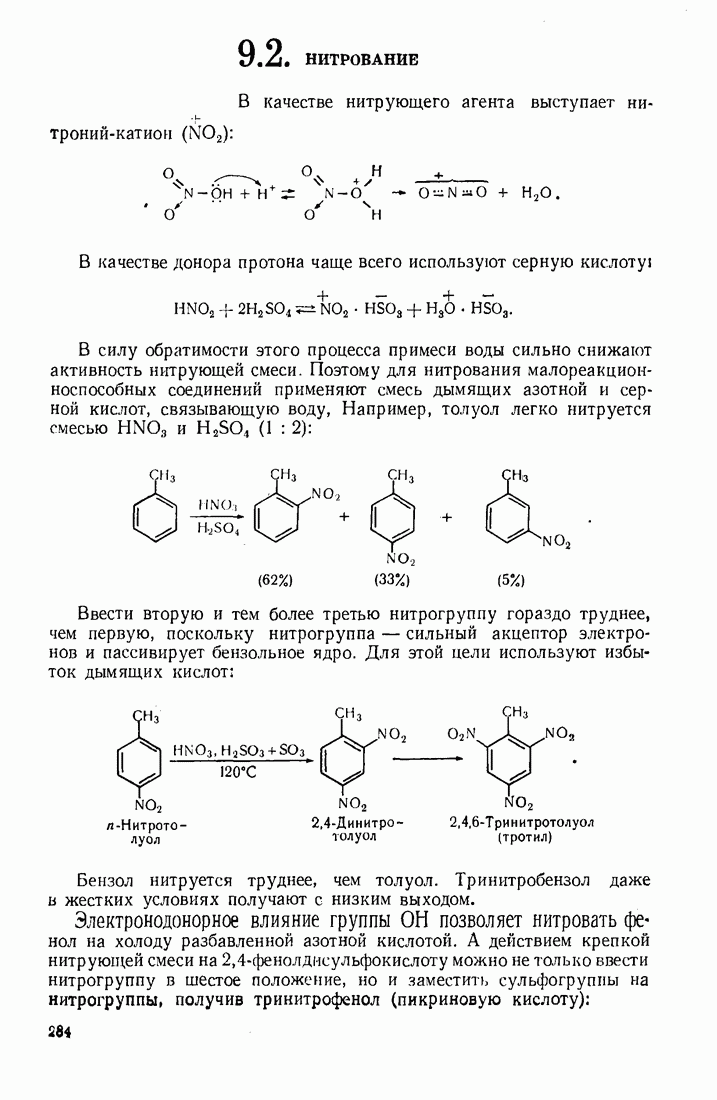
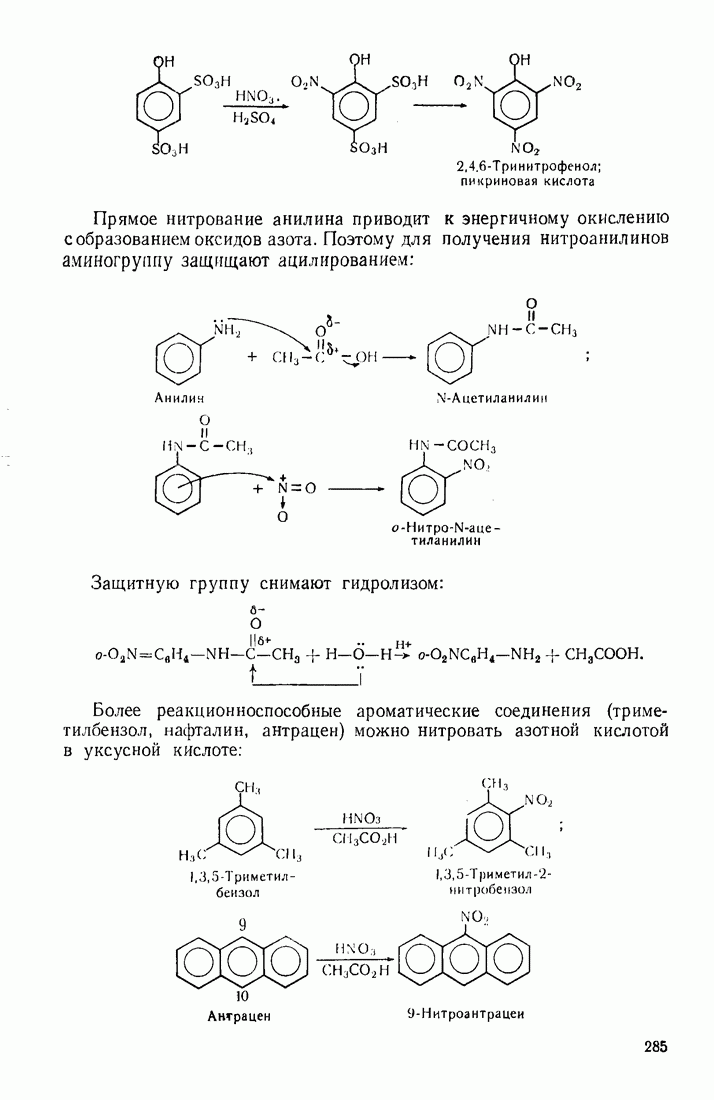
- 9.2. НИТРОВАНИЕ
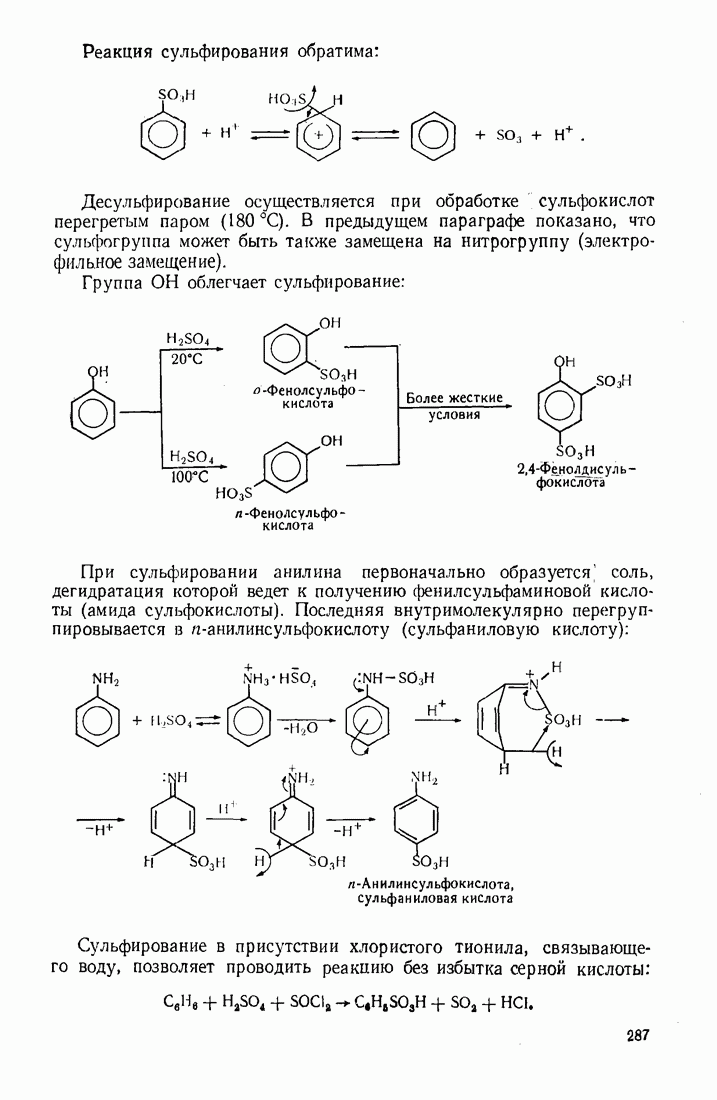
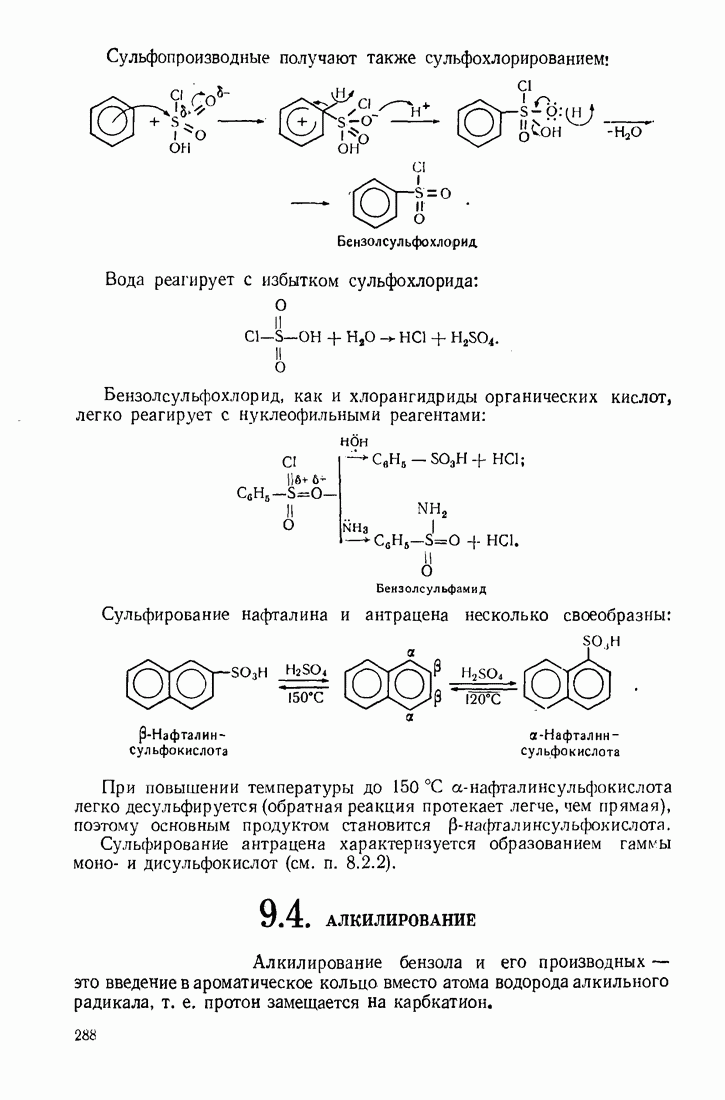
- 9.3. СУЛЬФИРОВАНИЕ
- 9.4. АЛКИЛИРОВАНИЕ
- 9.5. АЦИЛИРОВАНИЕ
- 9.6. ГИДРОКСИЛИРОВАНИЕ
- 9.7. АМИНИРОВАНИЕ
- 9.8. НИТРОЗИРОВАНИЕ
- 9.9. КАРБОНИЛИРОВАНИЕ
- 9.10. КАРБОКСИЛИРОВАНИЕ
- 9.11. ОКИСЛЕНИЕ
- 9.12. ВОССТАНОВЛЕНИЕ
- 10. Гетероциклические соединения
- 10.2. ОБЩАЯ ХАРАКТЕРИСТИКА СТРОЕНИЯ И РЕАКЦИОННОЙ СПОСОБНОСТИ
- 10.3. ПЯТИ- И ШЕСТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С ОДНИМ ГЕТЕРОАТОМОМ
- 10.4. ГЕТЕРОЦИКЛЫ С НЕСКОЛЬКИМИ ГЕТЕРОАТОМАМИ
- 10.5. МЕТОДЫ СИНТЕЗА ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ
- 10.6. П0НЯТИЕ О ПРИРОДНЫХ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЯХ
- 11. Зпементоорганические соединения
- 11.2. ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ НЕКОТОРЫХ НЕМЕТАЛЛОВ
- 11.3. МЕГАЛЛООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- 11.4. ОРГАНИЧЕСКИЕ ПРОИЗВОДНЫЕ ПЕРЕХОДНЫХ МЕТАЛЛОВ
- 12. Сырье и основные направления развития промышленности органического синтеза
- 12.1.1. Нефть и сопутствующий природный газ
- 12.1.2. Углехимическое сырье
- 12.1.3. Лесохимическое и сельскохозяйственное сырье
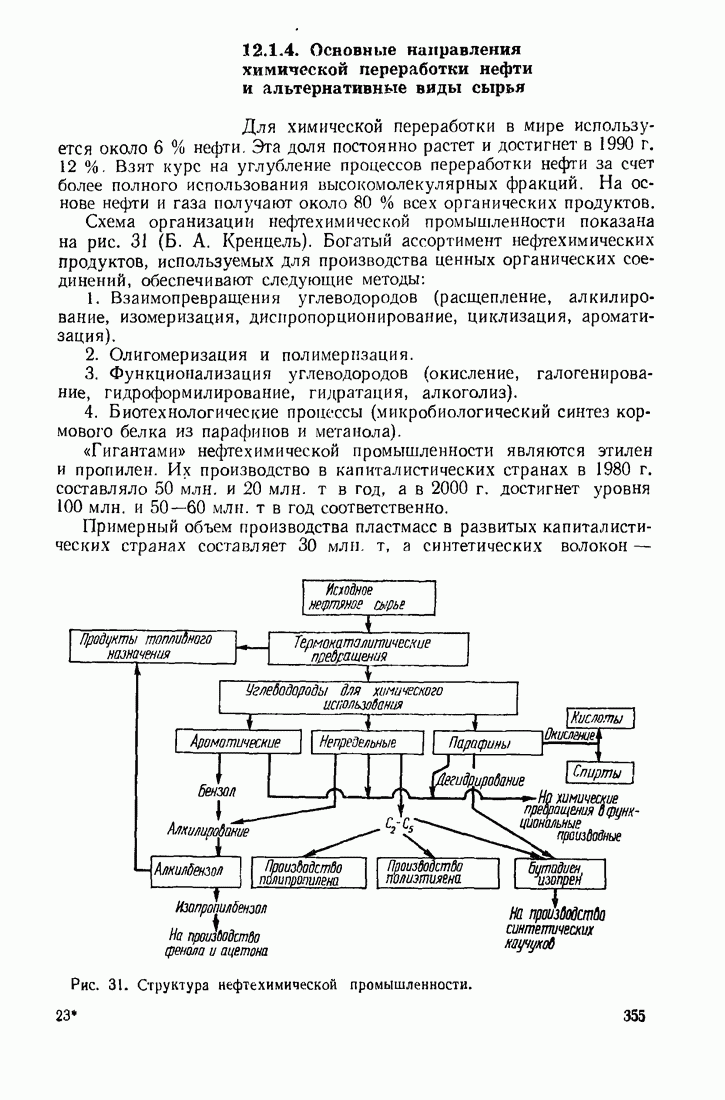
- 12.1.4. Основные направления химической переработки нефти и альтернативные виды сырья
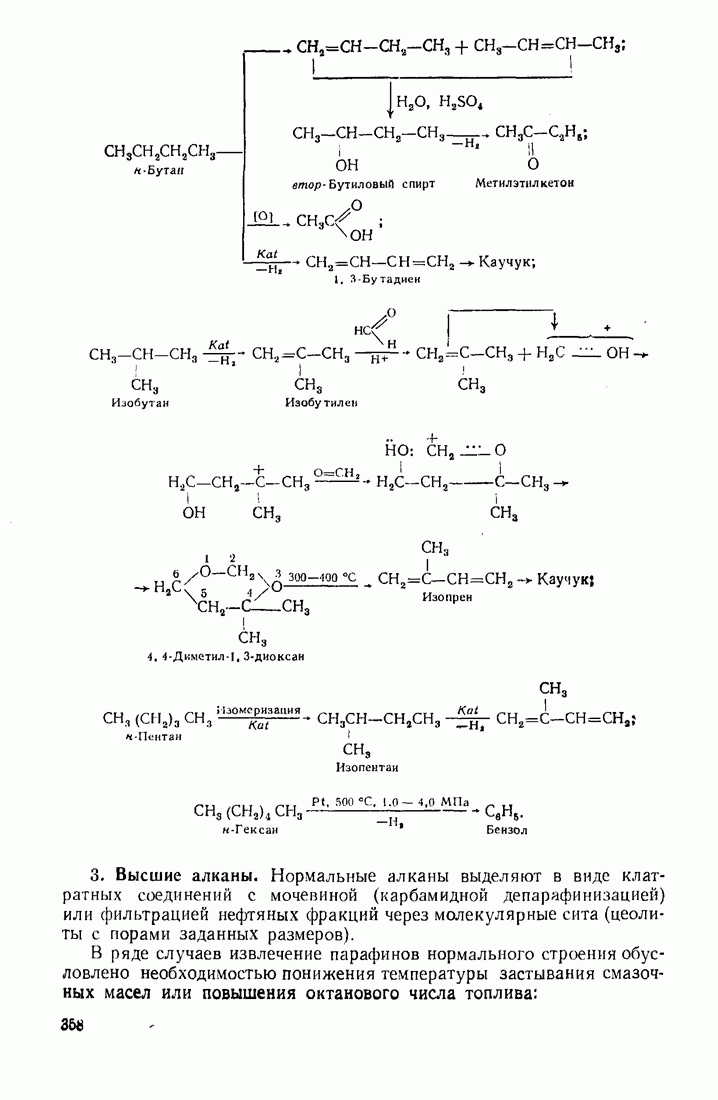
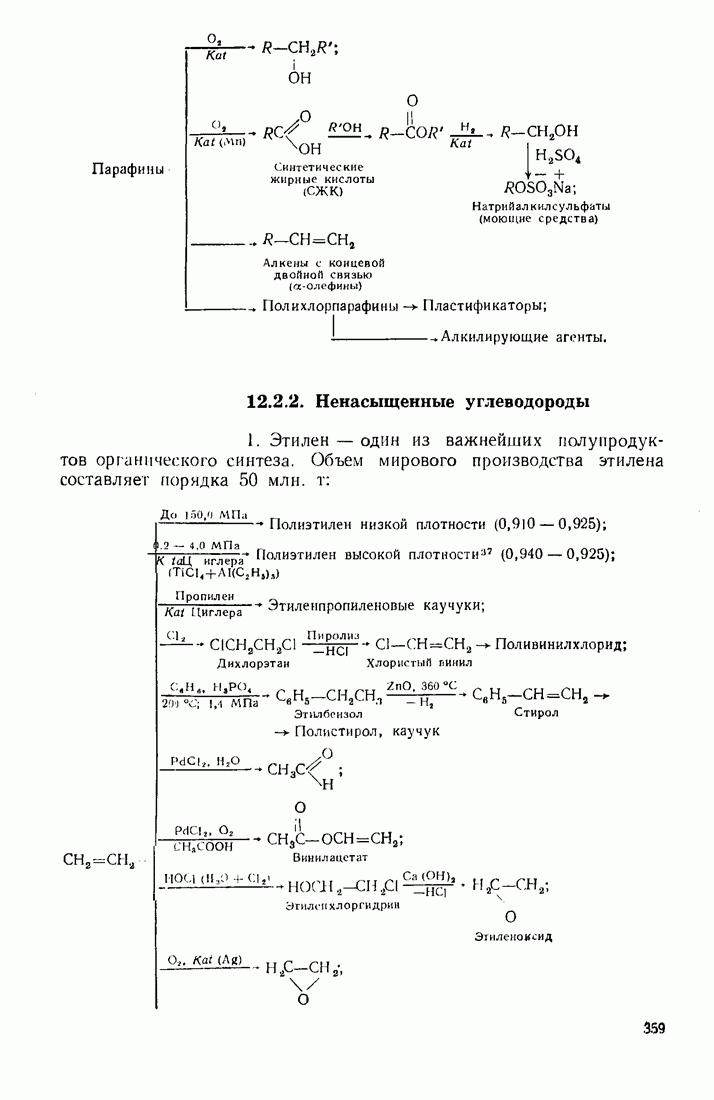
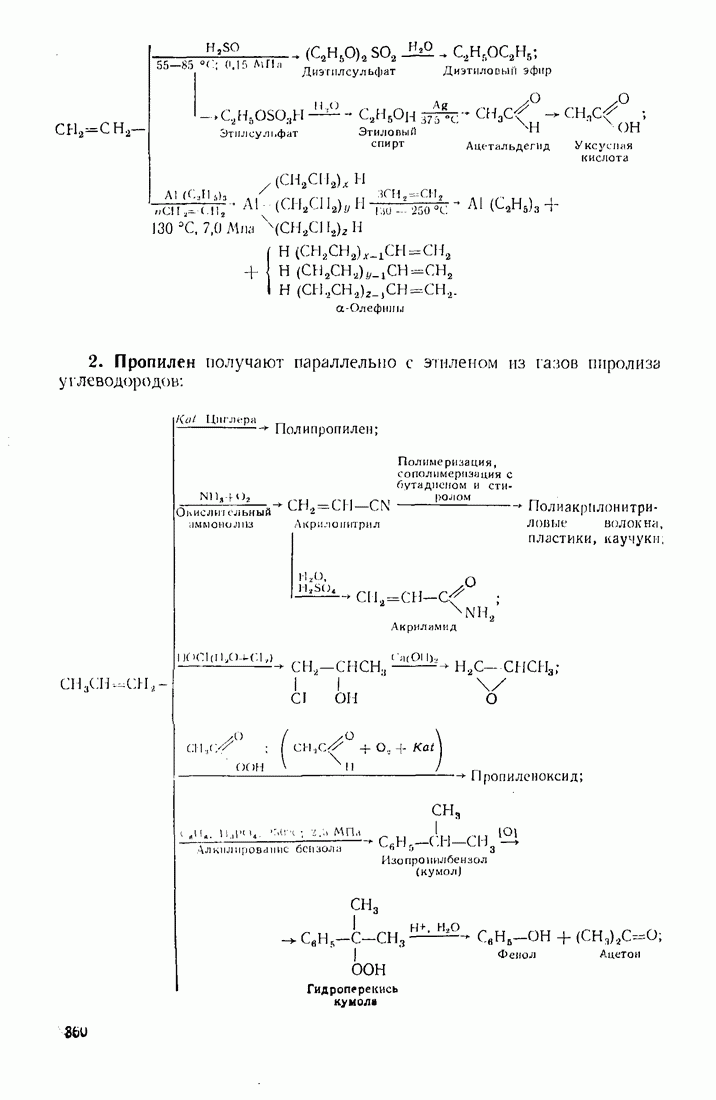
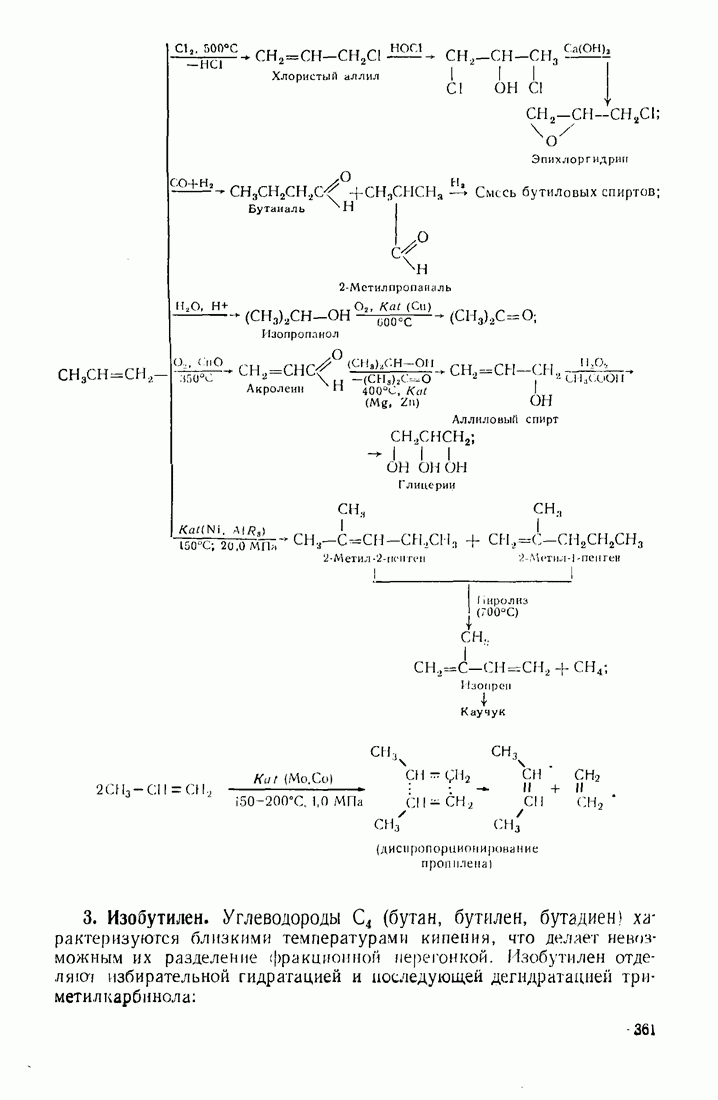
- 12.2. ПУТИ ИСПОЛЬЗОВАНИЯ УГЛЕВОДОРОДОВ И ИХ ПРОИЗВОДНЫХ
- 12.3. РАЗВИТИЕ ХИМИЧЕСКОЙ ПРОМЫШЛЕННОСТИ В СССР В ДВЕНАДЦАТОЙ ПЯТИЛЕТКЕ