| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
1.2. Основные этапы развития органической химии
Органическая химия начала свою историю как химия соединений, полученных из объектов животного и растительного мира (начало XVIII в.). Впоследствии химики научились искусственно синтезировать органические вещества из неорганических соединений и соединений, составляющих основу нефти, угля и природного газа.
Одной из первых попыток проникнуть в сущность органического вещества была теория радикалов Ж. Дюма и Я. Берцелиуса (начало
XIX в.). Согласно этой теории, признаком органических веществ являются группы атомов—радикалы (бензил, ацетил, метил и др.), способные в неизменном виде переходить от одного вещества к другому. В рамках теории радикалов Я, Берцелиус развил дуалистические представления о том, что каждое соединение состоит из двух частей: электроотрицательной — кислорода и электроположительной, представляющей собой органический радикал.
Поиски в молекулах неизменных фрагментов вскоре уступили место изучению ее изменяющихся частей (говоря современным языком — функциональных групп). Этот этап привел к развитию унитарной теории типов Ш. Жерара (середина XIX в.), в которой вещество рассматривалось как единое целое, Известные в то время соединения были классифицированы как продукты замещения водорода на органические остатки в соединениях  Так, спирт относился к типу воды, а хлористый этил — к типу хлороводорода. Немецкий химик А. Кекуле установил тип метана.
Так, спирт относился к типу воды, а хлористый этил — к типу хлороводорода. Немецкий химик А. Кекуле установил тип метана.
50-е годы XIX в. ознаменовались развитием теории валентности (Э. Франкланд, А. Купер, А. Кекуле), были построены первые структурные формулы. А. Кекуле установил четырехвалентность углерода (1857 г.) и способность его атомов насыщать друг друга, т. е. образовывать цепи. Чтобы соблюсти постоянство валентности атомов углерода, А. Кекуле допустил существование двойных и тройных связей  д.), предложил структурную формулу бензола (1865 г.). Однако А. Кекуле не создал новой теории, поскольку он стоял на идеалистических позициях, полагая, что конституция (строение) молекул непознаваема, а их формулы представляют собой лишь удобный способ описания свойств. Часто одному и тому же веществу приписывались разные формулы.
д.), предложил структурную формулу бензола (1865 г.). Однако А. Кекуле не создал новой теории, поскольку он стоял на идеалистических позициях, полагая, что конституция (строение) молекул непознаваема, а их формулы представляют собой лишь удобный способ описания свойств. Часто одному и тому же веществу приписывались разные формулы.
Новое слово в органической химии было сказано русским ученым А. М. Бутлеровым. Обобщив накопленные к тому времени данные, он создал стройную теорию химического строения и подтвердил ее новыми экспериментальными примерами (1861 г.). Были объяснены явления изомерии и таутомерии (динамической изомерии). Развивая материалистический образ мышления в познании химических явлений, А. М. Бутлеров решил коренную методологическую проблему органической химии.
Основные положения теории Бутлерова:
1. Молекулы существуют объективно и могут быть познаны с помощью эксперимента, наблюдения и мышления.
2. Порядок связывания атомов в молекуле называется «химическим строением». Каждому химическому соединению соответствует одна структурная формула, т. е. строгая последовательность связи атомов в соответствии с их валентностью. Валентность атомов переменная.
3. Химическое строение вещества определяет его физические и химические свойства. Изменение последовательности связи атомов приводит к появлению нового вещества. Этим объясняется явление изомерии, суть которого заключается в том, что вещества с одинаковым качественным и количественным составом имеют разное строение и поэтому обладают различными свойствами.
4. Атомы в молекулах взаимно влияют друг на друга. Свойства определенного атома в молекуле зависят от тою, с каким атомом он связан. Например, химическое поведение атома водорода гидроксильной группы в спиртах существенно отличается от поведения атомов водорода алкильного радикала. Изолированные атомы также влияют друг на друга, хотя это влияние и более слабое.
5. Структуру органического соединения можно установить путем химических превращений, и наоборот — зная структуру вещества, можно предсказать его реакционную способность.
С появлением теории Бутлерова центральная проблема химической науки «состав — свойства» уступила место проблеме «строение — свойства».
Развитие электронных представлений о строении атома и молекулы (начало XX в.; Н. Бор, В. Коссель, Г. Льюис) привело к поискам решения этой проблемы на электронном уровне, а разработка в 30-х годах основ квантовой механики (В. Гейзенберг, Э. Шредингер, Э. Хюккель) послужила толчком для развития в теории строения и реакционной способности качественно нового метода — метода молекулярных орбиталей. Узловой теоретической проблемой современной органической химии стала теория активированного комплекса и механизма реакций.
«Сфера влияния» современной органической химии чрезвычайно широка и простирается от крупнотоннажных производств метанола и полимеров до синтеза витаминов, биополимеров, генов и других сложнейших биологических систем. При этом проникновение ее в смежные области науки и практики — материаловедение, биологию, медицину, сельское хозяйство — постоянно углубляется.
В последнее время чрезвычайно интенсивное развитие получила химия элементоорганических соединений, стирающих границу между органическим и неорганическим миром.
Основными тенденциями в развитии теоретической и промышленной органической химии являются:
1. Применение квантовой механики для описания структуры и реакционной способности соединений, нестабильных промежуточных частиц и комплексов. Развитие новых воззрений на механизм реакций.
2. Использование ЭВМ для кпантово-химическнх расчетов, конформационного анализа, установления корреляций «строение — свойства», прогнозирования направления реакций, выбора оптимальных режимов и автоматизации систем управления технологическими процессами.
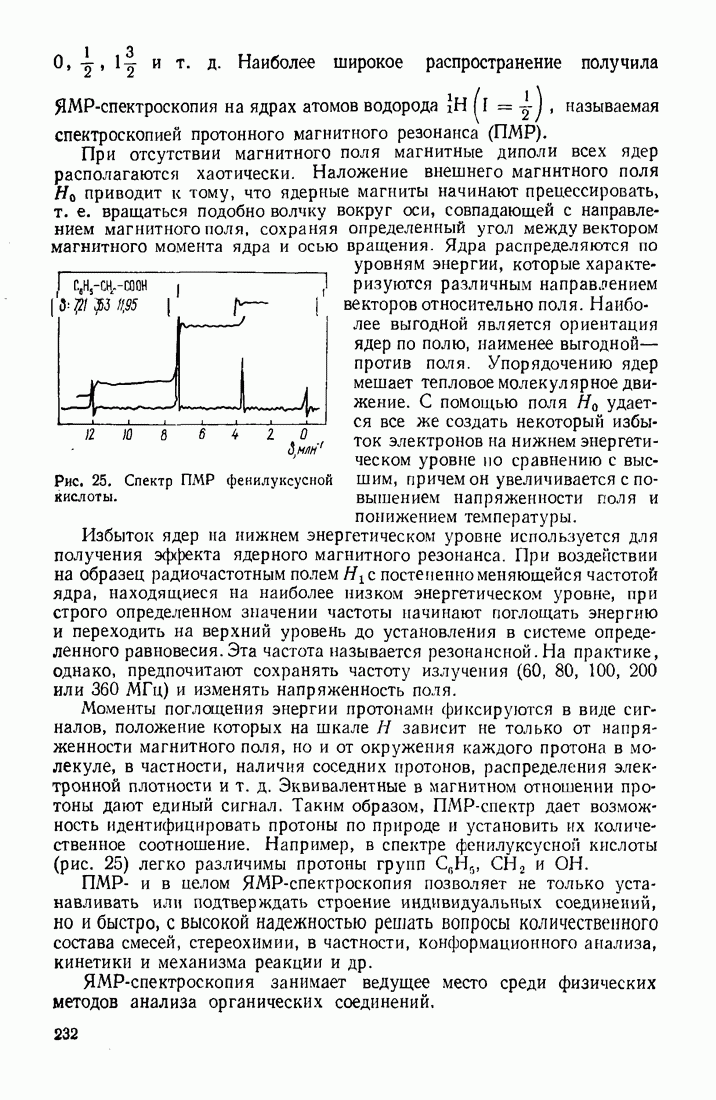
3. Широкое применение новейших физических методов исследования: ИФ- и УФ-спектроскопии, спектроскопии ядерного магнитного резонанса и электронного парамагнитного резонанса, ион-циклотронного резонанса, масс-спектроскопии, лазерной техники, рентгено-структурного анализа и т. д.
4. Разработка новых каталитических процессов, прежде всего в области полимеризации низших олефинов и превращений одноуглеродных соединений  в условиях металлокомплексного катализа (
в условиях металлокомплексного катализа ( -химия»).
-химия»).
5. Моделирование фотохимических и каталитических процессов, протекающих в растительных и животных организмах, синтез биологически активных соединений.
6. Создание новых конструкционных материалов и полимерных композиций, способных конкурировать с металлами и обладающих такими качествами, как термостойкость, высокая прочность, электропроводимость и т. д.
Химическая наука во многом определяет уровень развития технологии (см. п. 12.3), в то же время технология ставит крупные проблемы перед наукой и намечает пути научно-технического прогресса.
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие
- 1. Введение
- 1.1. Предмет органической химии
- 1.2. Основные этапы развития органической химии
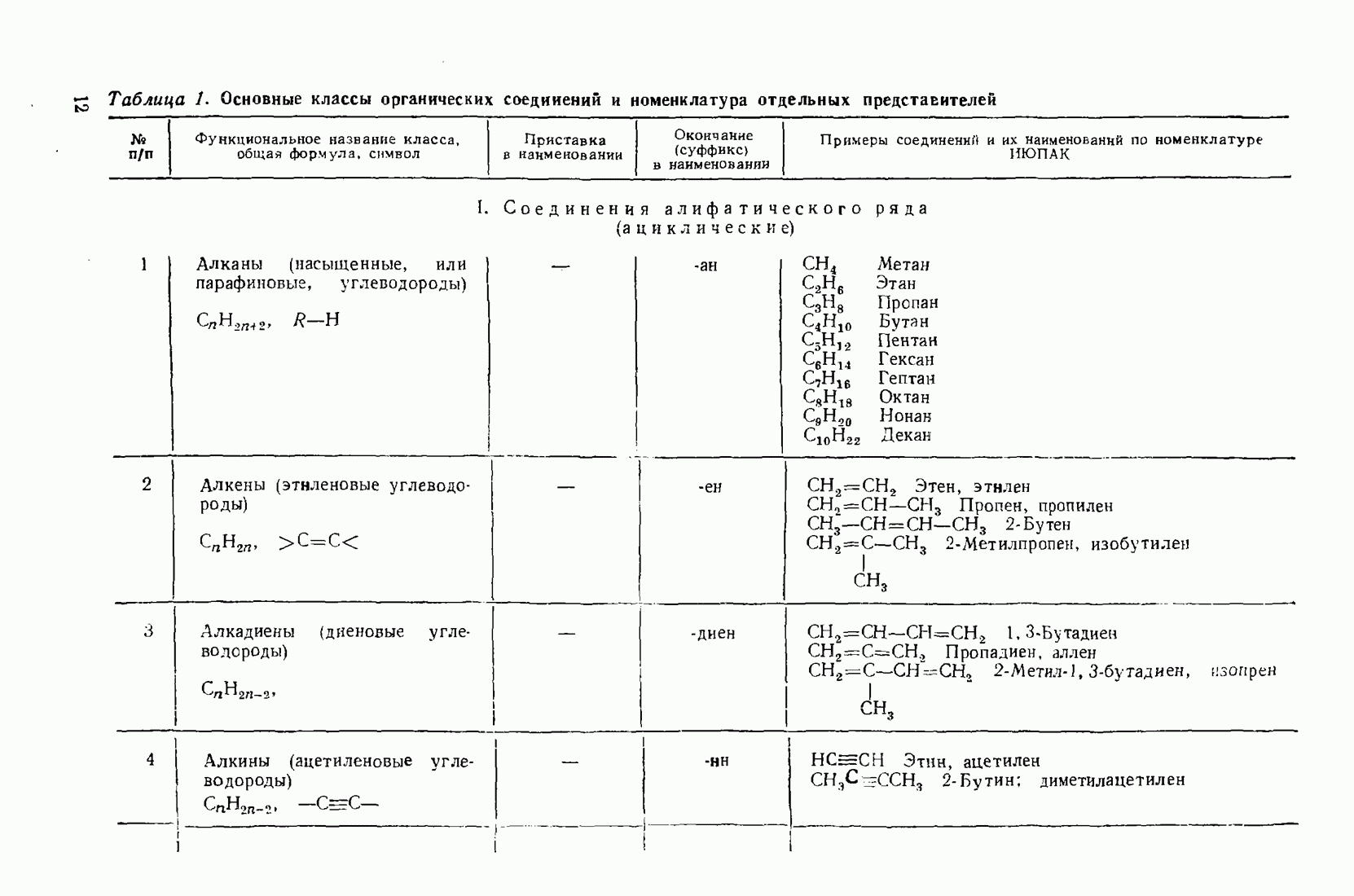
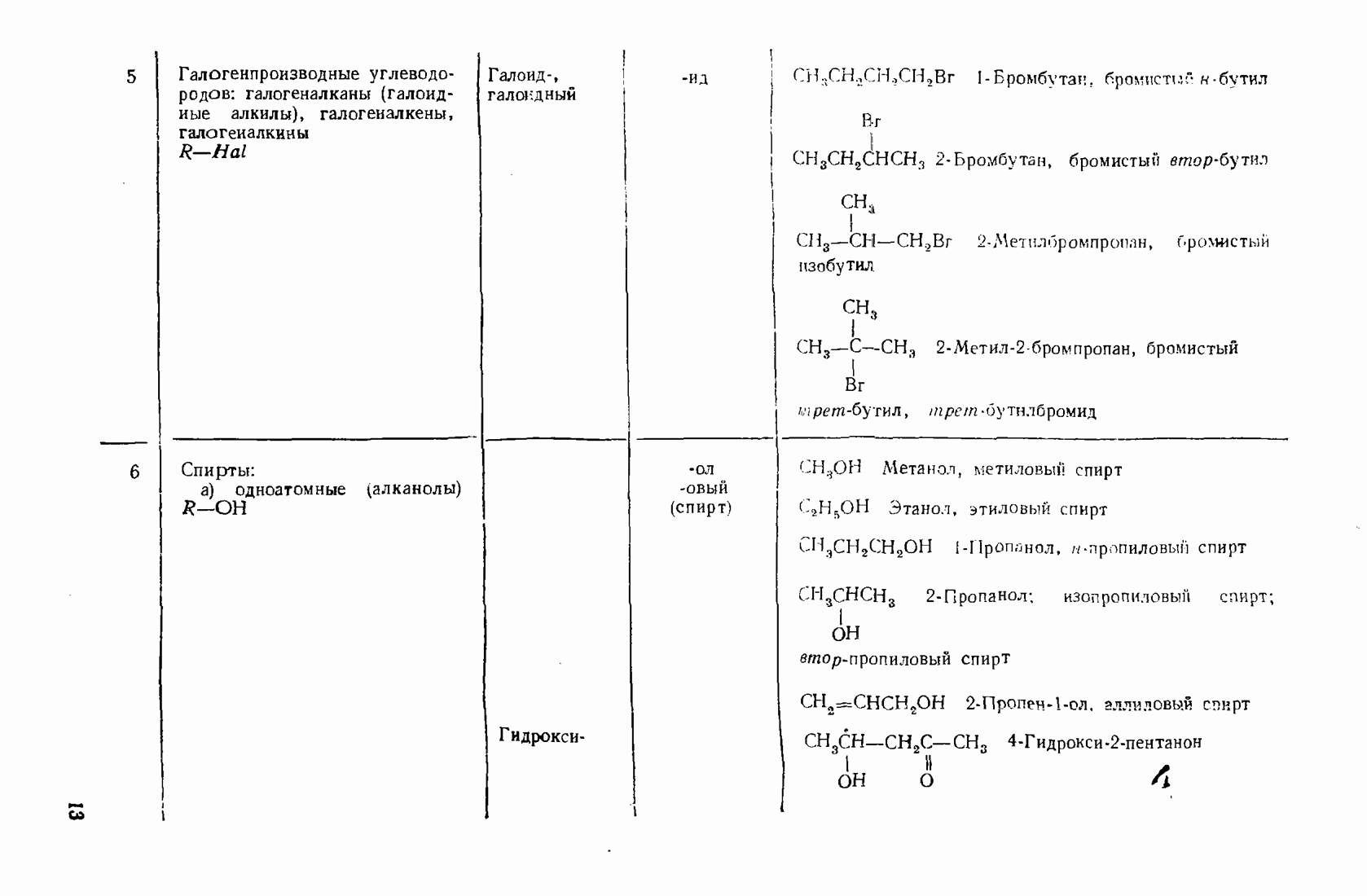
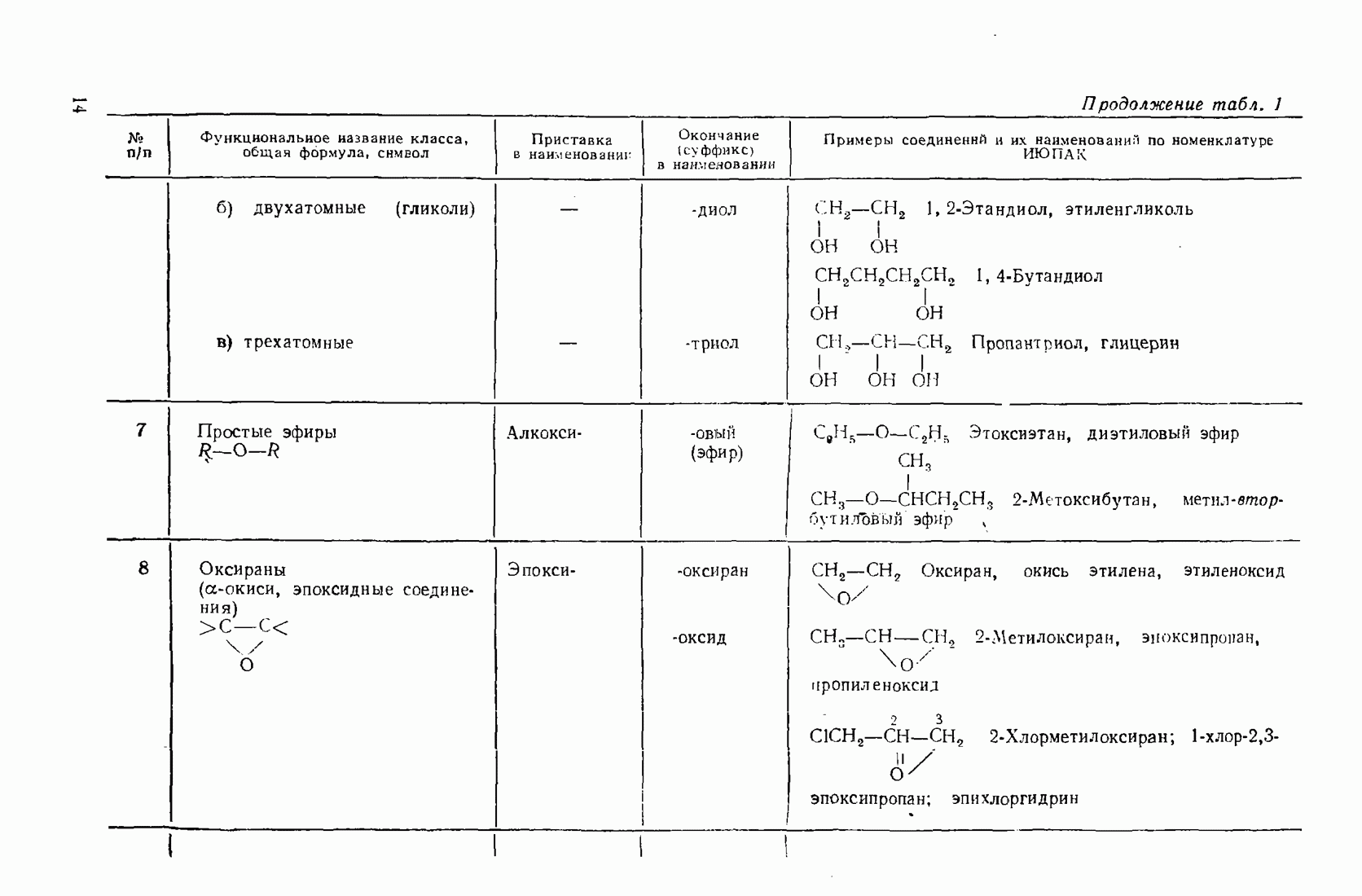
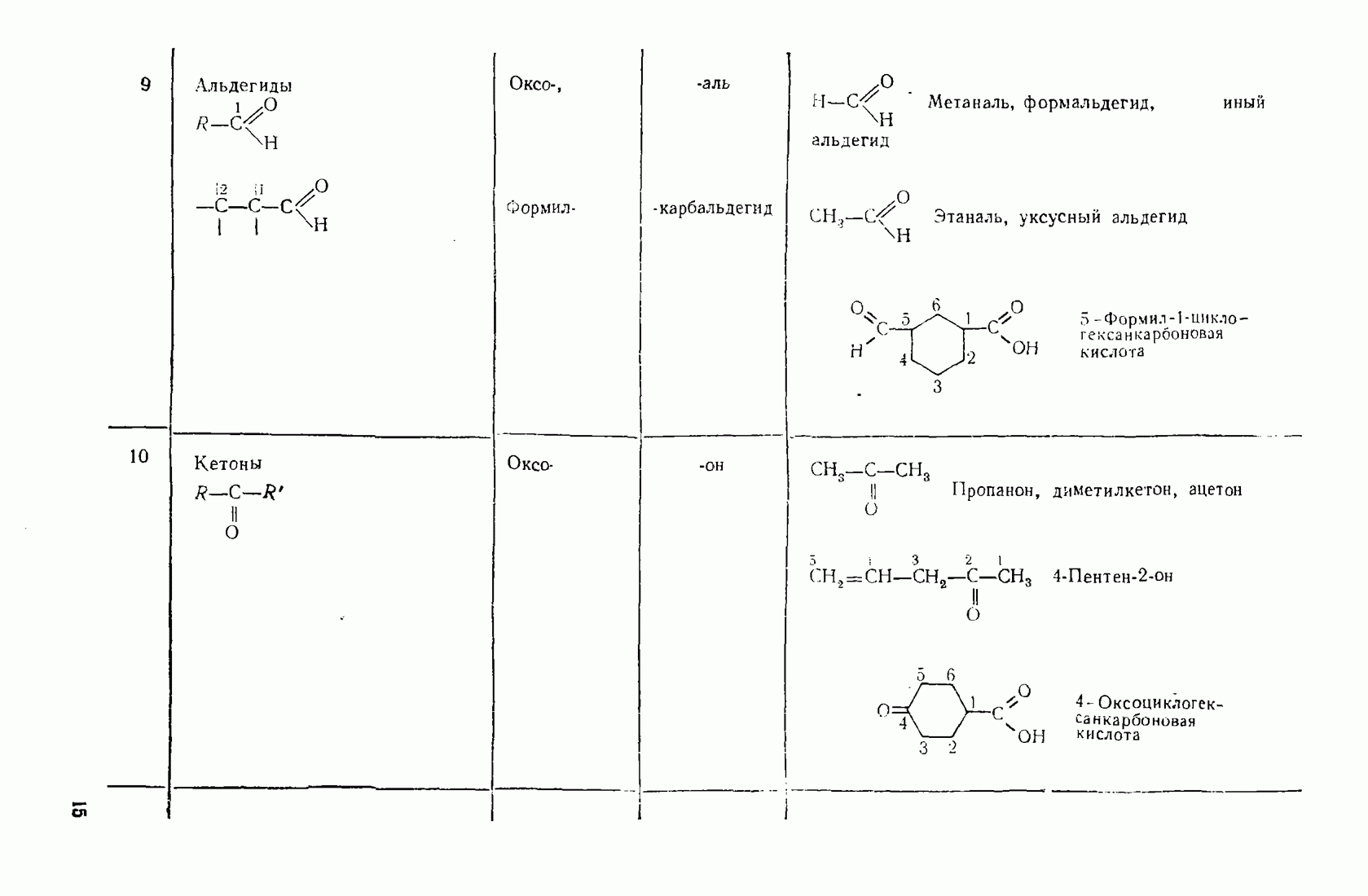
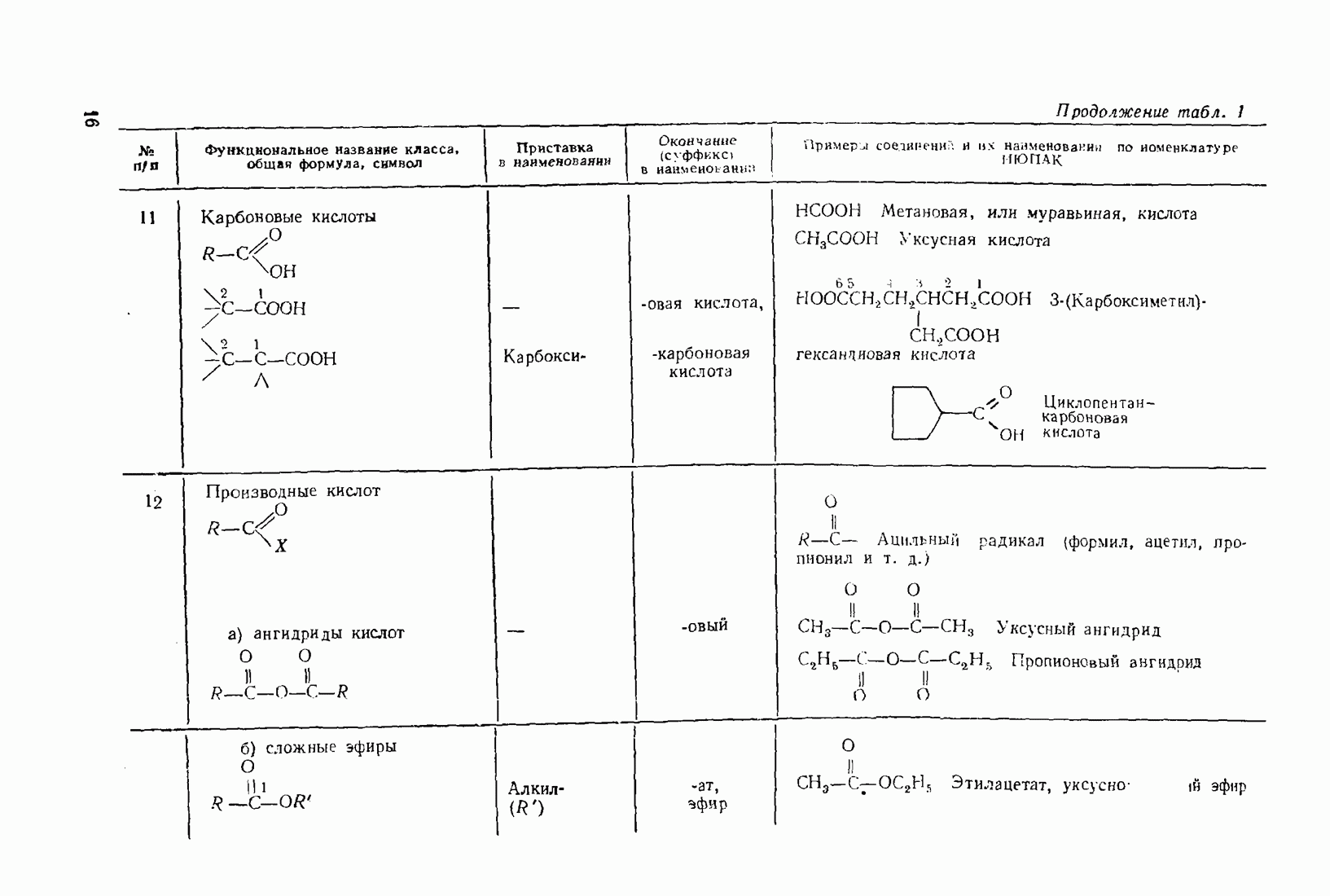
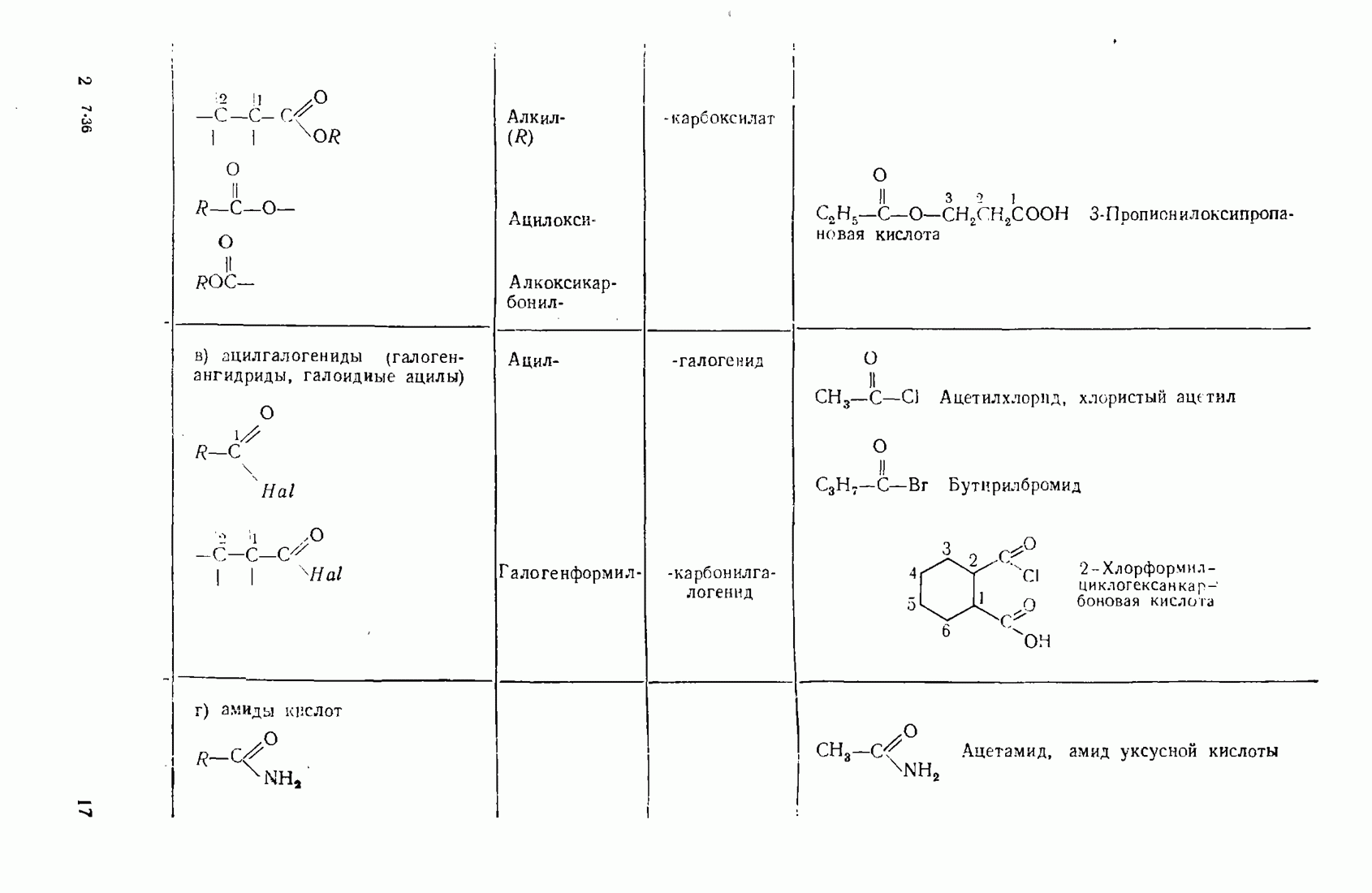
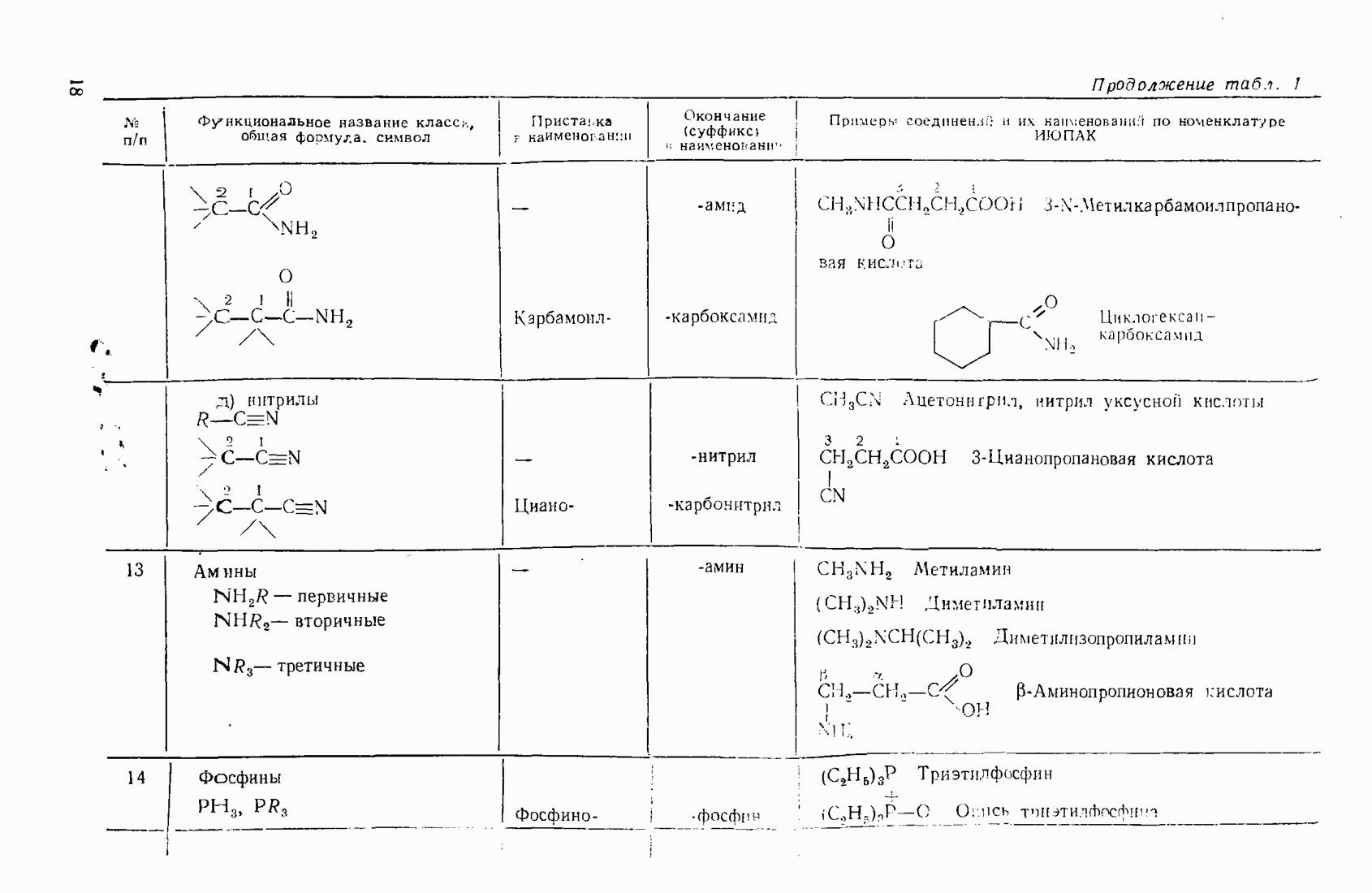
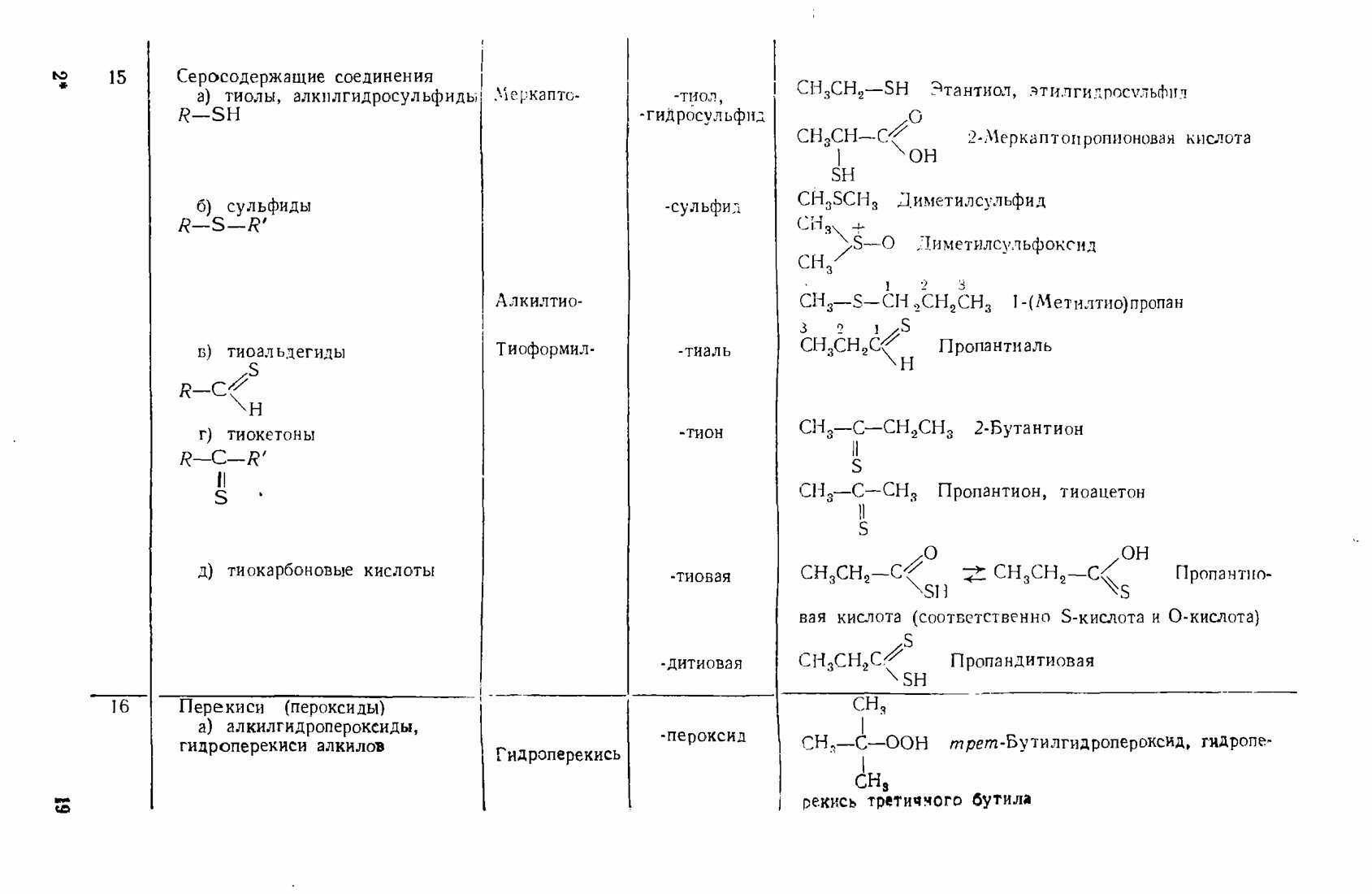
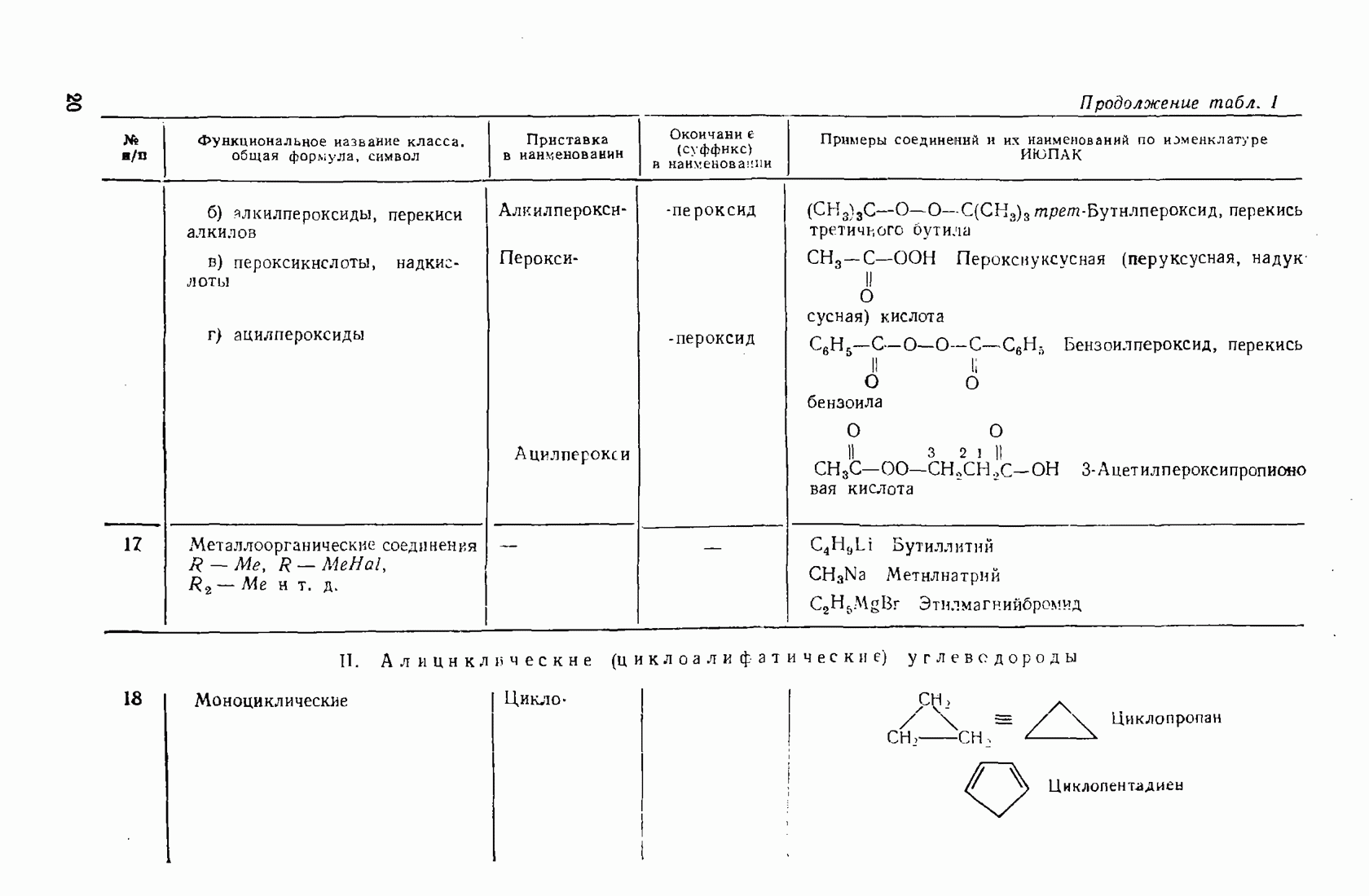
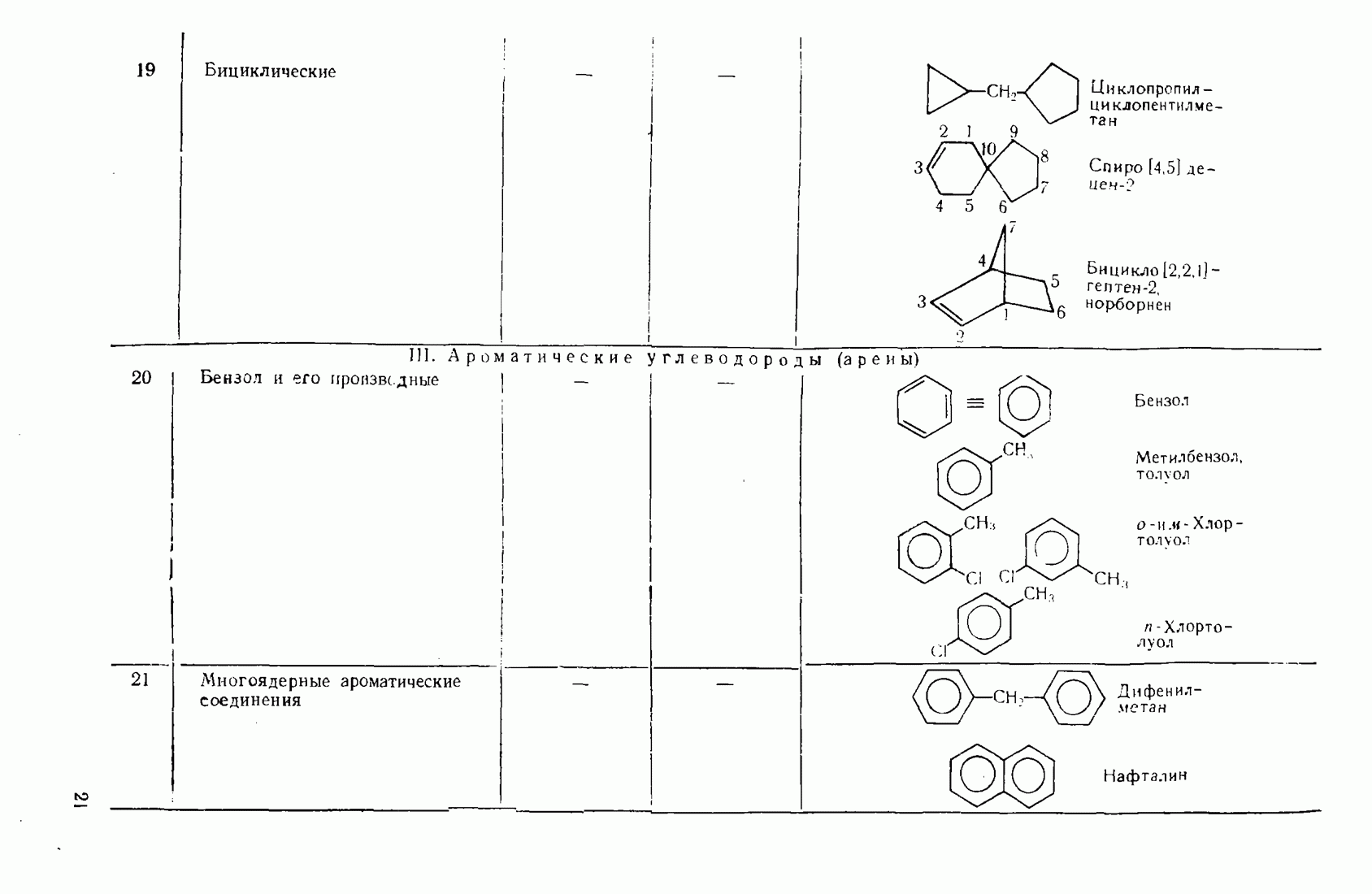
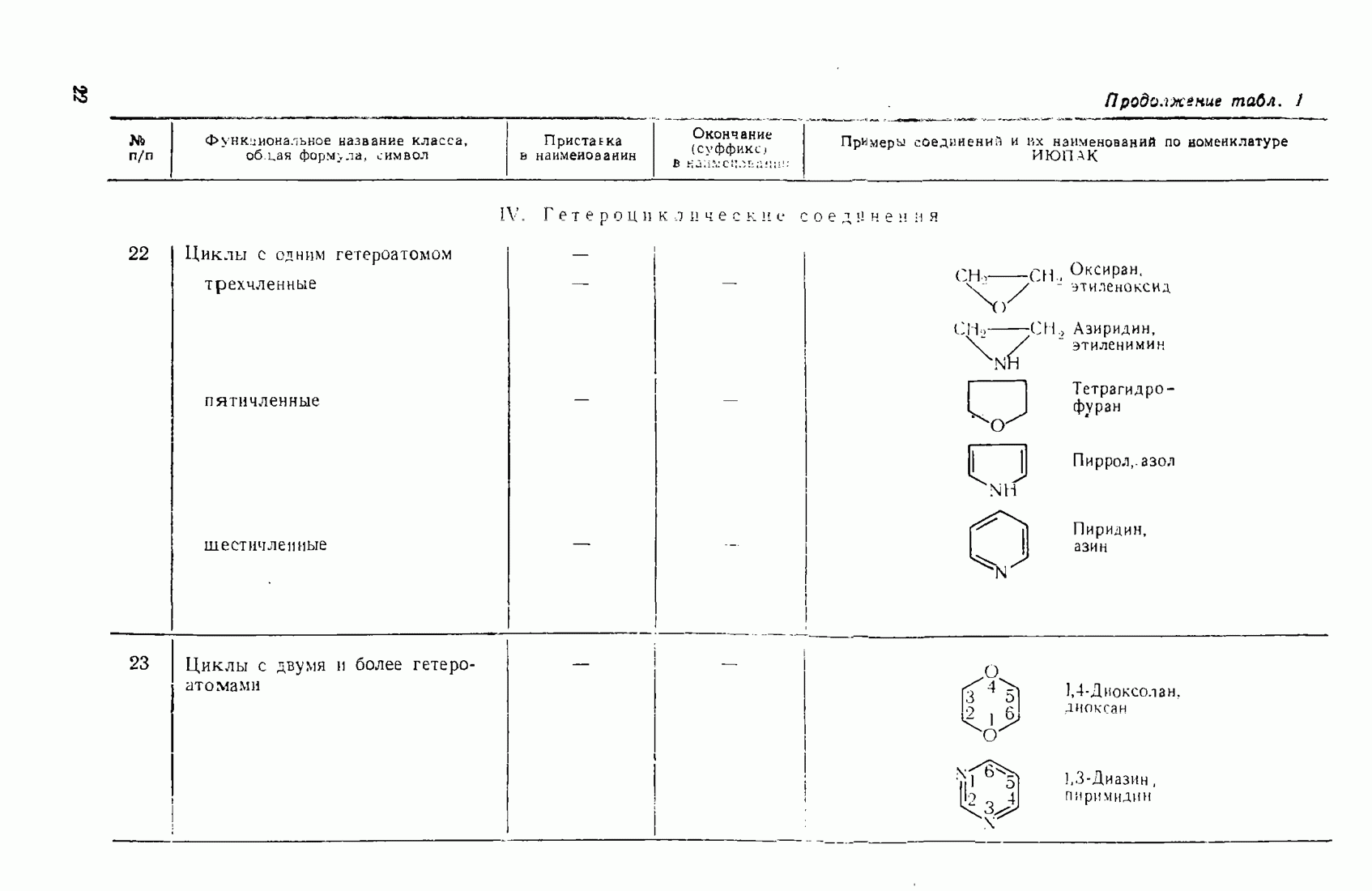
- 1.3. Классификация и номенклатура органических соединений
- 2 Общие теоретические положения органической химии
- 2.1. Природа химической связи
- 2.1.1. Типы химических связей
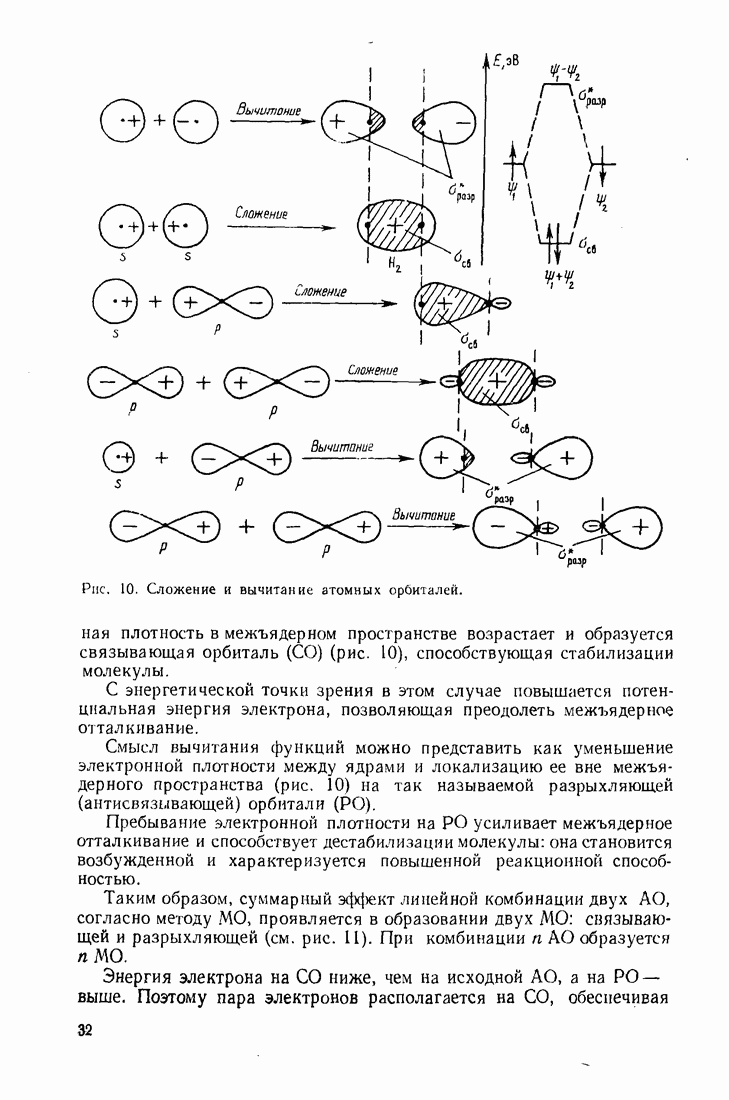
- 2.1.2. Молекулярные орбитали
- 2.2. ТИПЫ ЭЛЕКТРОННЫХ СМЕЩЕНИЙ В МОЛЕКУЛАХ
- 2.3. ОБЩИЕ ПРЕДСТАВЛЕНИЯ ОБ ОРГАНИЧЕСКОЙ РЕАКЦИИ
- 2.4. КЛАССИФИКАЦИЯ РЕАГЕНТОВ И РЕАКЦИЙ
- 2.5. КРАТКАЯ ХАРАКТЕРИСТИКА РЕАКЦИОННОЙ СПОСОБНОСТИ НЕКОТОРЫХ СОЕДИНЕНИЙ АЛИФАТИЧЕСКОГО РЯДА
- 2.5.1. Алканы (парафины)
- 2.5.2. Непредельные углеводороды
- 2.5.3. Галогеналканы (галоидные алкилы R-Hal)
- 2.5.4. Спирты (R0Н)
- 2.5.5. Альдегиды и кетоны
- 2.5.6. Карбоновые кислоты (R-СООН) и их производные (R-СО-X)
- 2.5.7. Амины (NH2R, NHR2, NR3)
- 3. Реакционная способность соединений алифатического ряда
- 3.1. Алканы (насыщенные углеводороды)
- 3.2. АЛКЕНЫ (ОЛЕФИНЫ)
- 3.3. ДИЕНОВЫЕ УГЛЕВОДОРОДЫ
- 3.4. АЦЕТИЛЕНЫ
- 3.5. ГАЛОГЕНАЛКАНЫ (ГАЛОИДНЫЕ АЛКИЛЫ)
- 3.6. СПИРТЫ
- 3.7. ПРОСТЫЕ ЭФИРЫ (R-O-R)
- 3.8. ОКСИРАНЫ (ЭПОКСИДНЫЕ СОЕДИНЕНИЯ, a-ОКИСИ)
- 3.9. АЛЬДЕГИДЫ И КЕТОНЫ
- 3.10. КАРБОНОВЫЕ КИСЛОТЫ
- 3.11. НЕКОТОРЫЕ ПРОИЗВОДНЫЕ КИСЛОТ
- 3.12. АМИНЫ
- 3.13. ФОСФОРОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- 3.14. СЕРООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- 3.15. ОРГАНИЧЕСКИЕ ПЕРЕКИСИ (ПЕРОКСИДНЫЕ СОЕДИНЕНИЯ)
- 3.16. ПРОИЗВОДНЫЕ УГОЛЬНОЙ КИСЛОТЫ
- 3.17. ГЕТЕРОАНАЛОГИ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ
- 3.18. АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- 3.18.2. Пространственное расположение и напряженность циклов
- 3.18.3. Особенности химических свойств алициклических соединений
- 4. Полифункциональные производные алифатического ряда
- 4.1. ДВУХОСНОВНЫЕ КАРБОНОВЫЕ КИСЛОТЫ
- 4.2. НЕПРЕДЕЛЬНЫЕ КИСЛОТЫ
- 4.3. ОКСОКИСЛОТЫ (АЛЬДЕГИДО- И КЕТОКИСЛОТЫ)
- 4.4. ОКСИКИСЛОТЫ. ПОНЯТИЕ ОБ ОПТИЧЕСКОЙ ИЗОМЕРИИ
- 4.5. УГЛЕВОДЫ
- 4.5.2. Стереохимия моносахаридов
- 4.5.3. Дисахариды
- 4.5.4. Полисахариды
- 4.5.5. Нахождение в природе и пути превращения углеводов
- 4.6. АМИНОКИСЛОТЫ
- 5. Методы синтеза органических юединений алифатическою рада
- 5.1. АЛКИЛИРОВАНИЕ
- 5.2. АЦИЛИРОВАНИЕ
- 5.3. ГАЛОГЕНИРОВАНИЕ
- 5.4. ГИДРОКСИЛИРОВАНИЕ
- 5.5. КАРБОНИЛИРОВАНИЕ (ВВЕДЕНИЕ КАРБОНИЛЬНОЙ ГРУППЫ)
- 5.6. КАРБОКСИЛИРОВАНИЕ
- 5.7. ЭПОКСИДИРОВАНИЕ (ОКСИРАНИРОВАИИЕ)
- 5.8. АМИНИРОВАНИЕ
- 5.9. ОКИСЛЕНИЕ
- 5.10. ВОССТАНОВЛЕНИЕ
- 5.11. АЛКАНЫ
- 5.12 АЛКЕНЫ
- 5.13. ДИЕНОВЫЕ УГЛЕВОДОРОДЫ (1,3-ДИЕНЫ)
- 5.14. АЦЕТИЛЕНЫ
- 5.15 АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- 5.16. ГАЛОГЕН АЛКАНЫ
- 5.17. СПИРТЫ
- 5.18. АЛЬДЕГИДЫ И КЕТОНЫ
- 5.19. КАРБОНОВЫЕ КИСЛОТЫ
- 5.20. ДИКАРБОНОВЫЕ КИСЛОТЫ
- 5.21. НЕПРЕДЕЛЬНЫЕ КИСЛОТЫ
- 5.22. КЕТО- И АЛЬДЕГИДОКИСЛОТЫ (ОКСОКИСЛОТЫ)
- 5.23. ОКСИКИСЛОТЫ
- 5.24. АМИНОКИСЛОТЫ
- 5.25 СИНТЕЗ АСИММЕТРИЧЕСКИХ СОЕДИНЕНИЙ
- 6. Некоторые понятия физической органической химии
- 6.1. СВЯЗЬ СОСТАВА И СТРОЕНИЯ СОЕДИНЕНИЙ С ФИЗИЧЕСКИМИ СВОЙСТВАМИ
- 6.2. ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 6.3. КИСЛОТЫ И ОСНОВАНИЯ В ОРГАНИЧЕСКОЙ ХИМИИ
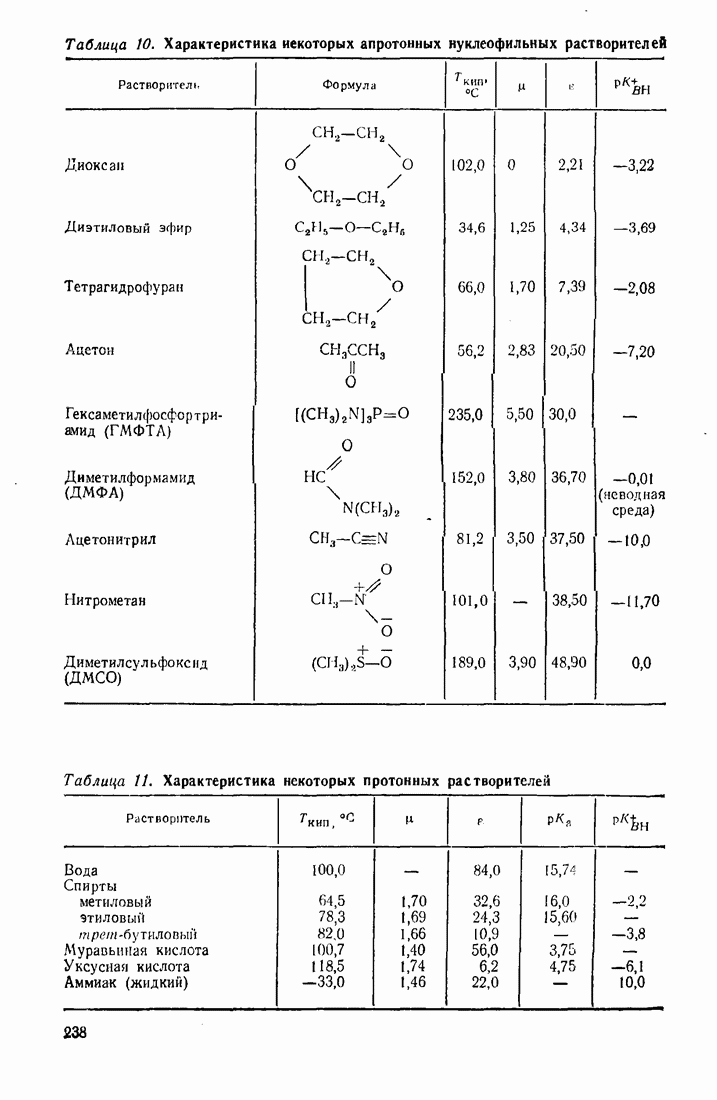
- 6.4. ОРГАНИЧЕСКИЕ РАСТВОРИТЕЛИ И ИХ ВЛИЯНИЕ НА СКОРОСТЬ И МЕХАНИЗМ РЕАКЦИЙ
- 6.5. КАТАЛИЗ ОРГАНИЧЕСКИХ РЕАКЦИЙ
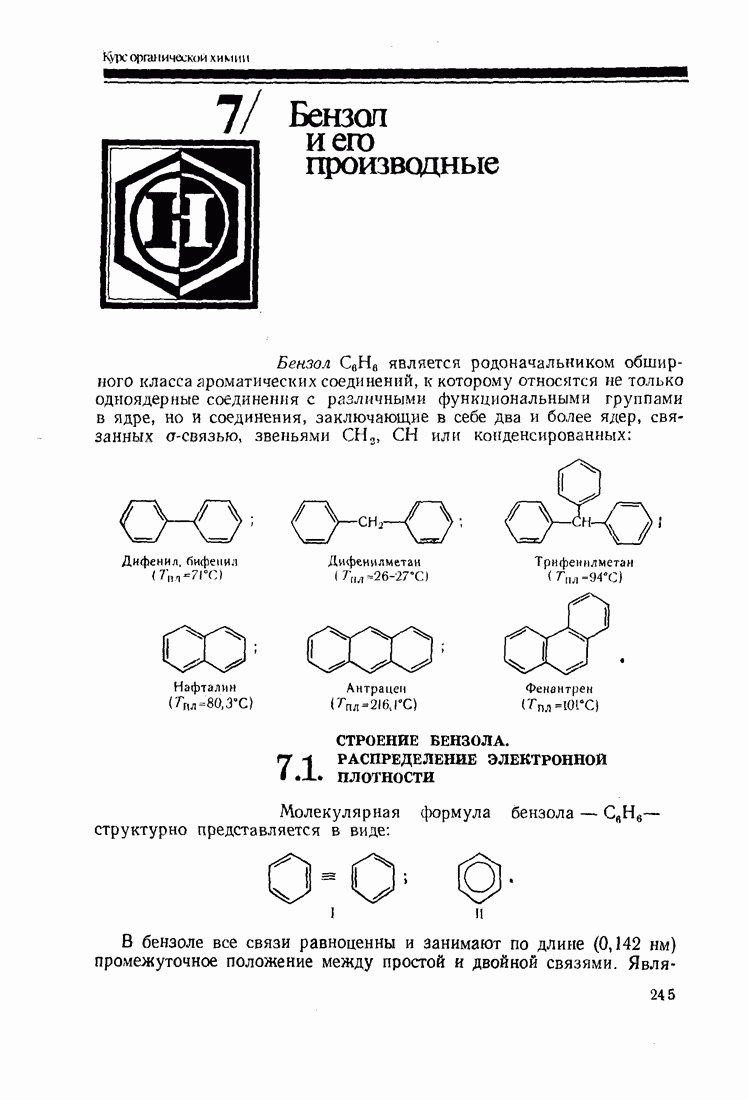
- 7. Бензол и его производные
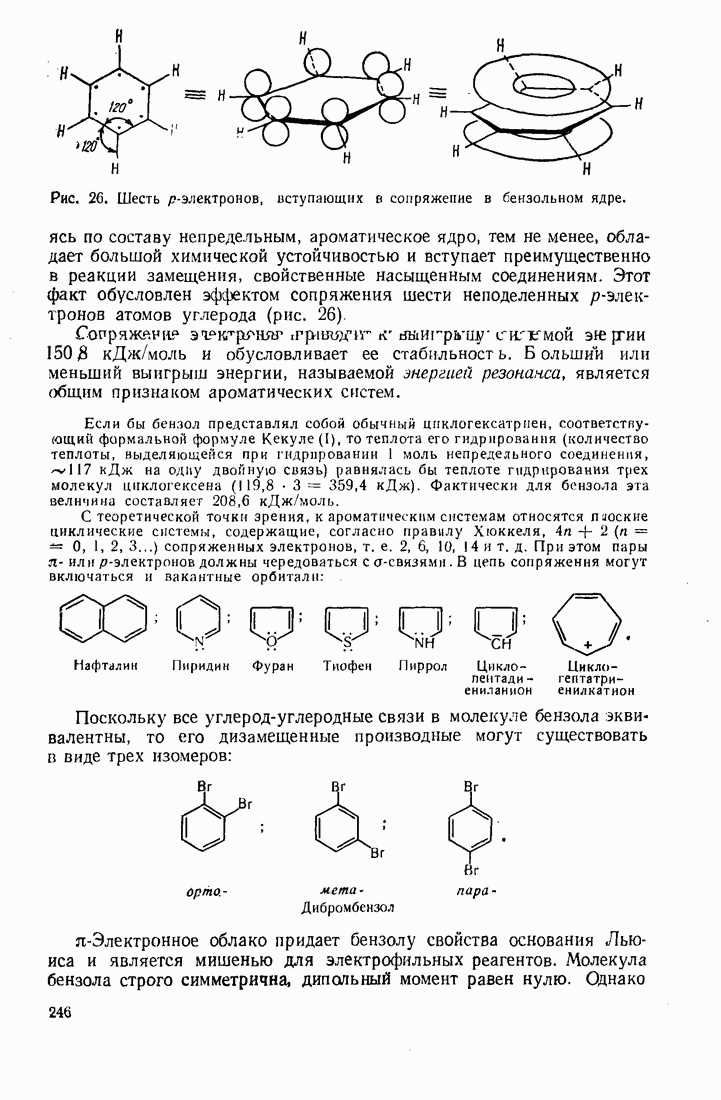
- 7.1. СТРОЕНИЕ БЕНЗОЛА. РАСПРЕДЕЛЕНИЕ ЭЛЕКТРОННОЙ ПЛОТНОСТИ
- 7.2. ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ В БЕНЗОЛЬНОМ ЯДРЕ
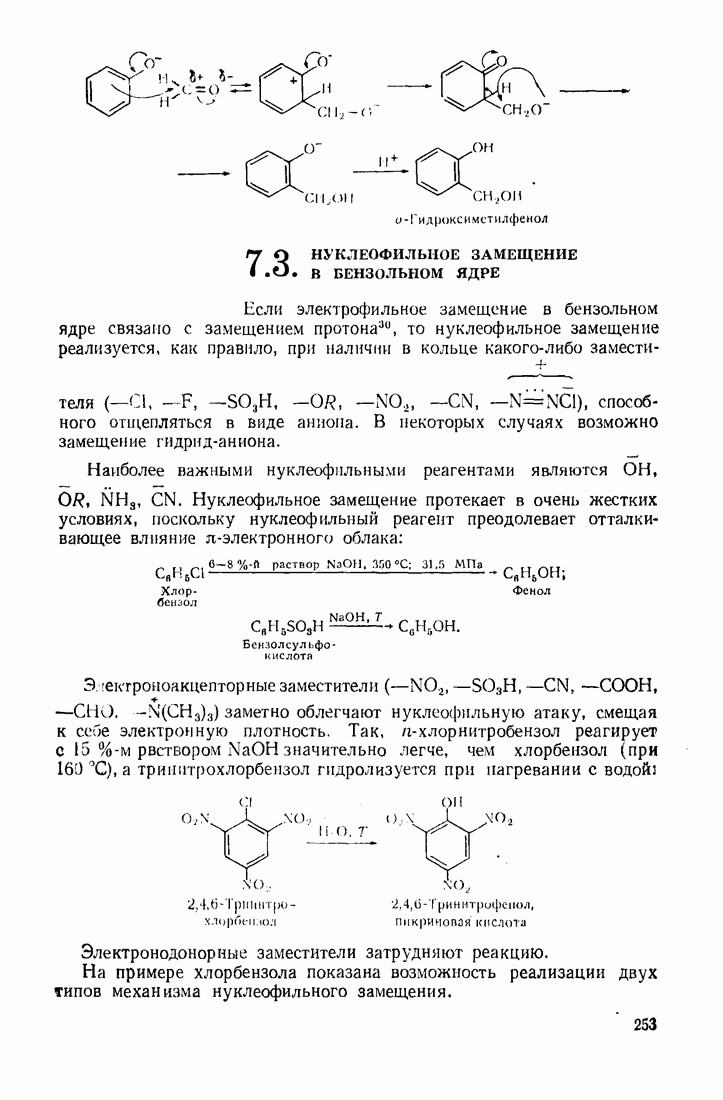
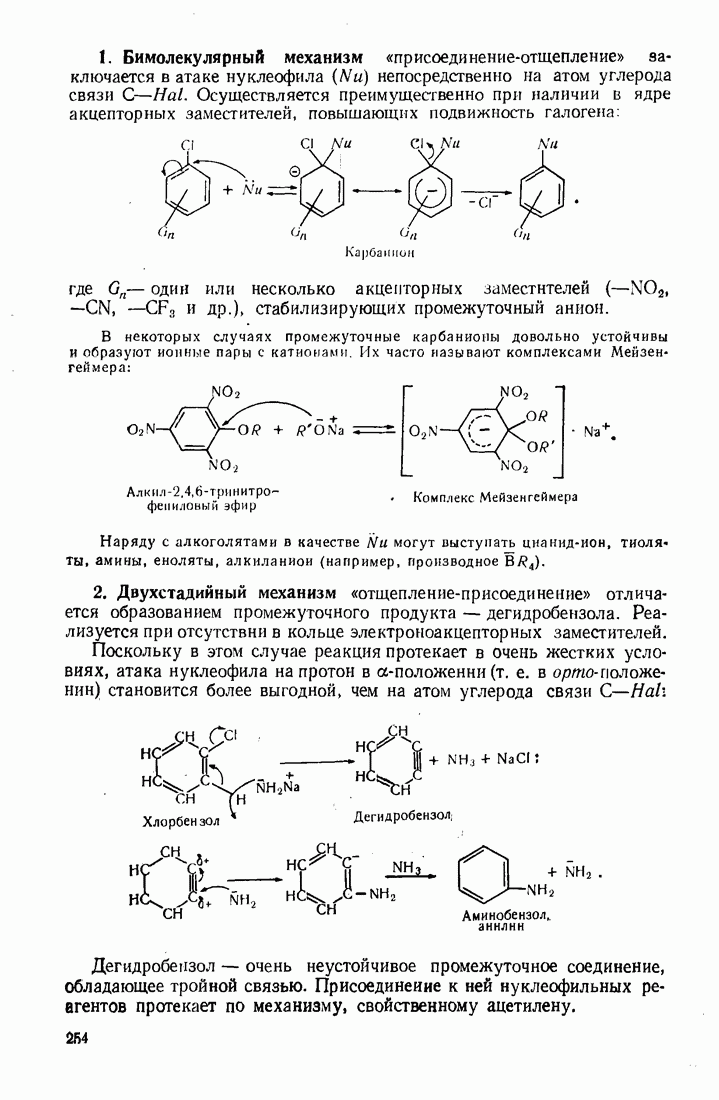
- 7.3. НУКЛЕОФИЛЬНОЕ ЗАМЕЩЕНИЕ В БЕНЗОЛЬНОМ ЯДРЕ
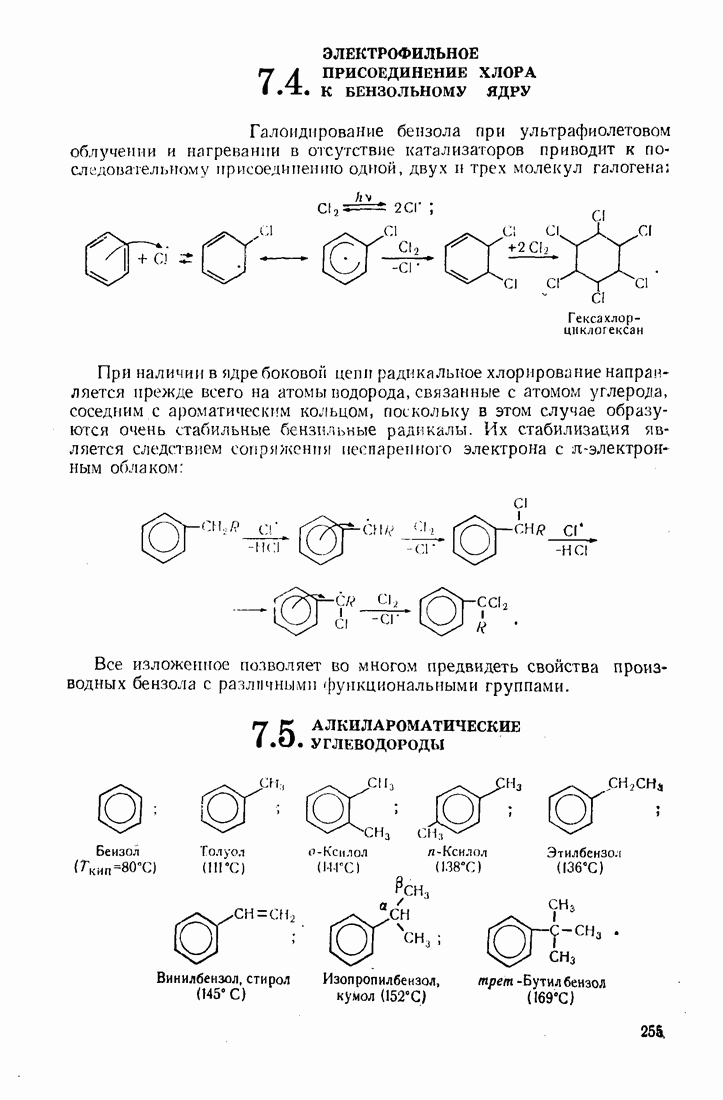
- 7.4. ЭЛЕКТРОФИЛЬНОЕ ПРИСОЕДИНЕНИЕ ХЛОРА К БЕНЗОЛЬНОМУ ЯДРУ
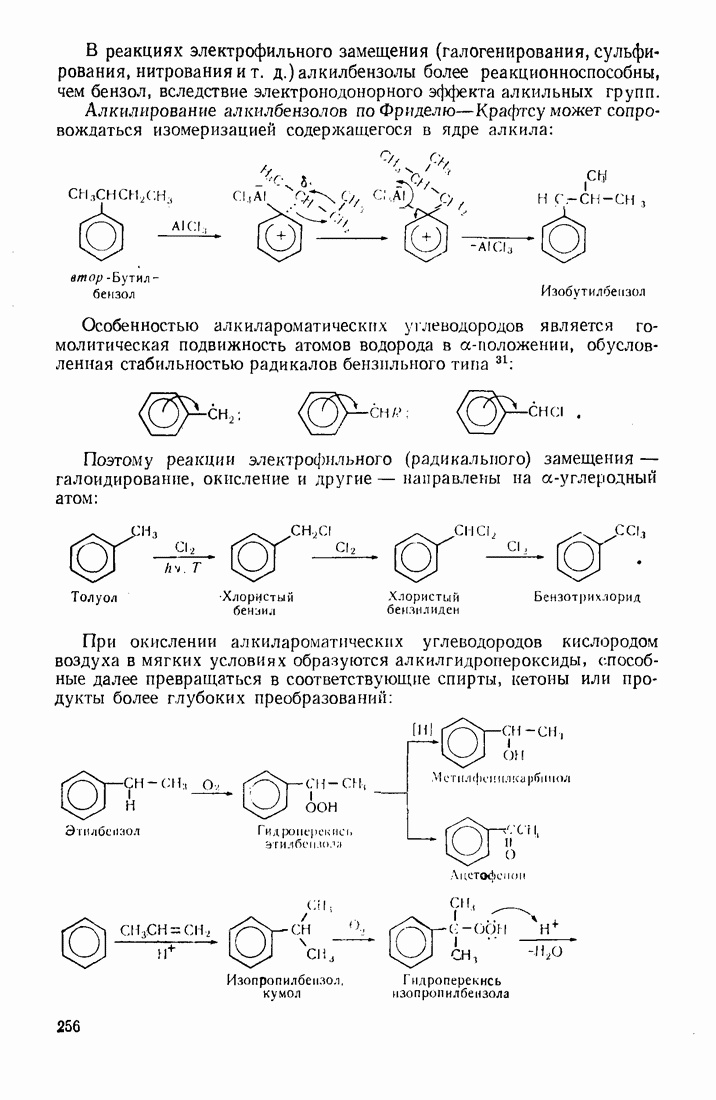
- 7.5. АЛКИЛАРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ
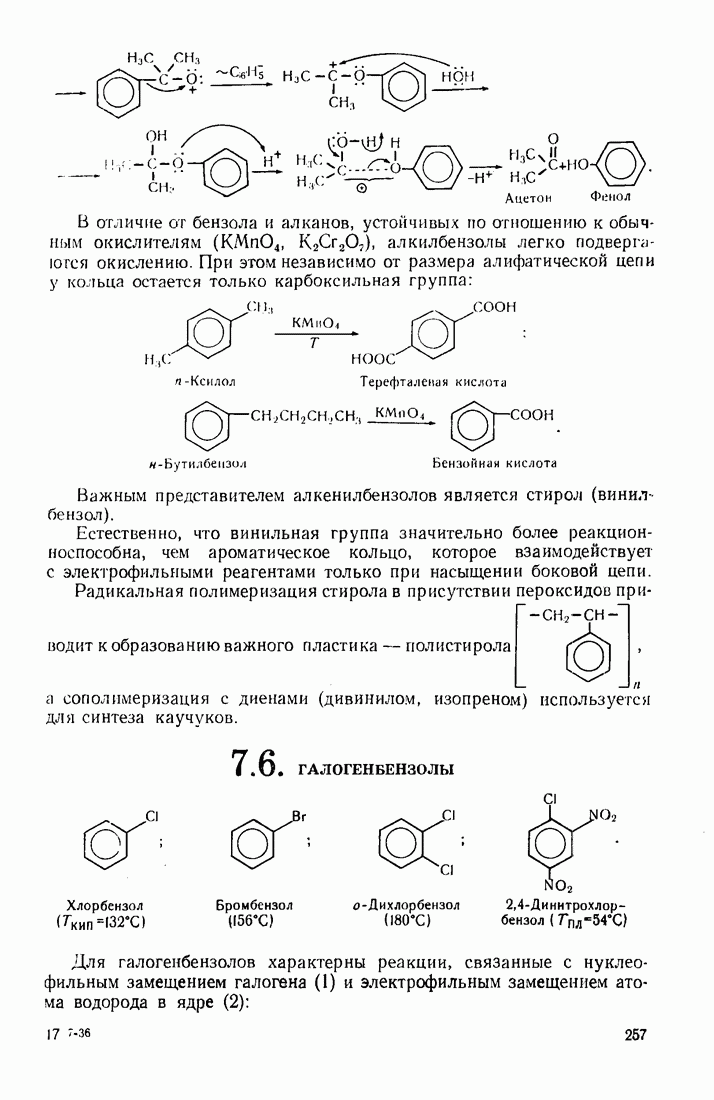
- 7.6. ГАЛОГЕНБЕНЗОЛЫ
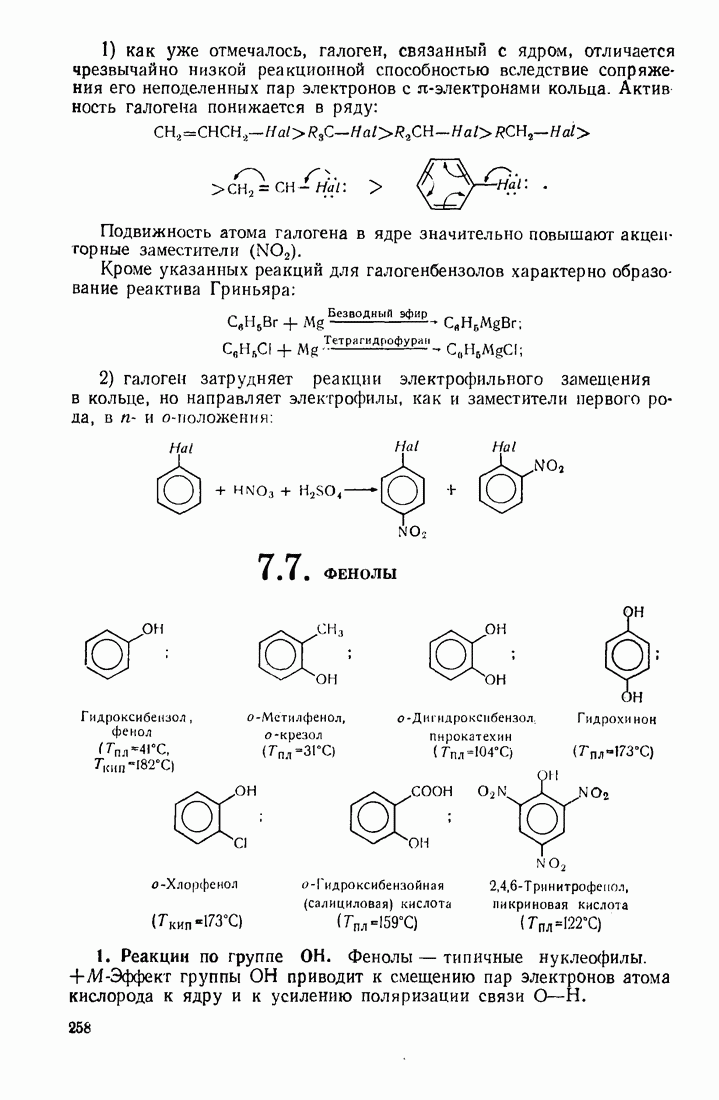
- 7.7. ФЕНОЛЫ
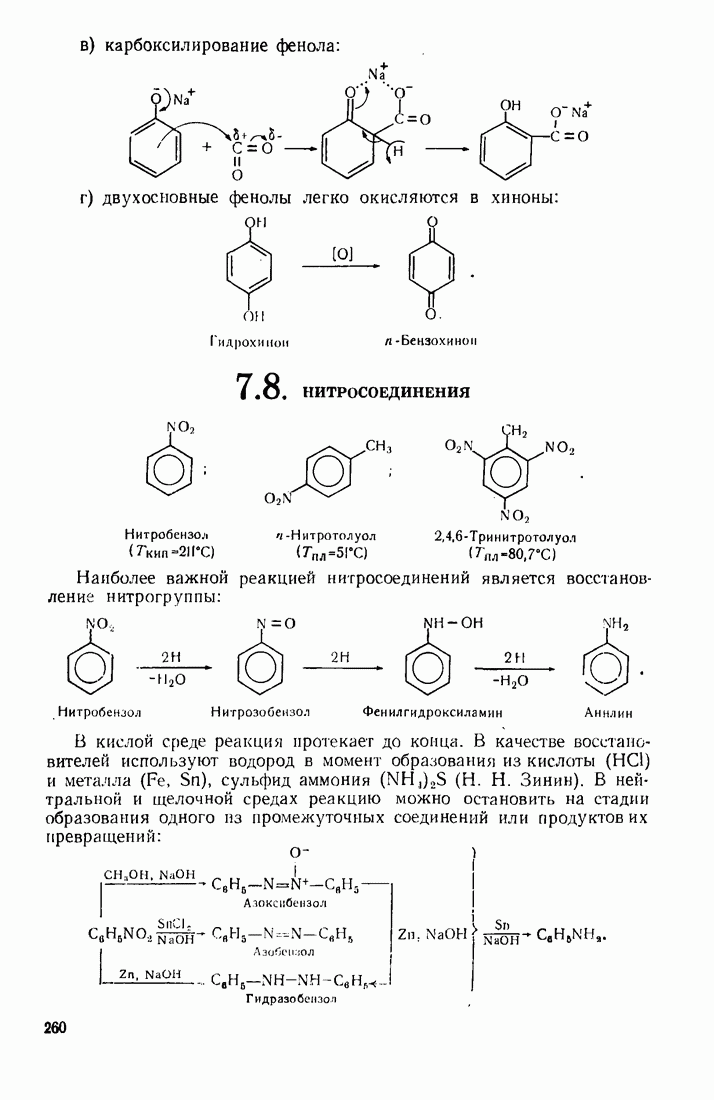
- 7.8. НИТРОСОЕД ИНЕНИЯ
- 7.9. АРОМАТИЧЕСКИЕ АМИНЫ
- 7.10. ДИАЗОСОЕДИНЕНИЯ
- 7.11. АЗОСОЕДИНЕНИЯ
- 7.12. СУЛЬФОКИСЛОТЫ
- 7.13. АЛЬДЕГИДЫ И КЕТОНЫ
- 8. Многоядерные ароматические соединения
- 8.1. СОЕДИНЕНИЯ С ИЗОЛИРОВАННЫМИ БЕНЗОЛЬНЫМИ ЯДРАМИ
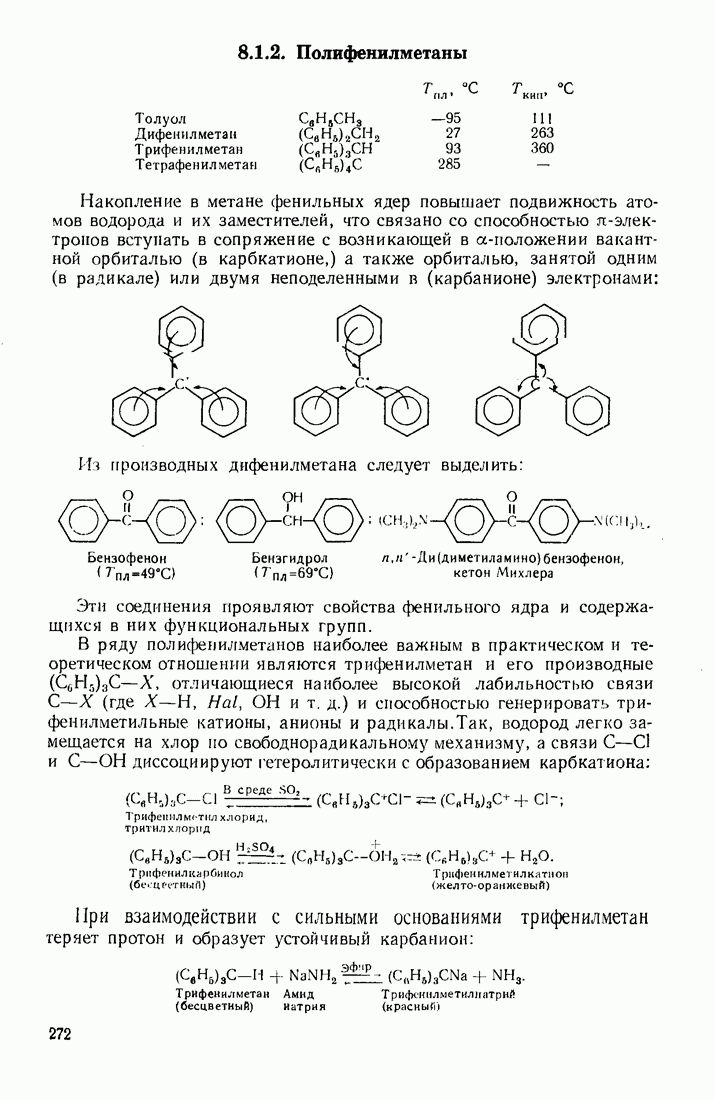
- 8.1.2. Полифенилметаны
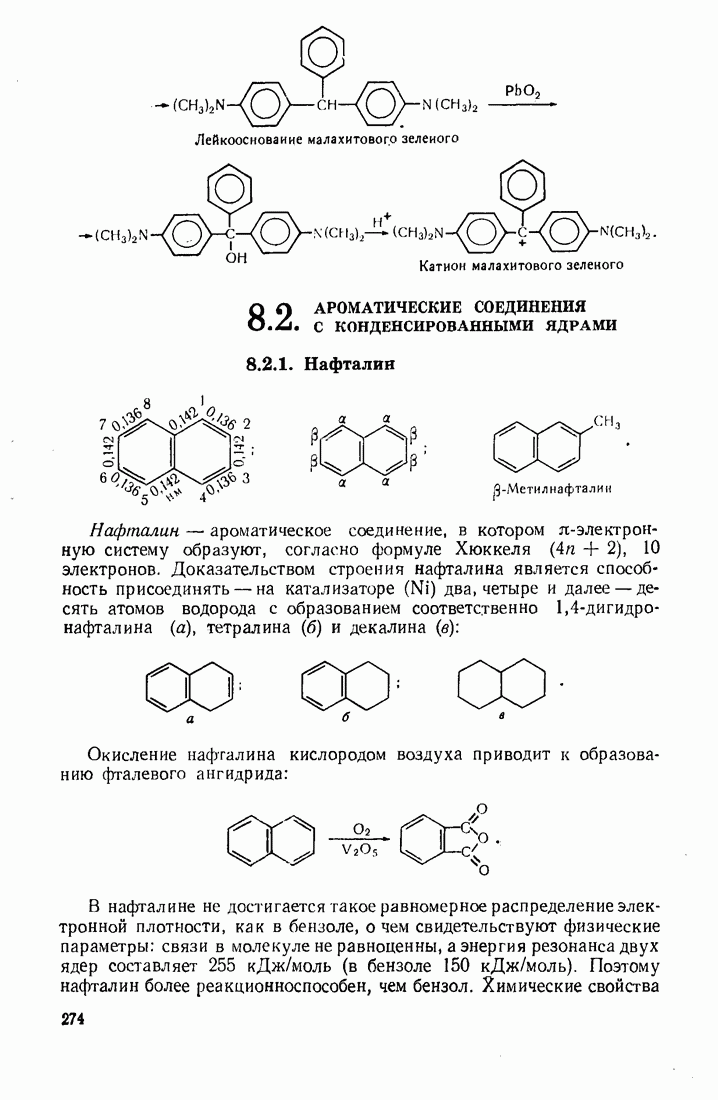
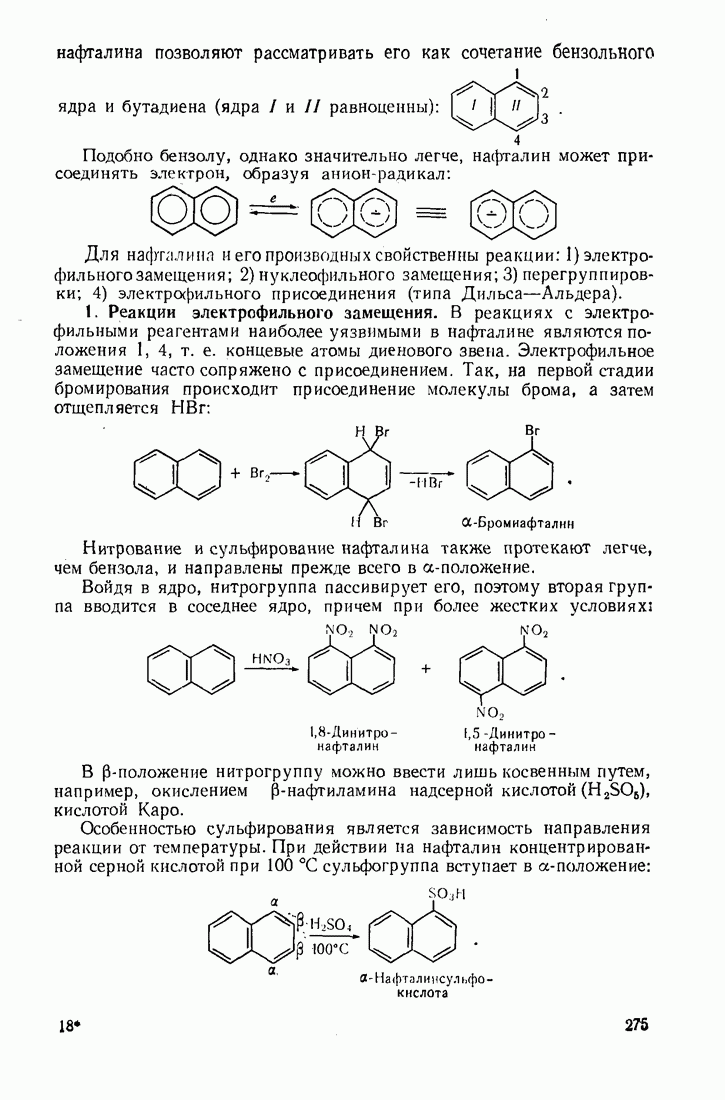
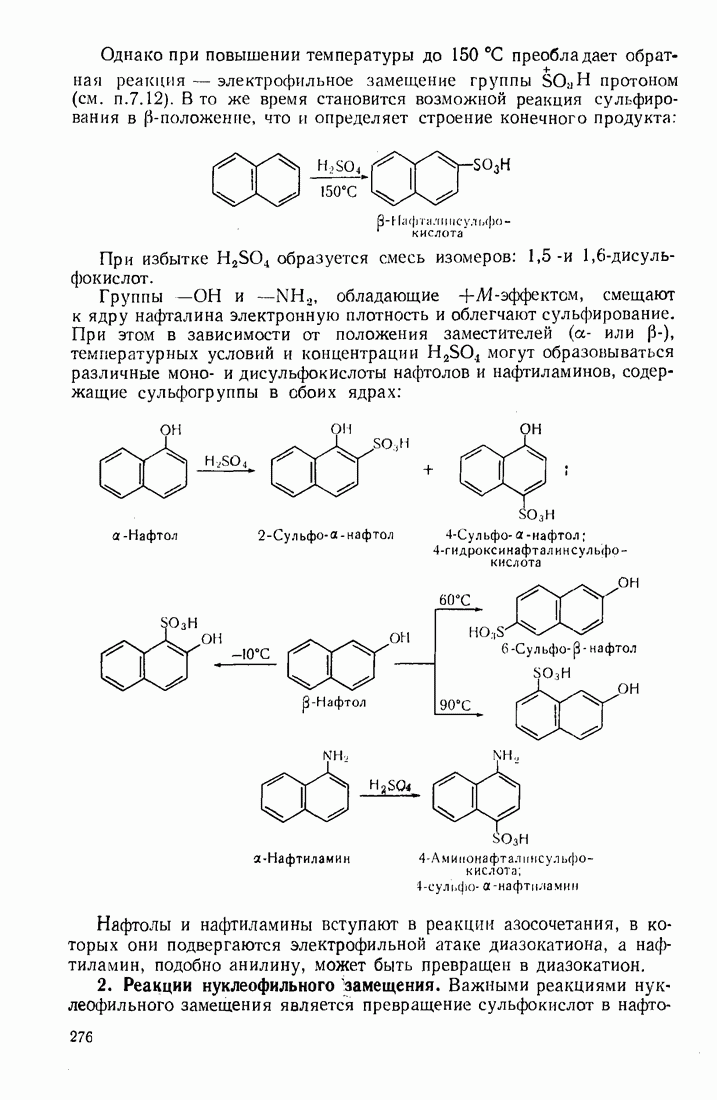
- 8.2. АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ С КОНДЕНСИРОВАННЫМИ ЯДРАМИ
- 8.2.2. Антрацен
- 8.2.3. Фенантрен
- 9. Методы синтеза в ряду ароматических соединений
- 9.1. ГАЛОГЕНИРОВАНИЕ
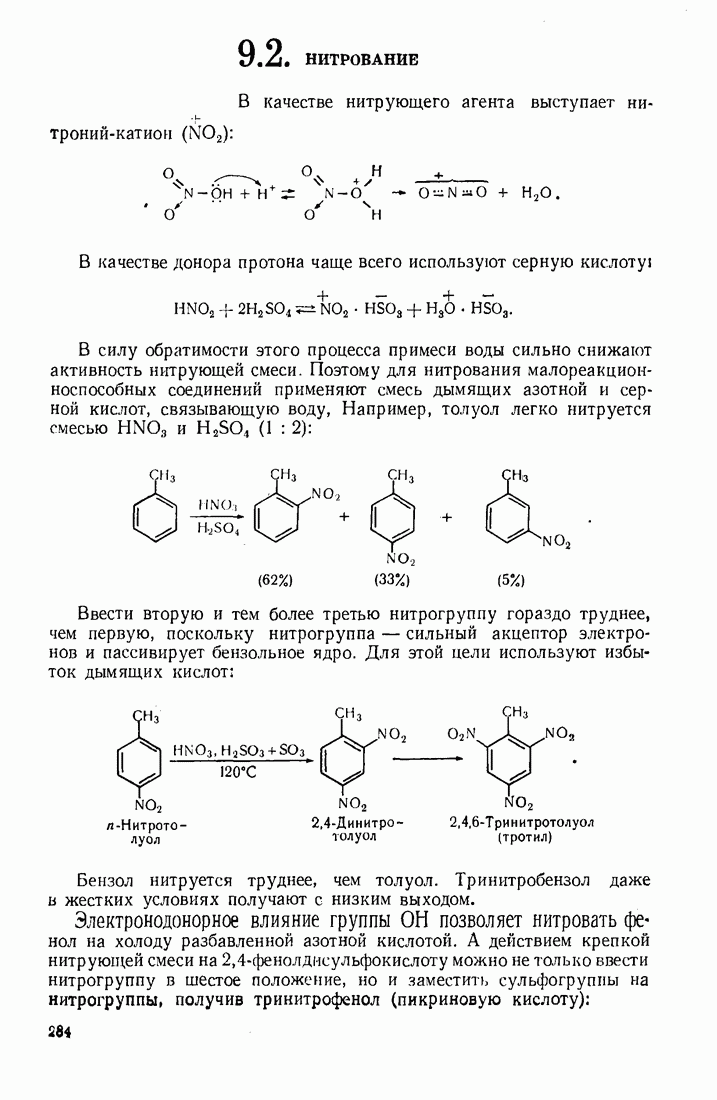
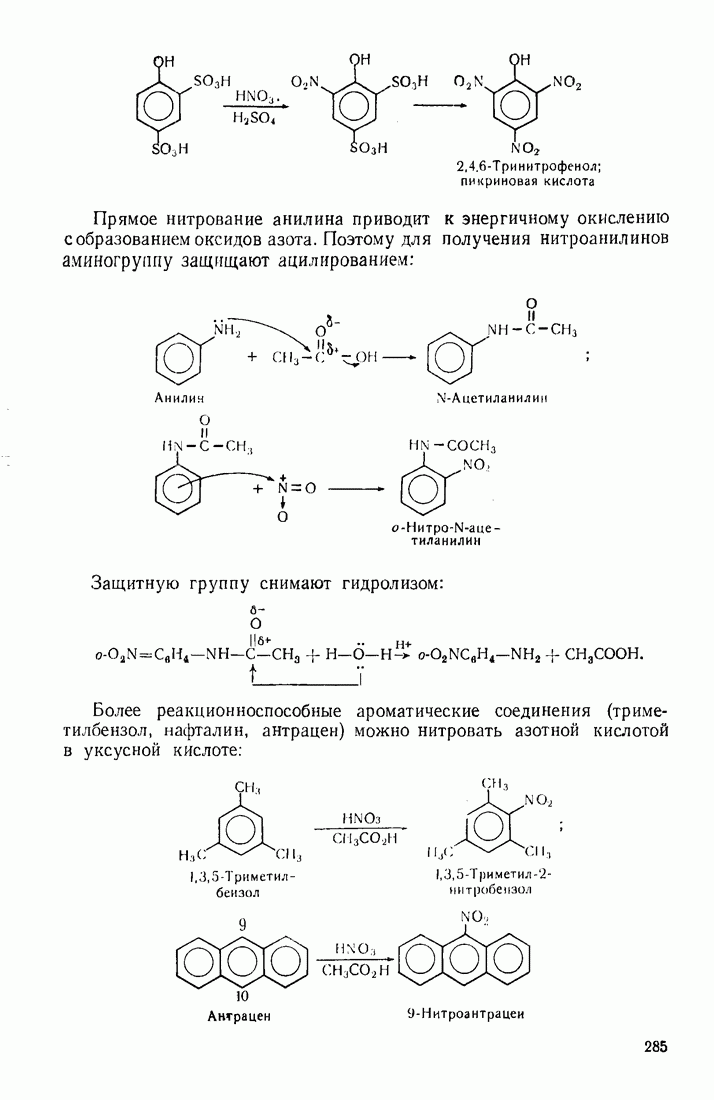
- 9.2. НИТРОВАНИЕ
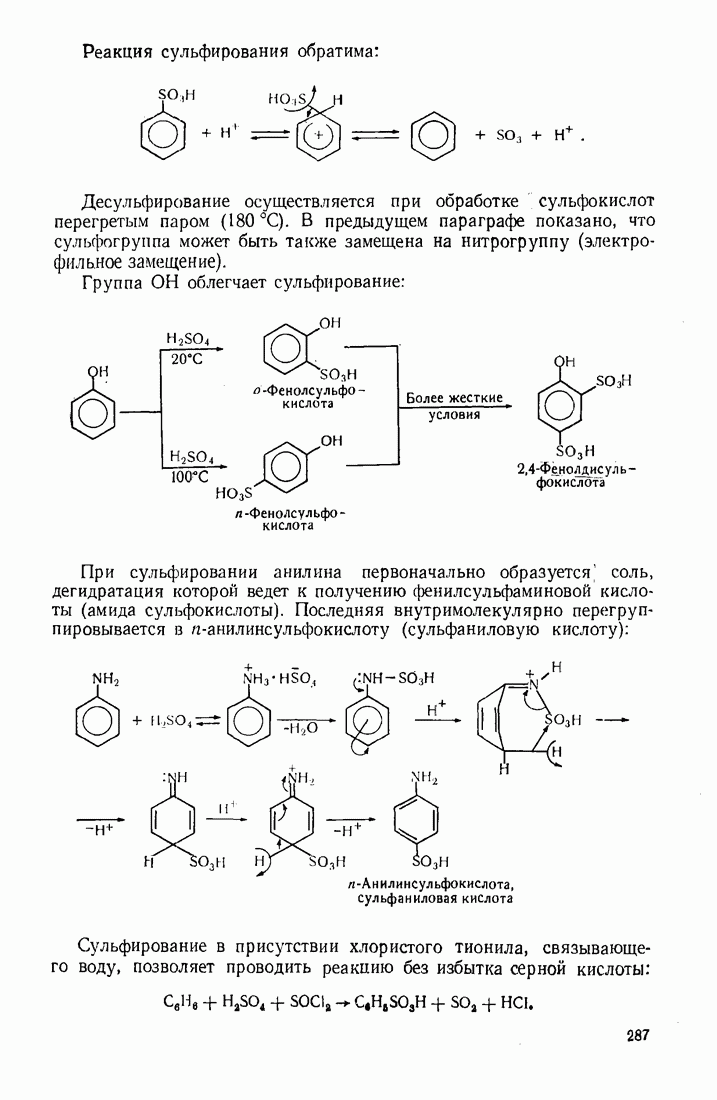
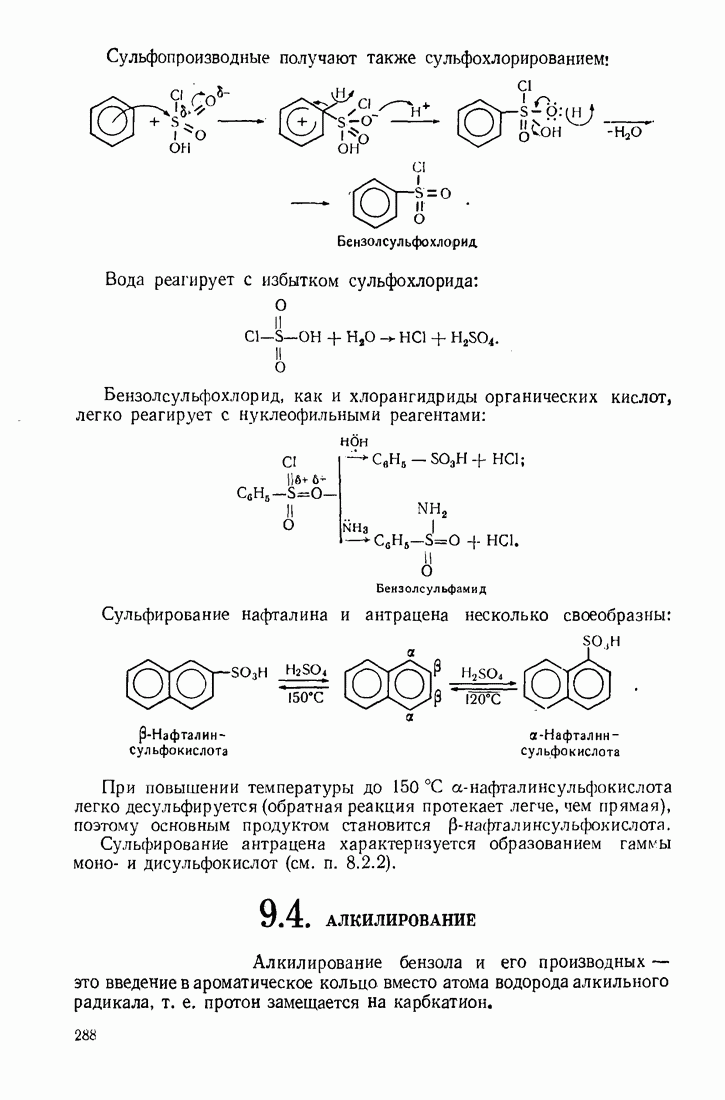
- 9.3. СУЛЬФИРОВАНИЕ
- 9.4. АЛКИЛИРОВАНИЕ
- 9.5. АЦИЛИРОВАНИЕ
- 9.6. ГИДРОКСИЛИРОВАНИЕ
- 9.7. АМИНИРОВАНИЕ
- 9.8. НИТРОЗИРОВАНИЕ
- 9.9. КАРБОНИЛИРОВАНИЕ
- 9.10. КАРБОКСИЛИРОВАНИЕ
- 9.11. ОКИСЛЕНИЕ
- 9.12. ВОССТАНОВЛЕНИЕ
- 10. Гетероциклические соединения
- 10.2. ОБЩАЯ ХАРАКТЕРИСТИКА СТРОЕНИЯ И РЕАКЦИОННОЙ СПОСОБНОСТИ
- 10.3. ПЯТИ- И ШЕСТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С ОДНИМ ГЕТЕРОАТОМОМ
- 10.4. ГЕТЕРОЦИКЛЫ С НЕСКОЛЬКИМИ ГЕТЕРОАТОМАМИ
- 10.5. МЕТОДЫ СИНТЕЗА ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ
- 10.6. П0НЯТИЕ О ПРИРОДНЫХ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЯХ
- 11. Зпементоорганические соединения
- 11.2. ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ НЕКОТОРЫХ НЕМЕТАЛЛОВ
- 11.3. МЕГАЛЛООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- 11.4. ОРГАНИЧЕСКИЕ ПРОИЗВОДНЫЕ ПЕРЕХОДНЫХ МЕТАЛЛОВ
- 12. Сырье и основные направления развития промышленности органического синтеза
- 12.1.1. Нефть и сопутствующий природный газ
- 12.1.2. Углехимическое сырье
- 12.1.3. Лесохимическое и сельскохозяйственное сырье
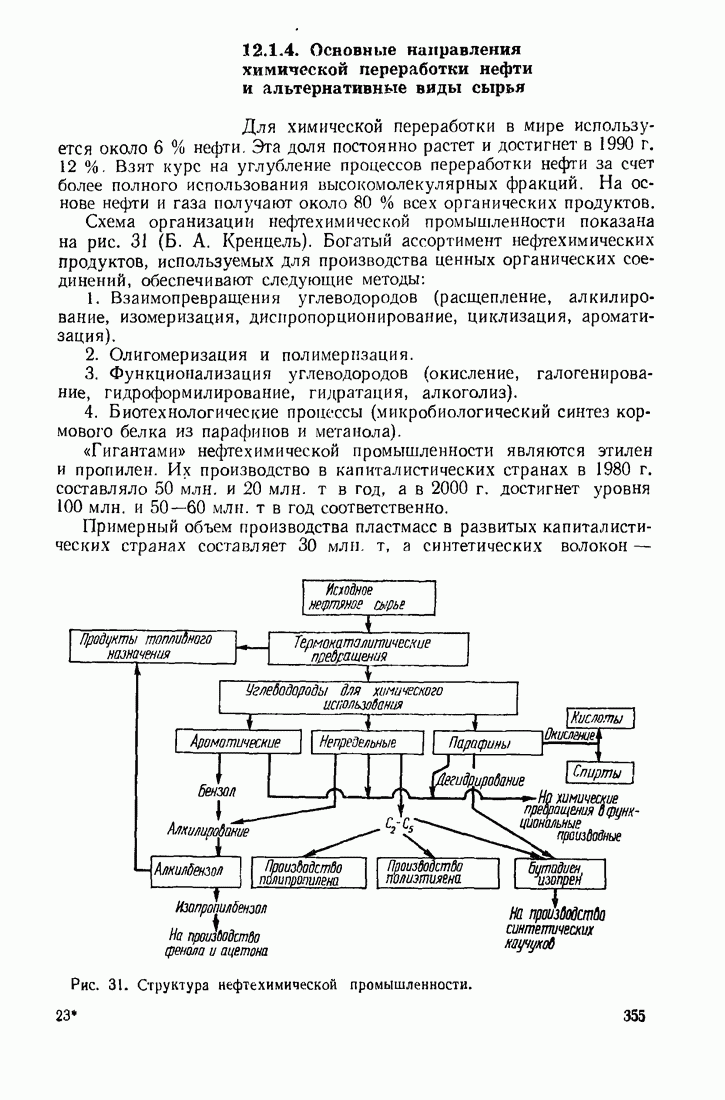
- 12.1.4. Основные направления химической переработки нефти и альтернативные виды сырья
- 12.2. ПУТИ ИСПОЛЬЗОВАНИЯ УГЛЕВОДОРОДОВ И ИХ ПРОИЗВОДНЫХ
- 12.3. РАЗВИТИЕ ХИМИЧЕСКОЙ ПРОМЫШЛЕННОСТИ В СССР В ДВЕНАДЦАТОЙ ПЯТИЛЕТКЕ