| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
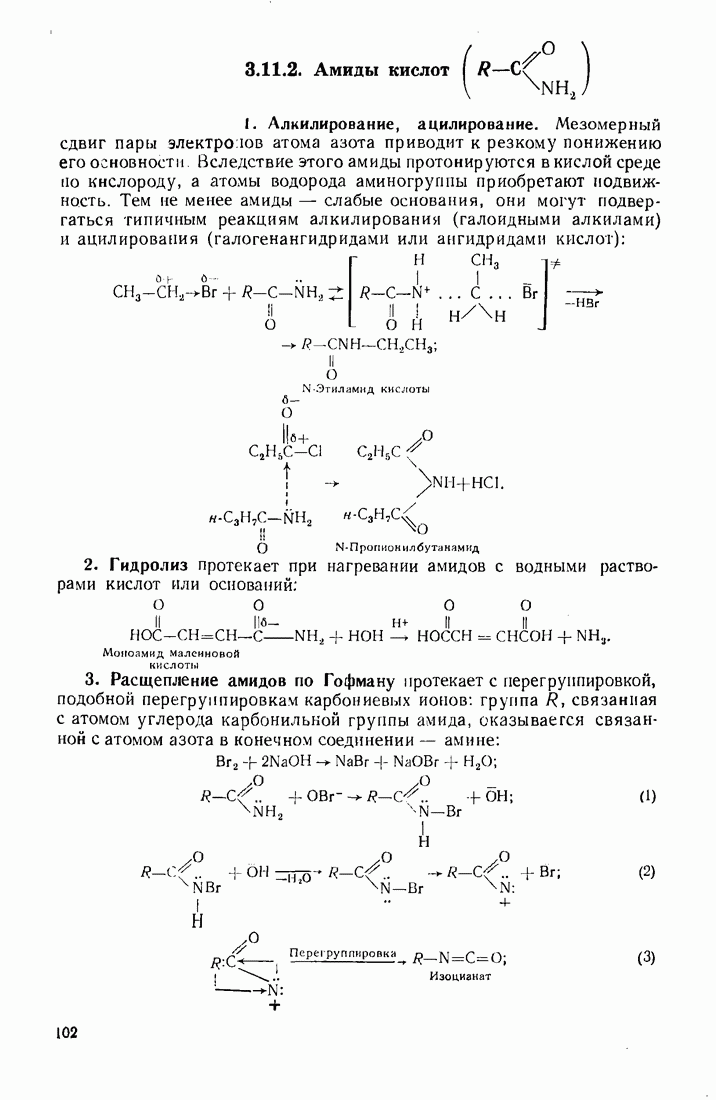
2 Общие теоретические положения органической химии
2.1. Природа химической связи
До развития квантовомеханических представлений (до 30-х гг. XX в.) в теории связи господствовал метод локализованных электронных пар, классифицирующий связи как ионные, ковалентные и координационные (семиполярные) (В. Коссель, Г. Льюис). Согласно теории Льюиса, элементы образуют связи до заполнения внешней оболочки и образования устойчивого октета электронов. Это правило соблюдается, однако, лишь для элементов периодической системы от бора до фтора. Кремний, фосфор и сера могут иметь на внешней оболочке до 12 электронов 
С развитием квантовомеханических представлений о природе электрона и атома в теории химической связи сложились два метода: валентных связей (ВС-метод) и молекулярных орбиталей (МО-метод)
Как известно, электрон имеет одновременно корпускулярную и волновую природу. Согласно принципу неопределенности В. Гейзенберга, нельзя определить местоположение электрона в данный момент. Можно говорить лишь о вероятности пребывания электрона в определенном элементе объема вокруг ядра атома, называемом электронным облаком, пли атомной орбиталыо  Если электрон описать волновой функцией
Если электрон описать волновой функцией  то вероятность его обнаружения в объеме
то вероятность его обнаружения в объеме  будет равна
будет равна 
Конфигурация АО (приближенная граничная поверхность) определяется ее типом: s, р, d и т. д. (рис. 1).
Метод валентных связей (метод ВС) сохранил некоторые черты теории Льюиса о локализированной химической связи. Согласно этому методу, атомы, составляющие молекулу, сохраняют свою индивидуальность, а связи возникаюг в результате взаимодействия их валентных электронов, т. е. атомных орбиталей. Это взаимодействие выражается набором схем спаривания электронов. Например, атомы  могут образовывать ковалентную структуру
могут образовывать ковалентную структуру  и ионные структуры
и ионные структуры  и Полная волновая функция, характеризующая электронное состояние молекулы
и Полная волновая функция, характеризующая электронное состояние молекулы  представляет собой сумму волновых функций всех структур. С точки зрения теории резонанса, получившей развитие в рамках метода
представляет собой сумму волновых функций всех структур. С точки зрения теории резонанса, получившей развитие в рамках метода  реальное электронное
реальное электронное
состояние молекулы А В является результатом наложения гипотетических предельных  и
и  В упрощенном варианте метода ВС электронное строение молекулы часто представляется одной структурой (приближение идеального спаривания). Эту задачу облегчило развитие концепции гибридизации атомных орбиталей (см. п. 2.1.1)
В упрощенном варианте метода ВС электронное строение молекулы часто представляется одной структурой (приближение идеального спаривания). Эту задачу облегчило развитие концепции гибридизации атомных орбиталей (см. п. 2.1.1)
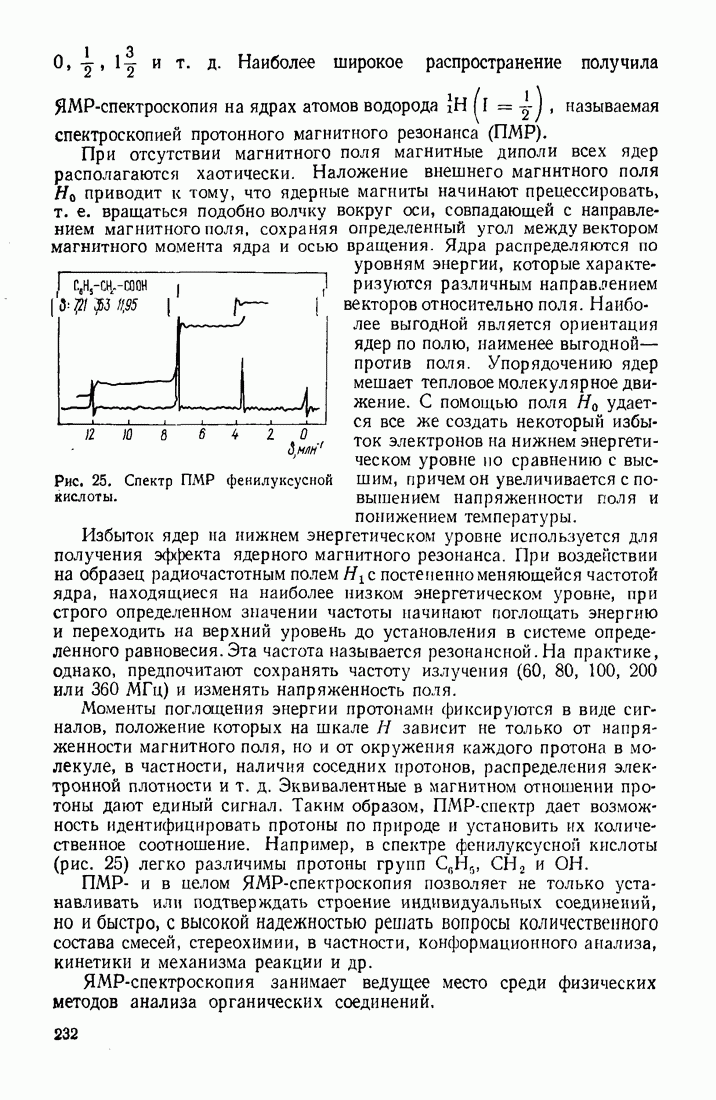
Молекулу бензола можно удовлетворительно описать двумя структурами Кекуле В ряде случаев, если химическая связь делокализо вана между тремя и большим числом атомов, весьма полезным становится учет нескольких резонансных структур,

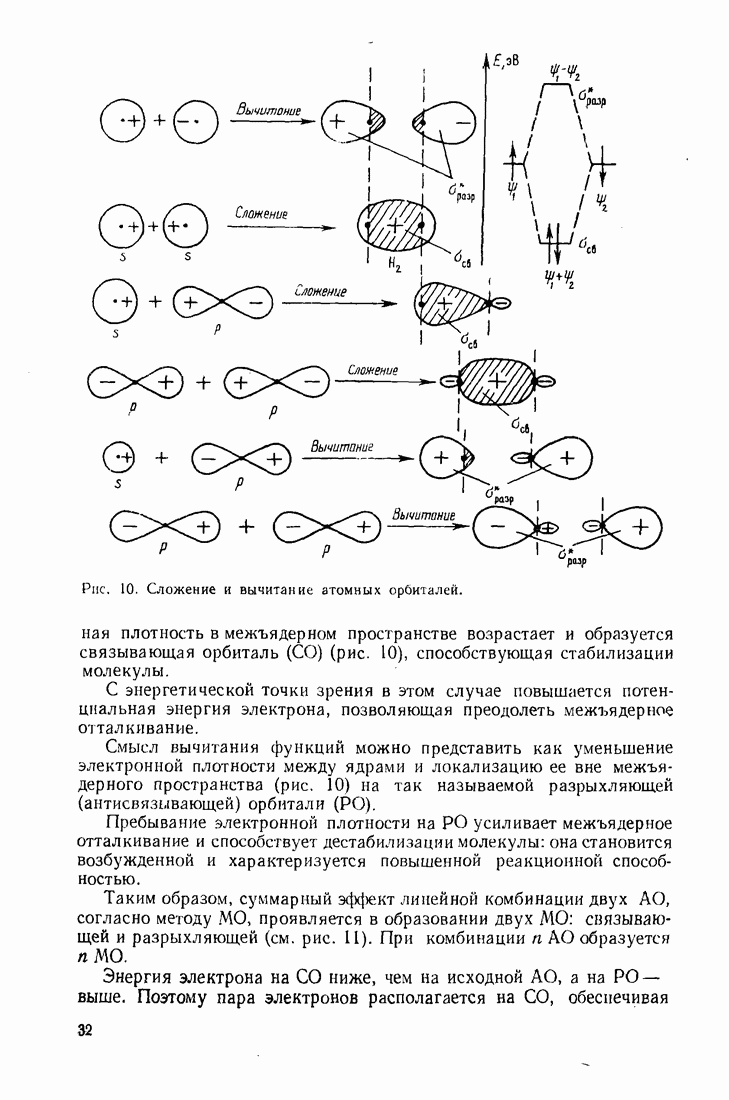
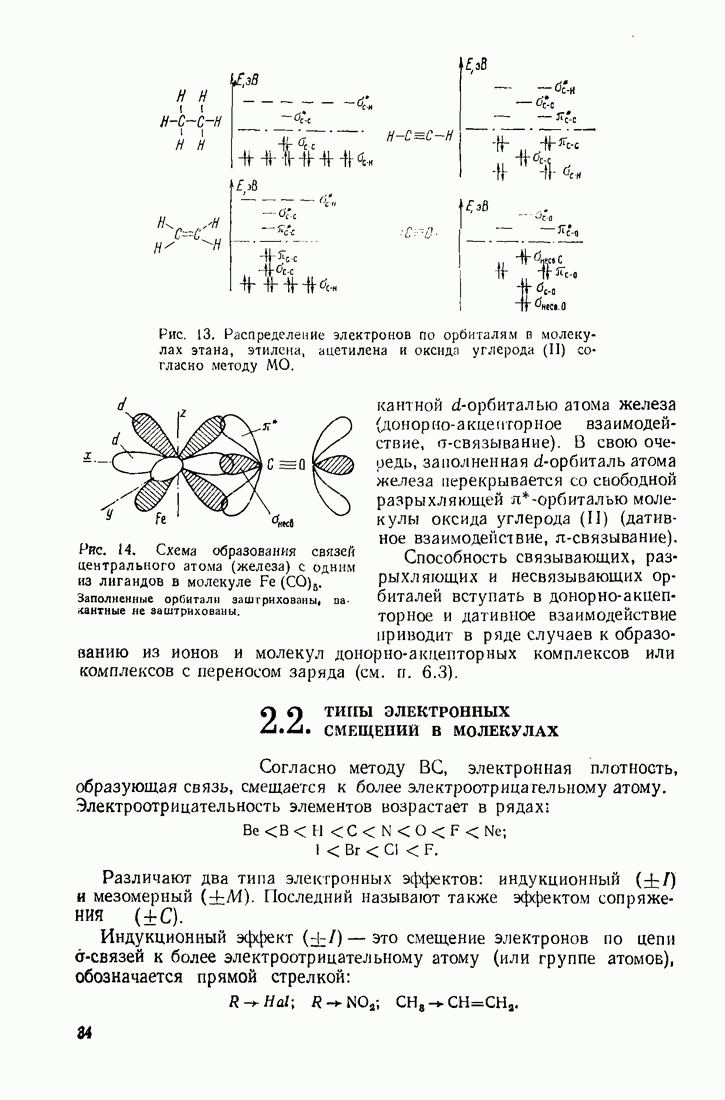
Рис. 1. Атомные орбитали: а — распределение электронов на атомных орбиталях (АО) атома углерода; б - конфигурация электронных облакоп (АО); в — схематическое изображение АО; г - функции описывающие 
Согласно методу молекулярных орбиталей, молекула представляет собой не простую совокупность индивидуальных атомов, а самостоятельное целое — каждый электрон принадлежит молекуле в целом и движется в поле всех ее ядер и электронов. Охарактеризовать молекулу по методу МО - это значит распределить все электроны но молекулярным орбиталям (МО). МО подобно АО имеют приближенное математическое описание, характеризуются набором квантовых чисел и определенной энергией.
Основные принципы построения электронной конфигурации молекулы: 1) электрон занимает свободную орбиталь с наименьшей энергией; 2) на одной МО не может находиться более двух электронов; 3) при переходе хотя бы одного электрона с занятой на более высокую по энергии свободную МО молекула в целом переходит из основного состояния в возбужденное.
Методы ВС и МО, несмотрн на существенные различия в подходах к описанию молекул, хорошо дополняют друг друга. Во многих случаях они приводят в конечном итоге к одинаковым результатам.
Метод МО более пригоден для описания спектральных свойств молекул и фотохимических процессов, строения и свойств сопряженных и ароматических соединений, С помощью метода МО можно легко объяснить парамагнитные свойства кислорода, природу трехцентровых орбиталей, комплексов металла с различными лигандами и т. д.
В то же время метод ВС не потерял своего значения для химиков в связи с большей наглядностью рассматриваемой им физической модели молекулы. С развитием вычислительной техники метод ВС позволил производить сложные количественные расчеты многоатомных молекул, более точно описывать энергетику и механизм химических процессов.
Детальное рассмотрение методов ВС и МО с описанием математических моделей химических связей выходит за пределы настоящего курса. Ограничимся лишь кратким качественным описанием физических моделей химических связей и молекулярных орбиталей, представления о которых будут использоваться ниже для интерпретации строения и реакционной способности органических соединений.
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие
- 1. Введение
- 1.1. Предмет органической химии
- 1.2. Основные этапы развития органической химии
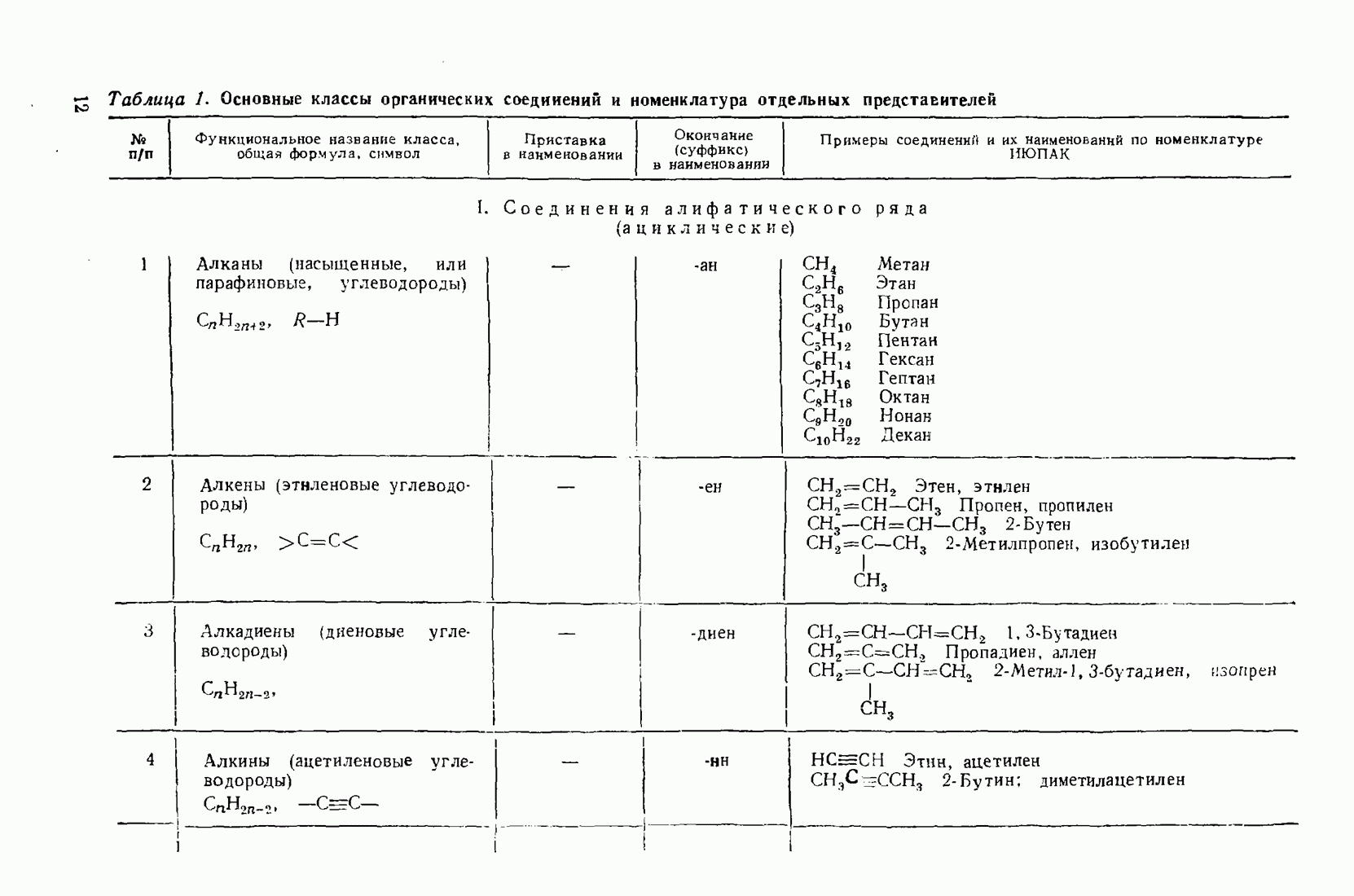
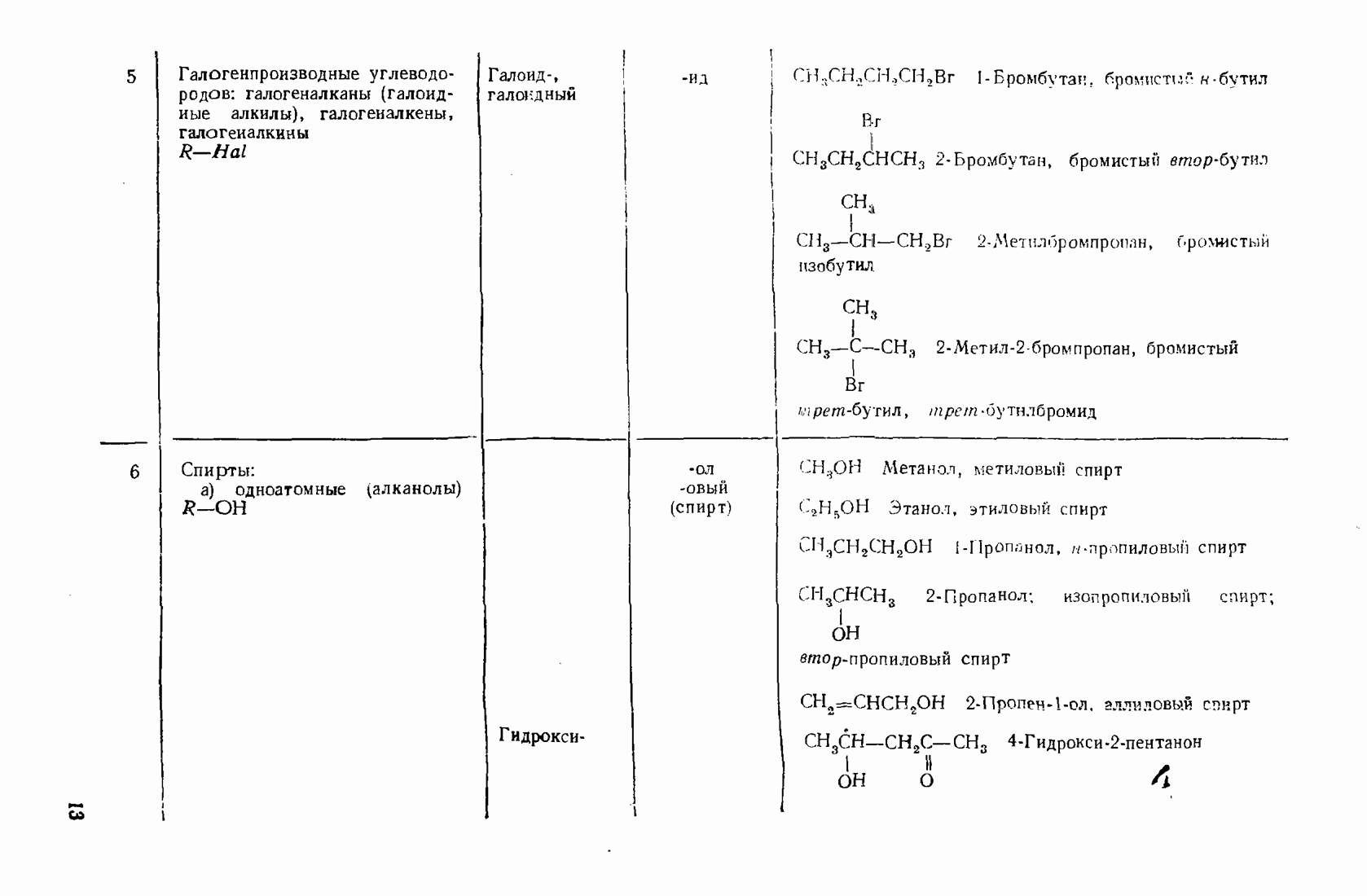
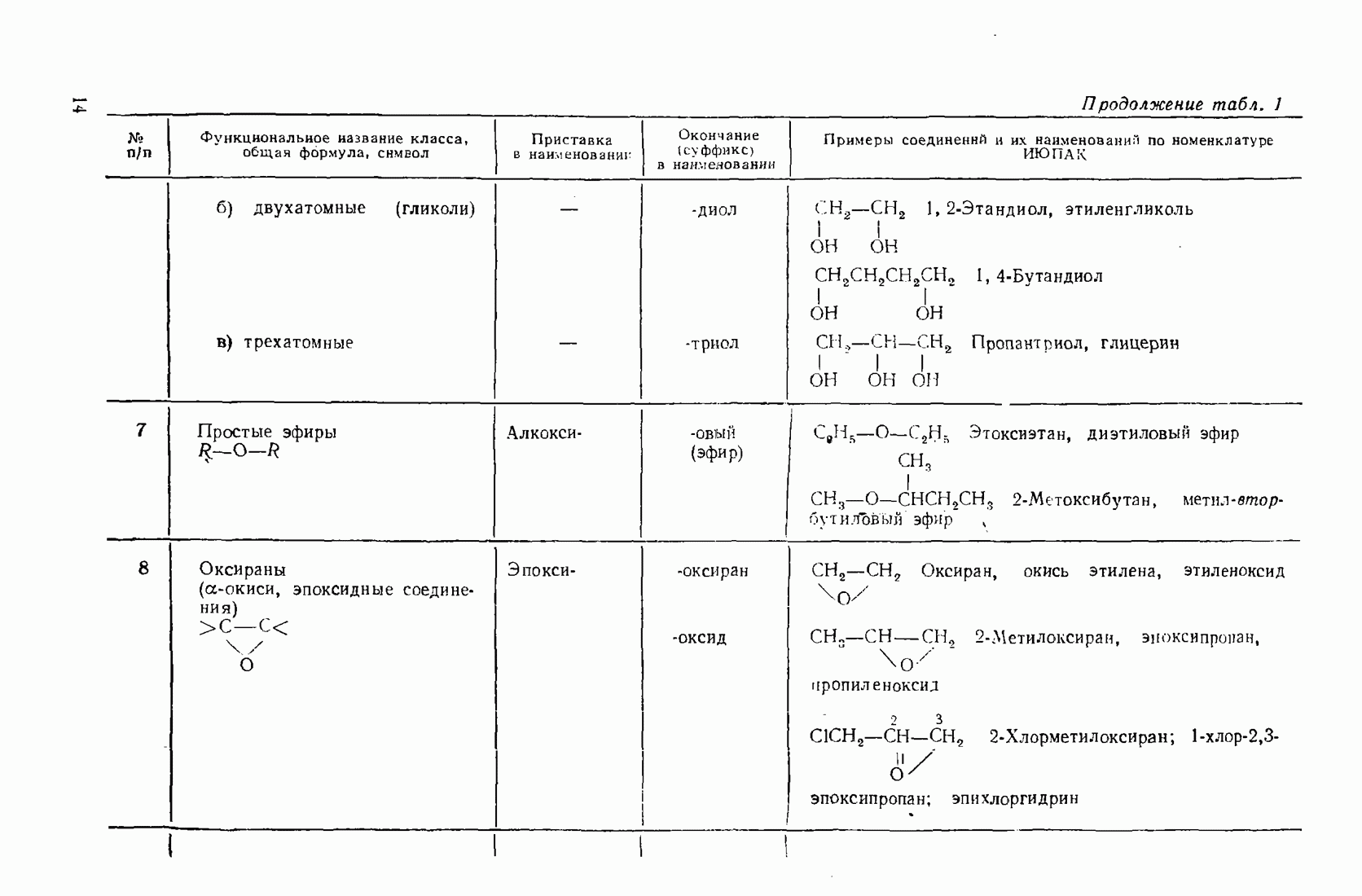
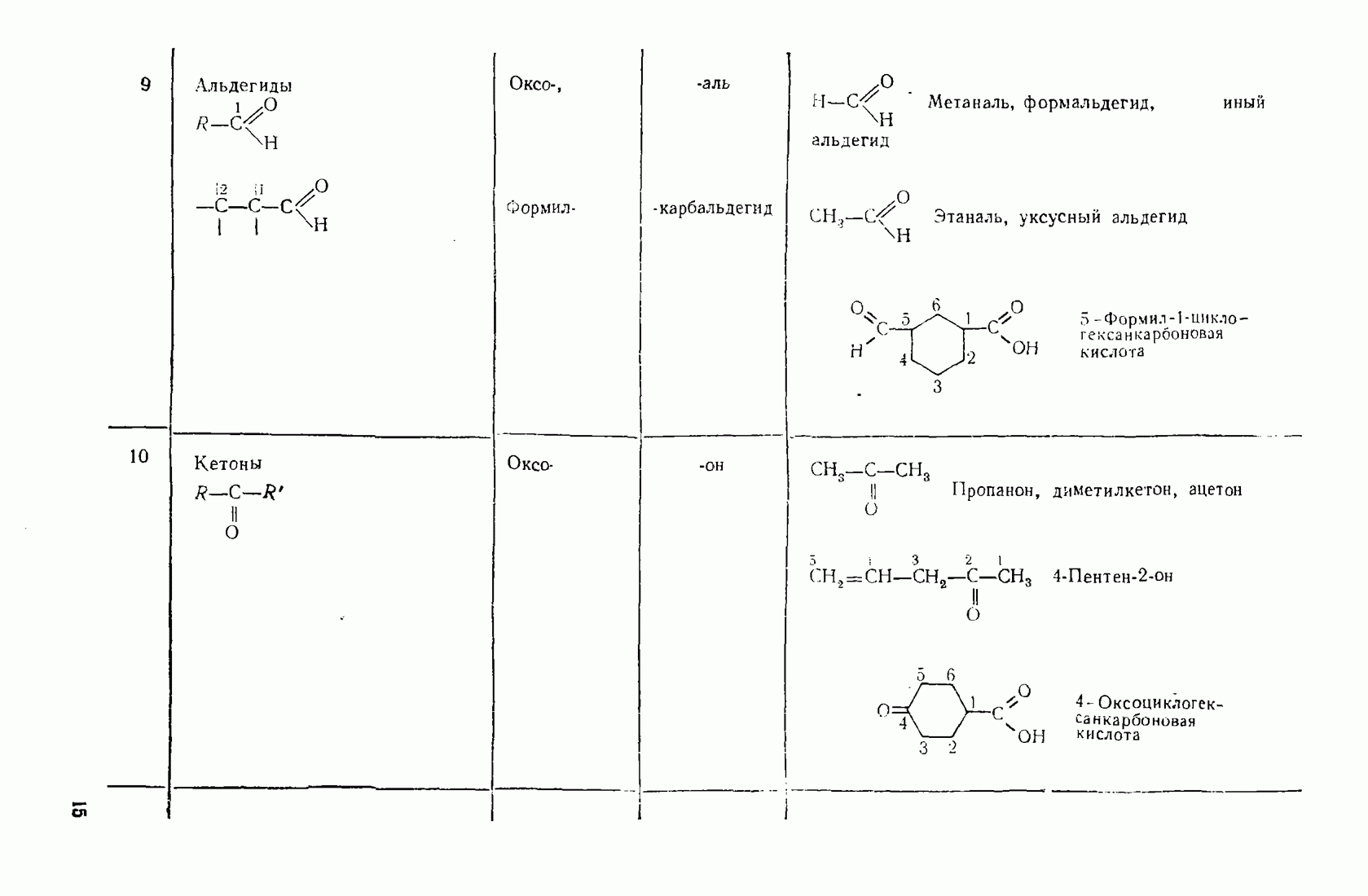
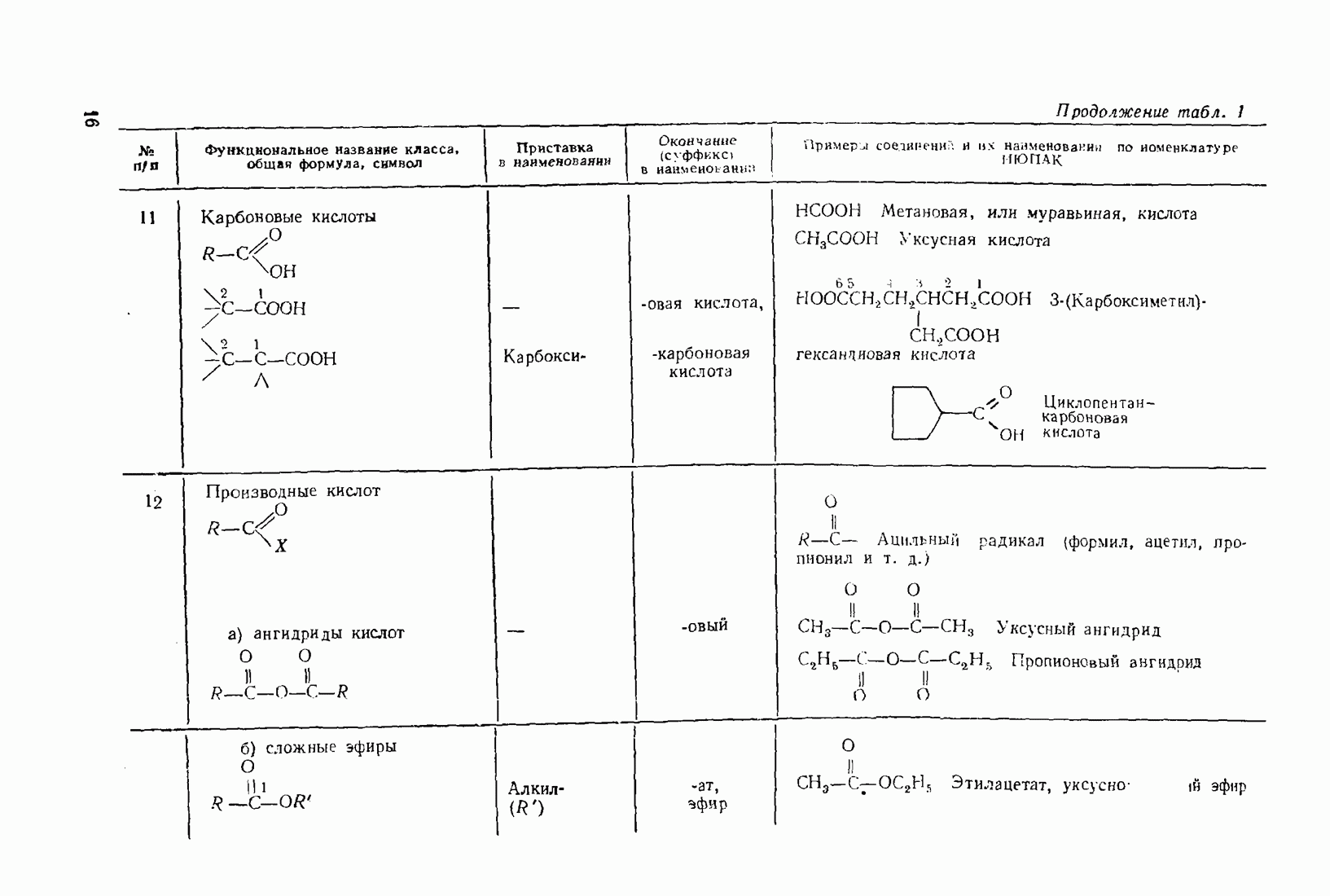
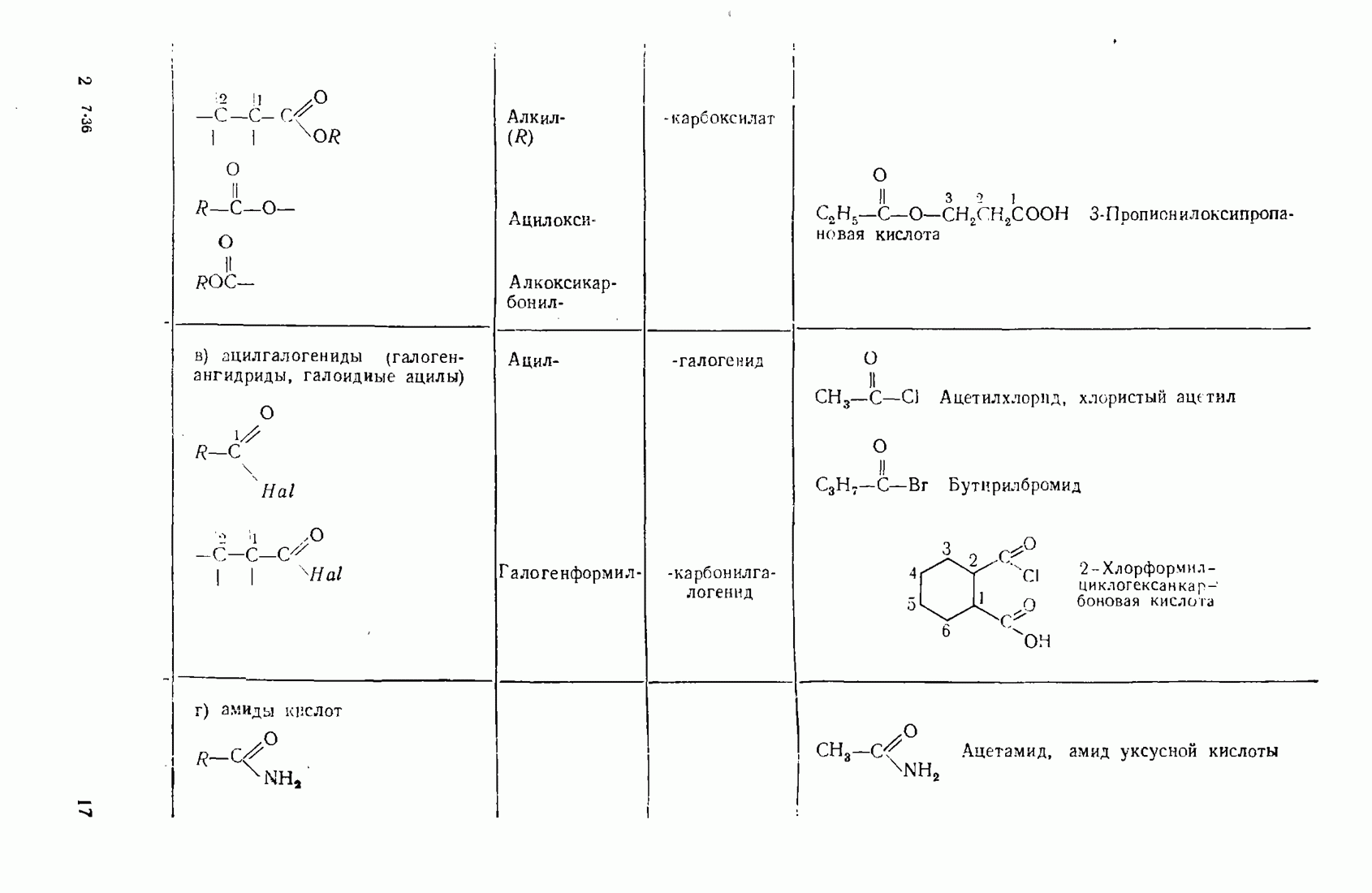
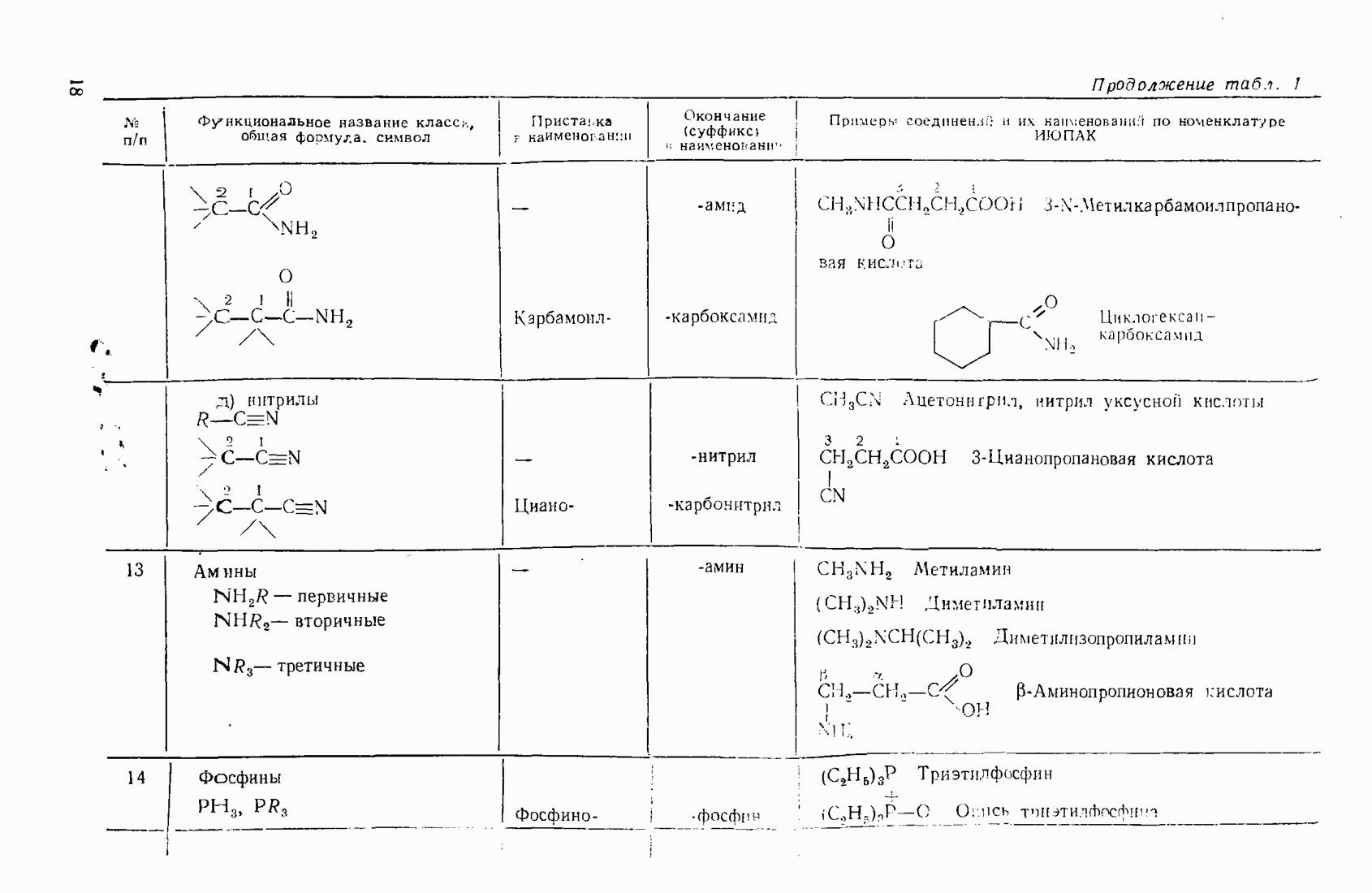
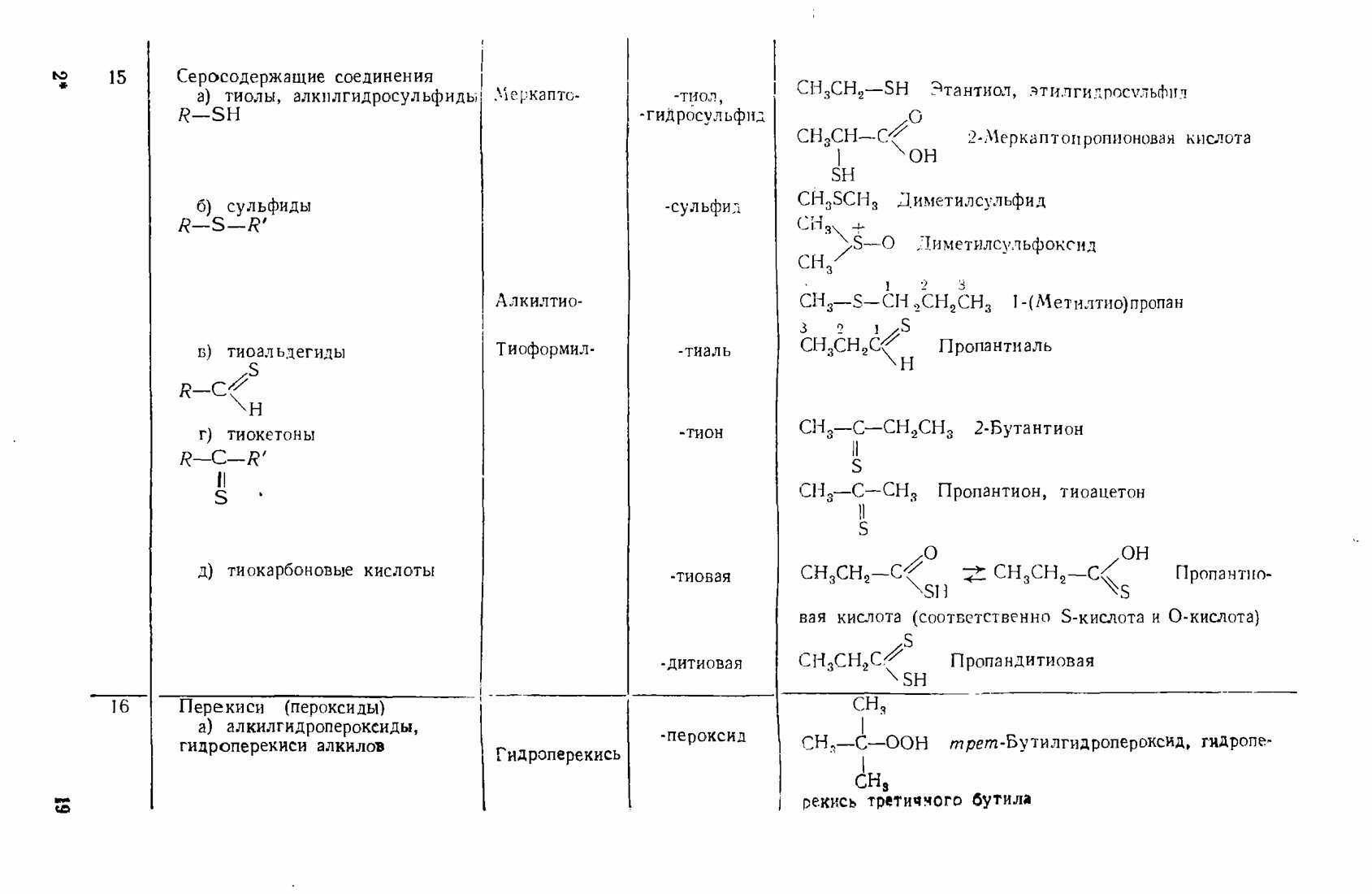
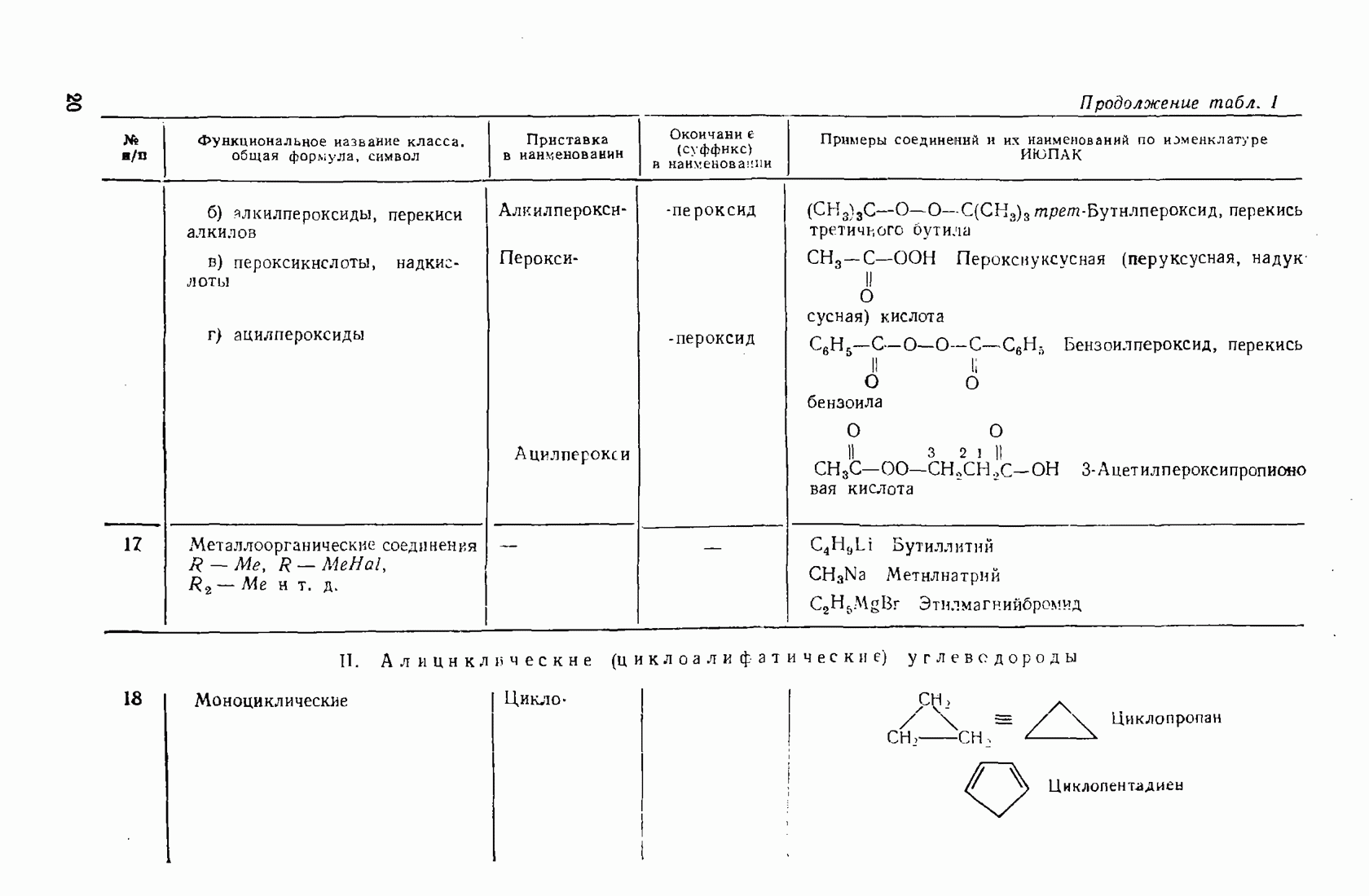
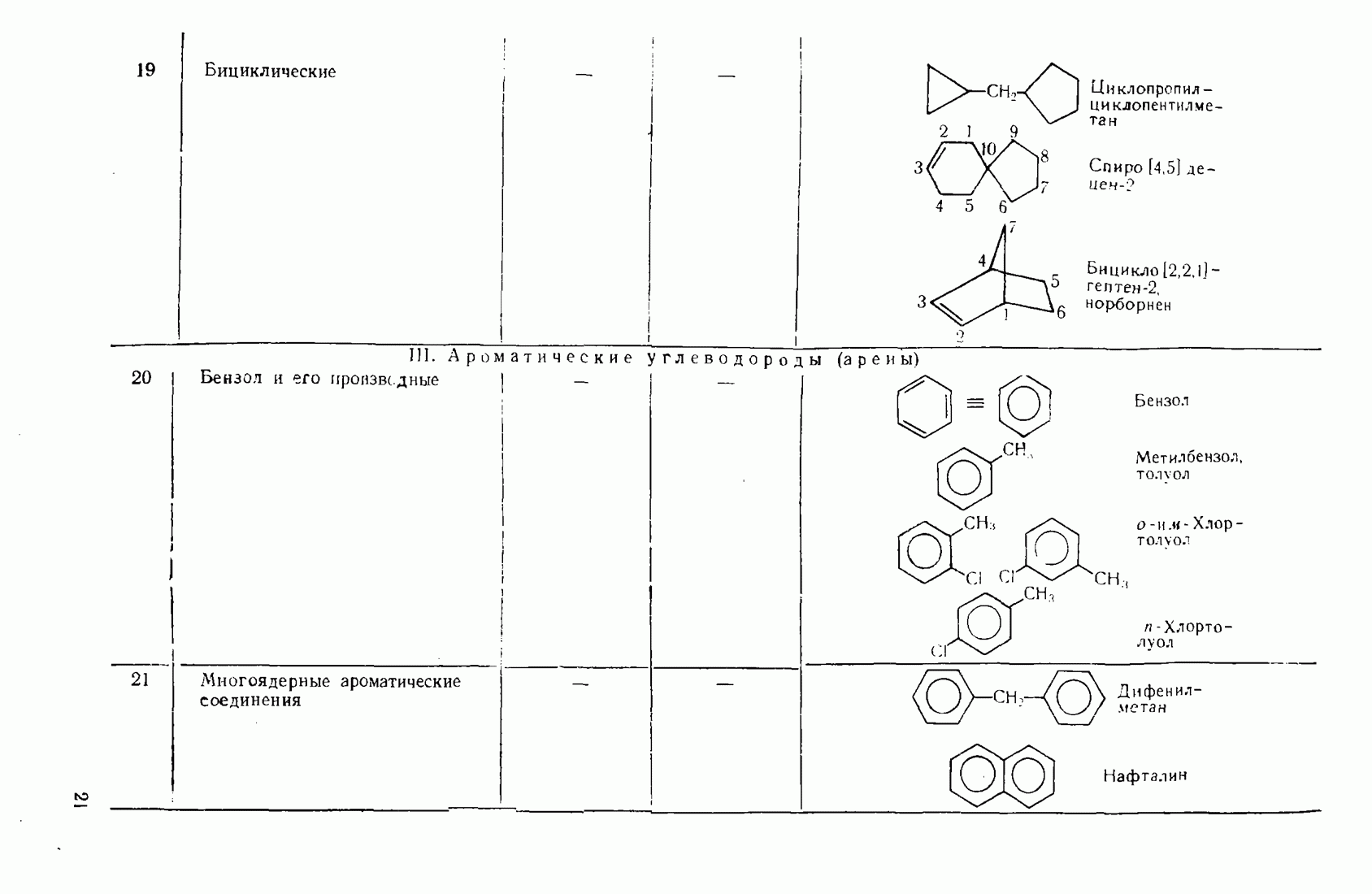
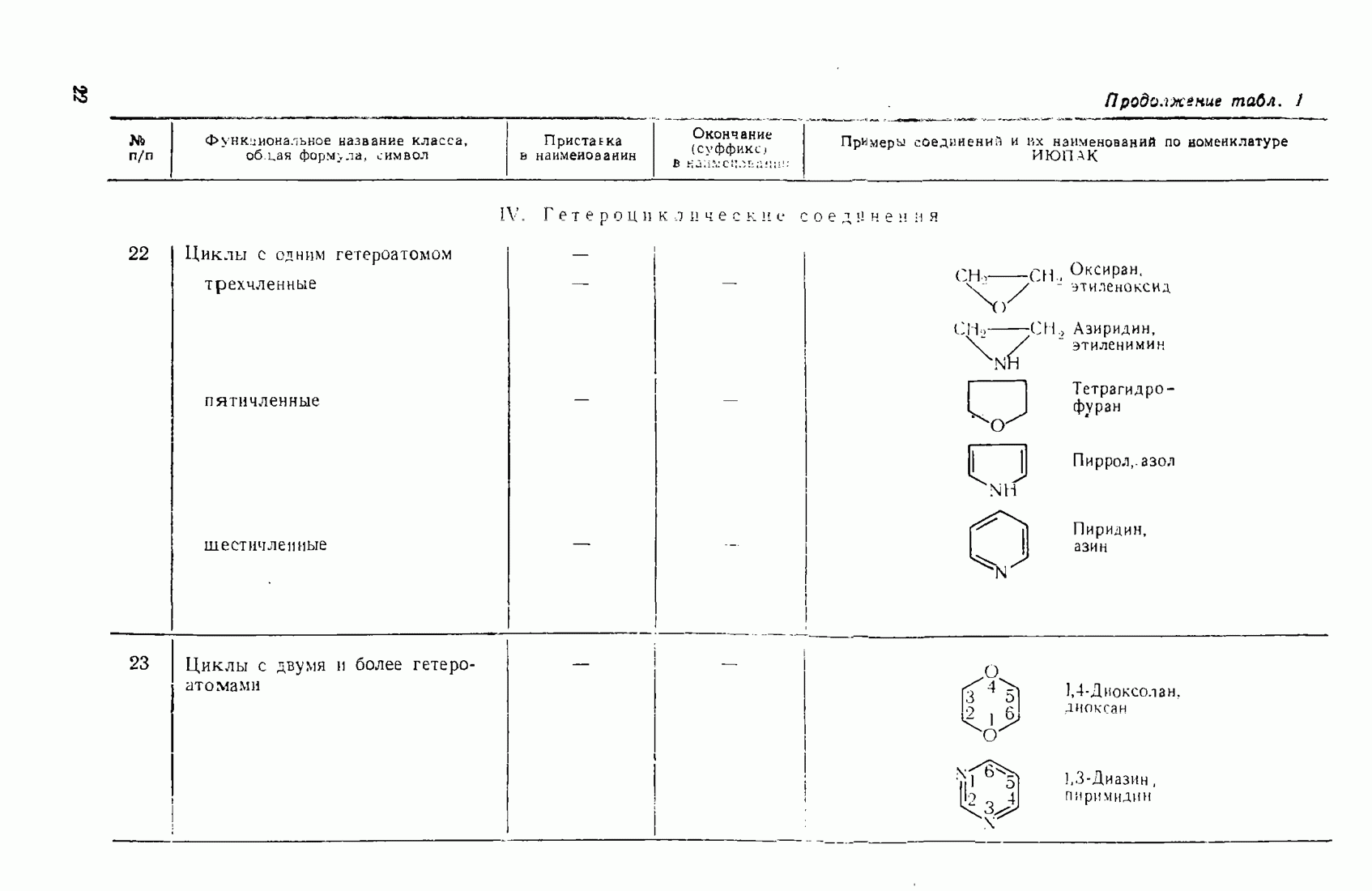
- 1.3. Классификация и номенклатура органических соединений
- 2 Общие теоретические положения органической химии
- 2.1. Природа химической связи
- 2.1.1. Типы химических связей
- 2.1.2. Молекулярные орбитали
- 2.2. ТИПЫ ЭЛЕКТРОННЫХ СМЕЩЕНИЙ В МОЛЕКУЛАХ
- 2.3. ОБЩИЕ ПРЕДСТАВЛЕНИЯ ОБ ОРГАНИЧЕСКОЙ РЕАКЦИИ
- 2.4. КЛАССИФИКАЦИЯ РЕАГЕНТОВ И РЕАКЦИЙ
- 2.5. КРАТКАЯ ХАРАКТЕРИСТИКА РЕАКЦИОННОЙ СПОСОБНОСТИ НЕКОТОРЫХ СОЕДИНЕНИЙ АЛИФАТИЧЕСКОГО РЯДА
- 2.5.1. Алканы (парафины)
- 2.5.2. Непредельные углеводороды
- 2.5.3. Галогеналканы (галоидные алкилы R-Hal)
- 2.5.4. Спирты (R0Н)
- 2.5.5. Альдегиды и кетоны
- 2.5.6. Карбоновые кислоты (R-СООН) и их производные (R-СО-X)
- 2.5.7. Амины (NH2R, NHR2, NR3)
- 3. Реакционная способность соединений алифатического ряда
- 3.1. Алканы (насыщенные углеводороды)
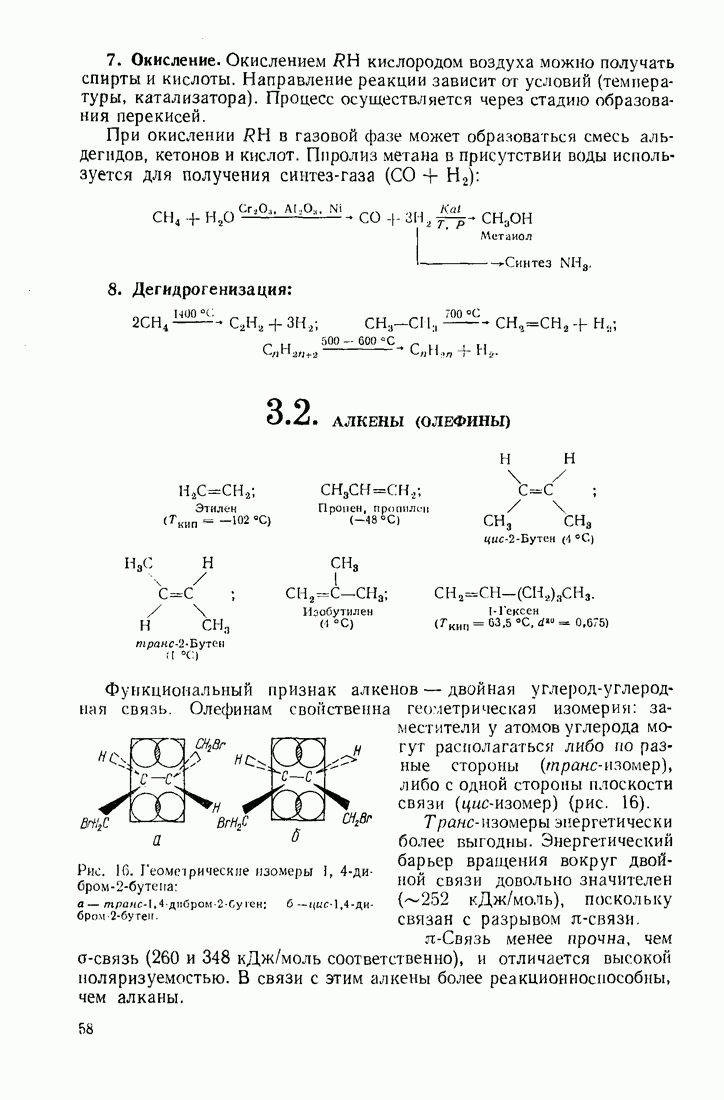
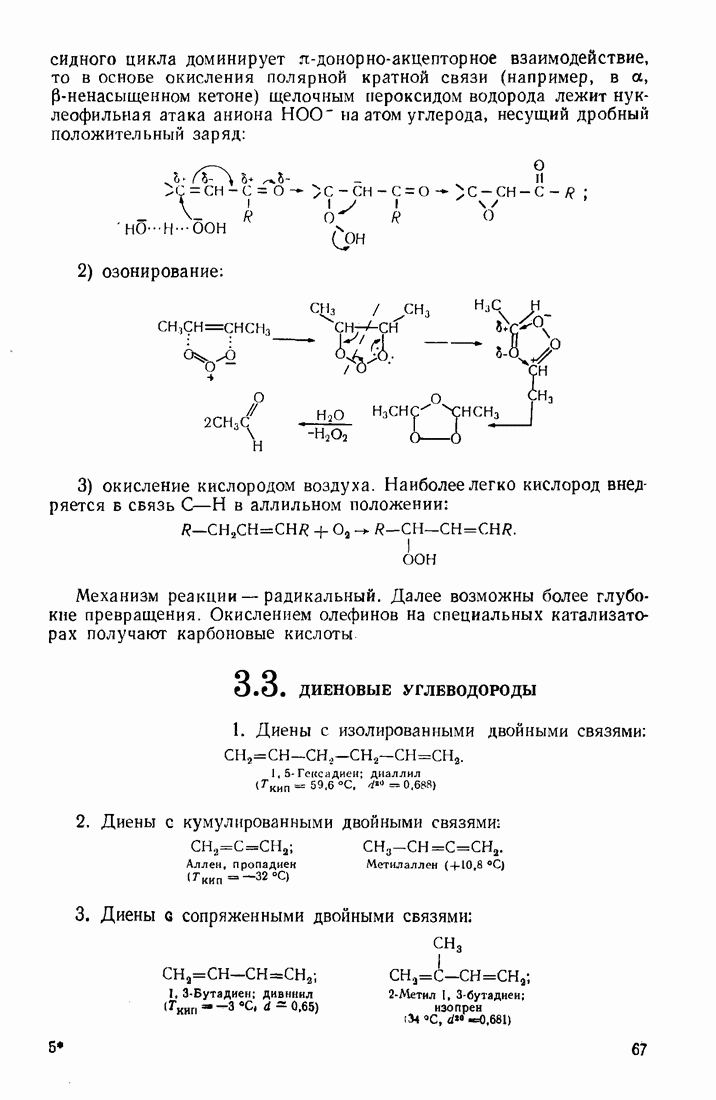
- 3.2. АЛКЕНЫ (ОЛЕФИНЫ)
- 3.3. ДИЕНОВЫЕ УГЛЕВОДОРОДЫ
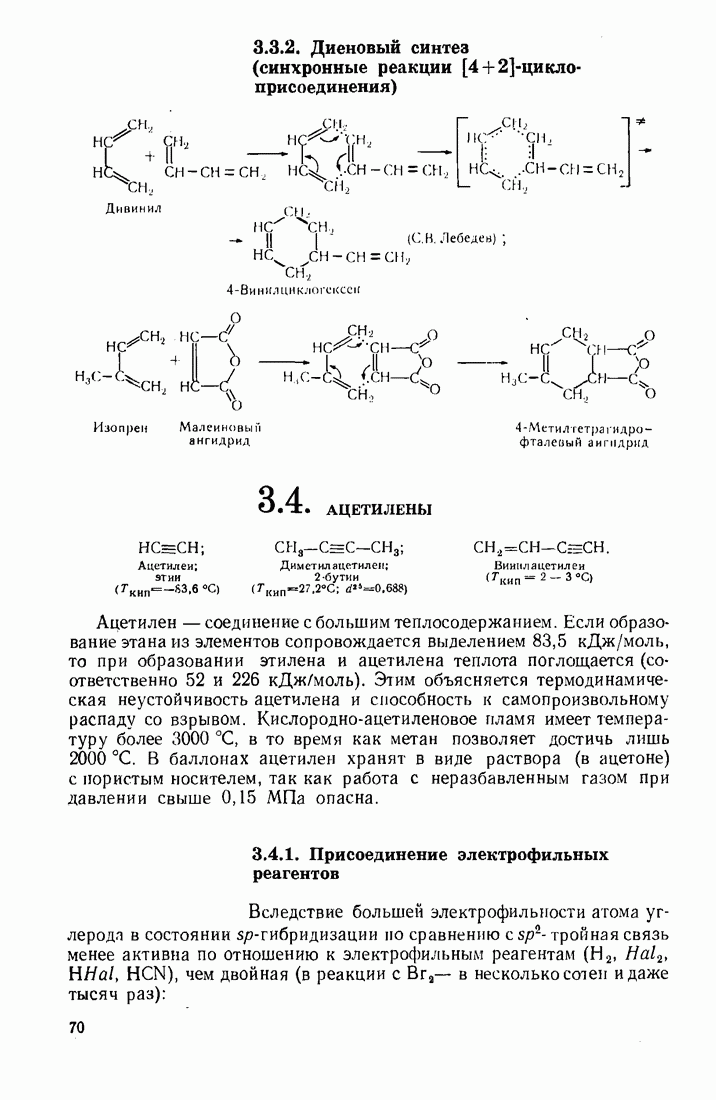
- 3.4. АЦЕТИЛЕНЫ
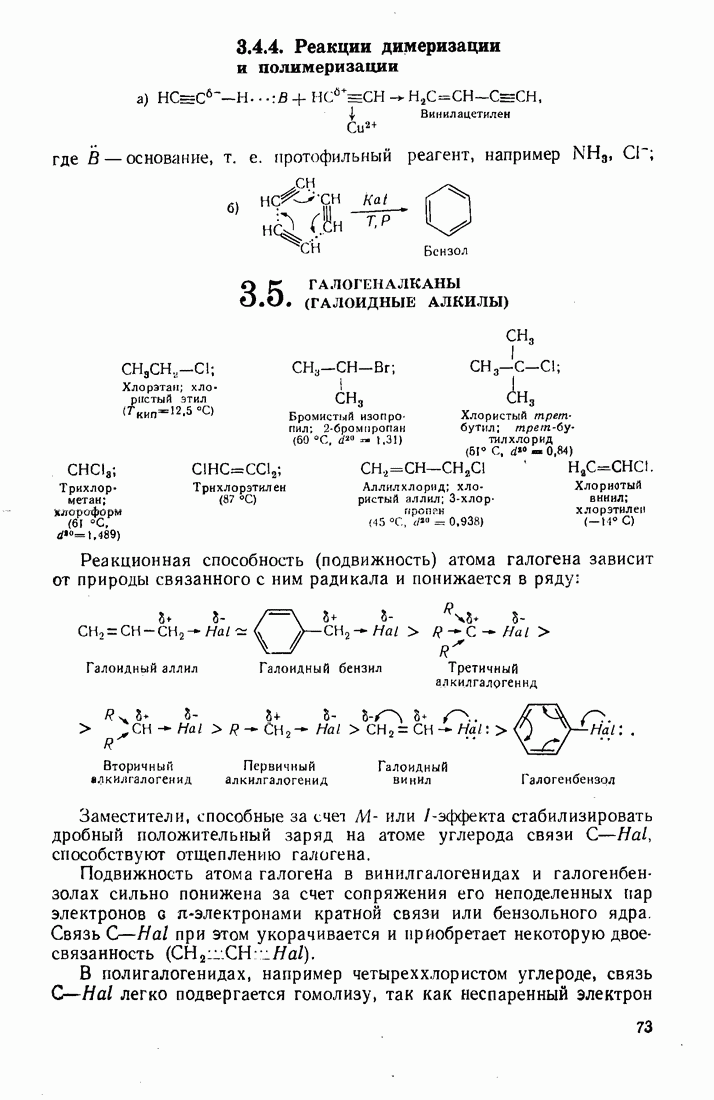
- 3.5. ГАЛОГЕНАЛКАНЫ (ГАЛОИДНЫЕ АЛКИЛЫ)
- 3.6. СПИРТЫ
- 3.7. ПРОСТЫЕ ЭФИРЫ (R-O-R)
- 3.8. ОКСИРАНЫ (ЭПОКСИДНЫЕ СОЕДИНЕНИЯ, a-ОКИСИ)
- 3.9. АЛЬДЕГИДЫ И КЕТОНЫ
- 3.10. КАРБОНОВЫЕ КИСЛОТЫ
- 3.11. НЕКОТОРЫЕ ПРОИЗВОДНЫЕ КИСЛОТ
- 3.12. АМИНЫ
- 3.13. ФОСФОРОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- 3.14. СЕРООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- 3.15. ОРГАНИЧЕСКИЕ ПЕРЕКИСИ (ПЕРОКСИДНЫЕ СОЕДИНЕНИЯ)
- 3.16. ПРОИЗВОДНЫЕ УГОЛЬНОЙ КИСЛОТЫ
- 3.17. ГЕТЕРОАНАЛОГИ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ
- 3.18. АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- 3.18.2. Пространственное расположение и напряженность циклов
- 3.18.3. Особенности химических свойств алициклических соединений
- 4. Полифункциональные производные алифатического ряда
- 4.1. ДВУХОСНОВНЫЕ КАРБОНОВЫЕ КИСЛОТЫ
- 4.2. НЕПРЕДЕЛЬНЫЕ КИСЛОТЫ
- 4.3. ОКСОКИСЛОТЫ (АЛЬДЕГИДО- И КЕТОКИСЛОТЫ)
- 4.4. ОКСИКИСЛОТЫ. ПОНЯТИЕ ОБ ОПТИЧЕСКОЙ ИЗОМЕРИИ
- 4.5. УГЛЕВОДЫ
- 4.5.2. Стереохимия моносахаридов
- 4.5.3. Дисахариды
- 4.5.4. Полисахариды
- 4.5.5. Нахождение в природе и пути превращения углеводов
- 4.6. АМИНОКИСЛОТЫ
- 5. Методы синтеза органических юединений алифатическою рада
- 5.1. АЛКИЛИРОВАНИЕ
- 5.2. АЦИЛИРОВАНИЕ
- 5.3. ГАЛОГЕНИРОВАНИЕ
- 5.4. ГИДРОКСИЛИРОВАНИЕ
- 5.5. КАРБОНИЛИРОВАНИЕ (ВВЕДЕНИЕ КАРБОНИЛЬНОЙ ГРУППЫ)
- 5.6. КАРБОКСИЛИРОВАНИЕ
- 5.7. ЭПОКСИДИРОВАНИЕ (ОКСИРАНИРОВАИИЕ)
- 5.8. АМИНИРОВАНИЕ
- 5.9. ОКИСЛЕНИЕ
- 5.10. ВОССТАНОВЛЕНИЕ
- 5.11. АЛКАНЫ
- 5.12 АЛКЕНЫ
- 5.13. ДИЕНОВЫЕ УГЛЕВОДОРОДЫ (1,3-ДИЕНЫ)
- 5.14. АЦЕТИЛЕНЫ
- 5.15 АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- 5.16. ГАЛОГЕН АЛКАНЫ
- 5.17. СПИРТЫ
- 5.18. АЛЬДЕГИДЫ И КЕТОНЫ
- 5.19. КАРБОНОВЫЕ КИСЛОТЫ
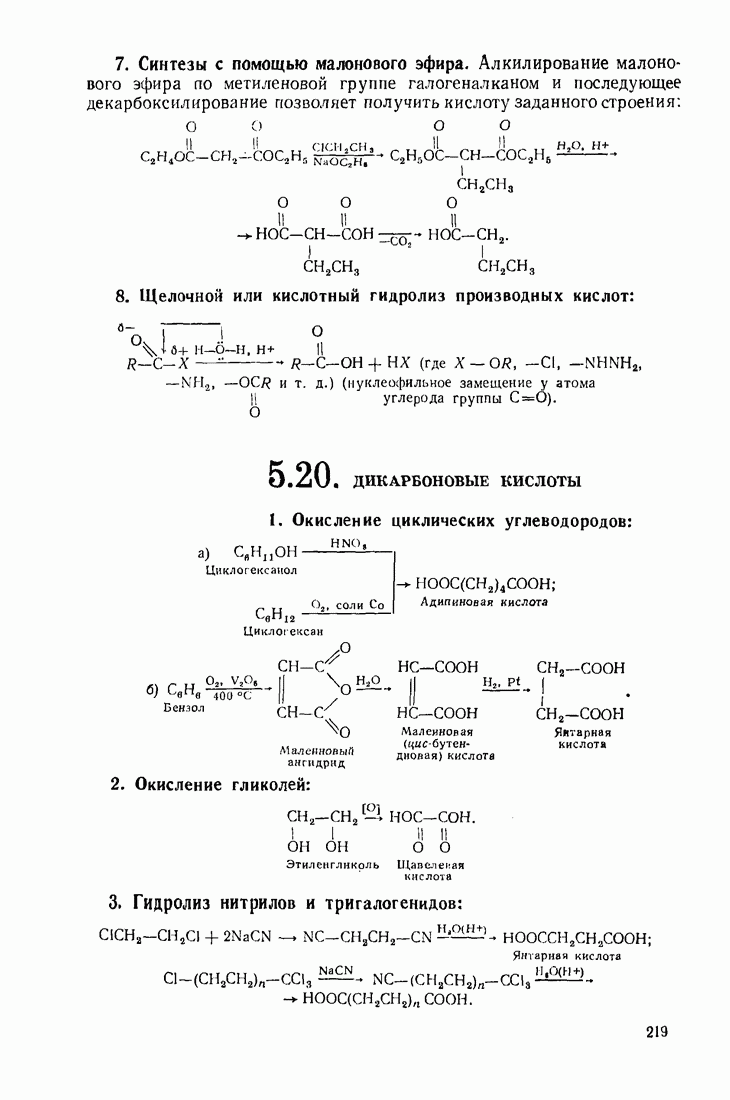
- 5.20. ДИКАРБОНОВЫЕ КИСЛОТЫ
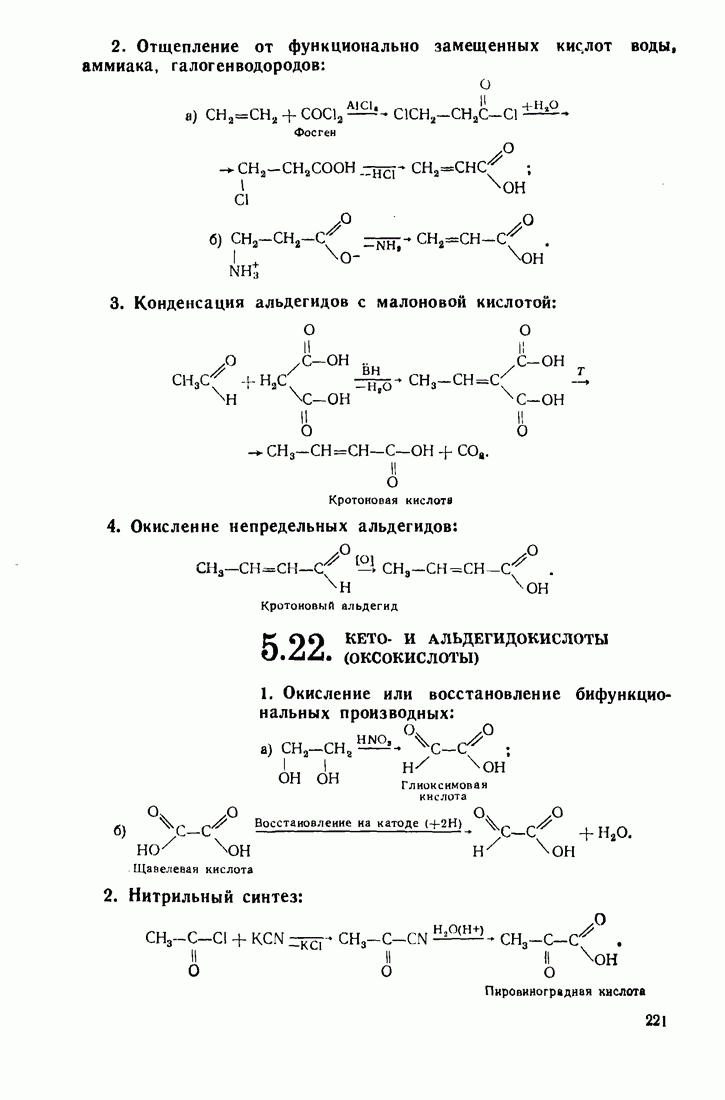
- 5.21. НЕПРЕДЕЛЬНЫЕ КИСЛОТЫ
- 5.22. КЕТО- И АЛЬДЕГИДОКИСЛОТЫ (ОКСОКИСЛОТЫ)
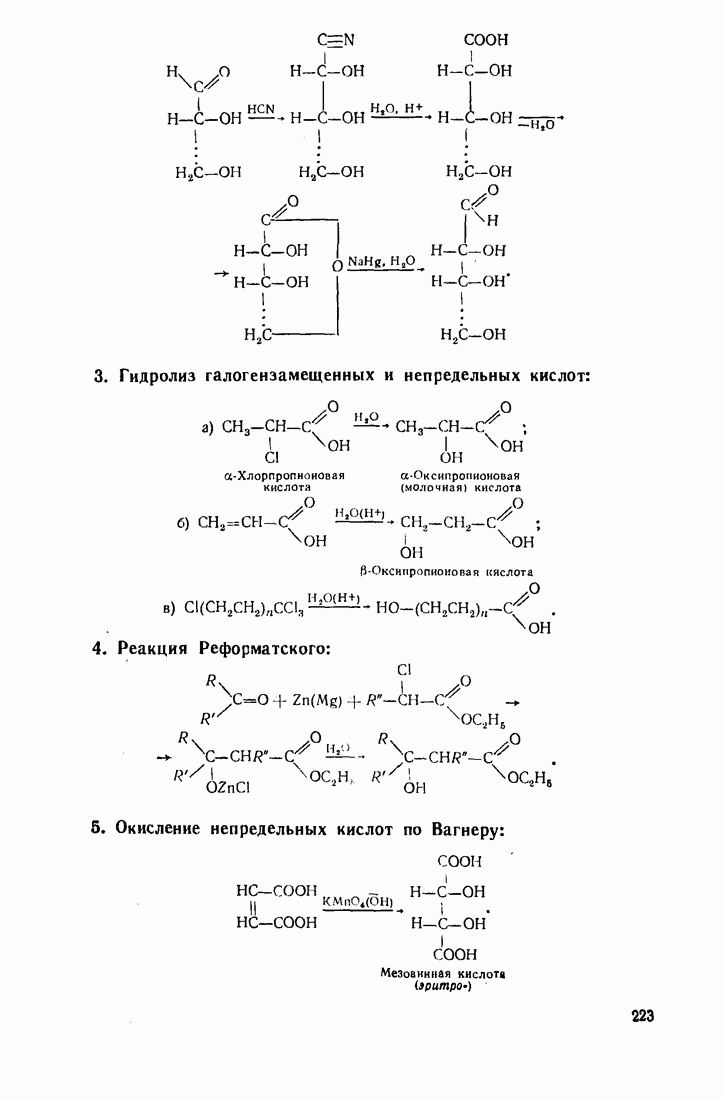
- 5.23. ОКСИКИСЛОТЫ
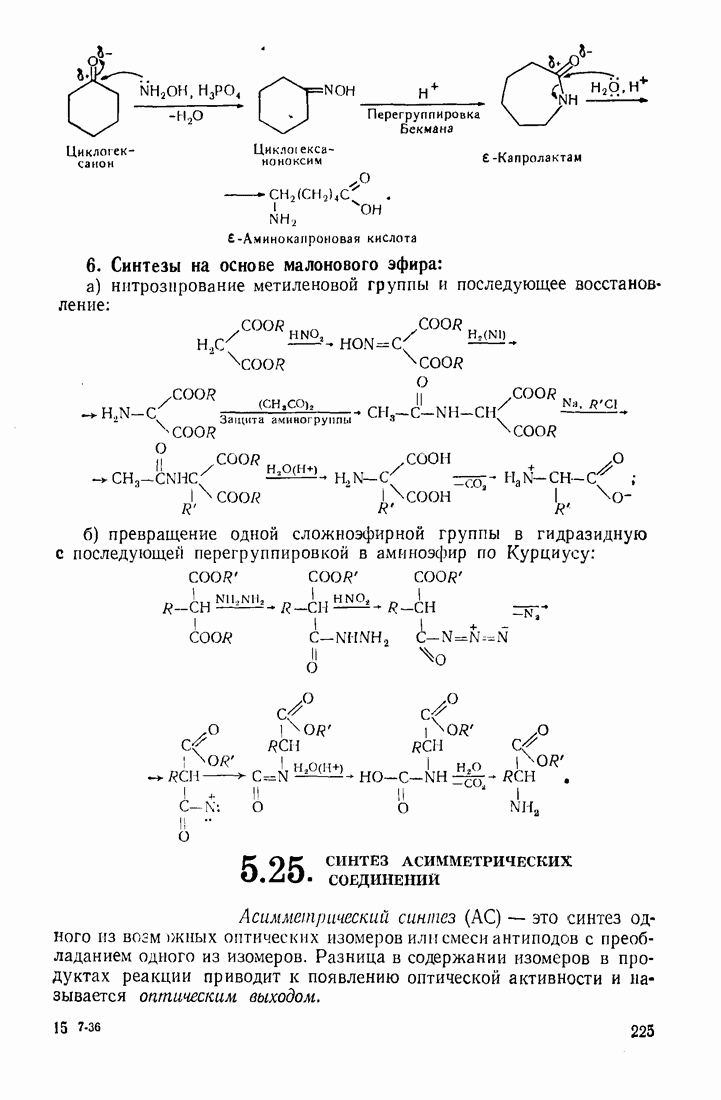
- 5.24. АМИНОКИСЛОТЫ
- 5.25 СИНТЕЗ АСИММЕТРИЧЕСКИХ СОЕДИНЕНИЙ
- 6. Некоторые понятия физической органической химии
- 6.1. СВЯЗЬ СОСТАВА И СТРОЕНИЯ СОЕДИНЕНИЙ С ФИЗИЧЕСКИМИ СВОЙСТВАМИ
- 6.2. ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 6.3. КИСЛОТЫ И ОСНОВАНИЯ В ОРГАНИЧЕСКОЙ ХИМИИ
- 6.4. ОРГАНИЧЕСКИЕ РАСТВОРИТЕЛИ И ИХ ВЛИЯНИЕ НА СКОРОСТЬ И МЕХАНИЗМ РЕАКЦИЙ
- 6.5. КАТАЛИЗ ОРГАНИЧЕСКИХ РЕАКЦИЙ
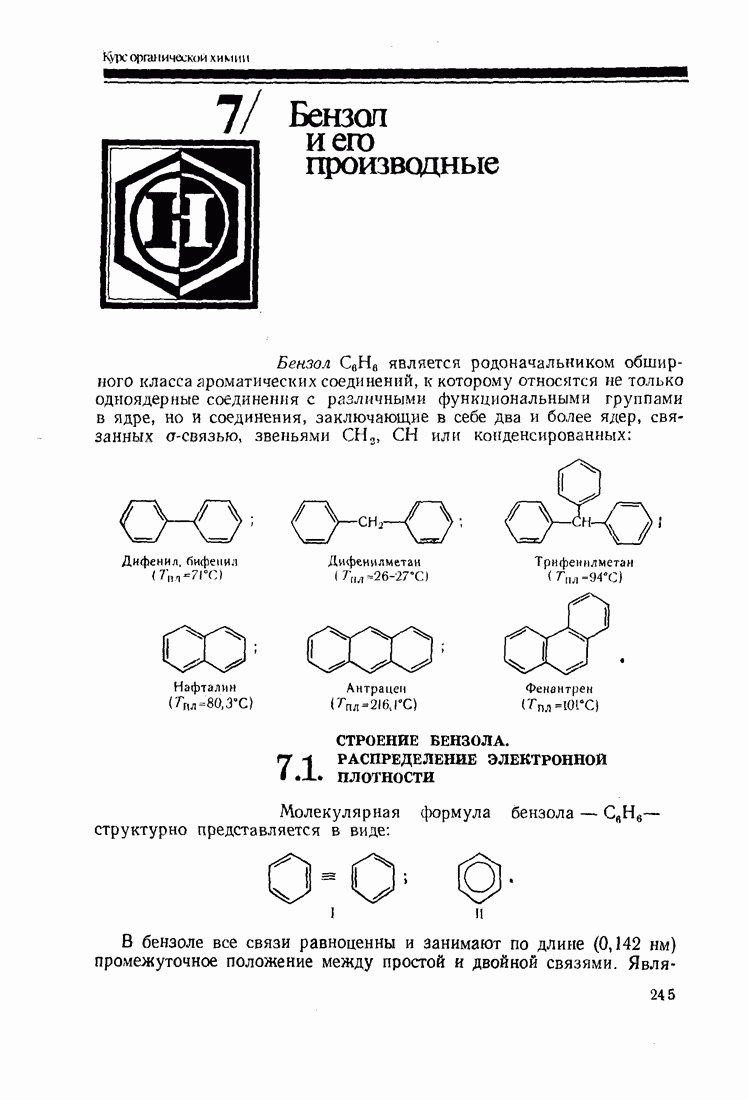
- 7. Бензол и его производные
- 7.1. СТРОЕНИЕ БЕНЗОЛА. РАСПРЕДЕЛЕНИЕ ЭЛЕКТРОННОЙ ПЛОТНОСТИ
- 7.2. ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ В БЕНЗОЛЬНОМ ЯДРЕ
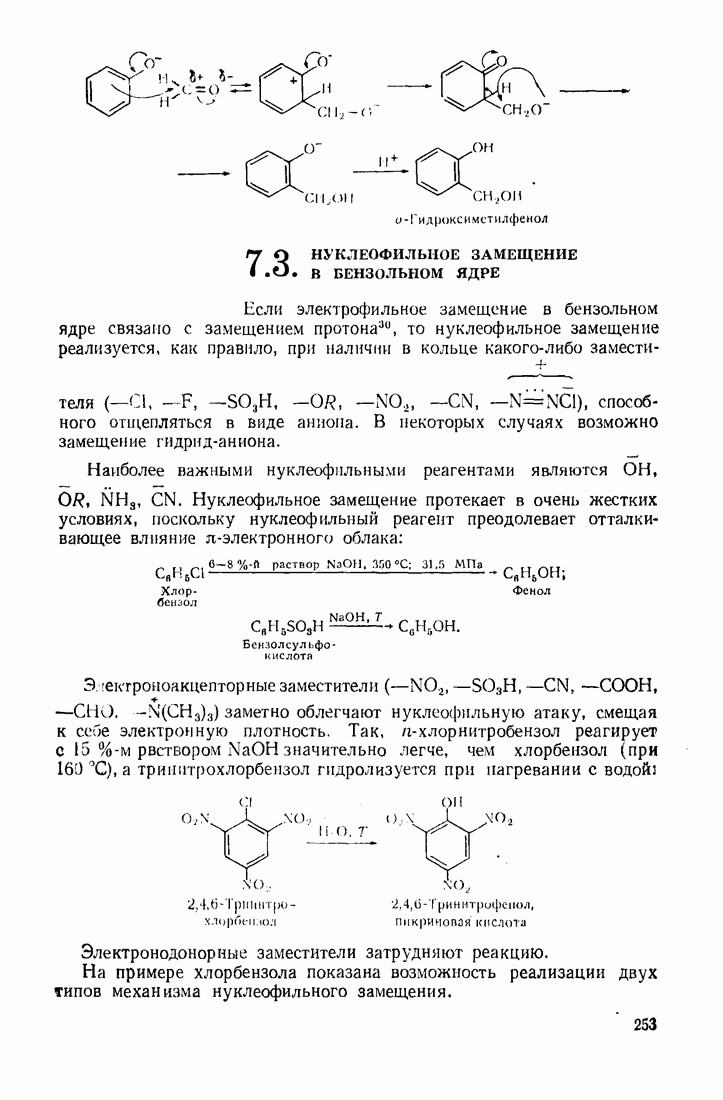
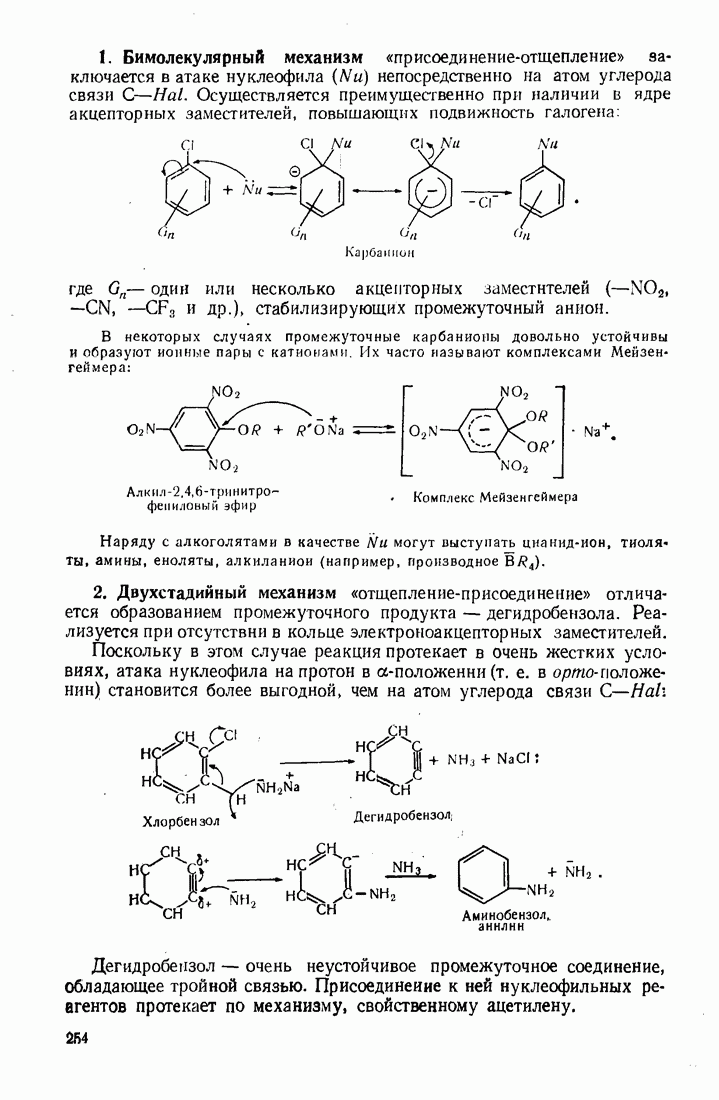
- 7.3. НУКЛЕОФИЛЬНОЕ ЗАМЕЩЕНИЕ В БЕНЗОЛЬНОМ ЯДРЕ
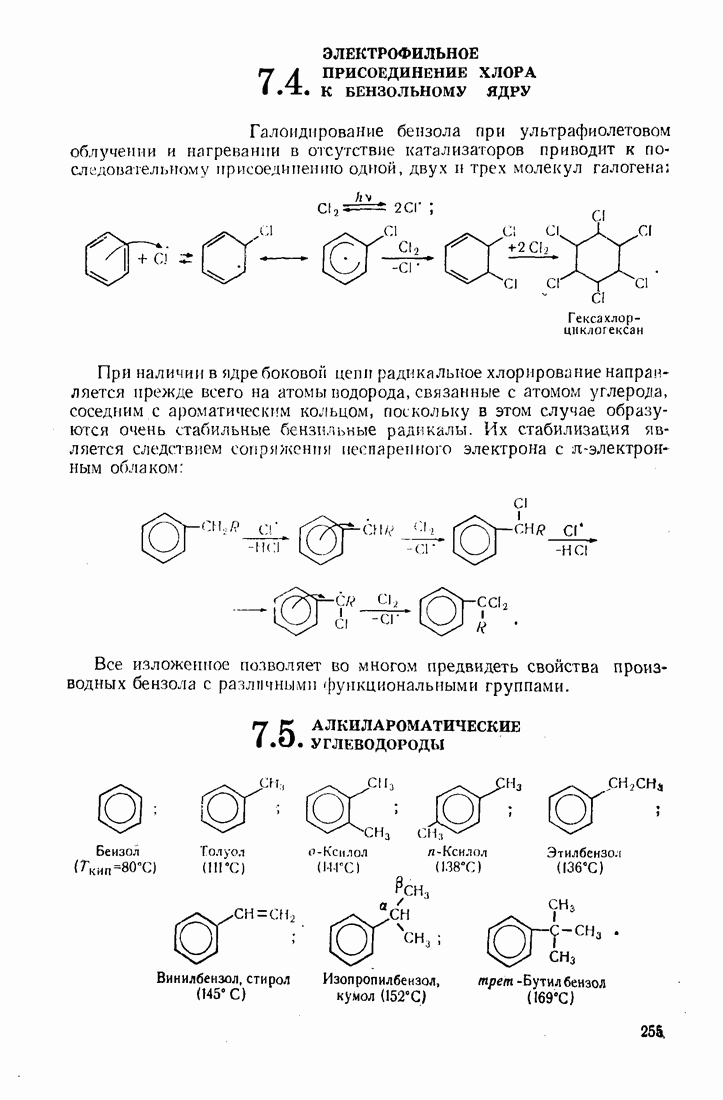
- 7.4. ЭЛЕКТРОФИЛЬНОЕ ПРИСОЕДИНЕНИЕ ХЛОРА К БЕНЗОЛЬНОМУ ЯДРУ
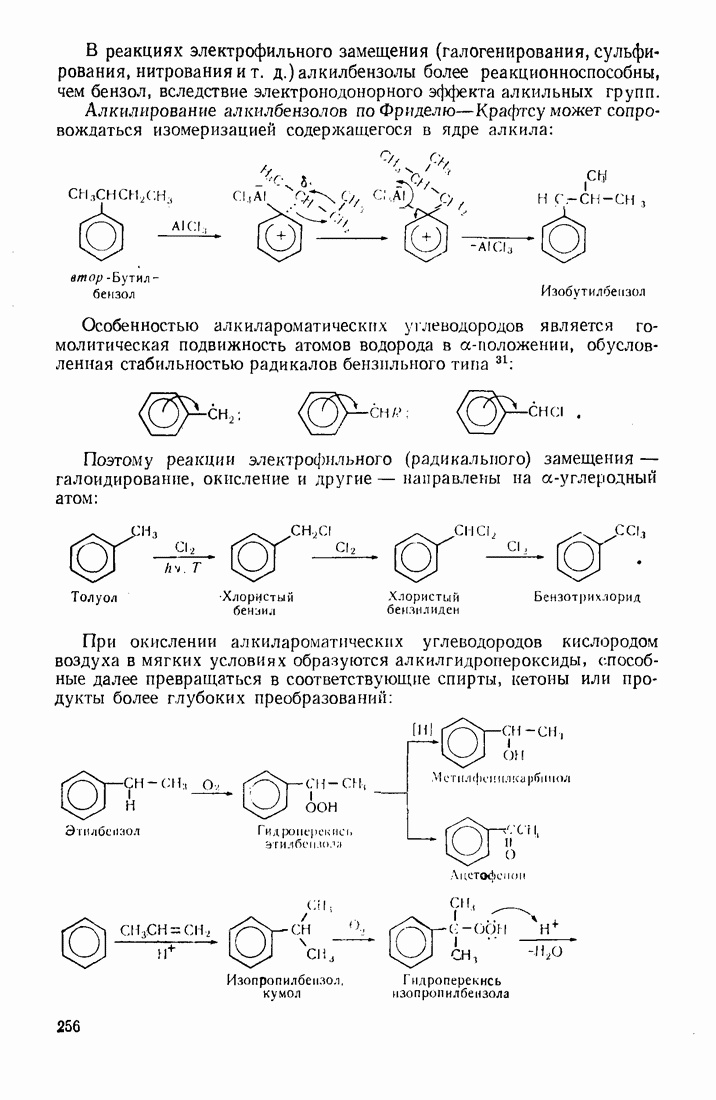
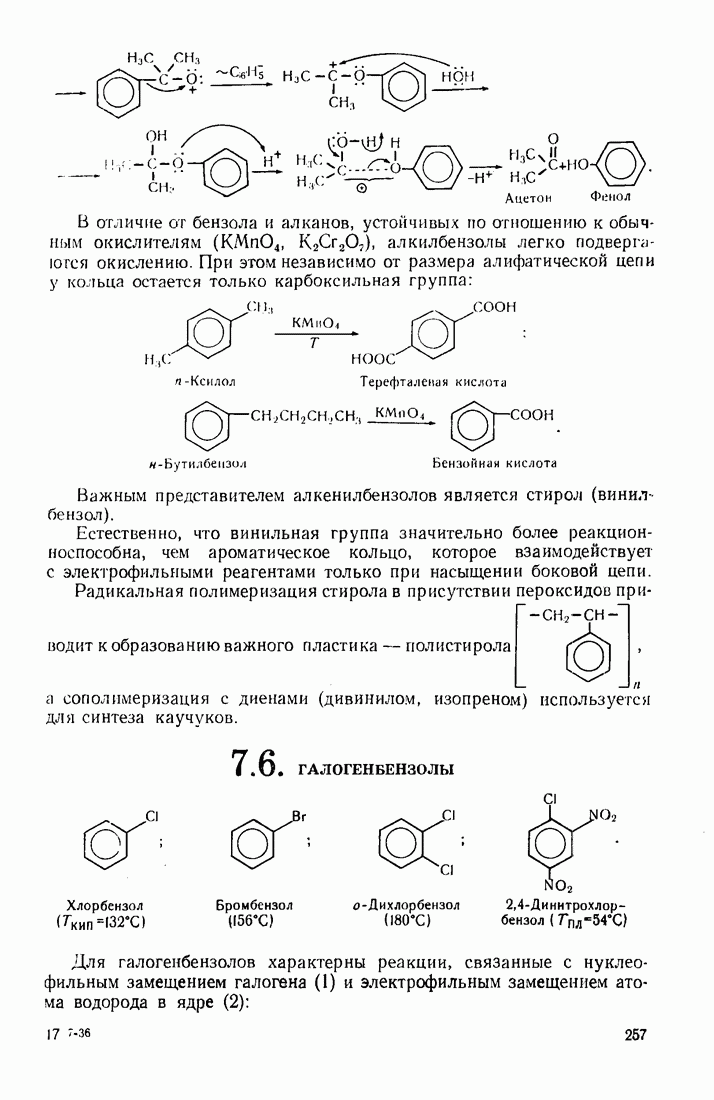
- 7.5. АЛКИЛАРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ
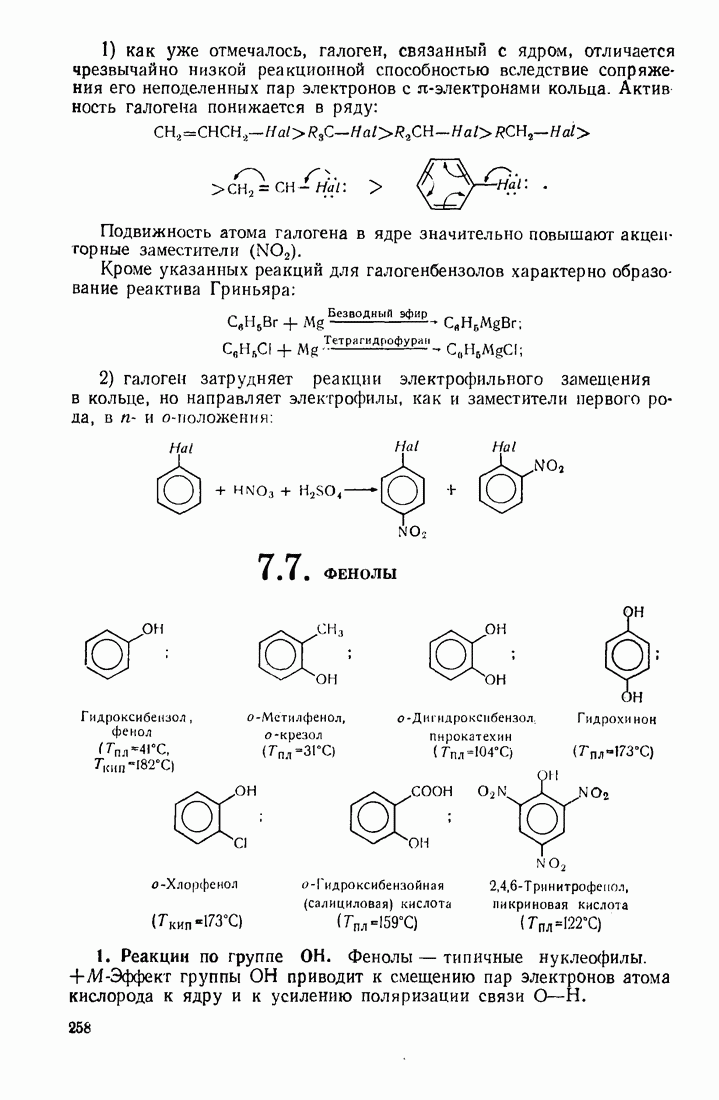
- 7.6. ГАЛОГЕНБЕНЗОЛЫ
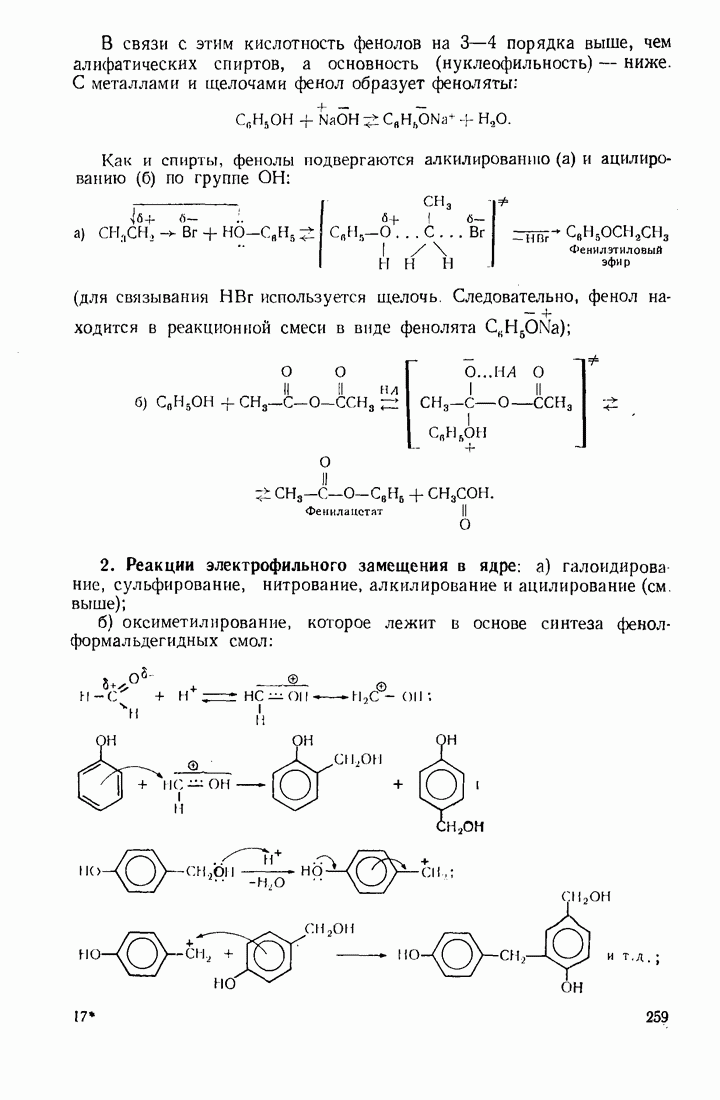
- 7.7. ФЕНОЛЫ
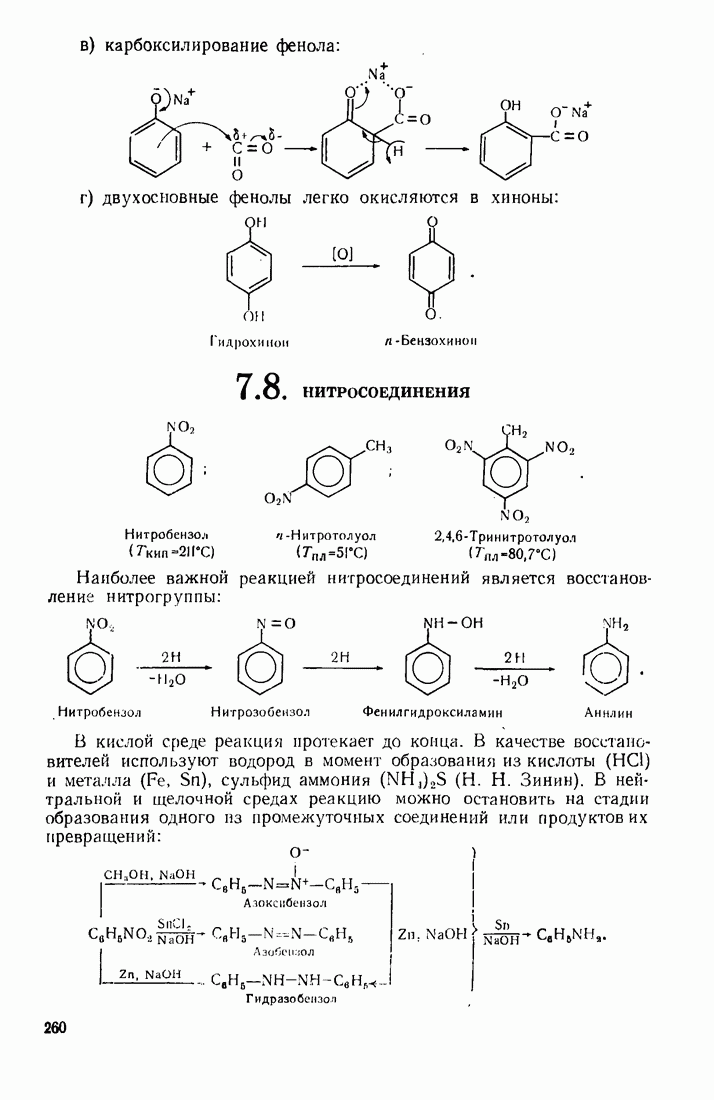
- 7.8. НИТРОСОЕД ИНЕНИЯ
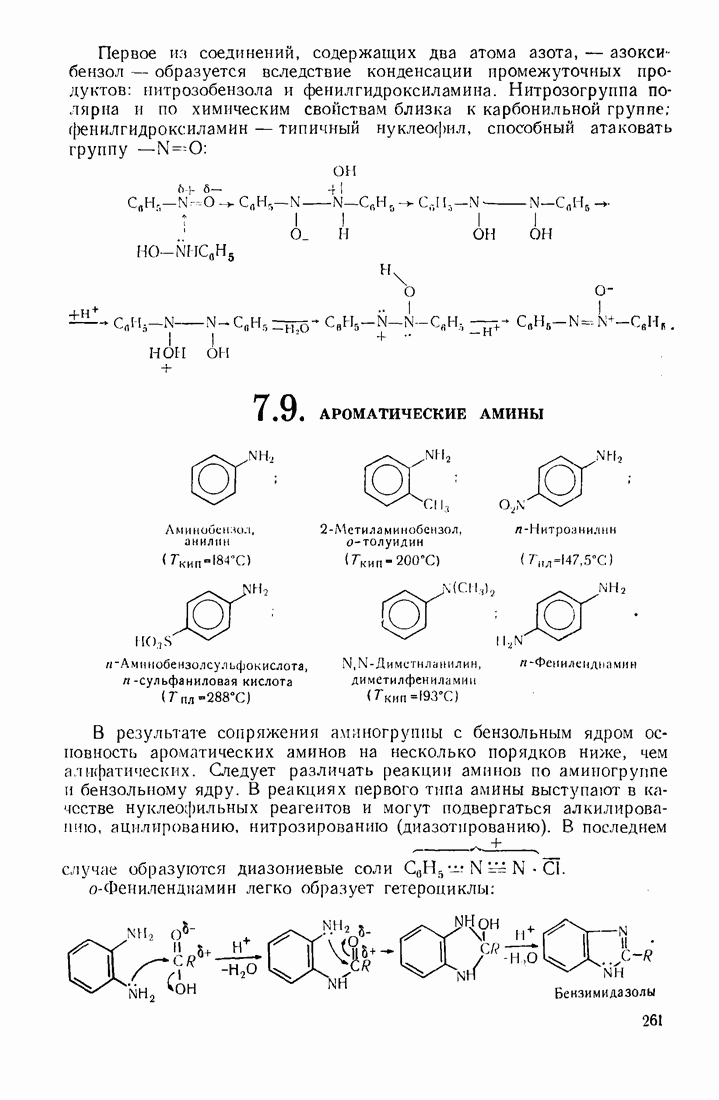
- 7.9. АРОМАТИЧЕСКИЕ АМИНЫ
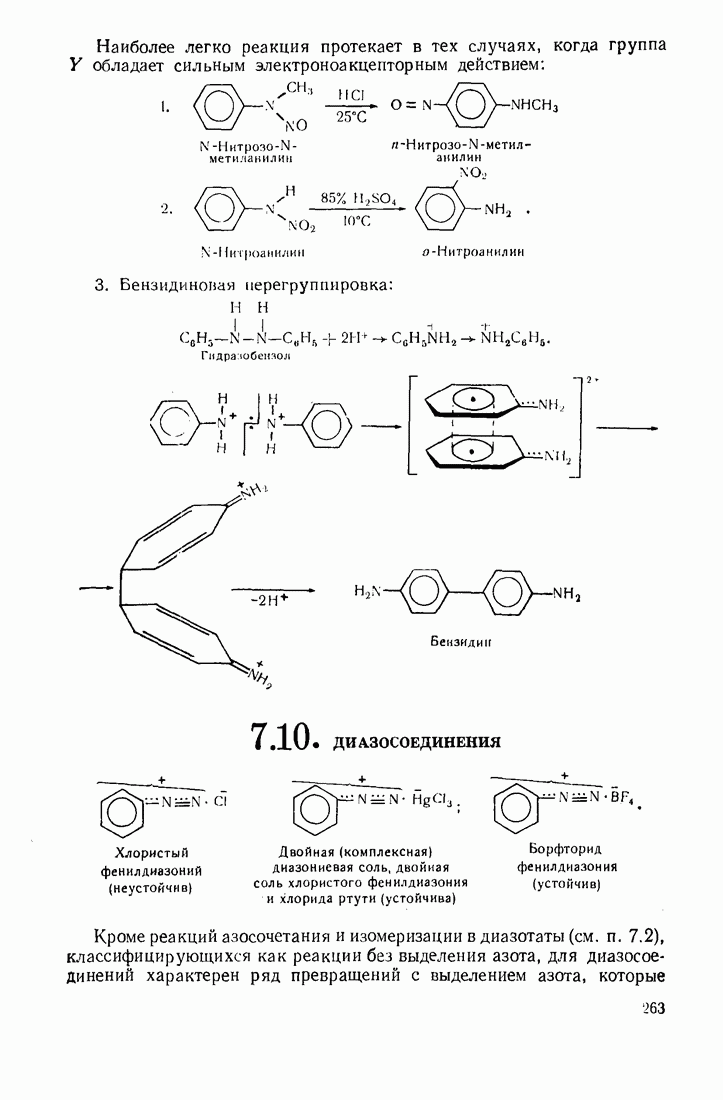
- 7.10. ДИАЗОСОЕДИНЕНИЯ
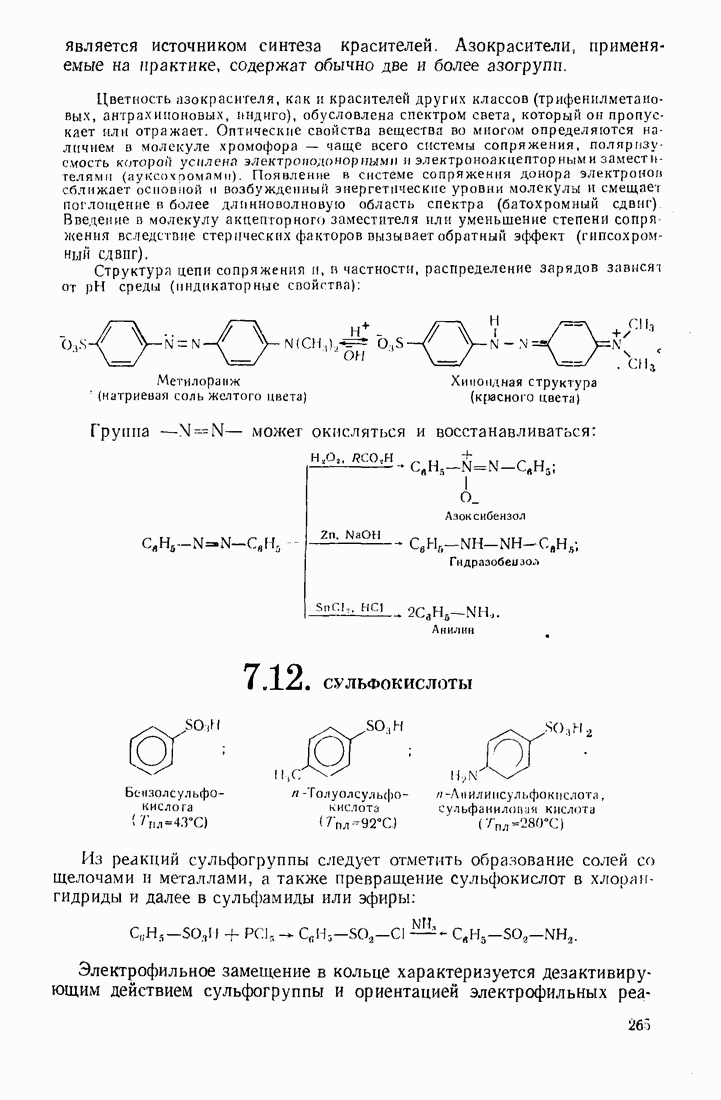
- 7.11. АЗОСОЕДИНЕНИЯ
- 7.12. СУЛЬФОКИСЛОТЫ
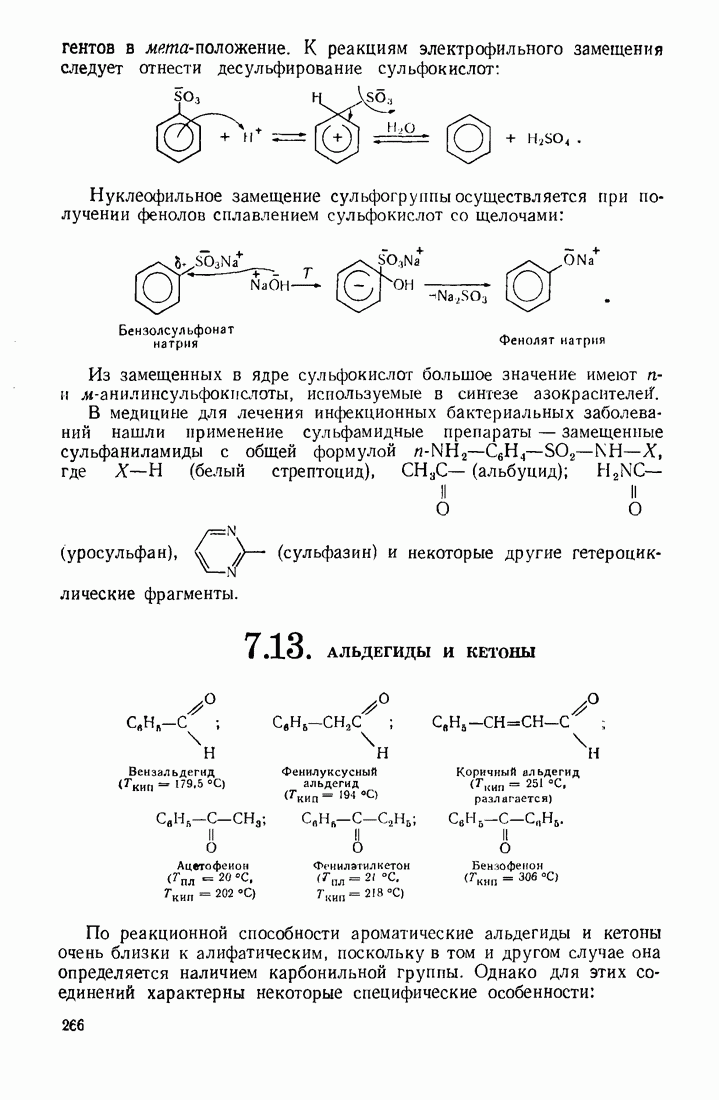
- 7.13. АЛЬДЕГИДЫ И КЕТОНЫ
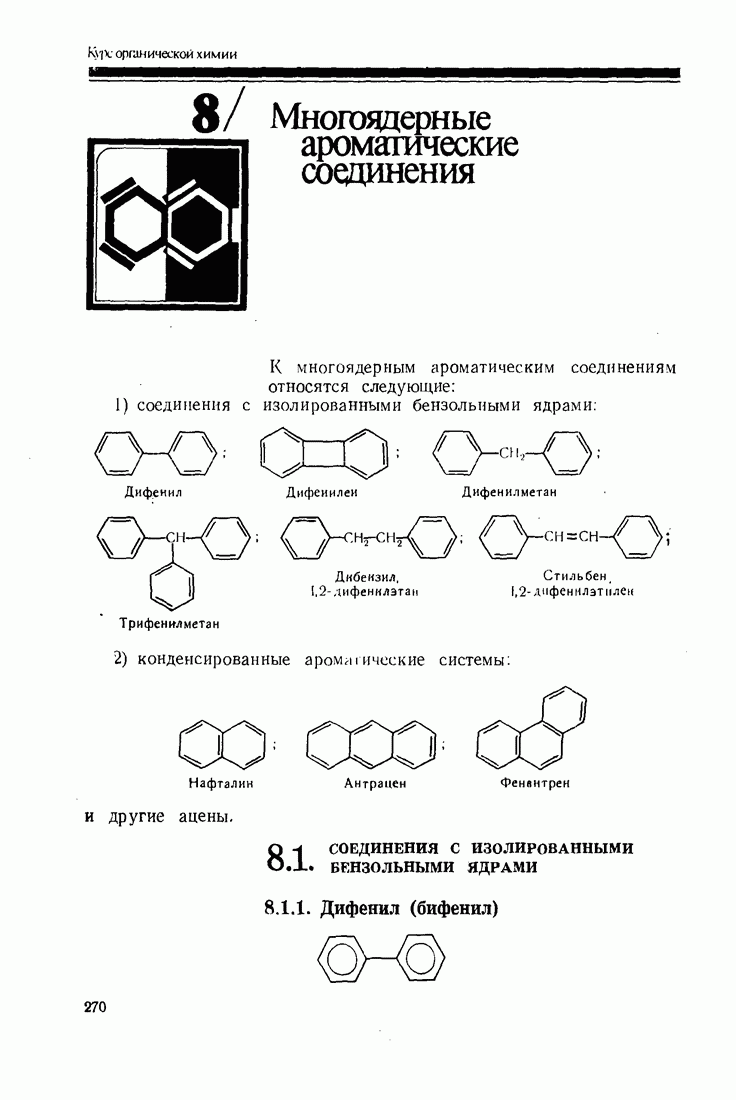
- 8. Многоядерные ароматические соединения
- 8.1. СОЕДИНЕНИЯ С ИЗОЛИРОВАННЫМИ БЕНЗОЛЬНЫМИ ЯДРАМИ
- 8.1.2. Полифенилметаны
- 8.2. АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ С КОНДЕНСИРОВАННЫМИ ЯДРАМИ
- 8.2.2. Антрацен
- 8.2.3. Фенантрен
- 9. Методы синтеза в ряду ароматических соединений
- 9.1. ГАЛОГЕНИРОВАНИЕ
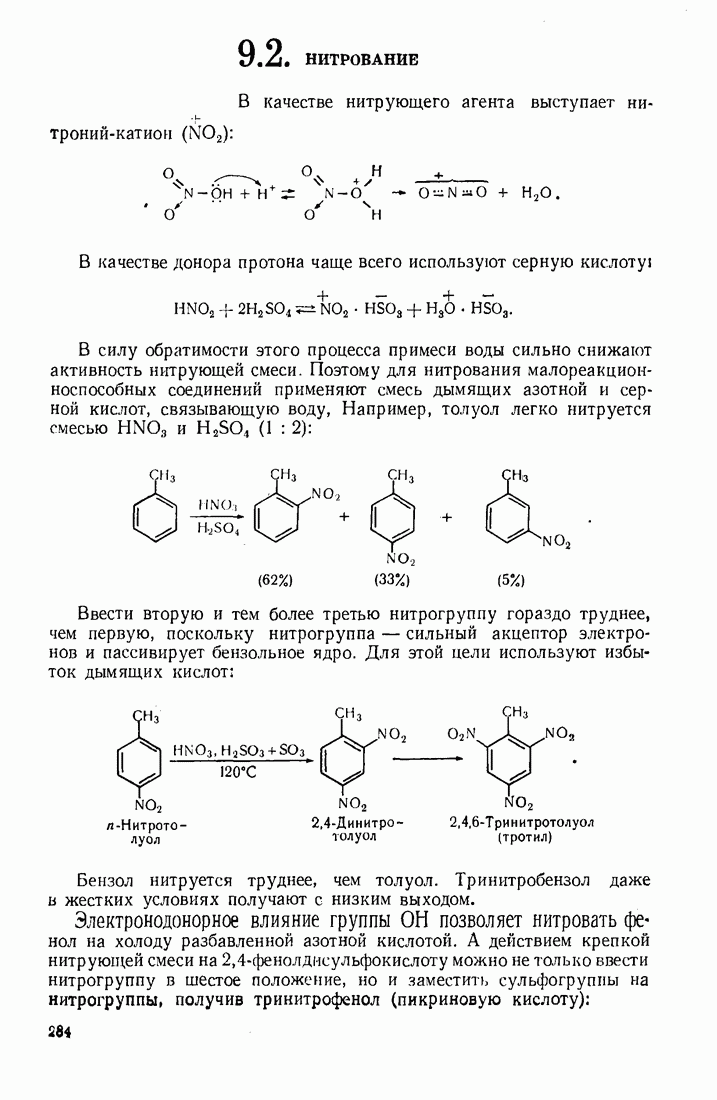
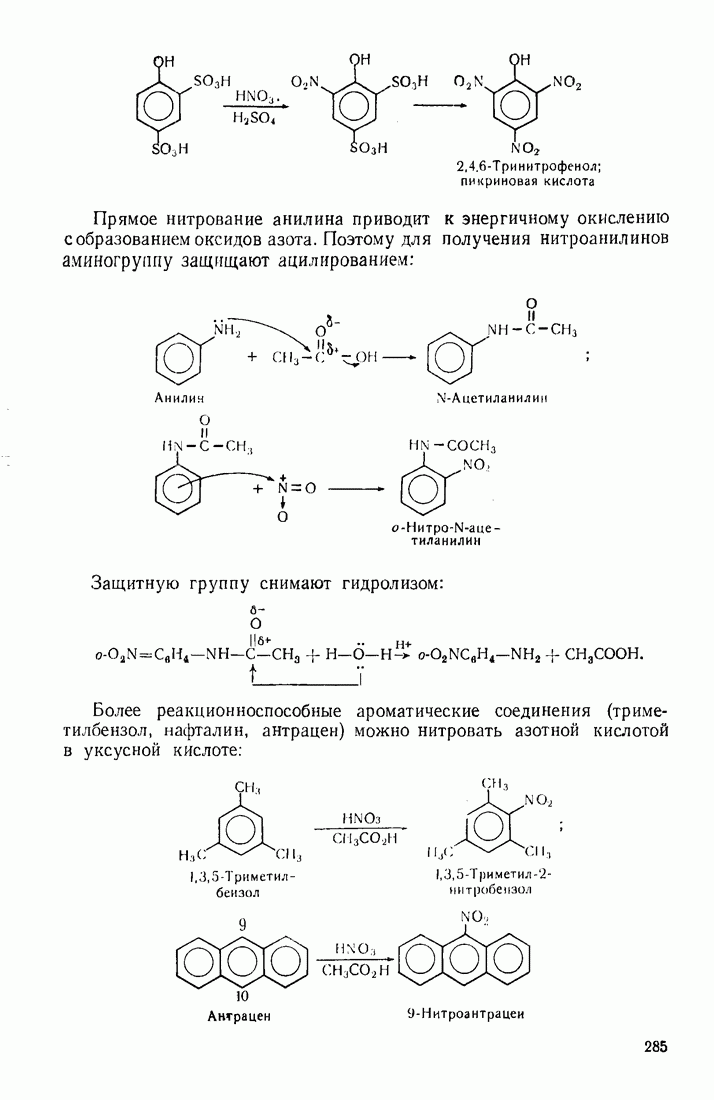
- 9.2. НИТРОВАНИЕ
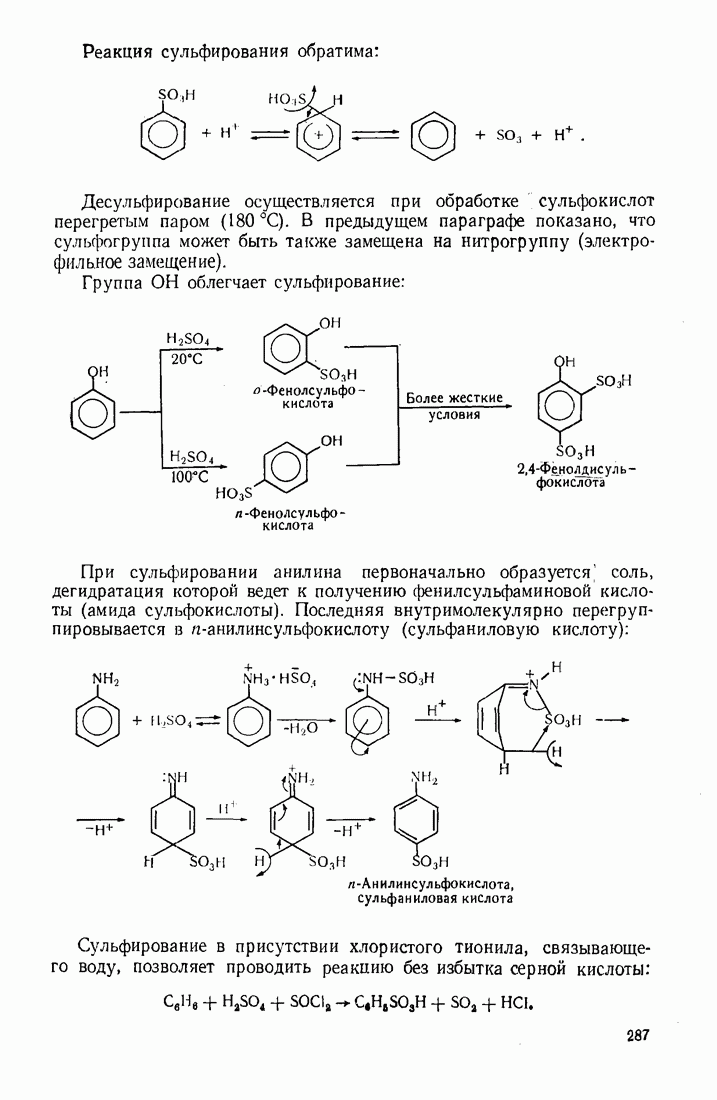
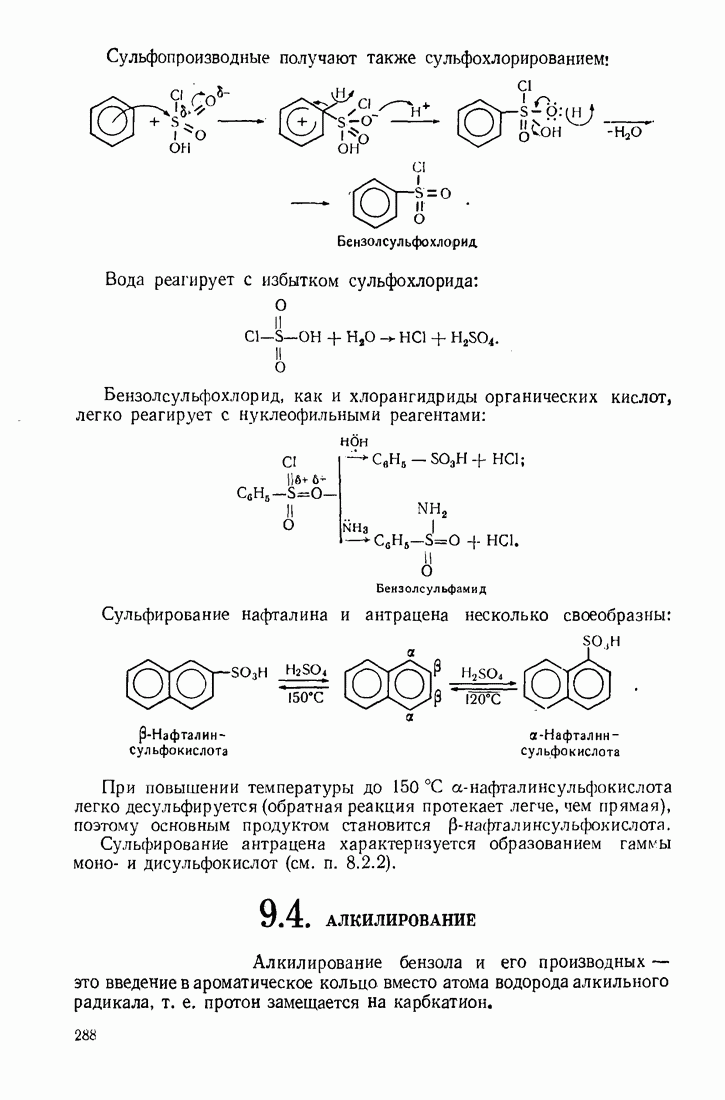
- 9.3. СУЛЬФИРОВАНИЕ
- 9.4. АЛКИЛИРОВАНИЕ
- 9.5. АЦИЛИРОВАНИЕ
- 9.6. ГИДРОКСИЛИРОВАНИЕ
- 9.7. АМИНИРОВАНИЕ
- 9.8. НИТРОЗИРОВАНИЕ
- 9.9. КАРБОНИЛИРОВАНИЕ
- 9.10. КАРБОКСИЛИРОВАНИЕ
- 9.11. ОКИСЛЕНИЕ
- 9.12. ВОССТАНОВЛЕНИЕ
- 10. Гетероциклические соединения
- 10.2. ОБЩАЯ ХАРАКТЕРИСТИКА СТРОЕНИЯ И РЕАКЦИОННОЙ СПОСОБНОСТИ
- 10.3. ПЯТИ- И ШЕСТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С ОДНИМ ГЕТЕРОАТОМОМ
- 10.4. ГЕТЕРОЦИКЛЫ С НЕСКОЛЬКИМИ ГЕТЕРОАТОМАМИ
- 10.5. МЕТОДЫ СИНТЕЗА ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ
- 10.6. П0НЯТИЕ О ПРИРОДНЫХ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЯХ
- 11. Зпементоорганические соединения
- 11.2. ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ НЕКОТОРЫХ НЕМЕТАЛЛОВ
- 11.3. МЕГАЛЛООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- 11.4. ОРГАНИЧЕСКИЕ ПРОИЗВОДНЫЕ ПЕРЕХОДНЫХ МЕТАЛЛОВ
- 12. Сырье и основные направления развития промышленности органического синтеза
- 12.1.1. Нефть и сопутствующий природный газ
- 12.1.2. Углехимическое сырье
- 12.1.3. Лесохимическое и сельскохозяйственное сырье
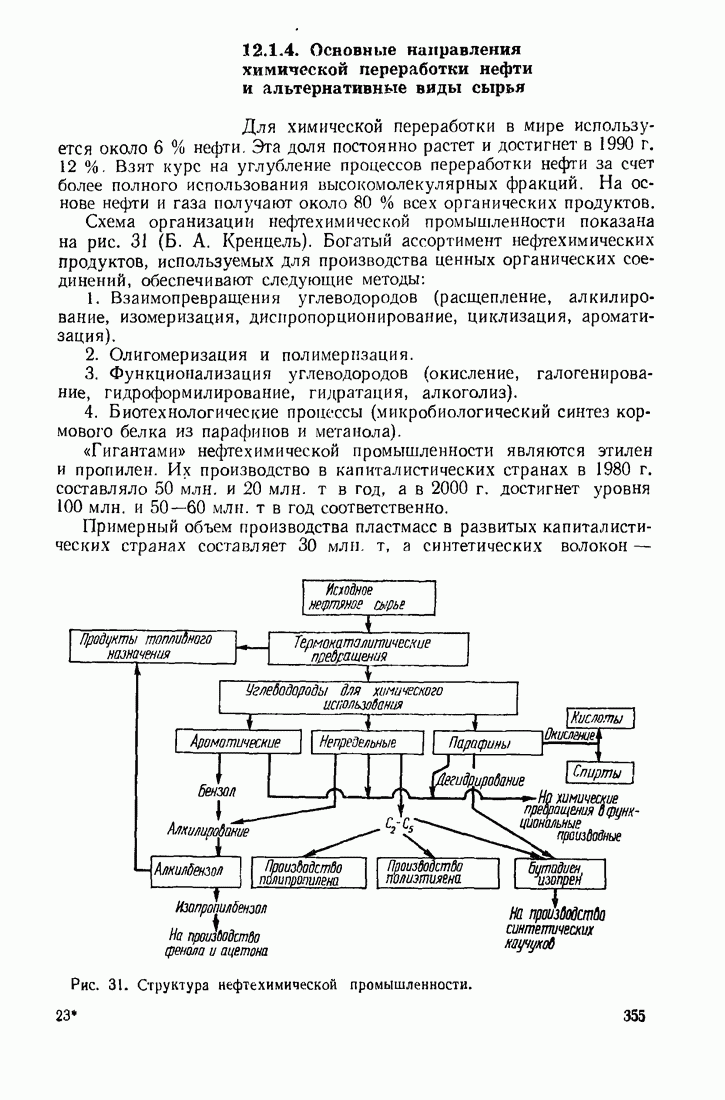
- 12.1.4. Основные направления химической переработки нефти и альтернативные виды сырья
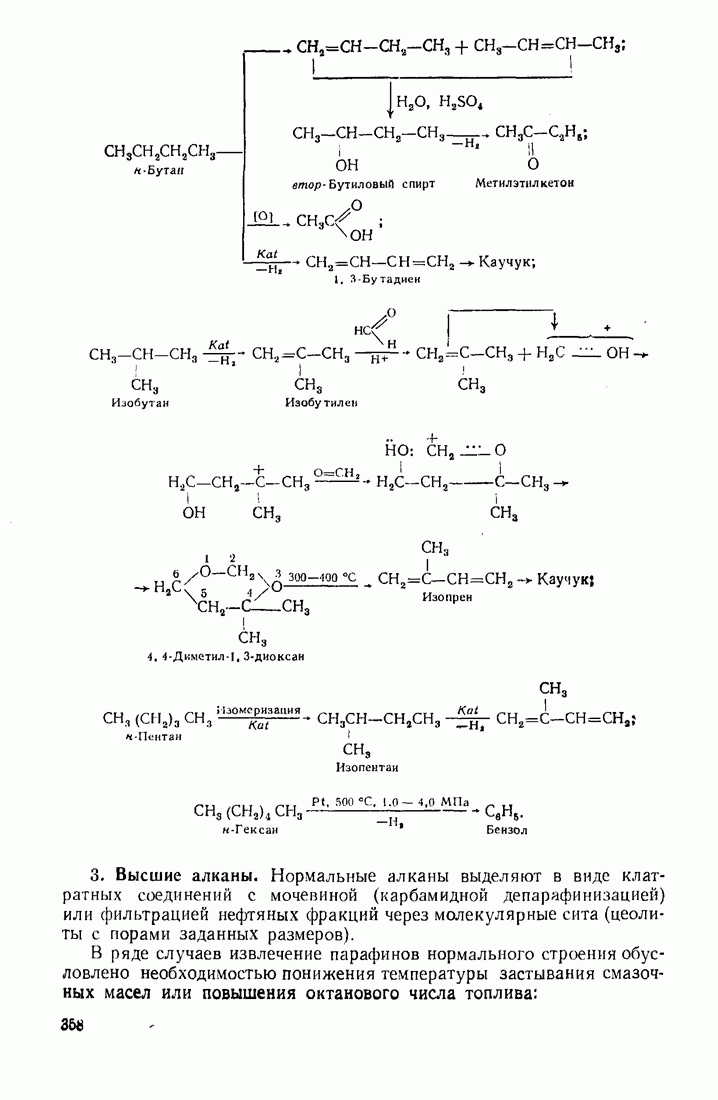
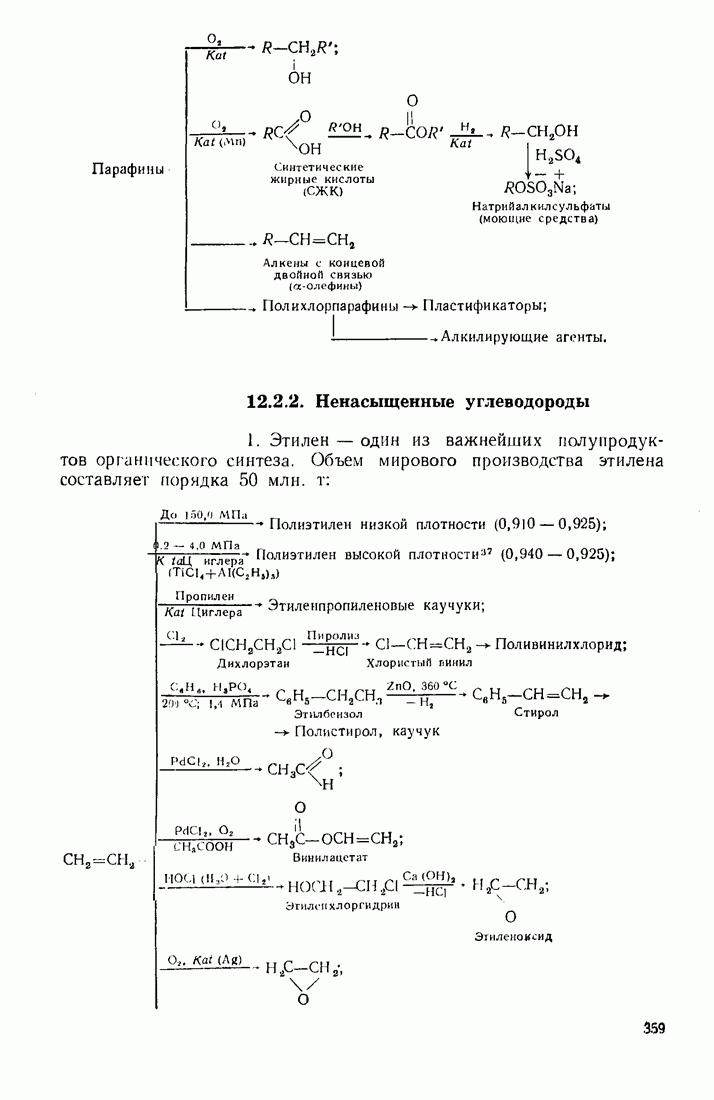
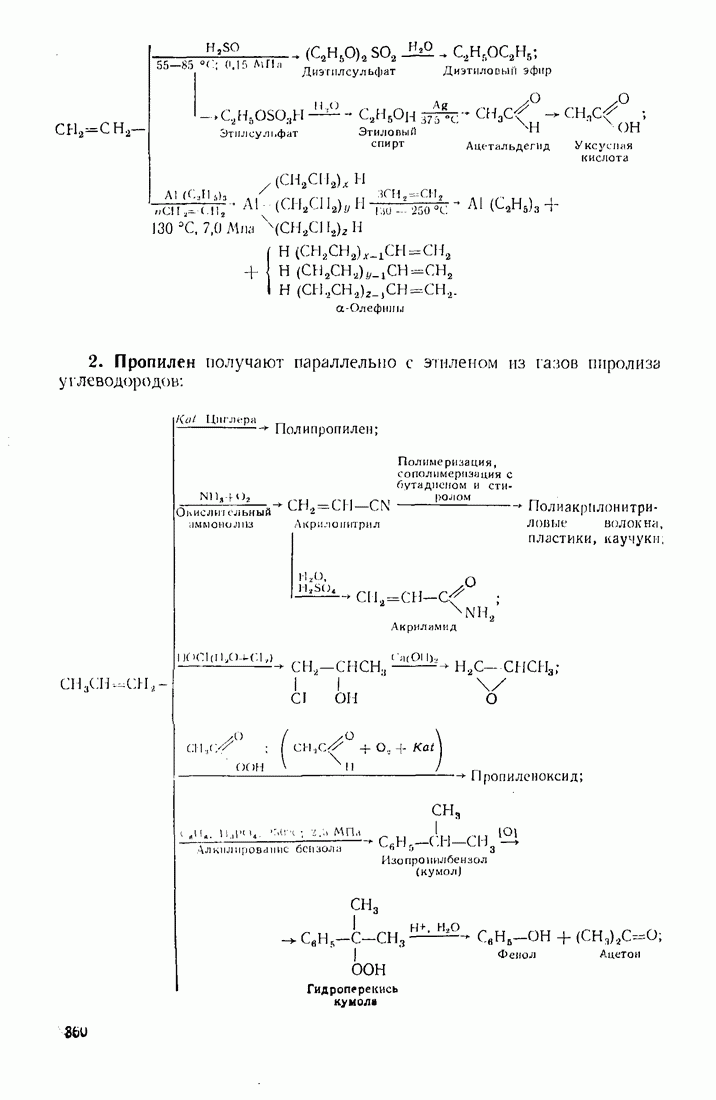
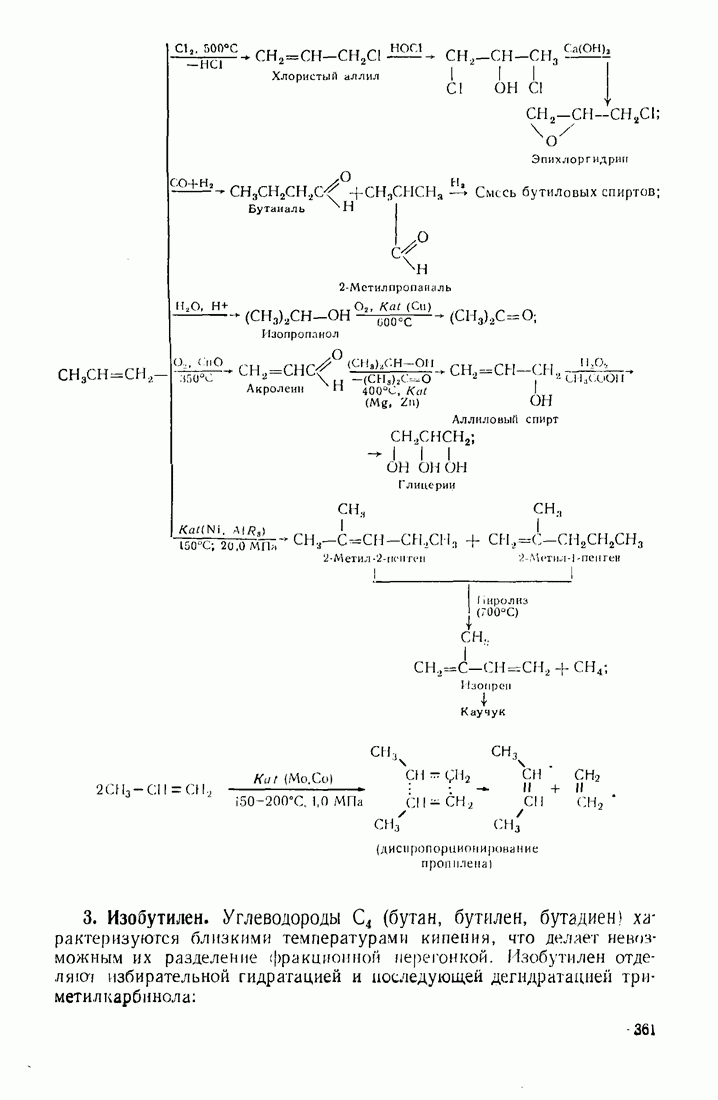
- 12.2. ПУТИ ИСПОЛЬЗОВАНИЯ УГЛЕВОДОРОДОВ И ИХ ПРОИЗВОДНЫХ
- 12.3. РАЗВИТИЕ ХИМИЧЕСКОЙ ПРОМЫШЛЕННОСТИ В СССР В ДВЕНАДЦАТОЙ ПЯТИЛЕТКЕ