| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
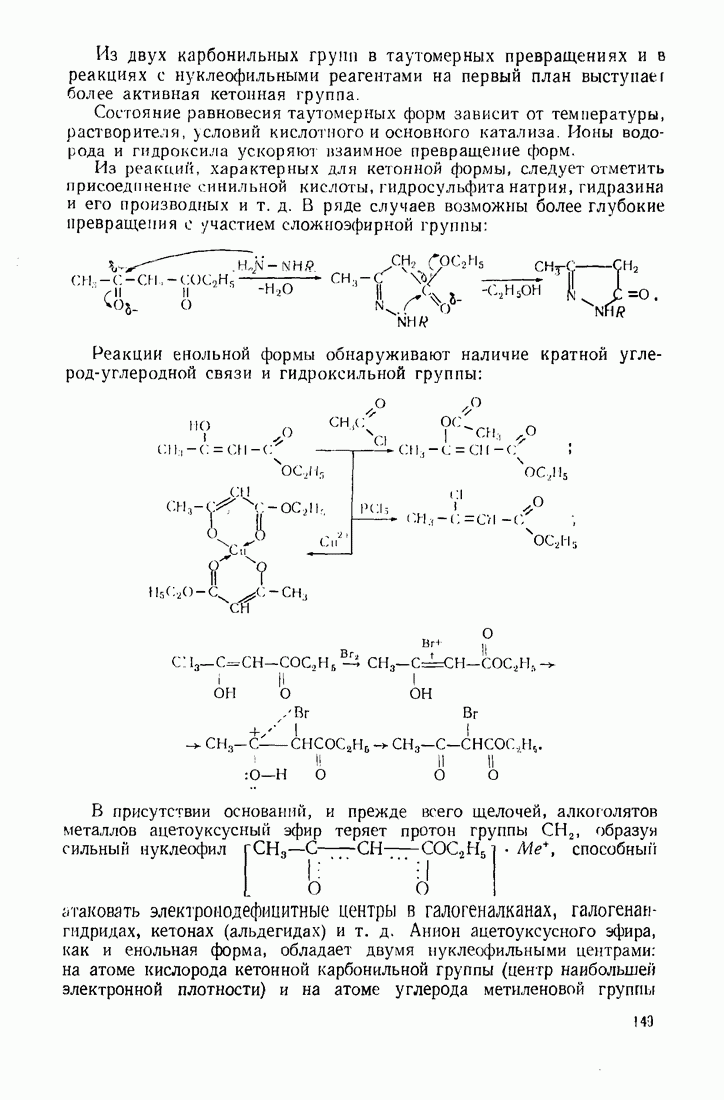
11.2. ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ НЕКОТОРЫХ НЕМЕТАЛЛОВ
11.2.1. Кремнийорганические соединения
Кремнии является ближайшим аналогом углерода но IV группе (такими же аналогами являются сера и кислород в VI группе и фосфор и азот — в V группе).
Количество электронов на внешних электронных оболочках углерода и кремния одинаково (рис. 28).
Особенности химических свойств кремния обусловлены тем, что в образовании связей могут участвовать  -орбитали, близкие по энергии
-орбитали, близкие по энергии  и
и  -орбиталям.
-орбиталям.
Энергия связи  на
на  меньше, чем связи
меньше, чем связи  Поэтому силаны
Поэтому силаны  в отличие от алканов
в отличие от алканов  неустойчивы
неустойчивы
и легко окисляются. В то же время связь  прочнее связи
прочнее связи  Это определяет ярко выраженную способность кремния образовывать силоксановые связи
Это определяет ярко выраженную способность кремния образовывать силоксановые связи 


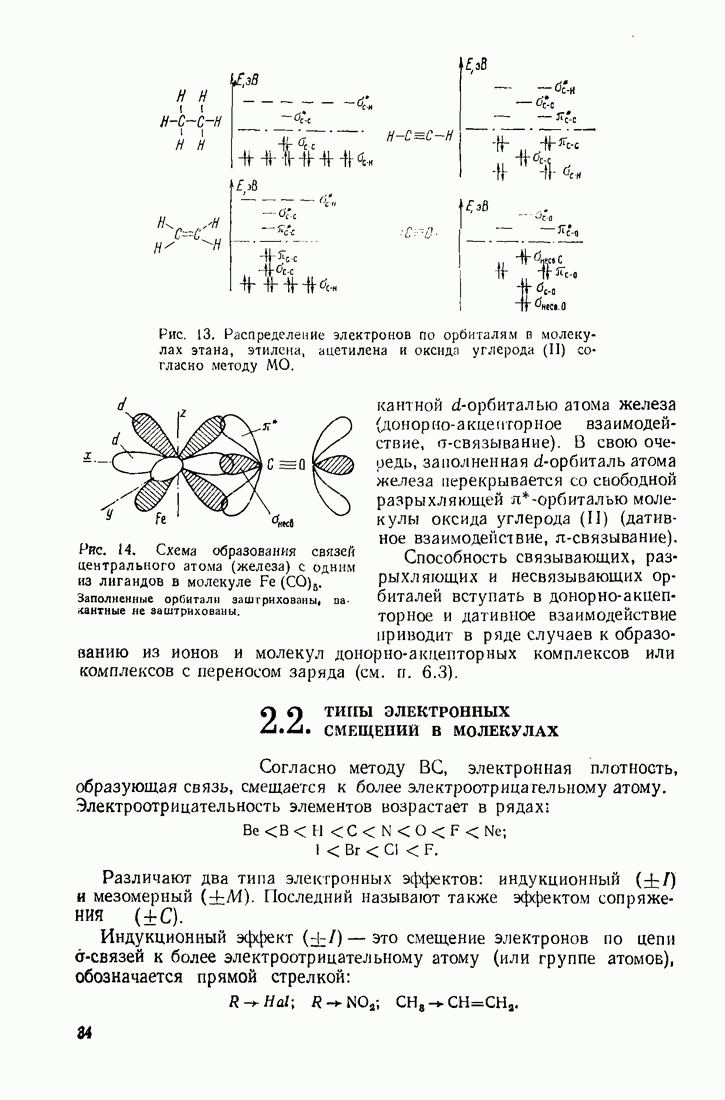
Рис. 28. Электронное строение атомов углерода (а) и кремния (б).
Подобно сере и фосфору кремний не способен образовывать  -связи, поскольку боковое перекрывание орбиталей типа
-связи, поскольку боковое перекрывание орбиталей типа  и
и  неэффективно. Вот почему кремний не образует соединений, подобных алкенам и алкинам. Вместе с тем с элементами, обладающими неподеленнымп парами электронов — кислородом, азотом, галогенами, кремний образует своеобразные двойные связи за счет дативного взаимодействия. Пару электронов соседнего атома кремний принимает на вакантную
неэффективно. Вот почему кремний не образует соединений, подобных алкенам и алкинам. Вместе с тем с элементами, обладающими неподеленнымп парами электронов — кислородом, азотом, галогенами, кремний образует своеобразные двойные связи за счет дативного взаимодействия. Пару электронов соседнего атома кремний принимает на вакантную  -орбиталь:
-орбиталь:

Взаимодействие такого типа обусловливает пониженную основность трисилиламинов и повышенную кислотность триалкилсиланолов:

Органоспланы и галогениды кремния более реакционноспособны, чем подобные соединения углерода.
Поскольку кремний более электроположителен, чем углерод, водород и тем более галоген, связи  довольно лабильны. Галогениды кремния настолько легко гидролизуют, что дымят на воздухе.
довольно лабильны. Галогениды кремния настолько легко гидролизуют, что дымят на воздухе.
Источником кремнийорганических соединении является кремнезем  из которого получают элементарный кремний и тетрагалогениды кремния:
из которого получают элементарный кремний и тетрагалогениды кремния:

Алкилированием и арилированием кремния получают органосиланы:

Атомы галогена и водорода, связанные с кремнием, можно замещать на алкильный радикал:

В реакциях кремний становится объектом атаки нуклеофильных реагентов, а углерод, водород и галоген — электрофильных:

Связь  разрывается при действии сильных злектрофилов
разрывается при действии сильных злектрофилов  и нуклеофилов
и нуклеофилов 
(см. скан)
Группа  связанная с атомом кремния, сохраняет нуклеофильные свойства. Важнейшим свойством силандиолов
связанная с атомом кремния, сохраняет нуклеофильные свойства. Важнейшим свойством силандиолов  является конденсация с образованием полисилоксанов (силиконовых полимеров). Реакция может катализироваться как кислотами, так и основаниями;
является конденсация с образованием полисилоксанов (силиконовых полимеров). Реакция может катализироваться как кислотами, так и основаниями;

Основания повышают нуклеофнльность реагента]

11.2.2. Борорганические соединения
На внешнем электронном слое атом бора имеет четыре орбитали, на которых расположены три электрона (рис. 29).
В соединениях бор может быть трех- или четырехковалентным.
Типичные соединения трехвалентного бора: борная кислота В гидрид бора (боран)
гидрид бора (боран)  фторид бора
фторид бора  триметилбор (три-метилборан)
триметилбор (три-метилборан) 
Соединения трехвалентного бора проявляют склонность к заполнению парой электронов четвертой вакантной орбитали, выступая, таким образом, в роли кислоты Льюиса. В качестве доноров электронов могут выступать анионы и нуклеофильные реагенты, обладающие неподеленными парами электронов (щелочи, амины, спирты, простые эфиры и т. д.):


Рис. 29. Электронное строение атома бора.
Родоначальником производных трехвалентного бора можно считать гидрид бора. Однако, являясь крайне реакционноспособным, он легко димеризуется, образуя диборан 
Известны также полибораны: тетраборан  пентаборан
пентаборан  гексаборан
гексаборан  и др.
и др.
Диборан является примером связывания двух молекул трехцентровыми орбиталями:

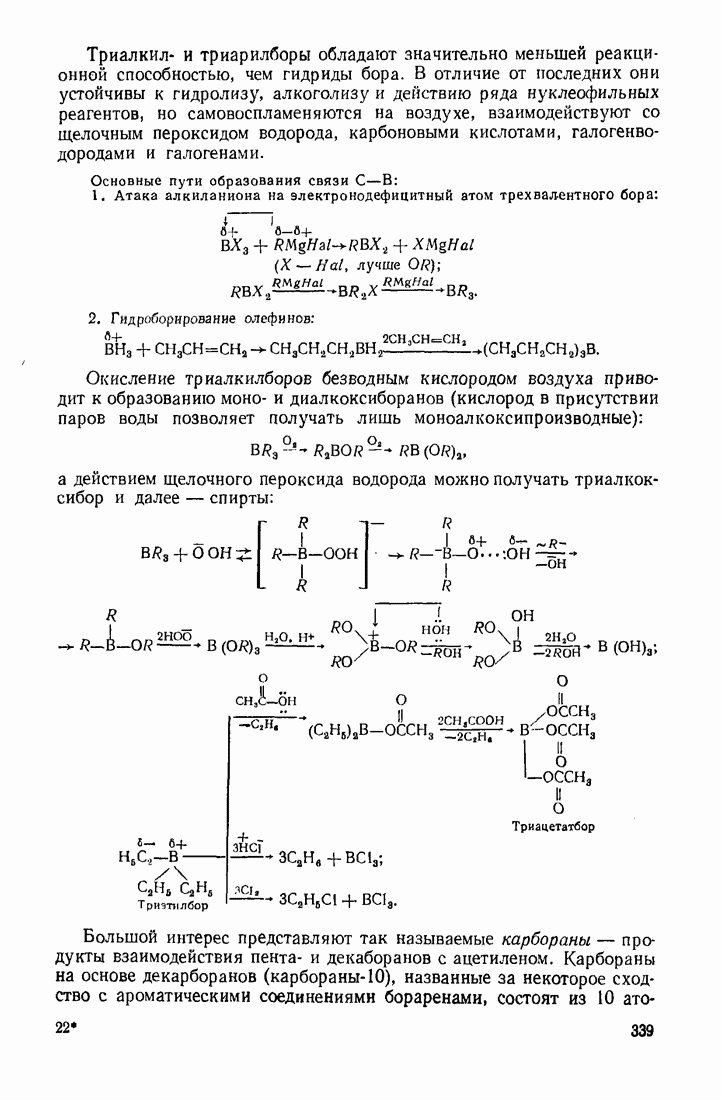
Триалкил- и триарилборы обладают значительно меньшей реакционной способностью, чем гидриды бора. В отличие от последних они устойчивы к гидролизу, алкоголизу и действию ряда нуклеофильных реагентов, но самовоспламеняются на воздухе, взаимодействуют со щелочным пероксидом водорода, карбоновыми кислотами, галогенводородами и галогенами.
Основные пути образования связи 
1. Атака алкиланиона на электронодефицитный атом трехвалентного бора:

2. Гидроборирование олефинов:

Окисление триалкилборов безводным кислородом воздуха приводит к образованию моно- и диалкоксиборанов (кислород в присутствии паров воды позволяет получать лишь моноалкоксипроизводные):

а действием щелочного пероксида водорода можно получать триалкоксибор и далее — спирты:
(см. скан)
Большой интерес представляют так называемые карбораны — продукты взаимодействия пента- и декаборанов с ацетиленом. Карбораны на основе декарборанов  названные за некоторое сходство с ароматическими соединениями бораренами, состоят из 10 атомов
названные за некоторое сходство с ароматическими соединениями бораренами, состоят из 10 атомов
бора и двух атомов углерода и образуют двадцатигранники, в которых каждый атом углерода связан с пятью атомами бора и одним атомом водорода.
Несмотря на чрезвычайно высокую устойчивость к действию кислот и окислителей, а также термическую стабильность карбораиа (до 600 °С), атомы водорода в его молекуле при действии литийалканов и алкилмагнийгалогенидов замещаются на металл. Далее могут образовываться ряды производных (спиртов, кислот и т. д.).
Известны также весьма своеобразные соединения на основе боразола:

Боразол, как и карбораиы, также проявляет сходство с бензолом, хотя в силу полярности связей  можно ожидать, что он более реакционноспособен.
можно ожидать, что он более реакционноспособен.
Атом водорода у атомов азота может быть замещен на алкильный радикал, а у атомов бора — на алкил или галоген.
В настоящее время проводятся работы по синтезу полимеров, содержащих боразольные кольца.
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие
- 1. Введение
- 1.1. Предмет органической химии
- 1.2. Основные этапы развития органической химии
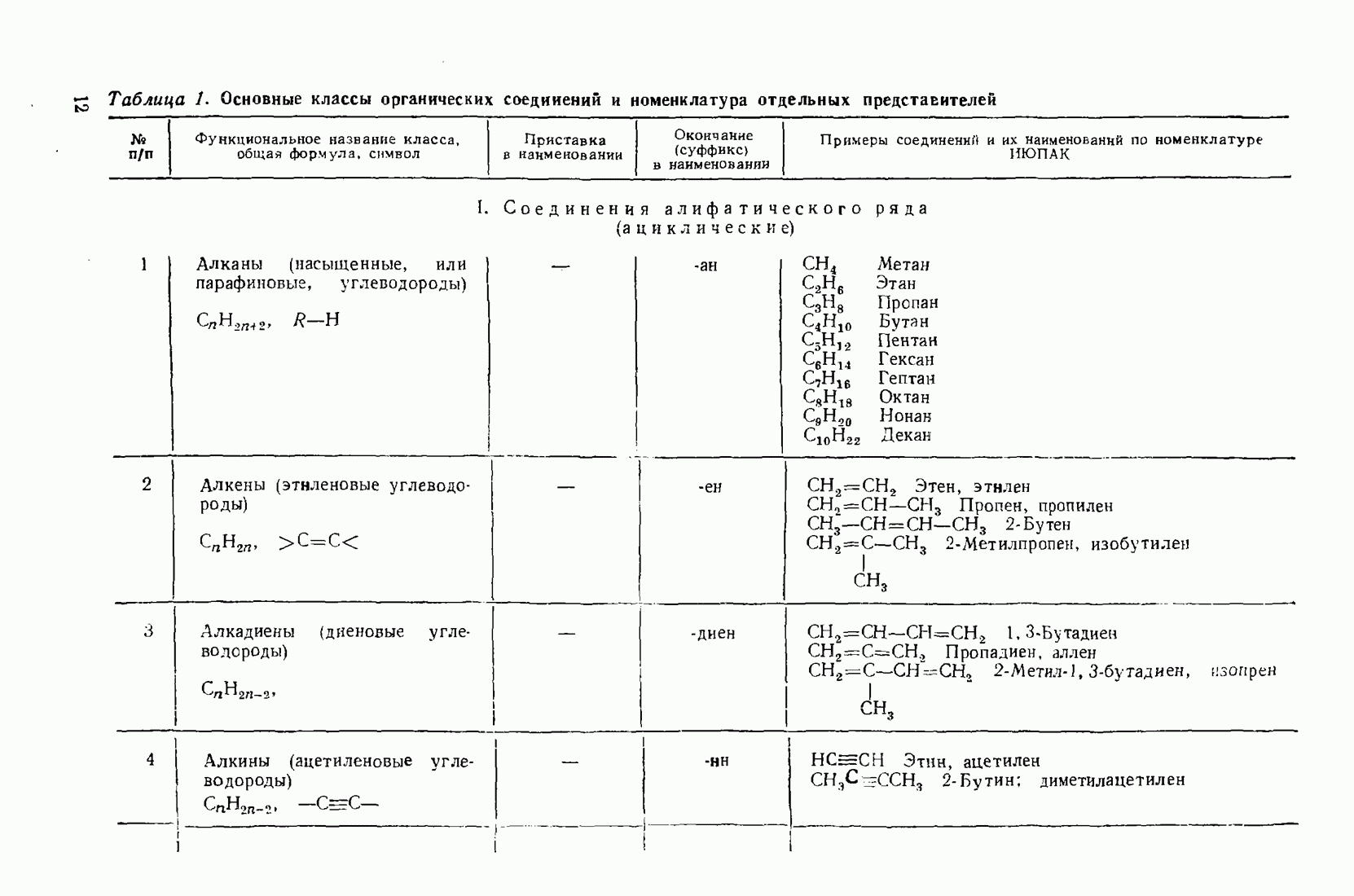
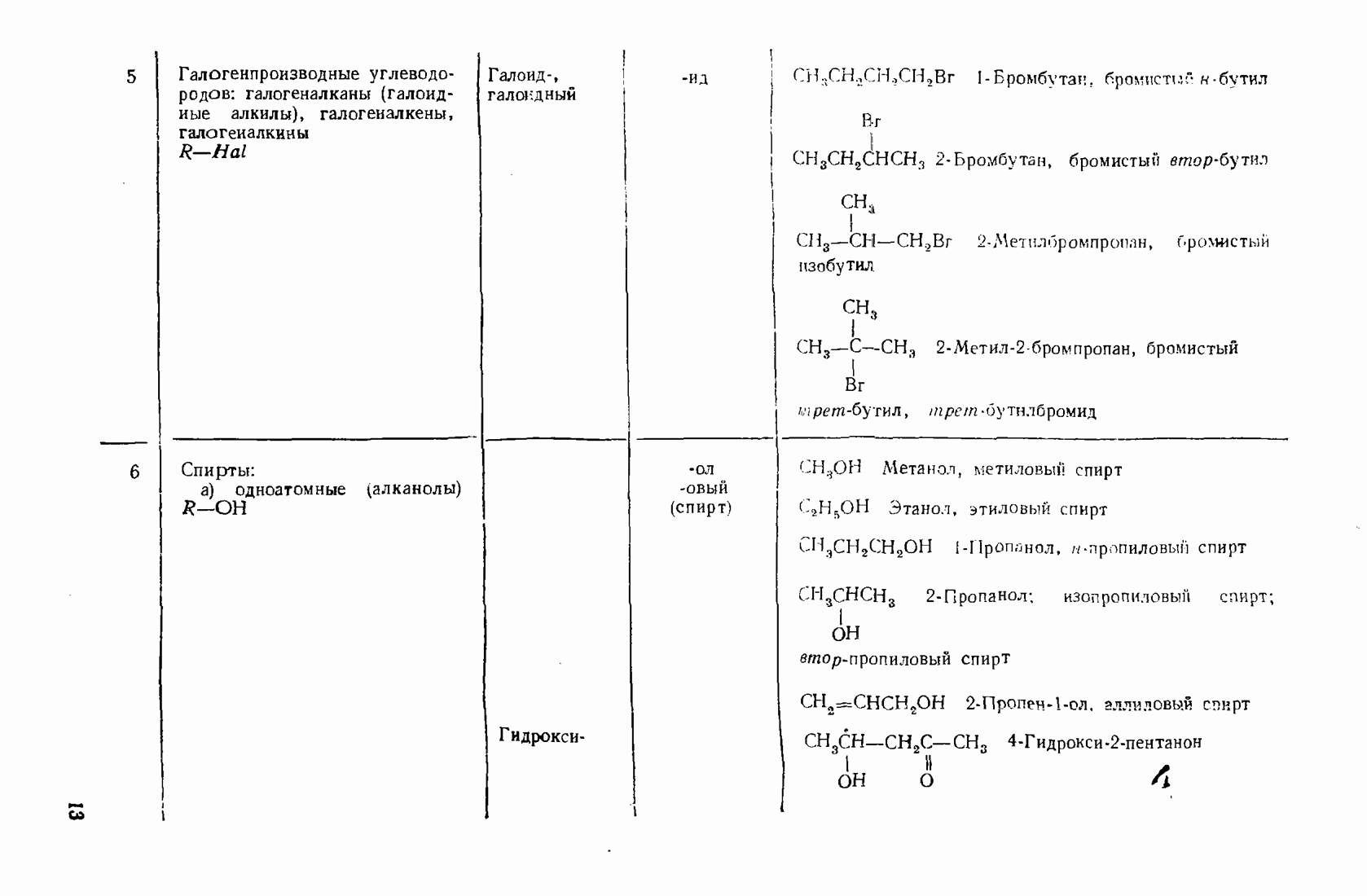
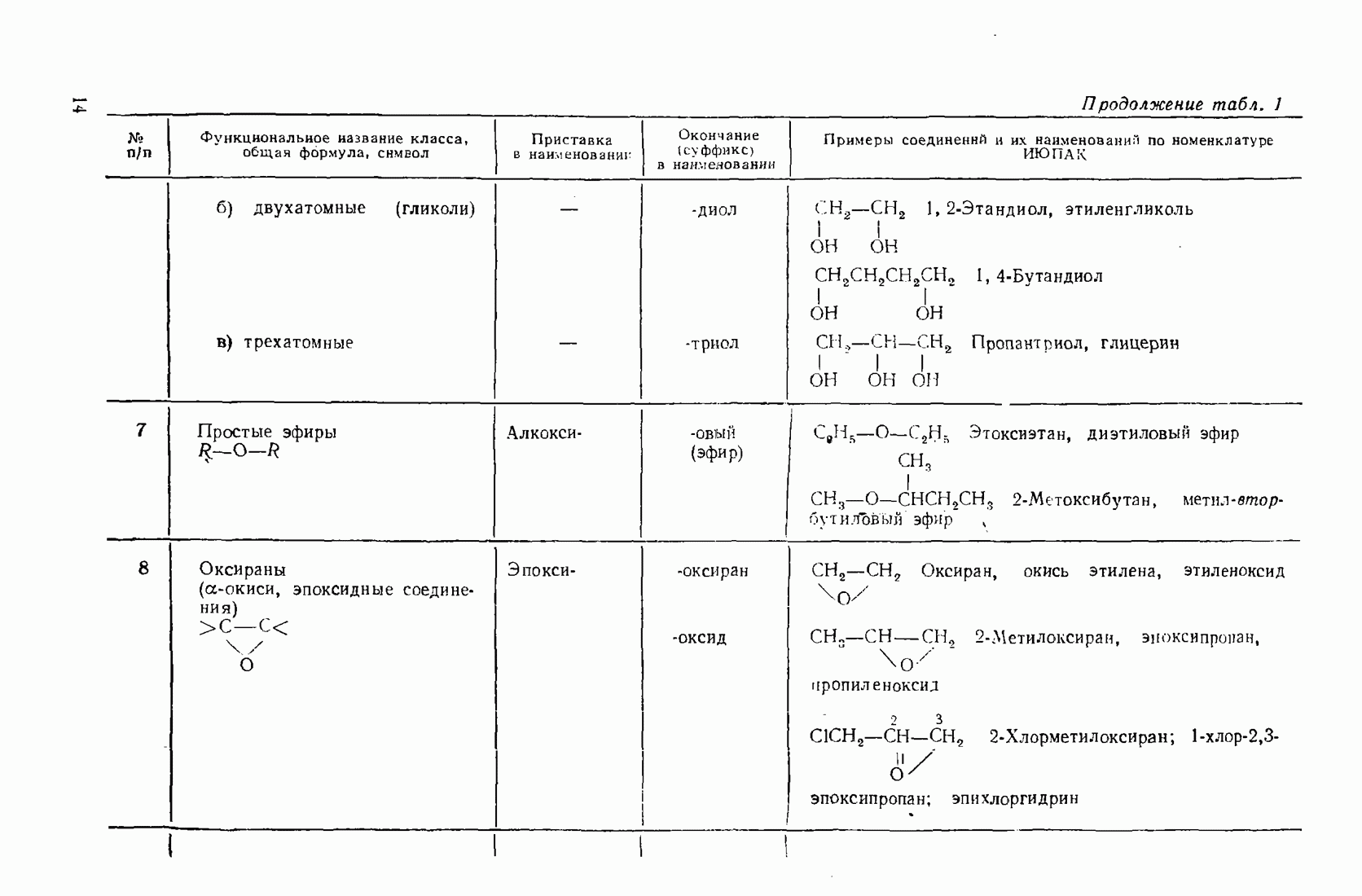
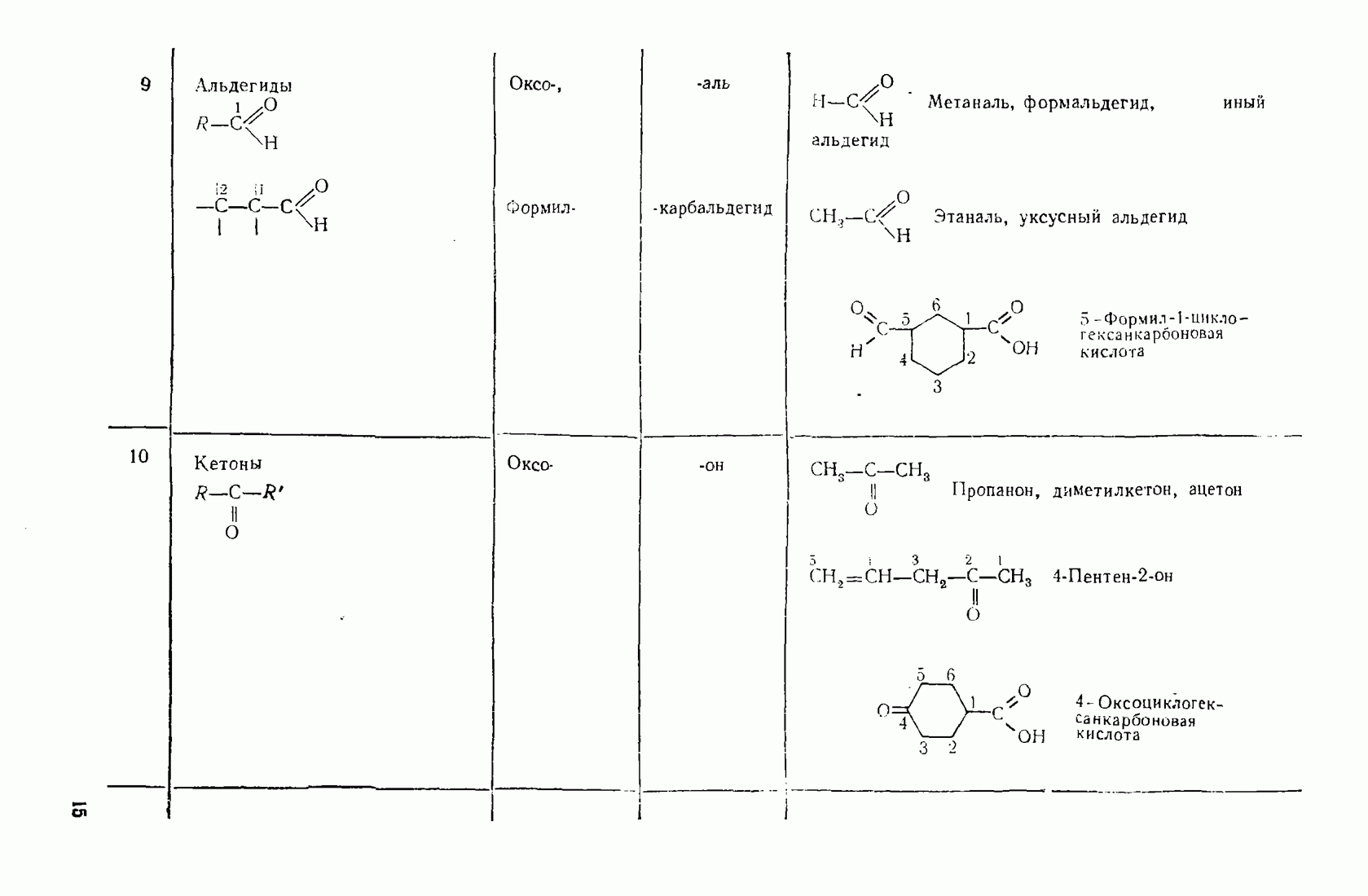
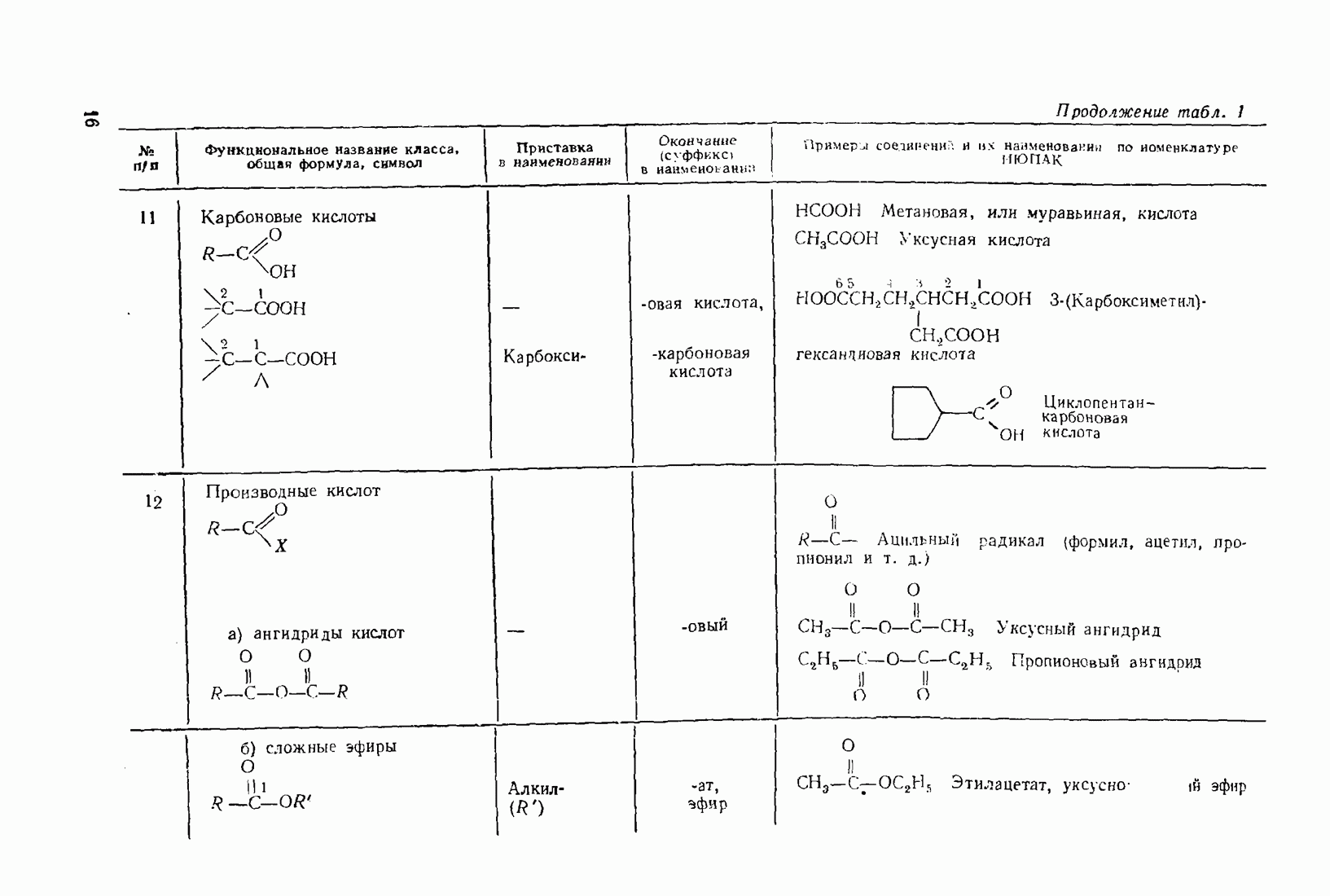
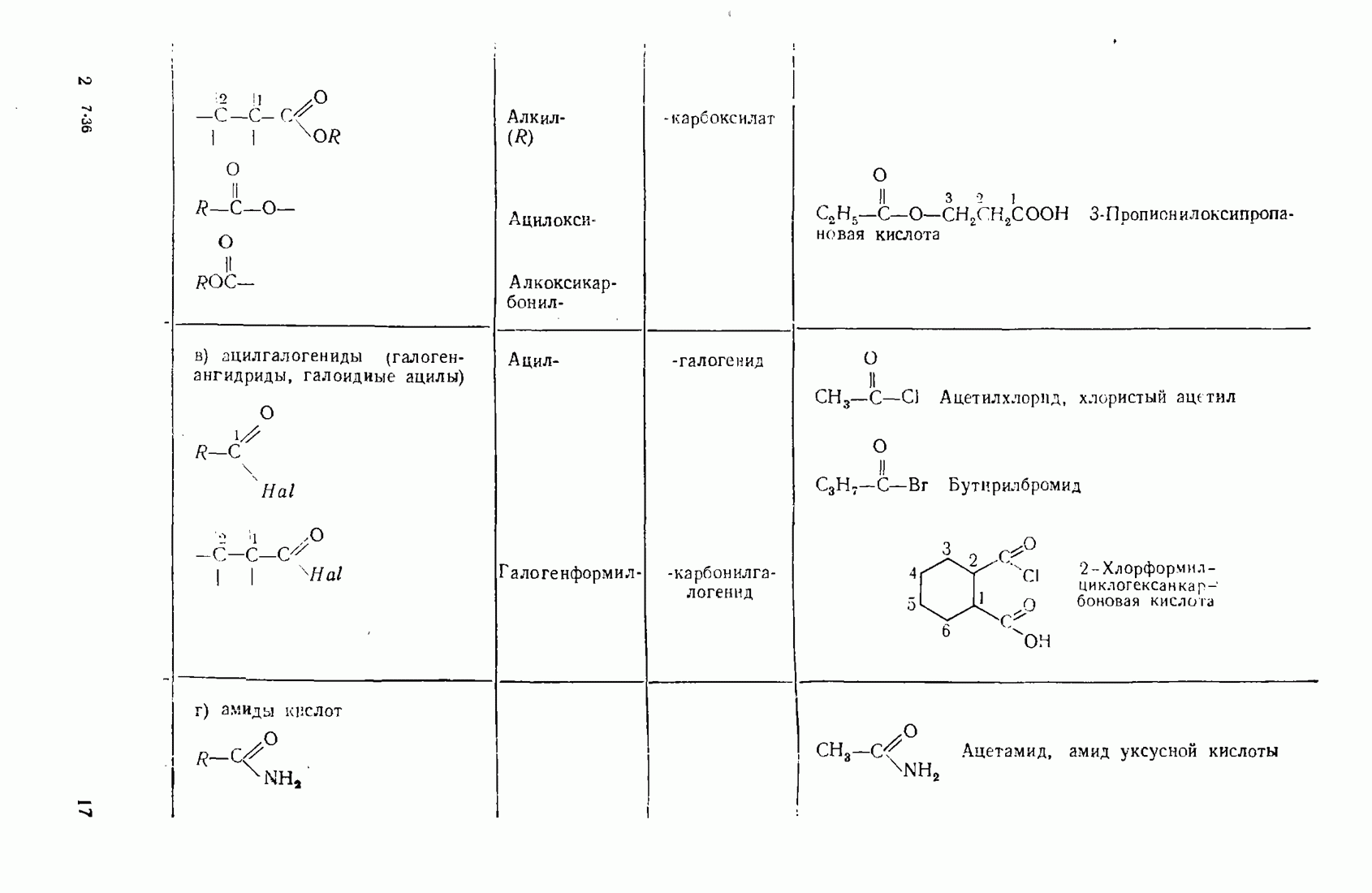
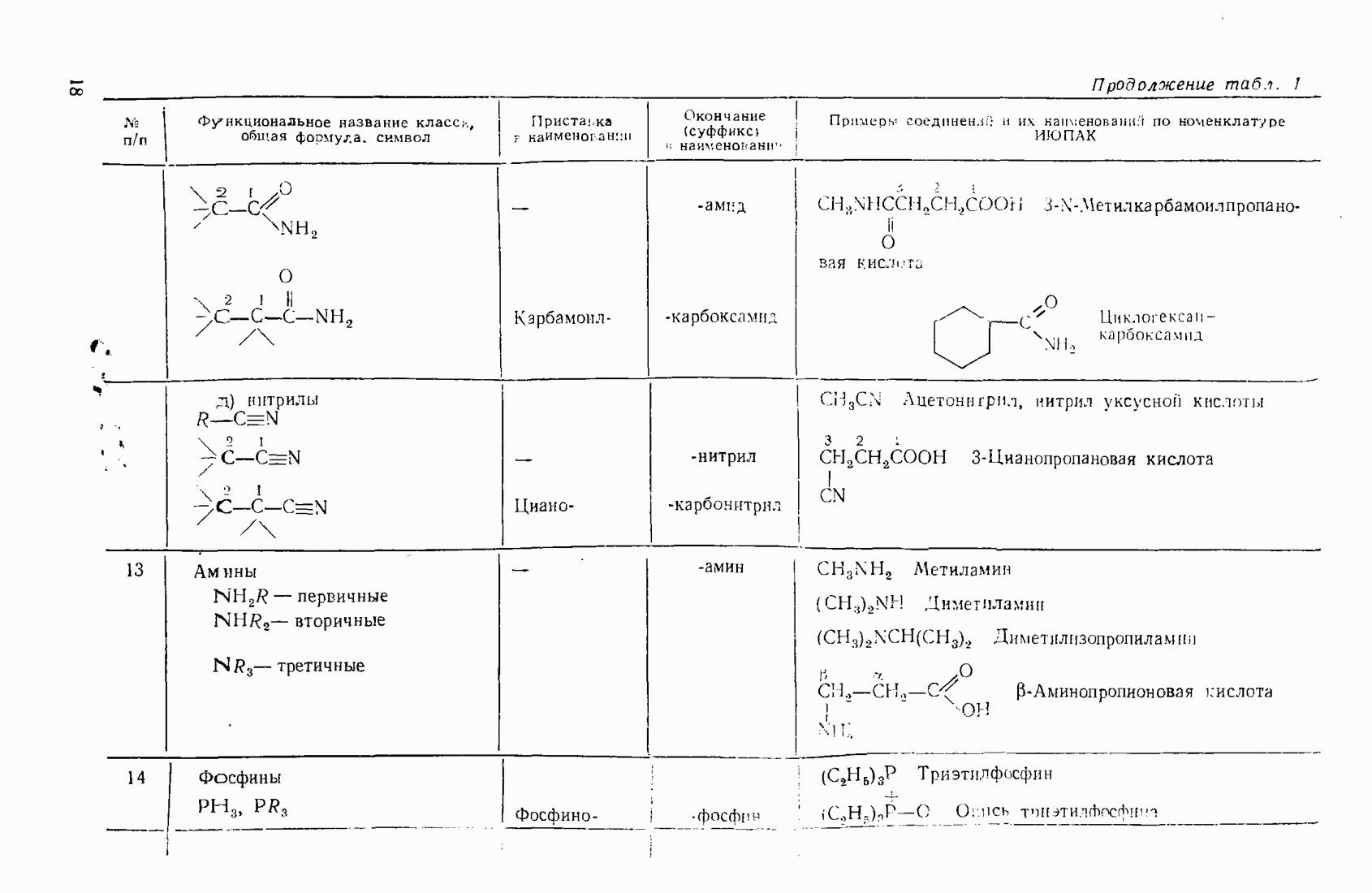
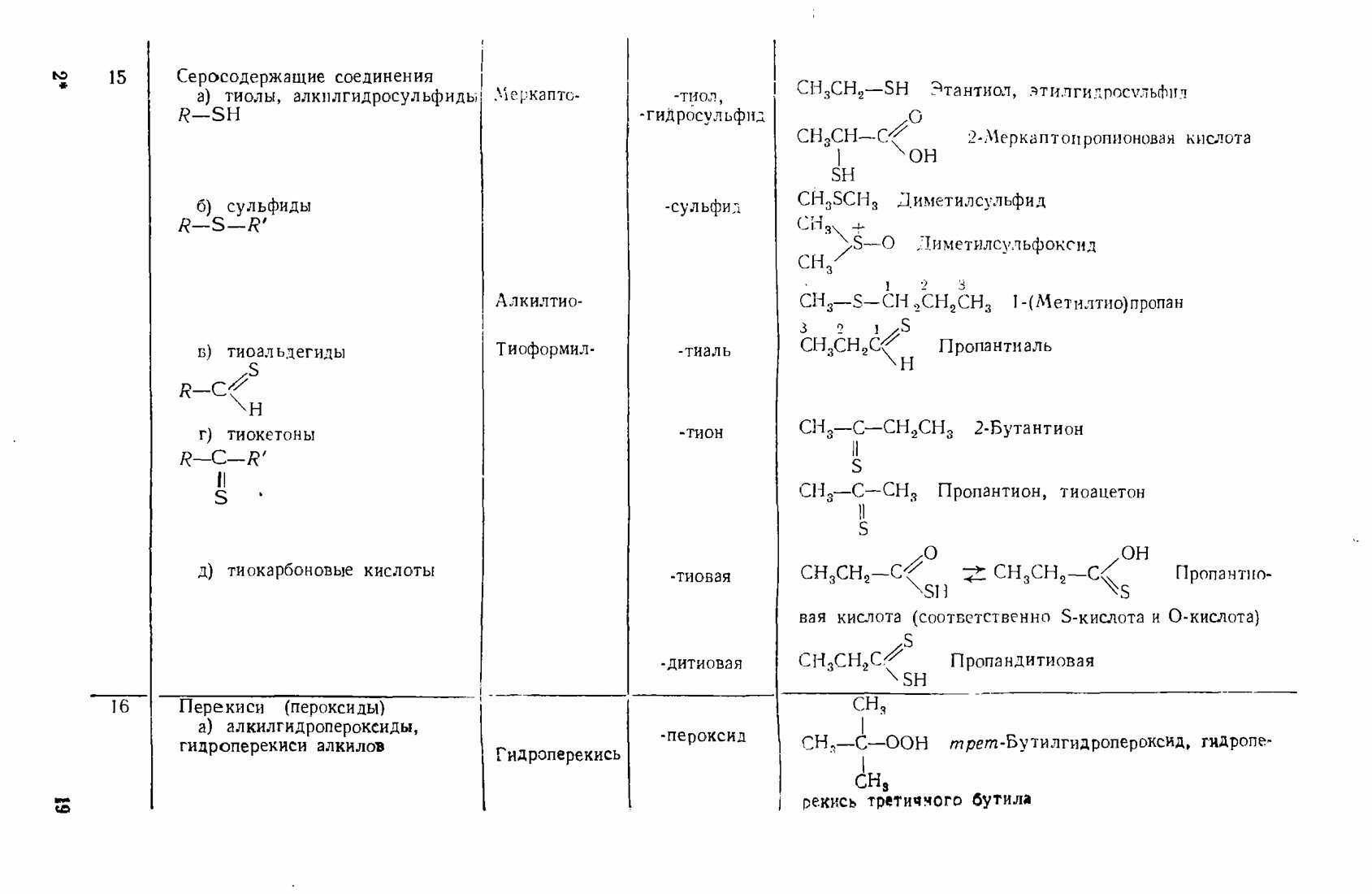
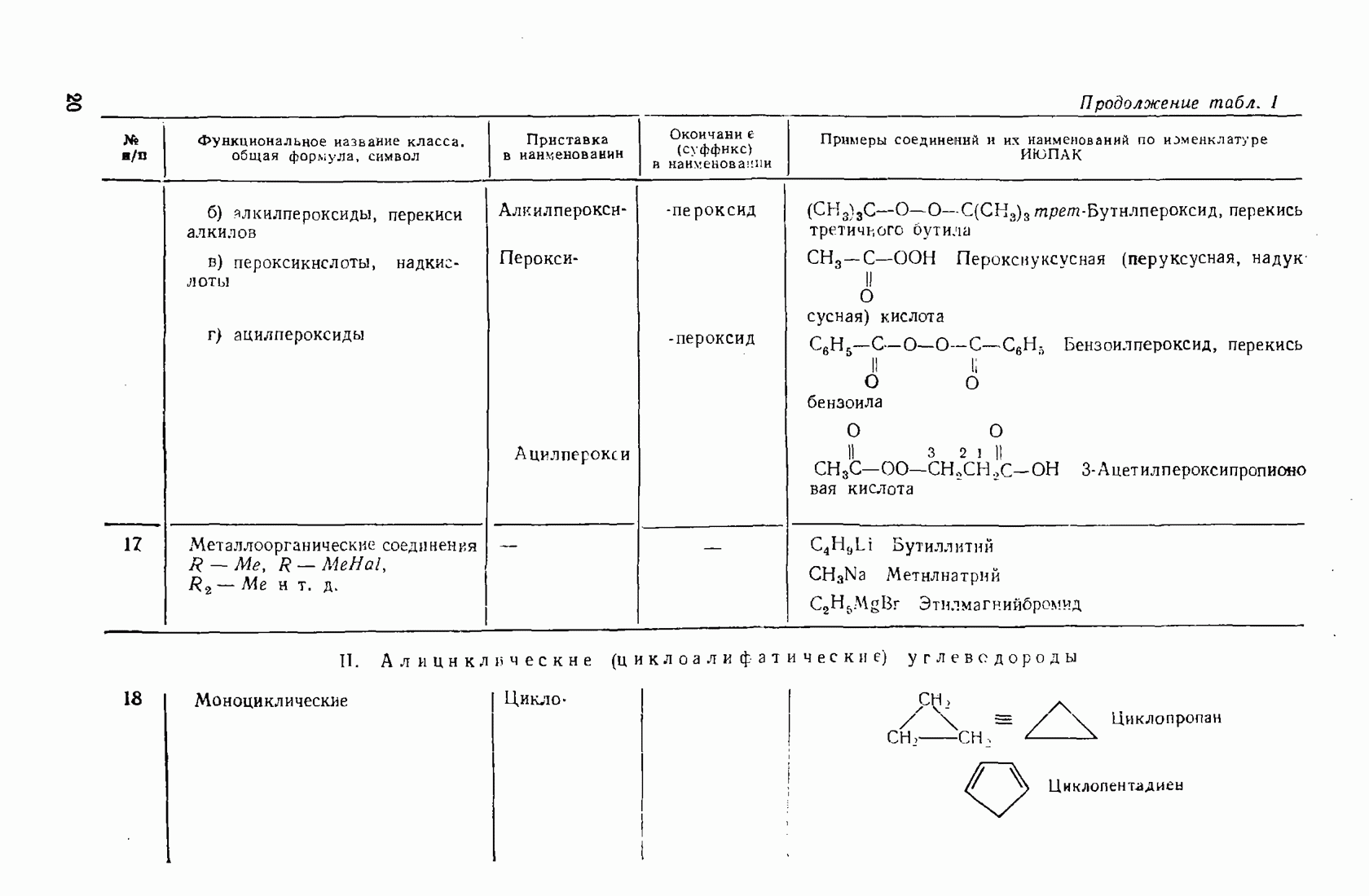
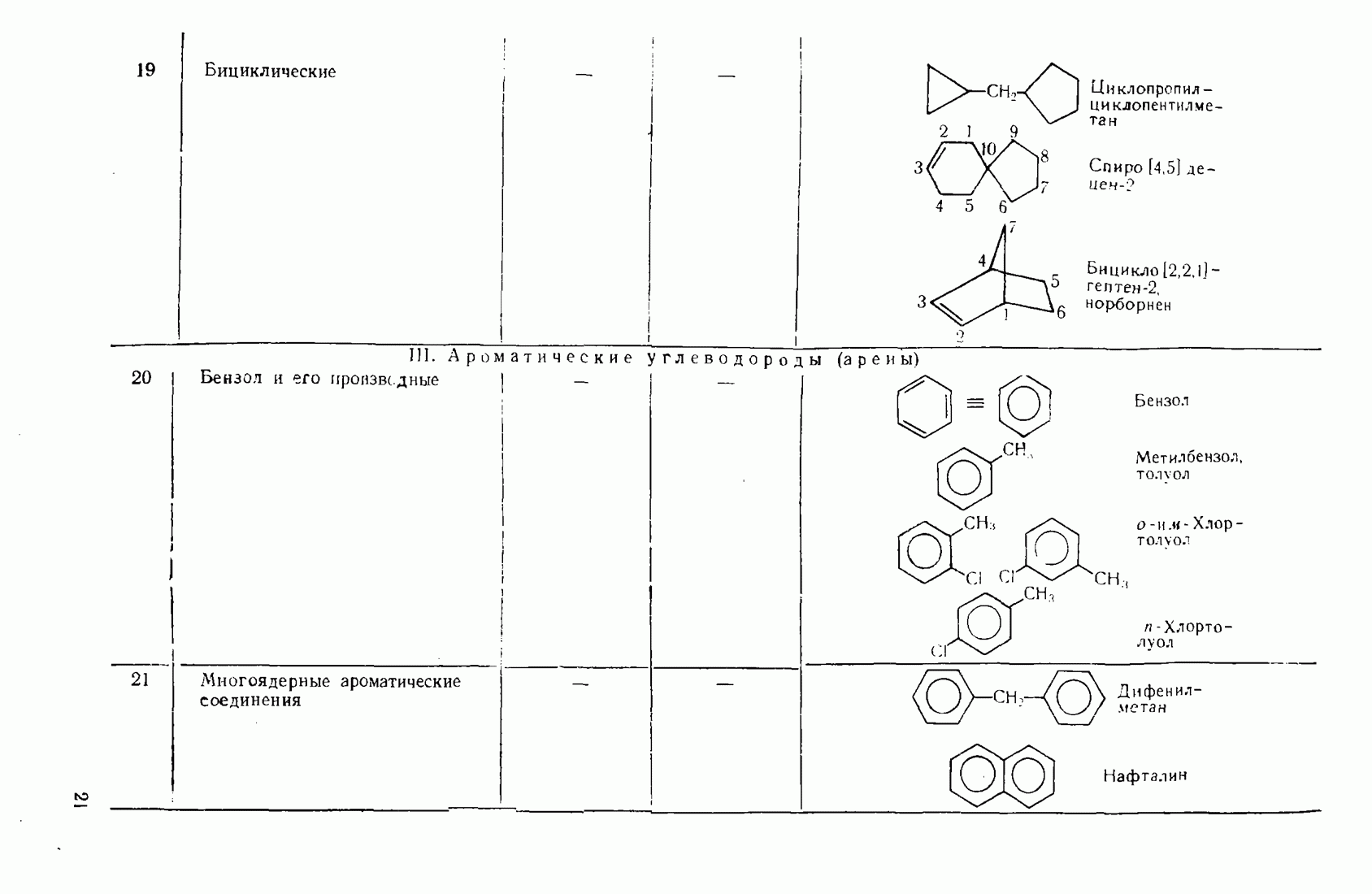
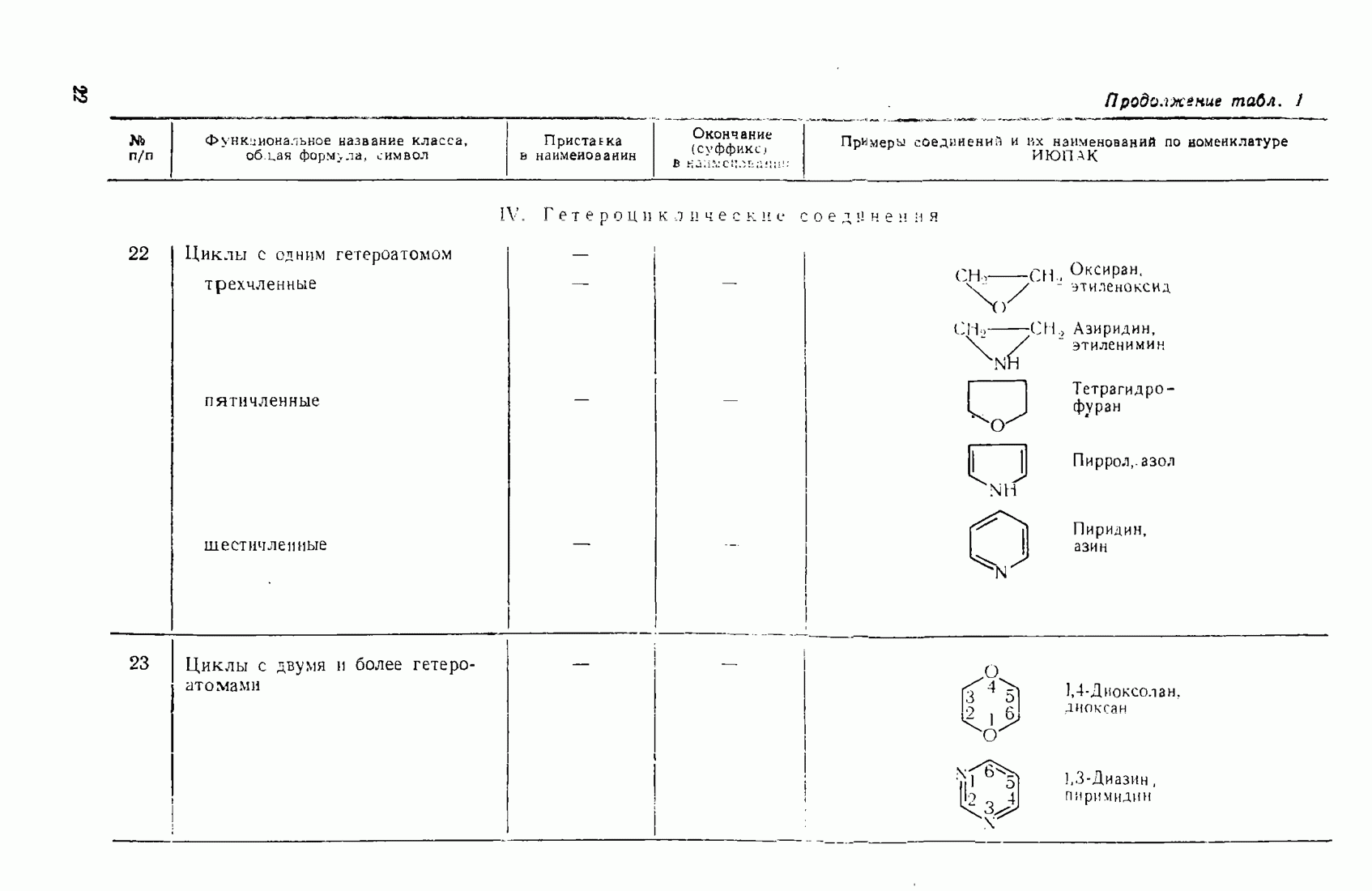
- 1.3. Классификация и номенклатура органических соединений
- 2 Общие теоретические положения органической химии
- 2.1. Природа химической связи
- 2.1.1. Типы химических связей
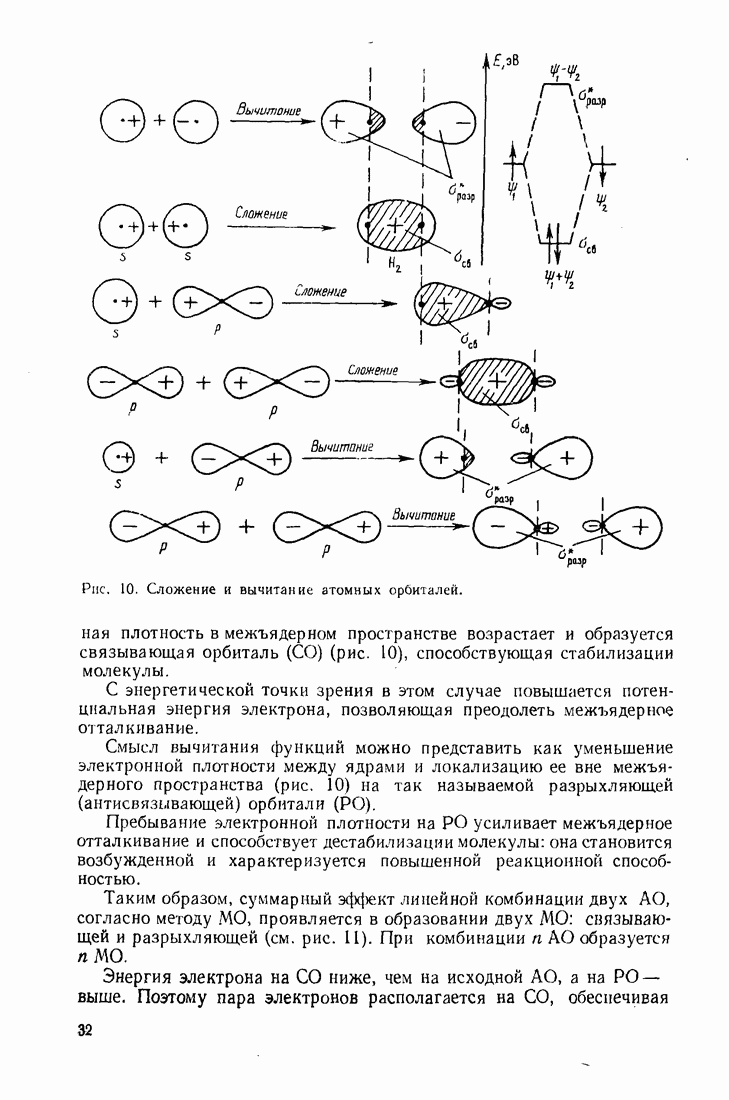
- 2.1.2. Молекулярные орбитали
- 2.2. ТИПЫ ЭЛЕКТРОННЫХ СМЕЩЕНИЙ В МОЛЕКУЛАХ
- 2.3. ОБЩИЕ ПРЕДСТАВЛЕНИЯ ОБ ОРГАНИЧЕСКОЙ РЕАКЦИИ
- 2.4. КЛАССИФИКАЦИЯ РЕАГЕНТОВ И РЕАКЦИЙ
- 2.5. КРАТКАЯ ХАРАКТЕРИСТИКА РЕАКЦИОННОЙ СПОСОБНОСТИ НЕКОТОРЫХ СОЕДИНЕНИЙ АЛИФАТИЧЕСКОГО РЯДА
- 2.5.1. Алканы (парафины)
- 2.5.2. Непредельные углеводороды
- 2.5.3. Галогеналканы (галоидные алкилы R-Hal)
- 2.5.4. Спирты (R0Н)
- 2.5.5. Альдегиды и кетоны
- 2.5.6. Карбоновые кислоты (R-СООН) и их производные (R-СО-X)
- 2.5.7. Амины (NH2R, NHR2, NR3)
- 3. Реакционная способность соединений алифатического ряда
- 3.1. Алканы (насыщенные углеводороды)
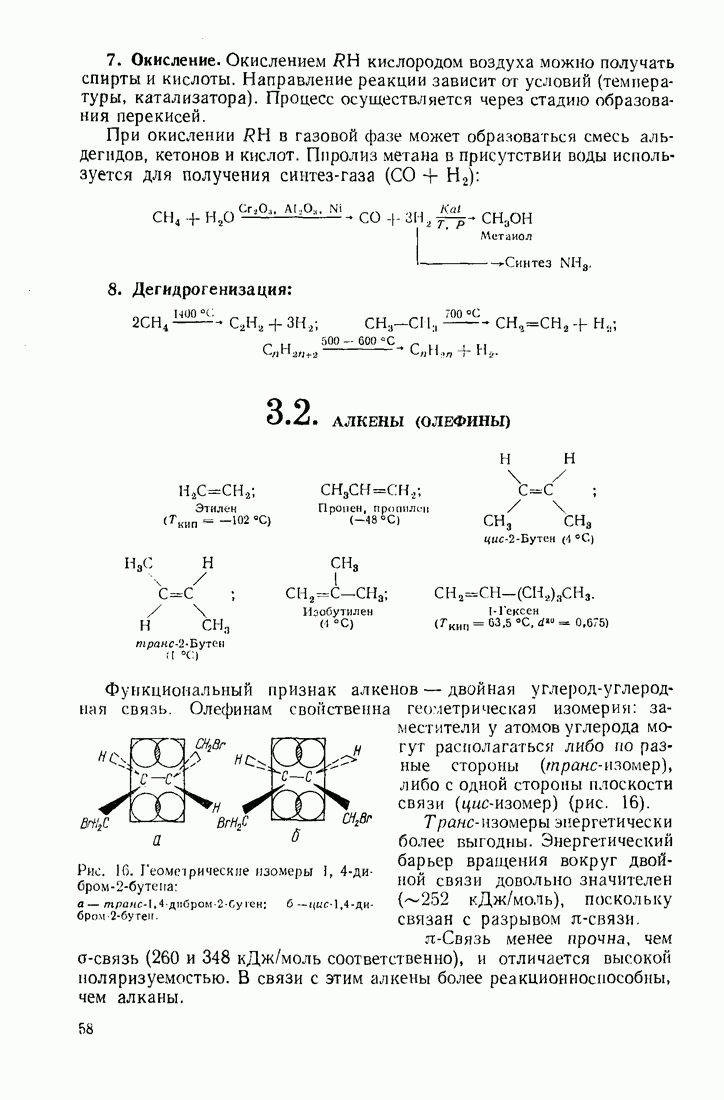
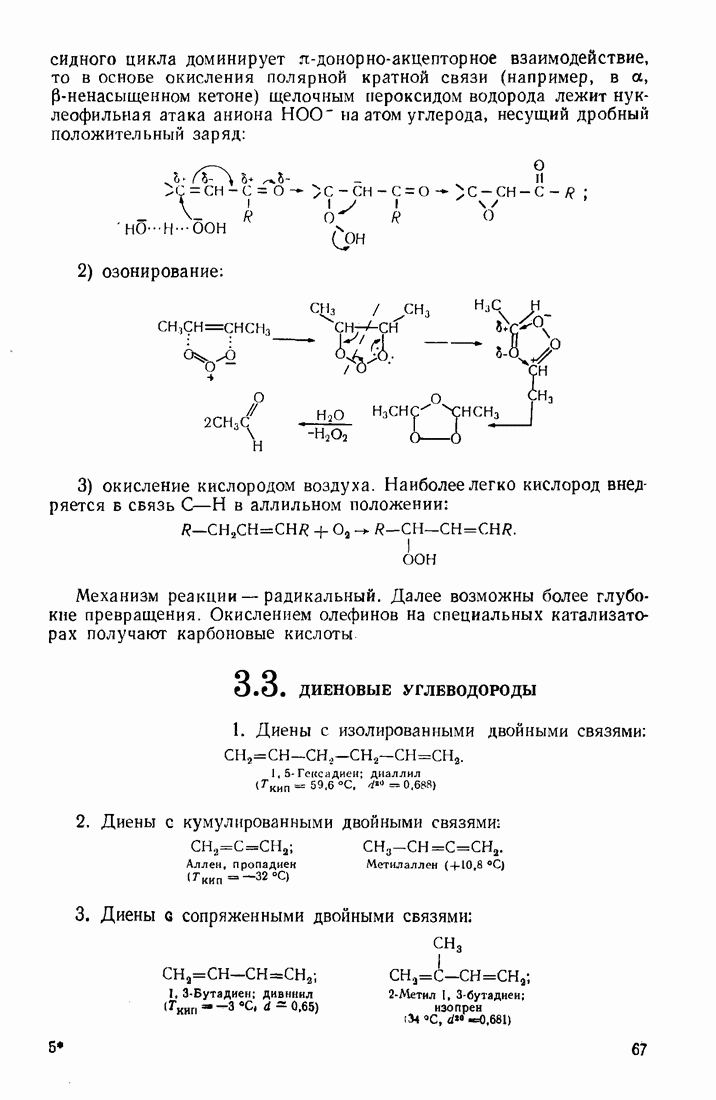
- 3.2. АЛКЕНЫ (ОЛЕФИНЫ)
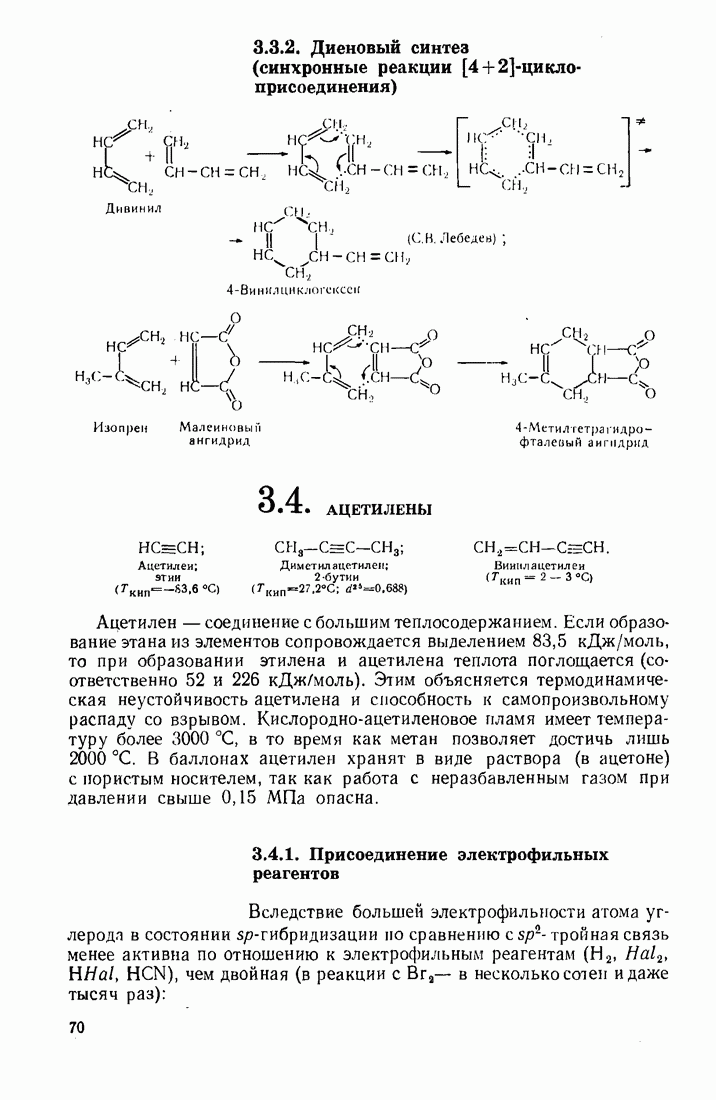
- 3.3. ДИЕНОВЫЕ УГЛЕВОДОРОДЫ
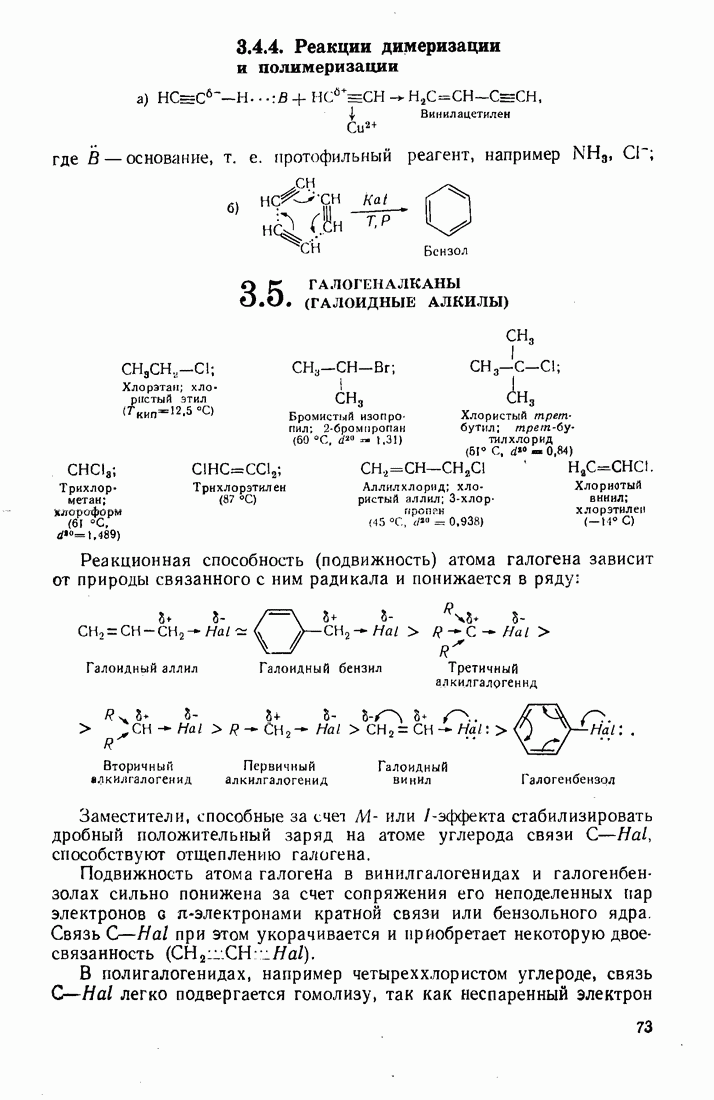
- 3.4. АЦЕТИЛЕНЫ
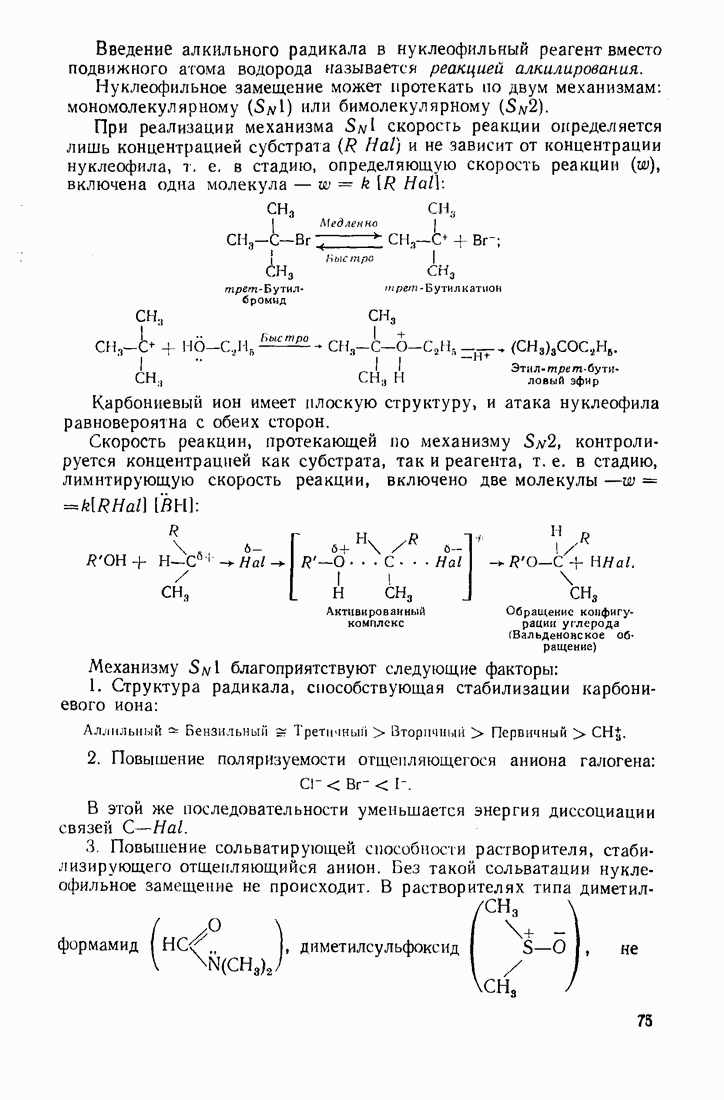
- 3.5. ГАЛОГЕНАЛКАНЫ (ГАЛОИДНЫЕ АЛКИЛЫ)
- 3.6. СПИРТЫ
- 3.7. ПРОСТЫЕ ЭФИРЫ (R-O-R)
- 3.8. ОКСИРАНЫ (ЭПОКСИДНЫЕ СОЕДИНЕНИЯ, a-ОКИСИ)
- 3.9. АЛЬДЕГИДЫ И КЕТОНЫ
- 3.10. КАРБОНОВЫЕ КИСЛОТЫ
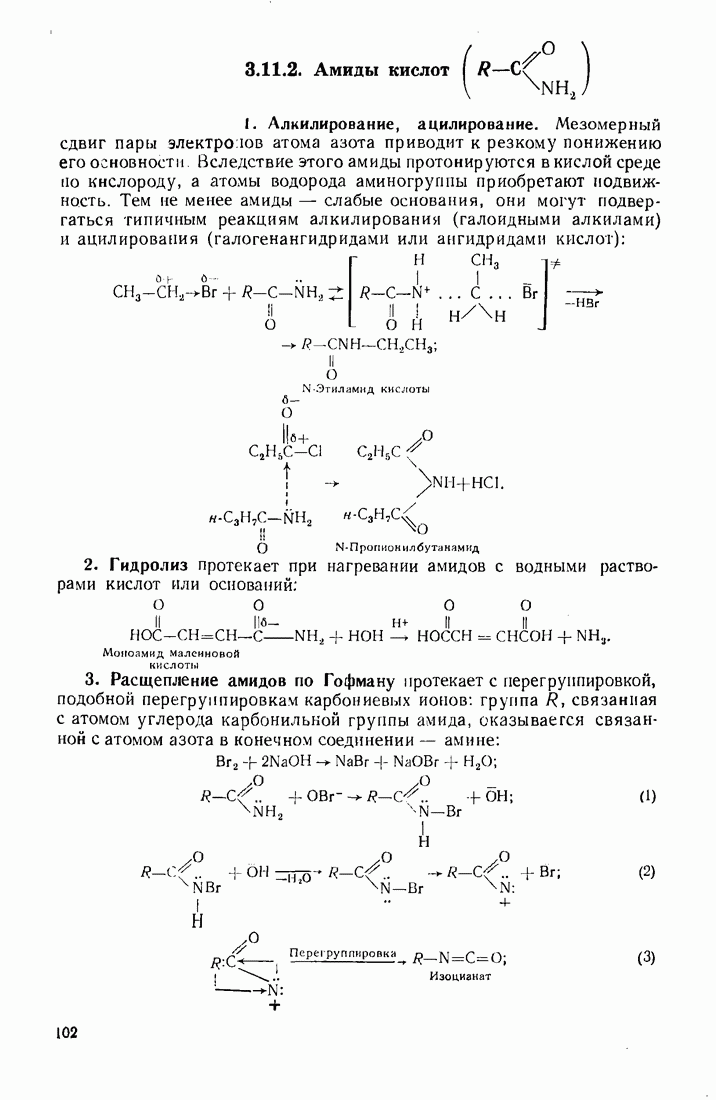
- 3.11. НЕКОТОРЫЕ ПРОИЗВОДНЫЕ КИСЛОТ
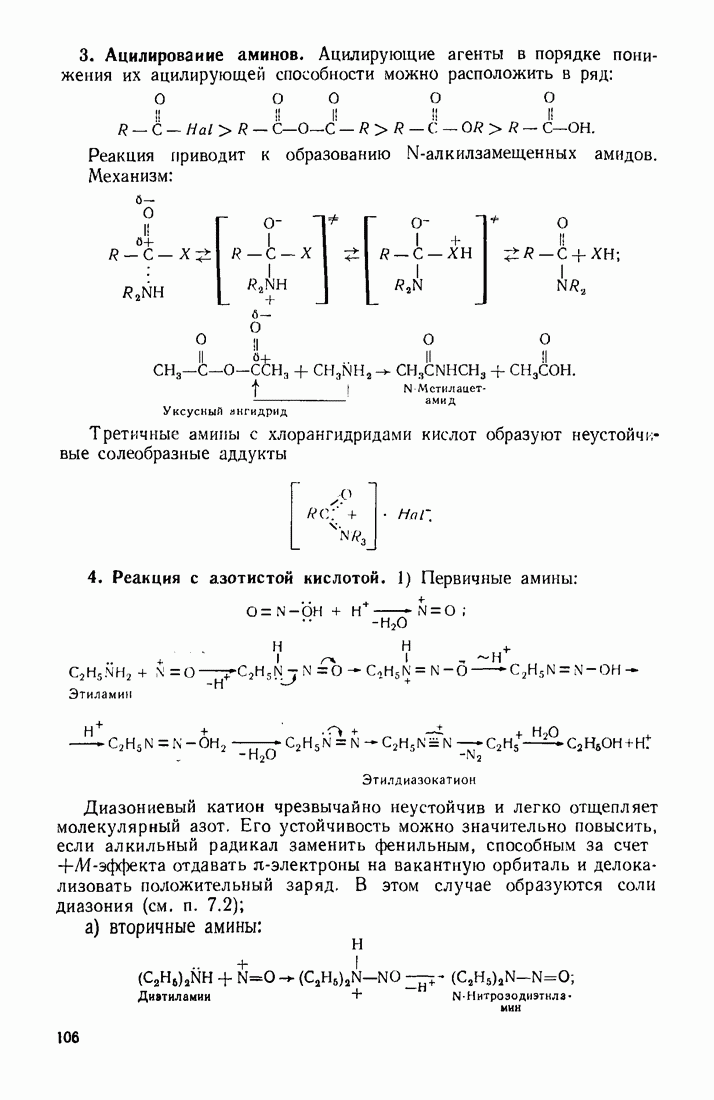
- 3.12. АМИНЫ
- 3.13. ФОСФОРОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- 3.14. СЕРООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
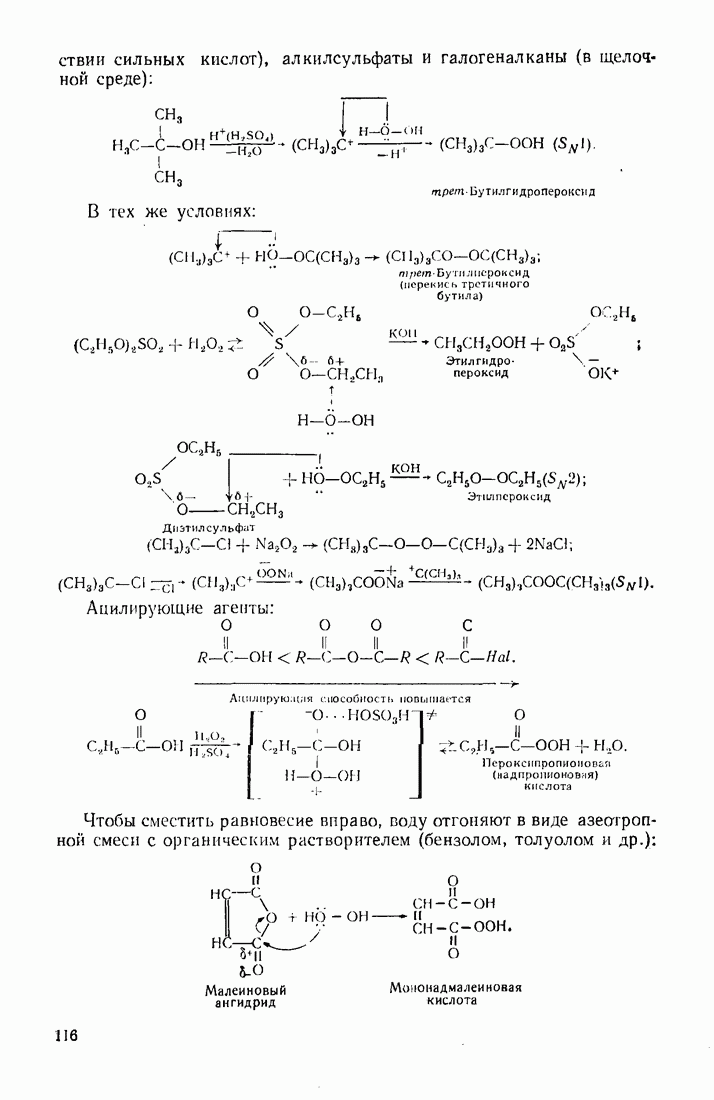
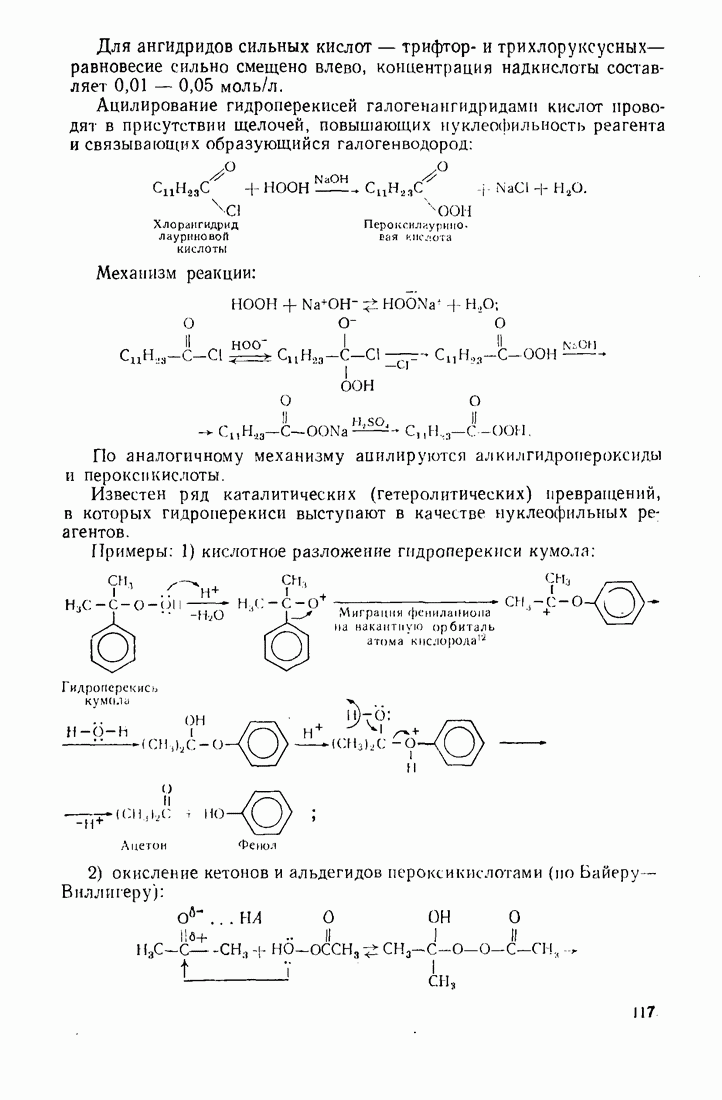
- 3.15. ОРГАНИЧЕСКИЕ ПЕРЕКИСИ (ПЕРОКСИДНЫЕ СОЕДИНЕНИЯ)
- 3.16. ПРОИЗВОДНЫЕ УГОЛЬНОЙ КИСЛОТЫ
- 3.17. ГЕТЕРОАНАЛОГИ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ
- 3.18. АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- 3.18.2. Пространственное расположение и напряженность циклов
- 3.18.3. Особенности химических свойств алициклических соединений
- 4. Полифункциональные производные алифатического ряда
- 4.1. ДВУХОСНОВНЫЕ КАРБОНОВЫЕ КИСЛОТЫ
- 4.2. НЕПРЕДЕЛЬНЫЕ КИСЛОТЫ
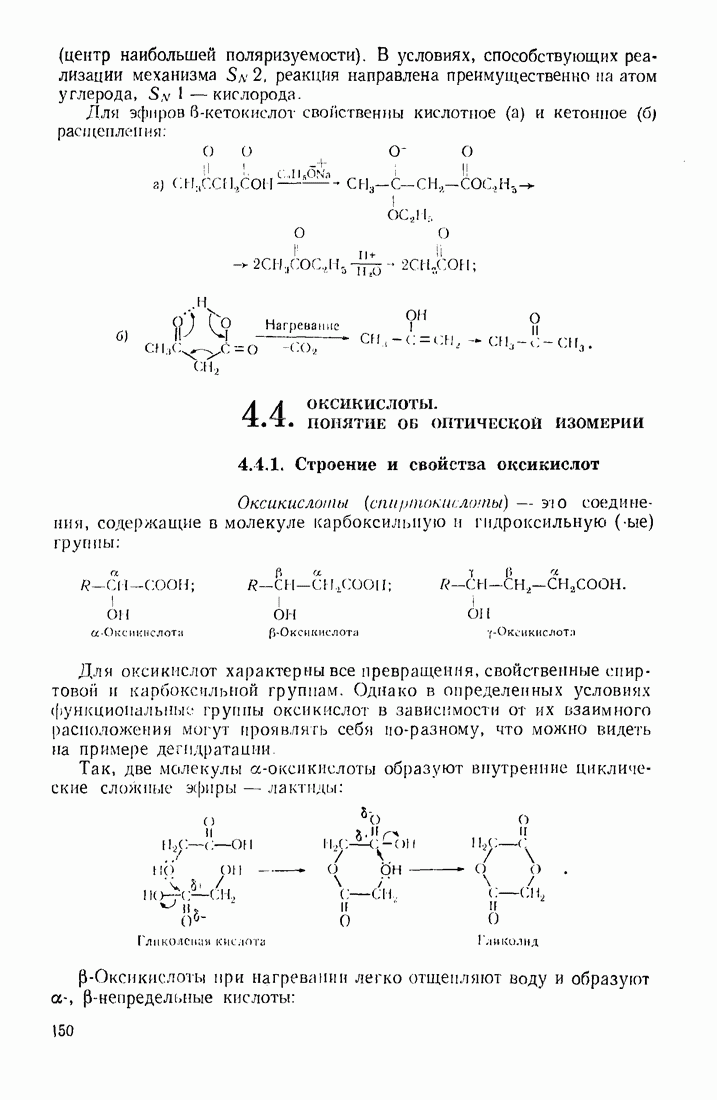
- 4.3. ОКСОКИСЛОТЫ (АЛЬДЕГИДО- И КЕТОКИСЛОТЫ)
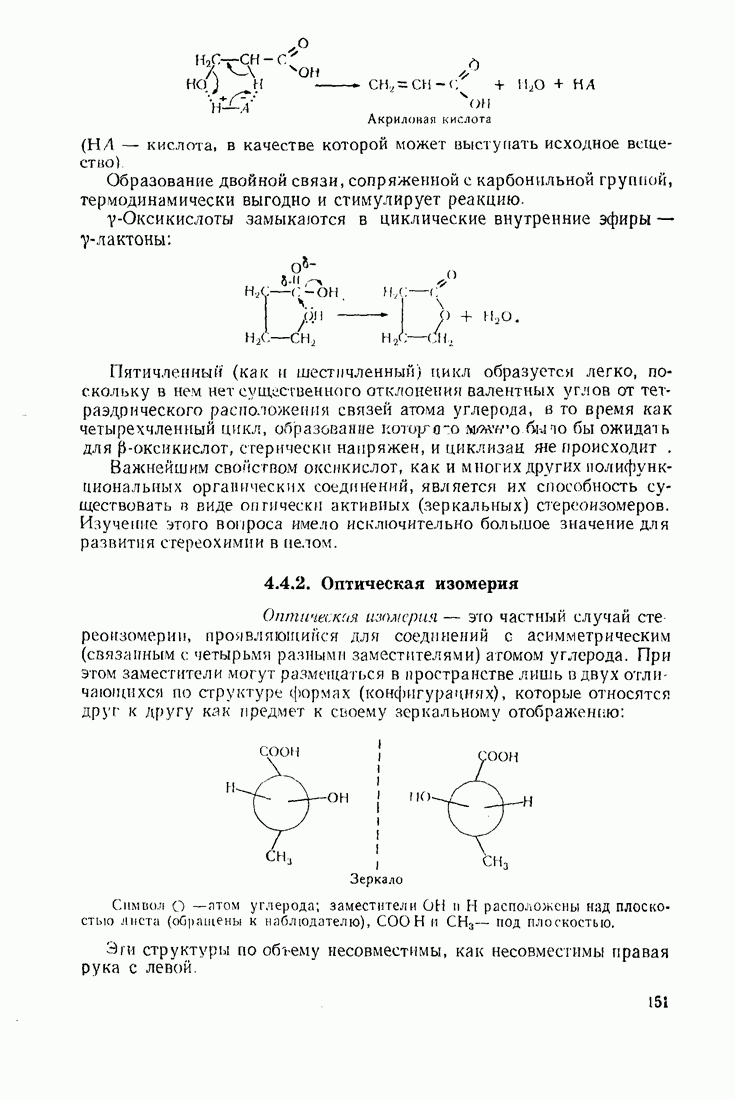
- 4.4. ОКСИКИСЛОТЫ. ПОНЯТИЕ ОБ ОПТИЧЕСКОЙ ИЗОМЕРИИ
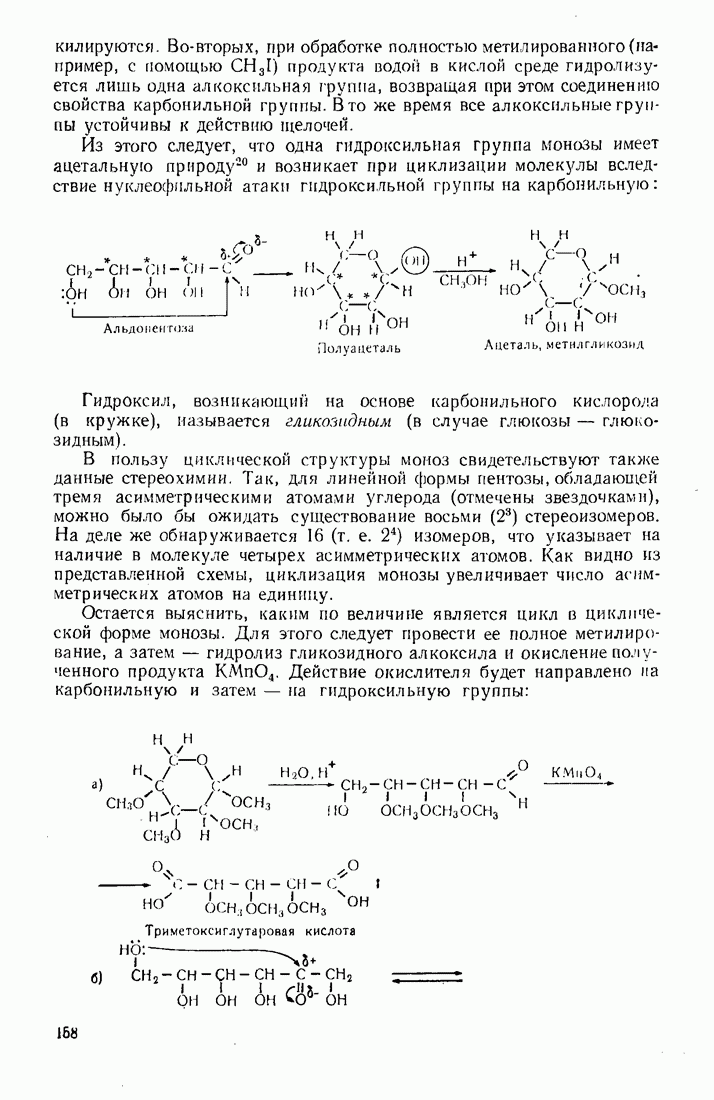
- 4.5. УГЛЕВОДЫ
- 4.5.2. Стереохимия моносахаридов
- 4.5.3. Дисахариды
- 4.5.4. Полисахариды
- 4.5.5. Нахождение в природе и пути превращения углеводов
- 4.6. АМИНОКИСЛОТЫ
- 5. Методы синтеза органических юединений алифатическою рада
- 5.1. АЛКИЛИРОВАНИЕ
- 5.2. АЦИЛИРОВАНИЕ
- 5.3. ГАЛОГЕНИРОВАНИЕ
- 5.4. ГИДРОКСИЛИРОВАНИЕ
- 5.5. КАРБОНИЛИРОВАНИЕ (ВВЕДЕНИЕ КАРБОНИЛЬНОЙ ГРУППЫ)
- 5.6. КАРБОКСИЛИРОВАНИЕ
- 5.7. ЭПОКСИДИРОВАНИЕ (ОКСИРАНИРОВАИИЕ)
- 5.8. АМИНИРОВАНИЕ
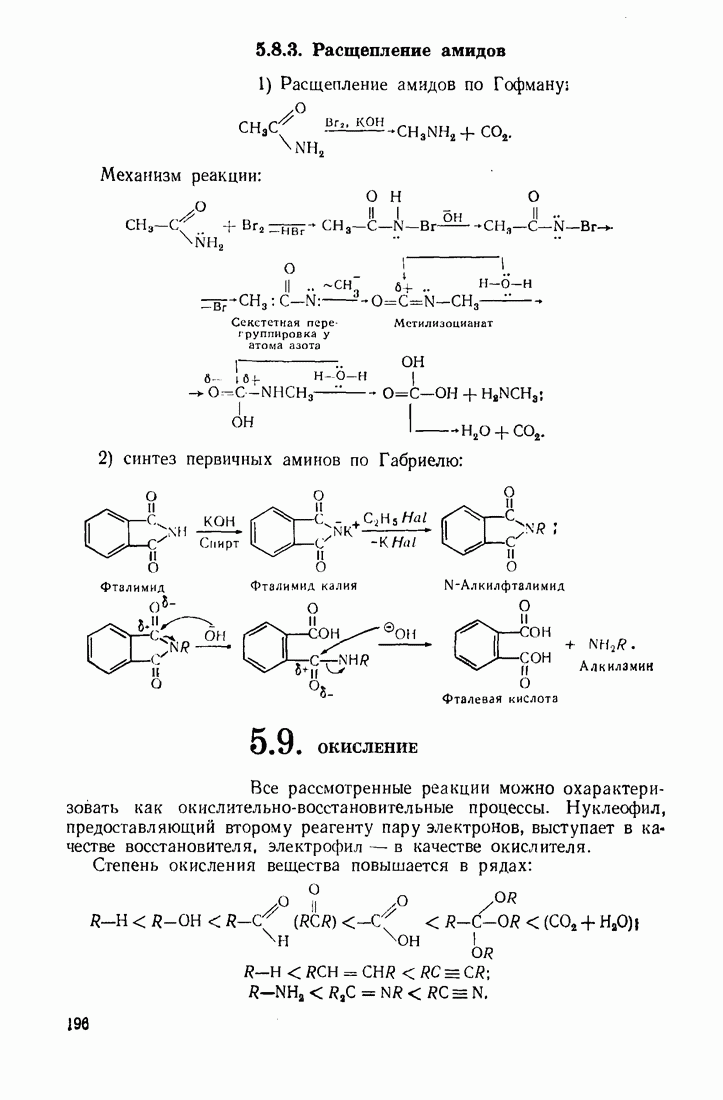
- 5.9. ОКИСЛЕНИЕ
- 5.10. ВОССТАНОВЛЕНИЕ
- 5.11. АЛКАНЫ
- 5.12 АЛКЕНЫ
- 5.13. ДИЕНОВЫЕ УГЛЕВОДОРОДЫ (1,3-ДИЕНЫ)
- 5.14. АЦЕТИЛЕНЫ
- 5.15 АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- 5.16. ГАЛОГЕН АЛКАНЫ
- 5.17. СПИРТЫ
- 5.18. АЛЬДЕГИДЫ И КЕТОНЫ
- 5.19. КАРБОНОВЫЕ КИСЛОТЫ
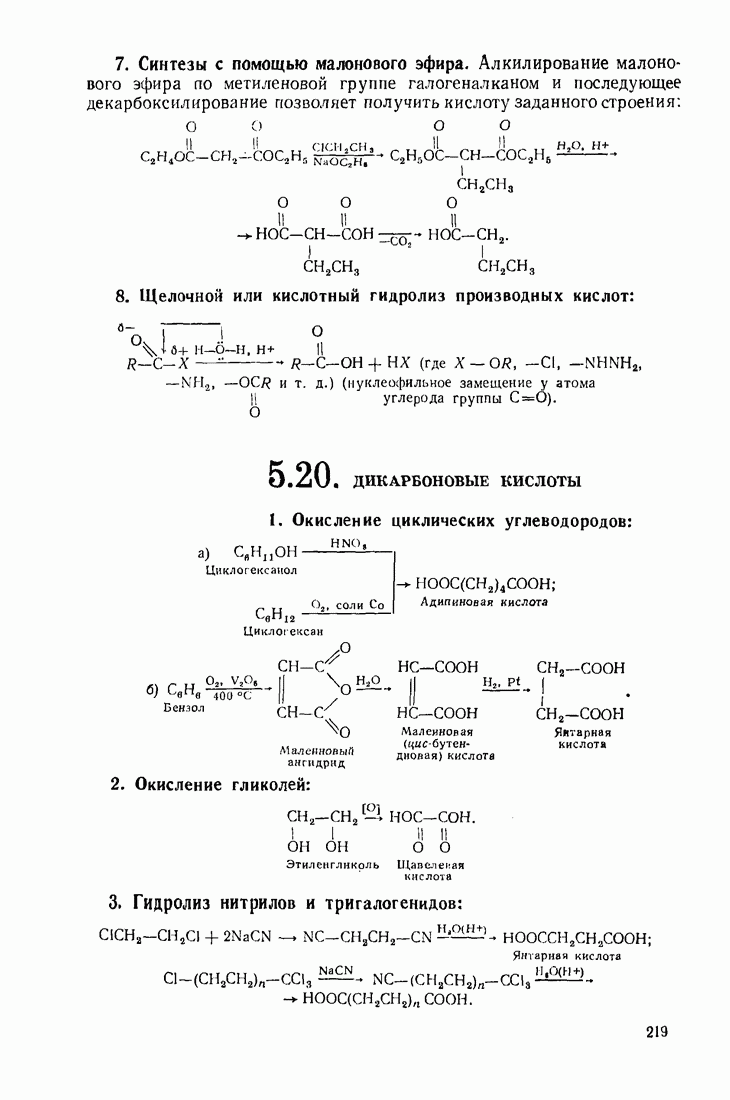
- 5.20. ДИКАРБОНОВЫЕ КИСЛОТЫ
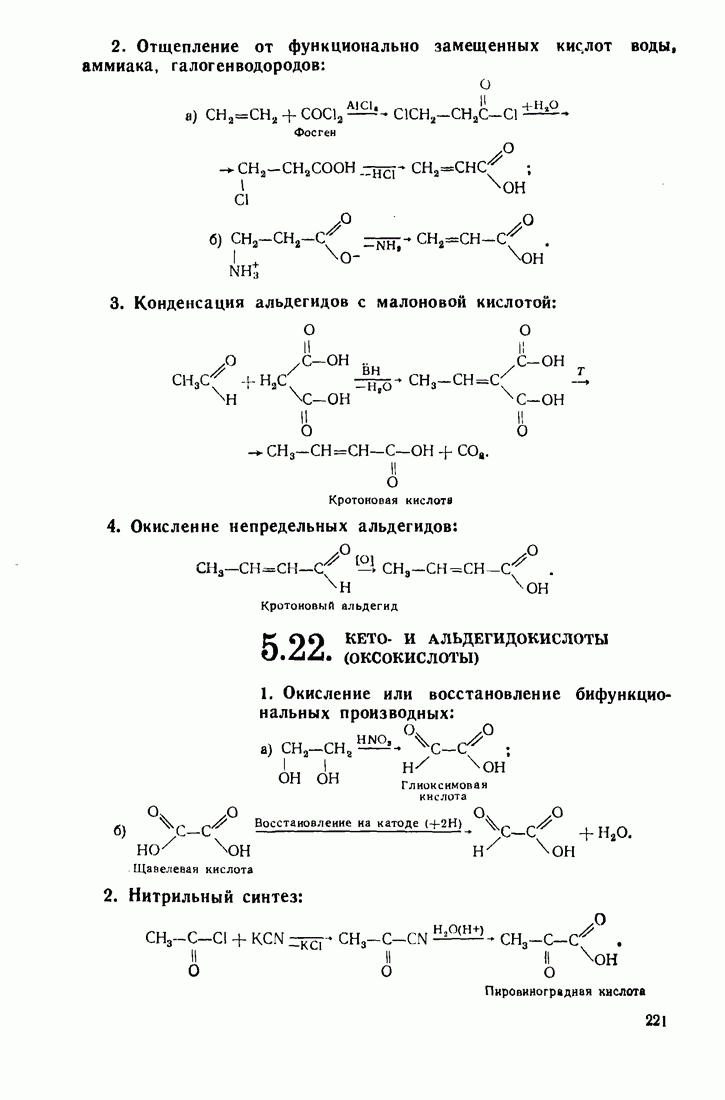
- 5.21. НЕПРЕДЕЛЬНЫЕ КИСЛОТЫ
- 5.22. КЕТО- И АЛЬДЕГИДОКИСЛОТЫ (ОКСОКИСЛОТЫ)
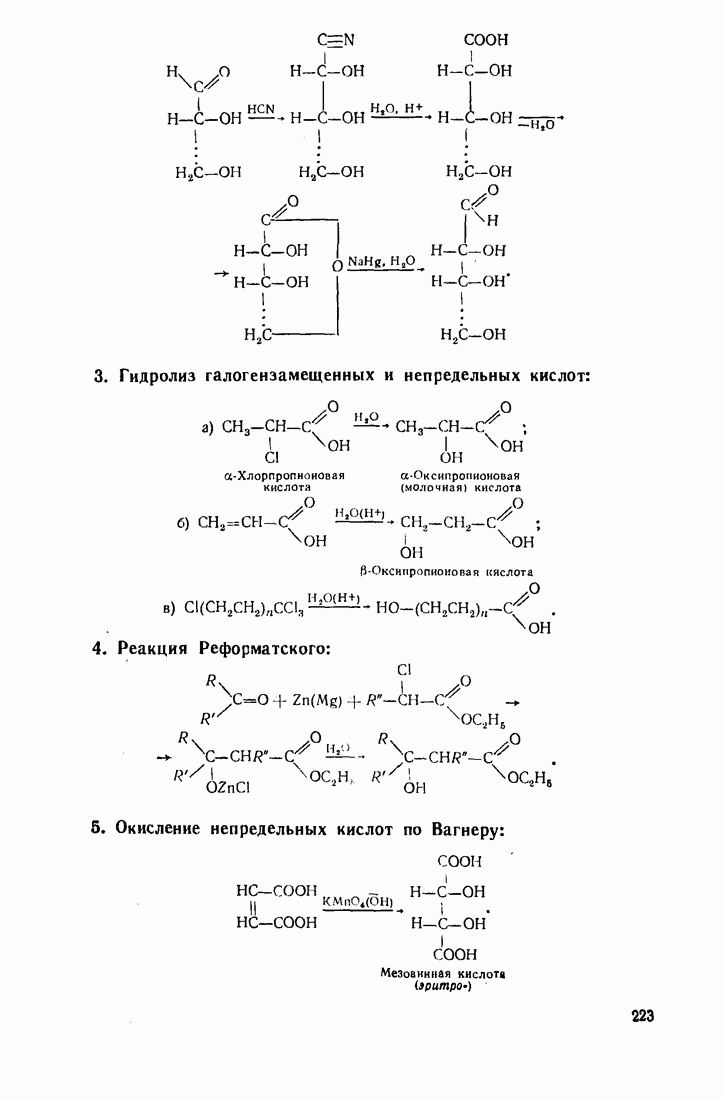
- 5.23. ОКСИКИСЛОТЫ
- 5.24. АМИНОКИСЛОТЫ
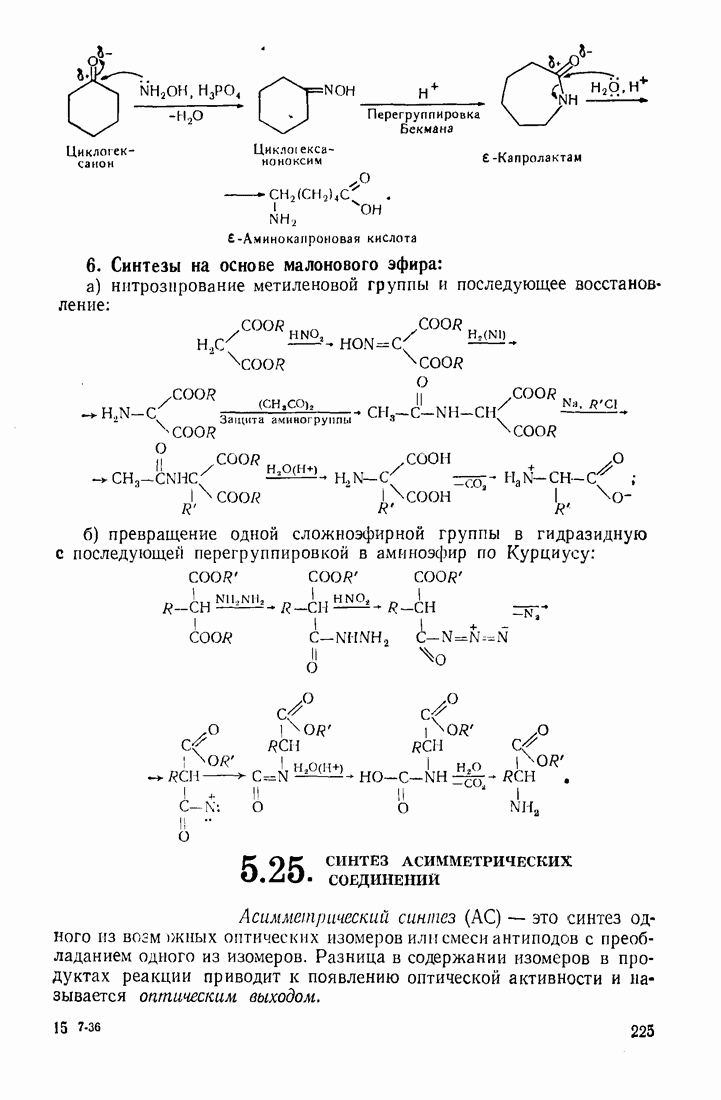
- 5.25 СИНТЕЗ АСИММЕТРИЧЕСКИХ СОЕДИНЕНИЙ
- 6. Некоторые понятия физической органической химии
- 6.1. СВЯЗЬ СОСТАВА И СТРОЕНИЯ СОЕДИНЕНИЙ С ФИЗИЧЕСКИМИ СВОЙСТВАМИ
- 6.2. ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 6.3. КИСЛОТЫ И ОСНОВАНИЯ В ОРГАНИЧЕСКОЙ ХИМИИ
- 6.4. ОРГАНИЧЕСКИЕ РАСТВОРИТЕЛИ И ИХ ВЛИЯНИЕ НА СКОРОСТЬ И МЕХАНИЗМ РЕАКЦИЙ
- 6.5. КАТАЛИЗ ОРГАНИЧЕСКИХ РЕАКЦИЙ
- 7. Бензол и его производные
- 7.1. СТРОЕНИЕ БЕНЗОЛА. РАСПРЕДЕЛЕНИЕ ЭЛЕКТРОННОЙ ПЛОТНОСТИ
- 7.2. ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ В БЕНЗОЛЬНОМ ЯДРЕ
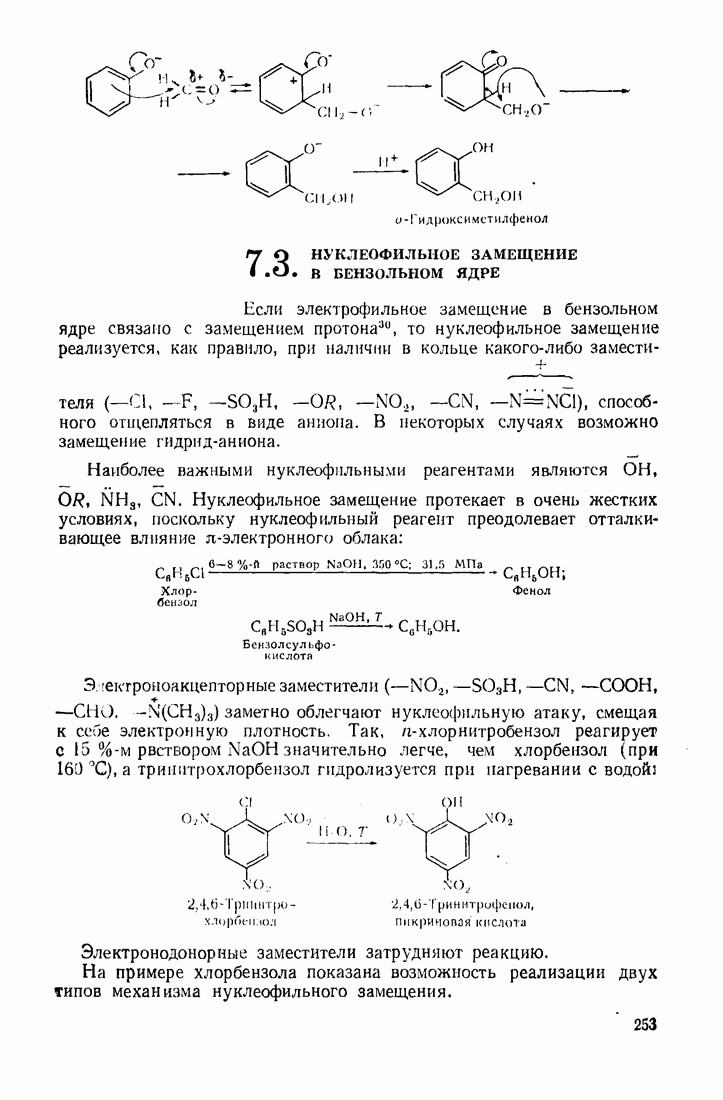
- 7.3. НУКЛЕОФИЛЬНОЕ ЗАМЕЩЕНИЕ В БЕНЗОЛЬНОМ ЯДРЕ
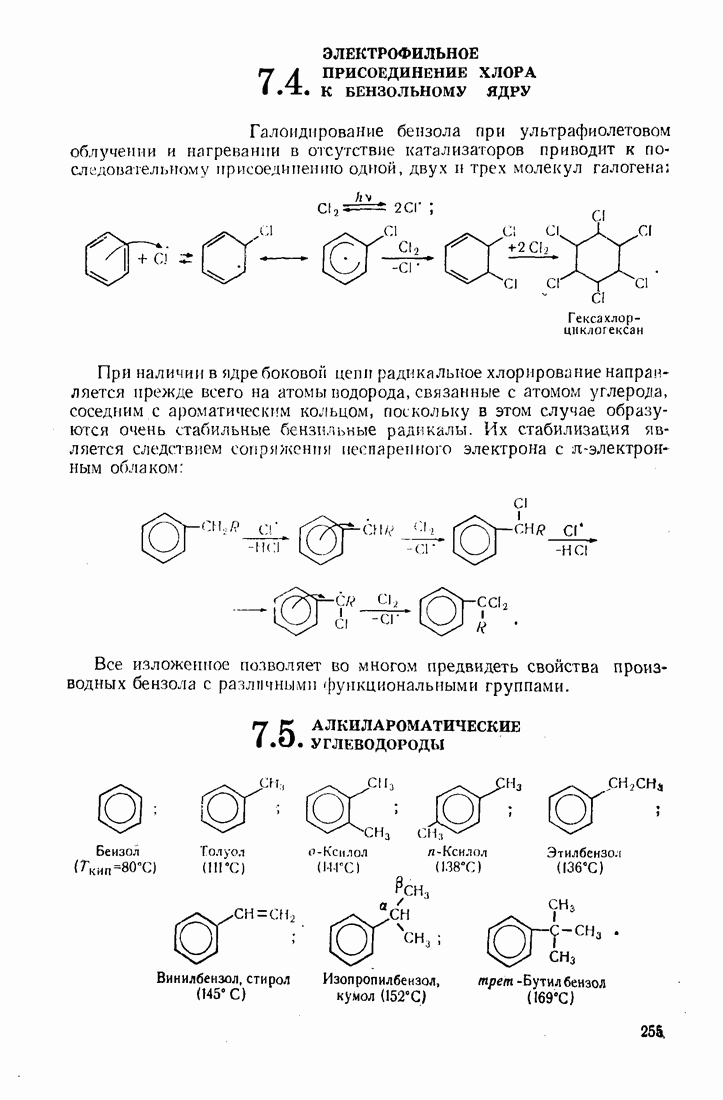
- 7.4. ЭЛЕКТРОФИЛЬНОЕ ПРИСОЕДИНЕНИЕ ХЛОРА К БЕНЗОЛЬНОМУ ЯДРУ
- 7.5. АЛКИЛАРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ
- 7.6. ГАЛОГЕНБЕНЗОЛЫ
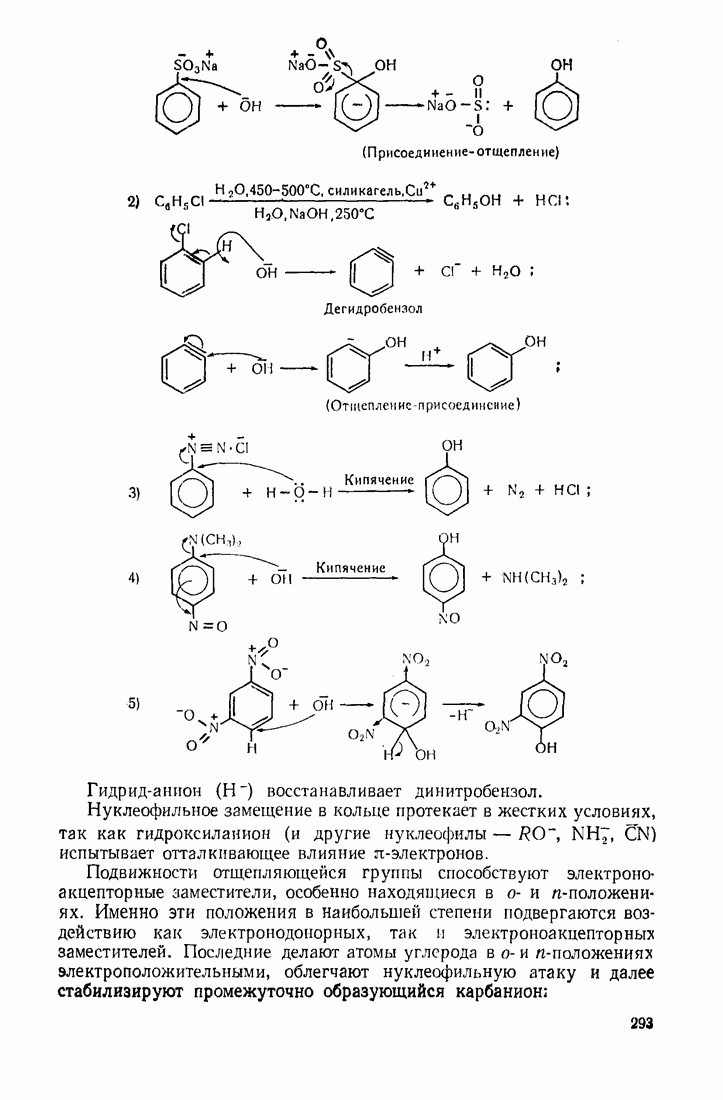
- 7.7. ФЕНОЛЫ
- 7.8. НИТРОСОЕД ИНЕНИЯ
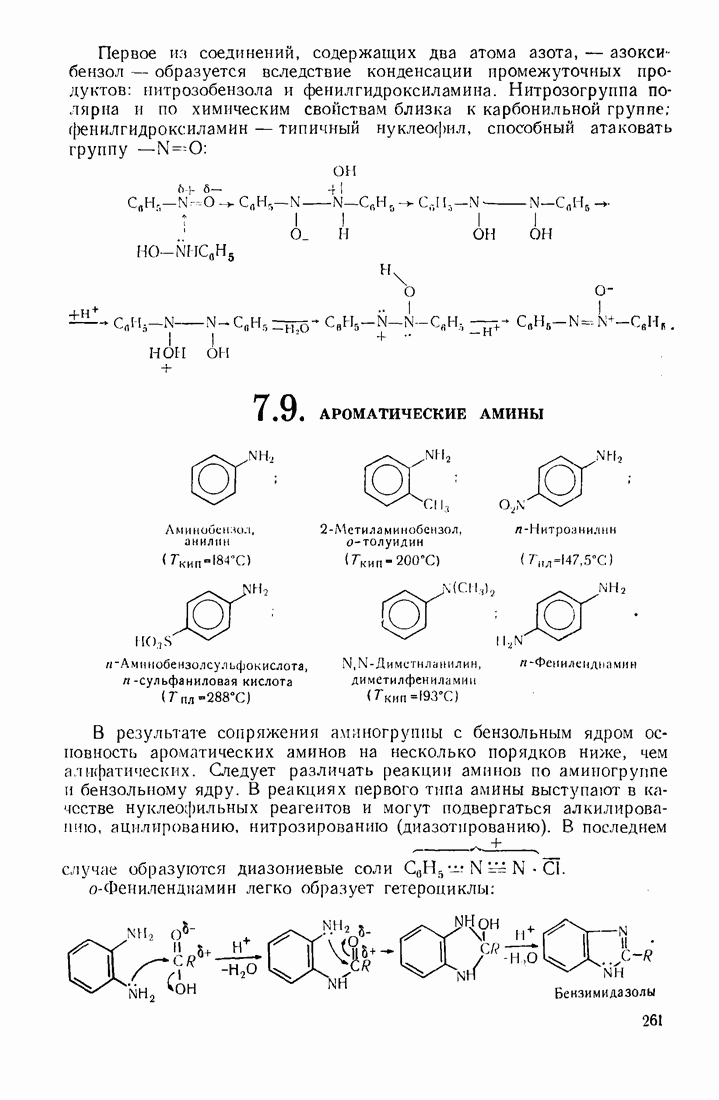
- 7.9. АРОМАТИЧЕСКИЕ АМИНЫ
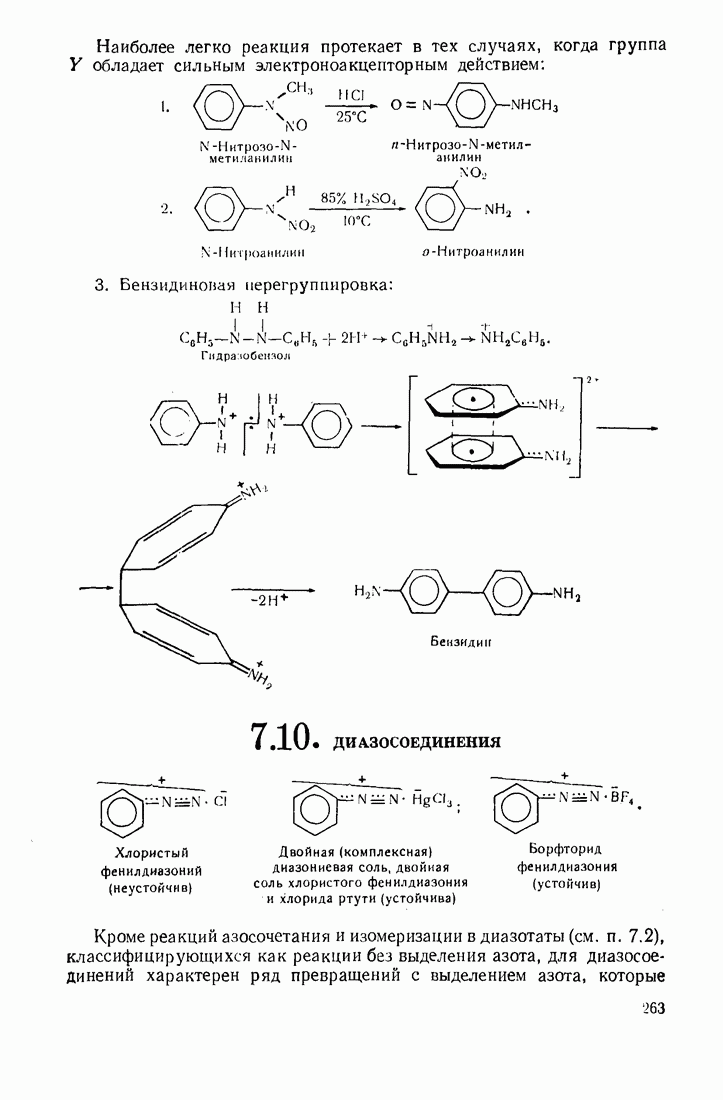
- 7.10. ДИАЗОСОЕДИНЕНИЯ
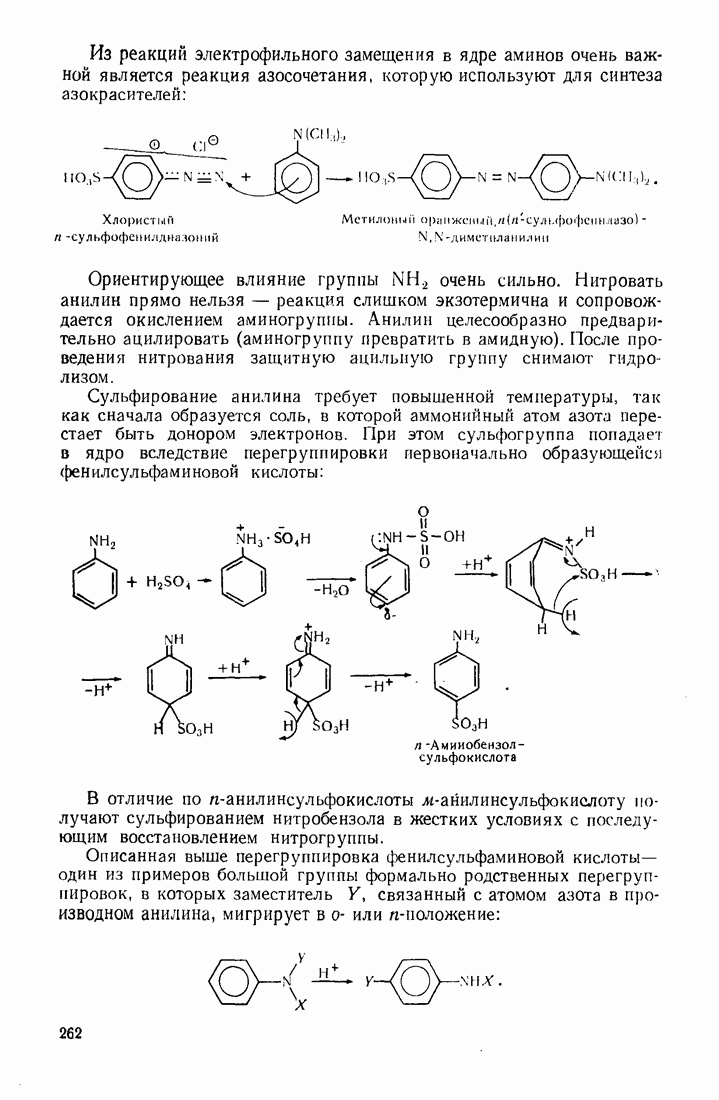
- 7.11. АЗОСОЕДИНЕНИЯ
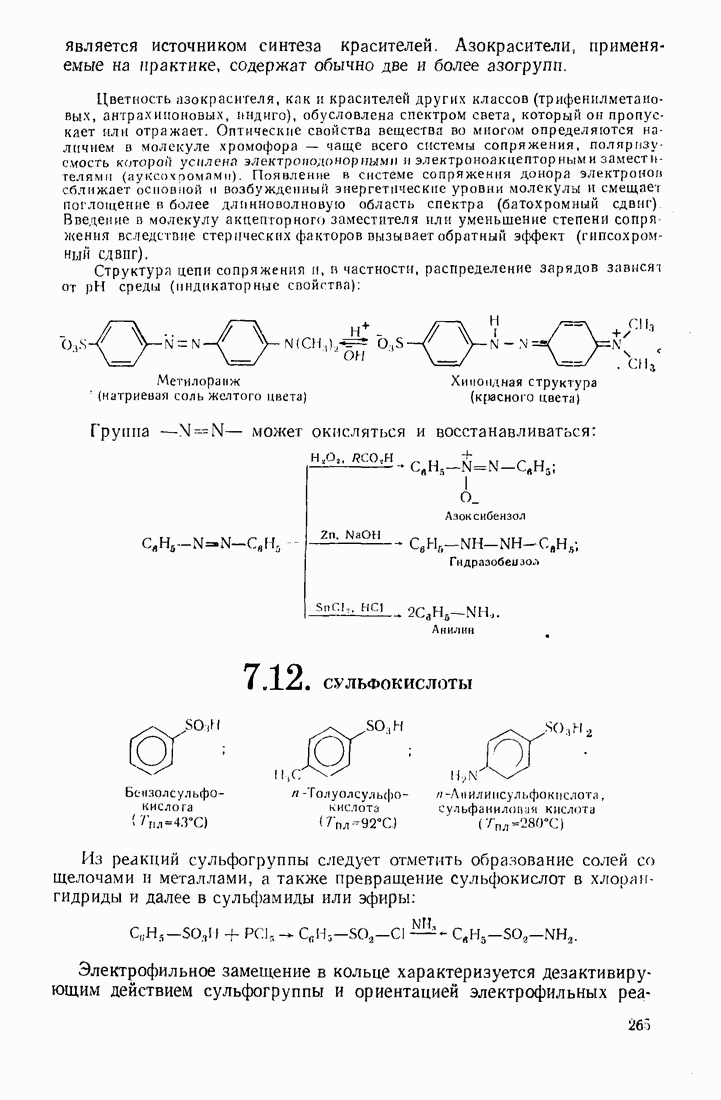
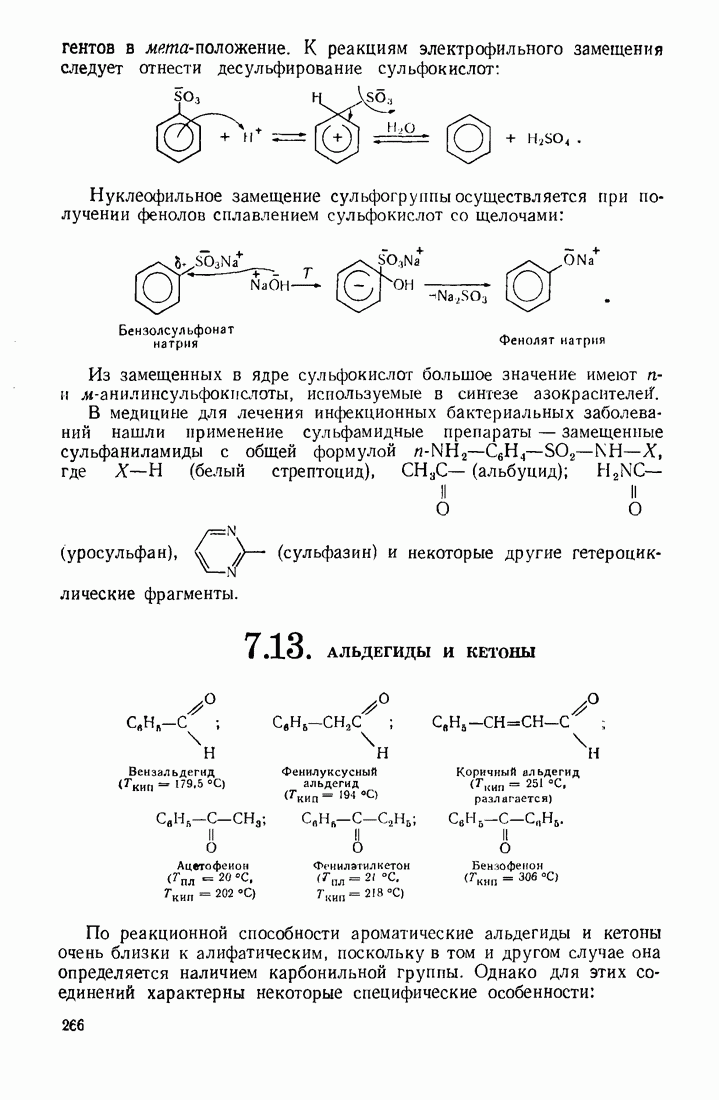
- 7.12. СУЛЬФОКИСЛОТЫ
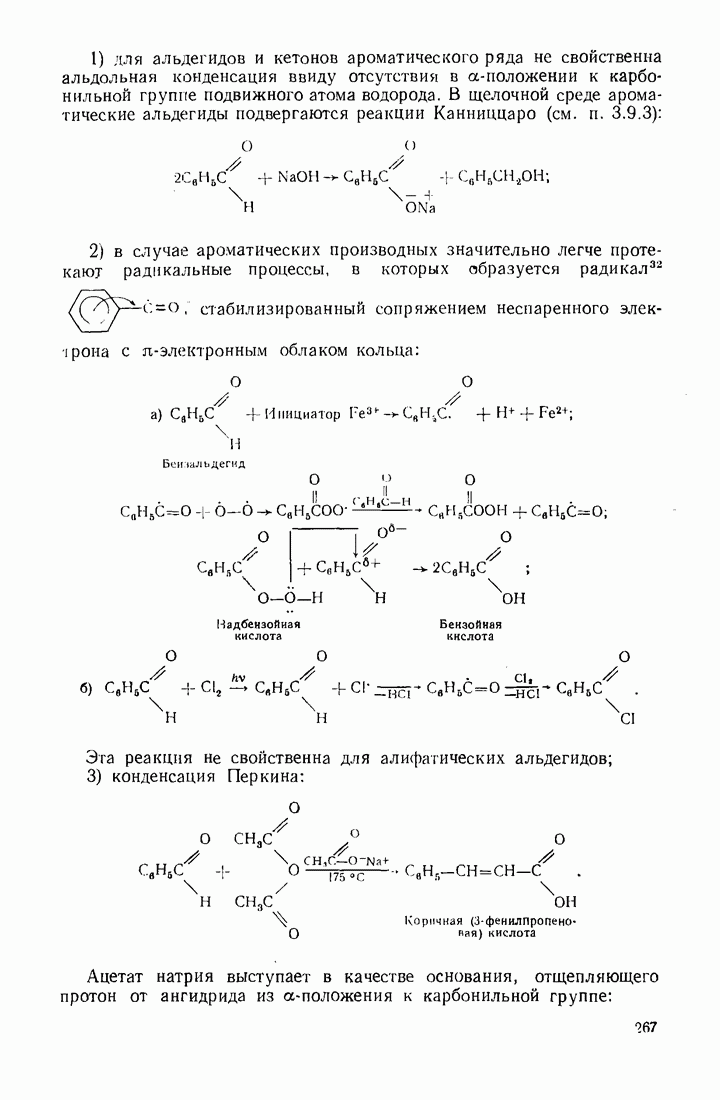
- 7.13. АЛЬДЕГИДЫ И КЕТОНЫ
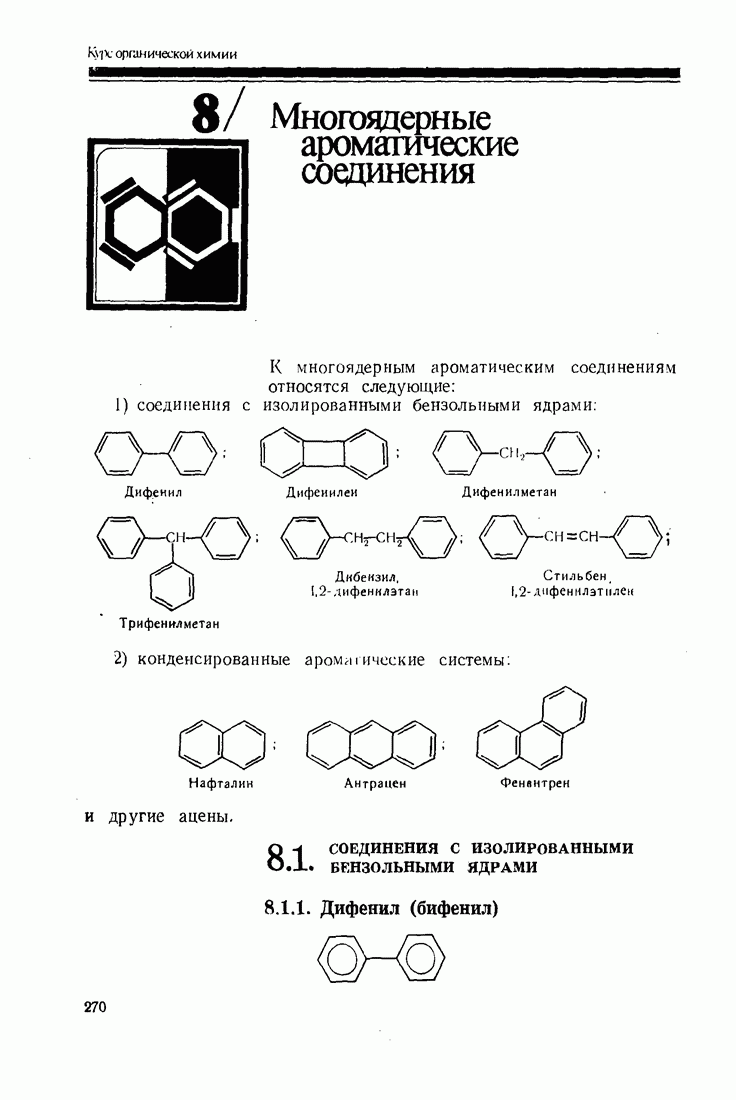
- 8. Многоядерные ароматические соединения
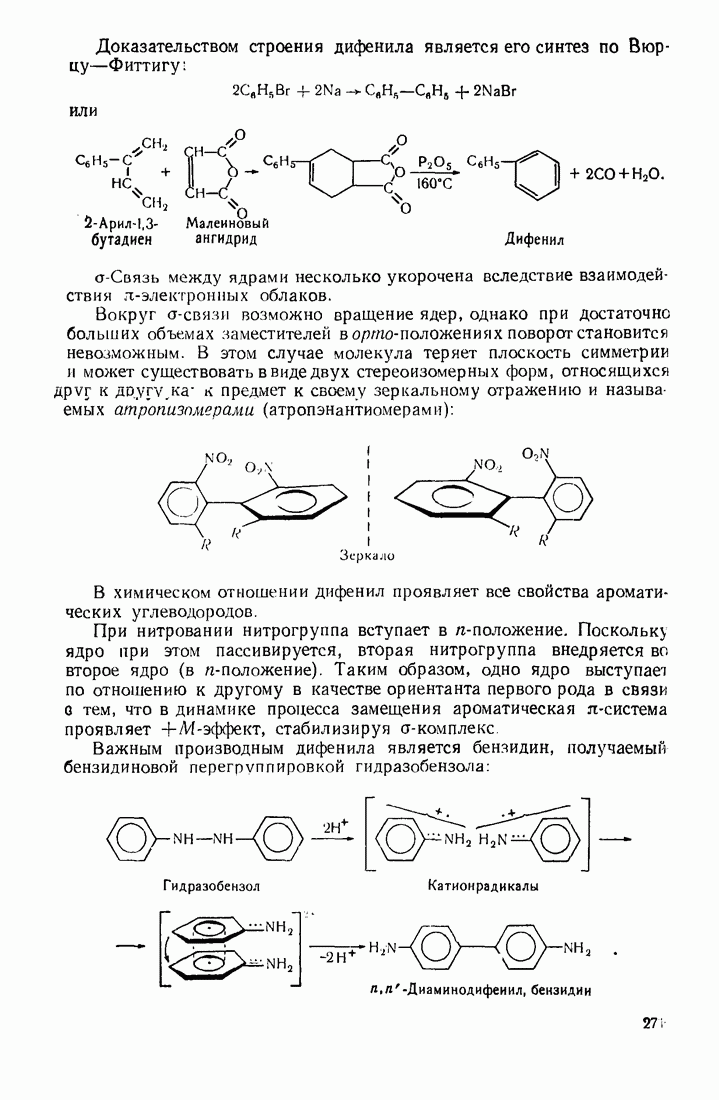
- 8.1. СОЕДИНЕНИЯ С ИЗОЛИРОВАННЫМИ БЕНЗОЛЬНЫМИ ЯДРАМИ
- 8.1.2. Полифенилметаны
- 8.2. АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ С КОНДЕНСИРОВАННЫМИ ЯДРАМИ
- 8.2.2. Антрацен
- 8.2.3. Фенантрен
- 9. Методы синтеза в ряду ароматических соединений
- 9.1. ГАЛОГЕНИРОВАНИЕ
- 9.2. НИТРОВАНИЕ
- 9.3. СУЛЬФИРОВАНИЕ
- 9.4. АЛКИЛИРОВАНИЕ
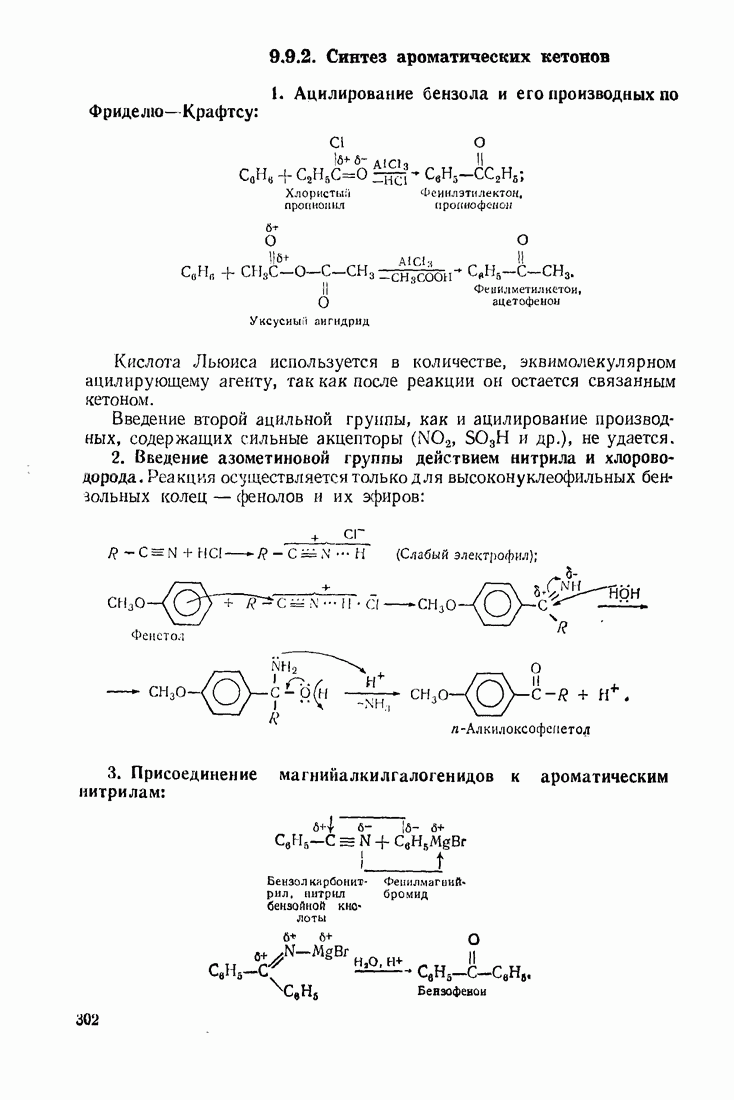
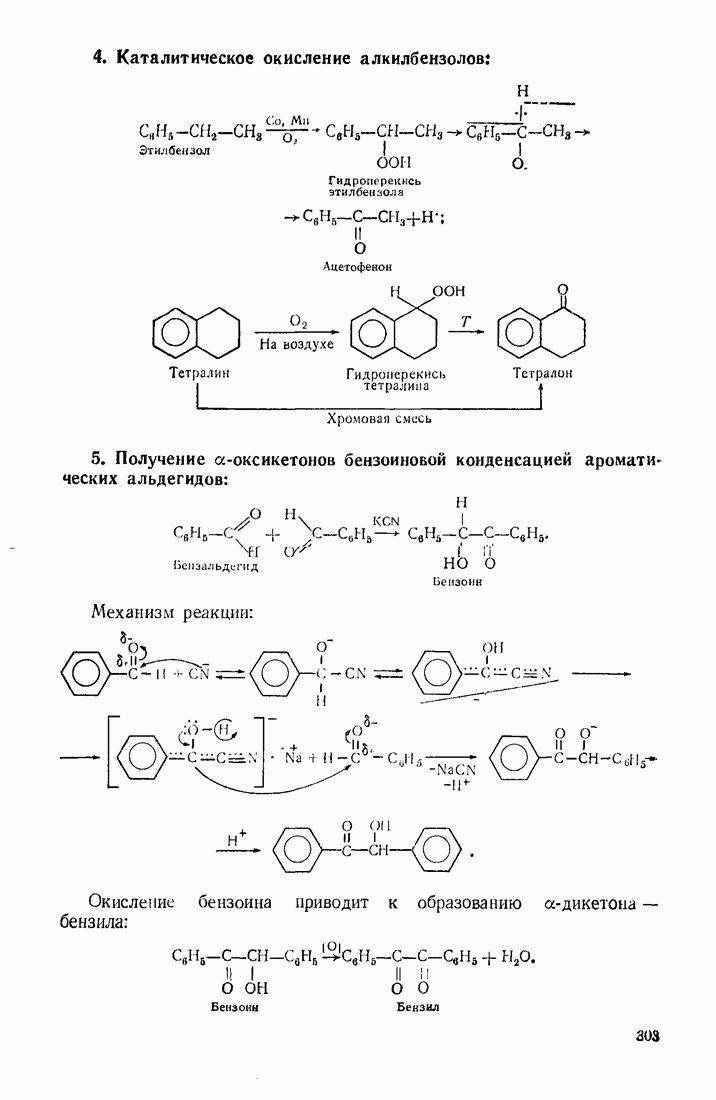
- 9.5. АЦИЛИРОВАНИЕ
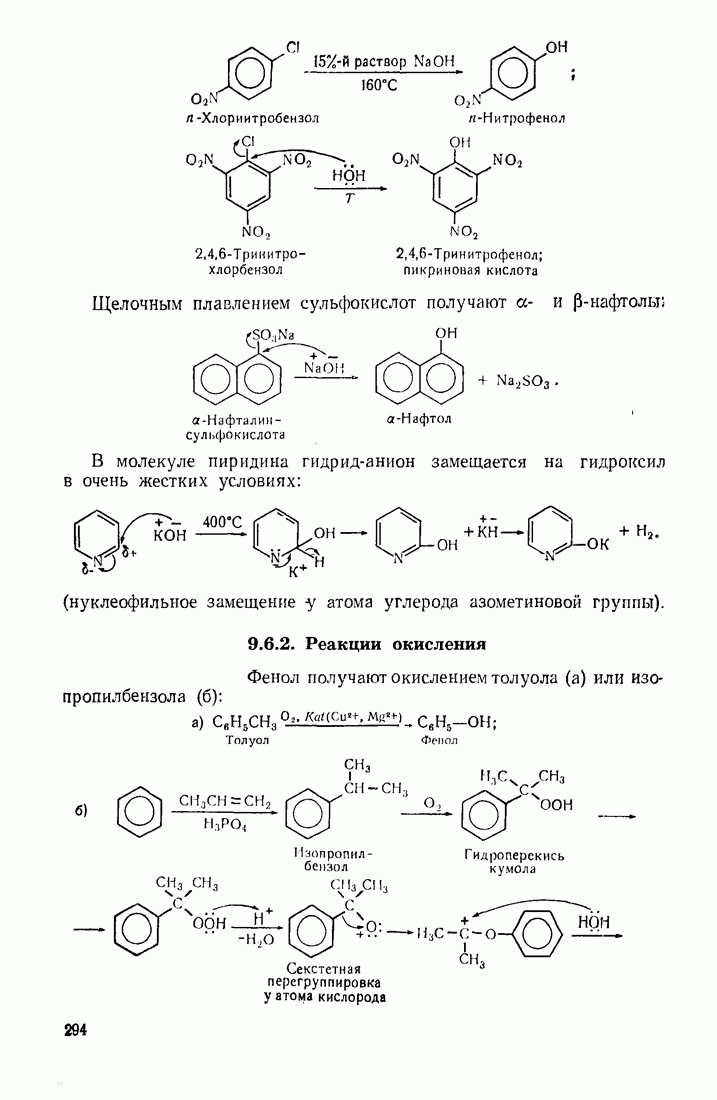
- 9.6. ГИДРОКСИЛИРОВАНИЕ
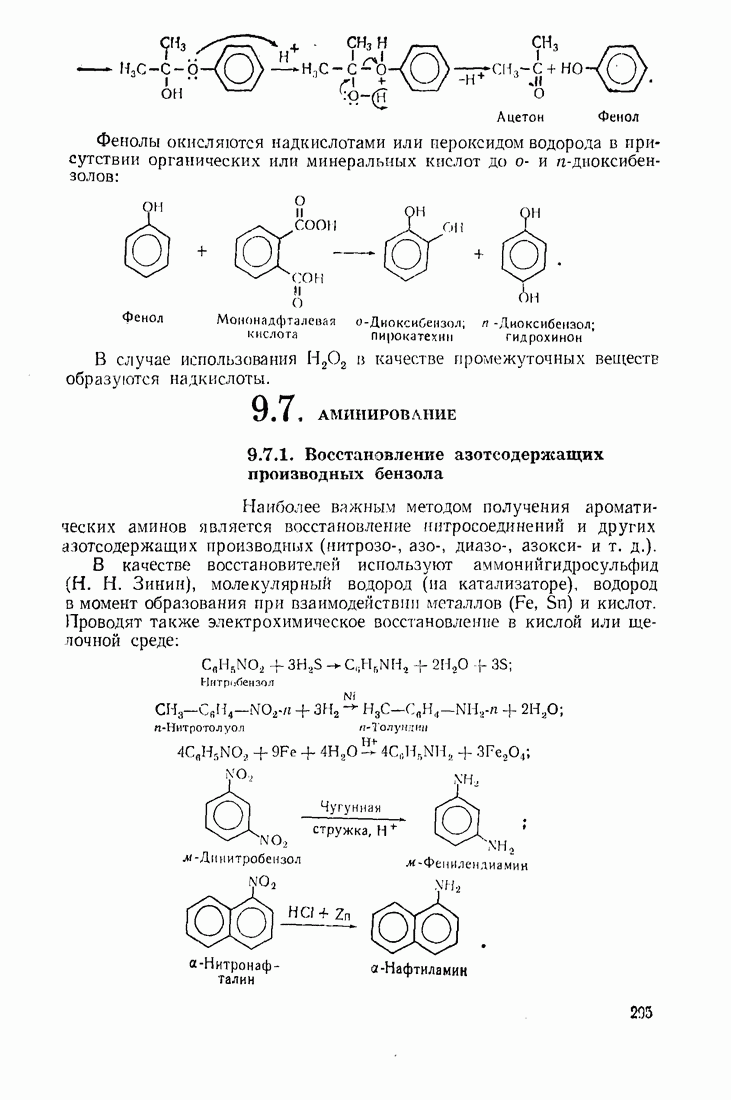
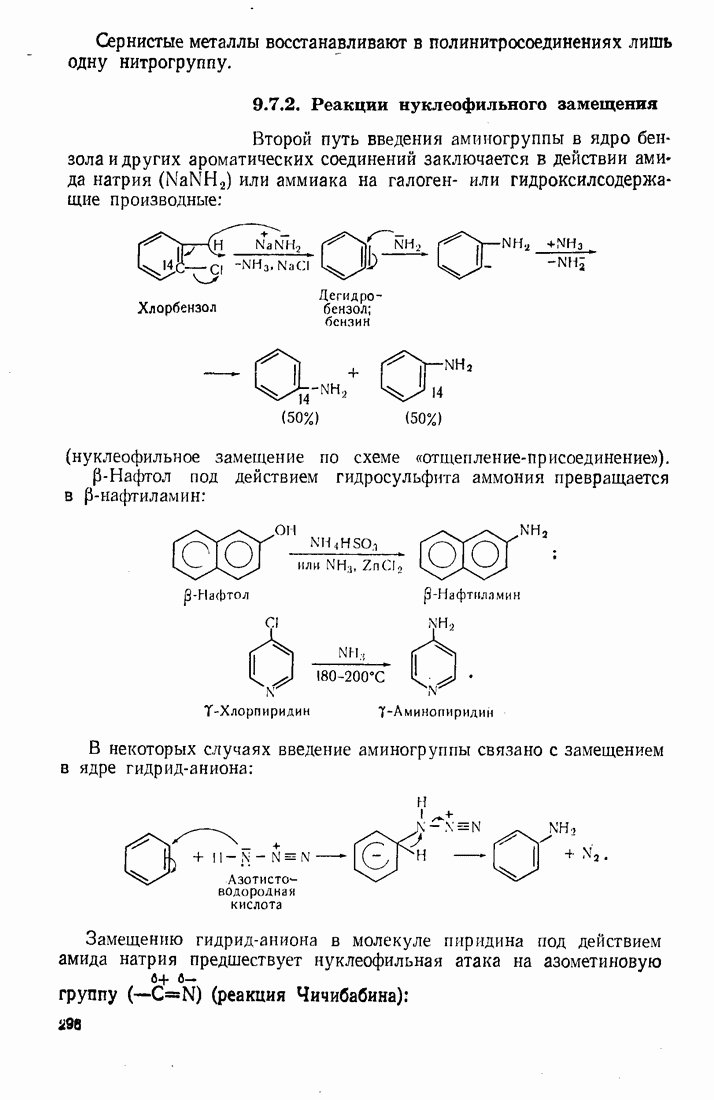
- 9.7. АМИНИРОВАНИЕ
- 9.8. НИТРОЗИРОВАНИЕ
- 9.9. КАРБОНИЛИРОВАНИЕ
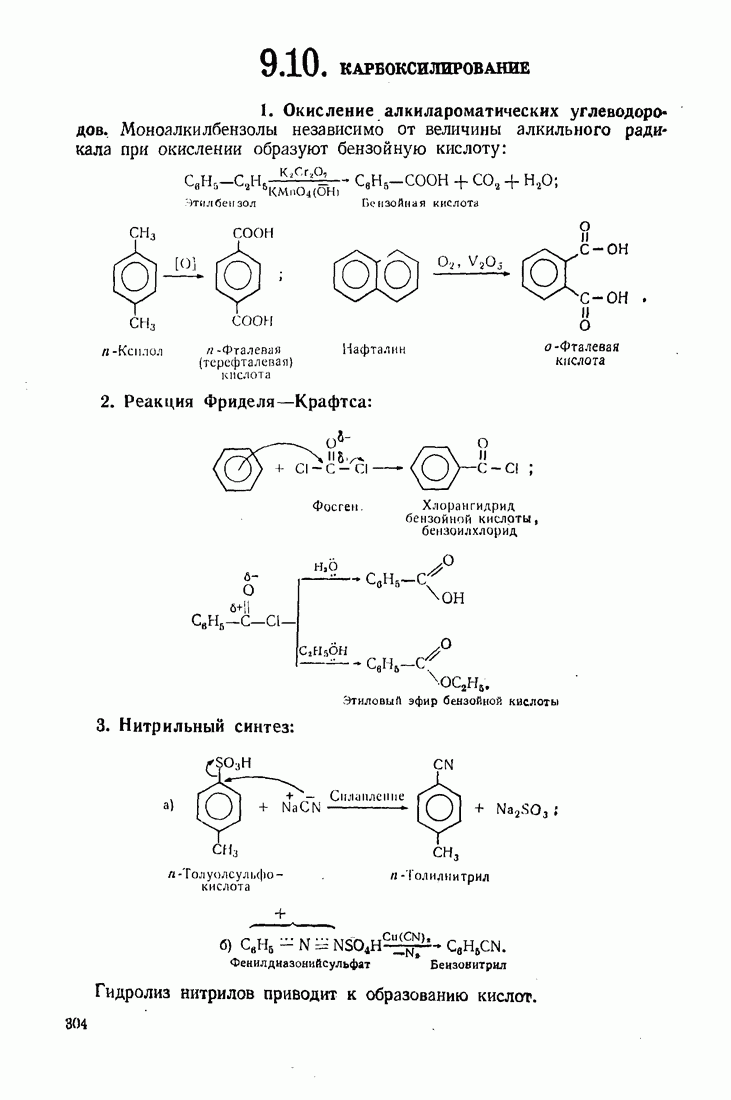
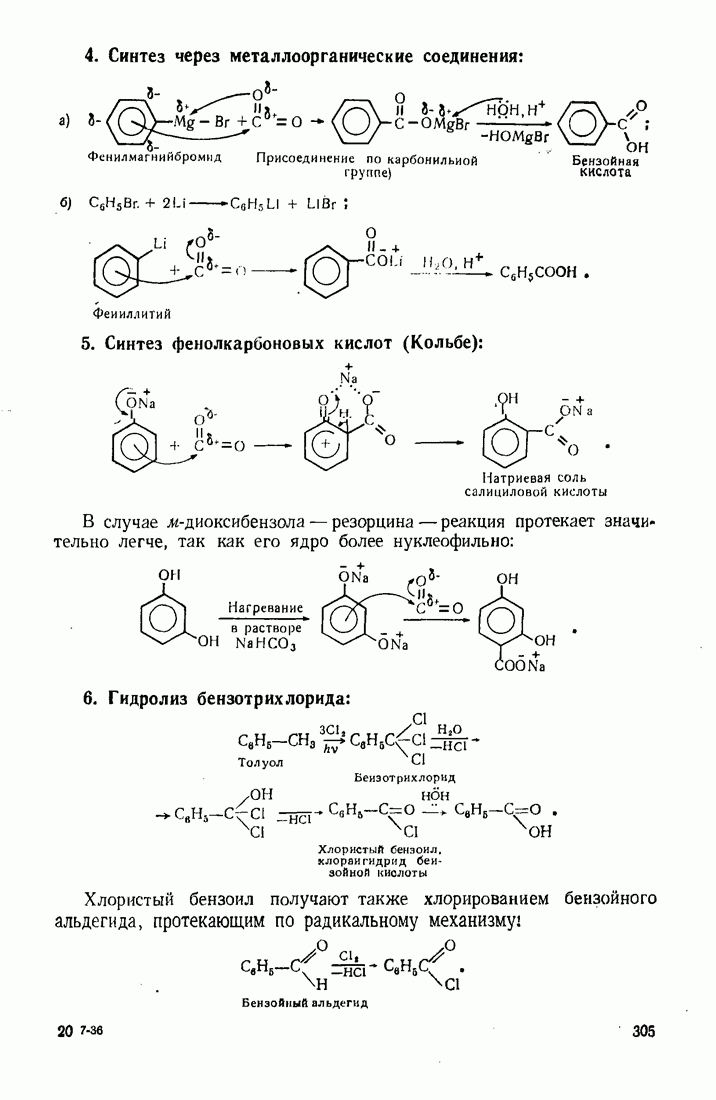
- 9.10. КАРБОКСИЛИРОВАНИЕ
- 9.11. ОКИСЛЕНИЕ
- 9.12. ВОССТАНОВЛЕНИЕ
- 10. Гетероциклические соединения
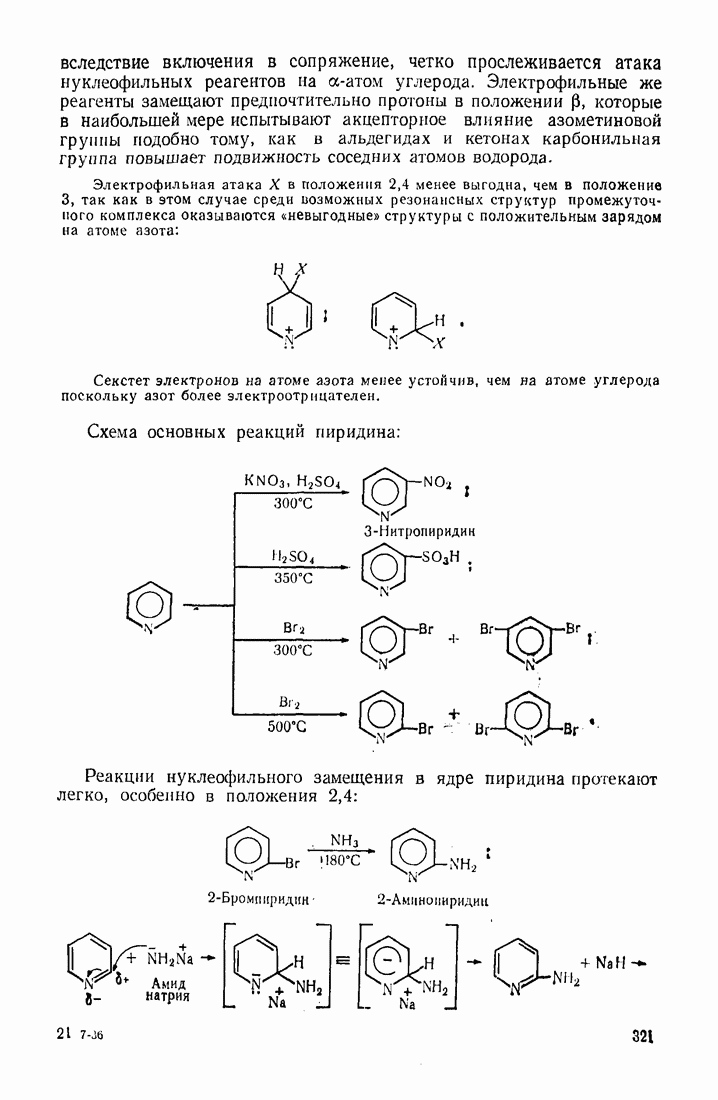
- 10.2. ОБЩАЯ ХАРАКТЕРИСТИКА СТРОЕНИЯ И РЕАКЦИОННОЙ СПОСОБНОСТИ
- 10.3. ПЯТИ- И ШЕСТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С ОДНИМ ГЕТЕРОАТОМОМ
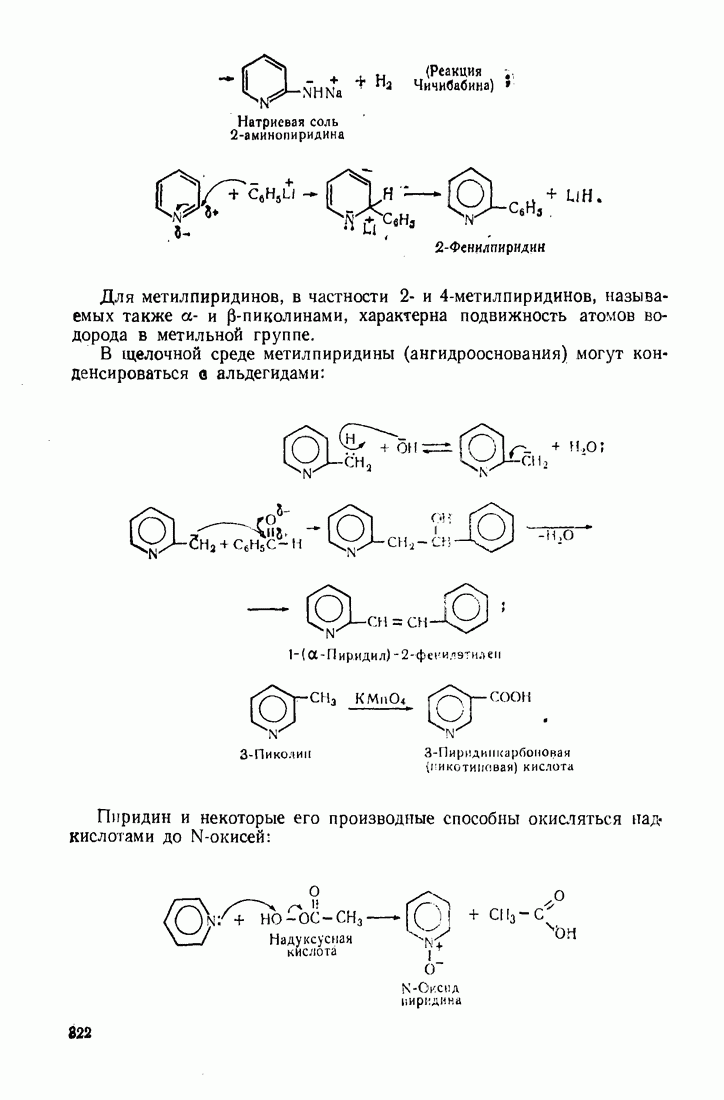
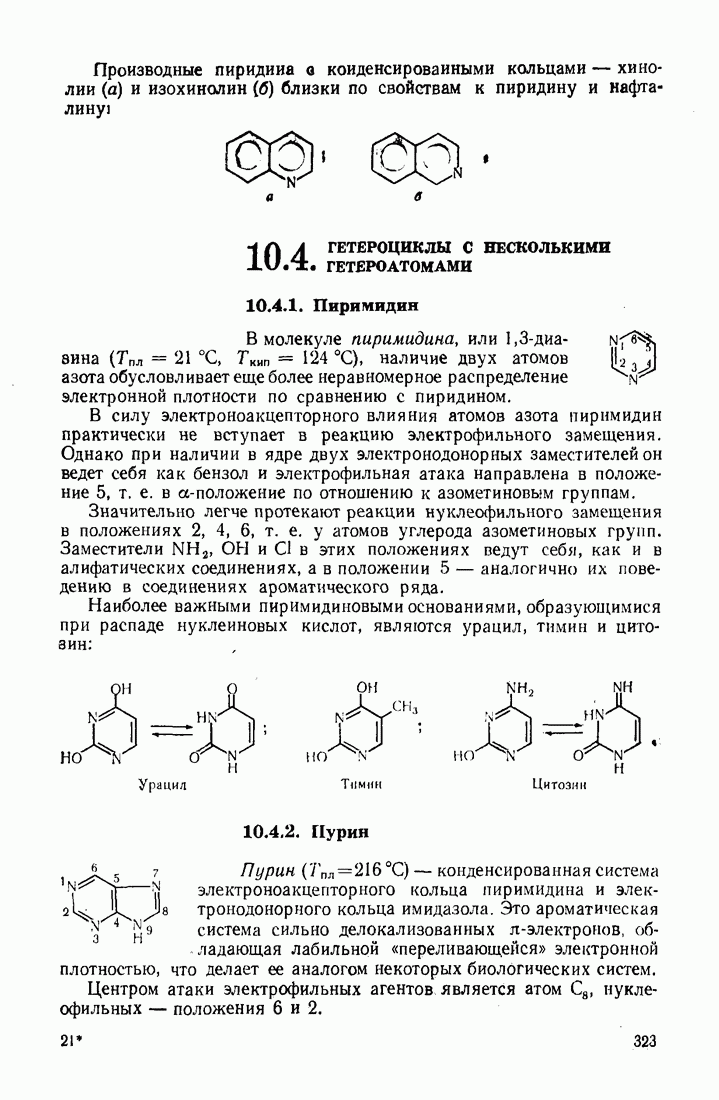
- 10.4. ГЕТЕРОЦИКЛЫ С НЕСКОЛЬКИМИ ГЕТЕРОАТОМАМИ
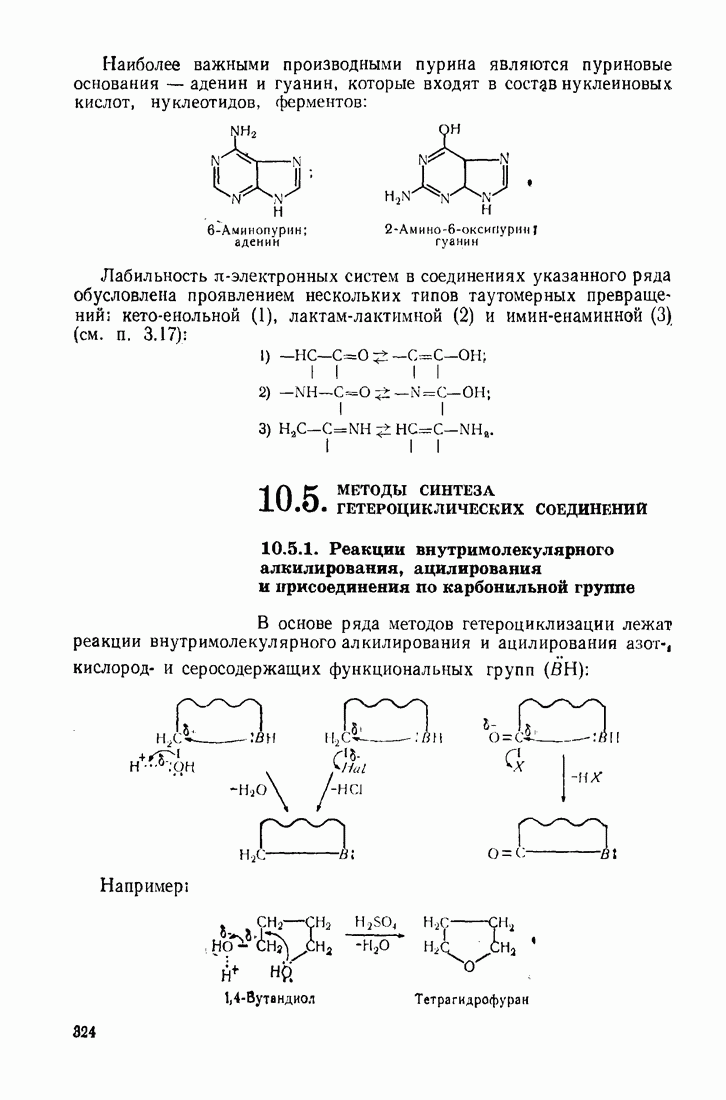
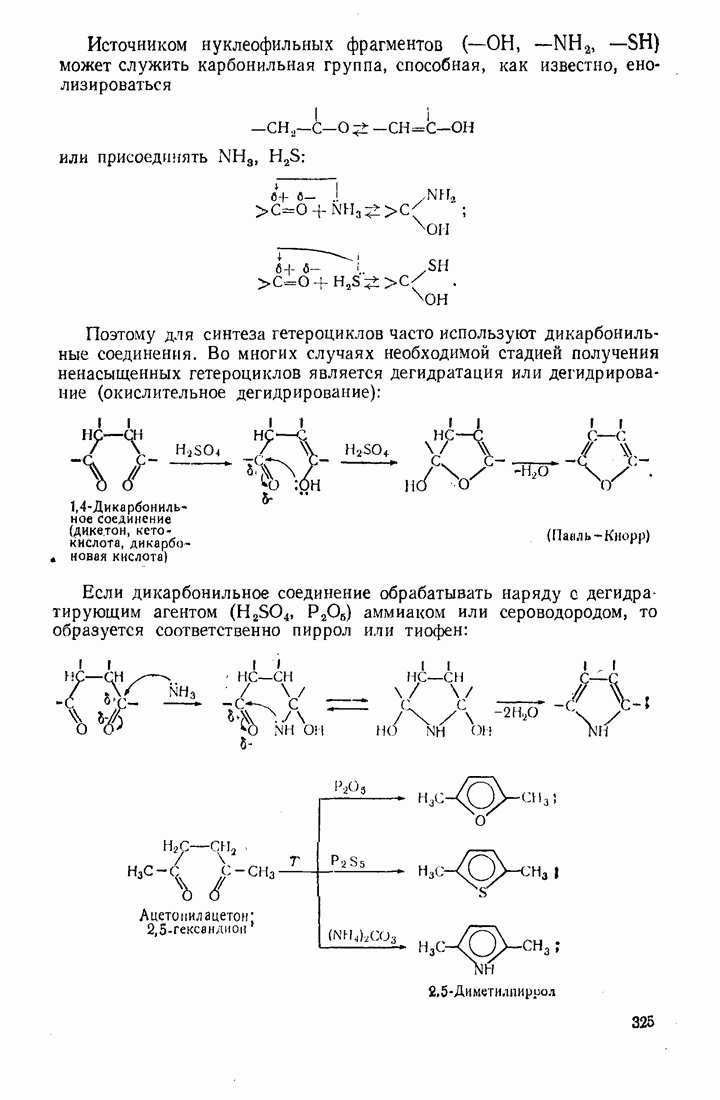
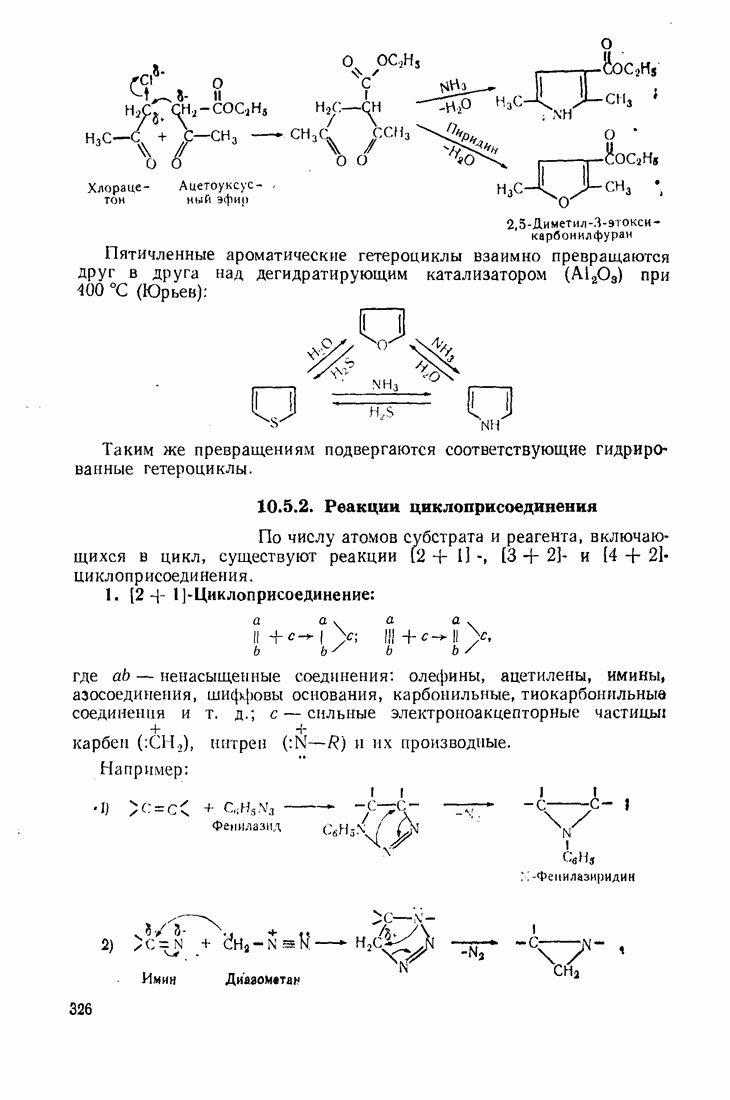
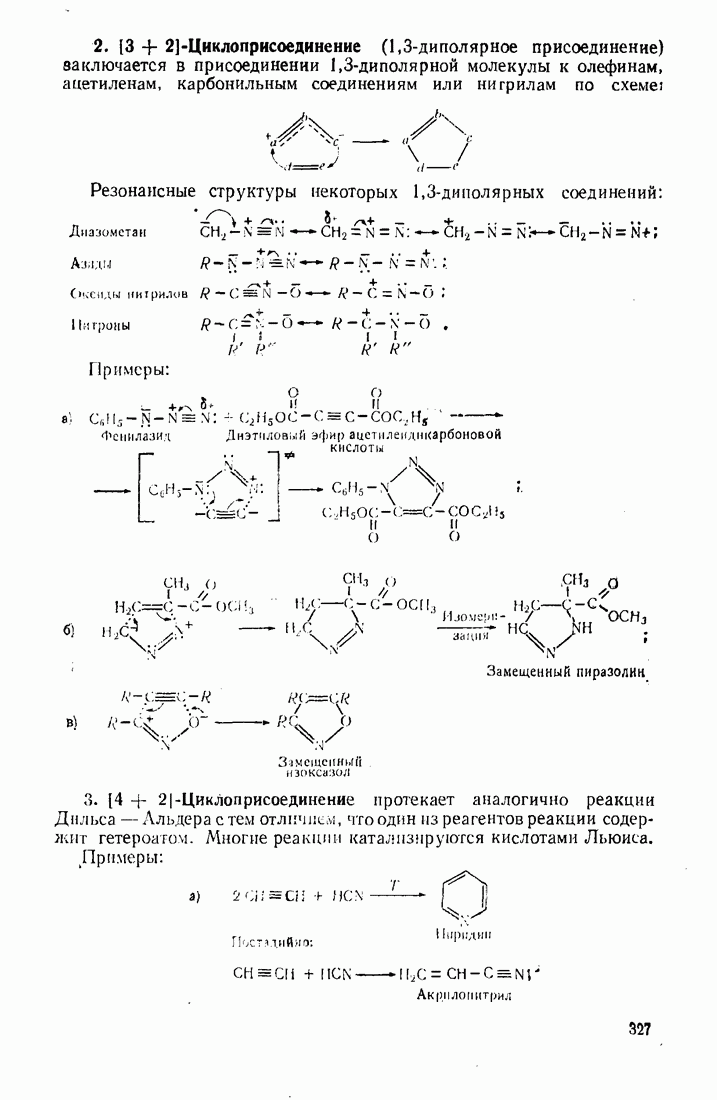
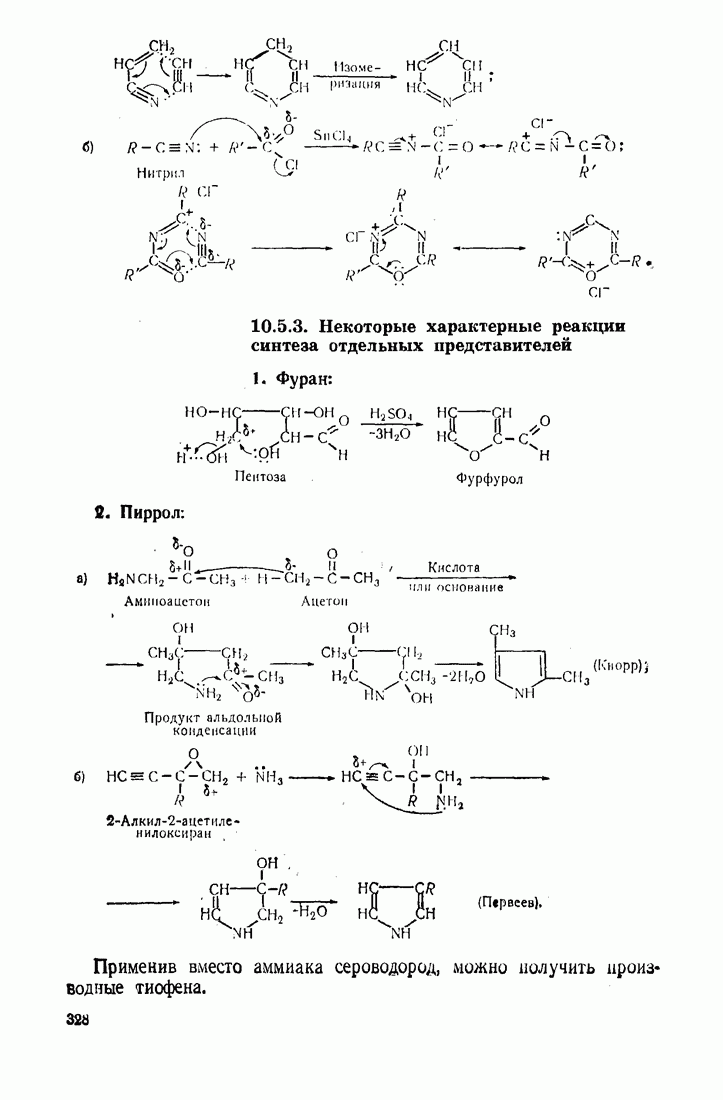
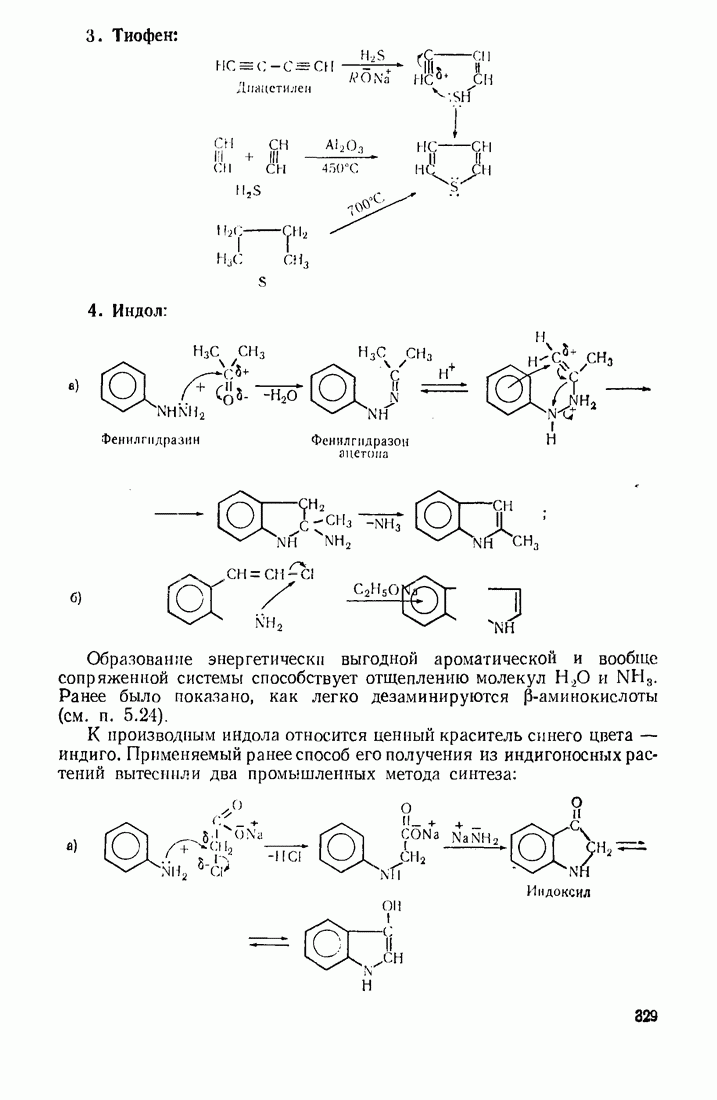
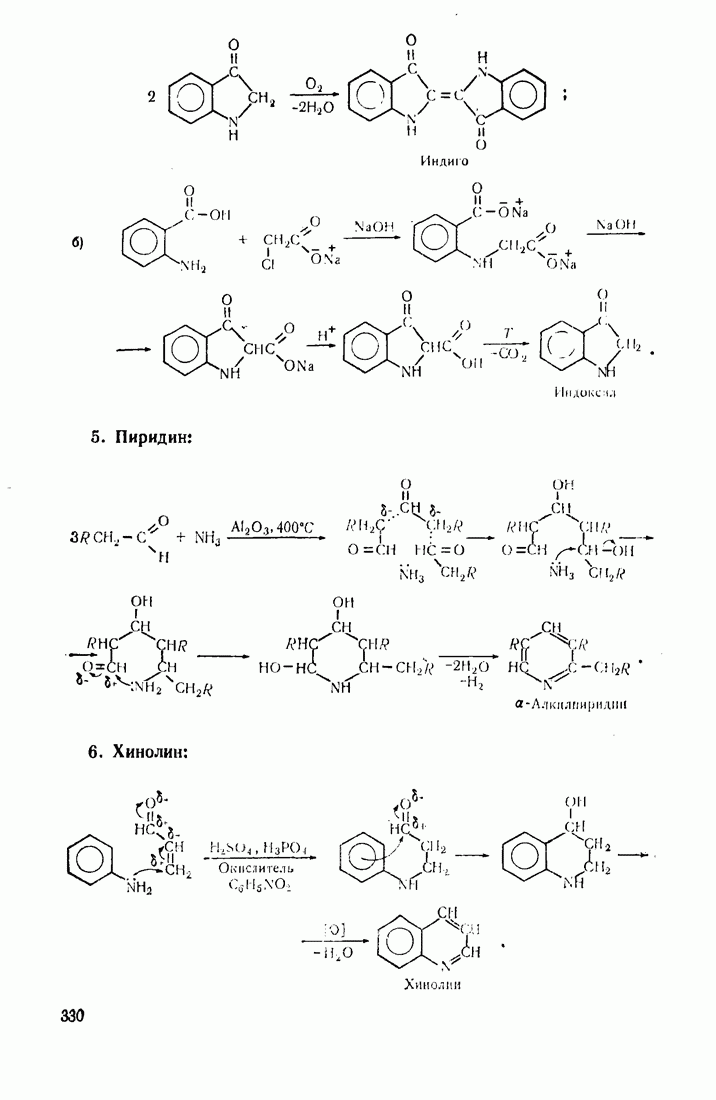
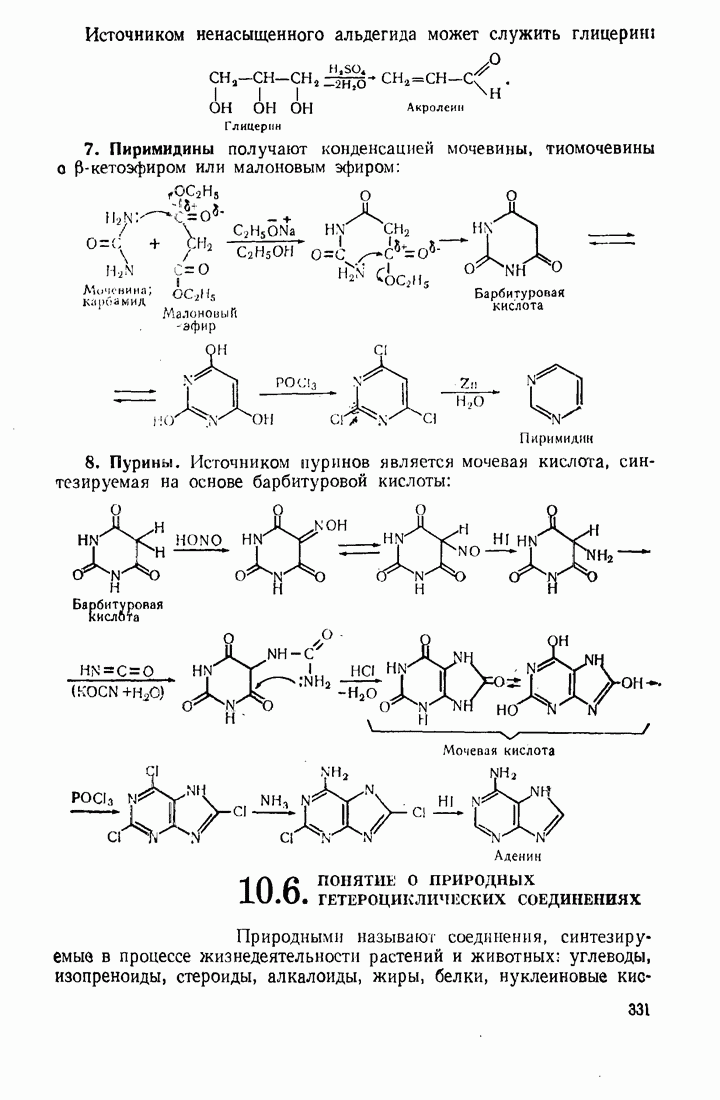
- 10.5. МЕТОДЫ СИНТЕЗА ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ
- 10.6. П0НЯТИЕ О ПРИРОДНЫХ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЯХ
- 11. Зпементоорганические соединения
- 11.2. ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ НЕКОТОРЫХ НЕМЕТАЛЛОВ
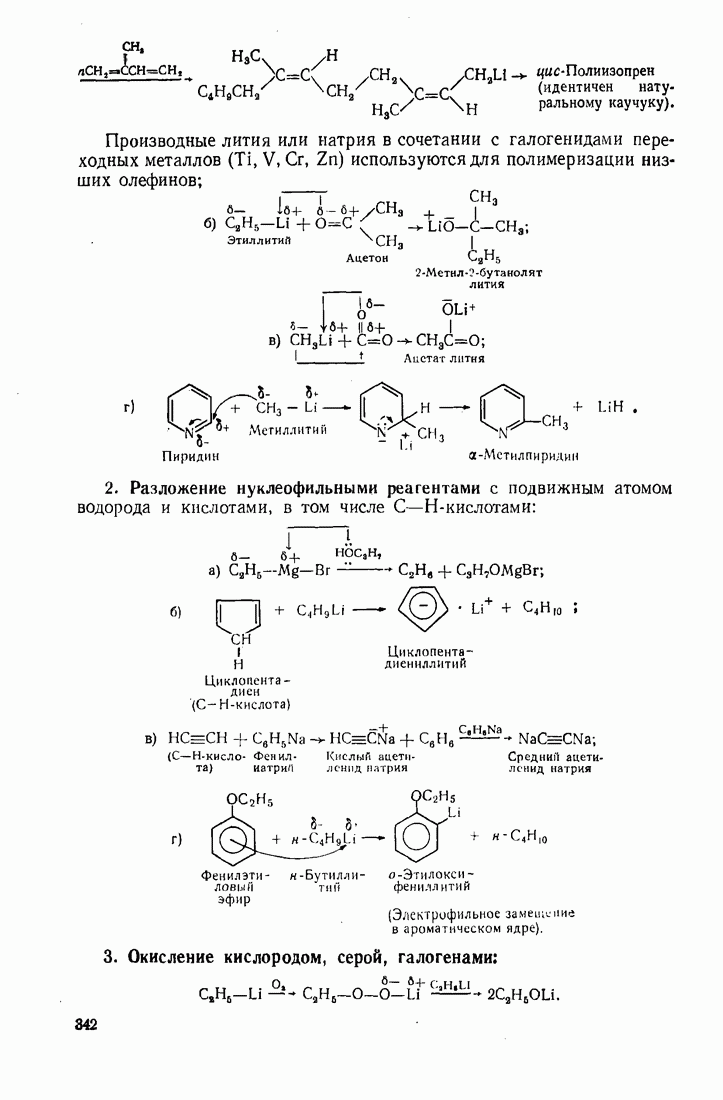
- 11.3. МЕГАЛЛООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
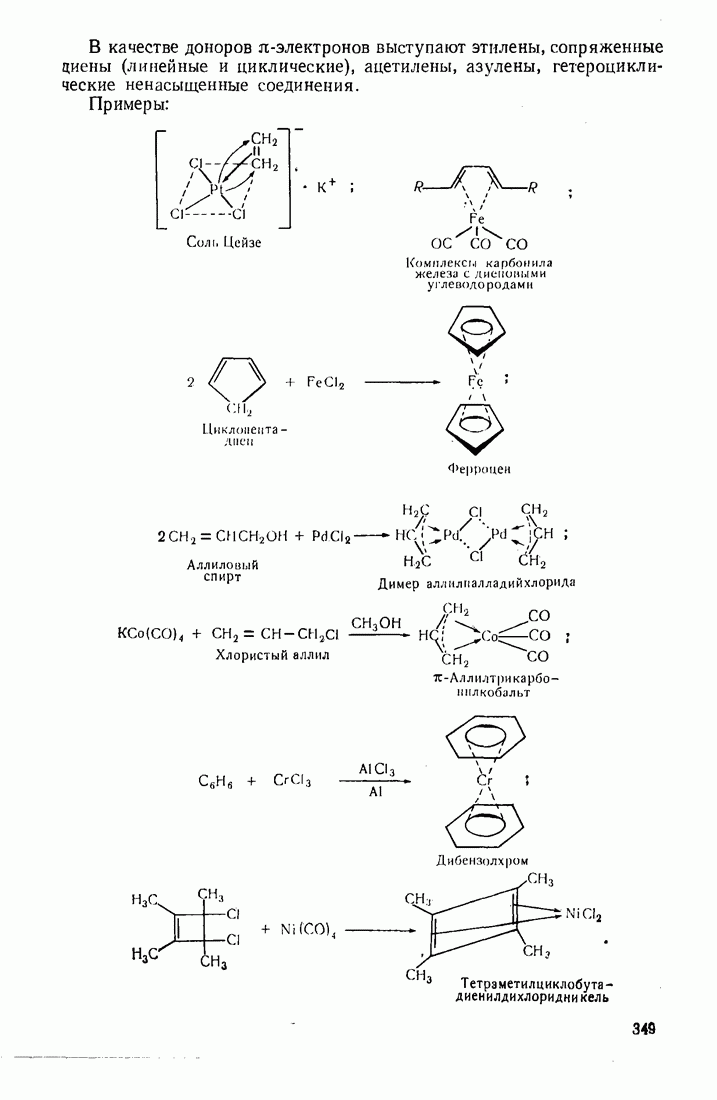
- 11.4. ОРГАНИЧЕСКИЕ ПРОИЗВОДНЫЕ ПЕРЕХОДНЫХ МЕТАЛЛОВ
- 12. Сырье и основные направления развития промышленности органического синтеза
- 12.1.1. Нефть и сопутствующий природный газ
- 12.1.2. Углехимическое сырье
- 12.1.3. Лесохимическое и сельскохозяйственное сырье
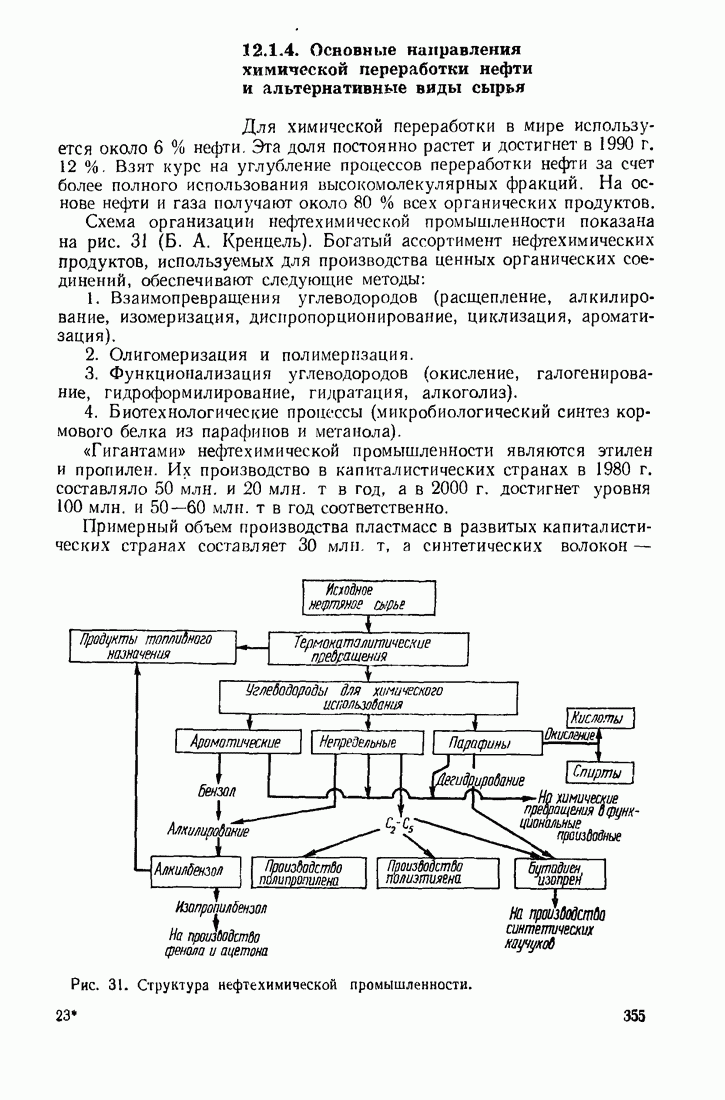
- 12.1.4. Основные направления химической переработки нефти и альтернативные виды сырья
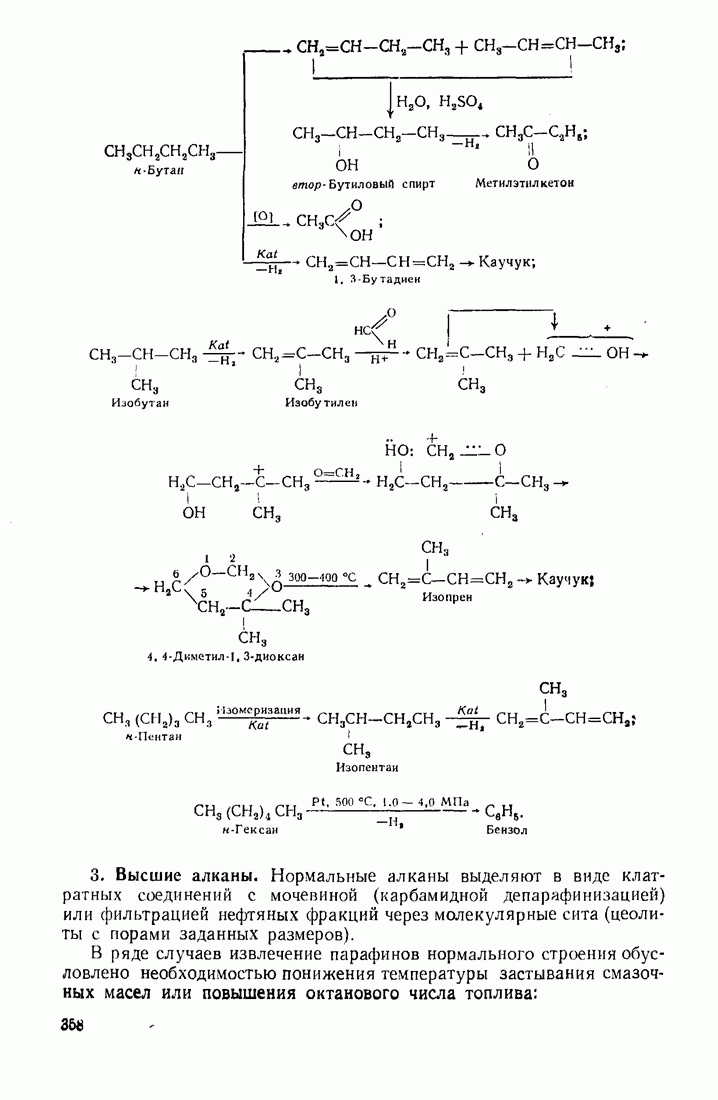
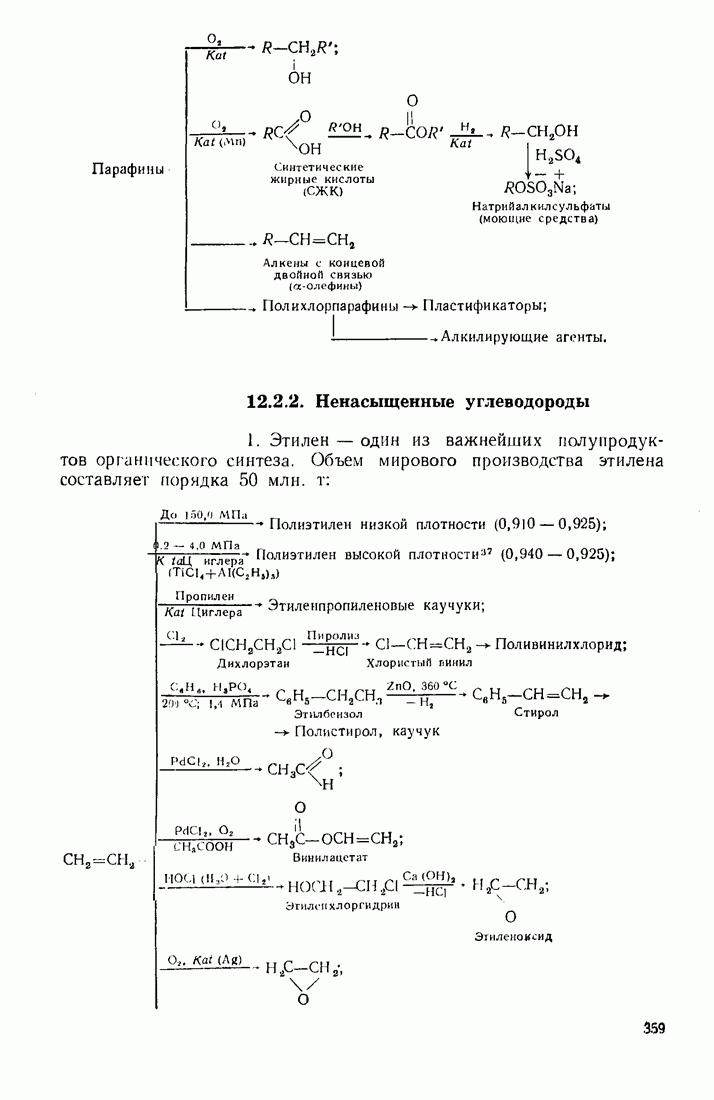
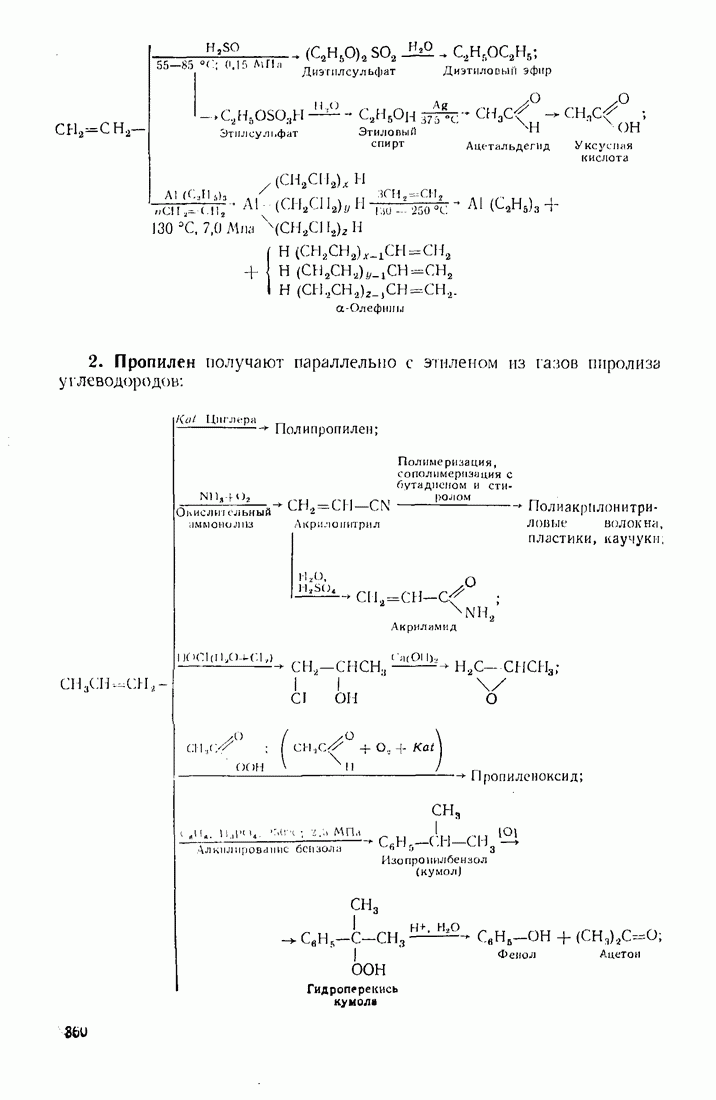
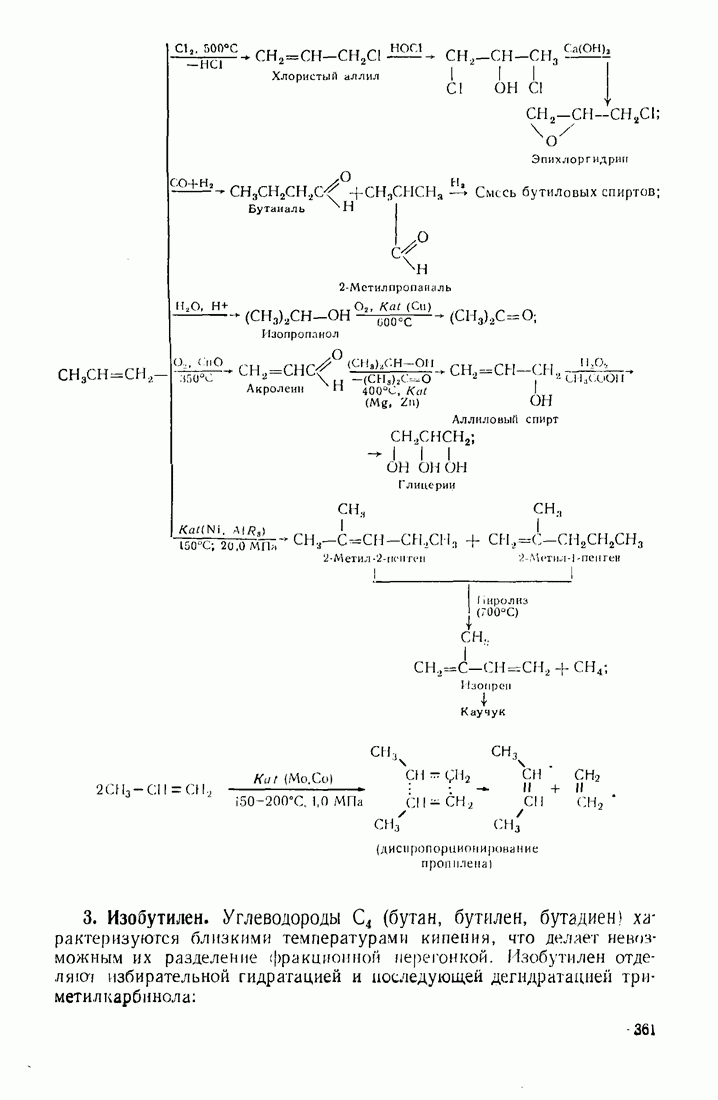
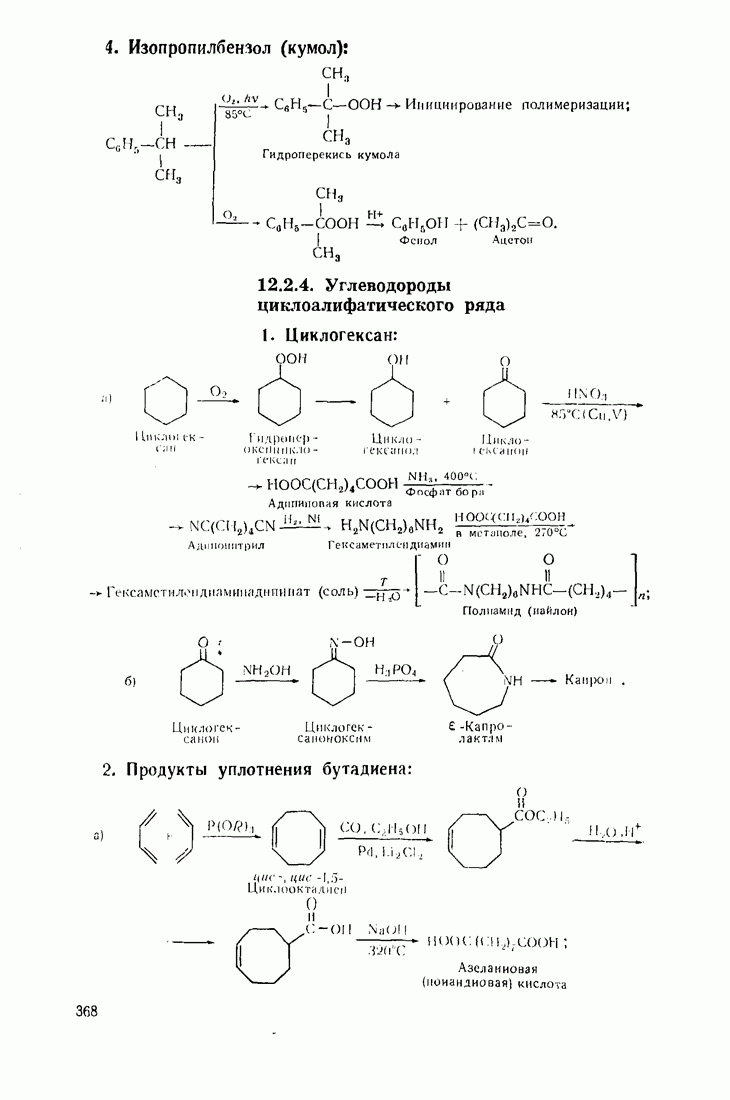
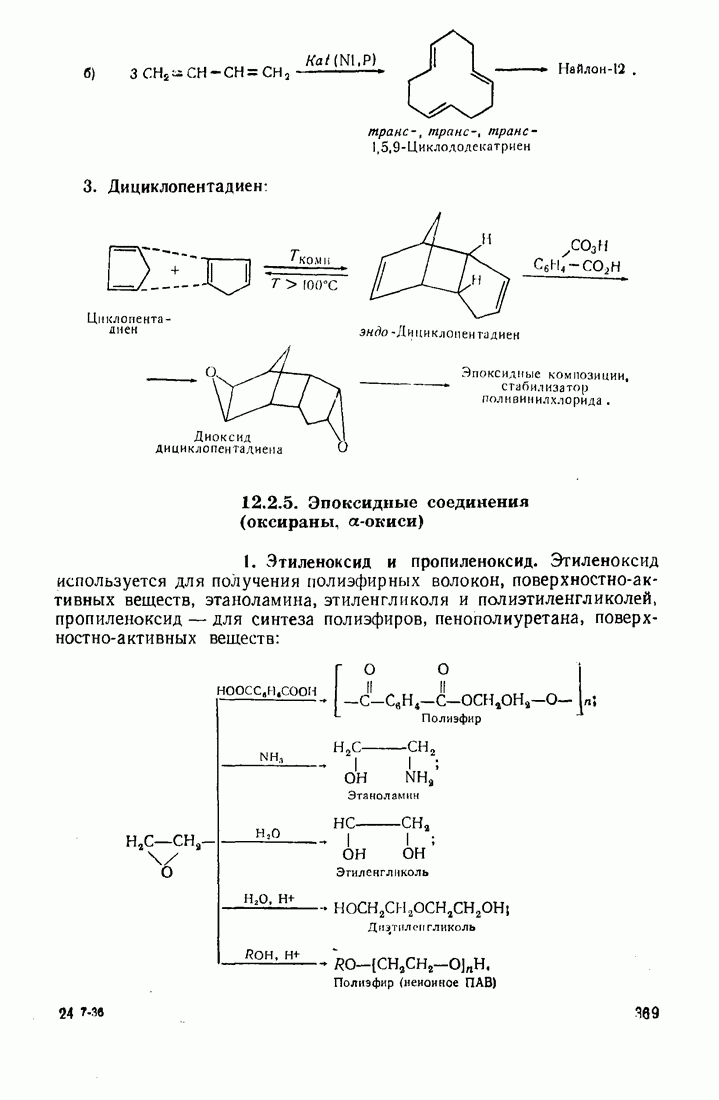
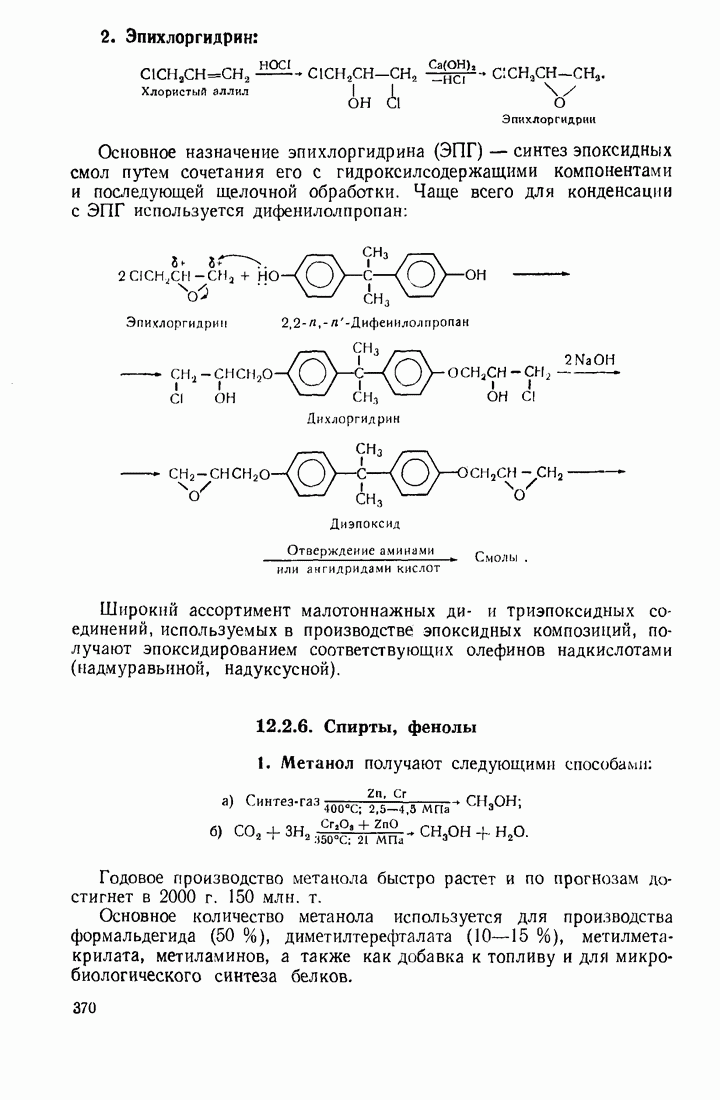
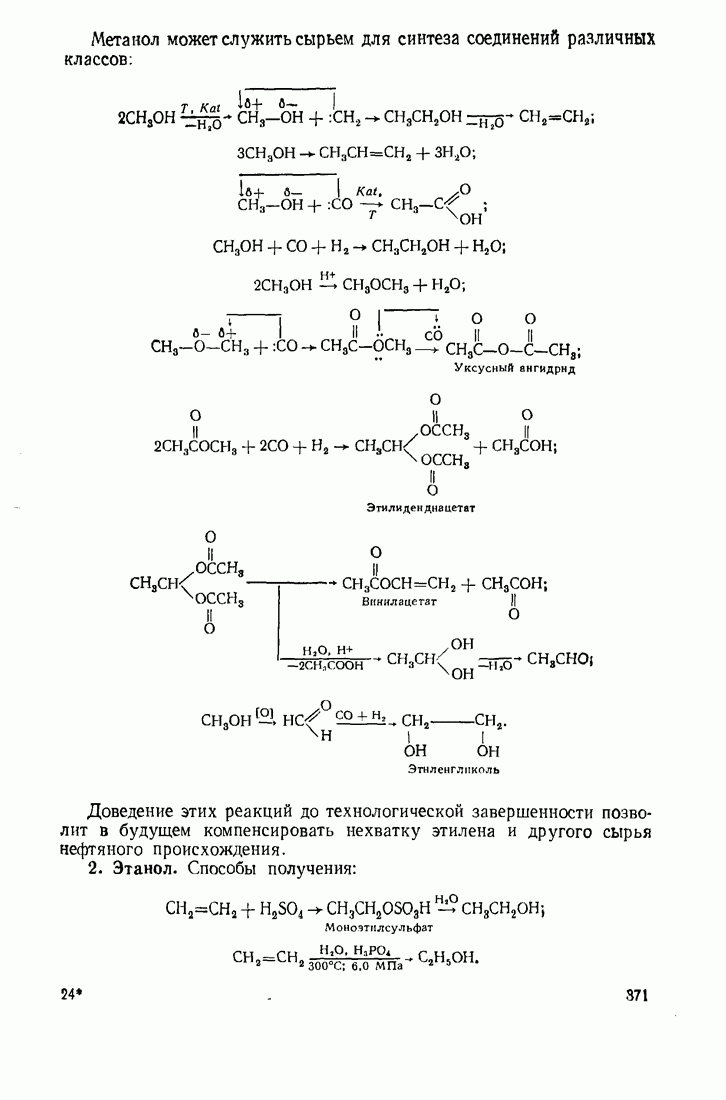
- 12.2. ПУТИ ИСПОЛЬЗОВАНИЯ УГЛЕВОДОРОДОВ И ИХ ПРОИЗВОДНЫХ
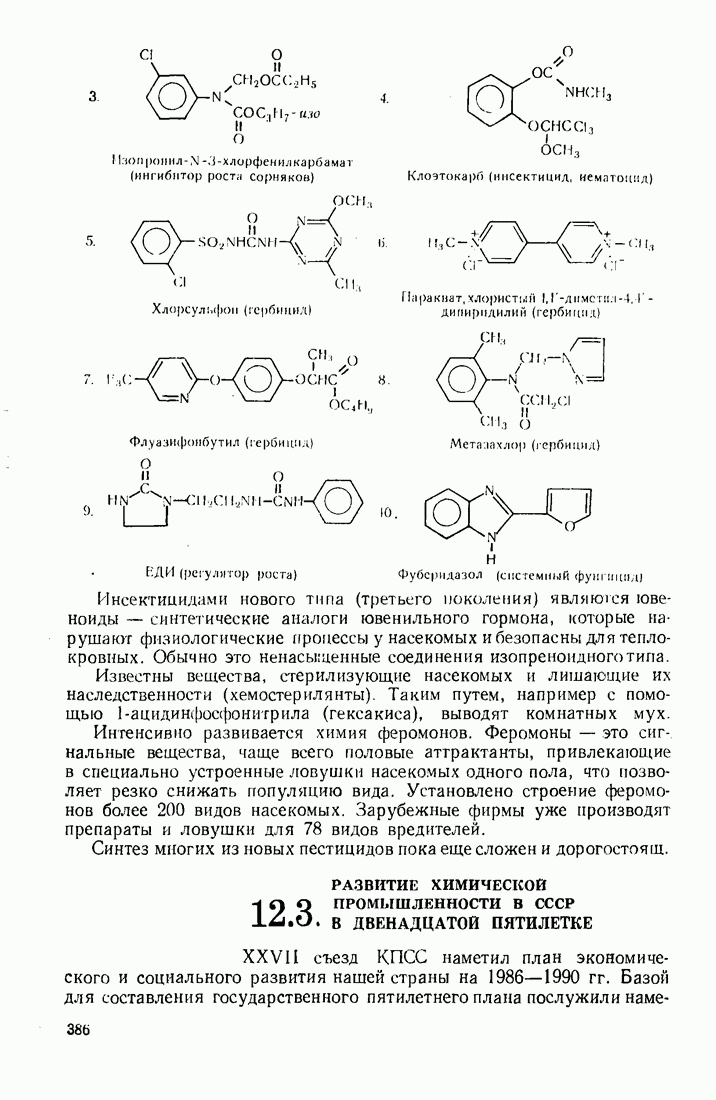
- 12.3. РАЗВИТИЕ ХИМИЧЕСКОЙ ПРОМЫШЛЕННОСТИ В СССР В ДВЕНАДЦАТОЙ ПЯТИЛЕТКЕ