| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
6.4. ОРГАНИЧЕСКИЕ РАСТВОРИТЕЛИ И ИХ ВЛИЯНИЕ НА СКОРОСТЬ И МЕХАНИЗМ РЕАКЦИЙ
В соответствии с природой межмолекулярных взаимодействий растворители делят на три группы.
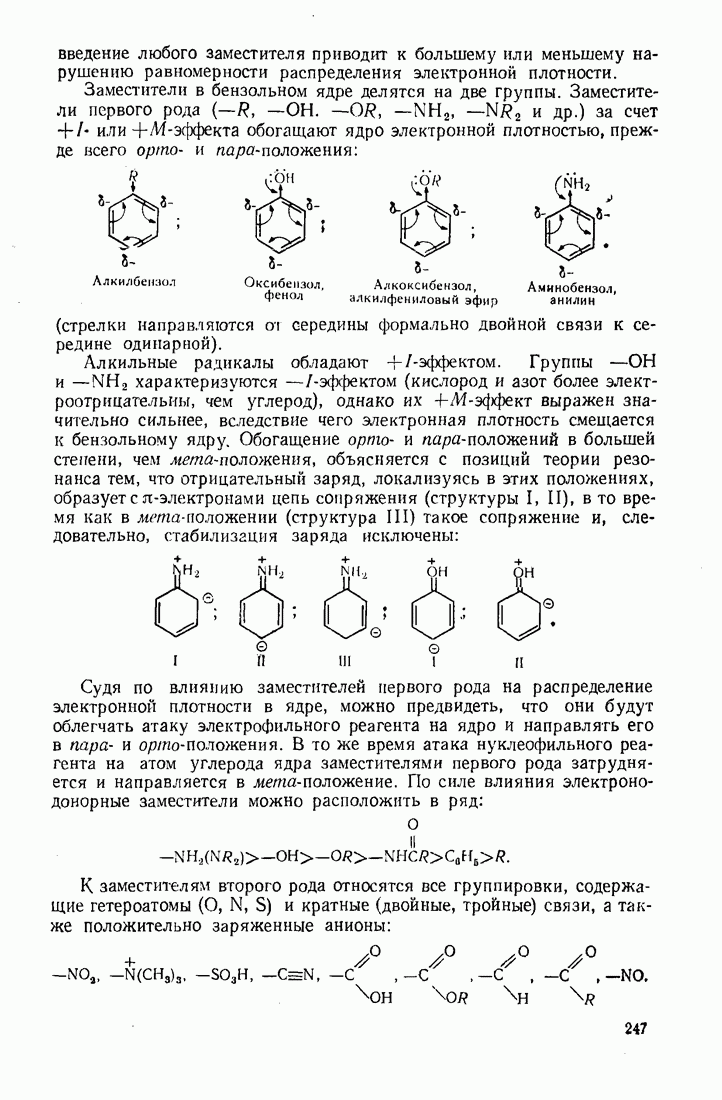
1. Неполярные апротонные растворители, обладающие небольшим или равным нулю дипольпым моментом  и малой диэлектрической проницаемостью
и малой диэлектрической проницаемостью  (табл. 9.).
(табл. 9.).
Таблица 9. (см. скан) Физические свойства некоторых неполярных апротонных растворителей
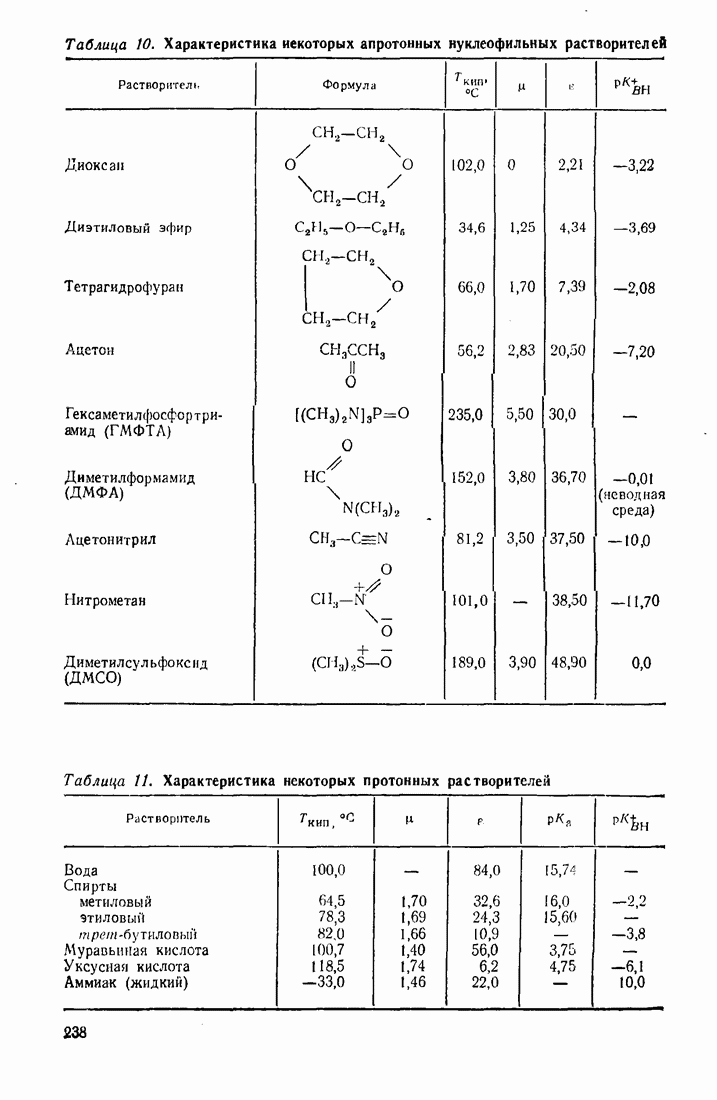
2. Апротонные нуклеофильные (основные) растворители, способные к образованию донорно-акцепторных комплексов, в том числе водородных связен (табл. 10). Эти растворители хорошо сольватируют катионы и реакционные центры, несущие дробный положительный заряд.
Как видно из таблицы, апротонные нуклеофильные растворители в большей или меньшей мере полярны. Многие из них характеризуются высокой диэлектрической проницаемостью  и классифицируются как биполярные.
и классифицируются как биполярные.
3. Третью группу составляют протонные растворители, отличающиеся ярко выраженной способностью образовывать водородные связи за счет подвижного протона (табл. 11). В целом растворители этого типа амфотерны и способны к лвтопротолизу.
Для растворителей, обладающих свойствами кислот или оснований, справедливы принципы ЖМКО. Например, водородные связи  (тип -
(тип - -жесткий») намного прочнее связей
-жесткий») намного прочнее связей  («мягкий—жесткий»). Жесткие растворители (вода, спирты, карбоновые кислоты) хорошо сольватируют малые жесткие катионы
(«мягкий—жесткий»). Жесткие растворители (вода, спирты, карбоновые кислоты) хорошо сольватируют малые жесткие катионы  и анноны
и анноны  Последние гораздо меньше сольватируются в ДМСО и ДМФА, в связи с чем повышается их нуклеофильность. «Мягкий» растворитель — ацетонитрил — плохо сольватирует
Последние гораздо меньше сольватируются в ДМСО и ДМФА, в связи с чем повышается их нуклеофильность. «Мягкий» растворитель — ацетонитрил — плохо сольватирует
(см. скан)
Н-кислоты, но хорошо комплексуется с мягкими кислотами ( и др.).
и др.).
Растворители активно участвуют в органических реакциях. Различают два типа взаимодействия растворителя с реагентом.
1. Неспецифическое взаимодействие, обусловленное электростатическими и дисперсионными силами (взаимодействие типа «диполь—диполь», «диполь — наведенный диполь» или «ион—диполь»).
2. Специфическое взаимодействие, обусловленное образованием различных по природе донорно-акцепторных комплексов, в том числе водородных связей.
Влияние растворителя проявляется в сольватации исходных реагентов, катализаторов, активированных комплексов, а также промежуточных частиц: катионов, анионов и радикалов. Перераспределение электронной плотности между реагентами и промежуточными комплексами или частицами требует разрушения сольватных оболочек, что связано с некоторыми энергетическими затратами.
В ряде случаев во влиянии растворителя на скорость ил равновесие процессов на первый план выступает полярность растворителя. Так, повышение полярности среды способствует разделению зарядов (поляризации) в исходных реагентах и активированных комплексах при галогеннровапин и гпдрогалогенировании непредельных углеводородов.
Полярный растворитель повышает скорость реакции нуклеофильного замещения, если в активированном комплексе разделение зарядов выражено сильнее, чем в исходных реагентах:

Если полярность системы при продвижении к активированному комплексу уменьшается, полярный растворитель препятствует реакции, так как исходные реагенты сольватируются более эффективно:

Гораздо чаще доминирующее влияние на скорость и направление процесса оказывают кислотно-основные (допорно-акцепторные) свойства растворителя, В реакциях отщепления и нуклеофильного замещения у атомов углерода, кислорода и других гетероатомов важным моментом является сольватация и отщепление аниона, что невозможно без эффективной специфической его сольватации прежде всего за счет образования водородных связен. Например, а  и
и  реакции типа
реакции типа  не протекают, так как они
не протекают, так как они  способнысольватировать анионы (положительные концы диполей их молекул экранированы метильпьшп заместителями). Если же под влиянием каких-либо факторов анион «оголяется», например при заключении спаренного с ним катиона
способнысольватировать анионы (положительные концы диполей их молекул экранированы метильпьшп заместителями). Если же под влиянием каких-либо факторов анион «оголяется», например при заключении спаренного с ним катиона  полость краун-эфира, то в силу слабой сольватации он обладает повышен
полость краун-эфира, то в силу слабой сольватации он обладает повышен  реакционной способностью (нуклеофильностыо).
реакционной способностью (нуклеофильностыо).
Изменение сольватирующей способности растворителя может изменить не только вклад механизмов  , но и соотношение
, но и соотношение
скоростей конкурирующих реакций  и
и  . В качестве примера можно привести реакцию сольволиза трет-бутилгалогенидов в воде и этиловом спирте. В водной среде реализуется чистый карбониево-ионный механизм, поэтому соотношение выходов продуктов замещения
. В качестве примера можно привести реакцию сольволиза трет-бутилгалогенидов в воде и этиловом спирте. В водной среде реализуется чистый карбониево-ионный механизм, поэтому соотношение выходов продуктов замещения  и отщепления
и отщепления  не зависит от природы галогена. В спирте же, обладающем более низкой сольватирующей способностью, при повышении нуклеофильности галогена
не зависит от природы галогена. В спирте же, обладающем более низкой сольватирующей способностью, при повышении нуклеофильности галогена  наблюдается преобладание реакции отщепления. Чувствительность реакции к природе галогена свидетельствует о том, что нуклеофил
наблюдается преобладание реакции отщепления. Чувствительность реакции к природе галогена свидетельствует о том, что нуклеофил  атакует не чистый карб-катион, а контактную ионную пару
атакует не чистый карб-катион, а контактную ионную пару 
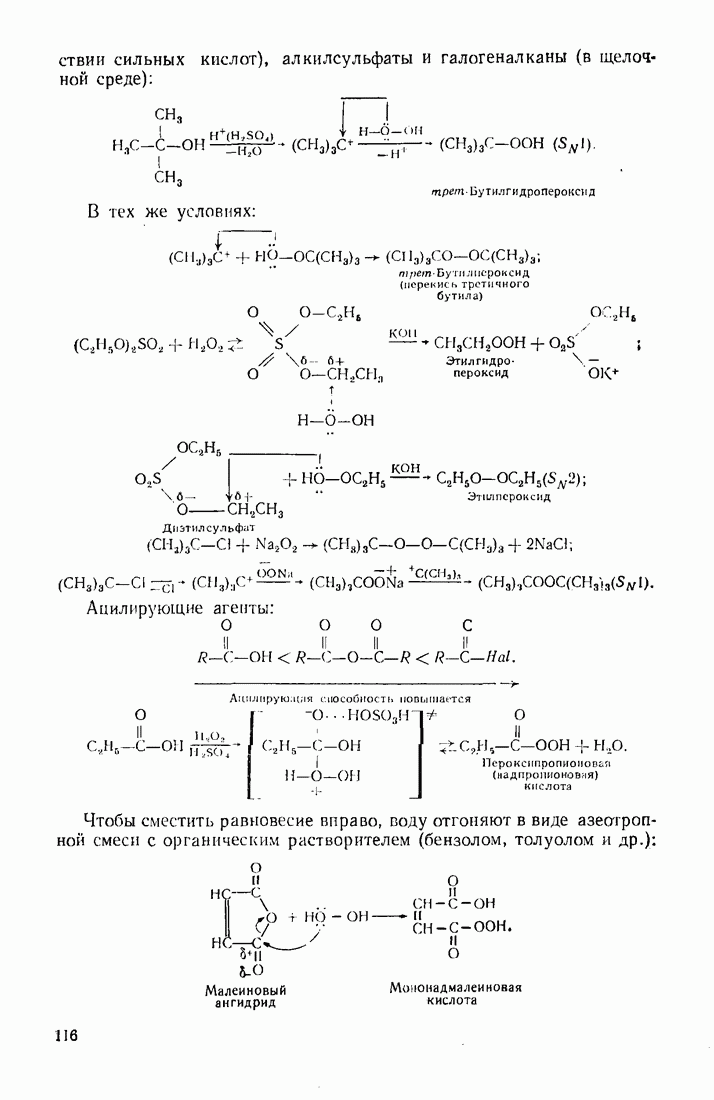
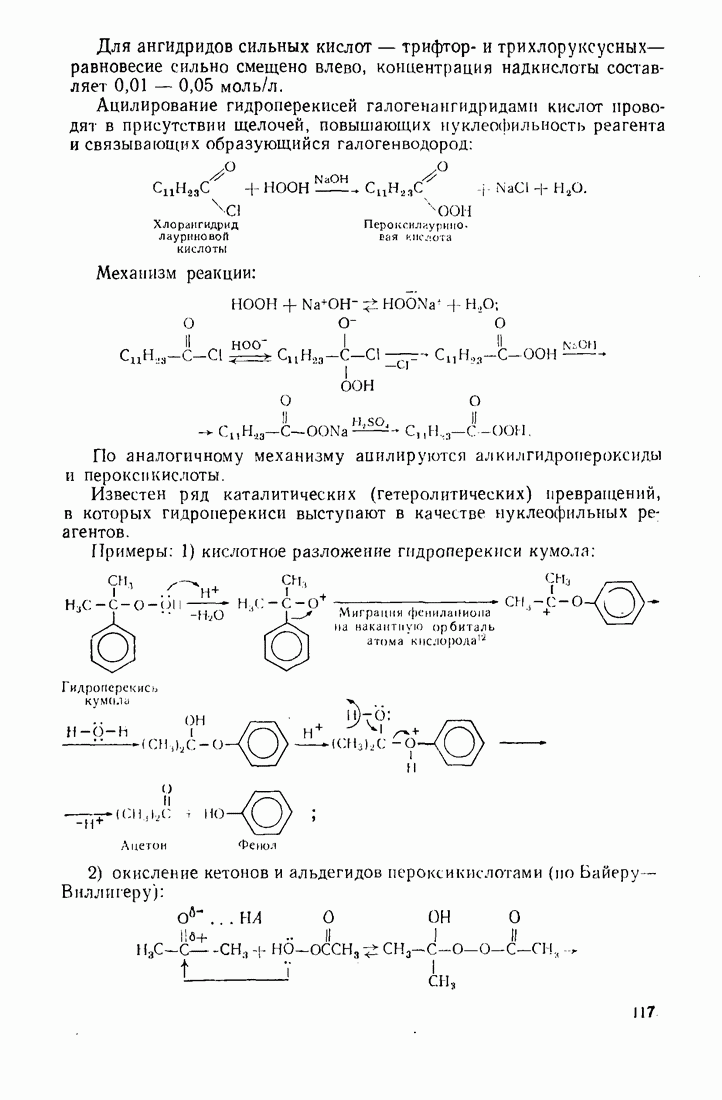
Нуклеофильные растворители могут полностью или частично блокировать электрофильный центр субстрата, препятствуя протеканию реакции. Например, ацилирование пероксида водорода уксусным ангидридом в метаноле при обычных условиях не протекает. В то же время  -бутиловый спирт способствует прохождению реакции, указывая на то, что, координируясь с реагентом, он может выполнять функцию основного катализатора:
-бутиловый спирт способствует прохождению реакции, указывая на то, что, координируясь с реагентом, он может выполнять функцию основного катализатора:

Сравнение свойств метилового и трет-бутилового спиртов позволяет судить о важной роли стерических особенностей растворителя в сольватационных явлениях.
Поскольку многие реакции подвержены бифункциональному катализу, амфотерные растворители способствуют осуществлению многоцентровых (пуш-пульных) механизмов, обеспечивая синхронность разрыва старых и образования новых связей:

Выгодно в энергетическом отношении образование циклических промежуточных комплексов, в которых реализуется синхронный электронный перенос:

Основный растворитель может связывать  -кислоту — катализатор, понижая эффективность ее действия, или блокировать электрофильный центр кислоты Льюиса, конкурируя с нуклеофильным реагентом. Примером может служить ингибирующее влияние спиртов и воды на эпоксидирование олефинов алкилгидропероксидами в присутствии соединений металлов с переменной валентностью. На первой стадии этого процесса алкилгидропероксид, как нуклеофил, образует с катализатором донорно-акцепторный комплекс.
-кислоту — катализатор, понижая эффективность ее действия, или блокировать электрофильный центр кислоты Льюиса, конкурируя с нуклеофильным реагентом. Примером может служить ингибирующее влияние спиртов и воды на эпоксидирование олефинов алкилгидропероксидами в присутствии соединений металлов с переменной валентностью. На первой стадии этого процесса алкилгидропероксид, как нуклеофил, образует с катализатором донорно-акцепторный комплекс.
Влияние растворителя на радикальные процессы проявляется значительно слабее, чем на гетеролитические или ион-радикальные, поскольку радикалы являются незаряженными частицами. В ряде случаев, однако, обнаруживается способность радикалов образовывать  или
или  -комплексы с растворителями:
-комплексы с растворителями:

При этом уменьшается реакционная способность и повышается селективность радикала.
Для радикальных реакций характерно проявление клеточного эффекта, суть которого заключается в том, что образующаяся радикальная пара заключена в оболочке из молекул растворителя и может многократно рекомбинироваться, прежде чем произойдут диффузия радикалов за пределы клетки и их дальнейшие преобразования.
Способность растворителя к гомо- и гетероассоциации определяет прочность сольватных оболочек, что, в свою очередь, влияет на скорость выхода радикалов за пределы клетки и направление развития процесса в целом.
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие
- 1. Введение
- 1.1. Предмет органической химии
- 1.2. Основные этапы развития органической химии
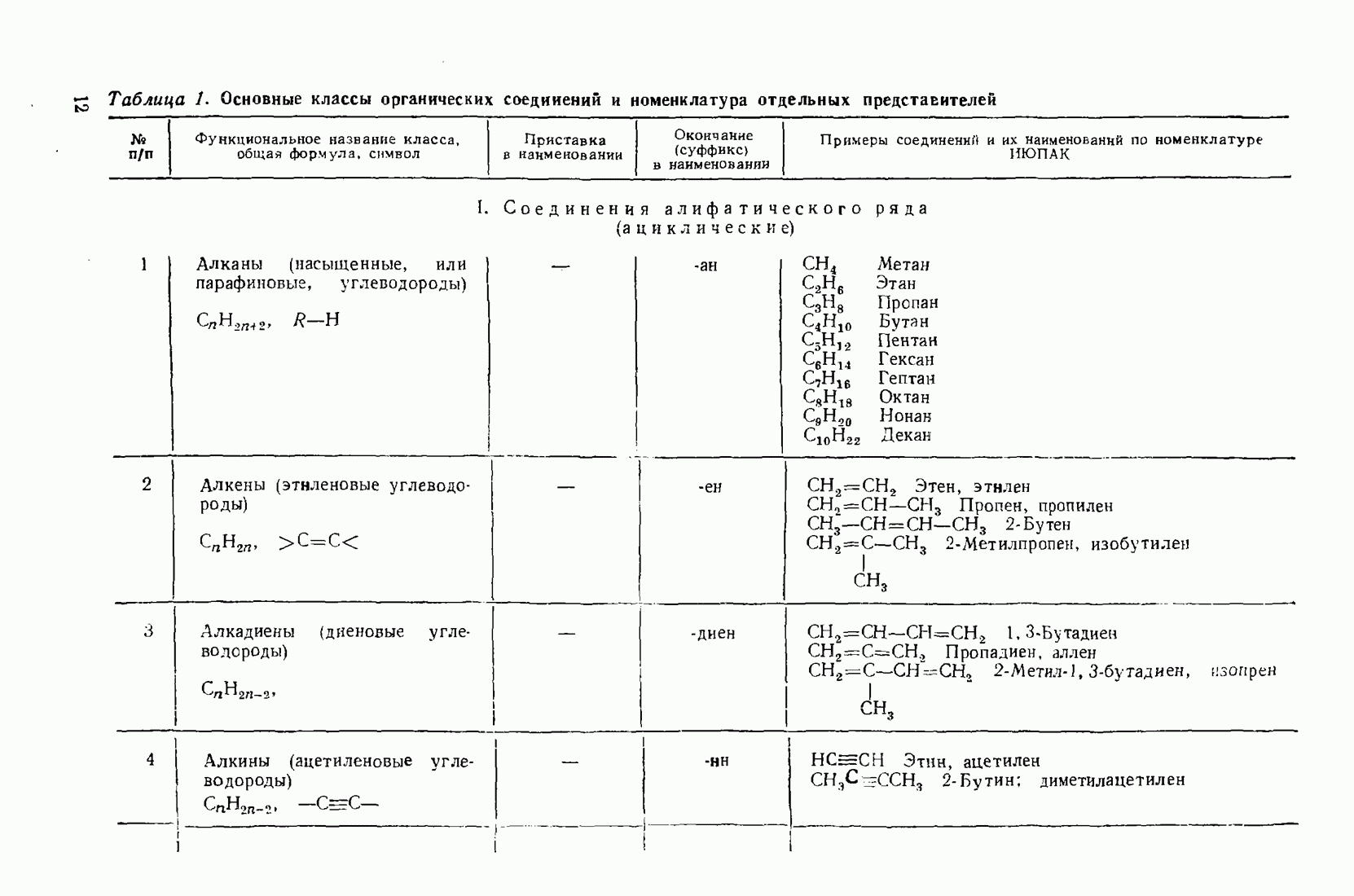
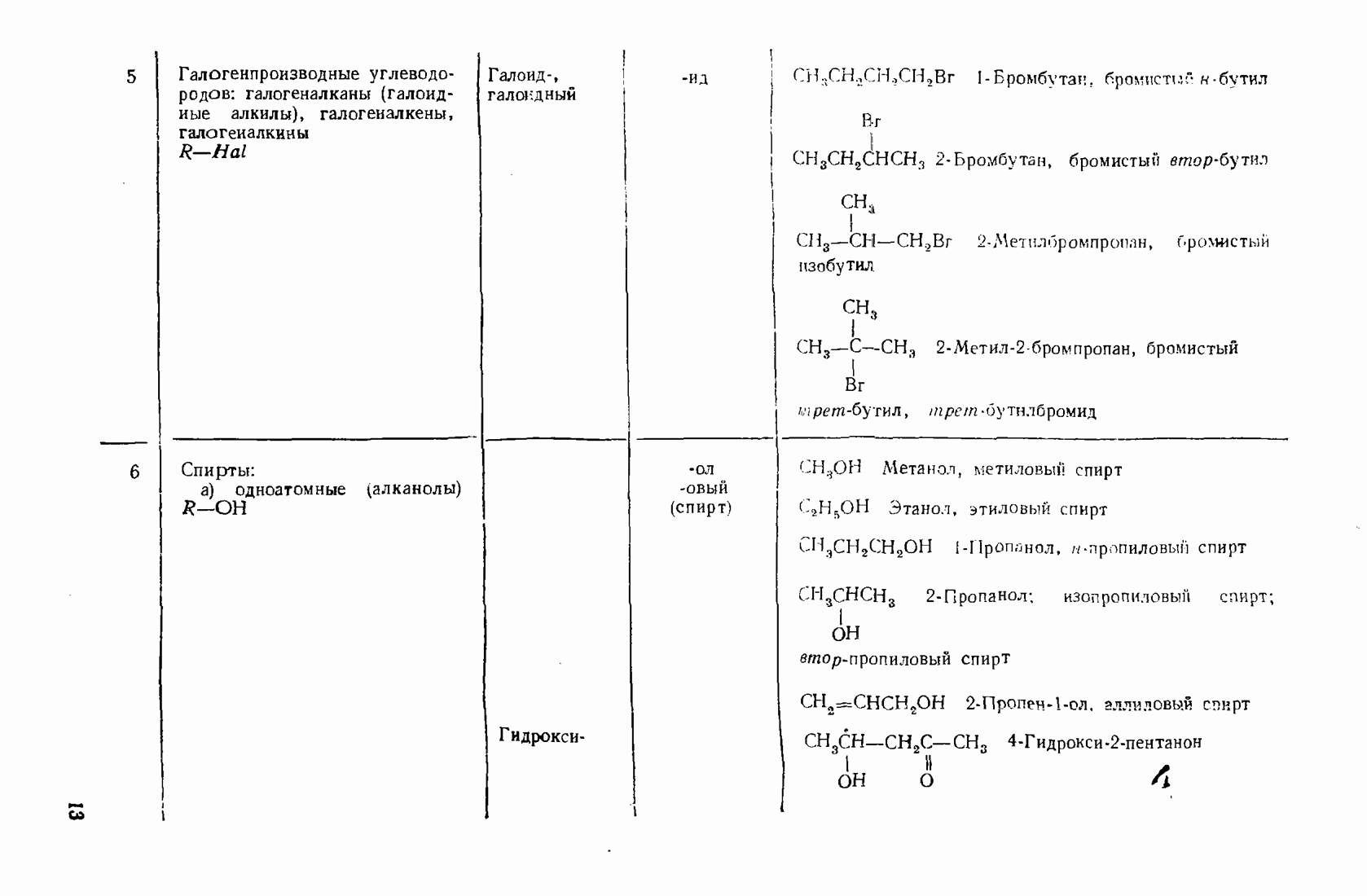
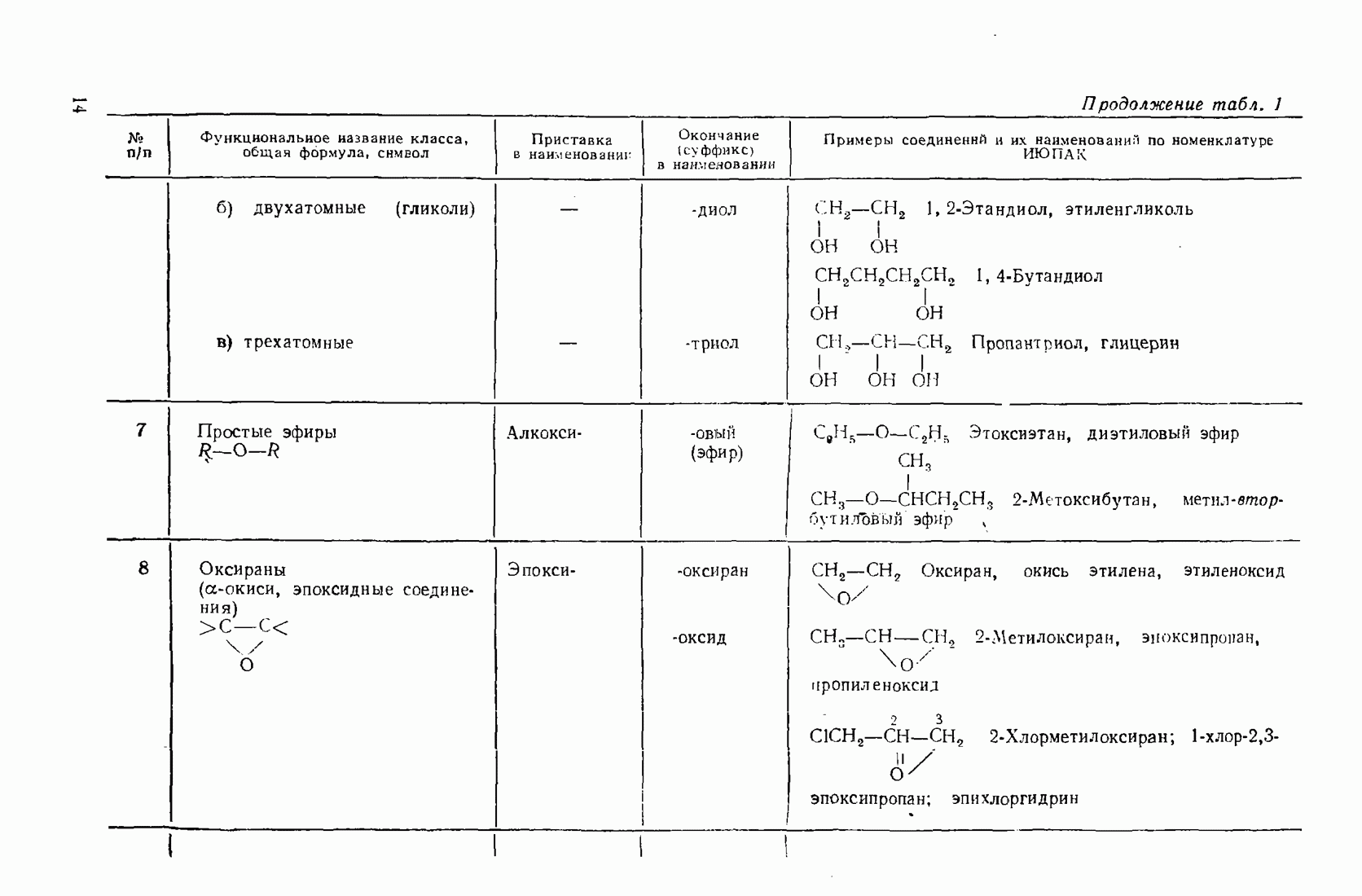
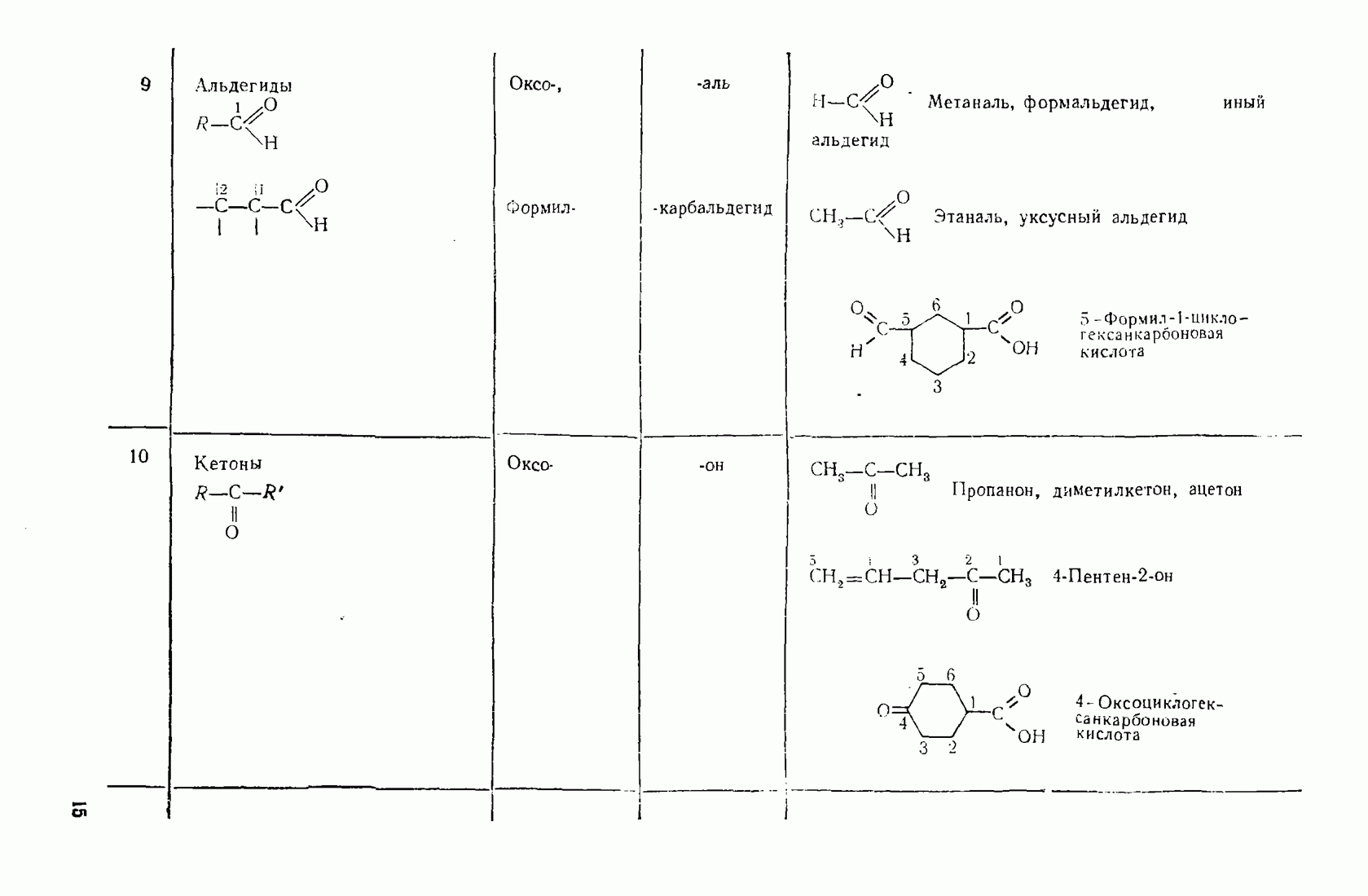
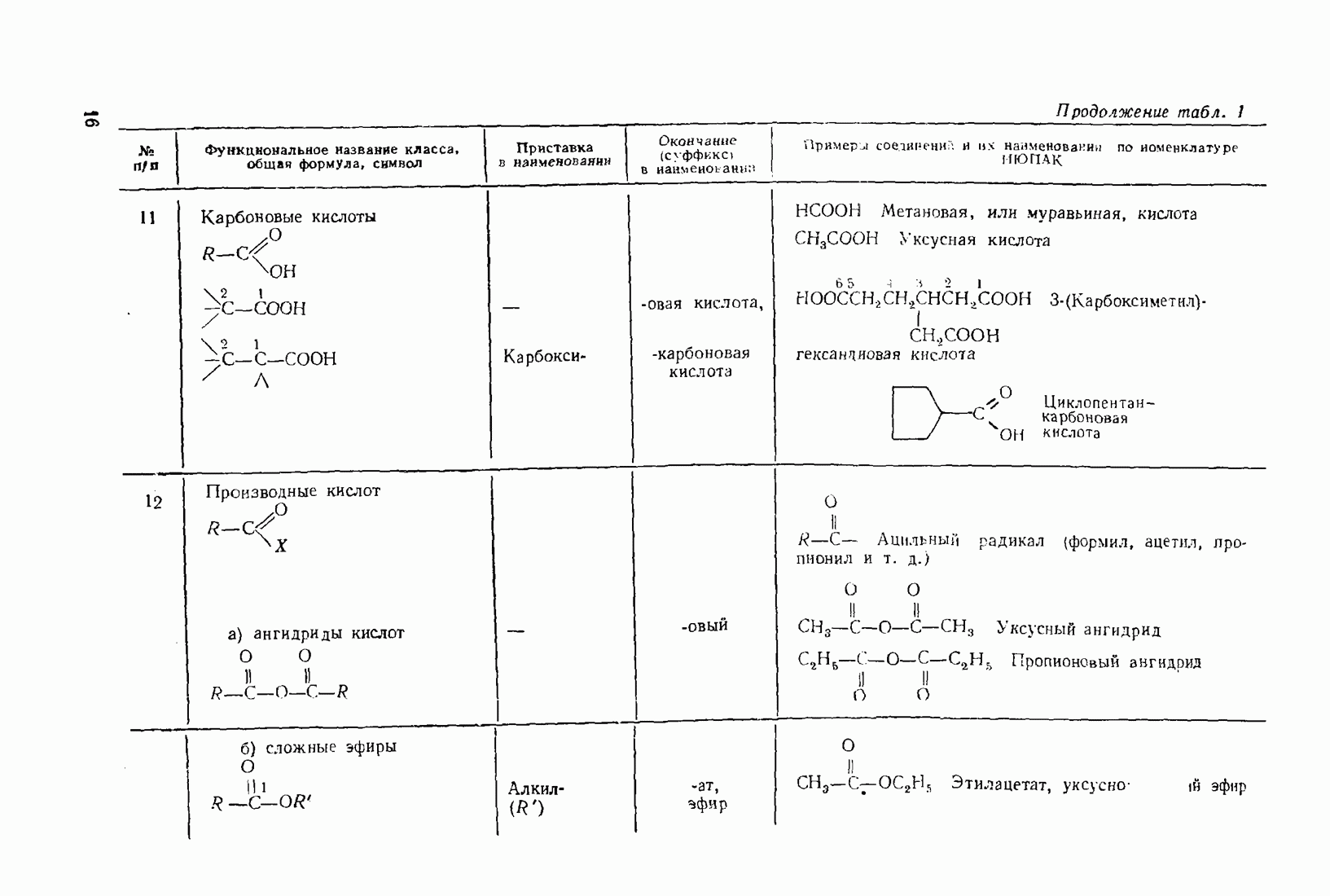
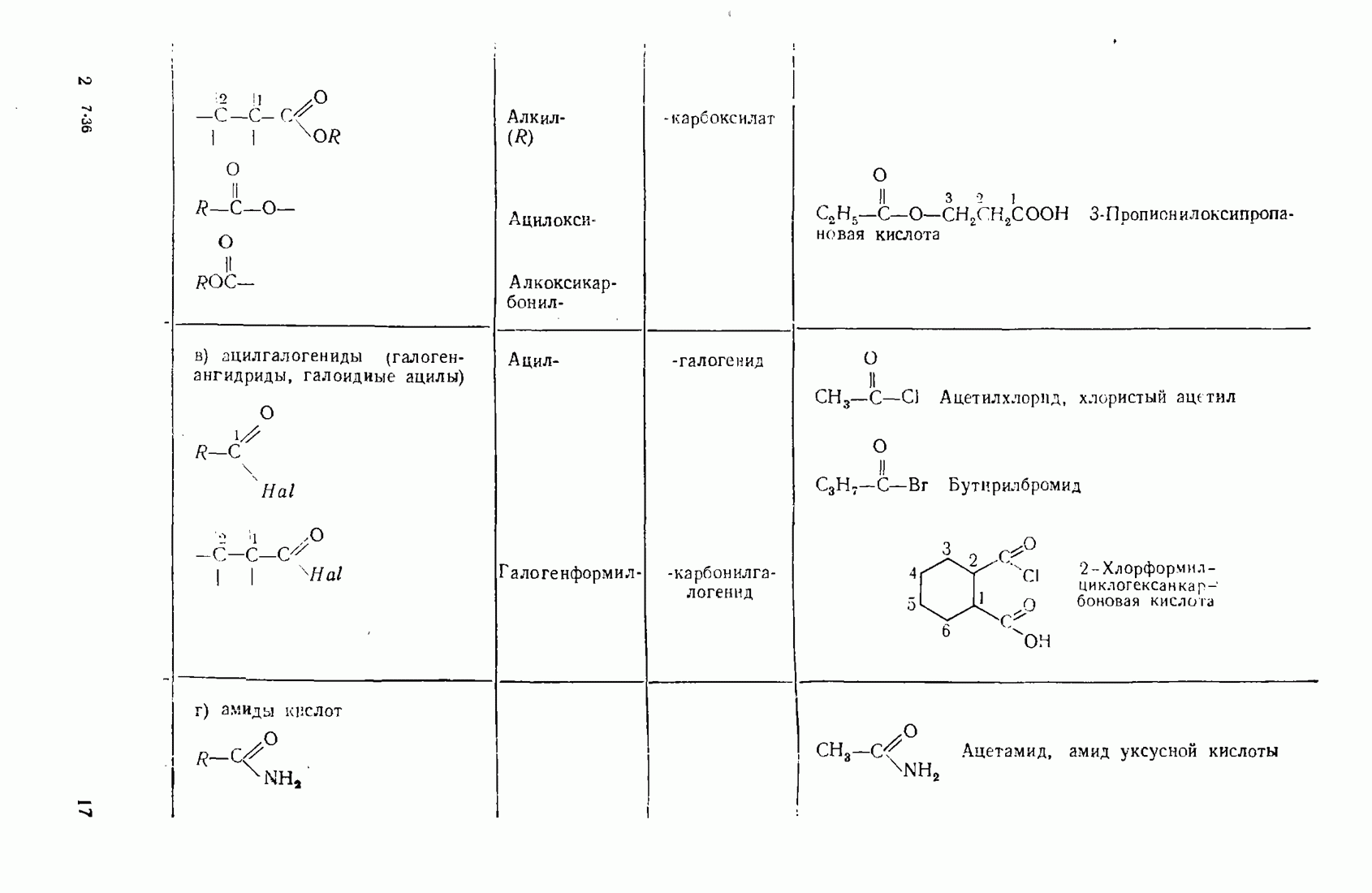
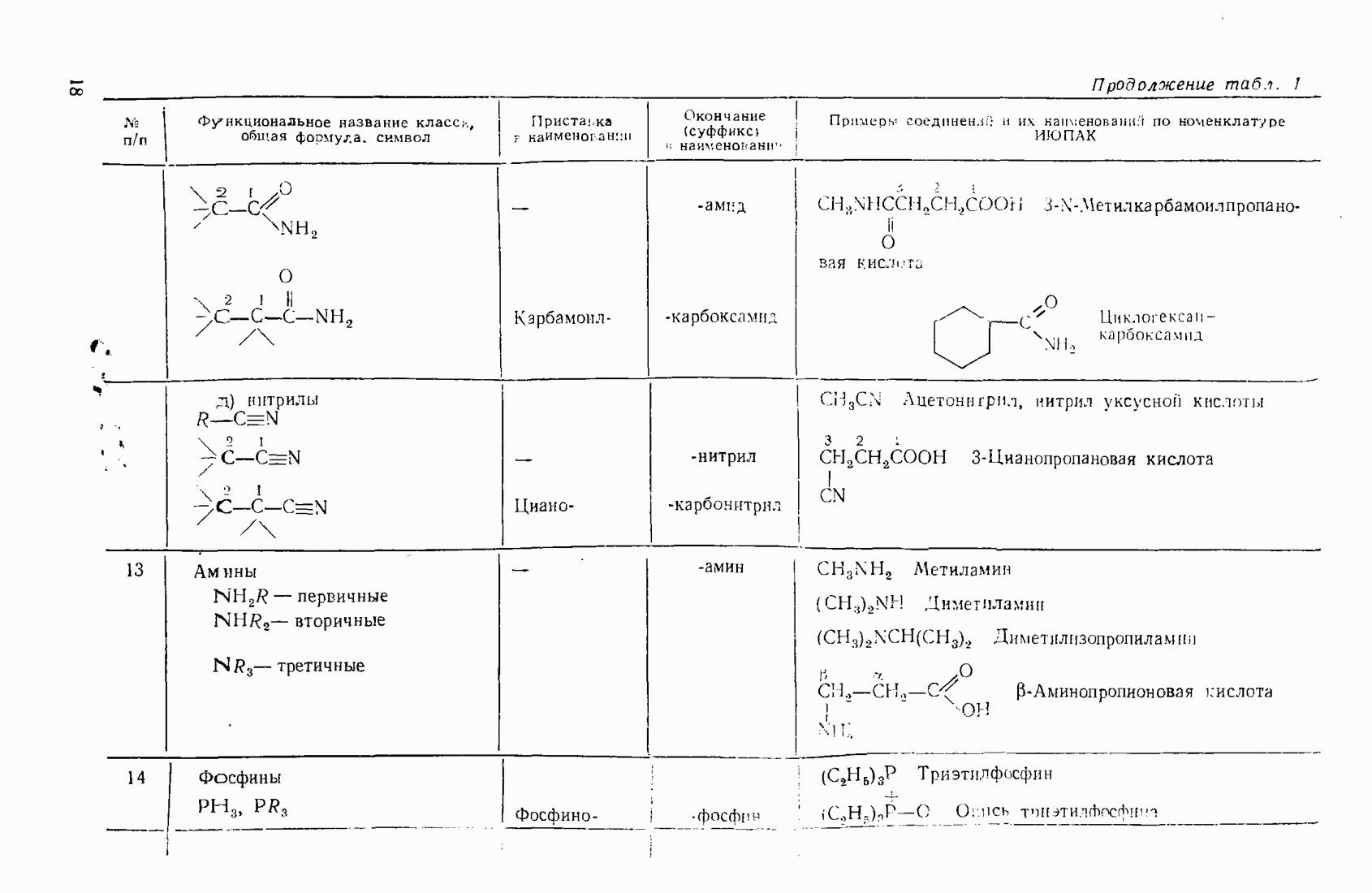
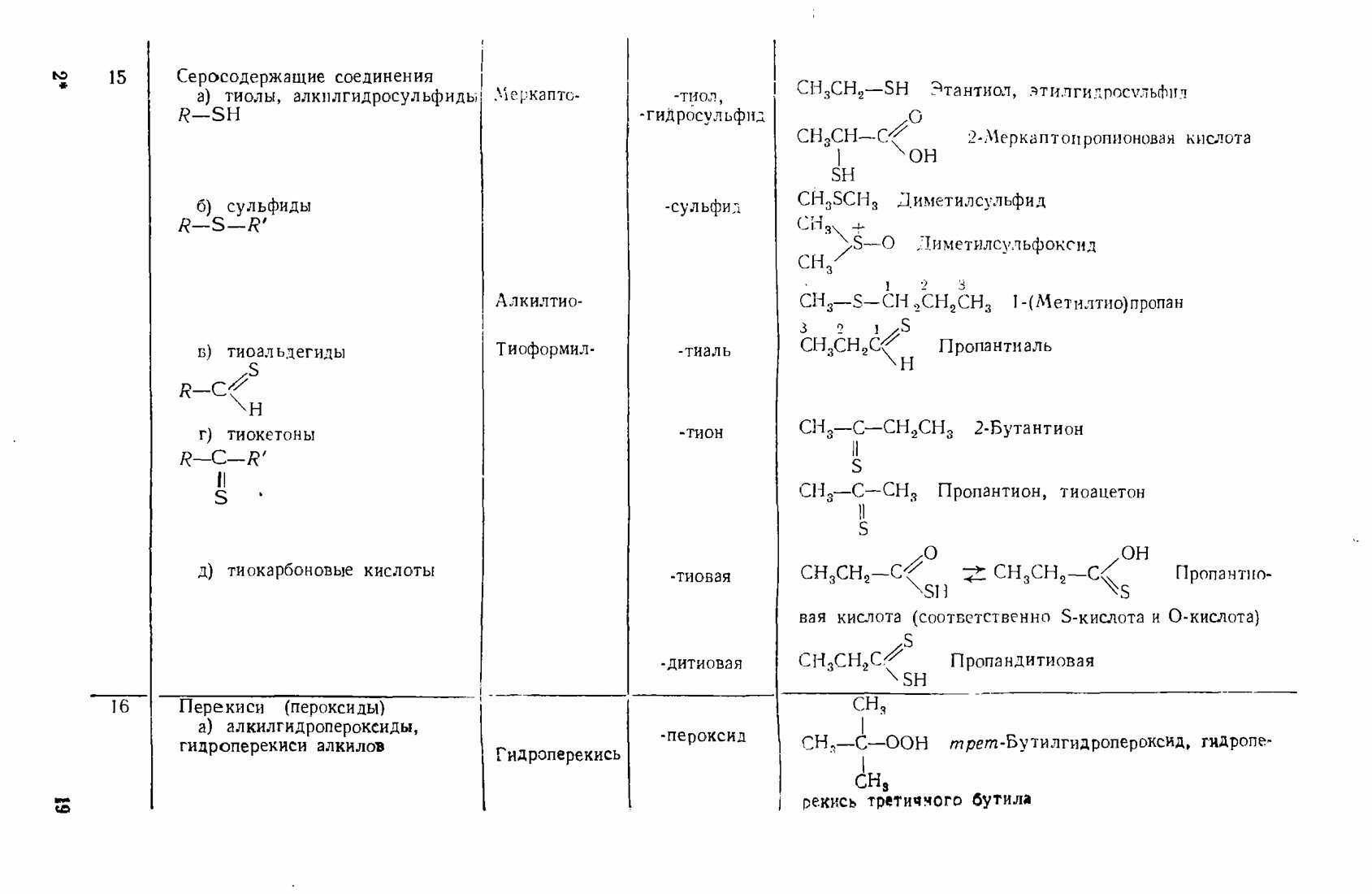
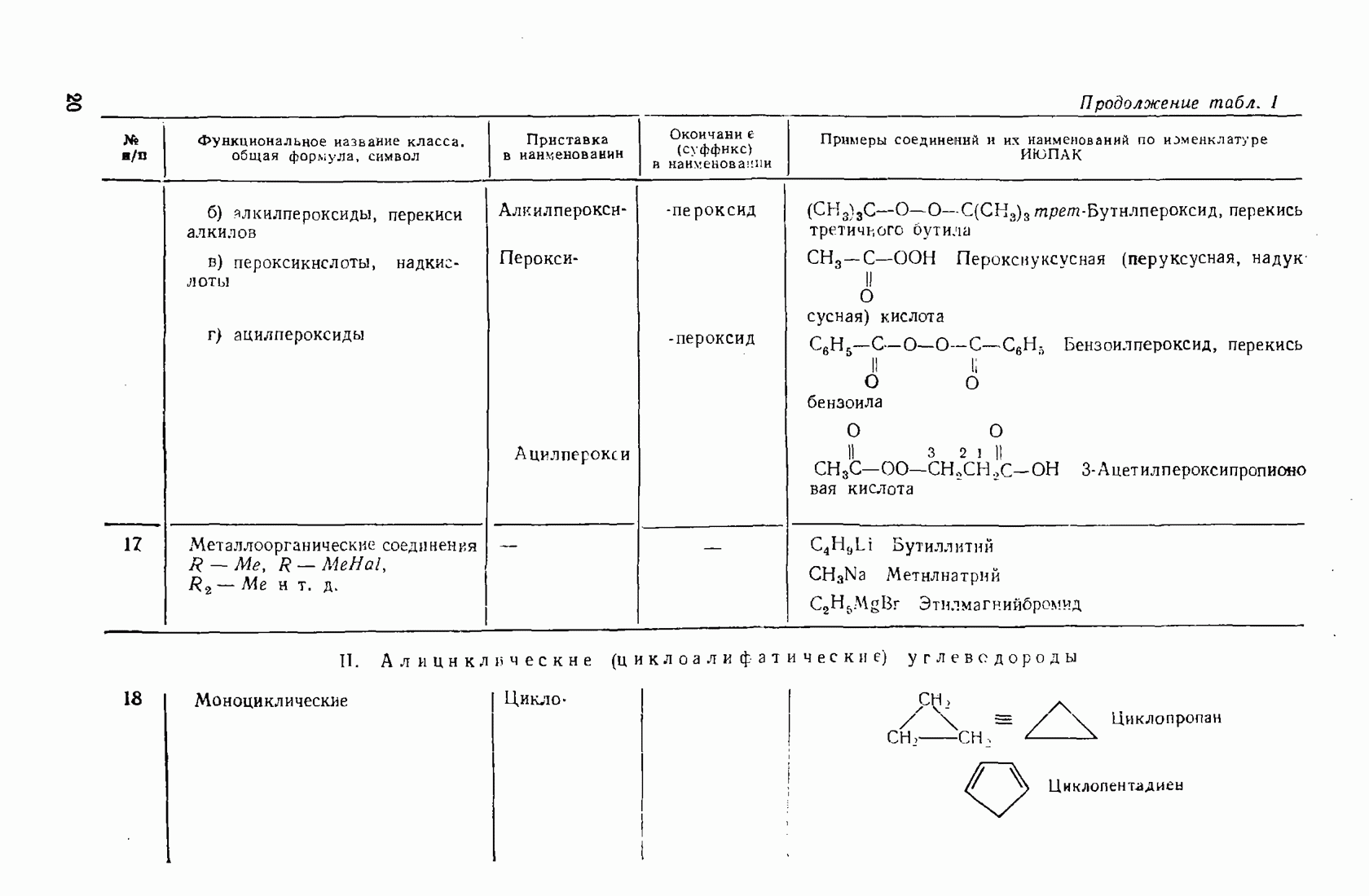
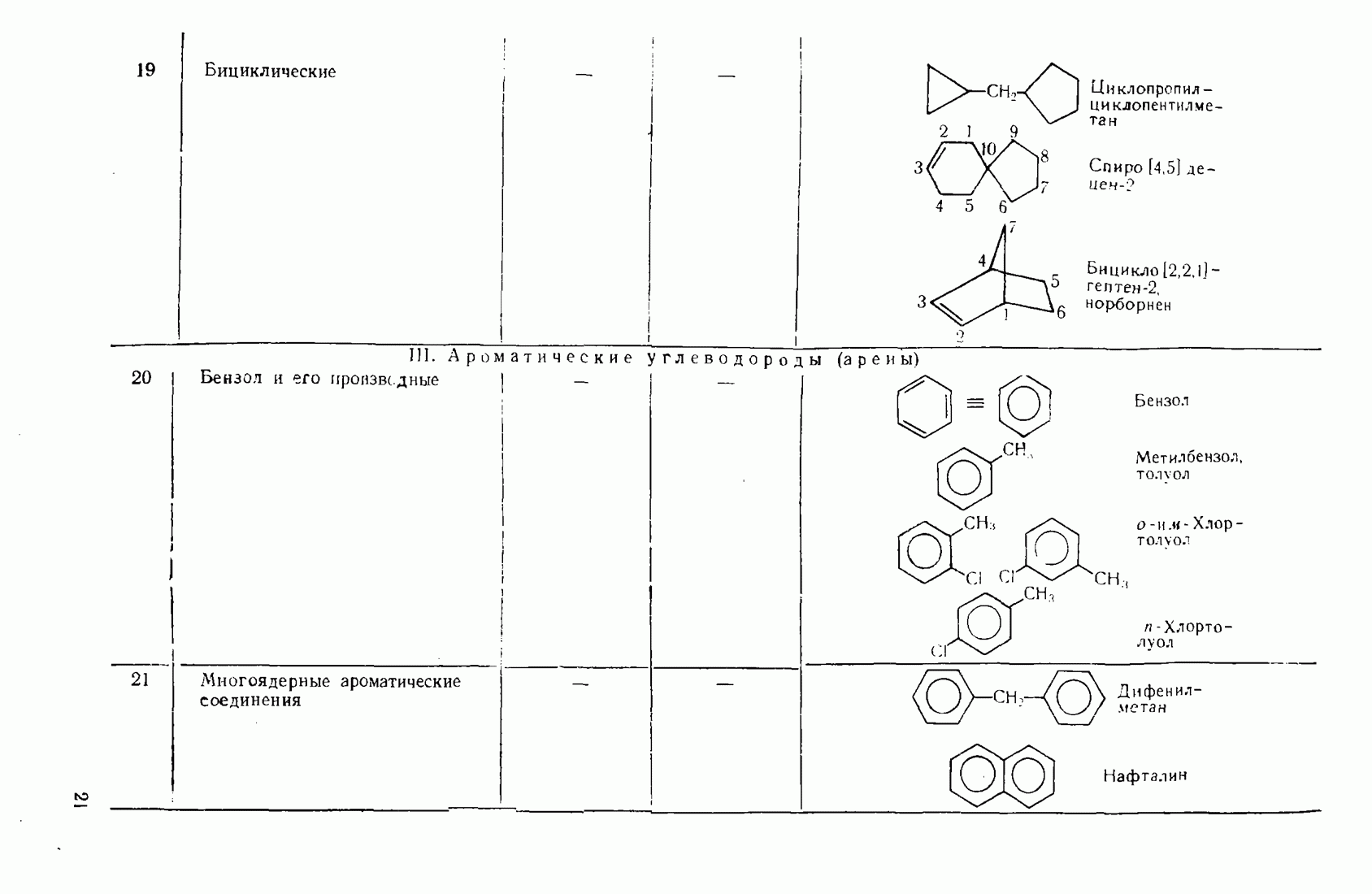
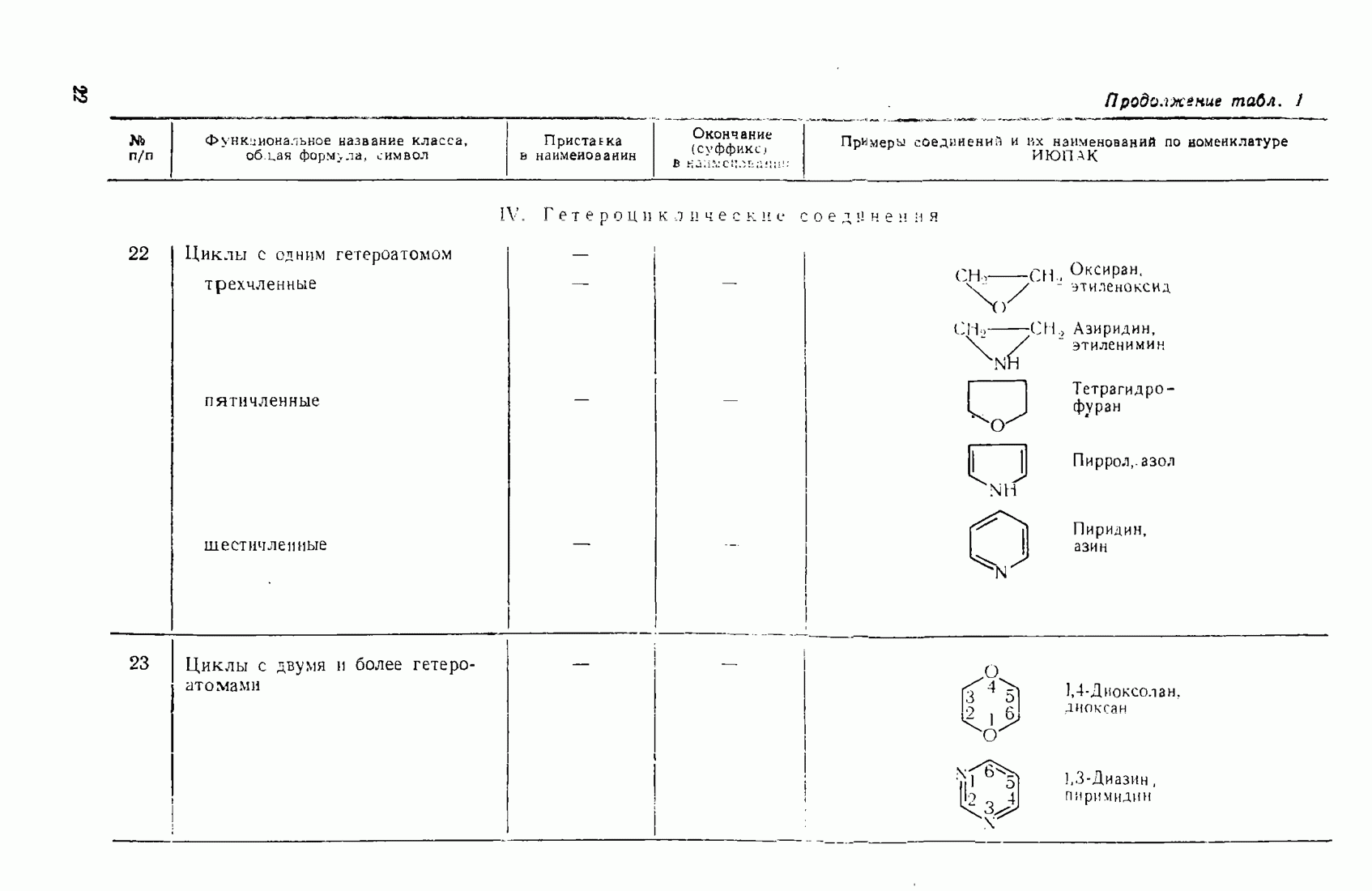
- 1.3. Классификация и номенклатура органических соединений
- 2 Общие теоретические положения органической химии
- 2.1. Природа химической связи
- 2.1.1. Типы химических связей
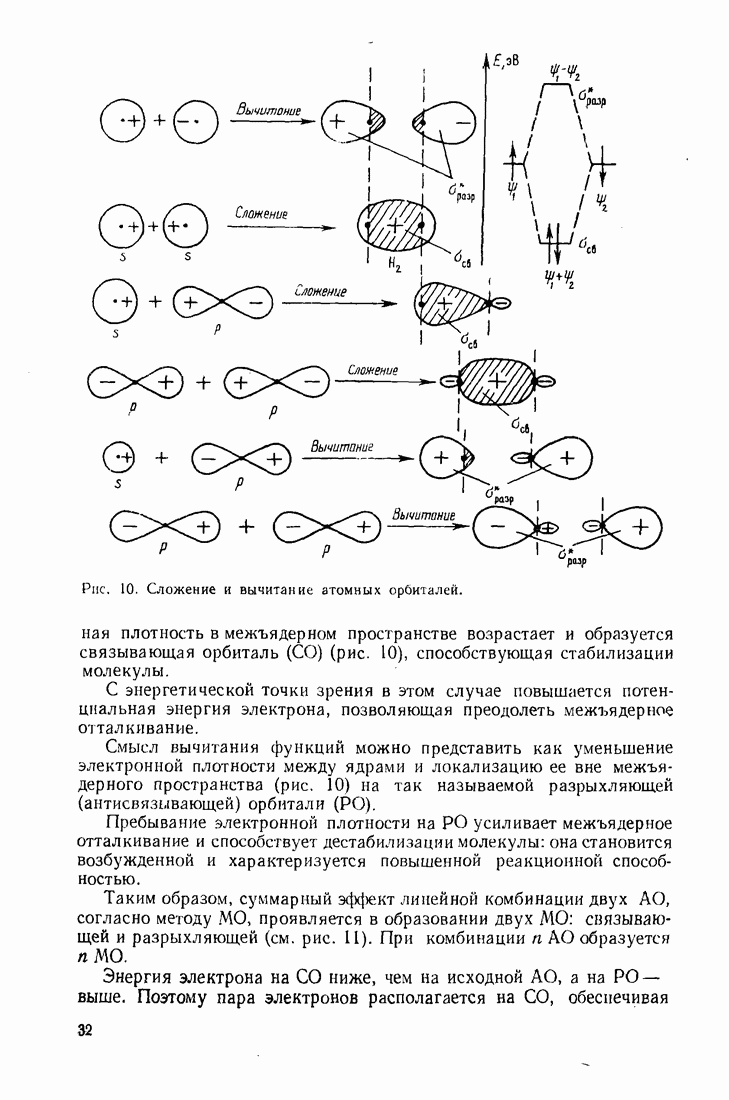
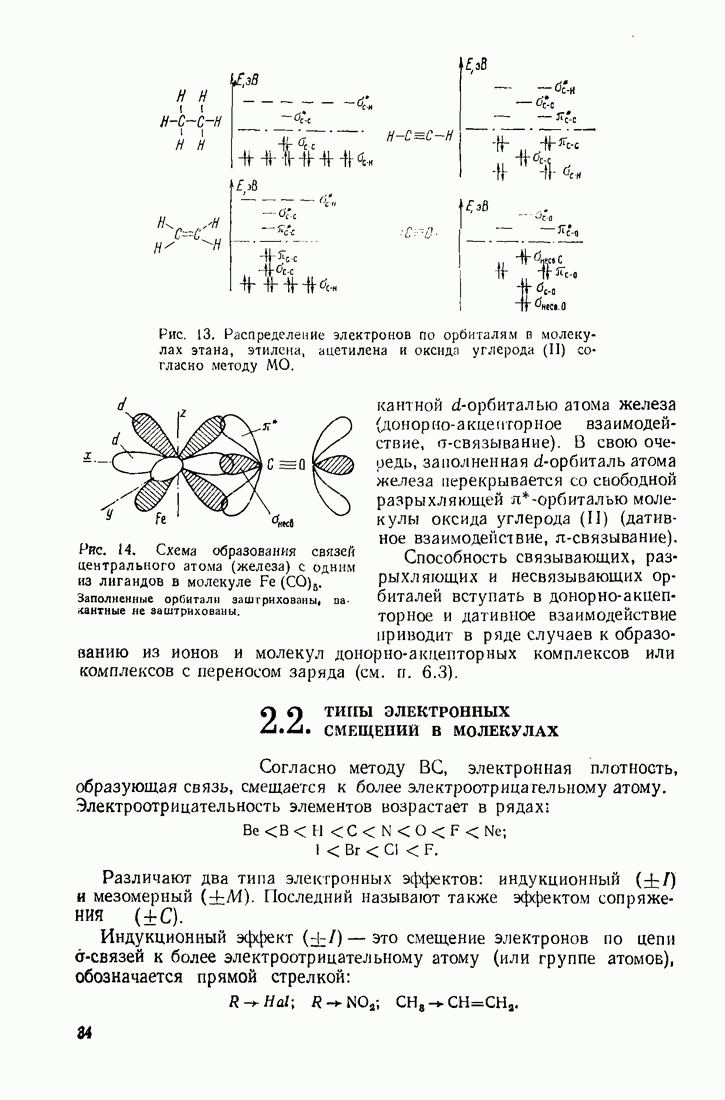
- 2.1.2. Молекулярные орбитали
- 2.2. ТИПЫ ЭЛЕКТРОННЫХ СМЕЩЕНИЙ В МОЛЕКУЛАХ
- 2.3. ОБЩИЕ ПРЕДСТАВЛЕНИЯ ОБ ОРГАНИЧЕСКОЙ РЕАКЦИИ
- 2.4. КЛАССИФИКАЦИЯ РЕАГЕНТОВ И РЕАКЦИЙ
- 2.5. КРАТКАЯ ХАРАКТЕРИСТИКА РЕАКЦИОННОЙ СПОСОБНОСТИ НЕКОТОРЫХ СОЕДИНЕНИЙ АЛИФАТИЧЕСКОГО РЯДА
- 2.5.1. Алканы (парафины)
- 2.5.2. Непредельные углеводороды
- 2.5.3. Галогеналканы (галоидные алкилы R-Hal)
- 2.5.4. Спирты (R0Н)
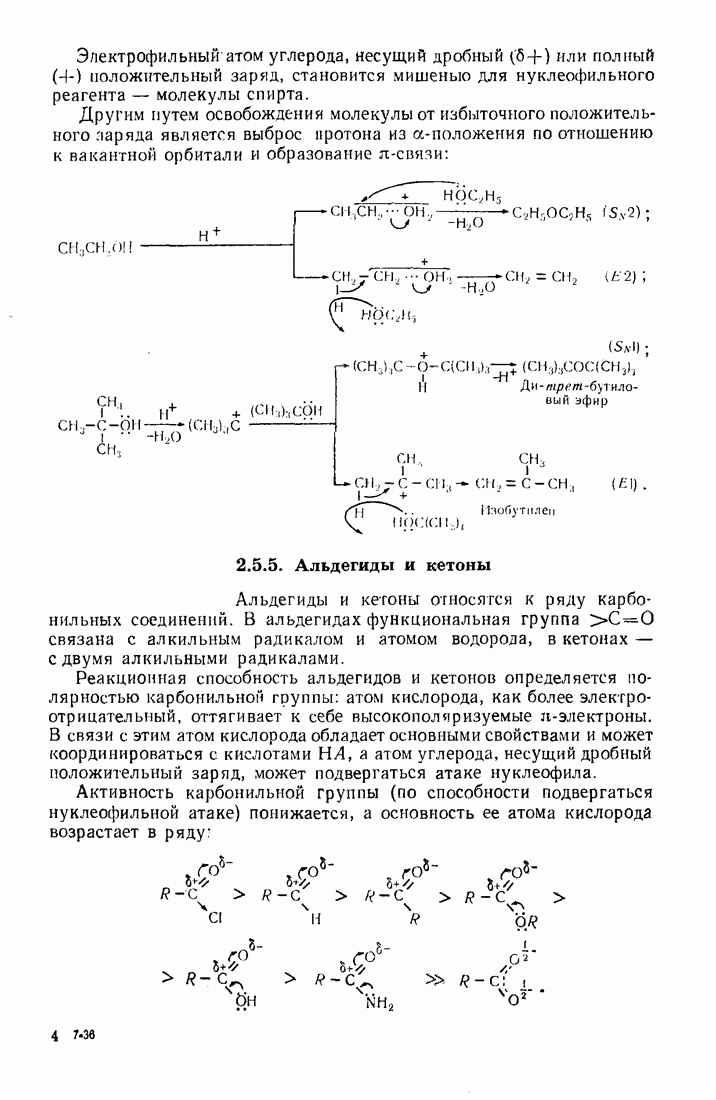
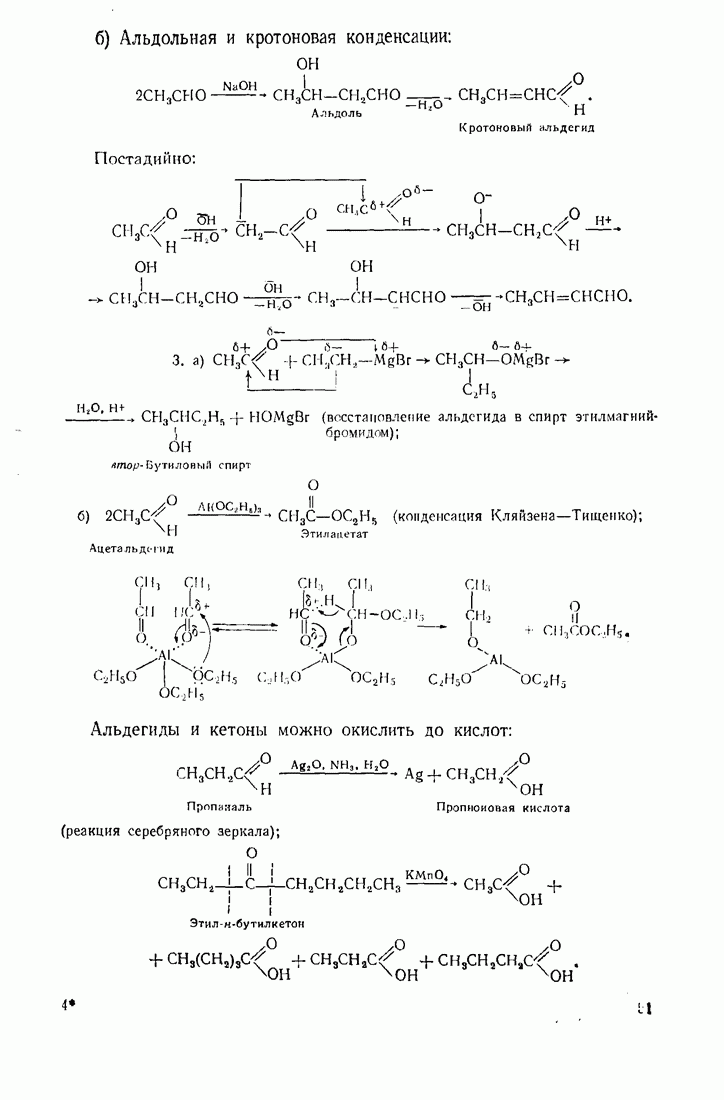
- 2.5.5. Альдегиды и кетоны
- 2.5.6. Карбоновые кислоты (R-СООН) и их производные (R-СО-X)
- 2.5.7. Амины (NH2R, NHR2, NR3)
- 3. Реакционная способность соединений алифатического ряда
- 3.1. Алканы (насыщенные углеводороды)
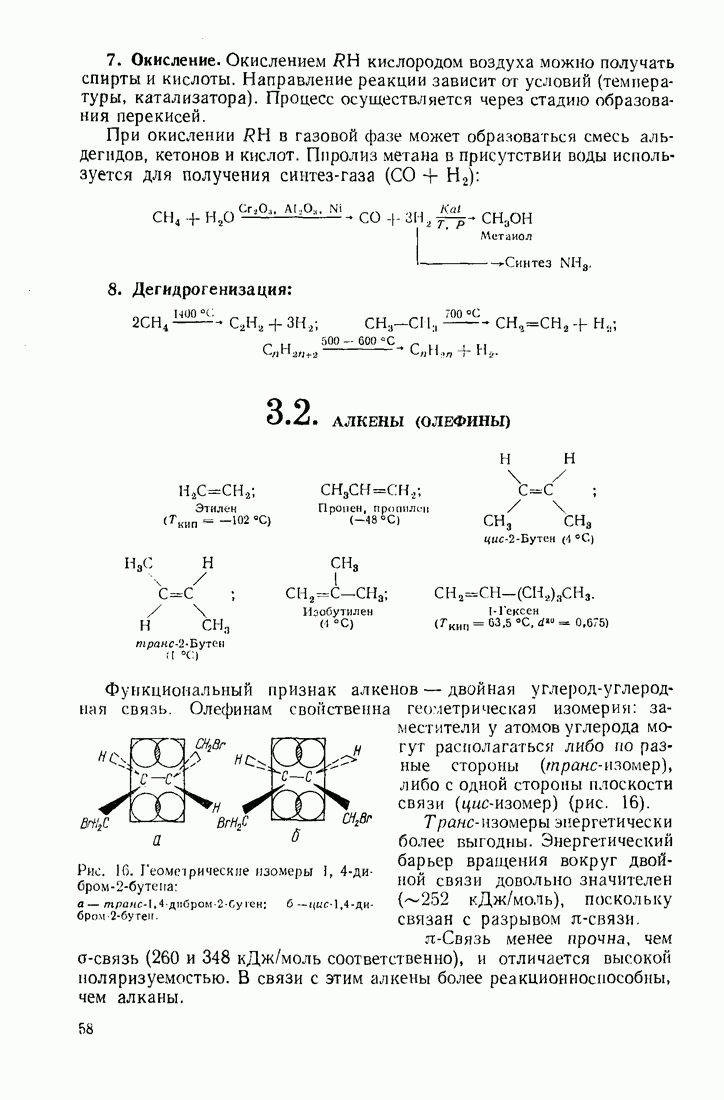
- 3.2. АЛКЕНЫ (ОЛЕФИНЫ)
- 3.3. ДИЕНОВЫЕ УГЛЕВОДОРОДЫ
- 3.4. АЦЕТИЛЕНЫ
- 3.5. ГАЛОГЕНАЛКАНЫ (ГАЛОИДНЫЕ АЛКИЛЫ)
- 3.6. СПИРТЫ
- 3.7. ПРОСТЫЕ ЭФИРЫ (R-O-R)
- 3.8. ОКСИРАНЫ (ЭПОКСИДНЫЕ СОЕДИНЕНИЯ, a-ОКИСИ)
- 3.9. АЛЬДЕГИДЫ И КЕТОНЫ
- 3.10. КАРБОНОВЫЕ КИСЛОТЫ
- 3.11. НЕКОТОРЫЕ ПРОИЗВОДНЫЕ КИСЛОТ
- 3.12. АМИНЫ
- 3.13. ФОСФОРОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- 3.14. СЕРООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- 3.15. ОРГАНИЧЕСКИЕ ПЕРЕКИСИ (ПЕРОКСИДНЫЕ СОЕДИНЕНИЯ)
- 3.16. ПРОИЗВОДНЫЕ УГОЛЬНОЙ КИСЛОТЫ
- 3.17. ГЕТЕРОАНАЛОГИ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ
- 3.18. АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
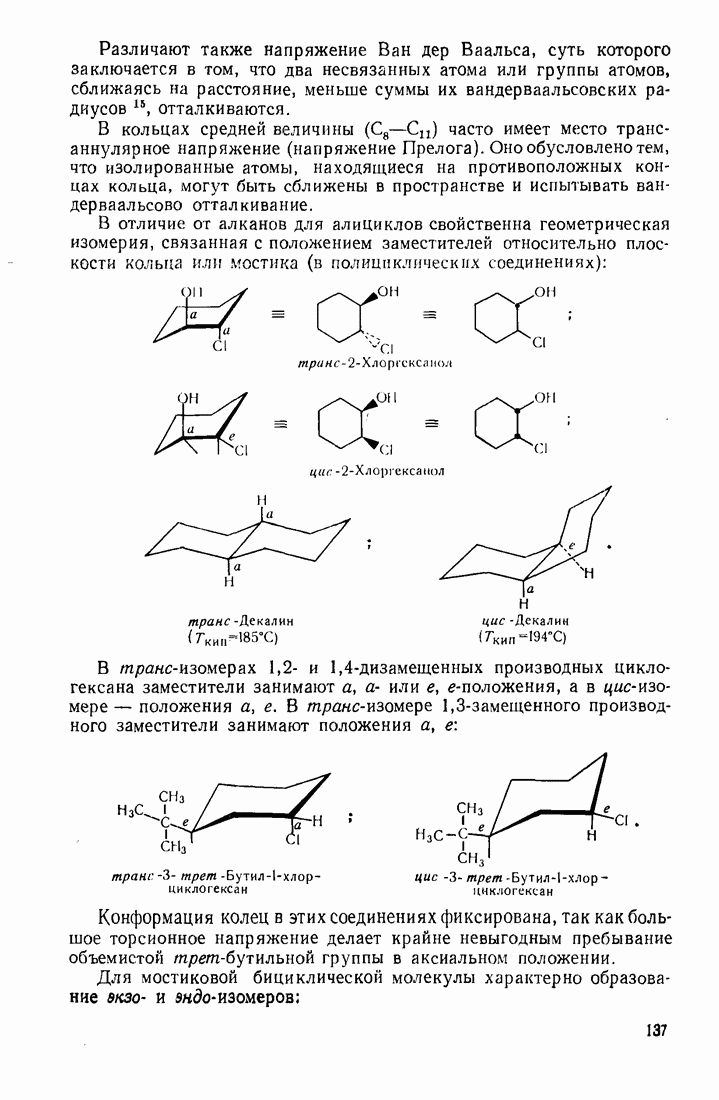
- 3.18.2. Пространственное расположение и напряженность циклов
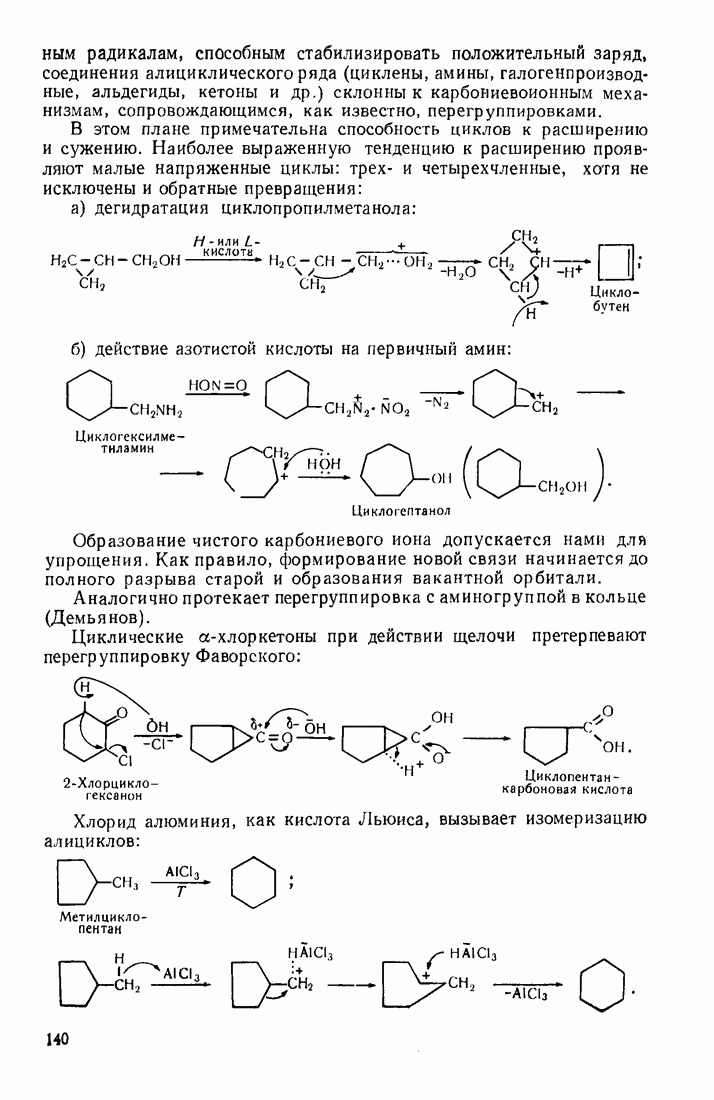
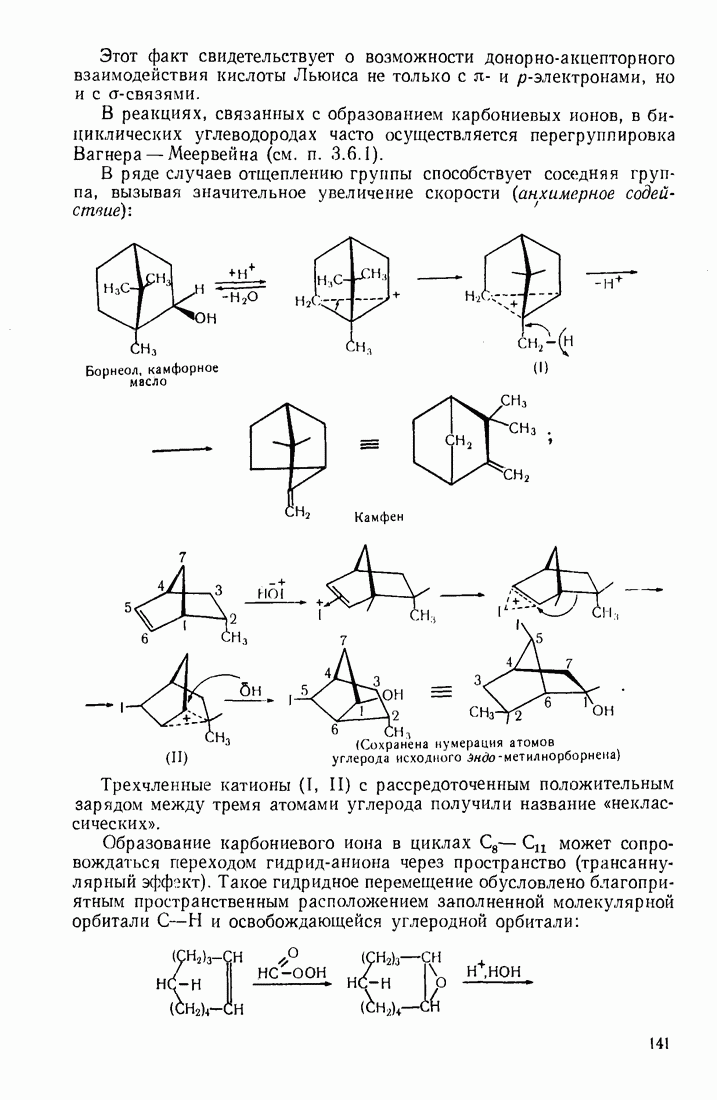
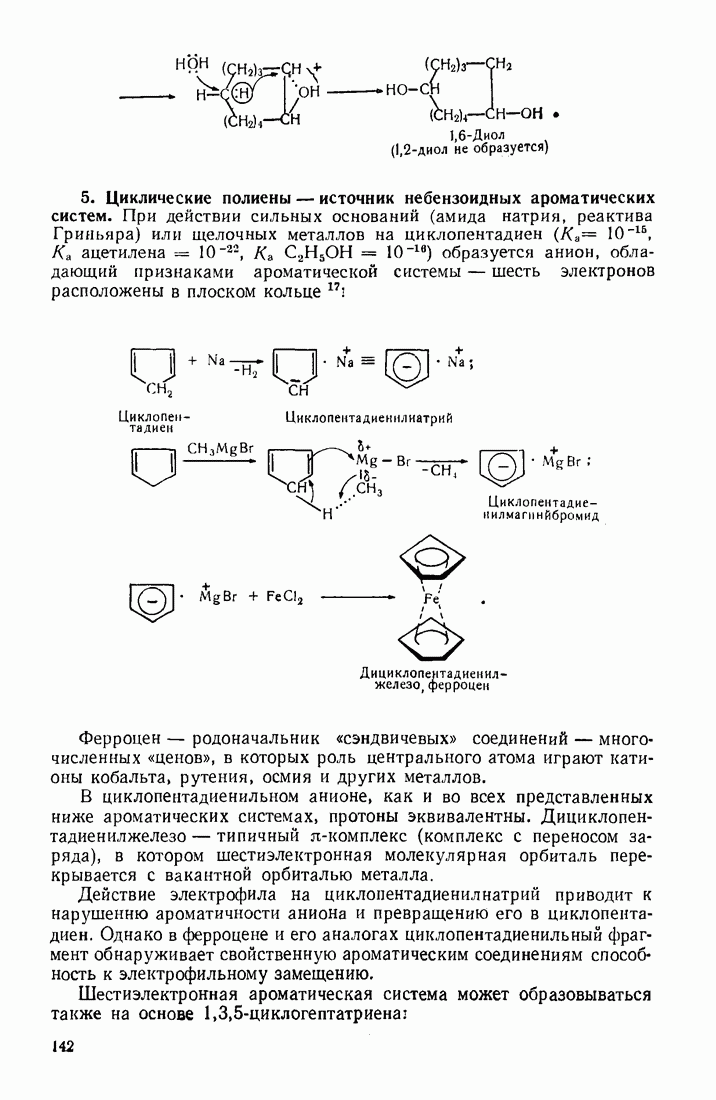
- 3.18.3. Особенности химических свойств алициклических соединений
- 4. Полифункциональные производные алифатического ряда
- 4.1. ДВУХОСНОВНЫЕ КАРБОНОВЫЕ КИСЛОТЫ
- 4.2. НЕПРЕДЕЛЬНЫЕ КИСЛОТЫ
- 4.3. ОКСОКИСЛОТЫ (АЛЬДЕГИДО- И КЕТОКИСЛОТЫ)
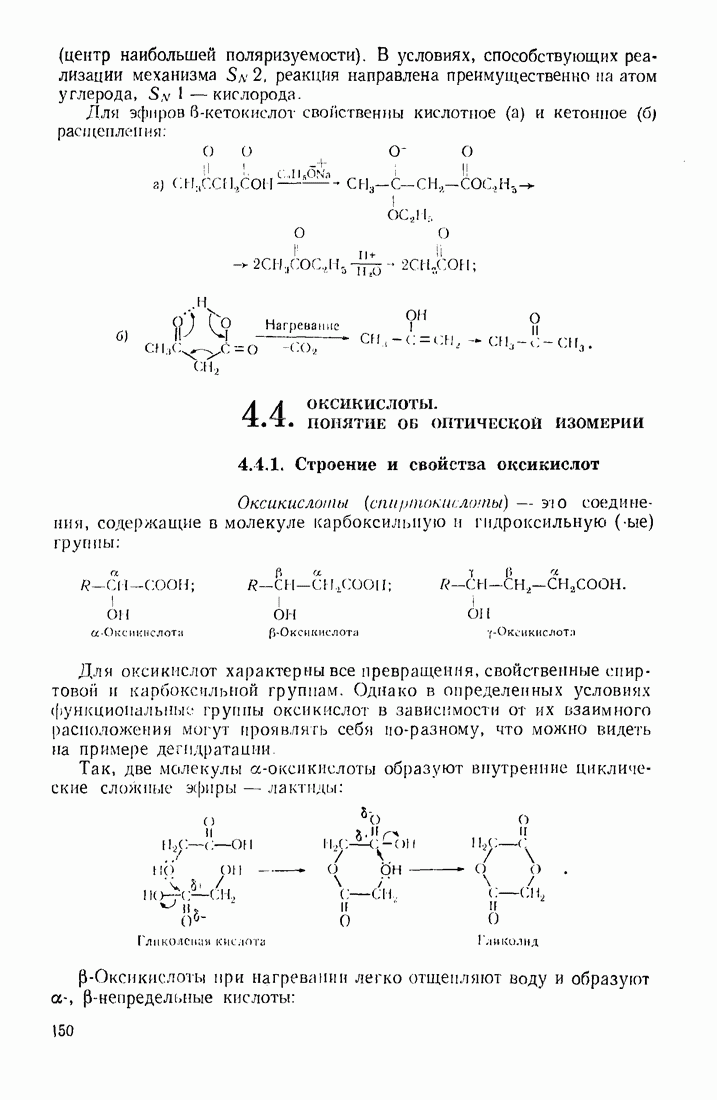
- 4.4. ОКСИКИСЛОТЫ. ПОНЯТИЕ ОБ ОПТИЧЕСКОЙ ИЗОМЕРИИ
- 4.5. УГЛЕВОДЫ
- 4.5.2. Стереохимия моносахаридов
- 4.5.3. Дисахариды
- 4.5.4. Полисахариды
- 4.5.5. Нахождение в природе и пути превращения углеводов
- 4.6. АМИНОКИСЛОТЫ
- 5. Методы синтеза органических юединений алифатическою рада
- 5.1. АЛКИЛИРОВАНИЕ
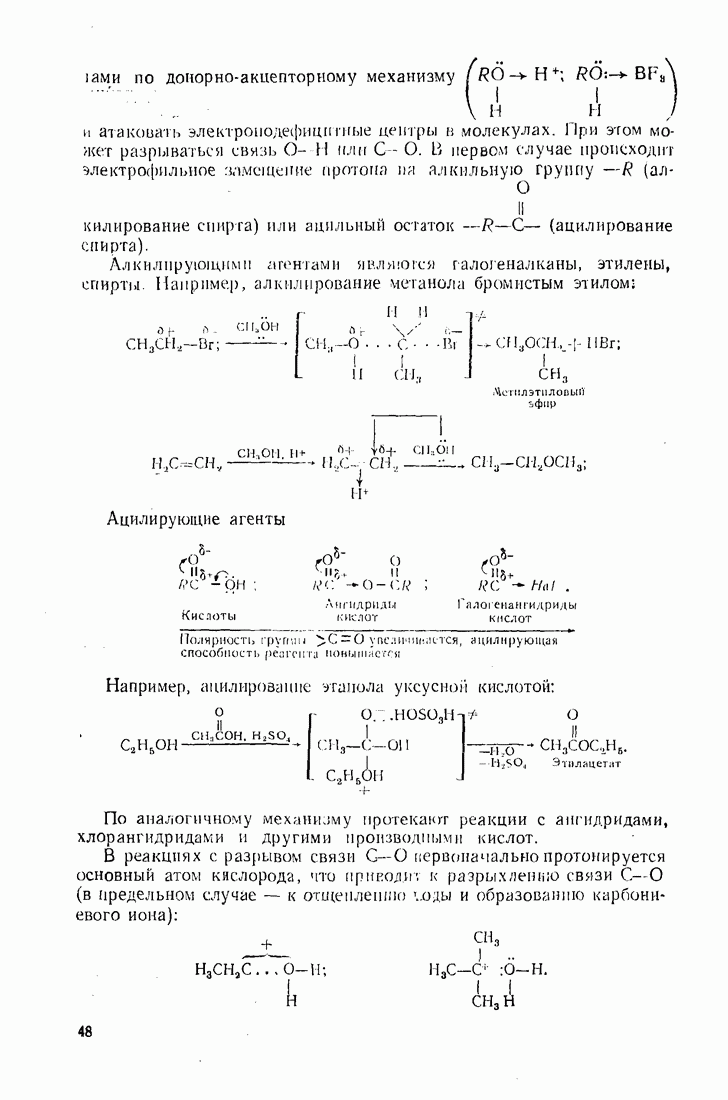
- 5.2. АЦИЛИРОВАНИЕ
- 5.3. ГАЛОГЕНИРОВАНИЕ
- 5.4. ГИДРОКСИЛИРОВАНИЕ
- 5.5. КАРБОНИЛИРОВАНИЕ (ВВЕДЕНИЕ КАРБОНИЛЬНОЙ ГРУППЫ)
- 5.6. КАРБОКСИЛИРОВАНИЕ
- 5.7. ЭПОКСИДИРОВАНИЕ (ОКСИРАНИРОВАИИЕ)
- 5.8. АМИНИРОВАНИЕ
- 5.9. ОКИСЛЕНИЕ
- 5.10. ВОССТАНОВЛЕНИЕ
- 5.11. АЛКАНЫ
- 5.12 АЛКЕНЫ
- 5.13. ДИЕНОВЫЕ УГЛЕВОДОРОДЫ (1,3-ДИЕНЫ)
- 5.14. АЦЕТИЛЕНЫ
- 5.15 АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- 5.16. ГАЛОГЕН АЛКАНЫ
- 5.17. СПИРТЫ
- 5.18. АЛЬДЕГИДЫ И КЕТОНЫ
- 5.19. КАРБОНОВЫЕ КИСЛОТЫ
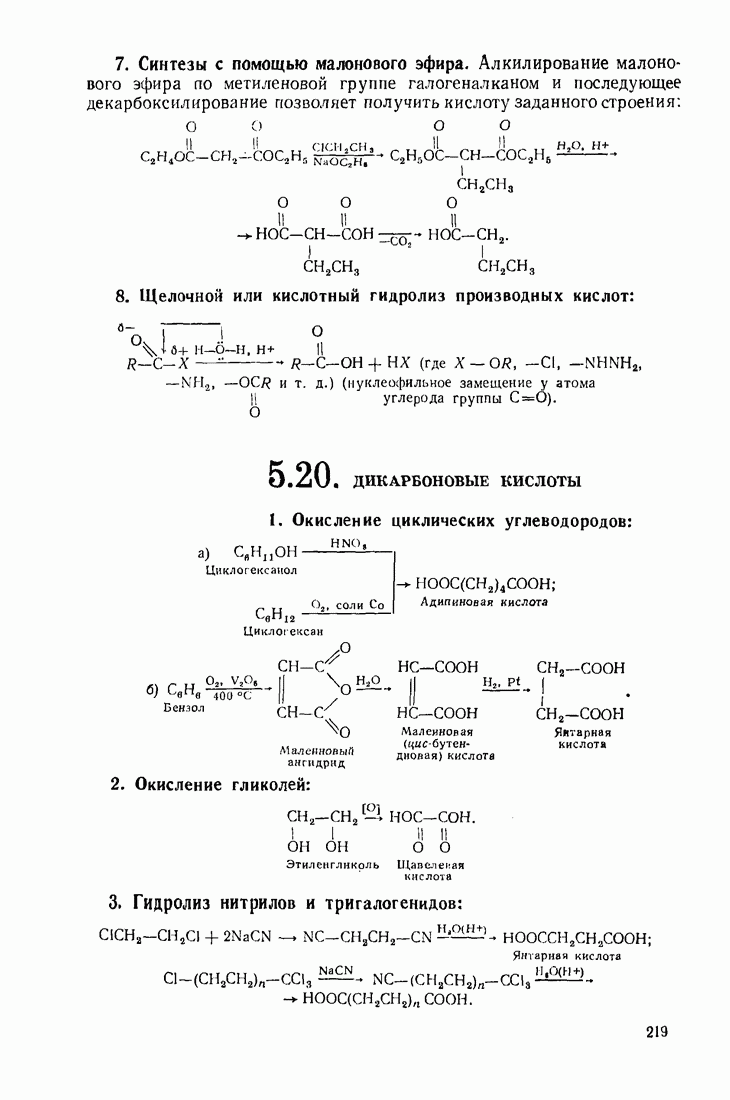
- 5.20. ДИКАРБОНОВЫЕ КИСЛОТЫ
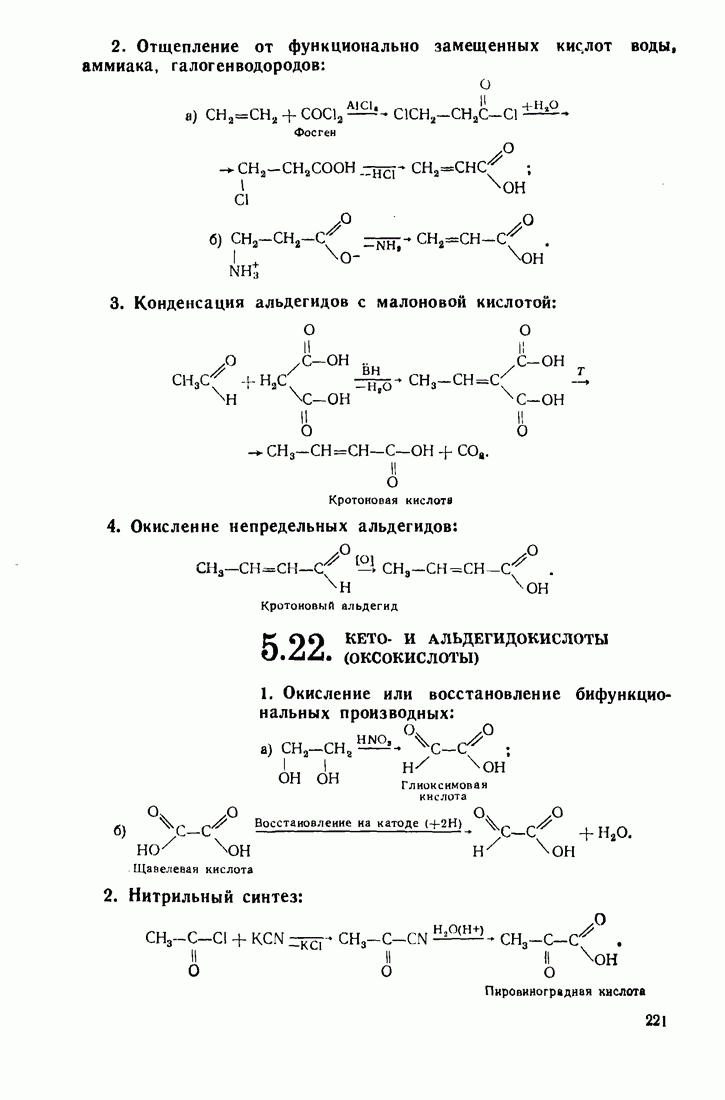
- 5.21. НЕПРЕДЕЛЬНЫЕ КИСЛОТЫ
- 5.22. КЕТО- И АЛЬДЕГИДОКИСЛОТЫ (ОКСОКИСЛОТЫ)
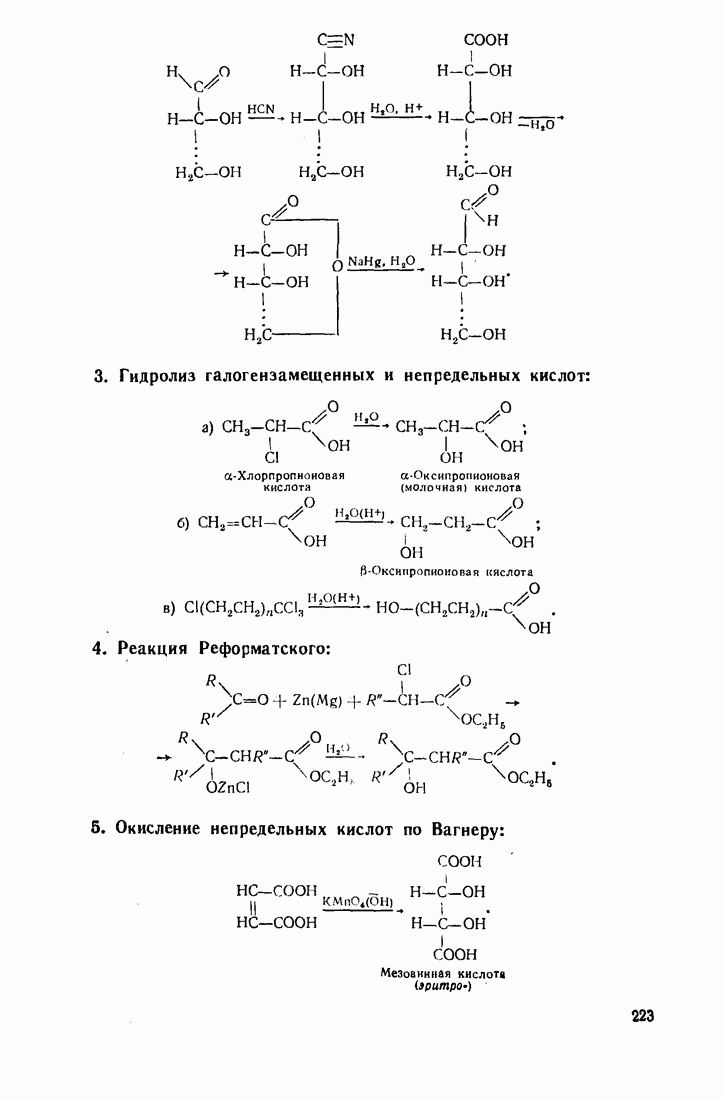
- 5.23. ОКСИКИСЛОТЫ
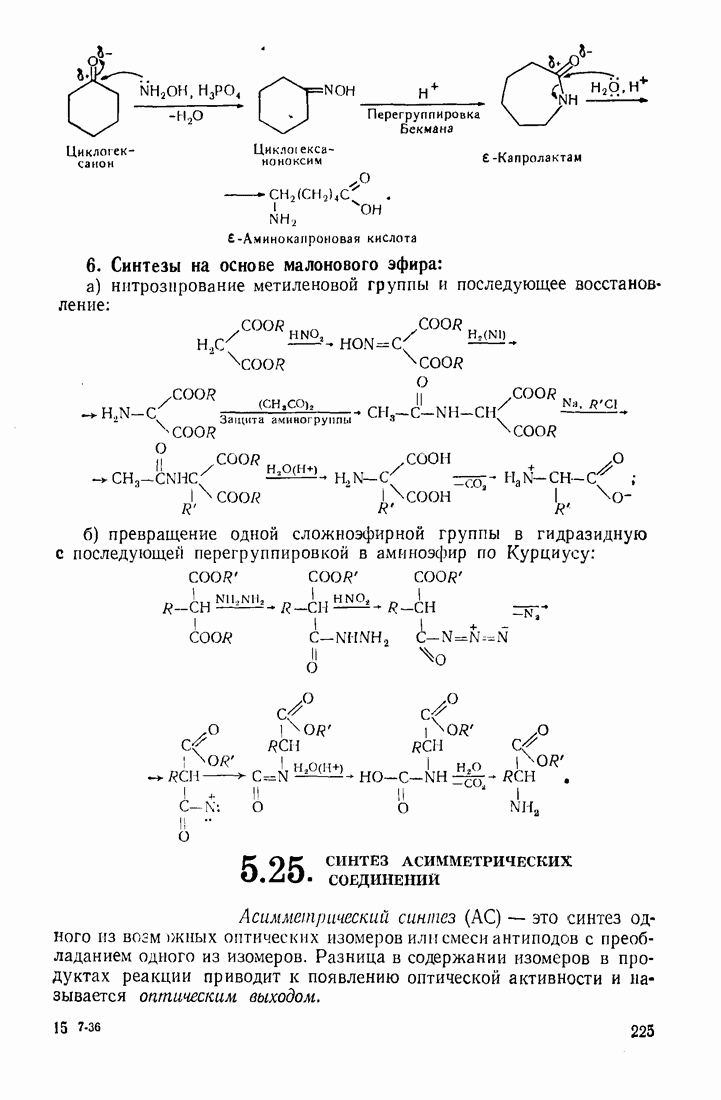
- 5.24. АМИНОКИСЛОТЫ
- 5.25 СИНТЕЗ АСИММЕТРИЧЕСКИХ СОЕДИНЕНИЙ
- 6. Некоторые понятия физической органической химии
- 6.1. СВЯЗЬ СОСТАВА И СТРОЕНИЯ СОЕДИНЕНИЙ С ФИЗИЧЕСКИМИ СВОЙСТВАМИ
- 6.2. ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 6.3. КИСЛОТЫ И ОСНОВАНИЯ В ОРГАНИЧЕСКОЙ ХИМИИ
- 6.4. ОРГАНИЧЕСКИЕ РАСТВОРИТЕЛИ И ИХ ВЛИЯНИЕ НА СКОРОСТЬ И МЕХАНИЗМ РЕАКЦИЙ
- 6.5. КАТАЛИЗ ОРГАНИЧЕСКИХ РЕАКЦИЙ
- 7. Бензол и его производные
- 7.1. СТРОЕНИЕ БЕНЗОЛА. РАСПРЕДЕЛЕНИЕ ЭЛЕКТРОННОЙ ПЛОТНОСТИ
- 7.2. ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ В БЕНЗОЛЬНОМ ЯДРЕ
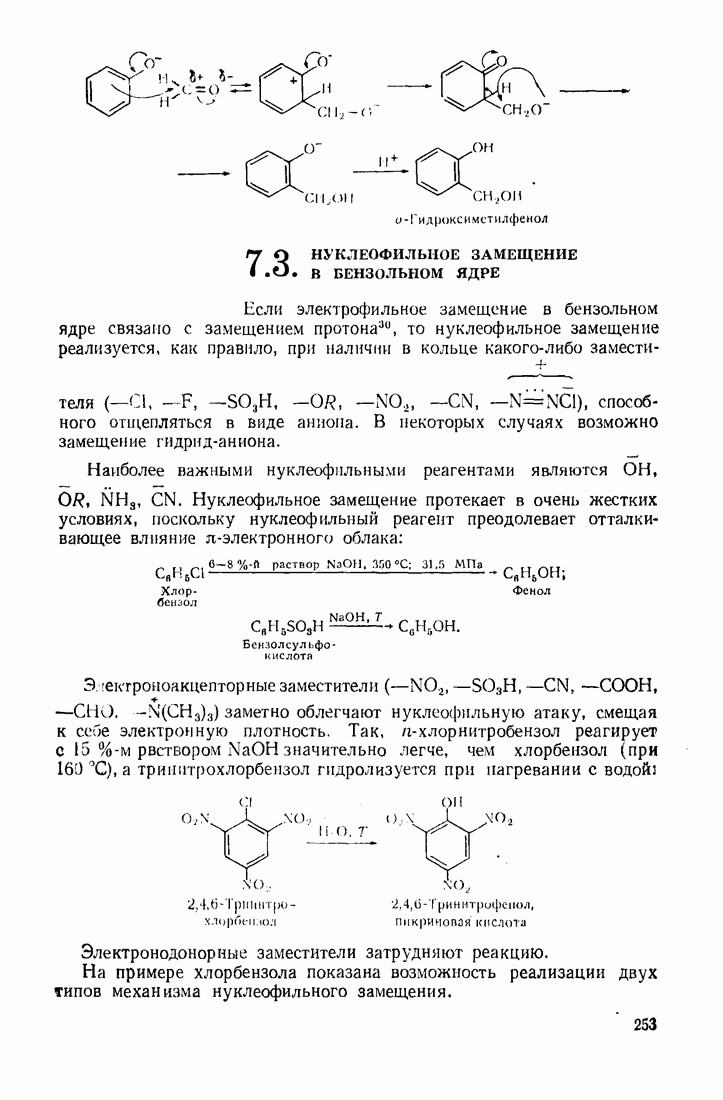
- 7.3. НУКЛЕОФИЛЬНОЕ ЗАМЕЩЕНИЕ В БЕНЗОЛЬНОМ ЯДРЕ
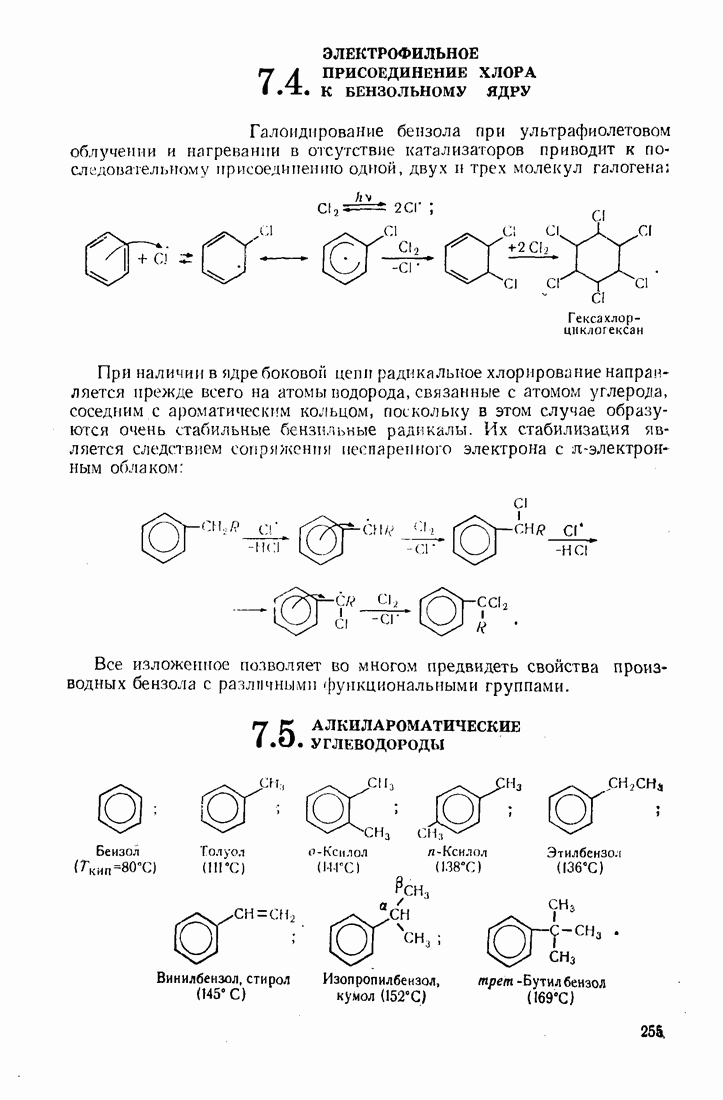
- 7.4. ЭЛЕКТРОФИЛЬНОЕ ПРИСОЕДИНЕНИЕ ХЛОРА К БЕНЗОЛЬНОМУ ЯДРУ
- 7.5. АЛКИЛАРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ
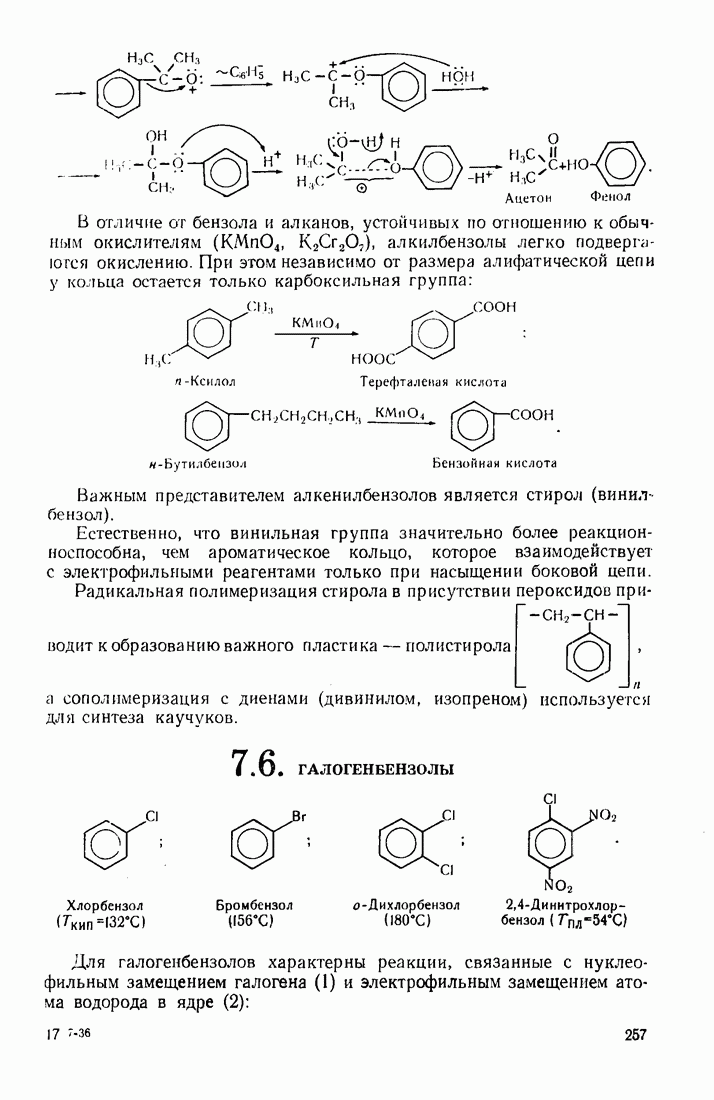
- 7.6. ГАЛОГЕНБЕНЗОЛЫ
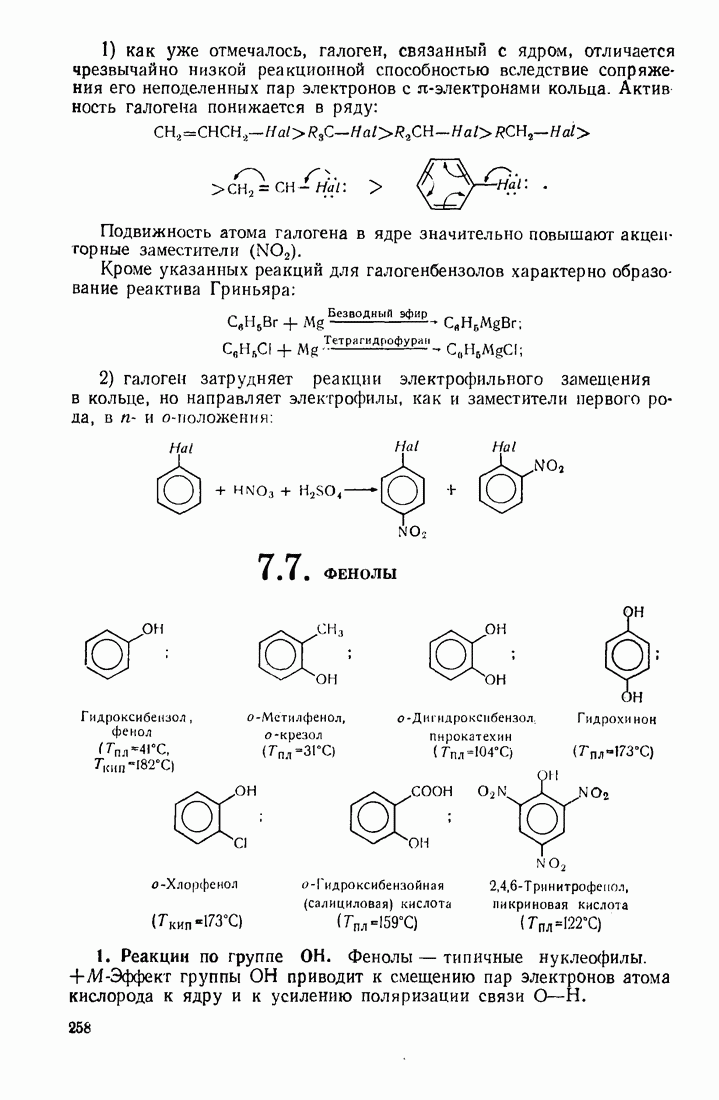
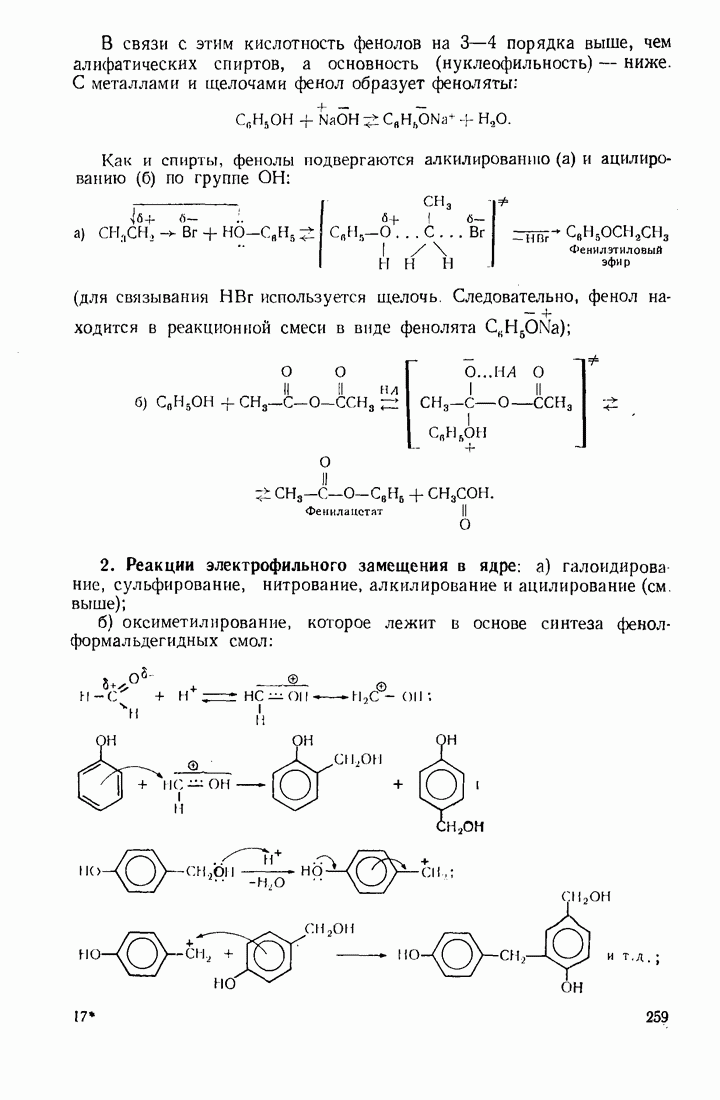
- 7.7. ФЕНОЛЫ
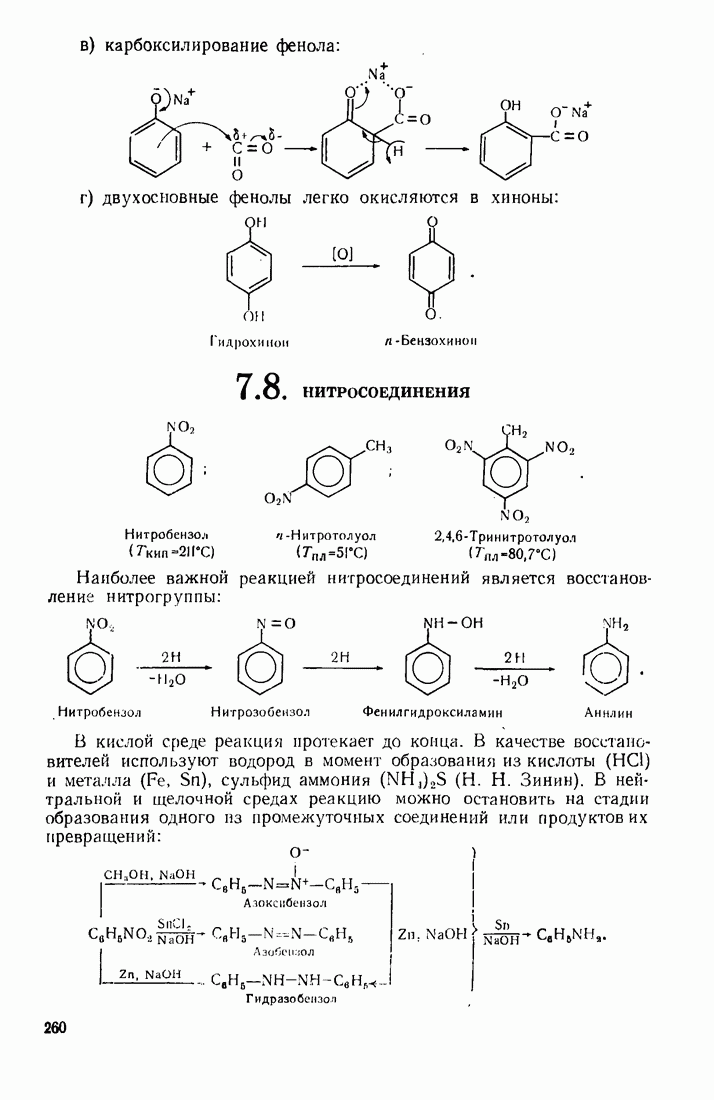
- 7.8. НИТРОСОЕД ИНЕНИЯ
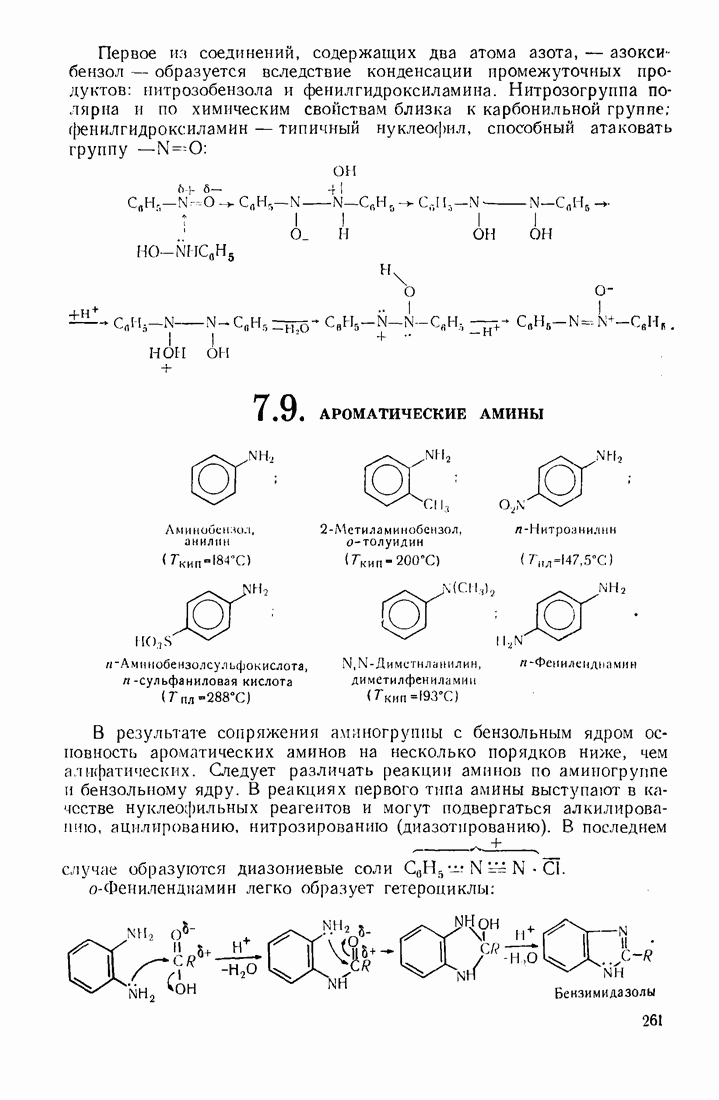
- 7.9. АРОМАТИЧЕСКИЕ АМИНЫ
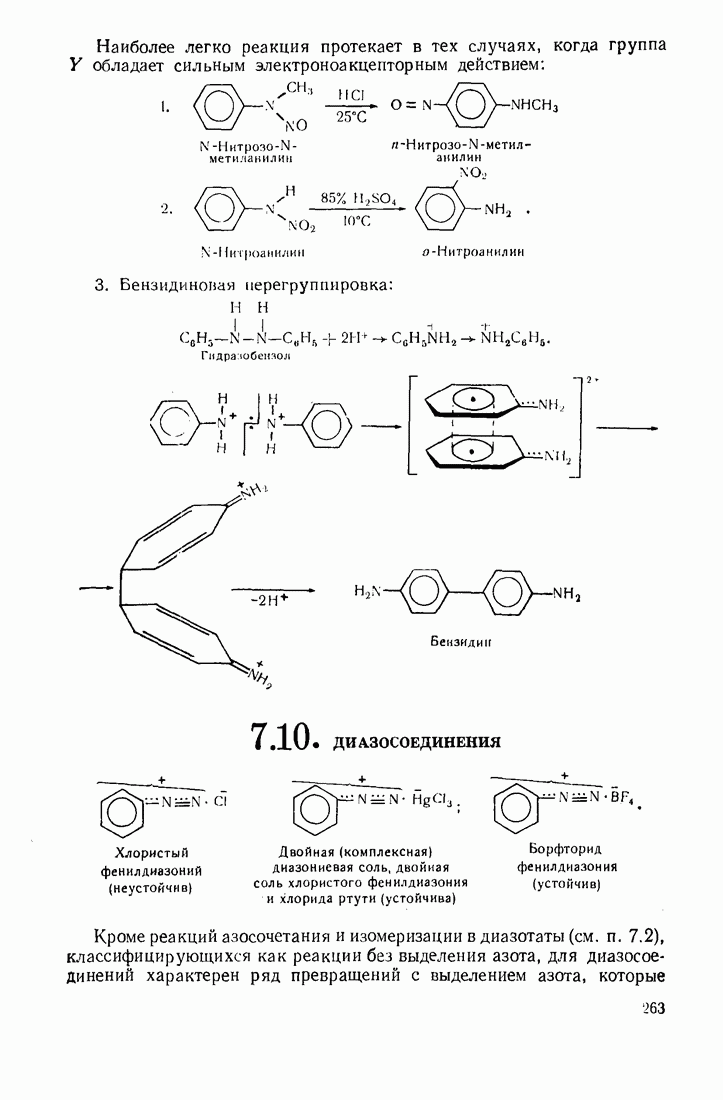
- 7.10. ДИАЗОСОЕДИНЕНИЯ
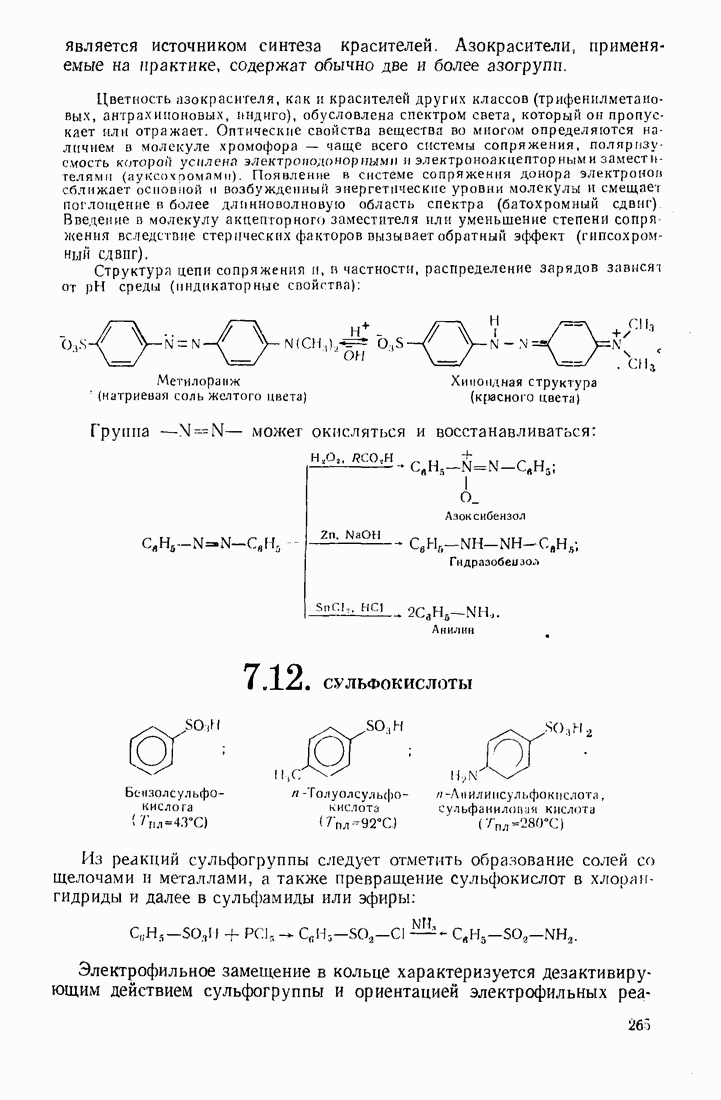
- 7.11. АЗОСОЕДИНЕНИЯ
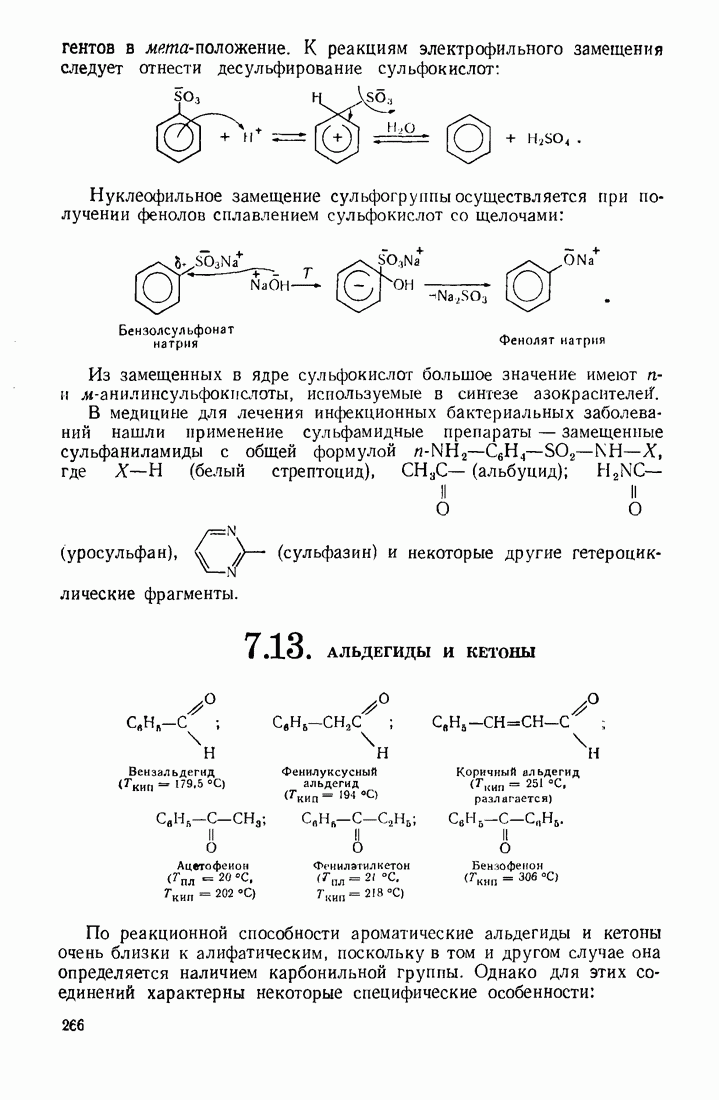
- 7.12. СУЛЬФОКИСЛОТЫ
- 7.13. АЛЬДЕГИДЫ И КЕТОНЫ
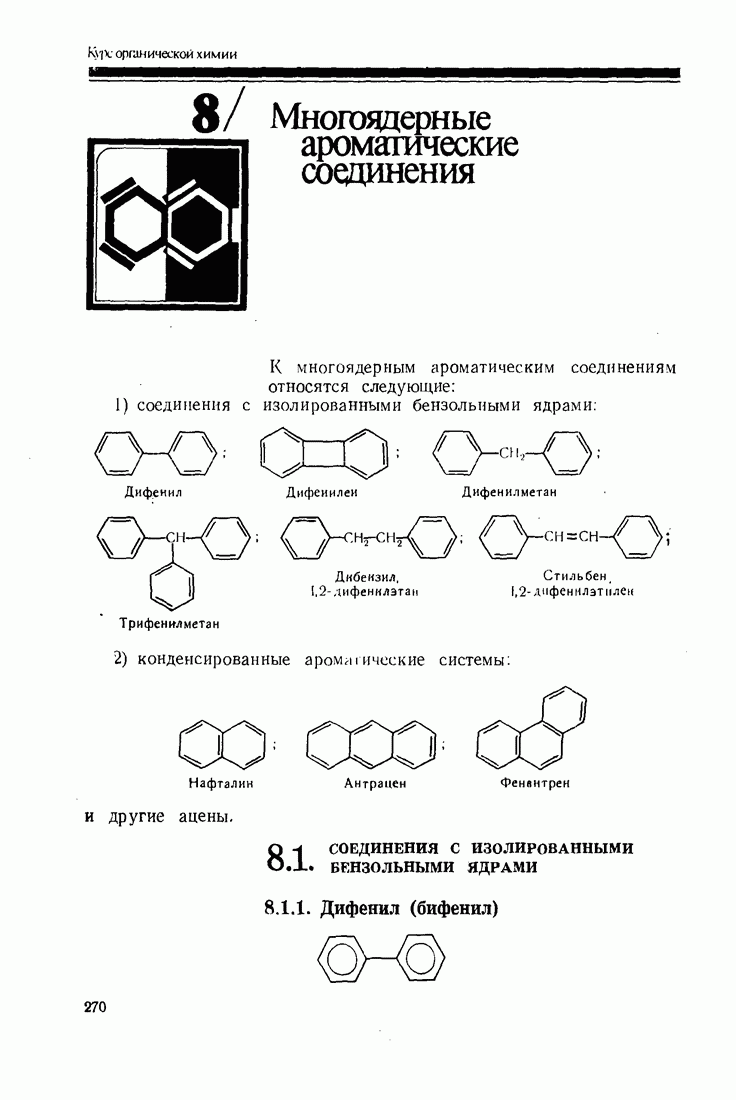
- 8. Многоядерные ароматические соединения
- 8.1. СОЕДИНЕНИЯ С ИЗОЛИРОВАННЫМИ БЕНЗОЛЬНЫМИ ЯДРАМИ
- 8.1.2. Полифенилметаны
- 8.2. АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ С КОНДЕНСИРОВАННЫМИ ЯДРАМИ
- 8.2.2. Антрацен
- 8.2.3. Фенантрен
- 9. Методы синтеза в ряду ароматических соединений
- 9.1. ГАЛОГЕНИРОВАНИЕ
- 9.2. НИТРОВАНИЕ
- 9.3. СУЛЬФИРОВАНИЕ
- 9.4. АЛКИЛИРОВАНИЕ
- 9.5. АЦИЛИРОВАНИЕ
- 9.6. ГИДРОКСИЛИРОВАНИЕ
- 9.7. АМИНИРОВАНИЕ
- 9.8. НИТРОЗИРОВАНИЕ
- 9.9. КАРБОНИЛИРОВАНИЕ
- 9.10. КАРБОКСИЛИРОВАНИЕ
- 9.11. ОКИСЛЕНИЕ
- 9.12. ВОССТАНОВЛЕНИЕ
- 10. Гетероциклические соединения
- 10.2. ОБЩАЯ ХАРАКТЕРИСТИКА СТРОЕНИЯ И РЕАКЦИОННОЙ СПОСОБНОСТИ
- 10.3. ПЯТИ- И ШЕСТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С ОДНИМ ГЕТЕРОАТОМОМ
- 10.4. ГЕТЕРОЦИКЛЫ С НЕСКОЛЬКИМИ ГЕТЕРОАТОМАМИ
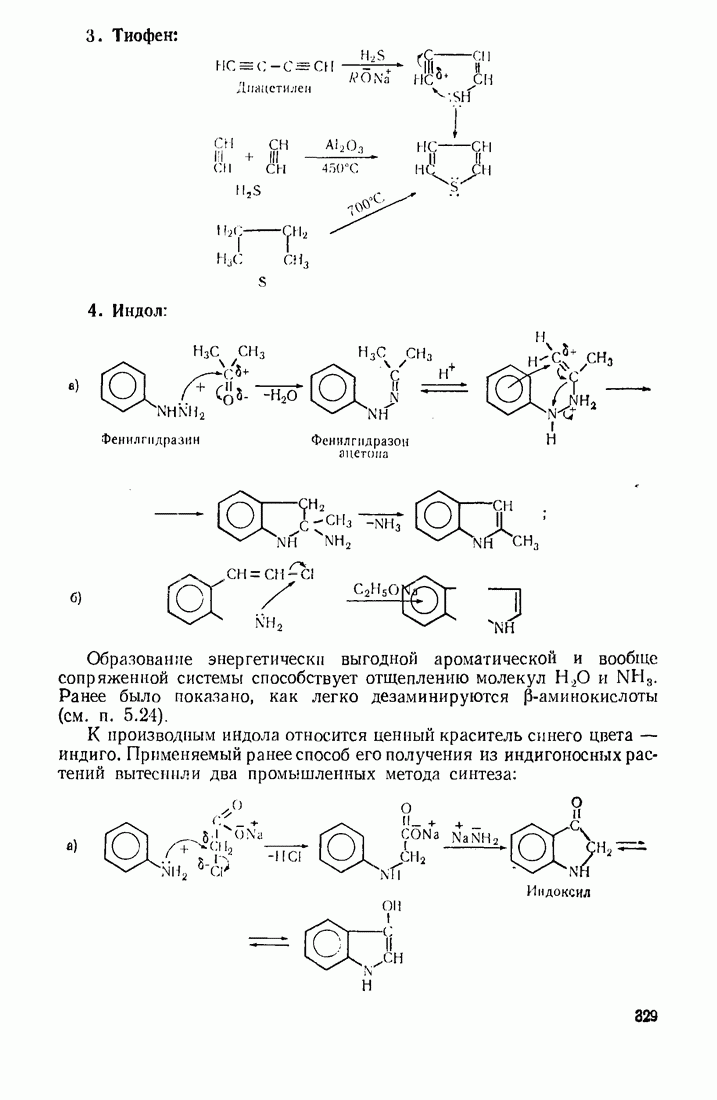
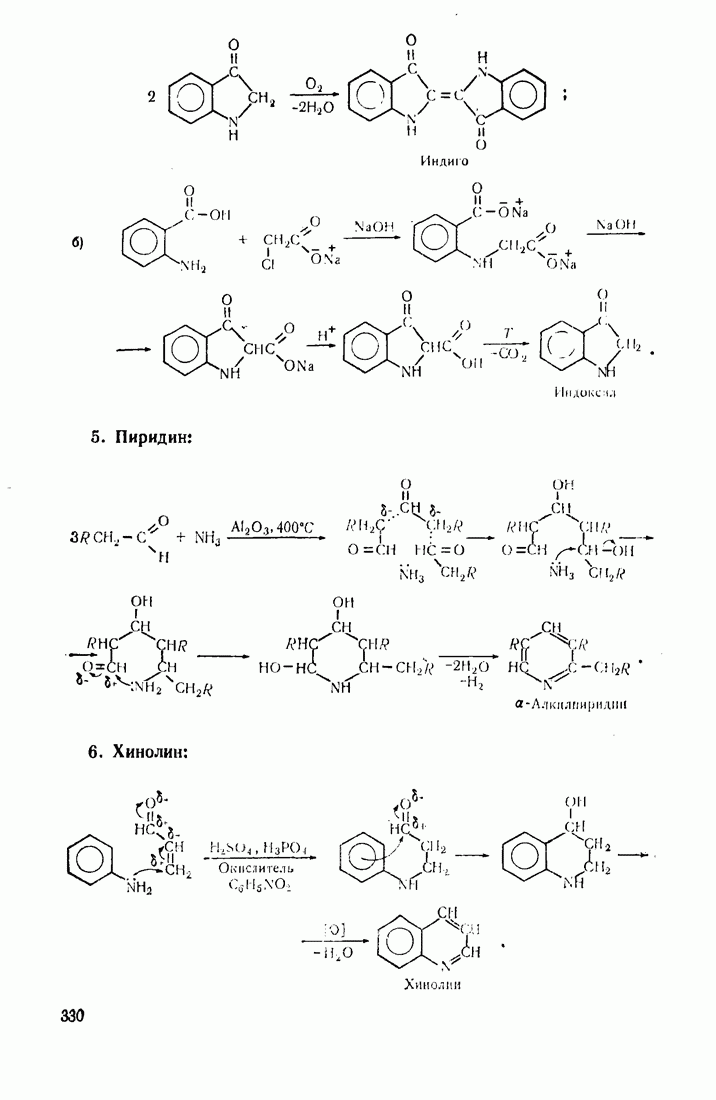
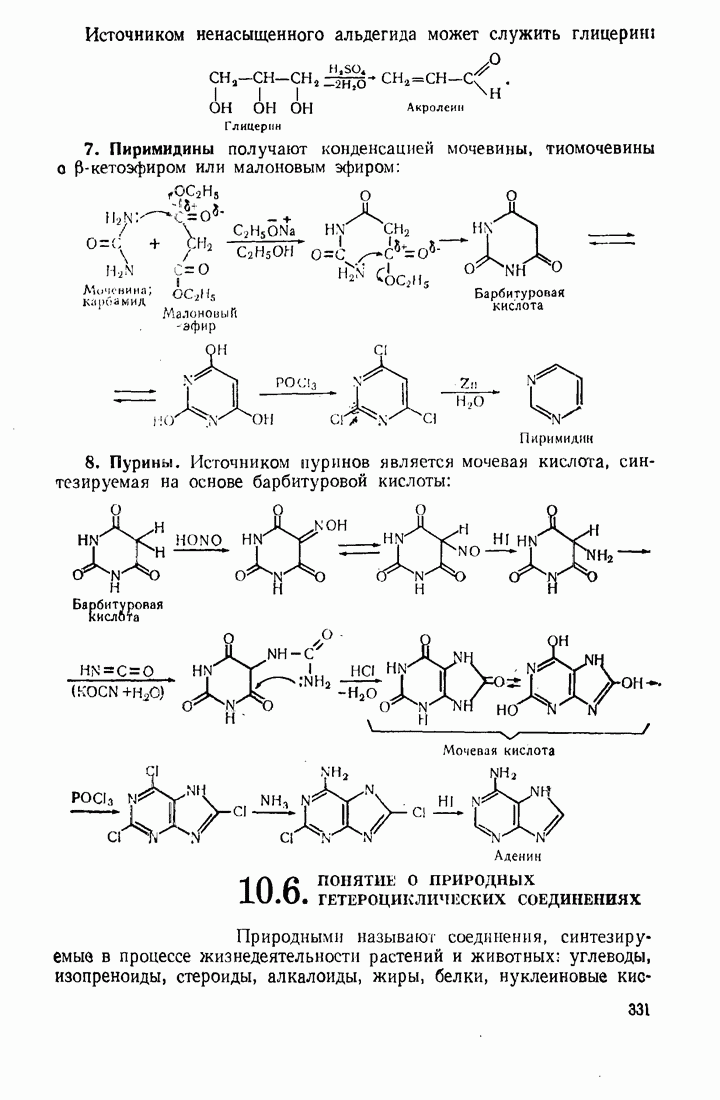
- 10.5. МЕТОДЫ СИНТЕЗА ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ
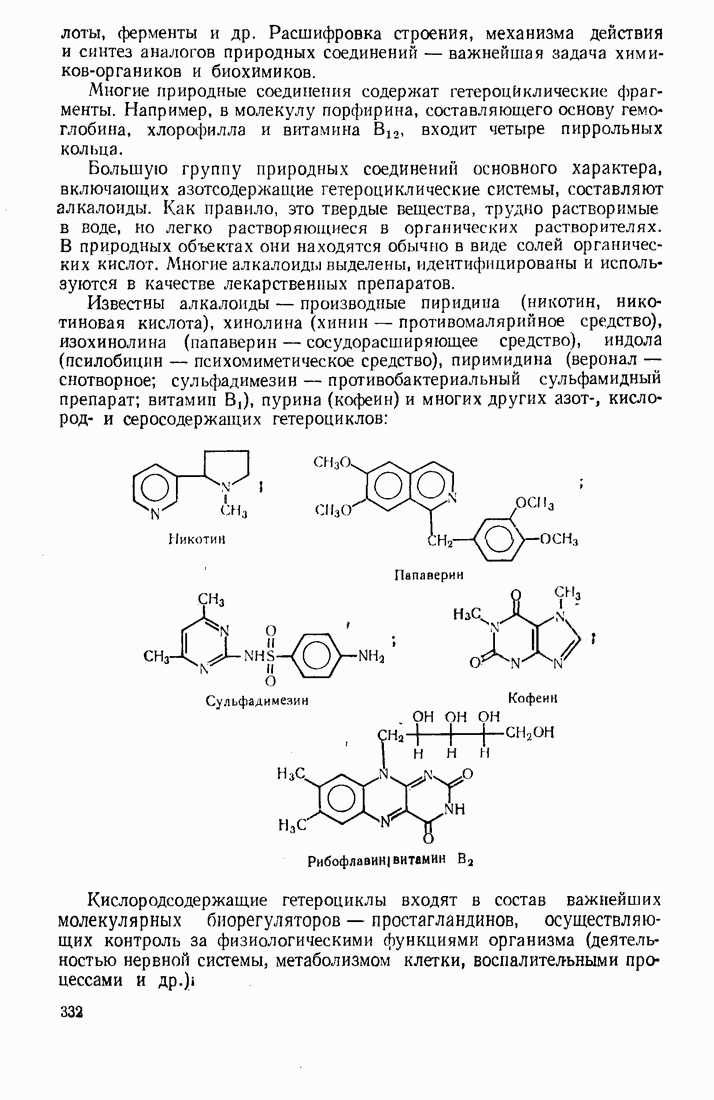
- 10.6. П0НЯТИЕ О ПРИРОДНЫХ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЯХ
- 11. Зпементоорганические соединения
- 11.2. ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ НЕКОТОРЫХ НЕМЕТАЛЛОВ
- 11.3. МЕГАЛЛООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- 11.4. ОРГАНИЧЕСКИЕ ПРОИЗВОДНЫЕ ПЕРЕХОДНЫХ МЕТАЛЛОВ
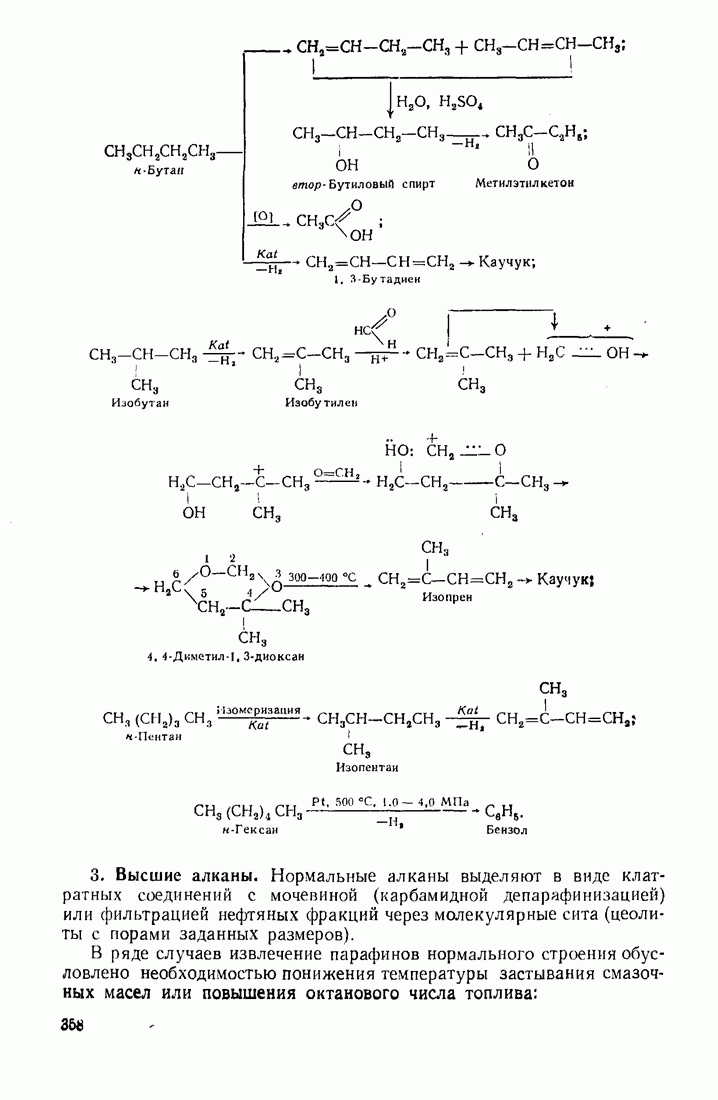
- 12. Сырье и основные направления развития промышленности органического синтеза
- 12.1.1. Нефть и сопутствующий природный газ
- 12.1.2. Углехимическое сырье
- 12.1.3. Лесохимическое и сельскохозяйственное сырье
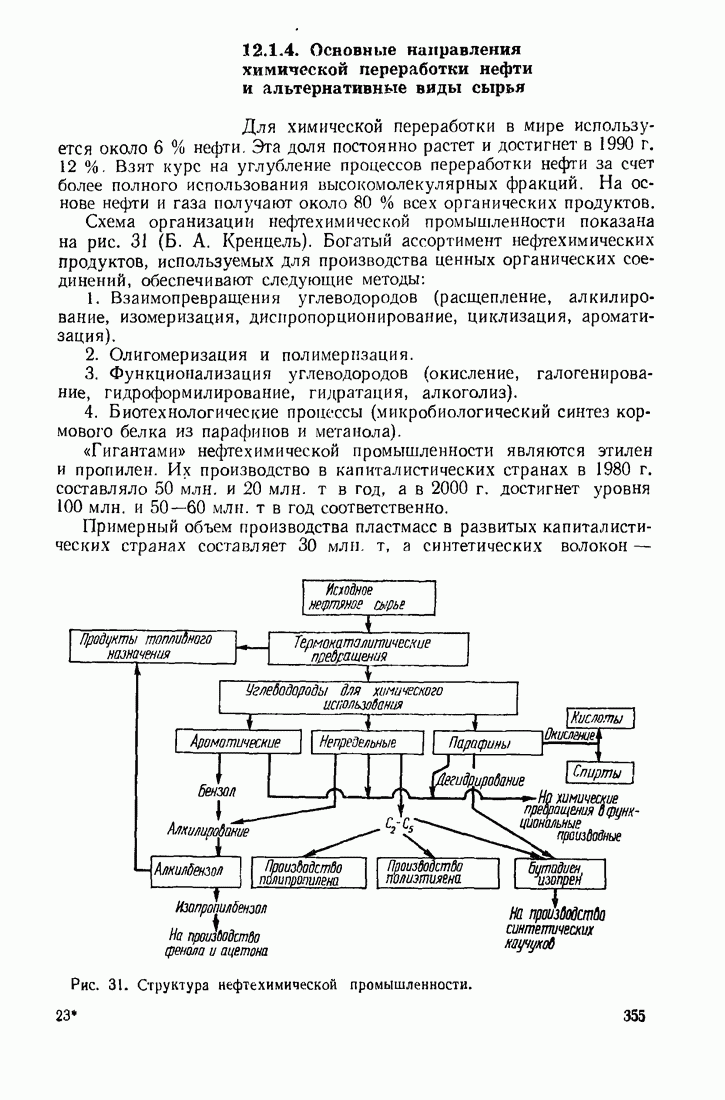
- 12.1.4. Основные направления химической переработки нефти и альтернативные виды сырья
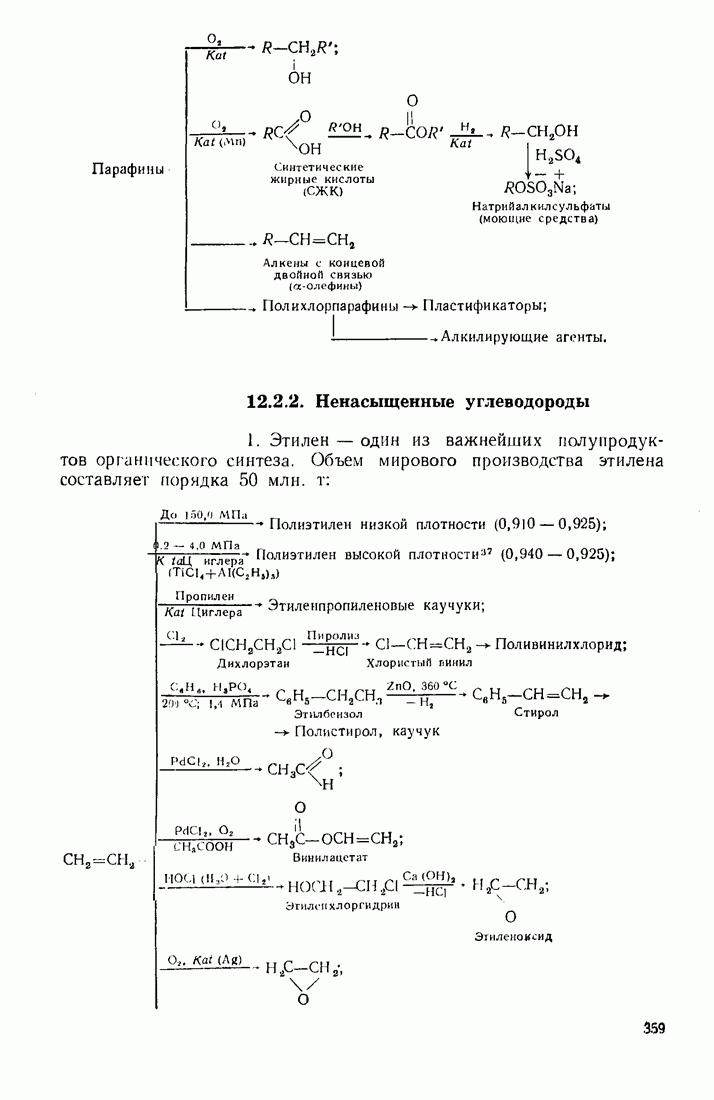
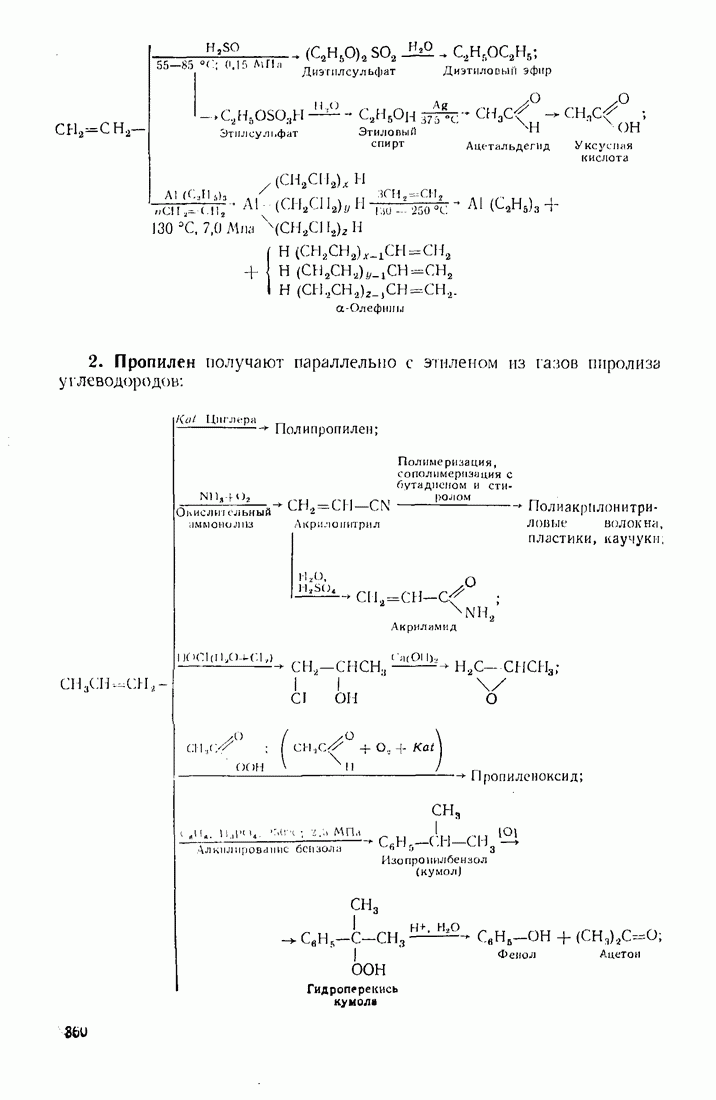
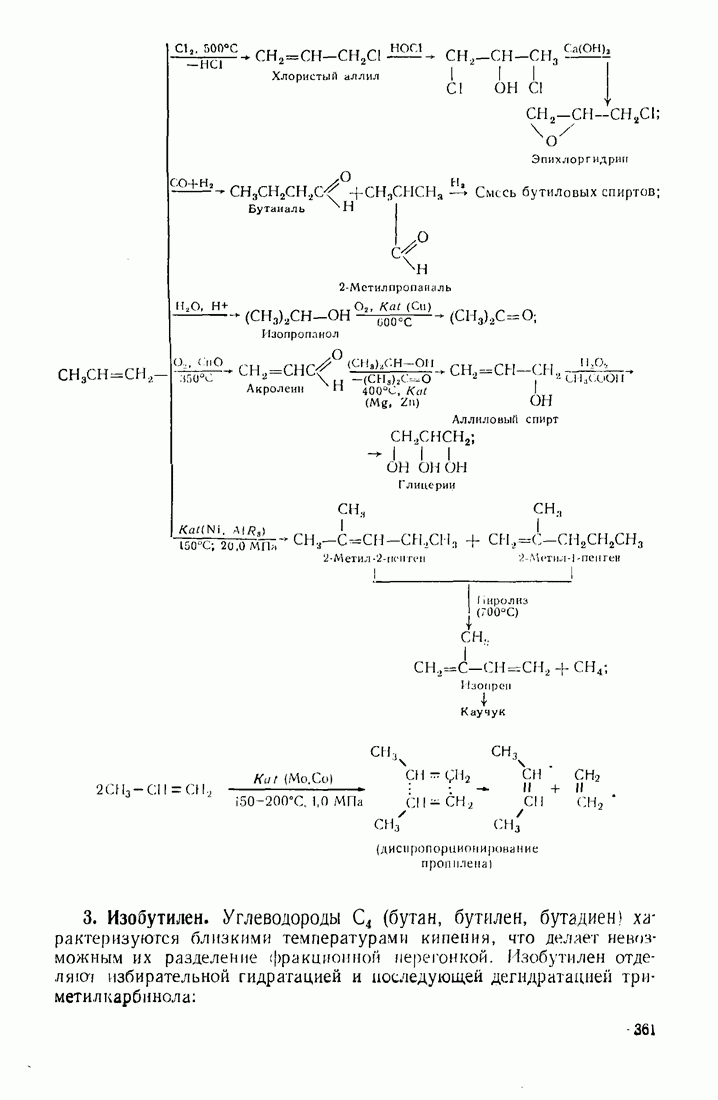
- 12.2. ПУТИ ИСПОЛЬЗОВАНИЯ УГЛЕВОДОРОДОВ И ИХ ПРОИЗВОДНЫХ
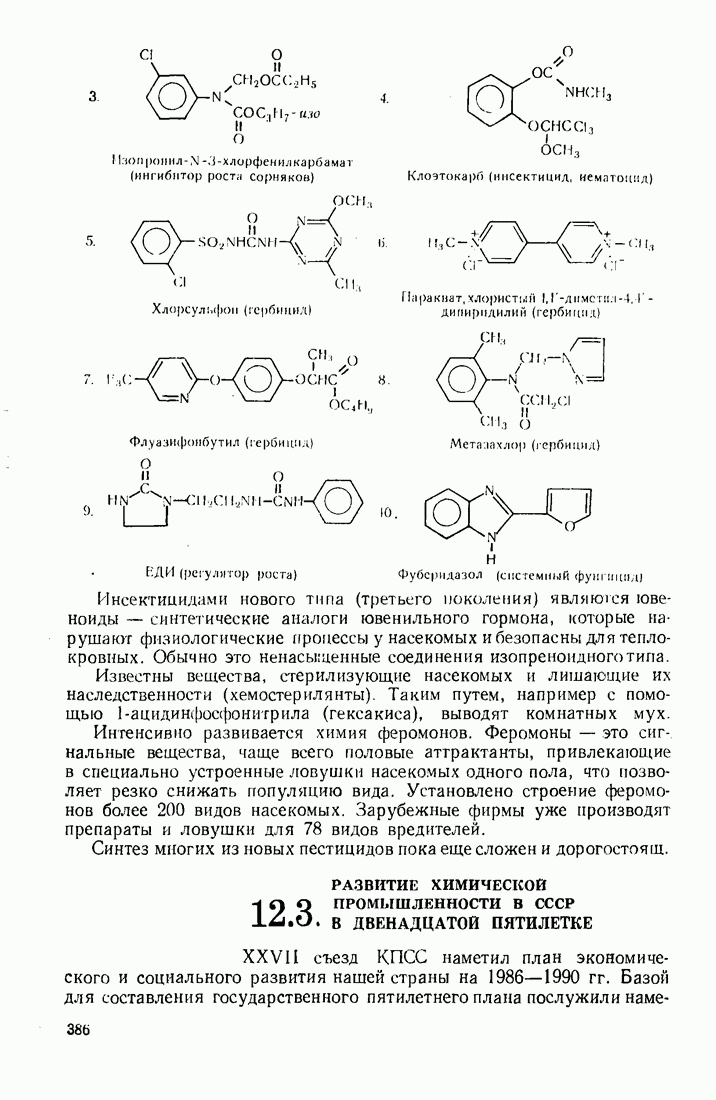
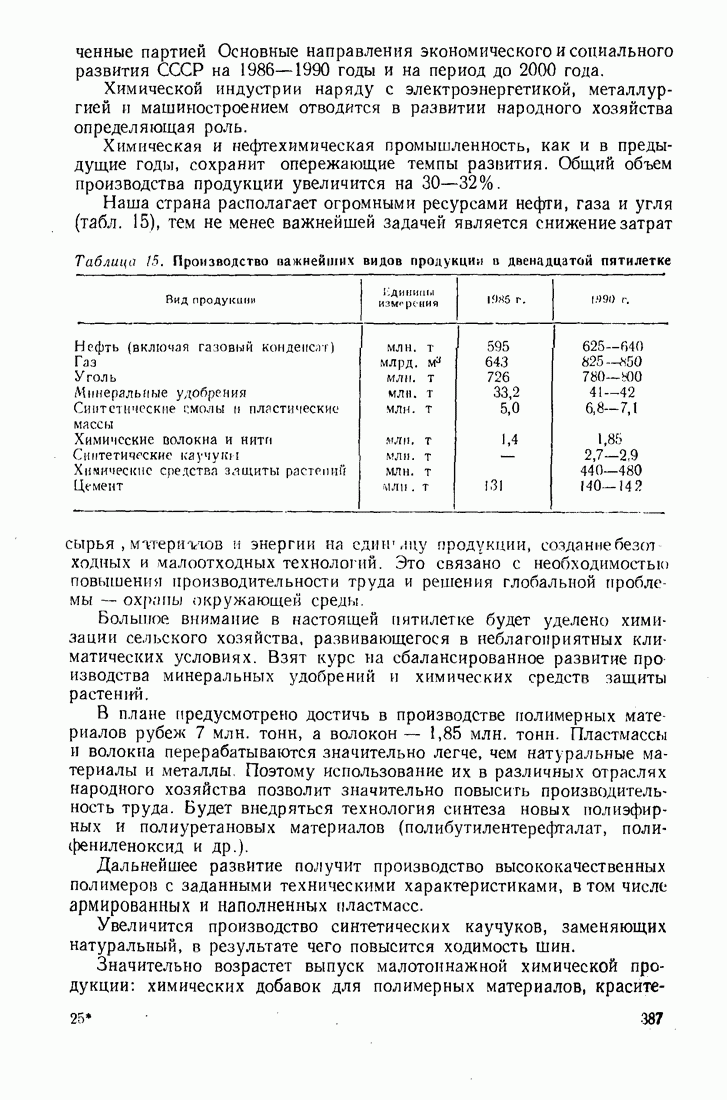
- 12.3. РАЗВИТИЕ ХИМИЧЕСКОЙ ПРОМЫШЛЕННОСТИ В СССР В ДВЕНАДЦАТОЙ ПЯТИЛЕТКЕ