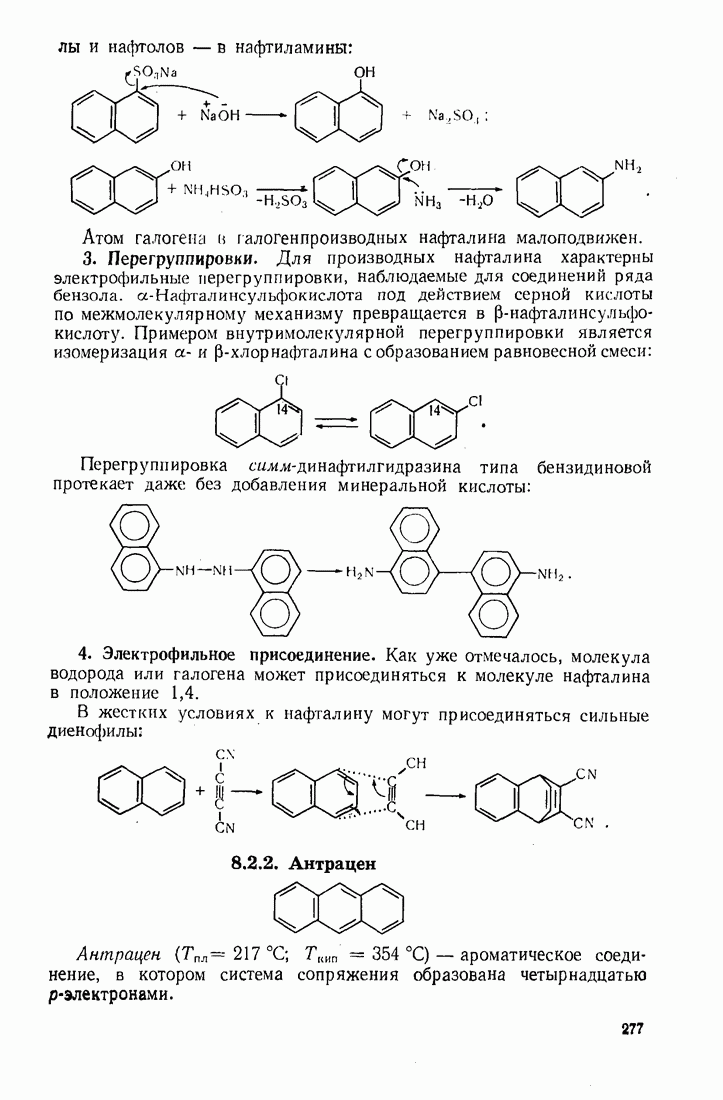
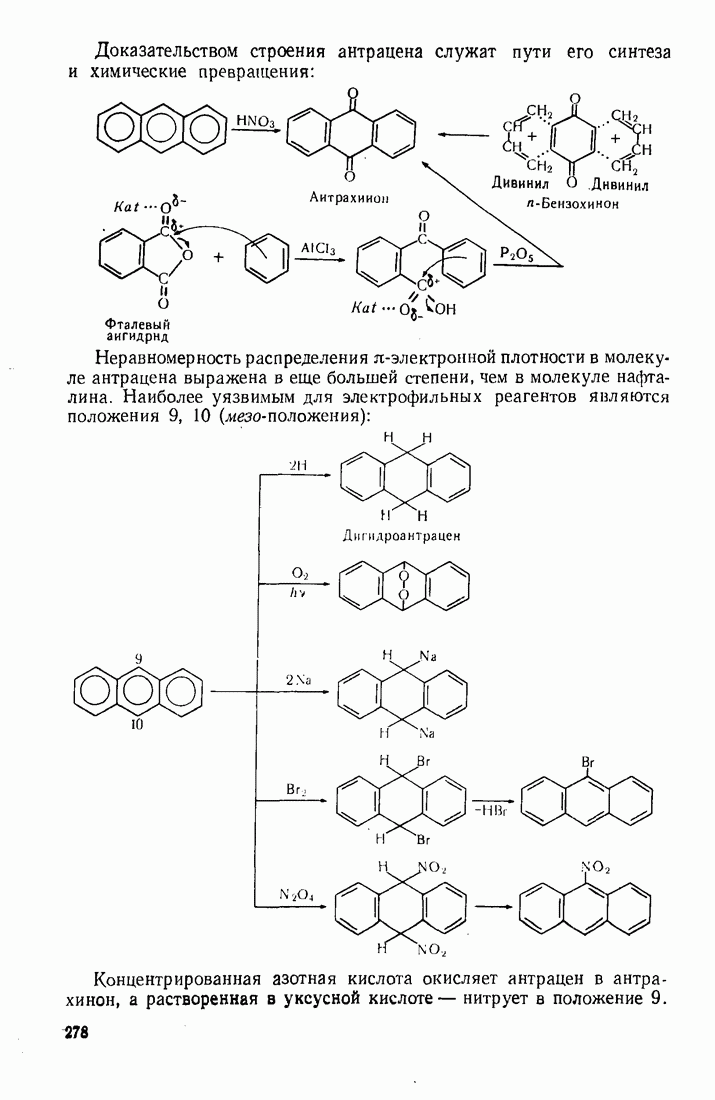
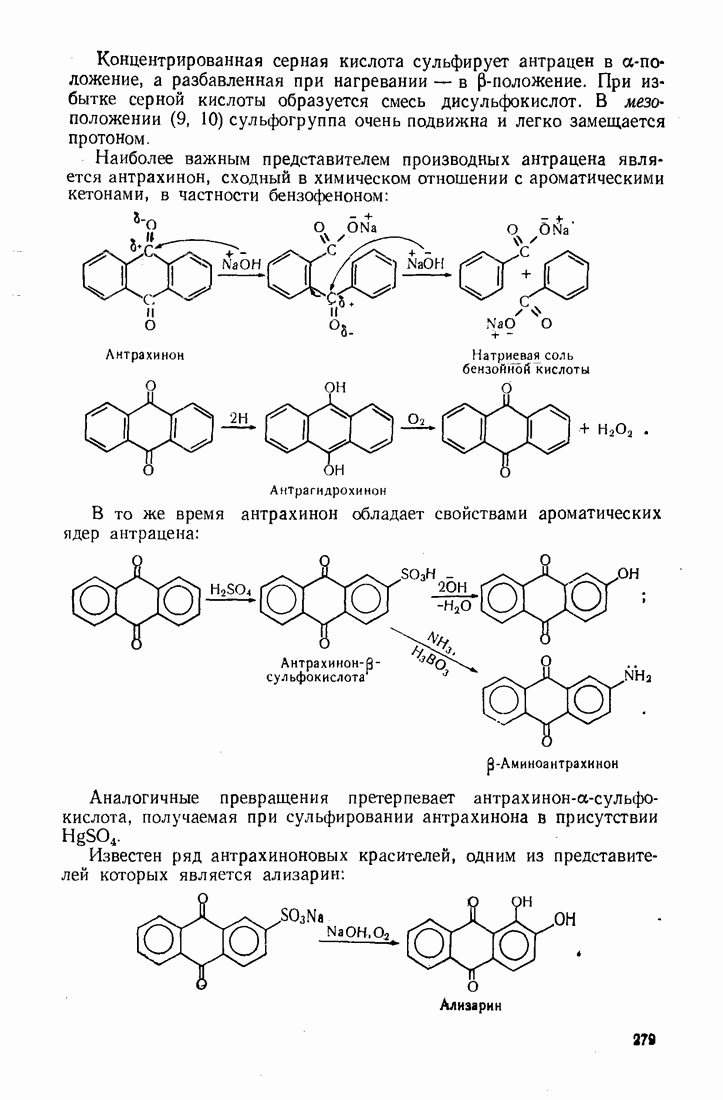
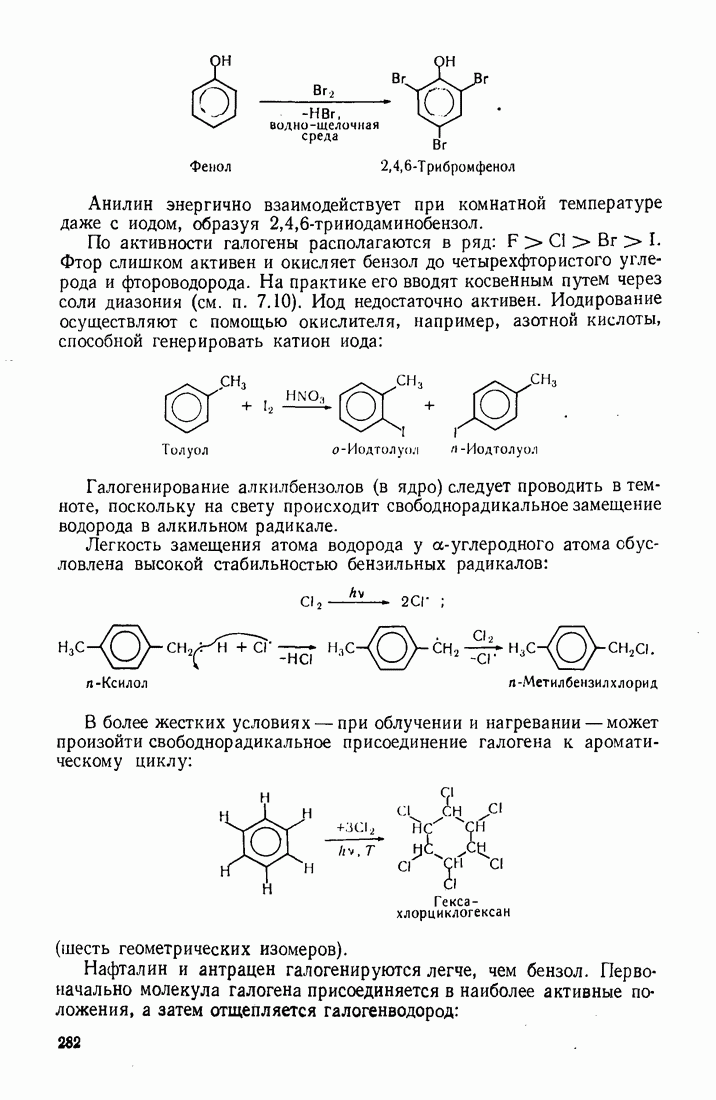
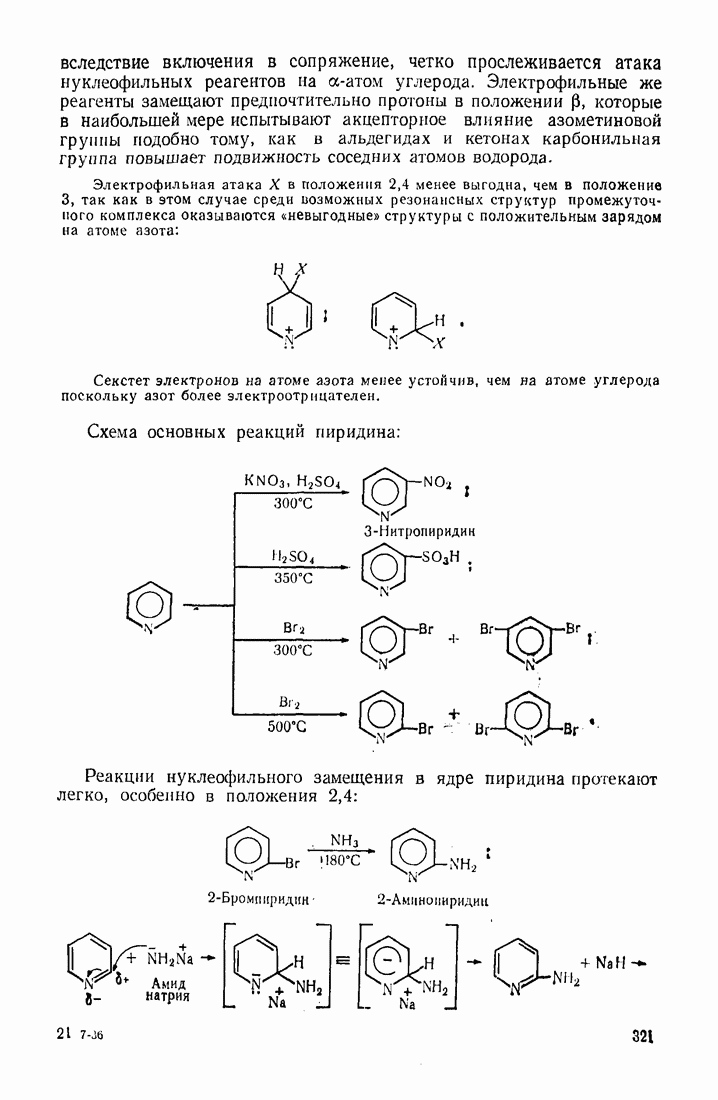
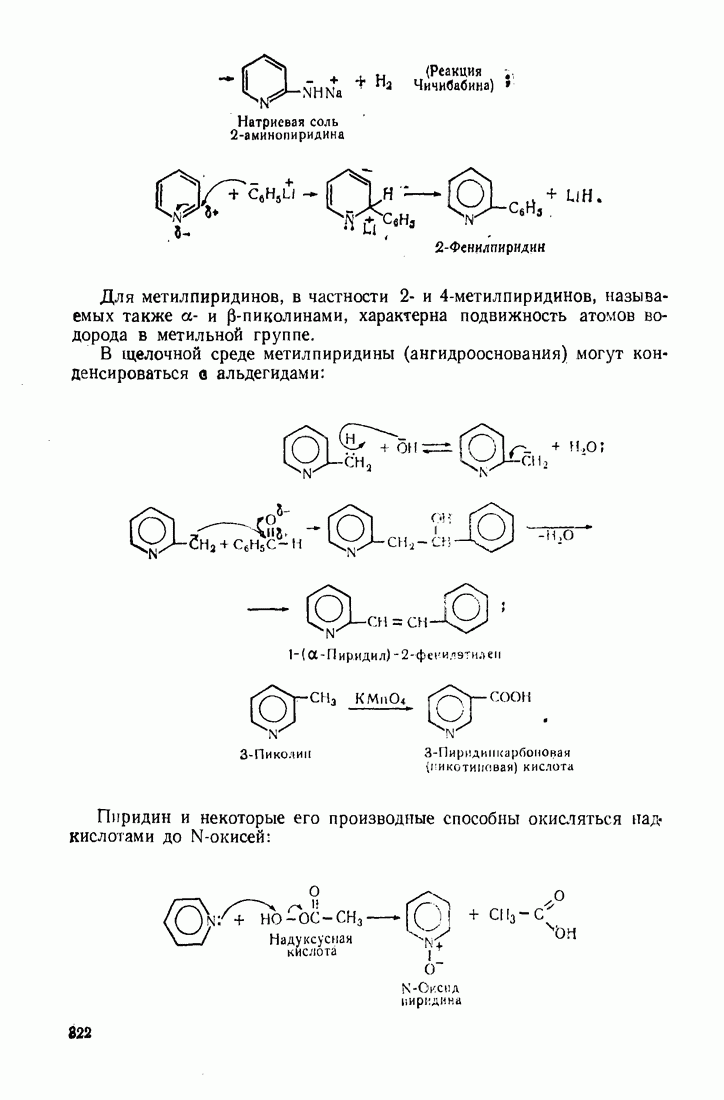
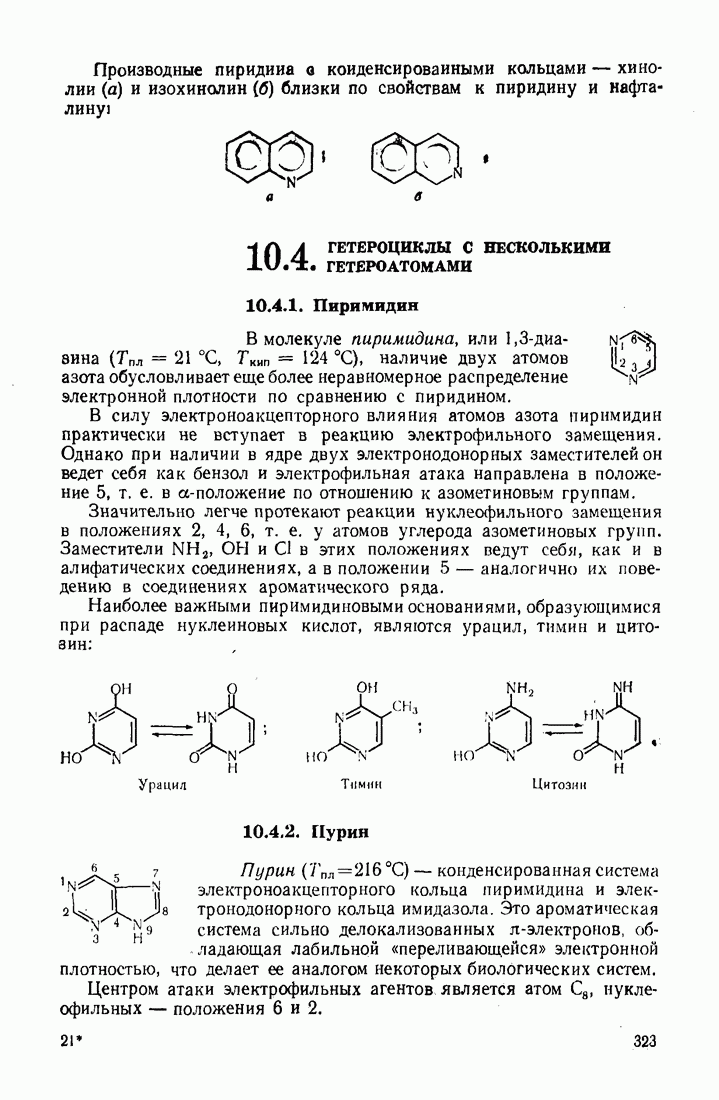
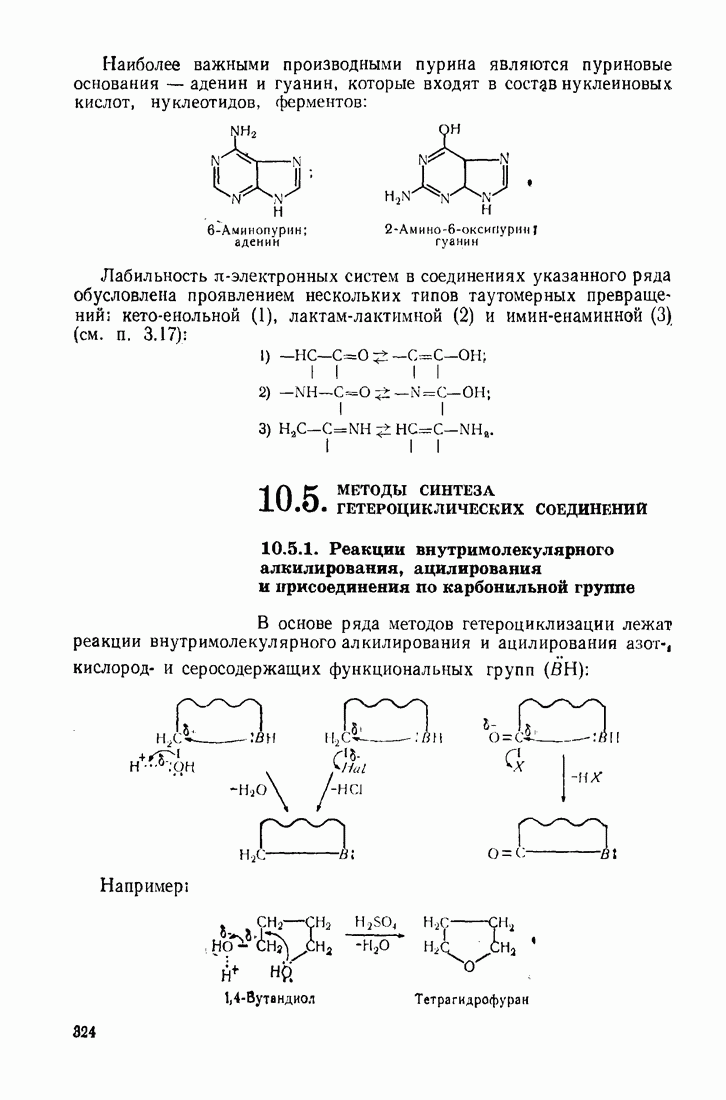
| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
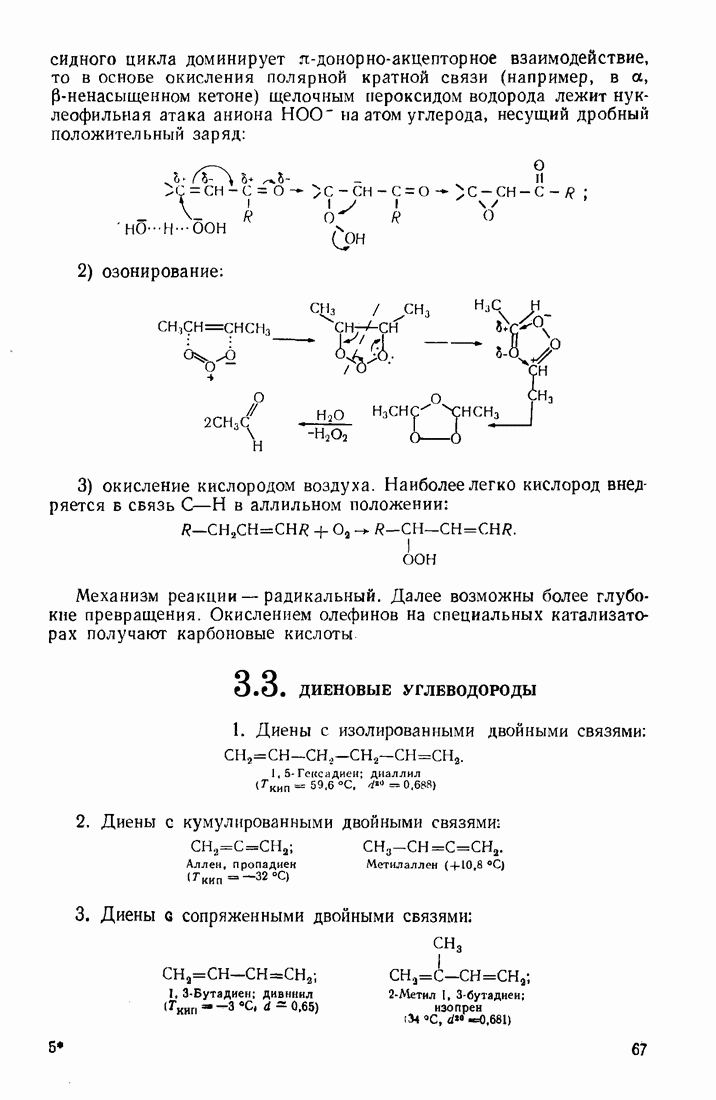
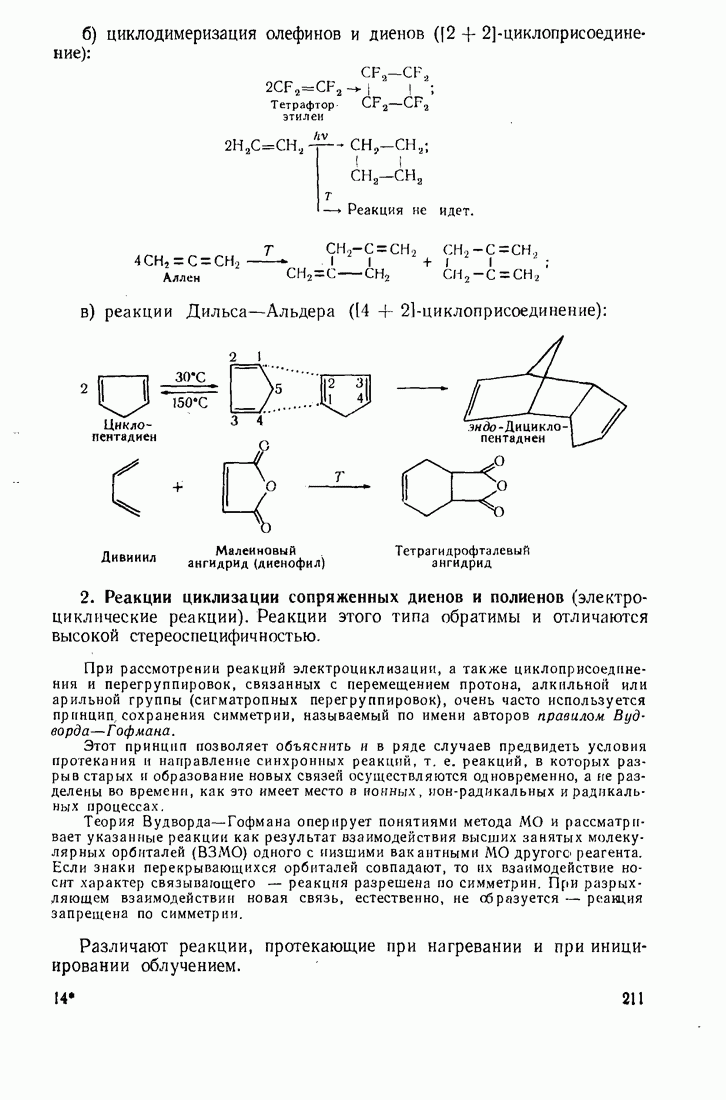
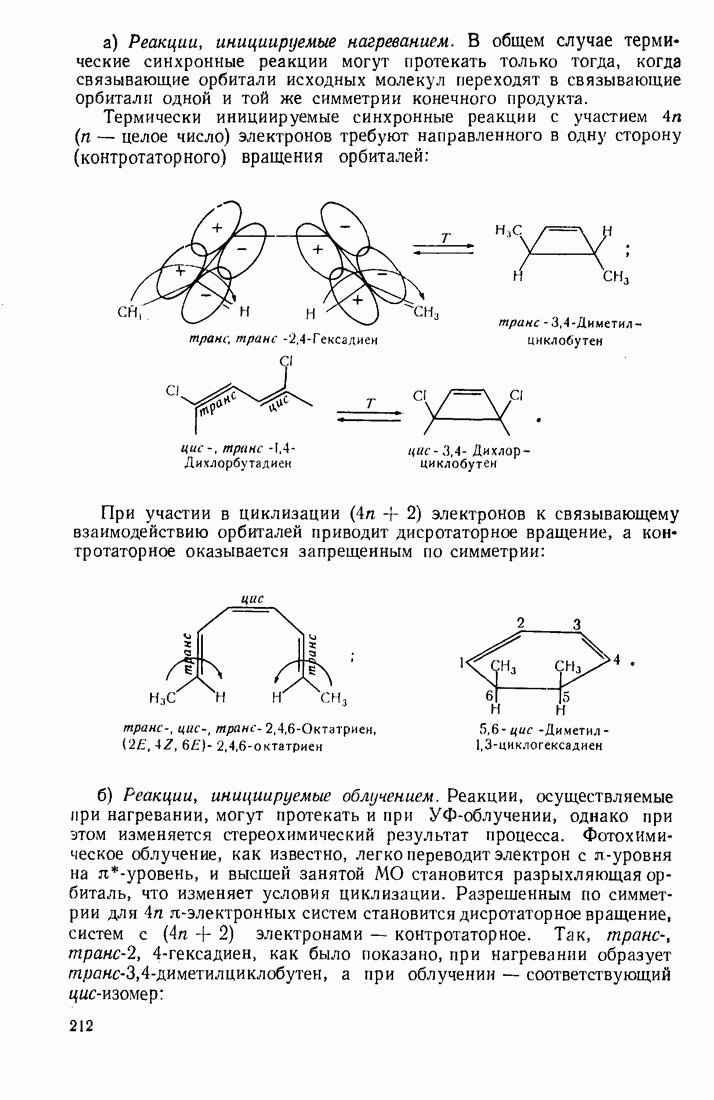
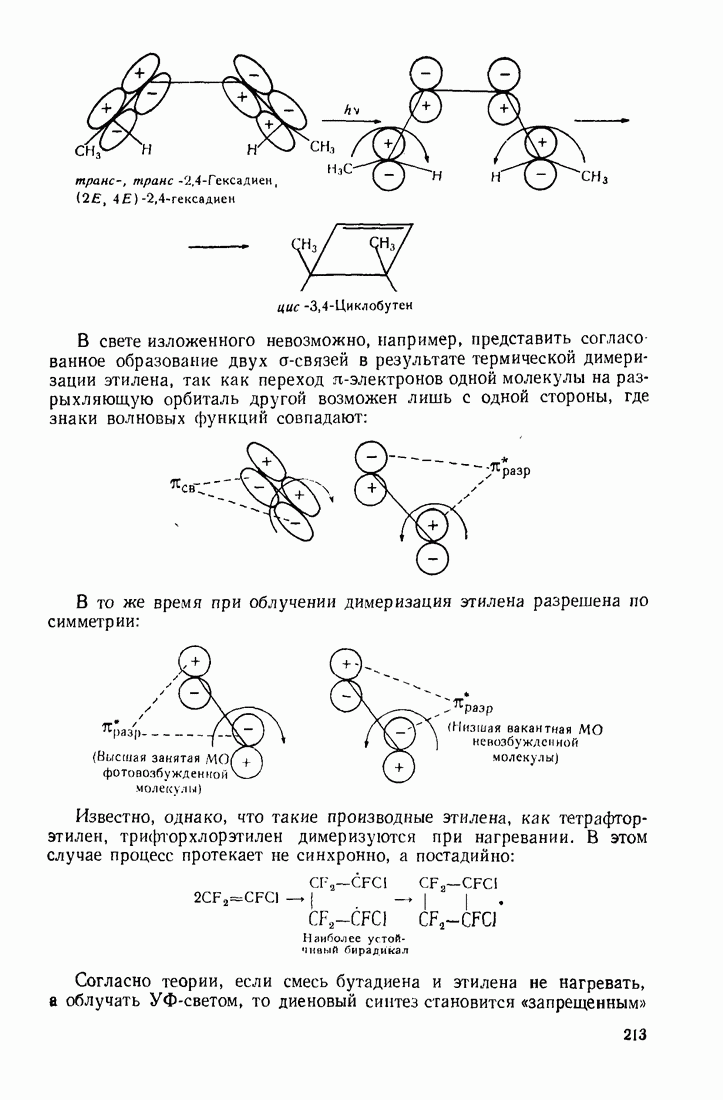
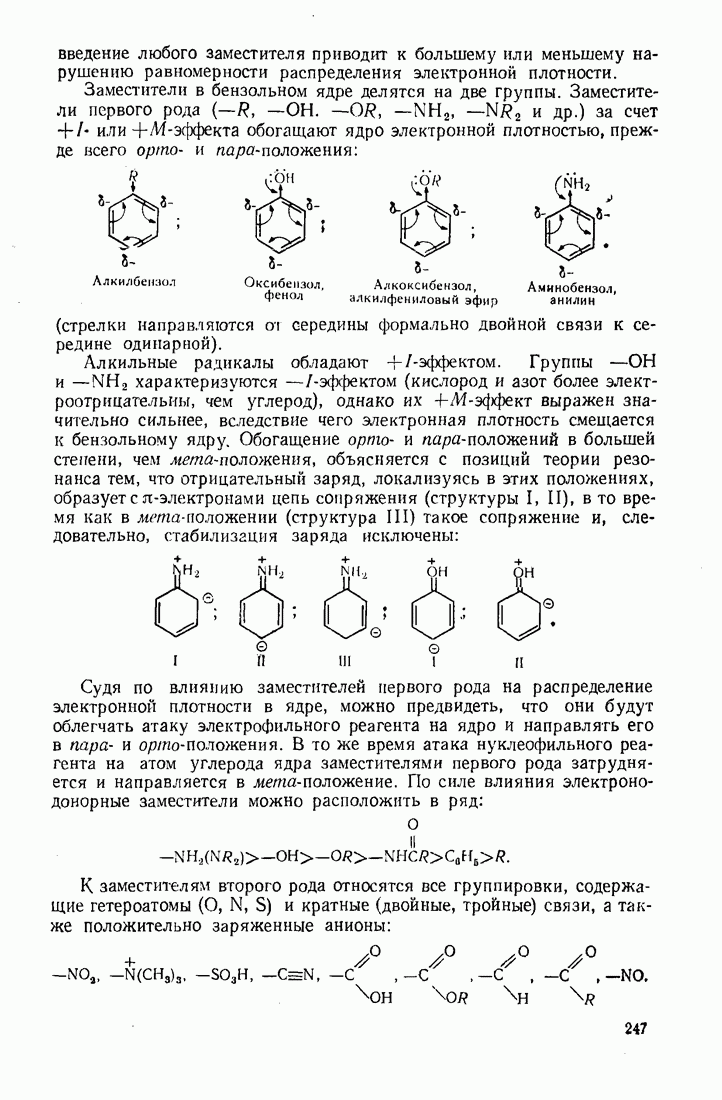
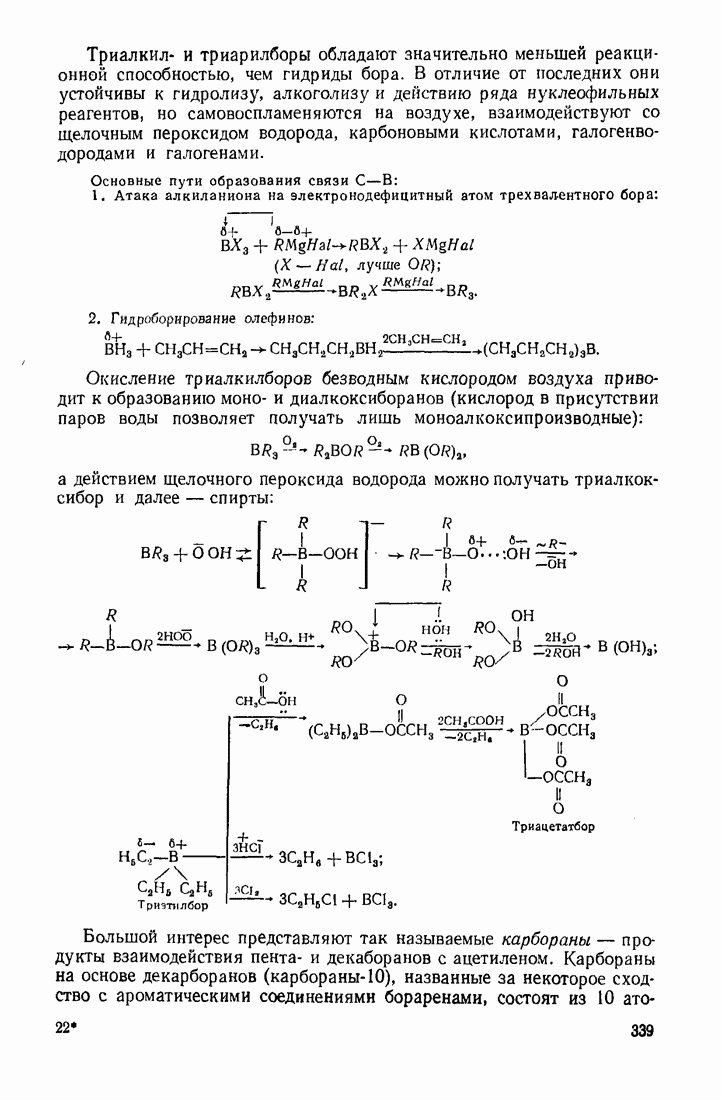
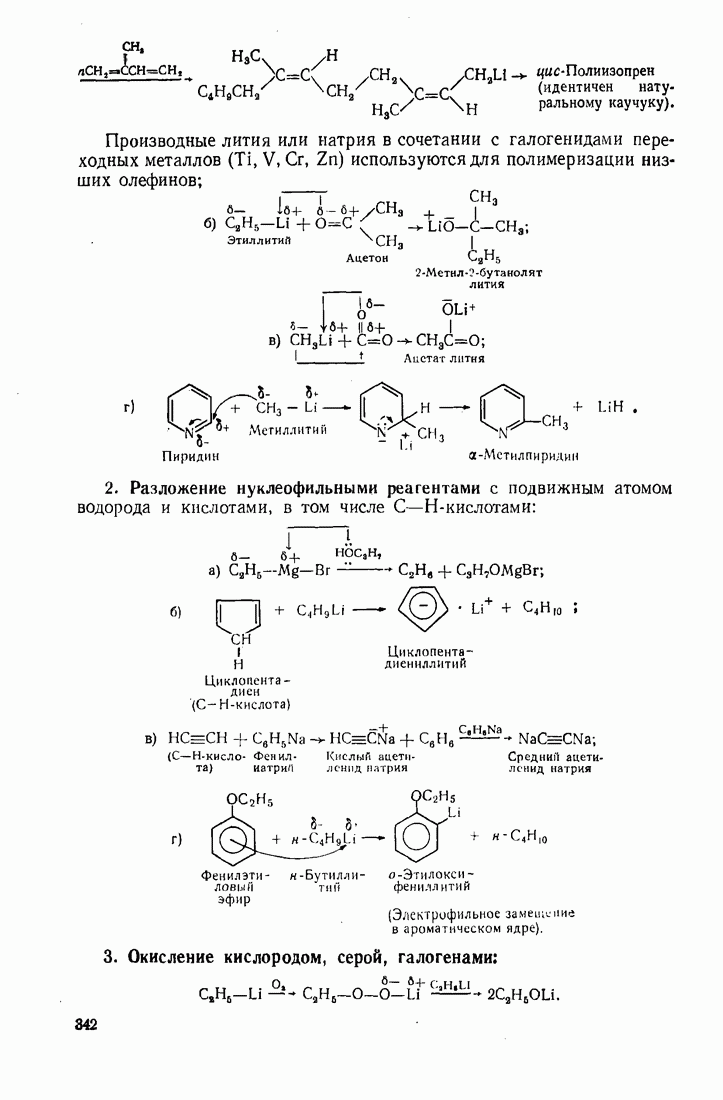
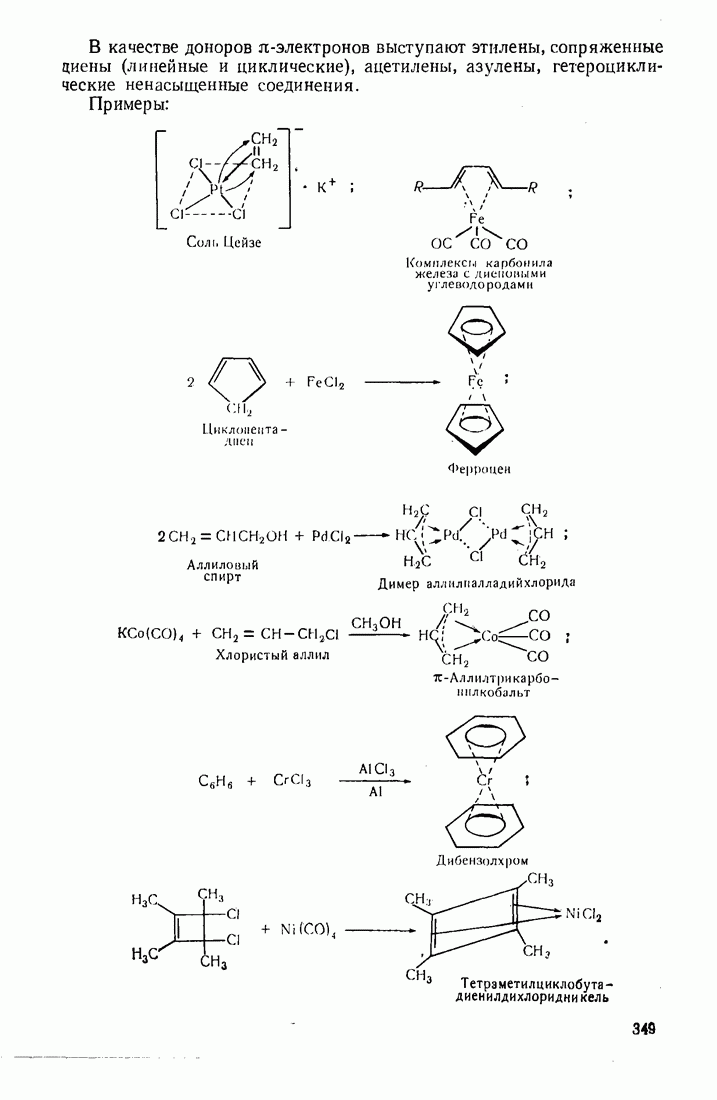
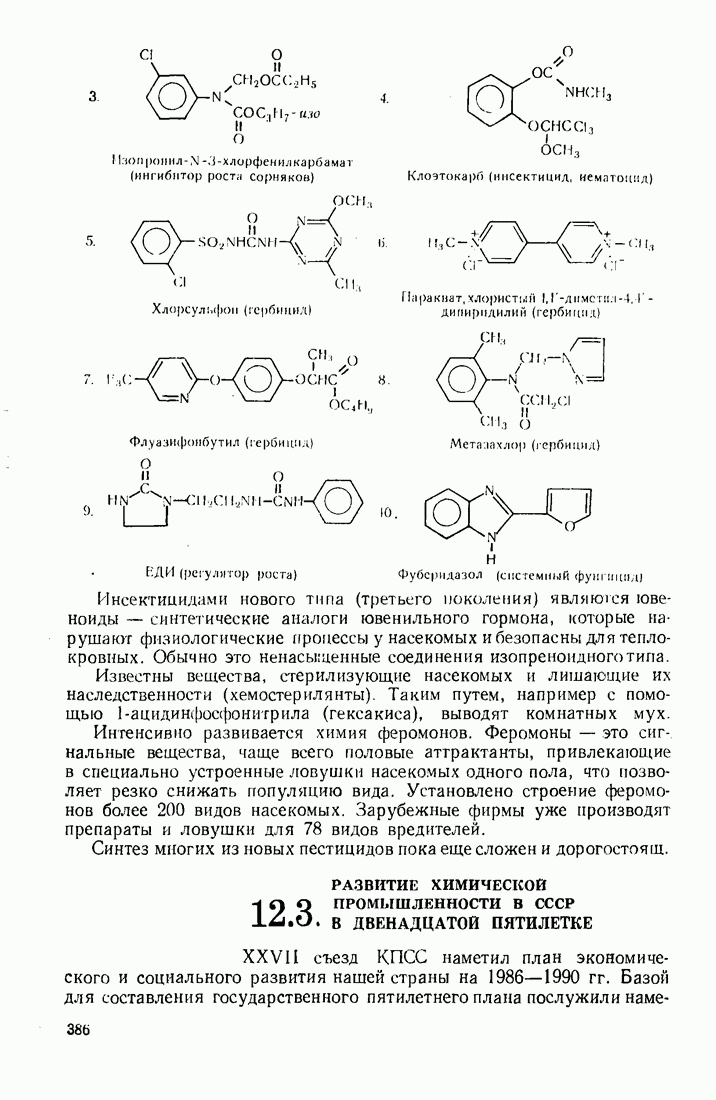
2.2. ТИПЫ ЭЛЕКТРОННЫХ СМЕЩЕНИЙ В МОЛЕКУЛАХ
Согласно методу  электронная плотность, образующая связь, смещается к более электроотрицательному атому. Электроотрицательность элементов возрастает в рядах:
электронная плотность, образующая связь, смещается к более электроотрицательному атому. Электроотрицательность элементов возрастает в рядах:

Различают два типа электронных эффектов: индукционный  и мезомерный
и мезомерный  Последний называют также эффектом сопряжения
Последний называют также эффектом сопряжения 
Индукционный эффект  это смещение электронов по цепи
это смещение электронов по цепи  -связей к более электроотрицательному атому (или группе атомов), обозначается прямой стрелкой:
-связей к более электроотрицательному атому (или группе атомов), обозначается прямой стрелкой:


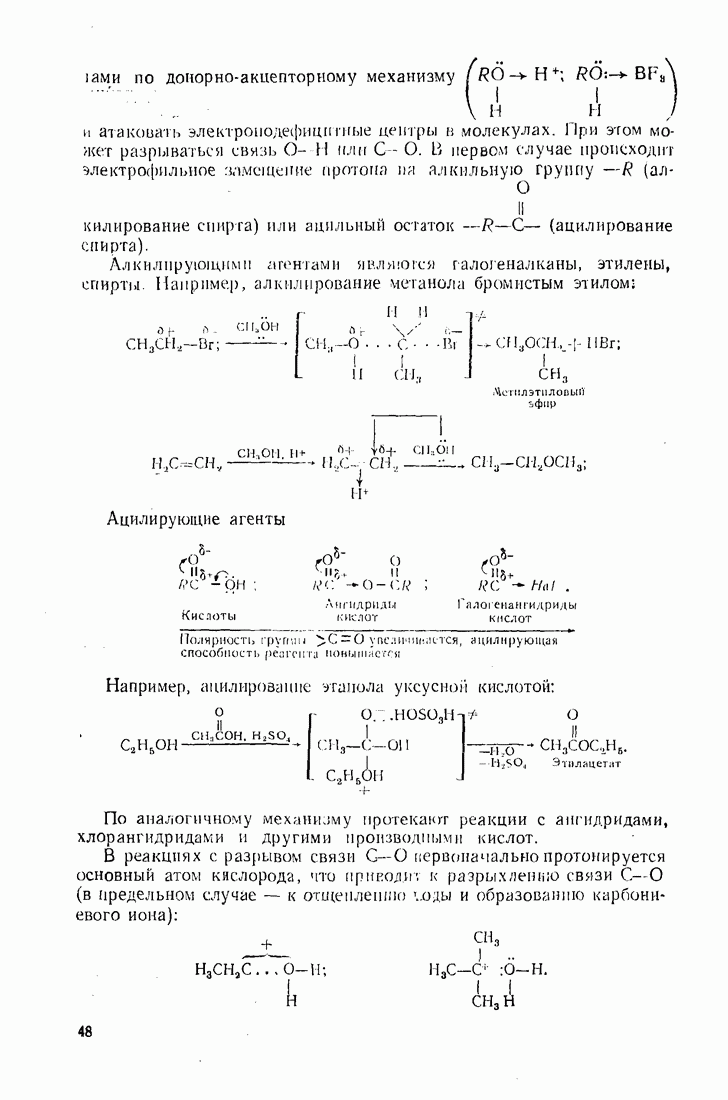
Рис. 14. Схема образования связей центрального атома (железа) с одним из лигандов в молекуле  Заполненные орбиталн заштрихованы; вакайтные не заштрихованы.
Заполненные орбиталн заштрихованы; вакайтные не заштрихованы.
Заместитель характеризуется отрицательным  -эффектом, если он оттягивает электронную плотность к себе, т. е. стремится приобрести отрицательный заряд. Положительный
-эффектом, если он оттягивает электронную плотность к себе, т. е. стремится приобрести отрицательный заряд. Положительный  -эффект указывает на то, что заместитель отталкивает электронную плотность от себя. Следовательно, —
-эффект указывает на то, что заместитель отталкивает электронную плотность от себя. Следовательно, — -эффектом по отношению к атому углерода
-эффектом по отношению к атому углерода  обладают все функциональные группы, включающие атомы
обладают все функциональные группы, включающие атомы  и кратные связи:
и кратные связи:

Положительным индукционным эффектом обладают заместители, несущие отрицательный заряд  и алкильные заместители
и алкильные заместители 
Мезомерный эффект  характеризует смещение высокополяризуемых
характеризует смещение высокополяризуемых  или
или  -электронов, изображается кривой стрелкой:
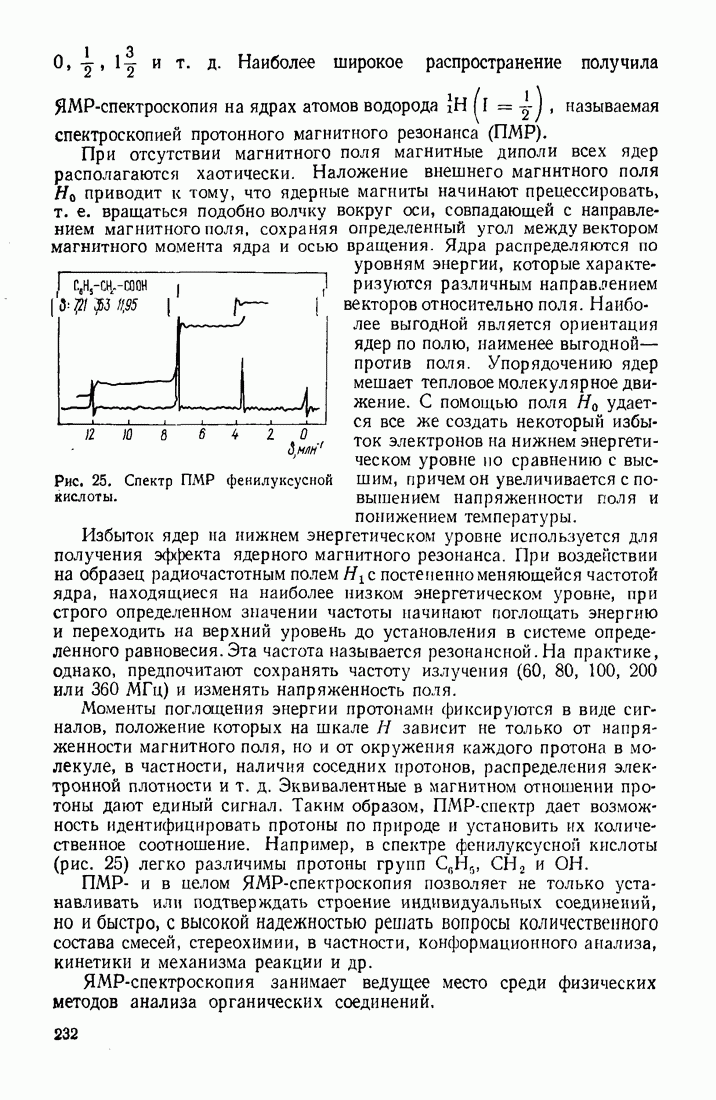
-электронов, изображается кривой стрелкой:

Истинное состояние группы  находится между мнимыми граничными структурами (а) и (б).
находится между мнимыми граничными структурами (а) и (б).
Мезомерный эффект особенно сильно проявляется в сопряженных системах, в которых кратные связи  и
и  и неподеленные пары
и неподеленные пары  -электронов чередуются с
-электронов чередуются с  -связями. Необходимым условием взаимодействия
-связями. Необходимым условием взаимодействия  и
и  -электронов является разделение их ординарной связью и копланарность соответствующих орбиталей (оси симметрии орбиталей должны находиться в одной плоскости):
-электронов является разделение их ординарной связью и копланарность соответствующих орбиталей (оси симметрии орбиталей должны находиться в одной плоскости):

М-эффекту заместителя знак («плюс» или «минус») приписывается по такому же принципу, как и  -эффекту. Так, в приведенных примерах по отношению к группировке
-эффекту. Так, в приведенных примерах по отношению к группировке  группы
группы  обладают
обладают  -эффектом, а
-эффектом, а  -эффектом.
-эффектом.
Следует отметить, что  -электроны могут вступать в сопряжение с вакантной орбиталью, а также с орбиталью, на которой располагается один (в радикале) или два (в карбанионе) неподеленных электрона, если они разделены
-электроны могут вступать в сопряжение с вакантной орбиталью, а также с орбиталью, на которой располагается один (в радикале) или два (в карбанионе) неподеленных электрона, если они разделены  -связью:
-связью:

Такое сопряжение стабилизирует карбониевые ионы и радикалы, способствуя протеканию реакций, в которых они образуются в качестве промежуточных частиц (интермедиатов).
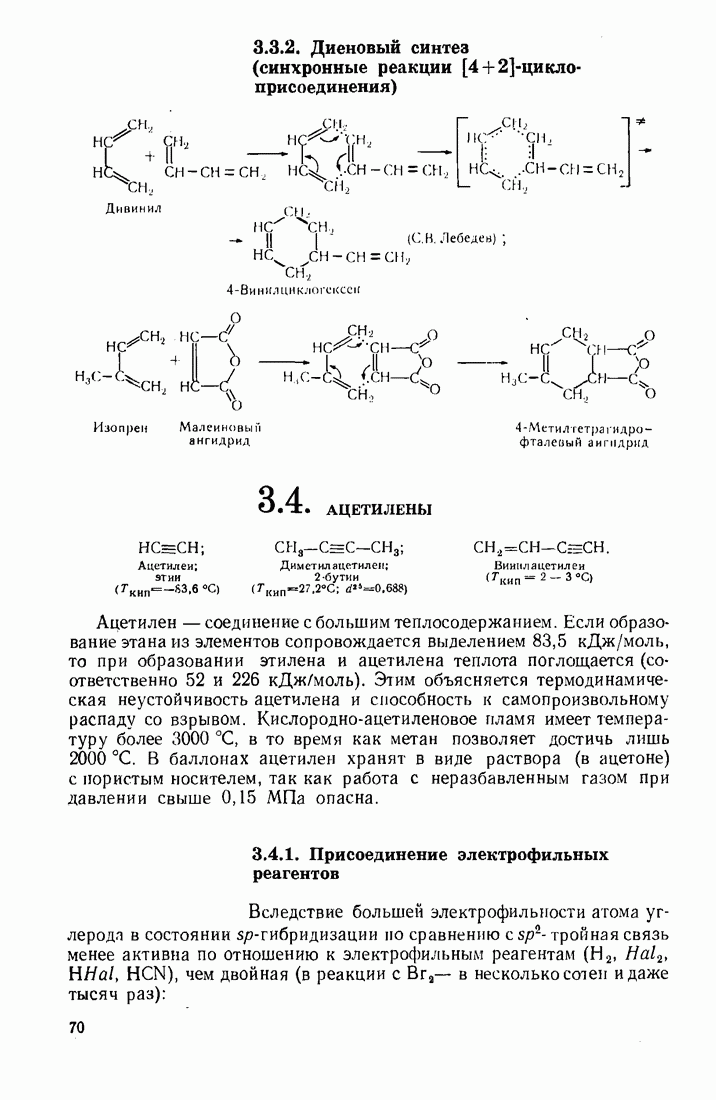
Близкой к теории мезомерии (К. Ингольд) является теория резонанса (Л. Полинг), согласно которой молекулу рассматривают как результат наложения (суперпозицшо) нескольких гипотетических предельных (резонансных) структур, имеющих одинаковое расположение атомов, но отличающихся распределением электронной плотности. Например, молекулу  -бутадиена можно представить как резонансный гибрид четырех структур:
-бутадиена можно представить как резонансный гибрид четырех структур:

Это не значит, что отдельные молекулы бутадиена могут существовать в виде структур (I - IV). В отличие от таутомеров, являющихся реальными соединениями, резонансные структуры не имеют физического смысла и не измеряются экспериментально.
Резонанс нельзя связывать с какими-либо электронными колебаниями или осцилляциями в молекулах.
Энергия реальной молекулы ниже расчетной энергии любой из структур. Выигрыш энергии резонансного гибрида относительно структуры, вносящей в него наибольший вклад, называют энергией резонанса.
Учет нескольких резонансных структур необходим в тех случаях, когда соединение нельзя представить одной структурной формулой, отражающей все его свойства.
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие
- 1. Введение
- 1.1. Предмет органической химии
- 1.2. Основные этапы развития органической химии
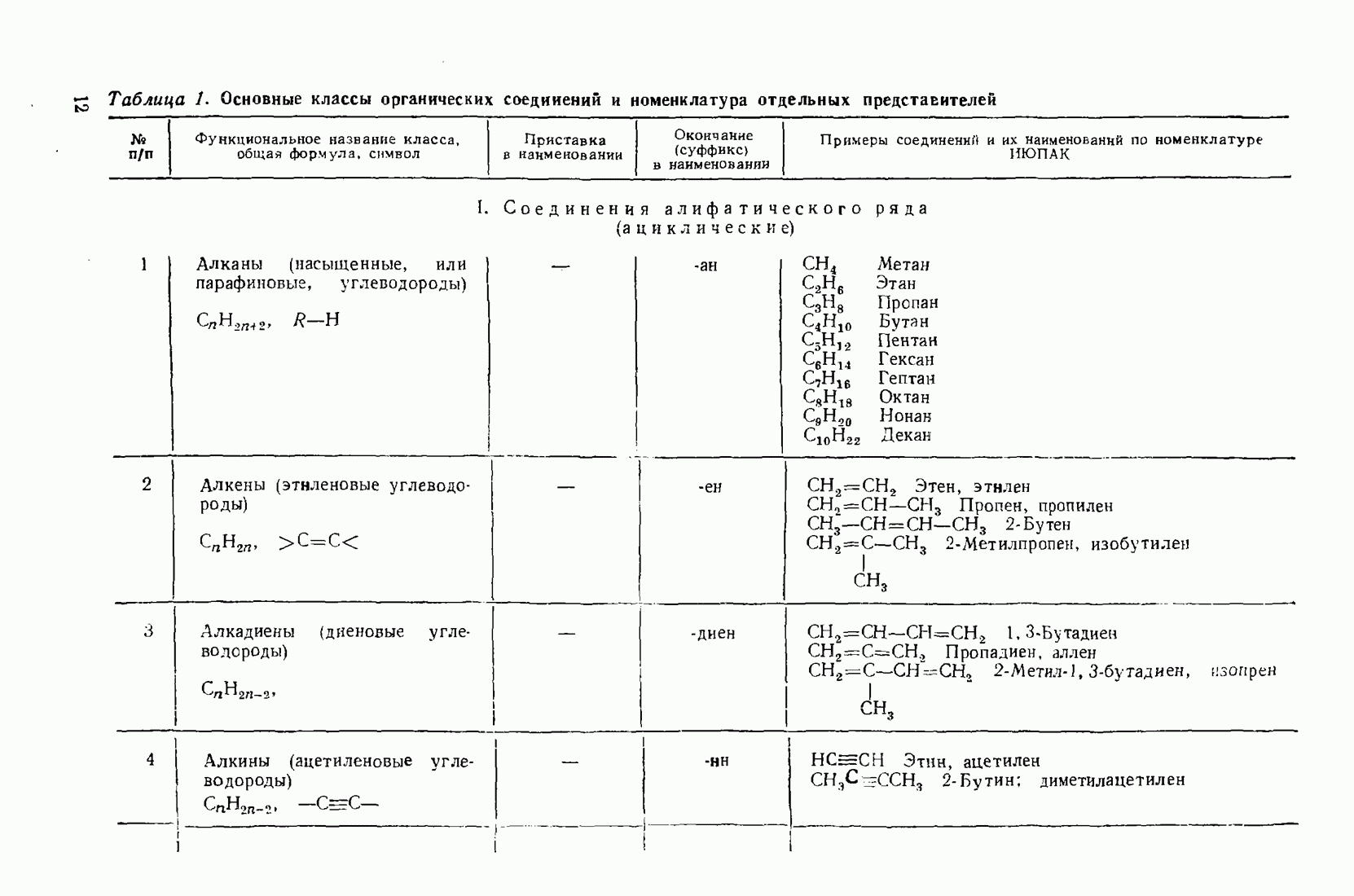
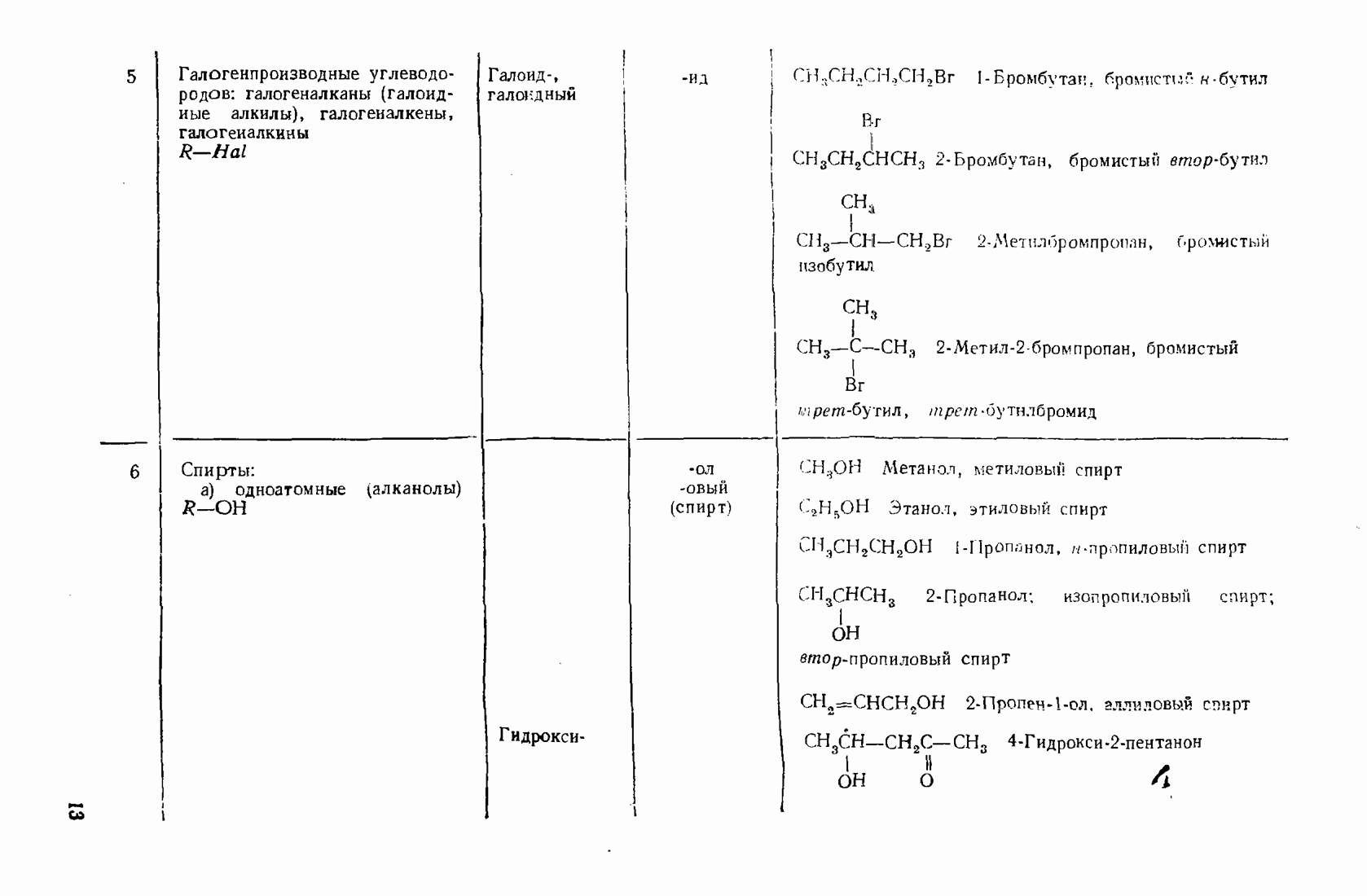
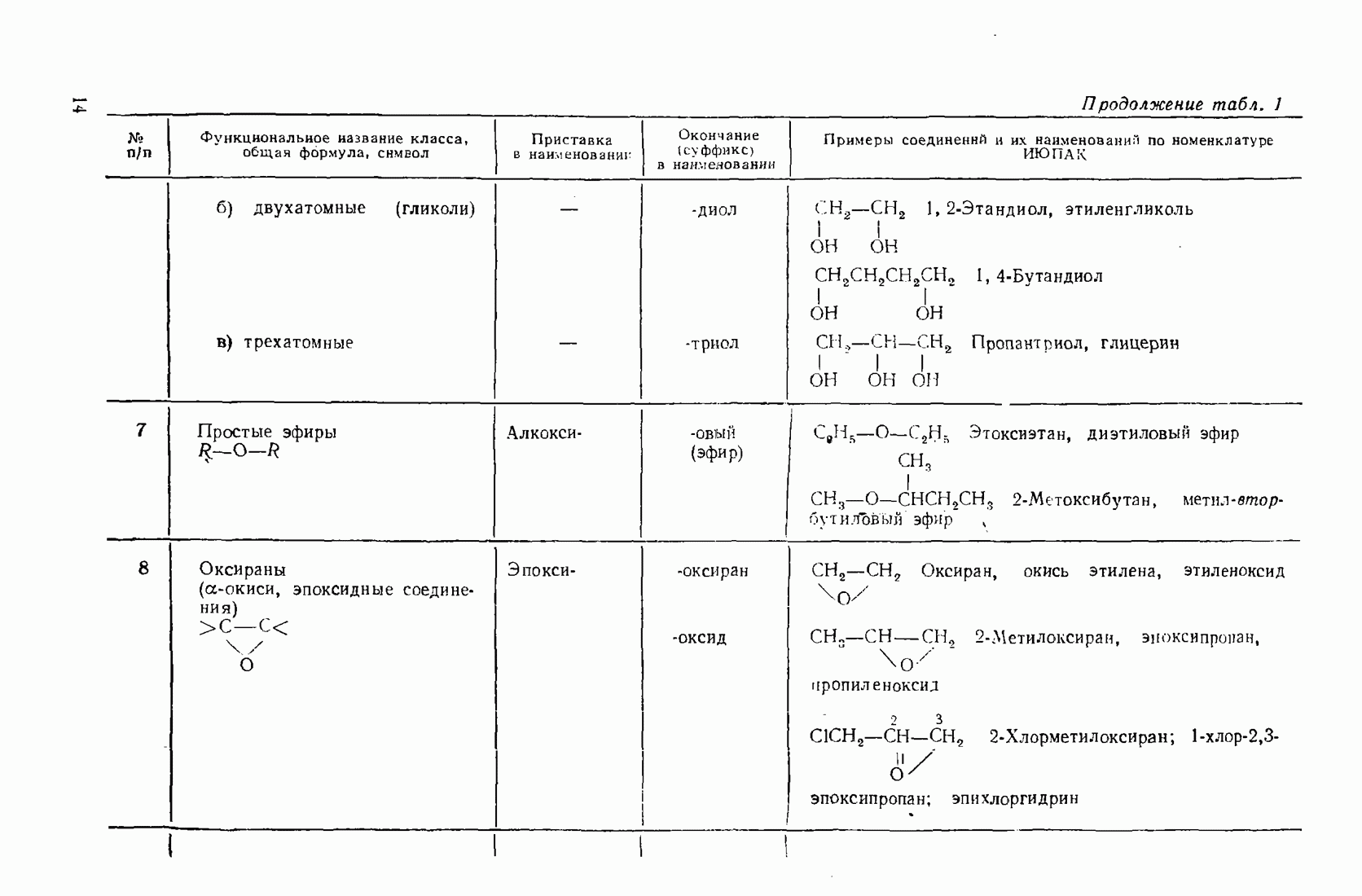
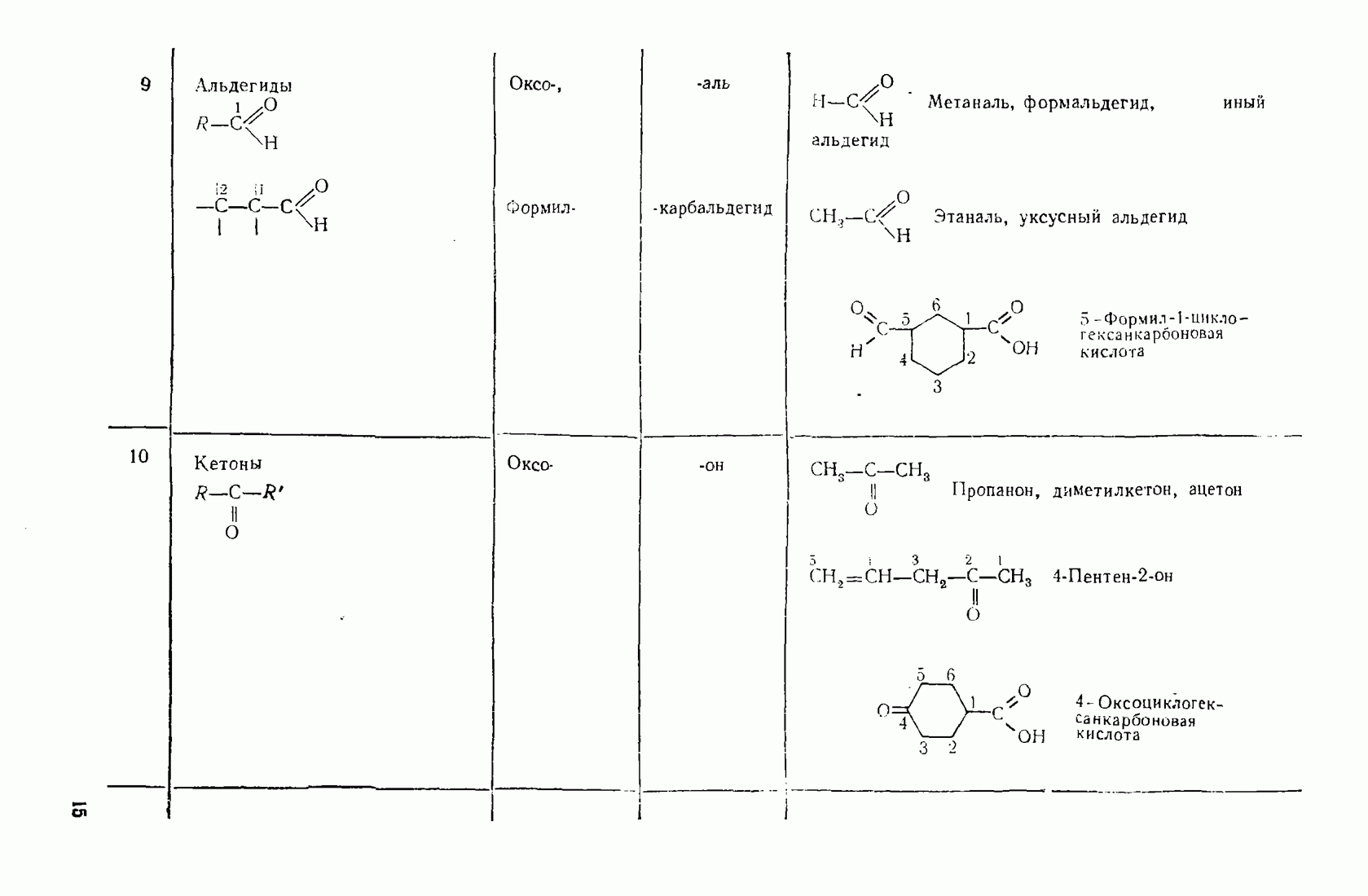
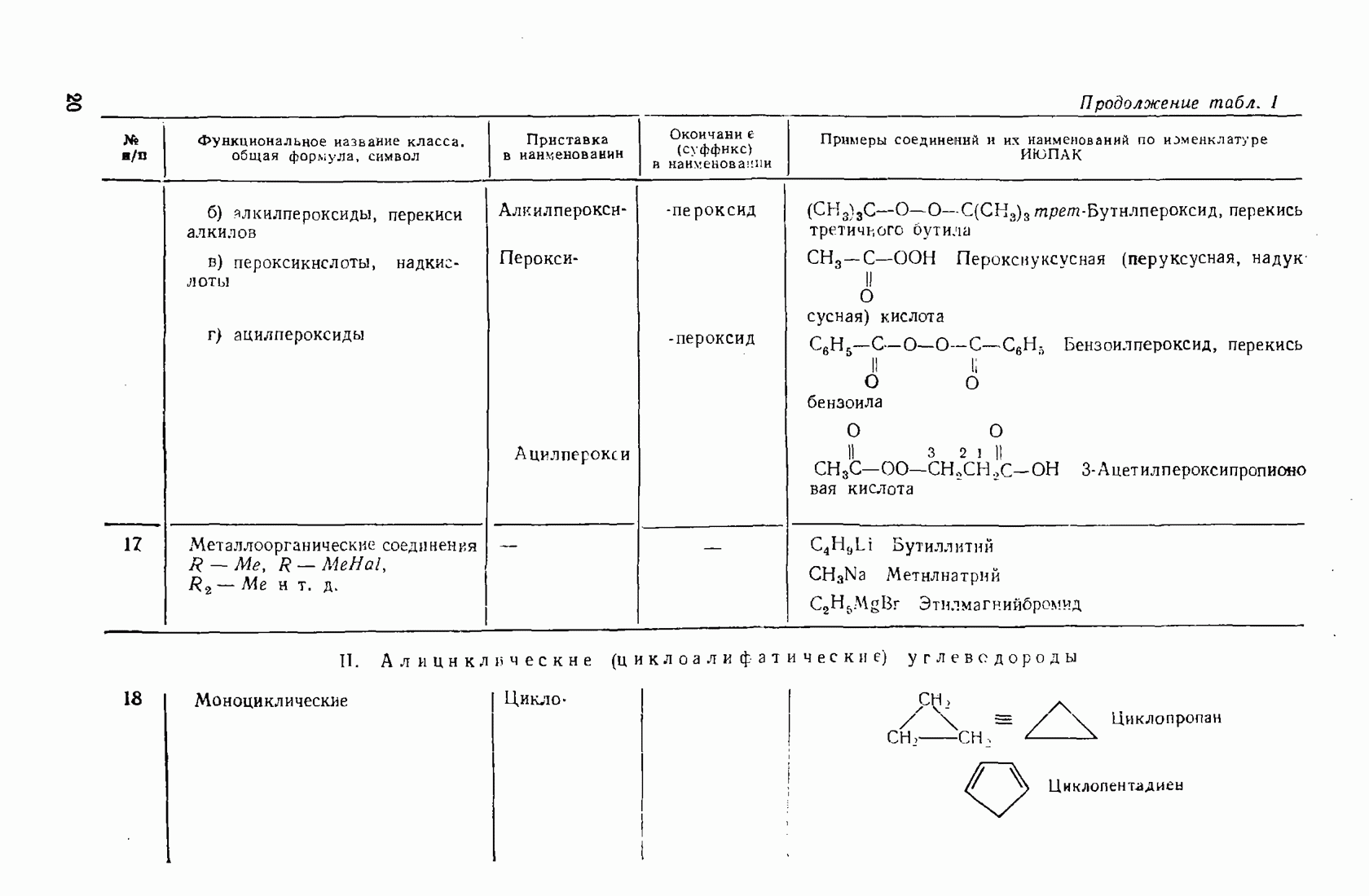
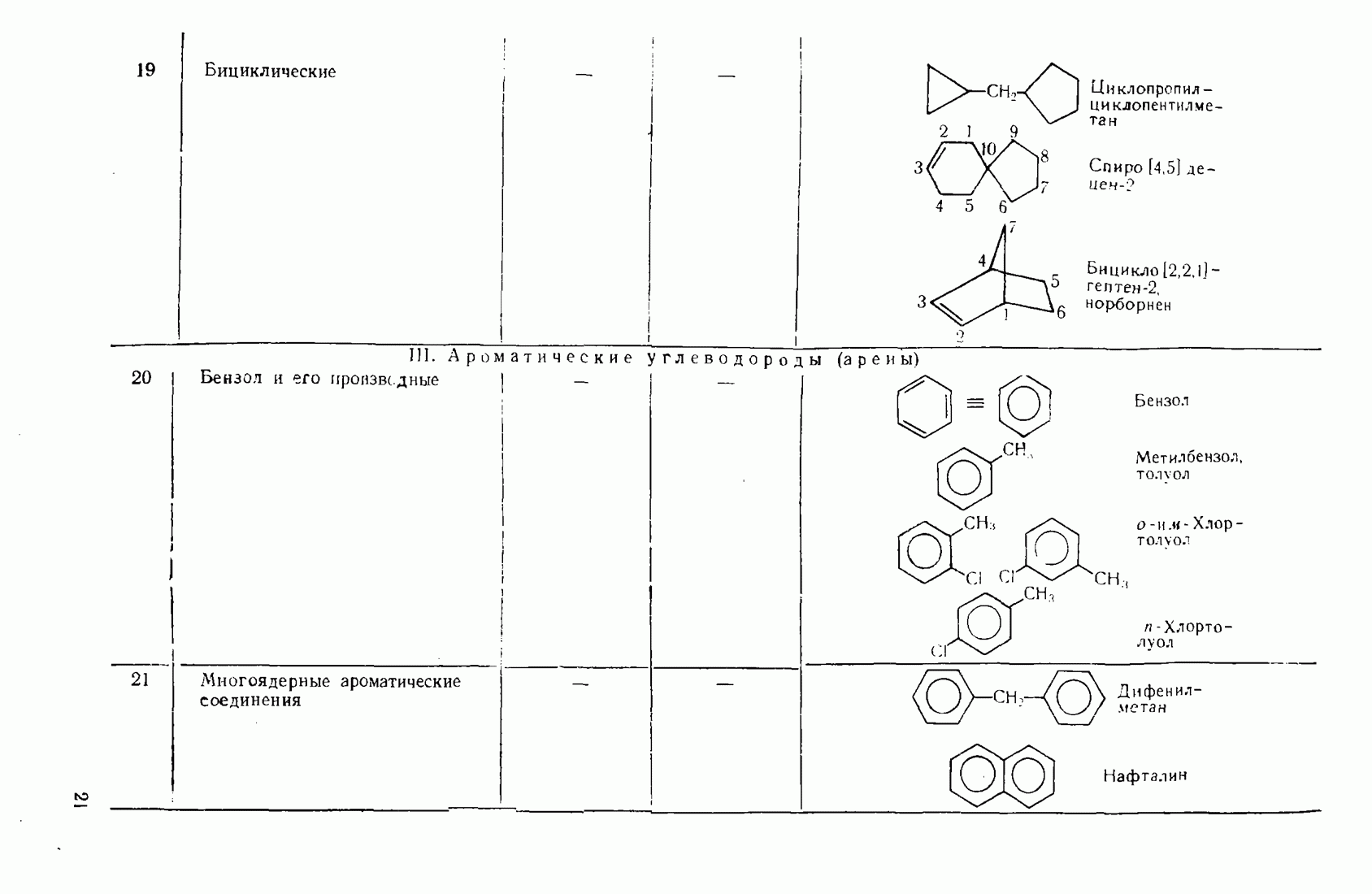
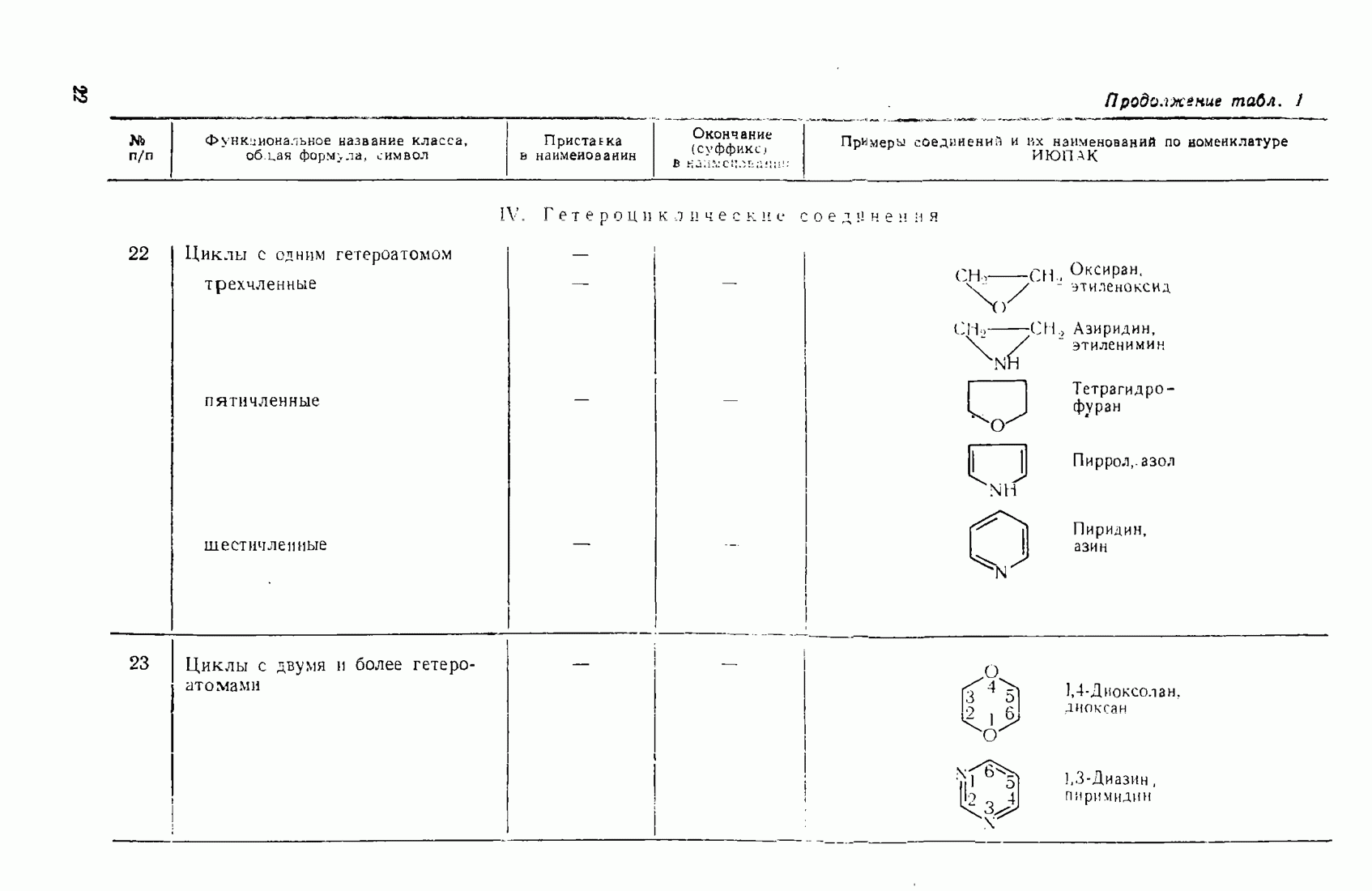
- 1.3. Классификация и номенклатура органических соединений
- 2 Общие теоретические положения органической химии
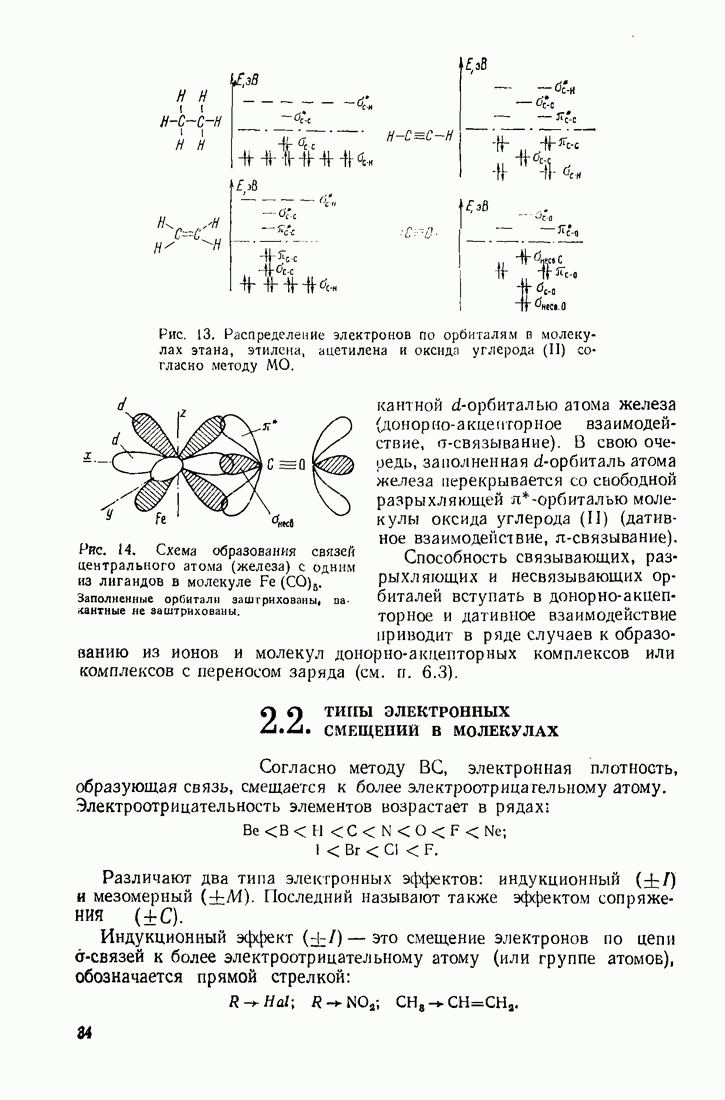
- 2.1. Природа химической связи
- 2.1.1. Типы химических связей
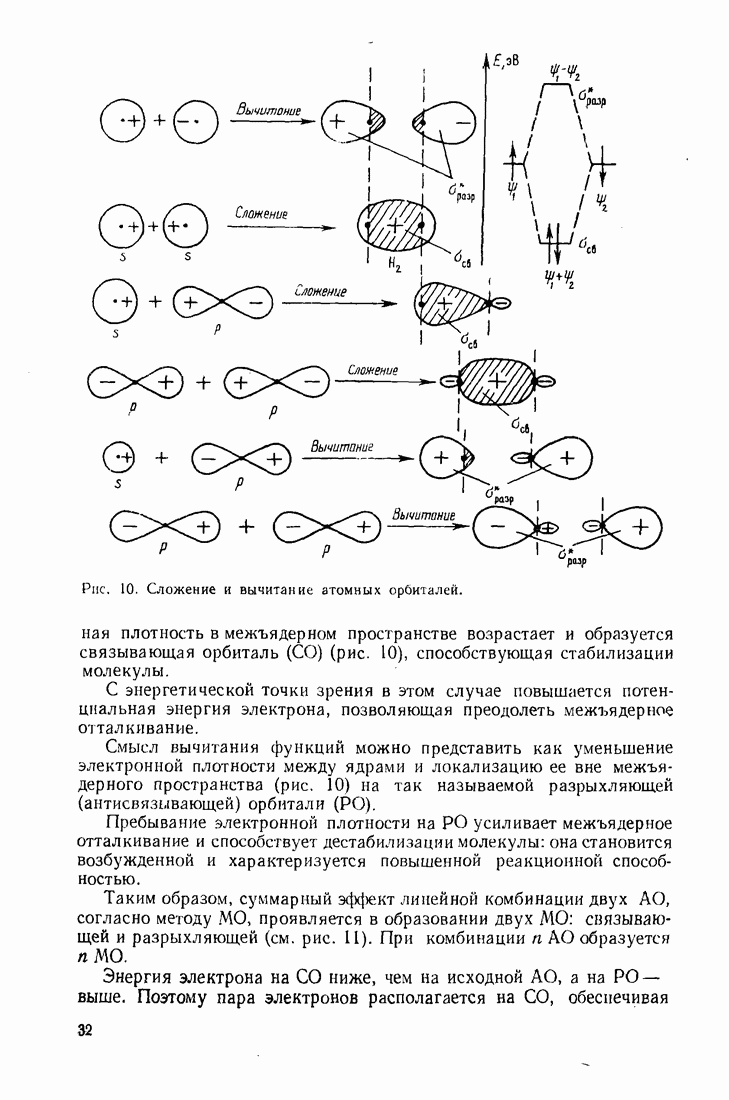
- 2.1.2. Молекулярные орбитали
- 2.2. ТИПЫ ЭЛЕКТРОННЫХ СМЕЩЕНИЙ В МОЛЕКУЛАХ
- 2.3. ОБЩИЕ ПРЕДСТАВЛЕНИЯ ОБ ОРГАНИЧЕСКОЙ РЕАКЦИИ
- 2.4. КЛАССИФИКАЦИЯ РЕАГЕНТОВ И РЕАКЦИЙ
- 2.5. КРАТКАЯ ХАРАКТЕРИСТИКА РЕАКЦИОННОЙ СПОСОБНОСТИ НЕКОТОРЫХ СОЕДИНЕНИЙ АЛИФАТИЧЕСКОГО РЯДА
- 2.5.1. Алканы (парафины)
- 2.5.2. Непредельные углеводороды
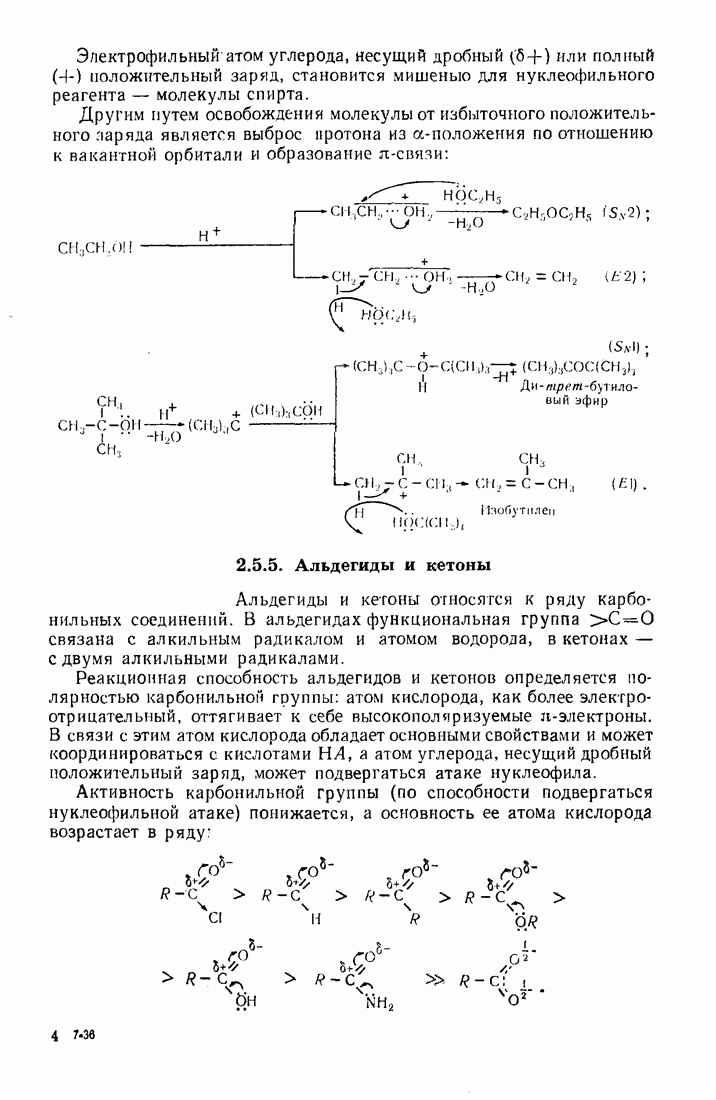
- 2.5.3. Галогеналканы (галоидные алкилы R-Hal)
- 2.5.4. Спирты (R0Н)
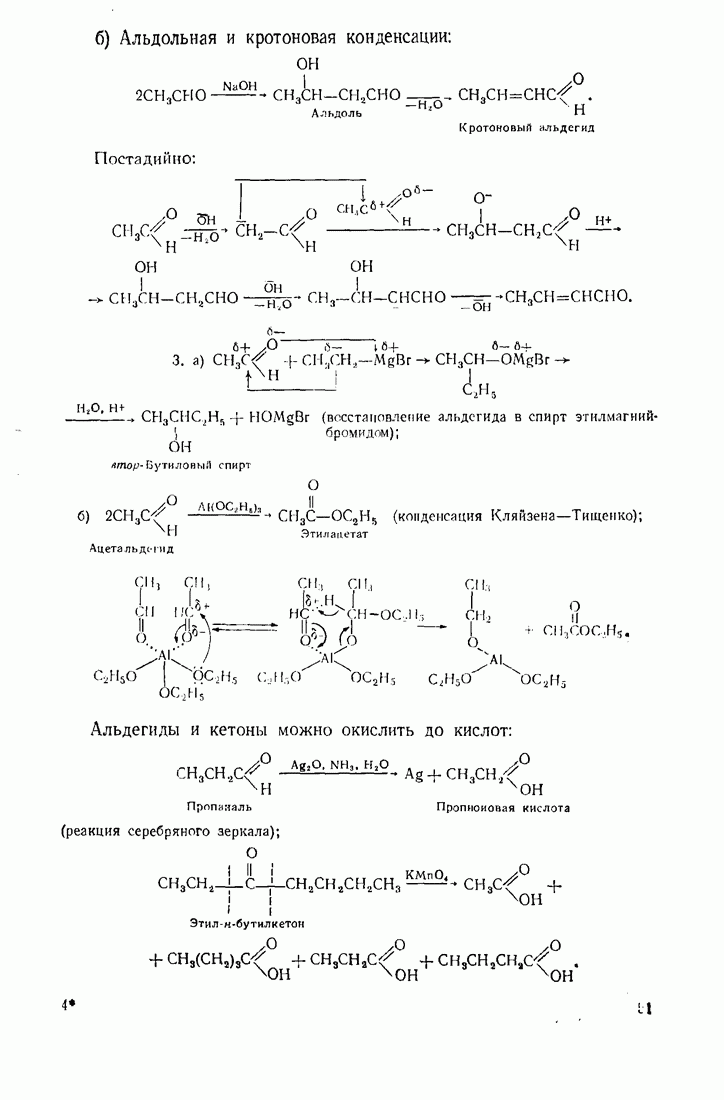
- 2.5.5. Альдегиды и кетоны
- 2.5.6. Карбоновые кислоты (R-СООН) и их производные (R-СО-X)
- 2.5.7. Амины (NH2R, NHR2, NR3)
- 3. Реакционная способность соединений алифатического ряда
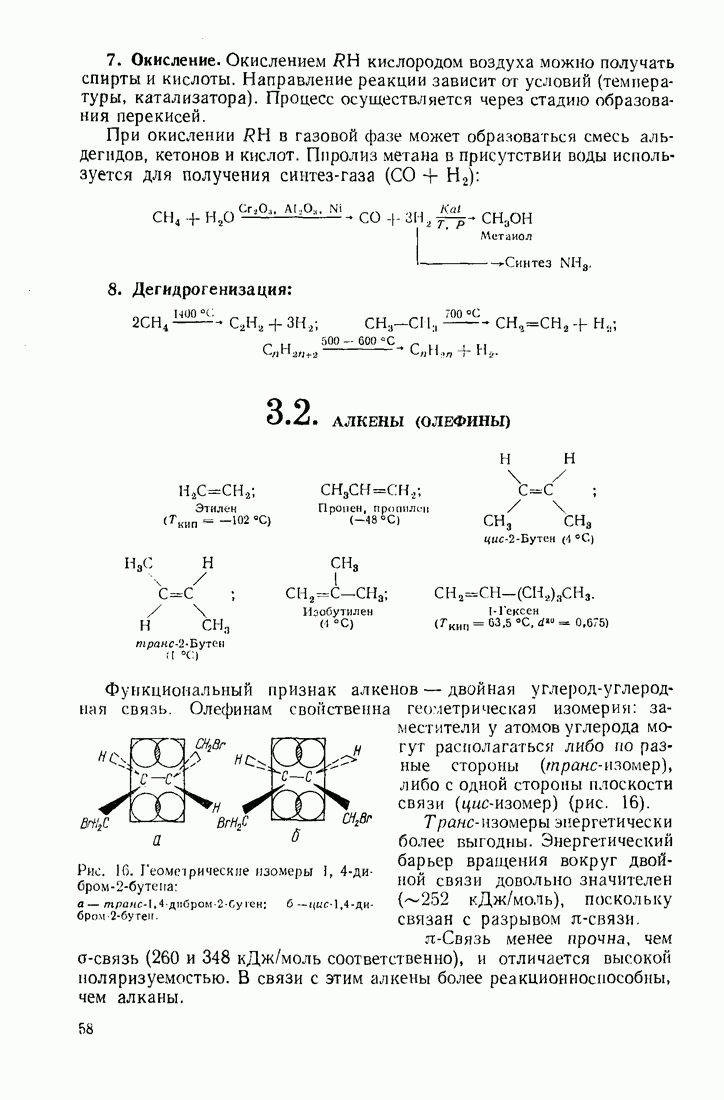
- 3.1. Алканы (насыщенные углеводороды)
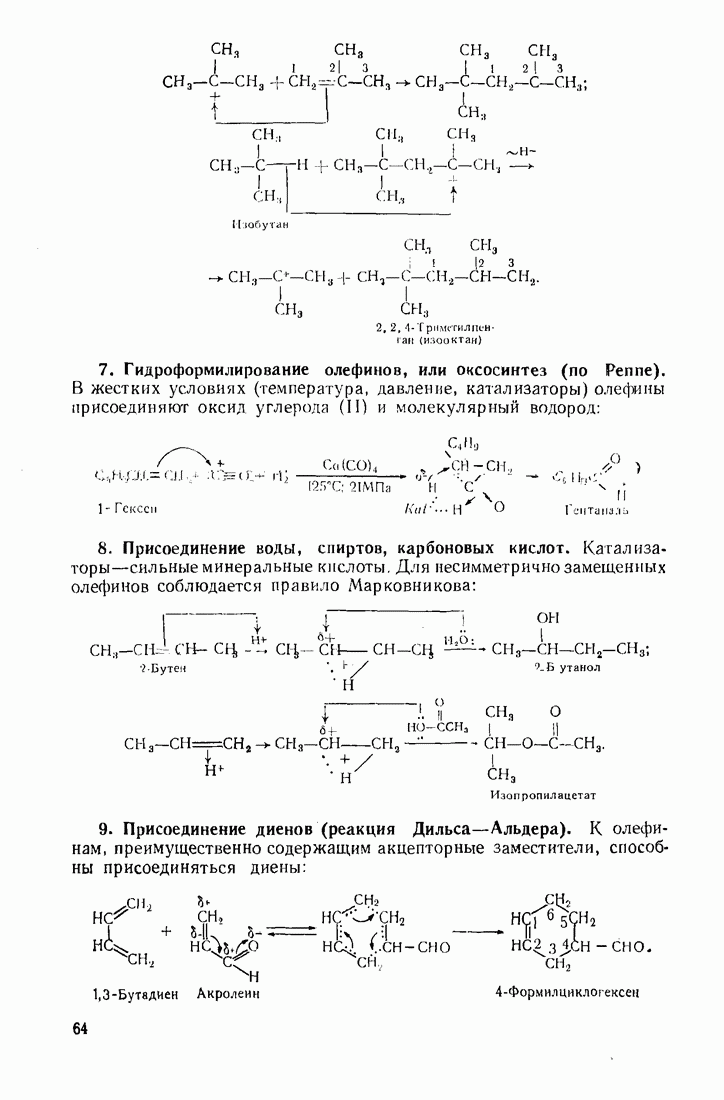
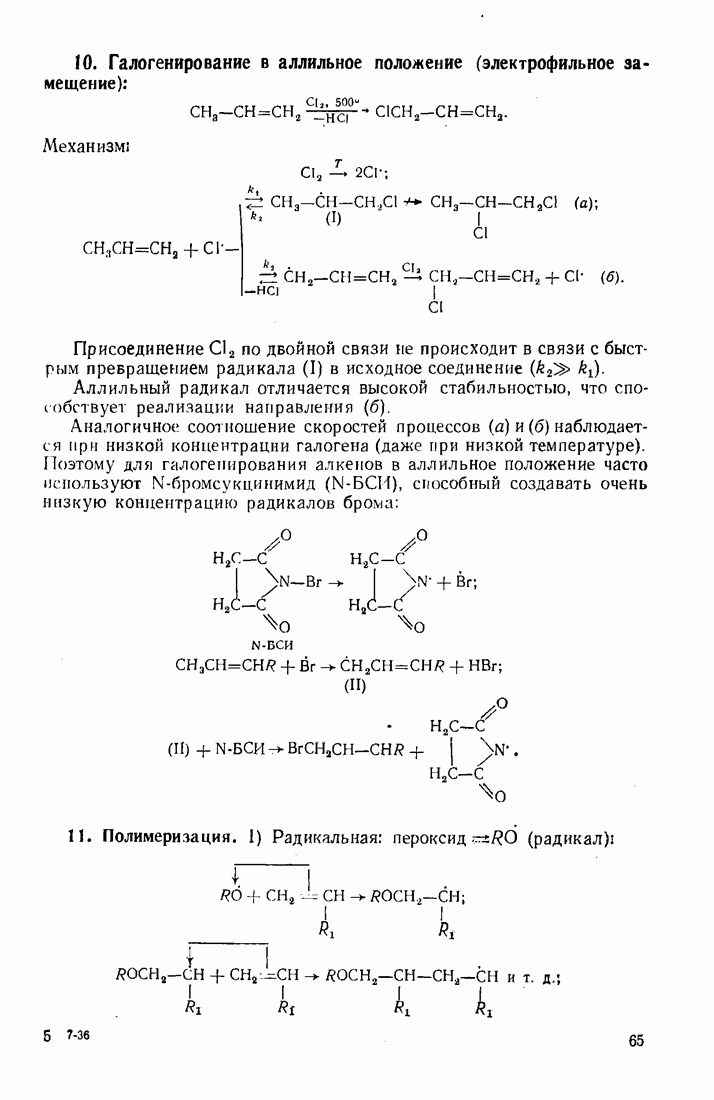
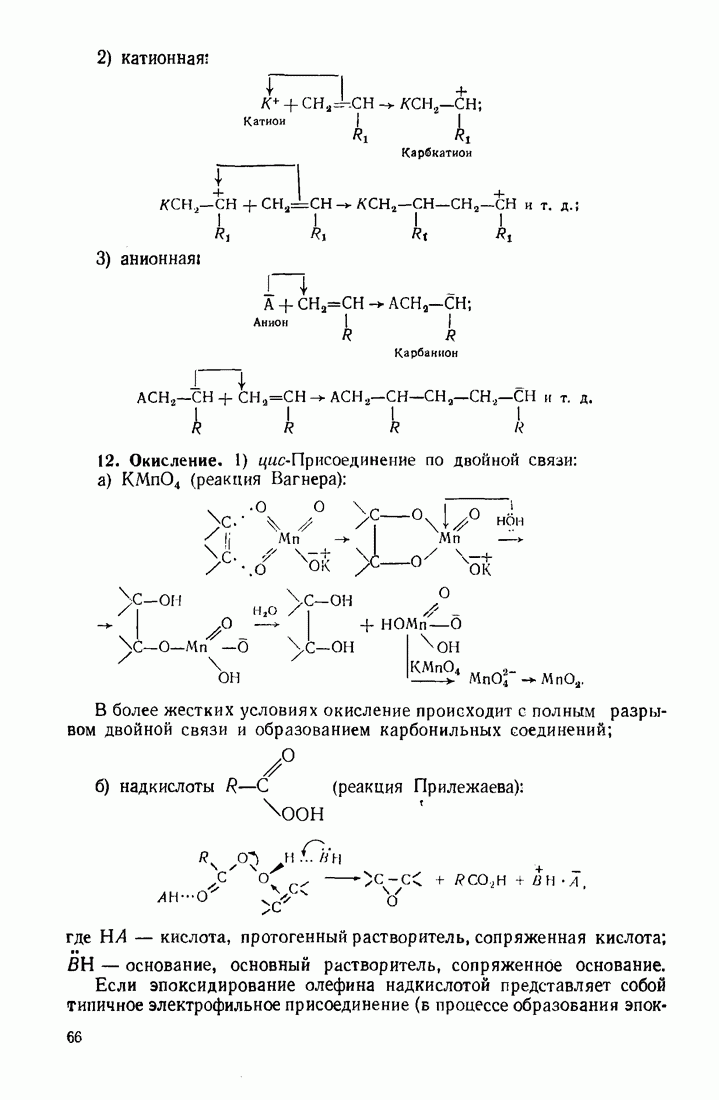
- 3.2. АЛКЕНЫ (ОЛЕФИНЫ)
- 3.3. ДИЕНОВЫЕ УГЛЕВОДОРОДЫ
- 3.4. АЦЕТИЛЕНЫ
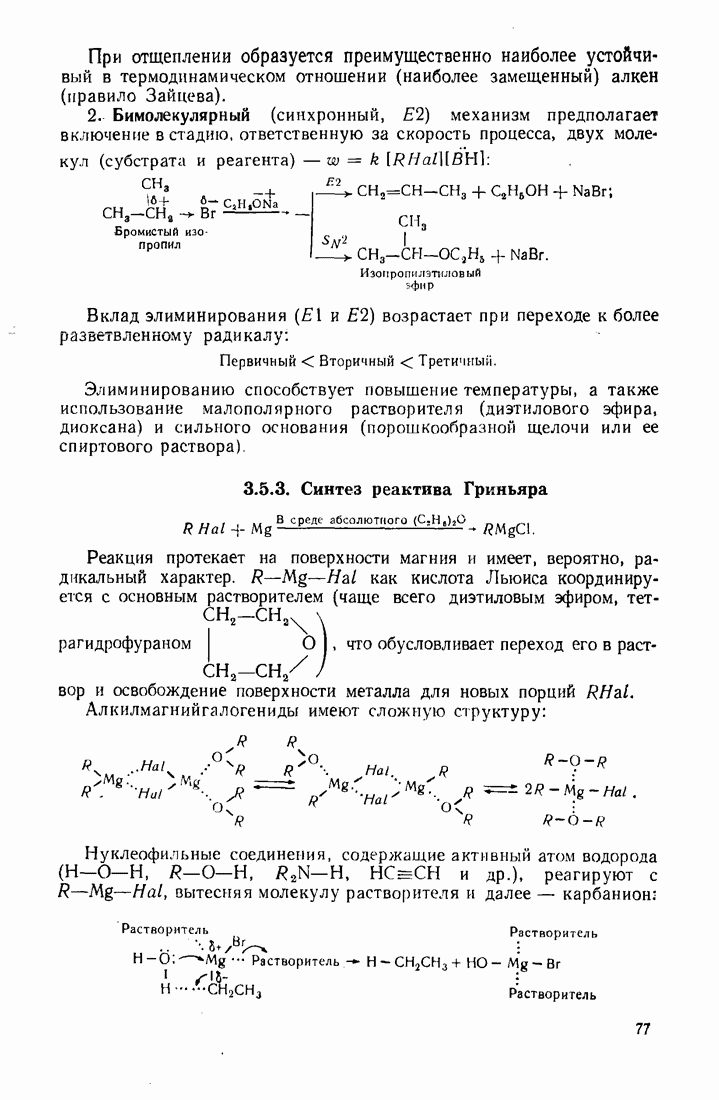
- 3.5. ГАЛОГЕНАЛКАНЫ (ГАЛОИДНЫЕ АЛКИЛЫ)
- 3.6. СПИРТЫ
- 3.7. ПРОСТЫЕ ЭФИРЫ (R-O-R)
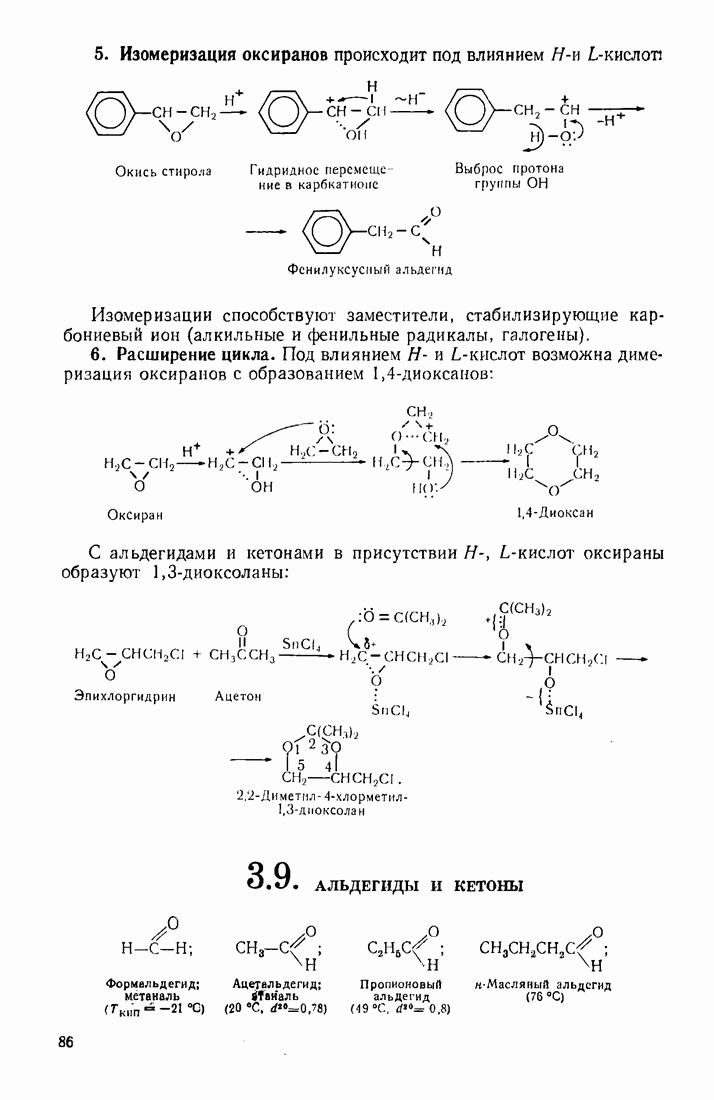
- 3.8. ОКСИРАНЫ (ЭПОКСИДНЫЕ СОЕДИНЕНИЯ, a-ОКИСИ)
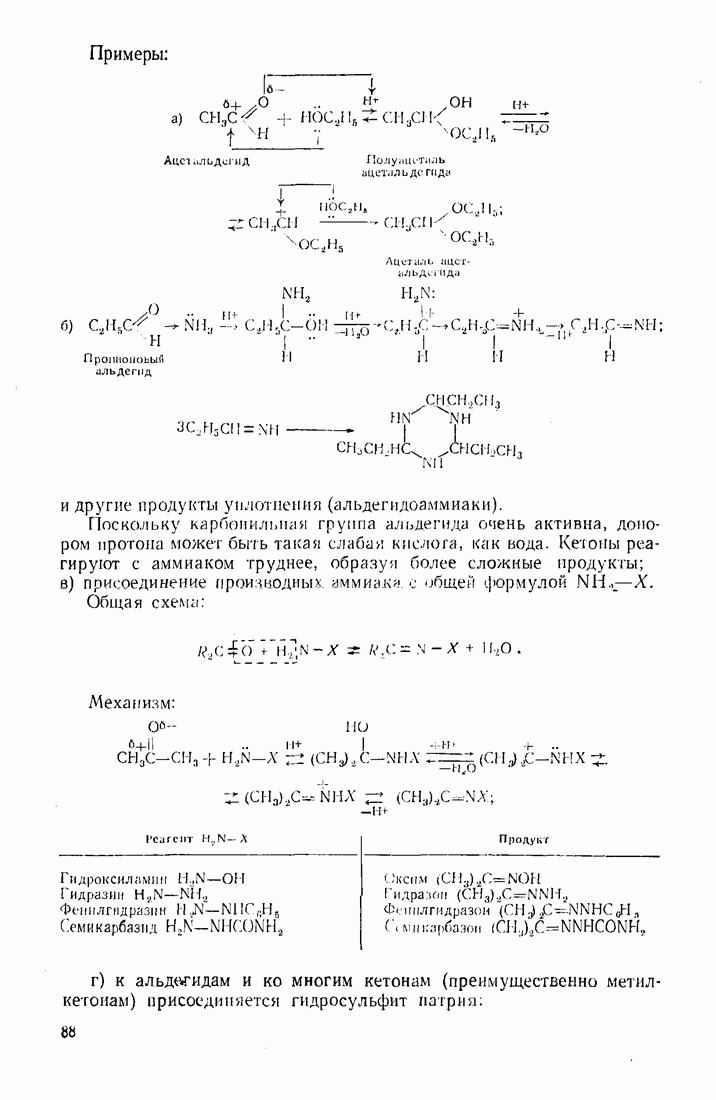
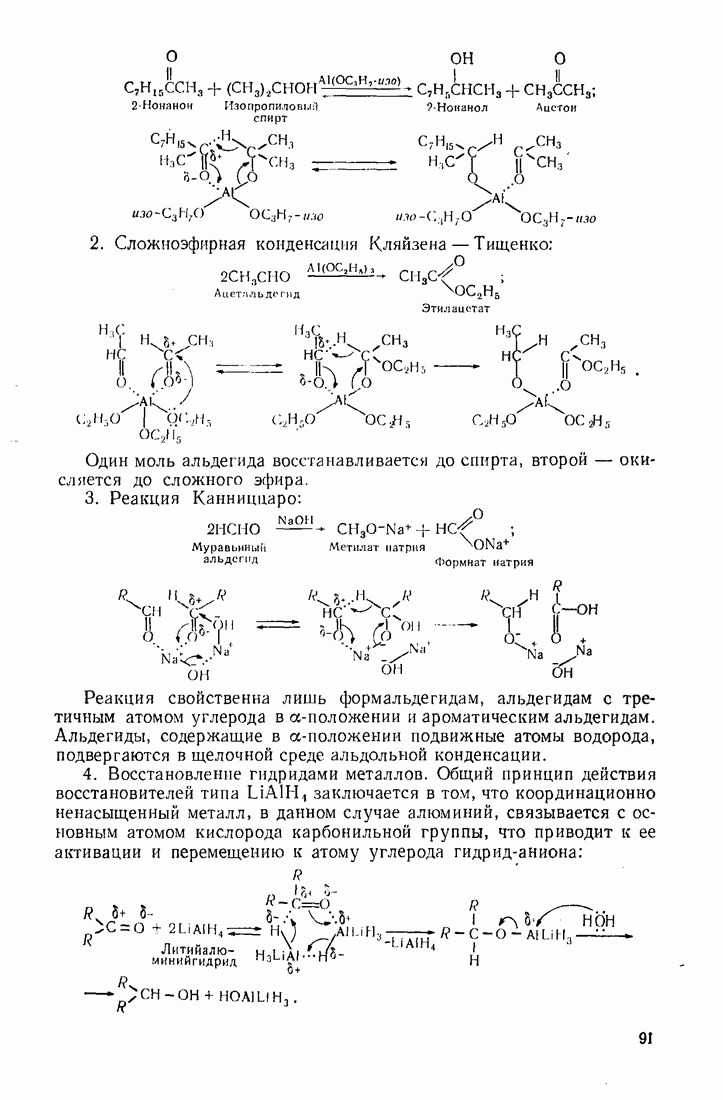
- 3.9. АЛЬДЕГИДЫ И КЕТОНЫ
- 3.10. КАРБОНОВЫЕ КИСЛОТЫ
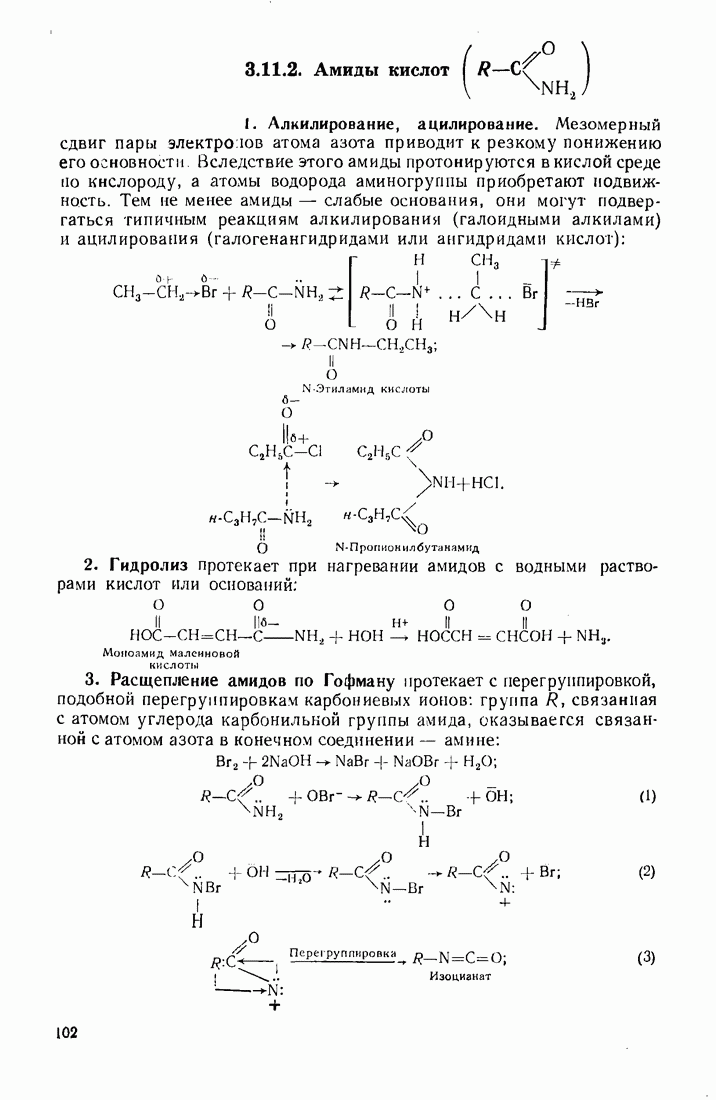
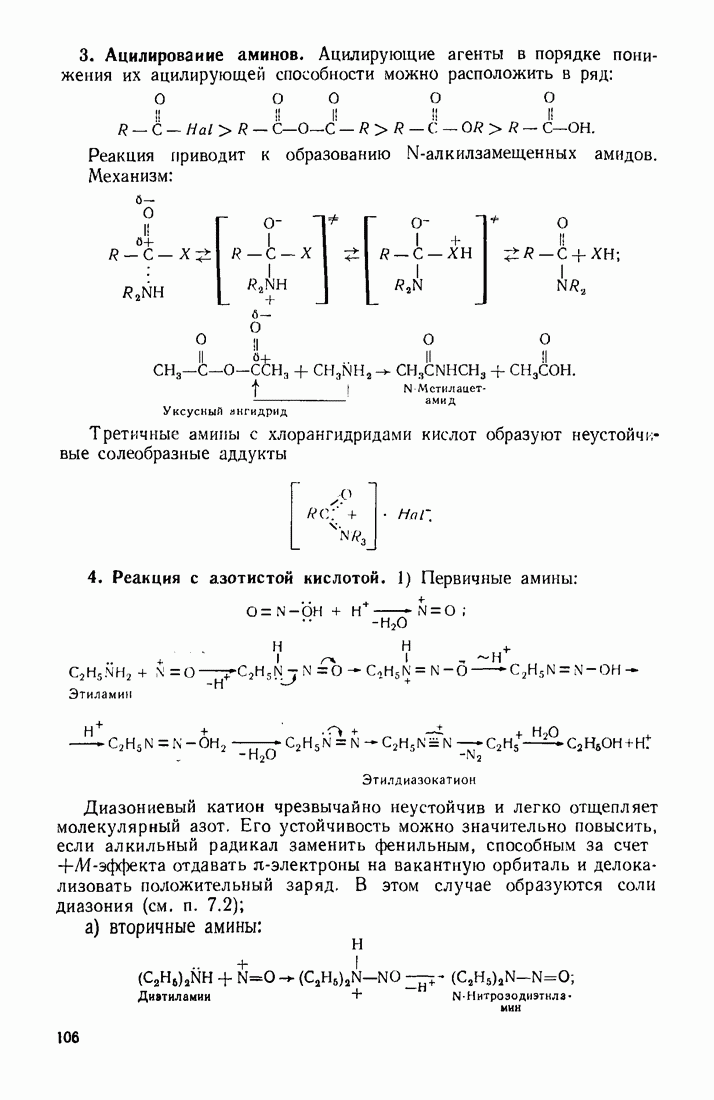
- 3.11. НЕКОТОРЫЕ ПРОИЗВОДНЫЕ КИСЛОТ
- 3.12. АМИНЫ
- 3.13. ФОСФОРОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- 3.14. СЕРООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
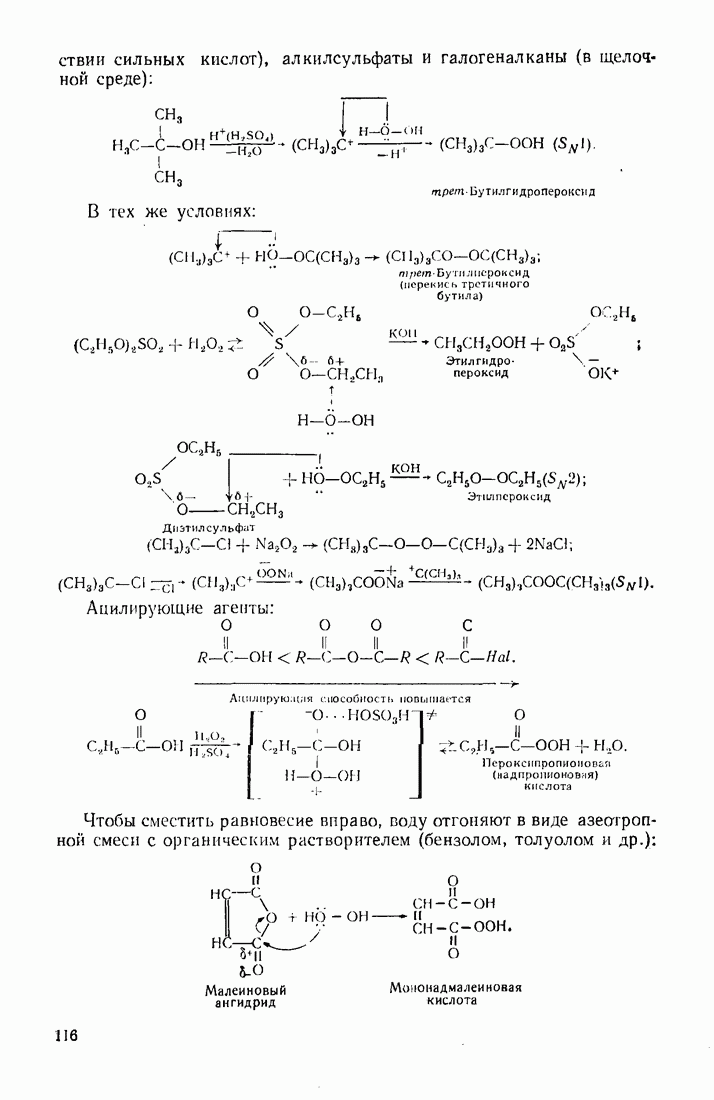
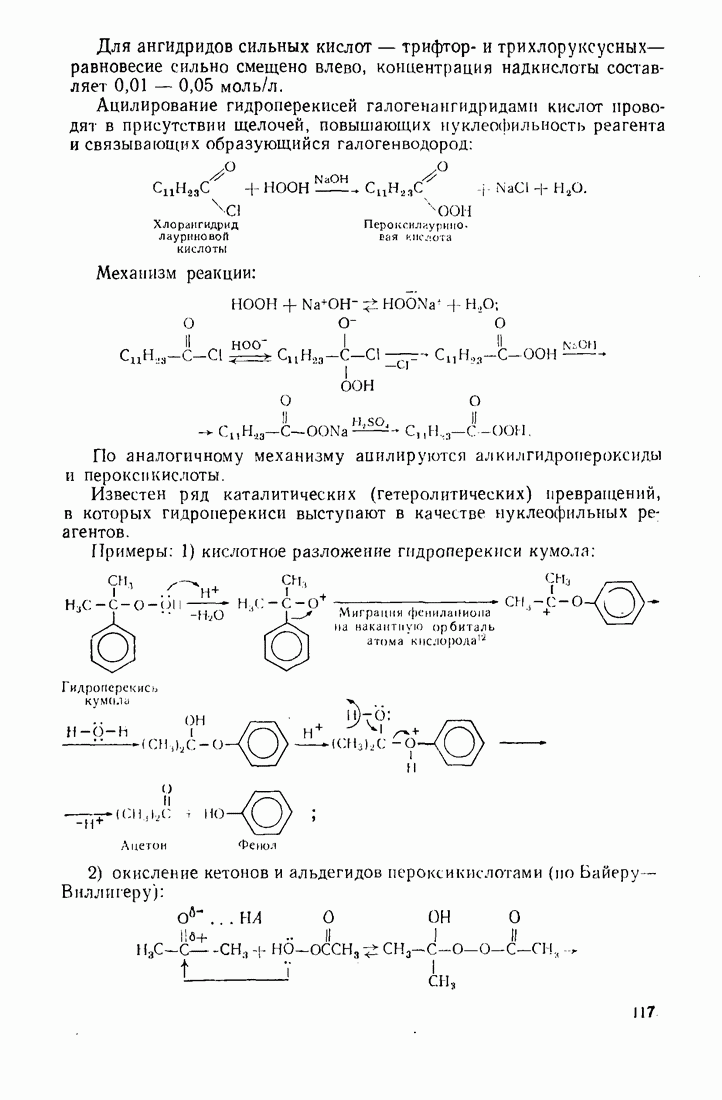
- 3.15. ОРГАНИЧЕСКИЕ ПЕРЕКИСИ (ПЕРОКСИДНЫЕ СОЕДИНЕНИЯ)
- 3.16. ПРОИЗВОДНЫЕ УГОЛЬНОЙ КИСЛОТЫ
- 3.17. ГЕТЕРОАНАЛОГИ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ
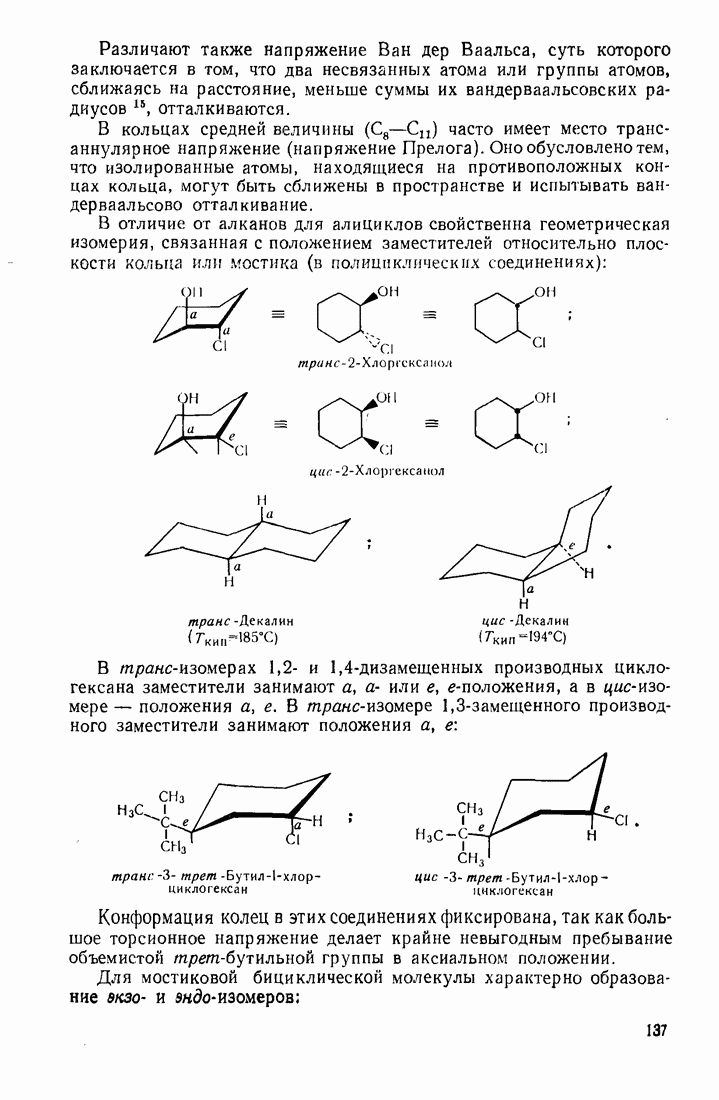
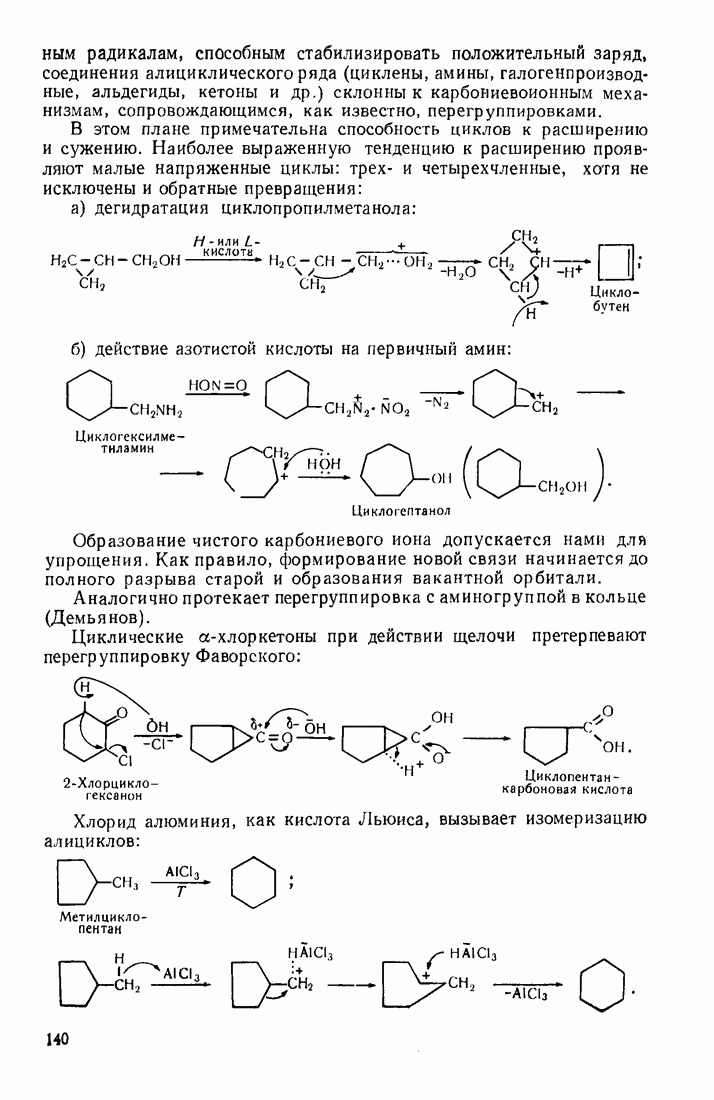
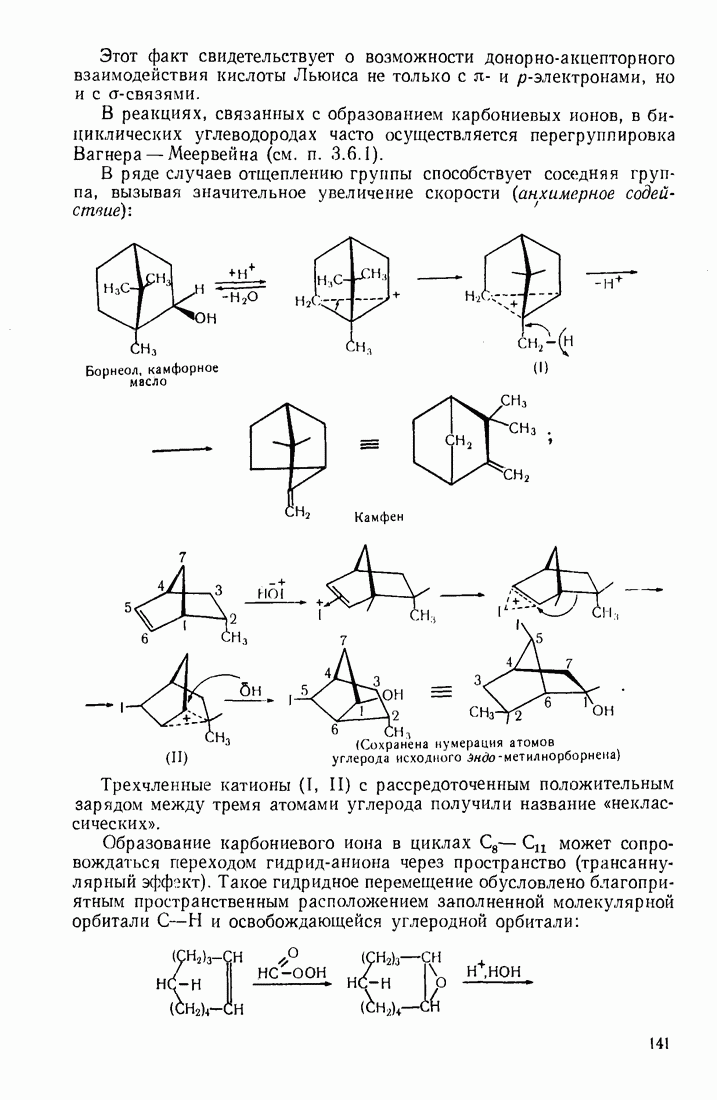
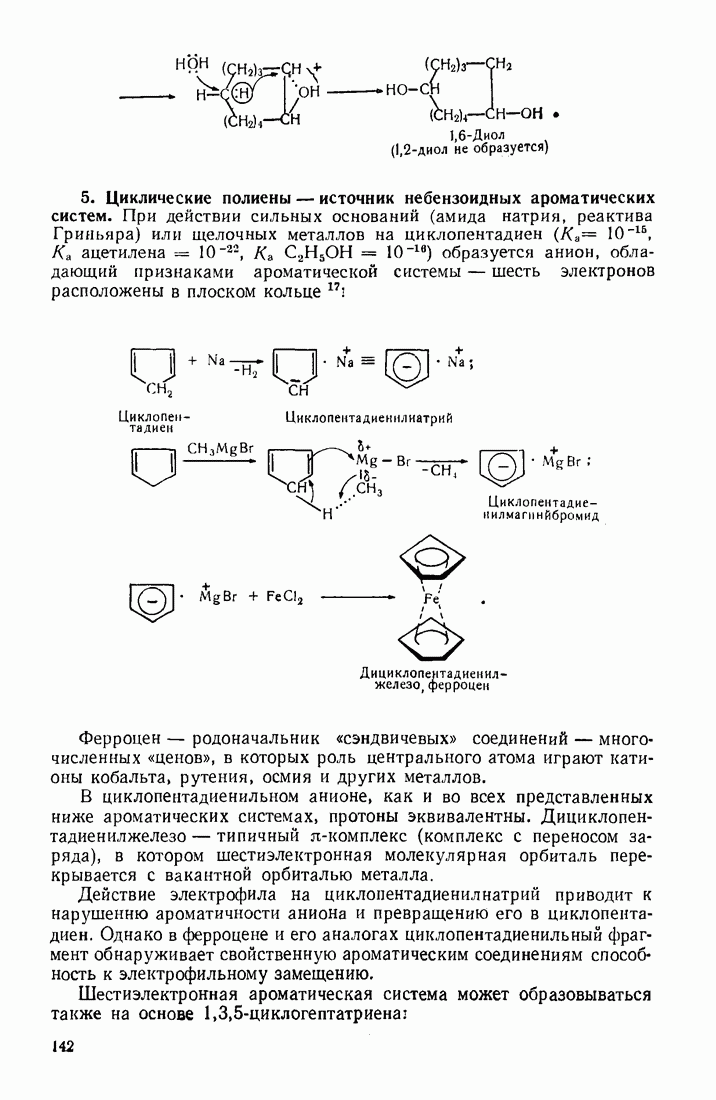
- 3.18. АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- 3.18.2. Пространственное расположение и напряженность циклов
- 3.18.3. Особенности химических свойств алициклических соединений
- 4. Полифункциональные производные алифатического ряда
- 4.1. ДВУХОСНОВНЫЕ КАРБОНОВЫЕ КИСЛОТЫ
- 4.2. НЕПРЕДЕЛЬНЫЕ КИСЛОТЫ
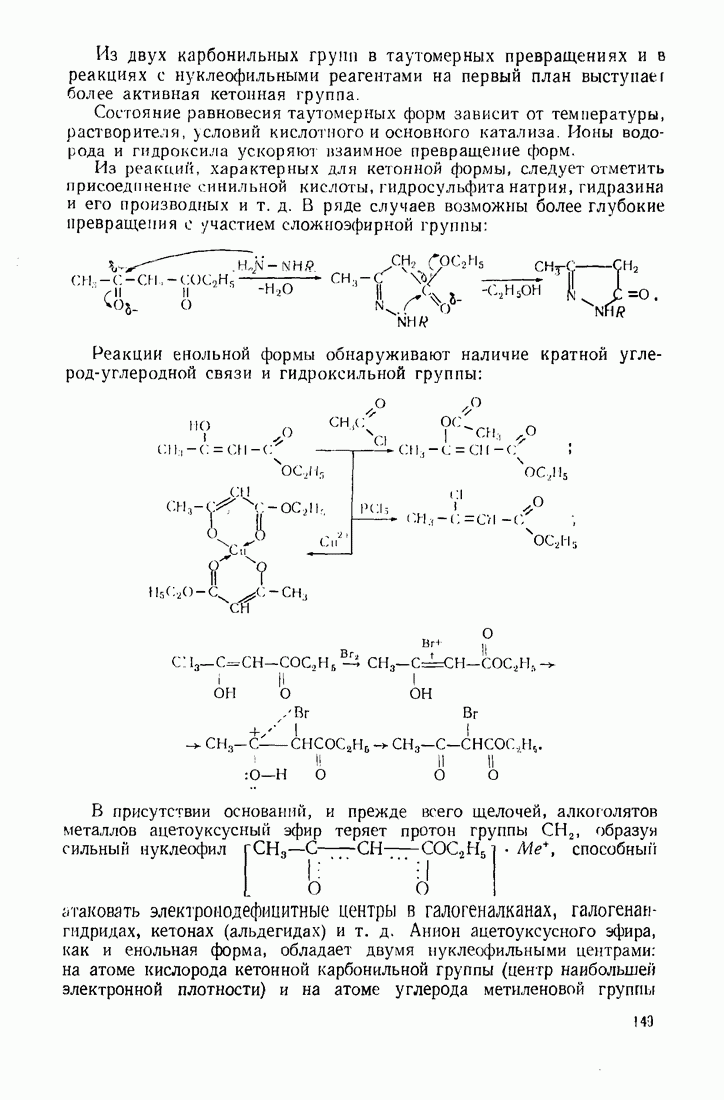
- 4.3. ОКСОКИСЛОТЫ (АЛЬДЕГИДО- И КЕТОКИСЛОТЫ)
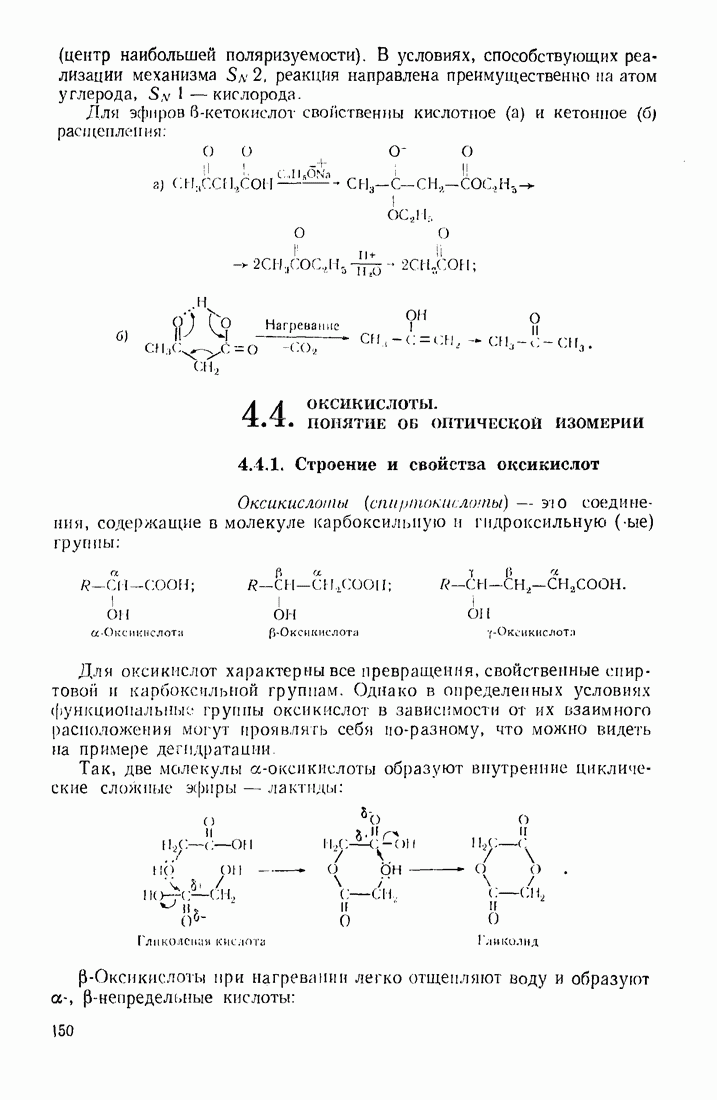
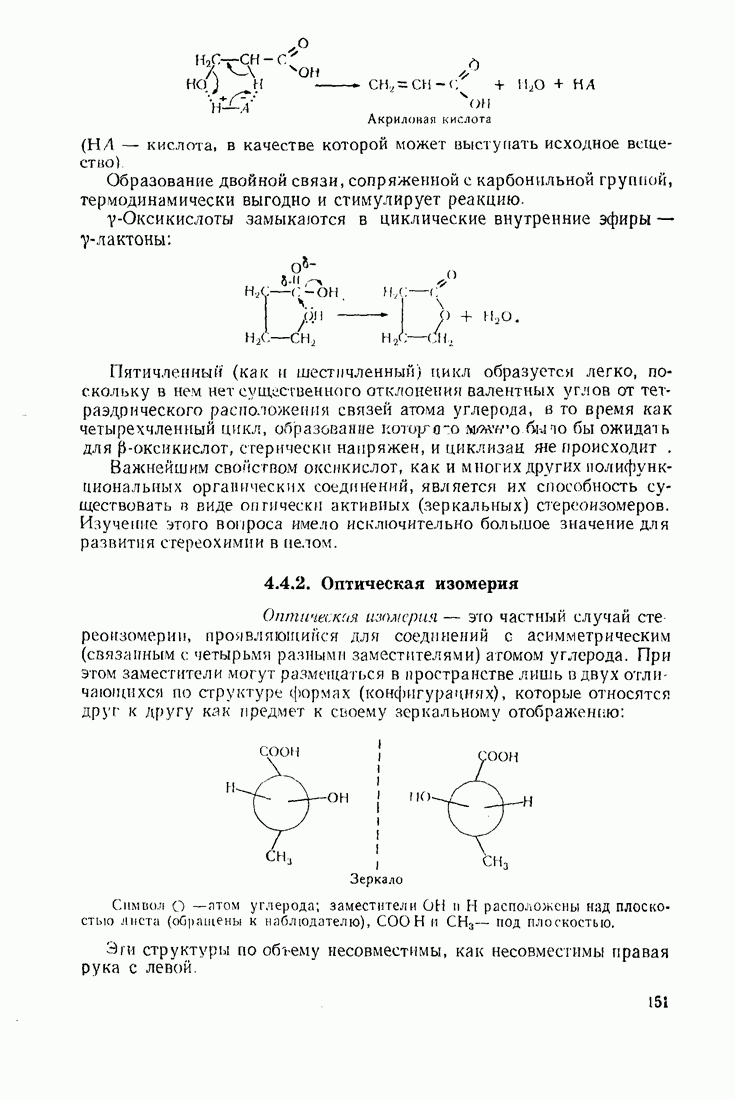
- 4.4. ОКСИКИСЛОТЫ. ПОНЯТИЕ ОБ ОПТИЧЕСКОЙ ИЗОМЕРИИ
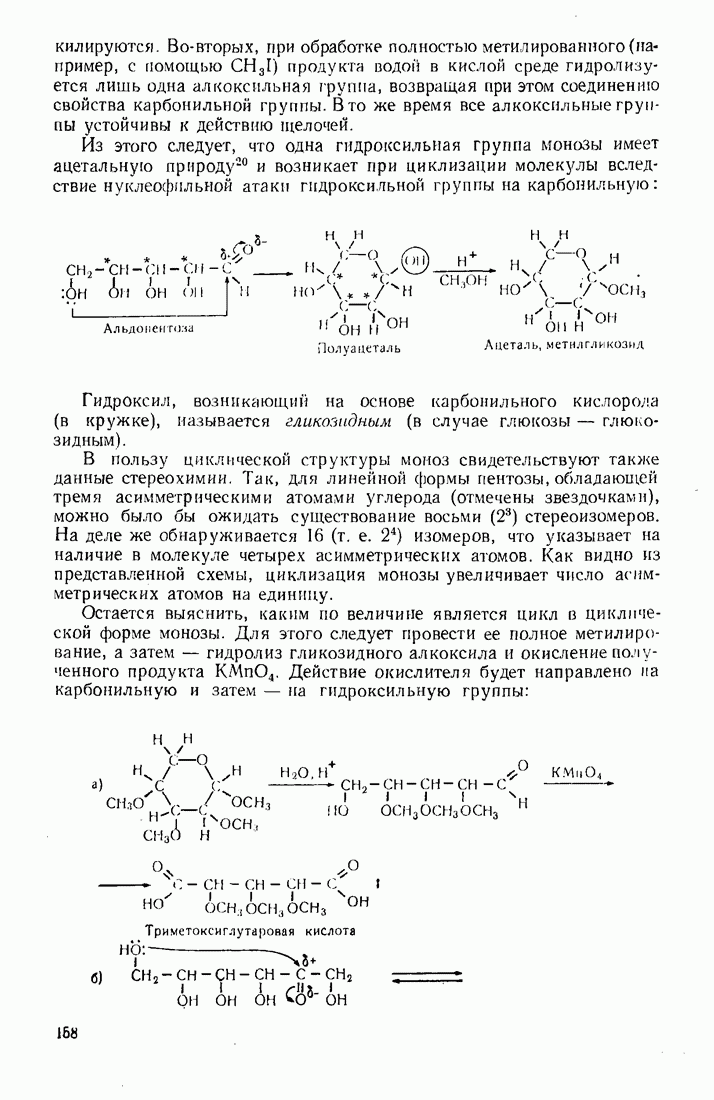
- 4.5. УГЛЕВОДЫ
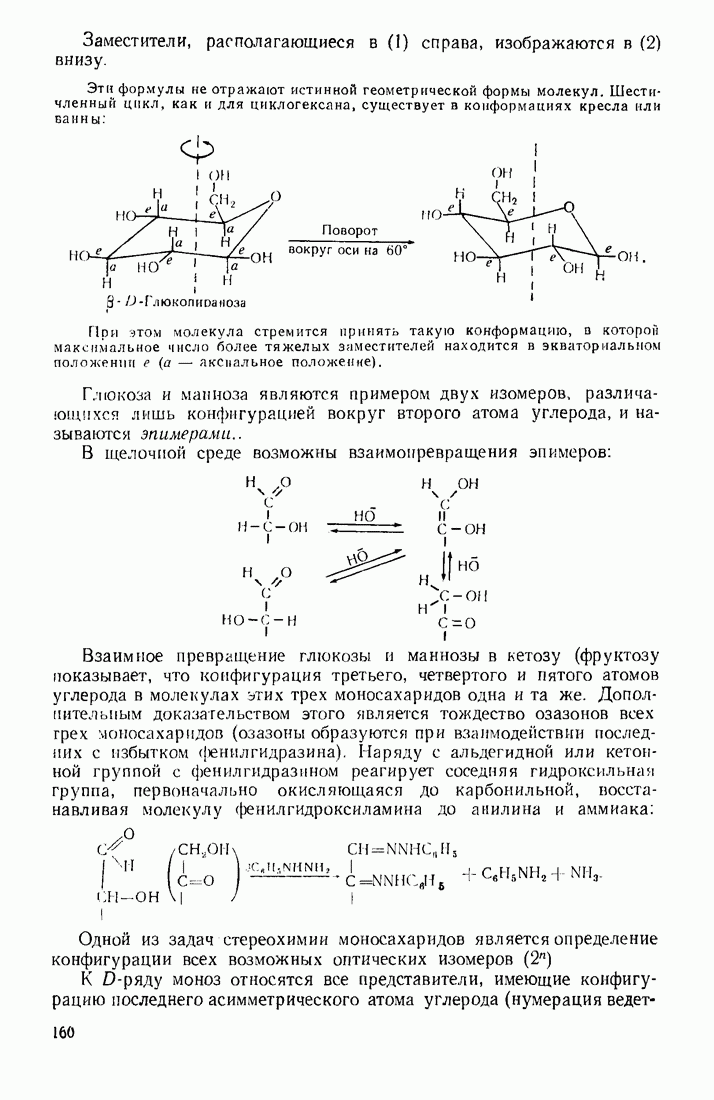
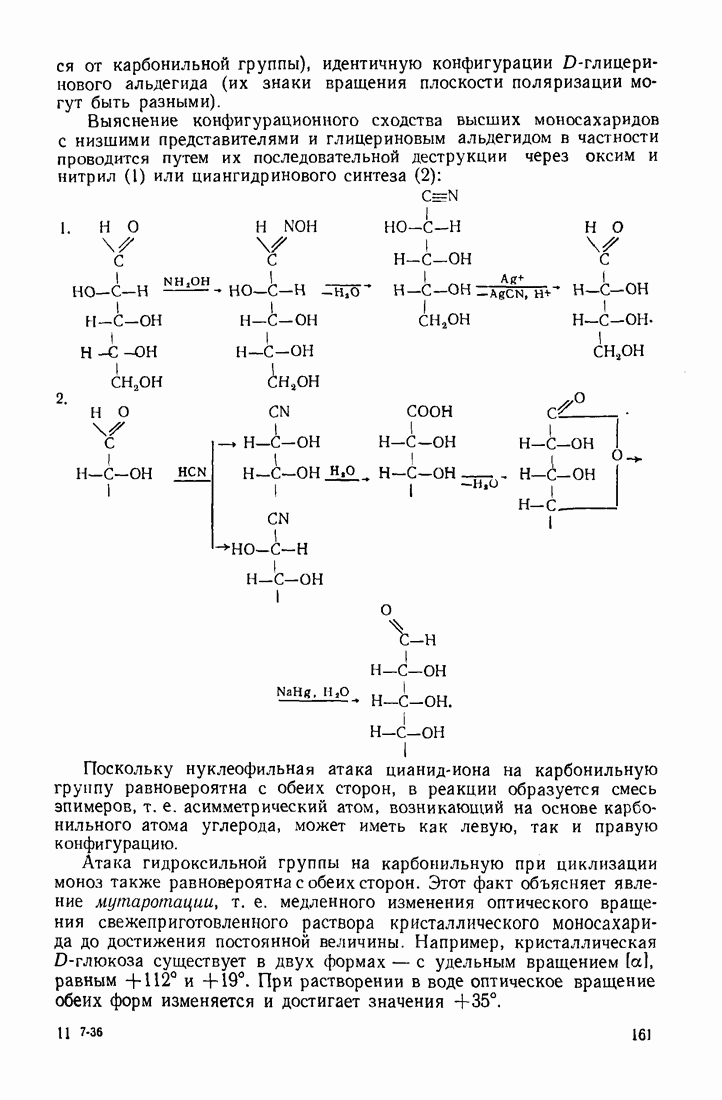
- 4.5.2. Стереохимия моносахаридов
- 4.5.3. Дисахариды
- 4.5.4. Полисахариды
- 4.5.5. Нахождение в природе и пути превращения углеводов
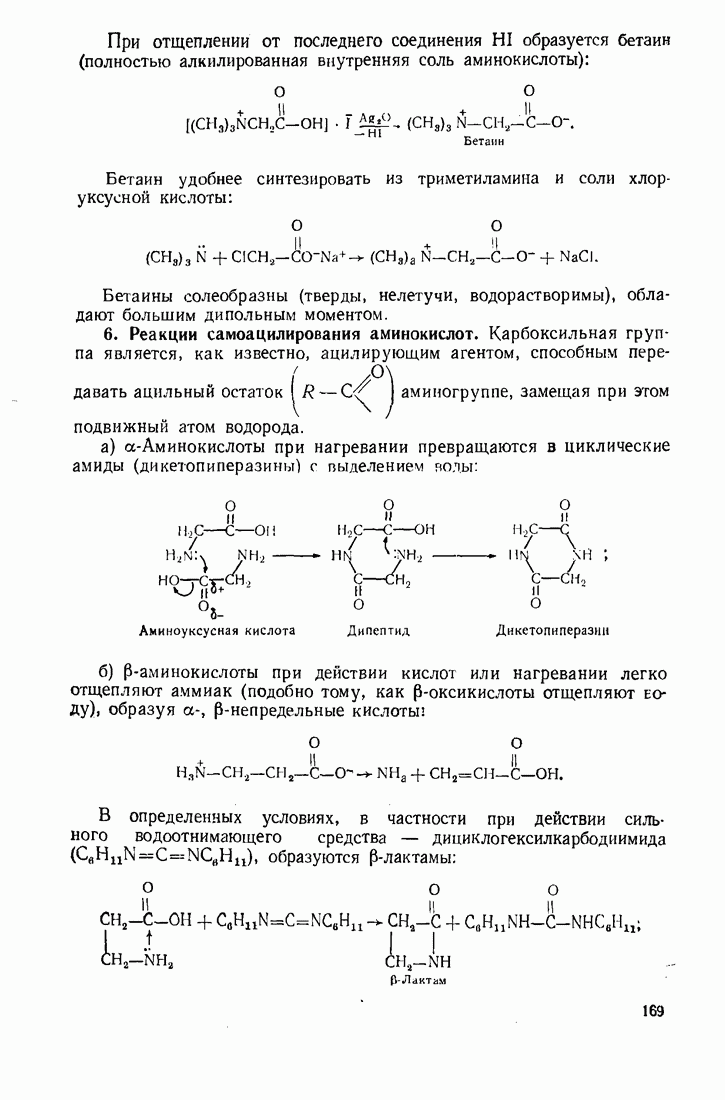
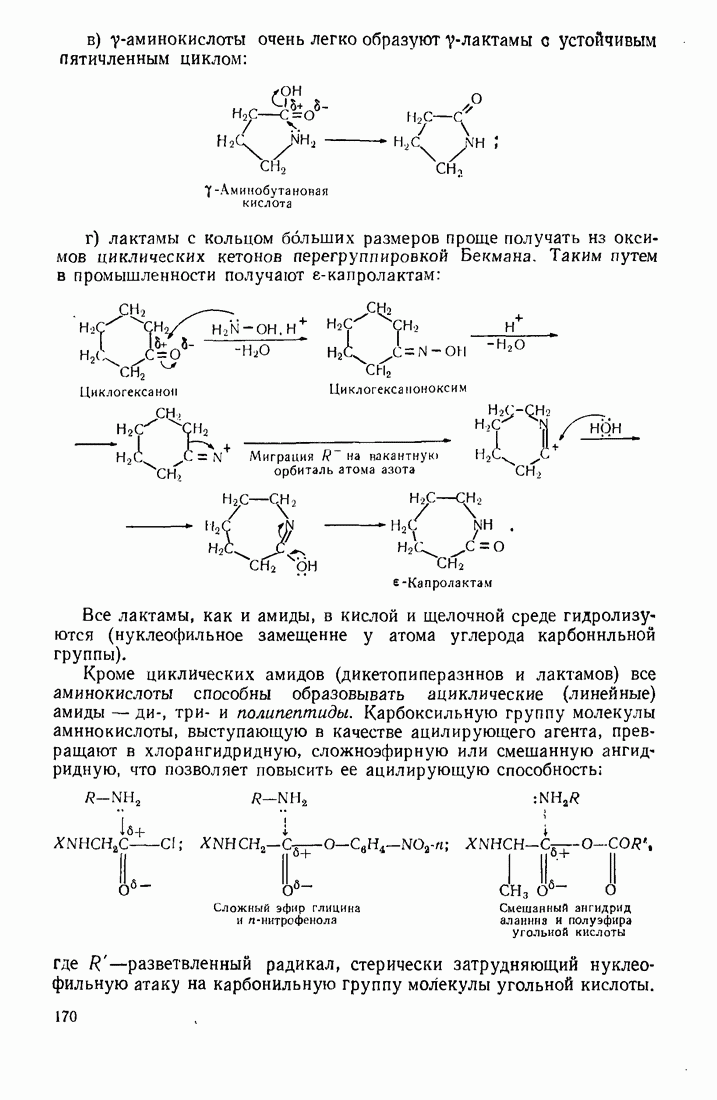
- 4.6. АМИНОКИСЛОТЫ
- 5. Методы синтеза органических юединений алифатическою рада
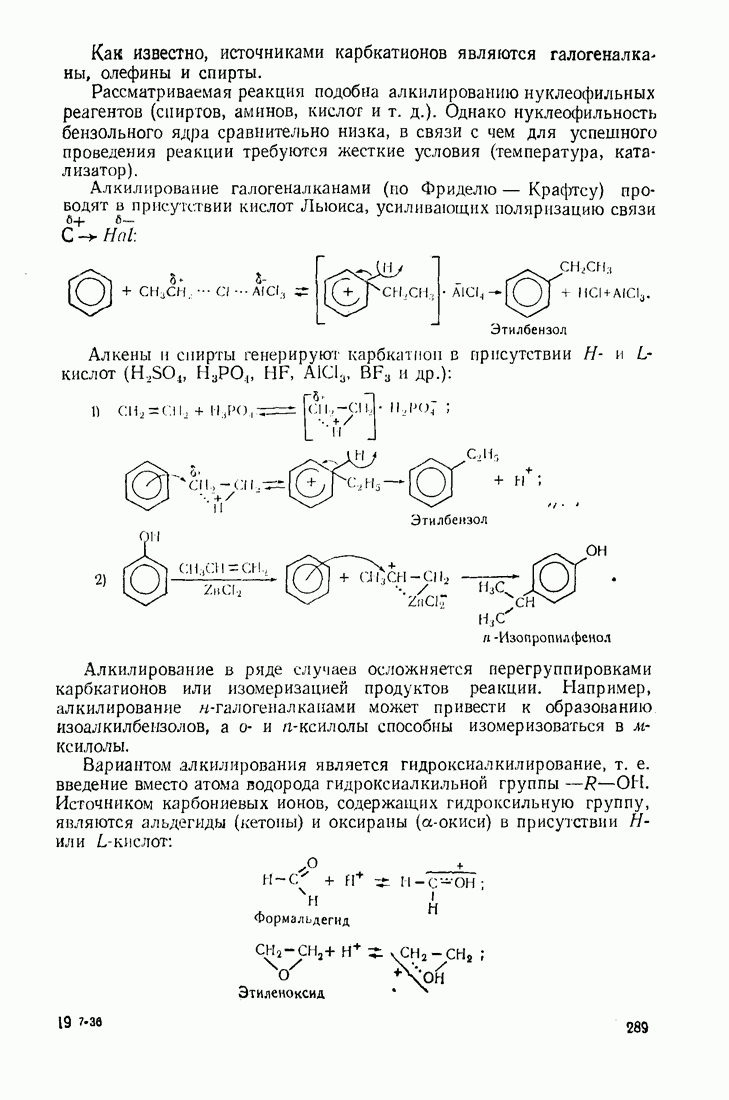
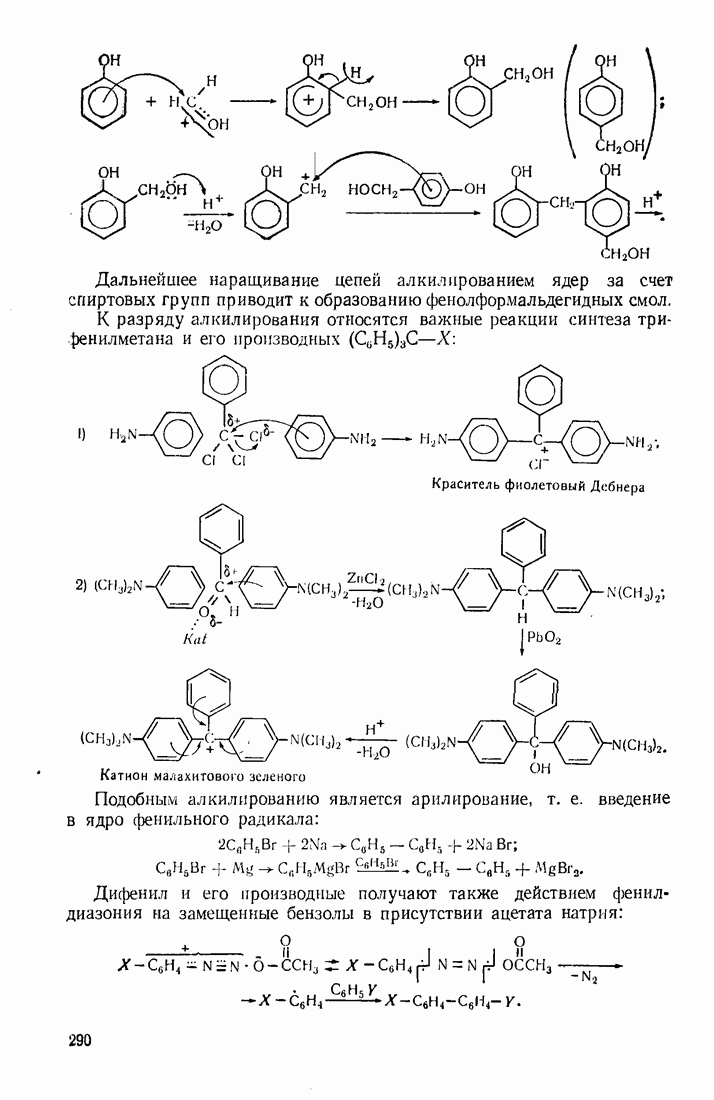
- 5.1. АЛКИЛИРОВАНИЕ
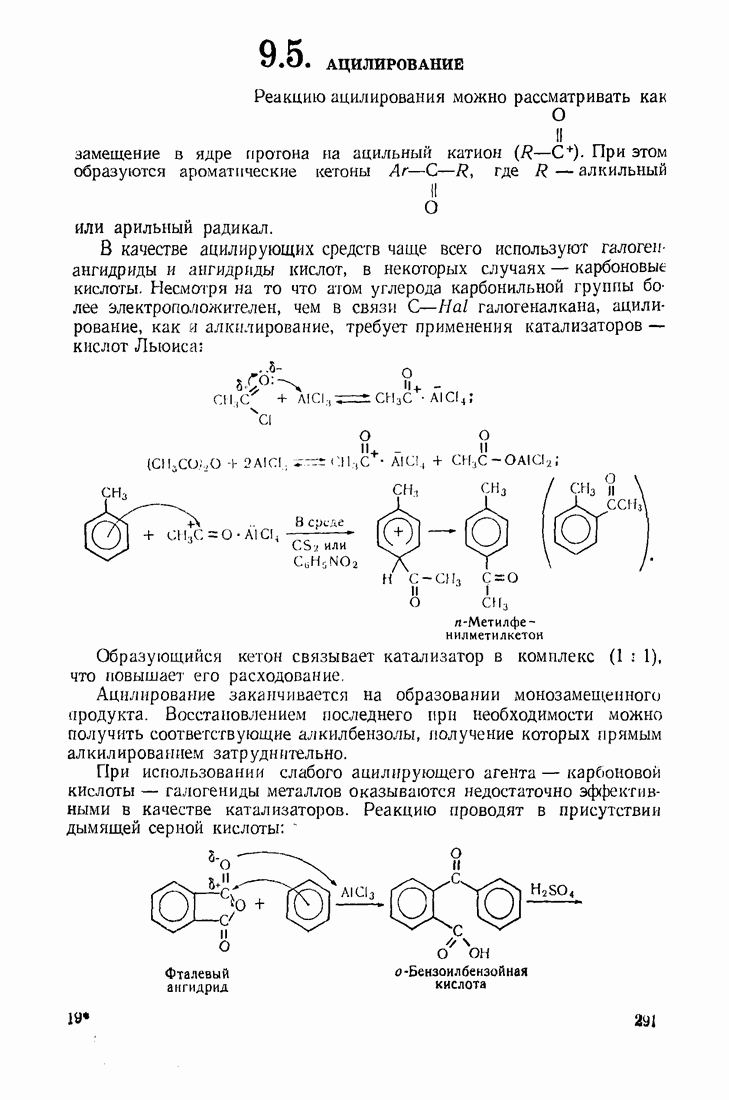
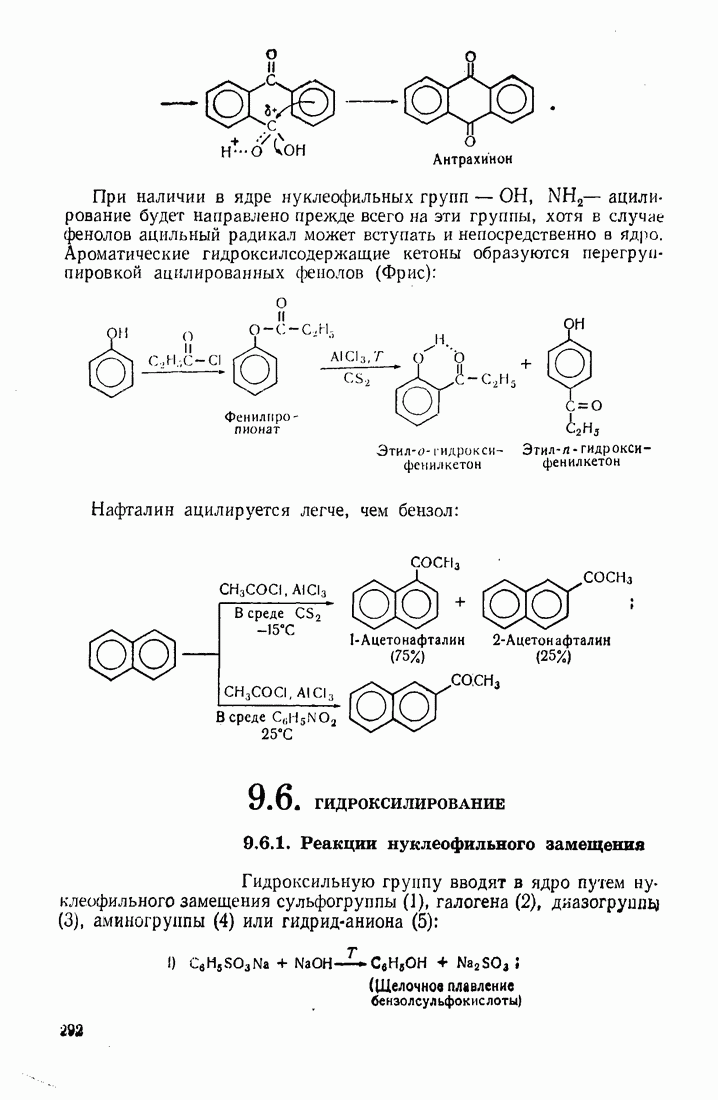
- 5.2. АЦИЛИРОВАНИЕ
- 5.3. ГАЛОГЕНИРОВАНИЕ
- 5.4. ГИДРОКСИЛИРОВАНИЕ
- 5.5. КАРБОНИЛИРОВАНИЕ (ВВЕДЕНИЕ КАРБОНИЛЬНОЙ ГРУППЫ)
- 5.6. КАРБОКСИЛИРОВАНИЕ
- 5.7. ЭПОКСИДИРОВАНИЕ (ОКСИРАНИРОВАИИЕ)
- 5.8. АМИНИРОВАНИЕ
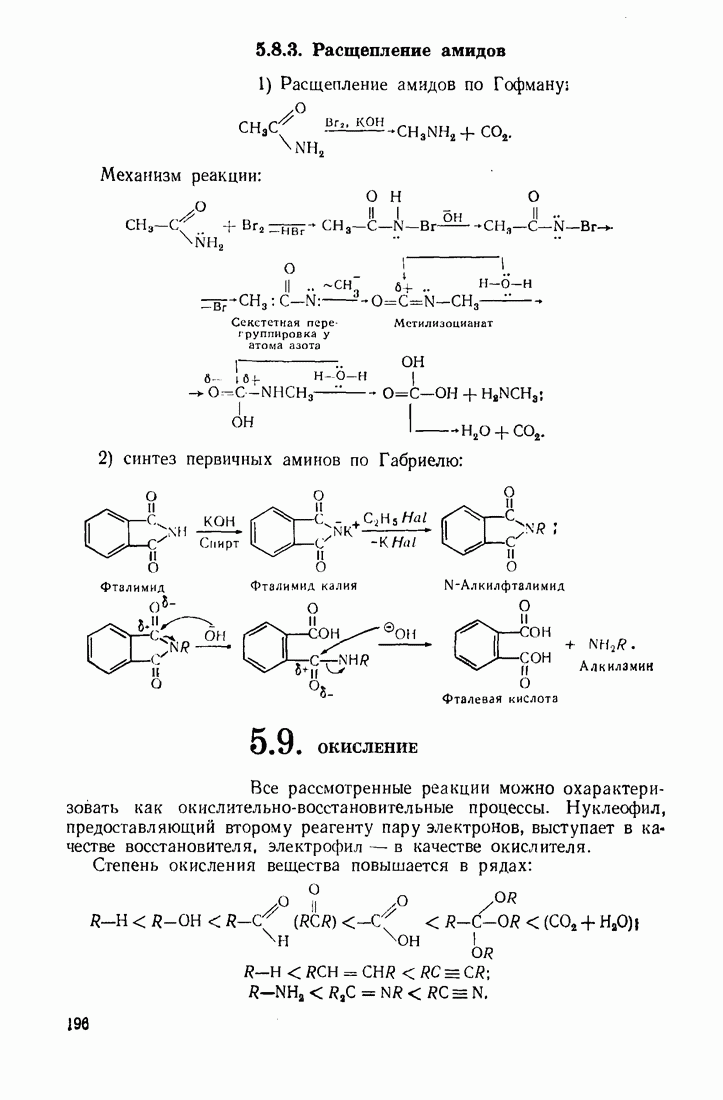
- 5.9. ОКИСЛЕНИЕ
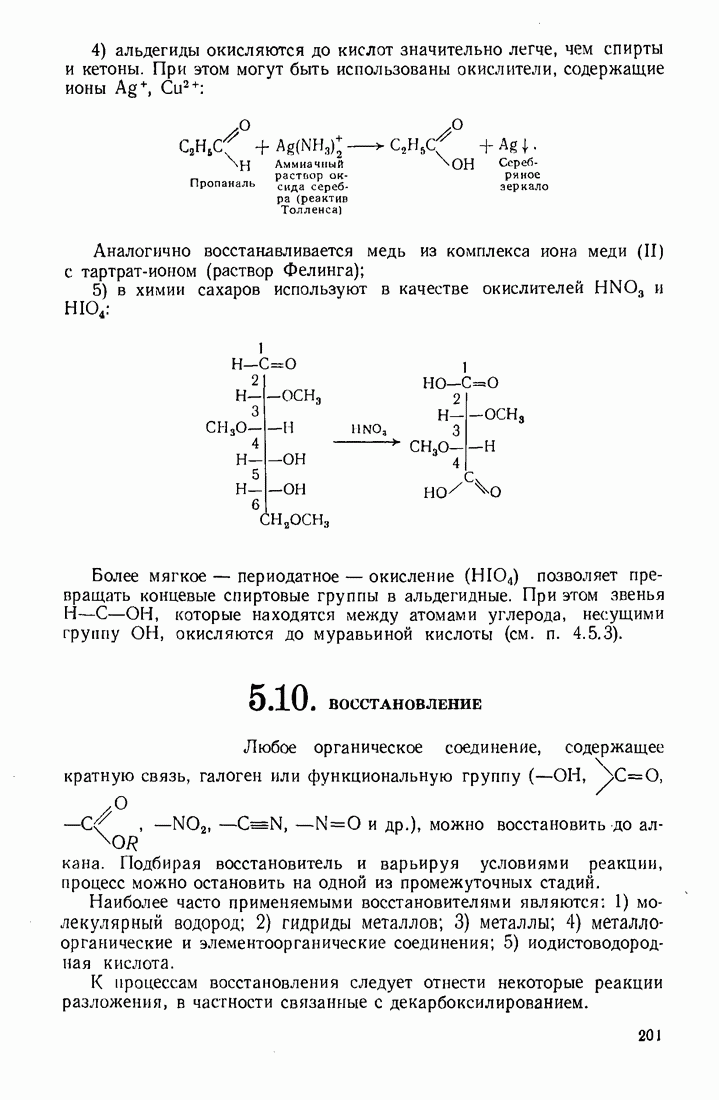
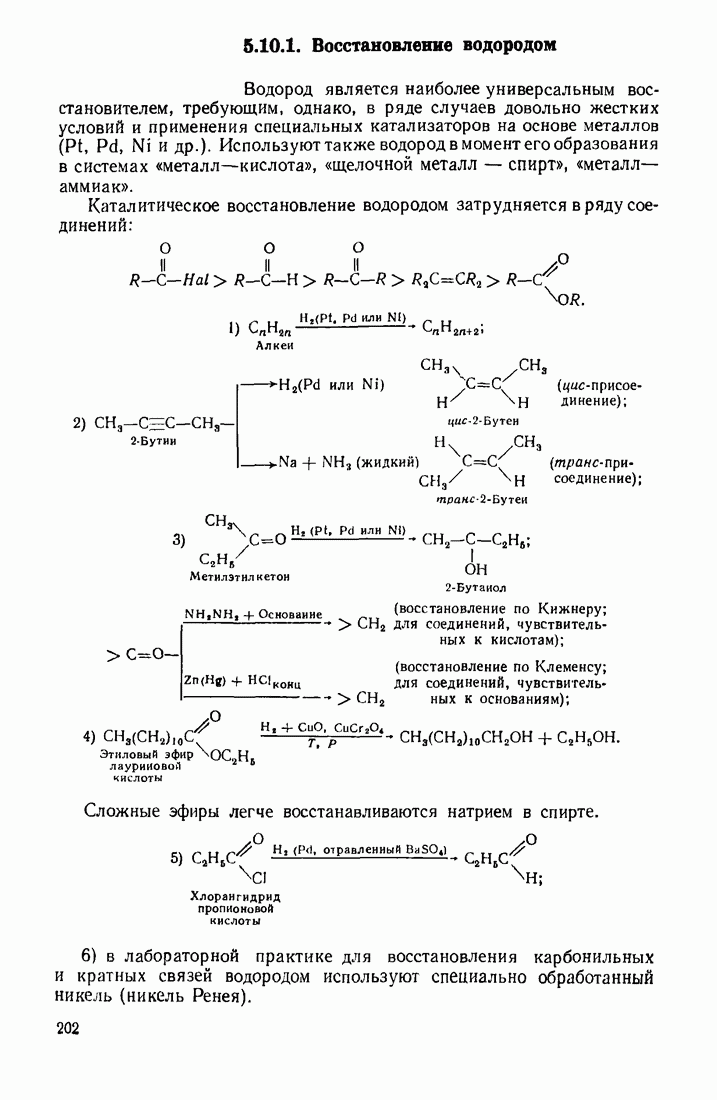
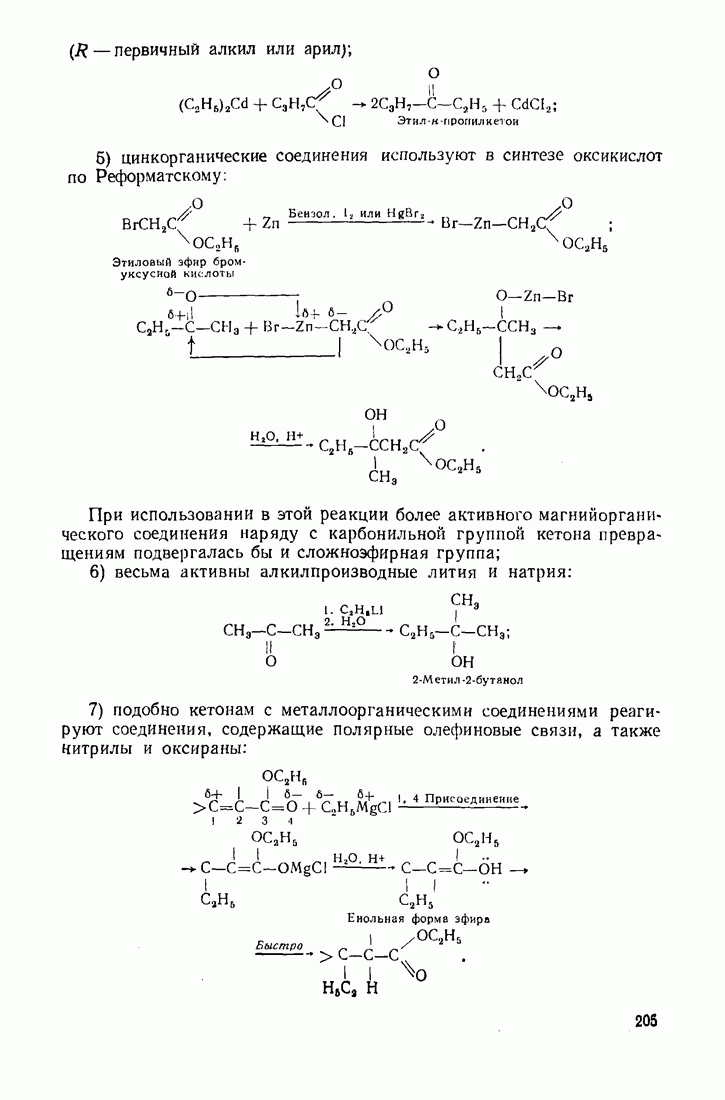
- 5.10. ВОССТАНОВЛЕНИЕ
- 5.11. АЛКАНЫ
- 5.12 АЛКЕНЫ
- 5.13. ДИЕНОВЫЕ УГЛЕВОДОРОДЫ (1,3-ДИЕНЫ)
- 5.14. АЦЕТИЛЕНЫ
- 5.15 АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- 5.16. ГАЛОГЕН АЛКАНЫ
- 5.17. СПИРТЫ
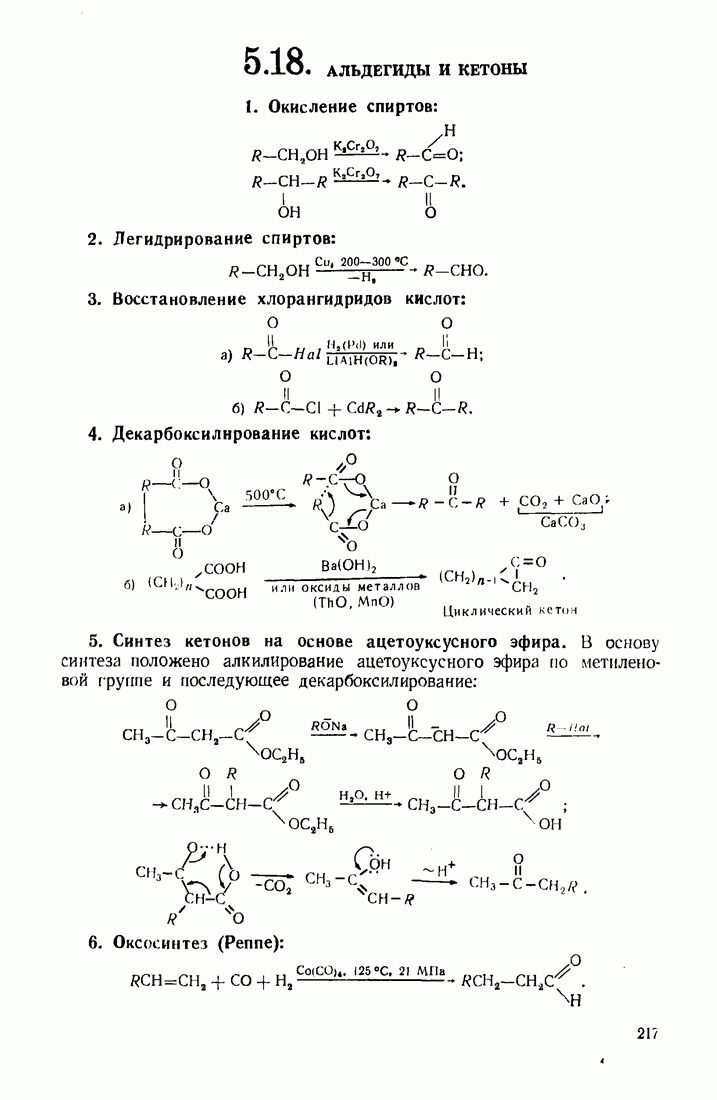
- 5.18. АЛЬДЕГИДЫ И КЕТОНЫ
- 5.19. КАРБОНОВЫЕ КИСЛОТЫ
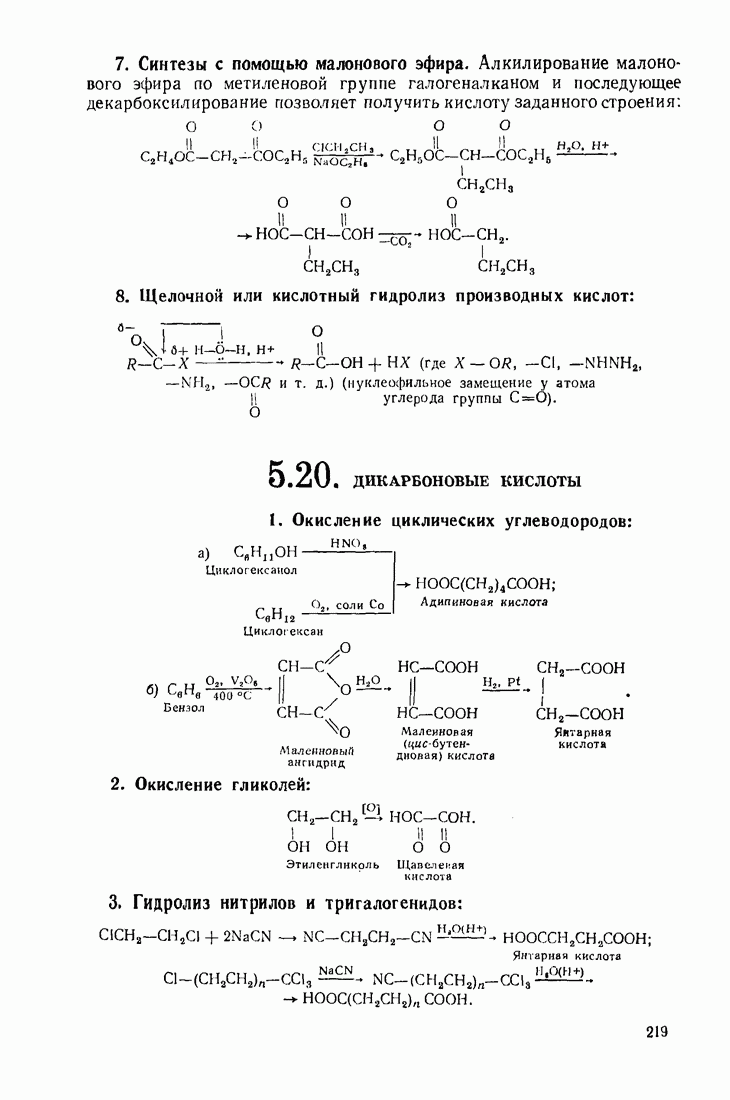
- 5.20. ДИКАРБОНОВЫЕ КИСЛОТЫ
- 5.21. НЕПРЕДЕЛЬНЫЕ КИСЛОТЫ
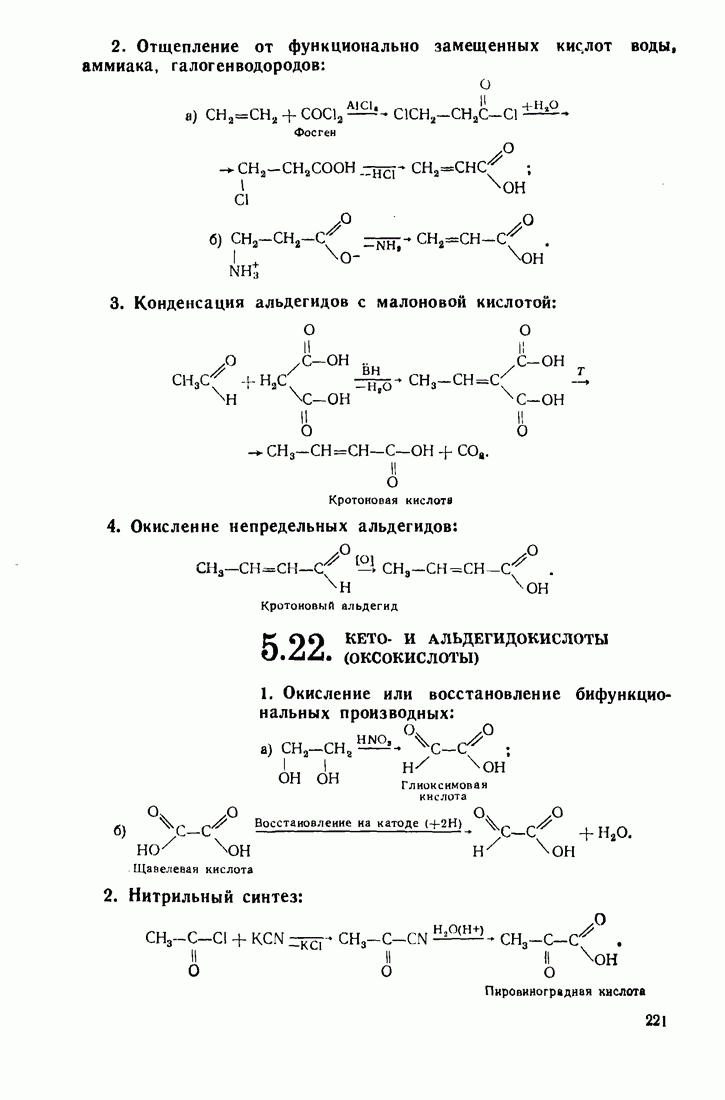
- 5.22. КЕТО- И АЛЬДЕГИДОКИСЛОТЫ (ОКСОКИСЛОТЫ)
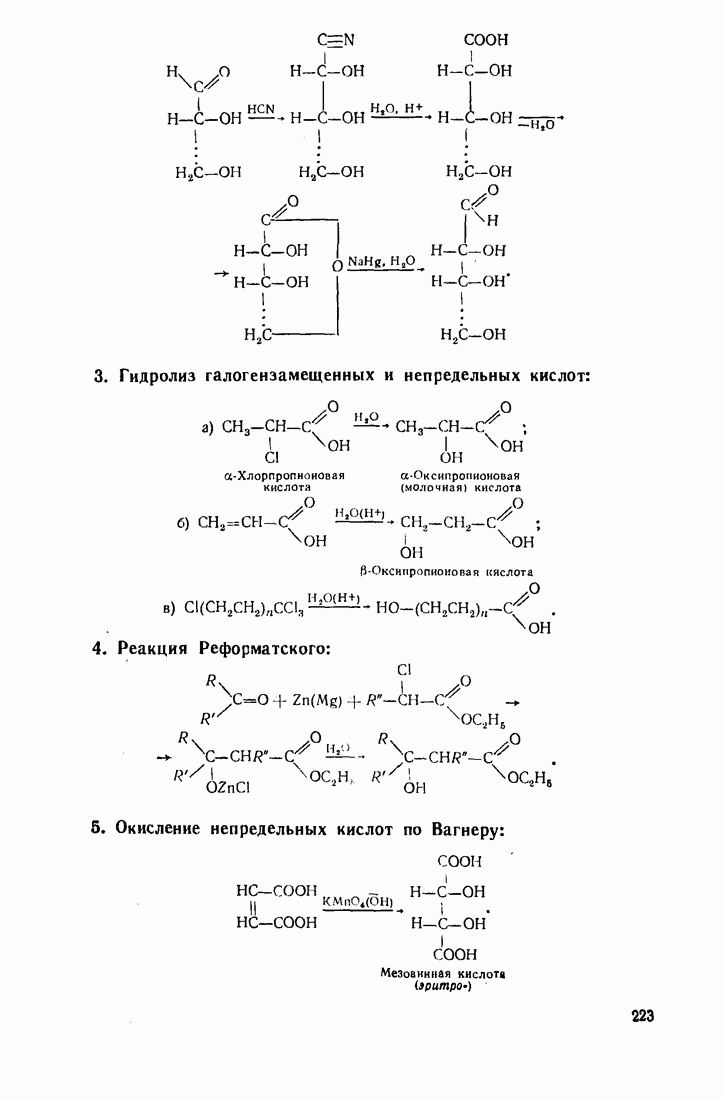
- 5.23. ОКСИКИСЛОТЫ
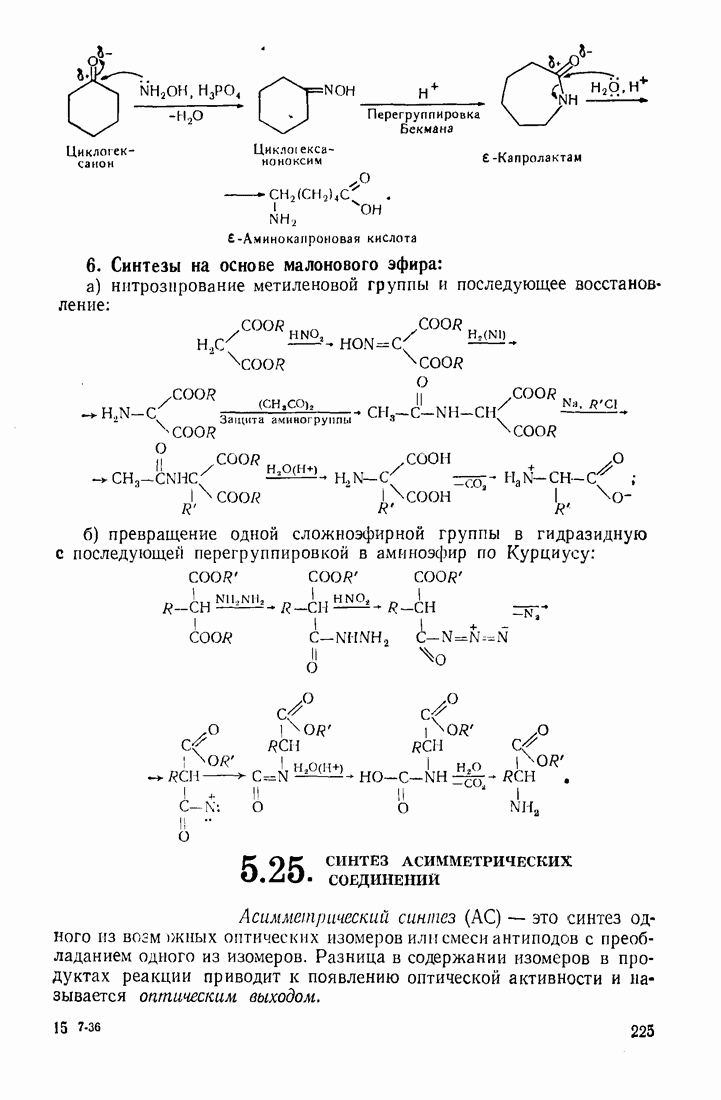
- 5.24. АМИНОКИСЛОТЫ
- 5.25 СИНТЕЗ АСИММЕТРИЧЕСКИХ СОЕДИНЕНИЙ
- 6. Некоторые понятия физической органической химии
- 6.1. СВЯЗЬ СОСТАВА И СТРОЕНИЯ СОЕДИНЕНИЙ С ФИЗИЧЕСКИМИ СВОЙСТВАМИ
- 6.2. ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 6.3. КИСЛОТЫ И ОСНОВАНИЯ В ОРГАНИЧЕСКОЙ ХИМИИ
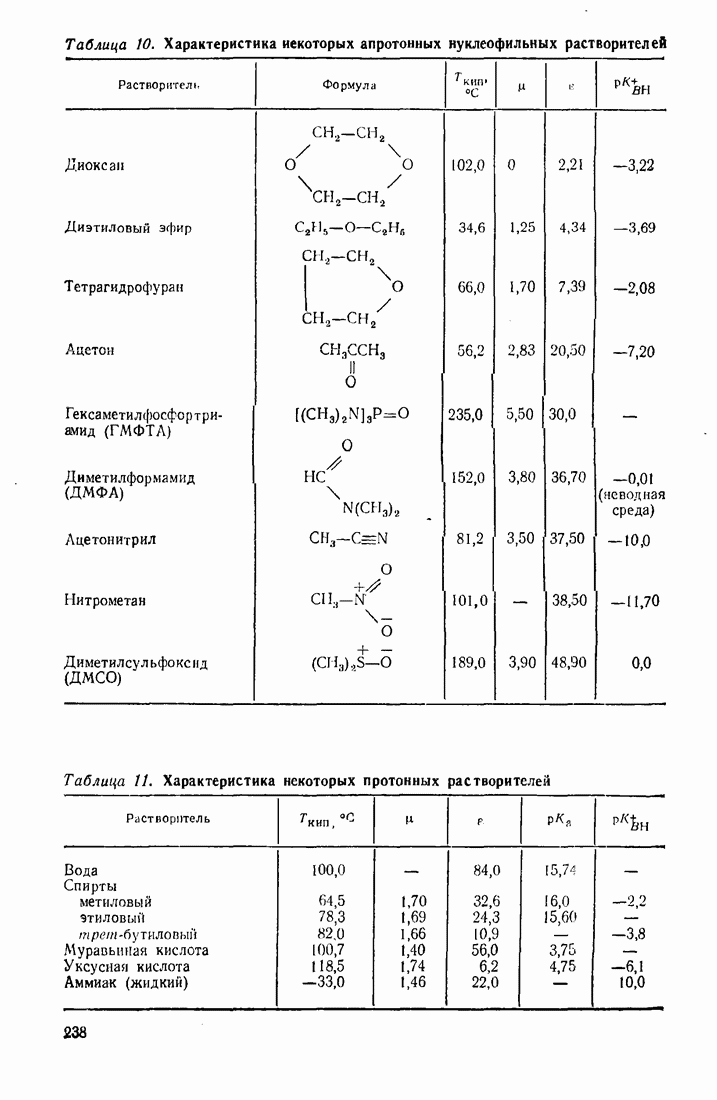
- 6.4. ОРГАНИЧЕСКИЕ РАСТВОРИТЕЛИ И ИХ ВЛИЯНИЕ НА СКОРОСТЬ И МЕХАНИЗМ РЕАКЦИЙ
- 6.5. КАТАЛИЗ ОРГАНИЧЕСКИХ РЕАКЦИЙ
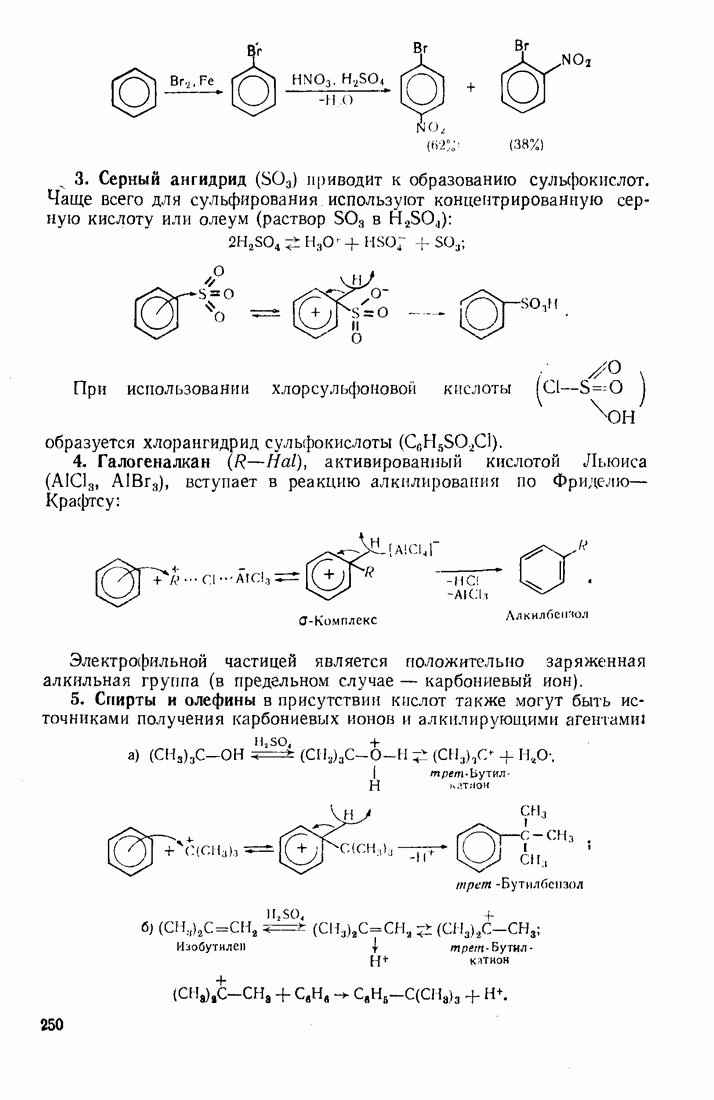
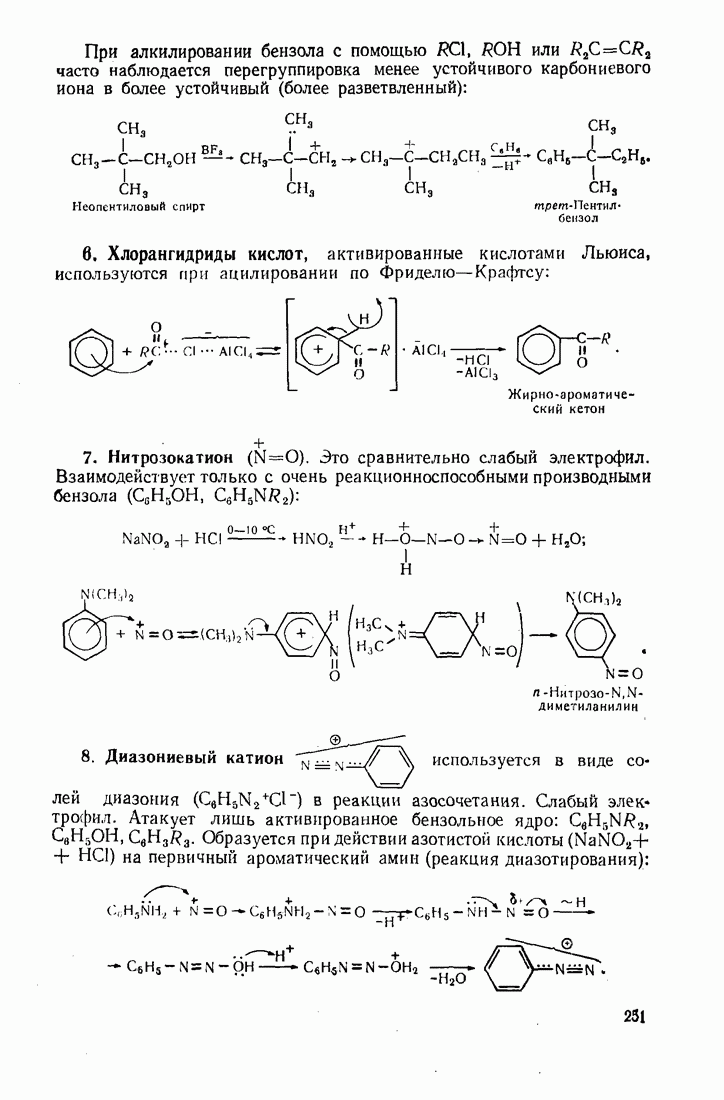
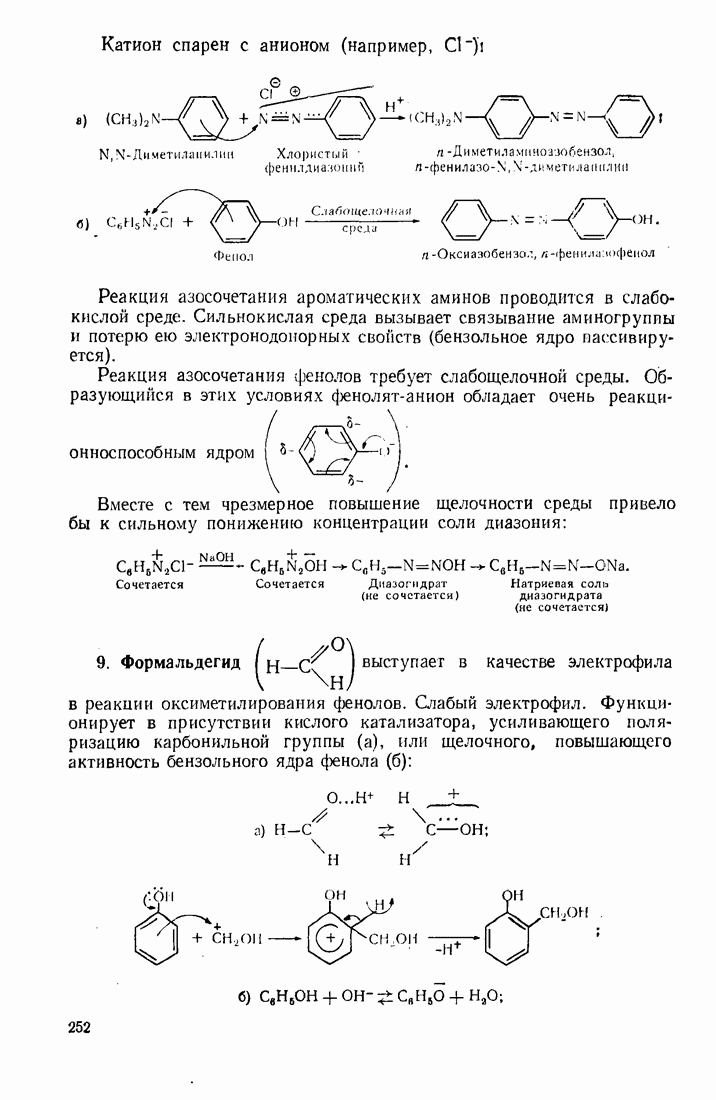
- 7. Бензол и его производные
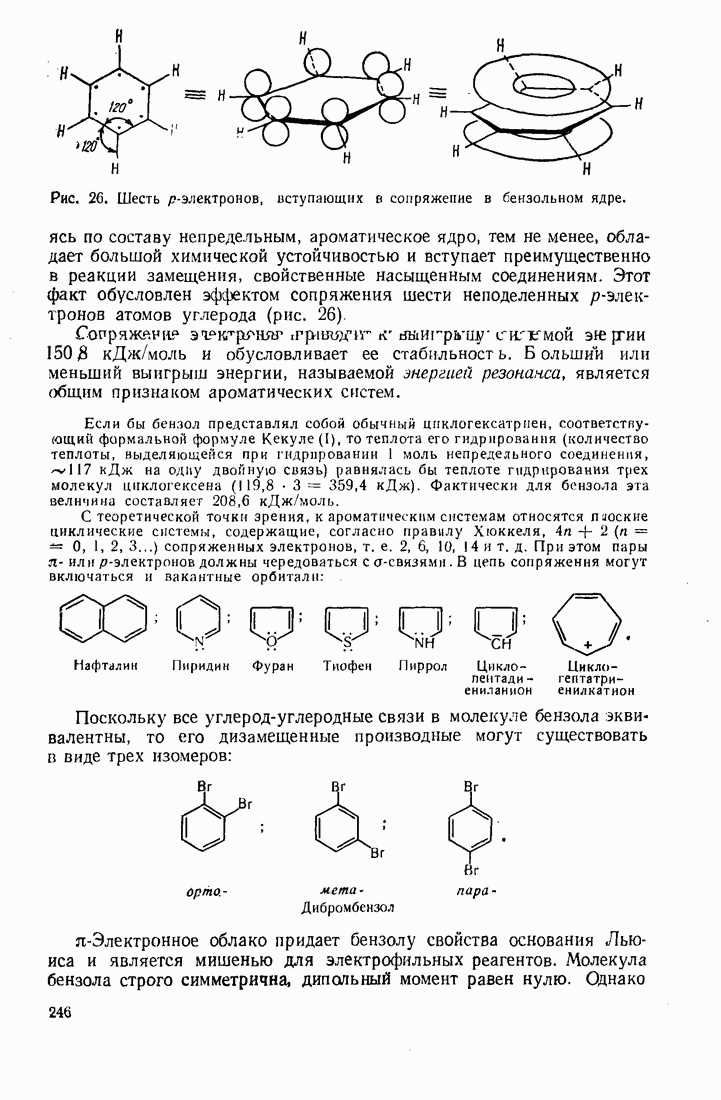
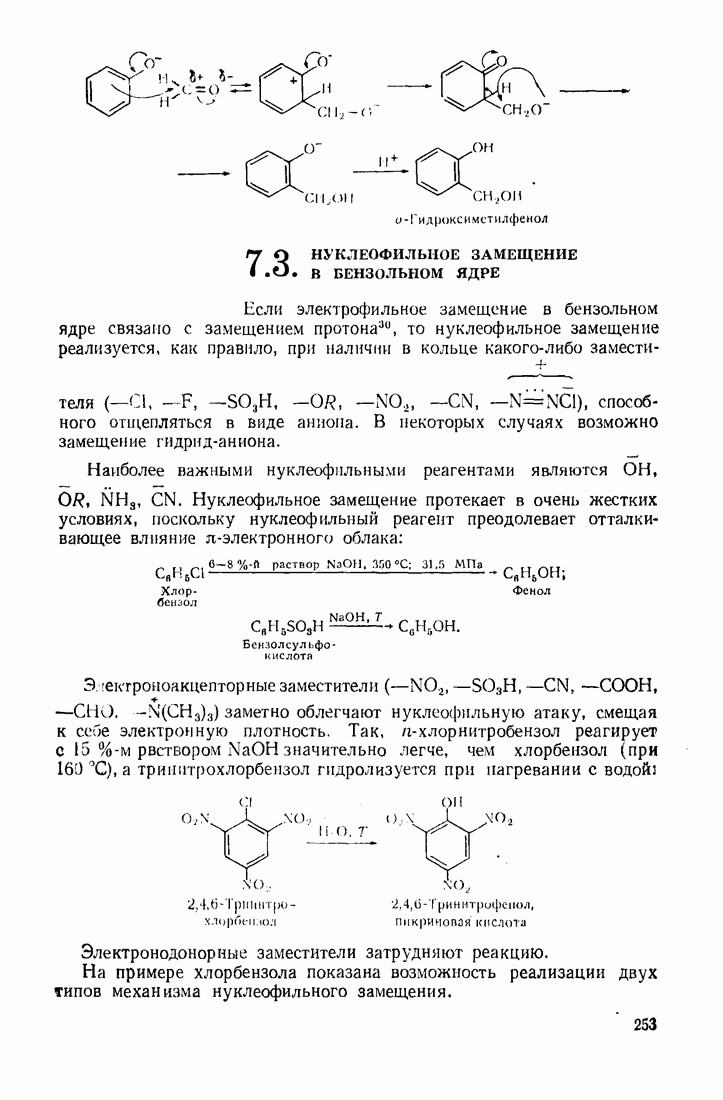
- 7.1. СТРОЕНИЕ БЕНЗОЛА. РАСПРЕДЕЛЕНИЕ ЭЛЕКТРОННОЙ ПЛОТНОСТИ
- 7.2. ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ В БЕНЗОЛЬНОМ ЯДРЕ
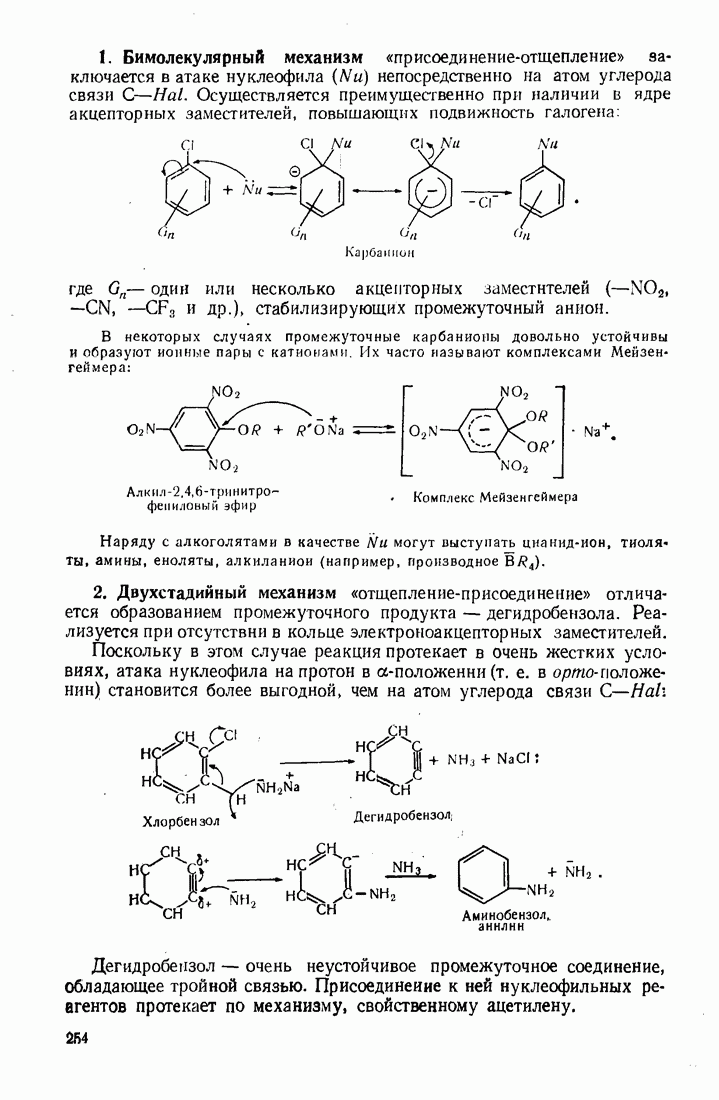
- 7.3. НУКЛЕОФИЛЬНОЕ ЗАМЕЩЕНИЕ В БЕНЗОЛЬНОМ ЯДРЕ
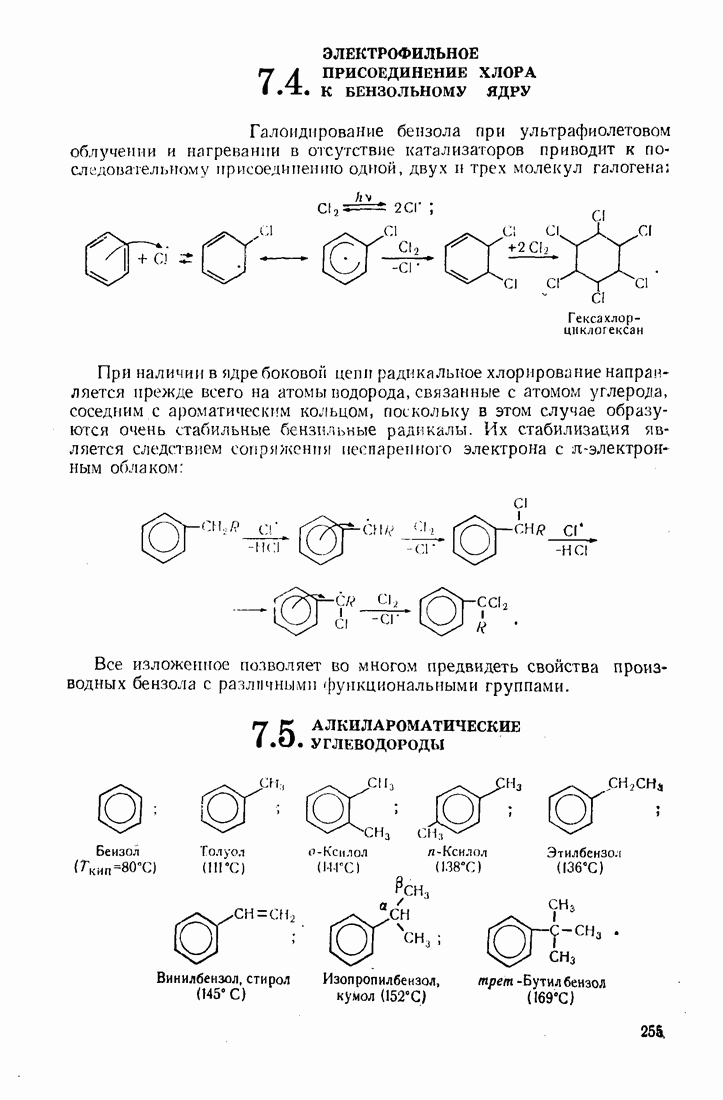
- 7.4. ЭЛЕКТРОФИЛЬНОЕ ПРИСОЕДИНЕНИЕ ХЛОРА К БЕНЗОЛЬНОМУ ЯДРУ
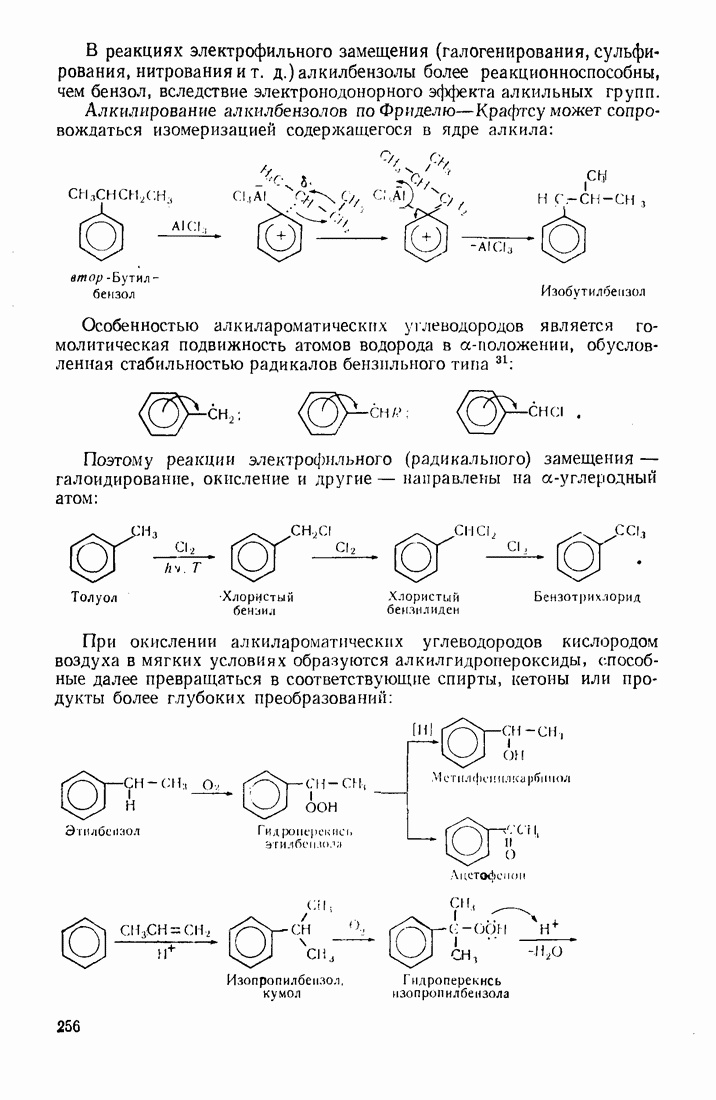
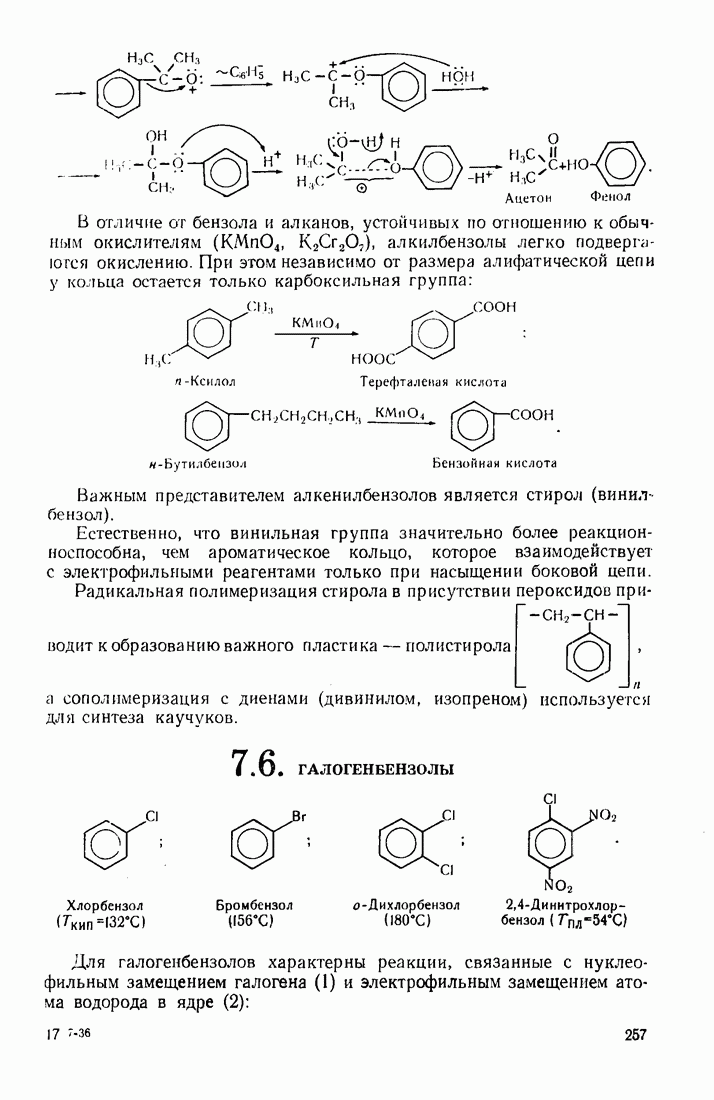
- 7.5. АЛКИЛАРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ
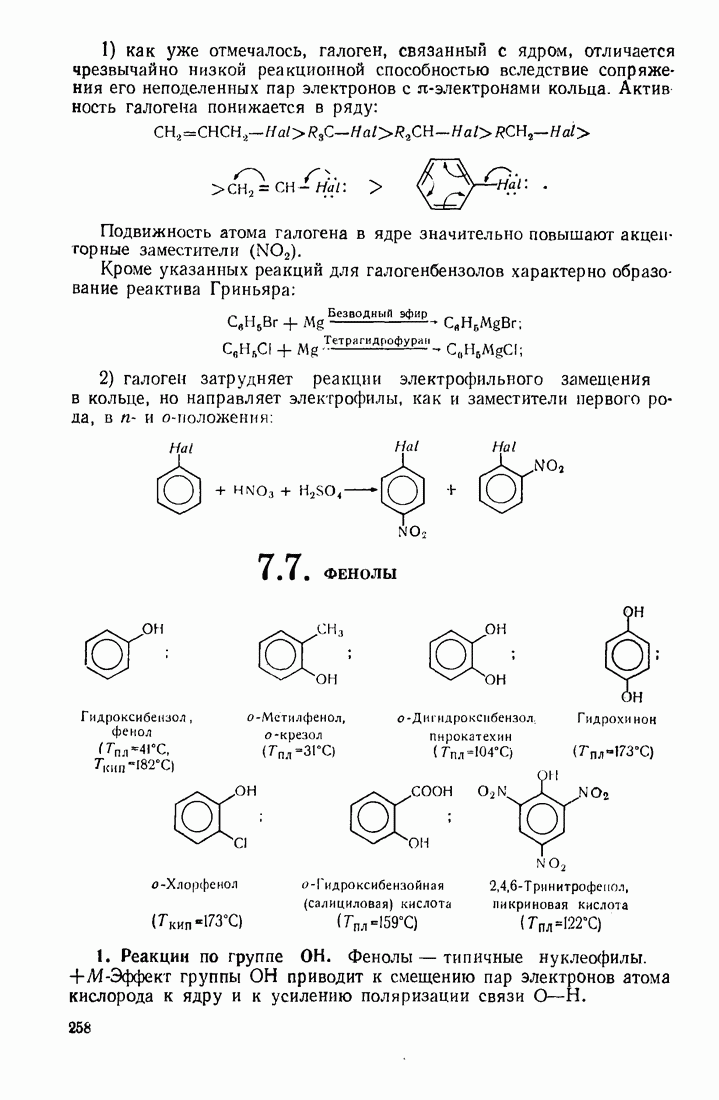
- 7.6. ГАЛОГЕНБЕНЗОЛЫ
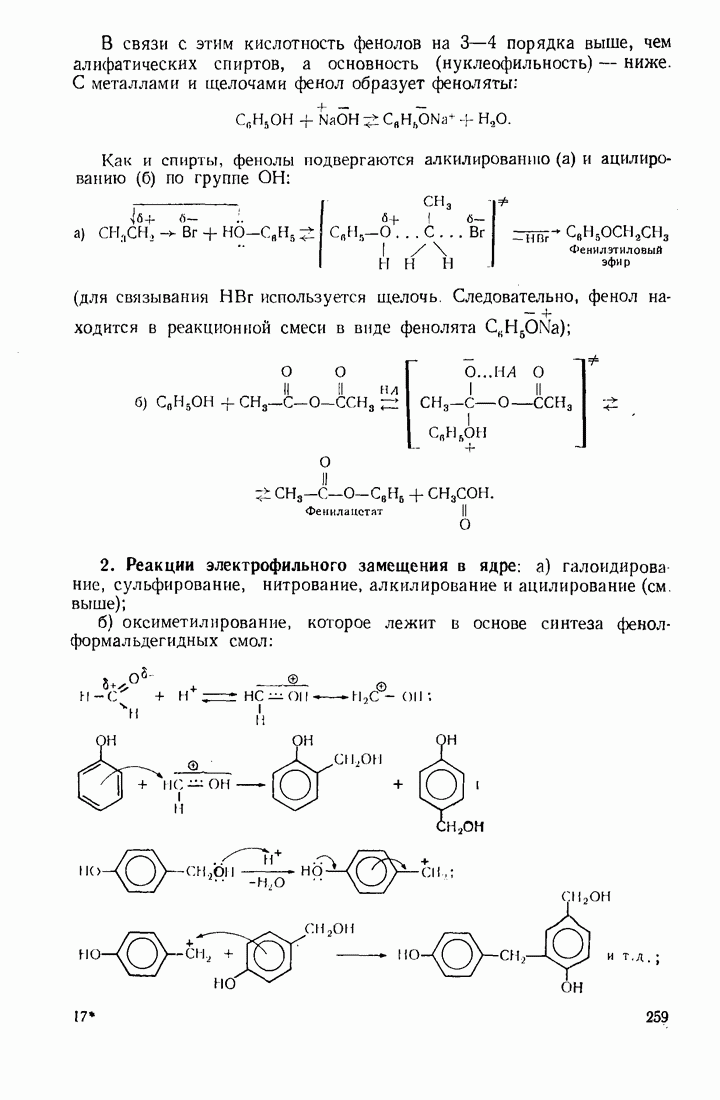
- 7.7. ФЕНОЛЫ
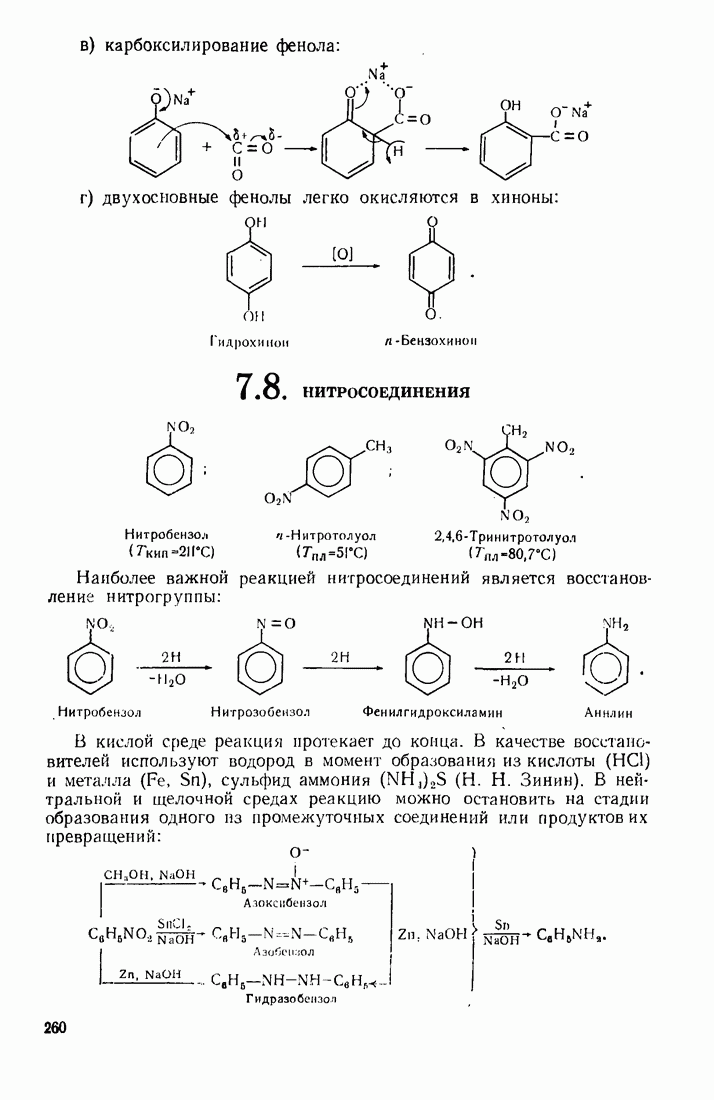
- 7.8. НИТРОСОЕД ИНЕНИЯ
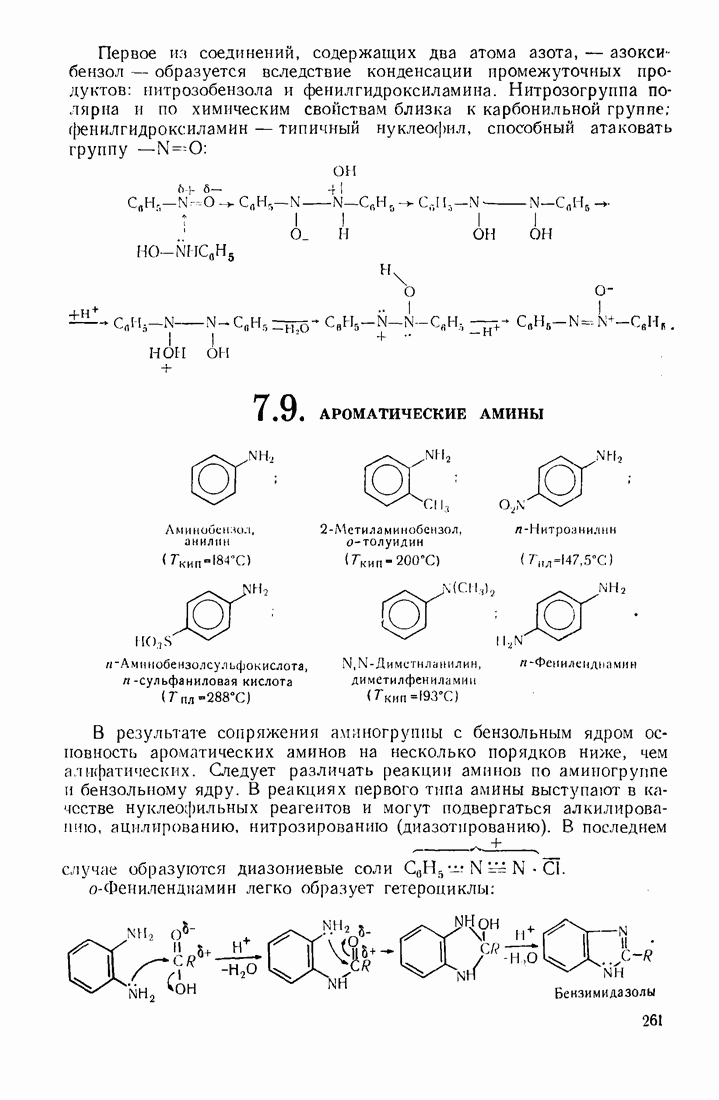
- 7.9. АРОМАТИЧЕСКИЕ АМИНЫ
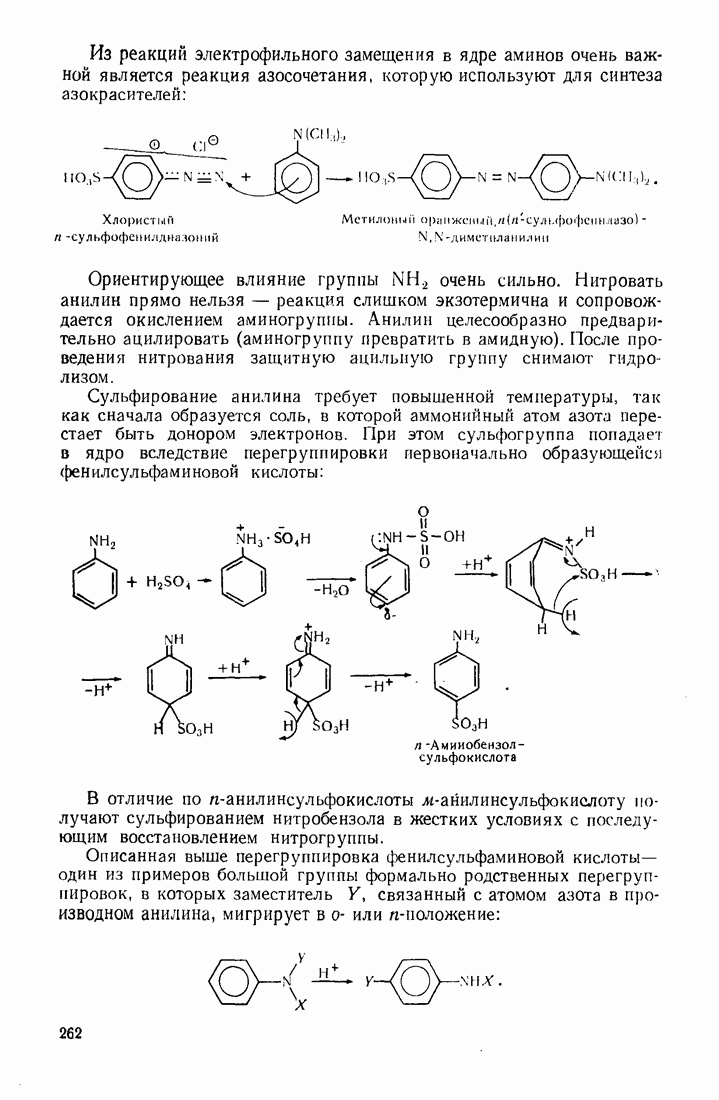
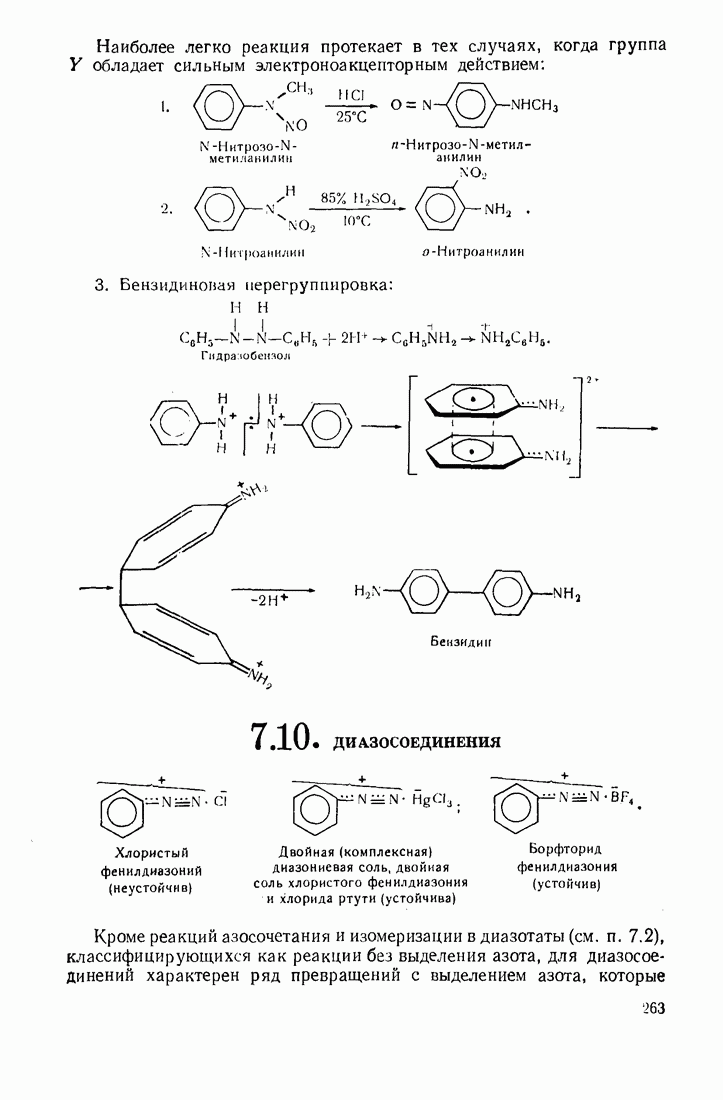
- 7.10. ДИАЗОСОЕДИНЕНИЯ
- 7.11. АЗОСОЕДИНЕНИЯ
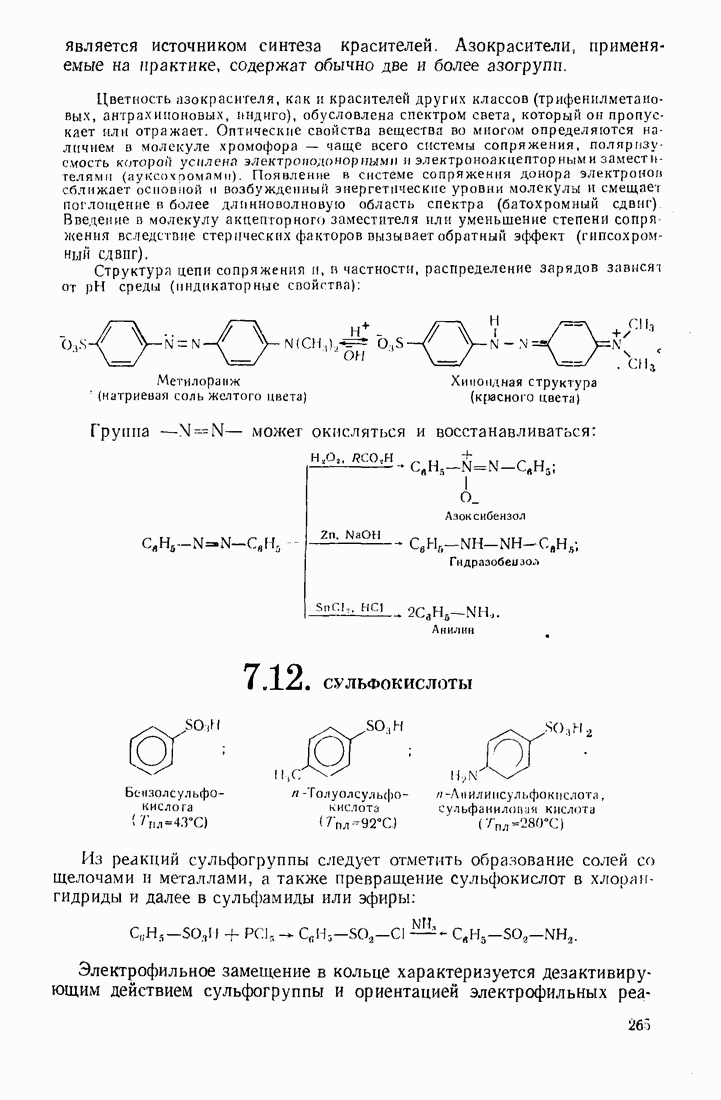
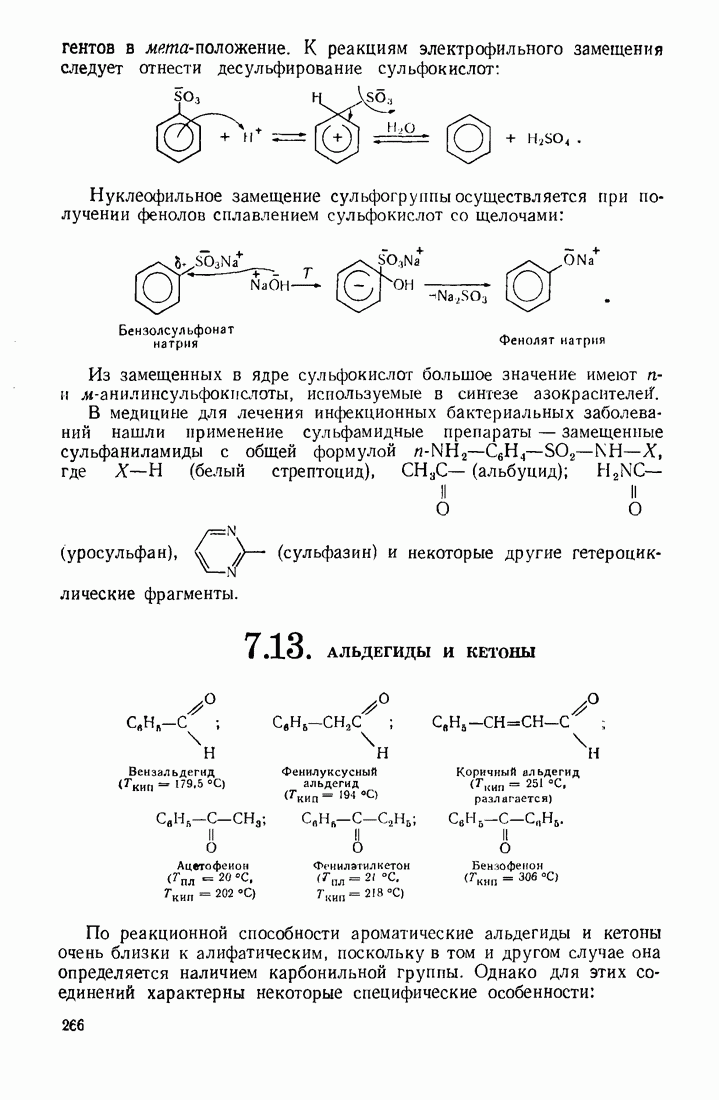
- 7.12. СУЛЬФОКИСЛОТЫ
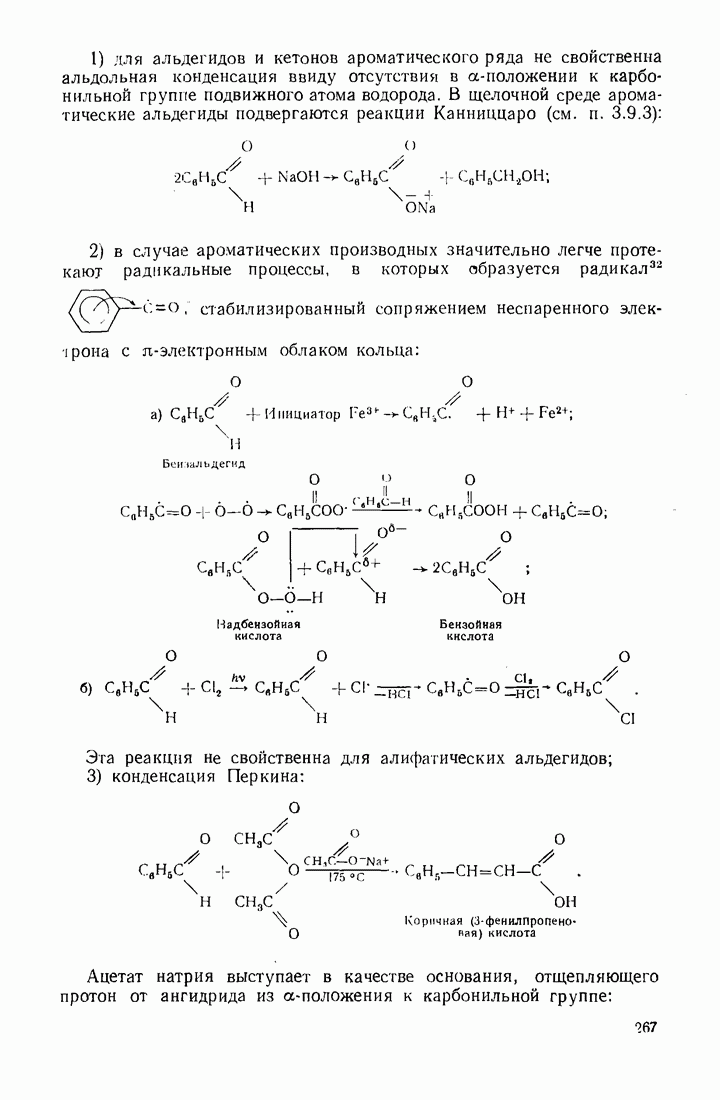
- 7.13. АЛЬДЕГИДЫ И КЕТОНЫ
- 8. Многоядерные ароматические соединения
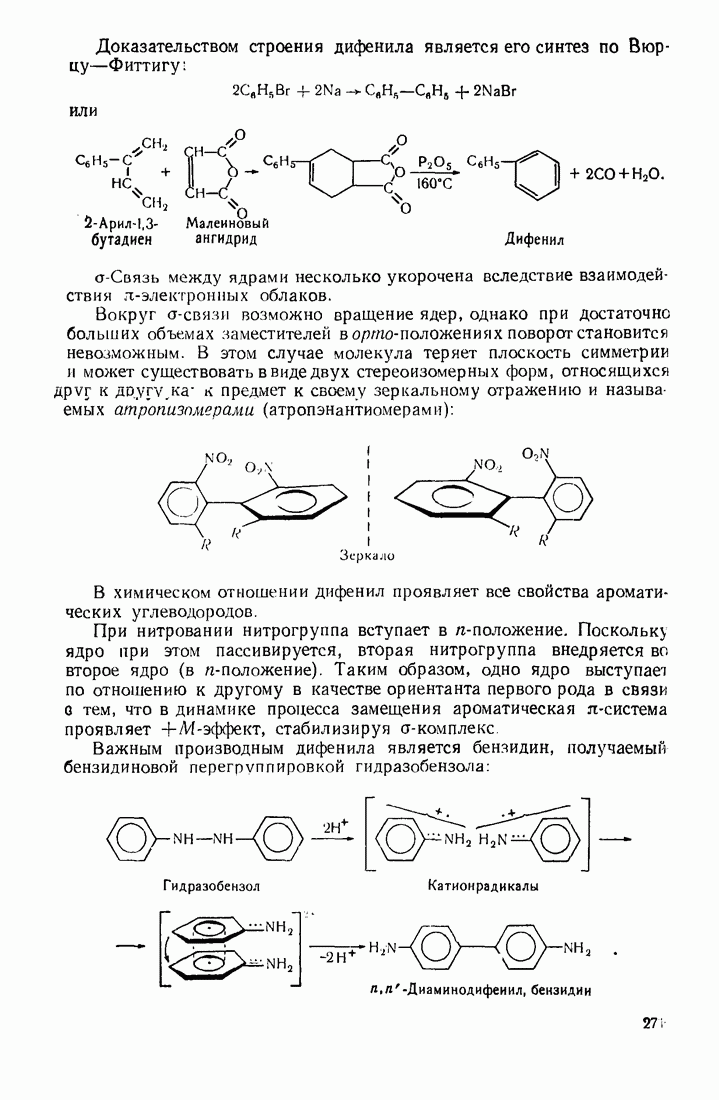
- 8.1. СОЕДИНЕНИЯ С ИЗОЛИРОВАННЫМИ БЕНЗОЛЬНЫМИ ЯДРАМИ
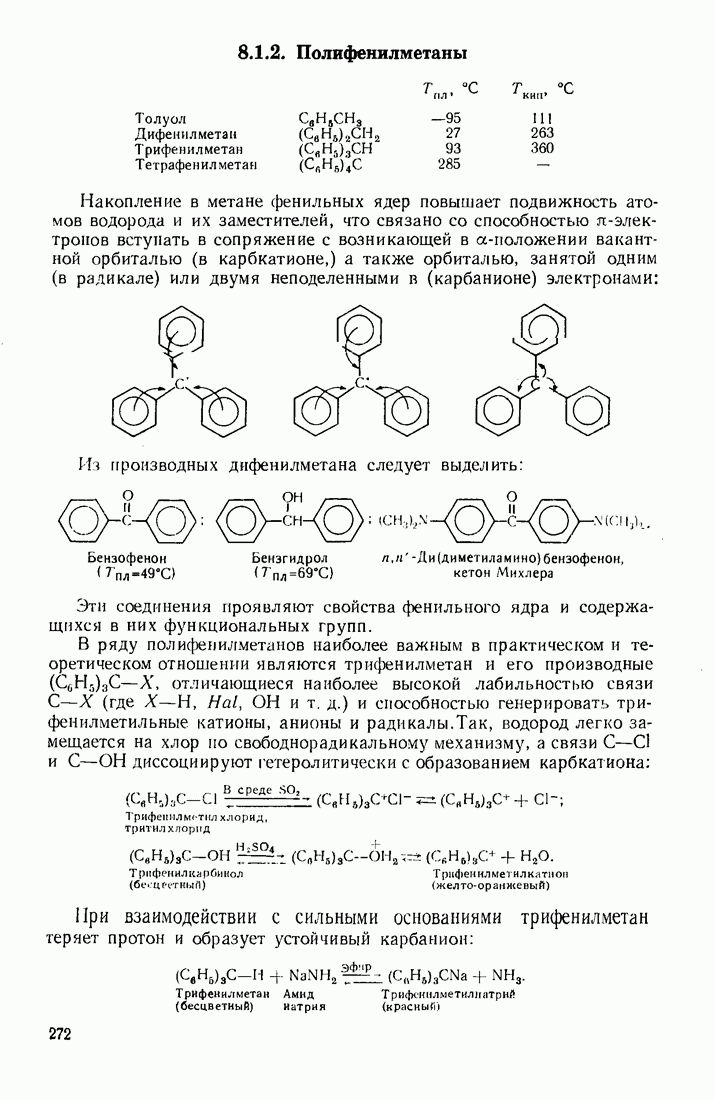
- 8.1.2. Полифенилметаны
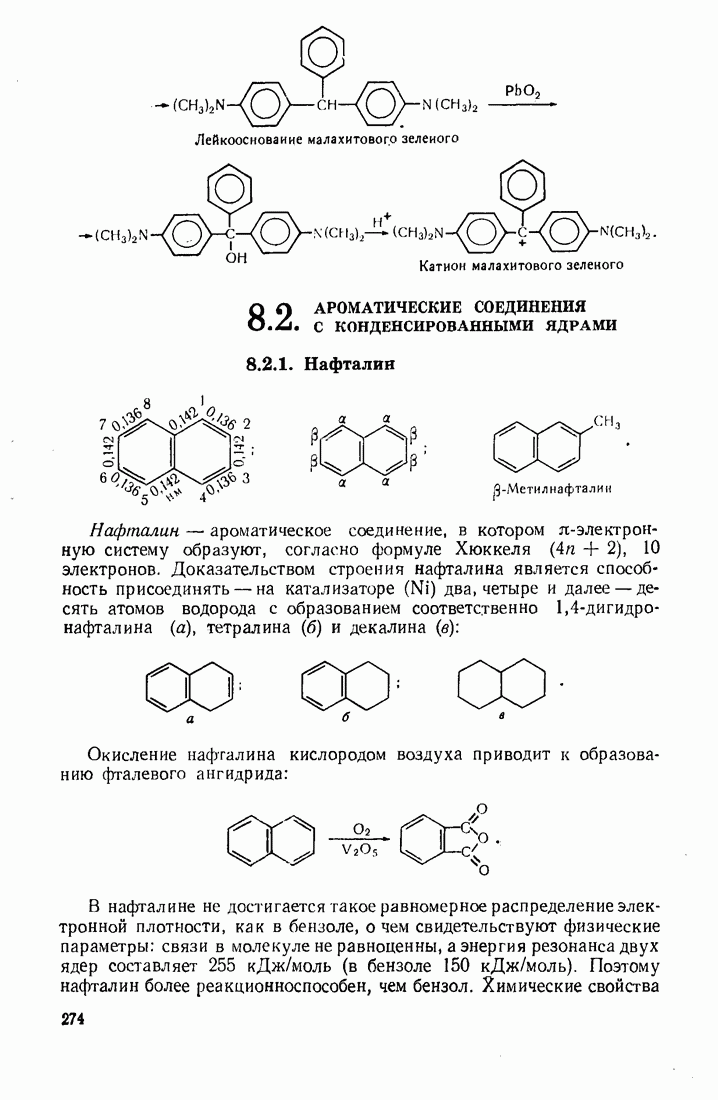
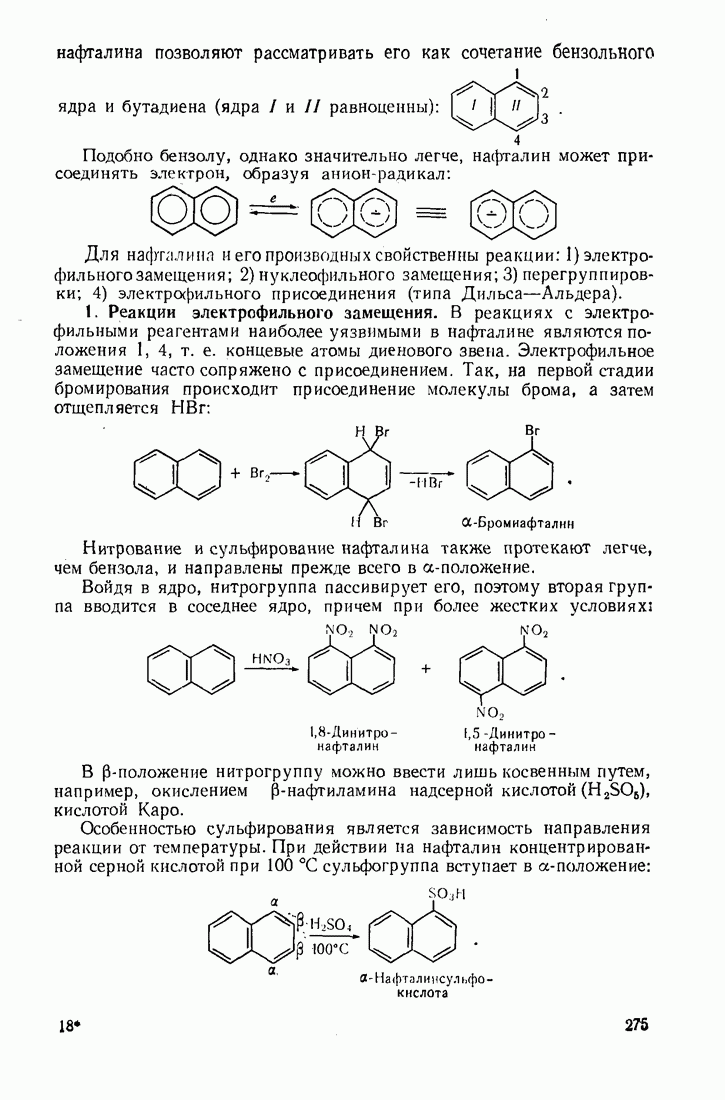
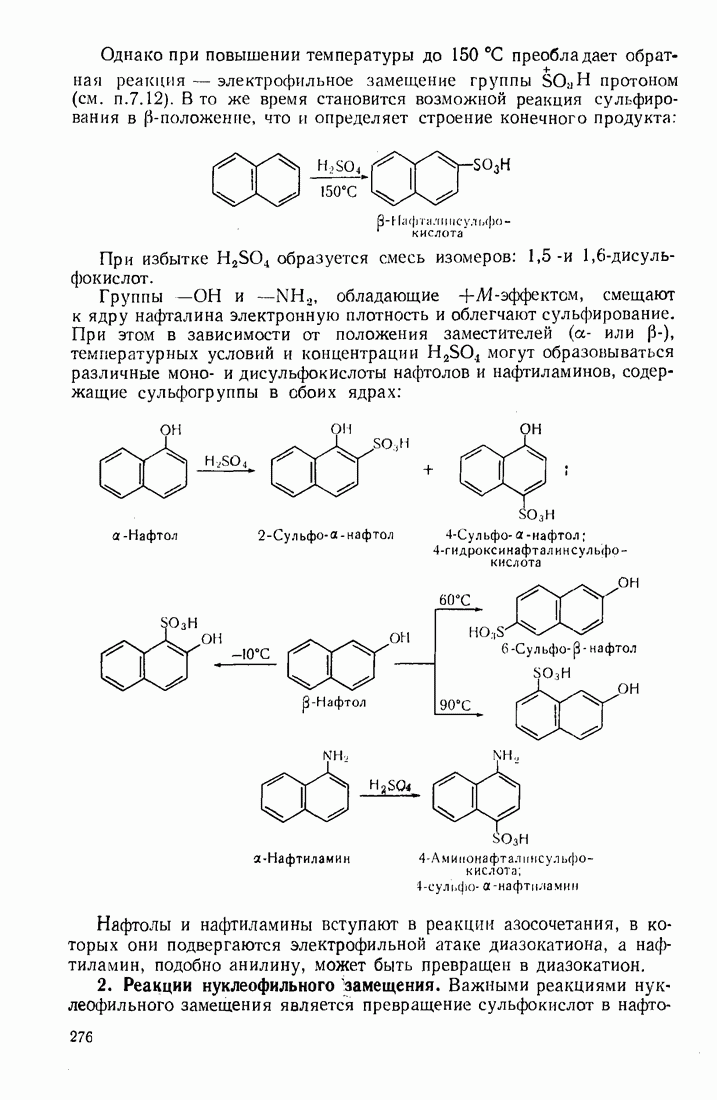
- 8.2. АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ С КОНДЕНСИРОВАННЫМИ ЯДРАМИ
- 8.2.2. Антрацен
- 8.2.3. Фенантрен
- 9. Методы синтеза в ряду ароматических соединений
- 9.1. ГАЛОГЕНИРОВАНИЕ
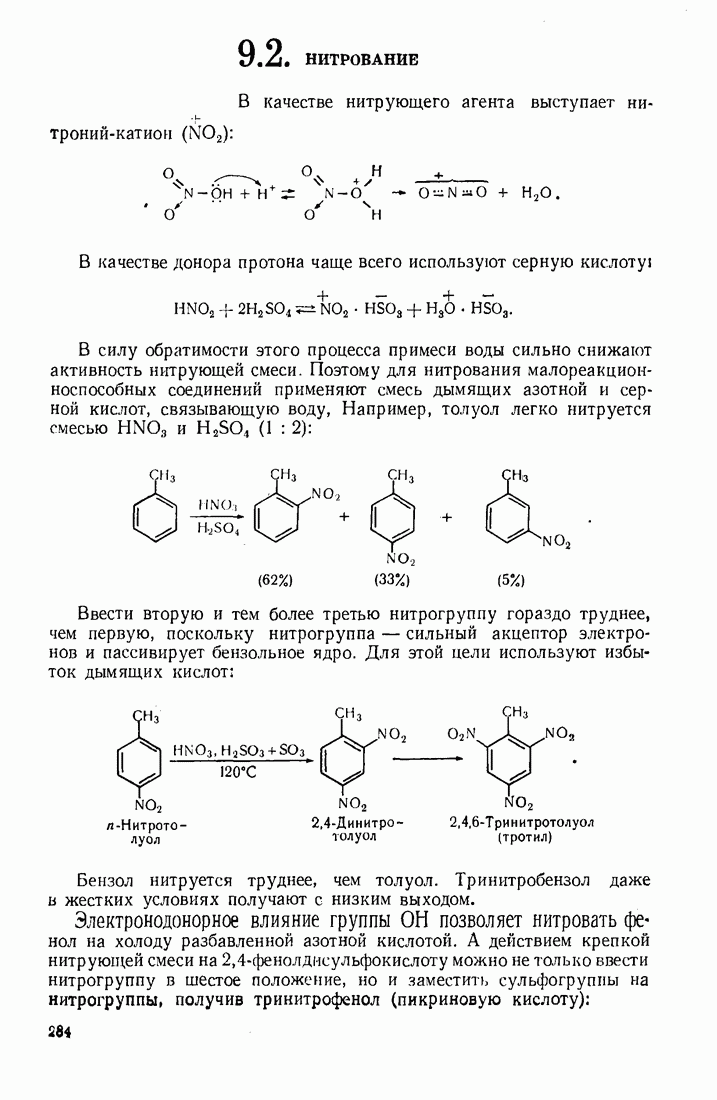
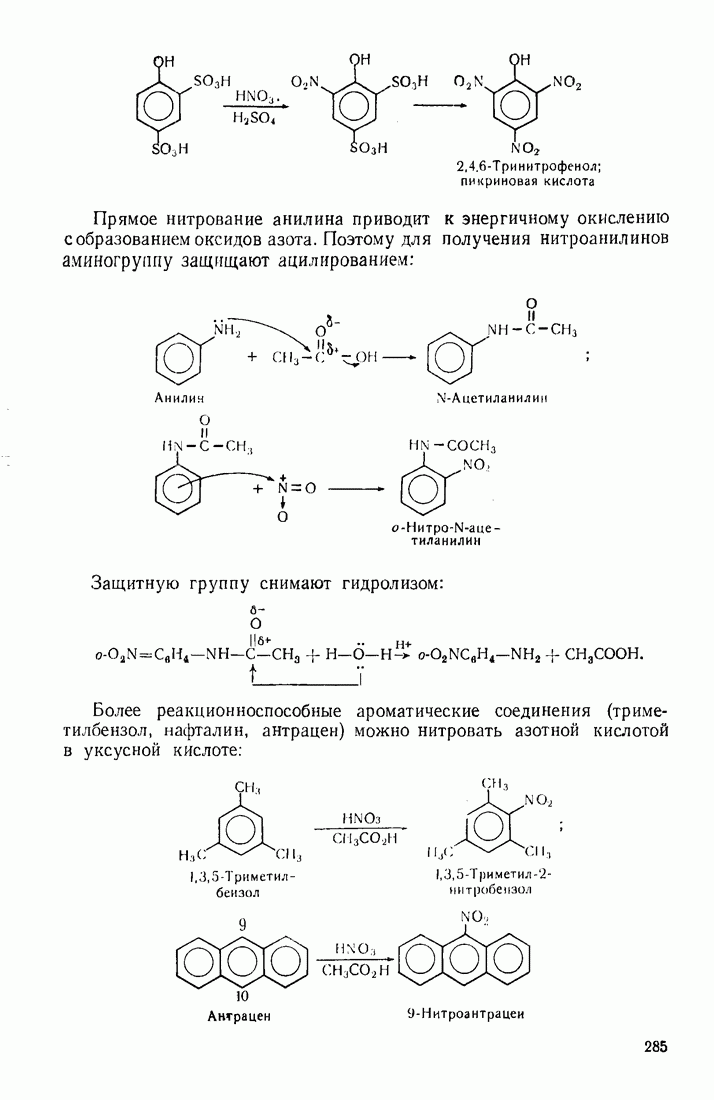
- 9.2. НИТРОВАНИЕ
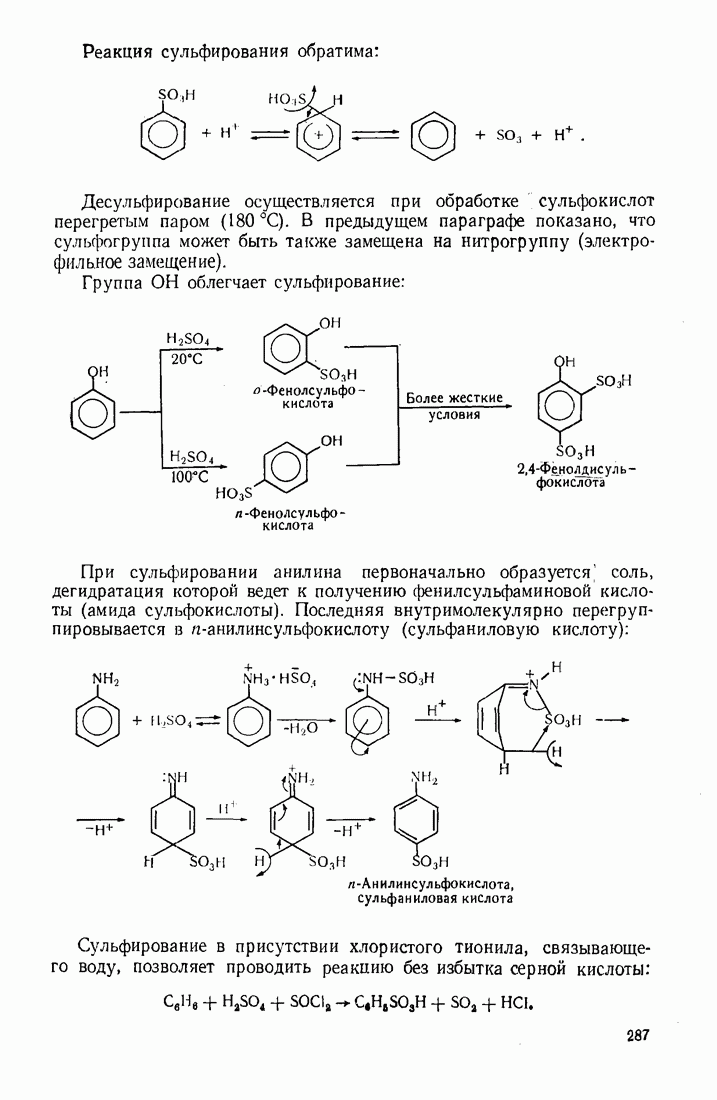
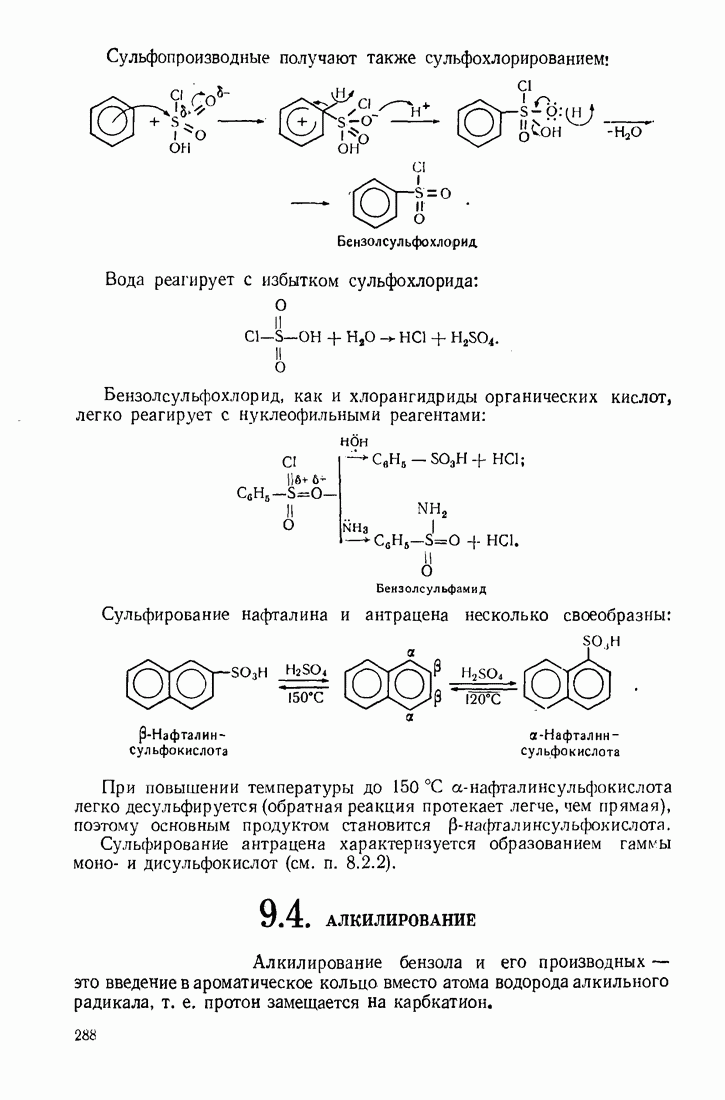
- 9.3. СУЛЬФИРОВАНИЕ
- 9.4. АЛКИЛИРОВАНИЕ
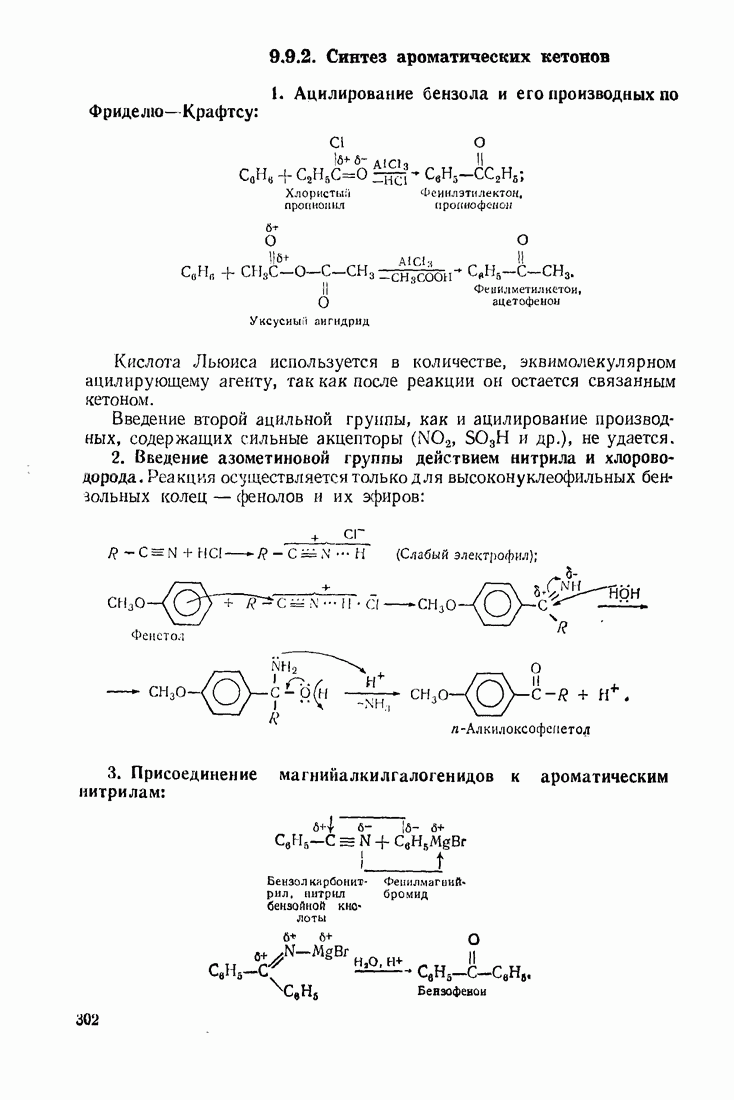
- 9.5. АЦИЛИРОВАНИЕ
- 9.6. ГИДРОКСИЛИРОВАНИЕ
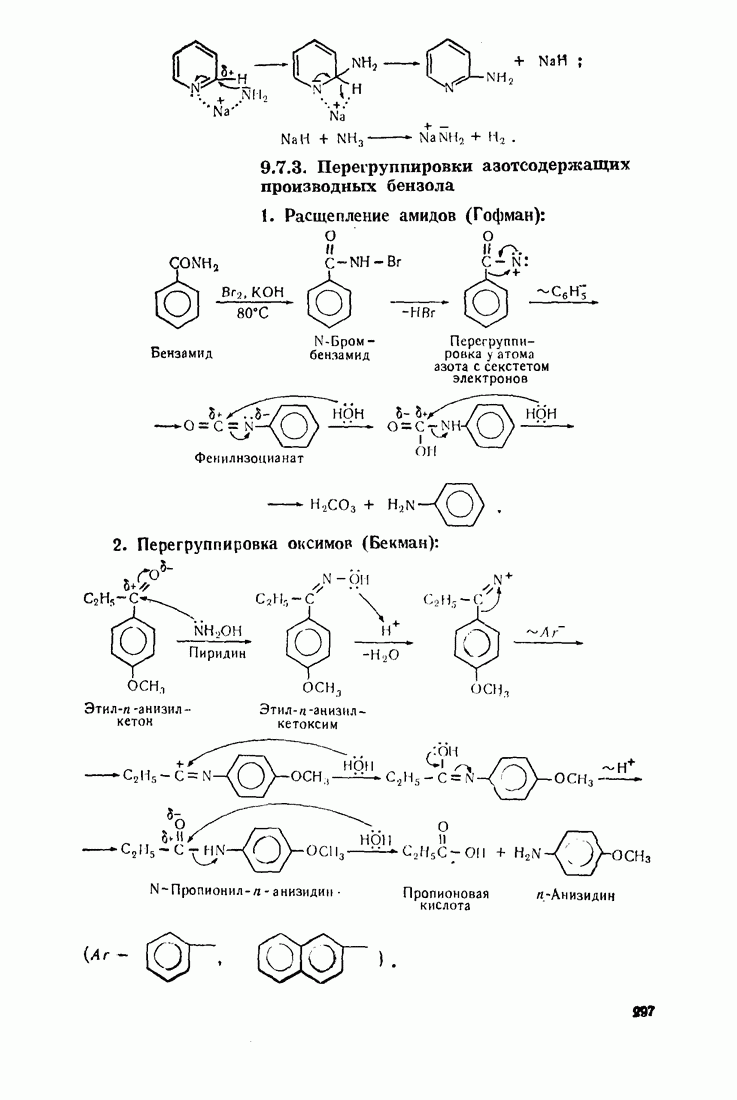
- 9.7. АМИНИРОВАНИЕ
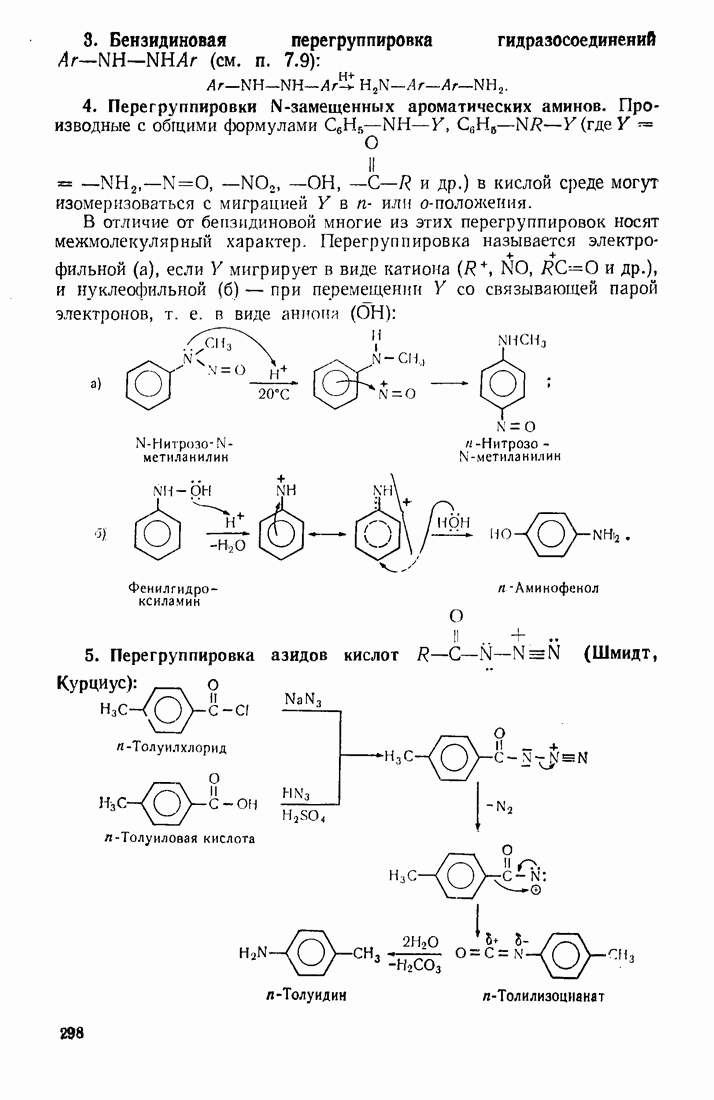
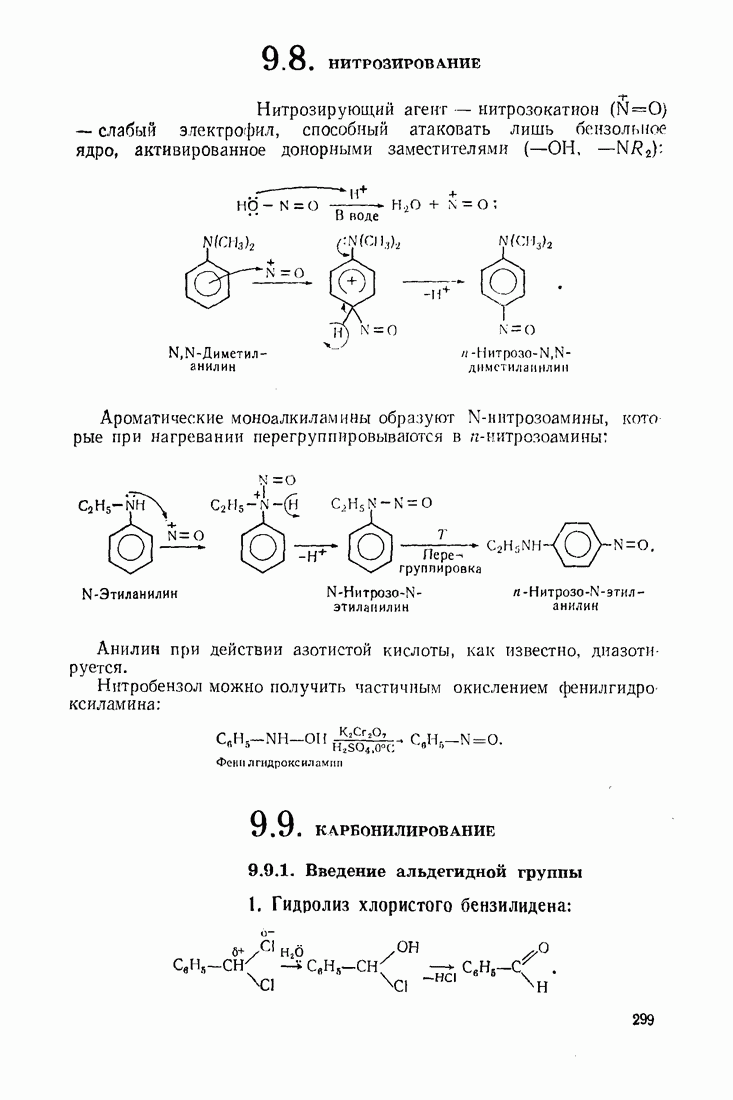
- 9.8. НИТРОЗИРОВАНИЕ
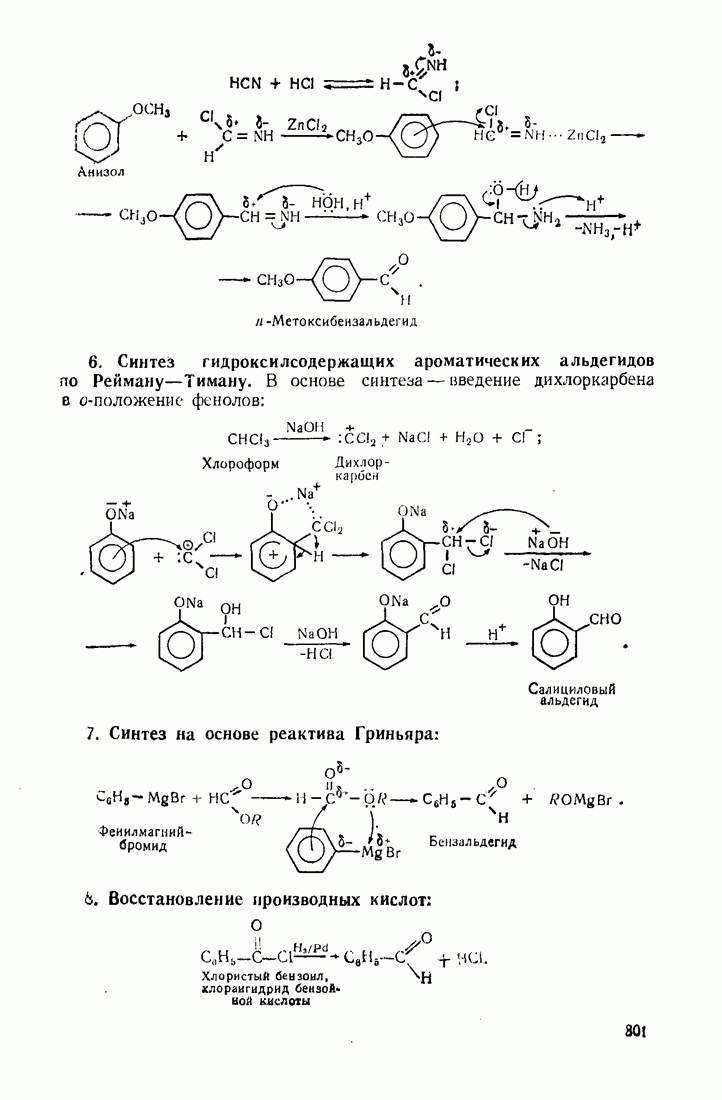
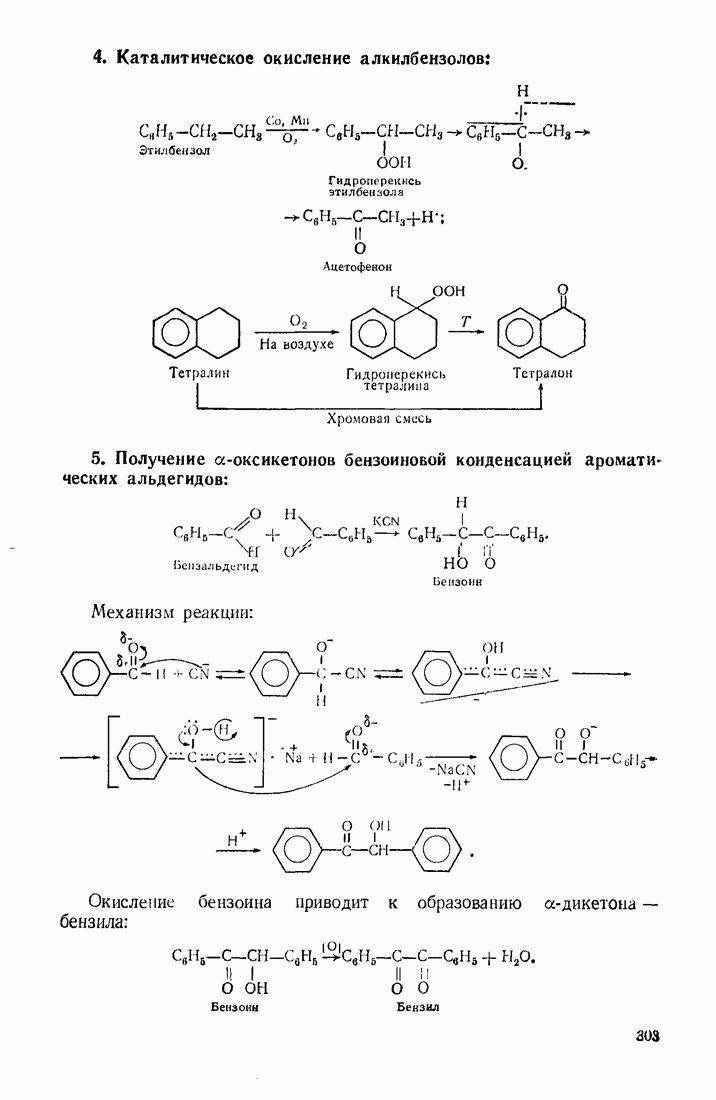
- 9.9. КАРБОНИЛИРОВАНИЕ
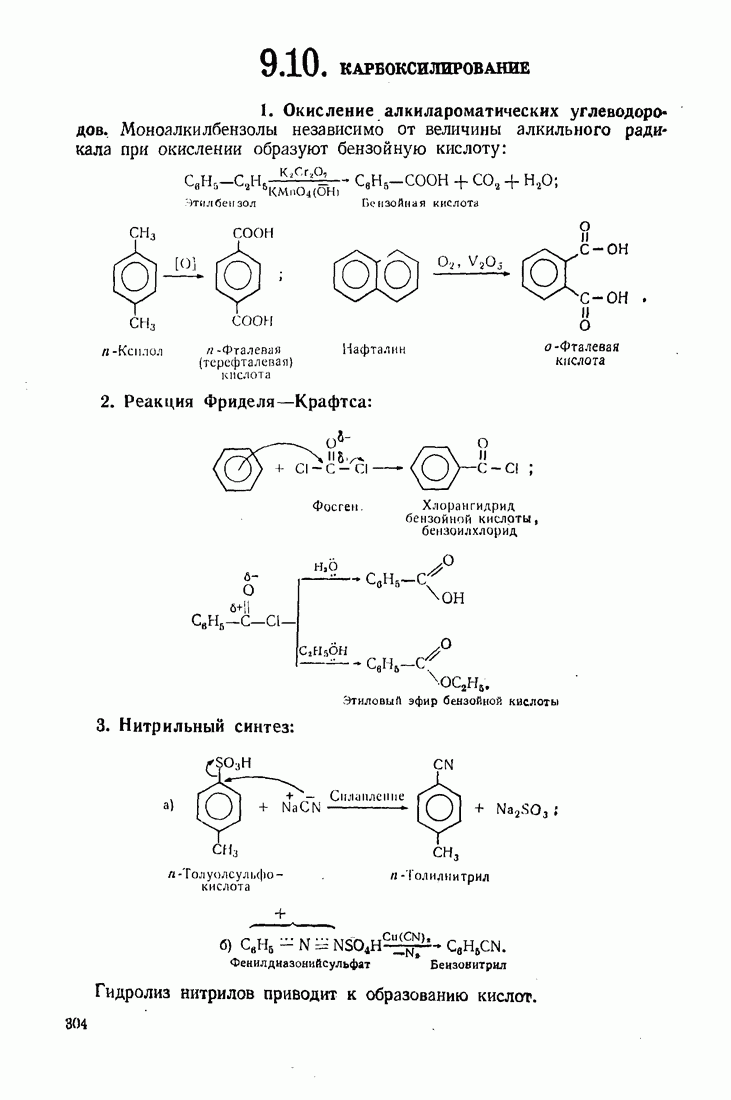
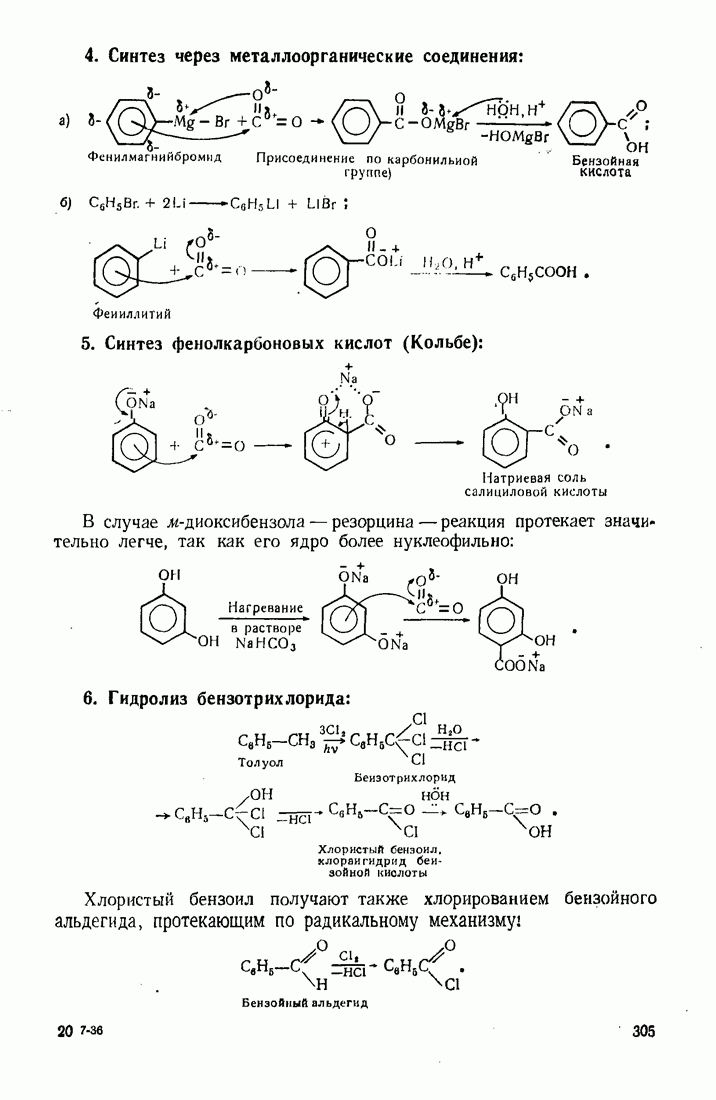
- 9.10. КАРБОКСИЛИРОВАНИЕ
- 9.11. ОКИСЛЕНИЕ
- 9.12. ВОССТАНОВЛЕНИЕ
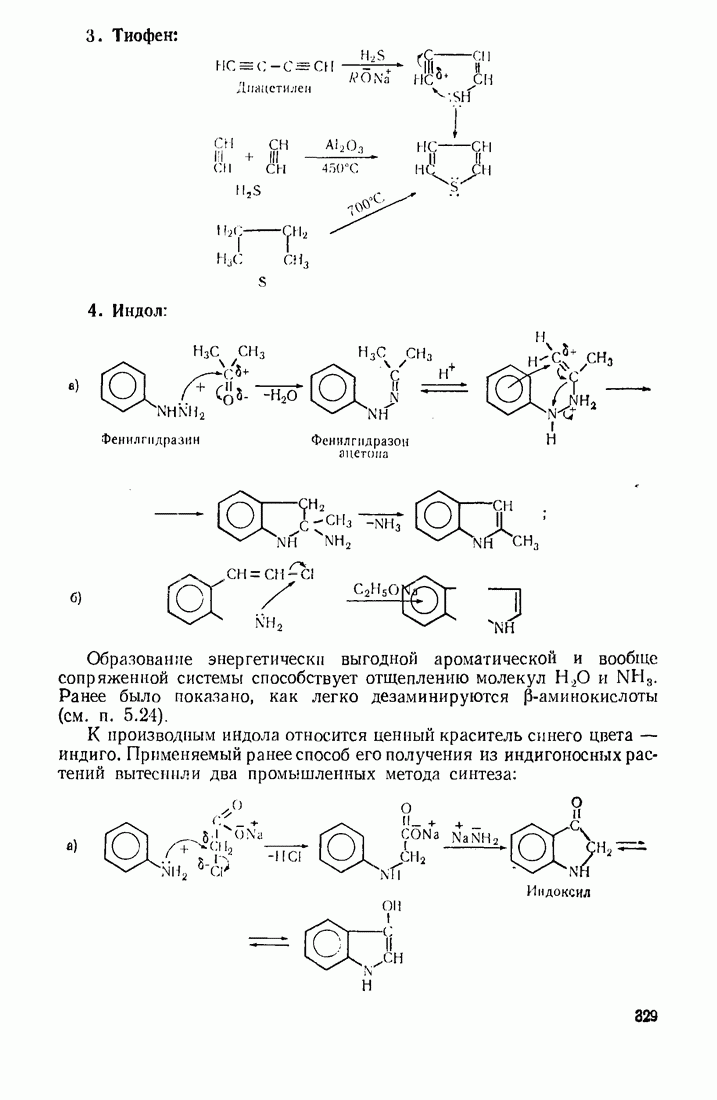
- 10. Гетероциклические соединения
- 10.2. ОБЩАЯ ХАРАКТЕРИСТИКА СТРОЕНИЯ И РЕАКЦИОННОЙ СПОСОБНОСТИ
- 10.3. ПЯТИ- И ШЕСТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С ОДНИМ ГЕТЕРОАТОМОМ
- 10.4. ГЕТЕРОЦИКЛЫ С НЕСКОЛЬКИМИ ГЕТЕРОАТОМАМИ
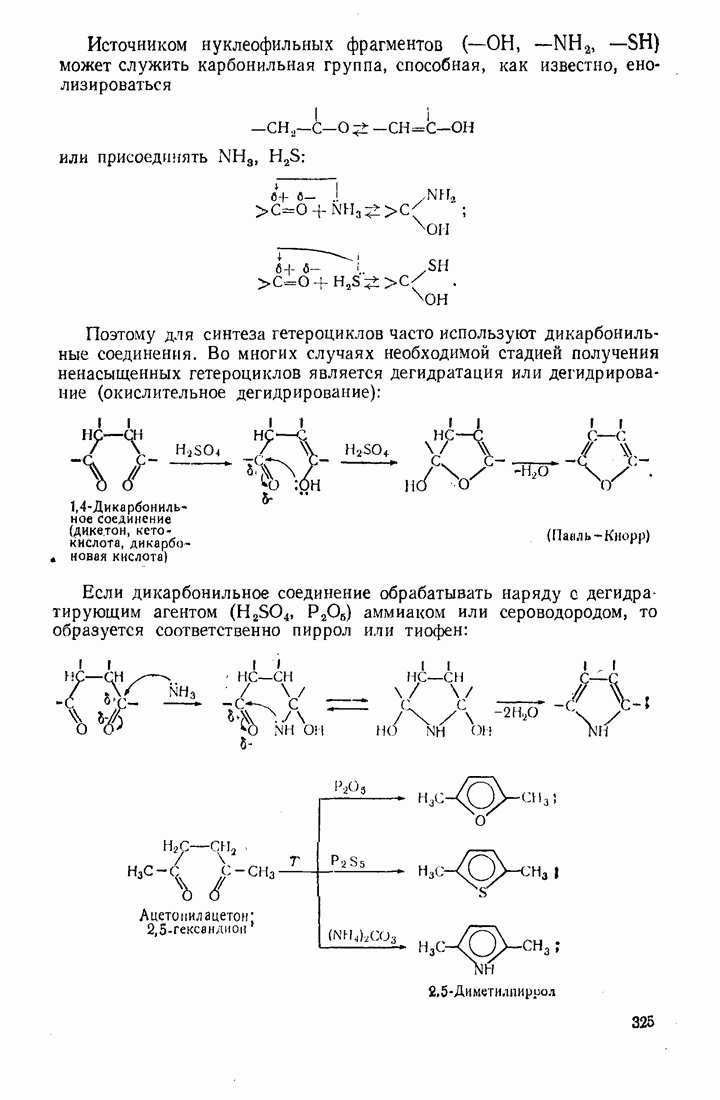
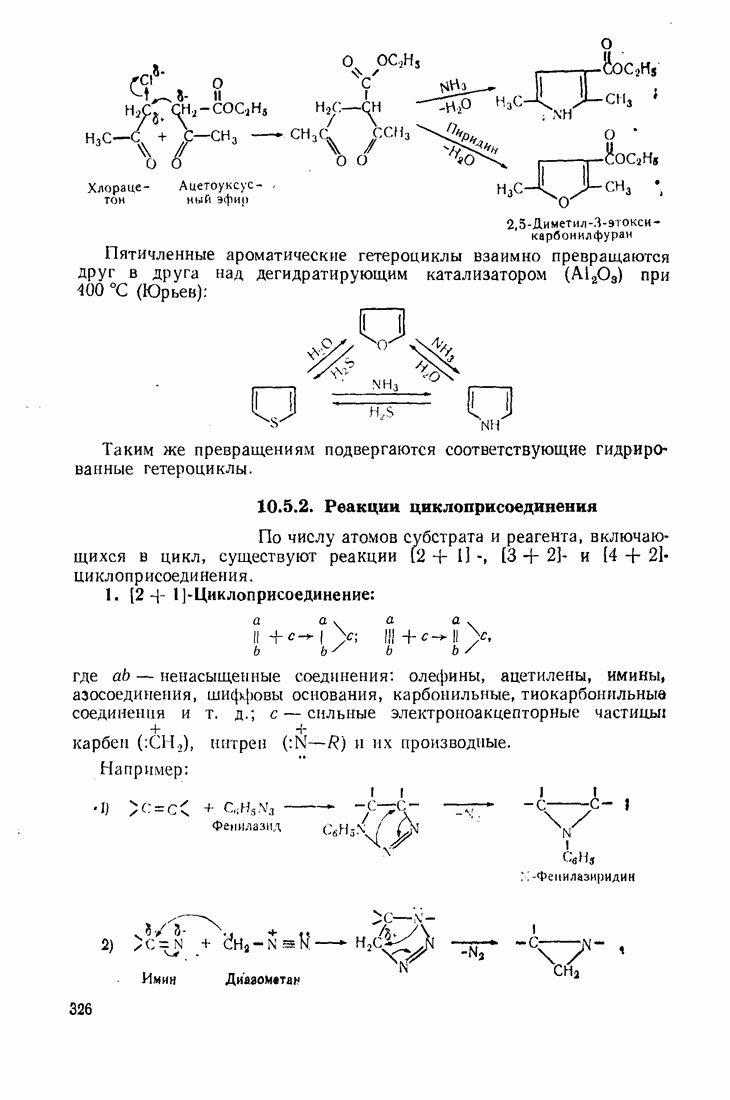
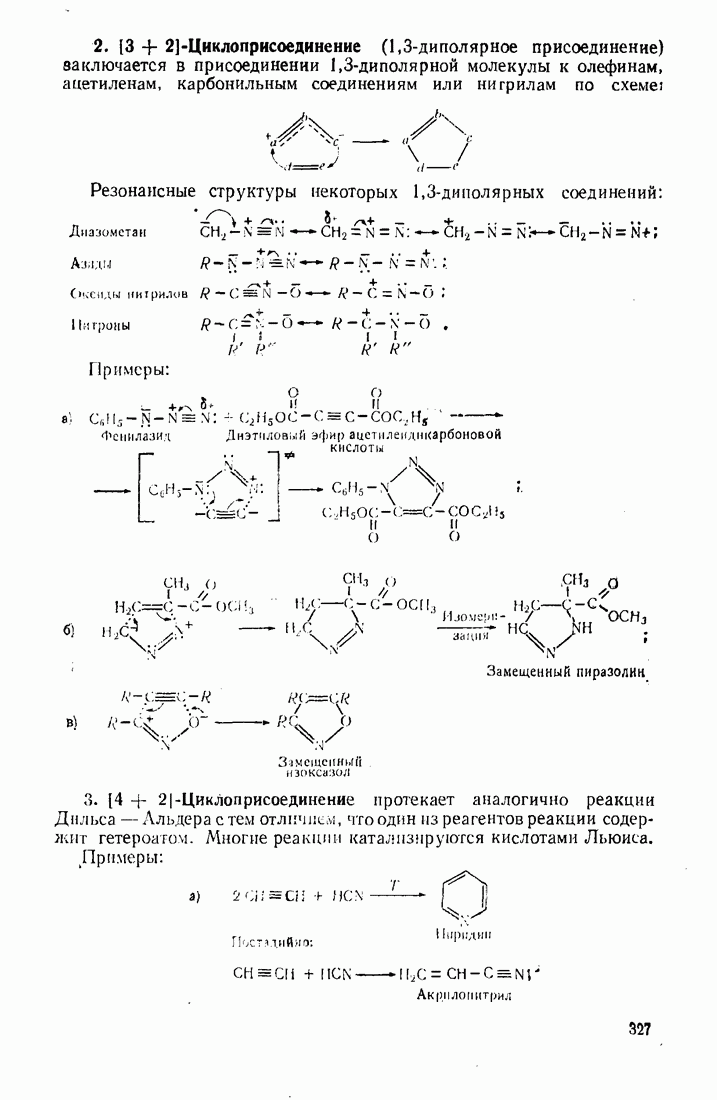
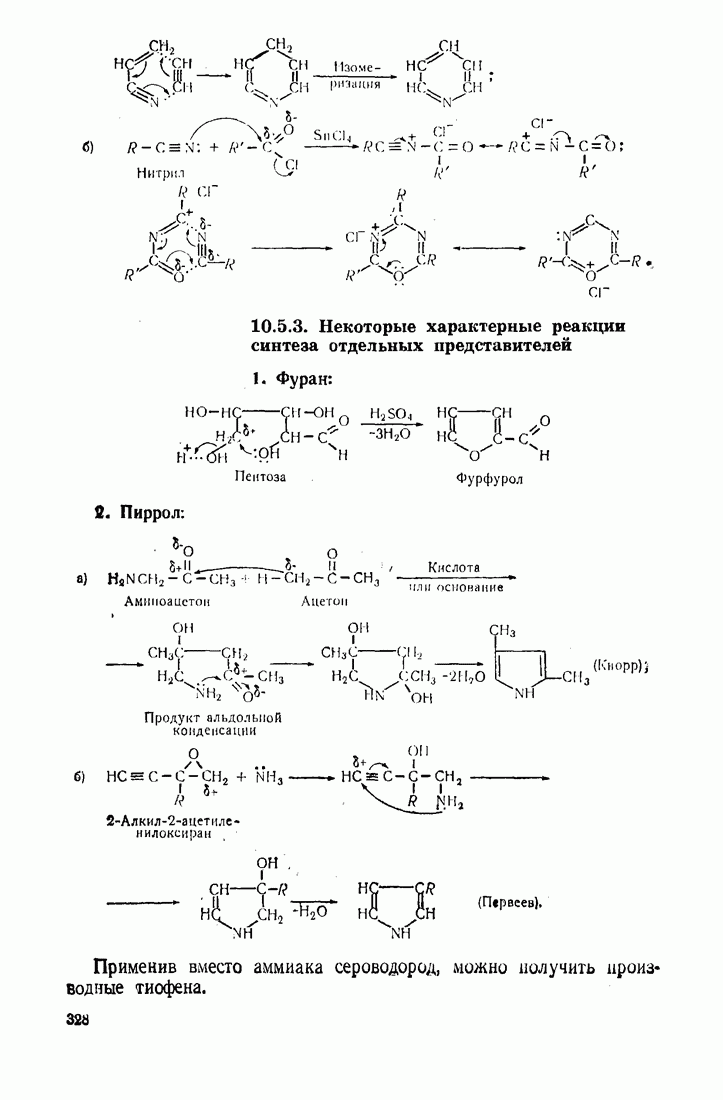
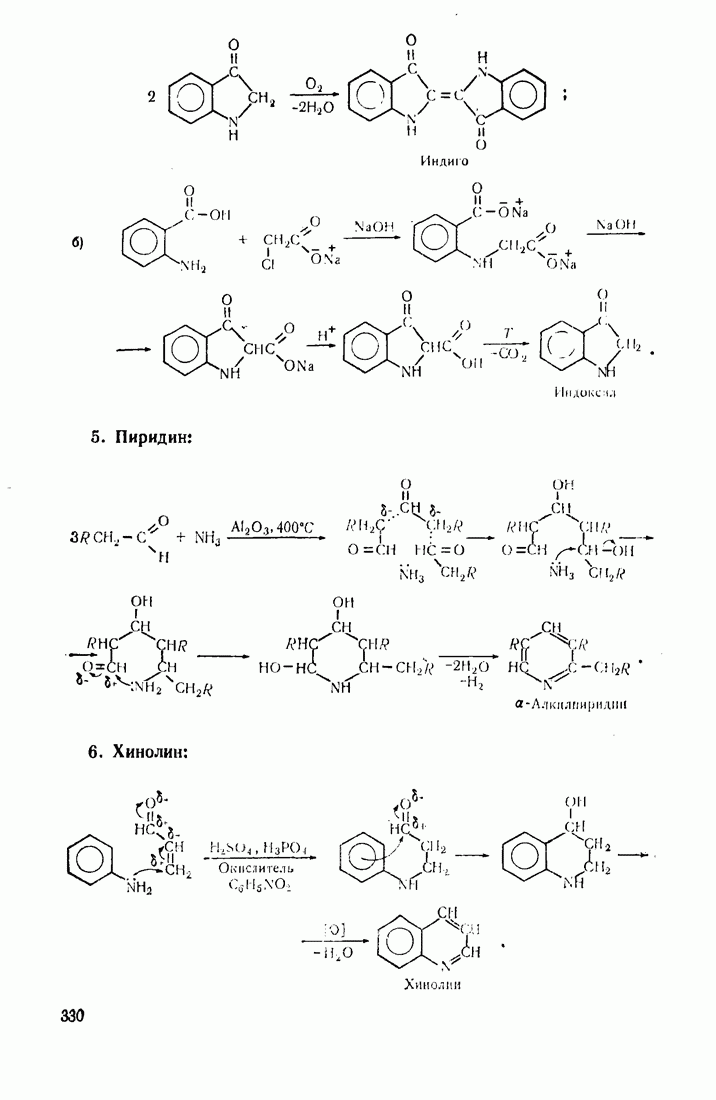
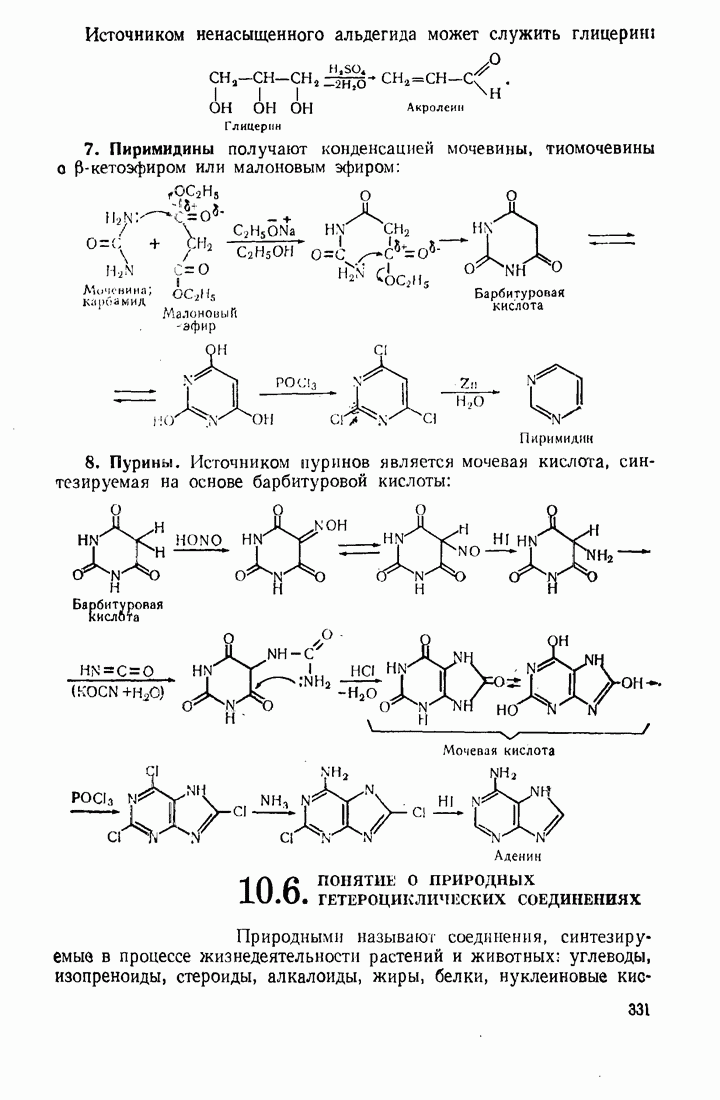
- 10.5. МЕТОДЫ СИНТЕЗА ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ
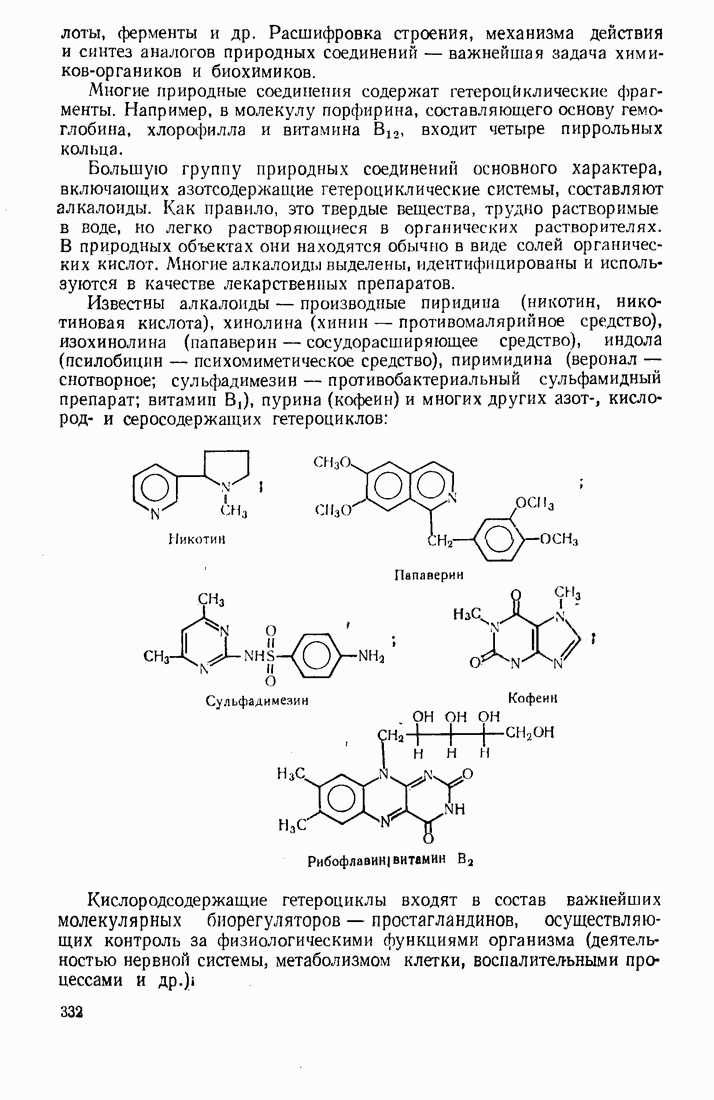
- 10.6. П0НЯТИЕ О ПРИРОДНЫХ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЯХ
- 11. Зпементоорганические соединения
- 11.2. ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ НЕКОТОРЫХ НЕМЕТАЛЛОВ
- 11.3. МЕГАЛЛООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- 11.4. ОРГАНИЧЕСКИЕ ПРОИЗВОДНЫЕ ПЕРЕХОДНЫХ МЕТАЛЛОВ
- 12. Сырье и основные направления развития промышленности органического синтеза
- 12.1.1. Нефть и сопутствующий природный газ
- 12.1.2. Углехимическое сырье
- 12.1.3. Лесохимическое и сельскохозяйственное сырье
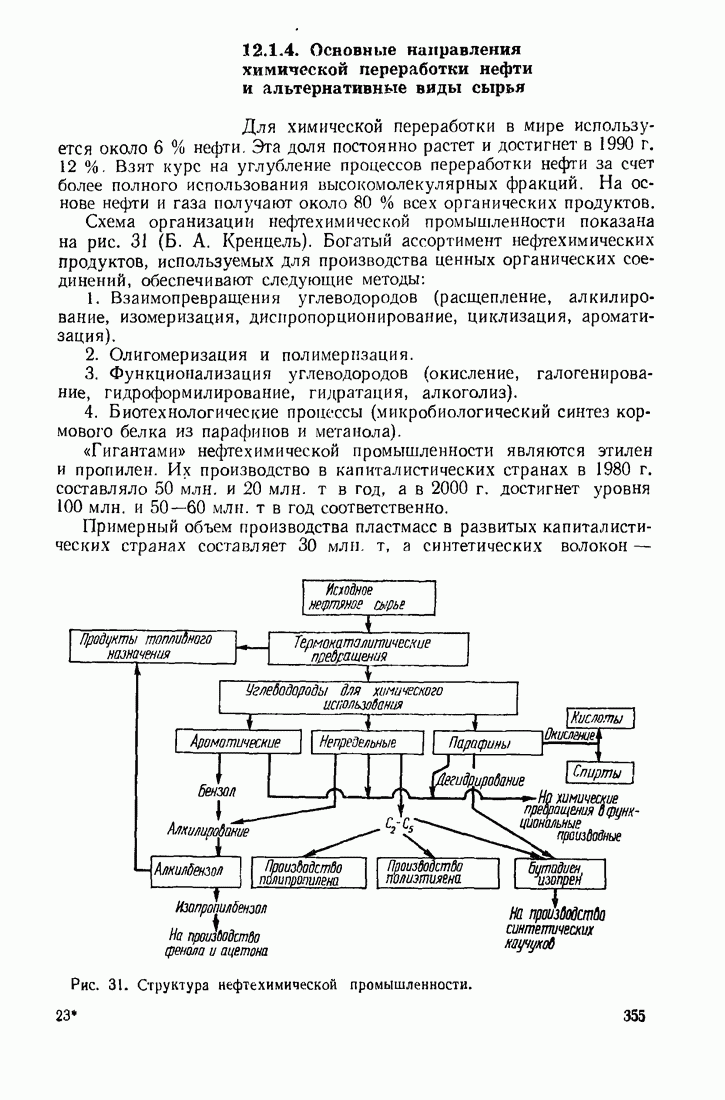
- 12.1.4. Основные направления химической переработки нефти и альтернативные виды сырья
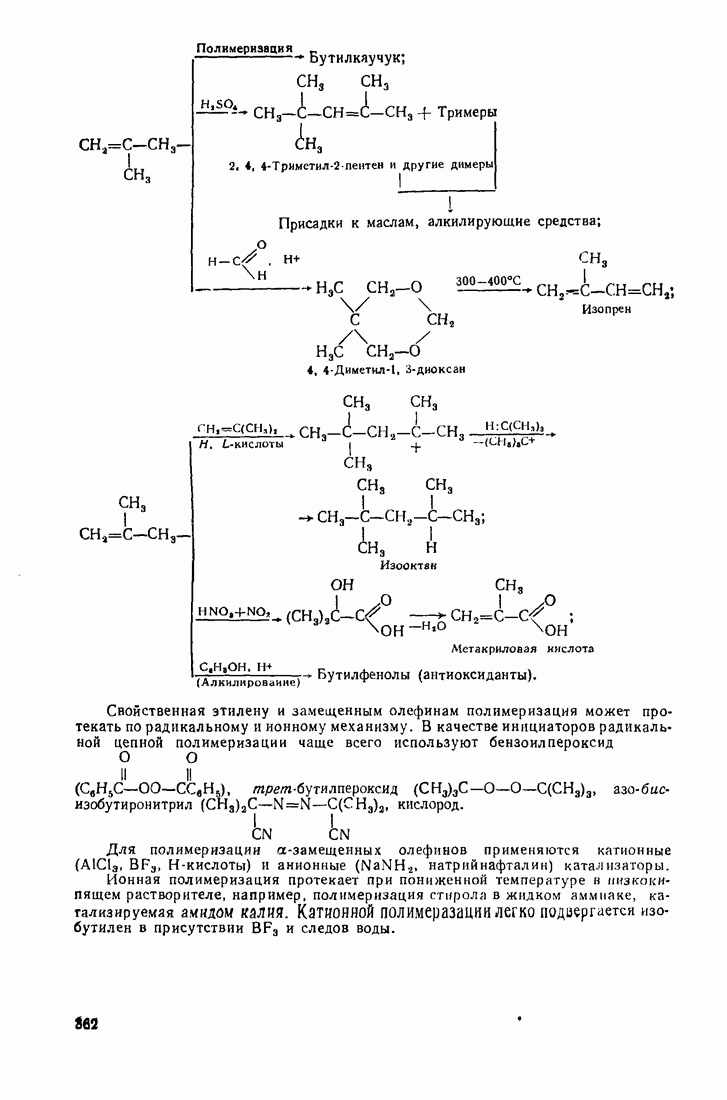
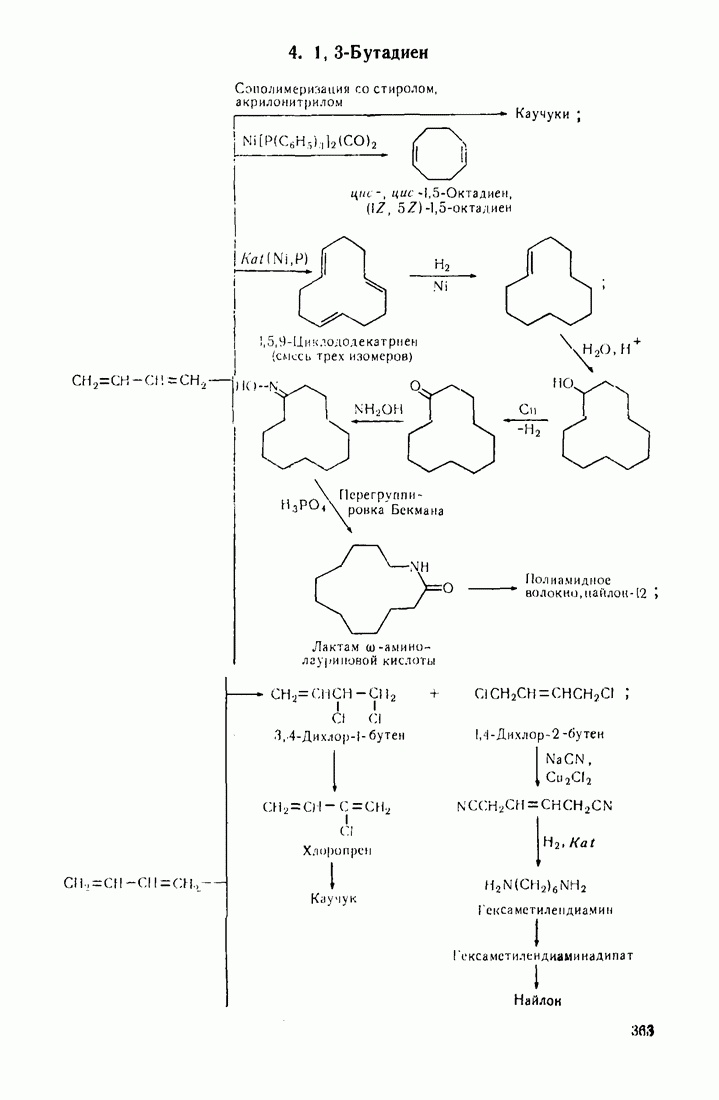
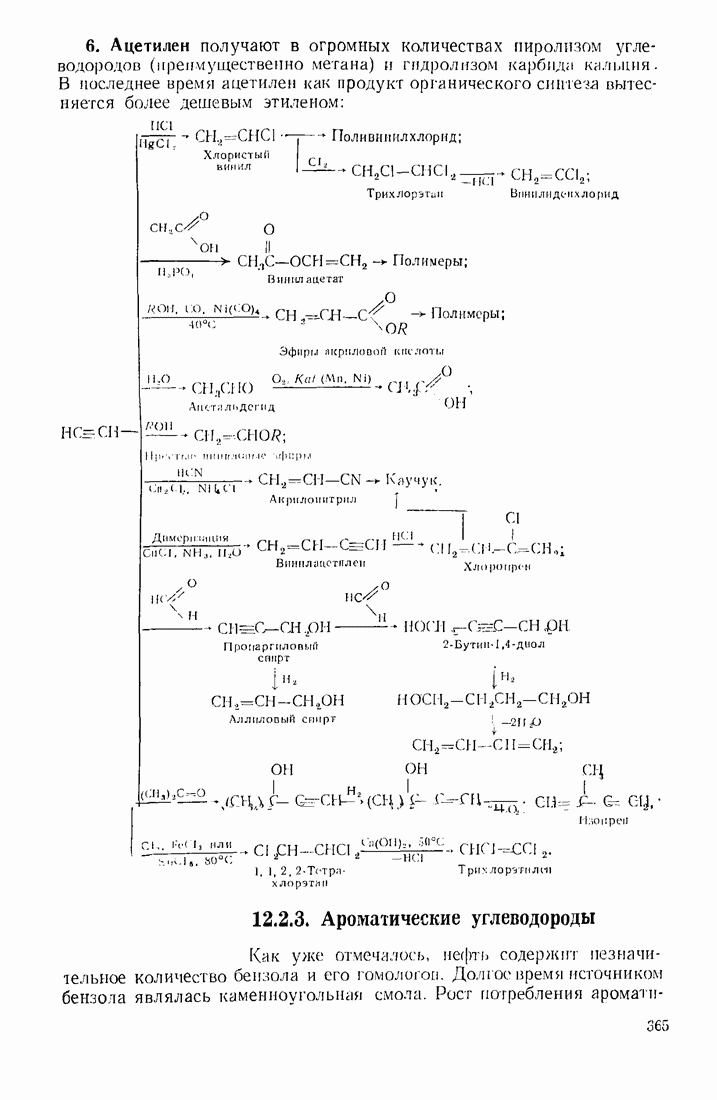
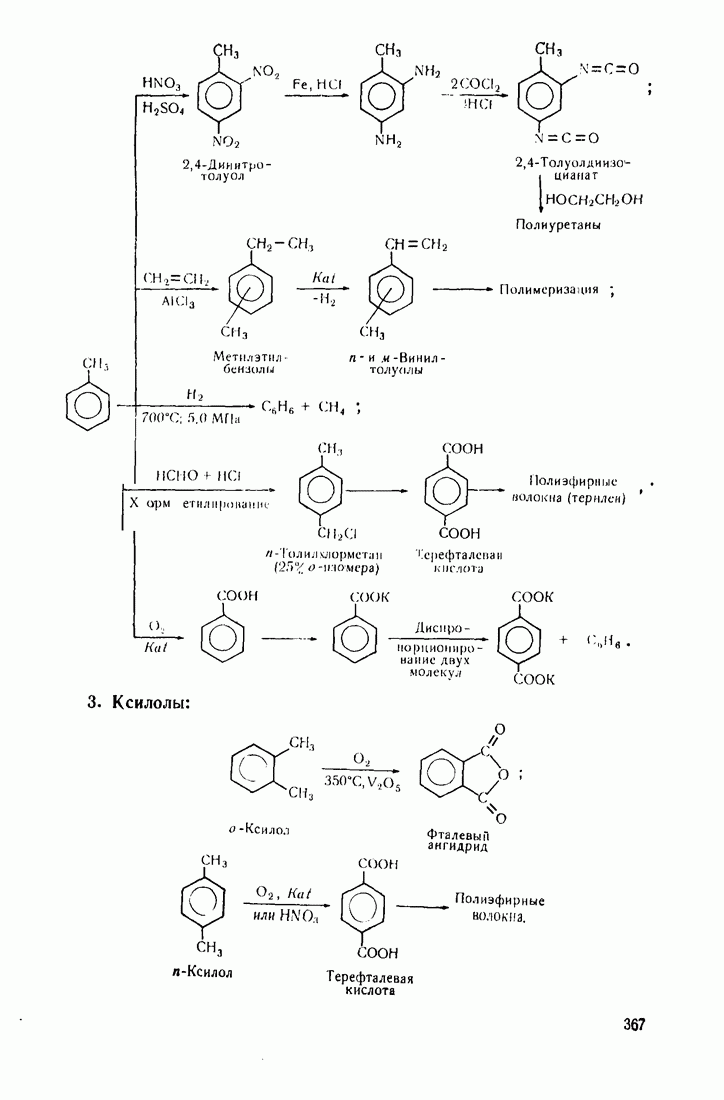
- 12.2. ПУТИ ИСПОЛЬЗОВАНИЯ УГЛЕВОДОРОДОВ И ИХ ПРОИЗВОДНЫХ
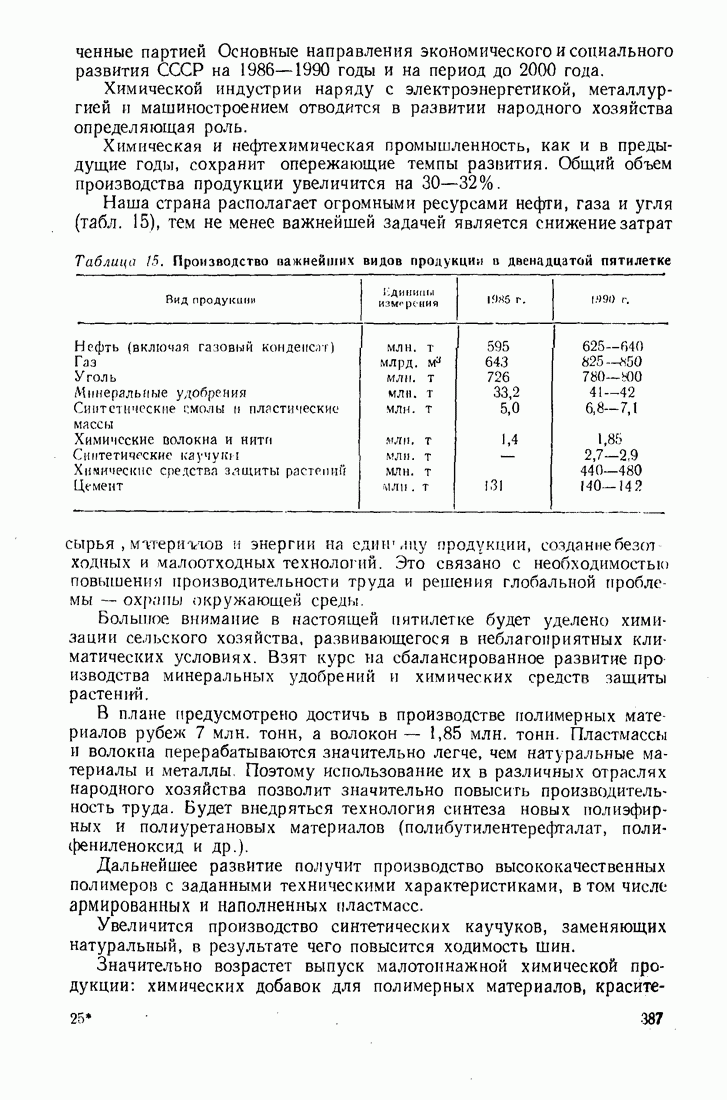
- 12.3. РАЗВИТИЕ ХИМИЧЕСКОЙ ПРОМЫШЛЕННОСТИ В СССР В ДВЕНАДЦАТОЙ ПЯТИЛЕТКЕ