| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
29.32. Модификация и сортировка гликопротеинов происходит в аппарате Гольджи
Белки, находящиеся во внутреннем пространстве ЭР и в его мембране, переносятся в аппарат Гольджи - стопку уплощенных мембранных мешков (рис. 29.47). В этой органелле олигосахаридное «ядро» гликопротеинов удаляется и к ним присоединяются новые сахара. Кроме того, аппарат Гольджи сортирует и упаковывает гликопротеины для транспортировки в другие участки клетки. Гликопротеины доставляются из ЭР к выпуклой поверхности аппарата Гольджи в пузырьках диаметром 500 А, окруженных оболочкой, покрытой чем-то вроде щетинок (рис. 29.48). Эта оболочка представляет собой многогранную решетчатую структуру, состоящую из субъединиц клатрина массой  (рис. 29.49). Эти так называемые окаймленные пузырьки отпочковываются от ЭР и затем сливаются с аппаратом Гольджи. Кроме того, они переносят мембранные белки от вогнутой поверхности аппарата Гольджи в лизосомы, к плазматической мембране и в другие участки клетки. К тому же окаймленные пузырьки переносят белки и липиды от плазматической мембраны к внутренним мембранам. Таким образом, клатрин играет ключевую роль в переносе фрагментов мембраны в пределах клетки. Важно отметить, что во время этих процессов переноса асимметрия мембран сохраняется. Внутренняя поверхность мембраны окаймленного пузырька и аппарата Гольджи соответствует внутренней стороне мембраны ЭР.
(рис. 29.49). Эти так называемые окаймленные пузырьки отпочковываются от ЭР и затем сливаются с аппаратом Гольджи. Кроме того, они переносят мембранные белки от вогнутой поверхности аппарата Гольджи в лизосомы, к плазматической мембране и в другие участки клетки. К тому же окаймленные пузырьки переносят белки и липиды от плазматической мембраны к внутренним мембранам. Таким образом, клатрин играет ключевую роль в переносе фрагментов мембраны в пределах клетки. Важно отметить, что во время этих процессов переноса асимметрия мембран сохраняется. Внутренняя поверхность мембраны окаймленного пузырька и аппарата Гольджи соответствует внутренней стороне мембраны ЭР.

Рис. 29.46. Активированное олигосахаридное ядро синтезируется путем последовательного присоединения отдельных остатков сахаров. Затем весь блок переносится на боковую цепь определенного остатка аспарагина новообразованного белка во внутреннем пространстве ЭР.
Когда окаймленные пузырьки сливаются с плазматической мембраной, их внутренняя поверхность становится наружной поверхностью плазматической мембраны. Следовательно, внутренние

Рис. 29.47. Электронная микрофотография (вверху) и схематическое изображение (внизу) аппарата Гольджи. В этой органелле происходит модификация, сортировка и упаковка гликопротеинов. (Электронная микрофотография печатается с любезного разрешения д-ра Lynne Mercer.)
поверхности мембраны ЭР и других органелл соответствуют наружной поверхности плазматической мембраны (рис. 29.50). По этой причине углеводные группы гликопротеинов плазматической мембраны всегда расположены на ее наружной поверхности (разд. 10.12).
В аппарате Гольджи происходит перестройка олигосахаридных групп гликопротеинов. Единственная оставшаяся глюкоза и несколько оставшихся манноз олигосахаридного «ядра» удаляются. На этом формирование углеводных остатков некоторых гликопротеинов заканчивается. Более сложные олигосахариды других гликопротеинов образуются путем последовательного присоединения сахаров к остаткам

Рис. 29.48. Электронная микрофотография окаймленных пузырьков (вверху). Схема окаймленного пузырька. (Печатается с любезного разрешения д-ра Barbara Pearse.)

Рис. 29.49. Изображение реконструированного окаймленного пузырька. Оно получено наложением многих электронных микрофотографий. [Woodwart M, Р., Roth Т. F., J. Supramol. Structure, 11, 240 (1979).]

Рис. 29.50. Асимметрия клеточных мембран. Внутренние поверхности ЭР и других органелл соответствуют наружной поверхности плазматической мембраны.
«ядра». Например, в качестве активированных доноров при синтезе концевого три-сахаридного остатка, обнаруженного в некоторых гликопротеинах, выступают UDP-N-ацетилглюкозамин, UDP-галактоза и СМР-нейраминидат (рис. 29.51). Этот последний этап биосинтеза, протекающий в аппарате Гольджи, получил название окончательного гликозилирования - в отличие от гликозилирования олигосахаридного «ядра», которое происходит в ЭР.
Как происходит сортировка гликопротеинов в аппарате Гольджи? Каким путем они доставляются в места назначения? Ответа на эти интригующие вопросы пока нет, но ключом к пониманию проблемы может послужить болезнь I-клеток (ее также называют муколипидозом II). Это нарушение функции лизосом наследуется как аутосомный рецессивный признак и характеризуется сильной задержкой психомоторного развития и деформацией скелета. Лизосомы в соединительных тканях больных содержат крупные включения (название болезни происходит от англ. inclusion - включение) непереваренных гликозаминогликанов и гликолипидов. Наличие этих включений обусловлено отсутствием в лизосомах больных по меньшей мере восьми ферментов, необходимых для их расщепления. В то же время огромные количества этих ферментов обнаруживаются в моче и крови больных. Следовательно, синтез активных ферментов при болезни I-клеток происходит, но вместо того, чтобы запасаться в лизосомах, они экспортируются из клетки. Другими словами. при болезни I-клеток целый ряд ферментов локализуется в неправильном месте. Эти ферменты не содержат маннозо-6-фосфата, который обычно с ними связан. Следовательно, маннозо-6-фосфат, по всей вероятности, представляет собой маркер, направляющий в норме многие гидролитические ферменты из аппарата Гольджи в лизосомы. Интересно выяснить, участвуют ли углеводные остатки других гликопротеинов в регуляции внутриклеточных передвижений.
Заключение
Эукариотическая хромосома содержит одну молекулу двухспиральной ДНК, которая по крайней мере в 100 раз длиннее, чем молекулы ДНК в клетках прокариот. ДНК прочно связана с основными белками, которые называются гистонами. Хроматиновая нить представляет собой гибкую цепь нуклеосом. «Ядро» этого повторяющегося элемента (минимальная нуклеосома, кор) содержит фрагмент ДНК длиной 140 пар оснований, накрученный на октамер гистонов, в состав которого входят по две молекулы гистонов  Минимальные нуклеосомы соединены между собой линкерной ДНК, длина которой обычно составляет 60 пар оснований, связанной с одной молекулой гистона
Минимальные нуклеосомы соединены между собой линкерной ДНК, длина которой обычно составляет 60 пар оснований, связанной с одной молекулой гистона  Благодаря нуклеосомам ДНК может укорачиваться в семь раз. Это - первый уровень конденсации ДНК. Эукариотическая ДНК реплицируется полуконсервативным путем и наполовину непрерывно (т.е. получает по одной из родительских цепей), причем репликация
Благодаря нуклеосомам ДНК может укорачиваться в семь раз. Это - первый уровень конденсации ДНК. Эукариотическая ДНК реплицируется полуконсервативным путем и наполовину непрерывно (т.е. получает по одной из родительских цепей), причем репликация

Рис. 29.51. Завершающая стадия синтеза содержащего нейраминидат углеводного остатка гликопротеина (трансферрина человека). Эта реакция происходит в аппарате Гольджи.
начинается в нескольких тысячах мест. Большое число точек инициации обусловлено огромной длиной эукариотической ДНК по сравнению с прокариотической.
Кинетика реассоциации денатурированной нагреванием ДНК показывает, что эукариотическая ДНК в отличие от прокариотической содержит много повторяющихся последовательностей оснований. ДНК с большим числом повторов (сателлитная ДНК) обычно расположена вблизи от центромер. Некоторые сателлитные ДНК представляют собой гептануклеотидную последовательность, повторенную более  раз. Другая фракция ДНК с умеренным числом повторов. В геноме многих эукариот гены рибосомных РНК и гистонов присутствуют в количестве десятков или сотен копий. Большая часть ДНК с умеренным числом повторов играет, по-видимому, какую-то регуляторную роль. Третья фракция - уникальная ДНК. Она состоит из последовательностей, которые встречаются в гаплоидном геноме только один или несколько раз. Многие из таких белков, как фиброин шелка, гемоглобин и овальбумин, кодируются уникальными генами. Эти гены дают большие количества стабильной мРНК. Уникальные последовательности обычно перемежаются с умеренно повторяющимися последовательностями. Кроме того, для высших эукариот характерно наличие вставочных последовательностей во многих генах, кодирующих белки.
раз. Другая фракция ДНК с умеренным числом повторов. В геноме многих эукариот гены рибосомных РНК и гистонов присутствуют в количестве десятков или сотен копий. Большая часть ДНК с умеренным числом повторов играет, по-видимому, какую-то регуляторную роль. Третья фракция - уникальная ДНК. Она состоит из последовательностей, которые встречаются в гаплоидном геноме только один или несколько раз. Многие из таких белков, как фиброин шелка, гемоглобин и овальбумин, кодируются уникальными генами. Эти гены дают большие количества стабильной мРНК. Уникальные последовательности обычно перемежаются с умеренно повторяющимися последовательностями. Кроме того, для высших эукариот характерно наличие вставочных последовательностей во многих генах, кодирующих белки.
РНК в эукариотических клетках синтезируется тремя типами РНК-полимераз. Первичные транскрипты претерпевают существенные изменения, прежде чем они перейдут из ядра в цитозоль в виде зрелых молекул рРНК, тРНК и мРНК. Информационные РНК получаются из гораздо более длинных первичных транскриптов (мРНК) путем расщепления и воссоединения фрагментов. Эукариотическая информационная РНК имеет на  -конце «колпачок» и на 3-конце обычно длинную
-конце «колпачок» и на 3-конце обычно длинную  -последовательность. Единственный транслируемый участок мРНК обрамлен некодирующими последовательностями, иногда очень длинными. Набор мРНК в эукариотической клетке зависит от избирательного процессинга первичных транскриптов, а также от скорости транскрипции различных генов. Регуляция на уровне трансляции, по-видимому, играет менее важную роль при детерминировании набора белков, синтезируемых каждой данной клеткой.
-последовательность. Единственный транслируемый участок мРНК обрамлен некодирующими последовательностями, иногда очень длинными. Набор мРНК в эукариотической клетке зависит от избирательного процессинга первичных транскриптов, а также от скорости транскрипции различных генов. Регуляция на уровне трансляции, по-видимому, играет менее важную роль при детерминировании набора белков, синтезируемых каждой данной клеткой.  -рибосома эукариот состоит из
-рибосома эукариот состоит из  и
и  -субчастиц. Как и у прокариот, у эукариот имеется особая инициаторная тРНК, но она не формилирована. Инициация у эукариот регулируется каскадом протеинкиназ, инактивирующих один из факторов инициации
-субчастиц. Как и у прокариот, у эукариот имеется особая инициаторная тРНК, но она не формилирована. Инициация у эукариот регулируется каскадом протеинкиназ, инактивирующих один из факторов инициации  Митохондрии и хлоропласты содержат собственную ДНК, которая не связана с гистонами. Синтез белка в этих органеллах
Митохондрии и хлоропласты содержат собственную ДНК, которая не связана с гистонами. Синтез белка в этих органеллах
напоминает синтез белка у бактерий.
Секреторные и мембранные белки синтезируются рибосомами, связанными с эндоплазматическим ретикулумом. Многие из этих белков содержат сильно гидрофобную N-концевую последовательность, которая служит сигналом для прикрепления рибосомы к мембране ЭР. Затем синтезирующаяся полипептидная цепь активно протягивается через мембрану ЭР, а сигнальная последовательность отщепляется на внутренней стороне. Почти ко всем белкам, синтезированным на связанных с мембранами полисомах, ковалентно присоединяется один или несколько углеводных остатков. В ЭР происходит перенос универсального олигосахаридного блока с активированного донора долихола на специфическую аспарагиновую боковую цепь. Гликопротеины переносятся из ЭР в аппарат Гольджи в окаймленных пузырьках. Эти пузырьки, покрытые клатрином, участвуют во многих процессах обмена между мембранными структурами. В аппарате Гольджи происходит укорачивание и окончательное гликозилирование олигосахаридных остатков. Кроме того, здесь гликопротеины сортируются и отправляются по назначению. Углеводные остатки, по-видимому, играют важную роль в этом процессе сортировки.

Рис. 29.52. Электронная микрофотография окаймленных пузырьков, лежащих на плазматической мембране клетки. (Печатается с любезного разрешения д-ра John Heuser.)
РЕКОМЕНДУЕМАЯ ЛИТЕРАТУРА
(см. скан)
(см. скан)
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ГЛАВА 24. ДНК: генетическая роль, структура и репликация
- 24.2. Трансформация пневмококков с помощью ДНК показала, что гены состоят из ДНК
- 24.3. Гены некоторых вирусов состоят из РНК
- 24.4. Двойная спираль ДНК Уотсона-Крика
- 24.5. Комплементарные цепи служат матрицами друг для друга при репликации ДНК
- 24.6. Репликация ДНК полуконсервативна
- 24.7. Некоторые вирусы содержат на определенных стадиях жизненного цикла одноцепочечную ДНК
- 24.8. Молекулы ДНК очень длинные
- 24.9. Двойная спираль может быть обратимо расплавлена
- 24.10. Некоторые молекулы ДНК имеют кольцевую форму
- 24.11. Кольцевые двухспиральные молекулы ДНК могут находиться в суперспирализованном состоянии
- 24.12. Открытие ДНК-полимеразы
- 24.13. ДНК-полимераза получает инструкции от матрицы
- 24.14. ДНК-полимераза I исправляет ошибки в ДНК
- 24.15. ДНК-лигаза соединяет фрагменты ДНК
- 24.16. Открытие ДНК-полимераз II и III
- 24.17. Расплетание родительской ДНК и синтез новой ДНК происходят в репликационной вилке
- 24.18. Репликация ДНК начинается в строго определенном месте и продолжается последовательно в обоих направлениях
- 24.19. Одна цепь ДНК синтезируется прерывисто
- 24.20. Затравкой синтеза ДНК служит РНК
- 24.21. Энергия гидролиза АТР используется для расплетания родительской ДНК в области репликационной вилки под действием белка rep
- 24.22. ДНК-гираза вводит отрицательные супервитки в родительскую ДНК, чтобы облегчить ее расплетание
- 24.23. Сложность аппарата репликации, по-видимому, необходима для обеспечения очень высокой надежности
- 24.24. Повреждения ДНК постоянно репарируются
- 24.25. Рак кожи при золотистой ксеродерме обусловлен нарушением нормальной репарации ДНК
- 24.26. ДНК содержит тимин вместо урацила, что делает возможной репарацию дезаминированного цитозина
- 24.27. Рестриктирующие эндонуклеазы совершили переворот в анализе ДНК
- 24.28. Последовательность нуклеотидов в ДНК можно быстро определить с помощью специфического химического расщепления
- 24.29. Полная последовательность оснований ДНК фага фХ174 была определена с помощью метода ферментативной репликации
- ГЛАВА 25. Информационная РНК и транскрипция
- 25.1. Структура РНК
- 25.2. Клетки содержат три типа РНК: рибосомную, транспортную и информационную
- 25.3. Формулирование концепции информационной РНК
- 25.4. Экспериментальные данные о существовании информационной РНК-посредника в синтезе белка
- 25.5. Опыты по гибридизации показали, что информационная РНК комплементарна кодирующей ее ДНК-матрице
- 25.6. Рибосомные РНК и транспортные РНК также синтезируются на ДНК-матрице
- 25.7. Все клеточные РНК синтезирует РНК-полимеразa
- 25.8. РНК-полимераза получает инструкции от ДНК-матрицы
- 25.9. Обычно в данном участке генома транскрибируется только одна цепь ДНК
- 25.10. РНК-полимераза Е. coli состоит из субъединиц
- 25.11. Транскрипция инициируется на промоторных участках матричной ДНК
- 25.12. сигма-Субъединица обеспечивает узнавание промоторных участков РНК-полимеразой
- 25.13. Цепи РНК начинаются с pppG или рррА
- 25.14. Цепи РНК синтезируются в направлении …
- 25.15. Матричная ДНК содержит стоп-сигналы для транскрипции
- 25.16. Белок р участвует в терминировании транскрипции
- 25.17. Многие молекулы РНК после транскрипции расщепляются и химически модифицируются
- 25.18. Антибиотики — ингибиторы транскрипции: рифамицин и актиномицин
- 25.19. Разработаны совершенные методы определения последовательности нуклеотидов в РНК
- ГЛАВА 26. Генетический код и зависимость между генами и белками
- 26.1. Транспортная РНК — адапторная молекула в синтезе белка
- 26.2. Аминокислоты кодируются группами из трех оснований, начиная со строго определенной точки
- 26.3. Расшифровка генетического кода: синтетические РНК могут служить информационными РНК
- 26.4. Состав кодонов многих аминокислот был определен с помощью сополимеров в качестве матриц
- 26.5. Тринуклеотиды способствуют связыванию определенных молекул тРНК с рибосомами
- 26.6. Еще один инструмент расшифровки кода — сополимеры с определенной последовательностью
- 26.7. Основные свойства генетического кода
- 26.8. Сигналы инициации и терминации синтеза белка
- 26.10. Последовательность оснований гена и последовательность аминокислот соответствующего полипептида коллинеарны
- 26.11. Некоторые последовательности вирусных ДНК кодируют более одного белка
- 26.12. Гены эукариот представляют собой мозаику из транслируемых и нетранслируемых последовательностей ДНК
- 26.13. Мутации возникают в результате изменений последовательности оснований ДНК
- 26.14. Некоторые химические мутагены весьма специфичны
- 26.15. Многие мутагенные канцерогены можно выявить по их мутагенному действию на бактерии
- ГЛАВА 27. Синтез белка
- 27.1. Аминокислоты активируются и присоединяются к транспортным РНК под действием специфических синтетаз
- 27.2. Надежность синтеза белка определяется высокой специфичностью аминоацил-тРНК-синтетаз
- 27.3. Молекулы транспортных РНК имеют общий план строения
- 27.4. Транспортная РНК имеет L-образную форму
- 27.5. В узнавании кодона участвует антикодон, а не активированная аминокислота
- 27.6. Молекула транспортной РНК может узнавать более одного кодона благодаря «качаниям»
- 27.7. Мутантные молекулы транспортных РНК могут подавлять другие мутации
- 27.8. Рибосомы — органеллы, в которых происходит синтез белка, — состоят из большой и малой субчастиц
- 27.9. Рибосомы можно реконструировать из составляющих их молекул белков и РНК
- 27.10 Белки синтезируются в направлении от аминоконца к карбоксильному концу
- 27.11. Информационная РНК транслируется в направлении …
- 27.12. Одну молекулу мРНК одновременно транслирует несколько рибосом
- 27.13. Синтез белка в бактериях инициируется формилметиониновой тРНК
- 27.14. Сигналом инициации служит кодон AUG (или GUG), которому предшествует несколько оснований, способных спариваться с 16S-PHK
- 27.15. В результате образования инициирующего 70S-комплекса формил-метиониновая тРНК связывается с Р-участком
- 27.16. Фактор элонгации Tu доставляет аминоацил-тРНК в А-участок рибосомы
- 27.17. После образования пептидной связи происходит транслокация
- 27.18. Синтез белка терминируется факторами освобождения
- 27.19. Многие белки модифицируются после трансляции
- 27.20. Стрептомицин ингибирует инициацию и вызывает неправильное считывание информационной РНК
- 27.21. Пуромицин вызывает преждевременную терминацию цепи, так как имитирует амииоацилированную транспортную РНК
- 27.22. Некоторые короткие пептиды синтезируются без участия рибосом
- ГЛАВА 28. Регуляция выражения гена в фенотипе
- 28.2. Открытие регуляторного гена
- 28.3. Оперон — единица координированной генетической экспрессии
- 28.4. lас-Репрессор — тетрамерный белок
- 28.5. Последовательность оснований в lас-операторе симметрична
- 28.6. Циклический AMP стимулирует транскрипцию многих индуцибельных катаболических оперонов
- 28.7. Различные формы одного и того же белка активируют и ингибируют транскрипцию арабинозного оперона
- 28.8. Транскрипция триптофанового оперона регулируется и аттенюатором, и оператором
- 28.9. Аттенюация опосредуется трансляцией лидерной мРНК
- 28.10. Аттенюаторный участок гистидинового оперона содержит семь гистидиновых кодонов подряд
- 28.11. Репрессоры и активаторы детерминируют развитие умеренных фагов
- 28.12. Два оператора фага лямбда содержат ряд участков связывания репрессора
- 28.13. «лямбда»-Репрессор регулирует собственный синтез
- ГЛАВА 29. Эукариотические хромосомы и выражение генов у эукариот
- 29.1. Эукариотическая хромосома содержит одну молекулу двухспиральной ДНК
- 29.2. Эукариотическая ДНК прочно связана с основными белками — гистонами
- 29.3. Последовательности аминокислот в гистонах Н3 и Н4 почти одинаковы у всех животных и растений
- 29.4. Нуклеосомы — повторяющиеся субъединицы хроматина
- 29.5. Минимальная нуклеосома («ядро» нуклеосомы) состоит из ДНК длиной 140 пар оснований, намотанной на октамер гистонов
- 29.6. Нуклеосома — первый уровень конденсации ДНК
- 29.7. Репликация эукариотической ДНК начинается во многих местах и идет в двух направлениях
- 29.8. Новые гистоны образуют новые нуклеосомы на отстающей дочерней цепи ДНК
- 29.9. Митохондрии и хлоропласты содержат собственную ДНК
- 29.10. Эукариотическая ДНК содержит много повторяющихся последовательностей оснований
- 29.11. Высокоповторяющаяся ДНК (сателлитная ДНК) локализована в центромерах
- 29.12. Гены, кодирующие рибосомные РНК, расположены один за другим тандемно и повторяются несколько сот раз
- 29.13. Гены гистонов собраны вместе и повторяются тандемно много раз
- 29.14. Многие белки, синтезирующиеся в больших количествах, кодируются уникальными генами
- 29.15. Большинство уникальных генов перемежается повторяющимися последовательностями
- 29.16 Почти все гены высших эукариот, кодирующие белки, имеют разорванное строение
- 29.17. РНК в эукариотических клетках синтезируется тремя различными РНК-полимеразами
- 29.18. Грибной яд а-аманитин — мощный ингибитор РНК-полимеразы II
- 29.19. Специфические гены могут активироваться для транскрипции
- 29.20. Три вида рибосомных РНК образуются в результате процессинга одного первичного транскрипта
- 29.21. Информационные РНК избирательно образуются из больших ядерных предшественников РНК (гетерогенной ядерной РНК, мРНК)
- 29.22. На 5-конце мРНК находятся «колпачки», а на 3-конце, как правило, poly(А)-последовательности
- 29.23. Ферменты сплайсинга с высокой точностью удаляют интроны из первичных транскриптов разорванных генов
- 29.24. В настоящее время известны последовательности оснований многих информационных РНК
- 29.25. Эукариотическая рибосома (80S) состоит из малой (40S) и большой (60S) субчастиц
- 29.26. Талассемия — генетически обусловленное нарушение синтеза гемоглобина
- 29.27. Трансляция регулируется каскадом протеинкиназ, инактивирующим один из факторов инициации
- 29.28. Дифтерийный токсин блокирует синтез белка у эукариот, ингибируя транслокацию
- 29.29. Рибосомы, связанные с эндоплазматическим ретикулумом, синтезируют секреторные и мембранные белки
- 29.30. Сигнальные последовательности позволяют секреторным белкам проходить через мембрану эндоплазматического ретикулума
- 29.31. Присоединение сахарных остатков «ядра» к гликопротеинам происходит в эндоплазматическом ретикулуме при участии донора долихола
- 29.32. Модификация и сортировка гликопротеинов происходит в аппарате Гольджи
- ГЛАВА 30. Вирусы
- 30.1 Оболочка мелких вирусов состоит из множества идентичных белковых субъединиц
- 30.2. Самосборка вируса табачной мозаики (ВТМ)
- 30.3. При сборке вирусной частицы ВТМ белковые диски присоединяются к петле РНК
- 30.4. Заражение фагом Т4 полностью перестраивает синтез макромолекул в клетке E. coli
- 30.5. В упорядоченной сборке фага Т4 участвуют вспомогательные белки и протеазы
- 30.6. В репликации фага T4 участвует конкатемерный промежуточный продукт
- 30.7. ДНК фага Т4 вводится в преобразованную головку
- 30.8. Гибкость белка оболочки ВККТ позволяет ему образовывать икосаэдрический капсид
- 30.9. Бактериальные рестрикционные эндонуклеазы расщепляют чужеродные молекулы ДНК
- 30.10. Стратегия репликации РНК-содержащих вирусов
- 30.11. Белки вируса полиомиелита образуются путем множественного расщепления гигантского предшественника
- 30.12. С геномной РНК вируса везикулярною стоматита транскрибируется пять моноцистронных мРНК
- 30.13. Геном реовируса состоит из десяти различных молекул двухцепочечной РНК
- 30.14. Мелкие РНК-содержащие фаги содержат перекрывающиеся гены
- 30.15. Дарвиновская эволюция фаговой РНК вне клетки
- 30.16. Лизогенные фаги могут включать свою ДНК в состав ДНК клетки-хозяина
- 30.17. Ретровирусы и некоторые ДНК-содержащие вирусы могут вызывать рак у чувствительных клеток-хозяев
- 30.18. Вирусы SV-40 и полиомы могут вызывать продуктивную инфекцию или трансформацию клеток-хозяев
- 30.19. Ретровирусы содержат обратную транскриптазу, которая синтезирует двухспиральную ДНК, используя в качестве матрицы ( + )РНК
- 30.20. Ретровирусная ДНК транскрибируется только в том случае, если она интегрирована с геном клетки-хозяина
- 30.21. Киназа, кодируемая геном src вируса саркомы птиц, участвует в трансформации
- 30.22. Двухцепочечная РНК подавляет синтез белка в клетках, обработанных интерфероном
- ГЛАВА 31. Перестройки генов: рекомбинация, транспозиция и клонирование
- 31.1 В основе генетической рекомбинации лежат разрыв и воссоединение цепей ДНК
- 31.2. При генетической рекомбинации происходит спаривание гомологичных цепей ДНК с образованием двухцепочечного промежуточного продукта
- 31.3. Белок recA катализирует АТР-зависимый обмен цепей ДНК при генетической рекомбинации
- 31.4. Бактерии содержат плазмиды и другие подвижные генетические элементы
- 31.5. Фактор F позволяет бактериям передавать гены реципиентам путем конъюгации
- 31.6. Плазмиды факторы R придают бактериям устойчивость к антибиотикам
- 31.7. IS-элементы могут присоединяться к неродственным генам
- 31.8. В лаборатории можно сконструировать новые геномы и клонировать их в клетках-хозяевах
- 31.9. Ферменты рестрикции и ДНК-лигаза — необходимые инструменты для получения рекомбинантных молекул ДНК
- 31.10. Плазмиды и фаг лямбда — наиболее подходящие векторы для клонирования ДНК в бактериях
- 31.11. Из суммарной геномной ДНК, расщепленной рестриктирующими эндонуклеазами, можно выделить с помощью клонирования определенные эукариотические гены
- 31.12. Эукариотические гены могут транскрибироваться в бактериальных клетках
- 31.13. Химически синтезированный ген пептидного гормона соматостатина экспрессируется в клетках Е. coli
- 31.14. Перспективы клонирования генов
- ГЛАВА 32. Оболочки бактериальных клеток
- 32.1. Клеточная стенка — это огромная мешковидная макромолекула
- 32.2. Стадии синтеза пептидогликана
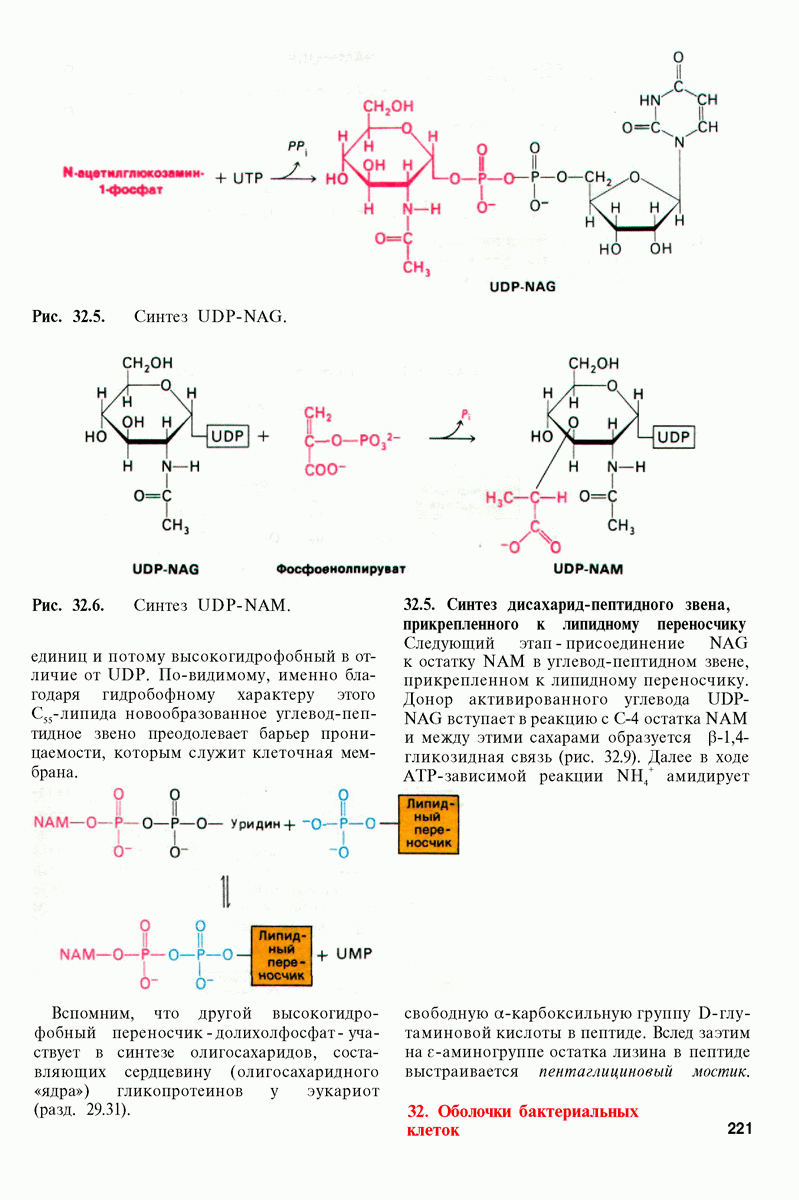
- 32.3. Синтез UDP-углевод-пептидного звена
- 32.4. Перенос углевод-пептидного звена на липидный переносчик
- 32.5. Синтез дисахарид-пептидного звена, прикрепленного к липидному переносчику
- 32.6. Перенос дисахарид-пептидного звена на растущую полисахаридную цепь
- 32.7. Поперечные мостики между полисахаридными цепями образуются в реакции транспептидирования
- 32.8. У грам-положительных бактерий пептидогликан покрыт тейхоевой кислотой
- 32.9. Пенициллин вызывает гибель растущих бактерий, ингибируя синтез клеточных стенок
- 32.10. Пенициллин блокирует синтез клеточных стенок путем ингибирования реакции транспептидирования
- 32.11. Некоторые бактерии резистентны к пенициллину, так как синтезируют разрушающий его фермент
- 32.12. Грам-отрицательные бактерии окружены наружной мембраной, богатой липополисахаридами
- 32.13. Благодаря разнообразию О-боковых цепей грам-отрицательные бактерии противостоят защитным силам организма-хозяина
- 32.14. Порин образует в наружной мембране каналы для небольших полярных молекул
- 32.15. Новообразованные белки наружной мембраны содержат отщепляемую сигнальную последовательность
- ГЛАВА 33. Иммуноглобулины
- 33.2. Синтез специфических антител в ответ на антиген
- 33.3. Участки антител, связывающие антиген, подобны активным центрам ферментов
- 33.4. Препараты антител с определенной специфичностью обычно гетерогенны
- 33.5. При ферментативном расщеплении иммуноглобулина G образуются активные фрагменты
- 33.6. Иммуноглобулин G состоит из L- и Н-цепей
- 33.7. Иммуноглобулин G — гибкая Y-образная молекула
- 33.8. Антитела образуются под действием отбора или инструкции?
- 33.9. Конец инструктивной теории
- 33.10. Иммуноглобулины миеломы и гибридомы гомогенны
- 33.11. Каждая L- и Н-цепь состоит из вариабельного и константного участков
- 33.12. Участок связывания антигена образован гипервариабельными фрагментами L- и Н-цепей
- 33.13. Вариабельная и константная области выполняют разные функции
- 33.14. Молекулы антител уложены с образованием компактных доменов, имеющих гомологичные последовательности
- 33.15. Рентгеноструктурный анализ связывающих участков антител показал, как происходит связывание некоторых гаптенов
- 33.16. Разные классы иммуноглобулинов различаются по биологической активности
- 33.17. Молекулы антител возникли в результате дупликации и последующей дивергенции генов
- 33.18. Вариабельные и константные области кодируются разными, но соединившимися генами
- 33.19. Как возникает разнообразие специфичности антител?
- 33.20. Вариабельные участки L- и Н-цепей кодируются несколькими сотнями генов
- 33.21. Открытие генов J (соединяющих) — дополнительного источника разнообразия антител
- 33.22. Соединение генов V и J в различных рамках также способствует разнообразию антител
- 33.23. мРНК для L- и Н-цепей образуются путем сращивания (сплайсинга) первичных продуктов транскрипции
- 33.24. Разные классы антител образуются в результате перескока генов …
- 33.25. Разнообразие антител обусловлено соматической рекомбинацией многих генов клеток зародышевого пути и соматической мутацией
- 33.26. Клонально-селекционная теория образования антител
- 33.27. На поверхности клеток, продуцирующих антитела, имеются рецепторы антигенов
- 33.28. Биологическое значение клональной селекции
- ГЛАВА 34. Мышечное сокращение и подвижность клеток
- 34.2. При мышечном сокращении происходит скольжение толстых и тонких нитей относительно друг друга
- 34.3. Миозин образует толстые нити; он гидролизует АТР и связывает актин
- 34.4. Миозин можно расщепить на активные фрагменты
- 34.5. Актин образует нити, которые соединяются с миозином
- 34.6. Актин повышает АТР-азную активность миозина
- 34.7. Толстые и тонкие нити мышечного волокна определенным образом ориентированы
- 34.8. Полярность толстых и тонких нитей в середине саркомера меняется на противоположную
- 34.9. «Рабочим ходом» является поворот связанной с актином S1-головки миозина
- 34.10. Тропонин и тропомиозин опосредуют регуляторное действие ионов кальция на мышечное сокращение
- 34.11. Поток ионов Са2+ регулируется саркоплазматическим ретикулумом
- 34.12. Фосфокреатин — форма запасания ~P
- 34.13. Актин и миозин служат сократительными элементами почти во всех эукариотических клетках
- 34.14. Распределение микрофиламентов в клетке выявляется методом иммунофлуоресцентной микроскопии
- 34.15. Прикрепленные к мембране нити актина опосредуют сокращение микроворсинок кишечника
- 34.16. Цитохалазин и фаллоидин тормозят подвижность, сопряженную с процессами сборки и дезагрегации нитей актина
- 34.17. Микротрубочки участвуют в различных видах клеточной подвижности и частично формируют цитоскелет
- 34.18. Биение ресничек и движение жгутиков обусловлено скольжением микротрубочек, индуцированным динеином
- ГЛАВА 35. Действие гормонов
- 35.2. Циклический AMP синтезируется аденилатциклазой и расщепляется фосфодиэстеразой
- 35.3. сАМР служит вторым посредником при действии многих гормонов
- 35.4. Сопряжение рецепторов гормонов с аденилатциклазой осуществляется белком, связывающим гуаниннуклеотиды
- 35.5. Циклический AMP активирует протеинкиназы
- 35.6. Циклический AMP — эволюционно древний сигнал голодания
- 35.7. Холерный токсин стимулирует аденилаткиназу, ингибируя GTP-азную активность G-белка
- 35.8. Инсулин стимулирует анаболические процессы и ингибирует катаболические процессы
- 35.9. Препроинсулин и проинсулин — предшественники активного гормона
- 35.10. Трехмерная структура инсулина
- 35.11. Рецепторы инсулина локализованы в плазматической мембране клеток-мишеней
- 35.12. Недостаточность инсулина вызывает диабет
- 35.13. Эндорфины — пептиды мозга, действующие подобно опиатам
- 35.14. При расщеплении проопиокортина образуется несколько пептидных гормонов
- 35.15. Простагландины — модуляторы действия гормонов
- 35.16. Простагландины образуются из ненасыщенных жирных кислот
- 35.17. Стероидные гормоны активируют специфические гены
- 35.18. Белковые факторы роста типа ФРН и ЭФР стимулируют пролиферацию клеток-мишеней
- ГЛАВА 36. Мембранный транспорт
- 36.1. Различие между пассивным и активным транспортом
- 36.2. Открытие системы активного транспорта ионов натрия и калия
- 36.3. И фермент, и насос ориентированы в мембране
- 36.4. АТР транзиторно фосфорилирует натрий-калиевый насос
- 36.5. Транспорт ионов и гидролиз АТР тесно сопряжены
- 36.6. Натрий-калиевый насос — олигомерный трансмембранный белок
- 36.7. Модель механизма действия натрий-калиевого насоса
- 36.8. Кардиотонические стероиды — специфические ингибиторы (Na+ + + К+)-АТРазы и (Na+ + К)-насоса
- 36.9. Транспорт кальция осуществляется другой АТРазой
- 36.10. Поток Na+ обеспечивает энергией активный транспорт сахаров и аминокислот в животных клетках
- 36.11. Поток протонов служит движущей силой во многих процессах транспорта у бактерий
- 36.12. Активный транспорт ряда сахаров сопряжен с их фосфорилированием
- 36.13. Транспортные антибиотики повышают ионную проницаемость мембран
- 36.14. Транспортные антибиотики функционируют либо как подвижные переносчики, либо как каналообразователи
- 36.15. Антибиотики-переносчики имеют форму скорлупы ореха и связывают ионы в своей центральной полости
- 36.16. Валиномицин связывает К+ в 1000 раз прочнее, чем Na+
- 36.17. Можно выявить поток ионов через единичный канал в мембране
- 36.18. Через щелевые соединения ионы и небольшие молекулы перетекают из клетки в клетку
- ГЛАВА 37. Возбудимые мембраны и сенсорные системы
- 37.1. Потенциалы действия опосредованы кратковременными изменениями проницаемости для Na+ и К+
- 37.2. Тетродотоксин и сакситоксин блокируют натриевые каналы в мембранах аксонов нервных клеток
- 37.3. Ацетилхолин является нейромедиатором
- 37.4. Ацетилхолин открывает в постсинаптической мембране каналы для катионов
- 37.5. Ацетилхолин высвобождается квантами
- 37.6. При добавлении ацетилхолина реконструированные мембранные пузырьки становятся проницаемыми для катионов
- 37.7. Ацетилхолин быстро гидролизуется, и концевая пластинка реполяризуется
- 37.8. Ингибиторы ацетилхолинэстеразы используются как лекарственные средства и как яды
- 37.9. Разработка антидота для лечения отравлений органическими фосфатами
- 37.10. Ингибиторы ацетилхолинового рецептора
- 37.11. К числу нейромедиаторов относятся также катехоламины и у-аминомасляная кислота (ГАМК)
- 37.12. Для возбуждения палочки сетчатки глаза достаточно одного фотона
- 37.13. Родопсин — фоторецепторный белок палочек
- 37.14. Свет вызывает изомеризацию 11-цис-ретиналя
- 37.15. Свет вызывает гиперполяризацию плазматической мембраны наружного сегмента палочек
- 37.16. Медиаторы передают сигнал от фотолизированного родопсина на плазматическую мембрану
- 37.17. Свет снижает содержание циклического GMP путем активации фосфодиэстеразы
- 37.18. Цветовое зрение опосредуется фоторецепторами трех типов
- 37.19. 11-цис-ретиналь — хромофор всех известных органов зрения
- 37.20. Хеморецепторы бактерий воспринимают специфические молекулы и передают сигналы на жгутики
- 37.21. В основании бактериального жгутика находится вращающий его реверсивный «мотор»
- 37.22. Бактерии различают временной градиент, а не одномоментный пространственный градиент концентраций
- 37.23. При бактериальном хемотаксисе передача информации обеспечивается метилированными белками