| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
35.10. Трехмерная структура инсулина
В лаборатории Дороти Ходжкин (Dorothy Hodgkin) было проведено рентгеноструктурное исследование инсулина свиньи и раскрыта его трехмерная пространственная структура при разрешении 1,9 А. Эта работа была завершена почти через 36 лет после того, как Ходжкин получила первые рентгенограммы кристалла белка (пепсина), будучи студенткой-дипломницей в лаборатории Джона Бернала (John Bernal). За прошедшие годы Ходжкин расшифровала структуры таких

Рис. 35.13. Электрононграмма содержащих инсулин секреторных гранул в  -клетках поджелудочной железы. Инсулин образует в гранулах мелкие кристаллы, что обусловлено его высокой концентрацией в этих структурах. (Печатается с любезного разрешения д-ра Arthur Like.)
-клетках поджелудочной железы. Инсулин образует в гранулах мелкие кристаллы, что обусловлено его высокой концентрацией в этих структурах. (Печатается с любезного разрешения д-ра Arthur Like.)
биологически важных веществ, как холестерол, пенициллин и витамин  Инсулин оказался компактным трехмерным образованием (рис. 35.14), из которого «торчат» только
Инсулин оказался компактным трехмерным образованием (рис. 35.14), из которого «торчат» только  и С-концы В-цепи. Между этими двумя вытянутыми ветвями
и С-концы В-цепи. Между этими двумя вытянутыми ветвями  -цепи располагается А-цепь. Структура имеет неполярную сердцевину, образованную обращенными внутрь алифатическими боковыми цепями остатков аминокислот, принадлежащих А- и
-цепи располагается А-цепь. Структура имеет неполярную сердцевину, образованную обращенными внутрь алифатическими боковыми цепями остатков аминокислот, принадлежащих А- и  -цепям. Помимо дисульфидных мостиков, инсулин стабилизирован несколькими солевыми связями, а также водородными связями между определенными группами А- и
-цепям. Помимо дисульфидных мостиков, инсулин стабилизирован несколькими солевыми связями, а также водородными связями между определенными группами А- и  -цепей. Конформация проинсулина еще не исследована, но, судя по данным спектроскопии, она очень сходна с конформацией инсулина. Об этом же свидетельствует способность проинсулина кристаллизоваться вместе с инсулином.
-цепей. Конформация проинсулина еще не исследована, но, судя по данным спектроскопии, она очень сходна с конформацией инсулина. Об этом же свидетельствует способность проинсулина кристаллизоваться вместе с инсулином.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ГЛАВА 24. ДНК: генетическая роль, структура и репликация
- 24.2. Трансформация пневмококков с помощью ДНК показала, что гены состоят из ДНК
- 24.3. Гены некоторых вирусов состоят из РНК
- 24.4. Двойная спираль ДНК Уотсона-Крика
- 24.5. Комплементарные цепи служат матрицами друг для друга при репликации ДНК
- 24.6. Репликация ДНК полуконсервативна
- 24.7. Некоторые вирусы содержат на определенных стадиях жизненного цикла одноцепочечную ДНК
- 24.8. Молекулы ДНК очень длинные
- 24.9. Двойная спираль может быть обратимо расплавлена
- 24.10. Некоторые молекулы ДНК имеют кольцевую форму
- 24.11. Кольцевые двухспиральные молекулы ДНК могут находиться в суперспирализованном состоянии
- 24.12. Открытие ДНК-полимеразы
- 24.13. ДНК-полимераза получает инструкции от матрицы
- 24.14. ДНК-полимераза I исправляет ошибки в ДНК
- 24.15. ДНК-лигаза соединяет фрагменты ДНК
- 24.16. Открытие ДНК-полимераз II и III
- 24.17. Расплетание родительской ДНК и синтез новой ДНК происходят в репликационной вилке
- 24.18. Репликация ДНК начинается в строго определенном месте и продолжается последовательно в обоих направлениях
- 24.19. Одна цепь ДНК синтезируется прерывисто
- 24.20. Затравкой синтеза ДНК служит РНК
- 24.21. Энергия гидролиза АТР используется для расплетания родительской ДНК в области репликационной вилки под действием белка rep
- 24.22. ДНК-гираза вводит отрицательные супервитки в родительскую ДНК, чтобы облегчить ее расплетание
- 24.23. Сложность аппарата репликации, по-видимому, необходима для обеспечения очень высокой надежности
- 24.24. Повреждения ДНК постоянно репарируются
- 24.25. Рак кожи при золотистой ксеродерме обусловлен нарушением нормальной репарации ДНК
- 24.26. ДНК содержит тимин вместо урацила, что делает возможной репарацию дезаминированного цитозина
- 24.27. Рестриктирующие эндонуклеазы совершили переворот в анализе ДНК
- 24.28. Последовательность нуклеотидов в ДНК можно быстро определить с помощью специфического химического расщепления
- 24.29. Полная последовательность оснований ДНК фага фХ174 была определена с помощью метода ферментативной репликации
- ГЛАВА 25. Информационная РНК и транскрипция
- 25.1. Структура РНК
- 25.2. Клетки содержат три типа РНК: рибосомную, транспортную и информационную
- 25.3. Формулирование концепции информационной РНК
- 25.4. Экспериментальные данные о существовании информационной РНК-посредника в синтезе белка
- 25.5. Опыты по гибридизации показали, что информационная РНК комплементарна кодирующей ее ДНК-матрице
- 25.6. Рибосомные РНК и транспортные РНК также синтезируются на ДНК-матрице
- 25.7. Все клеточные РНК синтезирует РНК-полимеразa
- 25.8. РНК-полимераза получает инструкции от ДНК-матрицы
- 25.9. Обычно в данном участке генома транскрибируется только одна цепь ДНК
- 25.10. РНК-полимераза Е. coli состоит из субъединиц
- 25.11. Транскрипция инициируется на промоторных участках матричной ДНК
- 25.12. сигма-Субъединица обеспечивает узнавание промоторных участков РНК-полимеразой
- 25.13. Цепи РНК начинаются с pppG или рррА
- 25.14. Цепи РНК синтезируются в направлении …
- 25.15. Матричная ДНК содержит стоп-сигналы для транскрипции
- 25.16. Белок р участвует в терминировании транскрипции
- 25.17. Многие молекулы РНК после транскрипции расщепляются и химически модифицируются
- 25.18. Антибиотики — ингибиторы транскрипции: рифамицин и актиномицин
- 25.19. Разработаны совершенные методы определения последовательности нуклеотидов в РНК
- ГЛАВА 26. Генетический код и зависимость между генами и белками
- 26.1. Транспортная РНК — адапторная молекула в синтезе белка
- 26.2. Аминокислоты кодируются группами из трех оснований, начиная со строго определенной точки
- 26.3. Расшифровка генетического кода: синтетические РНК могут служить информационными РНК
- 26.4. Состав кодонов многих аминокислот был определен с помощью сополимеров в качестве матриц
- 26.5. Тринуклеотиды способствуют связыванию определенных молекул тРНК с рибосомами
- 26.6. Еще один инструмент расшифровки кода — сополимеры с определенной последовательностью
- 26.7. Основные свойства генетического кода
- 26.8. Сигналы инициации и терминации синтеза белка
- 26.10. Последовательность оснований гена и последовательность аминокислот соответствующего полипептида коллинеарны
- 26.11. Некоторые последовательности вирусных ДНК кодируют более одного белка
- 26.12. Гены эукариот представляют собой мозаику из транслируемых и нетранслируемых последовательностей ДНК
- 26.13. Мутации возникают в результате изменений последовательности оснований ДНК
- 26.14. Некоторые химические мутагены весьма специфичны
- 26.15. Многие мутагенные канцерогены можно выявить по их мутагенному действию на бактерии
- ГЛАВА 27. Синтез белка
- 27.1. Аминокислоты активируются и присоединяются к транспортным РНК под действием специфических синтетаз
- 27.2. Надежность синтеза белка определяется высокой специфичностью аминоацил-тРНК-синтетаз
- 27.3. Молекулы транспортных РНК имеют общий план строения
- 27.4. Транспортная РНК имеет L-образную форму
- 27.5. В узнавании кодона участвует антикодон, а не активированная аминокислота
- 27.6. Молекула транспортной РНК может узнавать более одного кодона благодаря «качаниям»
- 27.7. Мутантные молекулы транспортных РНК могут подавлять другие мутации
- 27.8. Рибосомы — органеллы, в которых происходит синтез белка, — состоят из большой и малой субчастиц
- 27.9. Рибосомы можно реконструировать из составляющих их молекул белков и РНК
- 27.10 Белки синтезируются в направлении от аминоконца к карбоксильному концу
- 27.11. Информационная РНК транслируется в направлении …
- 27.12. Одну молекулу мРНК одновременно транслирует несколько рибосом
- 27.13. Синтез белка в бактериях инициируется формилметиониновой тРНК
- 27.14. Сигналом инициации служит кодон AUG (или GUG), которому предшествует несколько оснований, способных спариваться с 16S-PHK
- 27.15. В результате образования инициирующего 70S-комплекса формил-метиониновая тРНК связывается с Р-участком
- 27.16. Фактор элонгации Tu доставляет аминоацил-тРНК в А-участок рибосомы
- 27.17. После образования пептидной связи происходит транслокация
- 27.18. Синтез белка терминируется факторами освобождения
- 27.19. Многие белки модифицируются после трансляции
- 27.20. Стрептомицин ингибирует инициацию и вызывает неправильное считывание информационной РНК
- 27.21. Пуромицин вызывает преждевременную терминацию цепи, так как имитирует амииоацилированную транспортную РНК
- 27.22. Некоторые короткие пептиды синтезируются без участия рибосом
- ГЛАВА 28. Регуляция выражения гена в фенотипе
- 28.2. Открытие регуляторного гена
- 28.3. Оперон — единица координированной генетической экспрессии
- 28.4. lас-Репрессор — тетрамерный белок
- 28.5. Последовательность оснований в lас-операторе симметрична
- 28.6. Циклический AMP стимулирует транскрипцию многих индуцибельных катаболических оперонов
- 28.7. Различные формы одного и того же белка активируют и ингибируют транскрипцию арабинозного оперона
- 28.8. Транскрипция триптофанового оперона регулируется и аттенюатором, и оператором
- 28.9. Аттенюация опосредуется трансляцией лидерной мРНК
- 28.10. Аттенюаторный участок гистидинового оперона содержит семь гистидиновых кодонов подряд
- 28.11. Репрессоры и активаторы детерминируют развитие умеренных фагов
- 28.12. Два оператора фага лямбда содержат ряд участков связывания репрессора
- 28.13. «лямбда»-Репрессор регулирует собственный синтез
- ГЛАВА 29. Эукариотические хромосомы и выражение генов у эукариот
- 29.1. Эукариотическая хромосома содержит одну молекулу двухспиральной ДНК
- 29.2. Эукариотическая ДНК прочно связана с основными белками — гистонами
- 29.3. Последовательности аминокислот в гистонах Н3 и Н4 почти одинаковы у всех животных и растений
- 29.4. Нуклеосомы — повторяющиеся субъединицы хроматина
- 29.5. Минимальная нуклеосома («ядро» нуклеосомы) состоит из ДНК длиной 140 пар оснований, намотанной на октамер гистонов
- 29.6. Нуклеосома — первый уровень конденсации ДНК
- 29.7. Репликация эукариотической ДНК начинается во многих местах и идет в двух направлениях
- 29.8. Новые гистоны образуют новые нуклеосомы на отстающей дочерней цепи ДНК
- 29.9. Митохондрии и хлоропласты содержат собственную ДНК
- 29.10. Эукариотическая ДНК содержит много повторяющихся последовательностей оснований
- 29.11. Высокоповторяющаяся ДНК (сателлитная ДНК) локализована в центромерах
- 29.12. Гены, кодирующие рибосомные РНК, расположены один за другим тандемно и повторяются несколько сот раз
- 29.13. Гены гистонов собраны вместе и повторяются тандемно много раз
- 29.14. Многие белки, синтезирующиеся в больших количествах, кодируются уникальными генами
- 29.15. Большинство уникальных генов перемежается повторяющимися последовательностями
- 29.16 Почти все гены высших эукариот, кодирующие белки, имеют разорванное строение
- 29.17. РНК в эукариотических клетках синтезируется тремя различными РНК-полимеразами
- 29.18. Грибной яд а-аманитин — мощный ингибитор РНК-полимеразы II
- 29.19. Специфические гены могут активироваться для транскрипции
- 29.20. Три вида рибосомных РНК образуются в результате процессинга одного первичного транскрипта
- 29.21. Информационные РНК избирательно образуются из больших ядерных предшественников РНК (гетерогенной ядерной РНК, мРНК)
- 29.22. На 5-конце мРНК находятся «колпачки», а на 3-конце, как правило, poly(А)-последовательности
- 29.23. Ферменты сплайсинга с высокой точностью удаляют интроны из первичных транскриптов разорванных генов
- 29.24. В настоящее время известны последовательности оснований многих информационных РНК
- 29.25. Эукариотическая рибосома (80S) состоит из малой (40S) и большой (60S) субчастиц
- 29.26. Талассемия — генетически обусловленное нарушение синтеза гемоглобина
- 29.27. Трансляция регулируется каскадом протеинкиназ, инактивирующим один из факторов инициации
- 29.28. Дифтерийный токсин блокирует синтез белка у эукариот, ингибируя транслокацию
- 29.29. Рибосомы, связанные с эндоплазматическим ретикулумом, синтезируют секреторные и мембранные белки
- 29.30. Сигнальные последовательности позволяют секреторным белкам проходить через мембрану эндоплазматического ретикулума
- 29.31. Присоединение сахарных остатков «ядра» к гликопротеинам происходит в эндоплазматическом ретикулуме при участии донора долихола
- 29.32. Модификация и сортировка гликопротеинов происходит в аппарате Гольджи
- ГЛАВА 30. Вирусы
- 30.1 Оболочка мелких вирусов состоит из множества идентичных белковых субъединиц
- 30.2. Самосборка вируса табачной мозаики (ВТМ)
- 30.3. При сборке вирусной частицы ВТМ белковые диски присоединяются к петле РНК
- 30.4. Заражение фагом Т4 полностью перестраивает синтез макромолекул в клетке E. coli
- 30.5. В упорядоченной сборке фага Т4 участвуют вспомогательные белки и протеазы
- 30.6. В репликации фага T4 участвует конкатемерный промежуточный продукт
- 30.7. ДНК фага Т4 вводится в преобразованную головку
- 30.8. Гибкость белка оболочки ВККТ позволяет ему образовывать икосаэдрический капсид
- 30.9. Бактериальные рестрикционные эндонуклеазы расщепляют чужеродные молекулы ДНК
- 30.10. Стратегия репликации РНК-содержащих вирусов
- 30.11. Белки вируса полиомиелита образуются путем множественного расщепления гигантского предшественника
- 30.12. С геномной РНК вируса везикулярною стоматита транскрибируется пять моноцистронных мРНК
- 30.13. Геном реовируса состоит из десяти различных молекул двухцепочечной РНК
- 30.14. Мелкие РНК-содержащие фаги содержат перекрывающиеся гены
- 30.15. Дарвиновская эволюция фаговой РНК вне клетки
- 30.16. Лизогенные фаги могут включать свою ДНК в состав ДНК клетки-хозяина
- 30.17. Ретровирусы и некоторые ДНК-содержащие вирусы могут вызывать рак у чувствительных клеток-хозяев
- 30.18. Вирусы SV-40 и полиомы могут вызывать продуктивную инфекцию или трансформацию клеток-хозяев
- 30.19. Ретровирусы содержат обратную транскриптазу, которая синтезирует двухспиральную ДНК, используя в качестве матрицы ( + )РНК
- 30.20. Ретровирусная ДНК транскрибируется только в том случае, если она интегрирована с геном клетки-хозяина
- 30.21. Киназа, кодируемая геном src вируса саркомы птиц, участвует в трансформации
- 30.22. Двухцепочечная РНК подавляет синтез белка в клетках, обработанных интерфероном
- ГЛАВА 31. Перестройки генов: рекомбинация, транспозиция и клонирование
- 31.1 В основе генетической рекомбинации лежат разрыв и воссоединение цепей ДНК
- 31.2. При генетической рекомбинации происходит спаривание гомологичных цепей ДНК с образованием двухцепочечного промежуточного продукта
- 31.3. Белок recA катализирует АТР-зависимый обмен цепей ДНК при генетической рекомбинации
- 31.4. Бактерии содержат плазмиды и другие подвижные генетические элементы
- 31.5. Фактор F позволяет бактериям передавать гены реципиентам путем конъюгации
- 31.6. Плазмиды факторы R придают бактериям устойчивость к антибиотикам
- 31.7. IS-элементы могут присоединяться к неродственным генам
- 31.8. В лаборатории можно сконструировать новые геномы и клонировать их в клетках-хозяевах
- 31.9. Ферменты рестрикции и ДНК-лигаза — необходимые инструменты для получения рекомбинантных молекул ДНК
- 31.10. Плазмиды и фаг лямбда — наиболее подходящие векторы для клонирования ДНК в бактериях
- 31.11. Из суммарной геномной ДНК, расщепленной рестриктирующими эндонуклеазами, можно выделить с помощью клонирования определенные эукариотические гены
- 31.12. Эукариотические гены могут транскрибироваться в бактериальных клетках
- 31.13. Химически синтезированный ген пептидного гормона соматостатина экспрессируется в клетках Е. coli
- 31.14. Перспективы клонирования генов
- ГЛАВА 32. Оболочки бактериальных клеток
- 32.1. Клеточная стенка — это огромная мешковидная макромолекула
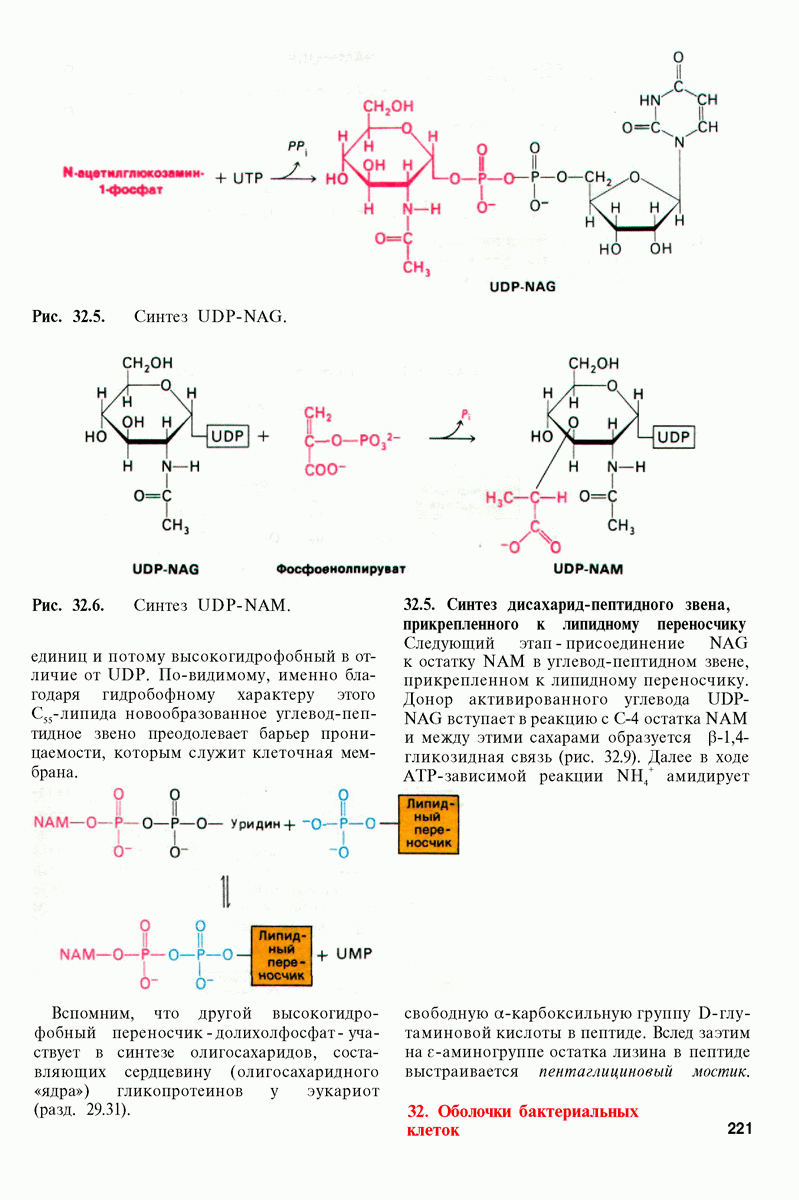
- 32.2. Стадии синтеза пептидогликана
- 32.3. Синтез UDP-углевод-пептидного звена
- 32.4. Перенос углевод-пептидного звена на липидный переносчик
- 32.5. Синтез дисахарид-пептидного звена, прикрепленного к липидному переносчику
- 32.6. Перенос дисахарид-пептидного звена на растущую полисахаридную цепь
- 32.7. Поперечные мостики между полисахаридными цепями образуются в реакции транспептидирования
- 32.8. У грам-положительных бактерий пептидогликан покрыт тейхоевой кислотой
- 32.9. Пенициллин вызывает гибель растущих бактерий, ингибируя синтез клеточных стенок
- 32.10. Пенициллин блокирует синтез клеточных стенок путем ингибирования реакции транспептидирования
- 32.11. Некоторые бактерии резистентны к пенициллину, так как синтезируют разрушающий его фермент
- 32.12. Грам-отрицательные бактерии окружены наружной мембраной, богатой липополисахаридами
- 32.13. Благодаря разнообразию О-боковых цепей грам-отрицательные бактерии противостоят защитным силам организма-хозяина
- 32.14. Порин образует в наружной мембране каналы для небольших полярных молекул
- 32.15. Новообразованные белки наружной мембраны содержат отщепляемую сигнальную последовательность
- ГЛАВА 33. Иммуноглобулины
- 33.2. Синтез специфических антител в ответ на антиген
- 33.3. Участки антител, связывающие антиген, подобны активным центрам ферментов
- 33.4. Препараты антител с определенной специфичностью обычно гетерогенны
- 33.5. При ферментативном расщеплении иммуноглобулина G образуются активные фрагменты
- 33.6. Иммуноглобулин G состоит из L- и Н-цепей
- 33.7. Иммуноглобулин G — гибкая Y-образная молекула
- 33.8. Антитела образуются под действием отбора или инструкции?
- 33.9. Конец инструктивной теории
- 33.10. Иммуноглобулины миеломы и гибридомы гомогенны
- 33.11. Каждая L- и Н-цепь состоит из вариабельного и константного участков
- 33.12. Участок связывания антигена образован гипервариабельными фрагментами L- и Н-цепей
- 33.13. Вариабельная и константная области выполняют разные функции
- 33.14. Молекулы антител уложены с образованием компактных доменов, имеющих гомологичные последовательности
- 33.15. Рентгеноструктурный анализ связывающих участков антител показал, как происходит связывание некоторых гаптенов
- 33.16. Разные классы иммуноглобулинов различаются по биологической активности
- 33.17. Молекулы антител возникли в результате дупликации и последующей дивергенции генов
- 33.18. Вариабельные и константные области кодируются разными, но соединившимися генами
- 33.19. Как возникает разнообразие специфичности антител?
- 33.20. Вариабельные участки L- и Н-цепей кодируются несколькими сотнями генов
- 33.21. Открытие генов J (соединяющих) — дополнительного источника разнообразия антител
- 33.22. Соединение генов V и J в различных рамках также способствует разнообразию антител
- 33.23. мРНК для L- и Н-цепей образуются путем сращивания (сплайсинга) первичных продуктов транскрипции
- 33.24. Разные классы антител образуются в результате перескока генов …
- 33.25. Разнообразие антител обусловлено соматической рекомбинацией многих генов клеток зародышевого пути и соматической мутацией
- 33.26. Клонально-селекционная теория образования антител
- 33.27. На поверхности клеток, продуцирующих антитела, имеются рецепторы антигенов
- 33.28. Биологическое значение клональной селекции
- ГЛАВА 34. Мышечное сокращение и подвижность клеток
- 34.2. При мышечном сокращении происходит скольжение толстых и тонких нитей относительно друг друга
- 34.3. Миозин образует толстые нити; он гидролизует АТР и связывает актин
- 34.4. Миозин можно расщепить на активные фрагменты
- 34.5. Актин образует нити, которые соединяются с миозином
- 34.6. Актин повышает АТР-азную активность миозина
- 34.7. Толстые и тонкие нити мышечного волокна определенным образом ориентированы
- 34.8. Полярность толстых и тонких нитей в середине саркомера меняется на противоположную
- 34.9. «Рабочим ходом» является поворот связанной с актином S1-головки миозина
- 34.10. Тропонин и тропомиозин опосредуют регуляторное действие ионов кальция на мышечное сокращение
- 34.11. Поток ионов Са2+ регулируется саркоплазматическим ретикулумом
- 34.12. Фосфокреатин — форма запасания ~P
- 34.13. Актин и миозин служат сократительными элементами почти во всех эукариотических клетках
- 34.14. Распределение микрофиламентов в клетке выявляется методом иммунофлуоресцентной микроскопии
- 34.15. Прикрепленные к мембране нити актина опосредуют сокращение микроворсинок кишечника
- 34.16. Цитохалазин и фаллоидин тормозят подвижность, сопряженную с процессами сборки и дезагрегации нитей актина
- 34.17. Микротрубочки участвуют в различных видах клеточной подвижности и частично формируют цитоскелет
- 34.18. Биение ресничек и движение жгутиков обусловлено скольжением микротрубочек, индуцированным динеином
- ГЛАВА 35. Действие гормонов
- 35.2. Циклический AMP синтезируется аденилатциклазой и расщепляется фосфодиэстеразой
- 35.3. сАМР служит вторым посредником при действии многих гормонов
- 35.4. Сопряжение рецепторов гормонов с аденилатциклазой осуществляется белком, связывающим гуаниннуклеотиды
- 35.5. Циклический AMP активирует протеинкиназы
- 35.6. Циклический AMP — эволюционно древний сигнал голодания
- 35.7. Холерный токсин стимулирует аденилаткиназу, ингибируя GTP-азную активность G-белка
- 35.8. Инсулин стимулирует анаболические процессы и ингибирует катаболические процессы
- 35.9. Препроинсулин и проинсулин — предшественники активного гормона
- 35.10. Трехмерная структура инсулина
- 35.11. Рецепторы инсулина локализованы в плазматической мембране клеток-мишеней
- 35.12. Недостаточность инсулина вызывает диабет
- 35.13. Эндорфины — пептиды мозга, действующие подобно опиатам
- 35.14. При расщеплении проопиокортина образуется несколько пептидных гормонов
- 35.15. Простагландины — модуляторы действия гормонов
- 35.16. Простагландины образуются из ненасыщенных жирных кислот
- 35.17. Стероидные гормоны активируют специфические гены
- 35.18. Белковые факторы роста типа ФРН и ЭФР стимулируют пролиферацию клеток-мишеней
- ГЛАВА 36. Мембранный транспорт
- 36.1. Различие между пассивным и активным транспортом
- 36.2. Открытие системы активного транспорта ионов натрия и калия
- 36.3. И фермент, и насос ориентированы в мембране
- 36.4. АТР транзиторно фосфорилирует натрий-калиевый насос
- 36.5. Транспорт ионов и гидролиз АТР тесно сопряжены
- 36.6. Натрий-калиевый насос — олигомерный трансмембранный белок
- 36.7. Модель механизма действия натрий-калиевого насоса
- 36.8. Кардиотонические стероиды — специфические ингибиторы (Na+ + + К+)-АТРазы и (Na+ + К)-насоса
- 36.9. Транспорт кальция осуществляется другой АТРазой
- 36.10. Поток Na+ обеспечивает энергией активный транспорт сахаров и аминокислот в животных клетках
- 36.11. Поток протонов служит движущей силой во многих процессах транспорта у бактерий
- 36.12. Активный транспорт ряда сахаров сопряжен с их фосфорилированием
- 36.13. Транспортные антибиотики повышают ионную проницаемость мембран
- 36.14. Транспортные антибиотики функционируют либо как подвижные переносчики, либо как каналообразователи
- 36.15. Антибиотики-переносчики имеют форму скорлупы ореха и связывают ионы в своей центральной полости
- 36.16. Валиномицин связывает К+ в 1000 раз прочнее, чем Na+
- 36.17. Можно выявить поток ионов через единичный канал в мембране
- 36.18. Через щелевые соединения ионы и небольшие молекулы перетекают из клетки в клетку
- ГЛАВА 37. Возбудимые мембраны и сенсорные системы
- 37.1. Потенциалы действия опосредованы кратковременными изменениями проницаемости для Na+ и К+
- 37.2. Тетродотоксин и сакситоксин блокируют натриевые каналы в мембранах аксонов нервных клеток
- 37.3. Ацетилхолин является нейромедиатором
- 37.4. Ацетилхолин открывает в постсинаптической мембране каналы для катионов
- 37.5. Ацетилхолин высвобождается квантами
- 37.6. При добавлении ацетилхолина реконструированные мембранные пузырьки становятся проницаемыми для катионов
- 37.7. Ацетилхолин быстро гидролизуется, и концевая пластинка реполяризуется
- 37.8. Ингибиторы ацетилхолинэстеразы используются как лекарственные средства и как яды
- 37.9. Разработка антидота для лечения отравлений органическими фосфатами
- 37.10. Ингибиторы ацетилхолинового рецептора
- 37.11. К числу нейромедиаторов относятся также катехоламины и у-аминомасляная кислота (ГАМК)
- 37.12. Для возбуждения палочки сетчатки глаза достаточно одного фотона
- 37.13. Родопсин — фоторецепторный белок палочек
- 37.14. Свет вызывает изомеризацию 11-цис-ретиналя
- 37.15. Свет вызывает гиперполяризацию плазматической мембраны наружного сегмента палочек
- 37.16. Медиаторы передают сигнал от фотолизированного родопсина на плазматическую мембрану
- 37.17. Свет снижает содержание циклического GMP путем активации фосфодиэстеразы
- 37.18. Цветовое зрение опосредуется фоторецепторами трех типов
- 37.19. 11-цис-ретиналь — хромофор всех известных органов зрения
- 37.20. Хеморецепторы бактерий воспринимают специфические молекулы и передают сигналы на жгутики
- 37.21. В основании бактериального жгутика находится вращающий его реверсивный «мотор»
- 37.22. Бактерии различают временной градиент, а не одномоментный пространственный градиент концентраций
- 37.23. При бактериальном хемотаксисе передача информации обеспечивается метилированными белками