| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
В. ПРАКТИЧЕСКИЕ РАБОТЫ ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ БЕЗ ТОКА (i=0)
§ 12. Кислотно-основное титрование
Определение уксусной кислоты
Потенциометрическое определение уксусной кислоты проводят титрованием 0,1 н. раствором сильного основания, проследив компенсационным методом за изменением э. д. с. гальванического элемента, составленного из хингидоонного индикаторного электрода  и насыщенного каломельного электрода сравнения.
и насыщенного каломельного электрода сравнения.
При этом протекает химическая реакция

и соответствующая электрохимическая реакция до точки эквивалентности

поскольку  (см. стр. 59)
(см. стр. 59)

Это уравнение показывает, что Е до точки эквивалентности уменьшается в соответствии с изменением соотношения концентрации недотитрованной кислоты и образовавшейся соли, иначе говоря, с возрастанием  раствора.
раствора.
При появлении избытка  -ионов после точки эквивалентности протекает следующая электрохимическая реакция:
-ионов после точки эквивалентности протекает следующая электрохимическая реакция:

т. е. потенциал электрода продолжает уменьшаться с увеличением избытка  -ионов (по мере дальнейшего возрастания
-ионов (по мере дальнейшего возрастания  раствора).
раствора).
Из уравнений (25) и (26) при введении соответствующих значений  и
и  и сопоставлении их с уравнением (23) легко доказать, что
и сопоставлении их с уравнением (23) легко доказать, что  так как
так как  , то
, то  следовательно, при небольшой степени недотитрованности и перетитрованности указанной кислоты должен возникать скачок потенциала, отвечающий конечной точке.
следовательно, при небольшой степени недотитрованности и перетитрованности указанной кислоты должен возникать скачок потенциала, отвечающий конечной точке.
Э. д. с. потенциометрической ячейки можно выразить формулой:

Однако вследствие изменения  во время титрования и согласно приведенным уравнениям настанет момент, когда Е станет равным э. д. с. равной 0. С этого момента (при
во время титрования и согласно приведенным уравнениям настанет момент, когда Е станет равным э. д. с. равной 0. С этого момента (при  )
)  , поэтому необходимо переключить электроды в полуэлементах к соответствующим клеммам потенциометра.
, поэтому необходимо переключить электроды в полуэлементах к соответствующим клеммам потенциометра.
Методика определения. Для измерения э. д. с. потенциометрической ячейки пользуются любым подходящим потенциометром и приводят его в рабочее состояние, согласно приложенной к прибору инструкции.
В стакан емкостью  пипеткой помещают испытуемый раствор уксусной кислоты, разбавляют водой до
пипеткой помещают испытуемый раствор уксусной кислоты, разбавляют водой до  , прибавляют около 50 мг хингидрона, опускают мешалку и устанавливают стакан на площадке магнитной мешалки. В другой стакан емкостью
, прибавляют около 50 мг хингидрона, опускают мешалку и устанавливают стакан на площадке магнитной мешалки. В другой стакан емкостью  наливают насыщенный раствор
наливают насыщенный раствор  , опускают туда
, опускают туда  КЭ и устанавливают рядом с титрационной ячейкой. Оба стакана соединяют электролитическим ключом, наполненным насыщенным раствором
КЭ и устанавливают рядом с титрационной ячейкой. Оба стакана соединяют электролитическим ключом, наполненным насыщенным раствором  . В ячейку с титруемым раствором погружают
. В ячейку с титруемым раствором погружают  -электрод и закрепляют с помощью лапки и штатива так, чтобы металлическая часть была полностью погружена в раствор, но
-электрод и закрепляют с помощью лапки и штатива так, чтобы металлическая часть была полностью погружена в раствор, но  время вращения мешалка не задевала электрод. Бюретку наполняют 0,1 н. стандартным раствором щелочи, закрывают верхнее ее отверстие хлоркальциевой трубкой, наполненной натронной известью для предупреждения проникновения двуокиси углерода из воздуха, и закрепляют в штативе над титрационной ячейкой. Индикаторный электрод присоединяют к положительной, а
время вращения мешалка не задевала электрод. Бюретку наполняют 0,1 н. стандартным раствором щелочи, закрывают верхнее ее отверстие хлоркальциевой трубкой, наполненной натронной известью для предупреждения проникновения двуокиси углерода из воздуха, и закрепляют в штативе над титрационной ячейкой. Индикаторный электрод присоединяют к положительной, а  . КЭ — к отрицательной клеммам потенциометра.
. КЭ — к отрицательной клеммам потенциометра.
Приступая к ориентировочному титрованию, сначала включают магнитную мешалку, затем прибавляют по  щелочи и измеряют э. д. с. гальванического элемента (см. стр. 51). Перед тем как вносить в раствор новую порцию титранта, записывают показание потенциометра в рабочий журнал (см. стр. 48). Титрование продолжают до тех пор, пока не будет найден скачок потенциала, затем выключают мешалку.
щелочи и измеряют э. д. с. гальванического элемента (см. стр. 51). Перед тем как вносить в раствор новую порцию титранта, записывают показание потенциометра в рабочий журнал (см. стр. 48). Титрование продолжают до тех пор, пока не будет найден скачок потенциала, затем выключают мешалку.
После нахождения объема титранта с точностью  , который соответствует приближенному значению конечной точки титрования, удаляют электрод, электролитический ключ и мешалку из стакана, промывают их дистиллированной водой и высушивают фильтровальной бумагой. В стакан снова вводят такую же порцию титруемого раствора, так же разбавляют водой и собирают всю установку, как описано выше. Бюретку снова наполняют титрантом до нулевой метки и, включив мешалку, приступают к точному титрованию. Для этого сразу вносят Объем титранта на
, который соответствует приближенному значению конечной точки титрования, удаляют электрод, электролитический ключ и мешалку из стакана, промывают их дистиллированной водой и высушивают фильтровальной бумагой. В стакан снова вводят такую же порцию титруемого раствора, так же разбавляют водой и собирают всю установку, как описано выше. Бюретку снова наполняют титрантом до нулевой метки и, включив мешалку, приступают к точному титрованию. Для этого сразу вносят Объем титранта на  меньше, чем это соответствует конечной точке, установленной при ориентировочном титровании, и, хорошо перемешав раствор, продолжают титрование по 2 капли, измеряя каждый раз э. д. с. ячейки с точностью до 1 мв и записывая данные, как указано в табл. 2 (см. стр. 46). В тот момент, когда компенсация э. д. с. становится невозможной
меньше, чем это соответствует конечной точке, установленной при ориентировочном титровании, и, хорошо перемешав раствор, продолжают титрование по 2 капли, измеряя каждый раз э. д. с. ячейки с точностью до 1 мв и записывая данные, как указано в табл. 2 (см. стр. 46). В тот момент, когда компенсация э. д. с. становится невозможной  , реверсируют полюса электродов к клеммам потенциометра и продолжают титрование и измерение э. д. с. до тех пор, пока после скачка потенциала не будет добавлено еще
, реверсируют полюса электродов к клеммам потенциометра и продолжают титрование и измерение э. д. с. до тех пор, пока после скачка потенциала не будет добавлено еще  титранта.
титранта.
Это необходимо для того, чтобы быть уверенным в уменьшении  после достижения максимального значения и для возможности графического изображения хода кривой титрования.
после достижения максимального значения и для возможности графического изображения хода кривой титрования.
Точное положение конечной точки титрования находят расчетным и графическим способами.
Расчет. Содержание  уксусной кислоты (в г) во взятом для титрования объеме испытуемого раствора вычисляют по формуле:
уксусной кислоты (в г) во взятом для титрования объеме испытуемого раствора вычисляют по формуле:

Анализ смеси хлористоводородной и борной кислот
Дифференцированное определение  (в присутствии маннита или глицерина) основано на потенциометрическом титровании их 0,1 н. раствором щелочи до достижения значений
(в присутствии маннита или глицерина) основано на потенциометрическом титровании их 0,1 н. раствором щелочи до достижения значений  раствора, отвечающих конечным точкам титрования хлористоводородной (
раствора, отвечающих конечным точкам титрования хлористоводородной ( ) и борноманнитовой кислот (при
) и борноманнитовой кислот (при  ). Титрование проводят со стеклянным индикаторным электродом и
). Титрование проводят со стеклянным индикаторным электродом и  сравнения.
сравнения.
Константа диссоциации борной кислоты  настолько мала, что сильная кислота в ее присутствии практически без осложнения может быть количественно оттитрована щелочью. По завершении титрования
настолько мала, что сильная кислота в ее присутствии практически без осложнения может быть количественно оттитрована щелочью. По завершении титрования  титруют
титруют  в присутствии маннита (или глицерина). При этом борная кислота образует комплексную маннитоборную кислоту, обладающую относительно большей константой диссоциации
в присутствии маннита (или глицерина). При этом борная кислота образует комплексную маннитоборную кислоту, обладающую относительно большей константой диссоциации 
Методика определения. Настройку  -метра проводят согласно приложенной к прибору инструкции.
-метра проводят согласно приложенной к прибору инструкции.
Сначала экспериментально находят значения  раствора в конечных точках титрования
раствора в конечных точках титрования  . Для этого в титрационный сосуд наливают пипеткой
. Для этого в титрационный сосуд наливают пипеткой  испытуемого раствора
испытуемого раствора  и разбавляют
и разбавляют  дистиллированной воды. Погружают предварительно промытые электроды и мешалку и при хорошем перемешивании измеряют
дистиллированной воды. Погружают предварительно промытые электроды и мешалку и при хорошем перемешивании измеряют  раствора
раствора  . Найденная величина
. Найденная величина  показывает, что в случае титрования смеси
показывает, что в случае титрования смеси  до достижения этого значения
до достижения этого значения  борная кислота еще не вступает в реакцию со щелочью. Когда
борная кислота еще не вступает в реакцию со щелочью. Когда  окажется недотитрованной на
окажется недотитрованной на  (если начальная концентрация ее
(если начальная концентрация ее  . Затем в этот же раствор прибавляют 1 г маннита (или
. Затем в этот же раствор прибавляют 1 г маннита (или  глицерина) и титруют 0,1 н. раствором
глицерина) и титруют 0,1 н. раствором  , прибавляя титрант небольшими порциями. После каждой внесенной порции титранта измеряют
, прибавляя титрант небольшими порциями. После каждой внесенной порции титранта измеряют  раствора. Результаты измерения
раствора. Результаты измерения  записывают в журнал и по максимальной величине
записывают в журнал и по максимальной величине  находят
находят  раствора в конечной точке титрования борноманнитовой кислоты
раствора в конечной точке титрования борноманнитовой кислоты  . Полученные значения
. Полученные значения  показывают, до какой величины
показывают, до какой величины  в дальнейшем следует титровать
в дальнейшем следует титровать  в присутствии
в присутствии  и борноманнитовую кислоту
и борноманнитовую кислоту  .
.
Титрант прибавляют вначале большими порциями, а затем медленно по каплям до тех пор, пока  раствора не достигнет ранее определенного значения
раствора не достигнет ранее определенного значения  раствора
раствора  . Записывают объем титранта (Умаон), израсходованный на определение
. Записывают объем титранта (Умаон), израсходованный на определение  . В тот же стакан вносят 1 г маннита (или 10 мг (Глицерина) и после его растворения титруют вначале большими порциями, а затем каплями титранта, следя за показанием
. В тот же стакан вносят 1 г маннита (или 10 мг (Глицерина) и после его растворения титруют вначале большими порциями, а затем каплями титранта, следя за показанием  -метра, до достижения значения
-метра, до достижения значения  , отвечающего конечной точке титрования борноманнитовой кислоты.
, отвечающего конечной точке титрования борноманнитовой кислоты.
Фиксируют в журнале общий объем израсходованного стандартного раствора щелочи  . Разность
. Разность  дает объем титранта, эквивалентный содержанию
дает объем титранта, эквивалентный содержанию  .
.
Расчет. Содержание  во взятом для титрования объеме испытуемого раствора рассчитывают по формулам:
во взятом для титрования объеме испытуемого раствора рассчитывают по формулам:

| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ
- ВВЕДЕНИЕ
- ГЛАВА I. ОСНОВЫ ФИЗИКО-ХИМИЧЕСКИХ (ИНСТРУМЕНТАЛЬНЫХ) МЕТОДОВ АНАЛИЗА
- § 1. Особенности физико-химических методов анализа
- § 2. Области применения инструментальных методов анализа
- § 3. Анализ веществ высокой чистоты
- § 4. Повышение чувствительности и точности методов определения следов примесей
- § 5. Инструментальные методы титрования
- § 6. Применение физико-химических методов анализа для определения индивидуальных соединений
- § 7. Применение физико-химических методов для анализа смесей веществ
- § 8. Классификация инструментальных количественных методов анализа
- § 9. Электрохимические методы анализа
- § 10. Спектральные (оптические) методы анализа
- § 11. Хроматографические методы анализа
- § 12. Радиометрические методы анализа
- § 13. Масс-спектрометрические методы анализа
- § 14. Физико-химический анализ по Н. С. Курнакову
- § 15. Другие методы анализа
- ГЛАВА II. ПОТЕНЦИОМЕТРИЯ И ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- § 1. Зависимость величины электродных потенциалов от концентрации (активности)
- § 2. Применение потенциометрического метода анализа
- § 3. Потенциометрическое титрование
- § 4. Потенциометрическое титрование без тока (i=0)
- § 5. Различные способы нахождения конечной точки потенциометрического титрования
- § 6. Некомпенсационный метод потенциометрического титрования
- § 7. Потенциометрическое титрование под током (i != 0)
- Б. АППАРАТУРА И ТЕХНИКА ВЫПОЛНЕНИЯ АНАЛИЗА
- § 8. Измерение электродвижущей силы
- § 9. Установка для поляризации электродов при потенциометрическом титровании под током
- § 10. Некоторые приборы, применяемые в потенциометрическом титровании
- § 11. Электроды
- В. ПРАКТИЧЕСКИЕ РАБОТЫ ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ БЕЗ ТОКА (i=0)
- § 12. Кислотно-основное титрование
- § 13. Титрование по методу окисления — восстановления
- § 14. Титрование по методу осаждения
- § 15. Титрование по методу комплексообразования
- ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ ПОД ТОКОМ (i != 0)
- § 16. Титрование по методу окисления — восстановления
- ГЛАВА III. КОНДУКТОМЕТРИЯ и КОНДУКТОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- § 1. Удельная и эквивалентная электропроводность
- § 2. Кондуктометрическне методы анализа
- § 3. Кислотно-основное титрование
- § 4. Титрование, основанное на реакциях осаждения
- § 5. Титрование, основанное на реакциях окисления — восстановления
- § 6. Титрование, основанное на реакциях комплексообразования
- Б. АППАРАТУРА И ТЕХНИКА ВЫПОЛНЕНИЯ АНАЛИЗА
- § 7. Измерение электропроводности растворов
- § 8. Конструкции электролитических ячеек
- § 9. Измерения в хронокондуктометрическом титровании
- В. ПРАКТИЧЕСКИЕ РАБОТЫ
- § 10. Подготовка к определению
- §11. Определение индивидуальных кислот методом кондуктометрического титрования
- § 12. Определение индивидуальных оснований методом кондуктометрического титрования
- § 13. Анализ смесей оснований методом кондуктометрического титрования
- § 14. Определение солей методом кондуктометрического титрования
- § 15. Анализ смесей кислот и солей слабых оснований методом кондуктометрического титрования
- § 16. Анализ смесей кислот методом хронокондуктометрического титрования
- § 17. Анализ смесей оснований и солей слабых кислот методом хронокондуктометрического титрования
- ГЛАВА IV. ВЫСОКОЧАСТОТНОЕ ТИТРОВАНИЕ
- § 1. Общие положения теории высокочастотного титрования
- § 2. Физические основы и погрешности метода высокочастотного титрования
- § 3. Физические основы метода диэлкометрического титрования
- § 4. Погрешности метода диэлкометрического титрования
- ТЕОРИЯ ИЗМЕРИТЕЛЬНЫХ ЯЧЕЕК ЕМКОСТНОГО ТИПА
- § 5. Электрическая эквивалентная схема ячейки и физические процессы, протекающие в ее объеме
- § 6. Импеданс и полная проводимость ячейки
- § 7. Характеристические кривые ячейки
- § 8. Чувствительность ячейки
- § 9. Критерий применимости и постоянная с-ячейки
- ТЕОРИЯ ИЗМЕРИТЕЛЬНЫХ ЯЧЕЕК ИНДУКТИВНОГО ТИПА
- § 10. Электрическая эквивалентная схема ячейки
- § 11. Импеданс и характеристические кривые ячейки
- § 12. Критерий применимости и постоянная L-ячейки
- § 13. Влияние на характеристические кривые ячейки ее некомпенсированного электрического поля
- ДИАГРАММЫ СООТВЕТСТВИЯ
- § 14. Диаграмма соответствия для титрования по активной составляющей полной проводимости
- § 15. Диаграмма соответствия для титрования по реактивной составляющей полной проводимости
- § 16. Выбор типа диаграмм
- Б. АППАРАТУРА И ТЕХНИКА ВЫПОЛНЕНИЯ АНАЛИЗА
- § 17. Измерительные ячейки (датчики) высокочастотного метода и области их применения
- § 18. Классификация аппаратуры высокочастотного метода
- § 19. Высокочастотные титраторы
- § 20. Общие правила работы с приборами для высокочастотного анализа
- В. ПРАКТИЧЕСКИЕ РАБОТЫ
- § 21. Высокочастотное титрование стандартных растворов
- § 22. Высокочастотное титрование растворов неизвестной концентрации
- ГЛАВА V. ПОЛЯРОГРАФИЧЕСКИЙ МЕТОД АНАЛИЗА И АМПЕРОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- § 1. Предельный, или диффузионный, ток
- § 2. Возникновение диффузионного тока на твердых микроэлектродах
- Б. АППАРАТУРА И ТЕХНИКА ВЫПОЛНЕНИЯ ПОЛЯРОГРАФИЧЕСКОГО АНАЛИЗА
- § 3. Полярографы
- § 4. Электролитическая ячейка
- § 5. Электролизеры
- § 6. Электроды сравнения
- § 7. Снятие полярограммы на полярографической установке с визуальным полярографом
- § 8. Методы количественного полярографического анализа
- § 9. Правила техники безопасности при работе с металлической ртутью
- В. НОВЫЕ НАПРАВЛЕНИЯ В ПОЛЯРОГРАФИИ
- § 10. Амальгамная полярография с накоплением
- § 11. Осциллографическая полярография
- § 12. Переменнотоковая полярография
- Г. ПРАКТИЧЕСКИЕ РАБОТЫ С ПРИМЕНЕНИЕМ ПОЛЯРОГРАФИЧЕСКОГО МЕТОДА АНАЛИЗА
- § 13. Примеры полярографических определений
- АМПЕРОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- § 14. Особенности амперометрического титрования
- Б. АППАРАТУРА И ТЕХНИКА ВЫПОЛНЕНИЯ АМПЕРОМЕТРИЧЕСКОГО ТИТРОВАНИЯ
- § 15. Схема установки и применяемые электроды
- § 16. Амперометрическое титрование с двумя индикаторными электродами
- В. ПРАКТИЧЕСКИЕ РАБОТЫ С ПРИМЕНЕНИЕМ АМПЕРОМЕТРИЧЕСКОГО ТИТРОВАНИЯ
- § 17. Примеры амперометрического титрования
- ГЛАВА VI. КУЛОНОМЕТРИЯ И КУЛОНОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- § 1. Сущность и классификация кулонометрических методов
- ПРЯМАЯ КУЛОНОМЕТРИЯ
- § 2. Прямая кулонометрия при постоянном потенциале рабочего электрода (прямая потенциостатическая кулонометрия)
- § 3. Использование прямой потенциостатической кулонометрии
- § 4. Прямая кулонометрия при постоянной силе тока электролиза (прямая амперостатическая кулонометрия)
- § 5. Использование прямой амперостатической кулонометрии
- КУЛОНОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- § 6. Кулонометрическое титрование при постоянной силе тока электролиза
- § 7. Использование амперостатического кулонометрического титрования
- § 8. Кулонометрическое титрование првд постоянном потенциале рабочего электрода
- § 9. Особенности кулонометрических методов анализа
- Б. АППАРАТУРА И ТЕХНИКА ВЫПОЛНЕНИЯ АНАЛИЗА
- § 10. Электроды
- § 11. Электролизеры
- § 12. Приборы для измерения количества электричества, израсходованного на электролиз вещества
- § 13. Приборы, обеспечивающие стабильность потенциала рабочего электрода или силы тока электролиза, и установки для кулонометрического анализа
- В. ПРАКТИЧЕСКИЕ РАБОТЫ
- § 14. Работы, выполняемые методом прямой кулонометрии
- § 15. Работы, выполняемые методом косвенной кулонометрии, или кулонометрического титрования, при постоянной силе тока электролиза
- ГЛАВА VII. СПЕКТРАЛЬНЫЕ (ОПТИЧЕСКИЕ) МЕТОДЫ АНАЛИЗА
- § 1. Общая характеристика метода
- § 2. Классификация методов эмиссионного спектрального анализа
- § 3. Качественный спектральный анализ
- § 4. Полуколичественные методы спектрального анализа
- § 5. Количественный спектральный анализ
- § 6. Основы фотографического метода эмиссионного количественного анализа
- § 7. Зависимость между почернением фотопластинки и интенсивностью излучения
- Б. АППАРАТУРА И ТЕХНИКА ВЫПОЛНЕНИЯ АНАЛИЗА
- § 8. Источники возбуждения спектров
- § 9. Спектральные приборы
- § 10. Вспомогательные приборы и принадлежности
- § 11. Микрофотометр МФ-2
- В. ПРАКТИЧЕСКИЕ РАБОТЫ
- § 12. Качественный анализ при помощи стилоскопа
- § 13. Качественный анализ фотографическим методом при помощи спектра железа в ультрафиолетовой области
- § 14. Полуколичественный анализ
- § 15. Количественный анализ
- СПЕКТРОФОТОМЕТРИЯ ПЛАМЕНИ
- § 16. Общая характеристика метода
- Б. АППАРАТУРА И ТЕХНИКА ВЫПОЛНЕНИЯ АНАЛИЗА
- § 17. Схема установки, применяемой для анализа методом спектрофотометрии пламени
- В. ПРАКТИЧЕСКИЕ РАБОТЫ
- § 18. Определения по методу спектрофотометрии пламени
- АТОМНО-АБСОРБЦИОННЫЙ СПЕКТРАЛЬНЫЙ АНАЛИЗ
- § 19. Общая характеристика метода
- МОЛЕКУЛЯРНО-АБСОРБЦИОННЫЙ СПЕКТРАЛЬНЫЙ АНАЛИЗ
- § 20. Общая характеристика метода
- § 21. Законы поглощения света
- § 22. Отклонения от закона Бугера—Ламберта—Бера
- § 23. Качественный анализ спектрофотометрическим методом
- § 24. Количественный анализ спектрофотометрическим методом
- § 25. Методы определения концентрации веществ, поглощающих в видимой и ультрафиолетовой областях спектра
- § 26. Определение нескольких компонентов в растворе
- § 27. Определение концентрации вещества в растворе дифференциальным методом
- § 28. Выбор толщины слоя и оптимальной концентрации исследуемого раствора
- § 29. Выбор длины волны поглощаемого излучения при спектрофотометрических измерениях
- Б. АППАРАТУРА И ТЕХНИКА ВЫПОЛНЕНИЯ АНАЛИЗА
- § 30. Приборы, применяемые для спектрофотометрического анализа в ультрафиолетовой и видимой областях спектра
- § 31. Приборы, применяемые для колориметрического анализа
- § 32. Приборы, применяемые для спектрофотометрического анализа в инфракрасной области спектра
- § 33. Нулевые растворы
- В. ПРАКТИЧЕСКИЕ РАБОТЫ
- § 34. Определение в ультрафиолетовой области спектра
- § 35. Определение в видимой области спектра
- § 36. Определение в инфракрасной области спектра
- СПЕКТРОФОТОМЕТРИЧЕСКИЕ (ФОТОМЕТРИЧЕСКИЕ) МЕТОДЫ ТИТРОВАНИЯ
- § 37. Общая характеристика метода
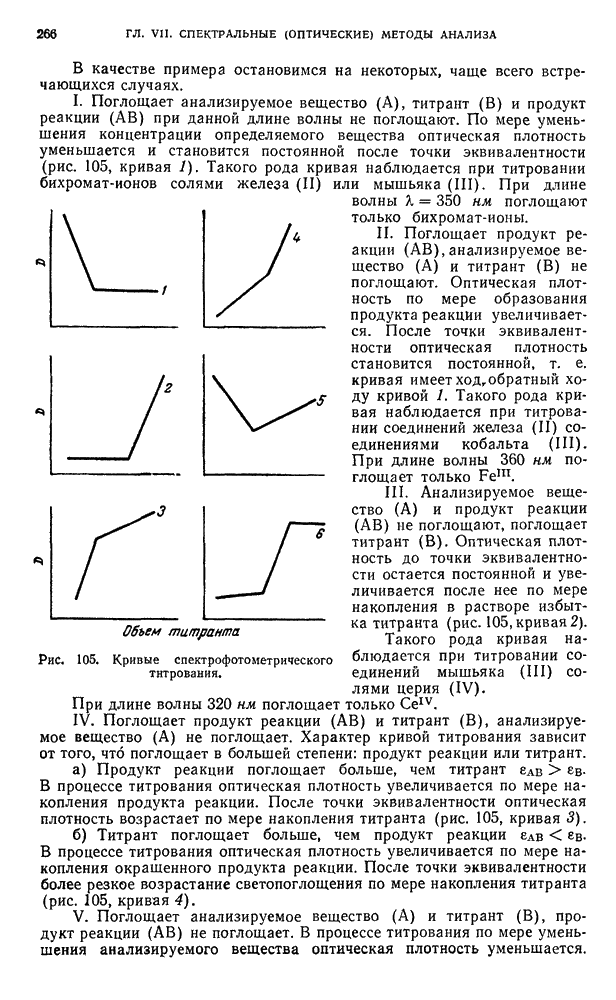
- § 38. Кривые спектрофотометрического титрования
- Б. АППАРАТУРА И ТЕХНИКА ВЫПОЛНЕНИЯ ТИТРОВАНИЯ
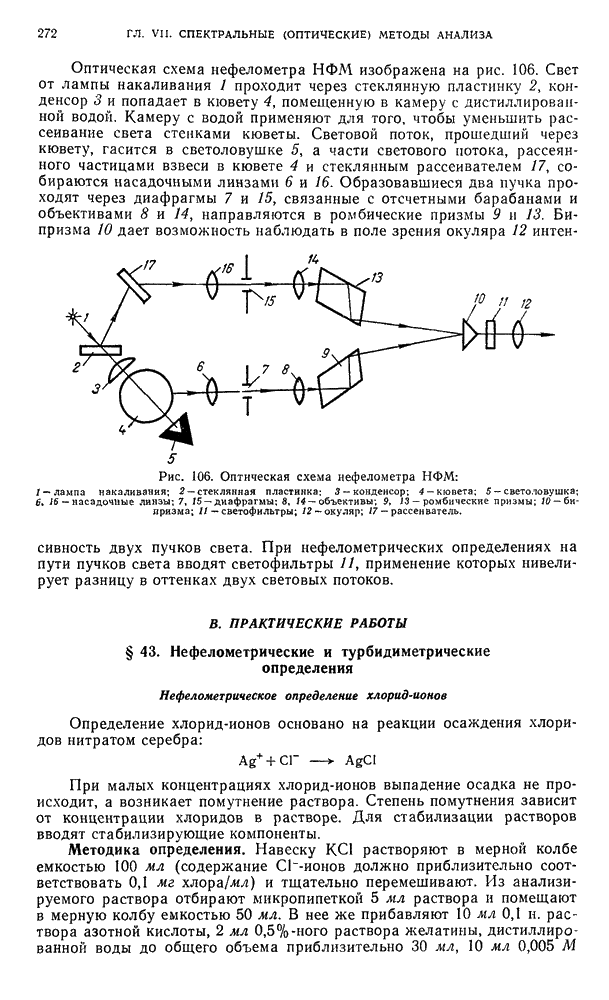
- § 39. Установки для спектрофотометрического титрования
- В. ПРАКТИЧЕСКИЕ РАБОТЫ
- § 40. Спектрофотометрическое титрование
- НЕФЕЛОМЕТРИЧЕСКИЙ И ТУРБИДИМЕТРИЧЕСКИЙ МЕТОДЫ АНАЛИЗА
- § 41. Общая характеристика методов
- Б. АППАРАТУРА И ТЕХНИКА ВЫПОЛНЕНИЯ АНАЛИЗА
- § 42. Приборы, применяемые для нефелометрических и турбидиметрических измерений
- В. ПРАКТИЧЕСКИЕ РАБОТЫ
- § 43. Нефелометрические и турбидиметрические определения
- § 44. Фототурбидиметрическое и фотонефелометрическое титрование
- ГЛАВА VIII. ХРОМАТОГРАФИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
- § 1. Классификация хроматографических методов анализа
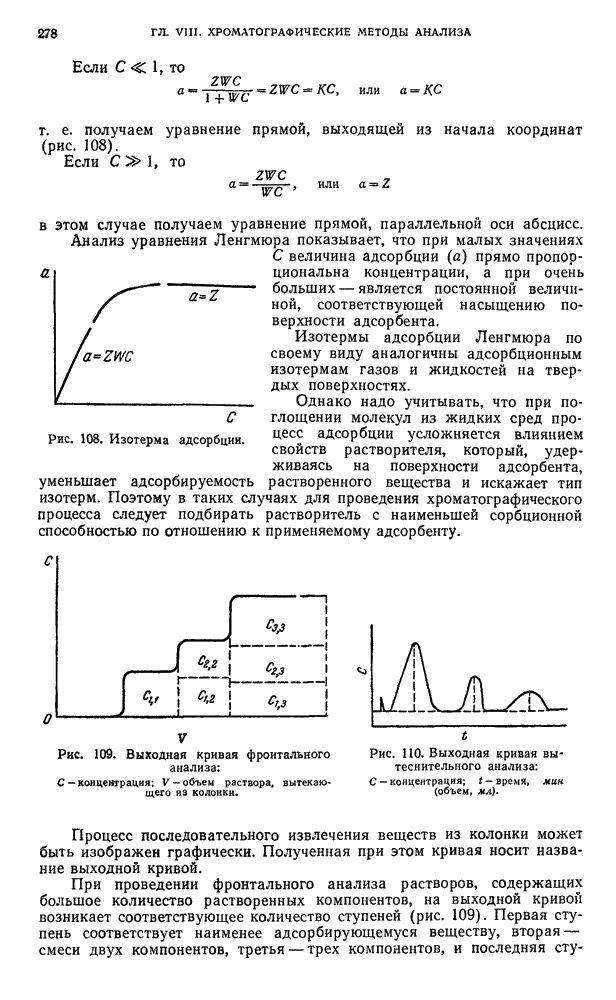
- § 2. Адсорбционная хроматография
- § 3. Разновидности газовой хроматографии
- § 4. Распределительная хроматография
- § 5. Ионообменная хроматография
- § 6. Константа ионного обмена
- § 7. Осадочная хроматография
- § 8. Окислительно-восстановительная хроматография
- § 9. Адсорбционно-комплексообразовательная хроматография
- § 10. Хроматографические колонки, применяемые в адсорбционно-жидкостной хроматографии
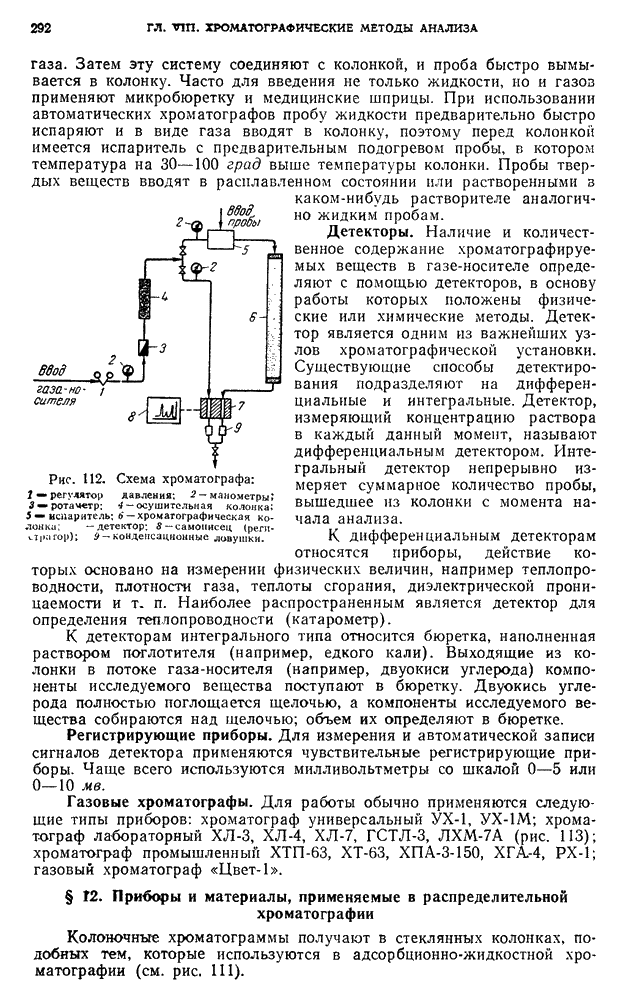
- § 11. Аппаратура, применяемая в газовой хроматографии
- § 12. Приборы и материалы, применяемые в распределительной хроматографии
- § 13. Колонки, применяемые в ионообменной хроматографии
- § 14. Колонки, применяемые в осадочной и окислительновосстановительной хроматографии
- В. ПРАКТИЧЕСКИЕ РАБОТЫ
- § 15. Работы по методу адсорбционной (жидкостной и газовой) хроматографии
- § 16. Работы по методу распределительной хроматографии
- § 17. Работы по методу ионообменной хроматографии
- § 18. Работы по методу осадочной хроматографии
- § 19. Работы по методу окислительно-восстановительной хроматографии
- § 20. Работы по методу адсорбционно-комплексообразовательной хроматографии
- ГЛАВА IX. РАДИОМЕТРИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
- § 1. Виды радиоактивного распада
- § 2. Скорость распада
- § 3. Взаимодействие излучения с веществом
- § 4. Ошибки при измерении радиоактивности
- Б. ЭЛЕМЕНТЫ ТЕХНИКИ БЕЗОПАСНОСТИ ПРИ РАБОТЕ С РАДИОАКТИВНЫМИ ВЕЩЕСТВАМИ
- § 5. Понятия и единицы измерения
- § 6. Классификация источников радиоактивного излучения и радиоактивных изотопов
- § 7. Классификация химических операций с радиоактивными веществами
- § 8. Устройство лабораторий и классификация работ
- § 9. Специальное оборудование для работ с радиоактивными веществами
- § 10. Средства индивидуальной защиты
- § 11. Проведение работ в химической лаборатории с радиоактивными веществами
- § 12. Правила работы с радиоактивными веществами
- В. МЕТОДЫ РЕГИСТРАЦИИ РАДИОАКТИВНОГО ИЗЛУЧЕНИЯ
- § 13. Ионизационные методы
- § 14. Сцинтилляционный метод
- Г. АППАРАТУРА И ТЕХНИКА ИЗМЕРЕНИЯ РАДИОАКТИВНОСТИ
- § 15. Радиометрические установки
- § 16. Измерение радиоактивности
- § 17. Измерение дозы на рабочем месте, индивидуальной дозы, полученной работающим, и загрязненности рабочих поверхностей, рук и одежды
- § 18. Абсолютные и относительные измерения активности
- Д. РАДИОМЕТРИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ
- § 19. Приготовление раствора с заданной активностью
- § 20. Прямое определение ионов химических элементов в растворе с помощью радиоактивных реагентов
- § 21. Практические работы, выполняемые методом прямого определения
- § 22. Метод радиометрического титрования
- § 23. Практические работы, выполняемые методом радиометрического титрования
- § 24. Метод изотопного разбавления
- § 25. Практические работы, выполняемые методом изотопного разбавления
- § 26. Метод активационного анализа
- § 27. Практические работы, выполняемые методом активационного анализа
- § 28. Фотонейтронный метод
- § 29. Практические работы, выполняемые фотонейтронным методом
- § 30. Методы определения содержания химических элементов по излучению их естественных радиоактивных изотопов
- § 31. Практические работы по определению содержания химических элементов методом измерения излучения их естественных радиоактивных изотопов
- § 32. Методы анализа, основанные на поглощении излучения
- § 33. Практические работы, выполняемые по методу анализа, основанному на поглощении излучения
- § 34. Метод, основанный на отражении бетта-излучения
- § 35. Практические работы, выполняемые по методу, основанному на отражении бетта-излучения
- ГЛАВА X. ФИЗИКО-ХИМИЧЕСКИЕ МЕТОДЫ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ РЕДКИХ ЭЛЕМЕНТОВ
- § 1. Работы, выполняемые методом амперометрического титрования
- § 2. Работы, выполняемые полярографическим методом
- § 3. Работы, выполняемые фотометрическим методом
- § 4. Работы, выполняемые экстракционно-фотометрическим методом
- § 5. Работы, выполняемые спектрофотометрическим методом
- § 6. Работы, выполняемые флуориметрическим методом
- § 7. Работы, выполняемые методом потенциометрического титрования
- ГЛАВА XI. ФИЗИКО-ХИМИЧЕСКИЕ (ИНСТРУМЕНТАЛЬНЫЕ) МЕТОДЫ АНАЛИЗА НЕВОДНЫХ РАСТВОРОВ
- § 1. Влияние химической природы и физико-химических свойств растворителей на свойства растворенного вещества
- § 2. Классификация неводных растворителей по их протонно-донорно-акцепторным свойствам
- § 3. Классификация неводных растворителей по признаку их влияния на относительную силу электролитов
- § 4. Дифференцирующее действие растворителей
- § 5. Константы диссоциации, потенциалы полунейтрализации в неводных средах и относительная шкала кислотности
- § 6. Шкала pH и константы автопротолиза неводных растворителей
- § 7. Абсолютная (единая) шкала кислотности растворителей
- § 8. Химико-аналитическое использование неводных растворителей
- Б. АППАРАТУРА И ТЕХНИКА ТИТРОВАНИЯ НЕВОДНЫХ РАСТВОРОВ
- § 9. Установки, используемые при амперометрическом титровании неводных растворов
- § 10. Установки, используемые при потенциометрическом титровании неводных растворов
- § 11. Установки, используемые при кондуктометрическом титровании неводных растворов
- § 12. Установки, используемые при высокочастотном титровании неводных растворов
- § 13. Установки, используемые при спектрофотометрическом титровании неводных растворов
- В. ПРАКТИЧЕСКИЕ РАБОТЫ
- § 14. Очистка и обезвоживание неводных растворителей
- § 15. Титранты, применяемые для титрования кислот и оснований в неводных растворах
- § 16. Амперометрическое титрование
- § 17. Методы прямого потенциометрического титрования
- § 18. Методы косвенного потенциометрического титрования
- § 19. Дифференцированное потенциометрическое титрование
- § 20. Комбинированные методы потенциометрического титрования
- § 21. Хронопотенциометрическое титрование
- § 22. Кондуктометрическое титрование
- § 23. Хронокондуктометрическое титрование
- § 24. Спектрофотометрическое титрование