| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
В. НОВЫЕ НАПРАВЛЕНИЯ В ПОЛЯРОГРАФИИ
Наряду с классической полярографией, которая широко применяется в научно-исследовательских и заводских лабораториях, за последнее время появилось много новых направлений в полярографии Рассмотрим важнейшие из них.
§ 10. Амальгамная полярография с накоплением
Чувствительность классического метода полярографии во многих случаях недостаточна. Новые отрасли техники предъявляют особые требования к чистоте материалов и соответственно к методам ее контроля. В связи с этим появилась необходимость в разработке методов, позволяющих определять примеси при содержании их в анализируемом веществе до  .
.
Одним из таких методов является метод амальгамной полярографии.
Принцип метода. Сущность метода состоит в том, что определяемое вещество в концентрации  некоторое время подвергается электролизу на стационарной ртутной капле при контролируемом потенциале, несколько более отрицательном (на
некоторое время подвергается электролизу на стационарной ртутной капле при контролируемом потенциале, несколько более отрицательном (на  в), чем потенциал полуволны определямого иона. Определяемый элемент при этом концентрируется в ртутной капле в виде амальгамы. Затем выделенный элемент анодно растворяют при потенциале, непрерывно изменяющемся от значения, при котором проводилось катодное выделение элемента на ртути, до более положительных потенциалов (обычно до нуля).
в), чем потенциал полуволны определямого иона. Определяемый элемент при этом концентрируется в ртутной капле в виде амальгамы. Затем выделенный элемент анодно растворяют при потенциале, непрерывно изменяющемся от значения, при котором проводилось катодное выделение элемента на ртути, до более положительных потенциалов (обычно до нуля).
Протекающий в процессе окисления амальгамы ток автоматически записывается или фотографируется регистрирующим полярографом (например, полярографами Гейровского  или
или  ). При этом кривая анодного тока имеет вид характерного зубца (пика), глубина которого пропорциональна концентрации определяемого иона в растворе при условии постоянства других факторов (рис. 52).
). При этом кривая анодного тока имеет вид характерного зубца (пика), глубина которого пропорциональна концентрации определяемого иона в растворе при условии постоянства других факторов (рис. 52).
Устройство ртутного катода. Схема установки для амальгамной полярографии подобна применяемой для обычной классической полярографии, но ртутный катод устроен иначе.
В литературе описано пять типов стандартных ртутных капельных электродов для амальгамной полярографии.
1. Подвешенная ртутная капля. Одна-две капли ртути из обычного капилляра с помощью лопаточки подвешиваются на металлическую проволоку — платиновую, золотую или серебряную.
2. Лежащая капля. Получается выдавливанием определенной порции ртути из капилляра, соединенного с резервуаром, наполненным ртутью.
3. Висящая капля. Получается выдавливанием ртути из капилляра с помощью винтового поршня.
4. Капля ртути электролитически выделяется на платиновой проволоке в определенных условиях.
5. Чашеобразный ртутный электрод. В маленькую чашечку капают определенное количество капель ртути, причем чашечку предварительно гидрофобизируют метилтрихлорсиланом.
Все эти виды электродов имеют достоинства и недостатки.
Для того чтобы метод мог быть использован в аналитической химии, в первую очередь необходимо иметь электрод со строго воспроизводимой величиной поверхности ртутной капли. Небольшая ошибка в размере капли уже дает существенную ошибку в высоте пика. Отсюда ясно, насколько важно стандартизировать каплю, чтобы получить воспроизводимые результаты. Это достигается различными методами, например, определенным углом поворота винтового поршня.

Рис. 52. Анодная полярограмма при амальгамной полярографии с накоплением.
Уравнение Шевчика. Величина максимального тока в методе амальгамной полярографии (равная глубине зубца) определяется уравнением Шевчика:

где  — глубина зубца, а; 217 — постоянный коэффициент;
— глубина зубца, а; 217 — постоянный коэффициент;  — площадь электрода,
— площадь электрода,  ;
;  — число электронов, участвующих в электродном процессе;
— число электронов, участвующих в электродном процессе;  — скорость изменения потенциала, в/сек;
— скорость изменения потенциала, в/сек;  — коэффициент диффузии,
— коэффициент диффузии,  ; С — концентрация восстанавливающегося иона,
; С — концентрация восстанавливающегося иона,  .
.
Из уравнения Шевчика видно, что с увеличением поверхности электрода сила тока увеличивается. Но слишком большое увеличение поверхности ртути ведет к расширению пиков. Это явление вызывает трудности в исследовании смеси ионов металлов вследствие возможного слияния анодных зубцов. Обычно применяют электроды диаметром  мм.
мм.
Из уравнения Шевчика также следует, что глубина зубца должна увеличиваться пропорционально корню квадратному из скорости изменения потенциала.
В обычных регистрирующих полярографах скорость изменения потенциала составляет  в/мин. Чувствительность метода повышается с увеличением скорости изменения потенциала до
в/мин. Чувствительность метода повышается с увеличением скорости изменения потенциала до  .
.
Однако увеличение скорости изменения потенциала ограничивается инерционностью прибора, регистрирующего величину тока, и особенно емкостными токами.
Влияние длительности электролиза. Очень интересным является вопрос о влиянии длительности электролиза на величину анодного тока. Здесь возможны два случая.
1. Объем раствора достаточно велик, радиус капли мал. Глубина анодного пика линейно возрастает со временем электролиза, так как при более продолжительном электролизе накапливается больше вещества в амальгаме.
2. Объем раствора мал  ) и капля относительно велика. Глубина анодного зубца быстро достигает предела, так как наступает обеднение раствора ионами восстанавливающегося вещества и дальнейшее увеличение времени электролиза не увеличивает величину зубца.
) и капля относительно велика. Глубина анодного зубца быстро достигает предела, так как наступает обеднение раствора ионами восстанавливающегося вещества и дальнейшее увеличение времени электролиза не увеличивает величину зубца.
Учитывая сказанное, работают обычно с достаточно большими объемами растворов. В этом случае, увеличивая время электролиза, можно повысить величину предельного тока, т. е. чувствительность определения. Величина предельного тока при окислении амальгамы пропорциональна концентрации вещества в амальгаме, а эта концентрация в свою очередь зависит от концентрации ионов в растворе и времени электролиза. Поэтому время электролиза устанавливают в зависимости от концентрации анализируемого вещества. Для получения анодных пиков удовлетворительной глубины при концентрации раствора около  достаточно 3—5 мин, для
достаточно 3—5 мин, для  мин и для
мин и для  мин.
мин.
Однако и при большом объеме раствора может оказаться, что линейная зависимость тока от времени электролиза сохраняется только до определенного времени, после чего ток достигает предельного значения. Это бывает в тех случаях, когда выделяемый на катоде элемент не образует амальгамы (например, никель), и увеличение времени электролиза не оказывает влияния на величину тока.
Время электролиза следует при этом устанавливать опытным путем, построив кривую зависимости анодного тока от времени электролиза.
Глубина анодного зубца при постоянстве условий опыта находится в линейной зависимости от концентрации определяемых ионов, что дает возможность определять их количественно.
При изменении концентрации ионов металла в растворе потенциал, при котором начинается анодный зубец, изменяется, но потенциал половины высоты зубца на отрицательной его ветви остается постоянным. Значение этого потенциала близко к значению катодного потенциала полуволны на ртутном капельном электроде, оно не зависит от концентрации ионов металла в растворе и скорости изменения потенциала. Измеряя потенциал половины высоты зубца, можно качественно определить наличие тех или иных ионов в растворе.
Рассмотрим, например, методику количественного определения ионов свинца в растворе.
Помещают в электролизер  раствора соли свияца на фоне 1 М растворов
раствора соли свияца на фоне 1 М растворов  . Через раствор в течение 30 мин продувают очищенный азот для удаления кислорода (последний окисляет амальгаму), затем в течение 15 мин при потенциале —0,8 в и перемешивании магнитной мешалкой проводят выделение металла на ртутном катоде. Через 30—45 сек после выключения мешалки потенциал катода автоматически со скоростью 0,4 в/мин изменяют от —0,8 в до нуля. Затем измеряют глубину зубца.
. Через раствор в течение 30 мин продувают очищенный азот для удаления кислорода (последний окисляет амальгаму), затем в течение 15 мин при потенциале —0,8 в и перемешивании магнитной мешалкой проводят выделение металла на ртутном катоде. Через 30—45 сек после выключения мешалки потенциал катода автоматически со скоростью 0,4 в/мин изменяют от —0,8 в до нуля. Затем измеряют глубину зубца.
Такой же обработке подвергают стандартный раствор и рассчитывают концентрацию  на основании пропорциональности концентрации и глубины зубца.
на основании пропорциональности концентрации и глубины зубца.
Преимущества амальгамной полярографии. Метод амальгамной полярографии дает возможность определять одновременно несколько элементов при их совместном присутствии в растворе. Если вести электролиз при потенциале более отрицательном, чем катодный потенциал полуволны наиболее электроотрицательного элемента, то и этот элемент, и все более электроположительные ионы выделяются на ртути с образованием смешанной амальгамы. На анодной полярограмме получается несколько зубцов, глубина которых пропорциональна концентрации каждого из элементов в растворе (рис. 53).
Если даже содержание одного из двух элементов преобладает, но потенциалы анодных зубцов достаточно различаются между собой (на  , то возможно совместное определение этих элементов. В случае преобладающего содержания более электроотрицательного элемента можно вести электролиз при потенциале более положительном по сравнению с потенциалом анодного зубца этого элемента. Тогда в амальгаму перейдет только микропримесь более электроположительного элемента, который можно определять по анодному зубцу. Например, в цинке или алюминии можно определять примеси
, то возможно совместное определение этих элементов. В случае преобладающего содержания более электроотрицательного элемента можно вести электролиз при потенциале более положительном по сравнению с потенциалом анодного зубца этого элемента. Тогда в амальгаму перейдет только микропримесь более электроположительного элемента, который можно определять по анодному зубцу. Например, в цинке или алюминии можно определять примеси  свинца, сурьмы, висмута, меди и других элементов, проводя электролиз этих металлов при потенциале более положительном, чем потенциал восстановления алюминия или цинка.
свинца, сурьмы, висмута, меди и других элементов, проводя электролиз этих металлов при потенциале более положительном, чем потенциал восстановления алюминия или цинка.
В случае преобладающего (не очень большого) содержания более электроположительного элемента, можно оба элемента перевести электролизом в амальгаму и, получив зубец более электроотрицательной примеси, прекратить съемку полярограммы перед большим зубцом второго элемента. При меньшей чувствительности гальванометра можно получить также зубец и второго элемента.
Иногда путем подбора комплексообразующего реагента можно изменить потенциалы восстановления обоих ионов и создать благоприятные условия, например, такие, в которых потенциал элемента, находящегося в большом количестве, оказывается более отрицательным.
Устранения мешающего влияния элементов можно достигнуть, применяя электрод в виде ртутной капли, подвешенной на металлический контакт.
Некоторые элементы — цинк, кадмий, галлий — дают с амальгамой золота интерметаллические соединения, которые окисляются при более положительных потенциалах, чем чистая амальгама данного металла. Например, на электроде с золотым контактом можно определять индий в присутствии кадмия, так как индий не образует интерметаллического соединения с золотом, а кадмий образует.
Вообще же образование интерметаллических соединений в амальгаме (между определяемыми элементами) может привести к неправильным результатам анализа, поскольку при выделении таких пар металлов, как  , наблюдается понижение анодного зубца первого металла при наличии второго. Иногда появляется третий зубец интерметаллического соединения. Образование интерметаллических соединений наблюдается при концентрациях
, наблюдается понижение анодного зубца первого металла при наличии второго. Иногда появляется третий зубец интерметаллического соединения. Образование интерметаллических соединений наблюдается при концентрациях  и мало заметно при низких концентрациях порядка
и мало заметно при низких концентрациях порядка  .
.
Необходимо каждый раз опытным путем устанавливать наличие или отсутствие взаимного влияния металлов при их совместном выделении в амальгаму.
При определении малых примесей в различных веществах удобнее всего пользоваться методом добавок. Так определяют, например, примесь свинца в ацетате цинка. Сначала измеряют глубину зубца для анализируемого раствора. Затем, стряхнув каплю ртути, на которой проводили определение, и подготовив новую каплю такого же размера, добавляют в тот же раствор строго определенное количество стандартного раствора (несколько капель из микробюретки) и снова проводят электролиз и съемку анодного пика при всех равных условиях.
Например, пусть глубина зубца для анализируемого раствора равна 37 мм а с добавкой стандартного раствора  она составляет 51 мм.
она составляет 51 мм.
Тогда расчет проводят следующим образом:

В методе амальгамной полярографии большое внимание следует уделять очистке реактивов и воды. Химически чистые реактивы обычно содержат примеси тяжелых металлов — цинка, свинца, меди в количествах, которые препятствуют определению этих элементов при содержании  . Очистить от тяжелых металлов многие легколетучие вещества — воду, кислоты и другие можно перегонкой в кварцевом аппарате.
. Очистить от тяжелых металлов многие легколетучие вещества — воду, кислоты и другие можно перегонкой в кварцевом аппарате.
Для извлечения микропримесей металлов из реактивов широко применяется экстракция, ионообменная хроматография, адсорбция и электролиз.
При работе с обычной посудой происходит выщелачивание ионов металлов, поэтому работают с кварцевой, полиэтиленовой и тефлоновой посудой.
Метод амальгамной полярографии позволяет достичь увеличения чувствительности на 3—4 порядка по сравнению с обычным полярографическим методом с капающим ртутным электродом.

Рис. 53. Анодная полярограмма раствора, содержащего несколько катионов.
Он применим для определения концентраций вещества от  до
до  и дает возможность определять в особо чистых реактивах и металлах микропримеси порядка
и дает возможность определять в особо чистых реактивах и металлах микропримеси порядка  с точностью 5—10%.
с точностью 5—10%.
Кроме того, метод обладает большой разрешающей способностью, применяя его можно определять несколько элементов из одного раствора без их предварительного химического разделения даже в том случае, когда концентрации этих элементов значительно различаются.
Полярография с накоплением может быть не только амальгамной. За последнее время быстро развивается так называемая пленочная полярография с накоплением. В качестве индикаторных электродов здесь используются твердые электроды, главным образом графитовый. Определяемые вещества накапливаются на электроде в чистом виде (металлы) или в виде различных соединений, а затем происходит растворение осадка при меняющемся потенциале.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ВВЕДЕНИЕ
- ГЛАВА I. ОСНОВЫ ФИЗИКО-ХИМИЧЕСКИХ (ИНСТРУМЕНТАЛЬНЫХ) МЕТОДОВ АНАЛИЗА
- § 1. Особенности физико-химических методов анализа
- § 2. Области применения инструментальных методов анализа
- § 3. Анализ веществ высокой чистоты
- § 4. Повышение чувствительности и точности методов определения следов примесей
- § 5. Инструментальные методы титрования
- § 6. Применение физико-химических методов анализа для определения индивидуальных соединений
- § 7. Применение физико-химических методов для анализа смесей веществ
- § 8. Классификация инструментальных количественных методов анализа
- § 9. Электрохимические методы анализа
- § 10. Спектральные (оптические) методы анализа
- § 11. Хроматографические методы анализа
- § 12. Радиометрические методы анализа
- § 13. Масс-спектрометрические методы анализа
- § 14. Физико-химический анализ по Н. С. Курнакову
- § 15. Другие методы анализа
- ГЛАВА II. ПОТЕНЦИОМЕТРИЯ И ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- § 1. Зависимость величины электродных потенциалов от концентрации (активности)
- § 2. Применение потенциометрического метода анализа
- § 3. Потенциометрическое титрование
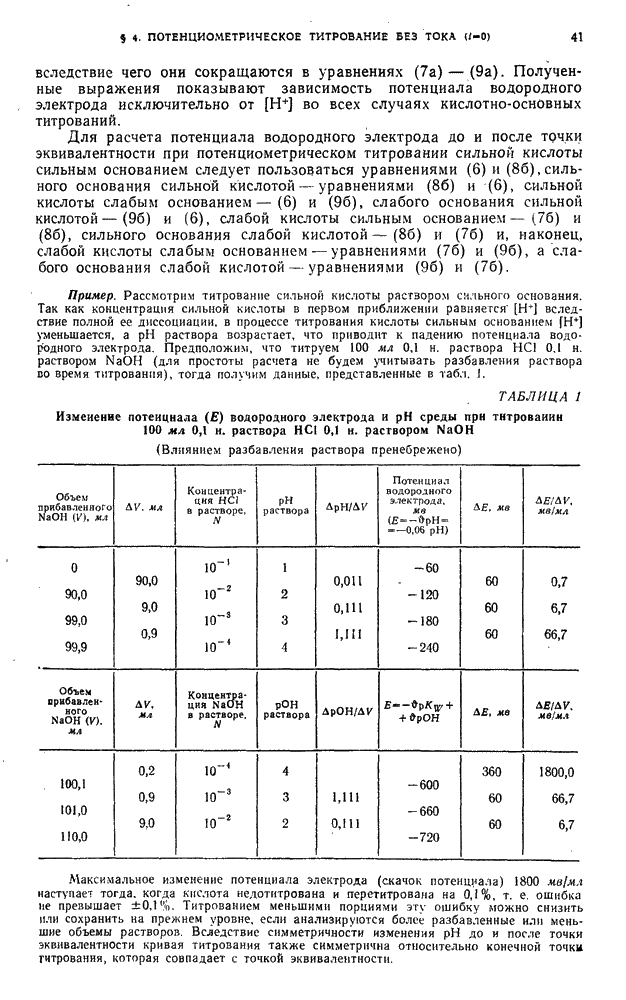
- § 4. Потенциометрическое титрование без тока (i=0)
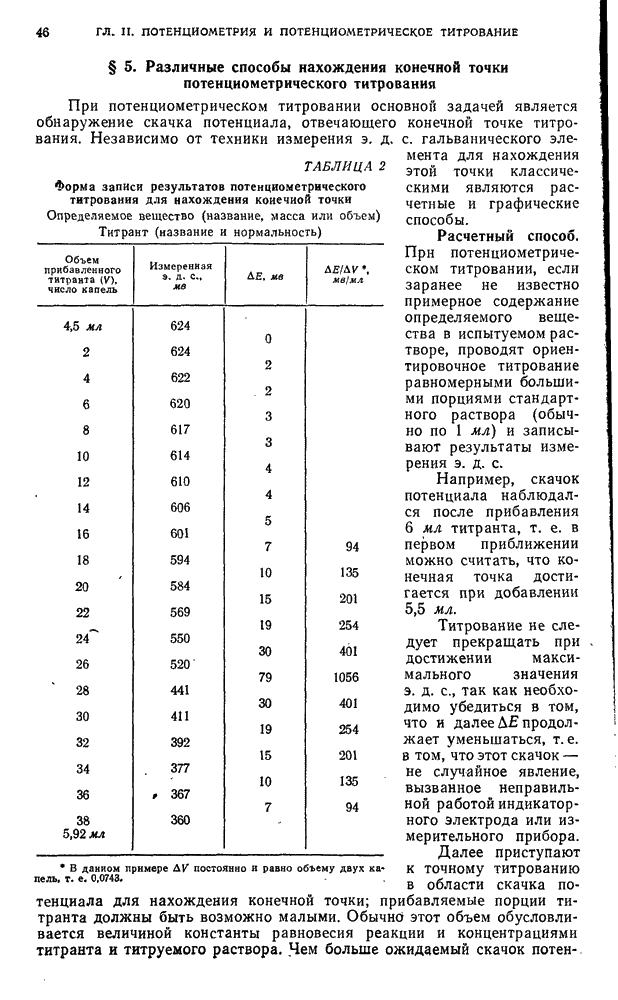
- § 5. Различные способы нахождения конечной точки потенциометрического титрования
- § 6. Некомпенсационный метод потенциометрического титрования
- § 7. Потенциометрическое титрование под током (i != 0)
- Б. АППАРАТУРА И ТЕХНИКА ВЫПОЛНЕНИЯ АНАЛИЗА
- § 8. Измерение электродвижущей силы
- § 9. Установка для поляризации электродов при потенциометрическом титровании под током
- § 10. Некоторые приборы, применяемые в потенциометрическом титровании
- § 11. Электроды
- В. ПРАКТИЧЕСКИЕ РАБОТЫ ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ БЕЗ ТОКА (i=0)
- § 12. Кислотно-основное титрование
- § 13. Титрование по методу окисления — восстановления
- § 14. Титрование по методу осаждения
- § 15. Титрование по методу комплексообразования
- ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ ПОД ТОКОМ (i != 0)
- § 16. Титрование по методу окисления — восстановления
- ГЛАВА III. КОНДУКТОМЕТРИЯ и КОНДУКТОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- § 1. Удельная и эквивалентная электропроводность
- § 2. Кондуктометрическне методы анализа
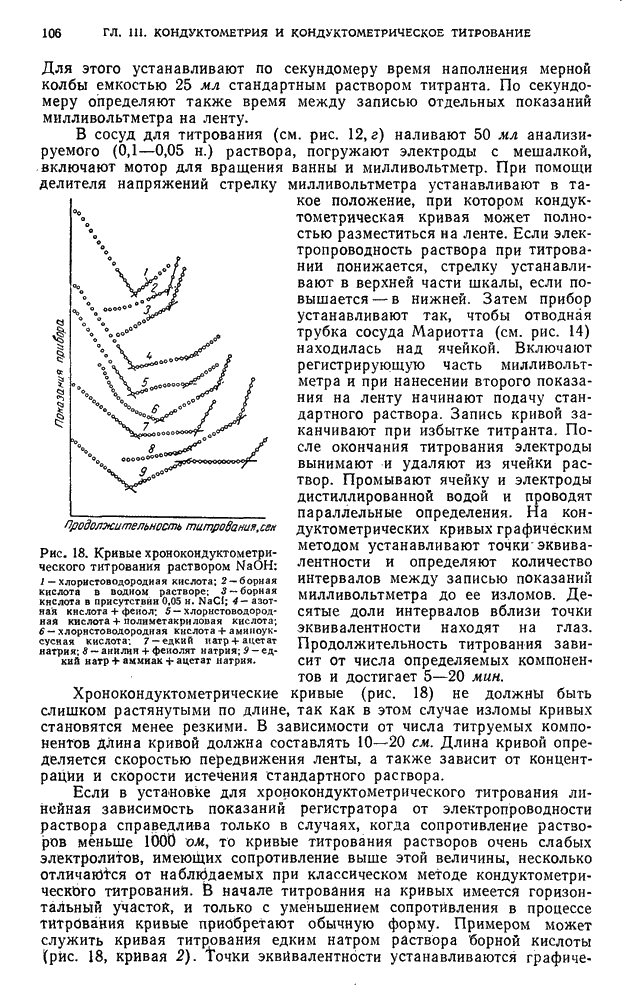
- § 3. Кислотно-основное титрование
- § 4. Титрование, основанное на реакциях осаждения
- § 5. Титрование, основанное на реакциях окисления — восстановления
- § 6. Титрование, основанное на реакциях комплексообразования
- Б. АППАРАТУРА И ТЕХНИКА ВЫПОЛНЕНИЯ АНАЛИЗА
- § 7. Измерение электропроводности растворов
- § 8. Конструкции электролитических ячеек
- § 9. Измерения в хронокондуктометрическом титровании
- В. ПРАКТИЧЕСКИЕ РАБОТЫ
- § 10. Подготовка к определению
- §11. Определение индивидуальных кислот методом кондуктометрического титрования
- § 12. Определение индивидуальных оснований методом кондуктометрического титрования
- § 13. Анализ смесей оснований методом кондуктометрического титрования
- § 14. Определение солей методом кондуктометрического титрования
- § 15. Анализ смесей кислот и солей слабых оснований методом кондуктометрического титрования
- § 16. Анализ смесей кислот методом хронокондуктометрического титрования
- § 17. Анализ смесей оснований и солей слабых кислот методом хронокондуктометрического титрования
- ГЛАВА IV. ВЫСОКОЧАСТОТНОЕ ТИТРОВАНИЕ
- § 1. Общие положения теории высокочастотного титрования
- § 2. Физические основы и погрешности метода высокочастотного титрования
- § 3. Физические основы метода диэлкометрического титрования
- § 4. Погрешности метода диэлкометрического титрования
- ТЕОРИЯ ИЗМЕРИТЕЛЬНЫХ ЯЧЕЕК ЕМКОСТНОГО ТИПА
- § 5. Электрическая эквивалентная схема ячейки и физические процессы, протекающие в ее объеме
- § 6. Импеданс и полная проводимость ячейки
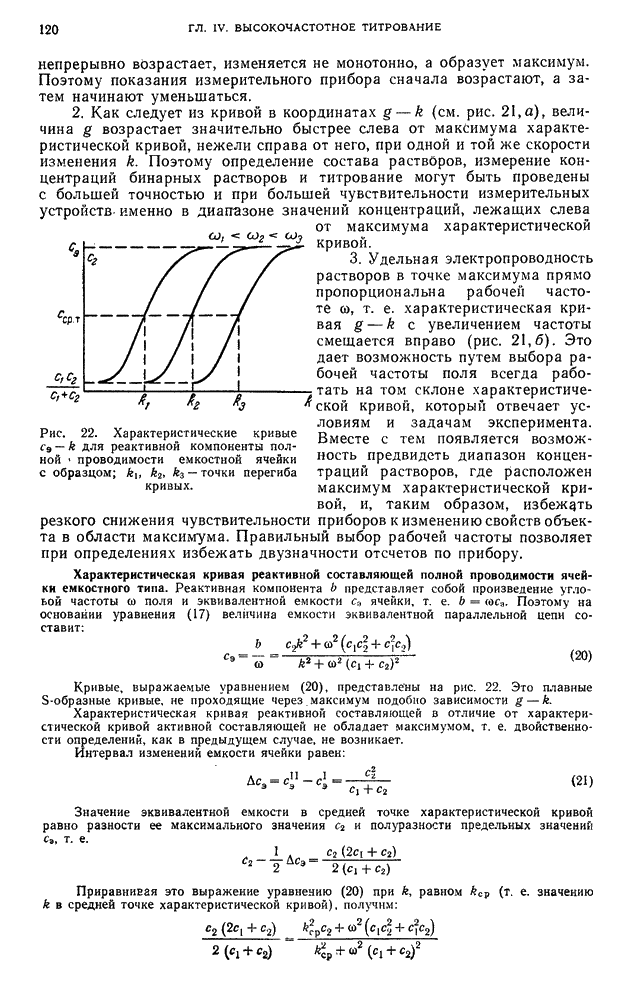
- § 7. Характеристические кривые ячейки
- § 8. Чувствительность ячейки
- § 9. Критерий применимости и постоянная с-ячейки
- ТЕОРИЯ ИЗМЕРИТЕЛЬНЫХ ЯЧЕЕК ИНДУКТИВНОГО ТИПА
- § 10. Электрическая эквивалентная схема ячейки
- § 11. Импеданс и характеристические кривые ячейки
- § 12. Критерий применимости и постоянная L-ячейки
- § 13. Влияние на характеристические кривые ячейки ее некомпенсированного электрического поля
- ДИАГРАММЫ СООТВЕТСТВИЯ
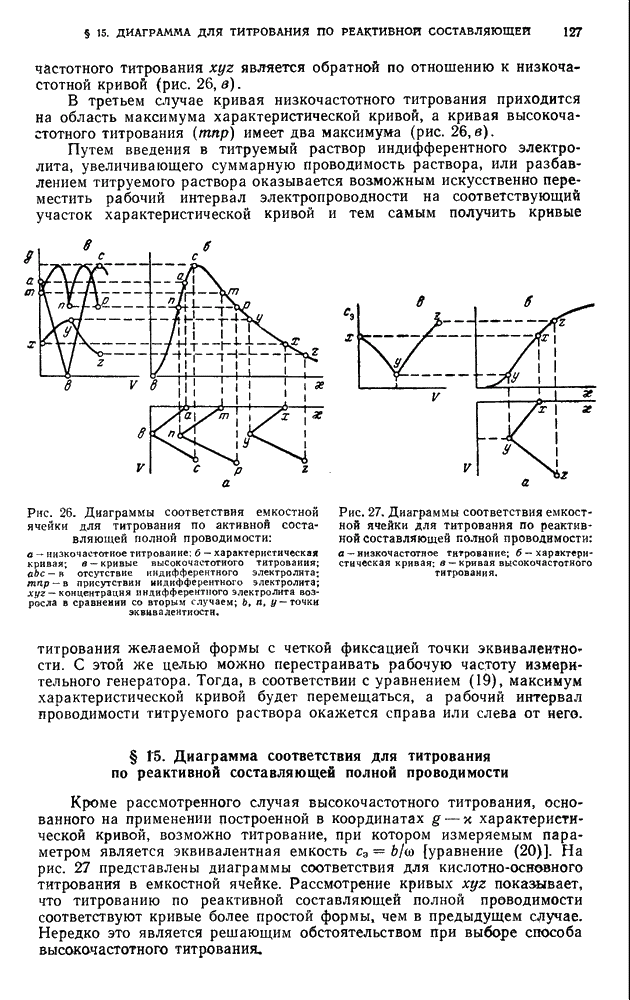
- § 14. Диаграмма соответствия для титрования по активной составляющей полной проводимости
- § 15. Диаграмма соответствия для титрования по реактивной составляющей полной проводимости
- § 16. Выбор типа диаграмм
- Б. АППАРАТУРА И ТЕХНИКА ВЫПОЛНЕНИЯ АНАЛИЗА
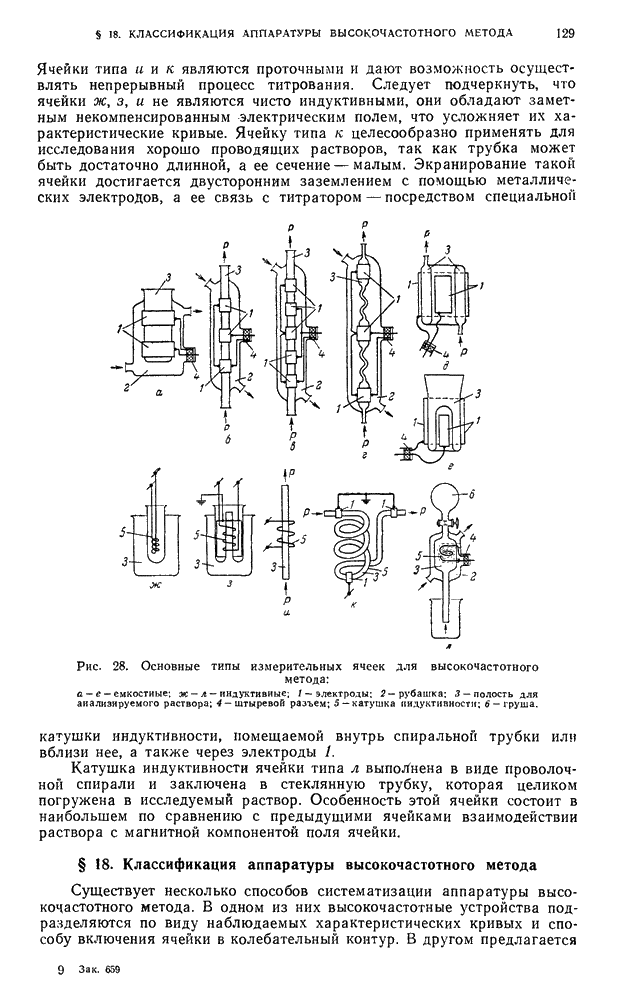
- § 17. Измерительные ячейки (датчики) высокочастотного метода и области их применения
- § 18. Классификация аппаратуры высокочастотного метода
- § 19. Высокочастотные титраторы
- § 20. Общие правила работы с приборами для высокочастотного анализа
- В. ПРАКТИЧЕСКИЕ РАБОТЫ
- § 21. Высокочастотное титрование стандартных растворов
- § 22. Высокочастотное титрование растворов неизвестной концентрации
- ГЛАВА V. ПОЛЯРОГРАФИЧЕСКИЙ МЕТОД АНАЛИЗА И АМПЕРОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
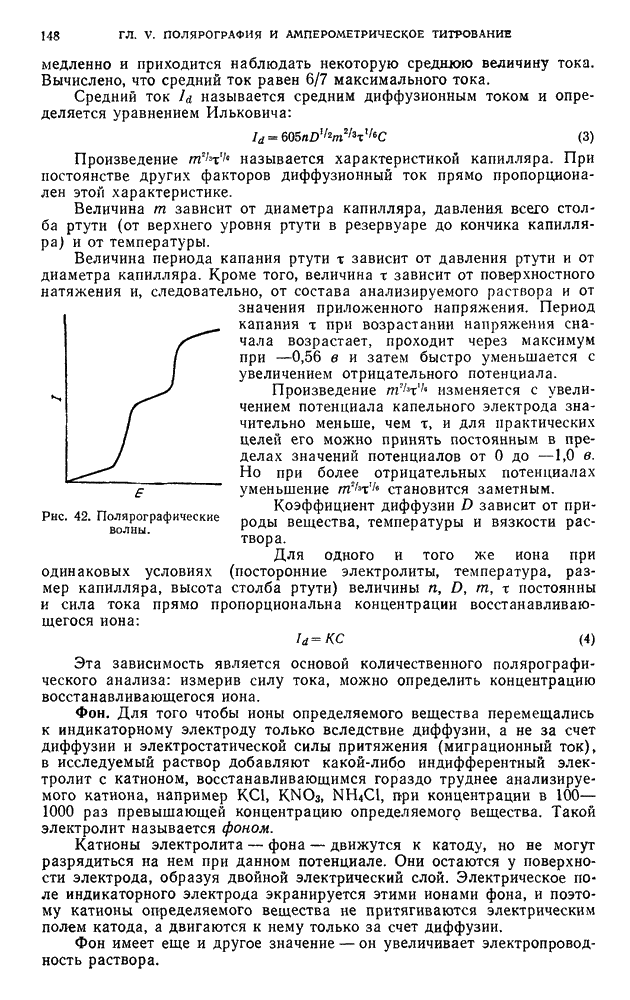
- § 1. Предельный, или диффузионный, ток
- § 2. Возникновение диффузионного тока на твердых микроэлектродах
- Б. АППАРАТУРА И ТЕХНИКА ВЫПОЛНЕНИЯ ПОЛЯРОГРАФИЧЕСКОГО АНАЛИЗА
- § 3. Полярографы
- § 4. Электролитическая ячейка
- § 5. Электролизеры
- § 6. Электроды сравнения
- § 7. Снятие полярограммы на полярографической установке с визуальным полярографом
- § 8. Методы количественного полярографического анализа
- § 9. Правила техники безопасности при работе с металлической ртутью
- В. НОВЫЕ НАПРАВЛЕНИЯ В ПОЛЯРОГРАФИИ
- § 10. Амальгамная полярография с накоплением
- § 11. Осциллографическая полярография
- § 12. Переменнотоковая полярография
- Г. ПРАКТИЧЕСКИЕ РАБОТЫ С ПРИМЕНЕНИЕМ ПОЛЯРОГРАФИЧЕСКОГО МЕТОДА АНАЛИЗА
- § 13. Примеры полярографических определений
- АМПЕРОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- § 14. Особенности амперометрического титрования
- Б. АППАРАТУРА И ТЕХНИКА ВЫПОЛНЕНИЯ АМПЕРОМЕТРИЧЕСКОГО ТИТРОВАНИЯ
- § 15. Схема установки и применяемые электроды
- § 16. Амперометрическое титрование с двумя индикаторными электродами
- В. ПРАКТИЧЕСКИЕ РАБОТЫ С ПРИМЕНЕНИЕМ АМПЕРОМЕТРИЧЕСКОГО ТИТРОВАНИЯ
- § 17. Примеры амперометрического титрования
- ГЛАВА VI. КУЛОНОМЕТРИЯ И КУЛОНОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- § 1. Сущность и классификация кулонометрических методов
- ПРЯМАЯ КУЛОНОМЕТРИЯ
- § 2. Прямая кулонометрия при постоянном потенциале рабочего электрода (прямая потенциостатическая кулонометрия)
- § 3. Использование прямой потенциостатической кулонометрии
- § 4. Прямая кулонометрия при постоянной силе тока электролиза (прямая амперостатическая кулонометрия)
- § 5. Использование прямой амперостатической кулонометрии
- КУЛОНОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- § 6. Кулонометрическое титрование при постоянной силе тока электролиза
- § 7. Использование амперостатического кулонометрического титрования
- § 8. Кулонометрическое титрование првд постоянном потенциале рабочего электрода
- § 9. Особенности кулонометрических методов анализа
- Б. АППАРАТУРА И ТЕХНИКА ВЫПОЛНЕНИЯ АНАЛИЗА
- § 10. Электроды
- § 11. Электролизеры
- § 12. Приборы для измерения количества электричества, израсходованного на электролиз вещества
- § 13. Приборы, обеспечивающие стабильность потенциала рабочего электрода или силы тока электролиза, и установки для кулонометрического анализа
- В. ПРАКТИЧЕСКИЕ РАБОТЫ
- § 14. Работы, выполняемые методом прямой кулонометрии
- § 15. Работы, выполняемые методом косвенной кулонометрии, или кулонометрического титрования, при постоянной силе тока электролиза
- ГЛАВА VII. СПЕКТРАЛЬНЫЕ (ОПТИЧЕСКИЕ) МЕТОДЫ АНАЛИЗА
- § 1. Общая характеристика метода
- § 2. Классификация методов эмиссионного спектрального анализа
- § 3. Качественный спектральный анализ
- § 4. Полуколичественные методы спектрального анализа
- § 5. Количественный спектральный анализ
- § 6. Основы фотографического метода эмиссионного количественного анализа
- § 7. Зависимость между почернением фотопластинки и интенсивностью излучения
- Б. АППАРАТУРА И ТЕХНИКА ВЫПОЛНЕНИЯ АНАЛИЗА
- § 8. Источники возбуждения спектров
- § 9. Спектральные приборы
- § 10. Вспомогательные приборы и принадлежности
- § 11. Микрофотометр МФ-2
- В. ПРАКТИЧЕСКИЕ РАБОТЫ
- § 12. Качественный анализ при помощи стилоскопа
- § 13. Качественный анализ фотографическим методом при помощи спектра железа в ультрафиолетовой области
- § 14. Полуколичественный анализ
- § 15. Количественный анализ
- СПЕКТРОФОТОМЕТРИЯ ПЛАМЕНИ
- § 16. Общая характеристика метода
- Б. АППАРАТУРА И ТЕХНИКА ВЫПОЛНЕНИЯ АНАЛИЗА
- § 17. Схема установки, применяемой для анализа методом спектрофотометрии пламени
- В. ПРАКТИЧЕСКИЕ РАБОТЫ
- § 18. Определения по методу спектрофотометрии пламени
- АТОМНО-АБСОРБЦИОННЫЙ СПЕКТРАЛЬНЫЙ АНАЛИЗ
- § 19. Общая характеристика метода
- МОЛЕКУЛЯРНО-АБСОРБЦИОННЫЙ СПЕКТРАЛЬНЫЙ АНАЛИЗ
- § 20. Общая характеристика метода
- § 21. Законы поглощения света
- § 22. Отклонения от закона Бугера—Ламберта—Бера
- § 23. Качественный анализ спектрофотометрическим методом
- § 24. Количественный анализ спектрофотометрическим методом
- § 25. Методы определения концентрации веществ, поглощающих в видимой и ультрафиолетовой областях спектра
- § 26. Определение нескольких компонентов в растворе
- § 27. Определение концентрации вещества в растворе дифференциальным методом
- § 28. Выбор толщины слоя и оптимальной концентрации исследуемого раствора
- § 29. Выбор длины волны поглощаемого излучения при спектрофотометрических измерениях
- Б. АППАРАТУРА И ТЕХНИКА ВЫПОЛНЕНИЯ АНАЛИЗА
- § 30. Приборы, применяемые для спектрофотометрического анализа в ультрафиолетовой и видимой областях спектра
- § 31. Приборы, применяемые для колориметрического анализа
- § 32. Приборы, применяемые для спектрофотометрического анализа в инфракрасной области спектра
- § 33. Нулевые растворы
- В. ПРАКТИЧЕСКИЕ РАБОТЫ
- § 34. Определение в ультрафиолетовой области спектра
- § 35. Определение в видимой области спектра
- § 36. Определение в инфракрасной области спектра
- СПЕКТРОФОТОМЕТРИЧЕСКИЕ (ФОТОМЕТРИЧЕСКИЕ) МЕТОДЫ ТИТРОВАНИЯ
- § 37. Общая характеристика метода
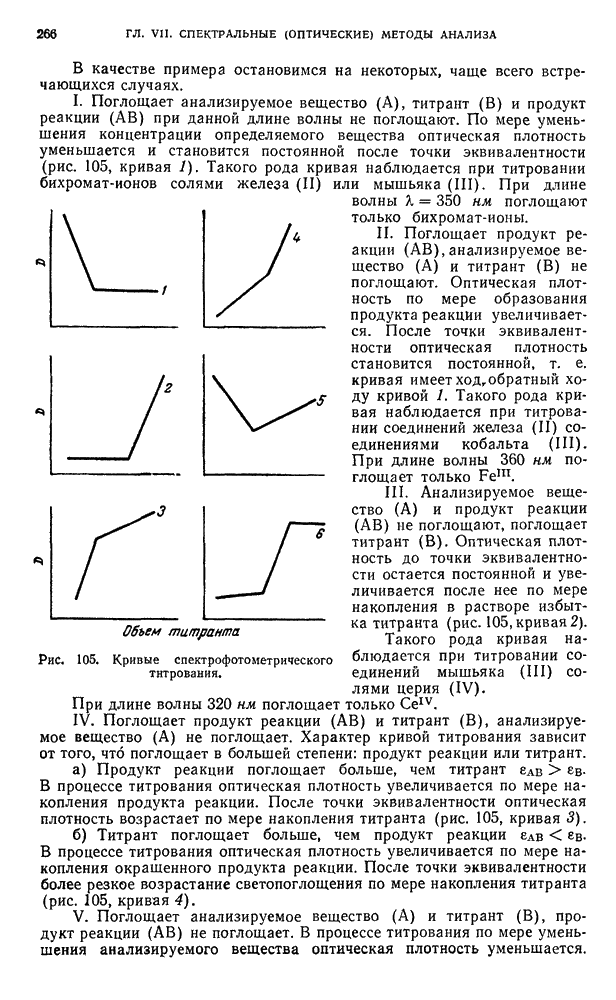
- § 38. Кривые спектрофотометрического титрования
- Б. АППАРАТУРА И ТЕХНИКА ВЫПОЛНЕНИЯ ТИТРОВАНИЯ
- § 39. Установки для спектрофотометрического титрования
- В. ПРАКТИЧЕСКИЕ РАБОТЫ
- § 40. Спектрофотометрическое титрование
- НЕФЕЛОМЕТРИЧЕСКИЙ И ТУРБИДИМЕТРИЧЕСКИЙ МЕТОДЫ АНАЛИЗА
- § 41. Общая характеристика методов
- Б. АППАРАТУРА И ТЕХНИКА ВЫПОЛНЕНИЯ АНАЛИЗА
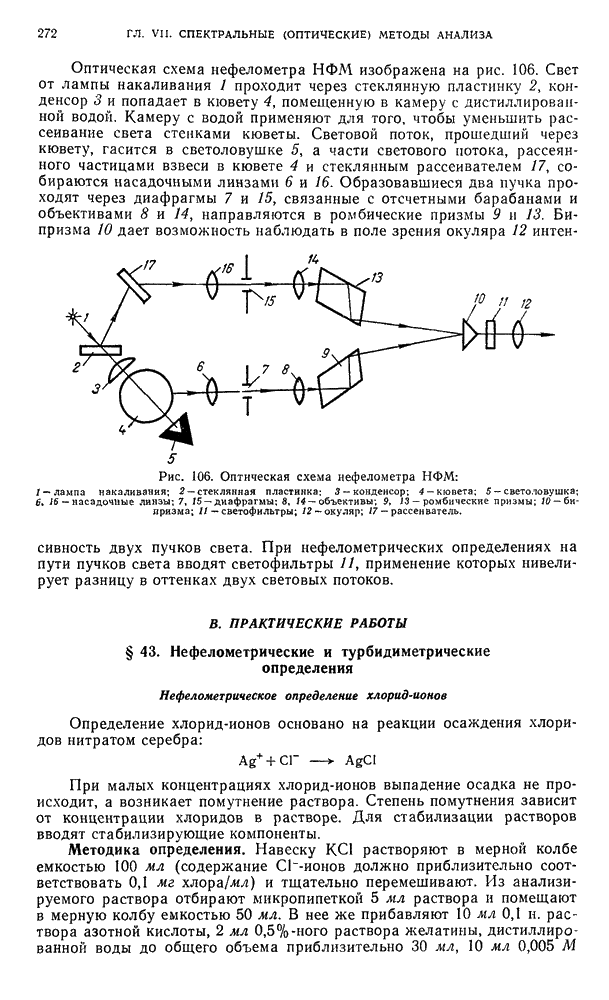
- § 42. Приборы, применяемые для нефелометрических и турбидиметрических измерений
- В. ПРАКТИЧЕСКИЕ РАБОТЫ
- § 43. Нефелометрические и турбидиметрические определения
- § 44. Фототурбидиметрическое и фотонефелометрическое титрование
- ГЛАВА VIII. ХРОМАТОГРАФИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
- § 1. Классификация хроматографических методов анализа
- § 2. Адсорбционная хроматография
- § 3. Разновидности газовой хроматографии
- § 4. Распределительная хроматография
- § 5. Ионообменная хроматография
- § 6. Константа ионного обмена
- § 7. Осадочная хроматография
- § 8. Окислительно-восстановительная хроматография
- § 9. Адсорбционно-комплексообразовательная хроматография
- § 10. Хроматографические колонки, применяемые в адсорбционно-жидкостной хроматографии
- § 11. Аппаратура, применяемая в газовой хроматографии
- § 12. Приборы и материалы, применяемые в распределительной хроматографии
- § 13. Колонки, применяемые в ионообменной хроматографии
- § 14. Колонки, применяемые в осадочной и окислительновосстановительной хроматографии
- В. ПРАКТИЧЕСКИЕ РАБОТЫ
- § 15. Работы по методу адсорбционной (жидкостной и газовой) хроматографии
- § 16. Работы по методу распределительной хроматографии
- § 17. Работы по методу ионообменной хроматографии
- § 18. Работы по методу осадочной хроматографии
- § 19. Работы по методу окислительно-восстановительной хроматографии
- § 20. Работы по методу адсорбционно-комплексообразовательной хроматографии
- ГЛАВА IX. РАДИОМЕТРИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
- § 1. Виды радиоактивного распада
- § 2. Скорость распада
- § 3. Взаимодействие излучения с веществом
- § 4. Ошибки при измерении радиоактивности
- Б. ЭЛЕМЕНТЫ ТЕХНИКИ БЕЗОПАСНОСТИ ПРИ РАБОТЕ С РАДИОАКТИВНЫМИ ВЕЩЕСТВАМИ
- § 5. Понятия и единицы измерения
- § 6. Классификация источников радиоактивного излучения и радиоактивных изотопов
- § 7. Классификация химических операций с радиоактивными веществами
- § 8. Устройство лабораторий и классификация работ
- § 9. Специальное оборудование для работ с радиоактивными веществами
- § 10. Средства индивидуальной защиты
- § 11. Проведение работ в химической лаборатории с радиоактивными веществами
- § 12. Правила работы с радиоактивными веществами
- В. МЕТОДЫ РЕГИСТРАЦИИ РАДИОАКТИВНОГО ИЗЛУЧЕНИЯ
- § 13. Ионизационные методы
- § 14. Сцинтилляционный метод
- Г. АППАРАТУРА И ТЕХНИКА ИЗМЕРЕНИЯ РАДИОАКТИВНОСТИ
- § 15. Радиометрические установки
- § 16. Измерение радиоактивности
- § 17. Измерение дозы на рабочем месте, индивидуальной дозы, полученной работающим, и загрязненности рабочих поверхностей, рук и одежды
- § 18. Абсолютные и относительные измерения активности
- Д. РАДИОМЕТРИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ
- § 19. Приготовление раствора с заданной активностью
- § 20. Прямое определение ионов химических элементов в растворе с помощью радиоактивных реагентов
- § 21. Практические работы, выполняемые методом прямого определения
- § 22. Метод радиометрического титрования
- § 23. Практические работы, выполняемые методом радиометрического титрования
- § 24. Метод изотопного разбавления
- § 25. Практические работы, выполняемые методом изотопного разбавления
- § 26. Метод активационного анализа
- § 27. Практические работы, выполняемые методом активационного анализа
- § 28. Фотонейтронный метод
- § 29. Практические работы, выполняемые фотонейтронным методом
- § 30. Методы определения содержания химических элементов по излучению их естественных радиоактивных изотопов
- § 31. Практические работы по определению содержания химических элементов методом измерения излучения их естественных радиоактивных изотопов
- § 32. Методы анализа, основанные на поглощении излучения
- § 33. Практические работы, выполняемые по методу анализа, основанному на поглощении излучения
- § 34. Метод, основанный на отражении бетта-излучения
- § 35. Практические работы, выполняемые по методу, основанному на отражении бетта-излучения
- ГЛАВА X. ФИЗИКО-ХИМИЧЕСКИЕ МЕТОДЫ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ РЕДКИХ ЭЛЕМЕНТОВ
- § 1. Работы, выполняемые методом амперометрического титрования
- § 2. Работы, выполняемые полярографическим методом
- § 3. Работы, выполняемые фотометрическим методом
- § 4. Работы, выполняемые экстракционно-фотометрическим методом
- § 5. Работы, выполняемые спектрофотометрическим методом
- § 6. Работы, выполняемые флуориметрическим методом
- § 7. Работы, выполняемые методом потенциометрического титрования
- ГЛАВА XI. ФИЗИКО-ХИМИЧЕСКИЕ (ИНСТРУМЕНТАЛЬНЫЕ) МЕТОДЫ АНАЛИЗА НЕВОДНЫХ РАСТВОРОВ
- § 1. Влияние химической природы и физико-химических свойств растворителей на свойства растворенного вещества
- § 2. Классификация неводных растворителей по их протонно-донорно-акцепторным свойствам
- § 3. Классификация неводных растворителей по признаку их влияния на относительную силу электролитов
- § 4. Дифференцирующее действие растворителей
- § 5. Константы диссоциации, потенциалы полунейтрализации в неводных средах и относительная шкала кислотности
- § 6. Шкала pH и константы автопротолиза неводных растворителей
- § 7. Абсолютная (единая) шкала кислотности растворителей
- § 8. Химико-аналитическое использование неводных растворителей
- Б. АППАРАТУРА И ТЕХНИКА ТИТРОВАНИЯ НЕВОДНЫХ РАСТВОРОВ
- § 9. Установки, используемые при амперометрическом титровании неводных растворов
- § 10. Установки, используемые при потенциометрическом титровании неводных растворов
- § 11. Установки, используемые при кондуктометрическом титровании неводных растворов
- § 12. Установки, используемые при высокочастотном титровании неводных растворов
- § 13. Установки, используемые при спектрофотометрическом титровании неводных растворов
- В. ПРАКТИЧЕСКИЕ РАБОТЫ
- § 14. Очистка и обезвоживание неводных растворителей
- § 15. Титранты, применяемые для титрования кислот и оснований в неводных растворах
- § 16. Амперометрическое титрование
- § 17. Методы прямого потенциометрического титрования
- § 18. Методы косвенного потенциометрического титрования
- § 19. Дифференцированное потенциометрическое титрование
- § 20. Комбинированные методы потенциометрического титрования
- § 21. Хронопотенциометрическое титрование
- § 22. Кондуктометрическое титрование
- § 23. Хронокондуктометрическое титрование
- § 24. Спектрофотометрическое титрование