| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
§ 109. Осмотическое давление
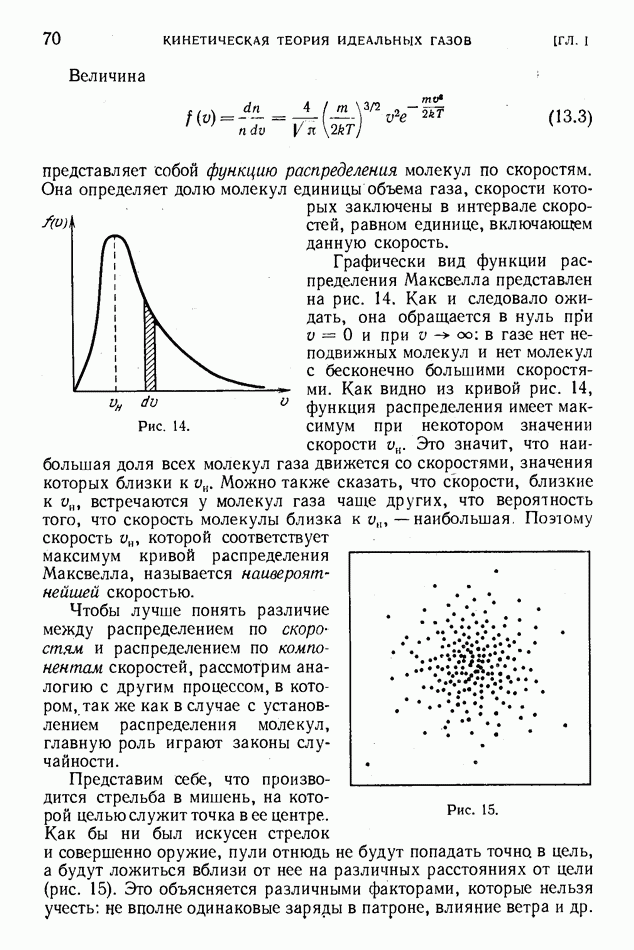
Представим себе, что в одном и том же сосуде находятся, соприкасаясь друг с другом, раствор и чистый растворитель. Очевидно, что частицы растворенного вещества будут переходить из раствора в растворитель, и этот процесс диффузии закончится только тогда, когда будет достигнуто равновесие, т. е. когда растворенное вещество равномерно распределится по всему объему растворителя. Точно так же, если соседствуют не раствор и чистый растворитель, а два раствора разных концентраций, то и в этом случае будет происходить диффузия частиц растворенного вещества из более концентрированного в более слабый раствор, пока концентрация не станет одинаковой во всем объеме. Растворенное вещество как бы расширяется, стремясь занять весь доступный емулэбъем
растворителя, совершенно так же, как расширяется газ, чтобы занять весь предоставленный ему объем.
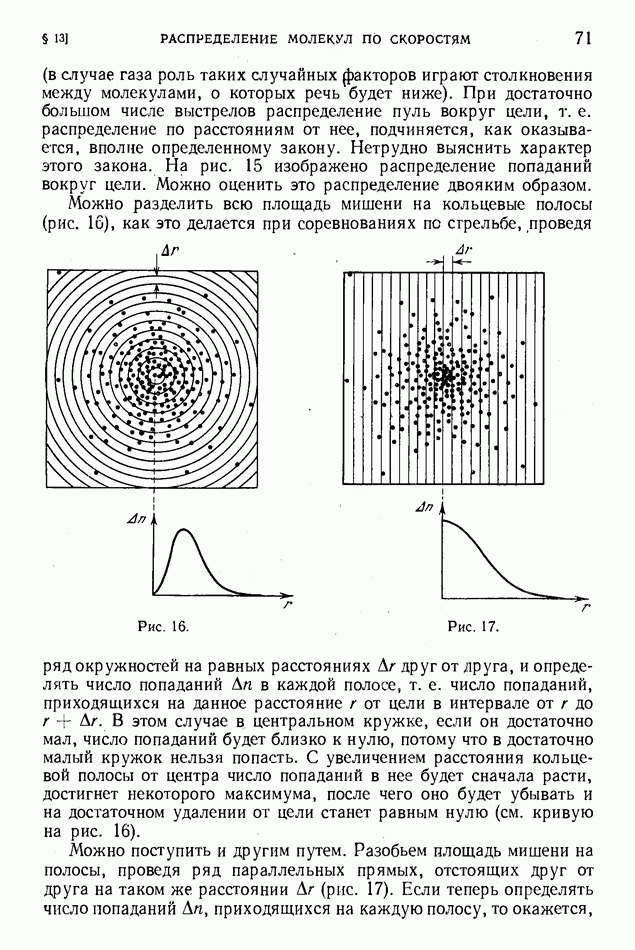
Подобно тому, как газ оказывает давление на стенки сосуда, а при расширении может совершить работу перемещения стенки, если она подвижна (поршень), растворенное вещество тоже должно оказывать давление на ту границу, которая разделяет раствор и чистый растворитель или два раствора с различными концентрациями (разность концентраций здесь играет такую же роль, какую в газах играет разность давлений). Давление это можно наблюдать, если поместить между раствором и чистым растворителем полупроницаемую перегородку, т. е. перегородку, через которую легко проходит растворитель, но не проходит растворенное вещество (рис. 136). Тогда растворитель будет переходить в райтвор и уровень жидкости в той части сосуда, где находится раствор, будет повышаться. Частицы растворенного вещества как бы стремятся продвинуть перегородку сквозь растворитель, но фактически смещается не жестко закрепленная перегородка, а уровень жидкости (если бы можно было сделать полупроницаемый подвижный поршень, то смещался бы именно он).

Рис. 136.
Давление, которое растворенное вещество оказывает на полупроницаемую перегородку, называется осмотическим - давлением, а вызванное этим проникновение растворителя в раствор называется осмосом. Подъем уровня жидкости раствора будет продолжаться до тех пор, пока возникшее гидростатическое давление не окажется равным осмотическому давлению. Можно не допустить подъема уровня, если приложить к раствору внешнее давление. То значение этого давления, которое требуется для сохранения равенства уровней по обе стороны перегородки, очевидно, и равно осмотическому давлению.
Осмотическое давление, как показывает опыт, пропорционально концентрации раствора и обратно пропорционально его объему. Оно зависит также от температуры. Вант-Гофф показал (1887 г.), что связь между этими величинами имеет вид:

Здесь  — осмотическое давление, V — объем раствора,
— осмотическое давление, V — объем раствора,  число молей растворенного вещества,
число молей растворенного вещества,  универсальная газовая постоянная и
универсальная газовая постоянная и  температура. Закон, выражаемый этим уравнением, называется законом Вант-Гоффа.
температура. Закон, выражаемый этим уравнением, называется законом Вант-Гоффа.
Полное сходство уравнения закона Вант-Гоффа с уравнением состояния идеальных газов показывает, что частицы растворенного
вещества в слабом растворе ведут себя так же, как молекулы идеального газа, так что закон Вант-Гоффа можно сформулировать так: осмотическое давление, оказываемое растворенным веществом, равно давлению, которое производило бы это же вещество в газообразном состоянии в том же объеме и при той же температуре.
Осмотическое давление, разумеется, не зависит от вида полупроницаемой перегородки или от рода растворителя. Понятно, что любые растворы с одинаковой молярной концентрацией оказывают одинаковое осмотическое давление.
Сходство в поведении растворенного вещества и идеального газа обусловлено тем, что в сильно разбавленном растворе частицы растворенного вещества не взаимодействуют между собой, так же как не взаимодействуют частицы идеального газа.
Следует отметить, что закон Вант-Гоффа оказывается несправедливым в тех случаях, когда растворенное вещество при растворении разлагается на ионы (диссоциирует). Это, следовательно, относится ко всем растворам кислот, солей и щелочей (электролитам).
Осмотическое давление играет большую роль в жизни животных и растений. Им в значительной степени определяется распределение воды и растворенных в ней веществ в тканях. Это связано с тем, что оболочки многих органов представляют собой полупроницаемые перегородки.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ
- ВВЕДЕНИЕ
- Глава I. КИНЕТИЧЕСКАЯ ТЕОРИЯ ИДЕАЛЬНЫХ ГАЗОВ
- § 1. Идеальный газ
- § 2. Давление газа
- § 3. Температура
- § 4. Уравнение состояния идеального газа
- § 5. Законы идеального газа
- § 6. Скорости газовых молекул
- § 7. Броуновское движение
- § 8. Барометрическая формула
- § 9. Закон Больцмана
- § 10. Понятие о вероятности
- § 11. Понятие о распределении. Функция распределения
- § 12. Распределение молекул по компонентам скорости
- § 13. Распределение молекул по скоростям
- § 14. Средние скорости молекул
- § 15. Наивероятнейшая скорость молекул
- § 16. Формула Максвелла для относительных скоростей
- § 17. Закон распределения молекул по скоростям и атмосферы планет
- § 18. Экспериментальная проверка закона распределения
- § 19. Измерение параметров состояния
- Глава II. КИНЕТИЧЕСКАЯ ТЕОРИЯ ТЕПЛОТЫ. ЗАКОН СОХРАНЕНИЯ ЭНЕРГИИ
- § 20. Внутренняя энергия идеального газа
- § 21. Количество теплоты
- § 22. Механический эквивалент теплоты
- § 23. Первое начало термодинамики
- § 24. Теплоемкость идеальных газов
- § 25. Теплоемкость одноатомных газов
- § 26. Теплоемкость газов и число степеней свободы молекул
- § 27. Теплоемкость двухатомных и многоатомных газов
- § 28. Изменение состояния при изменении объема газа
- § 29. Работа при изотермическом изменении объема идеального газа
- § 30. Адиабатное изменение объема идеального газа
- § 31. Работа при адиабатном изменении объема газа
- § 32. Политропический процесс
- § 33. Расширение газа в пустоту
- § 34. Измерение количества теплоты и теплоемкости
- Глава III. СТОЛКНОВЕНИЯ МОЛЕКУЛ И ЯВЛЕНИЯ ПЕРЕНОСА
- § 35. Молекулярные движения и явления переноса
- § 36. Среднее число столкновений в единицу времени и средняя длина свободного пробега молекул
- § 37. Эффективное поперечное сечение частицы и вероятность
- § 38. Рассеяние молекулярного пучка в газе
- § 39. Экспериментальное определение длины свободного пробега
- § 40. Диффузия в газах
- § 41. Нестационарная диффузия
- § 42. Стационарная диффузия. Вычисление коэффициента диффузии
- § 43. Коэффициент взаимной диффузии
- § 44. Термическая диффузия
- § 45. Теплопроводность газов
- § 46. Нестационарная теплопроводность
- § 47. Стационарная теплопроводность. Вычисление коэффициента теплопроводности
- § 48. Вязкость газов (внутреннее трение)
- § 49. Измерение коэффициента вязкости (вискозиметрия)
- § 50. Соотношения между коэффициентами переноса
- Глава IV. ФИЗИЧЕСКИЕ ЯВЛЕНИЯ В РАЗРЕЖЕННЫХ ГАЗАХ (ВАКУУМЕ)
- § 51. Теплопередача в газах при малых давлениях
- § 52. Течение газов при малых давлениях (молекулярное течение)
- § 53. Молекулярное течение газа в цилиндрической трубе
- § 54. Молекулярное течение смеси газов. Разделение газовых смесей
- § 55. Диффузия газов в вакууме
- § 56. Разность давлений между различно нагретыми частями газа (тепловая транспирация)
- § 57. Элементы вакуумной техники
- § 58. Измерение малых давлений
- § 59. Вакуумная установка
- Глава V. НЕИДЕАЛЬНЫЕ (РЕАЛЬНЫЕ) ГАЗЫ. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА
- § 60. Отклонения свойств газов от идеальности
- § 61. Сжижение газов (конденсация)
- § 62. Фазовый переход
- § 63. Фазовые диаграммы
- § 64. Методы определения критических параметров
- § 65. Уравнение Ван-дер-Ваальса
- § 66. Изотермы Ван-дер-Ваальса
- § 67. Критическая температура и критическое состояние
- § 68. Экспериментальное определение констант уравнения Ван-дер-Ваальса
- § 69. Сравнение уравнения Ван-дер-Ваальса с данными опыта
- § 70. Приведенное уравнение Ван-дер-Ваальса. Закон соответственных состояний
- § 71. Межмолекулярные силы взаимодействия в реальном газе
- § 72. Теплоемкость неидеальных газов
- Глава VI. ЭЛЕМЕНТЫ ТЕРМОДИНАМИКИ
- § 73. Равновесные состояния
- § 74. Обратимые и необратимые процессы
- § 75. Квазистатические процессы
- § 76. Необратимость и вервятность
- § 77. Взаимные превращения механической и тепловой энергии
- § 78. Первое начало термодинамики
- § 79. Преобразование теплоты в механическую работу
- § 80. Цикл Карно
- § 81. Холодильная машина
- § 82. Доказательство теорем Карно
- § 83. Свободная энергия
- § 84. Энтропия
- § 85. Некоторые термодинамические соотношения
- § 86. Энтропия при обратимых процессах в замкнутой системе
- § 87. Энтропия при необратимых процессах в замкнутой системе, акон возрастания энтропии
- § 88. Второе начало термодинамики и превращение теплоты в работу
- § 89. Физический смысл энтропии. Энтропия и вероятность
- § 90. Энтропия и беспорядок
- § 91. «Демон» Максвелла
- § 92. Термодинамическая шкала температур
- § 93. Третье начало термодинамики
- § 94. Отрицательные температуры
- Глава VII. СВОЙСТВА ЖИДКОСТЕЙ
- § 95. Объемные свойства жидкостей
- § 96. Теплоемкость жидкостей
- § 97. Явления переноса в жидкостях
- § 98. Явления на границе жидкости
- § 99. Условия равновесия на границе двух сред. Краевой угол
- § 100. Силы, возникающие на кривой поверхности жидкости
- § 101. Капиллярные явления
- § 102. Некоторые методы измерения коэффициента поверхностного натяжения
- § 103. Зависимость коэффициента поверхностного натяжения от температуры
- § 104. Испарение и кипение жидкостей
- § 105. Температурная зависимость упругости насыщенных паров
- § 106. Упругость насыщенного пара над кривой поверхностью жидкости
- § 107. Кипение жидкостей
- § 108. Жидкие растворы
- § 109. Осмотическое давление
- Глава VIII. НИЗКИЕ ТЕМПЕРАТУРЫ
- § 110. Сжижение газов
- § 111. Эффект Джоуля-Томсона
- § 112. Адиабатное расширение газа с совершением внешней работы
- § 113. Сжижение газов с использованием эффекта Джоуля — Томсона (метод Линде)
- § 114. Сжижение газов методом адиабатного расширения в детандерах (метод Клода)
- § 115. Некоторые свойства сжиженных газов
- § 116. Сверхнизкие температуры
- § 117. Свойства вещества при низких температурах
- § 118. Жидкий гелий
- Глава IX. ТВЕРДОЕ ТЕЛО
- § 120. Кристаллическая решетка
- § 121. Дефекты в кристаллах
- § 122. Механические свойства твердых тел. Деформации
- § 123. Деформация растяжения и сжатия. Сдвиг
- § 124. Связь между модулями упругости
- § 125. Упругая деформация и тепловое расширение
- § 126. Зависимость деформации от напряжения
- § 127. Механизм пластической деформации
- § 128. Дислокации в кристаллах
- § 129. Переход в твердое состояние
- § 130. Диаграмма состояния. Тройная точка
- § 131. Фазовые переходы первого и второго рода
- § 132. Твердый гелий
- § 133. Растворение и кристаллизация из раствора
- § 134. Сплавы. Диаграммы плавкости
- § 135. Зонная очистка металлов
- § 136. Опытное определение температуры плавления
- § 137. Тепловые свойства твердых тел
- § 138. Измерение теплоемкости
- § 139. Тепловое расширение твердых тел
- § 140. Теплопроводность
- § 141. Диффузия в твердых телах