| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ 84. Энтропия
Вернемся к уже рассмотренному круговому процессу Карно и обратим более пристальное внимание на те изменения состояния, которые претерпело рабочее тело в этом процессе.
Напомним, что из исходного состояния  характеризуемого давлением
характеризуемого давлением  и температурой
и температурой  рабочее тело путем последовательного проведения изотермического и адиабатного расширений перешлов состояние С, когда оно приняло температуру холодильника. Это изменение состояния произошло за счет тепла
рабочее тело путем последовательного проведения изотермического и адиабатного расширений перешлов состояние С, когда оно приняло температуру холодильника. Это изменение состояния произошло за счет тепла  доставленного рабочему телу нагревателем. Обратный переход рабочего тела из состояния С в первоначальное состояние А был осуществлен двумя последовательно проведенными изотермическим и адиабатным сжатиями тела. Выделившееся при этом возвращении в исходное состояние количество тепла равно
доставленного рабочему телу нагревателем. Обратный переход рабочего тела из состояния С в первоначальное состояние А был осуществлен двумя последовательно проведенными изотермическим и адиабатным сжатиями тела. Выделившееся при этом возвращении в исходное состояние количество тепла равно  причем, как мы видели,
причем, как мы видели,  Таким образом, оказывается, что обратимый переход одного и того же тела из состояния
Таким образом, оказывается, что обратимый переход одного и того же тела из состояния  и обратный переход из
и обратный переход из  сопровождаются не одинаковыми количествами поглощенного и выделенного тепла. Очевидно, что это связано с тем, что оба перехода были произведены различными путями: в одном случае (из
сопровождаются не одинаковыми количествами поглощенного и выделенного тепла. Очевидно, что это связано с тем, что оба перехода были произведены различными путями: в одном случае (из  процесс расширения происходил при давлении более высоком, чем процессы сжатия в другом (при переходе из
процесс расширения происходил при давлении более высоком, чем процессы сжатия в другом (при переходе из  Ясно, что если бы мы осуществили переход из
Ясно, что если бы мы осуществили переход из  таким же путем, как и прямой переход, т. е. по кривой
таким же путем, как и прямой переход, т. е. по кривой  а не
а не  (см. рис. 93), то количество тепла, затраченного при прямом переходе, в точности равнялось бы количеству тепла, выделившемуся при обратном переходе.
(см. рис. 93), то количество тепла, затраченного при прямом переходе, в точности равнялось бы количеству тепла, выделившемуся при обратном переходе.
Отсюда следует важный вывод, на который мы уже обращали внимание читателей, что количество тепла, которое должно быть доставлено телу или отнято у него при переходе из одного состояния в другое, не определяется однозначно начальным и конечным состояниями, но существенно зависит от способа осуществления этого перехода. Иначе говоря, количество тепла  не является функцией состояния тела, как, например, внутренняя энергия U (или свободная энергия
не является функцией состояния тела, как, например, внутренняя энергия U (или свободная энергия  Это, впрочем, следует из уравнения первого начала термодинамики
Это, впрочем, следует из уравнения первого начала термодинамики

ибо работа  совершенная телом (или над телом), зависит от того, каким путем она совершается, тогда как изменение внутренней энергии
совершенная телом (или над телом), зависит от того, каким путем она совершается, тогда как изменение внутренней энергии  не зависит от того, каким именно образом произошло изменение состояния.
не зависит от того, каким именно образом произошло изменение состояния.
Но если сами количества тепла —  доставленное телу от нагревателя при температуре
доставленное телу от нагревателя при температуре  переданное им холодильнику при температуре
переданное им холодильнику при температуре  не равны между собой, то, как мы видели (см. формулу (80.11)), отношения этих теплот к тем температурам,
не равны между собой, то, как мы видели (см. формулу (80.11)), отношения этих теплот к тем температурам,
при которых они были поглощены или отданы, численно равны междуобой (но имеют противоположные знаки):

Отношение иногда называют, - по Лоренцу, приведенной теплотой, так что последнее уравнение говорит о равенстве приведенных теплот, полученных и отданных рабочим телом при круговом процессе.
Эта особенность теплоты позволяет ввести особую термодинамическую величину — энтропию, имеющую фундаментальное значение в физике. Важность этой величины определяется тем, что, как сейчас будет показано, она является функцией состояния, и той ролью, которую она играет во всех процессах в природе, в частности в процессе преобразования теплоты в работу.
Любое изменение состояния тела или системы тел в общем случае можно представить как результат бесконечно большого числа бесконечно малых изменений. При каждом таком бесконечно малом изменении состояния система либо поглощает, либо выделяет бесконечно малое количество тепла  (если процесс не адиабатный). Условимся считать
(если процесс не адиабатный). Условимся считать  положительным, когда система поглощает тепло, и отрицательным, когда она его выделяет.
положительным, когда система поглощает тепло, и отрицательным, когда она его выделяет.
Можно показать, что если система в результате каких-либо изменений состояния обратимым путем переходит из состояния А в состояние В, то сумма приведенных количеств теплоты, т. е. величина

не зависит от пути, по которому происходит переход из  Для этого достаточно показать, что при круговом процессе, когда начальное и конечное состояния совпадают, этот интеграл равен нулю:
Для этого достаточно показать, что при круговом процессе, когда начальное и конечное состояния совпадают, этот интеграл равен нулю:

Докажем сначала, что при любом круговом процессе интеграл

не может быть положительной величиной.
Пусть некоторое тело  в результате каких-либо изменений состояния возвращается в исходное состояние, т. е. совершает круговой процесс. Во время прбцесса тело отдавало и поглощало теплоту. Представим себе, что тепло, выделяемое телом
в результате каких-либо изменений состояния возвращается в исходное состояние, т. е. совершает круговой процесс. Во время прбцесса тело отдавало и поглощало теплоту. Представим себе, что тепло, выделяемое телом  передается некоторому тепловому резервуару (телу большой теплоемкости), температура которого равна
передается некоторому тепловому резервуару (телу большой теплоемкости), температура которого равна  Эту передачу можно осуществить обратимым путем, например с помощью промежуточного тела, совершающего круговой процесс Карно, так что тело
Эту передачу можно осуществить обратимым путем, например с помощью промежуточного тела, совершающего круговой процесс Карно, так что тело  будет служить для промежуточного тела нагревателем, а резервуар — холодильником.
будет служить для промежуточного тела нагревателем, а резервуар — холодильником.
Как уже было показано при рассмотрении цикла Карно, количество тепла  отнятое от тела
отнятое от тела  при температуре
при температуре  и количество тепла переданное резервуару при температуре
и количество тепла переданное резервуару при температуре  не равны
не равны

друг другу, но равны отношения и  Отсюда следует:
Отсюда следует:

Если  резервуар выполняет роль холодильника, а тело
резервуар выполняет роль холодильника, а тело  нагревателя. Если, наоборот,
нагревателя. Если, наоборот,  резервуар и тело
резервуар и тело  меняются ролями.
меняются ролями.
После того как телом  будет завершен круговой процесс, общее количество теплоты, потерянное телом, должно быть равно, как это видно из (84.2), или, поскольку теплоемкость резервуара велика и его температура остается поэтому постоянной, эта величина равна:
будет завершен круговой процесс, общее количество теплоты, потерянное телом, должно быть равно, как это видно из (84.2), или, поскольку теплоемкость резервуара велика и его температура остается поэтому постоянной, эта величина равна:

Процесс, совершенный телом, — круговой. Поэтому оно в конце концов не испытало никаких изменений. Промежуточное тело тоже совершило круговой процесс. Значит, и в нем не произошло никаких изменений.
Если бы интеграл (84.1) оказался положительным, то это означало бы, что потерянное телом количество тепла, равное целиком превратилось в работу, тогда как ни тело  ни промежуточное тело не изменили своего состояния. Но это по принципу Томсона невозможно. Значит, предположение о том, что несостоятельно.
ни промежуточное тело не изменили своего состояния. Но это по принципу Томсона невозможно. Значит, предположение о том, что несостоятельно.
Легко видеть, что интеграл (84.1) не может быть и отрицательным. В самом деле, если все изменения состояния произвести в обратном порядке, то каждое количество теплоты изменит свой знак,
и если при прямом процессе  , то при обратном процессе этот интеграл станет положительным, что, как мы только что видели, невозможно. Значит, этот интеграл не может быть и отрицательным. Но если он не может быть ни положительным, ни отрицательным, то это значит, что для обратимых круговых процессов, которые мы здесь рассматриваем,
, то при обратном процессе этот интеграл станет положительным, что, как мы только что видели, невозможно. Значит, этот интеграл не может быть и отрицательным. Но если он не может быть ни положительным, ни отрицательным, то это значит, что для обратимых круговых процессов, которые мы здесь рассматриваем,

(Частным случаем этого уравнения является уравнение (82.3).)
Это, в свою очередь, означает, что при всяком обратимом не круговом процессе значение  не зависит от пути, по которому происходит процесс.
не зависит от пути, по которому происходит процесс.
Это дает нам право утверждать, что существует некоторая величина, — обозначим, ее буквой  являющаяся функцией состояния системы, изменение которой
являющаяся функцией состояния системы, изменение которой  при обратимом переходе системы из состояния А в состояние В равно:
при обратимом переходе системы из состояния А в состояние В равно:

Равенство (84.4) позволяет определить не абсолютное значение функции, соответствующее данному состоянию, а лишь ее изменение при переходе от одного состояния к другому. Но, как всегда в таких случаях делается, можно выбрать некоторое состояние, которому приписывается значение  равное нулю, и сравнивать с ним все прочие состояния. Поэтому в дальнейшем будем считать, что именно функция
равное нулю, и сравнивать с ним все прочие состояния. Поэтому в дальнейшем будем считать, что именно функция  равна интегралу (84.1):
равна интегралу (84.1):

Определенная таким образом величина  и называется энтропией.
и называется энтропией.
На практике всегда требуется знать не саму величину  а только ее изменение при изменении состояния системы. Поэтому безразлично, какому именно состоянию приписать нулевую энтропию. Принято (и на это есть достаточные основания) считать, что энтропия равна нулю при абсолютном нуле температуры.
а только ее изменение при изменении состояния системы. Поэтому безразлично, какому именно состоянию приписать нулевую энтропию. Принято (и на это есть достаточные основания) считать, что энтропия равна нулю при абсолютном нуле температуры.
Значит, для нахожденйя энтропии системы в данном состоянии надо перевести систему (это можно сделать мысленно) из этого состояния в нулевое состояние каким-либо обратимым путем (безразлично, каким именно) и найти значение  вдоль этого пути. Разумеется, сама энтропия системы совершенно не зависит от того, будет ли в действительности совершен этот обратимый процесс или нет.
вдоль этого пути. Разумеется, сама энтропия системы совершенно не зависит от того, будет ли в действительности совершен этот обратимый процесс или нет.
То же касается изменения энтропии. Согласно (84.4), чтобы определить разность значений энтропии системы в двух ее состояниях (равновесных)  нужно перевести систему каким-нибудь обратимым процессом из состояния А в состояние В и вычислить значение
нужно перевести систему каким-нибудь обратимым процессом из состояния А в состояние В и вычислить значение  для такого процесса.
для такого процесса.
Изменение энтропии системы, которой сообщено бесконечно малое количесгво тепла  определяется, очевидно, соотношением:
определяется, очевидно, соотношением:

В математическом отношении это равенство интересно тем, что величина  которая не является полным дифференциалом, так как
которая не является полным дифференциалом, так как  не является функцией состояния (см. примечание на стр. 253), становится, однако, полным дифференциалом после деления на
не является функцией состояния (см. примечание на стр. 253), становится, однако, полным дифференциалом после деления на  Величина 1/7 является, таким образом, интегрирующим Множителем для
Величина 1/7 является, таким образом, интегрирующим Множителем для  Формально математически температуру можно даже определить как величину, обратное значение которой является интегрирующим множителем для
Формально математически температуру можно даже определить как величину, обратное значение которой является интегрирующим множителем для 
Воспользовавшись уравнением (84.6) и вспомнив, что  (первое начало термодинамики), получаем:
(первое начало термодинамики), получаем:

Это уравнение носит название термодинамического тождества. Его часто называют вторым началом термодинамики для обратимых процессов.
Собственно, второе начало термодинамики для обратимых процессов заключается в том, что система может быть охарактеризована функцией состояния — энтропией, определяемой уравнениями (84.6) или (84.7). Глубокий физический смысл этой функции будет выяснен ниже.
Если круговой процесс, претерпеваемый системой, необратим, то

Это неравенство называется неравенством Клаузиуса. Для частного случая необратимого цикла Карно мы уже убедились [см, (82.2)] в том, что сумма приведенных теплот

Неравенство (84.8) является обобщением этого для любой системы. За строгим доказательством этого неравенства мы отсылаем читателя к специальным курсам термодинамики.
В такой же мере уравнение (84.3) является обобщением (82.3).
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ВВЕДЕНИЕ
- Глава I. КИНЕТИЧЕСКАЯ ТЕОРИЯ ИДЕАЛЬНЫХ ГАЗОВ
- § 1. Идеальный газ
- § 2. Давление газа
- § 3. Температура
- § 4. Уравнение состояния идеального газа
- § 5. Законы идеального газа
- § 6. Скорости газовых молекул
- § 7. Броуновское движение
- § 8. Барометрическая формула
- § 9. Закон Больцмана
- § 10. Понятие о вероятности
- § 11. Понятие о распределении. Функция распределения
- § 12. Распределение молекул по компонентам скорости
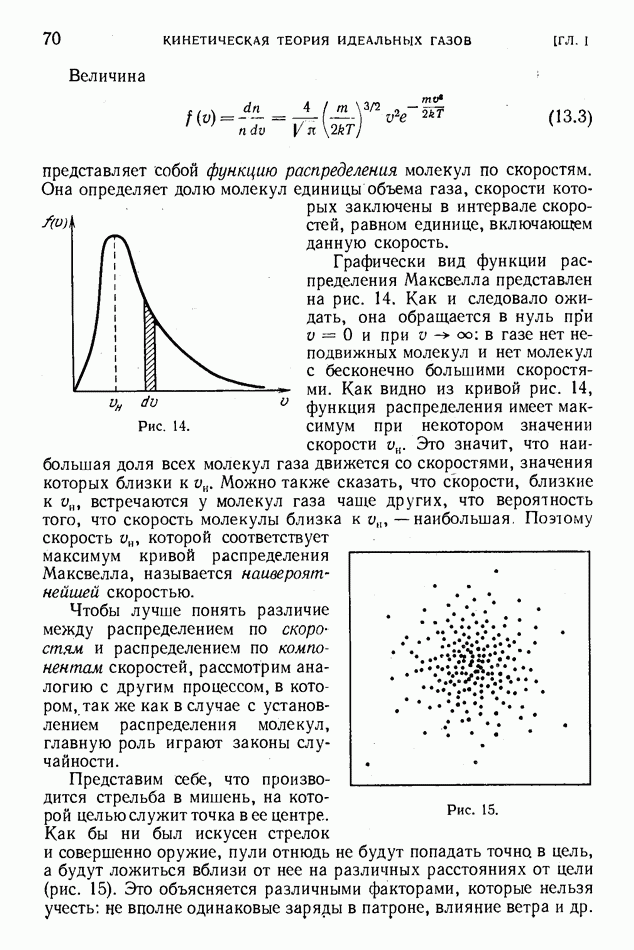
- § 13. Распределение молекул по скоростям
- § 14. Средние скорости молекул
- § 15. Наивероятнейшая скорость молекул
- § 16. Формула Максвелла для относительных скоростей
- § 17. Закон распределения молекул по скоростям и атмосферы планет
- § 18. Экспериментальная проверка закона распределения
- § 19. Измерение параметров состояния
- Глава II. КИНЕТИЧЕСКАЯ ТЕОРИЯ ТЕПЛОТЫ. ЗАКОН СОХРАНЕНИЯ ЭНЕРГИИ
- § 20. Внутренняя энергия идеального газа
- § 21. Количество теплоты
- § 22. Механический эквивалент теплоты
- § 23. Первое начало термодинамики
- § 24. Теплоемкость идеальных газов
- § 25. Теплоемкость одноатомных газов
- § 26. Теплоемкость газов и число степеней свободы молекул
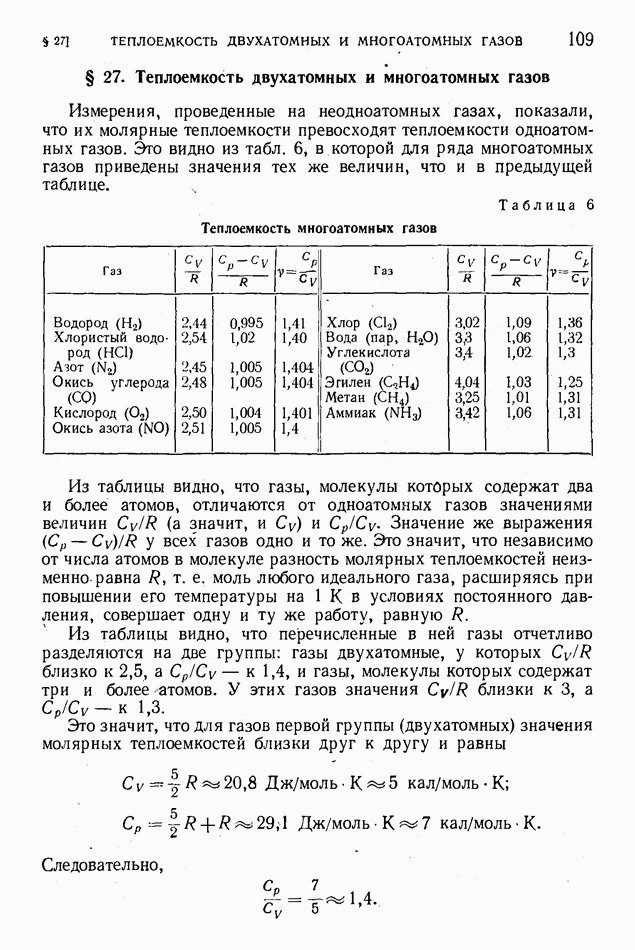
- § 27. Теплоемкость двухатомных и многоатомных газов
- § 28. Изменение состояния при изменении объема газа
- § 29. Работа при изотермическом изменении объема идеального газа
- § 30. Адиабатное изменение объема идеального газа
- § 31. Работа при адиабатном изменении объема газа
- § 32. Политропический процесс
- § 33. Расширение газа в пустоту
- § 34. Измерение количества теплоты и теплоемкости
- Глава III. СТОЛКНОВЕНИЯ МОЛЕКУЛ И ЯВЛЕНИЯ ПЕРЕНОСА
- § 35. Молекулярные движения и явления переноса
- § 36. Среднее число столкновений в единицу времени и средняя длина свободного пробега молекул
- § 37. Эффективное поперечное сечение частицы и вероятность
- § 38. Рассеяние молекулярного пучка в газе
- § 39. Экспериментальное определение длины свободного пробега
- § 40. Диффузия в газах
- § 41. Нестационарная диффузия
- § 42. Стационарная диффузия. Вычисление коэффициента диффузии
- § 43. Коэффициент взаимной диффузии
- § 44. Термическая диффузия
- § 45. Теплопроводность газов
- § 46. Нестационарная теплопроводность
- § 47. Стационарная теплопроводность. Вычисление коэффициента теплопроводности
- § 48. Вязкость газов (внутреннее трение)
- § 49. Измерение коэффициента вязкости (вискозиметрия)
- § 50. Соотношения между коэффициентами переноса
- Глава IV. ФИЗИЧЕСКИЕ ЯВЛЕНИЯ В РАЗРЕЖЕННЫХ ГАЗАХ (ВАКУУМЕ)
- § 51. Теплопередача в газах при малых давлениях
- § 52. Течение газов при малых давлениях (молекулярное течение)
- § 53. Молекулярное течение газа в цилиндрической трубе
- § 54. Молекулярное течение смеси газов. Разделение газовых смесей
- § 55. Диффузия газов в вакууме
- § 56. Разность давлений между различно нагретыми частями газа (тепловая транспирация)
- § 57. Элементы вакуумной техники
- § 58. Измерение малых давлений
- § 59. Вакуумная установка
- Глава V. НЕИДЕАЛЬНЫЕ (РЕАЛЬНЫЕ) ГАЗЫ. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА
- § 60. Отклонения свойств газов от идеальности
- § 61. Сжижение газов (конденсация)
- § 62. Фазовый переход
- § 63. Фазовые диаграммы
- § 64. Методы определения критических параметров
- § 65. Уравнение Ван-дер-Ваальса
- § 66. Изотермы Ван-дер-Ваальса
- § 67. Критическая температура и критическое состояние
- § 68. Экспериментальное определение констант уравнения Ван-дер-Ваальса
- § 69. Сравнение уравнения Ван-дер-Ваальса с данными опыта
- § 70. Приведенное уравнение Ван-дер-Ваальса. Закон соответственных состояний
- § 71. Межмолекулярные силы взаимодействия в реальном газе
- § 72. Теплоемкость неидеальных газов
- Глава VI. ЭЛЕМЕНТЫ ТЕРМОДИНАМИКИ
- § 73. Равновесные состояния
- § 74. Обратимые и необратимые процессы
- § 75. Квазистатические процессы
- § 76. Необратимость и вервятность
- § 77. Взаимные превращения механической и тепловой энергии
- § 78. Первое начало термодинамики
- § 79. Преобразование теплоты в механическую работу
- § 80. Цикл Карно
- § 81. Холодильная машина
- § 82. Доказательство теорем Карно
- § 83. Свободная энергия
- § 84. Энтропия
- § 85. Некоторые термодинамические соотношения
- § 86. Энтропия при обратимых процессах в замкнутой системе
- § 87. Энтропия при необратимых процессах в замкнутой системе, акон возрастания энтропии
- § 88. Второе начало термодинамики и превращение теплоты в работу
- § 89. Физический смысл энтропии. Энтропия и вероятность
- § 90. Энтропия и беспорядок
- § 91. «Демон» Максвелла
- § 92. Термодинамическая шкала температур
- § 93. Третье начало термодинамики
- § 94. Отрицательные температуры
- Глава VII. СВОЙСТВА ЖИДКОСТЕЙ
- § 95. Объемные свойства жидкостей
- § 96. Теплоемкость жидкостей
- § 97. Явления переноса в жидкостях
- § 98. Явления на границе жидкости
- § 99. Условия равновесия на границе двух сред. Краевой угол
- § 100. Силы, возникающие на кривой поверхности жидкости
- § 101. Капиллярные явления
- § 102. Некоторые методы измерения коэффициента поверхностного натяжения
- § 103. Зависимость коэффициента поверхностного натяжения от температуры
- § 104. Испарение и кипение жидкостей
- § 105. Температурная зависимость упругости насыщенных паров
- § 106. Упругость насыщенного пара над кривой поверхностью жидкости
- § 107. Кипение жидкостей
- § 108. Жидкие растворы
- § 109. Осмотическое давление
- Глава VIII. НИЗКИЕ ТЕМПЕРАТУРЫ
- § 110. Сжижение газов
- § 111. Эффект Джоуля-Томсона
- § 112. Адиабатное расширение газа с совершением внешней работы
- § 113. Сжижение газов с использованием эффекта Джоуля — Томсона (метод Линде)
- § 114. Сжижение газов методом адиабатного расширения в детандерах (метод Клода)
- § 115. Некоторые свойства сжиженных газов
- § 116. Сверхнизкие температуры
- § 117. Свойства вещества при низких температурах
- § 118. Жидкий гелий
- Глава IX. ТВЕРДОЕ ТЕЛО
- § 120. Кристаллическая решетка
- § 121. Дефекты в кристаллах
- § 122. Механические свойства твердых тел. Деформации
- § 123. Деформация растяжения и сжатия. Сдвиг
- § 124. Связь между модулями упругости
- § 125. Упругая деформация и тепловое расширение
- § 126. Зависимость деформации от напряжения
- § 127. Механизм пластической деформации
- § 128. Дислокации в кристаллах
- § 129. Переход в твердое состояние
- § 130. Диаграмма состояния. Тройная точка
- § 131. Фазовые переходы первого и второго рода
- § 132. Твердый гелий
- § 133. Растворение и кристаллизация из раствора
- § 134. Сплавы. Диаграммы плавкости
- § 135. Зонная очистка металлов
- § 136. Опытное определение температуры плавления
- § 137. Тепловые свойства твердых тел
- § 138. Измерение теплоемкости
- § 139. Тепловое расширение твердых тел
- § 140. Теплопроводность
- § 141. Диффузия в твердых телах