| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ 94. Отрицательные температуры
Если исходить из того определения температуры, которое было дано в начале этой книги, т. е. что температура пропорциональна средней кинетической энергии частиц, то название этого параграфа как будто бы лишено а/ысла: ведь кинетическая энергия не может быть отрицательной! И для тех атомных систем, у которых энергия содержит в себе только кинетическую энергию движения частиц, отрицательная температура в самом деле не имеет физического смысла.
Но вспомним, что помимо молекулярно-кинетического определения температуры мы в гл. I отметили также роль температуры как величины, определяющей распределение частиц по энергиям (см. стр. 55). Если воспользоваться этим более общим понятием температуры, то мы придем к возможности существования (по крайней мере принципиальной) и отрицательных температур.
Нетрудно видеть, что формула Больцмана (9.2)

формально «позволяет» температуре принимать не только положительные, но и отрицательные значения.
В самом деле, в этой формуле  это доля частиц, находящихся в состоянии с энергией
это доля частиц, находящихся в состоянии с энергией  причем
причем  это число частиц в состоянии с некоторой начальной энергией, от которой ведется отсчет энергии
это число частиц в состоянии с некоторой начальной энергией, от которой ведется отсчет энергии  Из формулы видно, что чем выше
Из формулы видно, что чем выше  тем меньше доля частиц
тем меньше доля частиц  обладающих этой энергией. Так, например,
обладающих этой энергией. Так, например,  при
при  раз меньше, чем
раз меньше, чем  основание натуральных логарифмов). А энергией
основание натуральных логарифмов). А энергией  обладает уже значительно меньшая доля частиц: в этом случае
обладает уже значительно меньшая доля частиц: в этом случае  раз меньше
раз меньше  Ясно, что в равновесном состоянии, к которому, как мы знаем, и относится закон Больцмана,
Ясно, что в равновесном состоянии, к которому, как мы знаем, и относится закон Больцмана,  всегда меньше, чем
всегда меньше, чем 
Логарифмируя равенство (9.2), получим:  откуда
откуда

Из этого выражения для  видно, что если
видно, что если  то
то 
Если бы, однако, оказалось, что существует такая атомная система, в которой  может быть и больше, чем
может быть и больше, чем  то это означало бы, что температура может принимать и отрицательные значения, так как
то это означало бы, что температура может принимать и отрицательные значения, так как  при
при  становится отрицательной.
становится отрицательной.
Нам будет легче понять, при каких обстоятельствах это возможно, если мы рассмотрим не классическую систему (в которой отрицательная температура не может быть реализована), а квантовую, и воспользуемся, кроме того концепцией энтропии, которая,
как мы только что видели, является величиной, определяющей степень беспорядка в системе.
Пусть система представлена схемой ее энергетических уровней (см., например, рис. 1, стр. 17). При абсолютном нуле температуры все частицы нашей системы находятся на своих низших энергетических уровнях, а все остальные уровни пустуют. Система в таких условиях максимально упорядочена и ее энтропия равна нулю (нулю равна и ее теплоемкость).
Если теперь повышать температуру системы путем подвода к ней энергии, то частицы будут переходить и на более высокие уровни энергии, которые, таким образом, тоже оказываются частично заселенными, причем чем выше температура, тем больше «заселенность» более высоких энергетических уровней. Распределение частиц по энергетическим уровням определяется формулой Больцмана. Значит, оно будет таким, что на высших уровнях будет меньше частиц чем на низших. «Расселение» частиц по многим уровням увеличивает, конечно, беспорядок в системе и энтропия ее возрастает вместе с ростом температуры. Наибольший беспорядок, а значит, и максимум энтропии был бы достигнут при таком распределении частиц по энергиям, при котором они равномерно распределены по всем энергетическим уровням. Такое распределение означало бы, что в формуле  значит,
значит,  Следовательно, равномерное распределение частиц по энергиям соответствует бесконечно высокой температуре и максимальной энтропии.
Следовательно, равномерное распределение частиц по энергиям соответствует бесконечно высокой температуре и максимальной энтропии.
Однако в квантовой системе, о которой здесь идет речь, такое распределение невозможно, потому что число уровней бесконечно большое, а число частиц — конечное. Поэтому энтропия в такой системе не проходит через максимум, а монотонно растет с температурой. При бесконечно высокой температуре энтропия тоже будет бесконечно высокой.
Представим себе теперь такую систему (квантовую), у которой существует верхний предел ее внутренней энергии, а число энергетических уровней конечное. Это, разумеется, возможно только в такой системе, в которой энергия не включает в себя кинетическую энергию движения частиц.
В такой системе при абсолютном нуле температуры частицы тоже будут занимать только наинизшие энергетические уровни, а энтропия при этом будет равна нулю. С ростом температуры частицы «расселяются» и на более высоких уровнях, вызывая соответственный рост энтропии. На рис. 99, а представлена система с двумя энергетическими уровнями. Но, так как число энергетических уровней системы, как и число частиц в ней, теперь конечное, то в конце концов может быть достигнуто такое состояние, при котором частицы равномерно распределяются по энергетическим уровням. Как мы только что видели, этому состоянию соответствуют бесконечно высокая температура и максимальная энтропия.
Энергия системы при этом тоже будет некоторой максимальной, но не бесконечно большой, так что наше старое определение температуры, как средней энергии частиц, становится неприменимым.
Если теперь каким-нибудь образом сообщить системе, уже находящейся при бесконечно высокой температуре, дополнительную энергию, то частицы будут продолжать переходить на более высокий энергетический уровень, а это приведет к тому, что «заселенность» этого высокого уровня энергии станет больше, чем у нижнего (рис. 99, б). Ясно, что такое преимущественное скопление частиц на высоких уровнях означает уже некоторое упорядочение по сравнению с тем полным беспорядком, который существовал при  т. е. при равномерном распределении частиц по энергиям. Энтропия, достигшая максимума при
т. е. при равномерном распределении частиц по энергиям. Энтропия, достигшая максимума при  начинает, следовательно, уменьшаться при дальнейшем подводе энергии. Но если с ростом энергии энтропия не растет, а падает, то это значит, что температура не положительная, а отрицательная.
начинает, следовательно, уменьшаться при дальнейшем подводе энергии. Но если с ростом энергии энтропия не растет, а падает, то это значит, что температура не положительная, а отрицательная.

Рис. 99.
Чем больше энергии будет подводиться к системе, тем больше частиц окажется на самых высоких энергетических уровнях. В пределе можно себе представить состояние, при котором все частицы соберутся на самых высоких уровнях. Такое состояние, очевидно, тоже является вполне упорядоченным. Оно ничем не «хуже» того состояния, когда все частицы занимают наинизшие уровни: и в том и в другом случаях в системе господствует полный порядок, и энтропия равна нулю. Мы можем поэтому обозначить температуру, при которой устанавливается это второе вполне упорядоченное состояние, через —0, в отличие от «обычного» абсолютного нуля  Разница между этими двумя «нулями» заключается в том, что к первому из них мы приходим со стороны отрицательных, а ко второму — со стороны положительных температур.
Разница между этими двумя «нулями» заключается в том, что к первому из них мы приходим со стороны отрицательных, а ко второму — со стороны положительных температур.

Рис. 100.
Таким образом, мыслимые температуры системы не ограничиваются интервалом от абсолютного нуля до бесконечности, а простираются от  через
через  до
до  , причем
, причем  совпадают друг с другом. На рис. 100 представлена кривая зависимости энтропии от энергии системы. Часть кривой слева от максимума соответствует положительным температурам, справа от него — отрицательным. В точке максимума значение температуры равно
совпадают друг с другом. На рис. 100 представлена кривая зависимости энтропии от энергии системы. Часть кривой слева от максимума соответствует положительным температурам, справа от него — отрицательным. В точке максимума значение температуры равно 
С точки зрения упорядоченности, а значит, и энтропии возможны, следовательно, такие три крайние состояния:
1. Полное упорядочение — частицы сконцентрированы на наинизших уровнях энергии. Это состояние соответствует «обычному» абсолютному нулю 
2. Полный беспорядок — частицы равномерно распределены по всем энергетическим уровням. Этому состоянию соответствует температура 
3. Снова полное упорядочение — частицы занимают только самые высшие энергетические уровни. Температуре, соответствующей этому состоянию, приписывается значение —0.
Мы имеем здесь дело, следовательно, с парадоксальной ситуацией: чтобы прийти к отрицательным температурам, нам пришлось не охлаждать систему ниже абсолютного нуля, что невозможно, а, наоборот, увеличивать ее энергию; отрицательная температура  оказывается выше бесконечно высокой температуры!
оказывается выше бесконечно высокой температуры!
Существует очень важное различие между двумя вполне упорядоченными состояниями, о которых мы только что упоминали, — состояниями с температурами  .
.
Состояние «обычного» абсолютного нуля, если бы оно могло быть создано в системе, сохранялось бы в ней сколь угодно долго при условии, что она надежно изолирована от окружающей среды, изолирована в том смысле, что от этой среды к системе не подводится энергия. Это состояние является состоянием устойчивого равновесия, из которого система сама по себе, без вмешательства извне, не может выйти. Это связано с тем, что энергия системы в этом состоянии имеет минимальное значение.
С другой стороны, состояние отрицательного абсолютного нуля является состоянием крайне неравновесным, так как. энергия системы максимальная. Если бы можно было довести систему до этого состояния, а затем предоставить ее самой себе, то она бы немедленно вышла из этого неравновесного, неустойчивого состояния. Его можно было бы сохранить только при непрерывном подводе энергии к системе. Без этого частицы, находящиеся на высших энергетических уровнях, непременно «упадут» на более низкие уровни.
Общим свойством обоих «нулей» является их недостижимость: для их достижения требуется затрата бесконечно большой энергии.
Впрочем, неустойчивым, неравновесным является не только состояние, соответствующее температуре —0, но и все состояния с отрицательными температурами. Всем им соответствуют значения  а для равновесия необходимо обратное соотношение
а для равновесия необходимо обратное соотношение 
Мы уже отмечали, что отрицательные температуры — это более высокие температуры, чем положительные. Поэтому, если привести
тело, нагретое (нельзя сказать: охлажденное) до отрицательных температур, в соприкосновение с телом, температура которого положительна, то энергия будет переходить от первого ко второму, а не наоборот, а это и значит, что его температура выше, хотя она и отрицательна. При контакте двух тел с отрицательной температурой энергия будет переходить от тела с меньшей по абсолютному значению температурой к телу с большим численным значением температуры.
Находясь в крайне неравновесном состоянии, тело, нагретое до отрицательной температуры, очень охотно отдает энергию. Поэтому для того, чтобы такое состояние могло быть создано, система должна быть надежно изолирована от других тел (во всяком случае от систем, не похожих на нее, т. е. не имеющих конечного числа энергетических уровней).
Впрочем, - состояние с отрицательной температурой в такой степени неравновесно, что даже если система, находящаяся в этом состоянии, изолирована и передавать энергию ей некому, она все же может отдавать энергию в виде излучения, пока не перейдет в состояние (равновесное) с положительной температурой.
Остается еще добавить, что атомные системы с ограниченным набором энергетических уровней, в которых, как мы видели, можно осуществить состояние с отрицательной температурой, — это не только мыслимое теоретическое построение. Такие системы реально существуют и в них в самом деле может быть получена отрицательная температура. Излучение, возникающее при переходе из состояния с отрицательной в состояние с обычной температурой, практически используется в специальных приборах: молекулярных генераторах и усилителях — мазерах и лазерах. Но мы здесь не можем останавливаться на этом вопросе более подробно.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ВВЕДЕНИЕ
- Глава I. КИНЕТИЧЕСКАЯ ТЕОРИЯ ИДЕАЛЬНЫХ ГАЗОВ
- § 1. Идеальный газ
- § 2. Давление газа
- § 3. Температура
- § 4. Уравнение состояния идеального газа
- § 5. Законы идеального газа
- § 6. Скорости газовых молекул
- § 7. Броуновское движение
- § 8. Барометрическая формула
- § 9. Закон Больцмана
- § 10. Понятие о вероятности
- § 11. Понятие о распределении. Функция распределения
- § 12. Распределение молекул по компонентам скорости
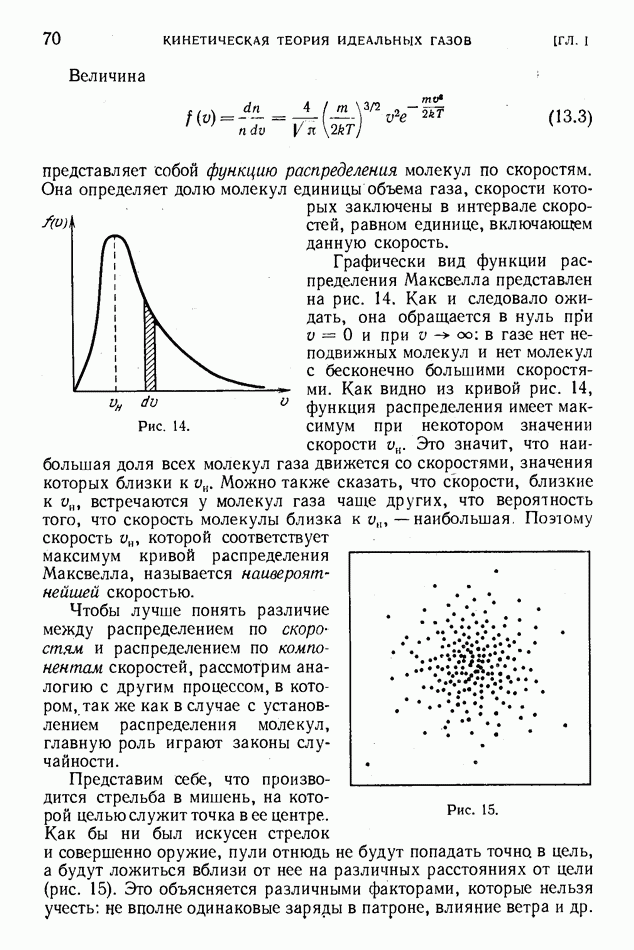
- § 13. Распределение молекул по скоростям
- § 14. Средние скорости молекул
- § 15. Наивероятнейшая скорость молекул
- § 16. Формула Максвелла для относительных скоростей
- § 17. Закон распределения молекул по скоростям и атмосферы планет
- § 18. Экспериментальная проверка закона распределения
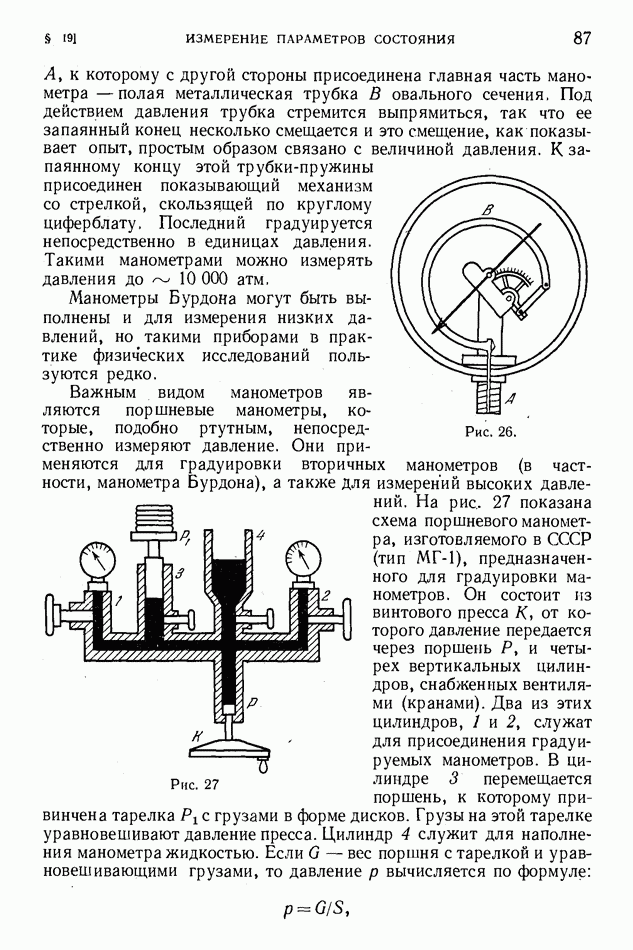
- § 19. Измерение параметров состояния
- Глава II. КИНЕТИЧЕСКАЯ ТЕОРИЯ ТЕПЛОТЫ. ЗАКОН СОХРАНЕНИЯ ЭНЕРГИИ
- § 20. Внутренняя энергия идеального газа
- § 21. Количество теплоты
- § 22. Механический эквивалент теплоты
- § 23. Первое начало термодинамики
- § 24. Теплоемкость идеальных газов
- § 25. Теплоемкость одноатомных газов
- § 26. Теплоемкость газов и число степеней свободы молекул
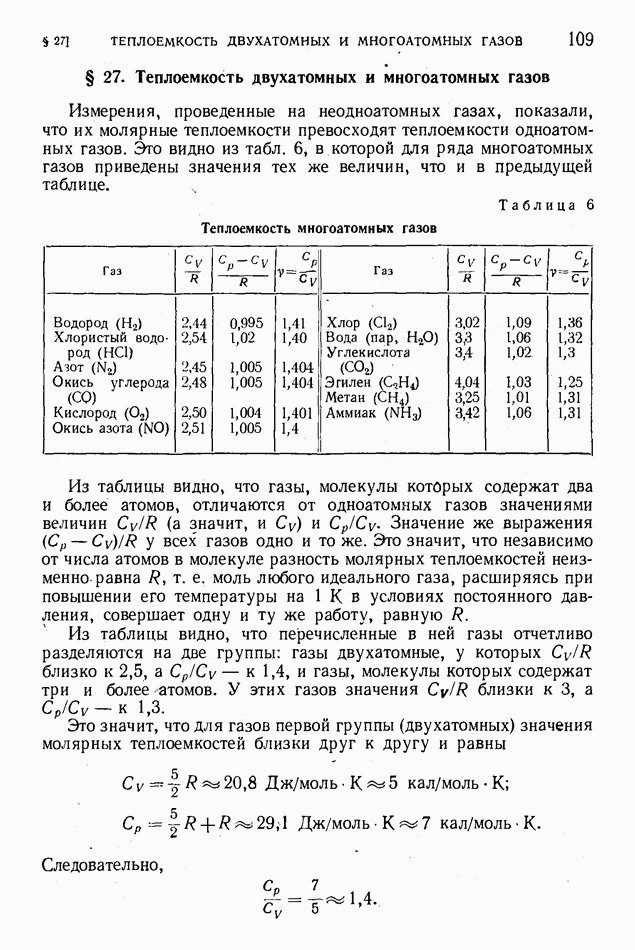
- § 27. Теплоемкость двухатомных и многоатомных газов
- § 28. Изменение состояния при изменении объема газа
- § 29. Работа при изотермическом изменении объема идеального газа
- § 30. Адиабатное изменение объема идеального газа
- § 31. Работа при адиабатном изменении объема газа
- § 32. Политропический процесс
- § 33. Расширение газа в пустоту
- § 34. Измерение количества теплоты и теплоемкости
- Глава III. СТОЛКНОВЕНИЯ МОЛЕКУЛ И ЯВЛЕНИЯ ПЕРЕНОСА
- § 35. Молекулярные движения и явления переноса
- § 36. Среднее число столкновений в единицу времени и средняя длина свободного пробега молекул
- § 37. Эффективное поперечное сечение частицы и вероятность
- § 38. Рассеяние молекулярного пучка в газе
- § 39. Экспериментальное определение длины свободного пробега
- § 40. Диффузия в газах
- § 41. Нестационарная диффузия
- § 42. Стационарная диффузия. Вычисление коэффициента диффузии
- § 43. Коэффициент взаимной диффузии
- § 44. Термическая диффузия
- § 45. Теплопроводность газов
- § 46. Нестационарная теплопроводность
- § 47. Стационарная теплопроводность. Вычисление коэффициента теплопроводности
- § 48. Вязкость газов (внутреннее трение)
- § 49. Измерение коэффициента вязкости (вискозиметрия)
- § 50. Соотношения между коэффициентами переноса
- Глава IV. ФИЗИЧЕСКИЕ ЯВЛЕНИЯ В РАЗРЕЖЕННЫХ ГАЗАХ (ВАКУУМЕ)
- § 51. Теплопередача в газах при малых давлениях
- § 52. Течение газов при малых давлениях (молекулярное течение)
- § 53. Молекулярное течение газа в цилиндрической трубе
- § 54. Молекулярное течение смеси газов. Разделение газовых смесей
- § 55. Диффузия газов в вакууме
- § 56. Разность давлений между различно нагретыми частями газа (тепловая транспирация)
- § 57. Элементы вакуумной техники
- § 58. Измерение малых давлений
- § 59. Вакуумная установка
- Глава V. НЕИДЕАЛЬНЫЕ (РЕАЛЬНЫЕ) ГАЗЫ. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА
- § 60. Отклонения свойств газов от идеальности
- § 61. Сжижение газов (конденсация)
- § 62. Фазовый переход
- § 63. Фазовые диаграммы
- § 64. Методы определения критических параметров
- § 65. Уравнение Ван-дер-Ваальса
- § 66. Изотермы Ван-дер-Ваальса
- § 67. Критическая температура и критическое состояние
- § 68. Экспериментальное определение констант уравнения Ван-дер-Ваальса
- § 69. Сравнение уравнения Ван-дер-Ваальса с данными опыта
- § 70. Приведенное уравнение Ван-дер-Ваальса. Закон соответственных состояний
- § 71. Межмолекулярные силы взаимодействия в реальном газе
- § 72. Теплоемкость неидеальных газов
- Глава VI. ЭЛЕМЕНТЫ ТЕРМОДИНАМИКИ
- § 73. Равновесные состояния
- § 74. Обратимые и необратимые процессы
- § 75. Квазистатические процессы
- § 76. Необратимость и вервятность
- § 77. Взаимные превращения механической и тепловой энергии
- § 78. Первое начало термодинамики
- § 79. Преобразование теплоты в механическую работу
- § 80. Цикл Карно
- § 81. Холодильная машина
- § 82. Доказательство теорем Карно
- § 83. Свободная энергия
- § 84. Энтропия
- § 85. Некоторые термодинамические соотношения
- § 86. Энтропия при обратимых процессах в замкнутой системе
- § 87. Энтропия при необратимых процессах в замкнутой системе, акон возрастания энтропии
- § 88. Второе начало термодинамики и превращение теплоты в работу
- § 89. Физический смысл энтропии. Энтропия и вероятность
- § 90. Энтропия и беспорядок
- § 91. «Демон» Максвелла
- § 92. Термодинамическая шкала температур
- § 93. Третье начало термодинамики
- § 94. Отрицательные температуры
- Глава VII. СВОЙСТВА ЖИДКОСТЕЙ
- § 95. Объемные свойства жидкостей
- § 96. Теплоемкость жидкостей
- § 97. Явления переноса в жидкостях
- § 98. Явления на границе жидкости
- § 99. Условия равновесия на границе двух сред. Краевой угол
- § 100. Силы, возникающие на кривой поверхности жидкости
- § 101. Капиллярные явления
- § 102. Некоторые методы измерения коэффициента поверхностного натяжения
- § 103. Зависимость коэффициента поверхностного натяжения от температуры
- § 104. Испарение и кипение жидкостей
- § 105. Температурная зависимость упругости насыщенных паров
- § 106. Упругость насыщенного пара над кривой поверхностью жидкости
- § 107. Кипение жидкостей
- § 108. Жидкие растворы
- § 109. Осмотическое давление
- Глава VIII. НИЗКИЕ ТЕМПЕРАТУРЫ
- § 110. Сжижение газов
- § 111. Эффект Джоуля-Томсона
- § 112. Адиабатное расширение газа с совершением внешней работы
- § 113. Сжижение газов с использованием эффекта Джоуля — Томсона (метод Линде)
- § 114. Сжижение газов методом адиабатного расширения в детандерах (метод Клода)
- § 115. Некоторые свойства сжиженных газов
- § 116. Сверхнизкие температуры
- § 117. Свойства вещества при низких температурах
- § 118. Жидкий гелий
- Глава IX. ТВЕРДОЕ ТЕЛО
- § 120. Кристаллическая решетка
- § 121. Дефекты в кристаллах
- § 122. Механические свойства твердых тел. Деформации
- § 123. Деформация растяжения и сжатия. Сдвиг
- § 124. Связь между модулями упругости
- § 125. Упругая деформация и тепловое расширение
- § 126. Зависимость деформации от напряжения
- § 127. Механизм пластической деформации
- § 128. Дислокации в кристаллах
- § 129. Переход в твердое состояние
- § 130. Диаграмма состояния. Тройная точка
- § 131. Фазовые переходы первого и второго рода
- § 132. Твердый гелий
- § 133. Растворение и кристаллизация из раствора
- § 134. Сплавы. Диаграммы плавкости
- § 135. Зонная очистка металлов
- § 136. Опытное определение температуры плавления
- § 137. Тепловые свойства твердых тел
- § 138. Измерение теплоемкости
- § 139. Тепловое расширение твердых тел
- § 140. Теплопроводность
- § 141. Диффузия в твердых телах