| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ 87. Энтропия при необратимых процессах в замкнутой системе, акон возрастания энтропии
Важной особенностью энтропии является ее поведение при необратимых процессах.
В § 84 мы видели, что для необратимого кругового процесса справедливо соотношение

Оно является обобщением частного уравнения

которое, в свою очередь, является следствием первой теоремы Карно.

Рис. 95.
Рассмотрим процесс, при котором система необратимым образом переходит из равновесного состояния 1 в равновесное состояние 2 (на рис. 95 он показан сплошной линией). Необратимость перехода означает, что промежуточные состояния неравновесны. Как при таком переходе изменяется энтропия системы? Чтобы это выяснить, вернем систему в первоначальное состояние каким-нибудь обратимым путем, например путем, показанным на рис. 95 пунктирной линией. Получившийся круговой процесс необратим, потому что одна его часть необратима. Поэтому для него справедливо уравнение

Но

Второй из двух интегралов, поскольку он относится к обратимому процессу, равен

Следовательно,

Если система замкнута, т. е. изолирована от источников теплоты, то  и
и

Отсюда следует, что энтропия замкнутой (т. е. адиабатно изолированной) системы при необратимом процессе возрастает.
Имея в виду то, что было сказано в предыдущем параграфе, можно сказать что энтропия замкнутой системы либо остается постоянной, либо возрастает.
Полученный нами закон возрастания энтропии при необратимых процессах — одна из важнейших особенностей величины энтропии. Он тем более важен, что, как уже указывалось, понятие об обратимом процессе является идеализацией. Ведь при обратимом процессе система на любой его стадии должна находиться в состоянии термодинамического равновесия. Для установления равновесия требуется время, и поэтому процесс, чтобы быть вполне обратимым, должен протекать бесконечно медленно, что, конечно, никогда не бывает.
Для необратимых же процессов в замкнутых системах энтропия, как показывают опыт и теория, всегда возрастает, и это свойство так же присуще энтропии, как энергии свойственно сохраняться при любых процессах в замкнутых системах.
Именно потому, что энергия обладает свойством сохраняться в замкнутой системе, она (энергия) не может служить функцией, показывающей, в каком направлении идут процессы в такой системе; ведь при любом изменении состояния энергия в начале и в конце процесса одна и та же и она поэтому не дает возможности отличить друг от друга начальное и конечное состояния. Энтропия же, в естественно идущих процессах всегда возрастающая, позволяет судить, какое направление процесса возможно и какое нет, какое состояние является начальным и какое конечным,
Если, например, мы смешиваем две массы воды с разными температурами, то нетрудно убедиться, что сумма энтропий обеих масс до смешения меньше энтропии смеси, имеющей промежуточную температуру. Ясно, что процесс смешения может идти сам собой, но обратный процесс разделения смешанных масс ни в коем случае идти не может, так как он сопровождался бы уменьшением энтропии.
Рост энтропии в любом процессе продолжается не беспредельно, а лишь до определенного максимального значения, характерного для данной системы. Это максимальное значение энтропии соответствует состоянию равновесия, и после того, как оно достигнуто, какие бы то ни было изменения состояния без внешнего воздействия прекращаются.
Таким образом, энтропия как функция состояния существенно отличается от энергии. В то время как энергия не может быть ни создана, ни уничтожена, энтропия может создаваться и она постоянно создается во всяком процессе перехода к равновесию. Но,
однажды созданная, она уже не может быть уничтожена: обратный процесс с уменьшением энтропии не может идти.
Закон возрастания энтропии при необратимых процессах также часто называют вторым началом термодинамики.
Приведем некоторые примеры, иллюстрирующие этот закон.
Увеличение энтропии при теплопередаче. Если привести в соприкосновение два тела  температуры которых соответственно равны
температуры которых соответственно равны  и
и  то теплота будет переходить от более нагретого тела к менее нагретому, в результате чего температуры обоих тел будут выравниваться.
то теплота будет переходить от более нагретого тела к менее нагретому, в результате чего температуры обоих тел будут выравниваться.
Пусть  Вычислим изменение энтропии, которым сопровождается этот необратимый процесс.
Вычислим изменение энтропии, которым сопровождается этот необратимый процесс.
Состояние тела А изменяется при этом за счет потери им некоторого количества теплоты  соответственно тело В изменяет свое состояние за счет получения такого же количества теплоты
соответственно тело В изменяет свое состояние за счет получения такого же количества теплоты 
Для определения изменения энтропии системы, состоящей из обоих тел, нужно вычислить значения  для какого-нибудь обратимого процесса, приводящего к тому же изменению состояния системы (см. стр. 274). Таким процессом может служить, например, процесс передачи тепла от тела А телу В при помощи третьего рабочего тела, как это было сделано при рассмотрении процесса Карно, который, как известно, осуществляется обратимым путем на всех стадиях. Тогда для тела А и соответственно для тела В
для какого-нибудь обратимого процесса, приводящего к тому же изменению состояния системы (см. стр. 274). Таким процессом может служить, например, процесс передачи тепла от тела А телу В при помощи третьего рабочего тела, как это было сделано при рассмотрении процесса Карно, который, как известно, осуществляется обратимым путем на всех стадиях. Тогда для тела А и соответственно для тела В

Общее изменение энтропии обоих тел равно:

Поскольку  то
то  т. е. энтропия системы возрастает.
т. е. энтропия системы возрастает.
Приведенное рассуждение не зависит от того, посредством какого процесса осуществлен переход теплоты от тела А к телу В — теплопроводностью или излучением. Существенно лишь, что температуры обоих тел различны.
Рост энтропии при адиабатном расширении идеального газа в пустоту. Мы уже отмечали, что расширение газа в пустоту — процесс необратимый. Покажем теперь, что этот процесс сопровождается возрастанием энтропии.
Представим себе сосуд с теплоизолирующими стенками, разделенный на две части перегородкой с отверстием, закрытым заслонкой (рис. 96). Пусть одна из частей сосуда, объемом  заполнена
заполнена
1 молем идеального газа, в то время как другая свободна от газа. Если открыть заслонку, то газ адиабатно расширится и заполнит весь объем V сосуда. Известно, что при этом температура газа не изменяется (опыт Джоуля; см. § 33).
На первый взгляд кажется, что энтропия газа при таком расширении не должна измениться, поскольку от него не отводится и к нему не подводится теплота. Однако это не так. Процесс расширения в описанном опыте — необратимый, и к нему нельзя применять соотношение  При необратимом процессе величина
При необратимом процессе величина  не является дифференциалом какой-либо функции состояния. В частности, интеграл
не является дифференциалом какой-либо функции состояния. В частности, интеграл  не равен изменению энтропии.
не равен изменению энтропии.

Рис. 96.
В действительности энтропия газа при адиабатном расширении в пустоту изменяется. Чтобы найти это изменение, нужно вычислить изменение энтропии при каком-нибудь обратимом процессе, приводящем к такому же изменению состояния. Таким процессом может быть, например, обратимое изотермическое расширение газа при той же температуре. В § 85 мы уже сделали такое вычисление, которое показало, что при изотермическом обратимом расширении 1 моля газа в пустоту изменение энтропии  равно [см. формулу (85.9)]
равно [см. формулу (85.9)]
Так как  т. е. энтропия при расширении газа возрастает.
т. е. энтропия при расширении газа возрастает.
Рост энтропии при взаимной диффузии газов. Если привести в соприкосновение два различных газа, то они сами собой, без всякого внешнего воздействия, перемешаются благодаря взаимной диффузии. Обратный процесс, т. е. разделение газовой смеси на ее компоненты, сам собой не происходит и возможен только при определенном внешнем воздействии. Перемешивание газов — это необратимый процесс, и он должен поэтому сопровождаться ростом энтропии.
Действительно, представим себе, что в сосуде объемом  находится 1 моль некоторого идеального газа. В другом сосуде объемом
находится 1 моль некоторого идеального газа. В другом сосуде объемом  содержится 1 моль другого газа. Соединим вместе оба сосуда. Газы тогда смешаются и образовавшаяся смесь займет объем
содержится 1 моль другого газа. Соединим вместе оба сосуда. Газы тогда смешаются и образовавшаяся смесь займет объем  Этот процесс можно рассматривать как расширение каждого из газов: первый расширился от объема
Этот процесс можно рассматривать как расширение каждого из газов: первый расширился от объема  до объема V, второй — от объема
до объема V, второй — от объема  до объема
до объема  При этом энтропия первого газа, как мы только что видели, изменяется на величину
При этом энтропия первого газа, как мы только что видели, изменяется на величину 
второго — на величину  Общее же изменение энтропии
Общее же изменение энтропии  выразится равенством
выразится равенством

Так как и  и
и  меньше, чем V, то
меньше, чем V, то  т. е. энтропия системы возросла.
т. е. энтропия системы возросла.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ВВЕДЕНИЕ
- Глава I. КИНЕТИЧЕСКАЯ ТЕОРИЯ ИДЕАЛЬНЫХ ГАЗОВ
- § 1. Идеальный газ
- § 2. Давление газа
- § 3. Температура
- § 4. Уравнение состояния идеального газа
- § 5. Законы идеального газа
- § 6. Скорости газовых молекул
- § 7. Броуновское движение
- § 8. Барометрическая формула
- § 9. Закон Больцмана
- § 10. Понятие о вероятности
- § 11. Понятие о распределении. Функция распределения
- § 12. Распределение молекул по компонентам скорости
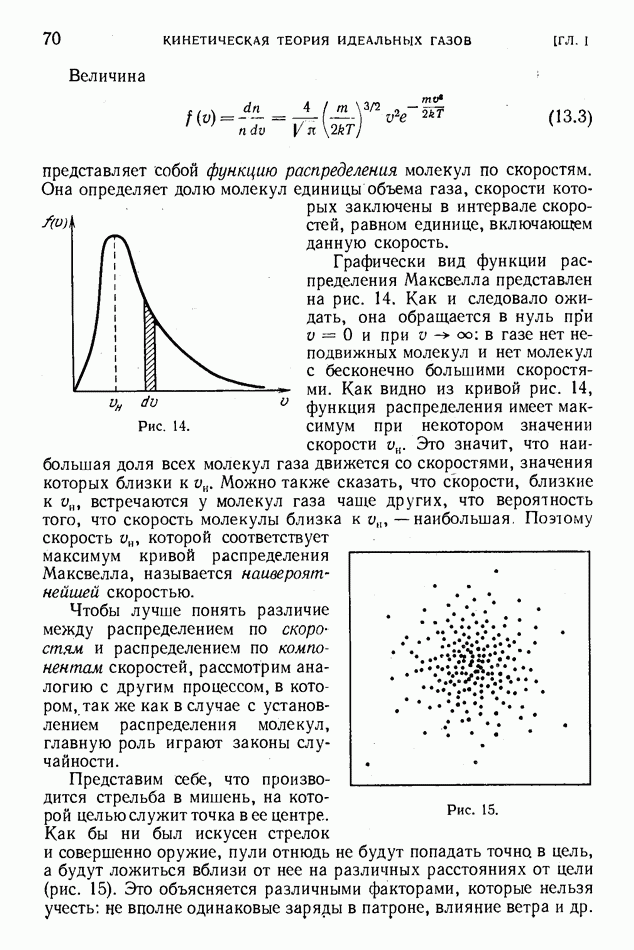
- § 13. Распределение молекул по скоростям
- § 14. Средние скорости молекул
- § 15. Наивероятнейшая скорость молекул
- § 16. Формула Максвелла для относительных скоростей
- § 17. Закон распределения молекул по скоростям и атмосферы планет
- § 18. Экспериментальная проверка закона распределения
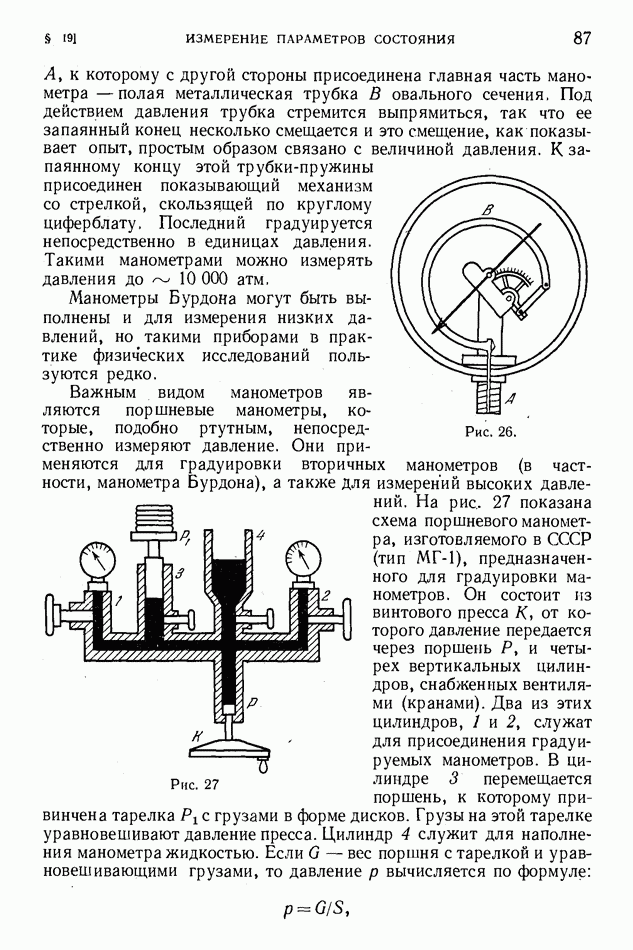
- § 19. Измерение параметров состояния
- Глава II. КИНЕТИЧЕСКАЯ ТЕОРИЯ ТЕПЛОТЫ. ЗАКОН СОХРАНЕНИЯ ЭНЕРГИИ
- § 20. Внутренняя энергия идеального газа
- § 21. Количество теплоты
- § 22. Механический эквивалент теплоты
- § 23. Первое начало термодинамики
- § 24. Теплоемкость идеальных газов
- § 25. Теплоемкость одноатомных газов
- § 26. Теплоемкость газов и число степеней свободы молекул
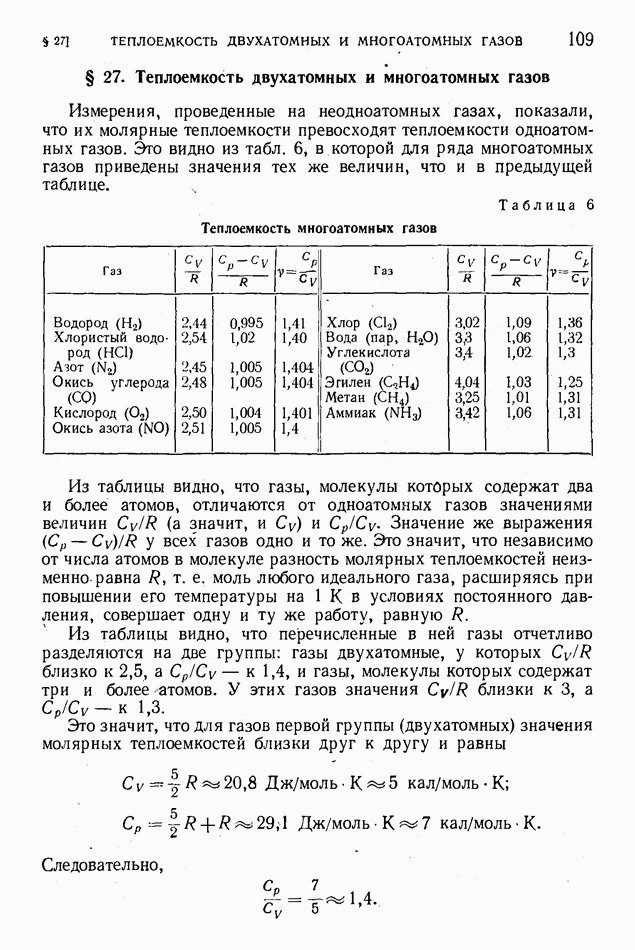
- § 27. Теплоемкость двухатомных и многоатомных газов
- § 28. Изменение состояния при изменении объема газа
- § 29. Работа при изотермическом изменении объема идеального газа
- § 30. Адиабатное изменение объема идеального газа
- § 31. Работа при адиабатном изменении объема газа
- § 32. Политропический процесс
- § 33. Расширение газа в пустоту
- § 34. Измерение количества теплоты и теплоемкости
- Глава III. СТОЛКНОВЕНИЯ МОЛЕКУЛ И ЯВЛЕНИЯ ПЕРЕНОСА
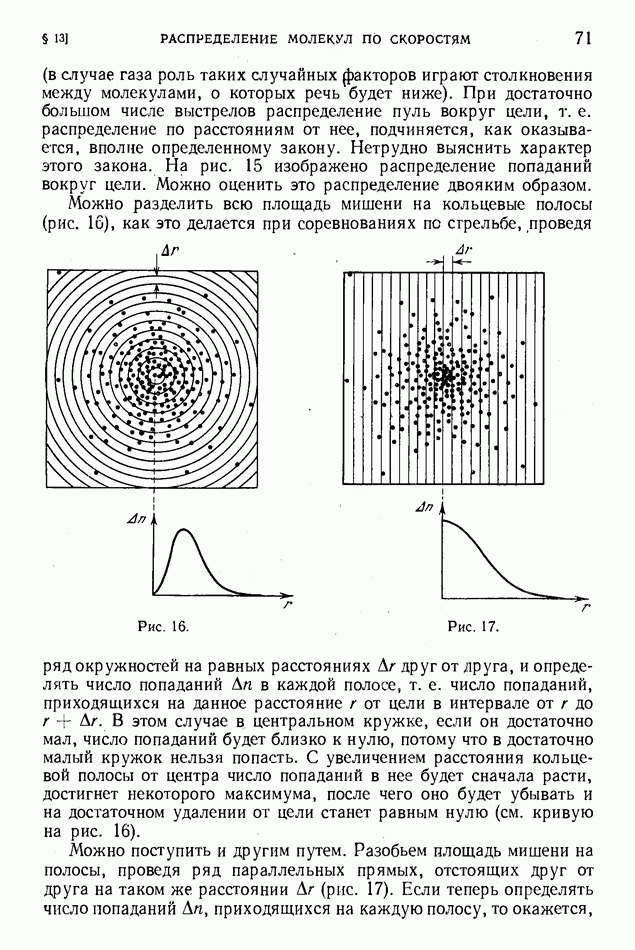
- § 35. Молекулярные движения и явления переноса
- § 36. Среднее число столкновений в единицу времени и средняя длина свободного пробега молекул
- § 37. Эффективное поперечное сечение частицы и вероятность
- § 38. Рассеяние молекулярного пучка в газе
- § 39. Экспериментальное определение длины свободного пробега
- § 40. Диффузия в газах
- § 41. Нестационарная диффузия
- § 42. Стационарная диффузия. Вычисление коэффициента диффузии
- § 43. Коэффициент взаимной диффузии
- § 44. Термическая диффузия
- § 45. Теплопроводность газов
- § 46. Нестационарная теплопроводность
- § 47. Стационарная теплопроводность. Вычисление коэффициента теплопроводности
- § 48. Вязкость газов (внутреннее трение)
- § 49. Измерение коэффициента вязкости (вискозиметрия)
- § 50. Соотношения между коэффициентами переноса
- Глава IV. ФИЗИЧЕСКИЕ ЯВЛЕНИЯ В РАЗРЕЖЕННЫХ ГАЗАХ (ВАКУУМЕ)
- § 51. Теплопередача в газах при малых давлениях
- § 52. Течение газов при малых давлениях (молекулярное течение)
- § 53. Молекулярное течение газа в цилиндрической трубе
- § 54. Молекулярное течение смеси газов. Разделение газовых смесей
- § 55. Диффузия газов в вакууме
- § 56. Разность давлений между различно нагретыми частями газа (тепловая транспирация)
- § 57. Элементы вакуумной техники
- § 58. Измерение малых давлений
- § 59. Вакуумная установка
- Глава V. НЕИДЕАЛЬНЫЕ (РЕАЛЬНЫЕ) ГАЗЫ. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА
- § 60. Отклонения свойств газов от идеальности
- § 61. Сжижение газов (конденсация)
- § 62. Фазовый переход
- § 63. Фазовые диаграммы
- § 64. Методы определения критических параметров
- § 65. Уравнение Ван-дер-Ваальса
- § 66. Изотермы Ван-дер-Ваальса
- § 67. Критическая температура и критическое состояние
- § 68. Экспериментальное определение констант уравнения Ван-дер-Ваальса
- § 69. Сравнение уравнения Ван-дер-Ваальса с данными опыта
- § 70. Приведенное уравнение Ван-дер-Ваальса. Закон соответственных состояний
- § 71. Межмолекулярные силы взаимодействия в реальном газе
- § 72. Теплоемкость неидеальных газов
- Глава VI. ЭЛЕМЕНТЫ ТЕРМОДИНАМИКИ
- § 73. Равновесные состояния
- § 74. Обратимые и необратимые процессы
- § 75. Квазистатические процессы
- § 76. Необратимость и вервятность
- § 77. Взаимные превращения механической и тепловой энергии
- § 78. Первое начало термодинамики
- § 79. Преобразование теплоты в механическую работу
- § 80. Цикл Карно
- § 81. Холодильная машина
- § 82. Доказательство теорем Карно
- § 83. Свободная энергия
- § 84. Энтропия
- § 85. Некоторые термодинамические соотношения
- § 86. Энтропия при обратимых процессах в замкнутой системе
- § 87. Энтропия при необратимых процессах в замкнутой системе, акон возрастания энтропии
- § 88. Второе начало термодинамики и превращение теплоты в работу
- § 89. Физический смысл энтропии. Энтропия и вероятность
- § 90. Энтропия и беспорядок
- § 91. «Демон» Максвелла
- § 92. Термодинамическая шкала температур
- § 93. Третье начало термодинамики
- § 94. Отрицательные температуры
- Глава VII. СВОЙСТВА ЖИДКОСТЕЙ
- § 95. Объемные свойства жидкостей
- § 96. Теплоемкость жидкостей
- § 97. Явления переноса в жидкостях
- § 98. Явления на границе жидкости
- § 99. Условия равновесия на границе двух сред. Краевой угол
- § 100. Силы, возникающие на кривой поверхности жидкости
- § 101. Капиллярные явления
- § 102. Некоторые методы измерения коэффициента поверхностного натяжения
- § 103. Зависимость коэффициента поверхностного натяжения от температуры
- § 104. Испарение и кипение жидкостей
- § 105. Температурная зависимость упругости насыщенных паров
- § 106. Упругость насыщенного пара над кривой поверхностью жидкости
- § 107. Кипение жидкостей
- § 108. Жидкие растворы
- § 109. Осмотическое давление
- Глава VIII. НИЗКИЕ ТЕМПЕРАТУРЫ
- § 110. Сжижение газов
- § 111. Эффект Джоуля-Томсона
- § 112. Адиабатное расширение газа с совершением внешней работы
- § 113. Сжижение газов с использованием эффекта Джоуля — Томсона (метод Линде)
- § 114. Сжижение газов методом адиабатного расширения в детандерах (метод Клода)
- § 115. Некоторые свойства сжиженных газов
- § 116. Сверхнизкие температуры
- § 117. Свойства вещества при низких температурах
- § 118. Жидкий гелий
- Глава IX. ТВЕРДОЕ ТЕЛО
- § 120. Кристаллическая решетка
- § 121. Дефекты в кристаллах
- § 122. Механические свойства твердых тел. Деформации
- § 123. Деформация растяжения и сжатия. Сдвиг
- § 124. Связь между модулями упругости
- § 125. Упругая деформация и тепловое расширение
- § 126. Зависимость деформации от напряжения
- § 127. Механизм пластической деформации
- § 128. Дислокации в кристаллах
- § 129. Переход в твердое состояние
- § 130. Диаграмма состояния. Тройная точка
- § 131. Фазовые переходы первого и второго рода
- § 132. Твердый гелий
- § 133. Растворение и кристаллизация из раствора
- § 134. Сплавы. Диаграммы плавкости
- § 135. Зонная очистка металлов
- § 136. Опытное определение температуры плавления
- § 137. Тепловые свойства твердых тел
- § 138. Измерение теплоемкости
- § 139. Тепловое расширение твердых тел
- § 140. Теплопроводность
- § 141. Диффузия в твердых телах