| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ 65. Уравнение Ван-дер-Ваальса
Особенности поведения газов при повышенных давлениях и фазовый переход газ — жидкость не описываются уравнением Клапейрона, которое оказывается пригодным лишь для газов при малых давлениях (идеальных газов). Можно, однако, усовершенствовать это уравнение так, чтобы оно не только правильно описывало свойства реальных газов при любых давлениях, но и описывало также, с определенным приближением, свойства жидкостей и фазовый переход из газообразного состояния в жидкое.
Для этого нужно, очевидно, отказаться от представления о газовых молекулах, как о лишенных размеров материальных точках и от предположения, что силы взаимодействия между молекулами отсутствуют. Если принять, что в действительности межмолекулярные силы существуют и что молекулы обладают определенными размерами, и внести в уравнение Клапейрона соответствующие поправки, то можно надеяться получить новое уравнение состояния реальных газов, которое будет в лучшем согласии с опытными фактами.
Такое улучшенное уравнение состояния, в котором учтены как конечные размеры молекул, так и силы взаимодействия между ними, было в 1873 г. предложено Ван-дер-Ваальсом и носит его имя.
Нужно сразу же отметить, что уравнение состояния реальных газов, к рассмотрению которого мы приступаем, — тоже приближенное, потому что не существует способа точного вычисления сил взаимодействия между молекулами.
Учет сил отталкивания между молекулами. В уравнении состояния идеальных газов

написанном для 1 моля, под V подразумевается объем сосуда, в котором заключен газ. В то же время это тот объем, который доступен для каждой из молекул газа, движущейся в этом объеме. Когда идет речь об идеальном газе, состоящем из частиц-точек, нет разницы между понятиями «объем сосуда» и «объем, доступный для каждой молекулы», потому что молекулы-точки не мешают друг другу двигаться. В действительном же газе не весь объем сосуда находится в распоряжении молекул, так как каждая молекула занимает определенную часть объема сосуда и эта часть недоступна для всех других.
Чтобы учесть это обстоятельство, нужно из объема сосуда вычесть ту его часть, которая недоступна для движения молекул. Обозначим ее через  Тогда уравнение (65.1) примет вид:
Тогда уравнение (65.1) примет вид:

Введенная таким образом поправка  представляет собой тот предельный объем, который занял бы газ при бесконечно большом давлении. Действительно, переписав (65.2) в виде:
представляет собой тот предельный объем, который занял бы газ при бесконечно большом давлении. Действительно, переписав (65.2) в виде:

находим, что при  объем
объем 
Вычисление постоянной b. Введением в уравнение состояния постоянной  мы учли то обстоятельство, что молекулы газа не могут сблизиться друг с другом до расстояния, равного нулю (даже при бесконечно большом давлении). Фактически здесь принимается во внимание существование сил отталкивания между молекулами, которые и мешают молекулам приближаться друг к другу на расстояние, меньшее некоторого минимального. Оно, это минимальное расстояние, и определяет то, что называется размером молекулы. Значит, учет размеров молекул фактически означает в то же время учет сил отталкивания между частицами газа, а постоянная
мы учли то обстоятельство, что молекулы газа не могут сблизиться друг с другом до расстояния, равного нулю (даже при бесконечно большом давлении). Фактически здесь принимается во внимание существование сил отталкивания между молекулами, которые и мешают молекулам приближаться друг к другу на расстояние, меньшее некоторого минимального. Оно, это минимальное расстояние, и определяет то, что называется размером молекулы. Значит, учет размеров молекул фактически означает в то же время учет сил отталкивания между частицами газа, а постоянная  введенная в уравнение состояния, может рассматриваться как характеристика этих сил.
введенная в уравнение состояния, может рассматриваться как характеристика этих сил.
Если сделать определенные предположения о структуре молекул и о характере действующих между ними сил, то можно вычислить значение постоянной  т. е. величину той части объема сосуда, которая оказывается недоступной для любой молекулы, так как она занята всеми остальными. Проще всего это сделать, если предположить, что молекулы являются твердыми шариками.
т. е. величину той части объема сосуда, которая оказывается недоступной для любой молекулы, так как она занята всеми остальными. Проще всего это сделать, если предположить, что молекулы являются твердыми шариками.

Рис. 84.
Представим себе сосуд в форме куба, объем которого V равен объему, занимаемому при данных давлении и температуре молем газа (рис. 84). Огорона куба равна, очевидно, У V? Пусть диаметр молекулы равен  а радиус
а радиус 
Допустим, что сначала в нашем сосуде содержится всего одна молекула. Для ее движения (точнее — для движения ее центра) доступен весь объем сосуда, за вычетом слоя толщиной  прилегающего к стенкам, так как центр молекулы не может приблизиться к стенке на расстояние, меньшее чем
прилегающего к стенкам, так как центр молекулы не может приблизиться к стенке на расстояние, меньшее чем  (на рис. 84 этот слой отделен пунктирной линией). Это значит, что наша молекула может двигаться в объеме куба со стороной на
(на рис. 84 этот слой отделен пунктирной линией). Это значит, что наша молекула может двигаться в объеме куба со стороной на  меньшей, чем сторона действительного куба — сосуда. Объем этот равен:
меньшей, чем сторона действительного куба — сосуда. Объем этот равен:

Введем теперь в сосуд вторую молекулу (именно этот момент и изображен на рис. 84). Центр любой из имеющихся теперь в сосуде двух молекул для своего движения имеет в своем распоряжении тот же объем, что и раньше, но за вычетом дополнительного объема, ставшего недоступным из-за присутствия второй молекулы. На рис. 84 пунктиром показан объем, окружающий каждую молекулу, в пределы которого не может попасть центр ее партнера. Этот объем равен  Следовательно, для любой из двух молекул оказывается доступным объем, равный
Следовательно, для любой из двух молекул оказывается доступным объем, равный

Если ввести в сосуд еще и третью молекулу, то для любой из трех частиц, находящихся теперь в сосуде, свободным для движения будет объем

Наконец, когда в сосуде окажутся все  молекул
молекул  число Авогадро), составляющих один, моль, каждая из них будет иметь возможность двигаться в объеме
число Авогадро), составляющих один, моль, каждая из них будет иметь возможность двигаться в объеме

При этом расчете мы, однако, не учли того обстоятельства, что в каждом акте сближения (столкновения) участвуют две молекулы. Для каждой из них существенна не вся запретная сфера, окружающая вторую участницу сближения, а только та ее половина (полусфера), которая обращена к ней. Если применить это соображение к любой паре из всех  молекул, то в выражении (65.4) мы должны будем вместо
молекул, то в выражении (65.4) мы должны будем вместо  написать
написать  Тогда свободным для движения любой молекулы окажется такой объем:
Тогда свободным для движения любой молекулы окажется такой объем:

Если, как это всегда, конечно, бывает,  (здесь
(здесь  сторона сосуда,
сторона сосуда,  диаметр молекулы), то, пренебрегая
диаметр молекулы), то, пренебрегая  по сравнению с
по сравнению с  получим:
получим:

Это и есть та величина  которую мы поставили вместо V в уравнение состояния (65.2). Следовательно,
которую мы поставили вместо V в уравнение состояния (65.2). Следовательно,

Значит, поправка на объем молекул равна не объему самих молекул, а учетверенному значению этой величины.
Мы получили этот результат, считая молекулы твердыми шариками. Нужно отметить, что такое представление является грубым приближением. Это видно из того, что при стремлении давления к бесконечности объем газа должен стремиться к значению  как мы это видели выше. Но при этом молекулы должны быть, очевидно, «упакованы» максимально плотно. При такой упаковке молекулы-шарики в самом деле занимают объем больший, чем сумма объемов всех шариков (за счет промежутков между ними). Но из геометрических соображений следует, что отношение объема, занятого всей совокупностью шариков, к их «чистому» объему равно
как мы это видели выше. Но при этом молекулы должны быть, очевидно, «упакованы» максимально плотно. При такой упаковке молекулы-шарики в самом деле занимают объем больший, чем сумма объемов всех шариков (за счет промежутков между ними). Но из геометрических соображений следует, что отношение объема, занятого всей совокупностью шариков, к их «чистому» объему равно  т. е. меньше двух, тогда как наш расчет показывает, что это отношение равно четырем. Тем не менее при не слишком больших давлениях наш расчет дает приблизительно правильный результат.
т. е. меньше двух, тогда как наш расчет показывает, что это отношение равно четырем. Тем не менее при не слишком больших давлениях наш расчет дает приблизительно правильный результат.
Учет сил притяжения между молекулами. Кроме сил отталкивания, которые уже учтены введением поправки  существуют и силы притяжения между молекулами. Эти силы приводят к тому, что давление, оказываемое молекулами газа на любую площадку, например на стенки сосуда, будет при прочих равных условиях меньше, чем в случае идеального газа.
существуют и силы притяжения между молекулами. Эти силы приводят к тому, что давление, оказываемое молекулами газа на любую площадку, например на стенки сосуда, будет при прочих равных условиях меньше, чем в случае идеального газа.
Действительно, любая молекула, находящаяся вблизи стенки сосуда, где она с одной стороны имеет больше «соседей», чем с другой, испытывает результирующую силу со стороны остальных молекул, и сила эта направлена внутрь газа. Благодаря этому давление на стенку сосуда станет меньше на некоторую величину  так что вместо выражения (65.4) мы получим для давления формулу:
так что вместо выражения (65.4) мы получим для давления формулу:

Силы притяжения между молекулами стремятся сблизить их между собой. Но точно таким же образом действует и внешнее давление 
Нетрудно установить, от чего должно зависеть это добавочное давление (или, что то же, уменьшение давления на стенку).
Давление, которое испытывает пристенный слой со стороны молекул газа, равно силе, действующей на все молекулы на единице поверхности слоя. Очевидно, что эта сила пропорциональна плотности молекул  С другой стороны, число молекул в пристенном слое, испытывающих силу притяжения, также пропорционально
С другой стороны, число молекул в пристенном слое, испытывающих силу притяжения, также пропорционально  Следовательно,
Следовательно,  Так как
Так как  обратно пропорционально объему, занимаемому молем газа, то
обратно пропорционально объему, занимаемому молем газа, то  где V — молярный объем газа и а — коэффициент пропорциональности, численное значение которого зависит от характера сил притяжения между
где V — молярный объем газа и а — коэффициент пропорциональности, численное значение которого зависит от характера сил притяжения между
молекулами. В настоящее время нет способа вычисления этого коэффициента.
Таким образом, выражение для давления газа с учетом сил притяжения между молекулами можно теперь написать в виде

отсюда

Это уравнение, связывающее давление, объем и температуру газа, является уравнением состояния реального газа. В нем учтены как силы притяжения (поправочный член  так и силы отталкивания (поправка
так и силы отталкивания (поправка  между молекулами. Оно называется уравнением Ван-дер-Ваальса. Как мы увидим, это уравнение довольно хорошо объясняет основные опытные факты, касающиеся реальных газов, изложенные в предыдущих параграфах.
между молекулами. Оно называется уравнением Ван-дер-Ваальса. Как мы увидим, это уравнение довольно хорошо объясняет основные опытные факты, касающиеся реальных газов, изложенные в предыдущих параграфах.
Уравнение (65.5) относится к одному молю газа. Для произвольного количества газа оно принимает вид:

Здесь  масса газа,
масса газа,  его молекулярный вес, V — объем, занимаемый газом.
его молекулярный вес, V — объем, занимаемый газом.
Коэффициент а в выражении для поправки к давлению и поправка  считаются постоянными величинами, численные значения которых различны для различных газов, так что уравнение (65.5) не является универсальным в такой мере, как уравнение Клапейрона.
считаются постоянными величинами, численные значения которых различны для различных газов, так что уравнение (65.5) не является универсальным в такой мере, как уравнение Клапейрона.
Постоянная  измеряется, очевидно, в единицах объема. Размерность же константы а определяется тем, что величина
измеряется, очевидно, в единицах объема. Размерность же константы а определяется тем, что величина  должна иметь размерность давления. Поэтому а измеряется в системе СИ в единицах
должна иметь размерность давления. Поэтому а измеряется в системе СИ в единицах  т. е. в
т. е. в  а в системе
а в системе  в дин
в дин  Иногда а измеряют также в атм-см.
Иногда а измеряют также в атм-см.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ВВЕДЕНИЕ
- Глава I. КИНЕТИЧЕСКАЯ ТЕОРИЯ ИДЕАЛЬНЫХ ГАЗОВ
- § 1. Идеальный газ
- § 2. Давление газа
- § 3. Температура
- § 4. Уравнение состояния идеального газа
- § 5. Законы идеального газа
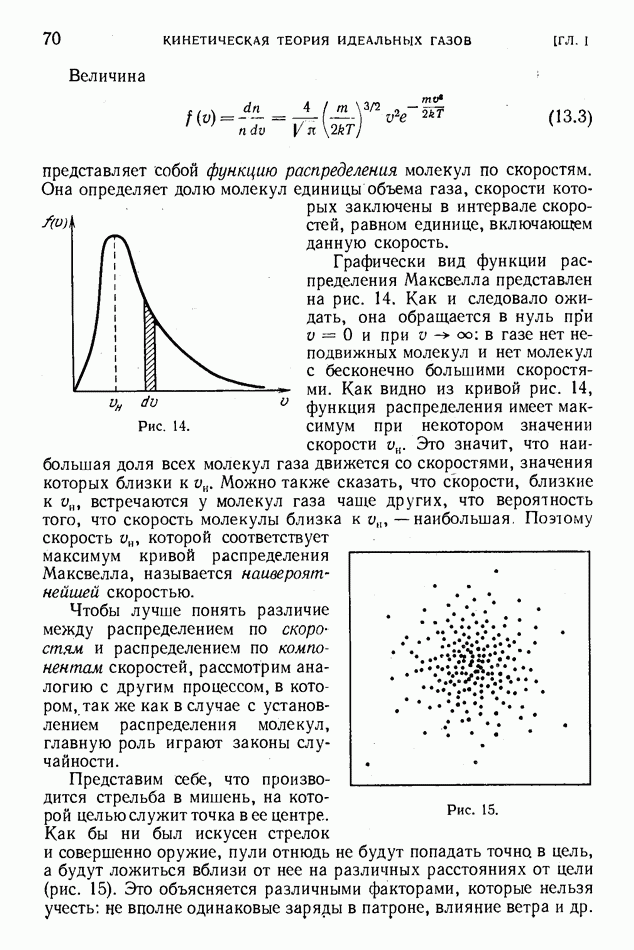
- § 6. Скорости газовых молекул
- § 7. Броуновское движение
- § 8. Барометрическая формула
- § 9. Закон Больцмана
- § 10. Понятие о вероятности
- § 11. Понятие о распределении. Функция распределения
- § 12. Распределение молекул по компонентам скорости
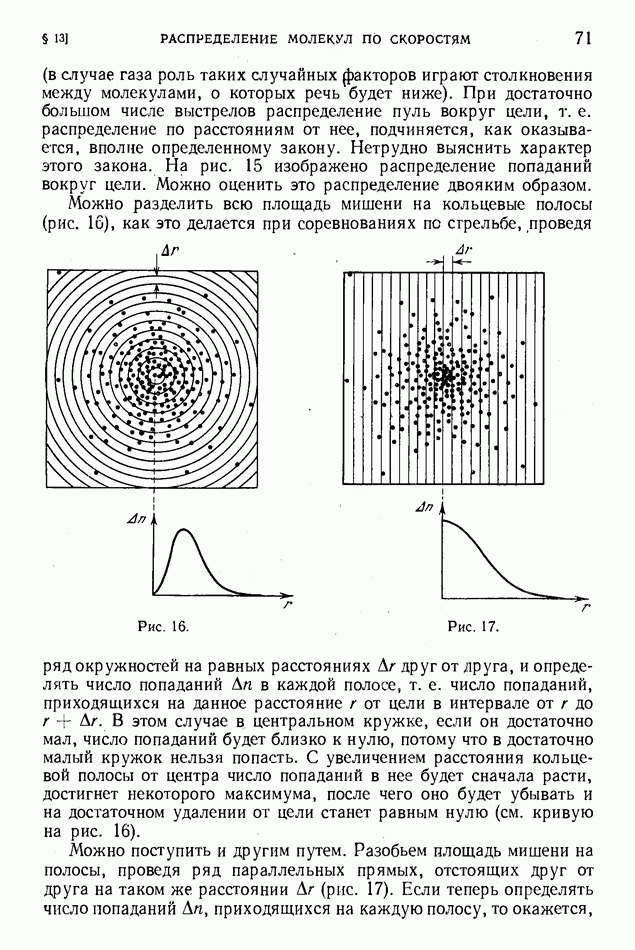
- § 13. Распределение молекул по скоростям
- § 14. Средние скорости молекул
- § 15. Наивероятнейшая скорость молекул
- § 16. Формула Максвелла для относительных скоростей
- § 17. Закон распределения молекул по скоростям и атмосферы планет
- § 18. Экспериментальная проверка закона распределения
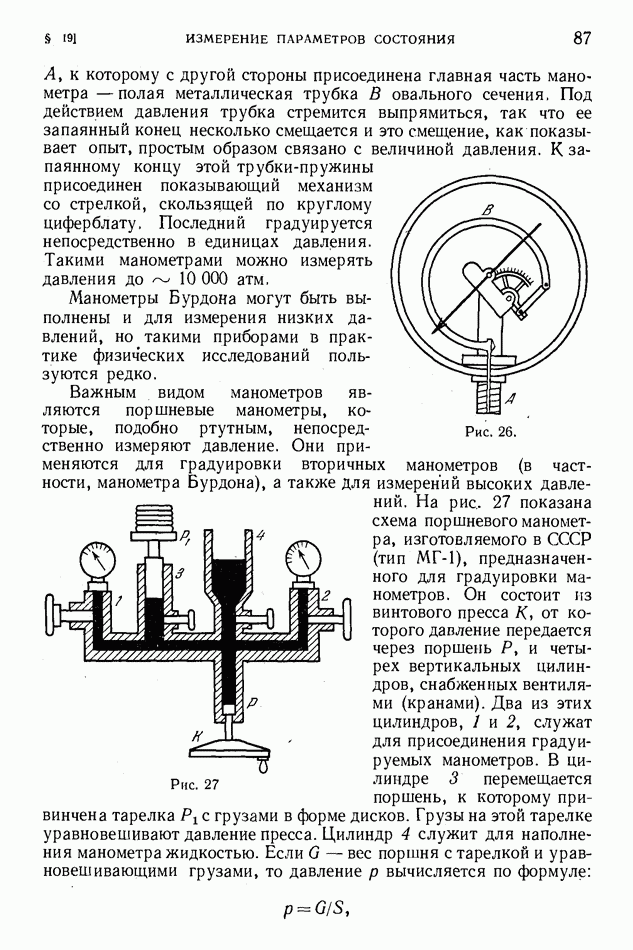
- § 19. Измерение параметров состояния
- Глава II. КИНЕТИЧЕСКАЯ ТЕОРИЯ ТЕПЛОТЫ. ЗАКОН СОХРАНЕНИЯ ЭНЕРГИИ
- § 20. Внутренняя энергия идеального газа
- § 21. Количество теплоты
- § 22. Механический эквивалент теплоты
- § 23. Первое начало термодинамики
- § 24. Теплоемкость идеальных газов
- § 25. Теплоемкость одноатомных газов
- § 26. Теплоемкость газов и число степеней свободы молекул
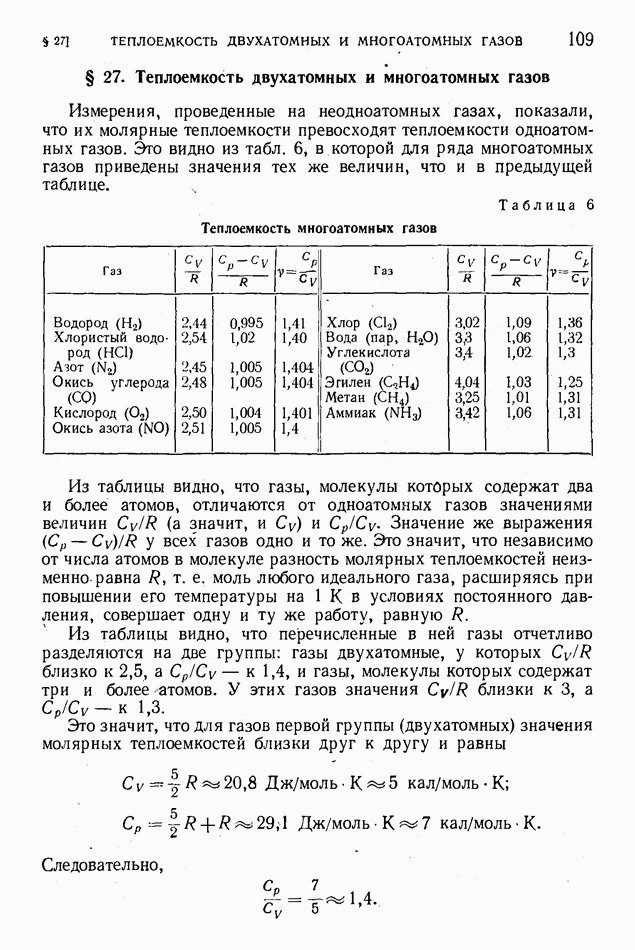
- § 27. Теплоемкость двухатомных и многоатомных газов
- § 28. Изменение состояния при изменении объема газа
- § 29. Работа при изотермическом изменении объема идеального газа
- § 30. Адиабатное изменение объема идеального газа
- § 31. Работа при адиабатном изменении объема газа
- § 32. Политропический процесс
- § 33. Расширение газа в пустоту
- § 34. Измерение количества теплоты и теплоемкости
- Глава III. СТОЛКНОВЕНИЯ МОЛЕКУЛ И ЯВЛЕНИЯ ПЕРЕНОСА
- § 35. Молекулярные движения и явления переноса
- § 36. Среднее число столкновений в единицу времени и средняя длина свободного пробега молекул
- § 37. Эффективное поперечное сечение частицы и вероятность
- § 38. Рассеяние молекулярного пучка в газе
- § 39. Экспериментальное определение длины свободного пробега
- § 40. Диффузия в газах
- § 41. Нестационарная диффузия
- § 42. Стационарная диффузия. Вычисление коэффициента диффузии
- § 43. Коэффициент взаимной диффузии
- § 44. Термическая диффузия
- § 45. Теплопроводность газов
- § 46. Нестационарная теплопроводность
- § 47. Стационарная теплопроводность. Вычисление коэффициента теплопроводности
- § 48. Вязкость газов (внутреннее трение)
- § 49. Измерение коэффициента вязкости (вискозиметрия)
- § 50. Соотношения между коэффициентами переноса
- Глава IV. ФИЗИЧЕСКИЕ ЯВЛЕНИЯ В РАЗРЕЖЕННЫХ ГАЗАХ (ВАКУУМЕ)
- § 51. Теплопередача в газах при малых давлениях
- § 52. Течение газов при малых давлениях (молекулярное течение)
- § 53. Молекулярное течение газа в цилиндрической трубе
- § 54. Молекулярное течение смеси газов. Разделение газовых смесей
- § 55. Диффузия газов в вакууме
- § 56. Разность давлений между различно нагретыми частями газа (тепловая транспирация)
- § 57. Элементы вакуумной техники
- § 58. Измерение малых давлений
- § 59. Вакуумная установка
- Глава V. НЕИДЕАЛЬНЫЕ (РЕАЛЬНЫЕ) ГАЗЫ. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА
- § 60. Отклонения свойств газов от идеальности
- § 61. Сжижение газов (конденсация)
- § 62. Фазовый переход
- § 63. Фазовые диаграммы
- § 64. Методы определения критических параметров
- § 65. Уравнение Ван-дер-Ваальса
- § 66. Изотермы Ван-дер-Ваальса
- § 67. Критическая температура и критическое состояние
- § 68. Экспериментальное определение констант уравнения Ван-дер-Ваальса
- § 69. Сравнение уравнения Ван-дер-Ваальса с данными опыта
- § 70. Приведенное уравнение Ван-дер-Ваальса. Закон соответственных состояний
- § 71. Межмолекулярные силы взаимодействия в реальном газе
- § 72. Теплоемкость неидеальных газов
- Глава VI. ЭЛЕМЕНТЫ ТЕРМОДИНАМИКИ
- § 73. Равновесные состояния
- § 74. Обратимые и необратимые процессы
- § 75. Квазистатические процессы
- § 76. Необратимость и вервятность
- § 77. Взаимные превращения механической и тепловой энергии
- § 78. Первое начало термодинамики
- § 79. Преобразование теплоты в механическую работу
- § 80. Цикл Карно
- § 81. Холодильная машина
- § 82. Доказательство теорем Карно
- § 83. Свободная энергия
- § 84. Энтропия
- § 85. Некоторые термодинамические соотношения
- § 86. Энтропия при обратимых процессах в замкнутой системе
- § 87. Энтропия при необратимых процессах в замкнутой системе, акон возрастания энтропии
- § 88. Второе начало термодинамики и превращение теплоты в работу
- § 89. Физический смысл энтропии. Энтропия и вероятность
- § 90. Энтропия и беспорядок
- § 91. «Демон» Максвелла
- § 92. Термодинамическая шкала температур
- § 93. Третье начало термодинамики
- § 94. Отрицательные температуры
- Глава VII. СВОЙСТВА ЖИДКОСТЕЙ
- § 95. Объемные свойства жидкостей
- § 96. Теплоемкость жидкостей
- § 97. Явления переноса в жидкостях
- § 98. Явления на границе жидкости
- § 99. Условия равновесия на границе двух сред. Краевой угол
- § 100. Силы, возникающие на кривой поверхности жидкости
- § 101. Капиллярные явления
- § 102. Некоторые методы измерения коэффициента поверхностного натяжения
- § 103. Зависимость коэффициента поверхностного натяжения от температуры
- § 104. Испарение и кипение жидкостей
- § 105. Температурная зависимость упругости насыщенных паров
- § 106. Упругость насыщенного пара над кривой поверхностью жидкости
- § 107. Кипение жидкостей
- § 108. Жидкие растворы
- § 109. Осмотическое давление
- Глава VIII. НИЗКИЕ ТЕМПЕРАТУРЫ
- § 110. Сжижение газов
- § 111. Эффект Джоуля-Томсона
- § 112. Адиабатное расширение газа с совершением внешней работы
- § 113. Сжижение газов с использованием эффекта Джоуля — Томсона (метод Линде)
- § 114. Сжижение газов методом адиабатного расширения в детандерах (метод Клода)
- § 115. Некоторые свойства сжиженных газов
- § 116. Сверхнизкие температуры
- § 117. Свойства вещества при низких температурах
- § 118. Жидкий гелий
- Глава IX. ТВЕРДОЕ ТЕЛО
- § 120. Кристаллическая решетка
- § 121. Дефекты в кристаллах
- § 122. Механические свойства твердых тел. Деформации
- § 123. Деформация растяжения и сжатия. Сдвиг
- § 124. Связь между модулями упругости
- § 125. Упругая деформация и тепловое расширение
- § 126. Зависимость деформации от напряжения
- § 127. Механизм пластической деформации
- § 128. Дислокации в кристаллах
- § 129. Переход в твердое состояние
- § 130. Диаграмма состояния. Тройная точка
- § 131. Фазовые переходы первого и второго рода
- § 132. Твердый гелий
- § 133. Растворение и кристаллизация из раствора
- § 134. Сплавы. Диаграммы плавкости
- § 135. Зонная очистка металлов
- § 136. Опытное определение температуры плавления
- § 137. Тепловые свойства твердых тел
- § 138. Измерение теплоемкости
- § 139. Тепловое расширение твердых тел
- § 140. Теплопроводность
- § 141. Диффузия в твердых телах