| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
Глава XX. Атомное ядро и внутриядерные процессы
§ 138. Общие сведения об атомных ядрах. Изотопы
Исследование атомных ядер началось в XX в., причем наиболее интенсивно оно проводилось в последние десятилетия (с 30-х годов по настоящее время). Таким образом, ядерная физика является одним из самых молодых разделов физики. Тем не менее результаты, которые уже удалось получить в этой области, оказались исключительно важными в научном и практическом отношении. Достаточно указать хотя бы на то, что исследование ядер и внутриядерных процессов привело к открытию и практическому использованию ядерной энергии.
Согласно гипотезе, высказанной в 1932 г. Д. Д. Иваненко и являющейся теперь общепризнанной, в состав всех атомных ядер входит только два вида элементарных частиц — протоны и нейтроны.
Протон имеет положительный заряд, равный заряду электрона  элементарному заряду
элементарному заряду  и массу покоя
и массу покоя  Нейтрон не имеет заряда; его масса немного больше массы протона:
Нейтрон не имеет заряда; его масса немного больше массы протона:  Протон принято обозначать буквой
Протон принято обозначать буквой  нейтрон — буквой
нейтрон — буквой  общее название этих частиц — нуклоны.
общее название этих частиц — нуклоны.
Массу ядер и элементарных частиц обычно выражают в атомных единицах массы (а. е. м.). За атомную единицу массы принята 1/12 массы изотопа углерода  Следовательно,
Следовательно,  Таким образом,
Таким образом,

В § 134 было показано, что заряд атомного ядра любого химического элемента, выраженный в элементарных зарядах, равен атомному номеру  этого элемента. Но заряд ядра слагается из зарядов протонов; следовательно,
этого элемента. Но заряд ядра слагается из зарядов протонов; следовательно,
число протонов  в атомном ядре элемента равно атомному номеру
в атомном ядре элемента равно атомному номеру  элемента:
элемента:

Почти вся масса атома заключена в его ядре (см. § 132). Но масса ядра слагается из масс всех нуклонов, входящих в ядро. Тогда, согласно соотношению (1), сумма чисел протонов  и нейтронов
и нейтронов  должна быть равна массовому числу атома, т. е. целому числу А, ближайшему к атомной массе (выраженной в а. е. м.):
должна быть равна массовому числу атома, т. е. целому числу А, ближайшему к атомной массе (выраженной в а. е. м.):  , или, учитывая формулу (2),
, или, учитывая формулу (2),  Следовательно, число нейтронов в атомном ядре элемента равно разности между массовым числом и атомным номером элемента:
Следовательно, число нейтронов в атомном ядре элемента равно разности между массовым числом и атомным номером элемента:

Таким образом, по массовому числу и атомному номеру химического элемента можно непосредственно определять число протонов и число нейтронов, содержащихся в атомном ядре этого элемента.
Атомные ядра химических элементов принято обозначать символом  где X — символ элемента, А — массовое число,
где X — символ элемента, А — массовое число,  атомный номер. Например,
атомный номер. Например,  означает атомное ядро гелия,
означает атомное ядро гелия,  — атомное ядро кислорода и т. п.
— атомное ядро кислорода и т. п.
На рис. 375 схематически изображены ядра атомов водорода  гелия
гелия  лития
лития  и бора
и бора  черными шариками представлены протоны, белыми — нейтроны.
черными шариками представлены протоны, белыми — нейтроны.
Атомы, ядра которых состоят из одинакового числа протонов, но из различного числа нейтронов, называются изотопами.

Рис. 375
Так, например, у водорода имеется четыре изотопа: протий (легкий водород)  дейтерий (тяжелый водород)
дейтерий (тяжелый водород)  тритий (сверхтяжелый водород)
тритий (сверхтяжелый водород)  и недавно открытый четырехнуклонный водород, еще не получивший специального названия. Ядро протия (протон)
и недавно открытый четырехнуклонный водород, еще не получивший специального названия. Ядро протия (протон)  состоит из одного протона
состоит из одного протона  ядро дейтерия (дейтон)
ядро дейтерия (дейтон)  из протона и нейтрона
из протона и нейтрона  ядро трития (тритон)
ядро трития (тритон)  из протона и двух нейтронов
из протона и двух нейтронов  ядро четырехнуклонного водорода
ядро четырехнуклонного водорода  из протона и трех нейтронов
из протона и трех нейтронов  В соединении с кислородом дейтерий образует тяжелую воду
В соединении с кислородом дейтерий образует тяжелую воду  тритий — сверхтяжелую воду
тритий — сверхтяжелую воду 
Тяжелая вода всегда содержится в природной воде, правда, в очень небольшом количестве — примерно  может быть выделена из природной воды путем многократной перегонки или посредством электролиза (см. § 91). Сверхтяжелая вода встречается в совершенно ничтожных количествах (порядка
может быть выделена из природной воды путем многократной перегонки или посредством электролиза (см. § 91). Сверхтяжелая вода встречается в совершенно ничтожных количествах (порядка  в дождевой воде.
в дождевой воде.
Все изотопы одного химического элемента имеют одинаковое строение электронных оболочек. Поэтому у изотопов данного элемента одинаковы как химические свойства, так и те физические свойства, которые обусловлены главным образом структурой электронной оболочки, Что касается физических свойств, обусловленных структурой ядра (массовое число, плотность, радиоактивность и т. д.), то они заметно различаются. Понятно, что это различие наиболее отчетливо выражено у самых легких химических элементов.
Из периодической системы Менделеева (см. в начале книги) видно, что атомные массы некоторых элементов значительно отличаются от целых чисел. В 1919 г. английский физик Астон с помощью масс-спектрографа (см. § 102) установил, что такие элементы представляют собой смесь нескольких изотопов. Это является главной причиной нецелочисленности атомных масс элементов; другая причина, связанная с так называемым дефектом массы, будет рассмотрена в § 142.
В настоящее время установлено, что большинство химических элементов, встречающихся в природе, представляет собой смесь изотопов. В частности, природный водород состоит на 99,985% из протия и на 0,015% из дейтерия.
Согласно теории Я. И. Френкеля, атомное ядро можно уподобить капле жидкости (капельная модель ядра). Нуклоны, составляющие ядро, связаны между собой особыми силами притяжения — ядерными силами, подобно тому как молекулы в капле жидкости связаны между собой молекулярными силами сцепления.
Устойчивость атомных ядер большинства элементов говорит о том, что ядерные силы исключительно велики: они должны превышать значительные кулоновские силы отталкивания, действующие между протонами, расположенными очень близко друг от друга. Ядерные силы проявляются только на очень малых расстояниях — порядка  см. При незначительном увеличении расстояния между нуклонами ядерные силы уменьшаются до нуля и кулоновские силы разъединяют протоны (разрушают ядро).
см. При незначительном увеличении расстояния между нуклонами ядерные силы уменьшаются до нуля и кулоновские силы разъединяют протоны (разрушают ядро).
Ядерные силы являются силами особого рода — не гравитационными и не электрическими. Их природа и свойства изучены еще недостаточно. В настоящее время наиболее вероятной считается мезонная теория ядерных сил, согласно которой нуклоны взаимодействуют друг с другом путем обмена особыми элементарными частицами— мезонами (см. § 145).
Благодаря ядерным силам нуклоны столь тесно «упакованы» в ядре, что плотность  вещества в атомных ядрах оказывается колоссальной. Определим порядок величины этой плотности. Будем считать ядро шарообразным, имеющим радиус
вещества в атомных ядрах оказывается колоссальной. Определим порядок величины этой плотности. Будем считать ядро шарообразным, имеющим радиус

где А — число нуклонов в ядре (т. е. массовое число). Масса ядра равна сумме масс всех входящих в него нуклонов:  Тогда
Тогда

Таким образом,  ядерного вещества весил бы около четырехсот миллионов тонн (1), тогда как
ядерного вещества весил бы около четырехсот миллионов тонн (1), тогда как  одного из наиболее тяжелых химических
одного из наиболее тяжелых химических
элементов — платины — весит всего лишь 22,5 грамма. Это сопоставление указывает на чрезвычайную ажурность структуры атомов, молекул и макроскопических объектов (тел).
Наиболее устойчивыми являются ядра легких элементов, состоящие из приблизительно одинакового числа протонов и нейтронов. У самых тяжелых элементов (расположенных в периодической системе после свинца), ядра которых состоят из большого числа нуклонов (с преобладанием нейтронов), ядерные силы уже не обеспечивают устойчивости ядра. Такие ядра могут самопроизвольно распадаться, превращаясь в ядра более легких элементов. Это явление носит название естественной радиоактивности.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- Предисловие
- Введение
- § 1. Предмет физики. Связь физики с другими науками и производством
- § 2. О единицах измерения и размерности физических величин
- § 3. О некоторых математических понятиях и символах
- 1. Физические основы механики
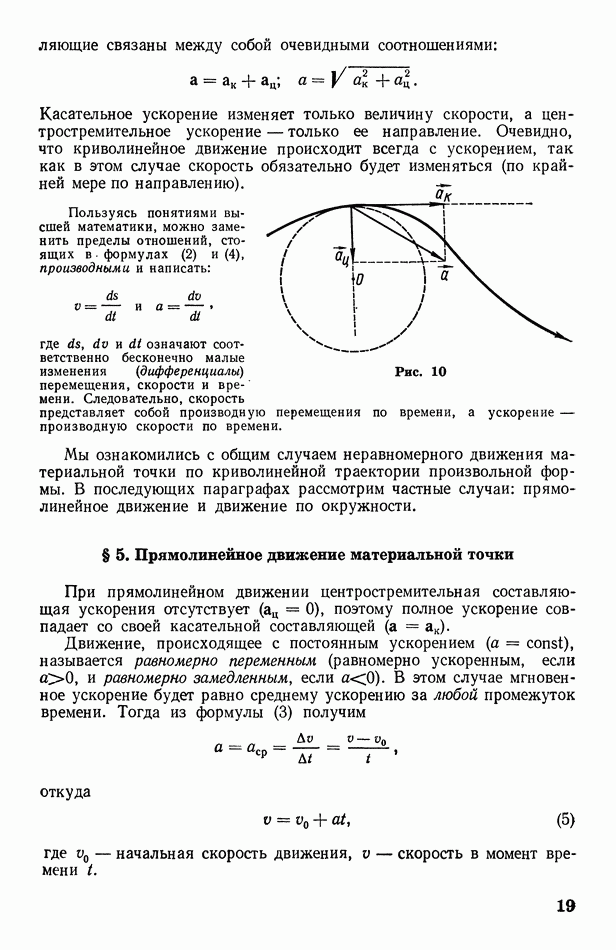
- § 4. Общий случай криволинейного движения материальной точки; основные характеристики движения
- § 5. Прямолинейное движение материальной точки
- § 6. Движение материальной точки по окружности
- Глава II. Основные законы динамики
- § 7. Законы Ньютона. Масса и сила
- § 8. Закон изменения количества движения (импульса)
- § 9. Закон сохранения количества движения в изолированной системе
- § 10. Силы упругости
- § 11. Силы трения
- § 12. Силы тяготения (гравитационные силы)
- § 13. Центростремительная сила
- § 14. Инерциальные и неинерциальные системы отсчета. Силы инерции
- § 15. Вес тел. Ускорение силы тяжести. Невесомость
- Глава III. Работа и энергия
- § 16. Работа и мощность
- § 17. Энергия
- § 18. Закон сохранения и превращения энергии
- § 19. О космических скоростях
- § 20. Границы применимости классической механики
- Глава IV. Вращательное движение твердого тела
- § 21. Основной закон динамики вращения
- § 22. Моменты инерции некоторых тел
- § 23. Закон сохранения момента количества движения. Кинетическая энергия вращающегося тела
- Глава V. Движение жидкости
- § 24. Основные определения. Уравнение неразрывности
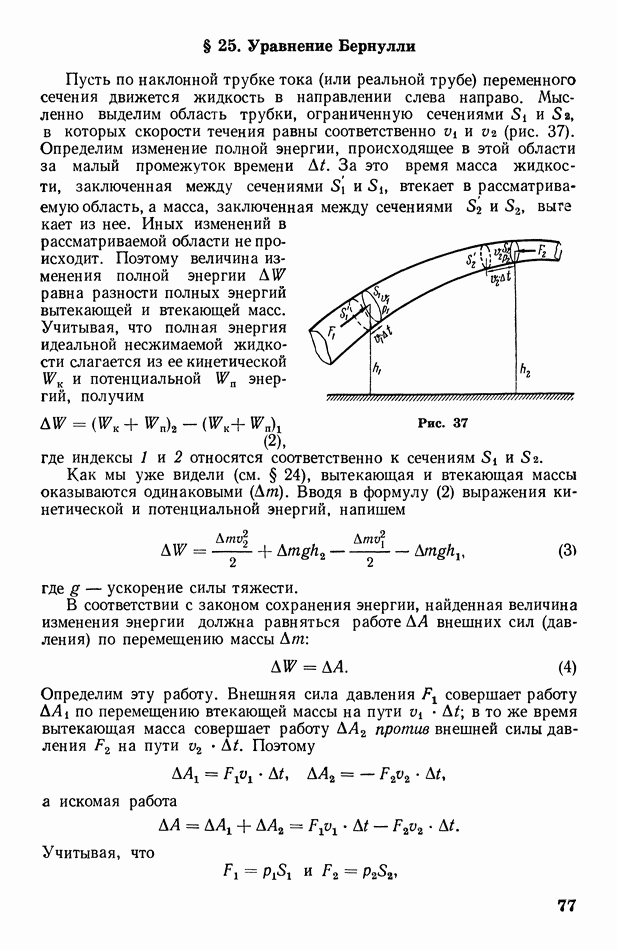
- § 25. Уравнение Бернулли
- § 26. О некоторых приложениях уравнения Бернулли
- Глава VI. Колебания и волны
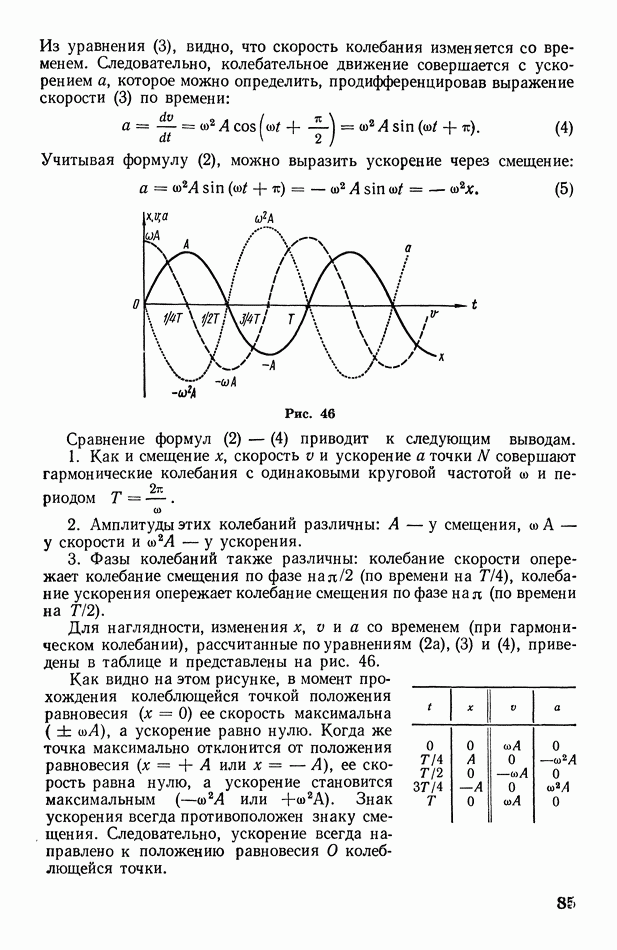
- § 27. Гармоническое колебание и его характеристики
- § 28. Сложение гармонических колебаний
- § 29. Динамика колебательного движения. Маятник
- § 30. О затухающих и вынужденных колебаниях
- § 31. Волновой процесс
- § 32. Уравнение волны. Интенсивность волны
- § 33. Интерференция волн. Стоячие волны
- § 34. Фронт волны. Принцип Гюйгенса-Френеля
- 2. Молекулярная физика и термодинамика
- § 35. Основные положения молекулярно-кинетической теории
- § 36. О некоторых явлениях, подтверждающих основные положения молекулярно-кинетической теории
- § 37. О теплоте и температуре
- § 38. О предмете и методах молекулярной физики
- Глава VIII. Газы
- § 39. Экспериментальные газовые законы: Бойля-Мариотта, Гей-Люссака, Дальтона, Авогадро. Абсолютная температура
- § 40. Уравнение Клапейрона — Менделеева. Универсальная газовая постоянная
- § 41. Основное уравнение кинетической теории идеального газа
- § 42. Средняя кинетическя энергия поступательного движения молекулы идеального газа
- § 43. О числе степеней свободы. Внутренняя энергия газа
- § 44. Теплоемкости газа. Физический смысл универсальной газовой постоянной
- § 45. Скорость поступательного движения молекул газа. Распределение числа молекул по скоростям
- § 46. Средняя длина свободного пробега молекул
- § 47. Явления переноса в газах. Уравнение переноса
- § 48. Диффузия
- § 49. Теплопроводность
- § 50. Внутреннее трение (вязкость)
- Глава IX. Жидкости и твердые тела
- § 51. Особенности строения жидкостей и твердых тел
- § 52. Деформация твердого тела
- § 53. Тепловое расширение твердых и жидких тел
- § 54. Теплоемкость твердых и жидких тел
- § 55. Диффузия в жидких и твердых телах
- § 56. Осмос
- § 57. Теплопроводность жидких и твердых тел
- § 58. Вязкость жидкости. Турбулентное движение жидкости
- § 59. Внутреннее давление в жидкости. Поверхностное натяжение и свободная энергия поверхности жидкости
- § 60. Дополнительное давление под искривленной поверхностью жидкости. Формула Лапласа
- § 61. Капиллярные явления; формула Жюрена
- Глава X. Изменение агрегатного состояния вещества (фазовые превращения)
- § 62. Понятие о фазовых превращениях и диаграмме состояний вещества
- § 63. Реальный газ. Уравнение Ван-дер-Ваальса
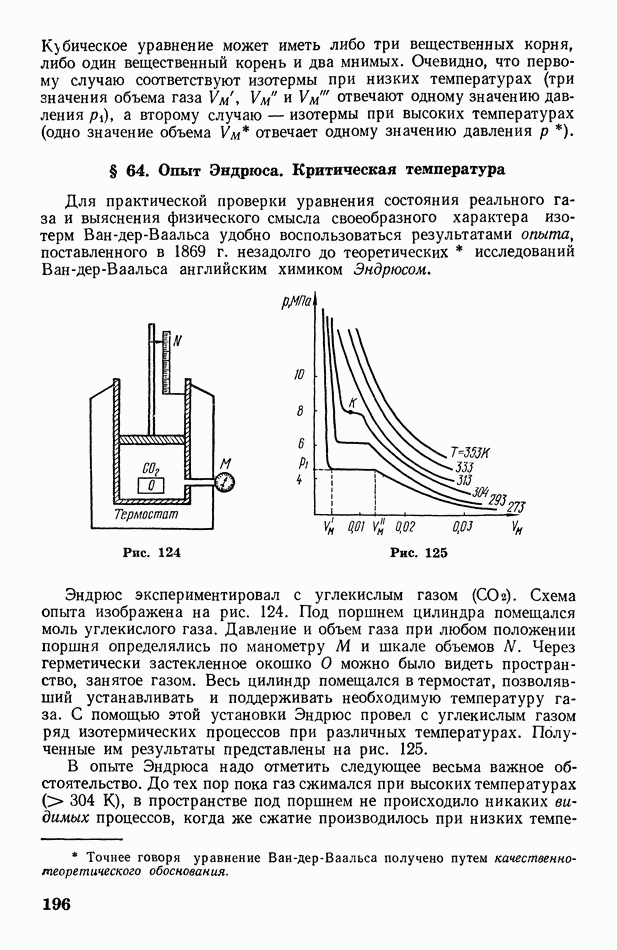
- § 64. Опыт Эндрюса. Критическая температура
- § 65. Сжижение газов. Эффект Джоуля-Томсона
- § 66. Испарение и конденсация. Кипение
- § 67. Упругость насыщенного пара над искривленной поверхностью жидкости и над раствором
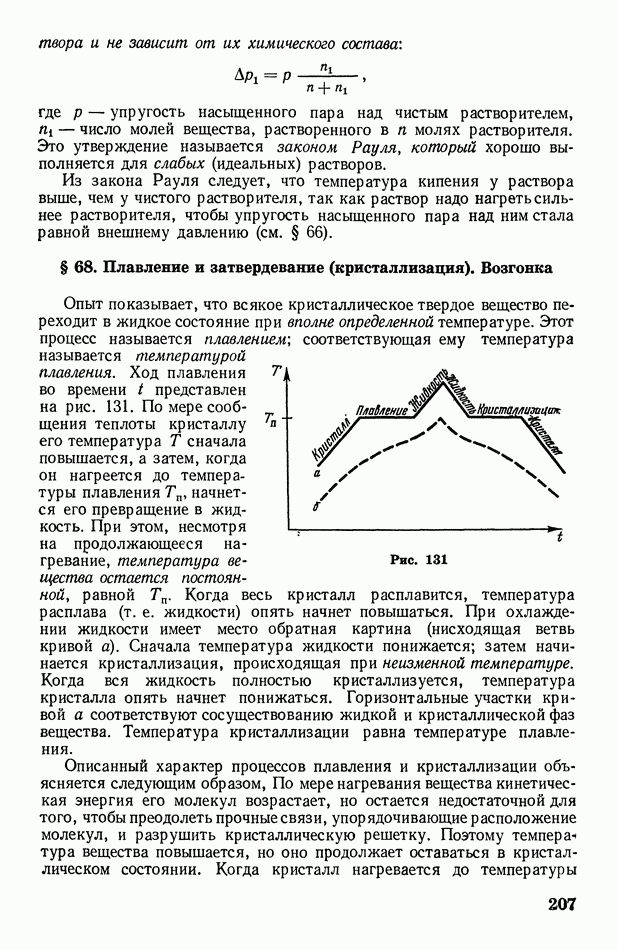
- § 68. Плавление и затвердевание (кристаллизация). Возгонка
- Глава XI. Основы термодинамики
- § 69. О некоторых общих понятиях термодинамики. Первое начало термодинамики
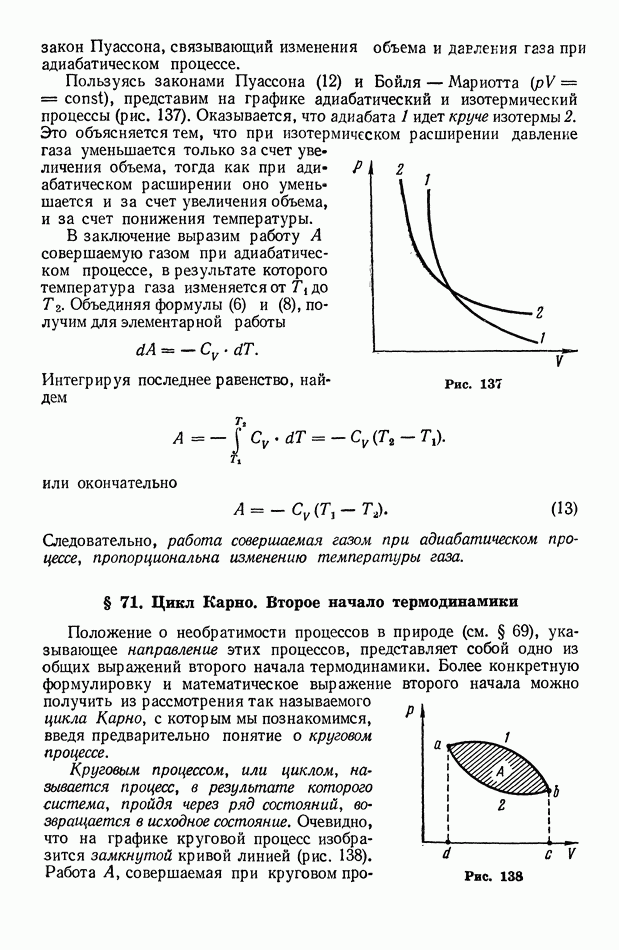
- § 70. Работа, совершаемая при изменении объема газа. Адиабатические процессы
- § 71. Цикл Карно. Второе начало термодинамики
- § 72. Энтропия
- § 73. О статистическом смысле энтропии и второго начала термодинамики
- 3. Электричество и магнетизм
- § 74. Электризация тел. Электрический заряд
- § 75. Взаимодействие электрических зарядов в вакууме. Электрическое поле и его напряженность
- § 76 Электрический диполь. Поле диполя
- § 77. Теорема Остроградского-Гаусса и ее приложения
- § 78. Работа перемещения заряда в электрическом поле. Потенциал
- § 79. О неустойчивости статических систем электрических зарядов
- § 80. Проводники в электрическом поле. Электроемкость. Энергия заряженного проводника
- § 81. Диэлектрики в электрическом поле. Поляризация диэлектриков
- § 82. Электрическое поле в диэлектрике. Диэлектрическая проницаемость. Вектор электрической индукции
- § 83. Конденсатор. Энергия электрического поля
- Глава XIII. Постоянный электрический ток
- § 84. Электрический ток. Сила тока. Электродвижущая сила. Напряжение
- § 85. Ток в металлических проводниках. Сопротивление. Законы Ома. Работа и мощность тока
- § 86. Разветвленная электрическая цепь. Правила Кирхгофа
- § 87. Контактная разность потенциалов. Термоэлектрические явления
- § 88. Эмиссия электронов. Термоэлектронная эмиссия. Электронные лампы
- § 89. Ток в полупроводниках. Собственная и примесная проводимости полупроводников
- § 90. Запирающий слой. Полупроводниковые выпрямители, усилители и термоэлектрические батареи
- § 91. Ток в жидкостях. Электролиз. Законы Фарадея
- § 92. Ток в газах. Несамостоятельный и самостоятельный газовые разряды
- § 93. Типы самостоятельного газового разряда
- Глава XIV. Электромагнетизм
- § 94. Постоянный магнит и круговой ток. Магнитные поля магнитов и токов
- § 95. Магнитное взаимодействие токов в вакууме; закон Ампера
- § 96. Напряженность магнитного поля. Формула Ампера. Закон Био-Савара-Лапласа
- § 97. Некоторые приложения закона Био-Савара-Лапласа
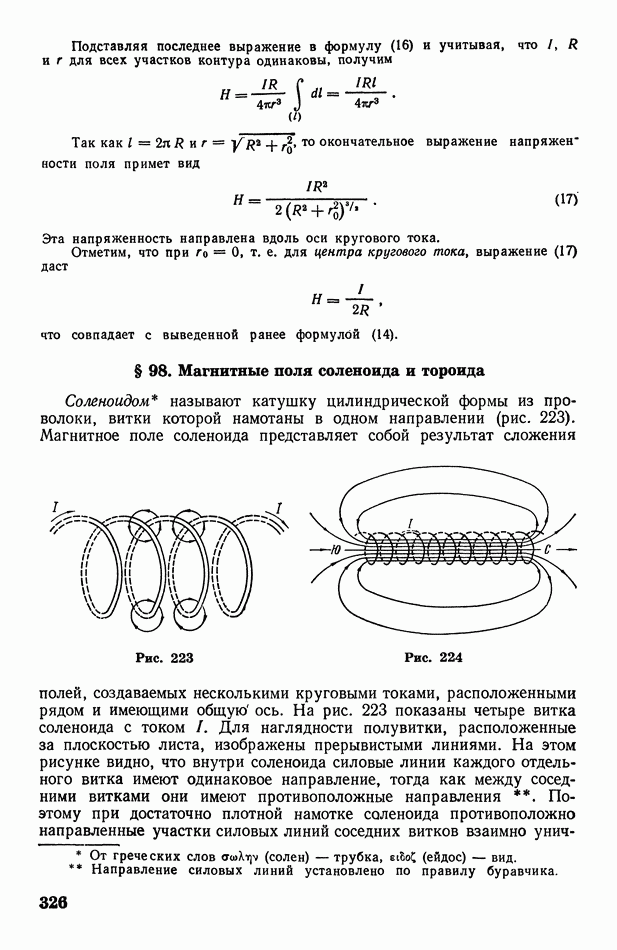
- § 98. Магнитные поля соленоида и тороида
- § 99. Диамагнитные, парамагнитные и ферромагнитные вещества. Магнитная проницаемость. Магнитная индукция. Поток магнитной индукции
- § 100. Действие магнитного поля на проводник с током. Определение ампера
- § 101. Движение заряженных частиц в электрическом и магнитном полях. Определение удельного заряда и массы электрона
- § 102. О некоторых приборах и установках, основанных на движении заряженных частиц в электрическом и магнитном полях
- Глава XV. Электромагнитная индукция и переменный ток
- § 103. Электромагнитная индукция. Закон Фарадея. Правило Ленца. Токи Фуко
- § 104. Взаимная индукция и самоиндукция
- § 105. Энергия магнитного поля. Понятие об электромагнитной теории Максвелла
- § 106. Контур, вращающийся в магнитном поле. Синусоидальный переменный ток. Работа и мощность переменного тока
- § 107. Емкостное и индуктивное сопротивления
- § 108. Обобщенный закон Ома. Электрический резонанс. Коэффициент мощности электрической цепи
- § 109. Понятие о трехфазном токе
- Глава XVI. Электрические колебания и электромагнитные волны
- § 110. Электромагнитные волны
- § 111. Закрытый колебательный контур
- § 112. Вибратор Герца. Автоколебательный контур. О диапазоне частот электромагнитных волн
- § 113. Радиосвязь
- 4. Оптика и атомная физика
- § 114. Природа света
- § 115. Отражение и преломление света. Полное отражение
- § 116. Дисперсия света. Спектры
- § 117. Тонкие линзы. Микроскоп
- § 118. Глаз как оптическая система. Спектральная чувствительность глаза
- § 119. Основные фотометрические характеристики
- § 120. Поглощение света. О физиологическом действии света
- Глава XVIII. Волновые свойства света
- § 121. Интерференция света. Интерферометр
- § 122. Об интерференции света, отраженного от прозрачных пленок
- § 123. Дифракция света. Разрешающая способность оптических приборов
- § 124. Дифракция от щелей. Дифракционные спектры. Дифракционная решетка. О рассеянии света в мутной среде
- § 125. Дифракция рентгеновских лучей. Формула Вульфа-Брэггов
- § 126. О дифракции микрочастиц и волнах де-Бройля
- § 127. Поляризация света. Естественный и поляризованный свет. Поляризация света в турмалине. Поляроиды
- § 128. Двойное лучепреломление. Поляризация света в исландском шпате. Призма Николя
- 129. Вращение плоскости колебаний поляризованного света. Поляриметр
- Глава XIX. Квантовые свойства света и строение атома
- § 130. Тепловое лучеиспускание и лучепоглощение. Абсолютно черное тело. Закон Кирхгофа
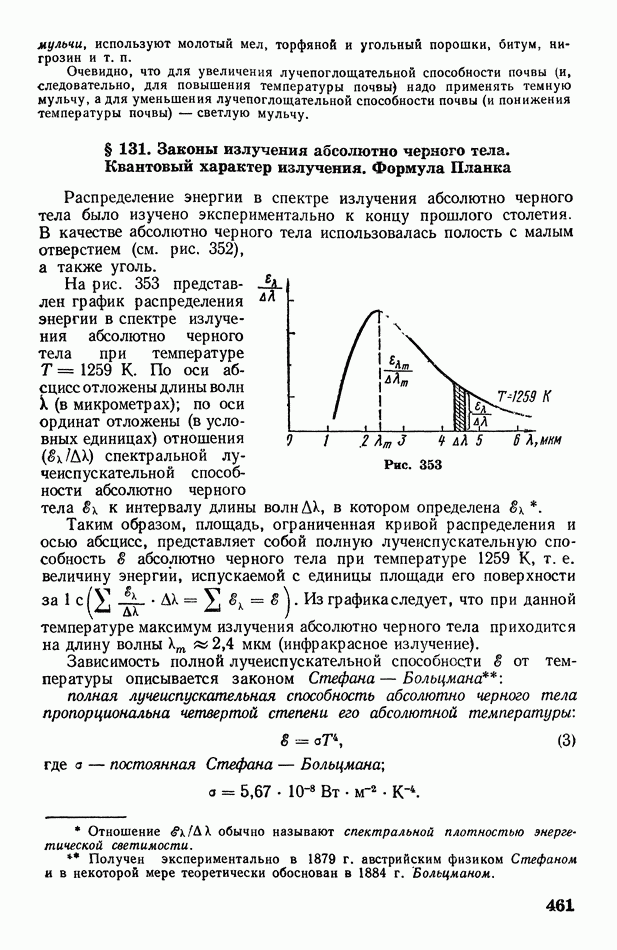
- § 131. Законы излучения абсолютно черного тела. Квантовый характер излучения. Формула Планка
- § 132. Строение атома (ядерная модель). Дискретность энергетических состояний атома. Постулаты Бора
- § 133. Квантовая теория строения атома водорода (по Бору). Объяснение спектров излучения и поглощения водорода
- § 134. Понятие о строении многоэлектронных атомов и образовании оптических и рентгеновских (характеристических) спектров
- § 135. Люминесценция. Законы фотолюминесценции и некоторые ее практические применения
- § 136. Фотоэффект. Законы фотоэффекта. Фотоэлементы
- § 137. Масса и импульс фотона. Световое давление. Эффект Комптона. Флуктуации света
- Глава XX. Атомное ядро и внутриядерные процессы
- § 138. Общие сведения об атомных ядрах. Изотопы
- § 139. Естественная радиоактивность. Альфа-, бета- и гамма-лучи. Законы радиоактивного распада
- § 140. О методах наблюдения и регистрации микрочастиц
- § 141. Ядерные реакции. Искусственная радиоактивность
- § 142. Энергия связи и дефект массы атомного ядра
- § 143. Реакция деления. Цепная реакция. Ядерный реактор
- § 144. Реакция синтеза (термоядерная реакция). Энергия звезд
- § 145. Космические лучи. Элементарные частицы
- § 146. Об использовании ядерной энергии