| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ 132. Строение атома (ядерная модель). Дискретность энергетических состояний атома. Постулаты Бора
К началу XX в. было с полной достоверностью установлено, что в состав каждого атома входят электроны. Вместе с тем было известно, что атом в целом электронейтрален. Отсюда следовало, что отрицательный заряд электронов должен компенсироваться положительным зарядом каких-то других частиц, также входящих в состав атома.
В 1911 г. английский физик Резерфорд предложил ядерную {планетарную) модель строения атома. Согласно этой модели, весь положительный заряд и почти вся масса  атома сосредоточены в атомном ядре, размер которого ничтожно мал (порядка
атома сосредоточены в атомном ядре, размер которого ничтожно мал (порядка  по сравнению с размером атома
по сравнению с размером атома  ). Вокруг ядра по замкнутым (эллиптическим) орбитам движутся электроны, образуя электронную оболочку атома. Заряд ядра равен по абсолютной величине суммарному заряду электронов.
). Вокруг ядра по замкнутым (эллиптическим) орбитам движутся электроны, образуя электронную оболочку атома. Заряд ядра равен по абсолютной величине суммарному заряду электронов.
Таким образом, атом в целом является чрезвычайно «ажурным» микрообразованием: совокупностью небольшого числа очень малых частиц вещества (ядра и электронов), распределенных в сравнительно очень большом объеме.
Предположение о вращении электронов вокруг ядра Резерфорд сделал в связи с тем, что, согласно теореме Ирншоу (см. § 79), атом в виде статической системы не может быть устойчивым.
Что касается предположения о наличии в центре атома одного массивного, но весьма малого ядра, то Резерфорд доказал это экспериментально на опытах с рассеянием альфа-частиц, проходящих через вещество. Альфа-частицы, испускаемые радиоактивными элементами, движутся со скоростью порядка  имеют положительный заряд, равный двум элементарным зарядам, и массу, в 7350 раз большую массы электрона (см. § 139).
имеют положительный заряд, равный двум элементарным зарядам, и массу, в 7350 раз большую массы электрона (см. § 139).

Рис. 355
Схема опытов Резерфорда показана на рис. 355;  -частицы, испускаемые радиоактивным веществом, двигались в вакууме и, проходя через фольгу
-частицы, испускаемые радиоактивным веществом, двигались в вакууме и, проходя через фольгу  (толщиной около 1 мкм), падали на люминесцирующий экран
(толщиной около 1 мкм), падали на люминесцирующий экран  Удар каждой
Удар каждой  -частицы об экран вызывал кратковременную вспышку — сцинтилляцию, наблюдаемую в микроскоп.
-частицы об экран вызывал кратковременную вспышку — сцинтилляцию, наблюдаемую в микроскоп.
Наблюдения показали, что большинство  -частиц проходит сквозь фольгу без заметного отклонения от первоначального направления, некоторые частицы отклоняются на небольшой угол и лишь немногие частицы претерпевают сильное отклонение.
-частиц проходит сквозь фольгу без заметного отклонения от первоначального направления, некоторые частицы отклоняются на небольшой угол и лишь немногие частицы претерпевают сильное отклонение.

Рис. 356
Естественно предположить, что отклонение  -частиц вызвано их взаимодействием («столкновением») с массивными атомными ядрами (рис. 356), поскольку легкие электроны не могут существенно изменить движение сравнительно тяжелых и очень быстрых
-частиц вызвано их взаимодействием («столкновением») с массивными атомными ядрами (рис. 356), поскольку легкие электроны не могут существенно изменить движение сравнительно тяжелых и очень быстрых  -частиц.
-частиц.
Из того факта, что значительное отклонение испытывают только немногие  -частицы, следует, что лишь некоторые из них проходят вблизи ядер; а это в свою очередь означает, что атомные ядра имеют малый размер и расположены в веществе фольги на очень больших расстояниях друг от друга.
-частицы, следует, что лишь некоторые из них проходят вблизи ядер; а это в свою очередь означает, что атомные ядра имеют малый размер и расположены в веществе фольги на очень больших расстояниях друг от друга.
Полагая, что ядро и  -частица взаимодействуют (отталкиваются) по закону Кулона, Резерфорд теоретически рассчитал картину рассеяния
-частица взаимодействуют (отталкиваются) по закону Кулона, Резерфорд теоретически рассчитал картину рассеяния  -частиц, получив результат, хорошо согласующийся с опытными данными.
-частиц, получив результат, хорошо согласующийся с опытными данными.
Исследования Резерфорда позволили определить порядок размера ядра  и величину его заряда. При этом оказалось, что заряд
и величину его заряда. При этом оказалось, что заряд  ядра, выраженный в элементарных зарядах
ядра, выраженный в элементарных зарядах  равен порядковому номеру
равен порядковому номеру  химического элемента в периодической системе Менделеева:
химического элемента в периодической системе Менделеева:

и вместе с тем равен числу электронов в электронной оболочке атома.
Однако резерфордовская модель строения атома не укладывалась в рамки законов классической физики. В самом деле, согласно законам классической электродинамики, электрон, вращаясь вокруг ядра (т. е. двигаясь с ускорением), должен непрерывно излучать электромагнитные волны, частота которых равна частоте вращения электрона. Так как это излучение сопровождается непрерывной потерей энергии, то электрон должен постепенно приближаться к ядру, двигаясь по спирали, и в конце концов упасть на ядро. По мере приближения электрона к ядру частота вращения электрона, а вместе с ней и частота электромагнитного излучения должны непрерывно изменяться. Следовательно, атом должен давать сплошной спектр излучения.
Таким образом, с точки зрения классической физики атом оказывается неустойчивой (недолговечной) системой, дающей сплошной спектр излучения. Между тем и то и другое противоречит опыту. В действительности атомы представляют собой весьма устойчивые образования, характеризующиеся линейчатым спектром излучения.
Тщательные исследования спектров излучения различных разреженных газов (т. е. спектров излучения атомов) показали, что каждому газу присущ вполне определенный линейчатый спектр. Более того, обнаружилось, что спектральные линии можно распределить по группам (сериям), линии, принадлежащие к одной серии, связаны между собой определенной закономерностью. Так, например, в видимой части спектра излучения водорода Бальмер обнаружил серию линий, частота которых выражается эмпирической формулой

где  постоянная Ридберга, равная
постоянная Ридберга, равная 

Рис. 357
Серия Бальмера схематически представлена на рис. 357. Над спектральными линиями проставлены соответствующие им значения длин волн X и частот  вычисленные по формуле (8). Первая слева линия На имеет ярко-красный цвет; в формуле Бальмера ей соответствует
вычисленные по формуле (8). Первая слева линия На имеет ярко-красный цвет; в формуле Бальмера ей соответствует  Линия — голубая
Линия — голубая  линия
линия  — синяя
— синяя 
 и линия
и линия  фиолетовая
фиолетовая  Остальные линии этой серии лежат в ультрафиолетовой части спектра.
Остальные линии этой серии лежат в ультрафиолетовой части спектра.
В спектре водорода имеется еще несколько серий, в частности серия, открытая в 1906 г. английским физиком Лайманом в ультрафиолетовой части спектра, и серия, открытая в 1908 г. немецким физиком Пашеном в инфракрасной части спектра. Серия Лаймана описывается формулой

где  серия Пашена — формулой
серия Пашена — формулой

где  Все сериальные эмпирические формулы имеют одинаковую структуру; причина этого сходства выяснена в следующем параграфе.
Все сериальные эмпирические формулы имеют одинаковую структуру; причина этого сходства выяснена в следующем параграфе.
Линейчатый характер спектров излучения (и поглощения) атомов говорит о том, что атом может излучать (и поглощать) энергию не в любых количествах (отличающихся друг от друга на сколь угодно малую величину), а только вполне определенными порциями — квантами. Отсюда следует, что атом может находиться лишь в определенных (дискретных) энергетических состояниях; переходя из одного состояния в другое, он излучает (или поглощает) квант энергии, равный разности энергий начального и конечного состояний (т. е. до излучения и после него).
Исходя из представления о дискретности энергетических состояний атома датский физик  Бор в 1913 г. усовершенствовал атомную модель Резерфорда, создав квантовую теорию строения атома. В ее основу положены следующие три постулата (постулаты Бора):
Бор в 1913 г. усовершенствовал атомную модель Резерфорда, создав квантовую теорию строения атома. В ее основу положены следующие три постулата (постулаты Бора):
1. Электроны могут двигаться в атоме не по любым орбитам, а только по орбитам вполне определенного радиуса.
На этих орбитах, называемых стационарными, или устойчивыми, момент количества движения электрона кратен величине 

где  масса электрона,
масса электрона,  его скорость;
его скорость;  радиус орбиты;
радиус орбиты;  целое число, называемое квантовым
целое число, называемое квантовым  постоянная Планка. Очевидно, что формула
постоянная Планка. Очевидно, что формула  является условием квантования радиуса орбит.
является условием квантования радиуса орбит.
2. Движение электронов по стационарным орбитам не сопровождается излучением (поглощением) энергии.
3. Переход электрона с одной стационарной орбиты на другую сопровождается излучением (или поглощением) кванта энергии.
Величина  этого кванта равна разности энергии
этого кванта равна разности энергии  стационарных состояний атома до и после излучения (поглощения):
стационарных состояний атома до и после излучения (поглощения):

Соотношение (12) называется условием частот.
Таким образом, частота электромагнитных волн, излучаемых атомом, определяется не частотой вращения электронов в атоме, а разностью энергии стационарных состояний атома.
Постулаты Бора, сохранив в основном модель атома Резерфорда, вместе с тем освободили ее от упомянутых ранее двух недостатков (противоречий опыту).
В настоящее время постулатам Бора придается более общая формулировка: атом устойчив только в состояниях, соответствующих определенным значениям энергии  переход атома из одного устойчивого состояния в другое сопровождается излучением или поглощением кванта энергии, величина которого определяется условием частот (12).
переход атома из одного устойчивого состояния в другое сопровождается излучением или поглощением кванта энергии, величина которого определяется условием частот (12).
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие
- Введение
- § 1. Предмет физики. Связь физики с другими науками и производством
- § 2. О единицах измерения и размерности физических величин
- § 3. О некоторых математических понятиях и символах
- 1. Физические основы механики
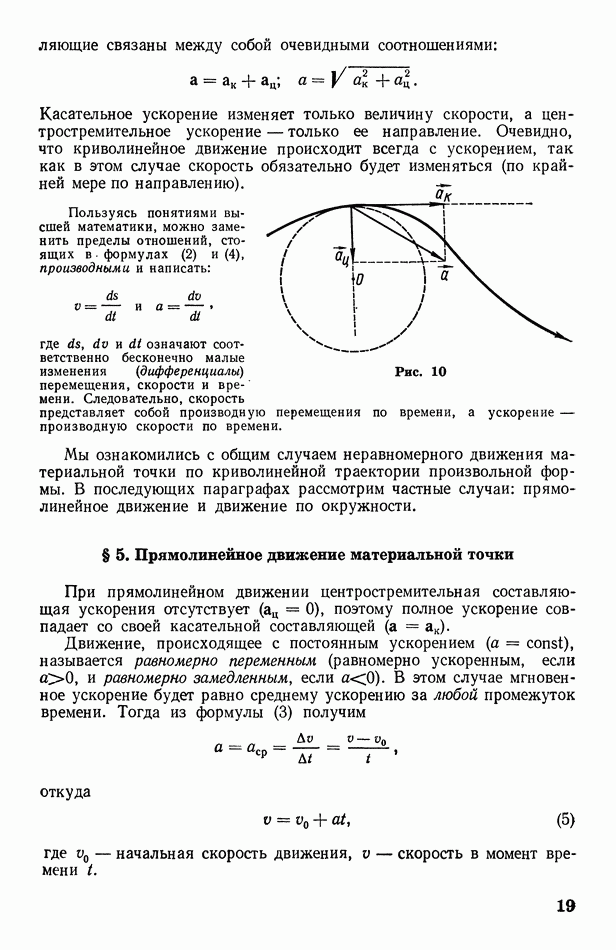
- § 4. Общий случай криволинейного движения материальной точки; основные характеристики движения
- § 5. Прямолинейное движение материальной точки
- § 6. Движение материальной точки по окружности
- Глава II. Основные законы динамики
- § 7. Законы Ньютона. Масса и сила
- § 8. Закон изменения количества движения (импульса)
- § 9. Закон сохранения количества движения в изолированной системе
- § 10. Силы упругости
- § 11. Силы трения
- § 12. Силы тяготения (гравитационные силы)
- § 13. Центростремительная сила
- § 14. Инерциальные и неинерциальные системы отсчета. Силы инерции
- § 15. Вес тел. Ускорение силы тяжести. Невесомость
- Глава III. Работа и энергия
- § 16. Работа и мощность
- § 17. Энергия
- § 18. Закон сохранения и превращения энергии
- § 19. О космических скоростях
- § 20. Границы применимости классической механики
- Глава IV. Вращательное движение твердого тела
- § 21. Основной закон динамики вращения
- § 22. Моменты инерции некоторых тел
- § 23. Закон сохранения момента количества движения. Кинетическая энергия вращающегося тела
- Глава V. Движение жидкости
- § 24. Основные определения. Уравнение неразрывности
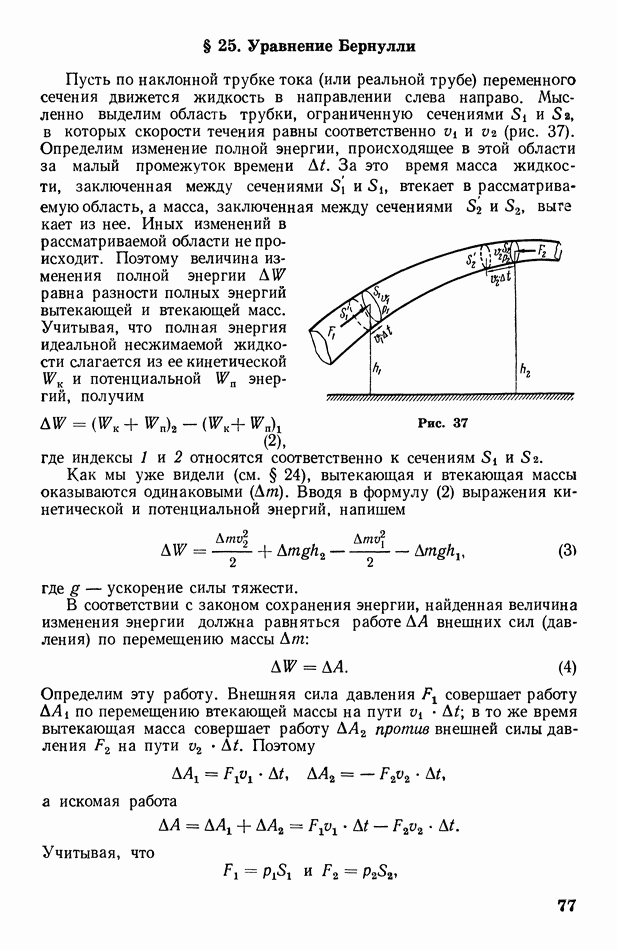
- § 25. Уравнение Бернулли
- § 26. О некоторых приложениях уравнения Бернулли
- Глава VI. Колебания и волны
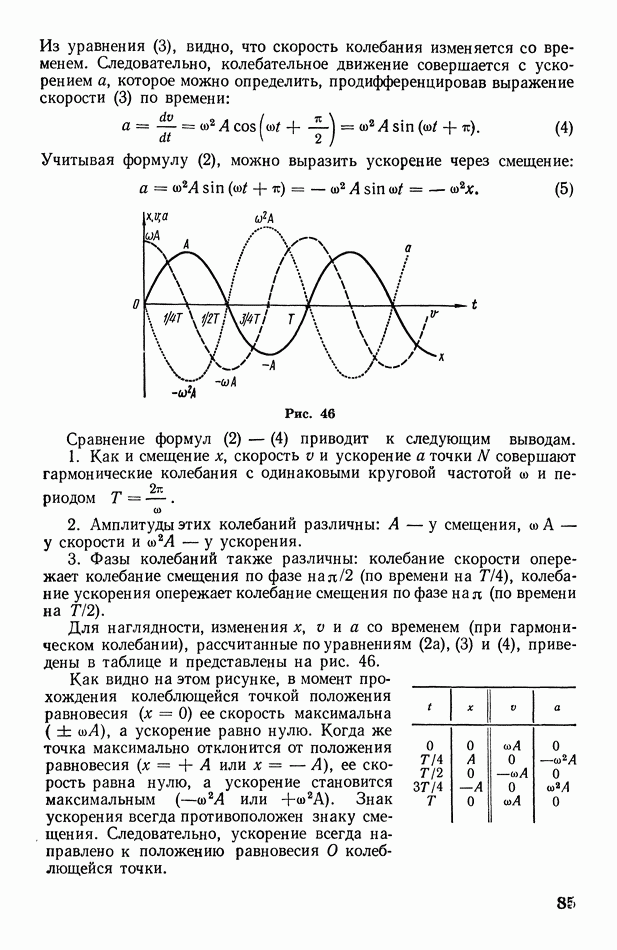
- § 27. Гармоническое колебание и его характеристики
- § 28. Сложение гармонических колебаний
- § 29. Динамика колебательного движения. Маятник
- § 30. О затухающих и вынужденных колебаниях
- § 31. Волновой процесс
- § 32. Уравнение волны. Интенсивность волны
- § 33. Интерференция волн. Стоячие волны
- § 34. Фронт волны. Принцип Гюйгенса-Френеля
- 2. Молекулярная физика и термодинамика
- § 35. Основные положения молекулярно-кинетической теории
- § 36. О некоторых явлениях, подтверждающих основные положения молекулярно-кинетической теории
- § 37. О теплоте и температуре
- § 38. О предмете и методах молекулярной физики
- Глава VIII. Газы
- § 39. Экспериментальные газовые законы: Бойля-Мариотта, Гей-Люссака, Дальтона, Авогадро. Абсолютная температура
- § 40. Уравнение Клапейрона — Менделеева. Универсальная газовая постоянная
- § 41. Основное уравнение кинетической теории идеального газа
- § 42. Средняя кинетическя энергия поступательного движения молекулы идеального газа
- § 43. О числе степеней свободы. Внутренняя энергия газа
- § 44. Теплоемкости газа. Физический смысл универсальной газовой постоянной
- § 45. Скорость поступательного движения молекул газа. Распределение числа молекул по скоростям
- § 46. Средняя длина свободного пробега молекул
- § 47. Явления переноса в газах. Уравнение переноса
- § 48. Диффузия
- § 49. Теплопроводность
- § 50. Внутреннее трение (вязкость)
- Глава IX. Жидкости и твердые тела
- § 51. Особенности строения жидкостей и твердых тел
- § 52. Деформация твердого тела
- § 53. Тепловое расширение твердых и жидких тел
- § 54. Теплоемкость твердых и жидких тел
- § 55. Диффузия в жидких и твердых телах
- § 56. Осмос
- § 57. Теплопроводность жидких и твердых тел
- § 58. Вязкость жидкости. Турбулентное движение жидкости
- § 59. Внутреннее давление в жидкости. Поверхностное натяжение и свободная энергия поверхности жидкости
- § 60. Дополнительное давление под искривленной поверхностью жидкости. Формула Лапласа
- § 61. Капиллярные явления; формула Жюрена
- Глава X. Изменение агрегатного состояния вещества (фазовые превращения)
- § 62. Понятие о фазовых превращениях и диаграмме состояний вещества
- § 63. Реальный газ. Уравнение Ван-дер-Ваальса
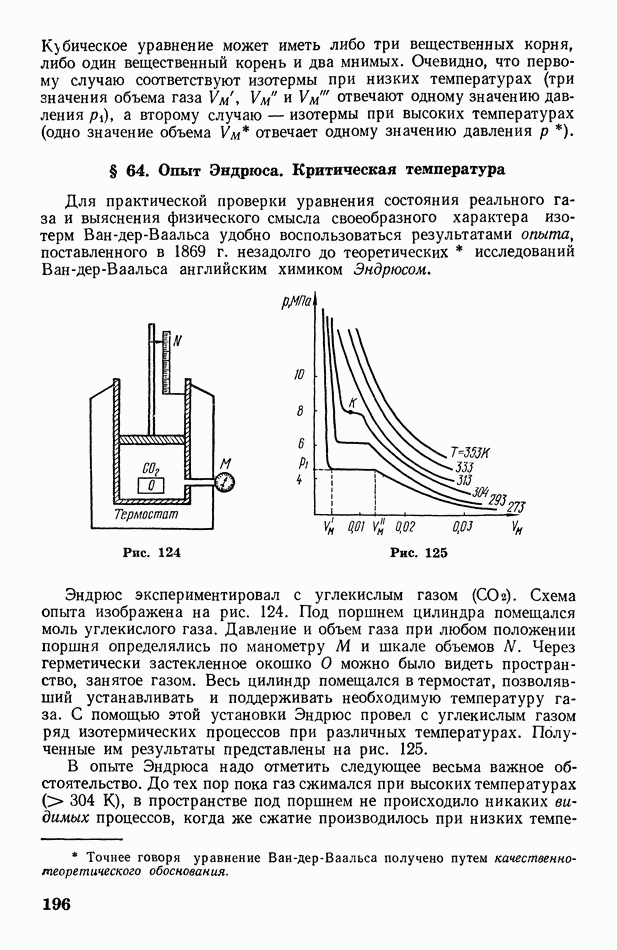
- § 64. Опыт Эндрюса. Критическая температура
- § 65. Сжижение газов. Эффект Джоуля-Томсона
- § 66. Испарение и конденсация. Кипение
- § 67. Упругость насыщенного пара над искривленной поверхностью жидкости и над раствором
- § 68. Плавление и затвердевание (кристаллизация). Возгонка
- Глава XI. Основы термодинамики
- § 69. О некоторых общих понятиях термодинамики. Первое начало термодинамики
- § 70. Работа, совершаемая при изменении объема газа. Адиабатические процессы
- § 71. Цикл Карно. Второе начало термодинамики
- § 72. Энтропия
- § 73. О статистическом смысле энтропии и второго начала термодинамики
- 3. Электричество и магнетизм
- § 74. Электризация тел. Электрический заряд
- § 75. Взаимодействие электрических зарядов в вакууме. Электрическое поле и его напряженность
- § 76 Электрический диполь. Поле диполя
- § 77. Теорема Остроградского-Гаусса и ее приложения
- § 78. Работа перемещения заряда в электрическом поле. Потенциал
- § 79. О неустойчивости статических систем электрических зарядов
- § 80. Проводники в электрическом поле. Электроемкость. Энергия заряженного проводника
- § 81. Диэлектрики в электрическом поле. Поляризация диэлектриков
- § 82. Электрическое поле в диэлектрике. Диэлектрическая проницаемость. Вектор электрической индукции
- § 83. Конденсатор. Энергия электрического поля
- Глава XIII. Постоянный электрический ток
- § 84. Электрический ток. Сила тока. Электродвижущая сила. Напряжение
- § 85. Ток в металлических проводниках. Сопротивление. Законы Ома. Работа и мощность тока
- § 86. Разветвленная электрическая цепь. Правила Кирхгофа
- § 87. Контактная разность потенциалов. Термоэлектрические явления
- § 88. Эмиссия электронов. Термоэлектронная эмиссия. Электронные лампы
- § 89. Ток в полупроводниках. Собственная и примесная проводимости полупроводников
- § 90. Запирающий слой. Полупроводниковые выпрямители, усилители и термоэлектрические батареи
- § 91. Ток в жидкостях. Электролиз. Законы Фарадея
- § 92. Ток в газах. Несамостоятельный и самостоятельный газовые разряды
- § 93. Типы самостоятельного газового разряда
- Глава XIV. Электромагнетизм
- § 94. Постоянный магнит и круговой ток. Магнитные поля магнитов и токов
- § 95. Магнитное взаимодействие токов в вакууме; закон Ампера
- § 96. Напряженность магнитного поля. Формула Ампера. Закон Био-Савара-Лапласа
- § 97. Некоторые приложения закона Био-Савара-Лапласа
- § 98. Магнитные поля соленоида и тороида
- § 99. Диамагнитные, парамагнитные и ферромагнитные вещества. Магнитная проницаемость. Магнитная индукция. Поток магнитной индукции
- § 100. Действие магнитного поля на проводник с током. Определение ампера
- § 101. Движение заряженных частиц в электрическом и магнитном полях. Определение удельного заряда и массы электрона
- § 102. О некоторых приборах и установках, основанных на движении заряженных частиц в электрическом и магнитном полях
- Глава XV. Электромагнитная индукция и переменный ток
- § 103. Электромагнитная индукция. Закон Фарадея. Правило Ленца. Токи Фуко
- § 104. Взаимная индукция и самоиндукция
- § 105. Энергия магнитного поля. Понятие об электромагнитной теории Максвелла
- § 106. Контур, вращающийся в магнитном поле. Синусоидальный переменный ток. Работа и мощность переменного тока
- § 107. Емкостное и индуктивное сопротивления
- § 108. Обобщенный закон Ома. Электрический резонанс. Коэффициент мощности электрической цепи
- § 109. Понятие о трехфазном токе
- Глава XVI. Электрические колебания и электромагнитные волны
- § 110. Электромагнитные волны
- § 111. Закрытый колебательный контур
- § 112. Вибратор Герца. Автоколебательный контур. О диапазоне частот электромагнитных волн
- § 113. Радиосвязь
- 4. Оптика и атомная физика
- § 114. Природа света
- § 115. Отражение и преломление света. Полное отражение
- § 116. Дисперсия света. Спектры
- § 117. Тонкие линзы. Микроскоп
- § 118. Глаз как оптическая система. Спектральная чувствительность глаза
- § 119. Основные фотометрические характеристики
- § 120. Поглощение света. О физиологическом действии света
- Глава XVIII. Волновые свойства света
- § 121. Интерференция света. Интерферометр
- § 122. Об интерференции света, отраженного от прозрачных пленок
- § 123. Дифракция света. Разрешающая способность оптических приборов
- § 124. Дифракция от щелей. Дифракционные спектры. Дифракционная решетка. О рассеянии света в мутной среде
- § 125. Дифракция рентгеновских лучей. Формула Вульфа-Брэггов
- § 126. О дифракции микрочастиц и волнах де-Бройля
- § 127. Поляризация света. Естественный и поляризованный свет. Поляризация света в турмалине. Поляроиды
- § 128. Двойное лучепреломление. Поляризация света в исландском шпате. Призма Николя
- 129. Вращение плоскости колебаний поляризованного света. Поляриметр
- Глава XIX. Квантовые свойства света и строение атома
- § 130. Тепловое лучеиспускание и лучепоглощение. Абсолютно черное тело. Закон Кирхгофа
- § 131. Законы излучения абсолютно черного тела. Квантовый характер излучения. Формула Планка
- § 132. Строение атома (ядерная модель). Дискретность энергетических состояний атома. Постулаты Бора
- § 133. Квантовая теория строения атома водорода (по Бору). Объяснение спектров излучения и поглощения водорода
- § 134. Понятие о строении многоэлектронных атомов и образовании оптических и рентгеновских (характеристических) спектров
- § 135. Люминесценция. Законы фотолюминесценции и некоторые ее практические применения
- § 136. Фотоэффект. Законы фотоэффекта. Фотоэлементы
- § 137. Масса и импульс фотона. Световое давление. Эффект Комптона. Флуктуации света
- Глава XX. Атомное ядро и внутриядерные процессы
- § 138. Общие сведения об атомных ядрах. Изотопы
- § 139. Естественная радиоактивность. Альфа-, бета- и гамма-лучи. Законы радиоактивного распада
- § 140. О методах наблюдения и регистрации микрочастиц
- § 141. Ядерные реакции. Искусственная радиоактивность
- § 142. Энергия связи и дефект массы атомного ядра
- § 143. Реакция деления. Цепная реакция. Ядерный реактор
- § 144. Реакция синтеза (термоядерная реакция). Энергия звезд
- § 145. Космические лучи. Элементарные частицы
- § 146. Об использовании ядерной энергии