| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
2. Молекулярная физика и термодинамика
Глава VII. Общие сведения о строении вещества
§ 35. Основные положения молекулярно-кинетической теории
Представление о том, что все тела построены из мельчайших частиц — атомов, возникло еще в глубокой древности и было достаточно отчетливо высказано греческим философом Демокритом (V в. до н. э.). Однако в дальнейшем эти атомистические воззрения были забыты и возрождены лишь во второй половине XVII в. Бойлем, а затем в XVIII—XIX вв. разработаны Ломоносовым, Дальтоном, Кренигом, Больцманом, Максвеллом и другими в качестве научной теории, получившей название классической молекулярно-кинетической теории. Эта теория основана на следующих положениях.
1. Все вещества состоят из очень маленьких отдельных частиц — молекул. Молекулы, образующие данное вещество, совершенно одинаковы; различные же вещества состоят их различных молекул. В соответствии с чрезвычайным многообразием встречающихся в природе веществ существует и чрезвычайно большое количество различных видов молекул.
Молекулы в свою очередь состоят из еще более мелких частиц — атомов. Число различных атомов сравнительно невелико и равно числу химических элементов и их изотопов. Различные комбинации из этих немногочисленных атомов и создают все множество видов молекул.
Атомы также не являются пределом делимости вещества, а представляют собой весьма сложные образования, состоящие из электрически положительно заряженного ядра, окруженного отрицательно заряженной электронной оболочкой. Однако классическая молекулярно-кинетическая теория не касается вопроса о строении атомов, рассматривая их упрощенно как твердые частички сферической формы.
Размеры (диаметры) атомов и молекул имеют в среднем порядок  см. Это означает, что десять миллионов молекул, уложенные, вплотную друг к другу вдоль прямой линии, составят молекулярную цепочку длиной всего лишь в
см. Это означает, что десять миллионов молекул, уложенные, вплотную друг к другу вдоль прямой линии, составят молекулярную цепочку длиной всего лишь в  Очевидно, что при столь малом размере атомов и молекул число их в физическом теле должно быть колоссальным. Действительно, например, в одной капле
Очевидно, что при столь малом размере атомов и молекул число их в физическом теле должно быть колоссальным. Действительно, например, в одной капле
воды содержится около  молекул. Молекулярная цепочка, составленная из такого количества молекул, имела бы длину в 300 млн. км, что в 800 раз превышает расстояние между Землей и Луной.
молекул. Молекулярная цепочка, составленная из такого количества молекул, имела бы длину в 300 млн. км, что в 800 раз превышает расстояние между Землей и Луной.
2. Между молекулами тела одновременно действуют силы взаимного притяжения (сцепления) и силы взаимного отталкивания. При этом силы отталкивания должны убывать с увеличением расстояния быстрее, чем силы сцепления.

Рис. 67
Только при этом условии молекулы могут находиться в устойчивом равновесии на некотором определенном расстоянии друг от друга (на котором силы сцепления равны силам отталкивания). Действительно, если под влиянием каких-либо причин молекулы сблизятся на расстояние, меньшее равновесного (т. е. соответствующего устойчивому равновесию), то силы отталкивания начнут преобладать над силами притяжения и восстановят равновесное расстояние между молекулами. Наоборот, если под влиянием каких-либо причин молекулы разойдутся на расстояние, большее равновесного, то начнут преобладать силы сцепления и сблизят молекулы на расстояние, соответствующее равновесному.
Согласно экспериментальным и теоретическим исследованиям, межмолекулярные силы взаимодействия  обратно пропорциональны
обратно пропорциональны  степени расстояния
степени расстояния  между молекулами:
между молекулами:

где для сил притяжения  а для сил отталкивания
а для сил отталкивания  принимает значения от 9 до 15. Таким образом, действительно, эти силы очень быстро убывают с увеличением расстояния между молекулами, причем особенно быстро убывают силы отталкивания.
принимает значения от 9 до 15. Таким образом, действительно, эти силы очень быстро убывают с увеличением расстояния между молекулами, причем особенно быстро убывают силы отталкивания.
На рис. 67, а представлен примерный характер взаимодействия молекул в зависимости от расстояния между ними. По оси абсцисс отложены расстояния  по оси ординат — величины сил отталкивания
по оси ординат — величины сил отталкивания  и сил притяжения
и сил притяжения  между молекулами, а также результирующей
между молекулами, а также результирующей  этих сил. Причем силы отталкивания приняты положительными, а
этих сил. Причем силы отталкивания приняты положительными, а
силы притяжения — отрицательными. Таким образом, для каждого расстояния  результирующая
результирующая  и положительные ее значения соответствуют отталкиванию, а отрицательные — притяжению между молекулами.
и положительные ее значения соответствуют отталкиванию, а отрицательные — притяжению между молекулами.
Очевидно, что равновесное расстояние  между молекулами составляет около
между молекулами составляет около  см, так как на этом расстоянии
см, так как на этом расстоянии  При
При  см преобладают силы отталкивания
см преобладают силы отталкивания  а при
а при  см преобладают силы притяжения
см преобладают силы притяжения  На расстоянии
На расстоянии  см межмолекулярные силы практически перестают действовать
см межмолекулярные силы практически перестают действовать  Таким образом, силы межмолекулярного взаимодействия проявляются на расстояниях такого же порядка, как размер самих молекул.
Таким образом, силы межмолекулярного взаимодействия проявляются на расстояниях такого же порядка, как размер самих молекул.
Установим теперь примерный характер зависимости потенциальной энергии взаимодействия молекул  от расстояния между ними. Потенциальную энергию тяготеющих тел, находящихся на бесконеч ном расстоянии друг от друга, мы условились считать равной нулю (см. § 17). Поэтому при
от расстояния между ними. Потенциальную энергию тяготеющих тел, находящихся на бесконеч ном расстоянии друг от друга, мы условились считать равной нулю (см. § 17). Поэтому при  будет
будет  Если молекулы окажутся на расстоянии
Если молекулы окажутся на расстоянии  см друг от друга, то они начнут сближаться за счет работы силы притяжения, а потенциальная энергия молекул будет при этом уменьшаться и достигнет минимального значения
см друг от друга, то они начнут сближаться за счет работы силы притяжения, а потенциальная энергия молекул будет при этом уменьшаться и достигнет минимального значения  Дальнейшее сближение молекул возможно только за счет работы, совершаемой против сил отталкивания. При этом потенциальная энергия молекул начнет резко возрастать. В результате кривая потенциальной энергии взаимодействия молекул (рис. 67, б) будет иметь минимум при
Дальнейшее сближение молекул возможно только за счет работы, совершаемой против сил отталкивания. При этом потенциальная энергия молекул начнет резко возрастать. В результате кривая потенциальной энергии взаимодействия молекул (рис. 67, б) будет иметь минимум при  Следовательно, положение устойчивого равновесия молекул соответствует минимуму их потенциальной энергии.
Следовательно, положение устойчивого равновесия молекул соответствует минимуму их потенциальной энергии.
График зависимости потенциальной энергии взаимодействия молекул от расстояния между ними называют потенциальной кривой, участок  этой кривой принято называть потенциальной ямой, точку В — дном потенциальной ямы, а ординату
этой кривой принято называть потенциальной ямой, точку В — дном потенциальной ямы, а ординату  глубиной потенциальной ямы.
глубиной потенциальной ямы.
Силы межмолекулярного взаимодействия имеют электрическую природу, обусловленную тем, что молекулы состоят из электрически заряженных частиц (положительных — атомных ядер и отрицательных — электронов), которым, как известно, свойственно взаимодействие (притяжение — для разноименно заряженных и отталкивание — для одноименно заряженных частиц).
Правда, в целом молекула электрически нейтральна. Однако заряды в молекуле расположены (или располагаются в процессе ее сближения с другой молекулой) не вполне симметрично. Благодаря этому молекулы оказываются полярными, подобными электрическим диполям (см. § 76); между их разноименно заряженными «полюсами» возникают силы притяжения, преобладающие над силами отталкивания одноименно заряженных «полюсов». Если же молекулы очень близко подойдут друг к другу, то решающую роль в их взаимодействии начинают уже играть силы отталкивания между сблизившимися электронными оболочками атомов, составляющих эти молекулы.
3. Молекулы, образующие тело, находятся в состоянии непрерывного беспорядочного движения. При этом они сталкиваются друг с другом и изменяют свою скорость как по направлению, так и по величине. Правда, столкновения в обычном смысле этого слова не происходит, так
как соприкосновению молекул препятствуют резко возрастающие при их сближении силы отталкивания. Однако действие этих сил приводит к тому же результату, что и при обычном столкновении, т. е. к отскакиванию сблизившихся молекул друг от друга.
Скорость движения молекул в теле связана с его температурой: чем больше эта скорость, тем выше температура тела. Таким образом, скорость движения молекул определяет тепловое состояние тела — величину его внутренней энергии; поэтому хаотическое движение молекул также называют тепловым движением. Под внутренней энергией тела подразумевают совокупность кинетической энергии молекул и атомов, образующих это тело, и потенциальной энергии их взаимодействия.
По мере увеличения интенсивности теплового движения среднее расстояние между молекулами возрастает, а сглы сцепления уменьшаются. Этому процессу соответствует переход тела из твердого состояния  жидкое, При достаточно интенсивном тепловом движении среднее расстояние между молекулами может стать настолько большим
жидкое, При достаточно интенсивном тепловом движении среднее расстояние между молекулами может стать настолько большим  , что силы сцепления между ними практически перестанут действовать. При этом тело перейдет в газоофазное состояние. Таким образом, от интенсивности теплового движения молекул и от внешних условий зависит, в каком из трех возможных агрегатных состояний находится вещество: твердом, жидком или газообразном.
, что силы сцепления между ними практически перестанут действовать. При этом тело перейдет в газоофазное состояние. Таким образом, от интенсивности теплового движения молекул и от внешних условий зависит, в каком из трех возможных агрегатных состояний находится вещество: твердом, жидком или газообразном.
Изложенные ранее основные положения молекулярно-кинетической теории подтверждаются многочисленными опытными фактами и физическими явлениями; некоторые из них будут рассмотрены в следующем параграфе.
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие
- Введение
- § 1. Предмет физики. Связь физики с другими науками и производством
- § 2. О единицах измерения и размерности физических величин
- § 3. О некоторых математических понятиях и символах
- 1. Физические основы механики
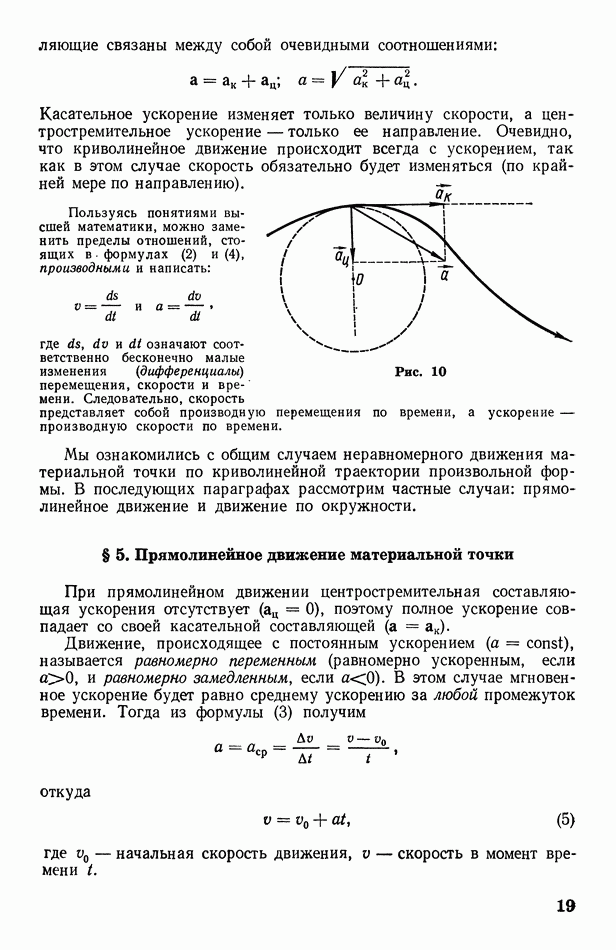
- § 4. Общий случай криволинейного движения материальной точки; основные характеристики движения
- § 5. Прямолинейное движение материальной точки
- § 6. Движение материальной точки по окружности
- Глава II. Основные законы динамики
- § 7. Законы Ньютона. Масса и сила
- § 8. Закон изменения количества движения (импульса)
- § 9. Закон сохранения количества движения в изолированной системе
- § 10. Силы упругости
- § 11. Силы трения
- § 12. Силы тяготения (гравитационные силы)
- § 13. Центростремительная сила
- § 14. Инерциальные и неинерциальные системы отсчета. Силы инерции
- § 15. Вес тел. Ускорение силы тяжести. Невесомость
- Глава III. Работа и энергия
- § 16. Работа и мощность
- § 17. Энергия
- § 18. Закон сохранения и превращения энергии
- § 19. О космических скоростях
- § 20. Границы применимости классической механики
- Глава IV. Вращательное движение твердого тела
- § 21. Основной закон динамики вращения
- § 22. Моменты инерции некоторых тел
- § 23. Закон сохранения момента количества движения. Кинетическая энергия вращающегося тела
- Глава V. Движение жидкости
- § 24. Основные определения. Уравнение неразрывности
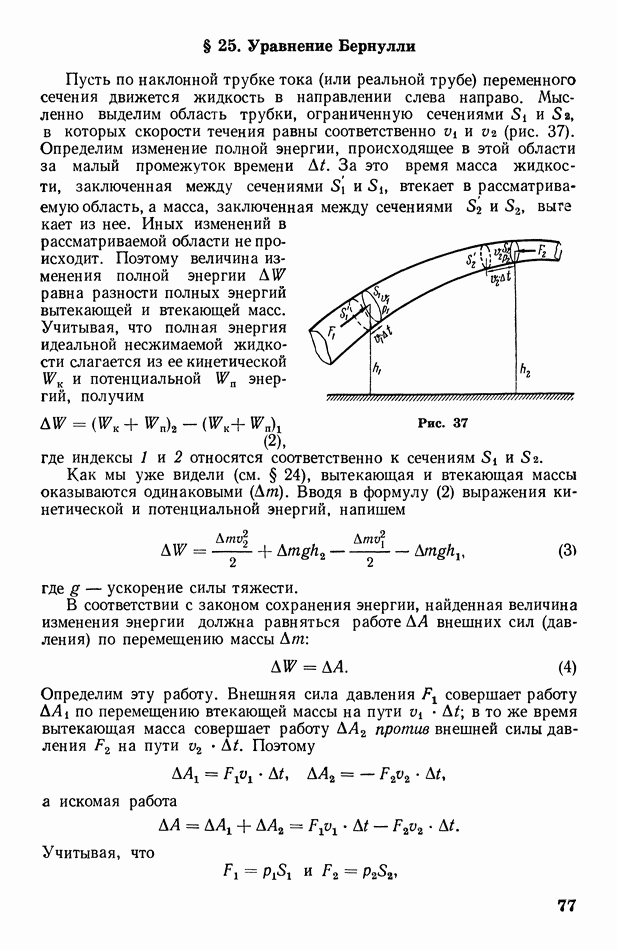
- § 25. Уравнение Бернулли
- § 26. О некоторых приложениях уравнения Бернулли
- Глава VI. Колебания и волны
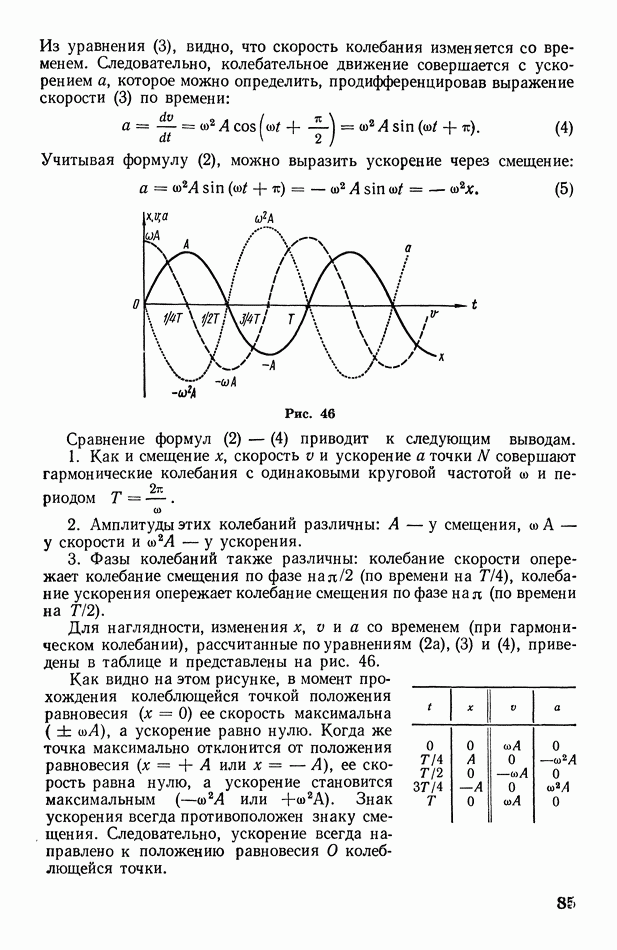
- § 27. Гармоническое колебание и его характеристики
- § 28. Сложение гармонических колебаний
- § 29. Динамика колебательного движения. Маятник
- § 30. О затухающих и вынужденных колебаниях
- § 31. Волновой процесс
- § 32. Уравнение волны. Интенсивность волны
- § 33. Интерференция волн. Стоячие волны
- § 34. Фронт волны. Принцип Гюйгенса-Френеля
- 2. Молекулярная физика и термодинамика
- § 35. Основные положения молекулярно-кинетической теории
- § 36. О некоторых явлениях, подтверждающих основные положения молекулярно-кинетической теории
- § 37. О теплоте и температуре
- § 38. О предмете и методах молекулярной физики
- Глава VIII. Газы
- § 39. Экспериментальные газовые законы: Бойля-Мариотта, Гей-Люссака, Дальтона, Авогадро. Абсолютная температура
- § 40. Уравнение Клапейрона — Менделеева. Универсальная газовая постоянная
- § 41. Основное уравнение кинетической теории идеального газа
- § 42. Средняя кинетическя энергия поступательного движения молекулы идеального газа
- § 43. О числе степеней свободы. Внутренняя энергия газа
- § 44. Теплоемкости газа. Физический смысл универсальной газовой постоянной
- § 45. Скорость поступательного движения молекул газа. Распределение числа молекул по скоростям
- § 46. Средняя длина свободного пробега молекул
- § 47. Явления переноса в газах. Уравнение переноса
- § 48. Диффузия
- § 49. Теплопроводность
- § 50. Внутреннее трение (вязкость)
- Глава IX. Жидкости и твердые тела
- § 51. Особенности строения жидкостей и твердых тел
- § 52. Деформация твердого тела
- § 53. Тепловое расширение твердых и жидких тел
- § 54. Теплоемкость твердых и жидких тел
- § 55. Диффузия в жидких и твердых телах
- § 56. Осмос
- § 57. Теплопроводность жидких и твердых тел
- § 58. Вязкость жидкости. Турбулентное движение жидкости
- § 59. Внутреннее давление в жидкости. Поверхностное натяжение и свободная энергия поверхности жидкости
- § 60. Дополнительное давление под искривленной поверхностью жидкости. Формула Лапласа
- § 61. Капиллярные явления; формула Жюрена
- Глава X. Изменение агрегатного состояния вещества (фазовые превращения)
- § 62. Понятие о фазовых превращениях и диаграмме состояний вещества
- § 63. Реальный газ. Уравнение Ван-дер-Ваальса
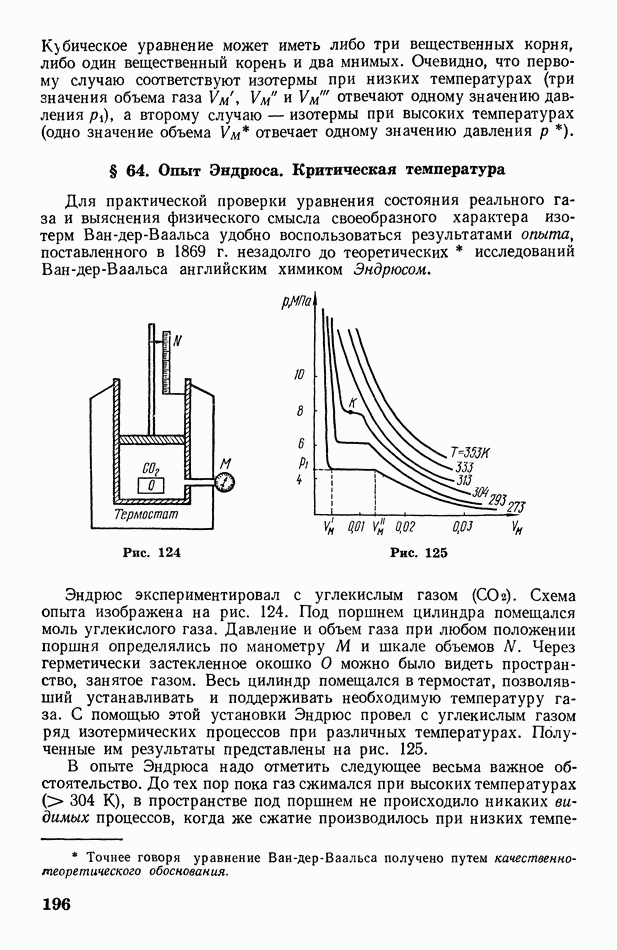
- § 64. Опыт Эндрюса. Критическая температура
- § 65. Сжижение газов. Эффект Джоуля-Томсона
- § 66. Испарение и конденсация. Кипение
- § 67. Упругость насыщенного пара над искривленной поверхностью жидкости и над раствором
- § 68. Плавление и затвердевание (кристаллизация). Возгонка
- Глава XI. Основы термодинамики
- § 69. О некоторых общих понятиях термодинамики. Первое начало термодинамики
- § 70. Работа, совершаемая при изменении объема газа. Адиабатические процессы
- § 71. Цикл Карно. Второе начало термодинамики
- § 72. Энтропия
- § 73. О статистическом смысле энтропии и второго начала термодинамики
- 3. Электричество и магнетизм
- § 74. Электризация тел. Электрический заряд
- § 75. Взаимодействие электрических зарядов в вакууме. Электрическое поле и его напряженность
- § 76 Электрический диполь. Поле диполя
- § 77. Теорема Остроградского-Гаусса и ее приложения
- § 78. Работа перемещения заряда в электрическом поле. Потенциал
- § 79. О неустойчивости статических систем электрических зарядов
- § 80. Проводники в электрическом поле. Электроемкость. Энергия заряженного проводника
- § 81. Диэлектрики в электрическом поле. Поляризация диэлектриков
- § 82. Электрическое поле в диэлектрике. Диэлектрическая проницаемость. Вектор электрической индукции
- § 83. Конденсатор. Энергия электрического поля
- Глава XIII. Постоянный электрический ток
- § 84. Электрический ток. Сила тока. Электродвижущая сила. Напряжение
- § 85. Ток в металлических проводниках. Сопротивление. Законы Ома. Работа и мощность тока
- § 86. Разветвленная электрическая цепь. Правила Кирхгофа
- § 87. Контактная разность потенциалов. Термоэлектрические явления
- § 88. Эмиссия электронов. Термоэлектронная эмиссия. Электронные лампы
- § 89. Ток в полупроводниках. Собственная и примесная проводимости полупроводников
- § 90. Запирающий слой. Полупроводниковые выпрямители, усилители и термоэлектрические батареи
- § 91. Ток в жидкостях. Электролиз. Законы Фарадея
- § 92. Ток в газах. Несамостоятельный и самостоятельный газовые разряды
- § 93. Типы самостоятельного газового разряда
- Глава XIV. Электромагнетизм
- § 94. Постоянный магнит и круговой ток. Магнитные поля магнитов и токов
- § 95. Магнитное взаимодействие токов в вакууме; закон Ампера
- § 96. Напряженность магнитного поля. Формула Ампера. Закон Био-Савара-Лапласа
- § 97. Некоторые приложения закона Био-Савара-Лапласа
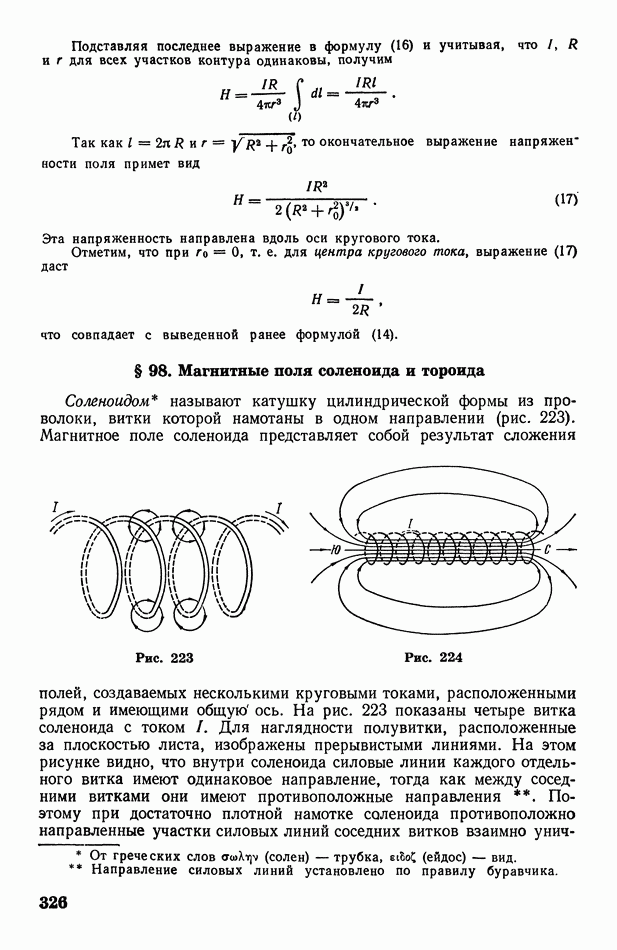
- § 98. Магнитные поля соленоида и тороида
- § 99. Диамагнитные, парамагнитные и ферромагнитные вещества. Магнитная проницаемость. Магнитная индукция. Поток магнитной индукции
- § 100. Действие магнитного поля на проводник с током. Определение ампера
- § 101. Движение заряженных частиц в электрическом и магнитном полях. Определение удельного заряда и массы электрона
- § 102. О некоторых приборах и установках, основанных на движении заряженных частиц в электрическом и магнитном полях
- Глава XV. Электромагнитная индукция и переменный ток
- § 103. Электромагнитная индукция. Закон Фарадея. Правило Ленца. Токи Фуко
- § 104. Взаимная индукция и самоиндукция
- § 105. Энергия магнитного поля. Понятие об электромагнитной теории Максвелла
- § 106. Контур, вращающийся в магнитном поле. Синусоидальный переменный ток. Работа и мощность переменного тока
- § 107. Емкостное и индуктивное сопротивления
- § 108. Обобщенный закон Ома. Электрический резонанс. Коэффициент мощности электрической цепи
- § 109. Понятие о трехфазном токе
- Глава XVI. Электрические колебания и электромагнитные волны
- § 110. Электромагнитные волны
- § 111. Закрытый колебательный контур
- § 112. Вибратор Герца. Автоколебательный контур. О диапазоне частот электромагнитных волн
- § 113. Радиосвязь
- 4. Оптика и атомная физика
- § 114. Природа света
- § 115. Отражение и преломление света. Полное отражение
- § 116. Дисперсия света. Спектры
- § 117. Тонкие линзы. Микроскоп
- § 118. Глаз как оптическая система. Спектральная чувствительность глаза
- § 119. Основные фотометрические характеристики
- § 120. Поглощение света. О физиологическом действии света
- Глава XVIII. Волновые свойства света
- § 121. Интерференция света. Интерферометр
- § 122. Об интерференции света, отраженного от прозрачных пленок
- § 123. Дифракция света. Разрешающая способность оптических приборов
- § 124. Дифракция от щелей. Дифракционные спектры. Дифракционная решетка. О рассеянии света в мутной среде
- § 125. Дифракция рентгеновских лучей. Формула Вульфа-Брэггов
- § 126. О дифракции микрочастиц и волнах де-Бройля
- § 127. Поляризация света. Естественный и поляризованный свет. Поляризация света в турмалине. Поляроиды
- § 128. Двойное лучепреломление. Поляризация света в исландском шпате. Призма Николя
- 129. Вращение плоскости колебаний поляризованного света. Поляриметр
- Глава XIX. Квантовые свойства света и строение атома
- § 130. Тепловое лучеиспускание и лучепоглощение. Абсолютно черное тело. Закон Кирхгофа
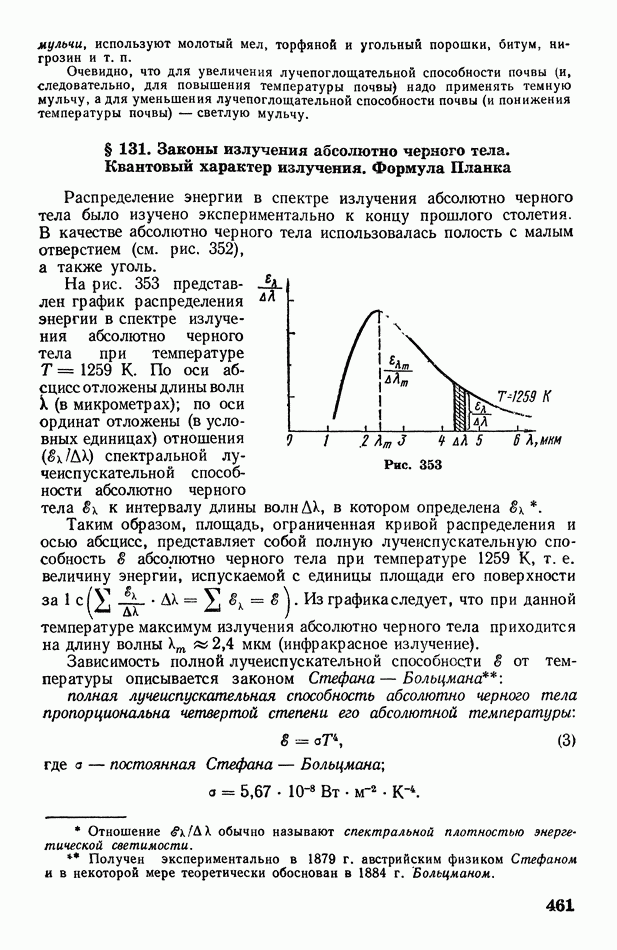
- § 131. Законы излучения абсолютно черного тела. Квантовый характер излучения. Формула Планка
- § 132. Строение атома (ядерная модель). Дискретность энергетических состояний атома. Постулаты Бора
- § 133. Квантовая теория строения атома водорода (по Бору). Объяснение спектров излучения и поглощения водорода
- § 134. Понятие о строении многоэлектронных атомов и образовании оптических и рентгеновских (характеристических) спектров
- § 135. Люминесценция. Законы фотолюминесценции и некоторые ее практические применения
- § 136. Фотоэффект. Законы фотоэффекта. Фотоэлементы
- § 137. Масса и импульс фотона. Световое давление. Эффект Комптона. Флуктуации света
- Глава XX. Атомное ядро и внутриядерные процессы
- § 138. Общие сведения об атомных ядрах. Изотопы
- § 139. Естественная радиоактивность. Альфа-, бета- и гамма-лучи. Законы радиоактивного распада
- § 140. О методах наблюдения и регистрации микрочастиц
- § 141. Ядерные реакции. Искусственная радиоактивность
- § 142. Энергия связи и дефект массы атомного ядра
- § 143. Реакция деления. Цепная реакция. Ядерный реактор
- § 144. Реакция синтеза (термоядерная реакция). Энергия звезд
- § 145. Космические лучи. Элементарные частицы
- § 146. Об использовании ядерной энергии