| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
§ 32. Приготовление стандартного (титрованного) раствора тиосульфата и установка его титра
Приготовление стандартного раствора тиосульфата натрия. Для приготовления требуемого объема (обычно  ) стандартного раствора (обычно 0,1 н. или 0,05 н.) тиосульфата необходимо 0,1 или 0,05 г-экв
) стандартного раствора (обычно 0,1 н. или 0,05 н.) тиосульфата необходимо 0,1 или 0,05 г-экв  растворить в воде и довести объем раствора до
растворить в воде и довести объем раствора до  . Грамм-эквивалент тиосульфата не является постоянной величиной и зависит от реакции, в которую он вступает.
. Грамм-эквивалент тиосульфата не является постоянной величиной и зависит от реакции, в которую он вступает.
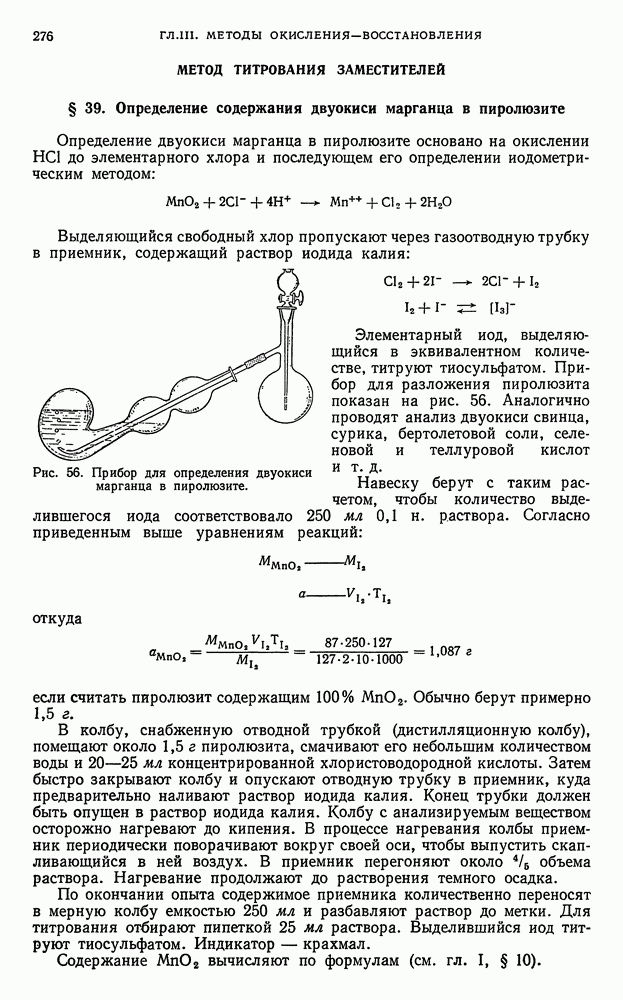
В методе иодометрии используют реакцию тиосульфата с иодом, протекающую по уравнению:

Из уравнения этой реакции видно, что тиосульфат реагирует с иодом в отношении два  -иона на два атома I, т. е. 2 молекулы тиосульфата, окисляясь иодом, отдают 2 электрона.
-иона на два атома I, т. е. 2 молекулы тиосульфата, окисляясь иодом, отдают 2 электрона.
Из этого делаем вывод, что величина грамм-эквивалента тиосульфата равна  т. е. его молекулярному весу
т. е. его молекулярному весу 
В реакции

молекула тиосульфата отдает 8 электронов. Следовательно, грамм-эквивалент тиосульфата в этом случае равен  .
.
В реакции с перманганатом, протекающей в щелочной среде

Для приготовления  н. раствора тиосульфата согласно уравнению (а) необходимо взять
н. раствора тиосульфата согласно уравнению (а) необходимо взять  .
.
Кристаллический  легко теряет кристаллизационную воду, поэтому его стандартный раствор по точной навеске приготовить очень трудно. Для приготовления приблизительно 0,1 н. раствора тиосульфата натрия взвешивают на технических весах около 25 г
легко теряет кристаллизационную воду, поэтому его стандартный раствор по точной навеске приготовить очень трудно. Для приготовления приблизительно 0,1 н. раствора тиосульфата натрия взвешивают на технических весах около 25 г  и растворяют в
и растворяют в  свежепрокипяченной и охлажденной дистиллированной воды. Воду кипятят для удаления
свежепрокипяченной и охлажденной дистиллированной воды. Воду кипятят для удаления  , чтобы предотвратить последующее изменение титра раствора тиосульфата, разлагаемого угольной кислотой (см. ниже).
, чтобы предотвратить последующее изменение титра раствора тиосульфата, разлагаемого угольной кислотой (см. ниже).
К полученному раствору тиосульфата прибавляют около 0,1 г карбоната натрия, связывающего попадающую в стандартный раствор двуокись углерода:

Стандартный раствор  для защиты от двуокиси углерода рекомендуется хранить в темной бутыли с пробкой, снабженной хлоркальциевой трубкой с натронной известью. Перед установкой титра раствор должен постоять не менее 1—2 дней. Титр раствора тиосульфата при стоянии может изменяться под влиянием двуокиси углерода (г) и кислорода воздуха (д):
для защиты от двуокиси углерода рекомендуется хранить в темной бутыли с пробкой, снабженной хлоркальциевой трубкой с натронной известью. Перед установкой титра раствор должен постоять не менее 1—2 дней. Титр раствора тиосульфата при стоянии может изменяться под влиянием двуокиси углерода (г) и кислорода воздуха (д):

Под влиянием  нормальность раствора тиосульфата увеличивается, ибо образующиеся ионы гидросульфита (бисульфита) реагируют с иодом согласно следующему уравнению:
нормальность раствора тиосульфата увеличивается, ибо образующиеся ионы гидросульфита (бисульфита) реагируют с иодом согласно следующему уравнению:

Под влияйием кислорода уменьшается нормальность раствора  , и результаты титрования получаются неправильными.
, и результаты титрования получаются неправильными.
При правильном приготовлении и хорошем хранении титр раствора тиосульфата не изменяется в течение 2—3 месяцев.
Крахмал как индикатор. Титрование иодом можно проводить без какого-либо индикатора в растворах, концентрация которых выше 0,2 н. Конечную точку титрования определяют по появлению или исчезновению желтой окраски. Но обычно при титровании иодом применяют специфический индикатор — раствор крахмала. Амилоза, входящая в состав крахмала, образует с иодом адсорбционное соединение синего цвета.
На каждые  титруемого раствора прибавляют по
титруемого раствора прибавляют по  раствора крахмала. При титровании иода тиосульфатом крахмал надо приливать перед концом титрования, когда желтая окраска иода начинает ослабевать, иначе большое количество иода будет адсорбировано крахмалом и реакция иода с тиосульфатом замедлится. Чувствительность иодо-крахмалькой реакции с повышением температуры понижается.
раствора крахмала. При титровании иода тиосульфатом крахмал надо приливать перед концом титрования, когда желтая окраска иода начинает ослабевать, иначе большое количество иода будет адсорбировано крахмалом и реакция иода с тиосульфатом замедлится. Чувствительность иодо-крахмалькой реакции с повышением температуры понижается.
Установка титра стандартного раствора тиосульфата. На практике в качестве установочного вещества для установки титра раствора тиосульфата обычно применяют бихромат калия. Бихромат калия легко получить в химически чистом виде перекристаллизацией его из водного раствора; он не содержит кристаллизационной воды, растворы его очень устойчивы. Бихромат калия — сильный окислитель 
Прямое титрование тиосульфата бихроматом не применяют вследствие того, что реакция протекает неоднозначно и не может быть выражена одним определенным уравнением. При установке титра раствора тиосульфата натрия по бихромату калия применяют метод замещения. К определенному количеству бихромата прибавляют избыток иодида калия и кислоты. При этом протекает реакция:

Указанная реакция в кислой среде проходит количественно. Выделяющийся иод оттитровывают раствором тиосульфата, титр которого устанавливают.
Так как титр стандартного раствора тиосульфата изменяется со временем, то его периодически следует проверять по бихромату калия. Помимо бихромата для установки титра тиосульфата в качестве установочных веществ применяют также иод, иодат калия  , бииодат калия
, бииодат калия  , бромат калия
, бромат калия  , гексацианоферрат (III) калия, персульфат калия
, гексацианоферрат (III) калия, персульфат калия  и стандартный раствор перманганата, установленный по какому-нибудь восстановителю. (Напишите уравнения реакции взаимодействия указанных веществ с иодидом калия.)
и стандартный раствор перманганата, установленный по какому-нибудь восстановителю. (Напишите уравнения реакции взаимодействия указанных веществ с иодидом калия.)
Установка титра раствора тиосульфата по бихромату методом пипетирования. Удобнее устанавливать раствор тиосульфата натрия по бихромату калия методом пипетирования. Раствор бихромата калия готовят примерно 0,1 н. или 0,05 н. В более разбавленных растворах реакция протекает очень медленно. Навеску рассчитывают для приготовления  н. раствора бихромата калия. Реакция протекает в присутствии иодида калия, который необходим и для окисления — восстановления и для растворения выделяющегося иода. Для полноты протекания реакции его берут обычно около 2—3 г.
н. раствора бихромата калия. Реакция протекает в присутствии иодида калия, который необходим и для окисления — восстановления и для растворения выделяющегося иода. Для полноты протекания реакции его берут обычно около 2—3 г.
Для увеличения скорости реакции необходим избыток кислоты. Опытным путем найдено, что желательно брать около  н. раствора кислоты на
н. раствора кислоты на  общего раствора. При меньшем количестве, например при
общего раствора. При меньшем количестве, например при  н. серной кислоты, реакция идет медленно и раствор должен постоять 5—10 мин для завершения реакции. Слишком большое количество кислоты вредно, так как увеличивается возможность окисления иодида калия кислородом воздуха.
н. серной кислоты, реакция идет медленно и раствор должен постоять 5—10 мин для завершения реакции. Слишком большое количество кислоты вредно, так как увеличивается возможность окисления иодида калия кислородом воздуха.
В коническую колбу переносят пипеткой  приготовленного раствора бихромата калия, прибавляют 2 г или соответствующий объем раствора иодида калия, затем
приготовленного раствора бихромата калия, прибавляют 2 г или соответствующий объем раствора иодида калия, затем  н. хлористоводородной или серной кислоты и хорошо перемешивают. Колбу закрывают часовым стеклом, дают постоять около 5 мин, разбавляют
н. хлористоводородной или серной кислоты и хорошо перемешивают. Колбу закрывают часовым стеклом, дают постоять около 5 мин, разбавляют  воды и титруют выделившийся иод тиосульфатом натрия. Когда бурая окраска выделившегося иода перейдет в лимонно-желтую, прибавляют
воды и титруют выделившийся иод тиосульфатом натрия. Когда бурая окраска выделившегося иода перейдет в лимонно-желтую, прибавляют  раствора крахмала. Светло-синяя окраска раствора в точке эквивалентности переходит в светло-зеленую. Иногда наблюдается посинение раствора после окончания титрования. Посинение через несколько минут может происходить вследствие окисления иодида калия кислородом воздуха и на результатах титрования не отражается. Посинение, происходящее тотчас же после окончания титрования, указывает, что выделение иода бихроматом калия не прошло до конца и разбавление было проведено слишком рано. Такое титрование неправильно, опыт должен быть повторен.
раствора крахмала. Светло-синяя окраска раствора в точке эквивалентности переходит в светло-зеленую. Иногда наблюдается посинение раствора после окончания титрования. Посинение через несколько минут может происходить вследствие окисления иодида калия кислородом воздуха и на результатах титрования не отражается. Посинение, происходящее тотчас же после окончания титрования, указывает, что выделение иода бихроматом калия не прошло до конца и разбавление было проведено слишком рано. Такое титрование неправильно, опыт должен быть повторен.
При расчетах титра и нормальности тиосульфата натрия надо помнить, что взятое число эквивалентов бихромата калия выделяет из иодида калия равное количество эквивалентов элементарного иода, а выделяющийся иод для своего восстановления требует точно такого же количества эквивалентов тиосульфата натрия:

Установка титра раствора тиосульфата натрия по бихромату калия методом отдельных навесок. Более точной является установка титра по методу отдельных навесок. Величина навески должна быть такова, чтобы на титрование выделенного иода расходовалось около  н. раствора тиосульфата. Необходимое количество бихромата
н. раствора тиосульфата. Необходимое количество бихромата  вычисляют по формуле:
вычисляют по формуле:

На аналитических весах взвешивают около 0,12 г чистого бихромата калия и растворяют его в  воды. К полученному раствору прибавляют 2 г иодида калия и
воды. К полученному раствору прибавляют 2 г иодида калия и  н. серной кислоты, закрывают колбу, тщательно перемешивают, дают постоять 5 мин и затем титруют выделившийся иод тиосульфатом, как указано выше.
н. серной кислоты, закрывают колбу, тщательно перемешивают, дают постоять 5 мин и затем титруют выделившийся иод тиосульфатом, как указано выше.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ К ПЕРВОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ КО ВТОРОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ К ТРЕТЬЕМУ ИЗДАНИЮ
- ВВЕДЕНИЕ
- § 1. Понятие о количественном анализе
- § 2. Классификация методов количественного анализа
- § 3. Характеристика методов количественного анализа
- § 4. Анализ больших и малых количеств вещества
- § 5. Отбор средней пробы
- § 6. Подготовка вещества для взвешивания
- § 7. Взвешивание
- § 8. Техника взвешивания на аналитических весах
- § 9. Правила обращения с аналитическими весами
- § 10. Приготовление раствора для анализа
- § 11. Запись результатов анализа
- Часть первая. Объемный анализ
- § 1. Сущность объемного анализа
- § 2. Общее уравнение реакции титрования и выводы из него
- Б. ТЕХНИКА ХИМИЧЕСКОГО ЭКСПЕРИМЕНТА В ОБЪЕМНОМ АНАЛИЗЕ
- § 3. Измерение объемов растворов
- § 4. Посуда, применяемая для измерения объемов растворов
- § 5. Работа с мерными колбами
- § 6. Работа с пипетками
- § 7. Работа с бюретками
- § 8. Приготовление стандартных растворов
- В. ВЫЧИСЛЕНИЯ В ОБЪЕМНОМ АНАЛИЗЕ
- § 9. Концентрация растворов и способы ее выражения
- § 10. Способы вычисления в объемном анализе
- § 11. Связь между точностью измерений и точностью вычислений
- § 12. Краткие сведения о статистической обработке экспериментальных данных
- Г. ПОЛУМИКРООБЪЕМНЫЙ МЕТОД АНАЛИЗА
- § 13. Понятие о полумикрообъемном анализе
- § 14. Особенности техники измерения объемов растворов в полумикрометоде
- Д. БЕЗБЮРЕТОЧНЫЕ МЕТОДЫ ТИТРОВАНИЯ
- § 15. Понятие о безбюреточных методах титрования
- § 16. Классификация методов безбюреточного титрования
- Е. АВТОМАТИЧЕСКИЕ МЕТОДЫ
- § 17. Химико-аналитический контроль производства
- § 18. Автоматические методы титрования
- ГЛАВА II. МЕТОДЫ НЕЙТРАЛИЗАЦИИ, ИЛИ МЕТОДЫ КИСЛОТНО-ОСНОВНОГО ТИТРОВАНИЯ
- § 1. Характеристика метода
- § 2. Установление точки эквивалентности
- § 3. Графический метод изображения процесса нейтрализации
- § 4. Вычисление концентрации ионов водорода в водных растворах сильных кислот и оснований
- § 5. Вычисление активности ионов водорода в водных растворах сильных кислот и оснований
- § 6. Титрование сильной кислоты сильным основанием
- § 7. Вычисление концентрации ионов водорода в растворах слабых кислот и оснований
- § 8. Вычисление активности ионов водорода в водных растворах слабых кислот и оснований
- § 9. Равновесия в водных буферных растворах слабых кислот в присутствии солей этих кислот
- § 10. Равновесия в водных буферных растворах слабых оснований в присутствии солей этих оснований
- § 11. Вычисление концентрации ионов водорода в водных буферных растворах
- § 12. Вычисление активности ионов водорода в водных буферных растворах
- § 13. Вычисление концентрации ионов водорода и степени гидролиза в водных растворах гидролизующихся бинарных солей
- § 14. Вычисление активности ионов водорода в водных растворах гидролизующихся бинарных солей
- § 15. Титрование слабой кислоты сильным основанием
- § 16. Титрование слабого основания сильной кислотой
- § 17. Титрование многоосновных кислот
- § 18. Титрование солей, образованных катионами сильных оснований и анионами слабых многоосновных кислот
- § 19. Изменение активности и показателя активности ионов водорода в процессе титрования водных растворов кислот и оснований
- § 20. Выводы, вытекающие из рассмотрения кривых нейтрализации
- § 21. Индикаторы
- § 22. Интервал перехода индикатора
- § 23. Выбор индикатора
- § 24. Ошибки титрования
- Б. ПРАКТИЧЕСКАЯ ЧАСТЬ
- § 25. Организация рабочего места
- § 26. Приготовление стандартных (титрованных) растворов
- § 27. Приготовление 0,1 н. раствора хлористоводородной кислоты
- § 28. Установка титра 0,1 н. раствора хлористоводородной кислоты
- § 29. Приготовление 0,1 н. раствора едкого натра
- § 30. Установка титра 0,1 н. раствора едкого натра
- § 31. Определение карбонатов
- § 32. Определение содержания H2SO4 в технической серной кислоте
- § 33. Определение содержания уксусной кислоты
- § 34. Определение содержания Na2CO3 и NaOH при их совместном присутствии
- § 35. Определение содержания Na2CO3 и NaHCO3 при их совместном присутствии
- § 36. Определение жесткости воды
- § 37. Определение аммонийного азота в солях аммония
- § 38. Определение содержания фосфорной кислоты
- В. КИСЛОТНО-ОСНОВНОЕ ТИТРОВАНИЕ В НЕВОДНЫХ СРЕДАХ
- § 39. Неводные растворы
- § 40. Современные представления о кислотах и основаниях
- § 41. Диссоциация электролитов в неводных растворах
- § 42. Влияние неводных растворителей на силу кислот и оснований
- § 43. Применение закона действия масс к растворам сильных электролитов
- § 44. Титрование кислот и оснований в неводных растворах
- § 45. Методы кислотно-основного титрования в неводных средах
- § 46. Примеры практических определений в неводных растворах
- ГЛАВА III. МЕТОДЫ ОКИСЛЕНИЯ—ВОССТАНОВЛЕНИЯ (ОКСИДИМЕТРИЯ, ОКСРЕДМЕТРИЯ, РЕД-ОКС-МЕТОДЫ)
- § 1. Значение окислительно-восстановительных потенциалов
- § 2. Реакции окисления—восстановления и комплексообразования
- § 3. Примеры окислительно-восстановительного титрования
- § 4. Константы равновесия окислительно-восстановительных реакций
- § 5. Связь между константами равновесия окислительно-восстановительных реакций и нормальными потенциалами
- § 6. Вычисление констант равновесия окислительно-восстановительных реакций
- § 8. Зависимость скорости реакций окисления—восстановления от различных факторов
- § 9. Графический метод изображения процесса окисления—восстановления
- § 10. Фиксирование точки эквивалентности в методах окисления—восстановления
- § 11. Окислительно-восстановительные индикаторы (ред-окс-индикаторы)
- Б. ПЕРМАНГАНАТОМЕТРИЯ
- § 12. Основы перманганатометрии
- § 13. Титрование перманганатом в кислой среде
- § 14. Титрование перманганатом в щелочной среде
- § 15. Приготовление стандартного (титрованного) раствора перманганата калия
- § 16. Установка титра стандартного раствора перманганата калия
- § 17. Установка титра и нормальности раствора перманганата калия по оксалату аммония
- § 18. Вещества, определяемые методом перманганатометрии
- ОПРЕДЕЛЕНИЕ ВОССТАНОВИТЕЛЕЙ
- § 19. Определение щавелевой кислоты и оксалатов
- § 20. Определение соединений железа (II)
- § 21. Определение содержания металлического железа в присутствии окислов железа
- § 22. Определение азотистой кислоты и нитритов
- § 23. Определение содержания марганца (II) в рудах
- ОПРЕДЕЛЕНИЕ ОКИСЛИТЕЛЕЙ
- § 24. Определение соединений железа (III)
- § 25. Определение нитратов
- § 26. Определение бихроматов
- § 27. Определение содержания MnO2 в пиролюзите
- ОПРЕДЕЛЕНИЕ ДРУГИХ ВЕЩЕСТВ
- § 28. Определение ионов кальция
- В. ИОДОМЕТРИЯ
- § 29. Основы иодометрии
- § 30. Методы иодометрического титрования
- § 31. Преимущества и недостатки иодометрического метода
- § 32. Приготовление стандартного (титрованного) раствора тиосульфата и установка его титра
- § 33. Приготовление стандартного (титрованного) раствора иода и установка его титра
- МЕТОДЫ ПРЯМОГО ТИТРОВАНИЯ
- § 34. Определение мышьяка (III)
- МЕТОДЫ ОБРАТНОГО ТИТРОВАНИЯ
- § 35. Определение сульфита натрия
- § 36. Определение содержания формальдегида в формалине
- МЕТОДЫ КОСВЕННОГО ОПРЕДЕЛЕНИЯ
- § 37. Определение ионов меди (II)
- § 38. Определение двуокиси свинца в сурике
- МЕТОД ТИТРОВАНИЯ ЗАМЕСТИТЕЛЕЙ
- § 39. Определение содержания двуокиси марганца в пиролюзите
- МЕТОД ОПРЕДЕЛЕНИЯ КИСЛОТ
- § 40. Определение хлористоводородной кислоты
- § 41. Определение воды по Фишеру
- Г. ПОНЯТИЕ О ДРУГИХ МЕТОДАХ ОКИСЛЕНИЯ — ВОССТАНОВЛЕНИЯ
- § 42. Хроматометрия
- § 43. Определение содержания железа (II)
- § 44. Цериметрия
- § 45. Броматометрия
- § 46. Ванадатометрия
- § 47. Аскорбинометрия
- § 48. Титанометрия
- ГЛАВА IV. МЕТОДЫ ОСАЖДЕНИЯ И КОМПЛЕКСООБРАЗОВАНИЯ
- § 1. Общая характеристика методов
- § 2. Классификация методов осаждения и комплексообразования
- § 3. Применение теории осаждения к объемному анализу
- § 4. Вычисление растворимости электролитов в воде с учетом коэффициентов активности
- § 5. Влияние одноименных ионов на растворимость малорастворимого электролита
- § 6. Солевой эффект
- § 7. Влияние концентрации ионов водорода на растворимость малорастворимых соединений
- § 8. Кривые титрования в методе осаждения
- § 9. Общие выводы, вытекающие из рассмотрения кривых осаждения
- § 10. Адсорбционные явления, наблюдаемые при титровании по методу осаждения
- Б. АРГЕНТОМЕТРИЯ
- § 11. Характеристика метода
- § 12. Приготовление 0,1 н. раствора нитрата серебра
- § 13. Приготовление стандартного раствора хлорида натрия
- § 14. Установка титра 0,1 н. раствора нитрата серебра по точной навеске хлорида натрия
- §15. Определение ионов хлора в техническом хлориде натрия по методу Мора
- § 16. Определение хлоридов по методу Фаянса
- В. РОДАНОМЕТРИЯ
- § 17. Характеристика метода
- § 18. Приготовление 0,1 н. раствора роданида аммония
- § 19. Определение ионов хлора в растворимых хлоридах по методу Фольгарда
- § 20. Определение серебра в сплавах
- Г. МЕРКУРИМЕТРИЯ
- § 21. Характеристика метода
- § 22. Приготовление 0,1 н. раствора нитрата ртути (II)
- § 23. Установка титра раствора нитрата ртути (II)
- § 24. Определение ионов хлора в воде меркуриметрическим методом
- Д. МЕРКУРОМЕТРИЯ
- § 25. Краткая характеристика метода
- Е. КОМПЛЕКСОНОМЕТРИЯ (ХЕЛАТОМЕТРИЯ)
- § 26. Характеристика метода
- § 27. Теоретические основы комплексонометрического титрования
- § 28. Классификация методов комплексонометрического титрования
- § 29. Установка титра раствора комплексона III
- § 30. Определение содержания кальция
- § 31. Определение жесткости воды комплексонометрическим методом
- § 32. Анализ смеси ионов кальция и магния
- § 33. Определение содержания алюминия
- § 34. Раздельное определение ионов кальция и алюминия
- § 35. Раздельное определение ионов алюминия и железа
- Часть вторая. Весовой анализ
- § 1. Сущность весового анализа
- § 2. Классификация методов весового анализа
- § 3. Расчеты в весовом анализе
- Б. ТЕХНИКА ВЕСОВОГО АНАЛИЗА
- § 4. Взятие и растворение навески
- § 5. Техника осаждения
- § 6. Фильтрование и промывание осадков
- § 7. Получение весовой формы
- § 8. Взвешивание весовой формы
- В. ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
- § 9. Теоретические основы выделения осадков из растворов с помощью специфических неорганических и органических реактивов
- § 10. Требования, предъявляемые к осадкам
- § 11. Методы повышения точности весовых определений
- § 12. Теоретические обоснования выбора оптимальных условий для весового определения
- Г. ПРАКТИЧЕСКАЯ ЧАСТЬ
- § 13. Определение кристаллизационной воды в BaCl2 2H2O
- § 14. Определение сульфат-ионов или серы
- § 15. Определение ионов железа (III)
- § 16. Определение содержания кальция в карбонате кальция
- § 17. Определение содержания магния
- § 18. Определение ионов хлора в растворимых хлоридах или в хлористоводородной кислоте
- § 19. Анализ силикатов
- § 20. Анализ доломита
- § 21. Анализ бронзы и латуни
- Д. МЕТОДЫ ВЕСОВЫХ ОПРЕДЕЛЕНИЙ, ОСНОВАННЫЕ НА ПРИМЕНЕНИИ ОРГАНИЧЕСКИХ РЕАКТИВОВ
- § 22. Определение никеля
- § 23. Определение алюминия
- Часть третья. Понятие о физических и физико-химических (инструментальных) методах анализа
- § 1. Электрохимические методы
- § 2. Спектральные (оптические) методы
- § 3. Хроматографические методы
- § 4. Радиометрические методы
- § 5. Масс-спектрометрические методы
- ГЛАВА VII ЭЛЕКТРОВЕСОВЫЕ МЕТОДЫ АНАЛИЗА
- § 1. Характеристика методов электроанализа
- § 2. Химические процессы, протекающие при электролизе
- § 3. Методы электроанализа
- § 4. Электровесовой анализ
- § 5. Метод внутреннего электролиза
- § 6. Определение меди в растворе сульфата меди с применением платиновых сетчатых электродов
- § 7. Определение меди и свинца в латуни с применением платиновых сетчатых электродов
- § 8. Определение малых количеств меди методом внутреннего электролиза
- ГЛАВА VIII. ОБЪЕМНЫЕ ЭЛЕКТРОХИМИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
- § 1. Особенности объемных электрохимических методов анализа
- § 2. Кондуктометрическое титрование
- § 3. Высокочастотное титрование
- § 4. Потенциометрическое титрование
- § 5. Полярографический метод анализа
- § 6. Амперометрическоб титрование
- § 7. Кулонометрическое титрование
- ГЛАВА IX. СПЕКТРАЛЬНЫЕ (ОПТИЧЕСКИЕ) МЕТОДЫ АНАЛИЗА
- § 1. Понятие об эмиссионном спектральном анализе
- Б. КОЛОРИМЕТРИЯ
- § 2. Особенности колориметрических методов анализа
- § 3. Характеристика колориметрических методов анализа
- В. ОПТИЧЕСКИЕ МЕТОДЫ УСТАНОВЛЕНИЯ ТОЧКИ ЭКВИВАЛЕНТНОСТИ
- § 4. Спектрофотометрическое титрование
- § 5. Фототурбидиметрическое и фотонефелометрическое титрование
- Г. ЛАБОРАТОРНЫЕ РАБОТЫ
- § 6. Определение содержания ионов железа методом колориметрического титрования
- § 7. Определение содержания титана
- ГЛАВА X. МЕТОДЫ РАЗДЕЛЕНИЯ, ВЫДЕЛЕНИЯ И КОНЦЕНТРИРОВАНИЯ ОТДЕЛЬНЫХ КОМПОНЕНТОВ АНАЛИЗИРУЕМЫХ СМЕСЕЙ
- § 1. Определение следов элементов (микропримесей)
- § 2. Метод осаждения малорастворимых соединений
- § 3. Электрохимические методы разделения
- § 4. Метод экстрагирования
- § 5. Методы отгонки летучих соединений
- § 6. Хроматографические методы разделения
- § 7. Метод флотации