| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ 28. Установка титра 0,1 н. раствора хлористоводородной кислоты
Способы установки титра раствора хлористоводородной кислоты.
Для установки титра раствора  применяют весовой или объемный способ.
применяют весовой или объемный способ.
Следует отметить, что установка титров весовым способом отнимает больше труда и времени, чем установка объемным способом. Поэтому применяют обычно объемный метод.
Объемный способ. Объемные способы установки титра основаны:
1) на титровании определенного объема кислоты раствором щелочи или
2) на титровании кислотой титрованных растворов установочных веществ, обладающих основными свойствами (см. гл. I, § 8).
Объемные способы установки не уступают по точности весовому и не требуют для своего выполнения много труда и времени. Поэтому объемные способы установки титра предпочитают весовому способу.
Установочные вещества, применяемые для установки титров стандартных растворов кислот. В качестве установочных веществ, применяемых для установки титров стандартных растворов кислот, используют разнообразные химически чистые соединения точно известного состава, реагирующие с кислотами в строго определенных стехиометрических соотношениях. Чаще всего для этой цели применяют:
1) безводный карбонат натрия 
2) тетраборат натрия  , кристаллизующийся с 10 молекулами воды,
, кристаллизующийся с 10 молекулами воды, 
3) оксалат натрия,  , термически разлагаемый с образованием карбоната натрия, который затем титруют кислотой;
, термически разлагаемый с образованием карбоната натрия, который затем титруют кислотой;
4) окись ртути (II);
5) хлорид натрия, подвергающийся ионному обмену на катионитах в Н-форме с образованием хлористоводородной кислоты;
6) дифенилгуанидин,  и др.
и др.
Установка титров стандартных растворов кислот посредством перечисленных выше установочных веществ основана на следующих реакциях:
По карбонату натрия. Водный раствор карбоната натрия вследствие его гидролитического разложения под влиянием ионов воды имеет сильно щелочную реакцию:

При титровании карбоната натрия кислотой гидролиз протекает полностью в сторону образования угольной кислоты, разлагающейся на воду и двуокись углерода. Поэтому суммарное уравнение реакции титрования карбоната натрия хлористоводородной кислотой можно представить следующим уравнением:

Эквивалент карбоната натрия в этом случае равен половине его молекулярного веса:

По тетраборату натрия. Водный раствор тетрабората натрия (подобно карбонату натрия) имеет сильно щелочную реакцию. Титрование кислотой тетрабората натрия можно представить следующим суммарным уравнением реакции:

Эквивалент тетрабората натрия в этом случае равен половине его молекулярного веса:

По оксалату натрия. Оксалат натрия непосредственно не титруется кислотой, так как его водный раствор не обладает сильно щелочной реакцией подобно карбонату или тетраборату натрия. Его предварительно переводят в карбонат натрия путем нагревания в платиновом тигле. Образующийся при этом карбонат натрия термически не разлагается даже при температуре плавления и может быть использован для установки титра кислоты. Уравнения протекающих при этом реакций можно представить следующим образом:

Эквивалент оксалата натрия в данном случае равен половине его молекулярного веса:

По окиси ртути (II). Окись ртути (II) является очень подходящим установочным веществом для стандартизации кислот, так как ее легко получить в химически чистом виде, однако она практически не растворяется в воде. Поэтому из нее нельзя приготовить установочный раствор путем растворения ее в воде. Ее нельзя непосредственно использовать для установки титра кислоты:

так как реакция обратима. Для приготовления раствора окиси ртути ее предварительно растворяют в нейтральном растворе йодида или бромида калия. При этом раствор окиси приобретает сильно щелочную реакцию вследствие связывания ионов ртути в комплекс, а ионов кислорода в гидроксильные группы:

Образующиеся при этом ионы гидроксила титруют кислотой.
Эквивалент окиси ртути (II) в данном случае равен половине ее молекулярного веса:

Установка стандартных (титрованных) растворов кислот с помощью катионитов. Наряду с описанными методами установки титров в последнее время стали устанавливать стандартные растворы кислот с помощью катионитов.
Метод основан на пропускании через колонку, заполненную катионитом в Н-форме, раствора определенного количества химически чистой соли (например,  ), которая подвергается ионному обмену согласно уравнению:
), которая подвергается ионному обмену согласно уравнению:

Образующуюся при этом в эквивалентном количестве по отношению к взятой навеске соли  кислоту вымывают из колонки, собирают в мерную колбу и доводят соответствующим растворителем до метки. Таким путем получают стандартный раствор кислоты, свободный от посторонних примесей. При этом отпадает необходимость дополнительной установки титра полученной кислоты с помощью установочных веществ.
кислоту вымывают из колонки, собирают в мерную колбу и доводят соответствующим растворителем до метки. Таким путем получают стандартный раствор кислоты, свободный от посторонних примесей. При этом отпадает необходимость дополнительной установки титра полученной кислоты с помощью установочных веществ.
Установка стандартных (титрованных) растворов кислот по карбонату натрия. Безводный химически чистый карбонат натрия является наиболее доступным установочным веществом для стандартизации растворов кислот.
Для приготовления безводного карбоната натрия применяют:
а) высушивание в сушильном шкафу в течение  при 250—270° С исходного
при 250—270° С исходного  . препарата;
. препарата;
б) нагревание в платиновом тигле на песочной бане гидрокарбоната (бикарбоната) при 250—270° С до постоянной массы:

в) термическое разложение в платиновом тигле  . оксалата натрия
. оксалата натрия

Водный раствор  имеет щелочную реакцию.
имеет щелочную реакцию.
Установка титра кислоты при помощи карбоната натрия основана на реакции:

Приготовление 0,1 н. раствора карбоната натрия. Для установки титра 0,1 н. раствора кислоты точно отвешивают рассчитанное количество карбоната натрия (в г):

Навеску растворяют в воде в мерной колбе емкостью  .
.
Следует иметь в виду, что нет никакой необходимости брать точно рассчитанную навеску  . Вполне достаточно предварительно взвесить на технических весах навеску, приближающуюся по своей массе к 1,3248 г, и затем взвесить ее на аналитических весах. В зависимости от взятой навески вводят соответствующий поправочный коэффициент:
. Вполне достаточно предварительно взвесить на технических весах навеску, приближающуюся по своей массе к 1,3248 г, и затем взвесить ее на аналитических весах. В зависимости от взятой навески вводят соответствующий поправочный коэффициент:

Для установки стандартного раствора кислоты из мерной колбы отбирают пипеткой аликвотные части приготовленного раствора карбоната и титруют их приготовленным раствором кислоты.
Вместо приготовленного раствора можно титровать устанавливаемым раствором кислоты уменьшенные в 10 раз навески сухого карбоната.
Титрование проводят в присутствии метилового оранжевого, желательно в присутствии раствора — «свидетеля», содержащего  .
.
Карбонат натрия используют не только для установки титров водных растворов кислот, но и для стандартизации неводных растворов кислот. Для этого рассчитанную навеску химически чистого карбоната натрия помещают в фарфоровую чашку, прибавляют несколько капель безводной уксусной кислоты.
Полученный раствор выпаривают досуха на водяной бане, остаток образовавшегося ацетата натрия растворяют в нужном растворителе, переносят в мерную колбу, доводят объем раствора до метки и тщательно перемешивают.
Затем отбирают аликвотную часть раствора и титруют неводным раствором кислоты. Чаще всего для этой цели применяют хлорную кислоту  . В качестве растворителей при установке титров обычно применяют те же растворители, которые используют для последующих количественных определений.
. В качестве растворителей при установке титров обычно применяют те же растворители, которые используют для последующих количественных определений.
Установка титра 0,1 н. раствора хлористоводородной кислоты по тетраборату натрия. Установка титра хлористоводородной кислоты по тетраборату натрия имеет ряд преимуществ по сравнению с другими способами:
1. Установка титра хлористоводородной кислоты по тетраборату может быть выполнена с метиловым оранжевым или метиловым красным. Установку же титра кислоты по карбонату проводят обычно в присутствии метилового оранжевого.
2. Тетраборат натрия  при хранении в плотно закрытой банке в течение долгого времени не изменяет своего состава. Карбонат натрия легче изменяет свой состав под влиянием
при хранении в плотно закрытой банке в течение долгого времени не изменяет своего состава. Карбонат натрия легче изменяет свой состав под влиянием  и влаги воздуха.
и влаги воздуха.
3. Тетраборат натрия имеет более высокий эквивалентный вес (см. стр. 162) по сравнению с эквивалентным весом карбоната натрия (см. стр. 161).
Поэтому тетраборату натрия отдается предпочтение при установке титров кислот.
К существенным недостаткам тетрабората натрия относится его плохая растворимость в воде и легкость, с которой он теряет части кристаллизационной воды при неправильном хранении, вследствие чего декагидрат (десятиводная соль)  превращается в пентагидрат (пятиводную соль)
превращается в пентагидрат (пятиводную соль)  . Однако этот недостаток тетрабората натрия легко устраним.
. Однако этот недостаток тетрабората натрия легко устраним.
Если кристаллический тетраборат натрия не отвечает составу  , то его тщательно перекристаллизовывают перед употреблением.
, то его тщательно перекристаллизовывают перед употреблением.
Приготовление 0,1 н. раствора тетрабората натрия. Установку титра кислоты по  . тетраборату натрия можно выполнить:
. тетраборату натрия можно выполнить:
а) методом пипетирования, т. е. титрованием аликвотных частей стандартного раствора тетрабората натрия приготовленным приблизительно 0,1 н. раствором 
б) титрованием кислотой отдельных точных навесок установочного вещества, рассчитанных на одно титрование (см. гл. I, § 8).
Оба способа имеют свои преимущества и недостатки. Так как тетраборат натрия плохо растворяется в воде, иногда предпочитают второй способ титрования или растворяют тетраборат в горячей дистиллированной воде. После полного растворения  в горячей воде раствор охлаждают и затем доводят водой до определенного объема.
в горячей воде раствор охлаждают и затем доводят водой до определенного объема.
а) Установка титра хлористоводородной кислоты по тетраборату натрия методом пипетирования. Величина навески тетрабората натрия, рассчитанная при приготовлении  н. раствора для многократного титрования аликвотных (кратных) частей, должна быть равна (см. гл. I, § 8, 10):
н. раствора для многократного титрования аликвотных (кратных) частей, должна быть равна (см. гл. I, § 8, 10):

Для приготовления  н. раствора тетрабората натрия необходимо взвесить около 4,767 г
н. раствора тетрабората натрия необходимо взвесить около 4,767 г  . Отвесить на аналитических весах в точности теоретически рассчитанное количество соли очень трудно. Поэтому сначала взвешивают в бюксе на технических весах с точностью до первого десятичного знака
. Отвесить на аналитических весах в точности теоретически рассчитанное количество соли очень трудно. Поэтому сначала взвешивают в бюксе на технических весах с точностью до первого десятичного знака  . Затем бюкс переносят на аналитические весы и взвешивают с точностью до четвертого десятичного знака
. Затем бюкс переносят на аналитические весы и взвешивают с точностью до четвертого десятичного знака  . Взвешенный тетраборат осторожно пересыпают через сухую воронку с широкой и короткой трубкой в мерную колбу емкостью
. Взвешенный тетраборат осторожно пересыпают через сухую воронку с широкой и короткой трубкой в мерную колбу емкостью  с сухим горлом.
с сухим горлом.
Кристаллы  , оставшиеся в бюксе и на воронке, тщательно смывают в колбу горячей водой из промывалки. В колбу через ту же воронку добавляют около
, оставшиеся в бюксе и на воронке, тщательно смывают в колбу горячей водой из промывалки. В колбу через ту же воронку добавляют около  горячей дистиллированной воды. Затем содержимое колбы осторожно перемешивают плавными вращательными движениями. После того как весь тетраборат растворится в воде, колбу охлаждают до комнатной температуры и доводят объем полученного раствора холодной дистиллированной водой до метки. Колбу закрывают пробкой. Приготовленный раствор тщательно перемешивают. После этого раствор тетрабората натрия готов для титрования.
горячей дистиллированной воды. Затем содержимое колбы осторожно перемешивают плавными вращательными движениями. После того как весь тетраборат растворится в воде, колбу охлаждают до комнатной температуры и доводят объем полученного раствора холодной дистиллированной водой до метки. Колбу закрывают пробкой. Приготовленный раствор тщательно перемешивают. После этого раствор тетрабората натрия готов для титрования.
Всю работу с мерной колбой выполняют, строго соблюдая все правила обращения с нею (см. гл. I, § 5).
Отбор проб для титрования. Для титрования берут при помощи пипетки  приготовленного раствора тетрабората натрия. Для этого оттянутый конец пипетки опускают в мерную колбу почти до дна и засасывают
приготовленного раствора тетрабората натрия. Для этого оттянутый конец пипетки опускают в мерную колбу почти до дна и засасывают  раствора. Затем закрывают верхнее отверстие пипетки указательным пальцем и вынимают ее из колбы. Слегка наклоняя пипетку в разные стороны, ополаскивают ее раствором. Использованный раствор отбрасывают. Снова набирают в пипетку
раствора. Затем закрывают верхнее отверстие пипетки указательным пальцем и вынимают ее из колбы. Слегка наклоняя пипетку в разные стороны, ополаскивают ее раствором. Использованный раствор отбрасывают. Снова набирают в пипетку  раствора и выливают его в коническую колбу емкостью
раствора и выливают его в коническую колбу емкостью  . Пробы отбирают параллельно в три колбы.
. Пробы отбирают параллельно в три колбы.
Всю работу с пипеткой выполняют, строго соблюдая все правила обращения с нею (см. гл. I, § 6).
Титрование аликвотных частей раствора тетрабората натрия соляной кислотой. Титрование тетрабората натрия как соли, образованной катионом сильного основания и анионом слабой кислоты, ведут в присутствии метилового красного, интервал перехода которого  (см. гл. II, § 22).
(см. гл. II, § 22).
Для более точного титрования применяют «свидетель». Для приготовления «свидетеля» используют  буферного раствора с
буферного раствора с  или
или  сильно разбавленного
сильно разбавленного  раствора борной кислоты, к которой добавляют
раствора борной кислоты, к которой добавляют  н. раствора
н. раствора  и 1—2 капли индикатора. Раствор «свидетеля» должен быть окрашен в оранжевый цвет.
и 1—2 капли индикатора. Раствор «свидетеля» должен быть окрашен в оранжевый цвет.
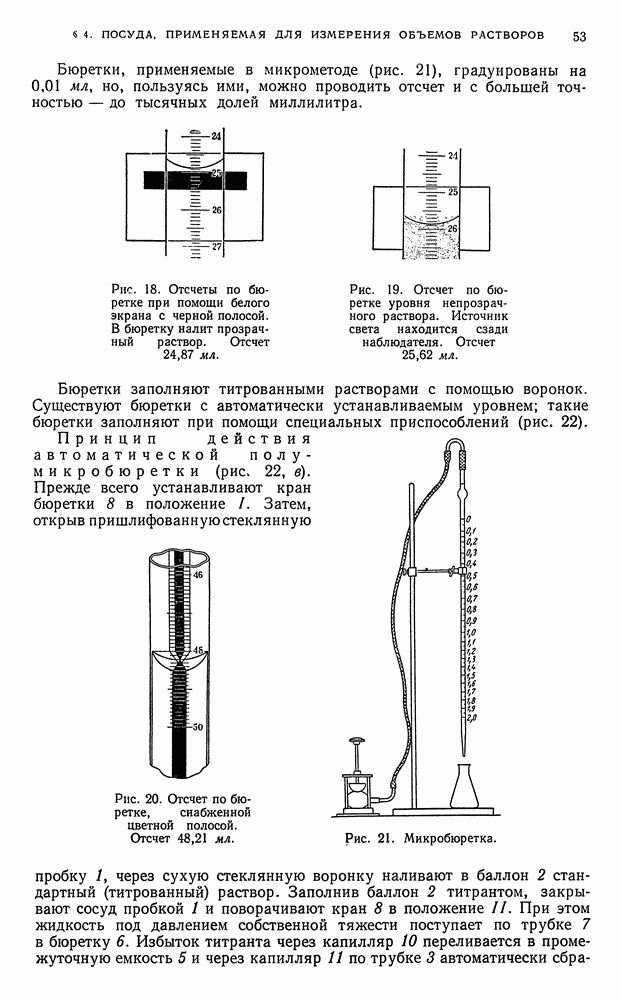
Бюретку емкостью  , снабженную стеклянным краном, укрепляют в штативе, заботясь о том, чтобы она приняла правильное вертикальное положение. Если бюретка была перед употреблением заполнена доверху водой, то сначала сливают воду. Во время работы с бюреткой следят за тем, чтобы ее кончик оставался заполненным раствором. Сначала 2—3 раза бюретку ополаскивают
, снабженную стеклянным краном, укрепляют в штативе, заботясь о том, чтобы она приняла правильное вертикальное положение. Если бюретка была перед употреблением заполнена доверху водой, то сначала сливают воду. Во время работы с бюреткой следят за тем, чтобы ее кончик оставался заполненным раствором. Сначала 2—3 раза бюретку ополаскивают  приготовленного раствора
приготовленного раствора  , который затем выливают. Потом бюретку наполняют раствором кислоты несколько выше нулевого деления. Лишь перед самым началом титрования устанавливают уровень кислоты на нулевое деление, осторожно сливая избыток кислоты из бюретки в подставленный стакан.
, который затем выливают. Потом бюретку наполняют раствором кислоты несколько выше нулевого деления. Лишь перед самым началом титрования устанавливают уровень кислоты на нулевое деление, осторожно сливая избыток кислоты из бюретки в подставленный стакан.
Всю работу с бюреткой выполняют, строго соблюдая правила обращения с ней (см. гл. I, § 7).
После окончания всех приготовлений приступают к титрованию. Для этого в каждую приготовленную ранее коническую колбу, содержащую раствор тетрабората натрия, приливают по 1—2 капли метилового красного. Первую колбу подставляют под бюретку. Под колбу подкладывают лист белой бумаги. Кончик бюретки опускают в горло колбы на 1—2 см. Придерживая бюретку в нижней части левой рукой, осторожно открывают правой рукой кран бюретки. При этом кислота начинает понемногу выливаться из бюретки в колбу.
По мере вытекания раствора из бюретки содержимое колбы непрерывно перемешивают плавными круговыми движениями. Титрование прекращают в тот момент, когда прибавление очередной капли раствора кислоты вызывает появление оранжевой окраски индикатора, похожей на окраску «свидетеля».
В случае сомнения в правильности окончания титрования прибегают к следующему приему. Записывают показания бюретки, добавляют в коническую колбу еще каплю титрованного раствора и наблюдают за изменением окраски. Если раствор покраснеет, значит тцтрование было закончено. В противном случае продолжают титрование до момента изменения окраски индикатора.
После первого титрования проводят второе и третье титрования. Последующие титрования проводят быстрее первого. Во время титрования следят за тем, чтобы не происходило разбрызгивания раствора. Нельзя допускать появления на внутренних стенках колбы капель раствора. В случае их появления капли смывают дистиллированной водой из промывалки. Разбавление раствора не отражается на результатах титрования. Необходимо следить также за тем, чтобы капли раствора не оставались висеть на кончике бюретки, так как объем висящей капли войдет при расчете в общий объем раствора, израсходованного на титрование, и это поведет к ошибочным результатам.
Порле окончания каждого титрования отсчитывают по шкале бюретки объем израсходованной на титрование кислоты и снова заполняют бюретку раствором кислоты до нулевого деления. Результаты титрования записывают в рабочий журнал.
Если результаты трех титрований не расходятся или отличаются на несколько сотых долей миллилитра, титрование считают законченным. Если расхождения превышают сотые доли миллилитра, то повторяют титрование до тех пор, пока не получат по крайней мере три не расходящихся результата. Сильно отличающиеся результаты титрования в расчет не принимают. Окончательный расчет проводят исходя из среднего арифметического близкосходящихся результатов титрований.
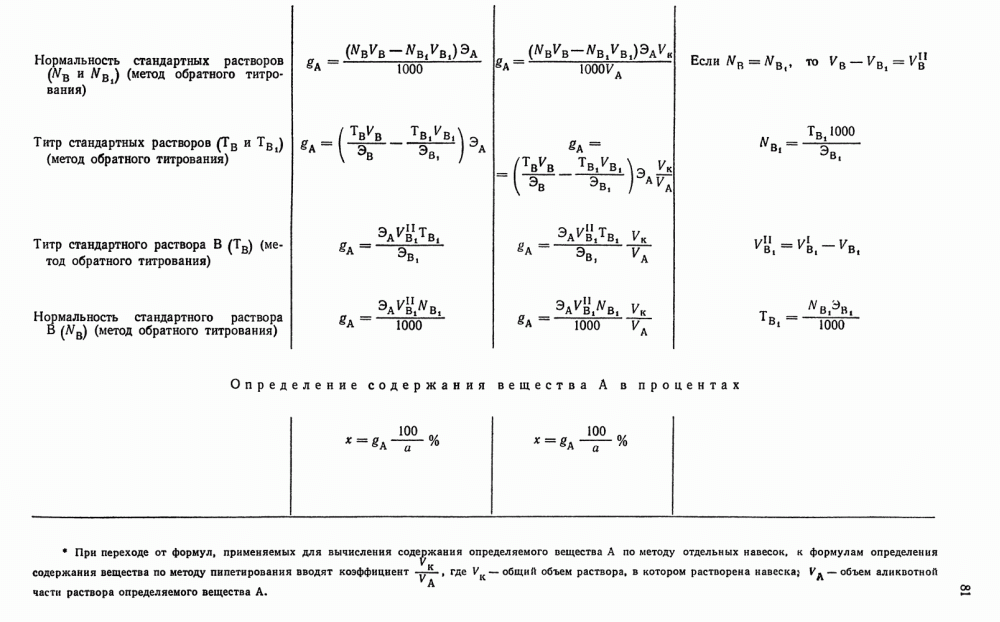
Вычисление  и
и  по данным титрования хлористоводородной кислотой аликвотных частей раствора тетрабората натрия. Расчеты проводят на основании уравнений реакций (см. гл. I, § 10) и исходят из
по данным титрования хлористоводородной кислотой аликвотных частей раствора тетрабората натрия. Расчеты проводят на основании уравнений реакций (см. гл. I, § 10) и исходят из  или
или  . Например, зная
. Например, зная  , т. е. нормальность раствора тетрабората натрик, можно вычислить
, т. е. нормальность раствора тетрабората натрик, можно вычислить  — нормальность раствора кислоты. Предположим, что навеска
— нормальность раствора кислоты. Предположим, что навеска  , взятая для приготовления
, взятая для приготовления  раствора, равна 4,8524 г. Следовательно
раствора, равна 4,8524 г. Следовательно

Допустим, что на титрование  раствора тетрабората натрия израсходовано 20,07; 20,08;
раствора тетрабората натрия израсходовано 20,07; 20,08;  раствора
раствора  . Среднее арифметическое составит:
. Среднее арифметическое составит:

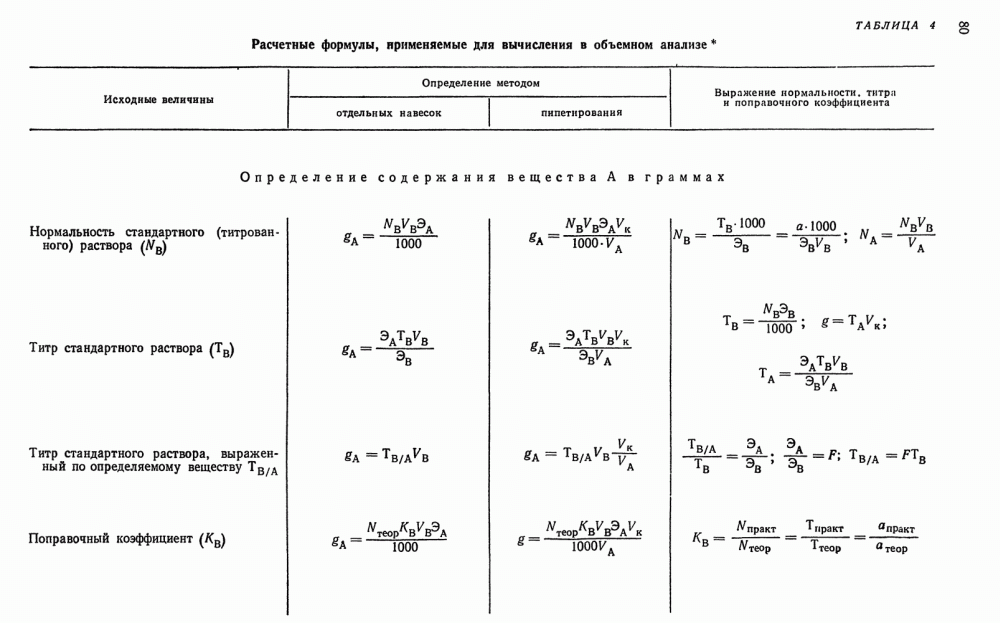
Так как произведения объемов (в  ) реагирующих между собой растворов на их нормальности равны между собой, т. е.
) реагирующих между собой растворов на их нормальности равны между собой, т. е.

то

В нашем примере

Зная нормальность, можно вычислить 

Проделайте самостоятельно расчет по значению  (см. гл. I, § 10).
(см. гл. I, § 10).
Пользуясь найденными величинами, можно проводить любые вычисления в процессе объемных определений при помощи приготовленного раствора  .
.
б) Установка титра хлористоводородной кислоты по тетраборату натрия методом отдельных навесок. Расчет навески тетрабората натрия. Для титрования методом отдельных навесок необходимо брать такие навески установочного вещества, чтобы на их титрование расходовалось  н. раствора (см. гл. I, § 8). Это означает, что величина отдельной навески
н. раствора (см. гл. I, § 8). Это означает, что величина отдельной навески  , рассчитанная только на одно титрование, должна быть эквивалентна
, рассчитанная только на одно титрование, должна быть эквивалентна  н. раствора тетрабората натрия. Расчет навески выполняют по формуле
н. раствора тетрабората натрия. Расчет навески выполняют по формуле

Поэтому навеска тетрабората должна быть равна:

где 190,69 — грамм-эквивалент  .
.
Взятие отдельной навески. В сухую пробирку с притертой пробкой и проволочной петлей для подвешивания к коромыслу аналитических весов помещают около 1,5  . Для взятия такой навески пробирку предварительно тарируют на технических весах, всыпают в нее примерно требуемое для трех титрований количество тетрабората натрия и взвешивают сначала на технических весах, а затем на аналитических. После этого отсыпают около V3 содержимого пробирки в коническую колбу емкостью
. Для взятия такой навески пробирку предварительно тарируют на технических весах, всыпают в нее примерно требуемое для трех титрований количество тетрабората натрия и взвешивают сначала на технических весах, а затем на аналитических. После этого отсыпают около V3 содержимого пробирки в коническую колбу емкостью  и прббирку снова взвешивают. Разность в массе после первого и второго взвешиваний на аналитических весах указывает массу отсыпанного
и прббирку снова взвешивают. Разность в массе после первого и второго взвешиваний на аналитических весах указывает массу отсыпанного  .
.
Таким же образом отсыпают вторую и третью навески во вторую и третью колбы. Колбы предварительно нумеруют. Все результаты взвешиваний записывают в рабочий журнал по следующей форме:

Взятые навески растворяют приблизительно в  дистиллированной воды и титруют приготовленным 0,1 н. раствором
дистиллированной воды и титруют приготовленным 0,1 н. раствором  .
.
Титрование растворов, приготовленных из отдельных навесок. Титрование растворов, приготовленных из отдельных навесок тетрабората натрия, ведут в присутствии метилового красного, интервал перехода которого  (см. § 22). Для более точного титрования применяют «свидетель».
(см. § 22). Для более точного титрования применяют «свидетель».
При титровании необходимо принять во внимание следующее.
Если взятые навески  еще полностью не растворились в воде, то колбы нагревают на песочной бане, затем дают им охладиться и добавляют в них столько же капель индикатора, сколько было прибавлено в «свидетель». Установив уровень кислоты в бюретке на нуль, приступают к титрованию. Титрование начинают с раствора, приготовленного из самой маленькой навески, и кончают раствором, приготовленным из самой большой. Такой порядок титрования позволяет заранее знать, что при каждом последующем титровании пойдет большее количество кислоты.
еще полностью не растворились в воде, то колбы нагревают на песочной бане, затем дают им охладиться и добавляют в них столько же капель индикатора, сколько было прибавлено в «свидетель». Установив уровень кислоты в бюретке на нуль, приступают к титрованию. Титрование начинают с раствора, приготовленного из самой маленькой навески, и кончают раствором, приготовленным из самой большой. Такой порядок титрования позволяет заранее знать, что при каждом последующем титровании пойдет большее количество кислоты.
Вычисление  и
и  на основании данных титрования хлористоводородной кислотой отдельных навесок тетрабората натрия. Когда определение ведут методом отдельных навесок, то вычисления проводят иначе, чем при расчете
на основании данных титрования хлористоводородной кислотой отдельных навесок тетрабората натрия. Когда определение ведут методом отдельных навесок, то вычисления проводят иначе, чем при расчете  на основании данных титрования аликвотных частей раствора. В этом случае нельзя применять уравнение
на основании данных титрования аликвотных частей раствора. В этом случае нельзя применять уравнение  так как неизвестными являются и
так как неизвестными являются и  и
и  . Поэтому исходят из соответствия эквивалентов
. Поэтому исходят из соответствия эквивалентов  (см. гл. I, § 10):
(см. гл. I, § 10):

откуда

где F — аналитический множитель (фактор) объемного анализа.
Следовательно

Величину  вычисляют для каждой навески отдельно. Значения
вычисляют для каждой навески отдельно. Значения  вычисляют по среднему значению
вычисляют по среднему значению  . Расчет может быть также проведен следующим путем: так как
. Расчет может быть также проведен следующим путем: так как

то

где  — число грамм-эквивалентов
— число грамм-эквивалентов  во взятой навеске;
во взятой навеске;  — число грамм-эквивалентов
— число грамм-эквивалентов  .
.

Отсюда

Если при расчете величины  , оказываются равными или близкими по значению, то это указывает на правильность результатов отдельных титрований. Если величины
, оказываются равными или близкими по значению, то это указывает на правильность результатов отдельных титрований. Если величины  сильно отличаются друг от друга, то повторяют титрование до тех пор? пока для трех титрований не получат близко сходящихся результатов. Величины, значительно отличающиеся друг от друга, в расчет не принимают.
сильно отличаются друг от друга, то повторяют титрование до тех пор? пока для трех титрований не получат близко сходящихся результатов. Величины, значительно отличающиеся друг от друга, в расчет не принимают.
Чтобы судить о порядке точности определений, нет необходимости проводить все вычисления полностью. Достаточно вычислить отношение  так как F — величина постоянная. Допускается расхождение этих отношений друг от друга на 3 единицы в четвертой значащей цифре.
так как F — величина постоянная. Допускается расхождение этих отношений друг от друга на 3 единицы в четвертой значащей цифре.
Полученные данные рекомендуется записывать в рабочий журнал по форме:

На основании данных титрования вычисляют среднее значение  . Зная среднее значение
. Зная среднее значение  , легко вычислить
, легко вычислить  и
и  :
:

Предположим, что для установки титра раствора  была взята навеска
была взята навеска  , равная 0,4680 г. На титрование ее было израсходовано
, равная 0,4680 г. На титрование ее было израсходовано  приготовленного приблизительно 0,1 н. раствора
приготовленного приблизительно 0,1 н. раствора  . Следовательно
. Следовательно

В нашем примере

| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ К ПЕРВОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ КО ВТОРОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ К ТРЕТЬЕМУ ИЗДАНИЮ
- ВВЕДЕНИЕ
- § 1. Понятие о количественном анализе
- § 2. Классификация методов количественного анализа
- § 3. Характеристика методов количественного анализа
- § 4. Анализ больших и малых количеств вещества
- § 5. Отбор средней пробы
- § 6. Подготовка вещества для взвешивания
- § 7. Взвешивание
- § 8. Техника взвешивания на аналитических весах
- § 9. Правила обращения с аналитическими весами
- § 10. Приготовление раствора для анализа
- § 11. Запись результатов анализа
- Часть первая. Объемный анализ
- § 1. Сущность объемного анализа
- § 2. Общее уравнение реакции титрования и выводы из него
- Б. ТЕХНИКА ХИМИЧЕСКОГО ЭКСПЕРИМЕНТА В ОБЪЕМНОМ АНАЛИЗЕ
- § 3. Измерение объемов растворов
- § 4. Посуда, применяемая для измерения объемов растворов
- § 5. Работа с мерными колбами
- § 6. Работа с пипетками
- § 7. Работа с бюретками
- § 8. Приготовление стандартных растворов
- В. ВЫЧИСЛЕНИЯ В ОБЪЕМНОМ АНАЛИЗЕ
- § 9. Концентрация растворов и способы ее выражения
- § 10. Способы вычисления в объемном анализе
- § 11. Связь между точностью измерений и точностью вычислений
- § 12. Краткие сведения о статистической обработке экспериментальных данных
- Г. ПОЛУМИКРООБЪЕМНЫЙ МЕТОД АНАЛИЗА
- § 13. Понятие о полумикрообъемном анализе
- § 14. Особенности техники измерения объемов растворов в полумикрометоде
- Д. БЕЗБЮРЕТОЧНЫЕ МЕТОДЫ ТИТРОВАНИЯ
- § 15. Понятие о безбюреточных методах титрования
- § 16. Классификация методов безбюреточного титрования
- Е. АВТОМАТИЧЕСКИЕ МЕТОДЫ
- § 17. Химико-аналитический контроль производства
- § 18. Автоматические методы титрования
- ГЛАВА II. МЕТОДЫ НЕЙТРАЛИЗАЦИИ, ИЛИ МЕТОДЫ КИСЛОТНО-ОСНОВНОГО ТИТРОВАНИЯ
- § 1. Характеристика метода
- § 2. Установление точки эквивалентности
- § 3. Графический метод изображения процесса нейтрализации
- § 4. Вычисление концентрации ионов водорода в водных растворах сильных кислот и оснований
- § 5. Вычисление активности ионов водорода в водных растворах сильных кислот и оснований
- § 6. Титрование сильной кислоты сильным основанием
- § 7. Вычисление концентрации ионов водорода в растворах слабых кислот и оснований
- § 8. Вычисление активности ионов водорода в водных растворах слабых кислот и оснований
- § 9. Равновесия в водных буферных растворах слабых кислот в присутствии солей этих кислот
- § 10. Равновесия в водных буферных растворах слабых оснований в присутствии солей этих оснований
- § 11. Вычисление концентрации ионов водорода в водных буферных растворах
- § 12. Вычисление активности ионов водорода в водных буферных растворах
- § 13. Вычисление концентрации ионов водорода и степени гидролиза в водных растворах гидролизующихся бинарных солей
- § 14. Вычисление активности ионов водорода в водных растворах гидролизующихся бинарных солей
- § 15. Титрование слабой кислоты сильным основанием
- § 16. Титрование слабого основания сильной кислотой
- § 17. Титрование многоосновных кислот
- § 18. Титрование солей, образованных катионами сильных оснований и анионами слабых многоосновных кислот
- § 19. Изменение активности и показателя активности ионов водорода в процессе титрования водных растворов кислот и оснований
- § 20. Выводы, вытекающие из рассмотрения кривых нейтрализации
- § 21. Индикаторы
- § 22. Интервал перехода индикатора
- § 23. Выбор индикатора
- § 24. Ошибки титрования
- Б. ПРАКТИЧЕСКАЯ ЧАСТЬ
- § 25. Организация рабочего места
- § 26. Приготовление стандартных (титрованных) растворов
- § 27. Приготовление 0,1 н. раствора хлористоводородной кислоты
- § 28. Установка титра 0,1 н. раствора хлористоводородной кислоты
- § 29. Приготовление 0,1 н. раствора едкого натра
- § 30. Установка титра 0,1 н. раствора едкого натра
- § 31. Определение карбонатов
- § 32. Определение содержания H2SO4 в технической серной кислоте
- § 33. Определение содержания уксусной кислоты
- § 34. Определение содержания Na2CO3 и NaOH при их совместном присутствии
- § 35. Определение содержания Na2CO3 и NaHCO3 при их совместном присутствии
- § 36. Определение жесткости воды
- § 37. Определение аммонийного азота в солях аммония
- § 38. Определение содержания фосфорной кислоты
- В. КИСЛОТНО-ОСНОВНОЕ ТИТРОВАНИЕ В НЕВОДНЫХ СРЕДАХ
- § 39. Неводные растворы
- § 40. Современные представления о кислотах и основаниях
- § 41. Диссоциация электролитов в неводных растворах
- § 42. Влияние неводных растворителей на силу кислот и оснований
- § 43. Применение закона действия масс к растворам сильных электролитов
- § 44. Титрование кислот и оснований в неводных растворах
- § 45. Методы кислотно-основного титрования в неводных средах
- § 46. Примеры практических определений в неводных растворах
- ГЛАВА III. МЕТОДЫ ОКИСЛЕНИЯ—ВОССТАНОВЛЕНИЯ (ОКСИДИМЕТРИЯ, ОКСРЕДМЕТРИЯ, РЕД-ОКС-МЕТОДЫ)
- § 1. Значение окислительно-восстановительных потенциалов
- § 2. Реакции окисления—восстановления и комплексообразования
- § 3. Примеры окислительно-восстановительного титрования
- § 4. Константы равновесия окислительно-восстановительных реакций
- § 5. Связь между константами равновесия окислительно-восстановительных реакций и нормальными потенциалами
- § 6. Вычисление констант равновесия окислительно-восстановительных реакций
- § 8. Зависимость скорости реакций окисления—восстановления от различных факторов
- § 9. Графический метод изображения процесса окисления—восстановления
- § 10. Фиксирование точки эквивалентности в методах окисления—восстановления
- § 11. Окислительно-восстановительные индикаторы (ред-окс-индикаторы)
- Б. ПЕРМАНГАНАТОМЕТРИЯ
- § 12. Основы перманганатометрии
- § 13. Титрование перманганатом в кислой среде
- § 14. Титрование перманганатом в щелочной среде
- § 15. Приготовление стандартного (титрованного) раствора перманганата калия
- § 16. Установка титра стандартного раствора перманганата калия
- § 17. Установка титра и нормальности раствора перманганата калия по оксалату аммония
- § 18. Вещества, определяемые методом перманганатометрии
- ОПРЕДЕЛЕНИЕ ВОССТАНОВИТЕЛЕЙ
- § 19. Определение щавелевой кислоты и оксалатов
- § 20. Определение соединений железа (II)
- § 21. Определение содержания металлического железа в присутствии окислов железа
- § 22. Определение азотистой кислоты и нитритов
- § 23. Определение содержания марганца (II) в рудах
- ОПРЕДЕЛЕНИЕ ОКИСЛИТЕЛЕЙ
- § 24. Определение соединений железа (III)
- § 25. Определение нитратов
- § 26. Определение бихроматов
- § 27. Определение содержания MnO2 в пиролюзите
- ОПРЕДЕЛЕНИЕ ДРУГИХ ВЕЩЕСТВ
- § 28. Определение ионов кальция
- В. ИОДОМЕТРИЯ
- § 29. Основы иодометрии
- § 30. Методы иодометрического титрования
- § 31. Преимущества и недостатки иодометрического метода
- § 32. Приготовление стандартного (титрованного) раствора тиосульфата и установка его титра
- § 33. Приготовление стандартного (титрованного) раствора иода и установка его титра
- МЕТОДЫ ПРЯМОГО ТИТРОВАНИЯ
- § 34. Определение мышьяка (III)
- МЕТОДЫ ОБРАТНОГО ТИТРОВАНИЯ
- § 35. Определение сульфита натрия
- § 36. Определение содержания формальдегида в формалине
- МЕТОДЫ КОСВЕННОГО ОПРЕДЕЛЕНИЯ
- § 37. Определение ионов меди (II)
- § 38. Определение двуокиси свинца в сурике
- МЕТОД ТИТРОВАНИЯ ЗАМЕСТИТЕЛЕЙ
- § 39. Определение содержания двуокиси марганца в пиролюзите
- МЕТОД ОПРЕДЕЛЕНИЯ КИСЛОТ
- § 40. Определение хлористоводородной кислоты
- § 41. Определение воды по Фишеру
- Г. ПОНЯТИЕ О ДРУГИХ МЕТОДАХ ОКИСЛЕНИЯ — ВОССТАНОВЛЕНИЯ
- § 42. Хроматометрия
- § 43. Определение содержания железа (II)
- § 44. Цериметрия
- § 45. Броматометрия
- § 46. Ванадатометрия
- § 47. Аскорбинометрия
- § 48. Титанометрия
- ГЛАВА IV. МЕТОДЫ ОСАЖДЕНИЯ И КОМПЛЕКСООБРАЗОВАНИЯ
- § 1. Общая характеристика методов
- § 2. Классификация методов осаждения и комплексообразования
- § 3. Применение теории осаждения к объемному анализу
- § 4. Вычисление растворимости электролитов в воде с учетом коэффициентов активности
- § 5. Влияние одноименных ионов на растворимость малорастворимого электролита
- § 6. Солевой эффект
- § 7. Влияние концентрации ионов водорода на растворимость малорастворимых соединений
- § 8. Кривые титрования в методе осаждения
- § 9. Общие выводы, вытекающие из рассмотрения кривых осаждения
- § 10. Адсорбционные явления, наблюдаемые при титровании по методу осаждения
- Б. АРГЕНТОМЕТРИЯ
- § 11. Характеристика метода
- § 12. Приготовление 0,1 н. раствора нитрата серебра
- § 13. Приготовление стандартного раствора хлорида натрия
- § 14. Установка титра 0,1 н. раствора нитрата серебра по точной навеске хлорида натрия
- §15. Определение ионов хлора в техническом хлориде натрия по методу Мора
- § 16. Определение хлоридов по методу Фаянса
- В. РОДАНОМЕТРИЯ
- § 17. Характеристика метода
- § 18. Приготовление 0,1 н. раствора роданида аммония
- § 19. Определение ионов хлора в растворимых хлоридах по методу Фольгарда
- § 20. Определение серебра в сплавах
- Г. МЕРКУРИМЕТРИЯ
- § 21. Характеристика метода
- § 22. Приготовление 0,1 н. раствора нитрата ртути (II)
- § 23. Установка титра раствора нитрата ртути (II)
- § 24. Определение ионов хлора в воде меркуриметрическим методом
- Д. МЕРКУРОМЕТРИЯ
- § 25. Краткая характеристика метода
- Е. КОМПЛЕКСОНОМЕТРИЯ (ХЕЛАТОМЕТРИЯ)
- § 26. Характеристика метода
- § 27. Теоретические основы комплексонометрического титрования
- § 28. Классификация методов комплексонометрического титрования
- § 29. Установка титра раствора комплексона III
- § 30. Определение содержания кальция
- § 31. Определение жесткости воды комплексонометрическим методом
- § 32. Анализ смеси ионов кальция и магния
- § 33. Определение содержания алюминия
- § 34. Раздельное определение ионов кальция и алюминия
- § 35. Раздельное определение ионов алюминия и железа
- Часть вторая. Весовой анализ
- § 1. Сущность весового анализа
- § 2. Классификация методов весового анализа
- § 3. Расчеты в весовом анализе
- Б. ТЕХНИКА ВЕСОВОГО АНАЛИЗА
- § 4. Взятие и растворение навески
- § 5. Техника осаждения
- § 6. Фильтрование и промывание осадков
- § 7. Получение весовой формы
- § 8. Взвешивание весовой формы
- В. ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
- § 9. Теоретические основы выделения осадков из растворов с помощью специфических неорганических и органических реактивов
- § 10. Требования, предъявляемые к осадкам
- § 11. Методы повышения точности весовых определений
- § 12. Теоретические обоснования выбора оптимальных условий для весового определения
- Г. ПРАКТИЧЕСКАЯ ЧАСТЬ
- § 13. Определение кристаллизационной воды в BaCl2 2H2O
- § 14. Определение сульфат-ионов или серы
- § 15. Определение ионов железа (III)
- § 16. Определение содержания кальция в карбонате кальция
- § 17. Определение содержания магния
- § 18. Определение ионов хлора в растворимых хлоридах или в хлористоводородной кислоте
- § 19. Анализ силикатов
- § 20. Анализ доломита
- § 21. Анализ бронзы и латуни
- Д. МЕТОДЫ ВЕСОВЫХ ОПРЕДЕЛЕНИЙ, ОСНОВАННЫЕ НА ПРИМЕНЕНИИ ОРГАНИЧЕСКИХ РЕАКТИВОВ
- § 22. Определение никеля
- § 23. Определение алюминия
- Часть третья. Понятие о физических и физико-химических (инструментальных) методах анализа
- § 1. Электрохимические методы
- § 2. Спектральные (оптические) методы
- § 3. Хроматографические методы
- § 4. Радиометрические методы
- § 5. Масс-спектрометрические методы
- ГЛАВА VII ЭЛЕКТРОВЕСОВЫЕ МЕТОДЫ АНАЛИЗА
- § 1. Характеристика методов электроанализа
- § 2. Химические процессы, протекающие при электролизе
- § 3. Методы электроанализа
- § 4. Электровесовой анализ
- § 5. Метод внутреннего электролиза
- § 6. Определение меди в растворе сульфата меди с применением платиновых сетчатых электродов
- § 7. Определение меди и свинца в латуни с применением платиновых сетчатых электродов
- § 8. Определение малых количеств меди методом внутреннего электролиза
- ГЛАВА VIII. ОБЪЕМНЫЕ ЭЛЕКТРОХИМИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
- § 1. Особенности объемных электрохимических методов анализа
- § 2. Кондуктометрическое титрование
- § 3. Высокочастотное титрование
- § 4. Потенциометрическое титрование
- § 5. Полярографический метод анализа
- § 6. Амперометрическоб титрование
- § 7. Кулонометрическое титрование
- ГЛАВА IX. СПЕКТРАЛЬНЫЕ (ОПТИЧЕСКИЕ) МЕТОДЫ АНАЛИЗА
- § 1. Понятие об эмиссионном спектральном анализе
- Б. КОЛОРИМЕТРИЯ
- § 2. Особенности колориметрических методов анализа
- § 3. Характеристика колориметрических методов анализа
- В. ОПТИЧЕСКИЕ МЕТОДЫ УСТАНОВЛЕНИЯ ТОЧКИ ЭКВИВАЛЕНТНОСТИ
- § 4. Спектрофотометрическое титрование
- § 5. Фототурбидиметрическое и фотонефелометрическое титрование
- Г. ЛАБОРАТОРНЫЕ РАБОТЫ
- § 6. Определение содержания ионов железа методом колориметрического титрования
- § 7. Определение содержания титана
- ГЛАВА X. МЕТОДЫ РАЗДЕЛЕНИЯ, ВЫДЕЛЕНИЯ И КОНЦЕНТРИРОВАНИЯ ОТДЕЛЬНЫХ КОМПОНЕНТОВ АНАЛИЗИРУЕМЫХ СМЕСЕЙ
- § 1. Определение следов элементов (микропримесей)
- § 2. Метод осаждения малорастворимых соединений
- § 3. Электрохимические методы разделения
- § 4. Метод экстрагирования
- § 5. Методы отгонки летучих соединений
- § 6. Хроматографические методы разделения
- § 7. Метод флотации