| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
§ 37. Определение аммонийного азота в солях аммония
Напомним, что азот входит в состав многочисленных неорганических и органических соединений. Соединения азота имеют громадное значение в природе и применяются в разнообразных отраслях промышленности и народного хозяйства. Поэтому определение азота в его соединениях имеет большое практическое значение.
Азот, входящий в состав различных соединений, очень часто определяют в виде  , который образуется:
, который образуется:
а) при кипячении солей аммония со щелочами;
б) при восстановлении нитратов и нитритов в щелочном растворе при помощи сплава Деварда  ;
;
в) при нагревании с концентрированной  азотсодержащих органических соединений и последующем разложении образовавшейся соли аммония
азотсодержащих органических соединений и последующем разложении образовавшейся соли аммония  щелочью (метод Кьельдаля). Метод основан на том, что азотсодержащее вещество полностью разрушается при нагревании с концентрированной
щелочью (метод Кьельдаля). Метод основан на том, что азотсодержащее вещество полностью разрушается при нагревании с концентрированной  в присутствии добавок, действующих как катализаторы.
в присутствии добавок, действующих как катализаторы.
Существует несколько способов определения  .
.
Определение аммиака в солях аммония методом обратного титрования.
Определение основано на титровании избытка щелочи, которую добавляют к соли аммония, разлагаемой при кипячении щелочного раствора с образованием  :
:

Зная количество  , добавленного в раствор соли аммония до кипячения и оставшегося после кипячений, можно по разности вычислить содержание
, добавленного в раствор соли аммония до кипячения и оставшегося после кипячений, можно по разности вычислить содержание  в исходной соли.
в исходной соли.
Методика определения. Рассчитывают навеску исходной соли аммония (см. § 28) для приготовления  н. раствора.
н. раствора.
Взятую навеску растворяют в воде или данный для анализа готовый раствор переносят в мерную колбу, точно нейтрализуют свободную кислоту несколькими каплями 0,1 н. раствора  в присутствии метилового красного и доводят объем раствора водой до метки. Три пробы по
в присутствии метилового красного и доводят объем раствора водой до метки. Три пробы по  приготовленного раствора переносят при помощи пипетки в три стакана. В каждый стакан добавляют по
приготовленного раствора переносят при помощи пипетки в три стакана. В каждый стакан добавляют по  н. раствора
н. раствора  . Стаканы ставят на песочную баню и нагревают почти до кипения, пока не улетучится весь аммиак. Выпаривание обычно прекращают тогда, когда испарится свыше
. Стаканы ставят на песочную баню и нагревают почти до кипения, пока не улетучится весь аммиак. Выпаривание обычно прекращают тогда, когда испарится свыше  содержимого стакана. Полноту удаления
содержимого стакана. Полноту удаления  проверяют при помощи фильтровальной бумаги, смоченной раствором
проверяют при помощи фильтровальной бумаги, смоченной раствором  . Если весь аммиак удален, бумага не чернеет.
. Если весь аммиак удален, бумага не чернеет.
По окончании удаления  стаканы снимают с бани, накрывают часовыми стеклами и дают им остыть. После охлаждения содержимого стаканов добавляют в них по 1—2 капли метилового красного и титруют 0,1 н. раствором кислоты.
стаканы снимают с бани, накрывают часовыми стеклами и дают им остыть. После охлаждения содержимого стаканов добавляют в них по 1—2 капли метилового красного и титруют 0,1 н. раствором кислоты.
Указанный метод определения  весьма прост, но менее точен, чем метод, описанный ниже.
весьма прост, но менее точен, чем метод, описанный ниже.
Расчет результатов анализа. Содержание аммиака вычисляют, как описано (в гл. I, § 10).
Определение аммиака в солях аммония методом отгонки. Определение основано на отгонке аммиака, выделяющегося при взаимодействии соли аммония со щелочью, улавливании его определенным объемом стандартного раствора кислоты и последующем титровании остатка неиспользованной кислоты щелочью в присутствии метилового оранжевого или еще лучше в присутствии метилового красного.
Зная количество кислоты, пошедшей на реакцию с  , можно легко вычислить содержание аммонийного азота в соли аммония.
, можно легко вычислить содержание аммонийного азота в соли аммония.
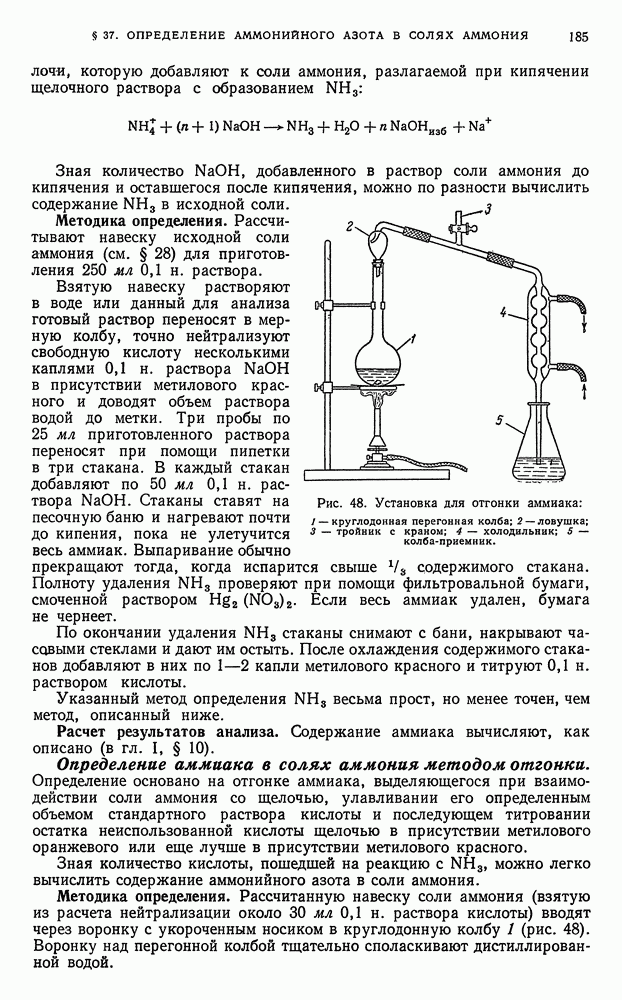
Методика определения. Рассчитанную навеску соли аммония (взятую из расчета нейтрализации около  н. раствора кислоты) вводят через воронку с укороченным носиком в круглодонную колбу 1 (рис. 48). Воронку над перегонной колбой тщательно споласкивают дистиллированной водой.
н. раствора кислоты) вводят через воронку с укороченным носиком в круглодонную колбу 1 (рис. 48). Воронку над перегонной колбой тщательно споласкивают дистиллированной водой.

Рис. 48. Установка для отгонки аммиака: 1 — круглодонная перегонная колба; 2 — ловушка; 3 — тройник с краном; 4 — холодильник; 5 — колба-приемник.
На дно колбы 1 опускают несколько кусочков неглазурованного фарфора или пемзы величиной с конопляное зерно для равномерного кипения жидкости при нагревании.
В некоторых руководствах для той же цели предлагается вместо фарфора или пемзы поместить в колбу немного цинковой пыли. Мы рекомендуем воздерживаться от введения цинка, восстанавливающего в щелочном растворе при нагревании нитраты и нитриты (которые могут содержаться в анализируемой смеси) до  . Это ведет к неизбежным ошибкам.
. Это ведет к неизбежным ошибкам.
В колбу 5 вводят пипеткой  н. раствора
н. раствора  и 2—3 капли метилового оранжевого или метилового красного. Нижний конец холодильника 4 должен быть опущен в кислоту на 1 см. Нижний отросток водяной рубашки холодильника через резиновую трубку присоединяют к водопроводному крану, а верхний — к сточной трубе и пускают в холодильник воду.
и 2—3 капли метилового оранжевого или метилового красного. Нижний конец холодильника 4 должен быть опущен в кислоту на 1 см. Нижний отросток водяной рубашки холодильника через резиновую трубку присоединяют к водопроводному крану, а верхний — к сточной трубе и пускают в холодильник воду.
Затем с помощью воронки с длинной трубкой быстро вливают в круглодонную колбу 1 около  -ного раствора КОН и немедленно закрывают колбу резиновой пробкой с вставленной в нее насадкой. Пробка заблаговременно должна быть хорошо пригнана к горлу колбы.
-ного раствора КОН и немедленно закрывают колбу резиновой пробкой с вставленной в нее насадкой. Пробка заблаговременно должна быть хорошо пригнана к горлу колбы.
При нагревании сначала из колбы вытесняется воздух, затем начинает выделяться аммиак. Как только воздух будет вытеснен из колбы 1, кислота начинает засасываться в алонж холодильника. На это не следует обращать особого внимания.
Пламя горелки регулируют таким образом, чтобы кипение в колбе 1 было равномерным и умеренным.
Если навеска соли аммония была рассчитана правильно, то жидкость в колбе 5 до конца опыта остается красной. В противном случае раствор начинает желтеть. Это указывает на то, что необходимо добавить еще некоторое (отмеренное) количество 0,1 н. раствора хлористоводородной кислоты.
Перегонку продолжают до тех пор, пока около 2/3 содержимого колбы 1 не перегонится в колбу 5. По окончании отгонки, не прекращая нагревания, вынимают из приемника алонж и ополаскивают его над колбой 5 дистиллированной водой из промывалки. Затем содержимое колбы 5 титруют. 0,1 н. раствором едкого натра до появления оранжево-желтой окраски. Иногда для отгонки  применяют упрощенную установку (рис. 49) и вместо
применяют упрощенную установку (рис. 49) и вместо  пользуются
пользуются  .
.
Расчет результатов анализа. Содержание аммиака рассчитывают, как описано в гл. I, § 10.

где  — объем хлористоводородной кислоты, израсходованный на нейтрализацию выделившегося аммиака,
— объем хлористоводородной кислоты, израсходованный на нейтрализацию выделившегося аммиака,  :
:

здесь  — объем взятого раствора
— объем взятого раствора  , нормальность которого
, нормальность которого  .
.

Рис. 49. Упрощенная установка для отгонки аммиака.
Определение аммиака в солях аммония формалиновым методом. При взаимодействии солей аммония с формальдегидом  , содержащимся в водном растворе в виде гидрата
, содержащимся в водном растворе в виде гидрата  , выделяется эквивалентное количество свободной кислоты:
, выделяется эквивалентное количество свободной кислоты:

Содержание выделяющейся при этом свободной кислоты определяют титрованием стандартным раствором едкого натра, установленным по щавелевой или янтарной кислоте в присутствии фенолфталеина.
Методика определения. В коническую колбу емкостью  наливают
наливают  -ного водного раствора формальдегида (формалина), добавляют
-ного водного раствора формальдегида (формалина), добавляют  дистиллированной воды, 2—3 капли фенолфталеина и точно нейтрализуют кислый раствор формалина (который может содержать свободную муравьиную кислоту) 0,1 н. раствором
дистиллированной воды, 2—3 капли фенолфталеина и точно нейтрализуют кислый раствор формалина (который может содержать свободную муравьиную кислоту) 0,1 н. раствором  до слаборозовой окраски. В случае если исходный раствор формалина более концентрирован или содержит менее 25% формальдегида, то берут его соответственно меньше или больше
до слаборозовой окраски. В случае если исходный раствор формалина более концентрирован или содержит менее 25% формальдегида, то берут его соответственно меньше или больше  .
.
В нейтрализованный раствор вносят навеску около  г соли аммония, взвешенной на аналитических весах с точностью до 0,0001 г. Смесь тщательно перемешивают, дают постоять 3—5 мин и затем титруют выделившуюся кислоту стандартным раствором
г соли аммония, взвешенной на аналитических весах с точностью до 0,0001 г. Смесь тщательно перемешивают, дают постоять 3—5 мин и затем титруют выделившуюся кислоту стандартным раствором  .
.
Расчет результатов анализа. Содержание аммиака в исследуемой соли рассчитывают исходя из правила эквивалентности, — см. гл. I, § 10.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ К ПЕРВОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ КО ВТОРОМУ ИЗДАНИЮ
- ПРЕДИСЛОВИЕ К ТРЕТЬЕМУ ИЗДАНИЮ
- ВВЕДЕНИЕ
- § 1. Понятие о количественном анализе
- § 2. Классификация методов количественного анализа
- § 3. Характеристика методов количественного анализа
- § 4. Анализ больших и малых количеств вещества
- § 5. Отбор средней пробы
- § 6. Подготовка вещества для взвешивания
- § 7. Взвешивание
- § 8. Техника взвешивания на аналитических весах
- § 9. Правила обращения с аналитическими весами
- § 10. Приготовление раствора для анализа
- § 11. Запись результатов анализа
- Часть первая. Объемный анализ
- § 1. Сущность объемного анализа
- § 2. Общее уравнение реакции титрования и выводы из него
- Б. ТЕХНИКА ХИМИЧЕСКОГО ЭКСПЕРИМЕНТА В ОБЪЕМНОМ АНАЛИЗЕ
- § 3. Измерение объемов растворов
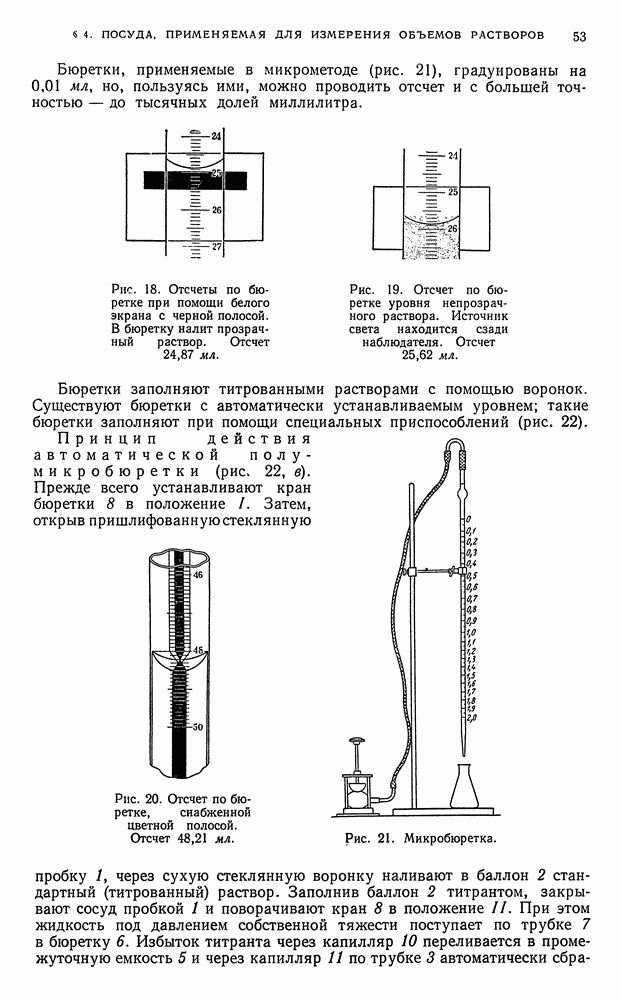
- § 4. Посуда, применяемая для измерения объемов растворов
- § 5. Работа с мерными колбами
- § 6. Работа с пипетками
- § 7. Работа с бюретками
- § 8. Приготовление стандартных растворов
- В. ВЫЧИСЛЕНИЯ В ОБЪЕМНОМ АНАЛИЗЕ
- § 9. Концентрация растворов и способы ее выражения
- § 10. Способы вычисления в объемном анализе
- § 11. Связь между точностью измерений и точностью вычислений
- § 12. Краткие сведения о статистической обработке экспериментальных данных
- Г. ПОЛУМИКРООБЪЕМНЫЙ МЕТОД АНАЛИЗА
- § 13. Понятие о полумикрообъемном анализе
- § 14. Особенности техники измерения объемов растворов в полумикрометоде
- Д. БЕЗБЮРЕТОЧНЫЕ МЕТОДЫ ТИТРОВАНИЯ
- § 15. Понятие о безбюреточных методах титрования
- § 16. Классификация методов безбюреточного титрования
- Е. АВТОМАТИЧЕСКИЕ МЕТОДЫ
- § 17. Химико-аналитический контроль производства
- § 18. Автоматические методы титрования
- ГЛАВА II. МЕТОДЫ НЕЙТРАЛИЗАЦИИ, ИЛИ МЕТОДЫ КИСЛОТНО-ОСНОВНОГО ТИТРОВАНИЯ
- § 1. Характеристика метода
- § 2. Установление точки эквивалентности
- § 3. Графический метод изображения процесса нейтрализации
- § 4. Вычисление концентрации ионов водорода в водных растворах сильных кислот и оснований
- § 5. Вычисление активности ионов водорода в водных растворах сильных кислот и оснований
- § 6. Титрование сильной кислоты сильным основанием
- § 7. Вычисление концентрации ионов водорода в растворах слабых кислот и оснований
- § 8. Вычисление активности ионов водорода в водных растворах слабых кислот и оснований
- § 9. Равновесия в водных буферных растворах слабых кислот в присутствии солей этих кислот
- § 10. Равновесия в водных буферных растворах слабых оснований в присутствии солей этих оснований
- § 11. Вычисление концентрации ионов водорода в водных буферных растворах
- § 12. Вычисление активности ионов водорода в водных буферных растворах
- § 13. Вычисление концентрации ионов водорода и степени гидролиза в водных растворах гидролизующихся бинарных солей
- § 14. Вычисление активности ионов водорода в водных растворах гидролизующихся бинарных солей
- § 15. Титрование слабой кислоты сильным основанием
- § 16. Титрование слабого основания сильной кислотой
- § 17. Титрование многоосновных кислот
- § 18. Титрование солей, образованных катионами сильных оснований и анионами слабых многоосновных кислот
- § 19. Изменение активности и показателя активности ионов водорода в процессе титрования водных растворов кислот и оснований
- § 20. Выводы, вытекающие из рассмотрения кривых нейтрализации
- § 21. Индикаторы
- § 22. Интервал перехода индикатора
- § 23. Выбор индикатора
- § 24. Ошибки титрования
- Б. ПРАКТИЧЕСКАЯ ЧАСТЬ
- § 25. Организация рабочего места
- § 26. Приготовление стандартных (титрованных) растворов
- § 27. Приготовление 0,1 н. раствора хлористоводородной кислоты
- § 28. Установка титра 0,1 н. раствора хлористоводородной кислоты
- § 29. Приготовление 0,1 н. раствора едкого натра
- § 30. Установка титра 0,1 н. раствора едкого натра
- § 31. Определение карбонатов
- § 32. Определение содержания H2SO4 в технической серной кислоте
- § 33. Определение содержания уксусной кислоты
- § 34. Определение содержания Na2CO3 и NaOH при их совместном присутствии
- § 35. Определение содержания Na2CO3 и NaHCO3 при их совместном присутствии
- § 36. Определение жесткости воды
- § 37. Определение аммонийного азота в солях аммония
- § 38. Определение содержания фосфорной кислоты
- В. КИСЛОТНО-ОСНОВНОЕ ТИТРОВАНИЕ В НЕВОДНЫХ СРЕДАХ
- § 39. Неводные растворы
- § 40. Современные представления о кислотах и основаниях
- § 41. Диссоциация электролитов в неводных растворах
- § 42. Влияние неводных растворителей на силу кислот и оснований
- § 43. Применение закона действия масс к растворам сильных электролитов
- § 44. Титрование кислот и оснований в неводных растворах
- § 45. Методы кислотно-основного титрования в неводных средах
- § 46. Примеры практических определений в неводных растворах
- ГЛАВА III. МЕТОДЫ ОКИСЛЕНИЯ—ВОССТАНОВЛЕНИЯ (ОКСИДИМЕТРИЯ, ОКСРЕДМЕТРИЯ, РЕД-ОКС-МЕТОДЫ)
- § 1. Значение окислительно-восстановительных потенциалов
- § 2. Реакции окисления—восстановления и комплексообразования
- § 3. Примеры окислительно-восстановительного титрования
- § 4. Константы равновесия окислительно-восстановительных реакций
- § 5. Связь между константами равновесия окислительно-восстановительных реакций и нормальными потенциалами
- § 6. Вычисление констант равновесия окислительно-восстановительных реакций
- § 8. Зависимость скорости реакций окисления—восстановления от различных факторов
- § 9. Графический метод изображения процесса окисления—восстановления
- § 10. Фиксирование точки эквивалентности в методах окисления—восстановления
- § 11. Окислительно-восстановительные индикаторы (ред-окс-индикаторы)
- Б. ПЕРМАНГАНАТОМЕТРИЯ
- § 12. Основы перманганатометрии
- § 13. Титрование перманганатом в кислой среде
- § 14. Титрование перманганатом в щелочной среде
- § 15. Приготовление стандартного (титрованного) раствора перманганата калия
- § 16. Установка титра стандартного раствора перманганата калия
- § 17. Установка титра и нормальности раствора перманганата калия по оксалату аммония
- § 18. Вещества, определяемые методом перманганатометрии
- ОПРЕДЕЛЕНИЕ ВОССТАНОВИТЕЛЕЙ
- § 19. Определение щавелевой кислоты и оксалатов
- § 20. Определение соединений железа (II)
- § 21. Определение содержания металлического железа в присутствии окислов железа
- § 22. Определение азотистой кислоты и нитритов
- § 23. Определение содержания марганца (II) в рудах
- ОПРЕДЕЛЕНИЕ ОКИСЛИТЕЛЕЙ
- § 24. Определение соединений железа (III)
- § 25. Определение нитратов
- § 26. Определение бихроматов
- § 27. Определение содержания MnO2 в пиролюзите
- ОПРЕДЕЛЕНИЕ ДРУГИХ ВЕЩЕСТВ
- § 28. Определение ионов кальция
- В. ИОДОМЕТРИЯ
- § 29. Основы иодометрии
- § 30. Методы иодометрического титрования
- § 31. Преимущества и недостатки иодометрического метода
- § 32. Приготовление стандартного (титрованного) раствора тиосульфата и установка его титра
- § 33. Приготовление стандартного (титрованного) раствора иода и установка его титра
- МЕТОДЫ ПРЯМОГО ТИТРОВАНИЯ
- § 34. Определение мышьяка (III)
- МЕТОДЫ ОБРАТНОГО ТИТРОВАНИЯ
- § 35. Определение сульфита натрия
- § 36. Определение содержания формальдегида в формалине
- МЕТОДЫ КОСВЕННОГО ОПРЕДЕЛЕНИЯ
- § 37. Определение ионов меди (II)
- § 38. Определение двуокиси свинца в сурике
- МЕТОД ТИТРОВАНИЯ ЗАМЕСТИТЕЛЕЙ
- § 39. Определение содержания двуокиси марганца в пиролюзите
- МЕТОД ОПРЕДЕЛЕНИЯ КИСЛОТ
- § 40. Определение хлористоводородной кислоты
- § 41. Определение воды по Фишеру
- Г. ПОНЯТИЕ О ДРУГИХ МЕТОДАХ ОКИСЛЕНИЯ — ВОССТАНОВЛЕНИЯ
- § 42. Хроматометрия
- § 43. Определение содержания железа (II)
- § 44. Цериметрия
- § 45. Броматометрия
- § 46. Ванадатометрия
- § 47. Аскорбинометрия
- § 48. Титанометрия
- ГЛАВА IV. МЕТОДЫ ОСАЖДЕНИЯ И КОМПЛЕКСООБРАЗОВАНИЯ
- § 1. Общая характеристика методов
- § 2. Классификация методов осаждения и комплексообразования
- § 3. Применение теории осаждения к объемному анализу
- § 4. Вычисление растворимости электролитов в воде с учетом коэффициентов активности
- § 5. Влияние одноименных ионов на растворимость малорастворимого электролита
- § 6. Солевой эффект
- § 7. Влияние концентрации ионов водорода на растворимость малорастворимых соединений
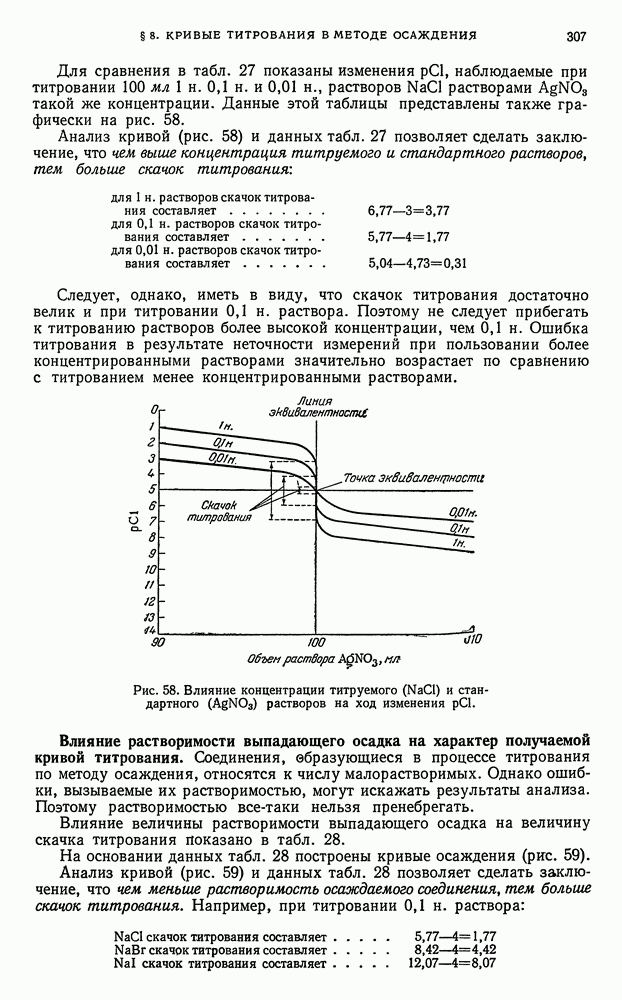
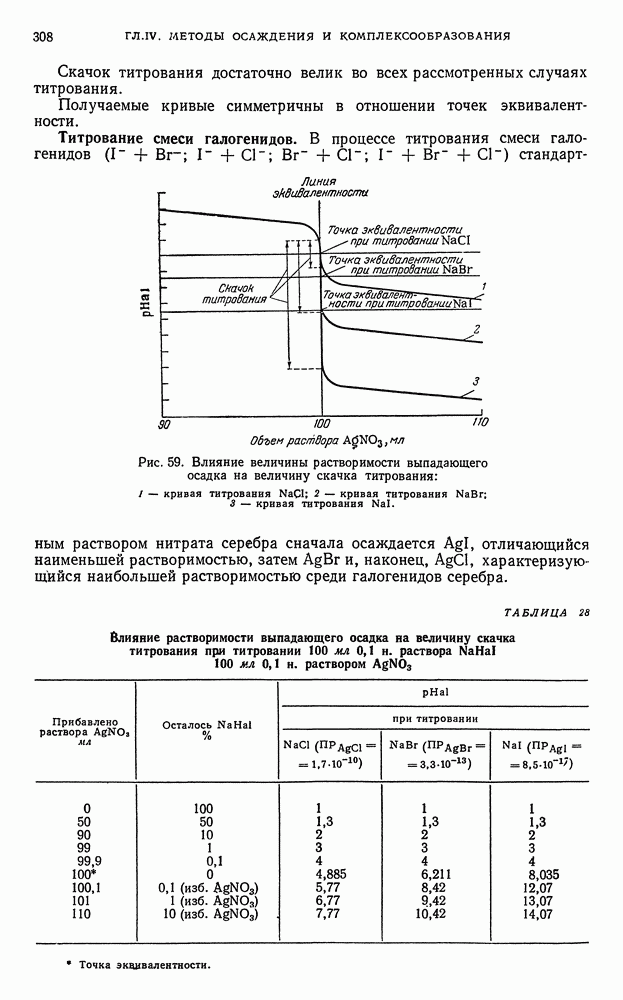
- § 8. Кривые титрования в методе осаждения
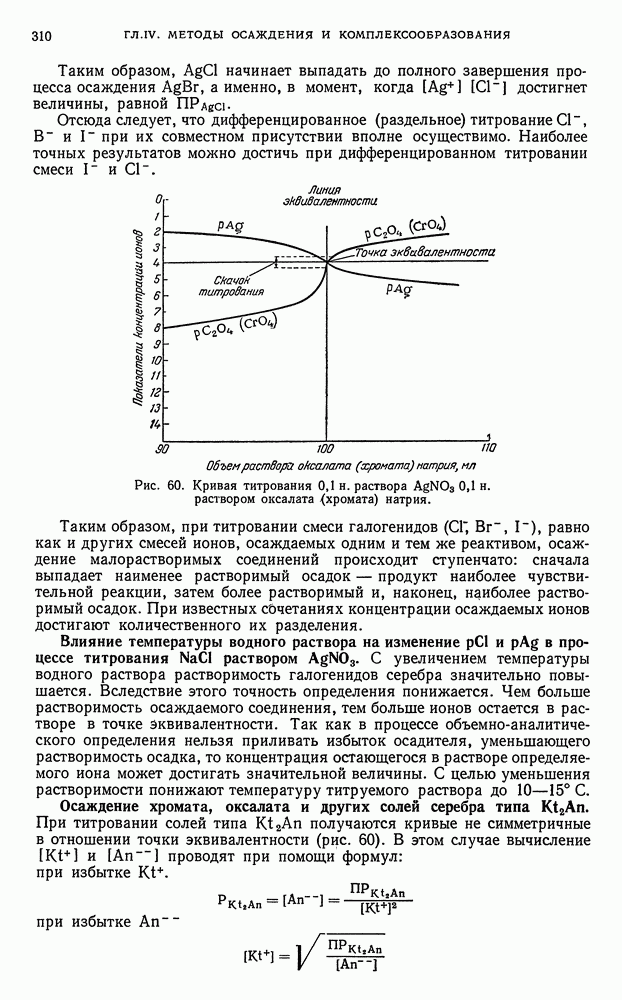
- § 9. Общие выводы, вытекающие из рассмотрения кривых осаждения
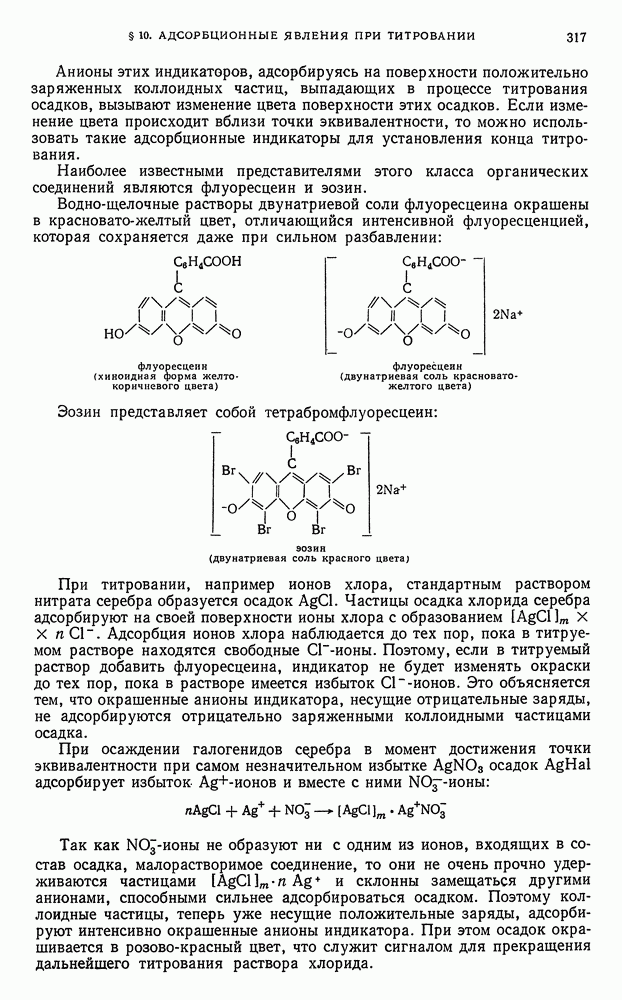
- § 10. Адсорбционные явления, наблюдаемые при титровании по методу осаждения
- Б. АРГЕНТОМЕТРИЯ
- § 11. Характеристика метода
- § 12. Приготовление 0,1 н. раствора нитрата серебра
- § 13. Приготовление стандартного раствора хлорида натрия
- § 14. Установка титра 0,1 н. раствора нитрата серебра по точной навеске хлорида натрия
- §15. Определение ионов хлора в техническом хлориде натрия по методу Мора
- § 16. Определение хлоридов по методу Фаянса
- В. РОДАНОМЕТРИЯ
- § 17. Характеристика метода
- § 18. Приготовление 0,1 н. раствора роданида аммония
- § 19. Определение ионов хлора в растворимых хлоридах по методу Фольгарда
- § 20. Определение серебра в сплавах
- Г. МЕРКУРИМЕТРИЯ
- § 21. Характеристика метода
- § 22. Приготовление 0,1 н. раствора нитрата ртути (II)
- § 23. Установка титра раствора нитрата ртути (II)
- § 24. Определение ионов хлора в воде меркуриметрическим методом
- Д. МЕРКУРОМЕТРИЯ
- § 25. Краткая характеристика метода
- Е. КОМПЛЕКСОНОМЕТРИЯ (ХЕЛАТОМЕТРИЯ)
- § 26. Характеристика метода
- § 27. Теоретические основы комплексонометрического титрования
- § 28. Классификация методов комплексонометрического титрования
- § 29. Установка титра раствора комплексона III
- § 30. Определение содержания кальция
- § 31. Определение жесткости воды комплексонометрическим методом
- § 32. Анализ смеси ионов кальция и магния
- § 33. Определение содержания алюминия
- § 34. Раздельное определение ионов кальция и алюминия
- § 35. Раздельное определение ионов алюминия и железа
- Часть вторая. Весовой анализ
- § 1. Сущность весового анализа
- § 2. Классификация методов весового анализа
- § 3. Расчеты в весовом анализе
- Б. ТЕХНИКА ВЕСОВОГО АНАЛИЗА
- § 4. Взятие и растворение навески
- § 5. Техника осаждения
- § 6. Фильтрование и промывание осадков
- § 7. Получение весовой формы
- § 8. Взвешивание весовой формы
- В. ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
- § 9. Теоретические основы выделения осадков из растворов с помощью специфических неорганических и органических реактивов
- § 10. Требования, предъявляемые к осадкам
- § 11. Методы повышения точности весовых определений
- § 12. Теоретические обоснования выбора оптимальных условий для весового определения
- Г. ПРАКТИЧЕСКАЯ ЧАСТЬ
- § 13. Определение кристаллизационной воды в BaCl2 2H2O
- § 14. Определение сульфат-ионов или серы
- § 15. Определение ионов железа (III)
- § 16. Определение содержания кальция в карбонате кальция
- § 17. Определение содержания магния
- § 18. Определение ионов хлора в растворимых хлоридах или в хлористоводородной кислоте
- § 19. Анализ силикатов
- § 20. Анализ доломита
- § 21. Анализ бронзы и латуни
- Д. МЕТОДЫ ВЕСОВЫХ ОПРЕДЕЛЕНИЙ, ОСНОВАННЫЕ НА ПРИМЕНЕНИИ ОРГАНИЧЕСКИХ РЕАКТИВОВ
- § 22. Определение никеля
- § 23. Определение алюминия
- Часть третья. Понятие о физических и физико-химических (инструментальных) методах анализа
- § 1. Электрохимические методы
- § 2. Спектральные (оптические) методы
- § 3. Хроматографические методы
- § 4. Радиометрические методы
- § 5. Масс-спектрометрические методы
- ГЛАВА VII ЭЛЕКТРОВЕСОВЫЕ МЕТОДЫ АНАЛИЗА
- § 1. Характеристика методов электроанализа
- § 2. Химические процессы, протекающие при электролизе
- § 3. Методы электроанализа
- § 4. Электровесовой анализ
- § 5. Метод внутреннего электролиза
- § 6. Определение меди в растворе сульфата меди с применением платиновых сетчатых электродов
- § 7. Определение меди и свинца в латуни с применением платиновых сетчатых электродов
- § 8. Определение малых количеств меди методом внутреннего электролиза
- ГЛАВА VIII. ОБЪЕМНЫЕ ЭЛЕКТРОХИМИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
- § 1. Особенности объемных электрохимических методов анализа
- § 2. Кондуктометрическое титрование
- § 3. Высокочастотное титрование
- § 4. Потенциометрическое титрование
- § 5. Полярографический метод анализа
- § 6. Амперометрическоб титрование
- § 7. Кулонометрическое титрование
- ГЛАВА IX. СПЕКТРАЛЬНЫЕ (ОПТИЧЕСКИЕ) МЕТОДЫ АНАЛИЗА
- § 1. Понятие об эмиссионном спектральном анализе
- Б. КОЛОРИМЕТРИЯ
- § 2. Особенности колориметрических методов анализа
- § 3. Характеристика колориметрических методов анализа
- В. ОПТИЧЕСКИЕ МЕТОДЫ УСТАНОВЛЕНИЯ ТОЧКИ ЭКВИВАЛЕНТНОСТИ
- § 4. Спектрофотометрическое титрование
- § 5. Фототурбидиметрическое и фотонефелометрическое титрование
- Г. ЛАБОРАТОРНЫЕ РАБОТЫ
- § 6. Определение содержания ионов железа методом колориметрического титрования
- § 7. Определение содержания титана
- ГЛАВА X. МЕТОДЫ РАЗДЕЛЕНИЯ, ВЫДЕЛЕНИЯ И КОНЦЕНТРИРОВАНИЯ ОТДЕЛЬНЫХ КОМПОНЕНТОВ АНАЛИЗИРУЕМЫХ СМЕСЕЙ
- § 1. Определение следов элементов (микропримесей)
- § 2. Метод осаждения малорастворимых соединений
- § 3. Электрохимические методы разделения
- § 4. Метод экстрагирования
- § 5. Методы отгонки летучих соединений
- § 6. Хроматографические методы разделения
- § 7. Метод флотации