| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
РЕАКЦИЯ КНЕВЕНАГЕЛЯ
Эмиль Кневенагель (Emil Knoevenage, 1865-1921) родился в Ганновере (Германия). Учился в Ганноверском техническом институте, а с 1886 г. в Геттингенском университете у В. Мейера и Л. Гаттермана. В 1889 г. получил степень доктора философии и начал работать в Гейдельбергском университете. С 1896 г. доцент, а с 1900 г. профессор кафедры органической химии этого университета. Много работал в области стереоизомерии. Обстоятельно исследовал реакцию альдегидов с ацетоуксусным эфиром в присутствии первичных аминов. Изучал соединения пиридинового ряда и показал, что производные пиридина могут быть получены нагреванием 1,5-дикетонов с гидроксиламином. Занимался также проблемами неорганической и физической химии.
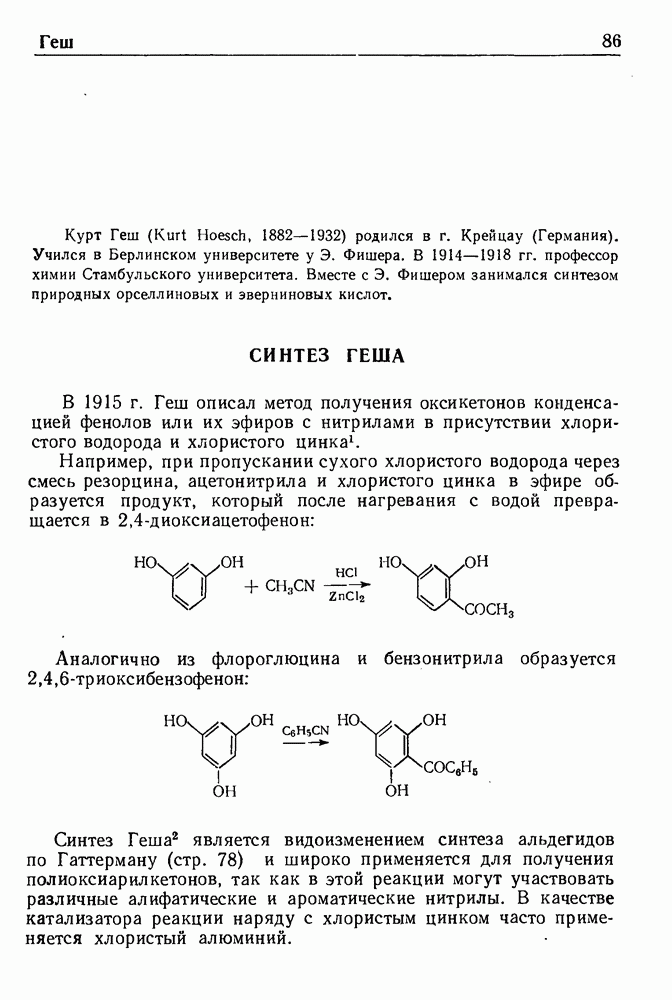
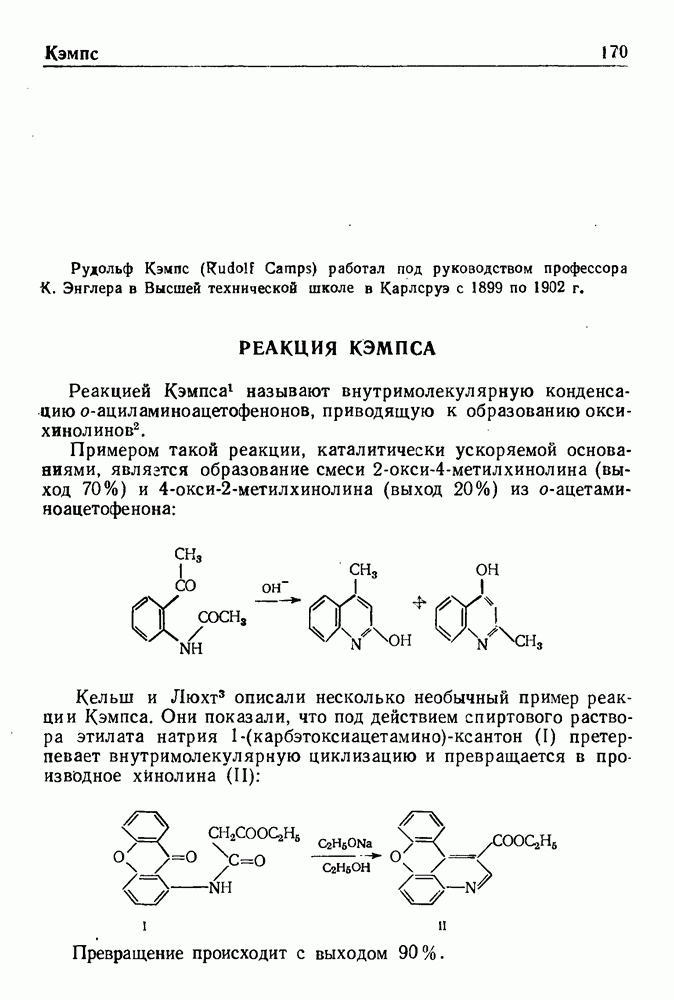
Конденсацию альдегидов или кетонов в присутствии оснований с соединениями, содержащими активные метиленовые группы, обычно называют реакцией Кневенагеля.
Эта реакция является модификацией известной реакции Перкина (стр. 201) и имеет сходный с ней механизм. Основания (первичные или вторичные амины) отщепляют протон от активной метиленовой группы, а образовавшийся карбанион реагирует с карбонильной группой альдегида или кетона. Следующая схема дает общее представление о течении реакции:

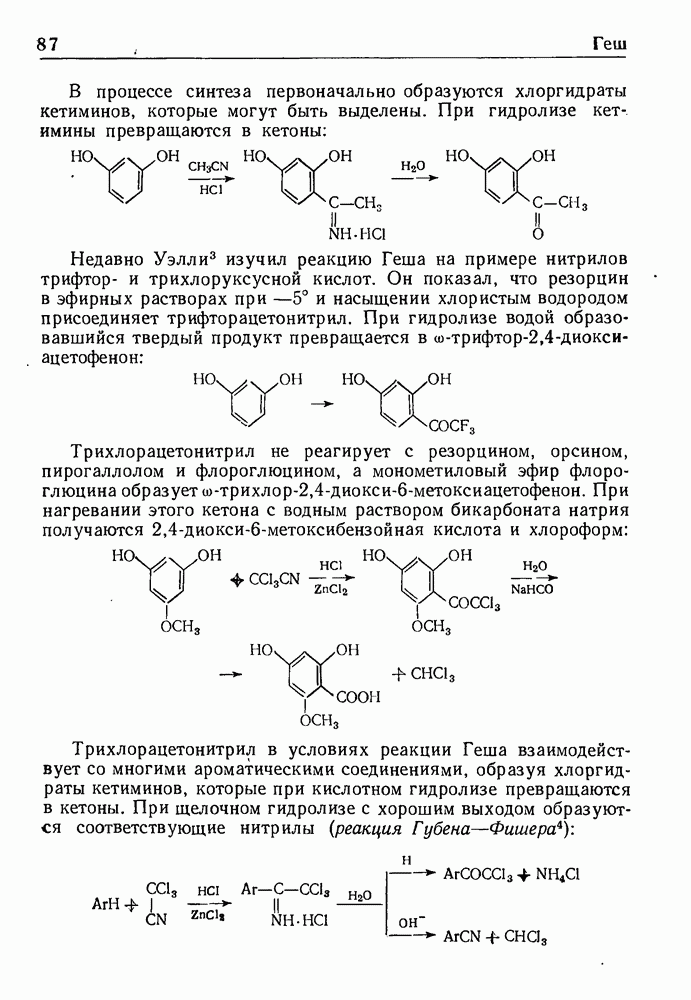
В реакции Кневенагеля могут использоваться самые различные соединения, содержащие активную метиленовую группу, а также ароматические и алифатические альдегиды и кетоны. Согласно Копу, лучшими катализаторами конденсации
алифатичёских и циклических кетонов с эфирами циануксусной кислоты являются соли аминов и аммонийные соли органических кислот. Очень эффективен в качестве катализатора также ацетамид в уксуснокислом растворе. Непрерывное удаление воды, выделяющейся в процессе реакции, приводит к получению с хорошим выходом эфиров алкилиденциануксусной кислоты. Реакция протекает по следующему уравнению:

Ароматические кетоны реагируют с этиловым эфиром циан-уксусной кислоты в присутствии уксуснокислого аммония и уксусной кислоты как конденсирующих агентов. При конденсации альдегидов с этиловым эфиром циануксусной кислоты применение пиперидина в спиртовой среде оказалось более успешным, чем использование ацетата пиперидина или ацетамида в среде уксусной кислоты.
Сравнительно недавно было показано, что уксуснокислый аммоний, добавляемый небольшими порциями, является очень эффективным катализатором конденсации диарилкетонов и некоторых малоактивных (пространственно-затрудненных) кетонов с этиловым эфиром циануксусной кислоты.
При конденсации бензофенона по этому методу выход продукта конденсации достигает 84%, т. е. значительно выше, чем получали ранее.
Позднее было описано успешное проведение реакций альдегидов или кетонов с малоновым, циануксусным и ацетоуксусным эфирами в присутствии эквимолекулярных количеств безводного  Так, в кипящем спиртовом растворе этиловый эфир бутилиденциануксусной кислоты получен с выходом 40,9%. При конденсации параформальдегида с диэтиловым эфиром малоновой кислоты в эфире (4,5 часа при 20—25°) в присутствии
Так, в кипящем спиртовом растворе этиловый эфир бутилиденциануксусной кислоты получен с выходом 40,9%. При конденсации параформальдегида с диэтиловым эфиром малоновой кислоты в эфире (4,5 часа при 20—25°) в присутствии  получается этиловый эфир метиленмалоновой кислоты с выходом 61%;
получается этиловый эфир метиленмалоновой кислоты с выходом 61%;

Побочно образуется также этиловый эфир метилендималоновой кислоты (выход 20%).
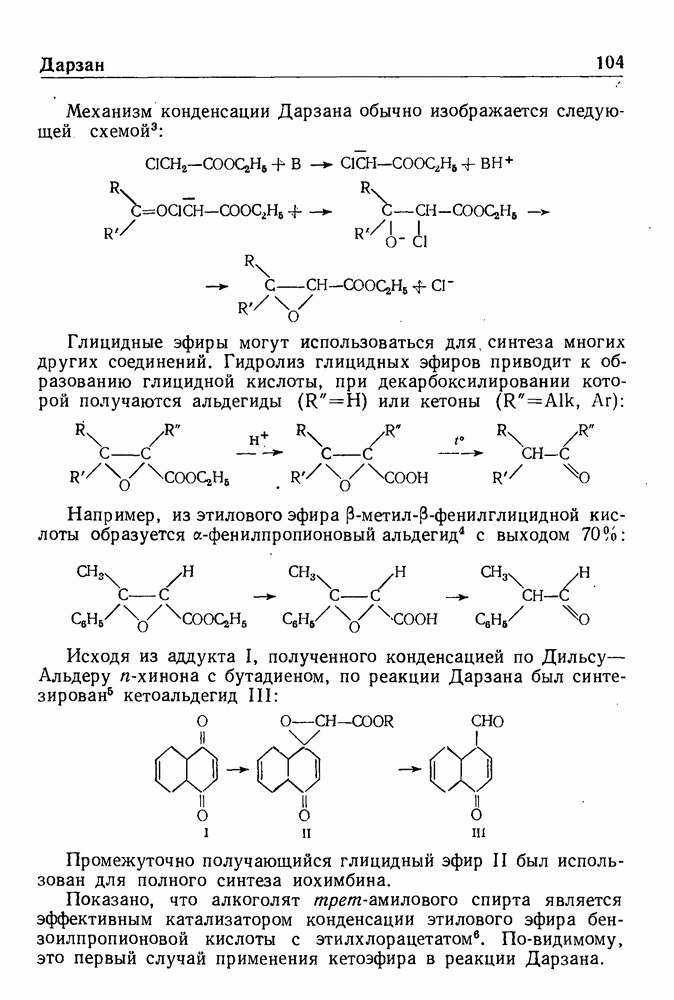
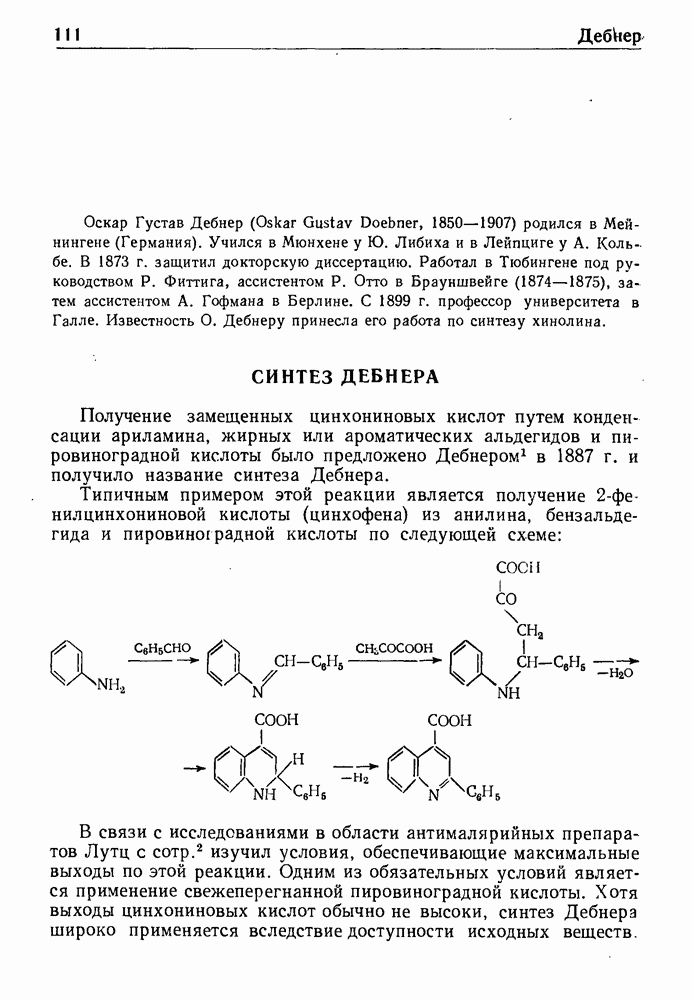
Видоизменение реакции Кневенагеля, известное под названием синтеза Дебнера, заключается в конденсации ароматических альдегидов с малоновой кислотой в присутствии пиридина и пиперидина; при этом получаются производные коричной кислоты.
ЛИТЕРАТУРА
(см. скан)
| << Предыдущий параграф | Следующий параграф >> |
- ОТ РЕДАКТОРА
- ПЕРЕГРУППИРОВКА АРБУЗОВА
- СИНТЕЗ АРНДТА—ЭЙСТЕРТА
- ОКИСЛЕНИЕ ПО БАЙЕРУ—ВИЛЛИГЕРУ
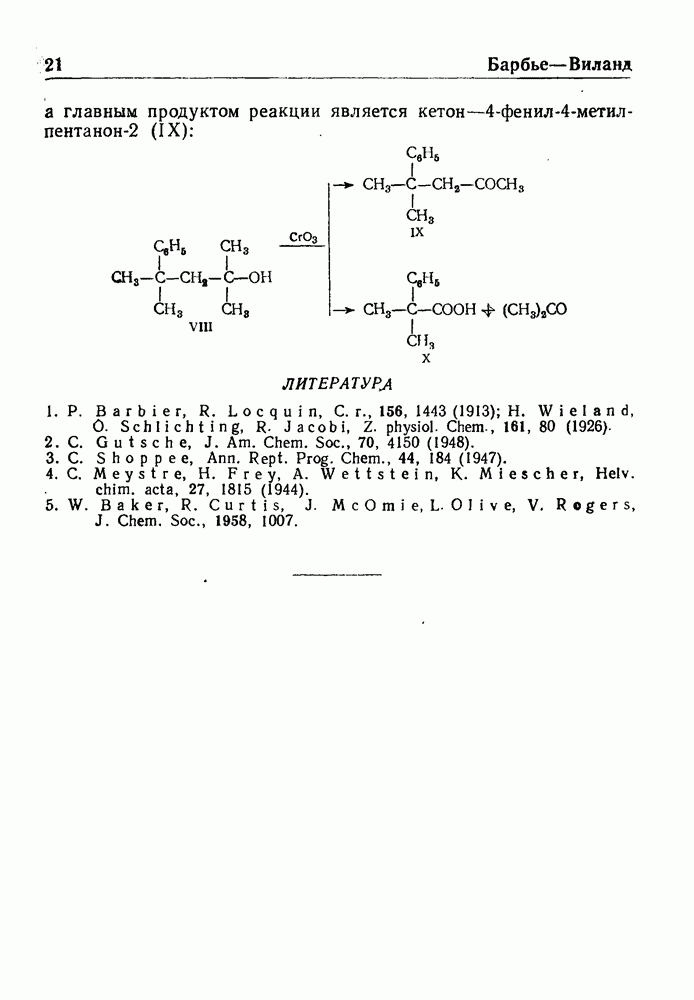
- РАСЩЕПЛЕНИЕ ПО БАРБЬЕ—ВИЛАНДУ
- РЕАКЦИЯ БАРТА
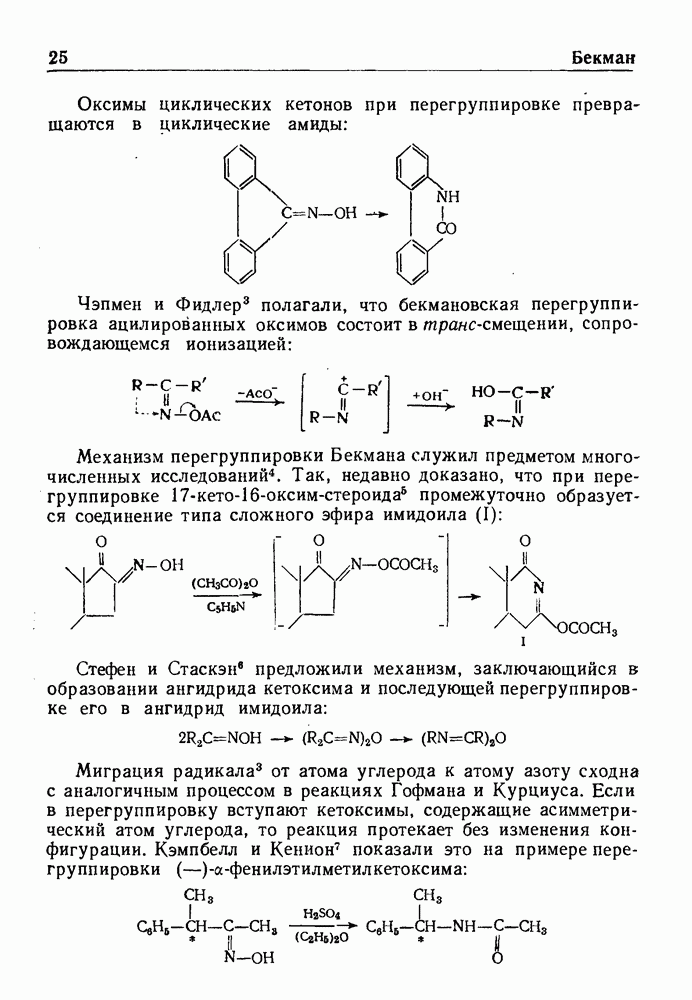
- ПЕРЕГРУППИРОВКА БЕКМАНА
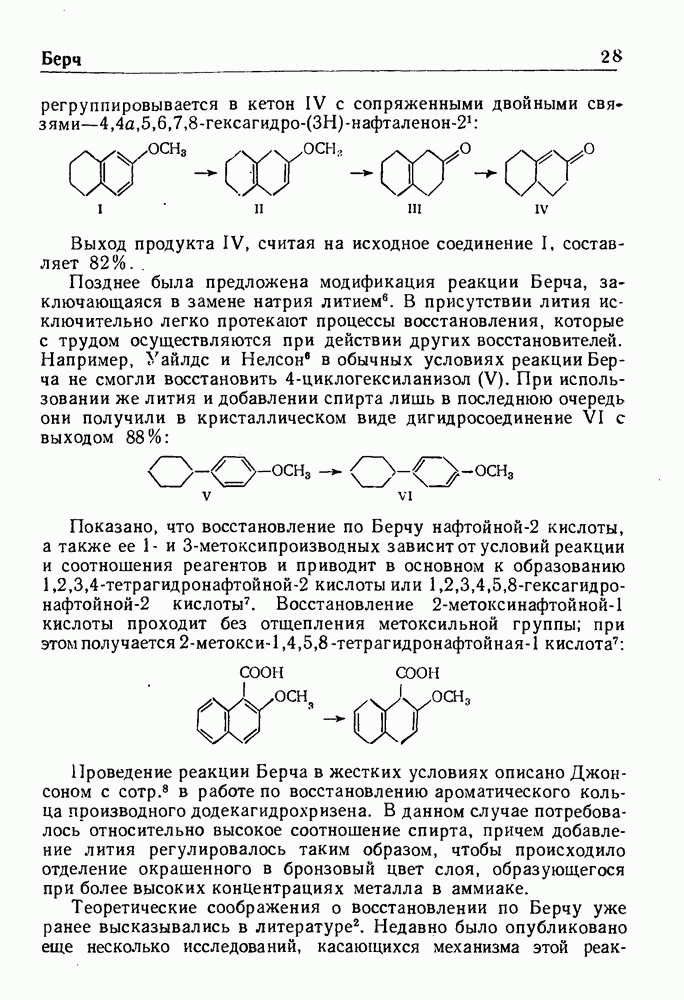
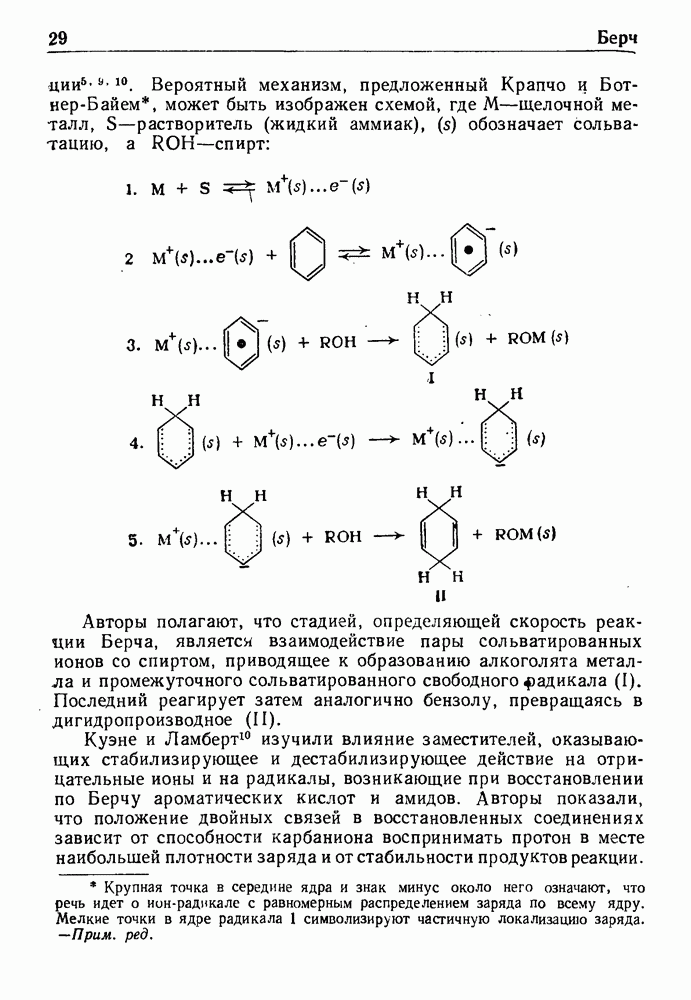
- ВОССТАНОВЛЕНИЕ ПО БЕРНУ
- ВОССТАНОВЛЕНИЕ ПО БЕШАНУ
- РЕАКЦИЯ БИШЛЕРА—НАПИРАЛЬСКОГО
- ХЛОРМЕТИЛИРОВАНИЕ ПО БЛАНУ
- РЕАКЦИЯ БРАУНА
- РАСЩЕПЛЕНИЕ АМИНОВ ПО БРАУНУ
- ВОССТАНОВЛЕНИЕ ПО БУВО—БЛАНУ
- СИНТЕЗ АЛЬДЕГИДОВ ПО БУВО
- РЕАКЦИЯ БУХЕРЕРА
- СИНТЕЗ ГИДАНТОИНОВ ПО БУХЕРЕРУ
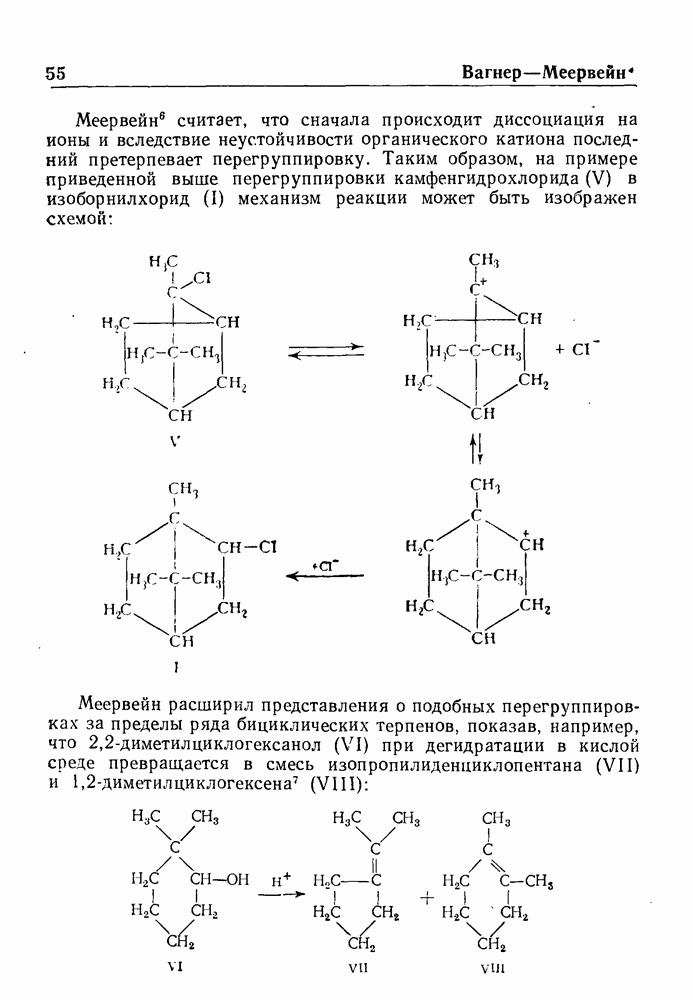
- ПЕРЕГРУППИРОВКА ВАГНЕРА—МЕЕРВЕЙНА
- РЕАКЦИЯ ВАЛЛАХА
- РЕАКЦИЯ ВИЛЬГЕРОДТА
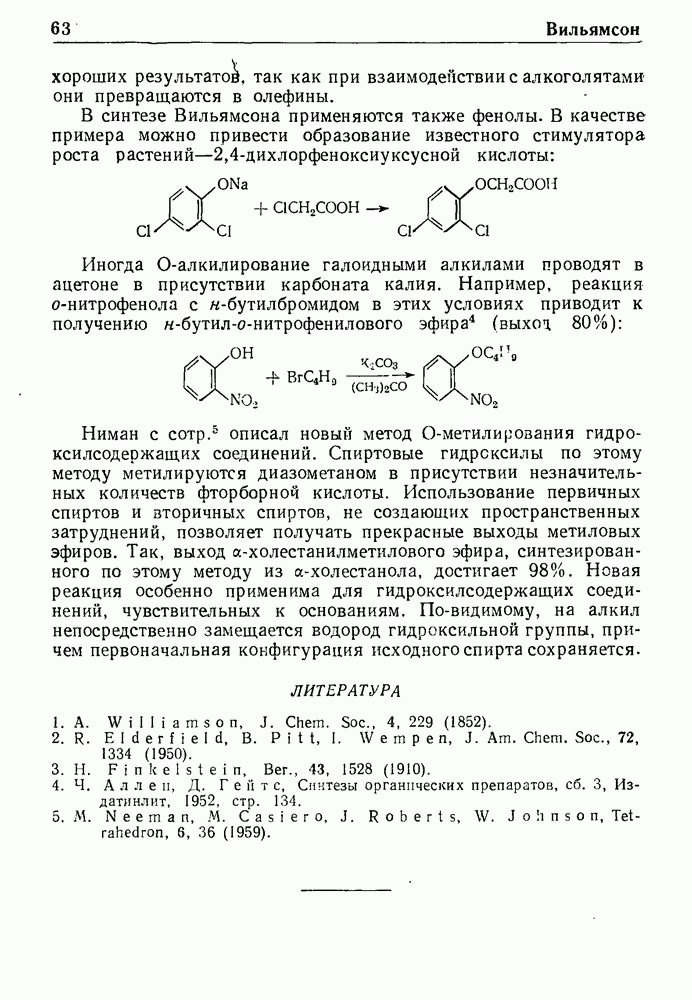
- СИНТЕЗ ВИЛЬЯМСОНА
- РЕАКЦИЯ ВИТТИГА
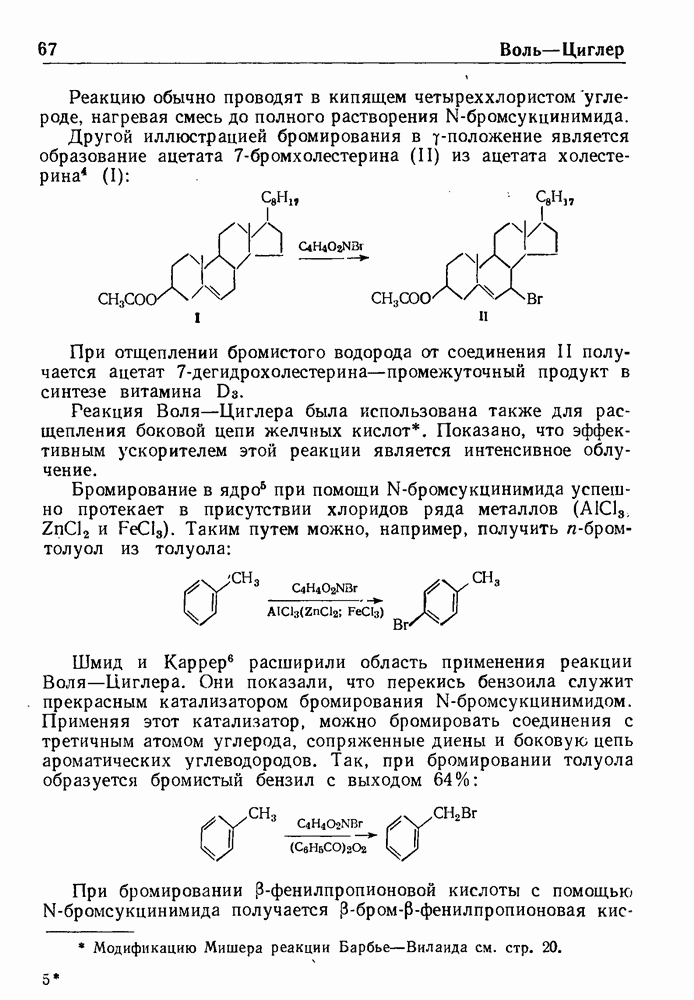
- РЕАКЦИЯ ВОЛЯ-ЦИГЛЕРА
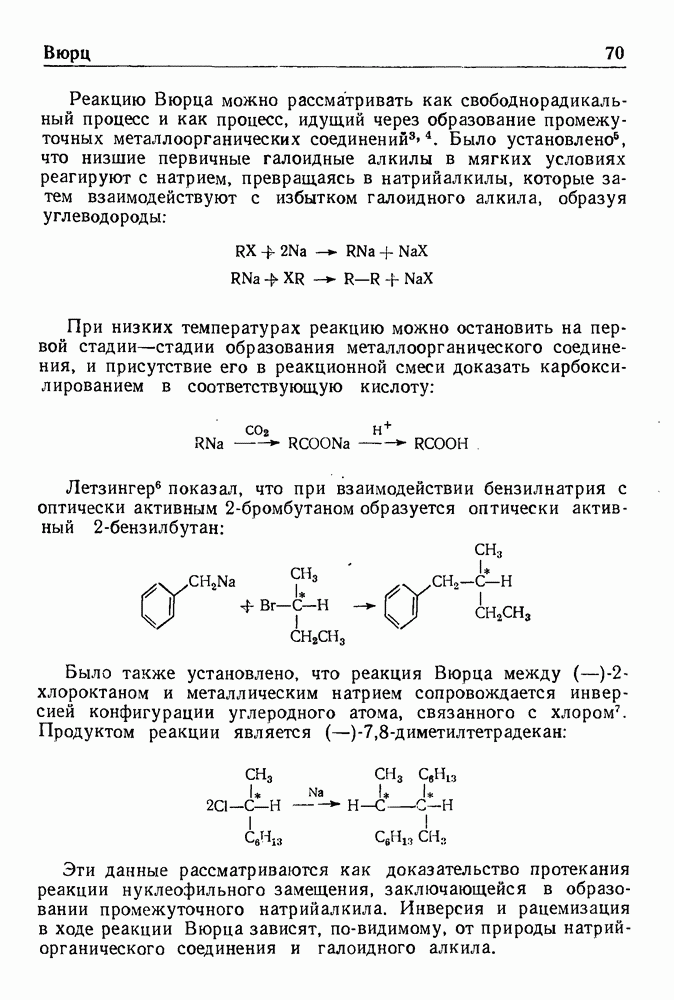
- РЕАКЦИЯ ВЮРЦА
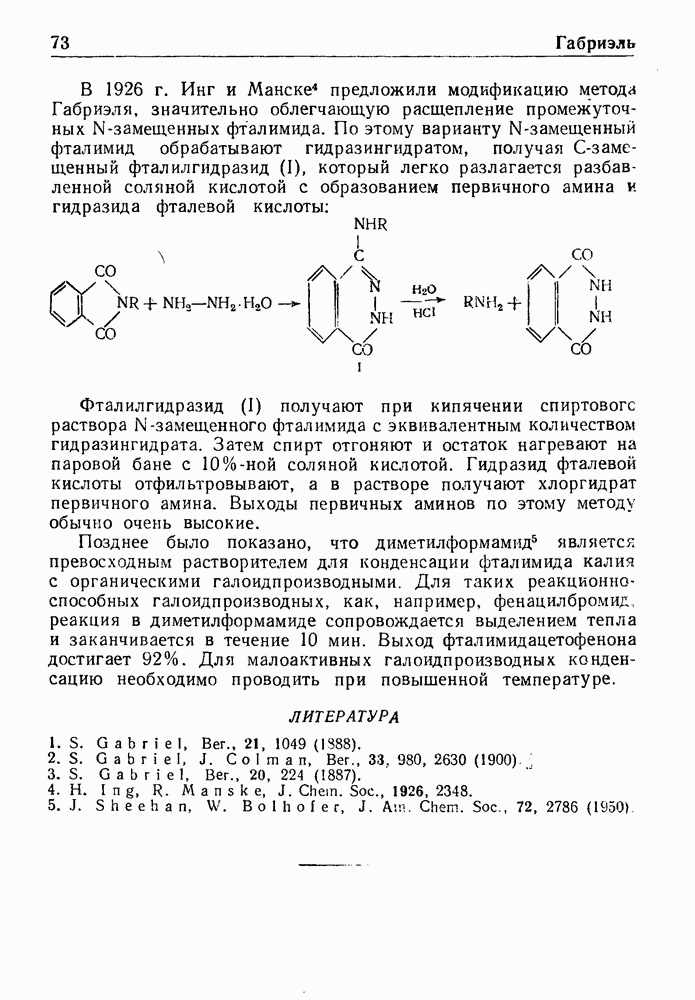
- СИНТЕЗ ГАБРИЭЛЯ
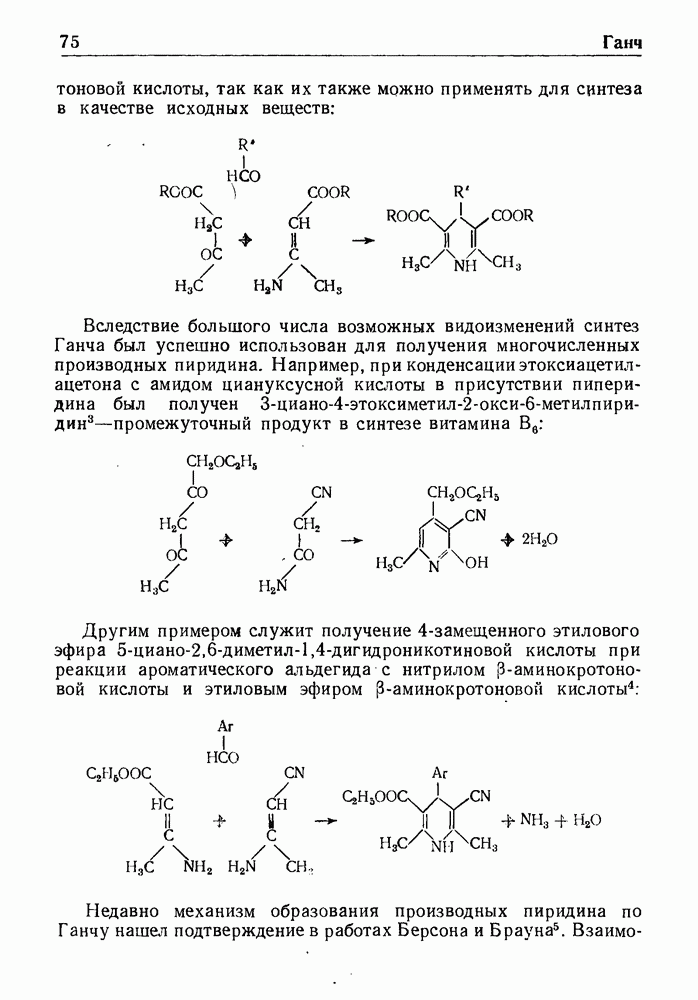
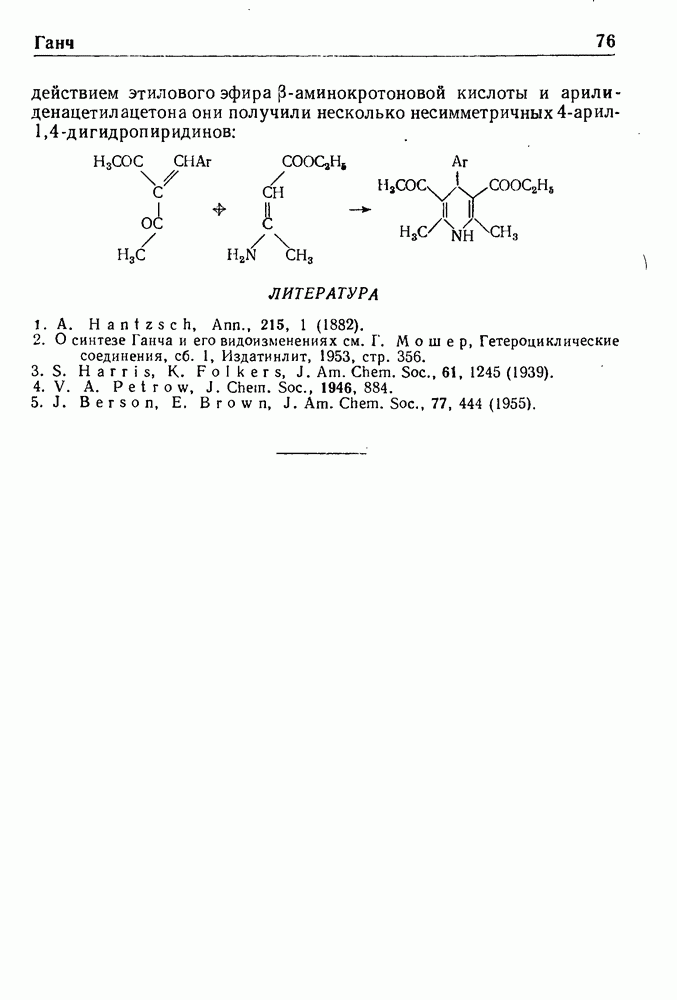
- СИНТЕЗ ГАНЧА
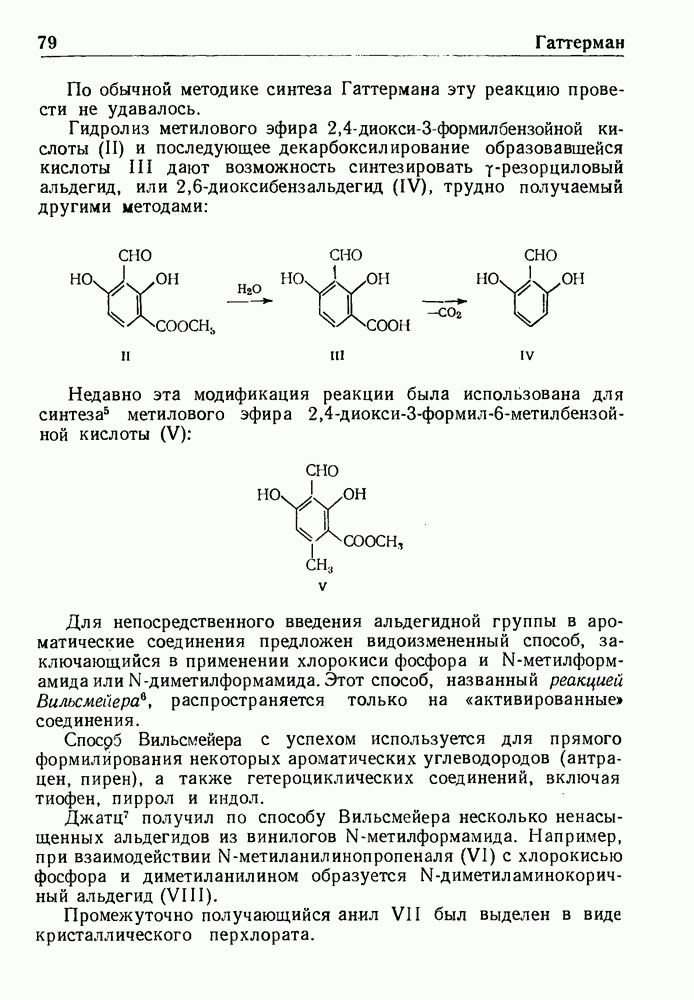
- РЕАКЦИЯ ГАТТЕРМАНА
- СИНТЕЗ АЛЬДЕГИДОВ ПО ГАТТЕРМАНУ
- РЕАКЦИЯ ГАТТЕРМАНА—КОХА
- РЕАКЦИЯ ГЕЛЛЯ—ФОЛЬГАРДА—ЗЕЛИНСКОГО
- СИНТЕЗ ГЕША
- РЕАКЦИЯ ГОМБЕРГА—БАХМАНА—ХЕЯ
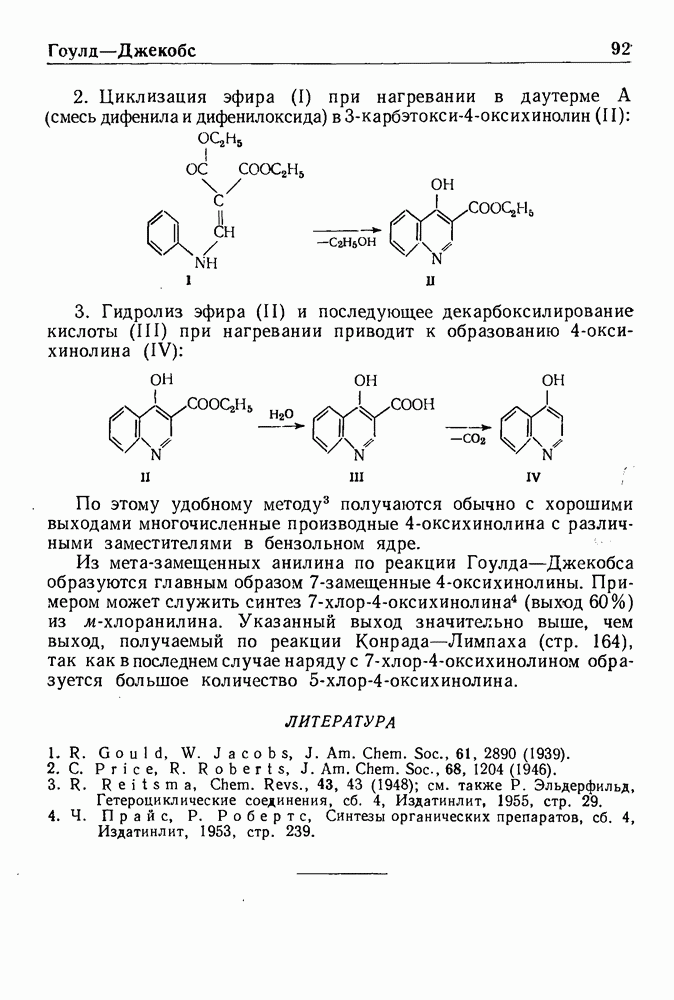
- РЕАКЦИЯ ГОУЛДА—ДЖЕКОБСА
- ПЕРЕГРУППИРОВКА ГОФМАНА
- РАСЩЕПЛЕНИЕ ПО ГОФМАНУ
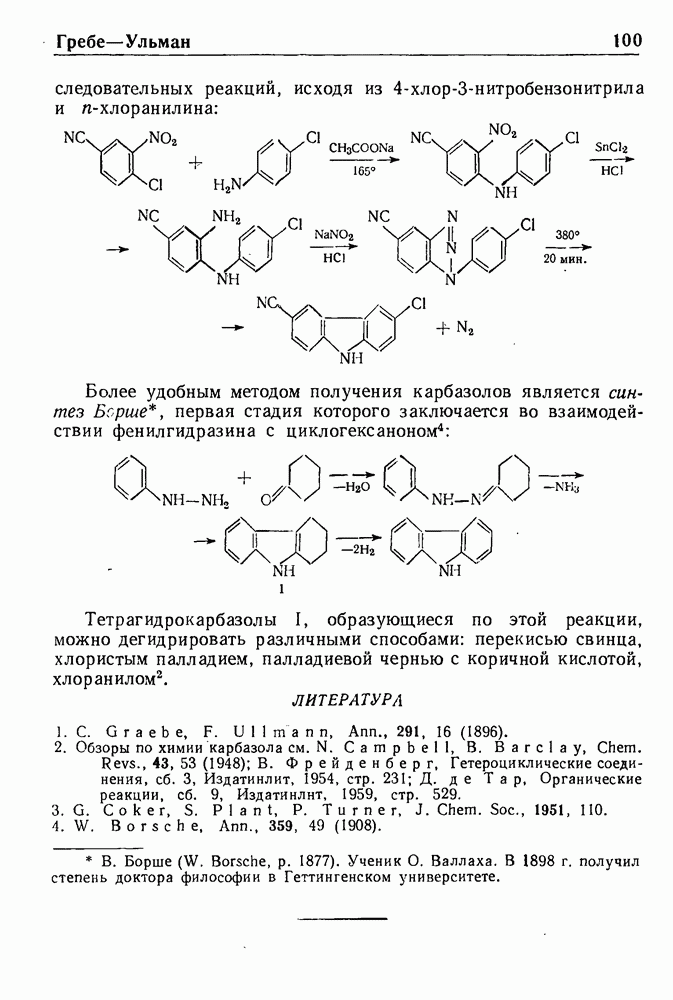
- СИНТЕЗ ГРЕБЕ—УЛЬМАНА
- РЕАКЦИЯ ГРИНЬЯРА
- СИНТЕЗ ГЛИЦИДНЫХ ЭФИРОВ ПО ДАРЗАНУ
- СИНТЕЗ НЕПРЕДЕЛЬНЫХ КЕТОНОВ ПО ДАРЗАНУ
- РЕАКЦИЯ ДАФФА
- СИНТЕЗ ДЕБНЕРА
- СИНТЕЗ ДЕБНЕРА—МИЛЛЕРА
- РЕАКЦИЯ ДЕЛЕПИНА
- РЕАКЦИЯ ДИКМАНА
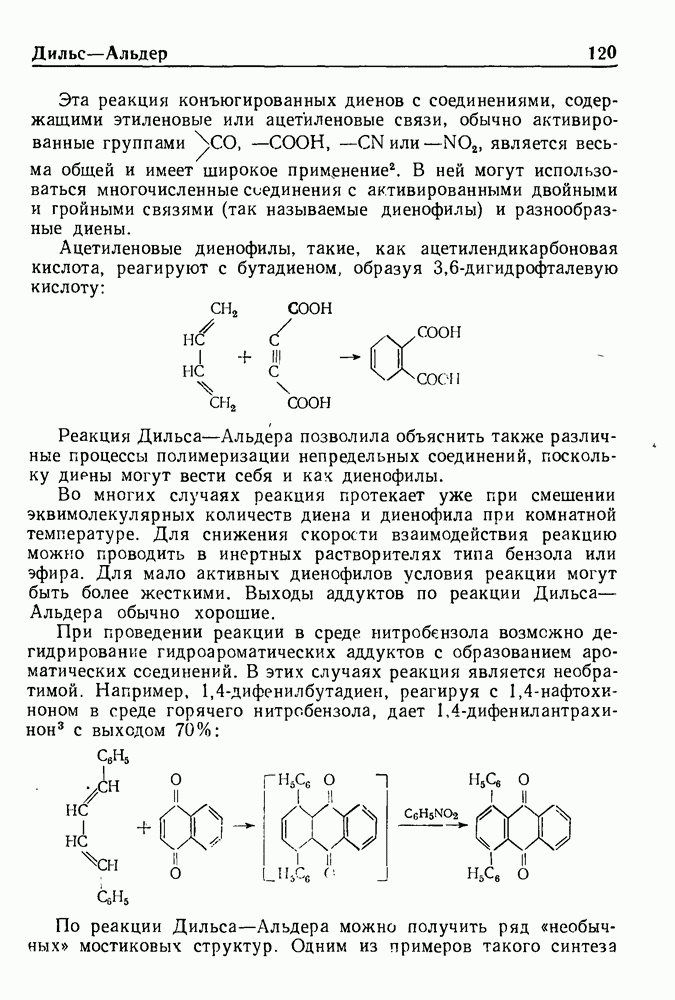
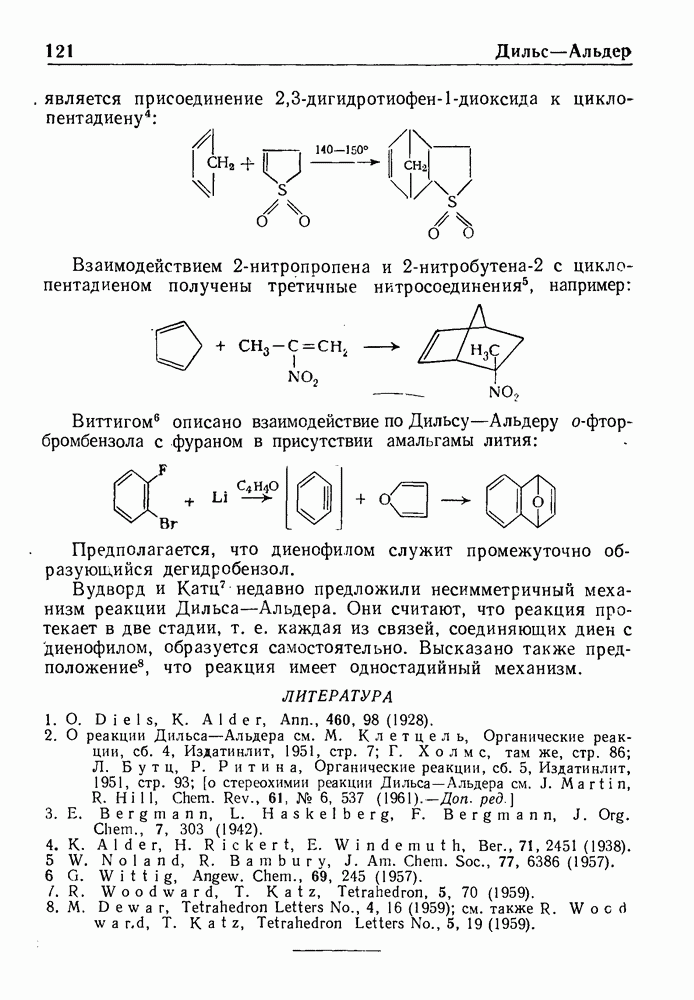
- РЕАКЦИЯ ДИЛЬСА-АЛЬДЕРА
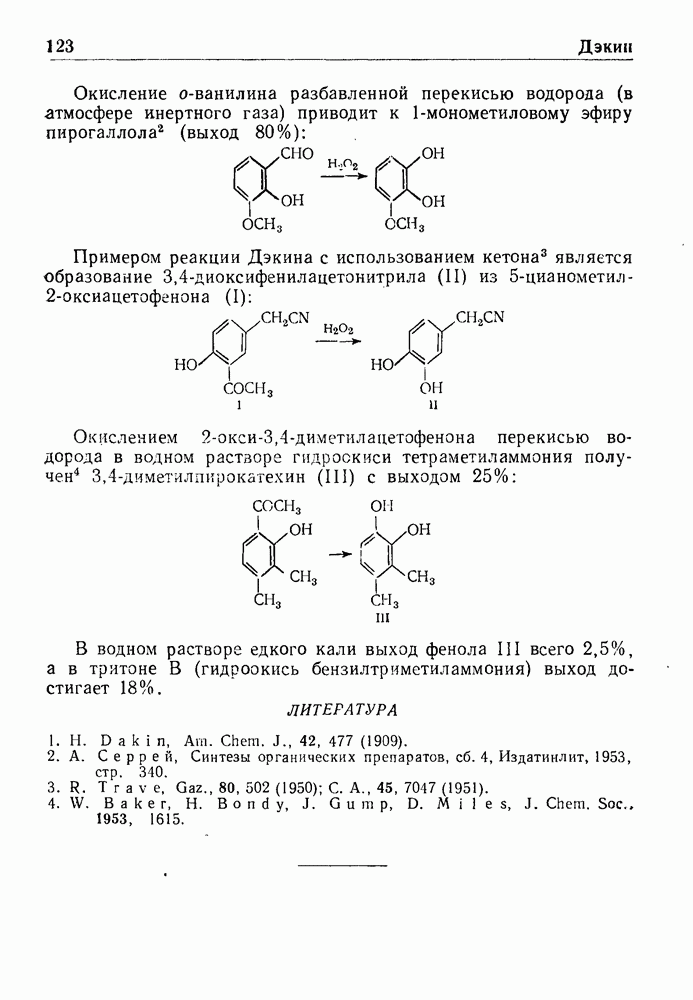
- РЕАКЦИЯ ДЭКИНА
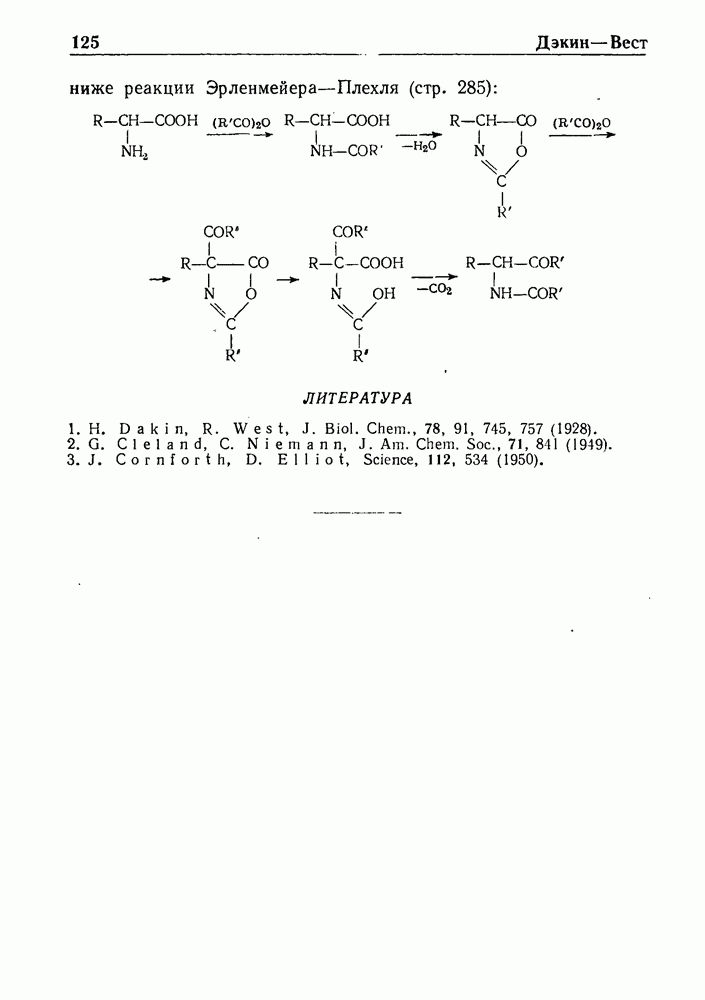
- РЕАКЦИЯ ДЭКИНА—ВЕСТА
- РЕАКЦИЯ ЗАНДМЕЙЕРА
- РЕАКЦИЯ ИВАНОВА
- РЕАКЦИЯ ИОЦИЧА
- РЕАКЦИЯ КАННИЦЦАРО
- РЕАКЦИЯ КИЖНЕРА
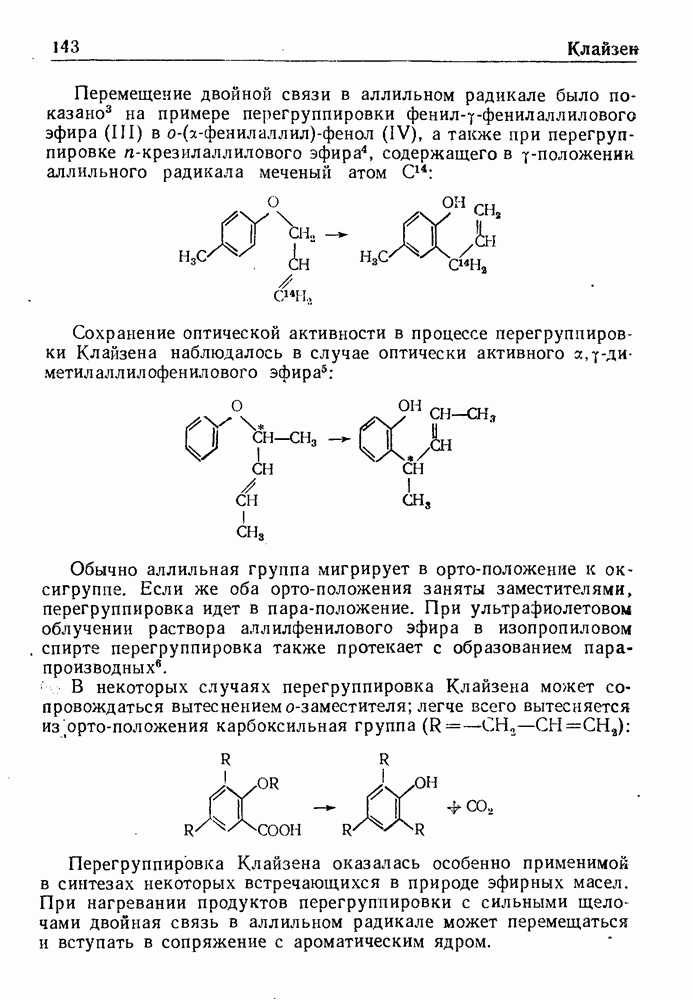
- КОНДЕНСАЦИЯ КЛАЙЗЕНА
- ПЕРЕГРУППИРОВКА КЛАЙЗЕНА
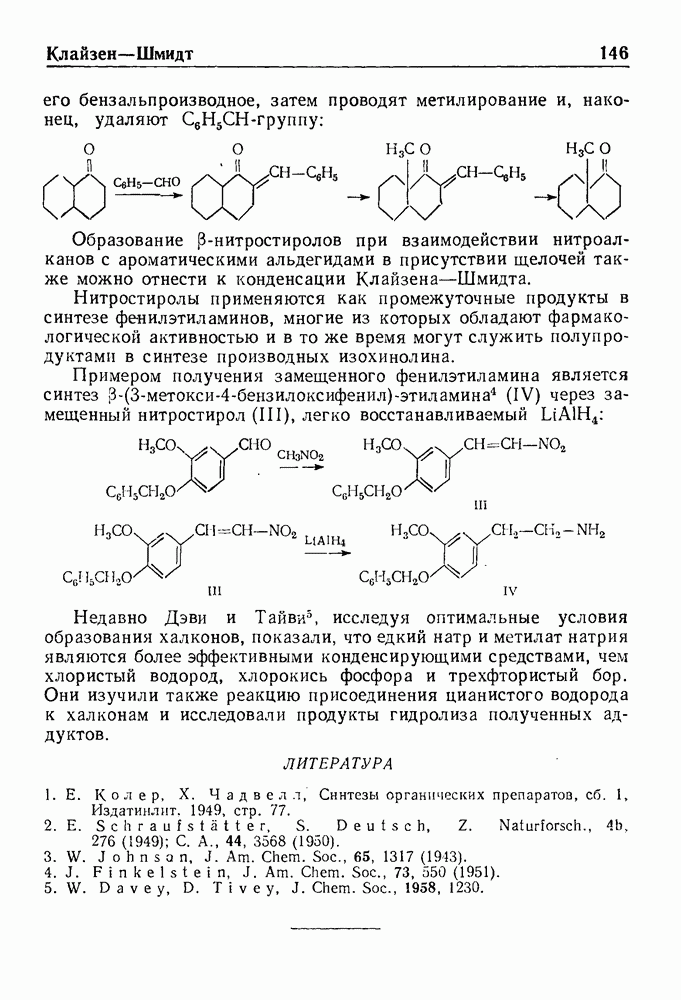
- КОНДЕНСАЦИЯ КЛАЙЗЕНА—ШМИДТА
- ВОССТАНОВЛЕНИЕ ПО КЛЕММЕНСЕНУ
- РЕАКЦИЯ КНЕВЕНАГЕЛЯ
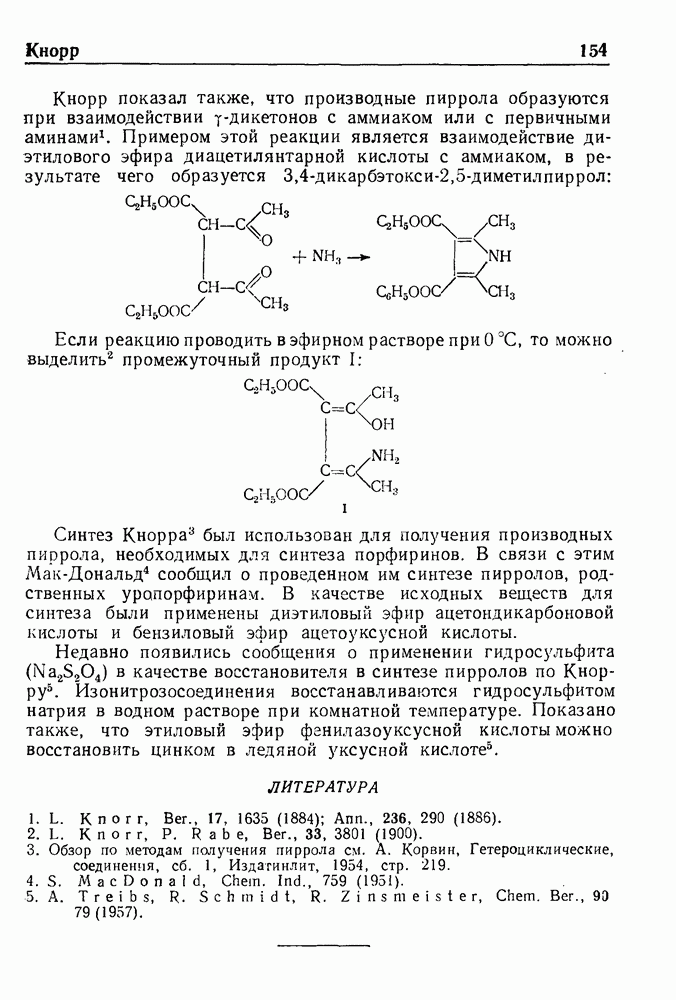
- СИНТЕЗ КНОРРА
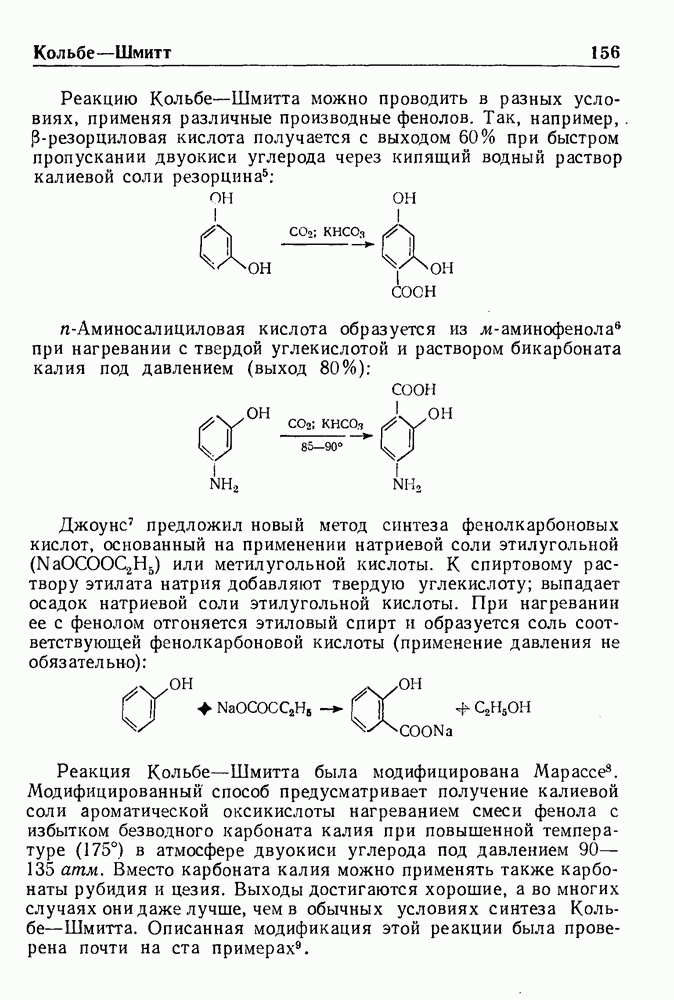
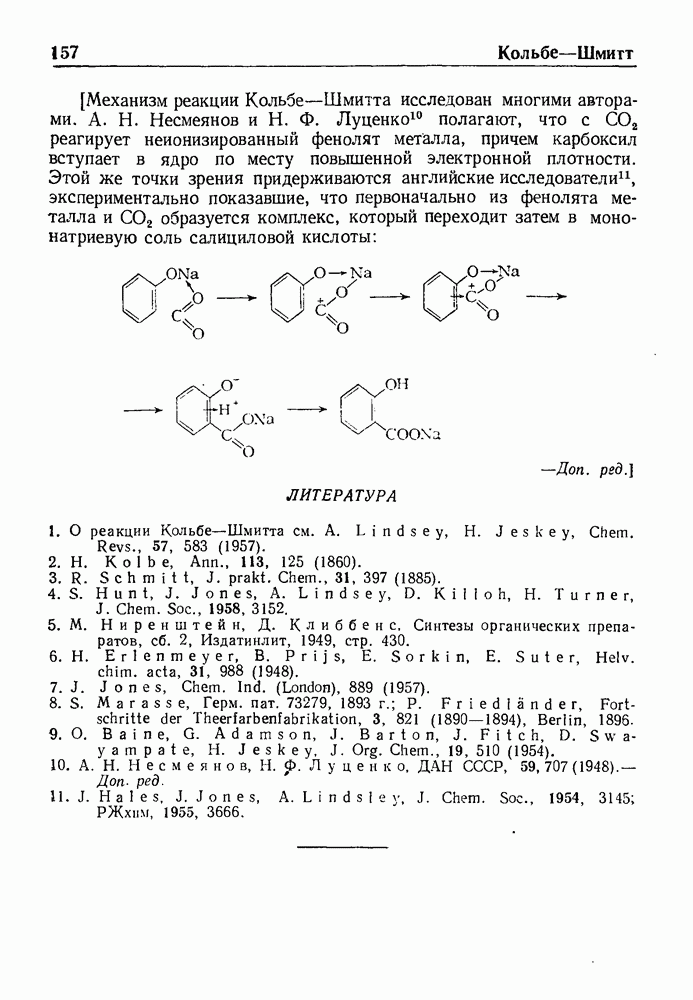
- РЕАКЦИЯ КОЛЬБЕ—ШМИТТА
- ЭЛЕКТРОХИМИЧЕСКАЯ РЕАКЦИЯ КОЛЬБЕ
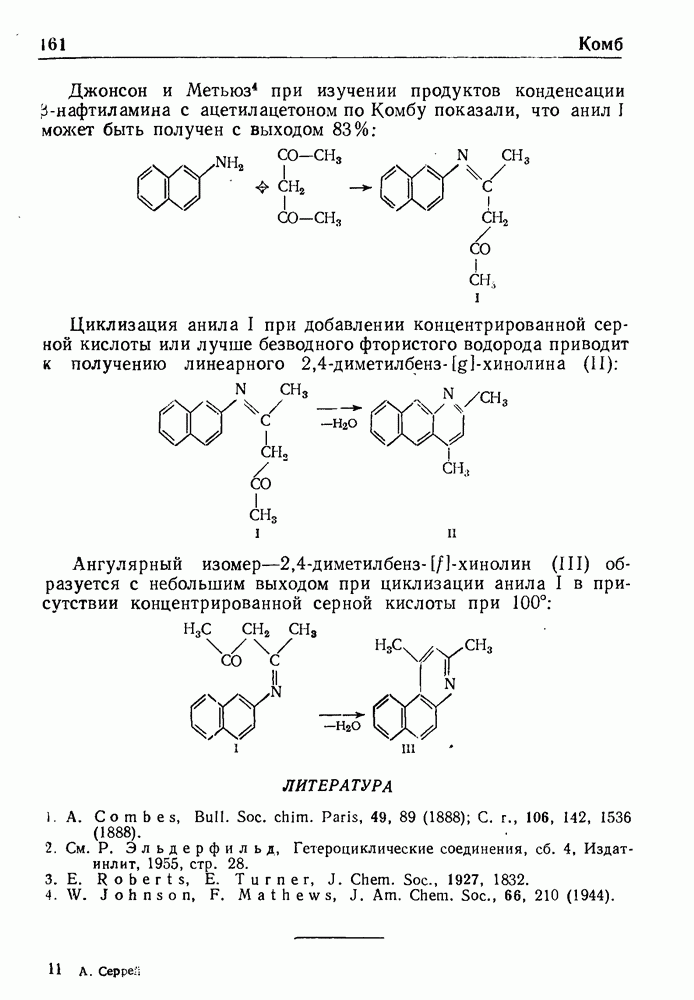
- СИНТЕЗ ХИНОЛИНА ПО КОМБУ
- РЕАКЦИЯ КОНОВАЛОВА
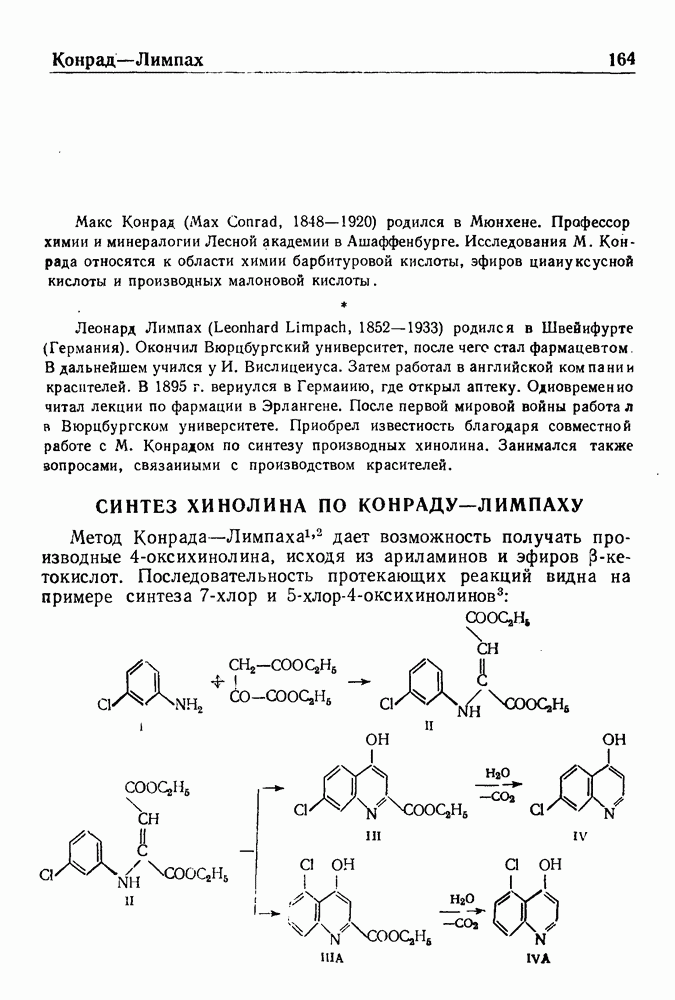
- СИНТЕЗ ХИНОЛИНА ПО КОНРАДУ—ЛИМПАХУ
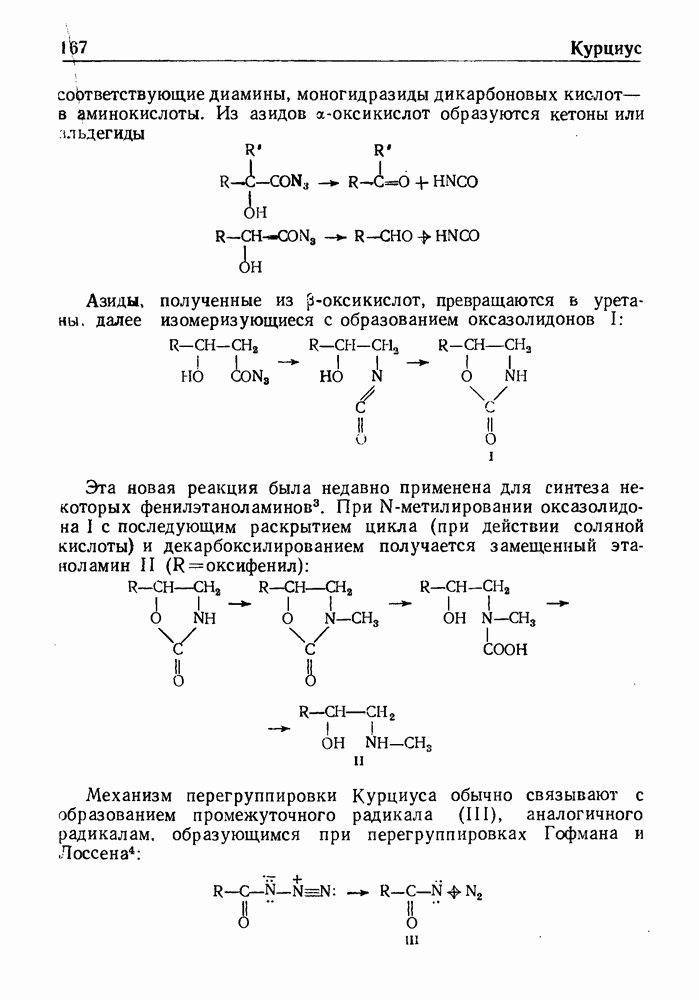
- РЕАКЦИЯ КУРЦИУСА
- РЕАКЦИЯ КУЧЕРОВА
- РЕАКЦИЯ КЭМПСА
- РЕАКЦИЯ ЛЕЙКАРТА
- РЕАКЦИЯ ЛОССЕНА
- ВОССТАНОВЛЕНИЕ ПО МАК ФАДИЕНУ—СТИВЕНСУ
- РЕАКЦИЯ МАННИХА
- КОНДЕНСАЦИЯ МЕЕРВЕЙНА
- ВОССТАНОВЛЕНИЕ ПО МЕЕРВЕЙНУ-ПОННДОРФУ-ВЕРЛЕЮ
- РЕАКЦИЯ МИХАЭЛЯ
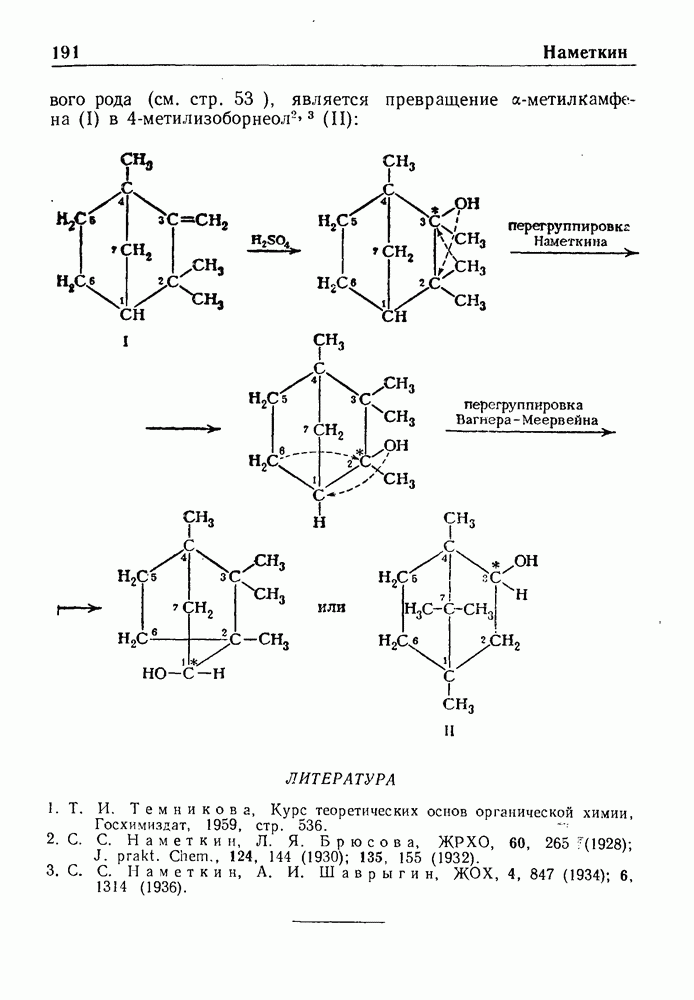
- ПЕРЕГРУППИРОВКА НАМЕТКИНА
- РЕАКЦИЯ НЕСМЕЯНОВА
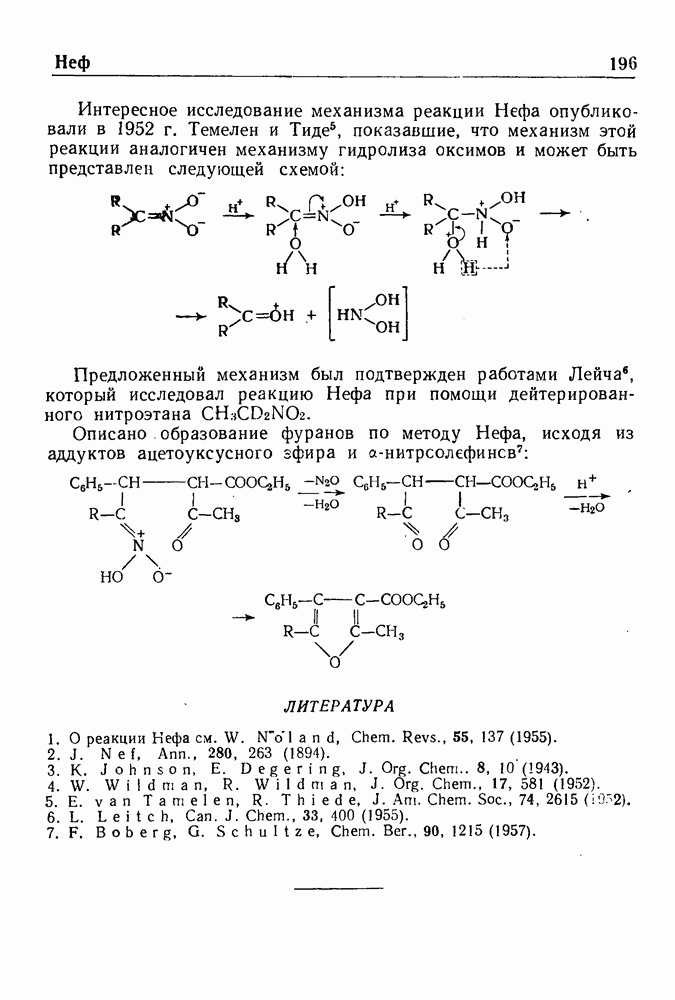
- РЕАКЦИЯ НЕФА
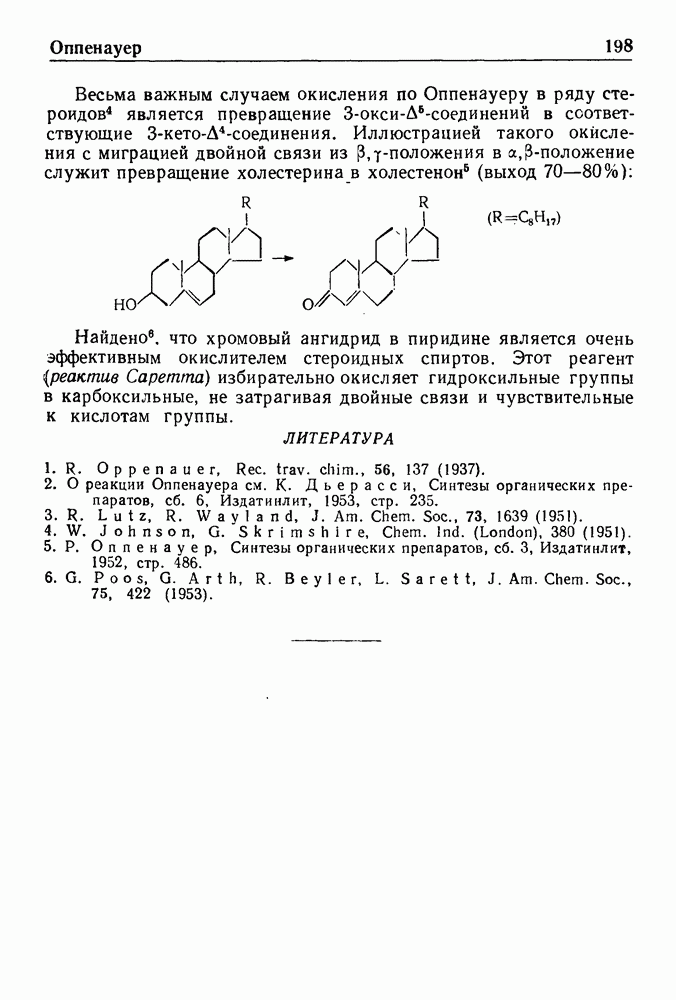
- ОКИСЛЕНИЕ ПО ОППЕНАУЕРУ
- РЕАКЦИЯ ПАССЕРИНИ
- РЕАКЦИЯ ПЕРКИНА
- КОНДЕНСАЦИЯ ПЕХМАНА
- РЕАКЦИЯ ПИКТЭ—ШПЕНГЛЕРА
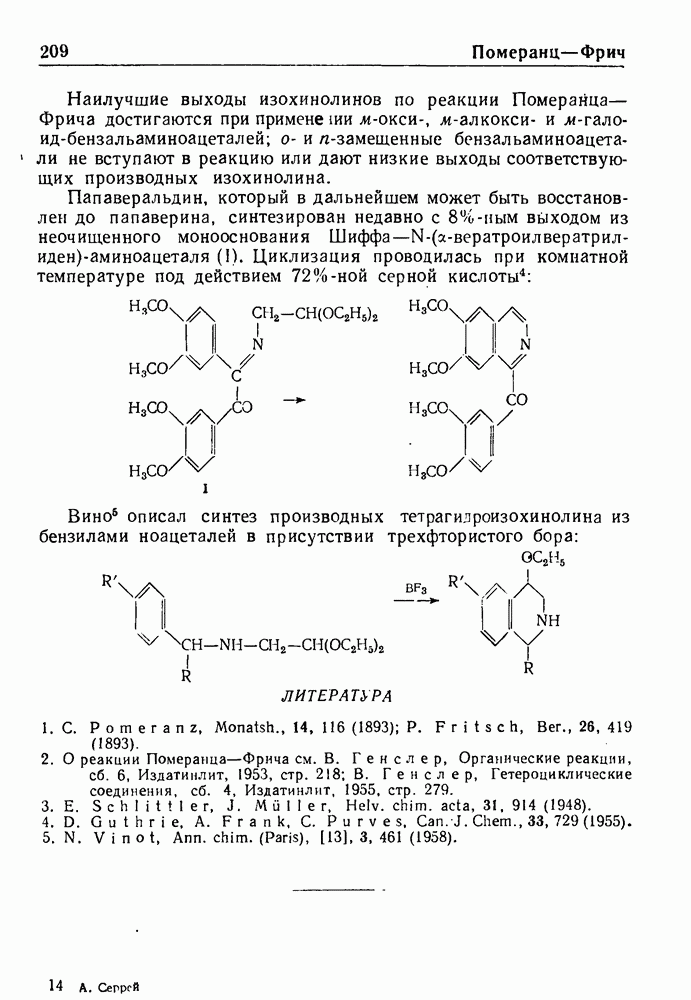
- РЕАКЦИЯ ПОМЕРАНЦА—ФРИЧА
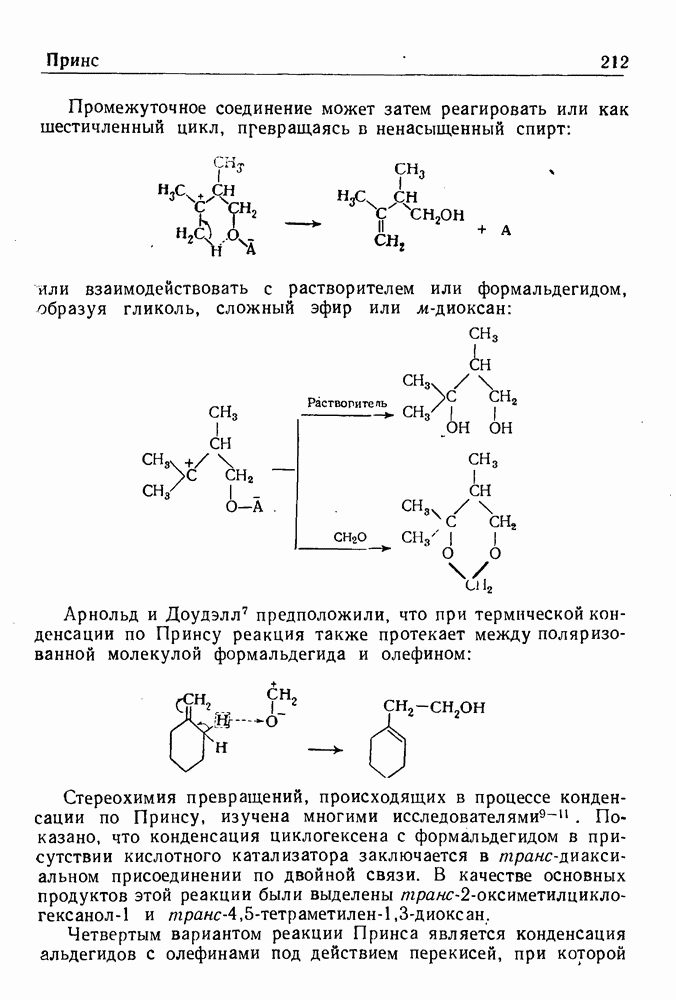
- РЕАКЦИЯ ПРИНСА
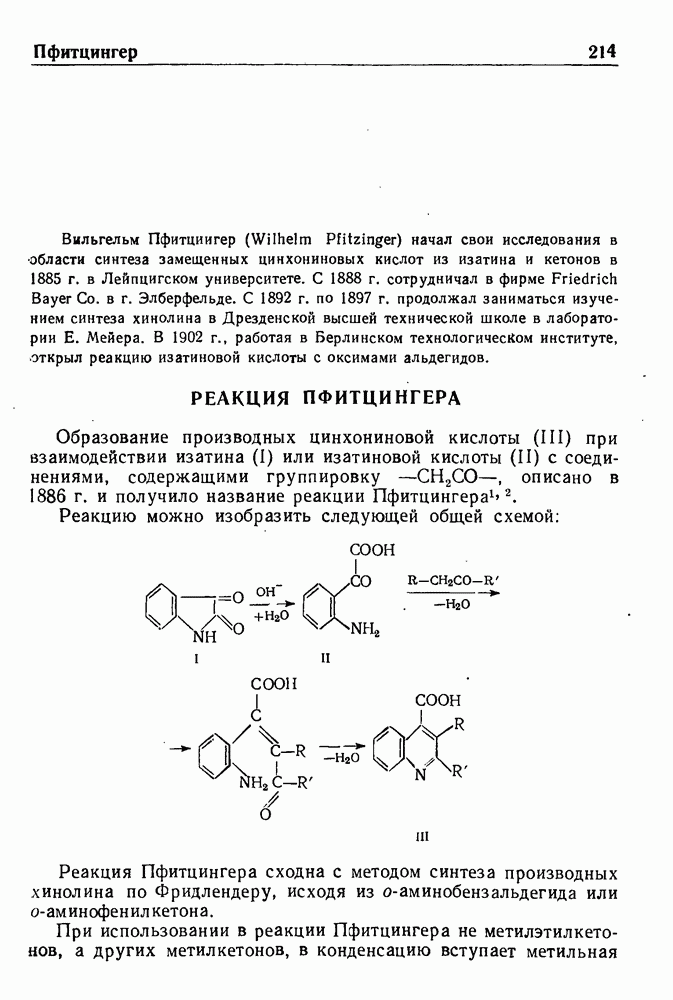
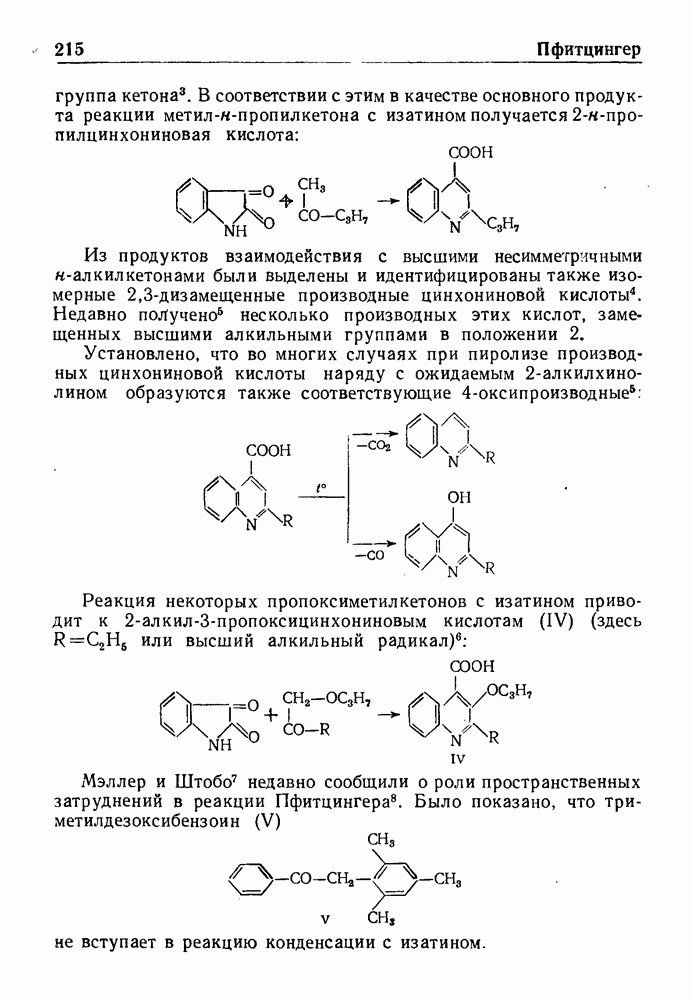
- РЕАКЦИЯ ПФИТЦИНГЕРА
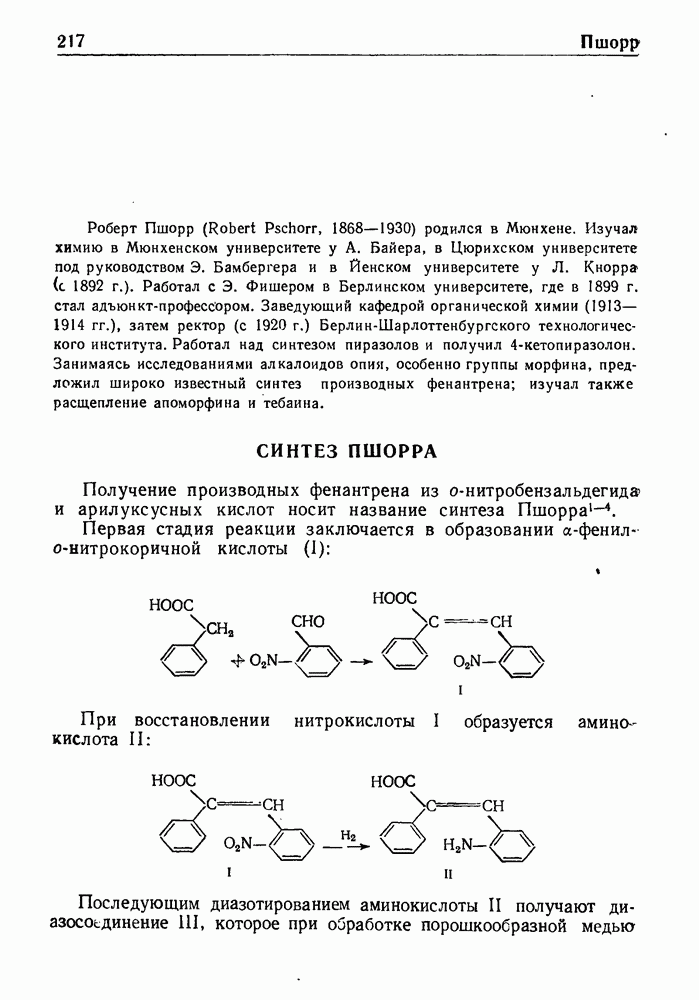
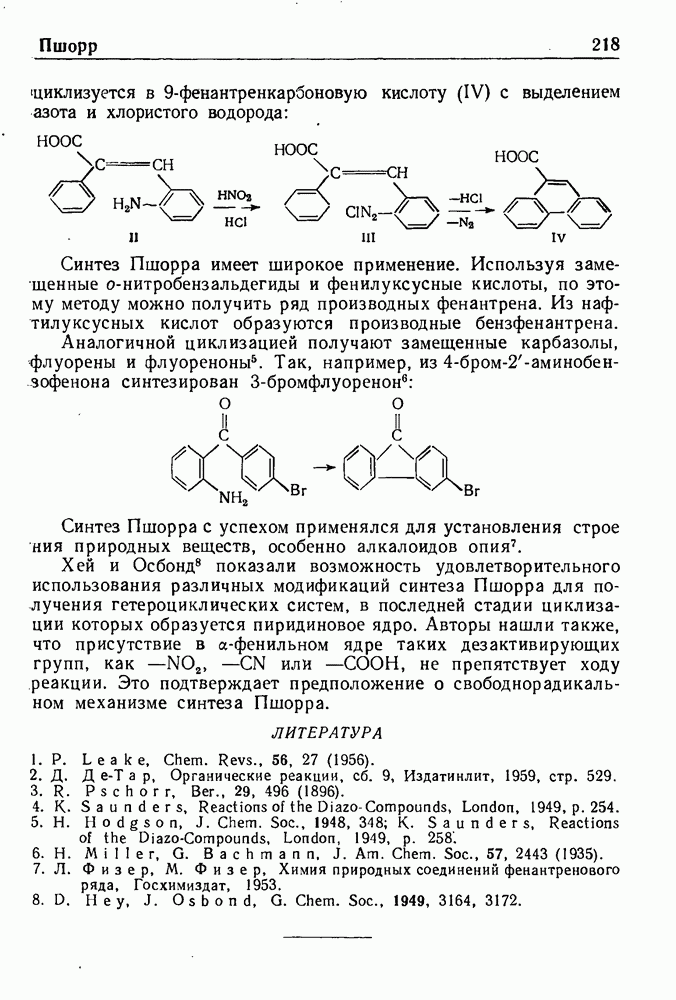
- СИНТЕЗ ПШОРРА
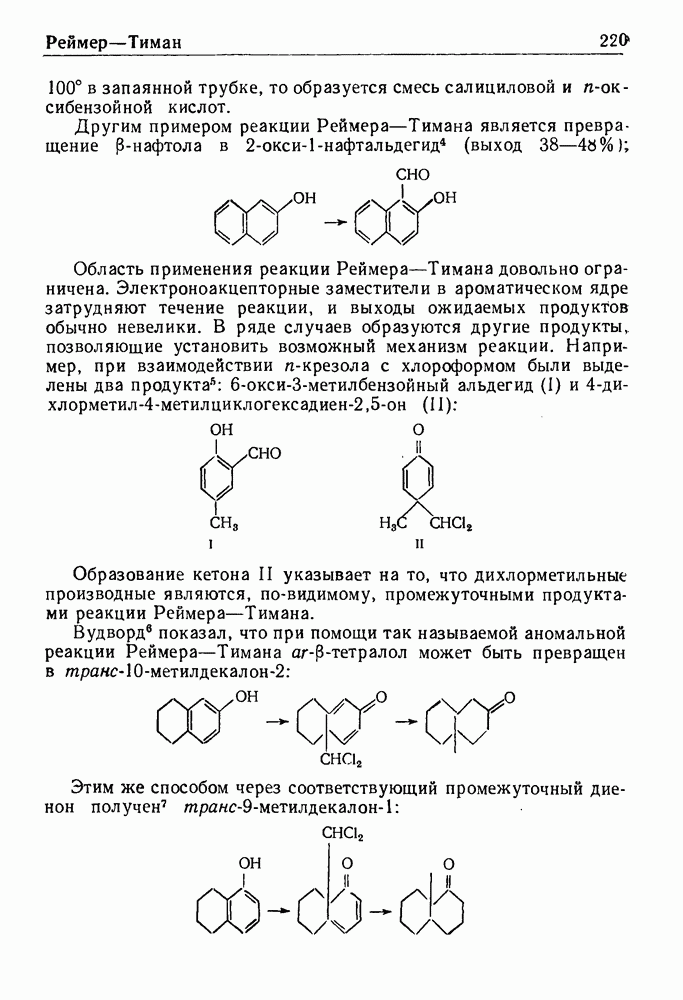
- РЕАКЦИЯ РЕЙМЕРА—ТИМАНА
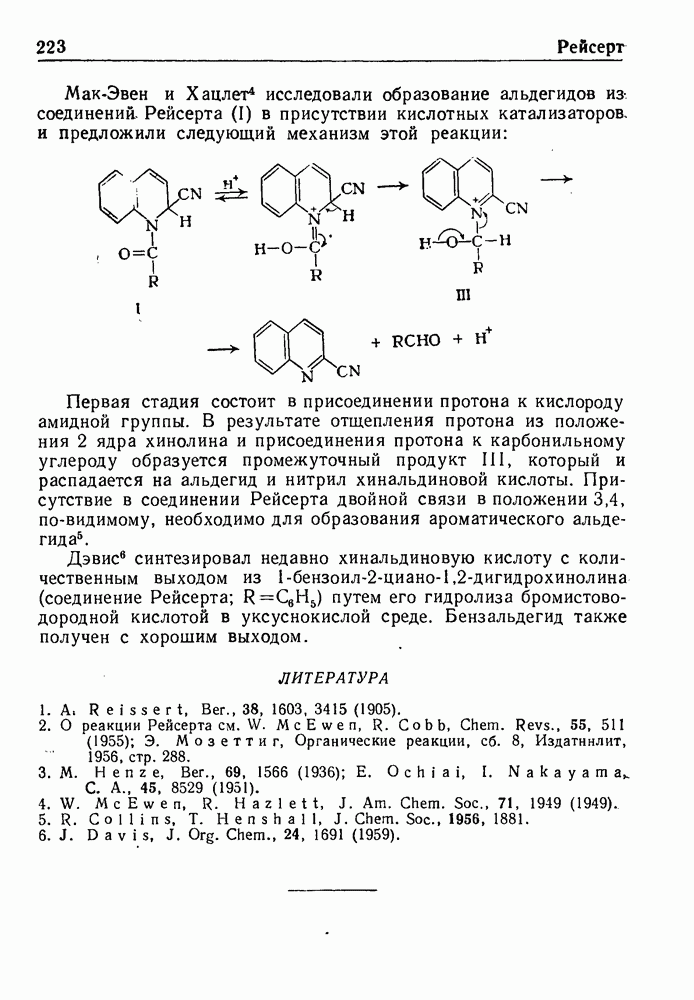
- РЕАКЦИЯ РЕЙСЕРТА
- РЕАКЦИЯ РЕФОРМАТСКОГО
- РЕАКЦИЯ РОДИОНОВА
- ВОССТАНОВЛЕНИЕ ПО РОЗЕНМУНДУ
- РЕАКЦИЯ СКРАУПА
- РЕАКЦИЯ СОММЛЕ
- РЕАКЦИЯ СТЕФЕНА
- ПЕРЕГРУППИРОВКА СТИВЕНСА
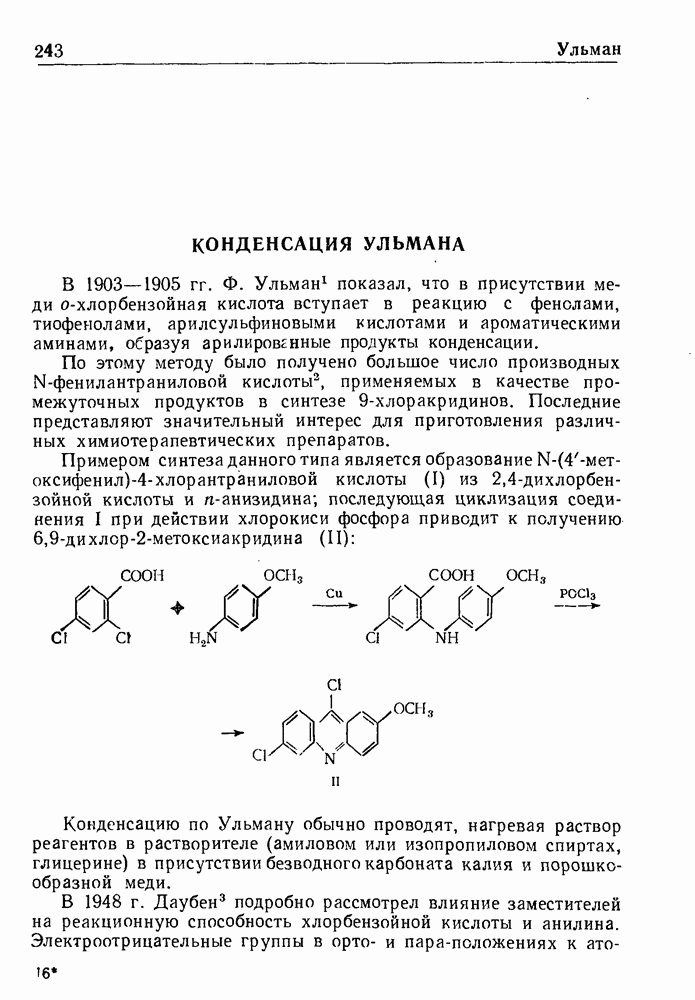
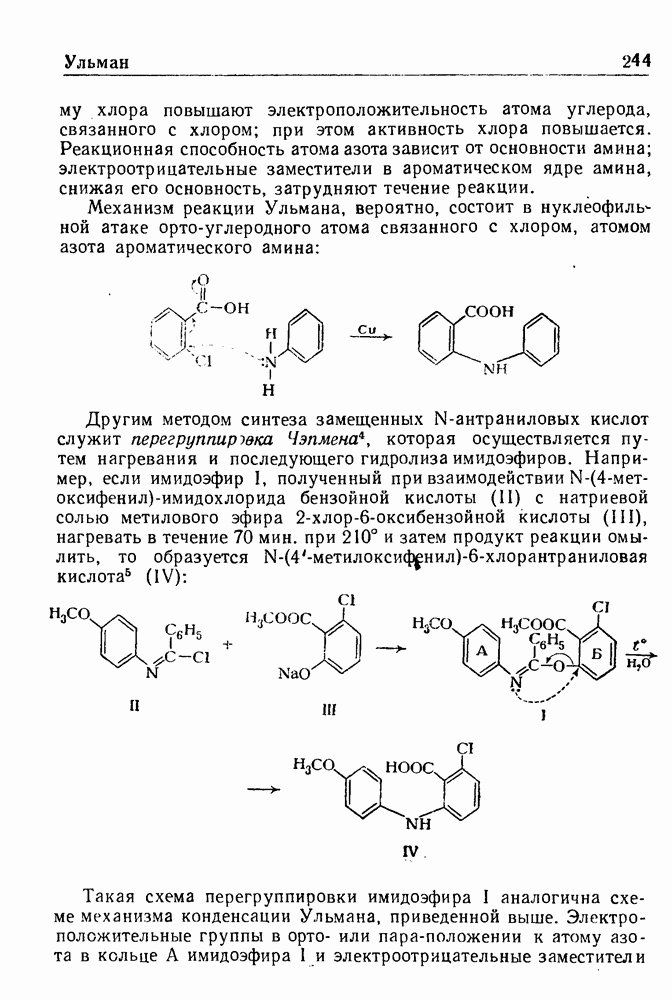
- РЕАКЦИЯ УЛЬМАНА
- КОНДЕНСАЦИЯ УЛЬМАНА
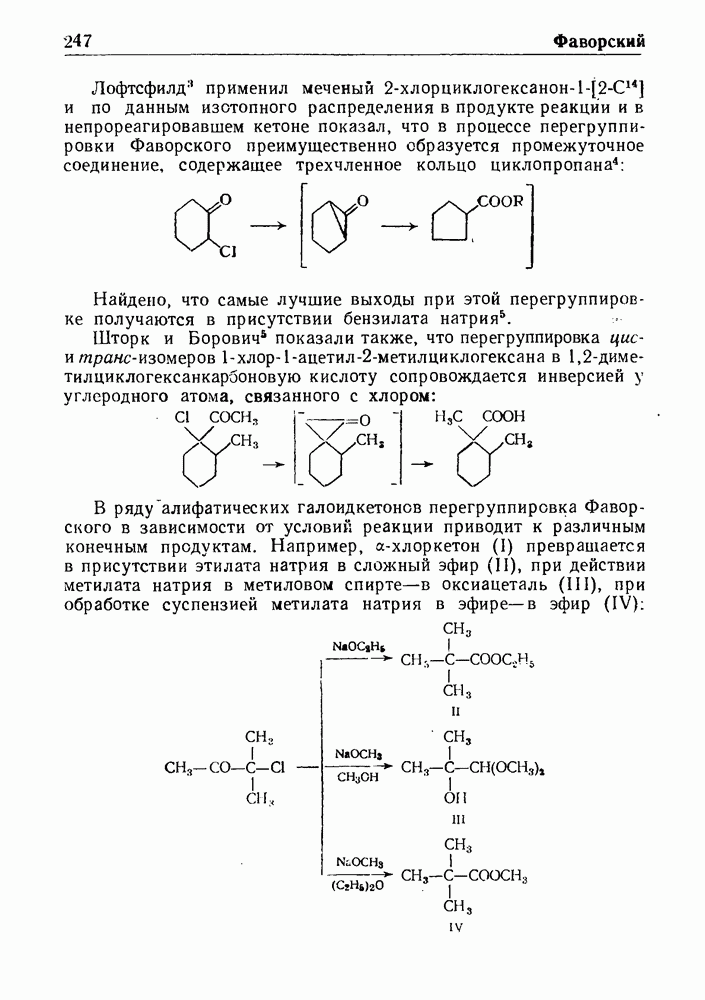
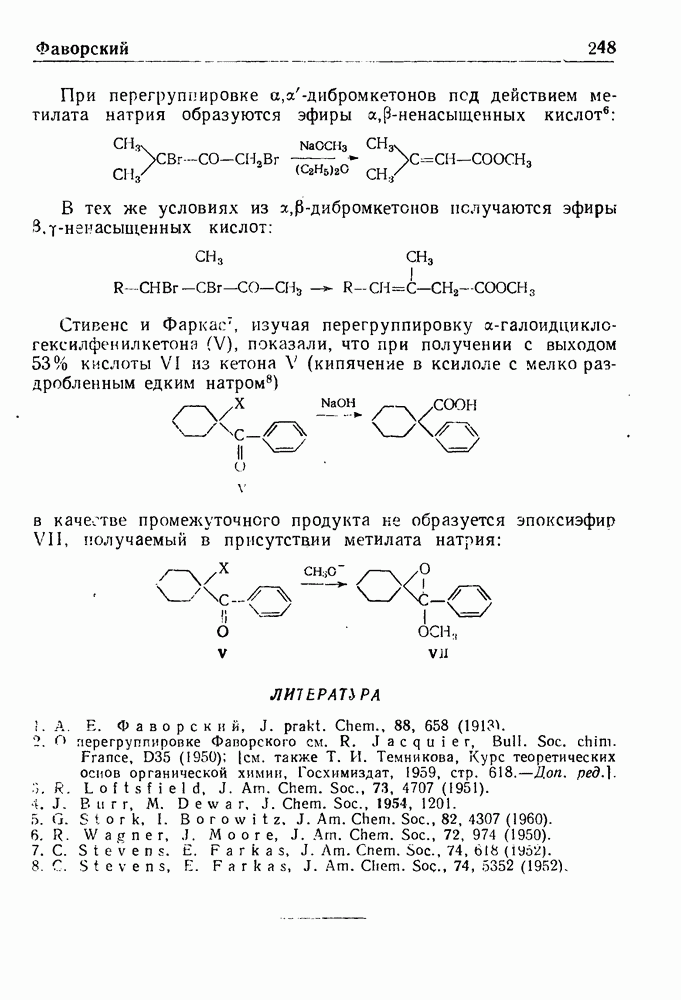
- ПЕРЕГРУППИРОВКА ФАВОРСКОГО
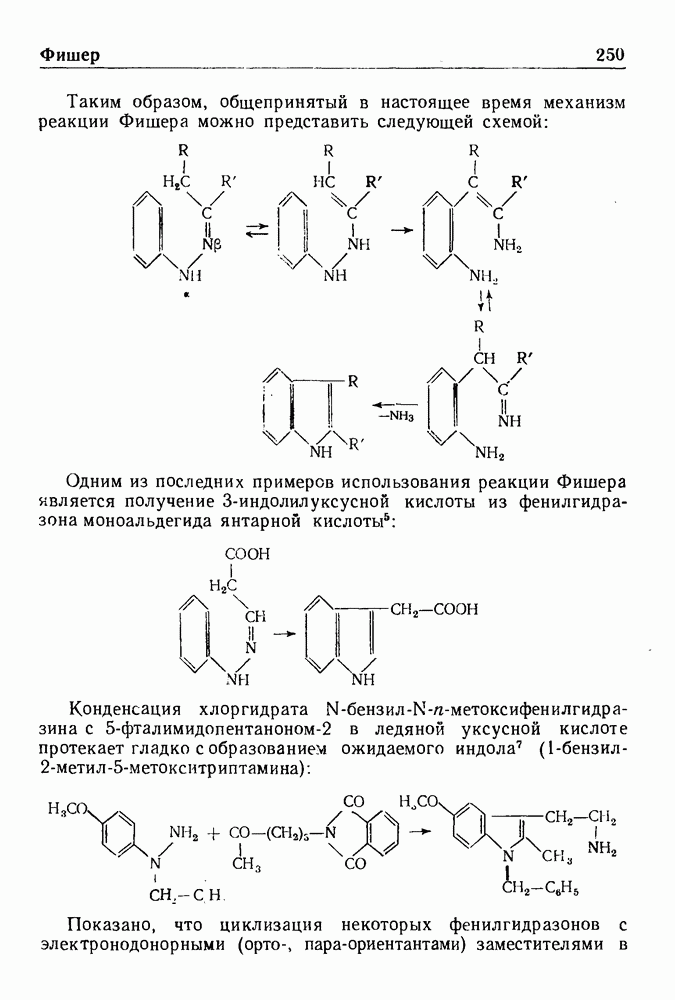
- СИНТЕЗ ИНДОЛА ПО ФИШЕРУ
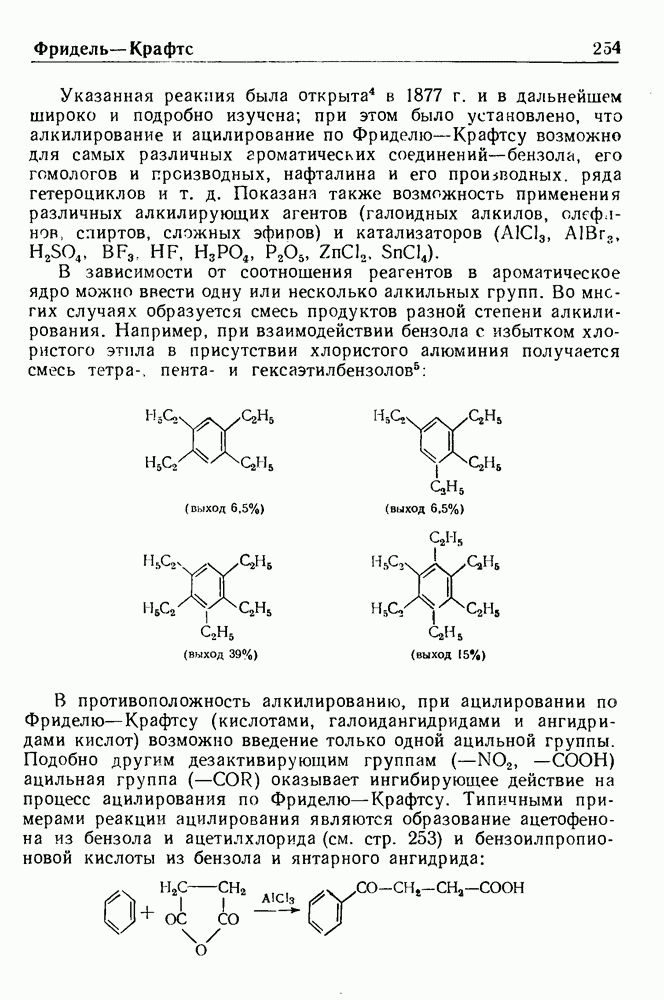
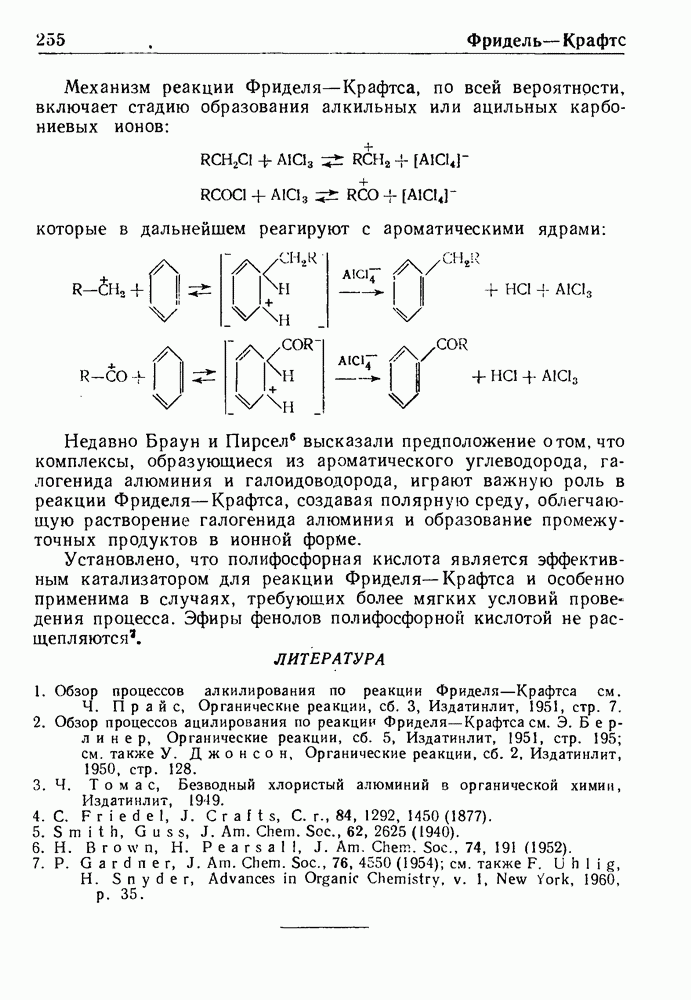
- РЕАКЦИЯ ФРИДЕЛЯ—КРАФТСА
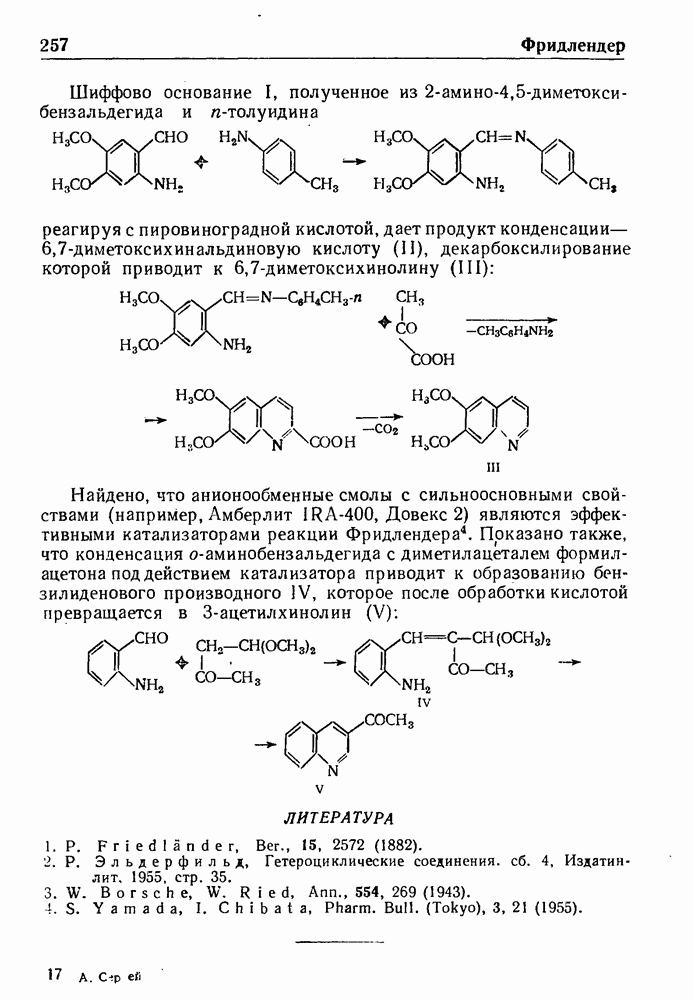
- СИНТЕЗ ФРИДЛЕНДЕРА
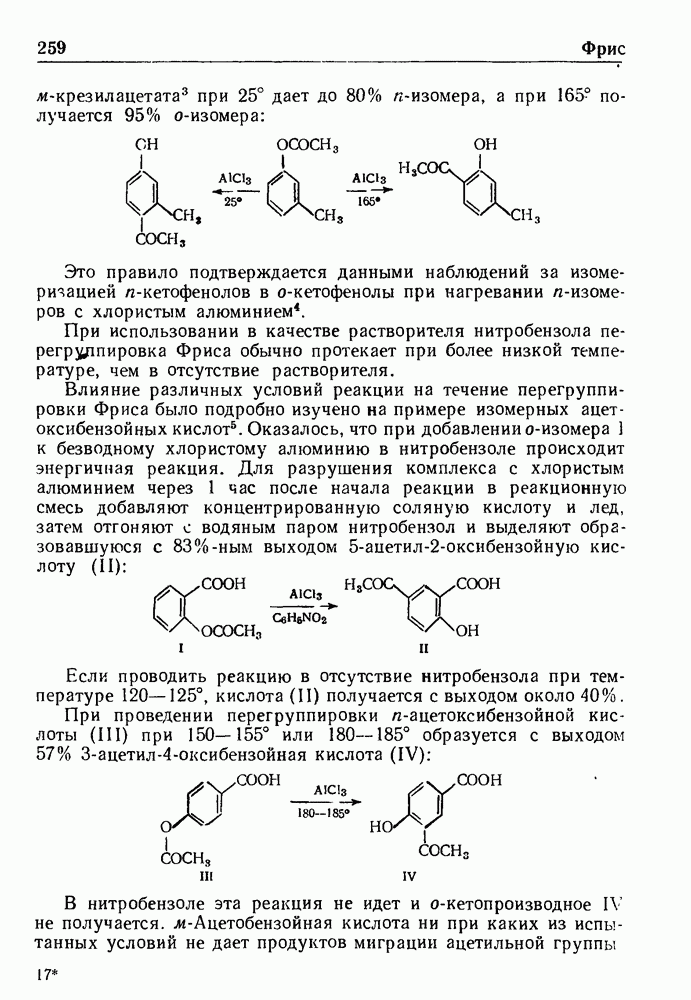
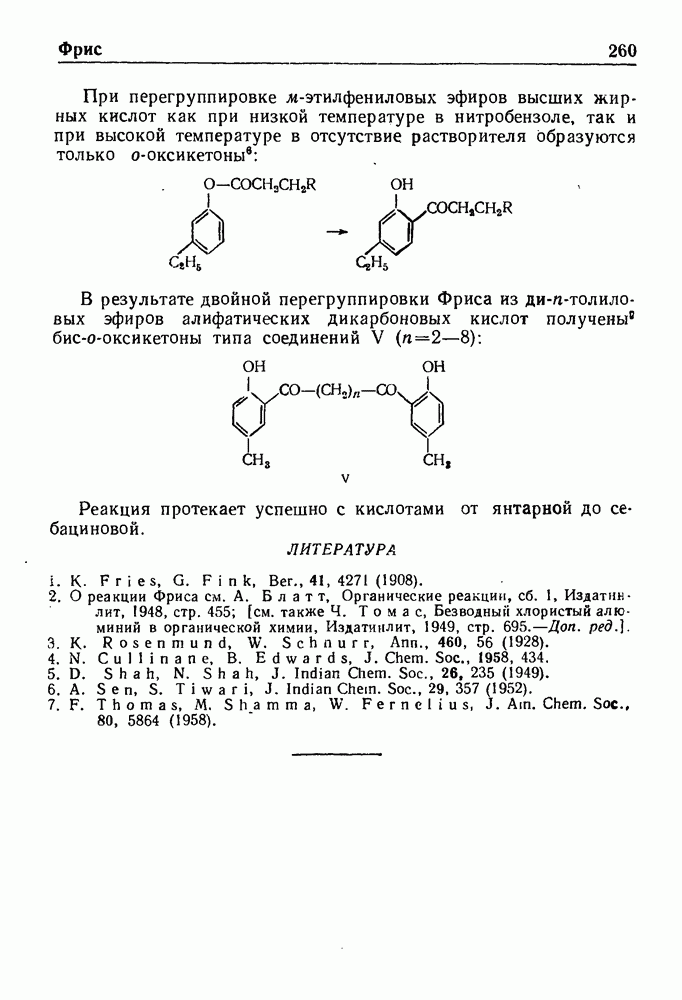
- РЕАКЦИЯ ФРИСА
- РЕАКЦИЯ ХУНСДИККЕРА
- РЕАКЦИЯ ЧИЧИБАБИНА
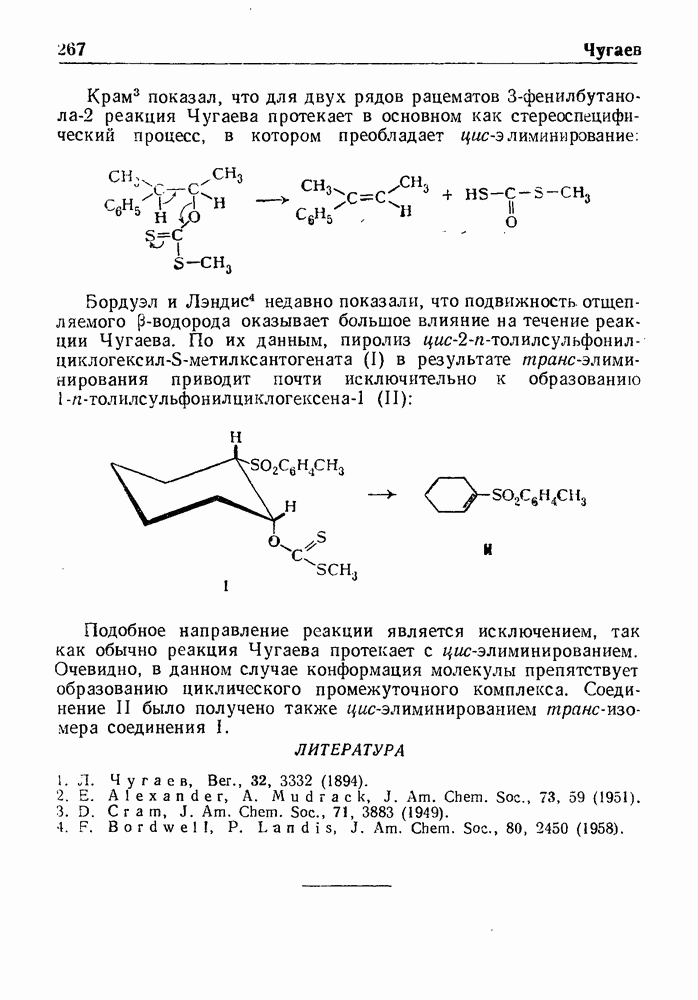
- РЕАКЦИЯ ЧУГАЕВА
- РЕАКЦИЯ ШИМАНА
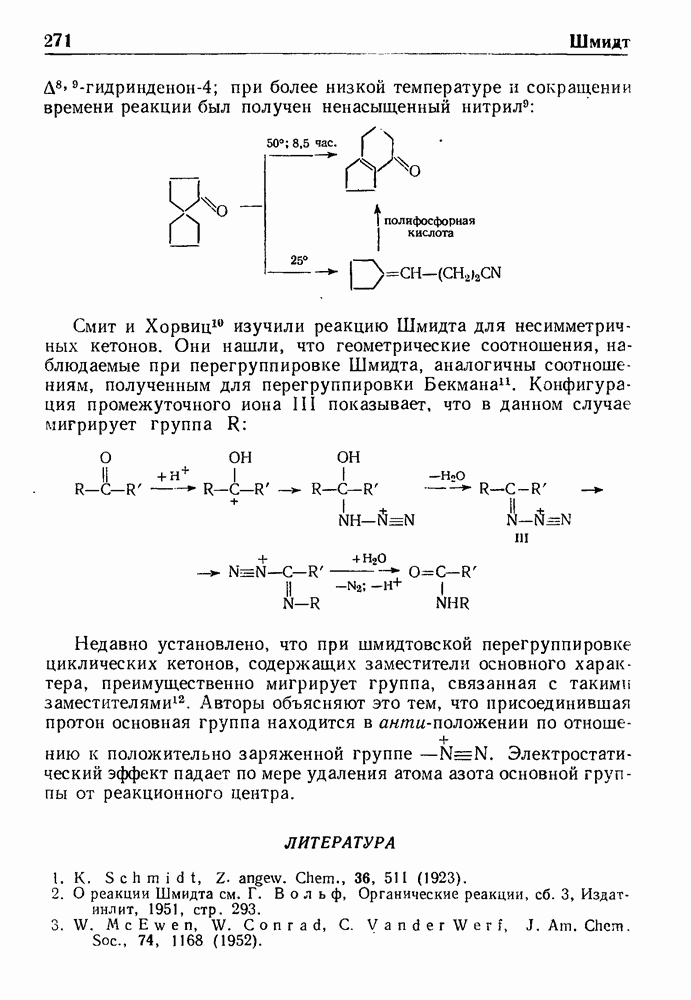
- РЕАКЦИИ ШМИДТА
- КОНДЕНСАЦИЯ ШТОББЕ
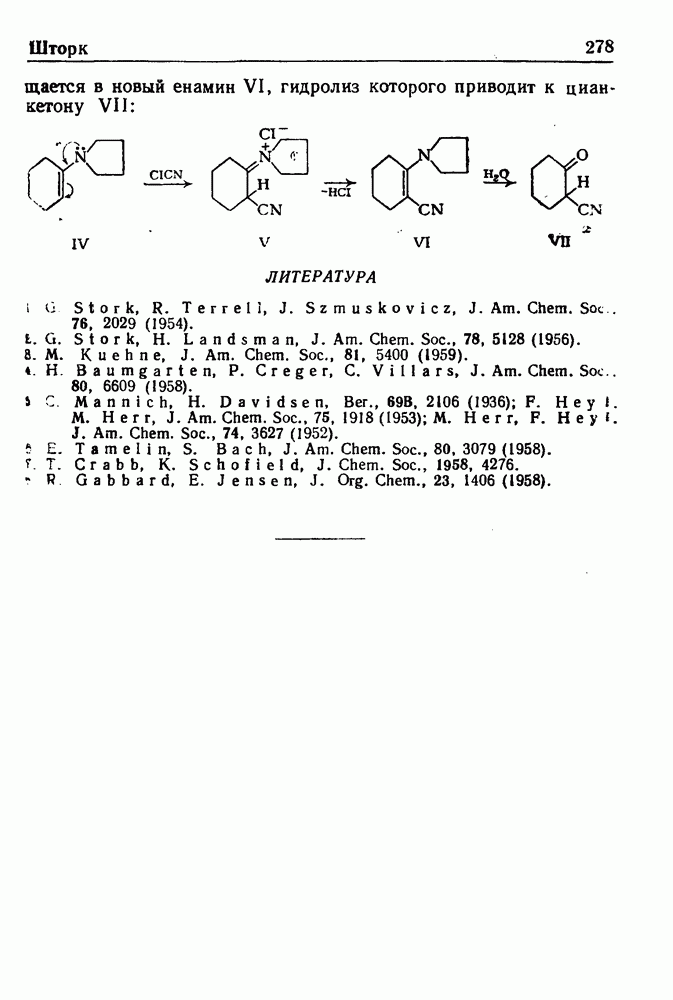
- РЕАКЦИЯ ШТОРКА
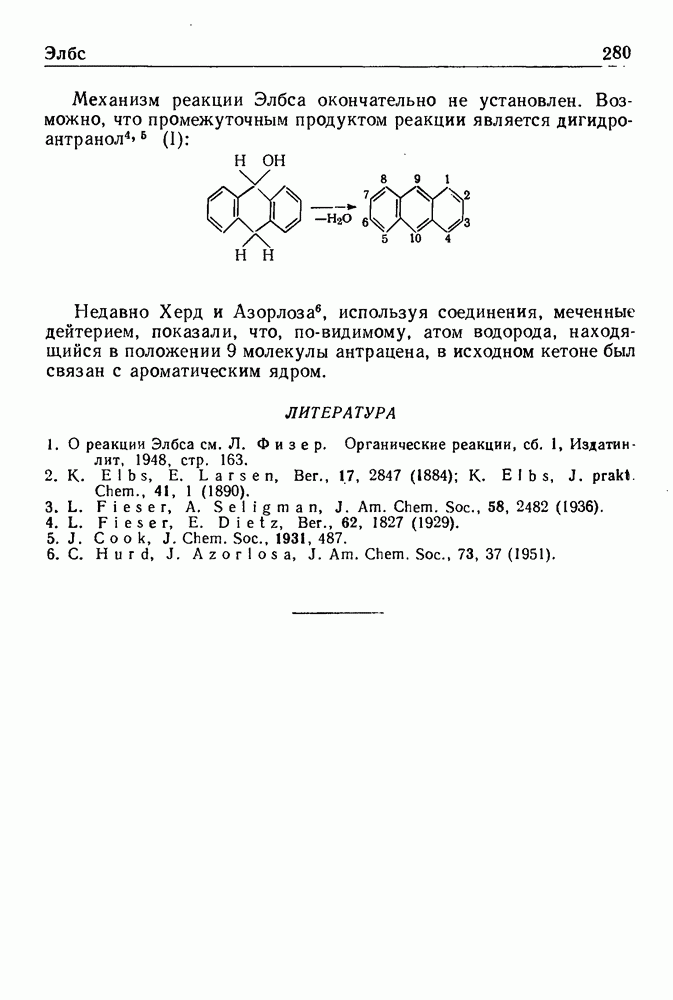
- РЕАКЦИЯ ЭЛБСА
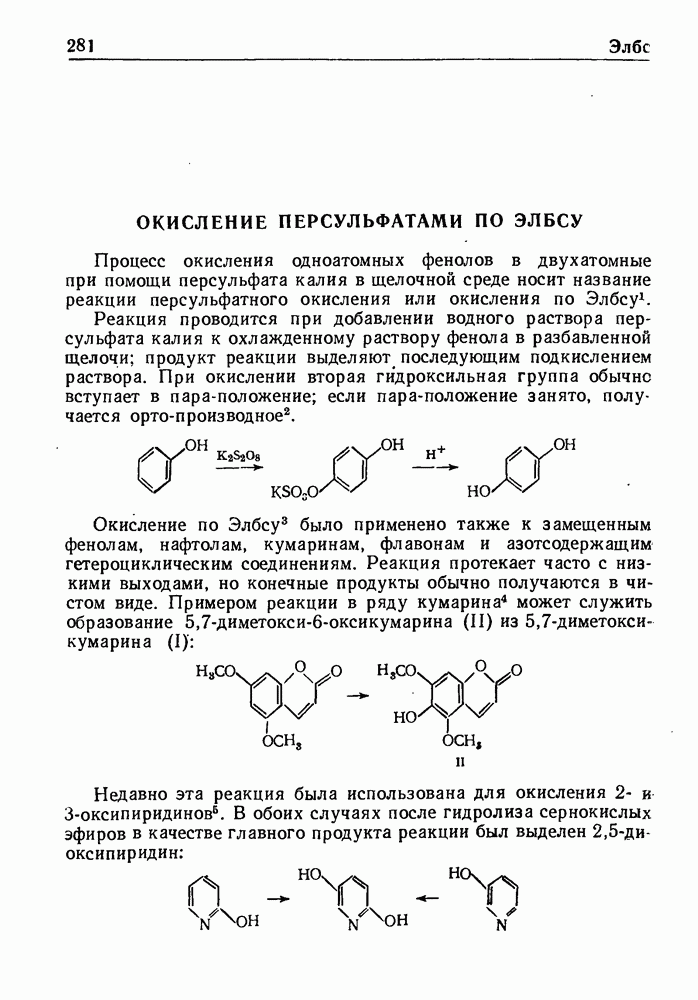
- ОКИСЛЕНИЕ ПЕРСУЛЬФАТАМИ ПО ЭЛБСУ
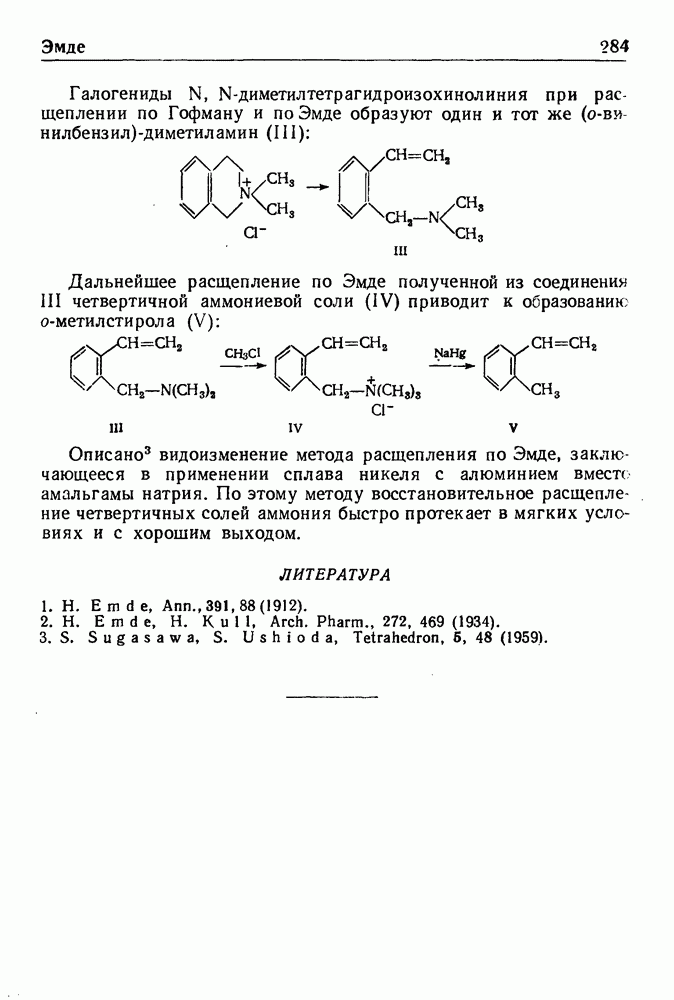
- РАСЩЕПЛЕНИЕ ПО ЭМДЕ
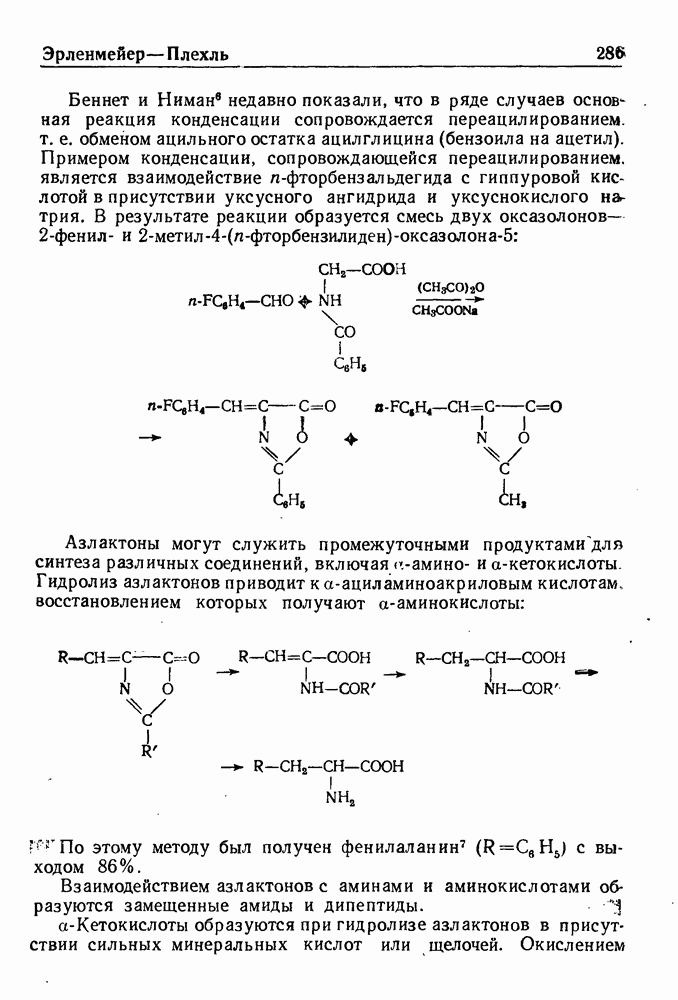
- СИНТЕЗ АЗЛАКТОНОВ ПО ЭРЛЕНМЕИЕРУ—ПЛЕХЛЮ
- РЕАКЦИЯ ЯКОБСЕНА