| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
РЕАКЦИЯ СОММЛЕ
Марсель Соммле (Marcel Sommelet, 1877-1952) родился в г. Ланж (Франция). В 1902 г. окончил Парижский университет, получив диплом фармацевта, затем работал под руководством Бехаля. В 1906 г. ему была присуждена степень доктора. После первой мировой войны преподавал на фармацевтическом факультете Парижского университета. С 1934 г. заведующий кафедрой органической химии этого университета. Получил алифатические альдегиды из замещенных оксиэтилэтиловых эфиров, а также хлористые бензилы, которые используются для приготовления бензиловых спиртов и бензальдегидов (реакция Соммле). Применил хлорметилэтиловый эфир для проведения реакции Гриньяра. Синтезировал  -изопропилбензальдегид и показал, что он идентичен природному куминовому альдегиду. Открыл, что под действием серной кислоты гидроокись бензгидрилтр и метил аммония превращается в
-изопропилбензальдегид и показал, что он идентичен природному куминовому альдегиду. Открыл, что под действием серной кислоты гидроокись бензгидрилтр и метил аммония превращается в  -бензилбензилди-метиламин (перегруппировка Соммле). В 1919 г. получил совместно с Фурно и Майаром премию Джекера.
-бензилбензилди-метиламин (перегруппировка Соммле). В 1919 г. получил совместно с Фурно и Майаром премию Джекера.
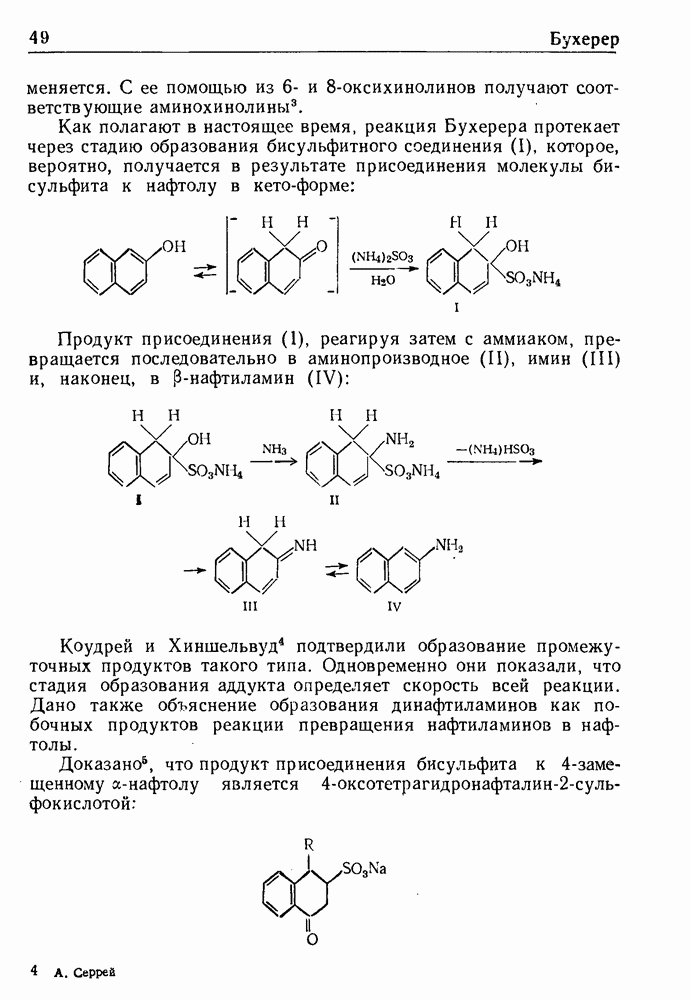
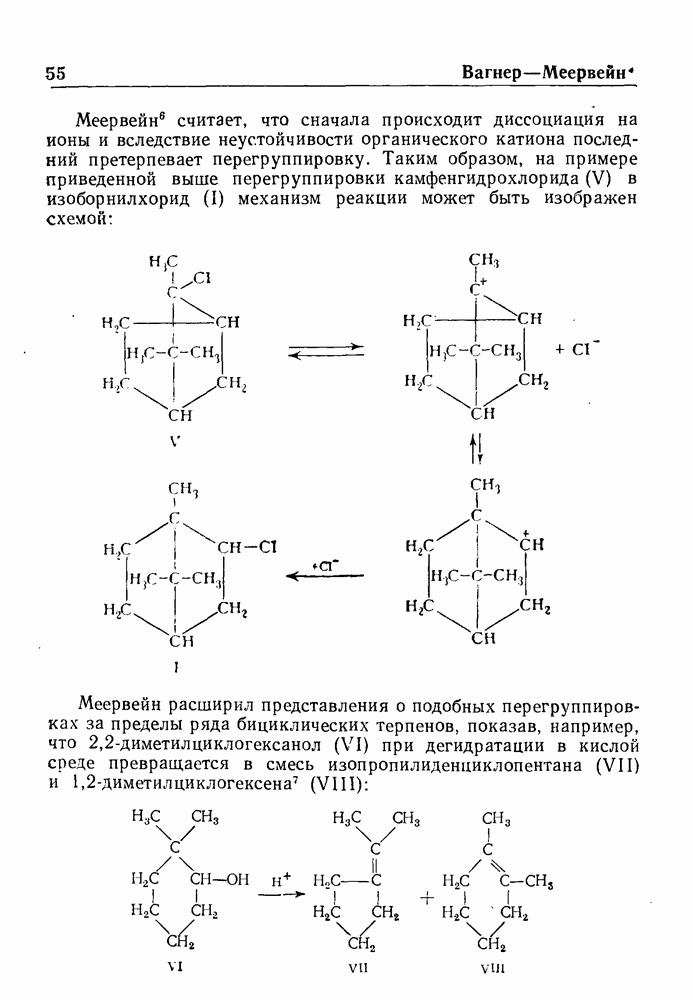
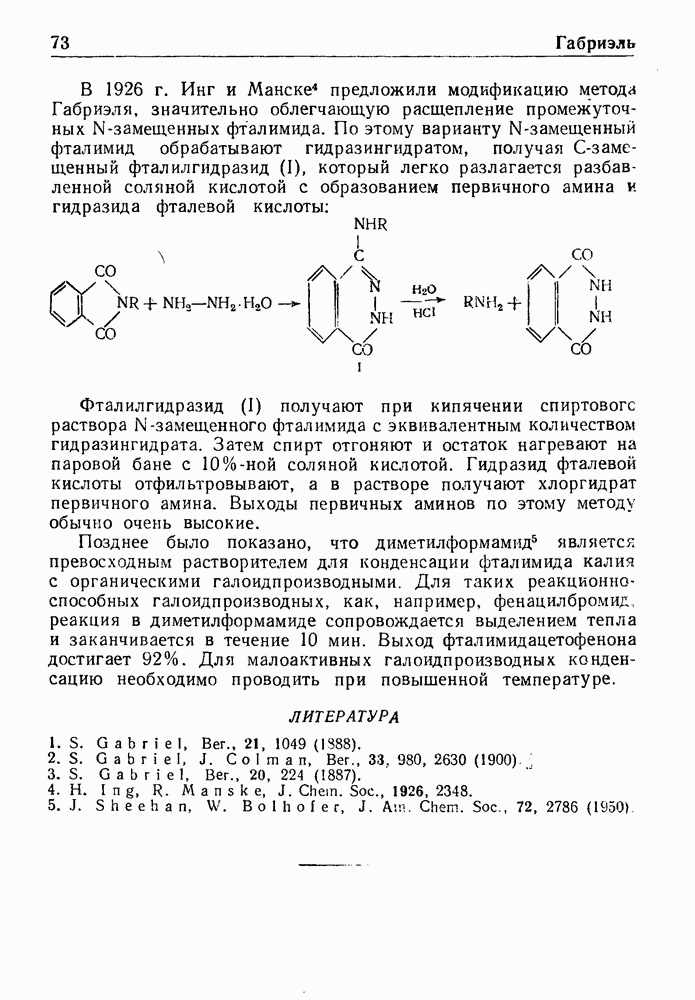
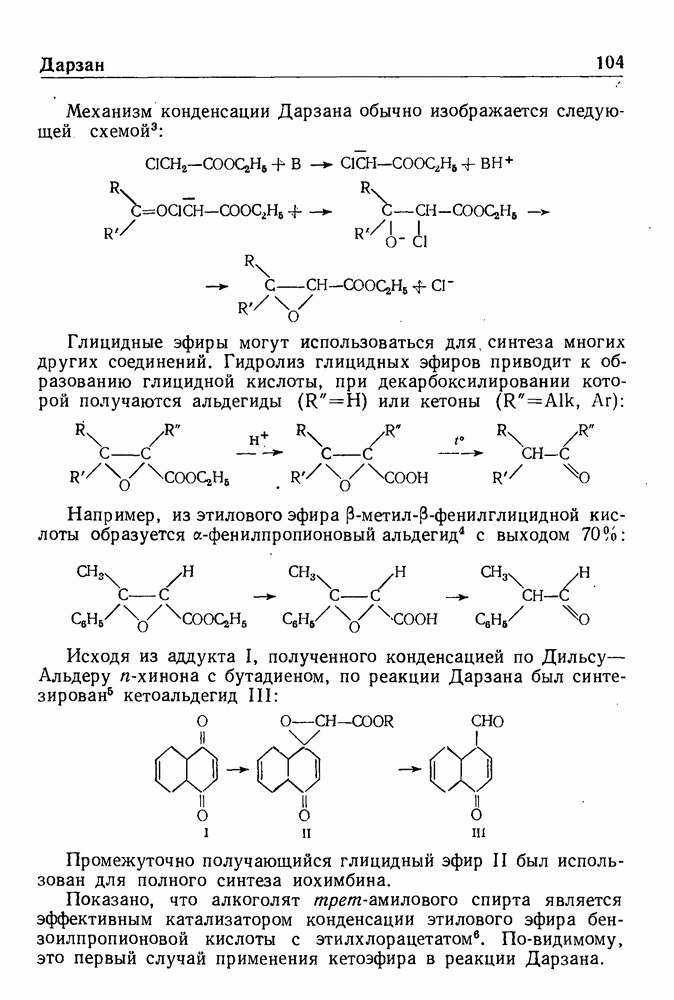
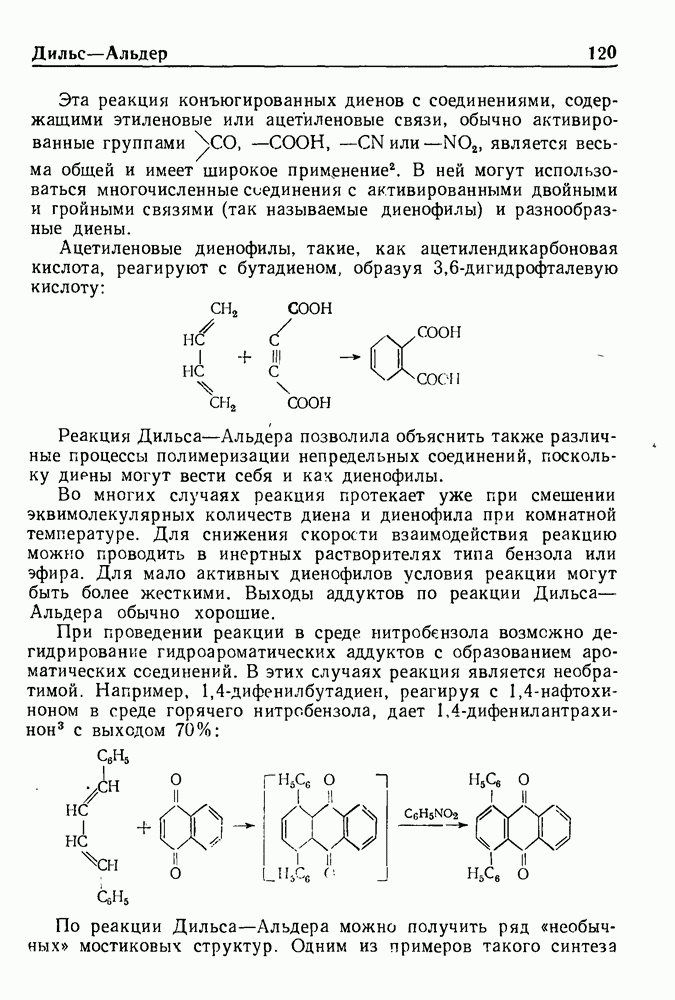
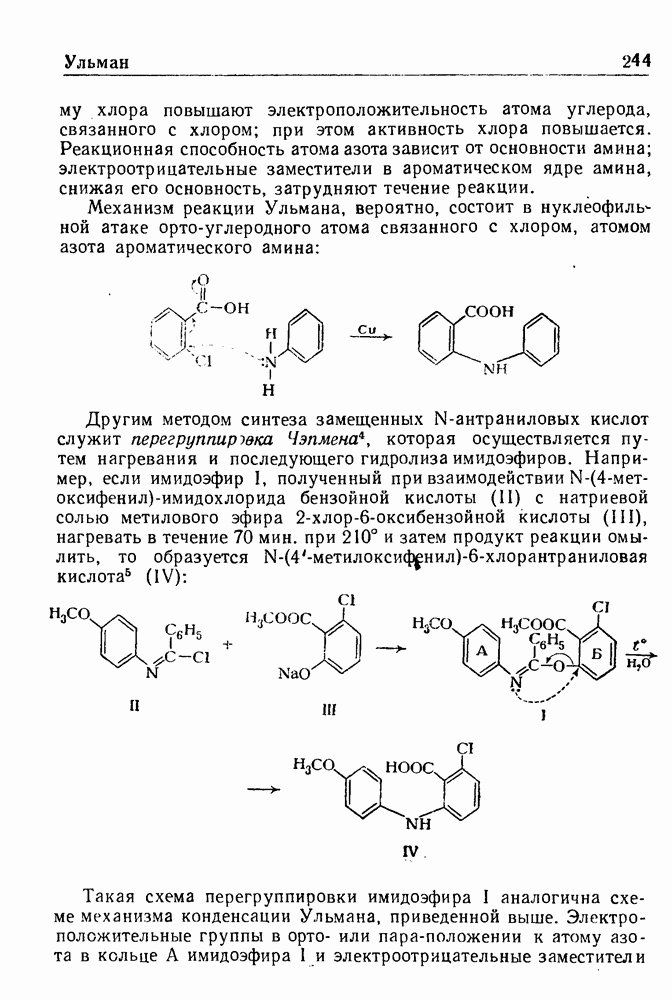
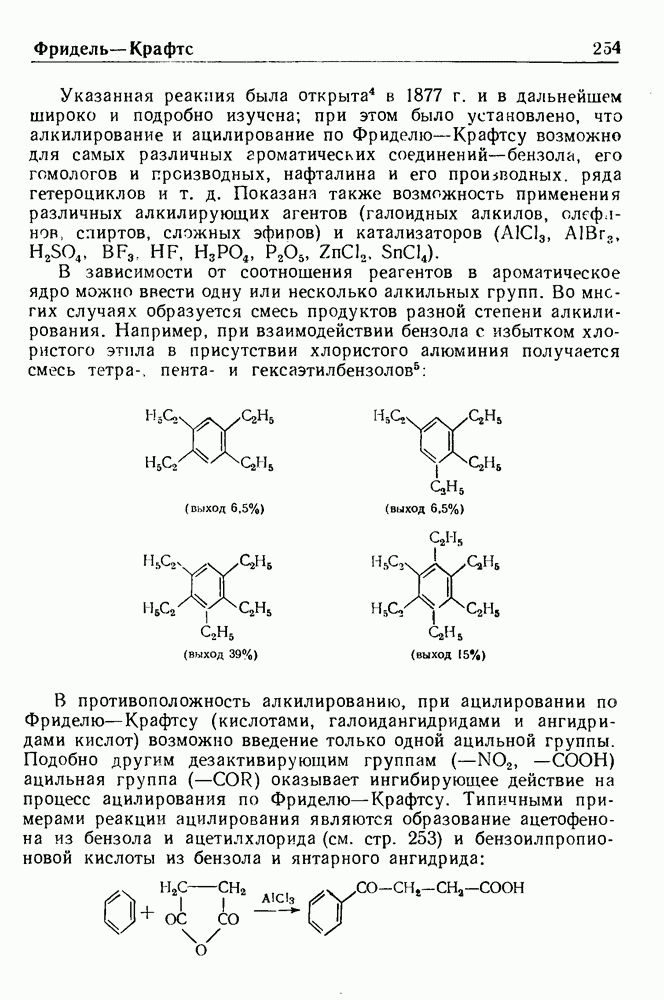
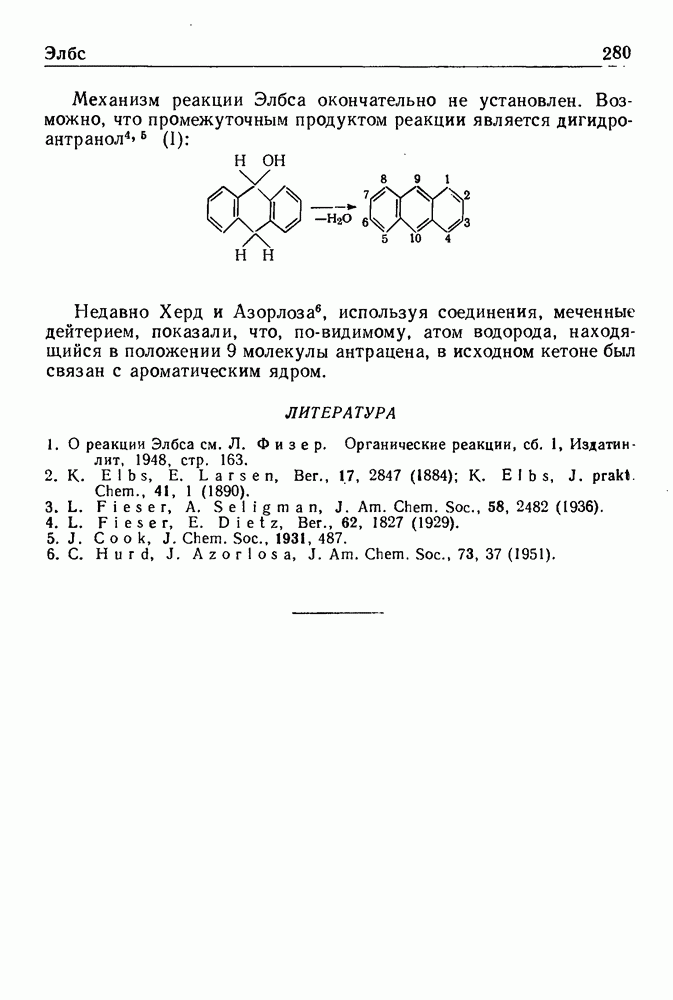
В 1913 г. Соммле показал, что четвертичные соли, получаемые из галоидного бензила и гексаметилентетрамина (уротропина), разлагаются при нагревании в присутствии воды с образованием соответствующего ароматического альдегида. Реакция служит общим методом синтеза ароматических альдегидов и обычно дает удовлетворительные выходы. Ее можно представить следующей схемой:

Из продуктов реакции выделены: аммиак, метил-, диметил- и триметиламины, а также некоторое количество бензиламина. Соммле установил, что выделять четвертичную соль не обязательно. При простом нагревании хлористого бензила с гексаметилен-тетрамином в водно-спиртовом растворе с хорошим выходом получается бензальдегид.
Реакция Соммле была изучена Анжиалем с сотр. Авторы показали, что электроноакцепторные заместители в ароматическом ядре снижают скорость образования и выход альдегидов. Лучшим растворителем для проведения реакции они считают 50%-ную
уксусную кислоту. Работами этих же авторов установлено, что при реакции Соммле сначала происходит гидролиз четвертичной соли I с образованием арилметиламина И, который подвергается дегидрогенизации до имина III, при гидролизе превращающегося в альдегид IV:

Возможно, что продукт гидролиза гексаметилентетрамина— метиленимин  является акцептором водорода в процессе превращения арилметиламина в имин и сам превращается при этом в метиламин. Описанный механизм подтверждается термодинамическими данными, полученными Шопи. Дегидрирующее действие гексаметилентетрамина было показано Даффом на примере синтеза щиффовых оснований из ди-(о-оксибеизил)-аминов:
является акцептором водорода в процессе превращения арилметиламина в имин и сам превращается при этом в метиламин. Описанный механизм подтверждается термодинамическими данными, полученными Шопи. Дегидрирующее действие гексаметилентетрамина было показано Даффом на примере синтеза щиффовых оснований из ди-(о-оксибеизил)-аминов:

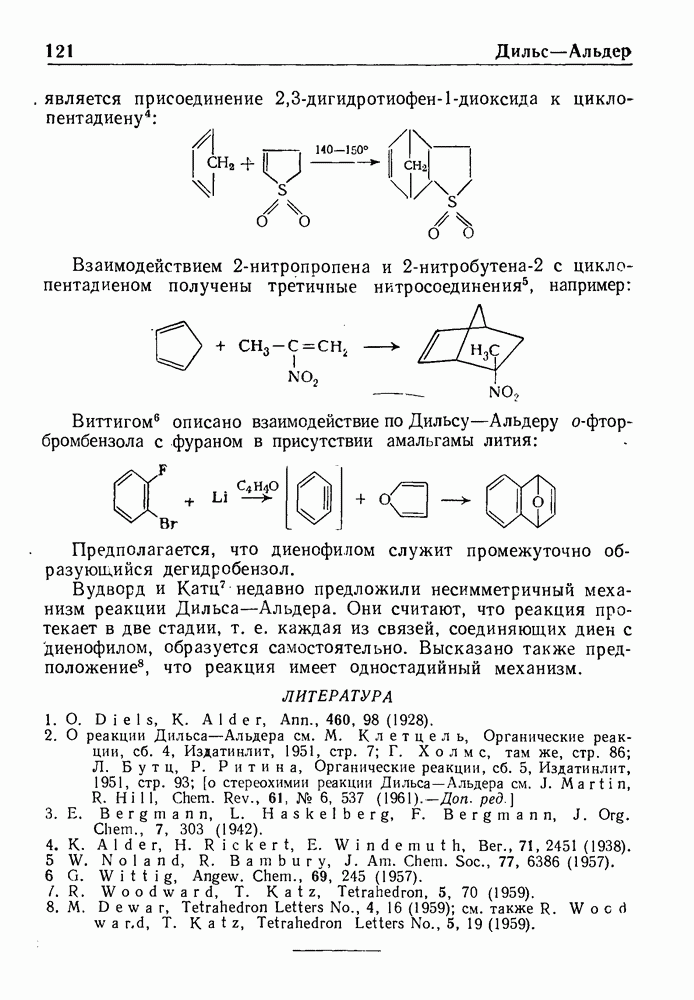
Образование ароматических диальдегидов по реакции Соммле протекает удовлетворительно только для  или
или  -ди-(хлор-метил)-производных при условии, что в ароматическом ядре имеется хотя бы одно свободное орто-положение. Из
-ди-(хлор-метил)-производных при условии, что в ароматическом ядре имеется хотя бы одно свободное орто-положение. Из  -бис-(хлорметил)-производных после гидролиза гексаметилентетраминовой соли получаются азотсодержащие основания.
-бис-(хлорметил)-производных после гидролиза гексаметилентетраминовой соли получаются азотсодержащие основания.
Хасс и Бендер недавно описали общий метод синтеза замещенных бензальдегидов, довольно сходный с методом Соммле. При обработке бензилгалогенидов спиртовым раствором натриевой соли  -нитропропана образуются ароматические альдегиды. Например, из
-нитропропана образуются ароматические альдегиды. Например, из  -ксилилбромида получен
-ксилилбромида получен  -кумиловый альдегид с выходом
-кумиловый альдегид с выходом 

По способу Хасса и Бендера терефталевый альдегид образуется с 70%-ным выходом при взаимодействии  -дибром-п-ксилола с
-дибром-п-ксилола с  -нитропропаном и спиртовым раствором едкого кали.
-нитропропаном и спиртовым раствором едкого кали.
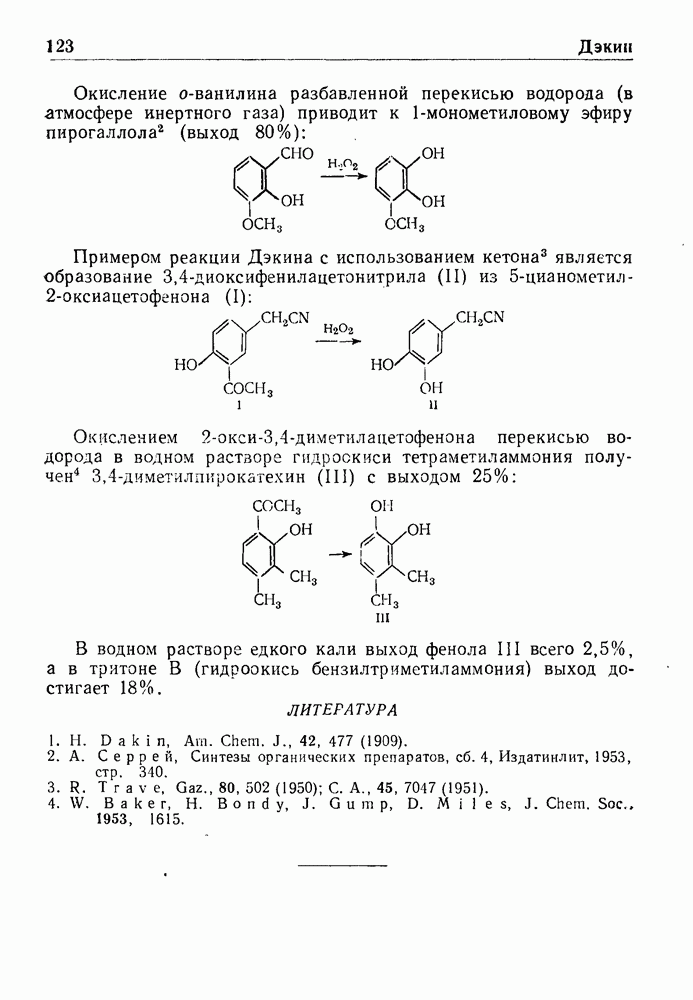
Другим методом синтеза альдегидов из бензилгалогенидов является реакция Кренке. Она состоит в превращении соли пиридиния в  -окись действием
-окись действием  -нитрозодиметиланилина. Кислотный гидролиз
-нитрозодиметиланилина. Кислотный гидролиз  -окиси приводит к образованию альдегида и
-окиси приводит к образованию альдегида и  -диметил-аминофенилгидроксил амина:
-диметил-аминофенилгидроксил амина:

Эта реакция находит широкое применение. С ее помощью могут быть получены в мягких условиях и с хорошими выходами многие ароматические, непредельные и  -кетоальдегиды.
-кетоальдегиды.
Гетероциклические соединения, содержащие активные метальные группы, реагируют с пиридином и иодом с образованием иодидов пиридиния, которые могут быть превращены в альдегиды по способу Кренке. Из  -метилбензтиазола этим методом получен
-метилбензтиазола этим методом получен  -формилбензтиазол с выходом 84%.
-формилбензтиазол с выходом 84%.
ЛИТЕРАТУРА
(см. скан)
| << Предыдущий параграф | Следующий параграф >> |
- ОТ РЕДАКТОРА
- ПЕРЕГРУППИРОВКА АРБУЗОВА
- СИНТЕЗ АРНДТА—ЭЙСТЕРТА
- ОКИСЛЕНИЕ ПО БАЙЕРУ—ВИЛЛИГЕРУ
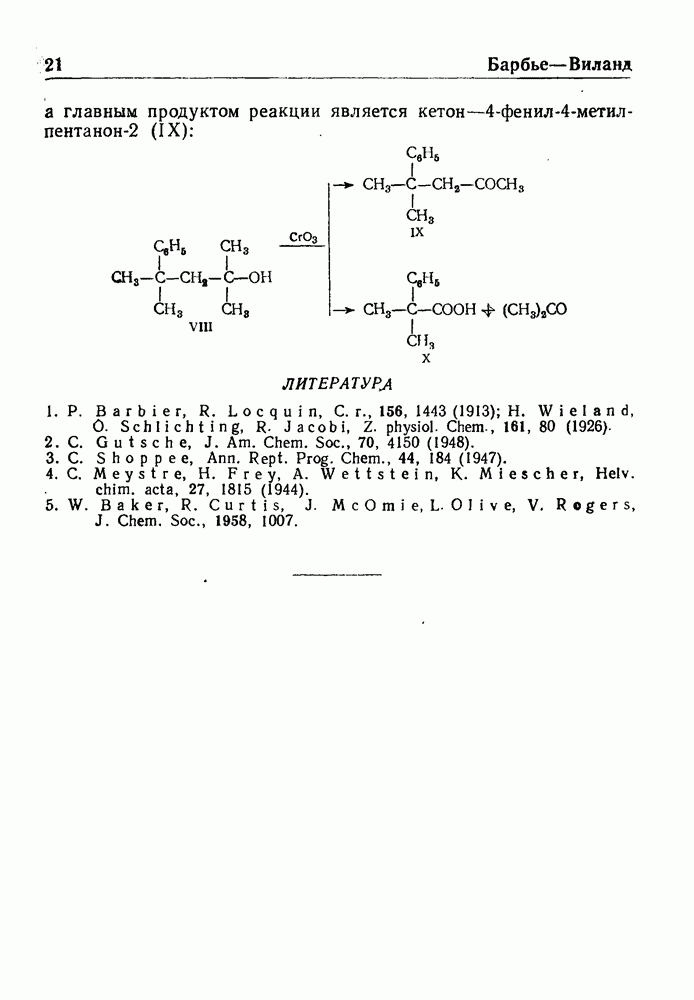
- РАСЩЕПЛЕНИЕ ПО БАРБЬЕ—ВИЛАНДУ
- РЕАКЦИЯ БАРТА
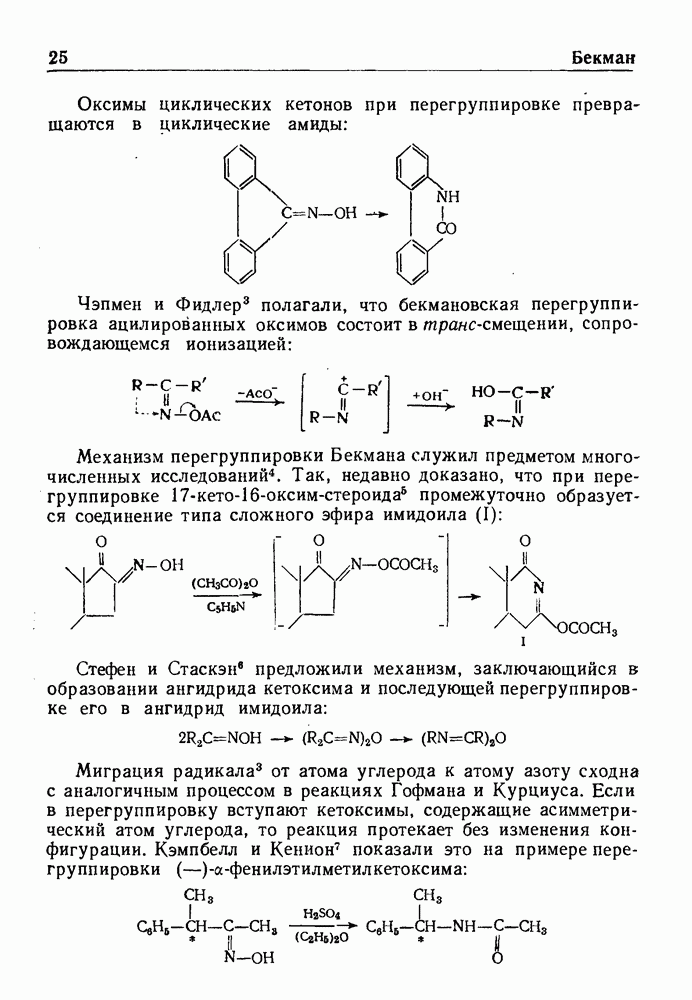
- ПЕРЕГРУППИРОВКА БЕКМАНА
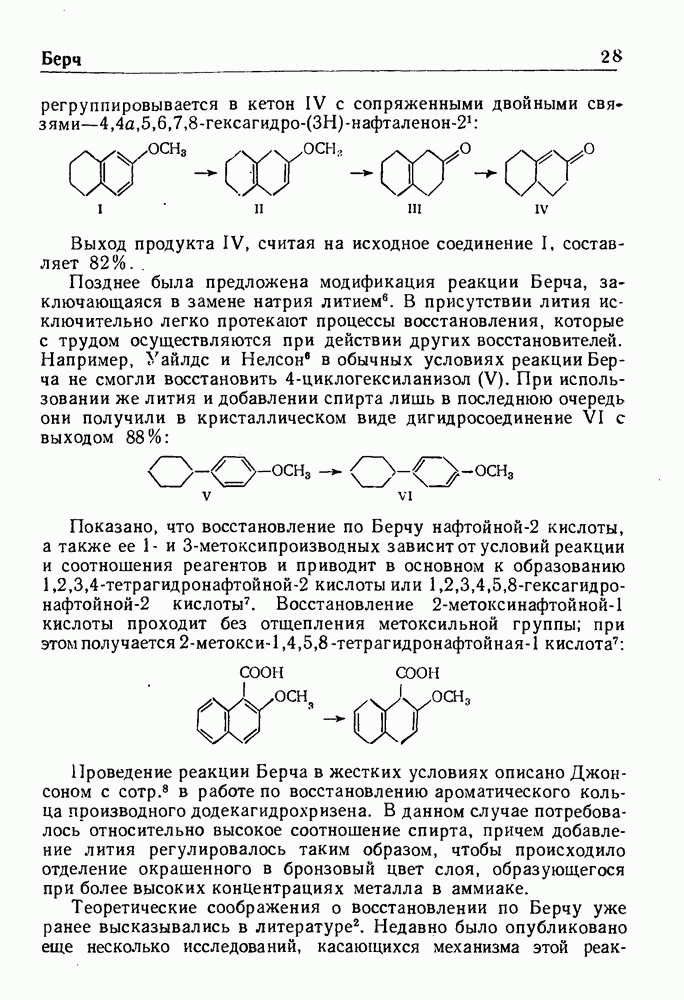
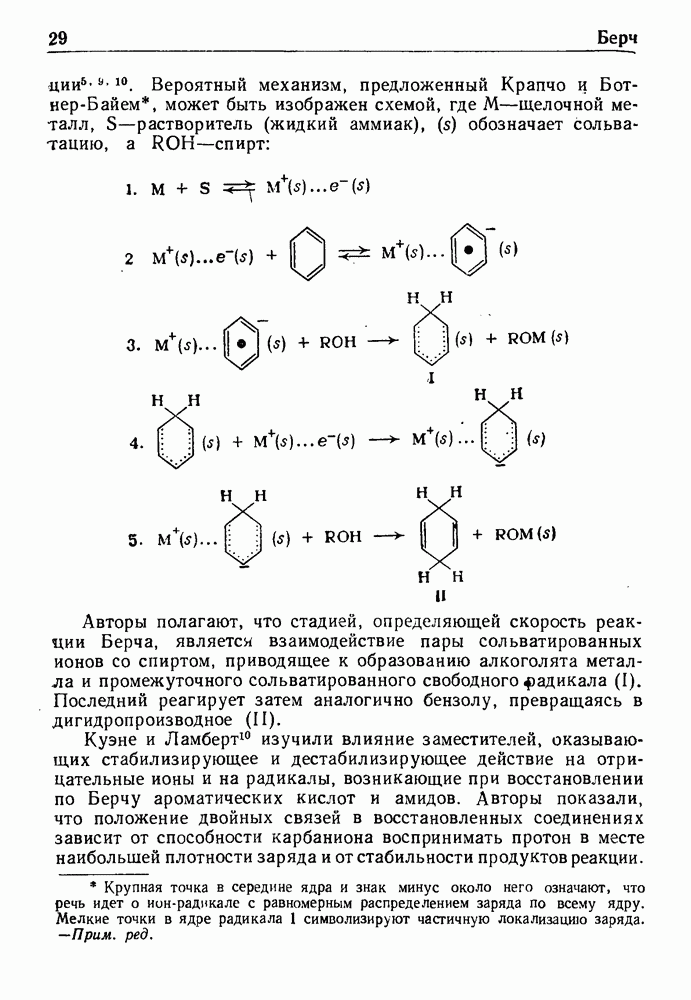
- ВОССТАНОВЛЕНИЕ ПО БЕРНУ
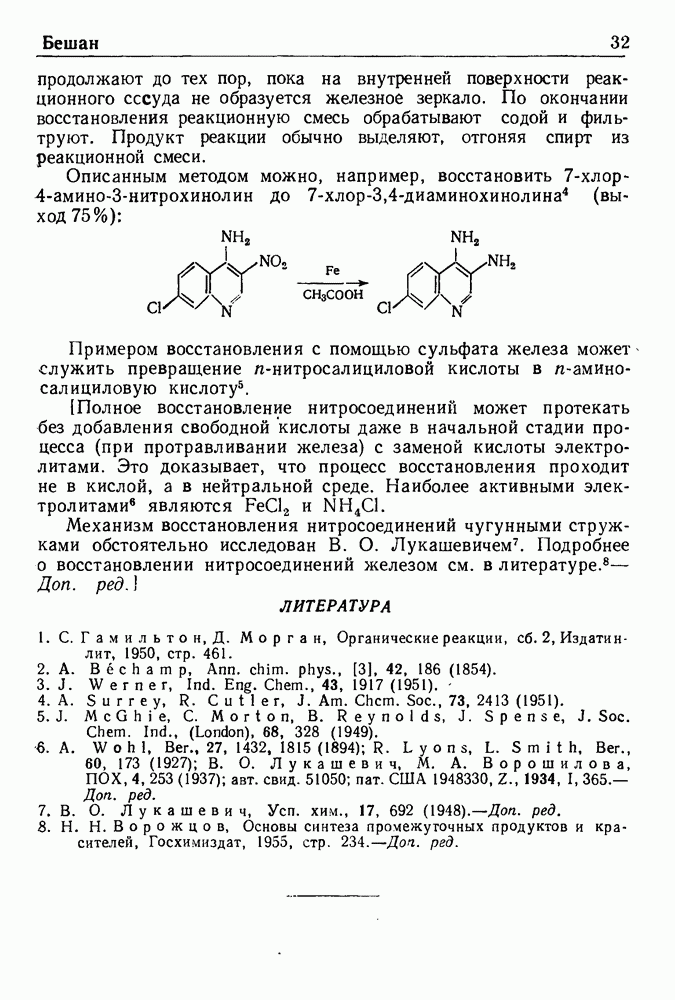
- ВОССТАНОВЛЕНИЕ ПО БЕШАНУ
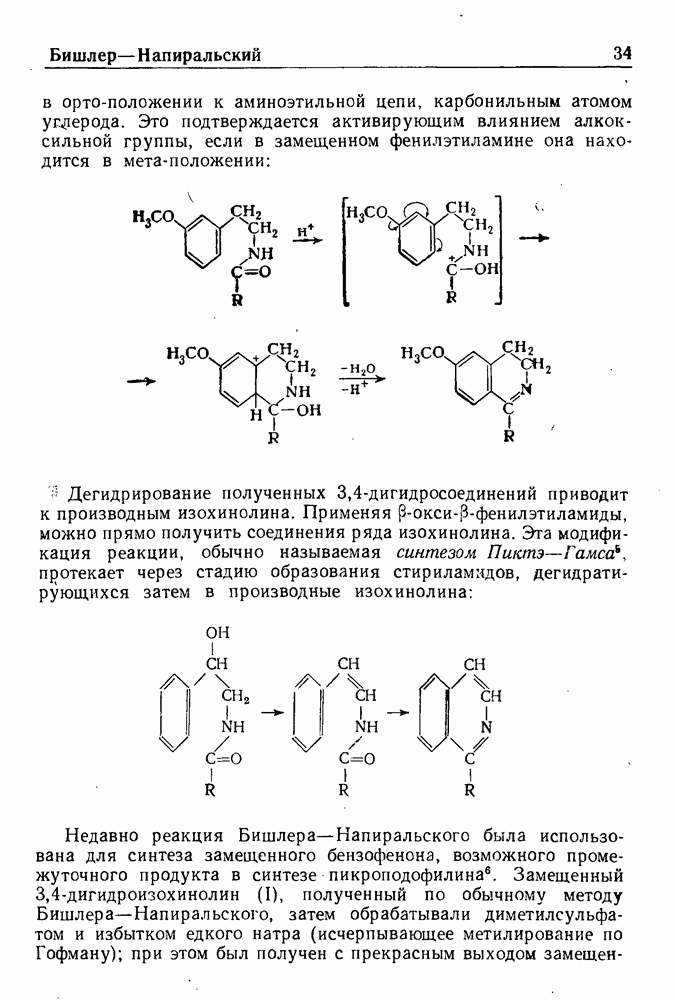
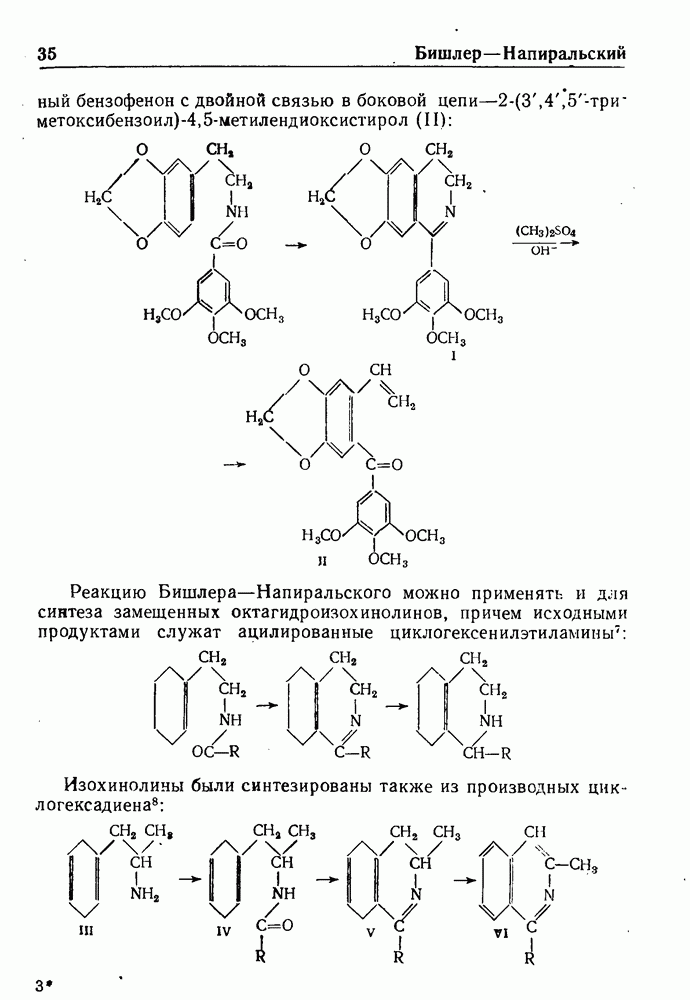
- РЕАКЦИЯ БИШЛЕРА—НАПИРАЛЬСКОГО
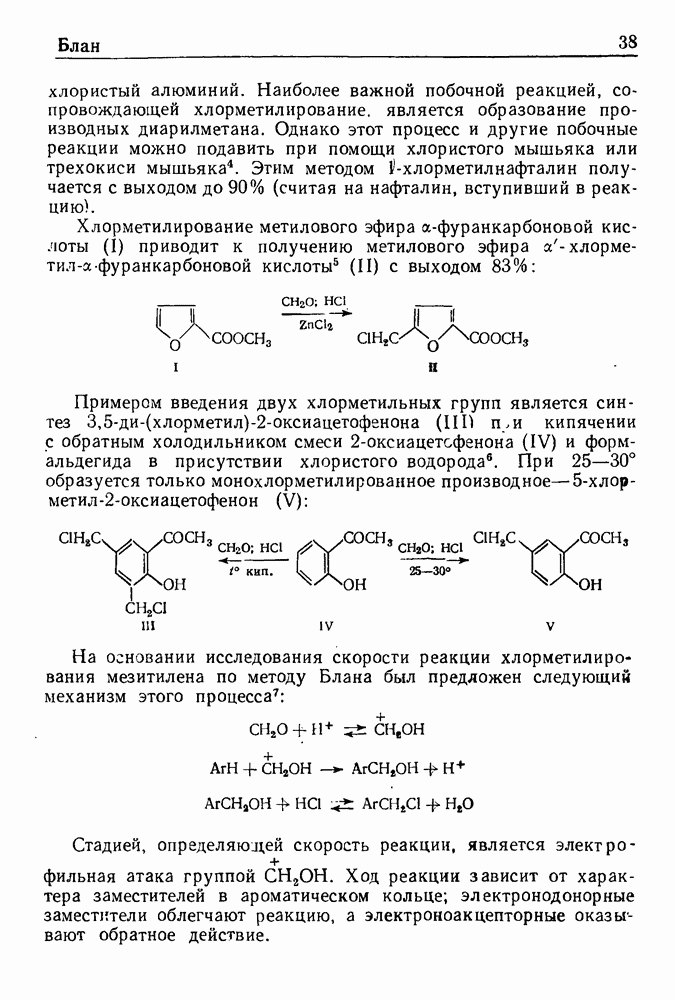
- ХЛОРМЕТИЛИРОВАНИЕ ПО БЛАНУ
- РЕАКЦИЯ БРАУНА
- РАСЩЕПЛЕНИЕ АМИНОВ ПО БРАУНУ
- ВОССТАНОВЛЕНИЕ ПО БУВО—БЛАНУ
- СИНТЕЗ АЛЬДЕГИДОВ ПО БУВО
- РЕАКЦИЯ БУХЕРЕРА
- СИНТЕЗ ГИДАНТОИНОВ ПО БУХЕРЕРУ
- ПЕРЕГРУППИРОВКА ВАГНЕРА—МЕЕРВЕЙНА
- РЕАКЦИЯ ВАЛЛАХА
- РЕАКЦИЯ ВИЛЬГЕРОДТА
- СИНТЕЗ ВИЛЬЯМСОНА
- РЕАКЦИЯ ВИТТИГА
- РЕАКЦИЯ ВОЛЯ-ЦИГЛЕРА
- РЕАКЦИЯ ВЮРЦА
- СИНТЕЗ ГАБРИЭЛЯ
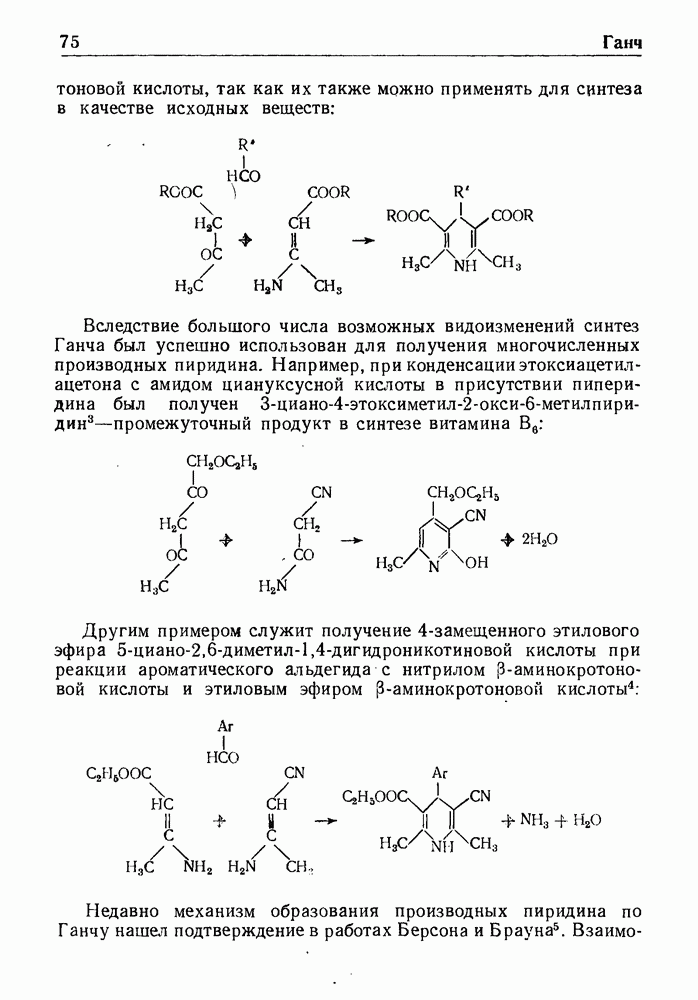
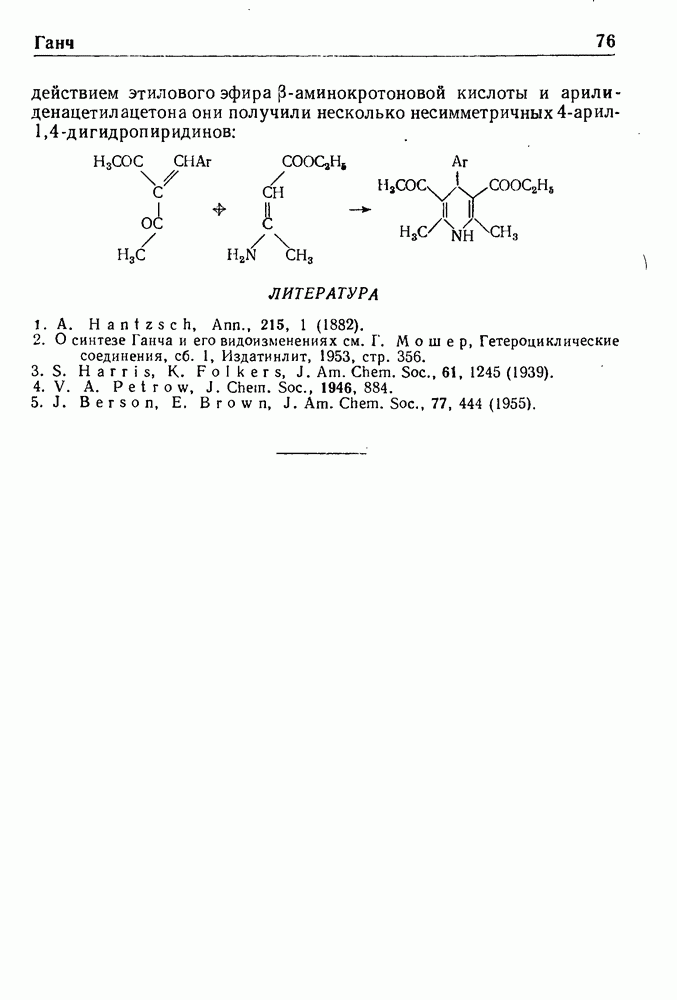
- СИНТЕЗ ГАНЧА
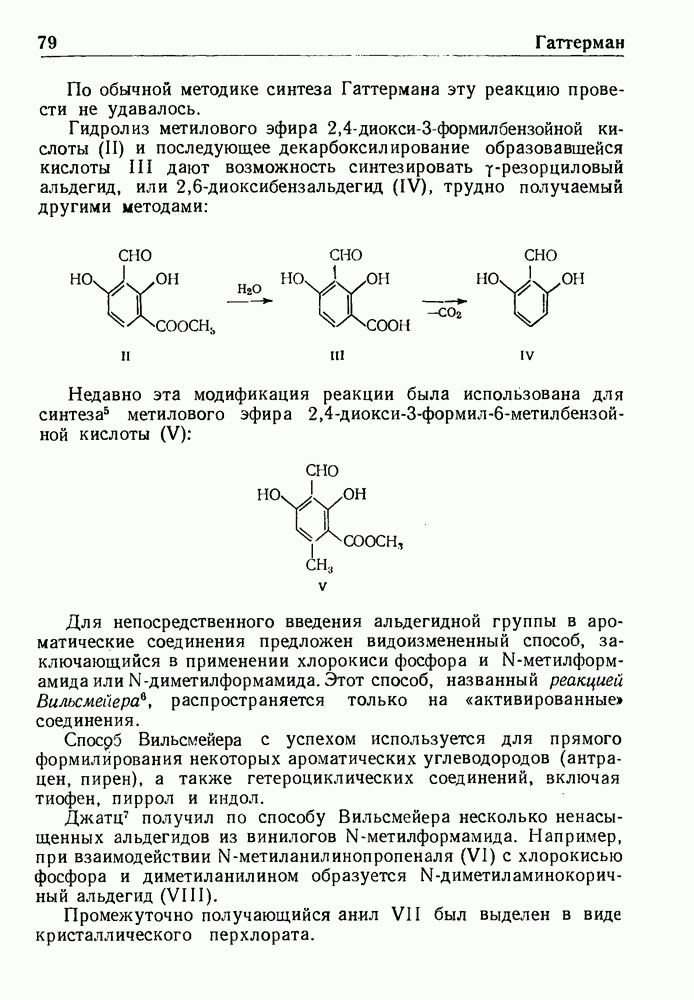
- РЕАКЦИЯ ГАТТЕРМАНА
- СИНТЕЗ АЛЬДЕГИДОВ ПО ГАТТЕРМАНУ
- РЕАКЦИЯ ГАТТЕРМАНА—КОХА
- РЕАКЦИЯ ГЕЛЛЯ—ФОЛЬГАРДА—ЗЕЛИНСКОГО
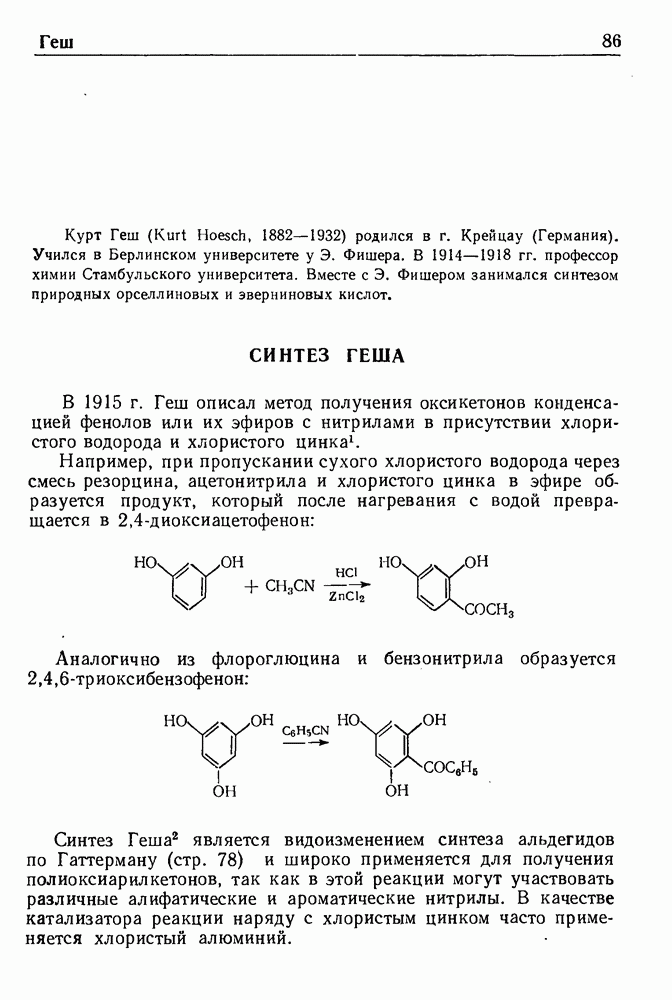
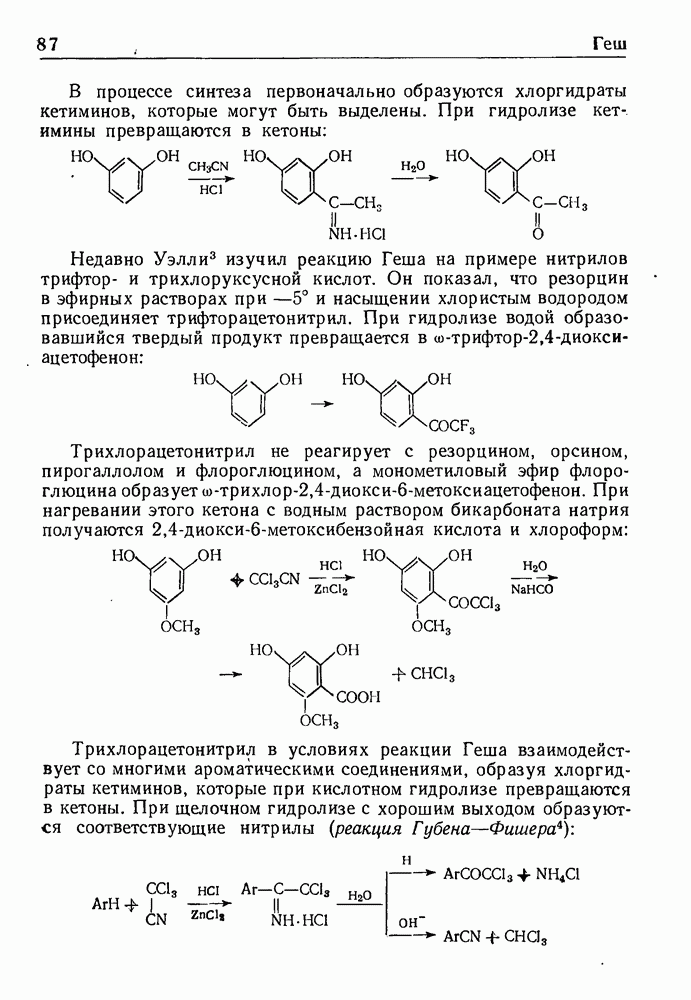
- СИНТЕЗ ГЕША
- РЕАКЦИЯ ГОМБЕРГА—БАХМАНА—ХЕЯ
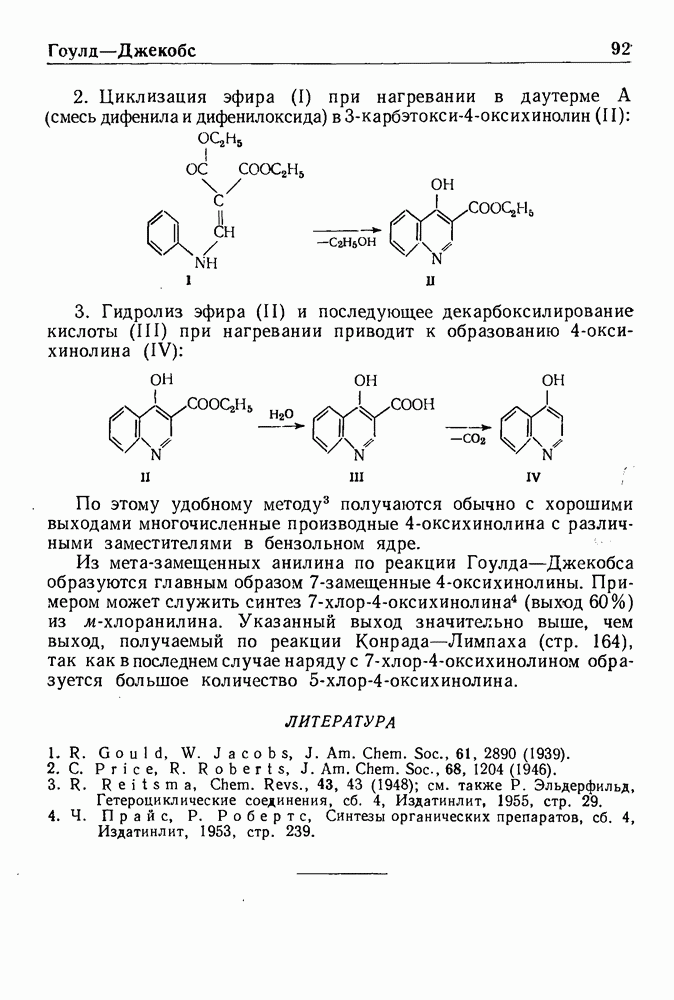
- РЕАКЦИЯ ГОУЛДА—ДЖЕКОБСА
- ПЕРЕГРУППИРОВКА ГОФМАНА
- РАСЩЕПЛЕНИЕ ПО ГОФМАНУ
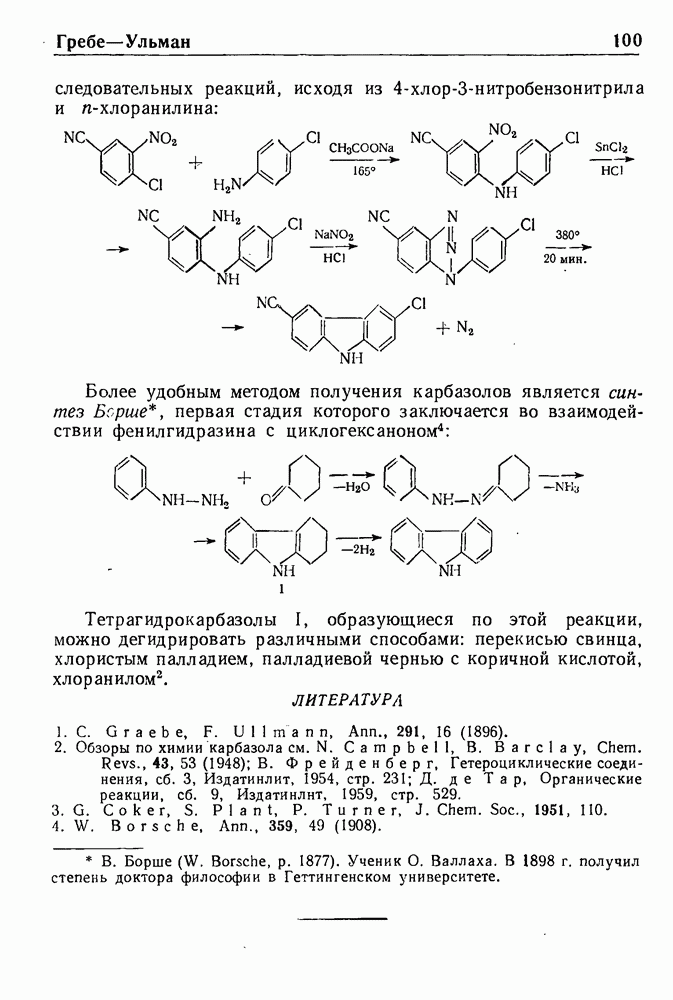
- СИНТЕЗ ГРЕБЕ—УЛЬМАНА
- РЕАКЦИЯ ГРИНЬЯРА
- СИНТЕЗ ГЛИЦИДНЫХ ЭФИРОВ ПО ДАРЗАНУ
- СИНТЕЗ НЕПРЕДЕЛЬНЫХ КЕТОНОВ ПО ДАРЗАНУ
- РЕАКЦИЯ ДАФФА
- СИНТЕЗ ДЕБНЕРА
- СИНТЕЗ ДЕБНЕРА—МИЛЛЕРА
- РЕАКЦИЯ ДЕЛЕПИНА
- РЕАКЦИЯ ДИКМАНА
- РЕАКЦИЯ ДИЛЬСА-АЛЬДЕРА
- РЕАКЦИЯ ДЭКИНА
- РЕАКЦИЯ ДЭКИНА—ВЕСТА
- РЕАКЦИЯ ЗАНДМЕЙЕРА
- РЕАКЦИЯ ИВАНОВА
- РЕАКЦИЯ ИОЦИЧА
- РЕАКЦИЯ КАННИЦЦАРО
- РЕАКЦИЯ КИЖНЕРА
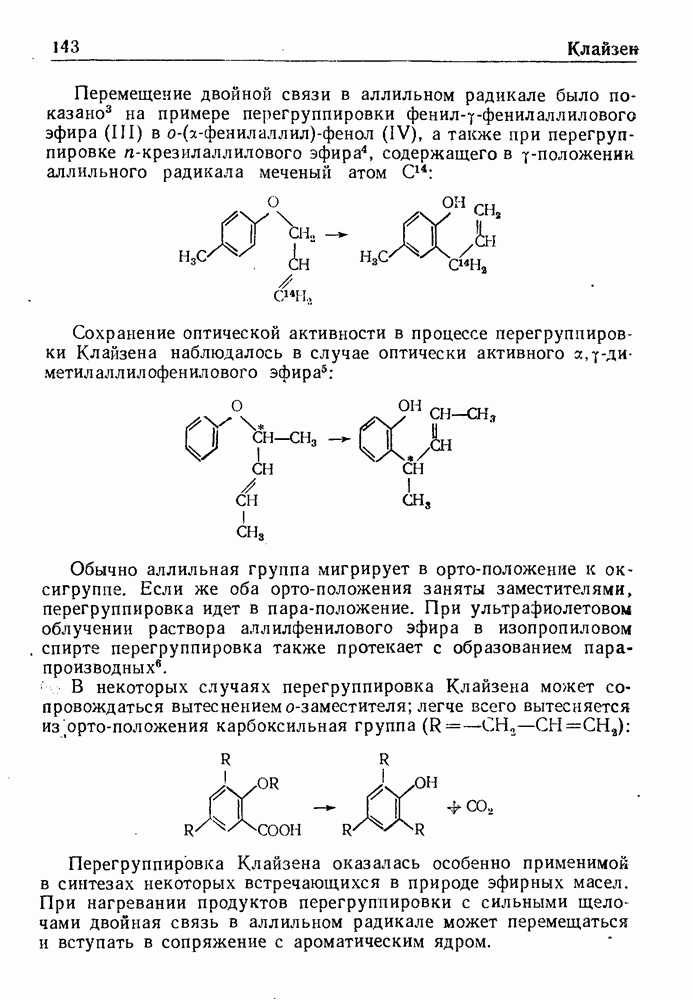
- КОНДЕНСАЦИЯ КЛАЙЗЕНА
- ПЕРЕГРУППИРОВКА КЛАЙЗЕНА
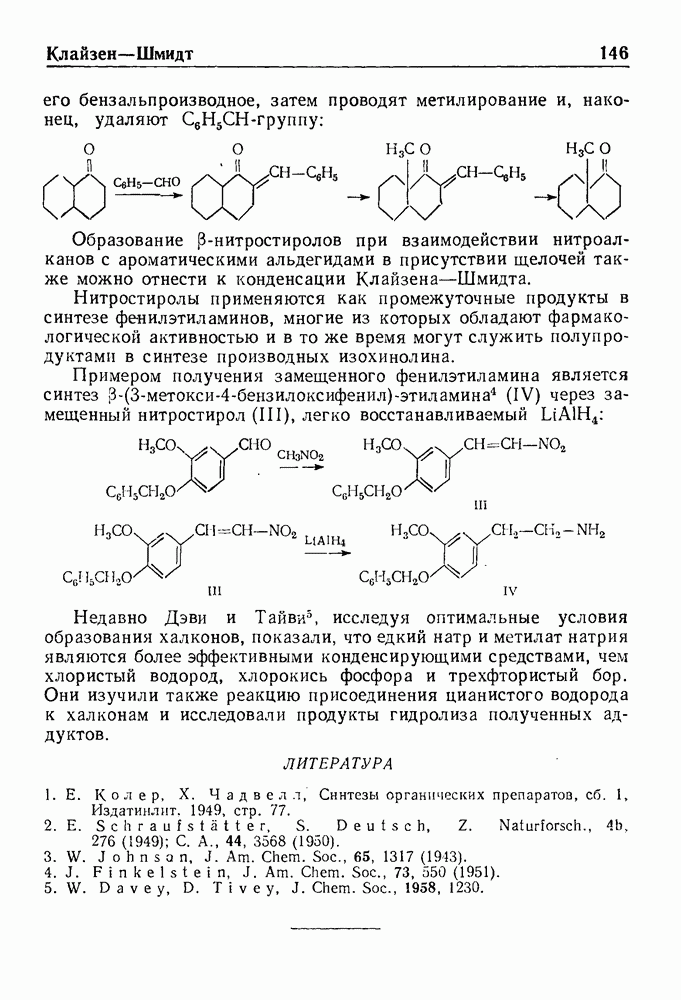
- КОНДЕНСАЦИЯ КЛАЙЗЕНА—ШМИДТА
- ВОССТАНОВЛЕНИЕ ПО КЛЕММЕНСЕНУ
- РЕАКЦИЯ КНЕВЕНАГЕЛЯ
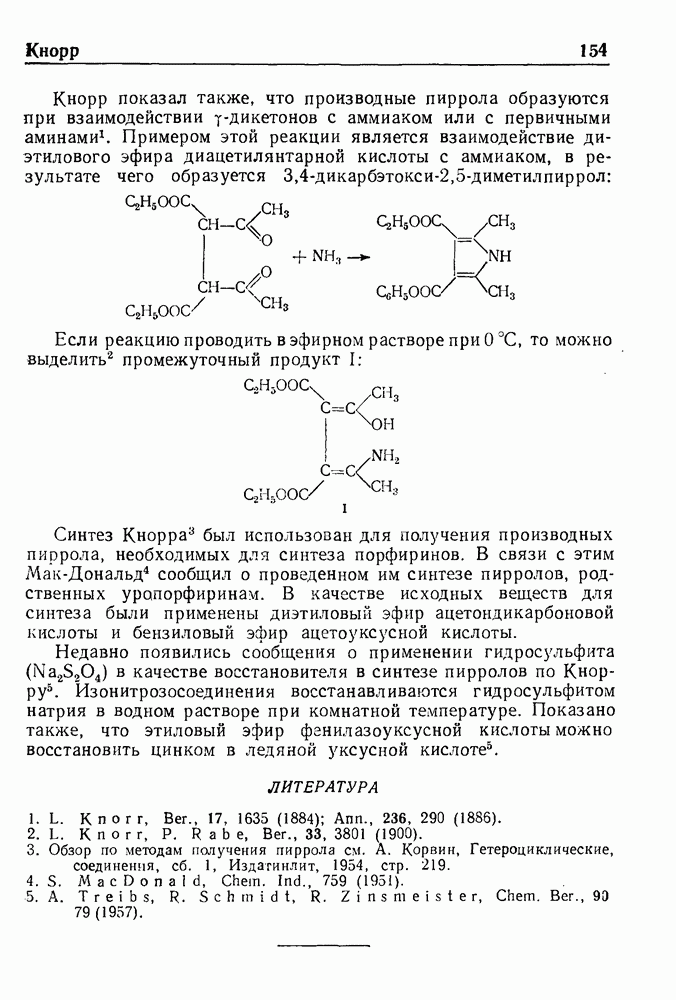
- СИНТЕЗ КНОРРА
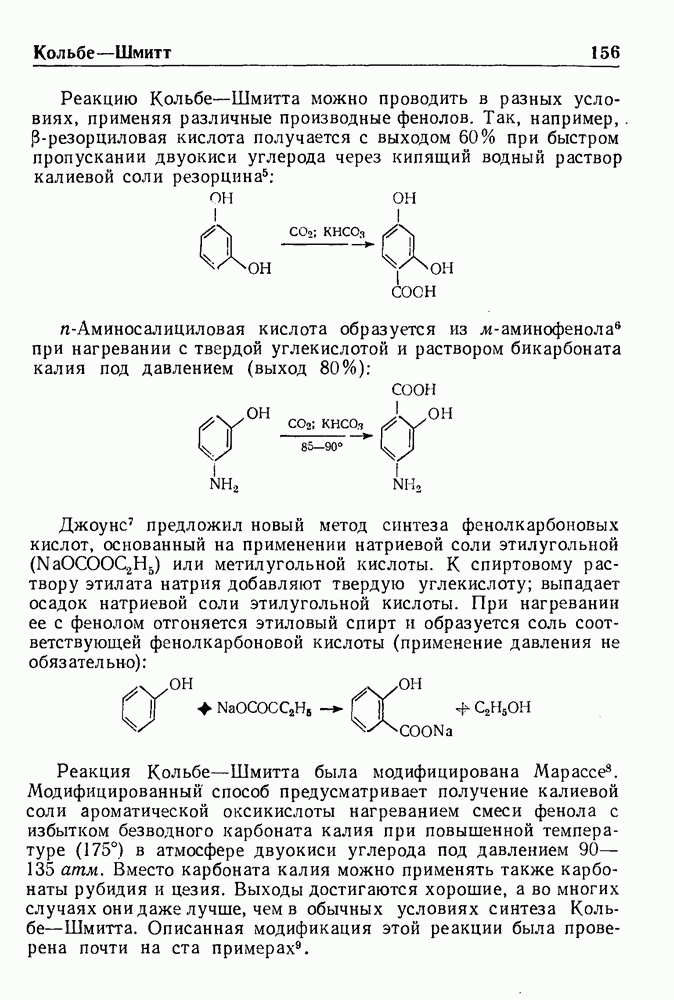
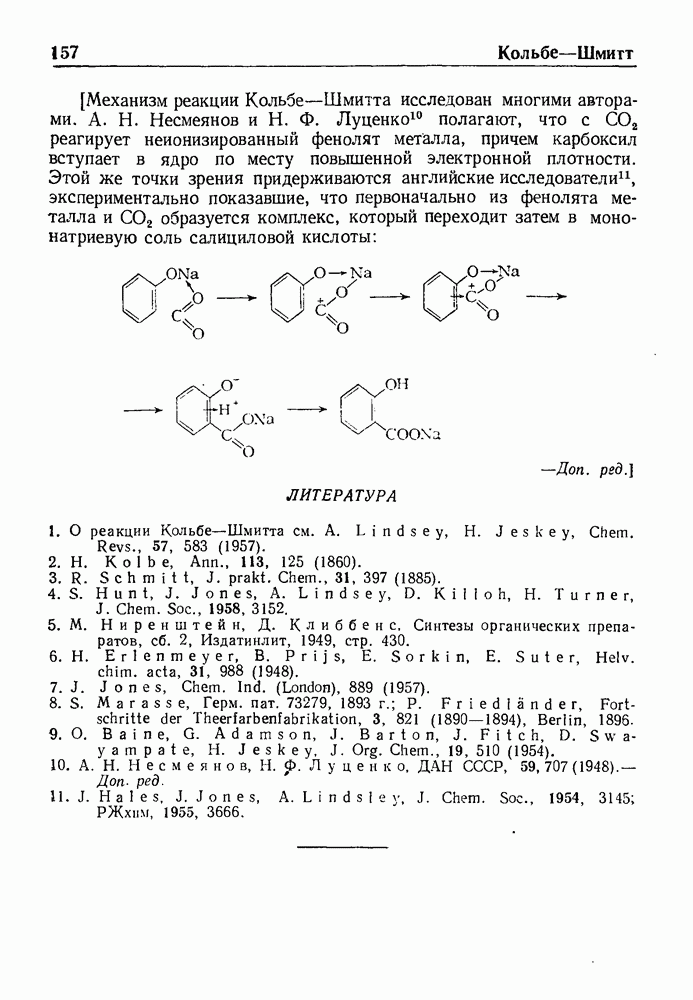
- РЕАКЦИЯ КОЛЬБЕ—ШМИТТА
- ЭЛЕКТРОХИМИЧЕСКАЯ РЕАКЦИЯ КОЛЬБЕ
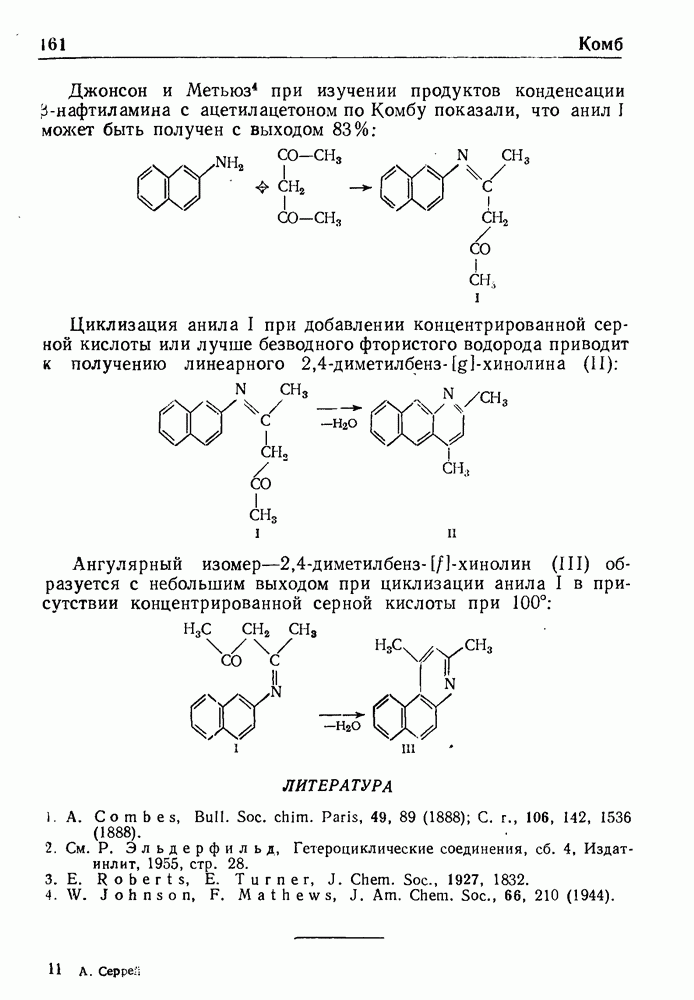
- СИНТЕЗ ХИНОЛИНА ПО КОМБУ
- РЕАКЦИЯ КОНОВАЛОВА
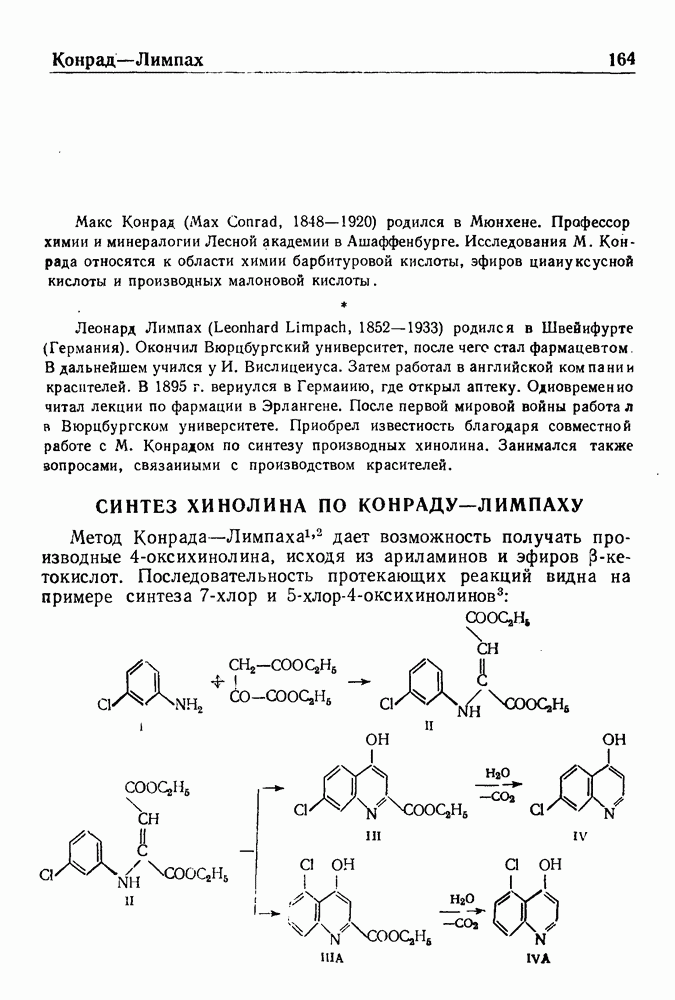
- СИНТЕЗ ХИНОЛИНА ПО КОНРАДУ—ЛИМПАХУ
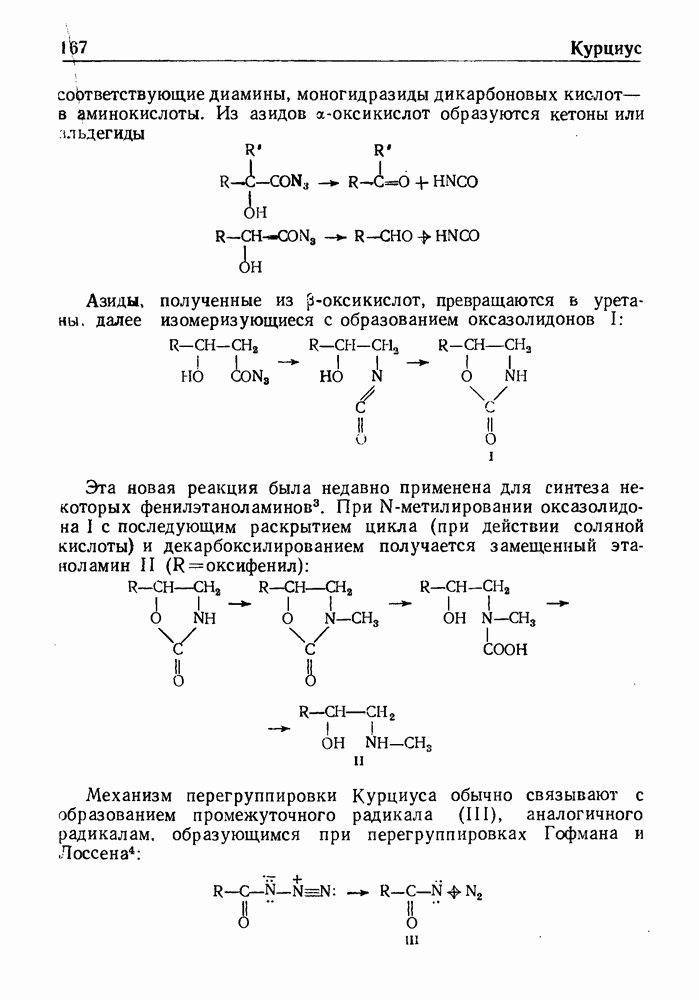
- РЕАКЦИЯ КУРЦИУСА
- РЕАКЦИЯ КУЧЕРОВА
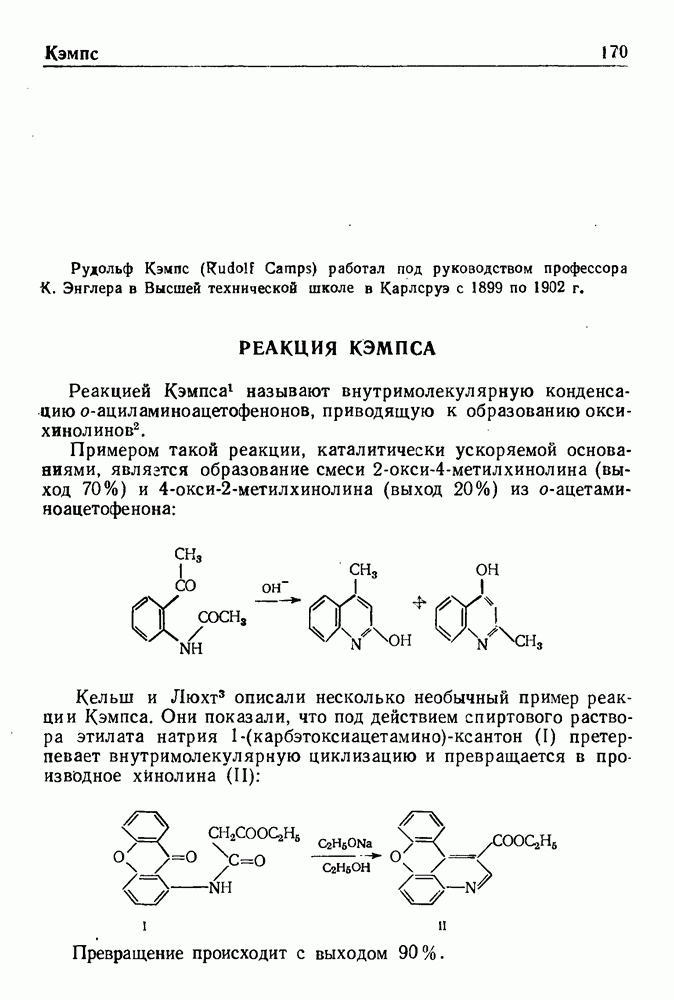
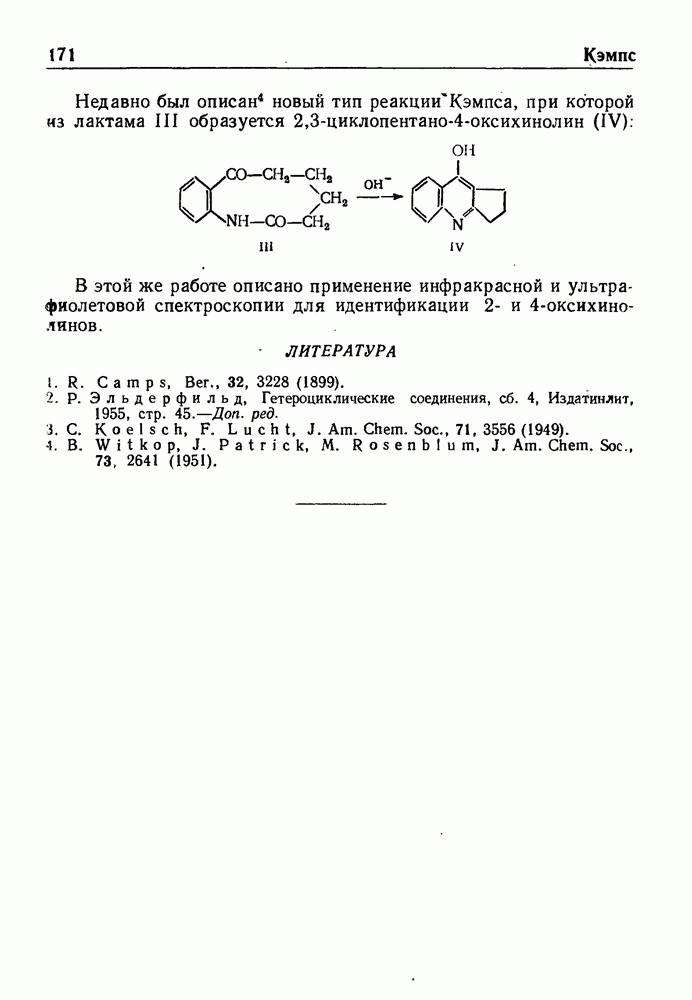
- РЕАКЦИЯ КЭМПСА
- РЕАКЦИЯ ЛЕЙКАРТА
- РЕАКЦИЯ ЛОССЕНА
- ВОССТАНОВЛЕНИЕ ПО МАК ФАДИЕНУ—СТИВЕНСУ
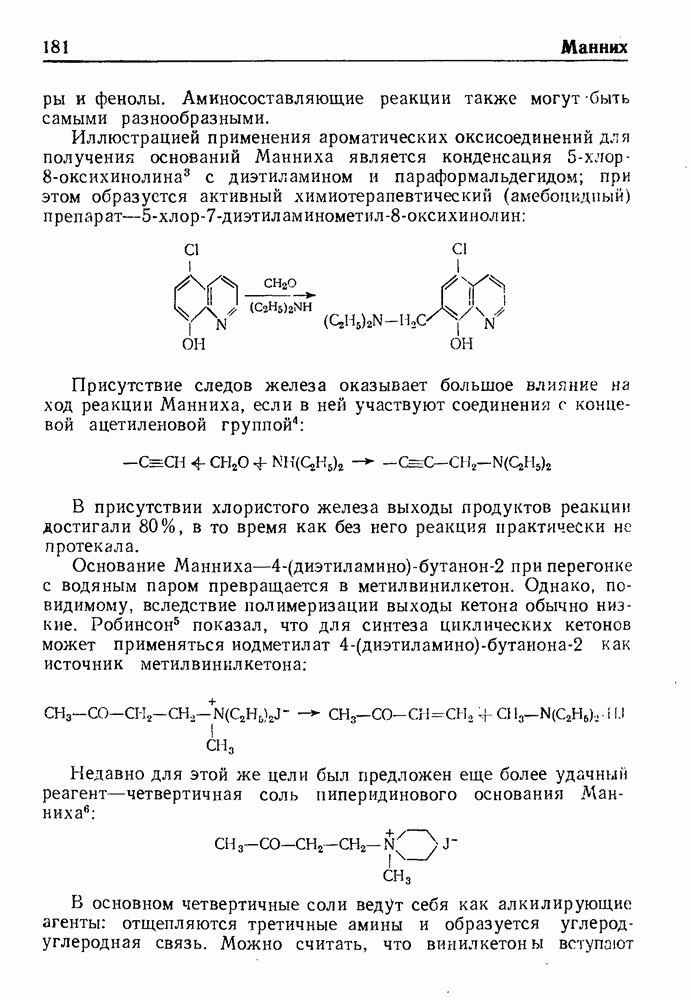
- РЕАКЦИЯ МАННИХА
- КОНДЕНСАЦИЯ МЕЕРВЕЙНА
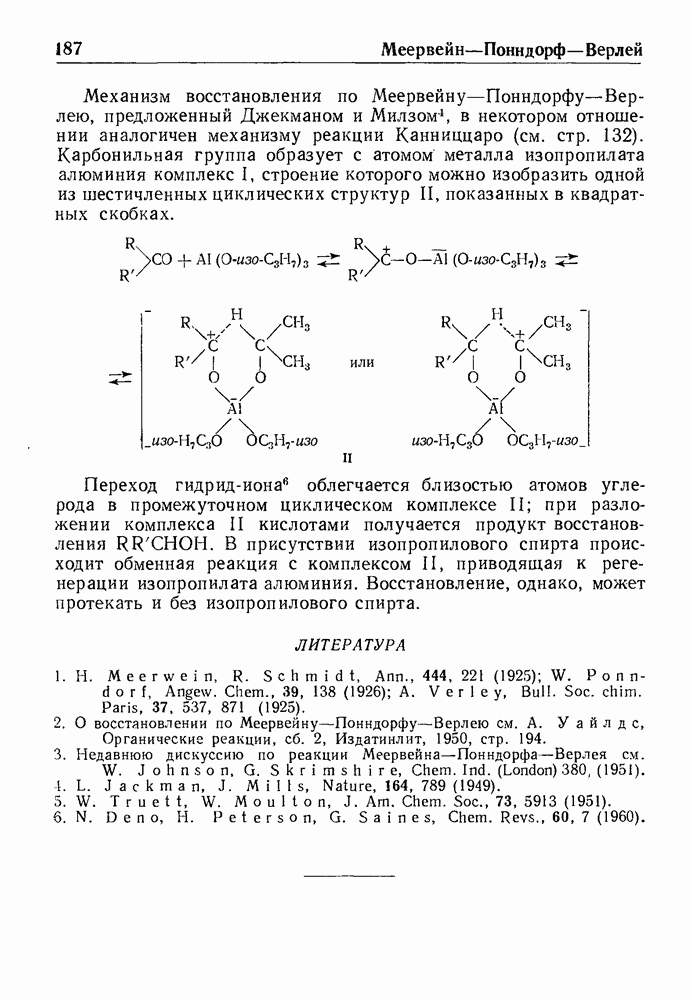
- ВОССТАНОВЛЕНИЕ ПО МЕЕРВЕЙНУ-ПОННДОРФУ-ВЕРЛЕЮ
- РЕАКЦИЯ МИХАЭЛЯ
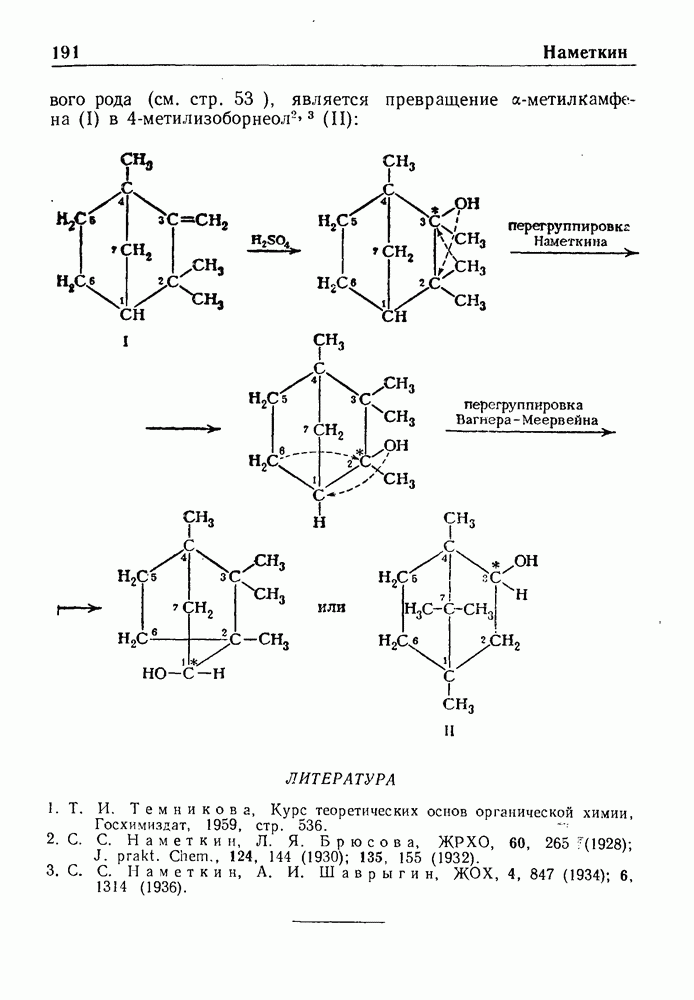
- ПЕРЕГРУППИРОВКА НАМЕТКИНА
- РЕАКЦИЯ НЕСМЕЯНОВА
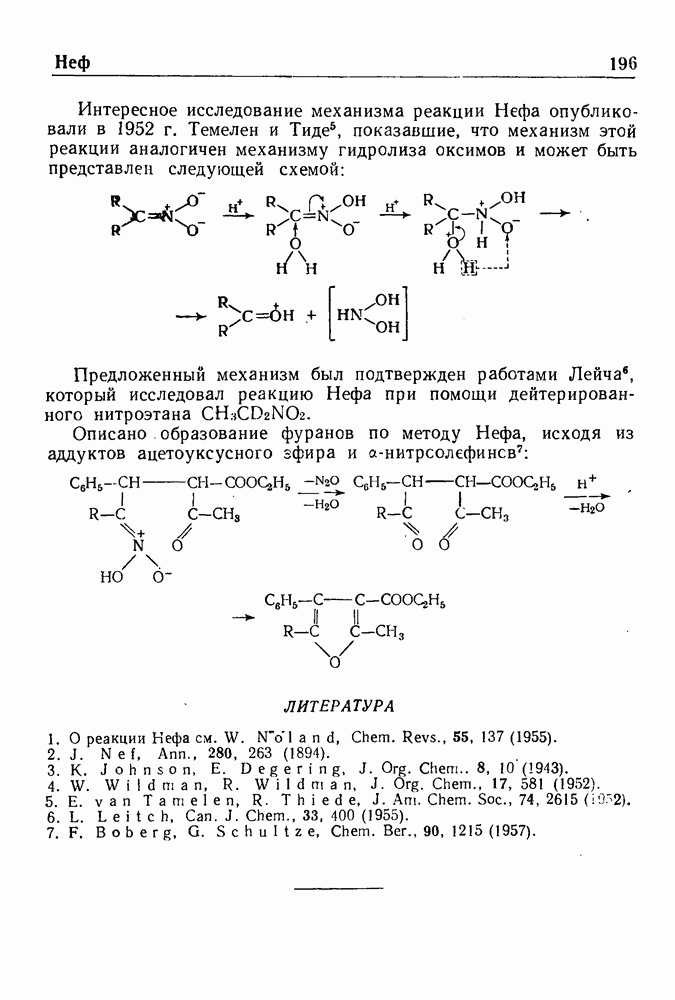
- РЕАКЦИЯ НЕФА
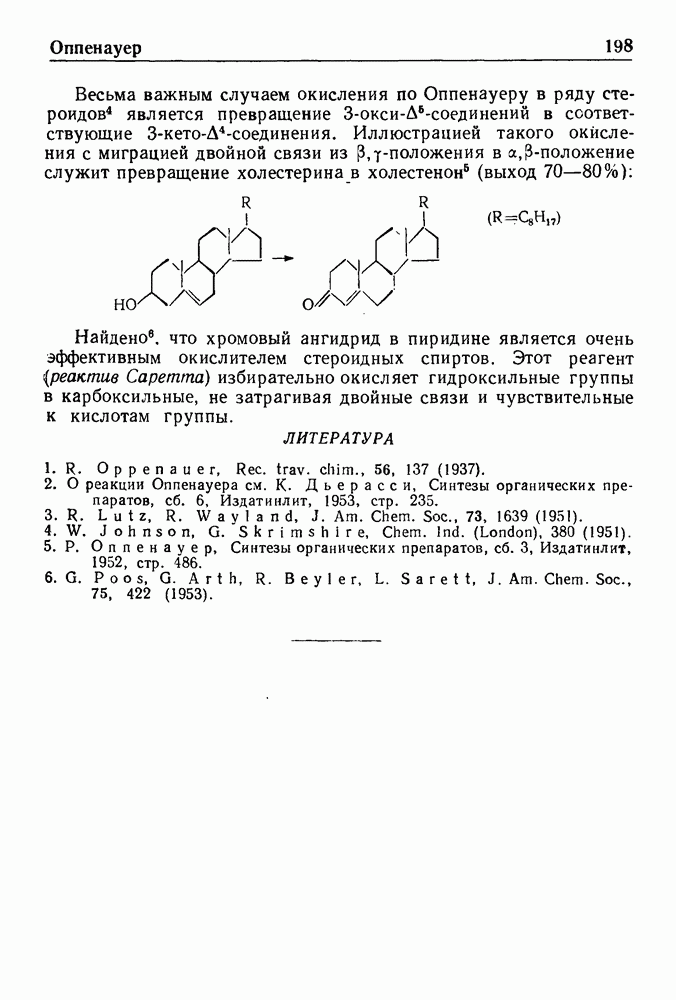
- ОКИСЛЕНИЕ ПО ОППЕНАУЕРУ
- РЕАКЦИЯ ПАССЕРИНИ
- РЕАКЦИЯ ПЕРКИНА
- КОНДЕНСАЦИЯ ПЕХМАНА
- РЕАКЦИЯ ПИКТЭ—ШПЕНГЛЕРА
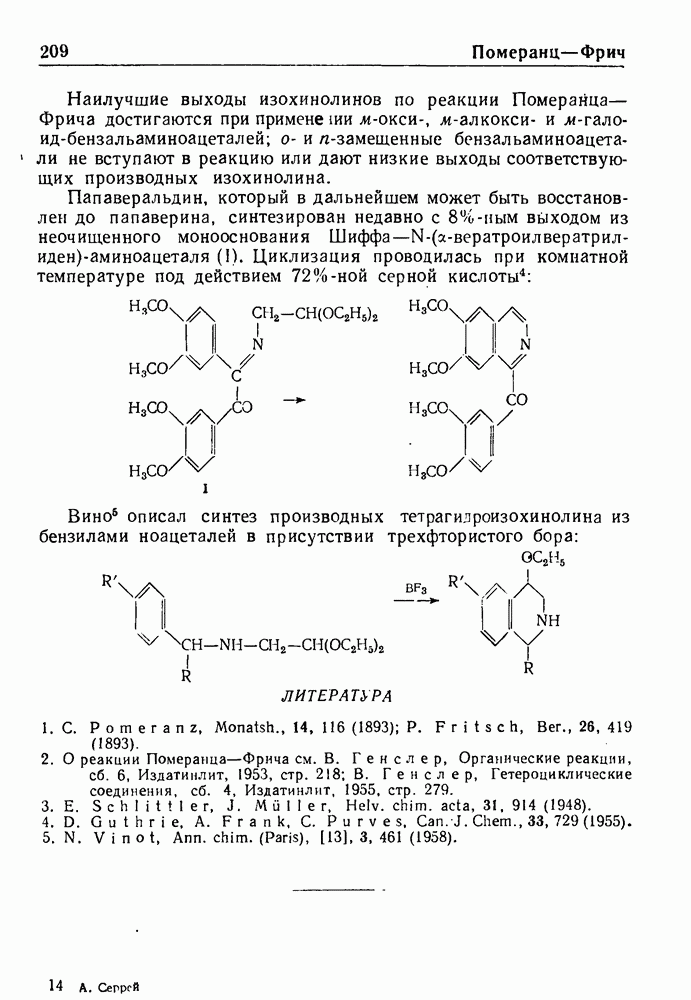
- РЕАКЦИЯ ПОМЕРАНЦА—ФРИЧА
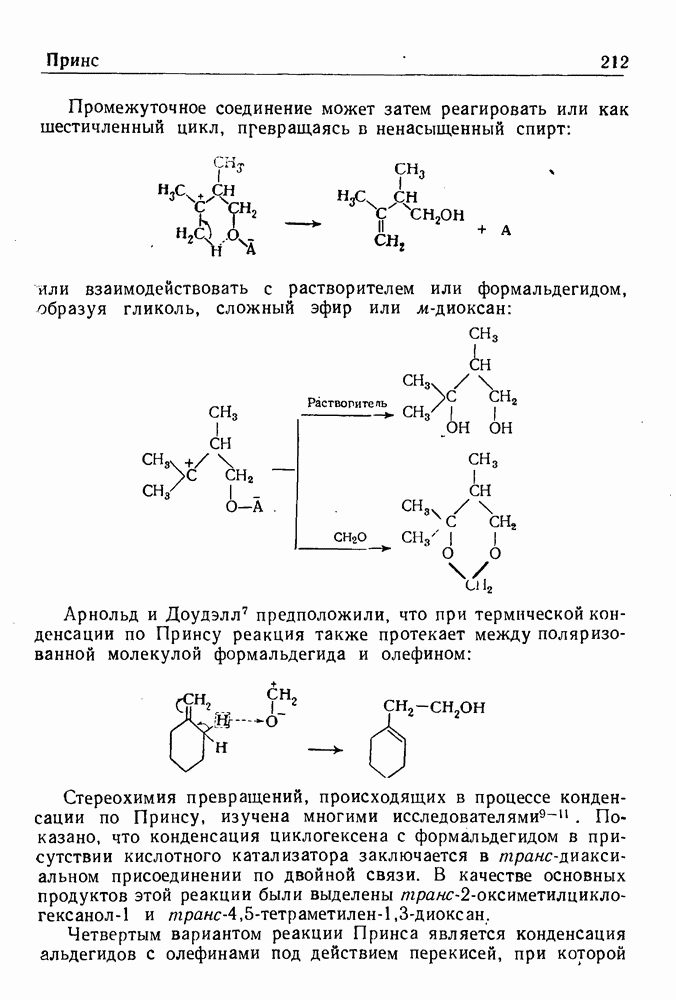
- РЕАКЦИЯ ПРИНСА
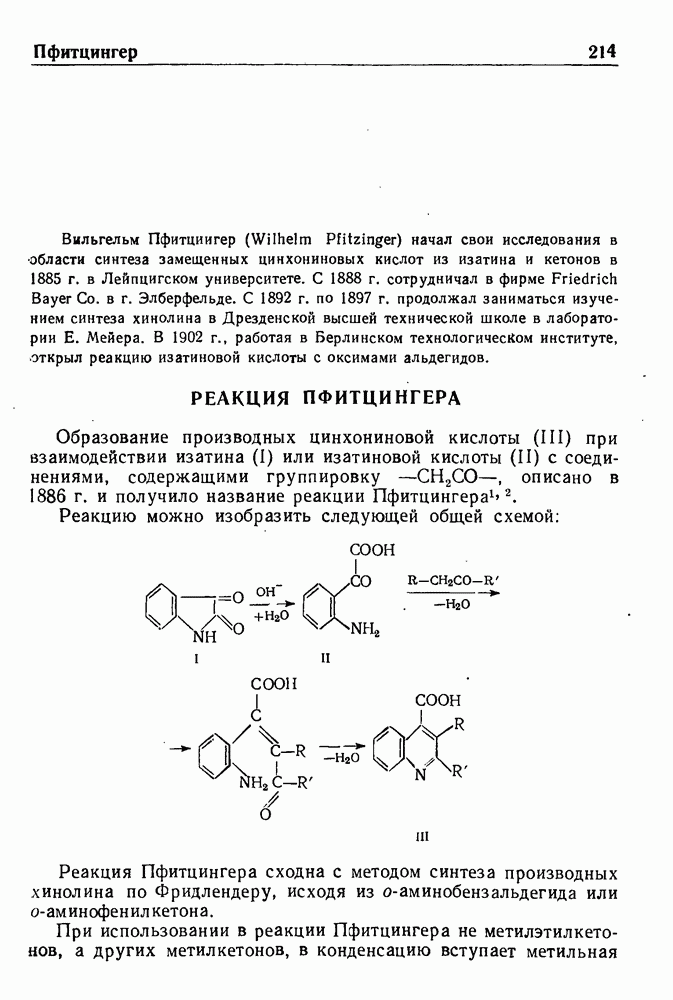
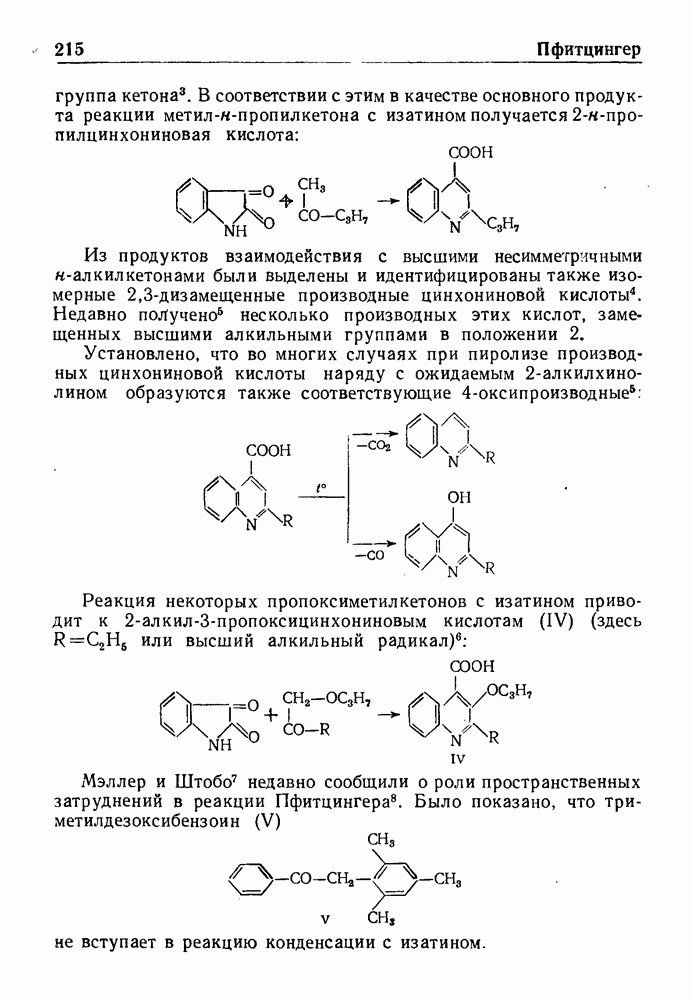
- РЕАКЦИЯ ПФИТЦИНГЕРА
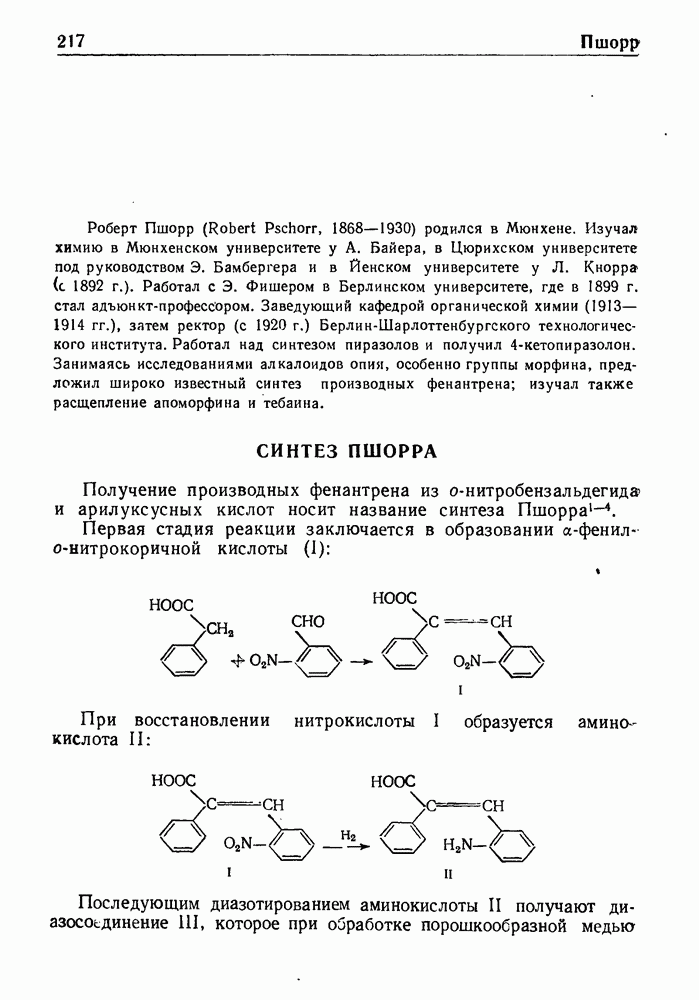
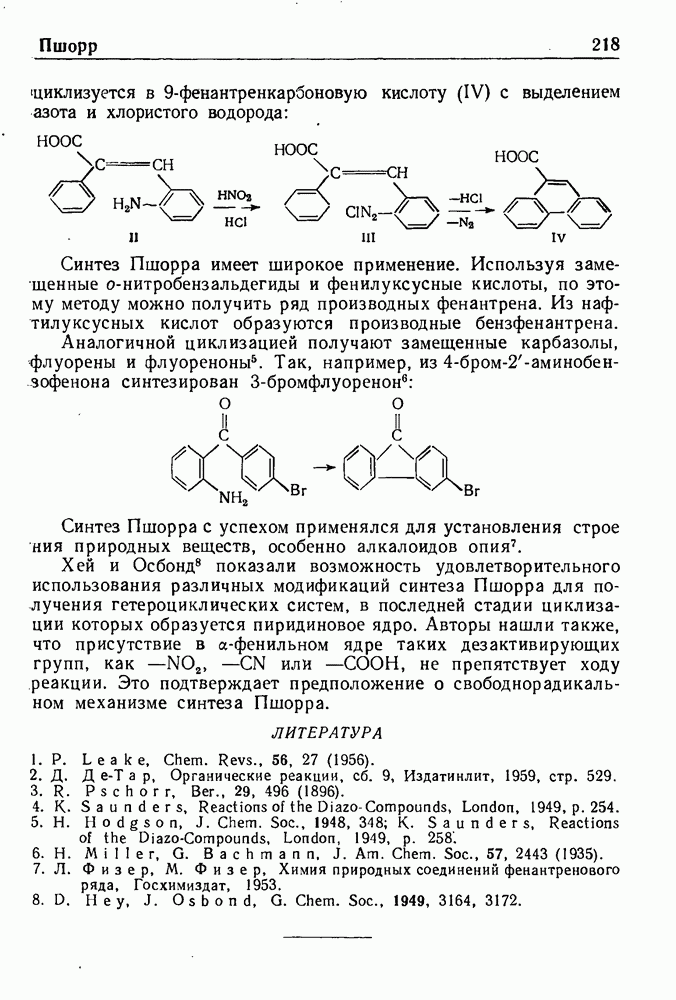
- СИНТЕЗ ПШОРРА
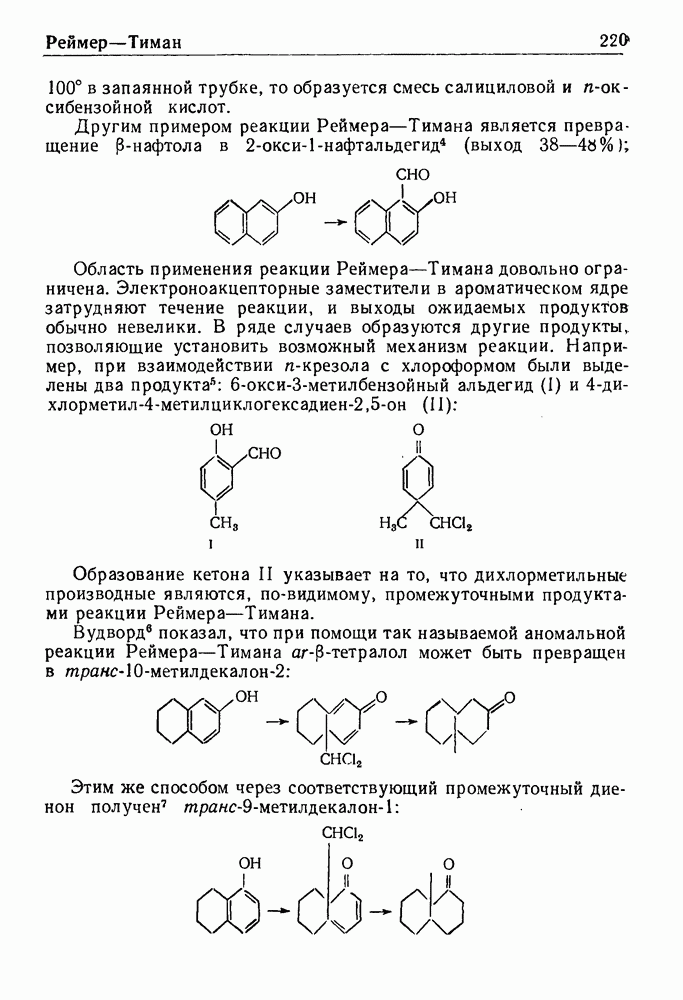
- РЕАКЦИЯ РЕЙМЕРА—ТИМАНА
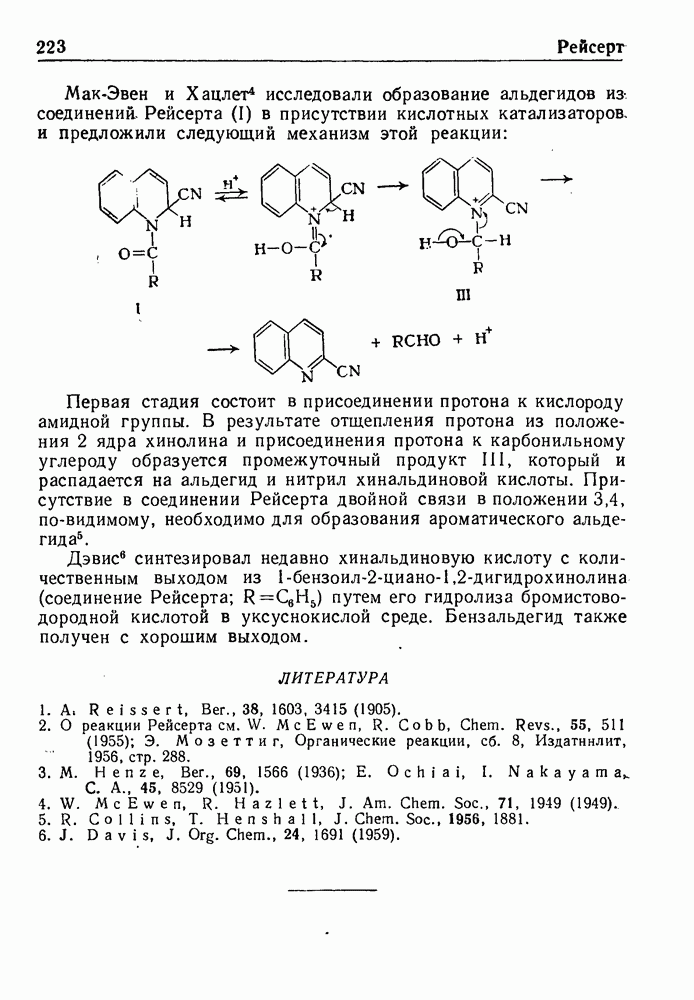
- РЕАКЦИЯ РЕЙСЕРТА
- РЕАКЦИЯ РЕФОРМАТСКОГО
- РЕАКЦИЯ РОДИОНОВА
- ВОССТАНОВЛЕНИЕ ПО РОЗЕНМУНДУ
- РЕАКЦИЯ СКРАУПА
- РЕАКЦИЯ СОММЛЕ
- РЕАКЦИЯ СТЕФЕНА
- ПЕРЕГРУППИРОВКА СТИВЕНСА
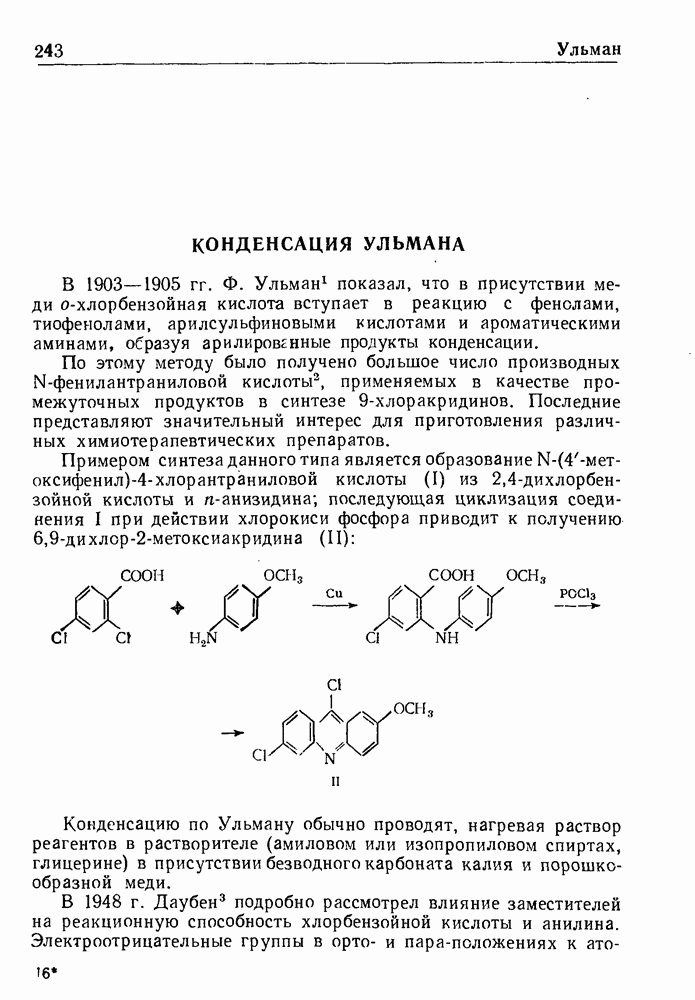
- РЕАКЦИЯ УЛЬМАНА
- КОНДЕНСАЦИЯ УЛЬМАНА
- ПЕРЕГРУППИРОВКА ФАВОРСКОГО
- СИНТЕЗ ИНДОЛА ПО ФИШЕРУ
- РЕАКЦИЯ ФРИДЕЛЯ—КРАФТСА
- СИНТЕЗ ФРИДЛЕНДЕРА
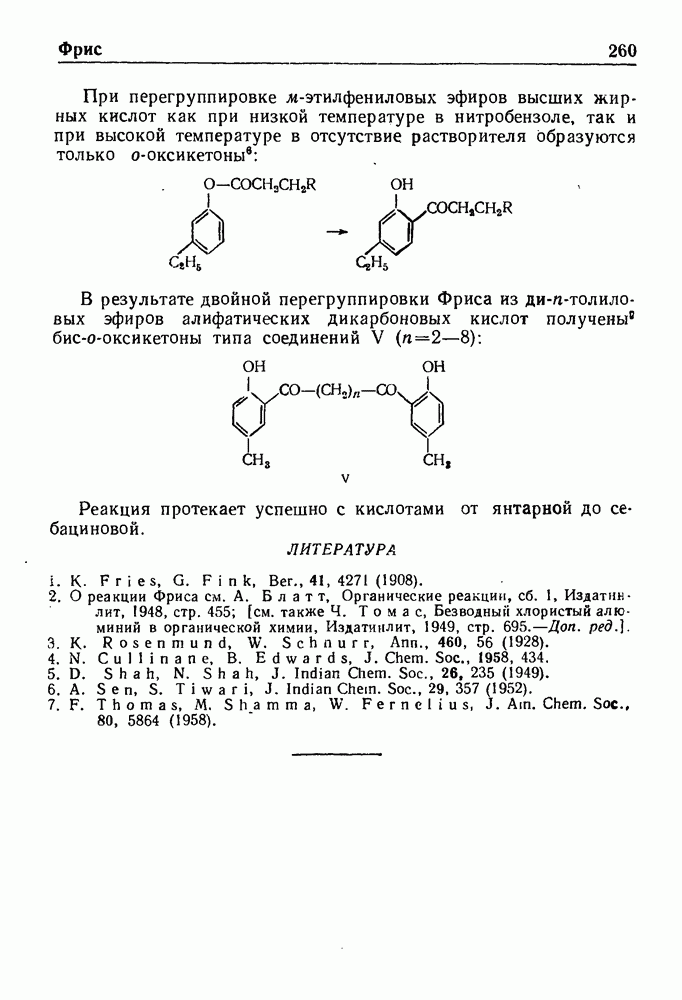
- РЕАКЦИЯ ФРИСА
- РЕАКЦИЯ ХУНСДИККЕРА
- РЕАКЦИЯ ЧИЧИБАБИНА
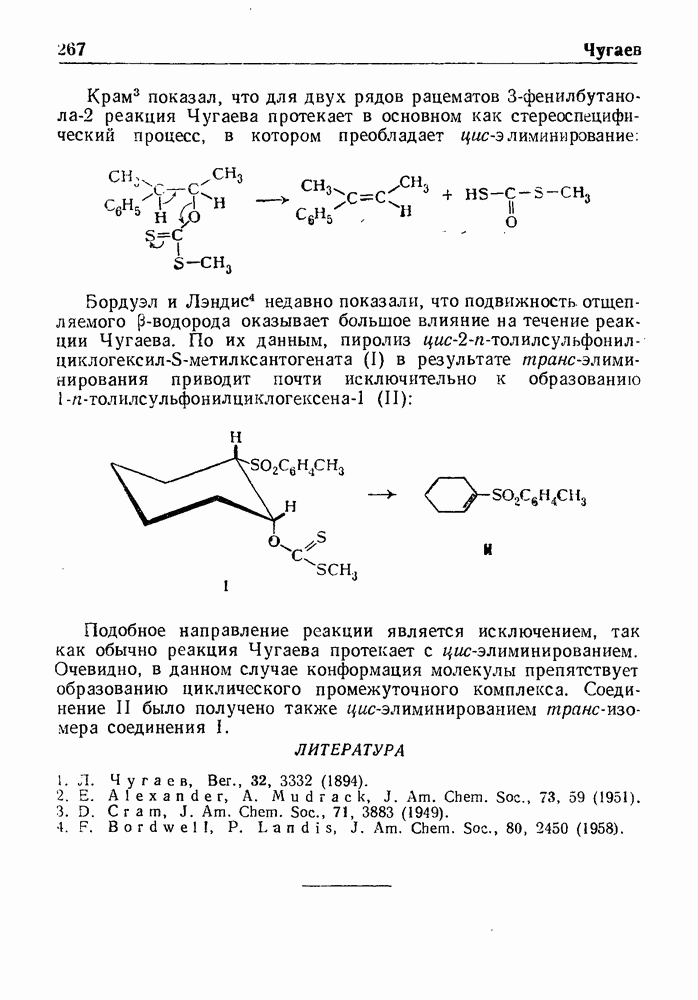
- РЕАКЦИЯ ЧУГАЕВА
- РЕАКЦИЯ ШИМАНА
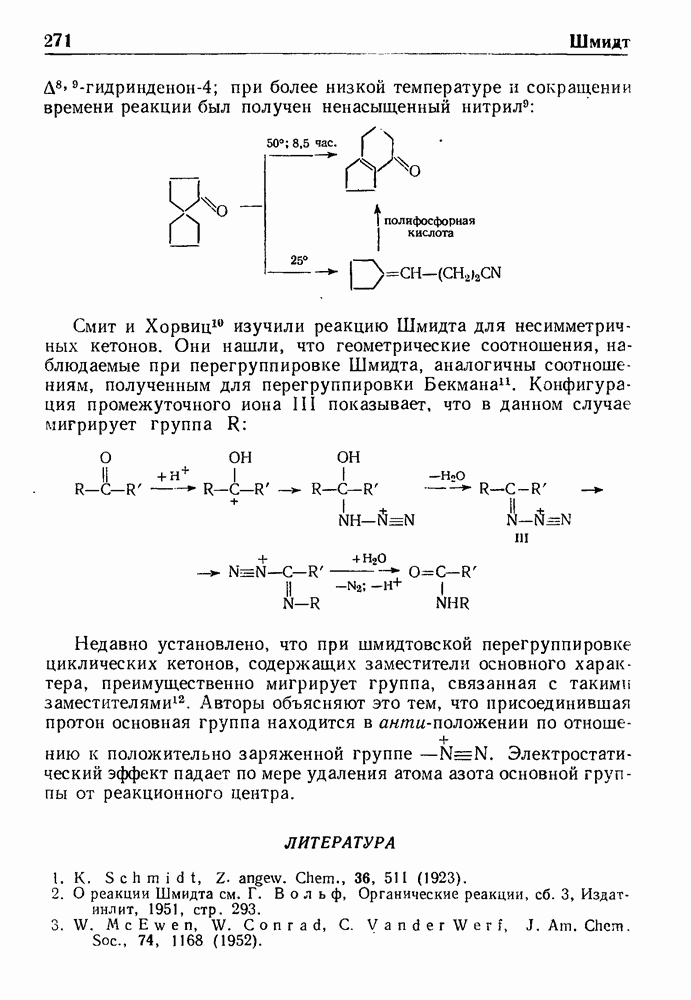
- РЕАКЦИИ ШМИДТА
- КОНДЕНСАЦИЯ ШТОББЕ
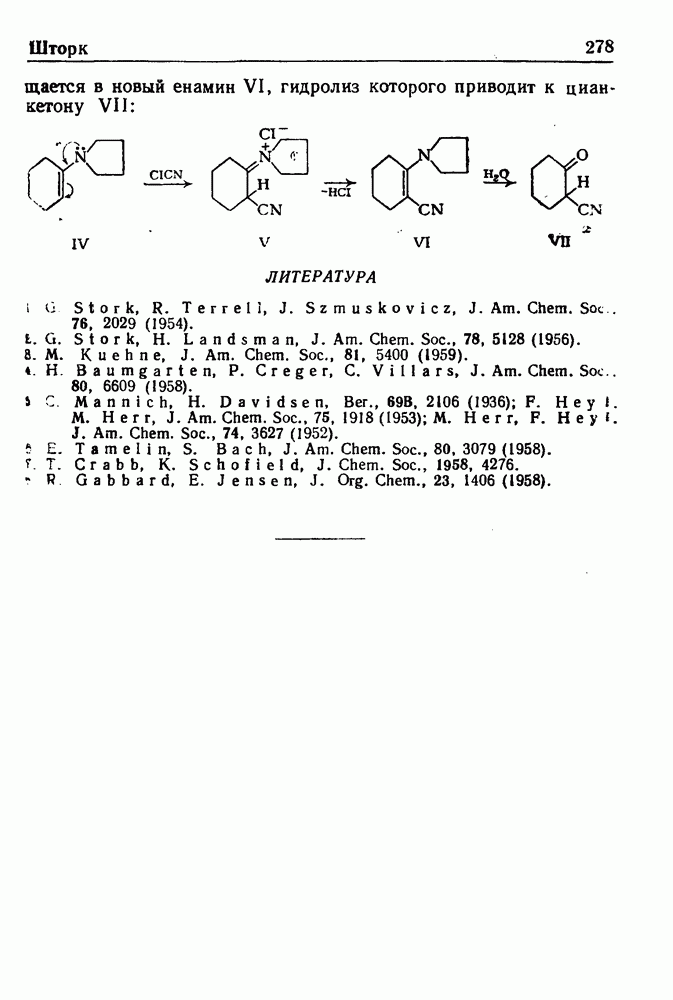
- РЕАКЦИЯ ШТОРКА
- РЕАКЦИЯ ЭЛБСА
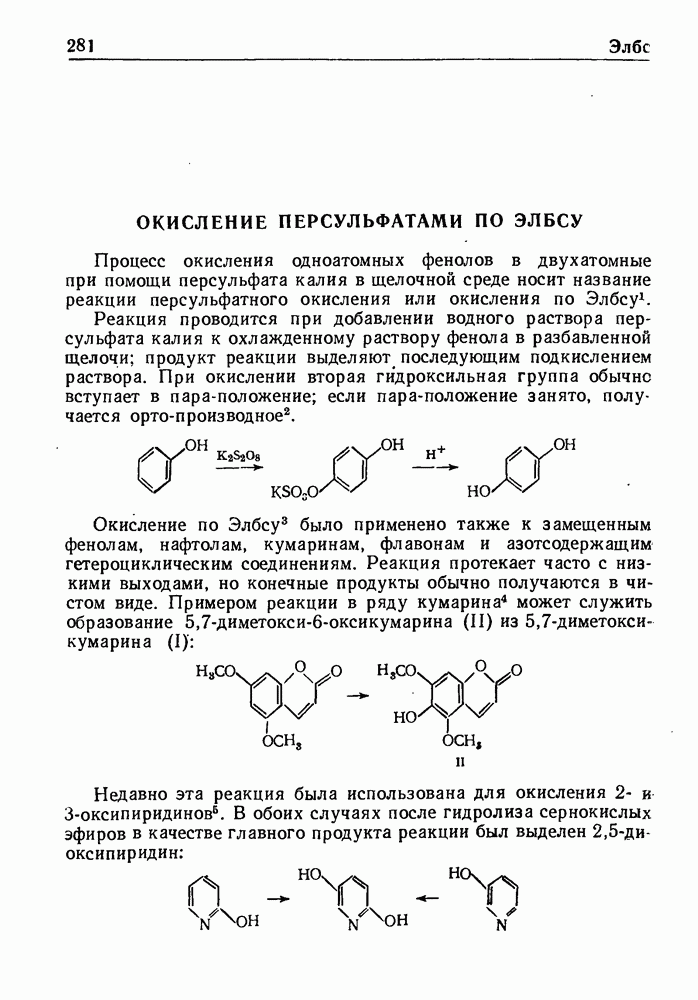
- ОКИСЛЕНИЕ ПЕРСУЛЬФАТАМИ ПО ЭЛБСУ
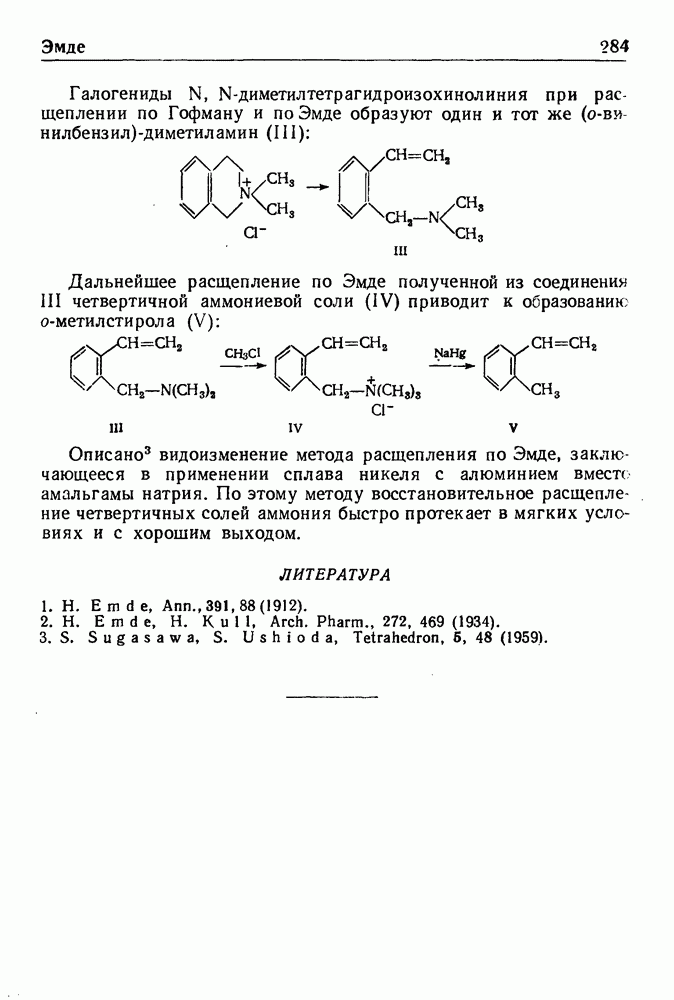
- РАСЩЕПЛЕНИЕ ПО ЭМДЕ
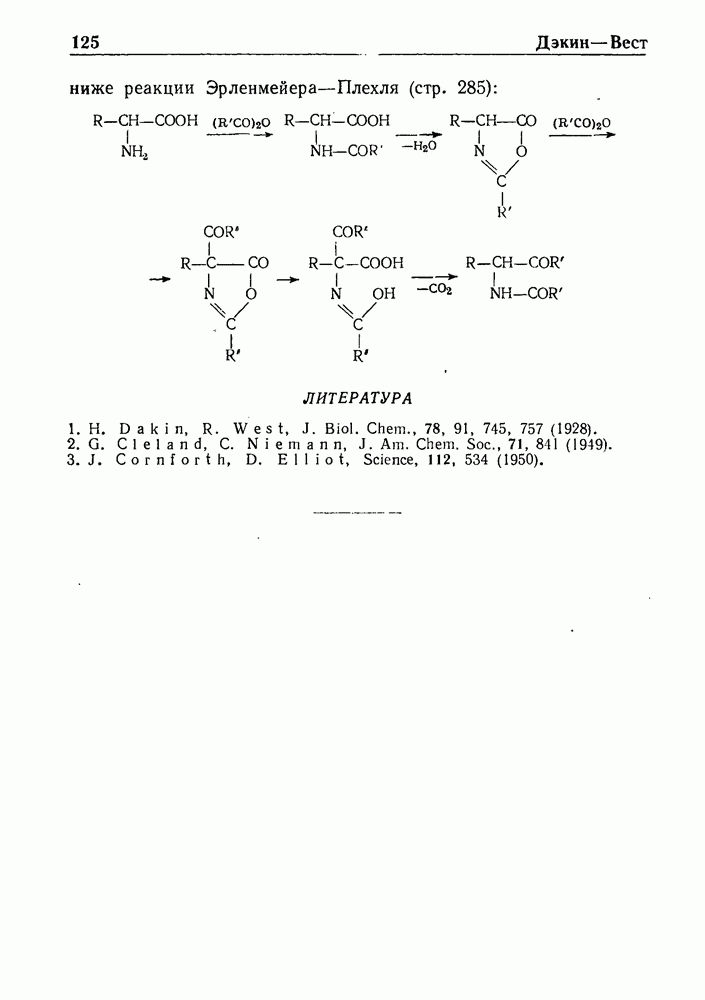
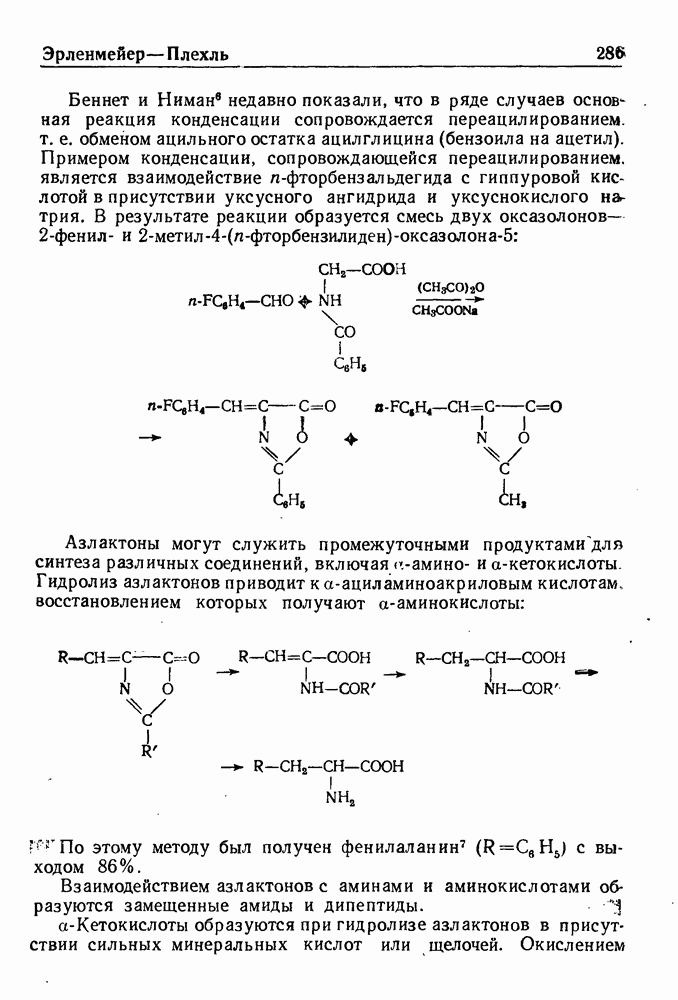
- СИНТЕЗ АЗЛАКТОНОВ ПО ЭРЛЕНМЕИЕРУ—ПЛЕХЛЮ
- РЕАКЦИЯ ЯКОБСЕНА