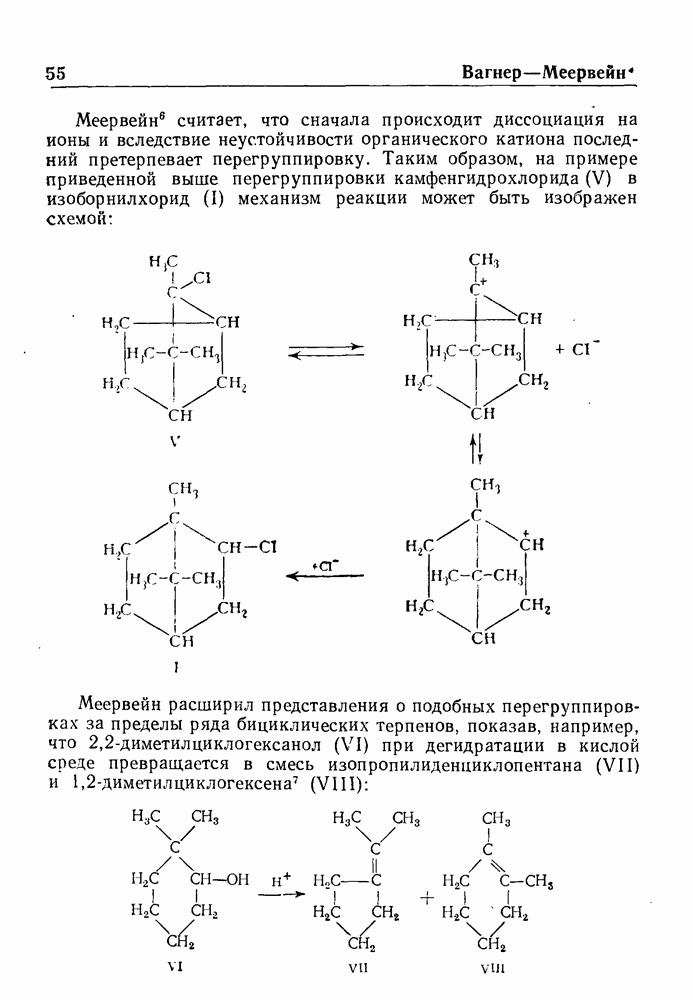
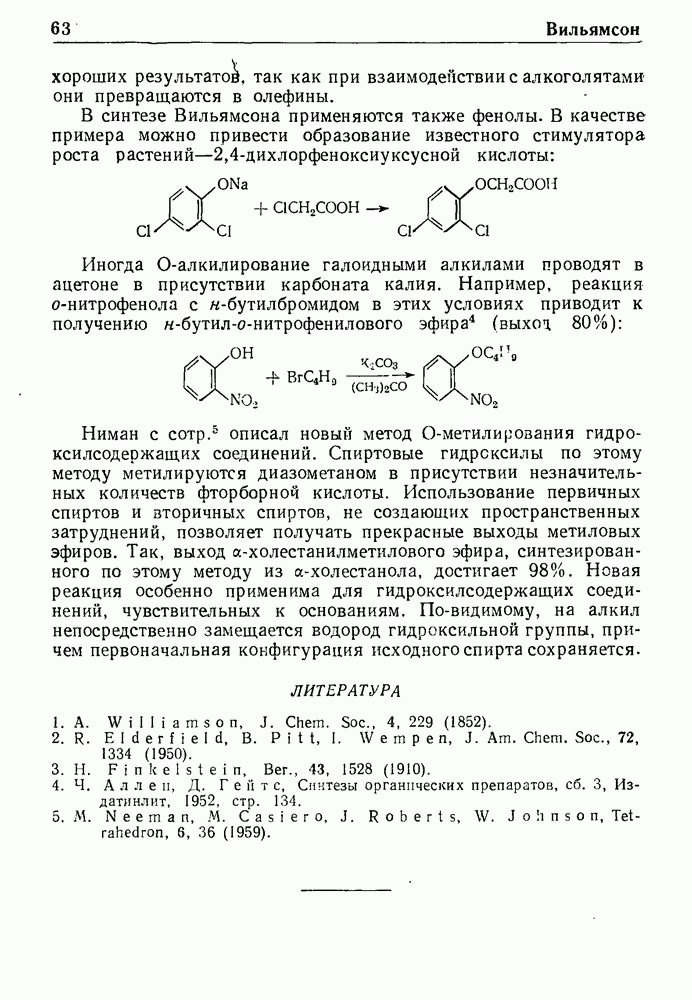
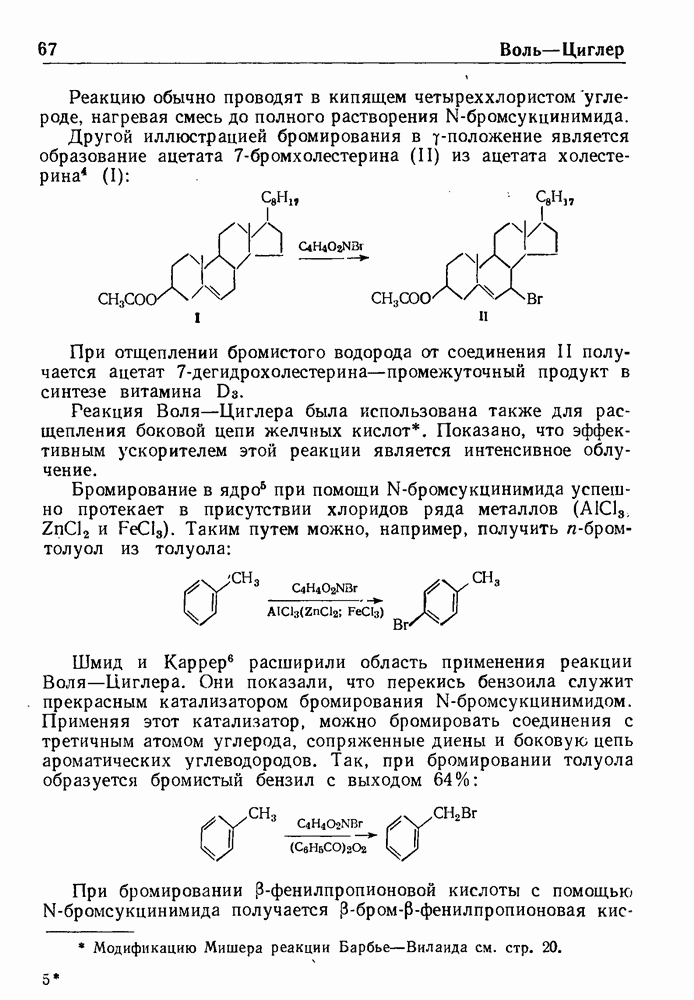
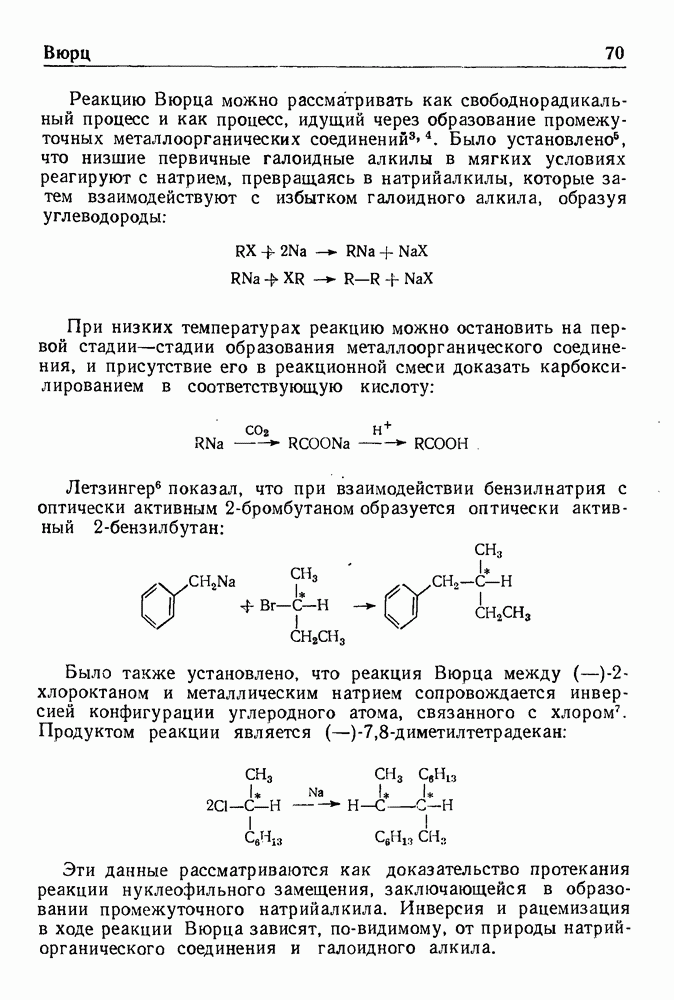
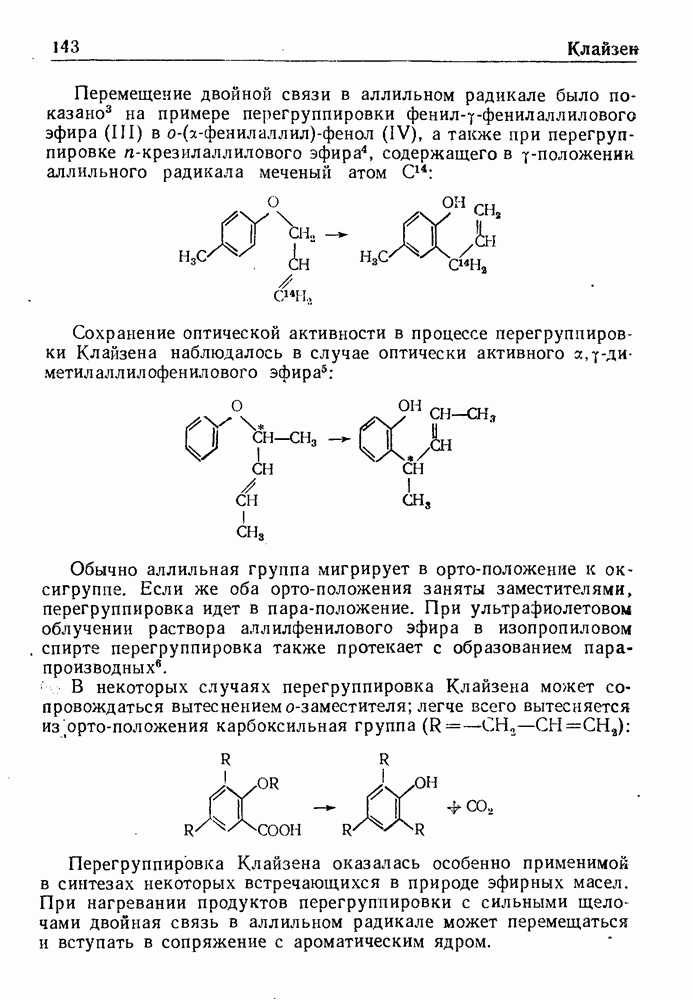
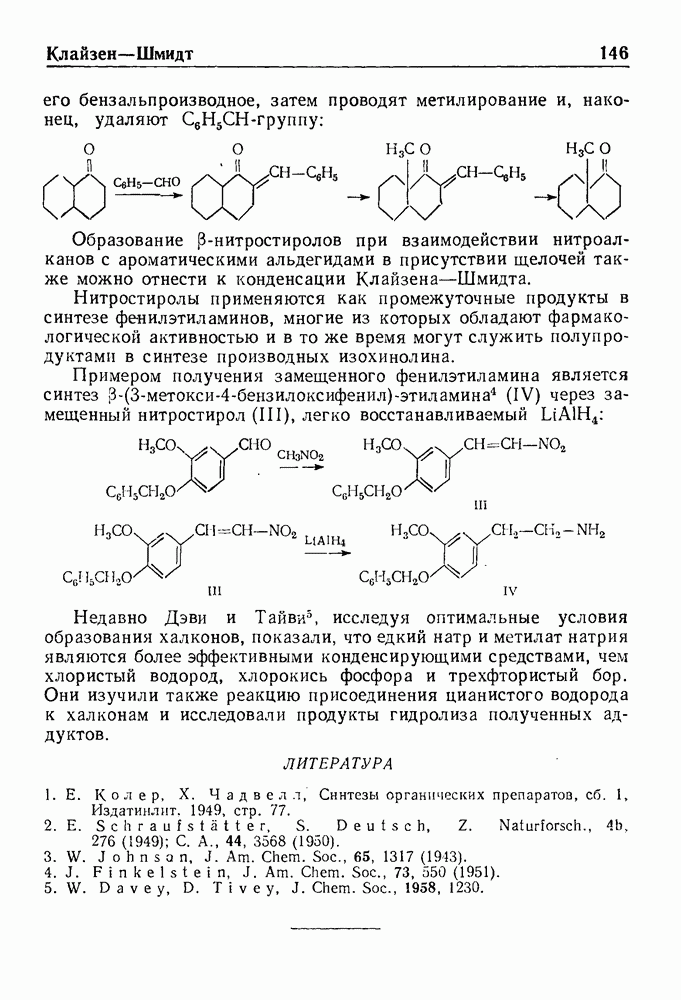
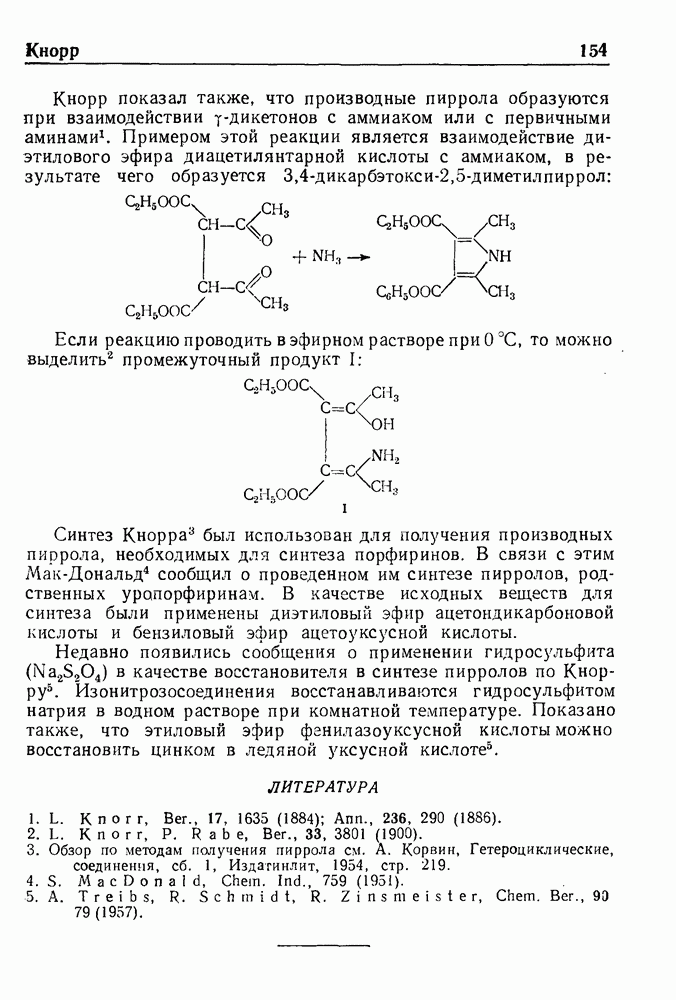
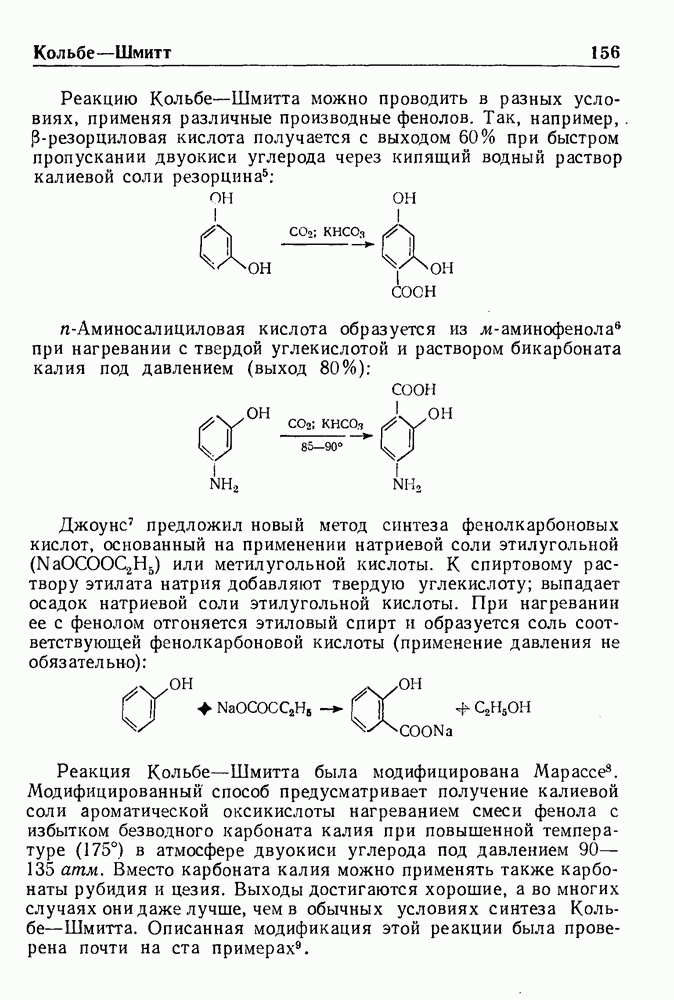
| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
КОНДЕНСАЦИЯ УЛЬМАНА
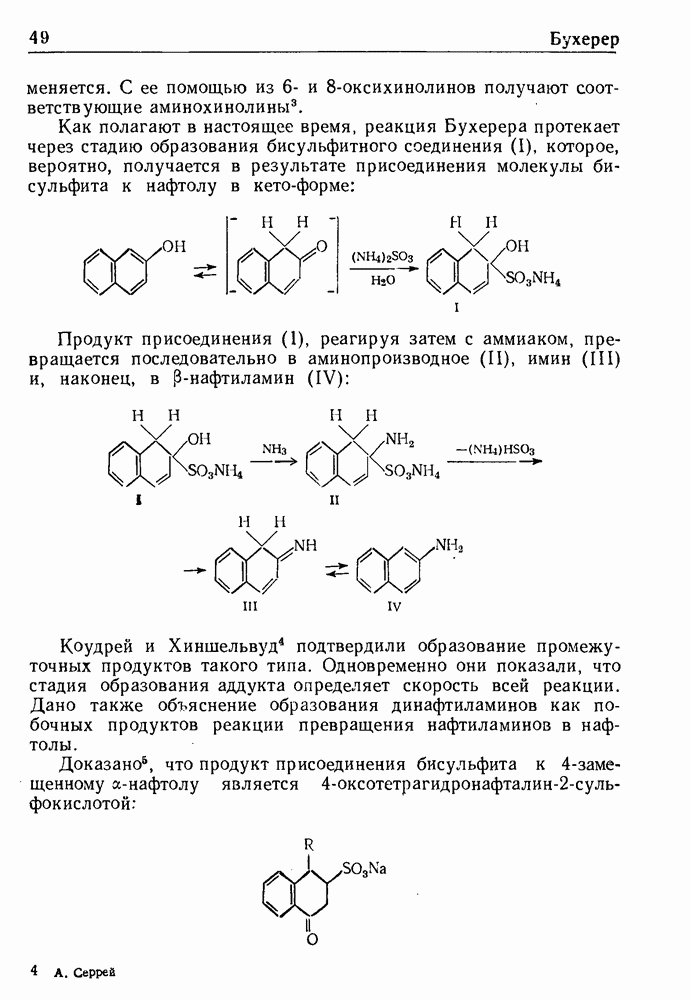
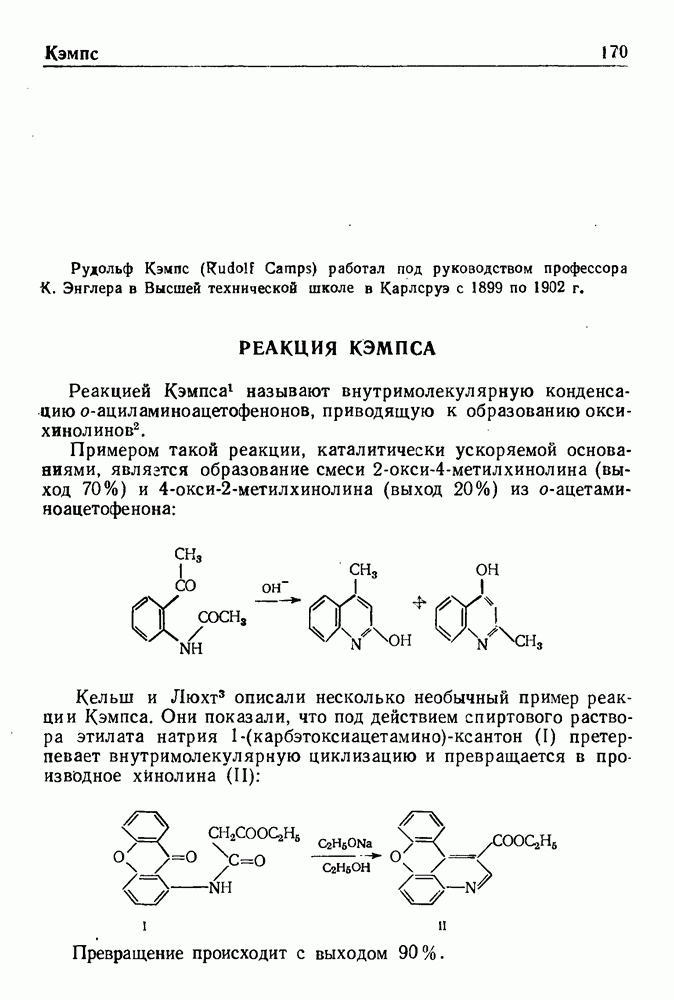
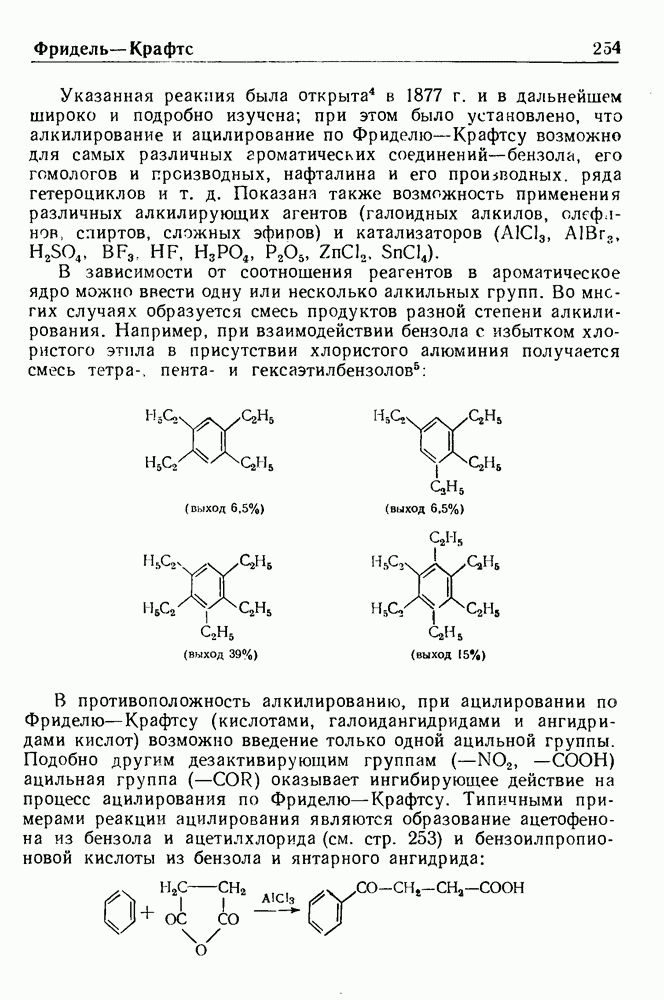
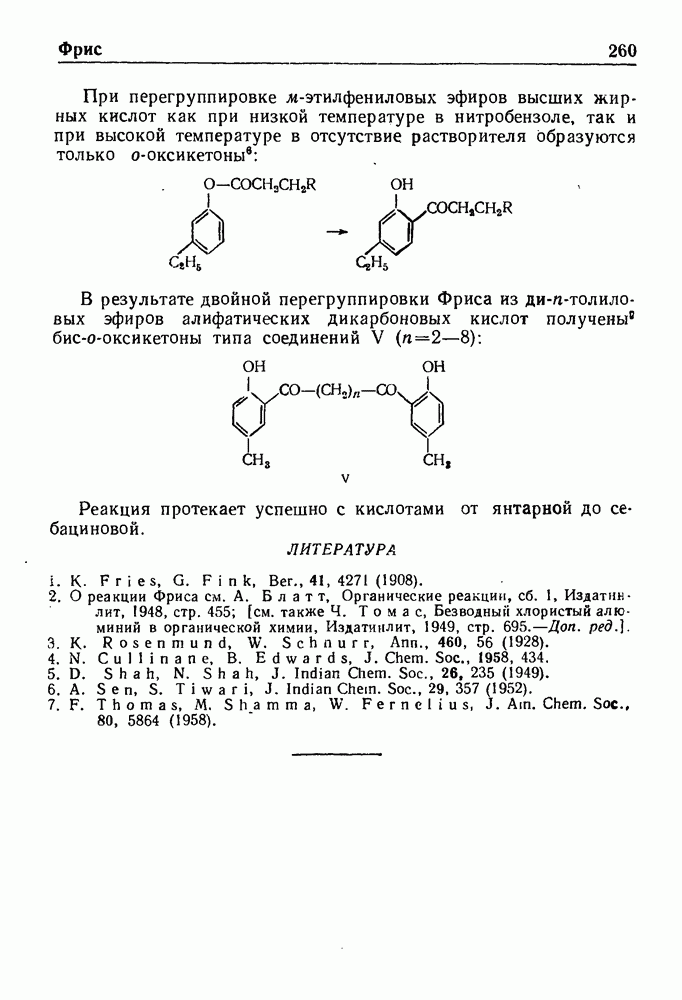
В 1903-1905 гг. Ф. Ульман показал, что в присутствии меди  -хлорбензойная кислота вступает в реакцию с фенолами, тиофенолами, арилсульфиновыми кислотами и ароматическими аминами, образуя арилировгнные продукты конденсации.
-хлорбензойная кислота вступает в реакцию с фенолами, тиофенолами, арилсульфиновыми кислотами и ароматическими аминами, образуя арилировгнные продукты конденсации.
По этому методу было получено большое число производных  -фенилантраниловой кислоты, применяемых в качестве промежуточных продуктов в синтезе
-фенилантраниловой кислоты, применяемых в качестве промежуточных продуктов в синтезе  -хлоракридинов. Последние представляют значительный интерес для приготовления различных химиотерапевтических препаратов.
-хлоракридинов. Последние представляют значительный интерес для приготовления различных химиотерапевтических препаратов.
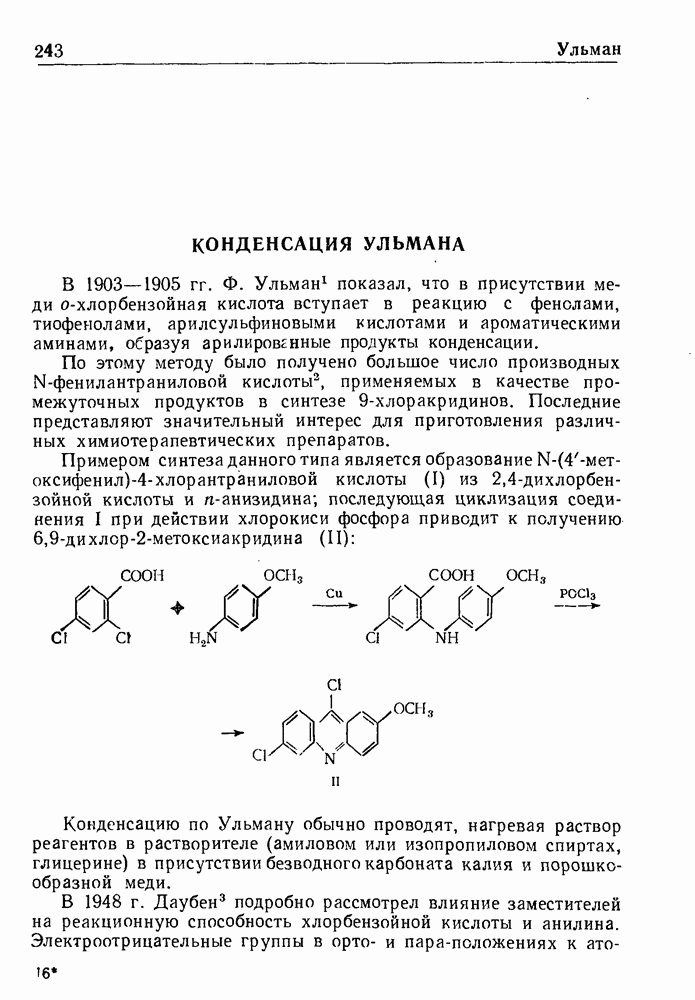
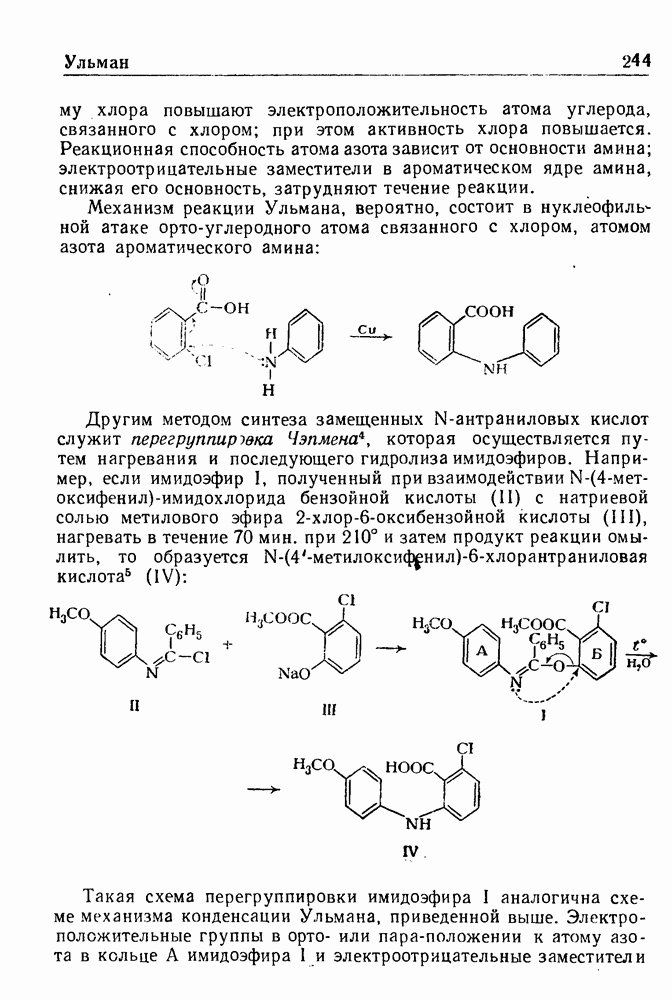
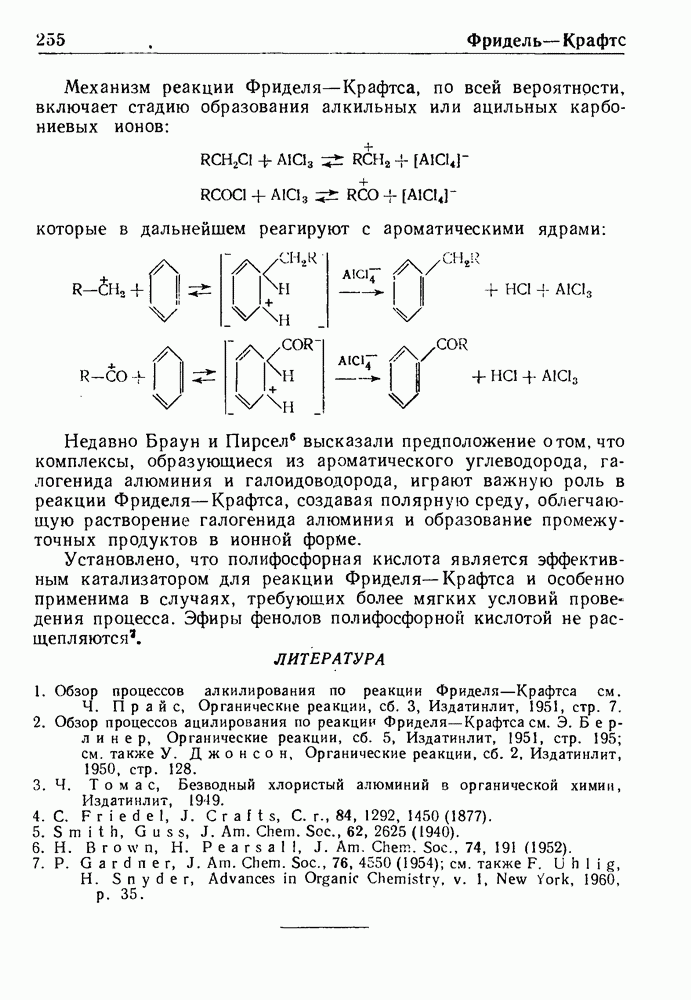
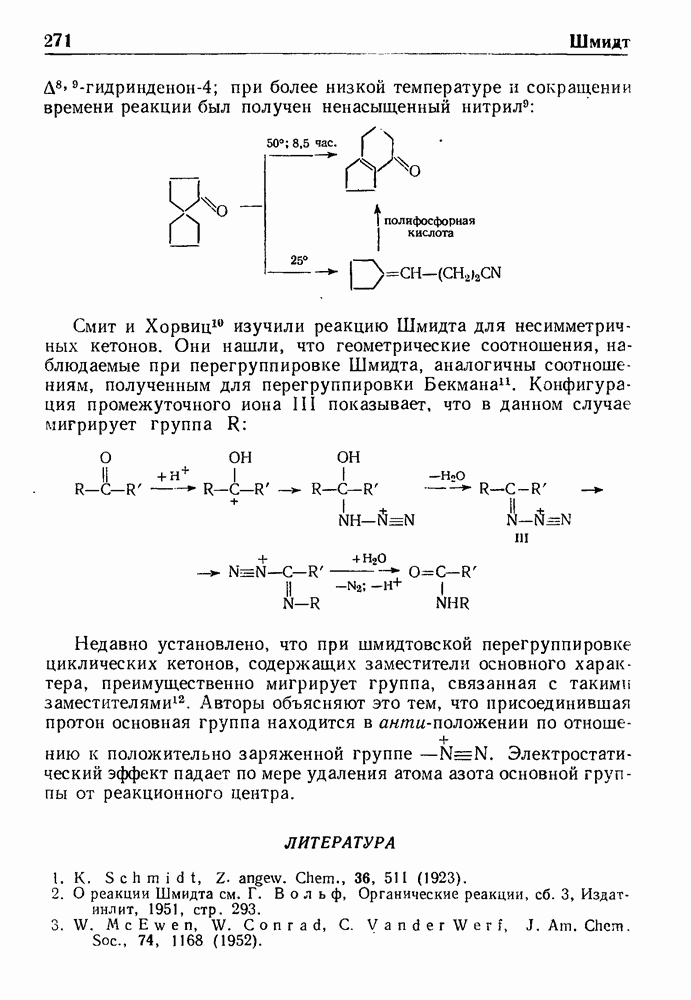
Примером синтеза данного типа является образование N-(4-мет-оксифенил)-4-хлорантраниловой кислоты (I) из  -дихлорбензойной кислоты и
-дихлорбензойной кислоты и  -анизидина; последующая циклизация соединения I при действии хлорокиси фосфора приводит к получению 6,9-дихлор-2-метоксиакридина (II):
-анизидина; последующая циклизация соединения I при действии хлорокиси фосфора приводит к получению 6,9-дихлор-2-метоксиакридина (II):

Конденсацию по Ульману обычно проводят, нагревая раствор реагентов в растворителе (амиловом или изопропиловом спиртах, глицерине) в присутствии безводного карбоната калия и порошкообразной меди.
В 1948 г. Даубен подробно рассмотрел влияние заместителей на реакционную способность хлорбензойной кислоты и анилина. Электроотрицательные группы в орто- и пара-положениях к
атому хлора повышают электроположительность атома углерода, связанного с хлором; при этом активность хлора повышается. Реакционная способность атома азота зависит от основности амина; электроотрицательные заместители в ароматическом ядре амина, снижая его основность, затрудняют течение реакции.
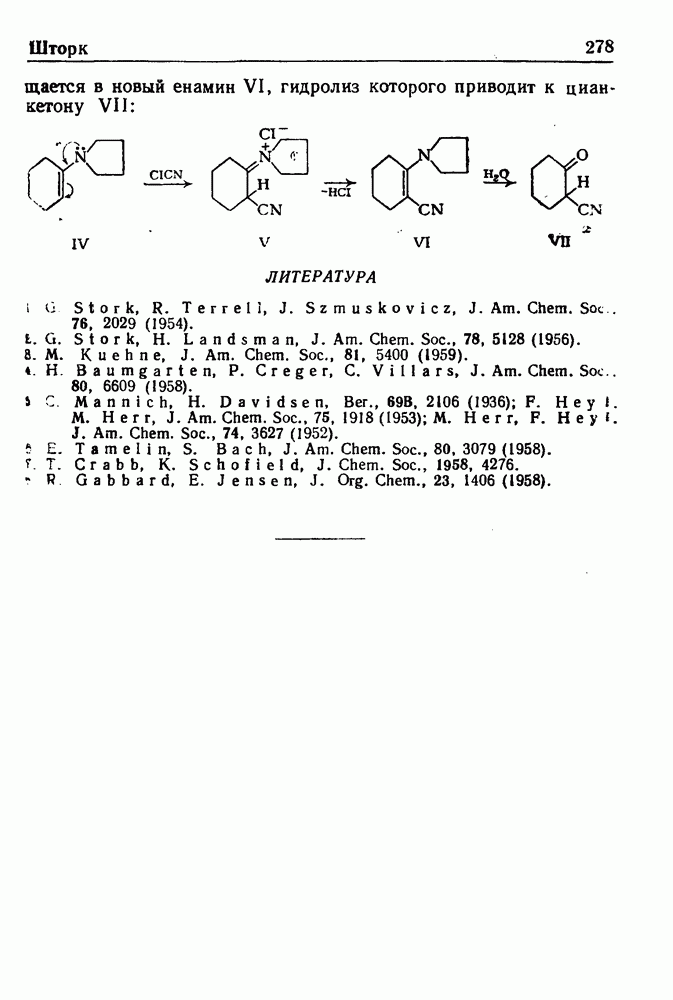
Механизм реакции Ульмана, вероятно, состоит в нуклеофильной атаке орто-углеродного атома связанного с хлором, атомом азота ароматического амина:

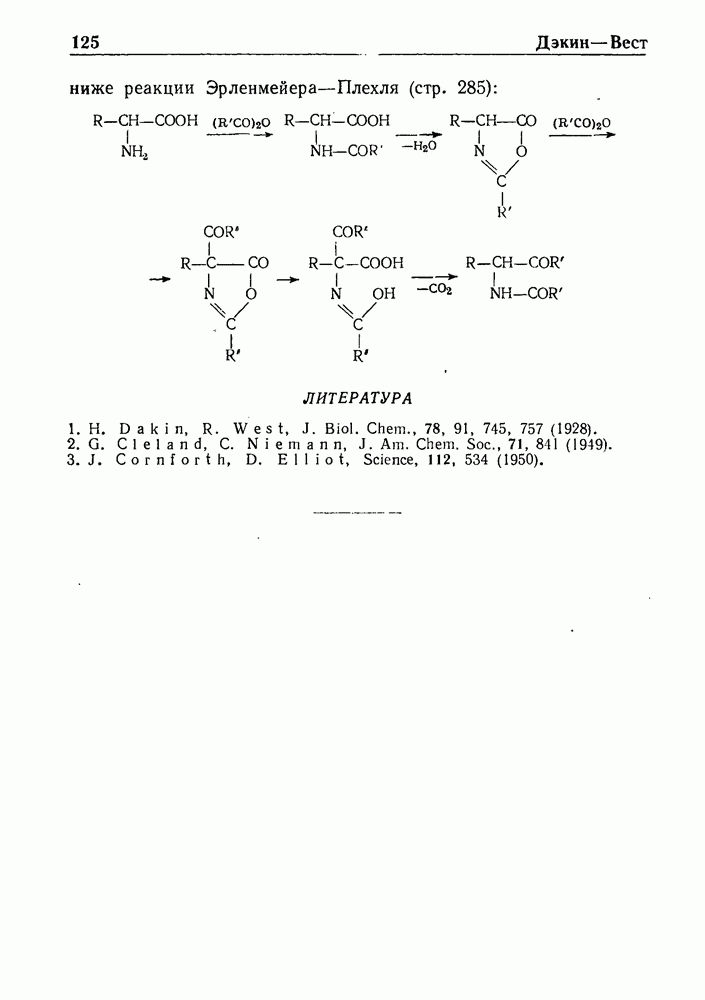
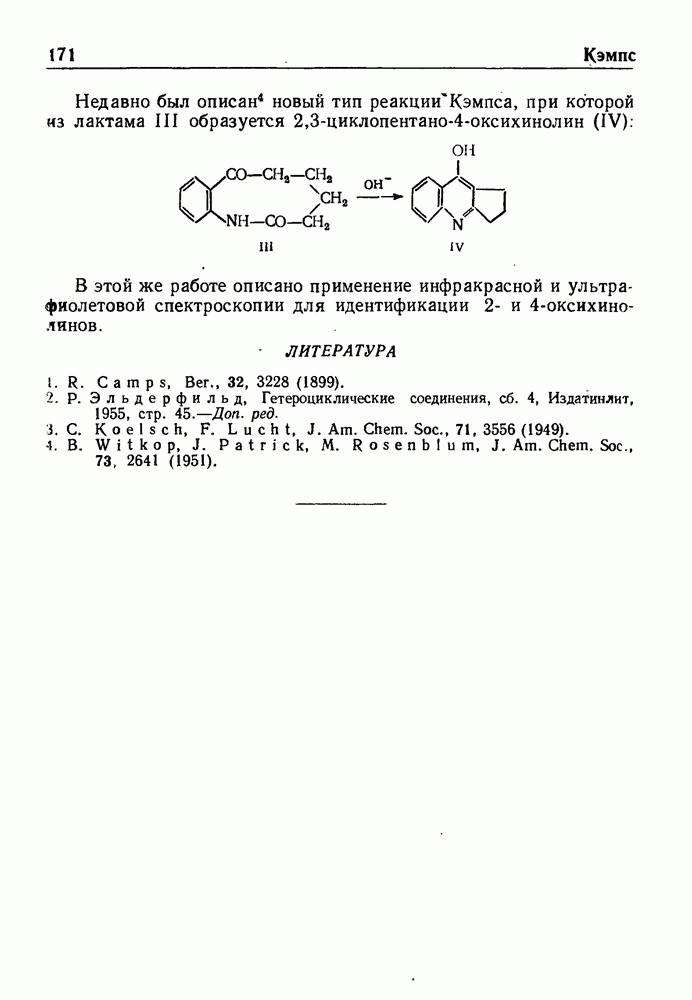
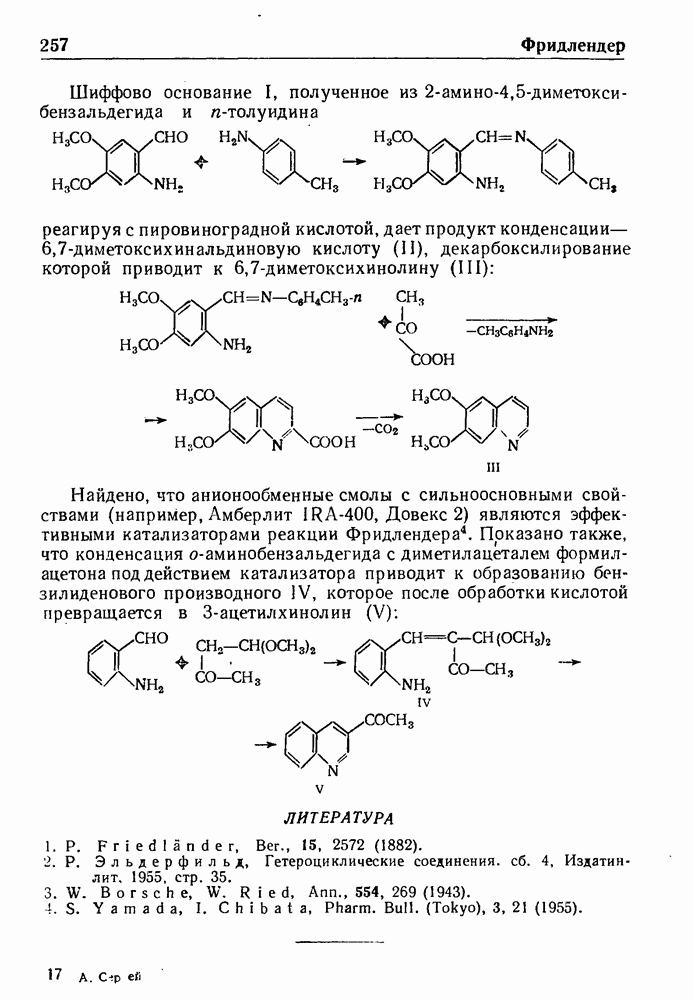
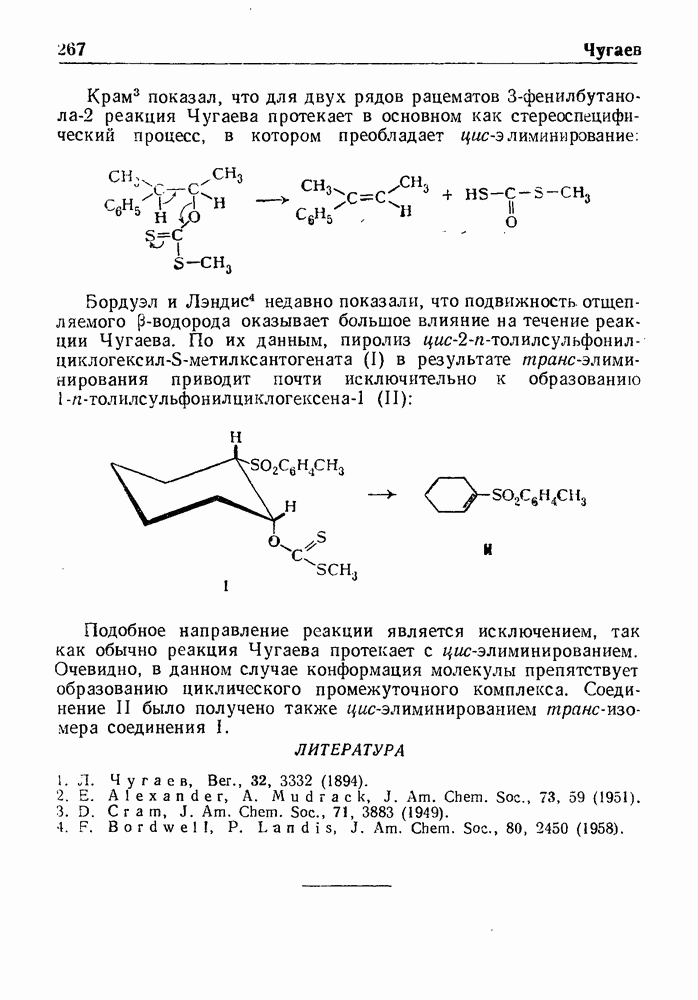
Другим методом синтеза замещенных N-антраниловых кислот служит перегруппировка Чэпмена у которая осуществляется путем нагревания и последующего гидролиза имидоэфиров. Например, если имидоэфир I, полученный при взаимодействии  бензойной кислоты (II) с натриевой солью метилового эфира 2-хлор-6-оксибензойной кислоты (III), нагревать в течение 70 мин. при 210° и затем продукт реакции омылить, то образуется
бензойной кислоты (II) с натриевой солью метилового эфира 2-хлор-6-оксибензойной кислоты (III), нагревать в течение 70 мин. при 210° и затем продукт реакции омылить, то образуется  кислота (IV):
кислота (IV):

Такая схема перегруппировки имидоэфира I аналогична схеме механизма конденсации Ульмана, приведенной выше. Электроположительные группы в орто- или пара-положении к атому азота в кольце А имидоэфира I и электроотрицательные заместители
в тех же положениях к атому кислорода в кольце Б облегчают перегруппировку.
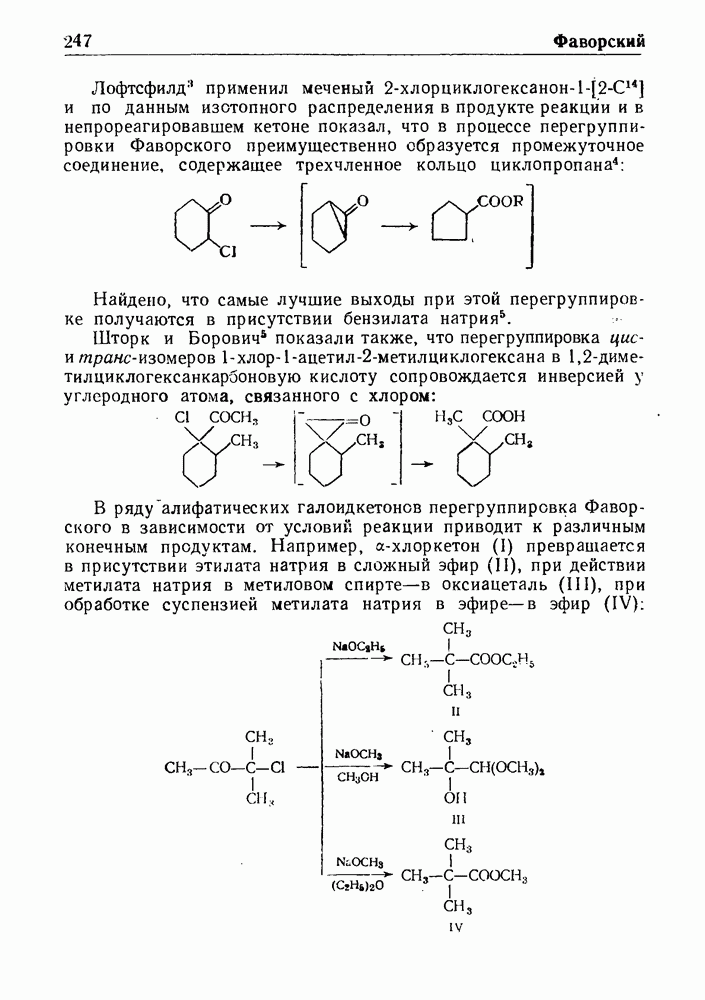
Механизм перегруппировки Чэпмена был изучен Вайбеогом и Роуляндом. Полученные ими данные подтверждают возможность образования промежуточного четырехчленного циклического комплекса (см. формулу I) при нуклеофильном замещении в ароматическом ядре.
ЛИТЕРАТУРА
(см. скан)
| << Предыдущий параграф | Следующий параграф >> |
- ОТ РЕДАКТОРА
- ПЕРЕГРУППИРОВКА АРБУЗОВА
- СИНТЕЗ АРНДТА—ЭЙСТЕРТА
- ОКИСЛЕНИЕ ПО БАЙЕРУ—ВИЛЛИГЕРУ
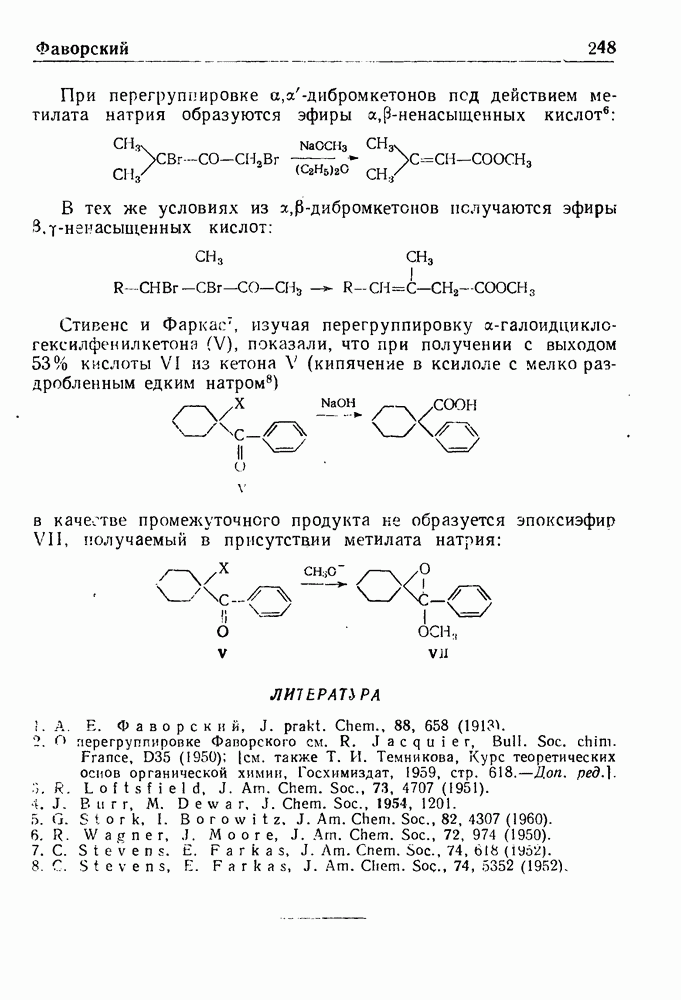
- РАСЩЕПЛЕНИЕ ПО БАРБЬЕ—ВИЛАНДУ
- РЕАКЦИЯ БАРТА
- ПЕРЕГРУППИРОВКА БЕКМАНА
- ВОССТАНОВЛЕНИЕ ПО БЕРНУ
- ВОССТАНОВЛЕНИЕ ПО БЕШАНУ
- РЕАКЦИЯ БИШЛЕРА—НАПИРАЛЬСКОГО
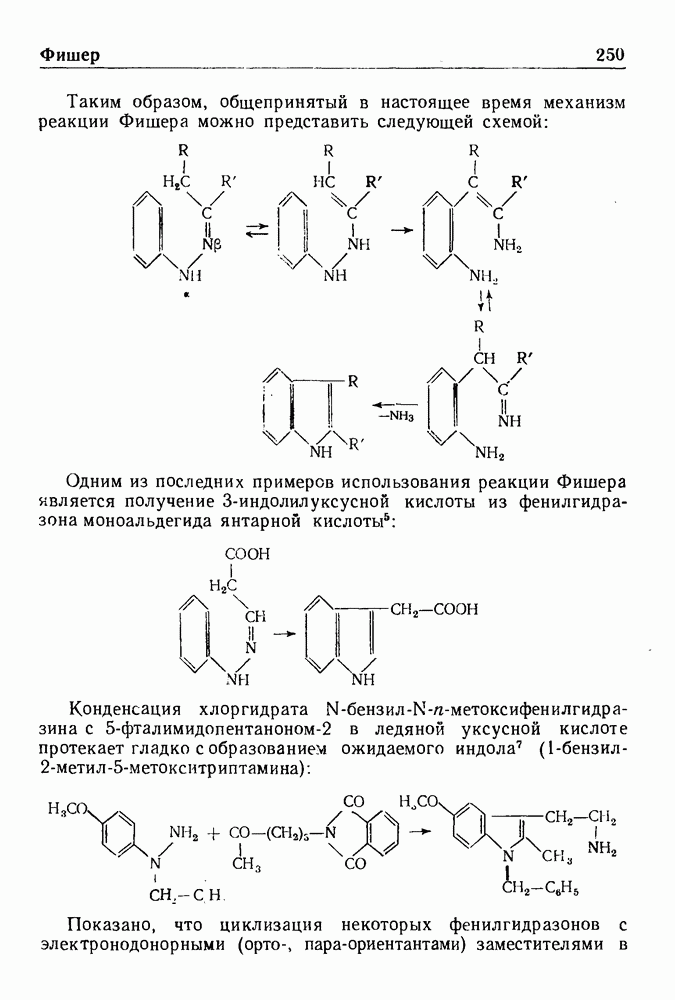
- ХЛОРМЕТИЛИРОВАНИЕ ПО БЛАНУ
- РЕАКЦИЯ БРАУНА
- РАСЩЕПЛЕНИЕ АМИНОВ ПО БРАУНУ
- ВОССТАНОВЛЕНИЕ ПО БУВО—БЛАНУ
- СИНТЕЗ АЛЬДЕГИДОВ ПО БУВО
- РЕАКЦИЯ БУХЕРЕРА
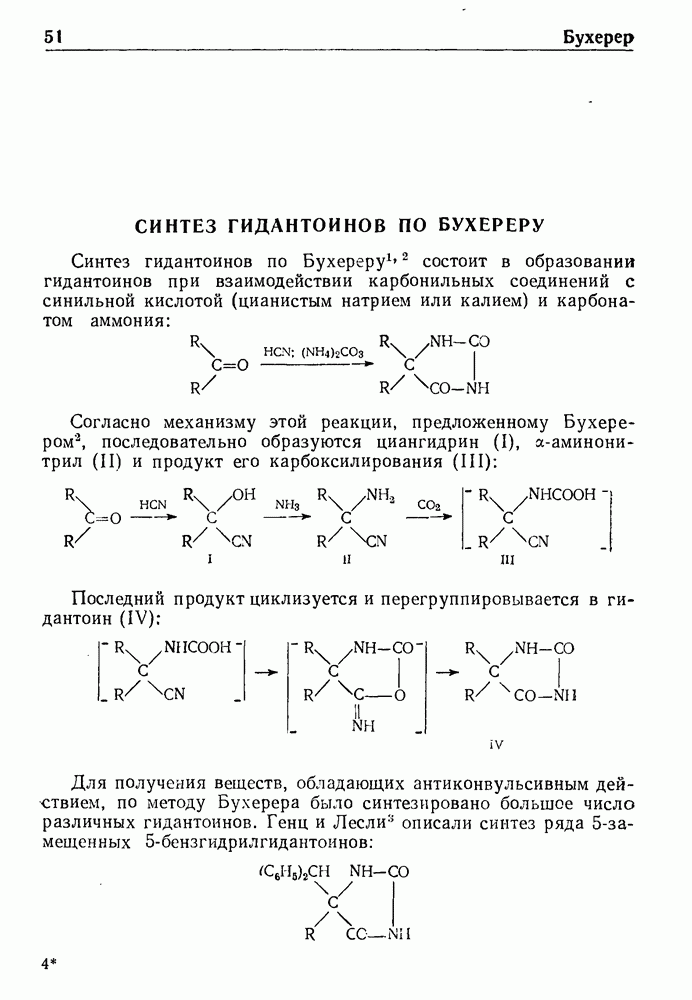
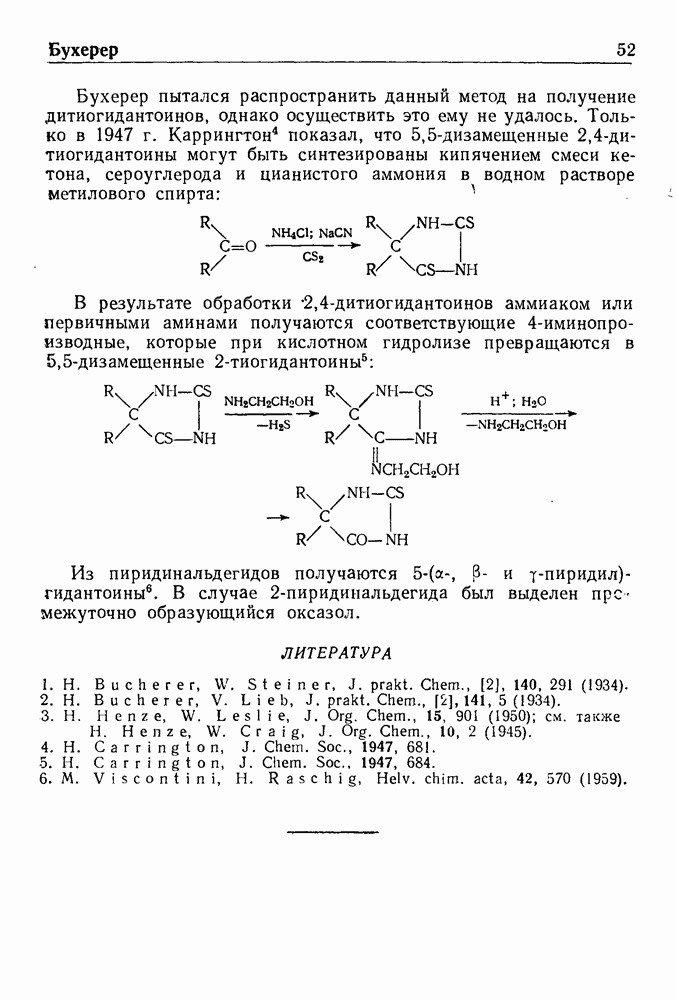
- СИНТЕЗ ГИДАНТОИНОВ ПО БУХЕРЕРУ
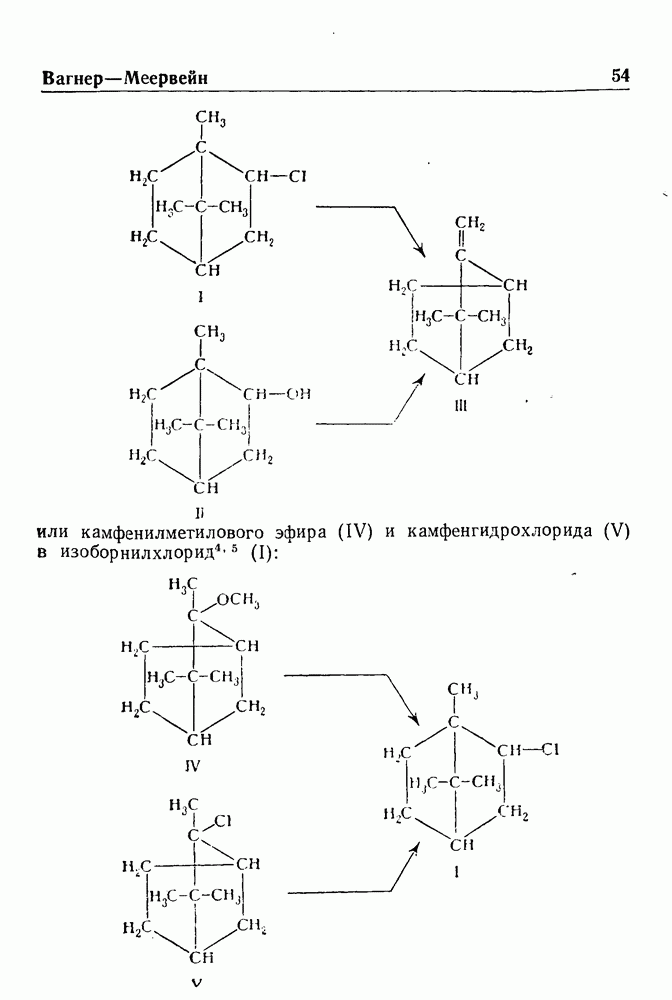
- ПЕРЕГРУППИРОВКА ВАГНЕРА—МЕЕРВЕЙНА
- РЕАКЦИЯ ВАЛЛАХА
- РЕАКЦИЯ ВИЛЬГЕРОДТА
- СИНТЕЗ ВИЛЬЯМСОНА
- РЕАКЦИЯ ВИТТИГА
- РЕАКЦИЯ ВОЛЯ-ЦИГЛЕРА
- РЕАКЦИЯ ВЮРЦА
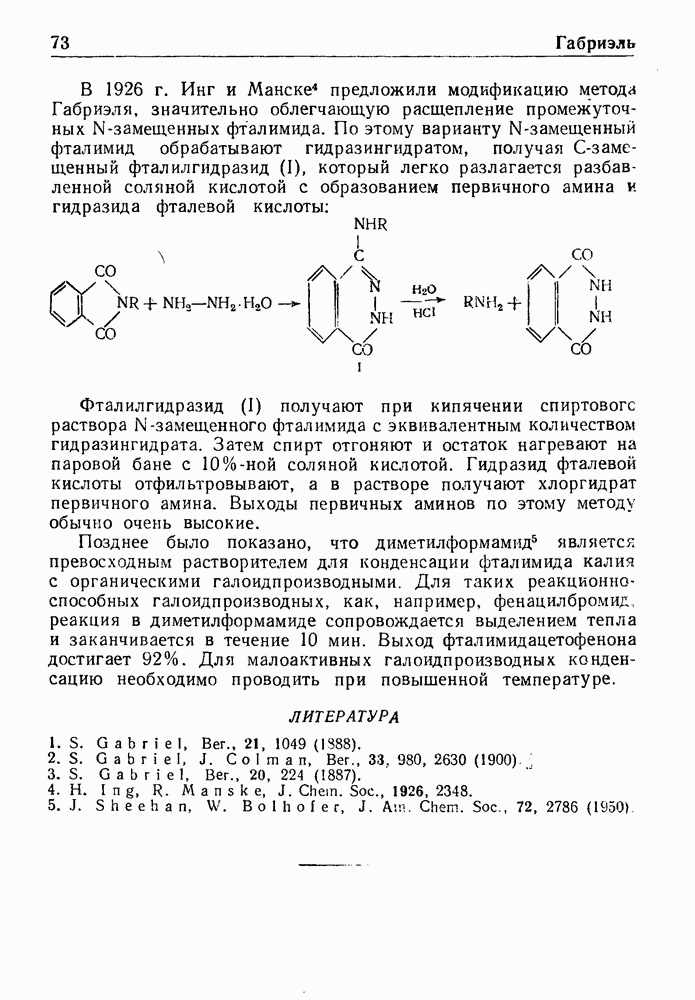
- СИНТЕЗ ГАБРИЭЛЯ
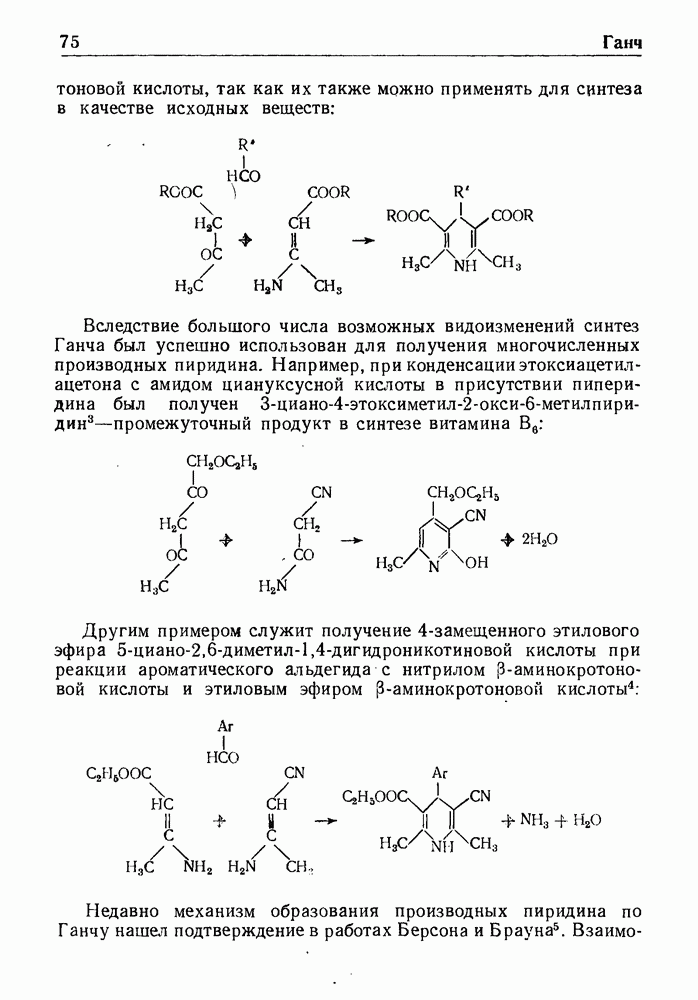
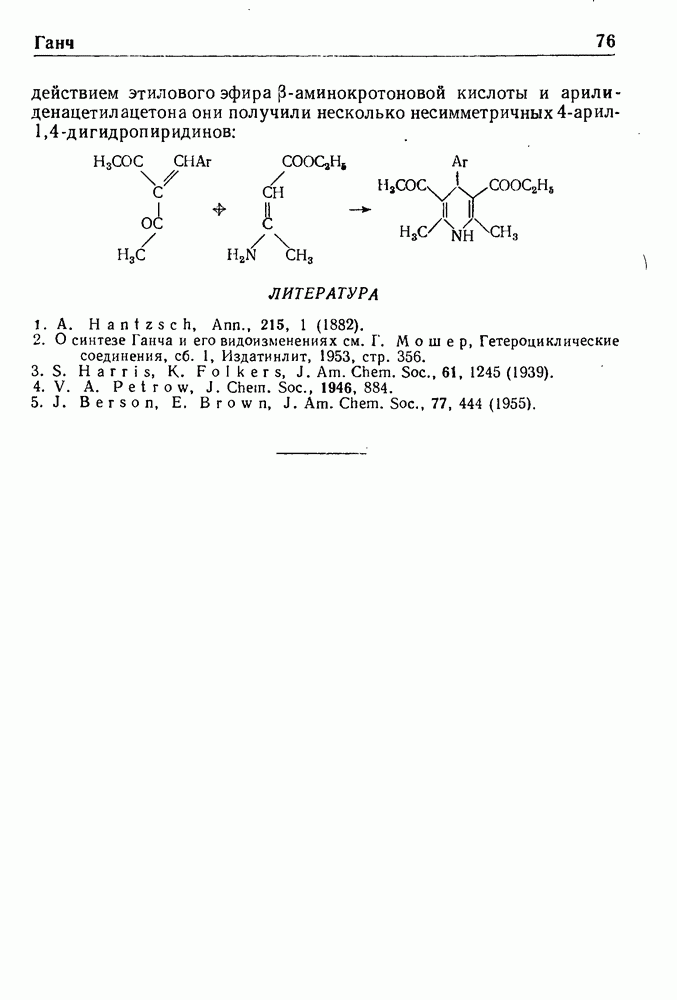
- СИНТЕЗ ГАНЧА
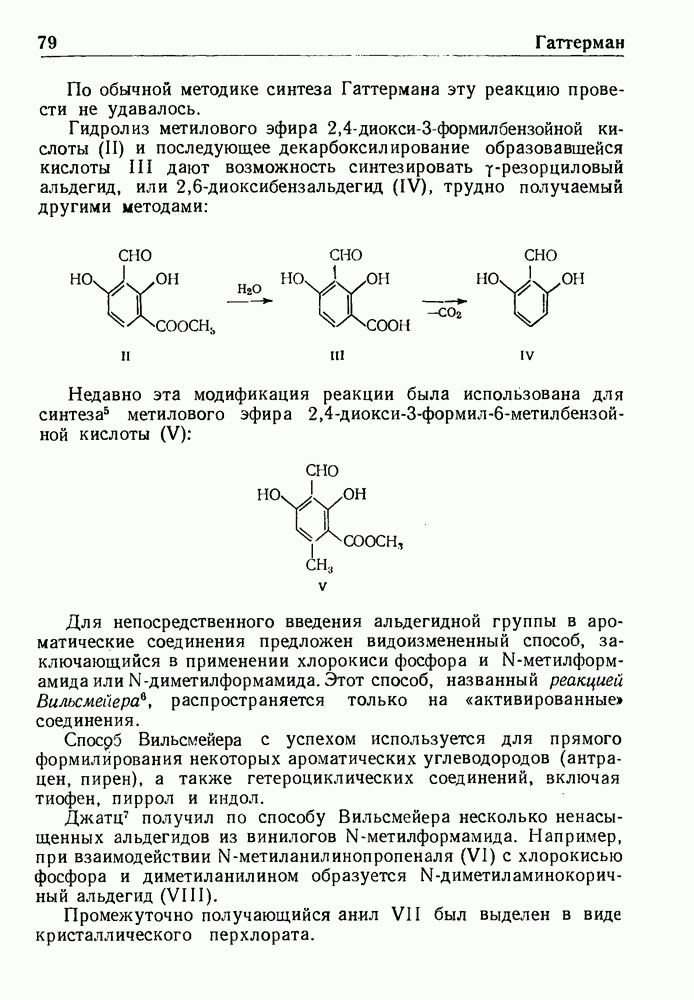
- РЕАКЦИЯ ГАТТЕРМАНА
- СИНТЕЗ АЛЬДЕГИДОВ ПО ГАТТЕРМАНУ
- РЕАКЦИЯ ГАТТЕРМАНА—КОХА
- РЕАКЦИЯ ГЕЛЛЯ—ФОЛЬГАРДА—ЗЕЛИНСКОГО
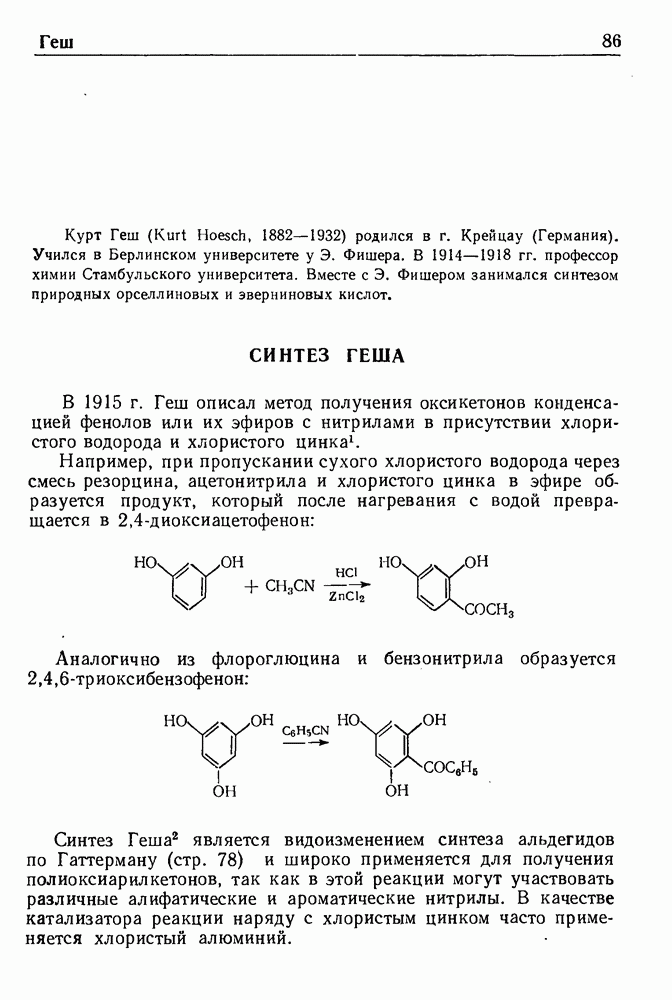
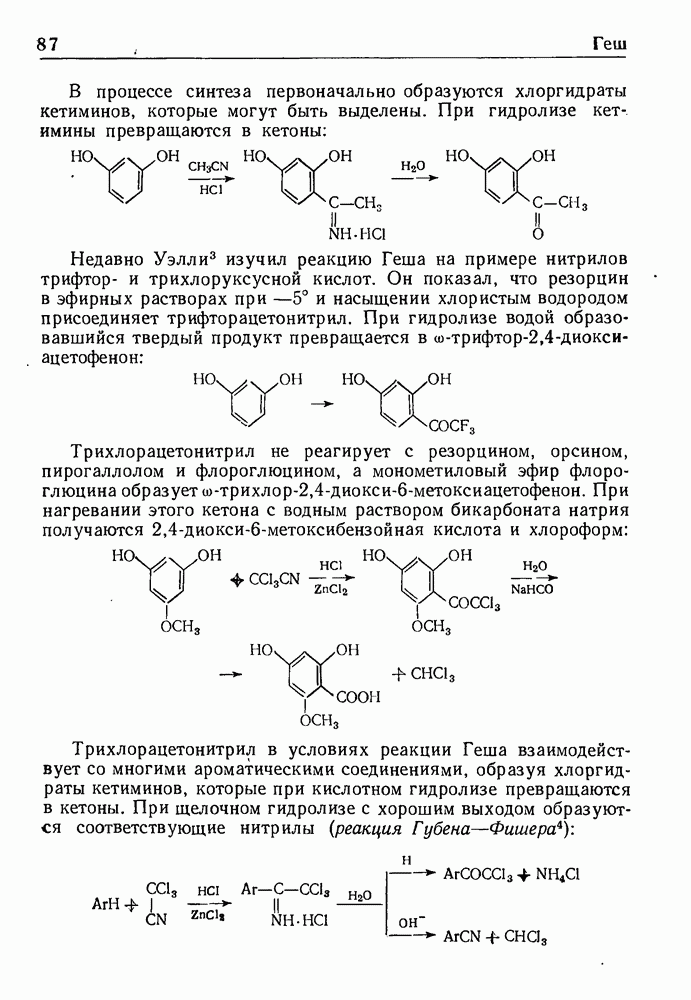
- СИНТЕЗ ГЕША
- РЕАКЦИЯ ГОМБЕРГА—БАХМАНА—ХЕЯ
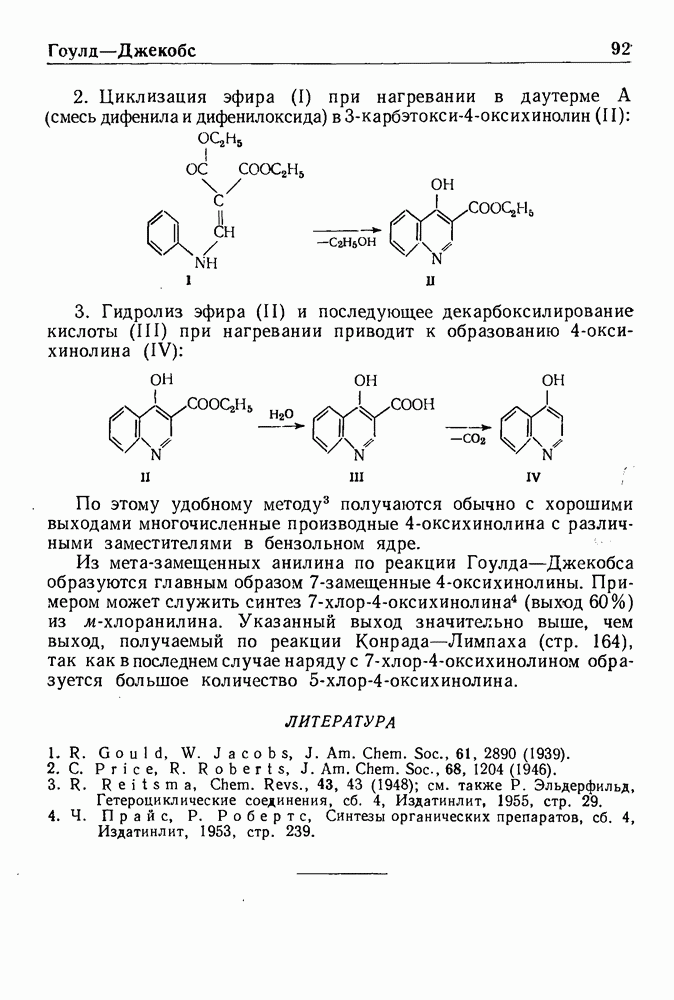
- РЕАКЦИЯ ГОУЛДА—ДЖЕКОБСА
- ПЕРЕГРУППИРОВКА ГОФМАНА
- РАСЩЕПЛЕНИЕ ПО ГОФМАНУ
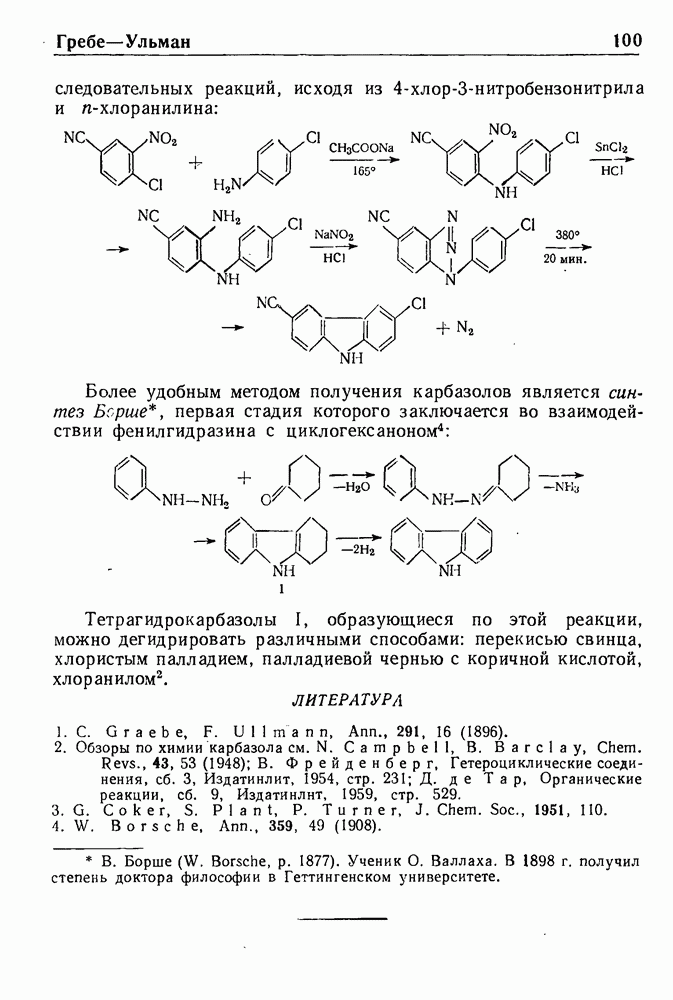
- СИНТЕЗ ГРЕБЕ—УЛЬМАНА
- РЕАКЦИЯ ГРИНЬЯРА
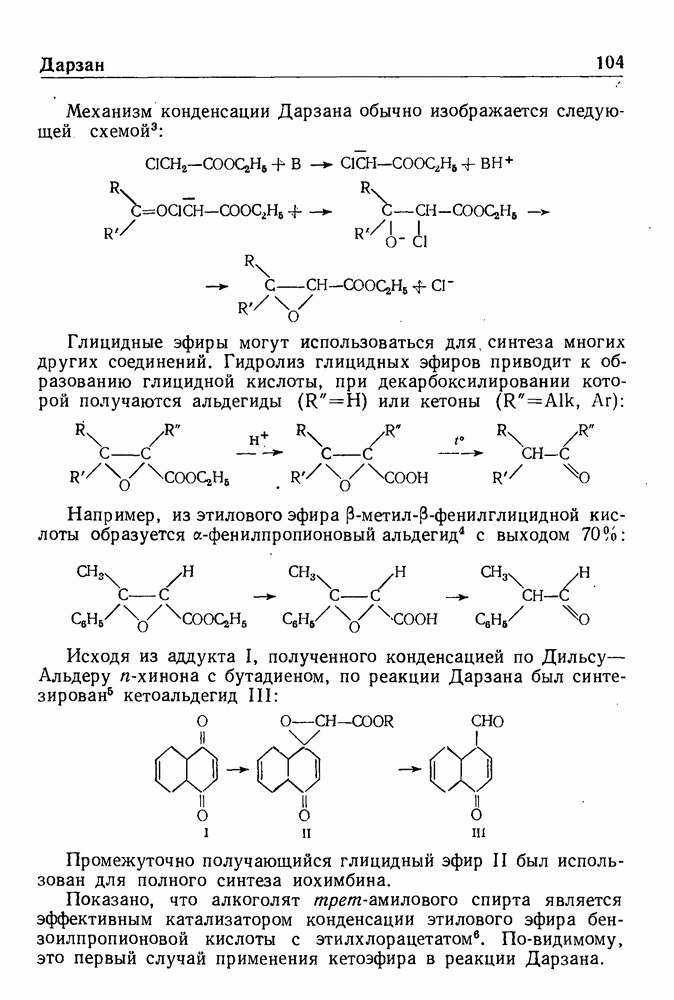
- СИНТЕЗ ГЛИЦИДНЫХ ЭФИРОВ ПО ДАРЗАНУ
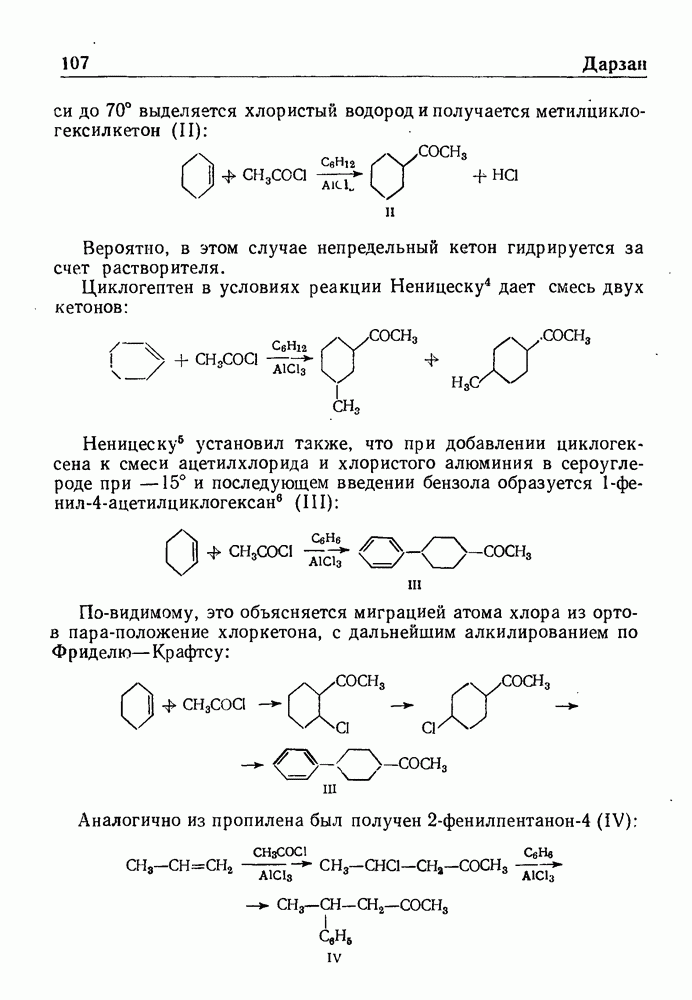
- СИНТЕЗ НЕПРЕДЕЛЬНЫХ КЕТОНОВ ПО ДАРЗАНУ
- РЕАКЦИЯ ДАФФА
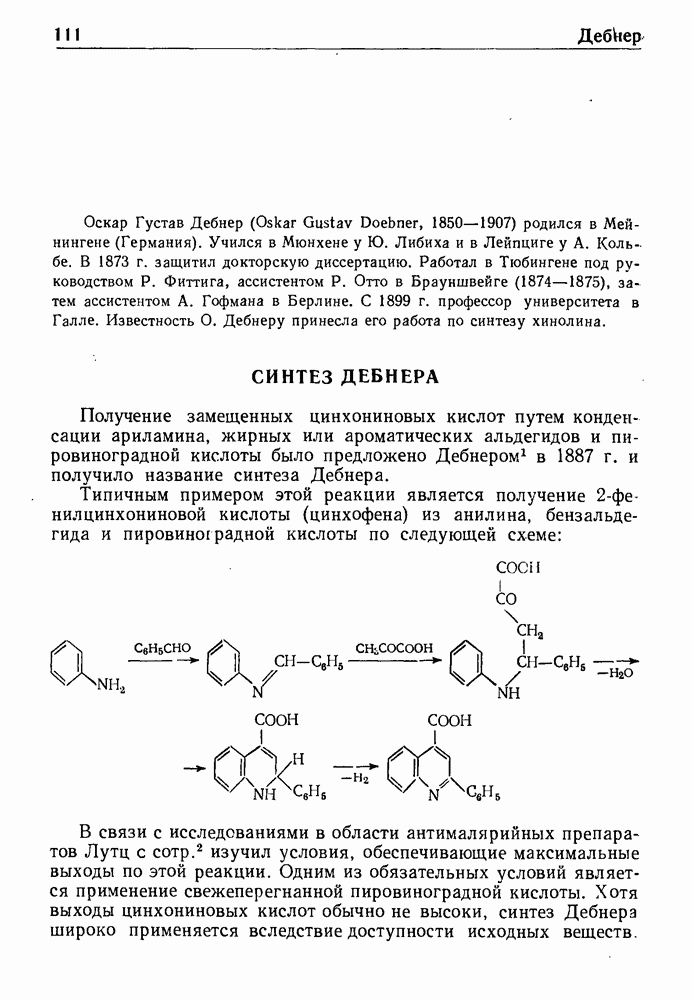
- СИНТЕЗ ДЕБНЕРА
- СИНТЕЗ ДЕБНЕРА—МИЛЛЕРА
- РЕАКЦИЯ ДЕЛЕПИНА
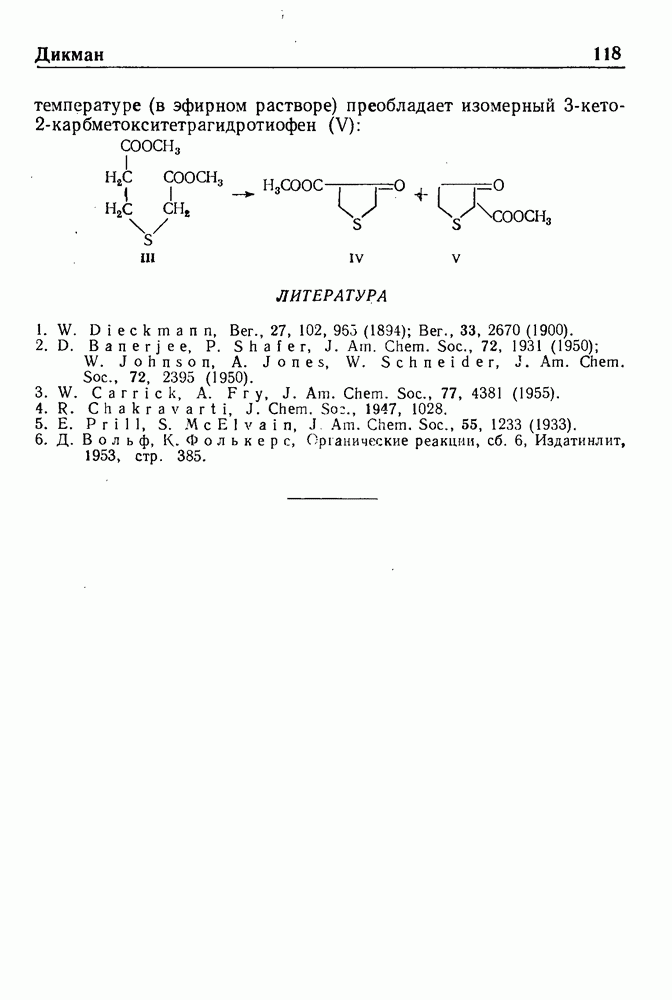
- РЕАКЦИЯ ДИКМАНА
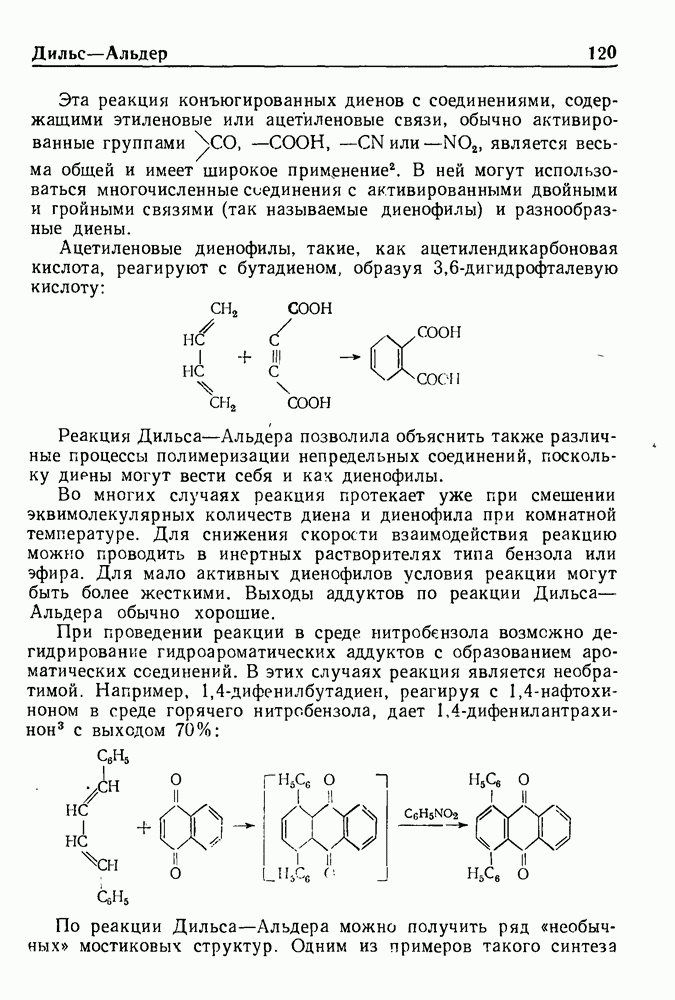
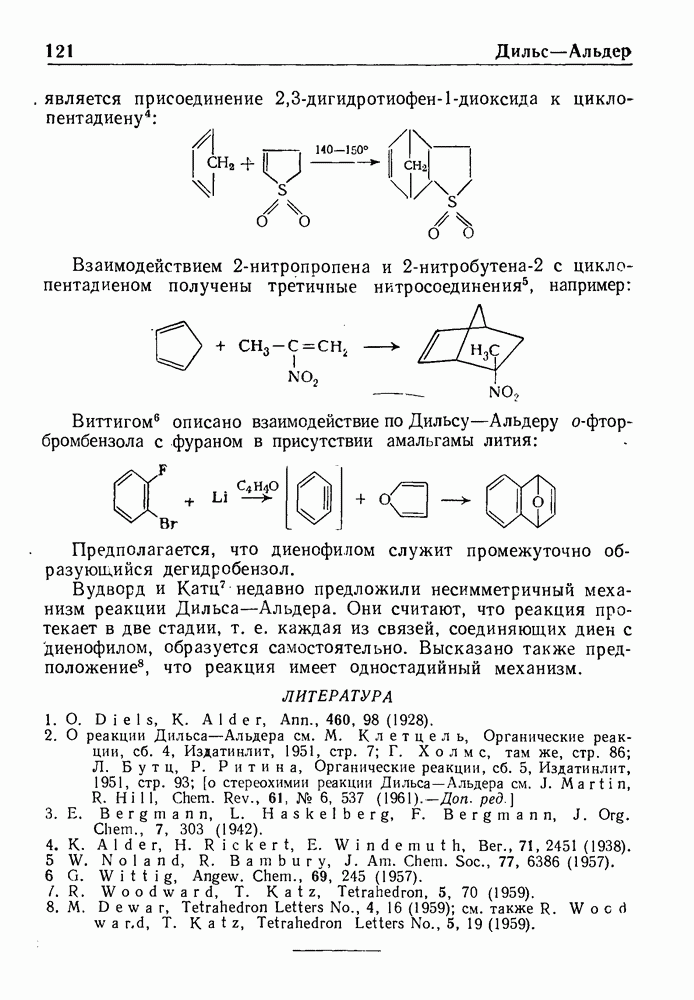
- РЕАКЦИЯ ДИЛЬСА-АЛЬДЕРА
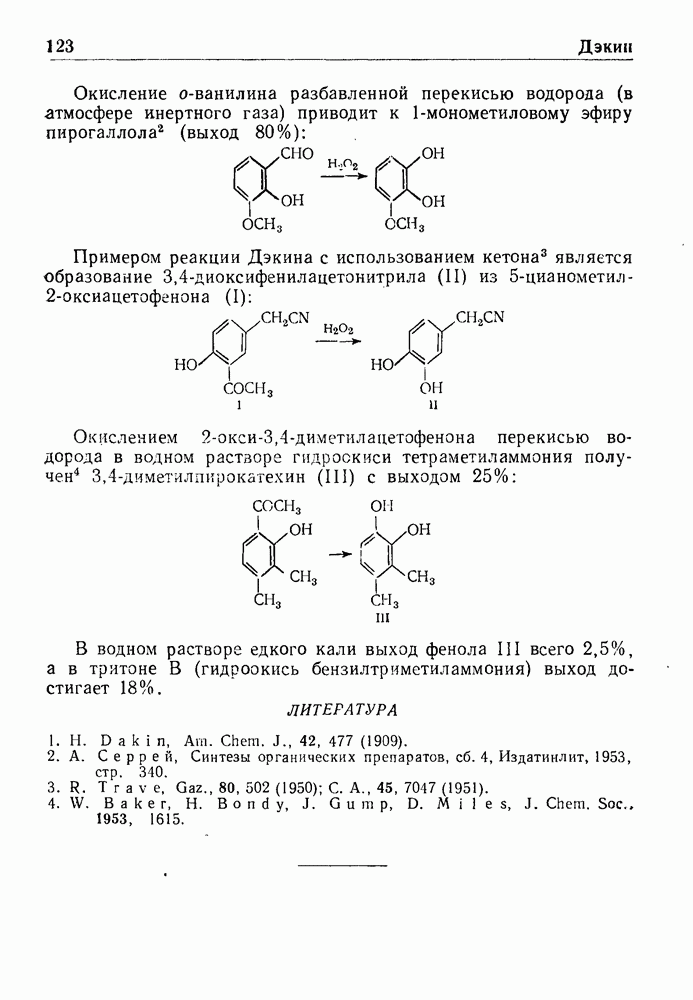
- РЕАКЦИЯ ДЭКИНА
- РЕАКЦИЯ ДЭКИНА—ВЕСТА
- РЕАКЦИЯ ЗАНДМЕЙЕРА
- РЕАКЦИЯ ИВАНОВА
- РЕАКЦИЯ ИОЦИЧА
- РЕАКЦИЯ КАННИЦЦАРО
- РЕАКЦИЯ КИЖНЕРА
- КОНДЕНСАЦИЯ КЛАЙЗЕНА
- ПЕРЕГРУППИРОВКА КЛАЙЗЕНА
- КОНДЕНСАЦИЯ КЛАЙЗЕНА—ШМИДТА
- ВОССТАНОВЛЕНИЕ ПО КЛЕММЕНСЕНУ
- РЕАКЦИЯ КНЕВЕНАГЕЛЯ
- СИНТЕЗ КНОРРА
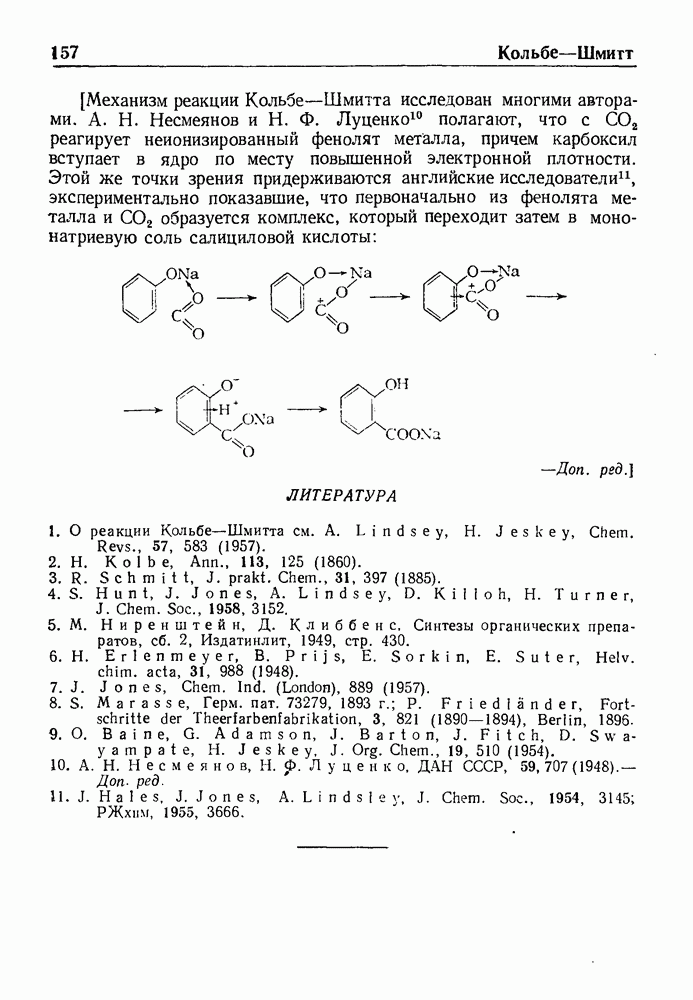
- РЕАКЦИЯ КОЛЬБЕ—ШМИТТА
- ЭЛЕКТРОХИМИЧЕСКАЯ РЕАКЦИЯ КОЛЬБЕ
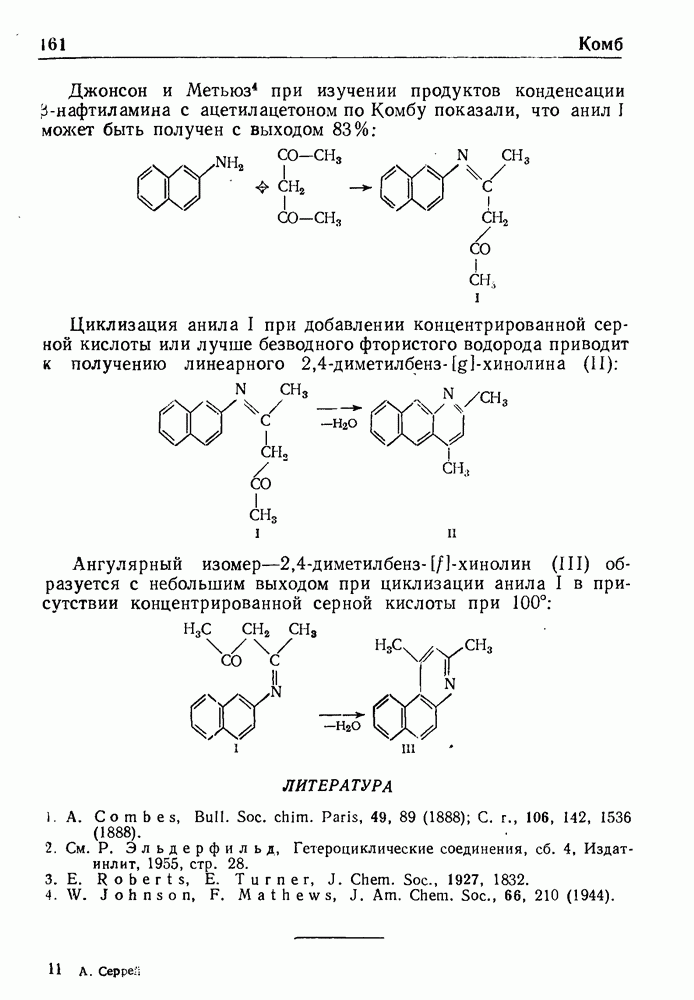
- СИНТЕЗ ХИНОЛИНА ПО КОМБУ
- РЕАКЦИЯ КОНОВАЛОВА
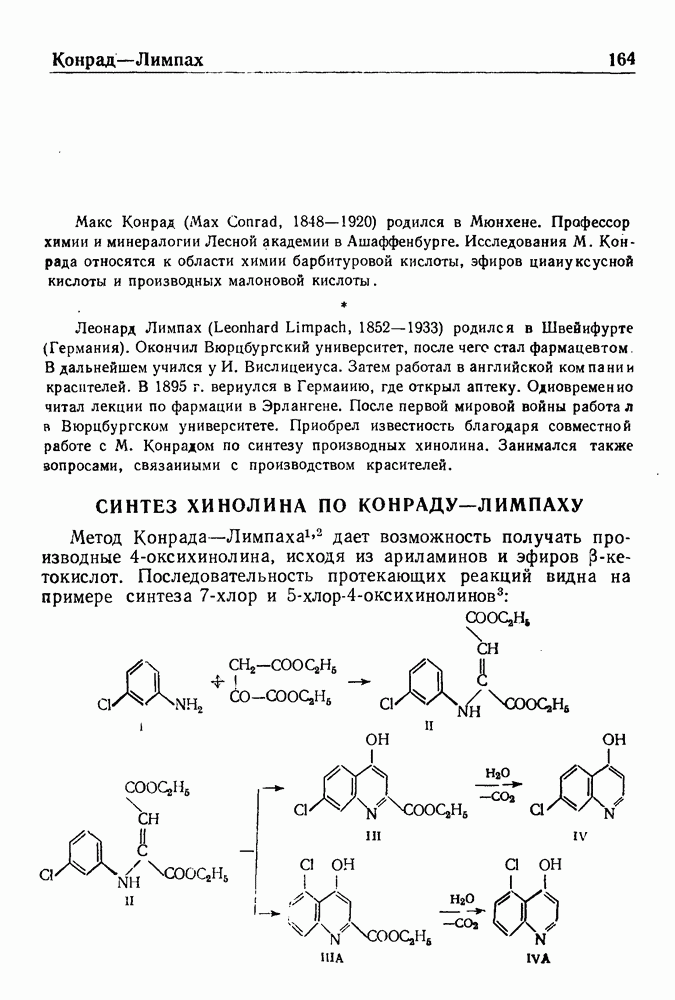
- СИНТЕЗ ХИНОЛИНА ПО КОНРАДУ—ЛИМПАХУ
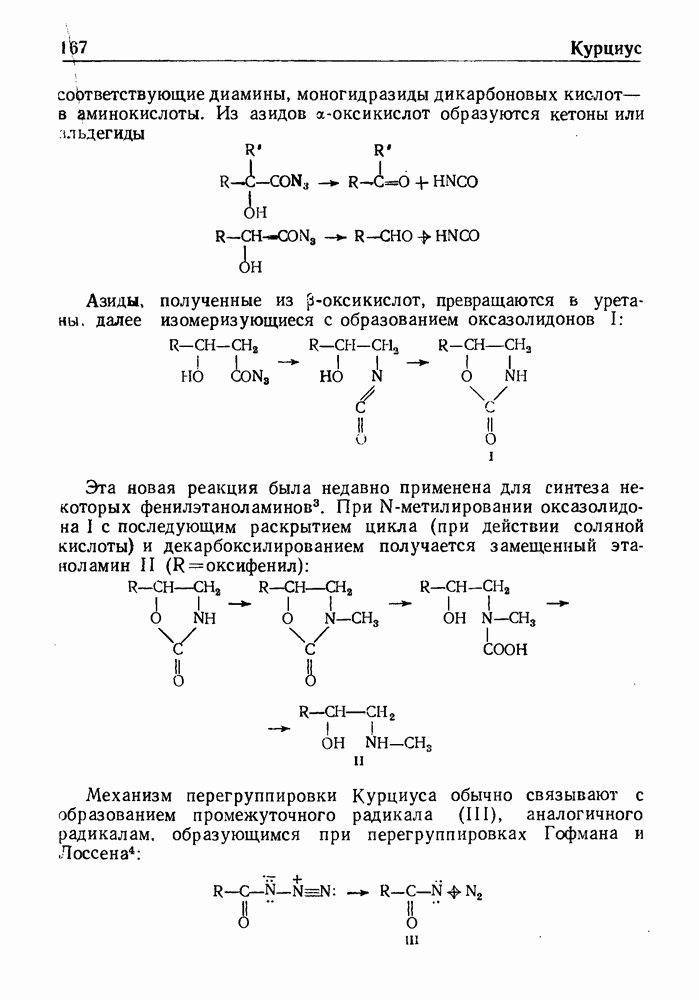
- РЕАКЦИЯ КУРЦИУСА
- РЕАКЦИЯ КУЧЕРОВА
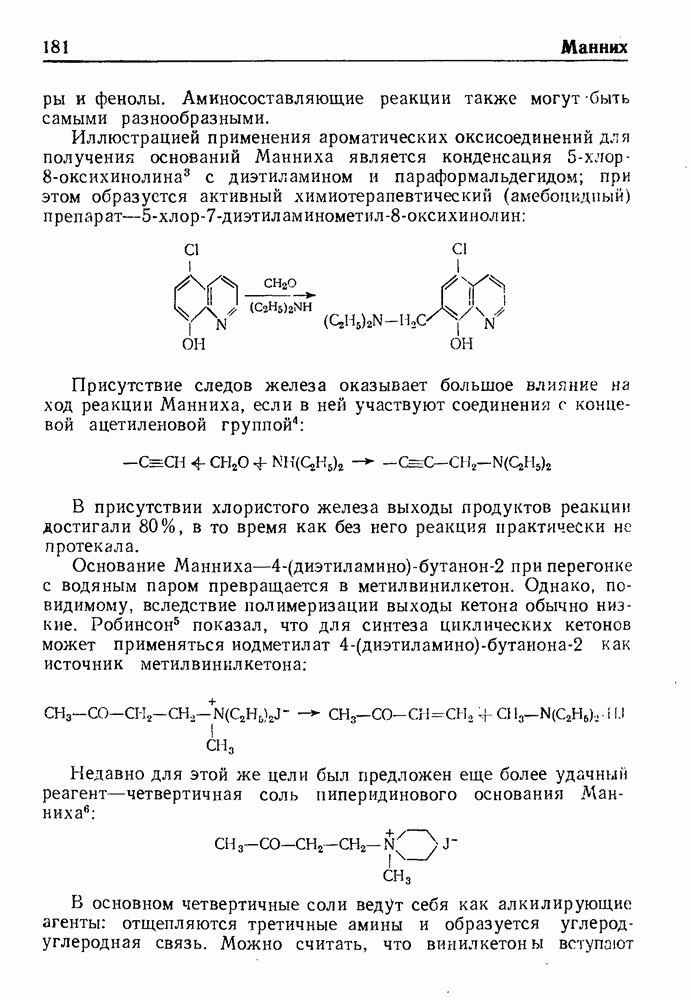
- РЕАКЦИЯ КЭМПСА
- РЕАКЦИЯ ЛЕЙКАРТА
- РЕАКЦИЯ ЛОССЕНА
- ВОССТАНОВЛЕНИЕ ПО МАК ФАДИЕНУ—СТИВЕНСУ
- РЕАКЦИЯ МАННИХА
- КОНДЕНСАЦИЯ МЕЕРВЕЙНА
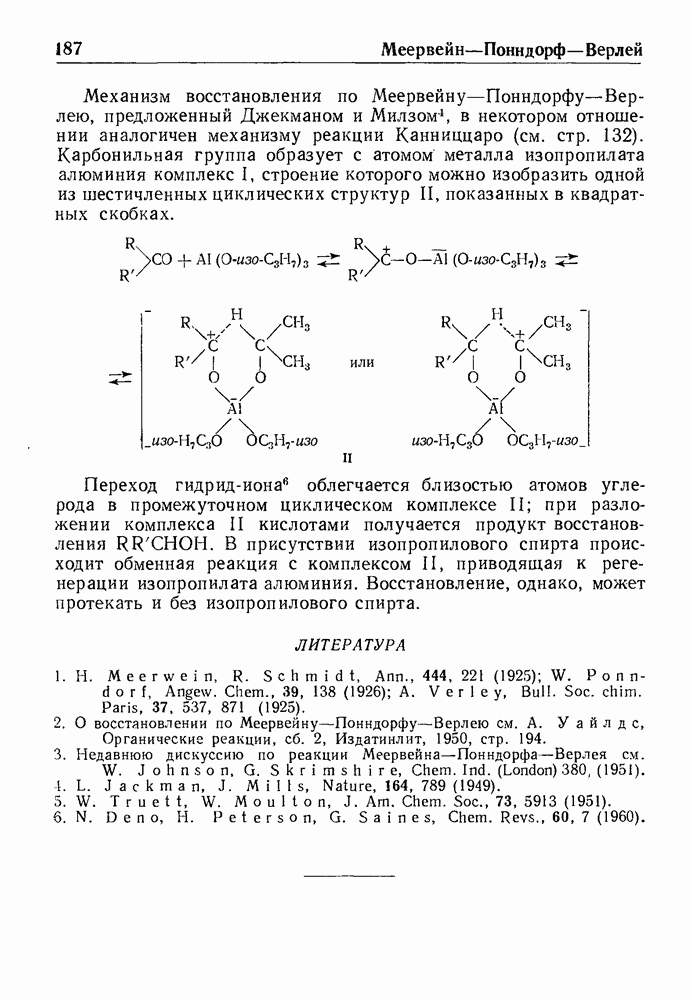
- ВОССТАНОВЛЕНИЕ ПО МЕЕРВЕЙНУ-ПОННДОРФУ-ВЕРЛЕЮ
- РЕАКЦИЯ МИХАЭЛЯ
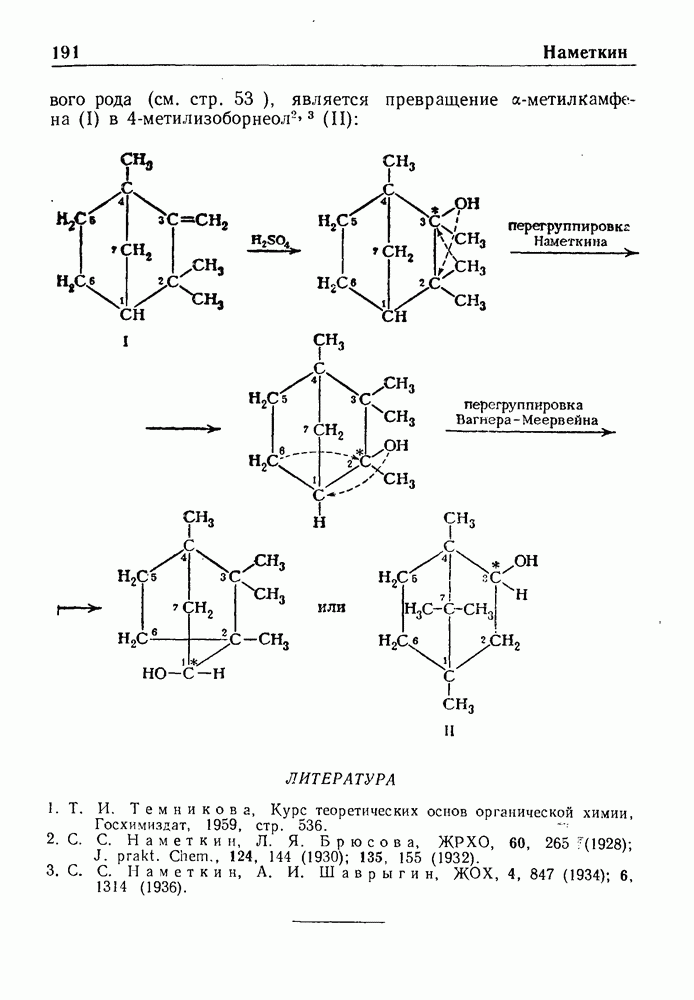
- ПЕРЕГРУППИРОВКА НАМЕТКИНА
- РЕАКЦИЯ НЕСМЕЯНОВА
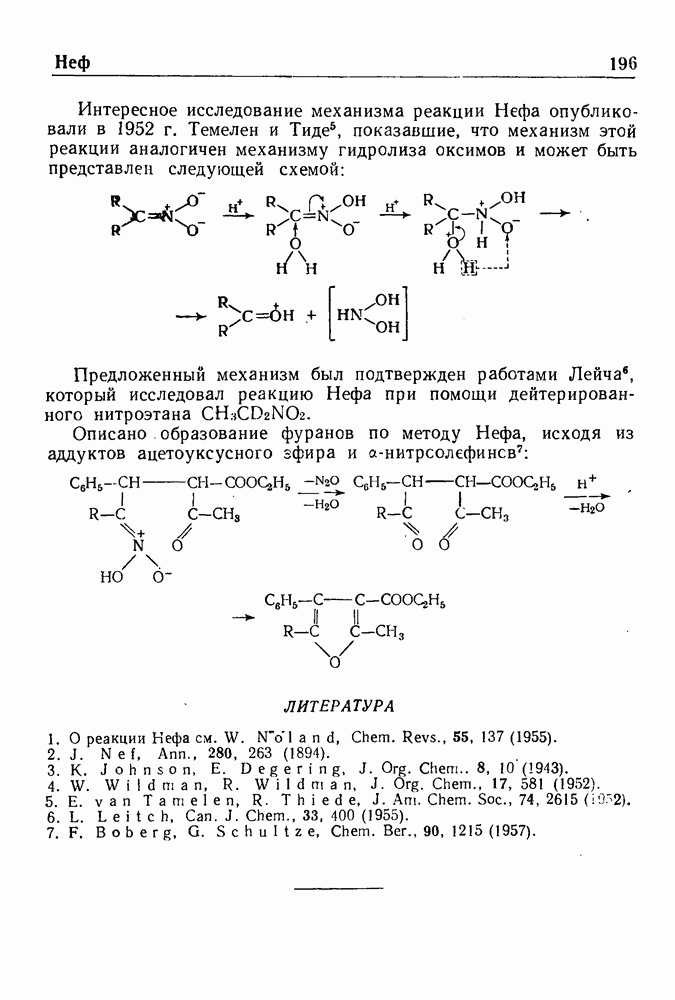
- РЕАКЦИЯ НЕФА
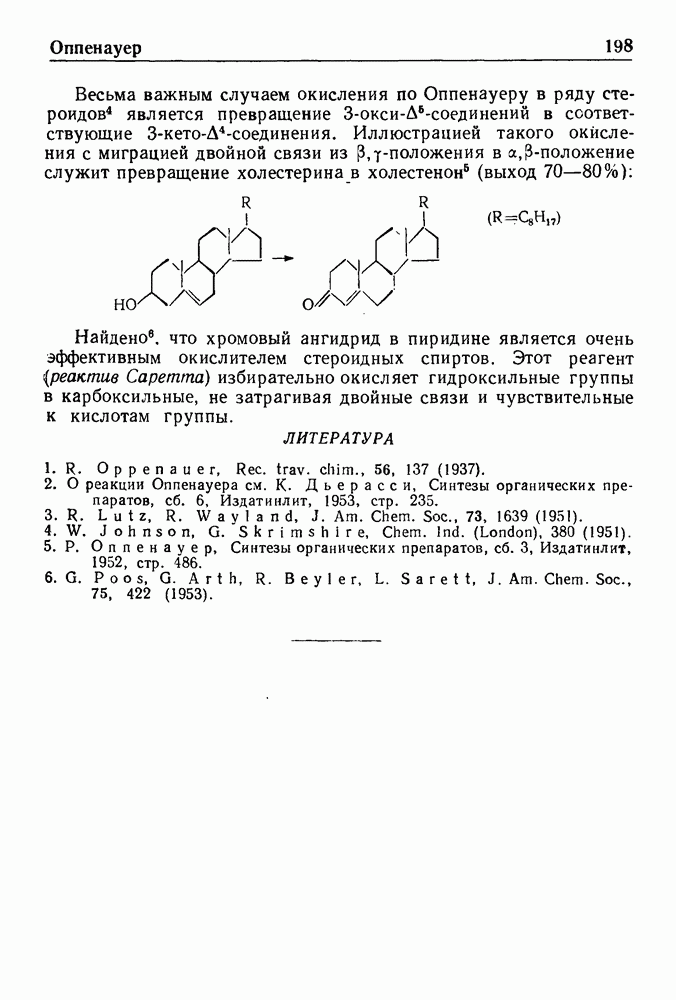
- ОКИСЛЕНИЕ ПО ОППЕНАУЕРУ
- РЕАКЦИЯ ПАССЕРИНИ
- РЕАКЦИЯ ПЕРКИНА
- КОНДЕНСАЦИЯ ПЕХМАНА
- РЕАКЦИЯ ПИКТЭ—ШПЕНГЛЕРА
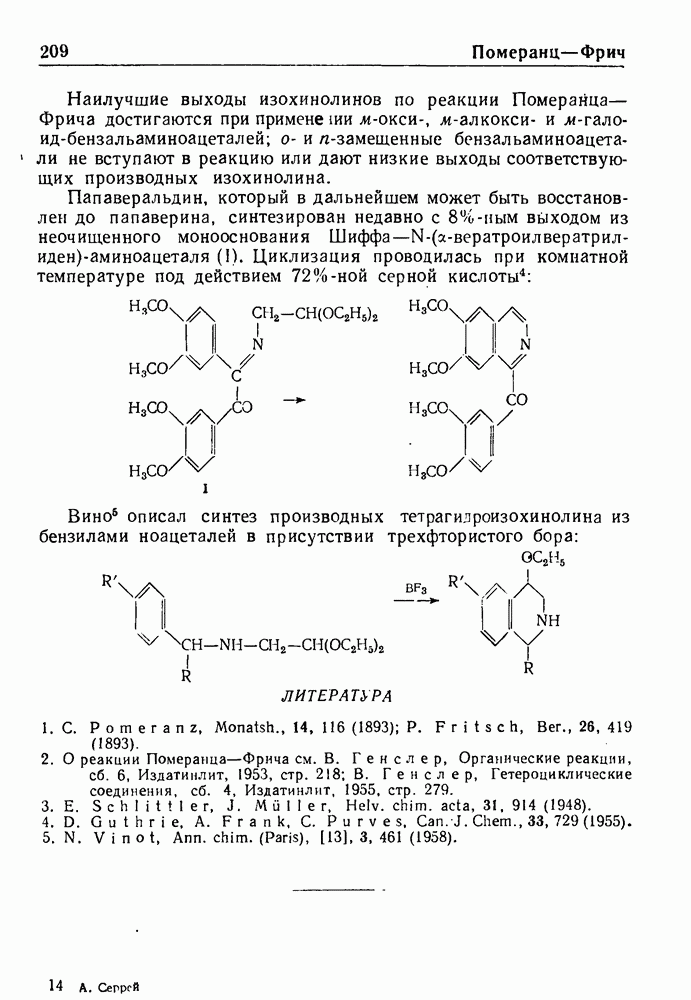
- РЕАКЦИЯ ПОМЕРАНЦА—ФРИЧА
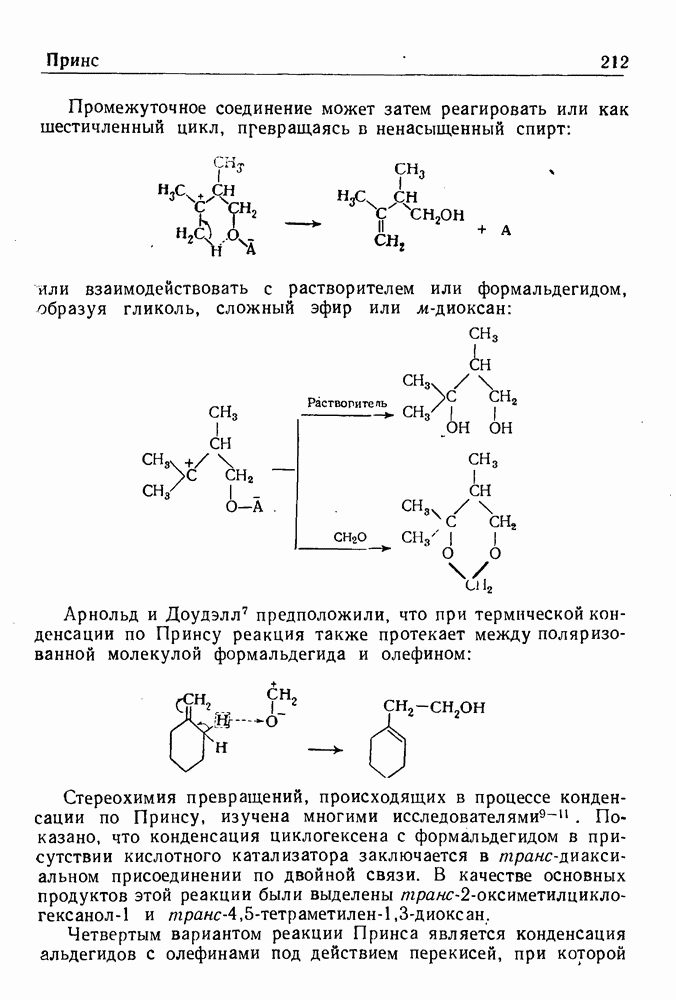
- РЕАКЦИЯ ПРИНСА
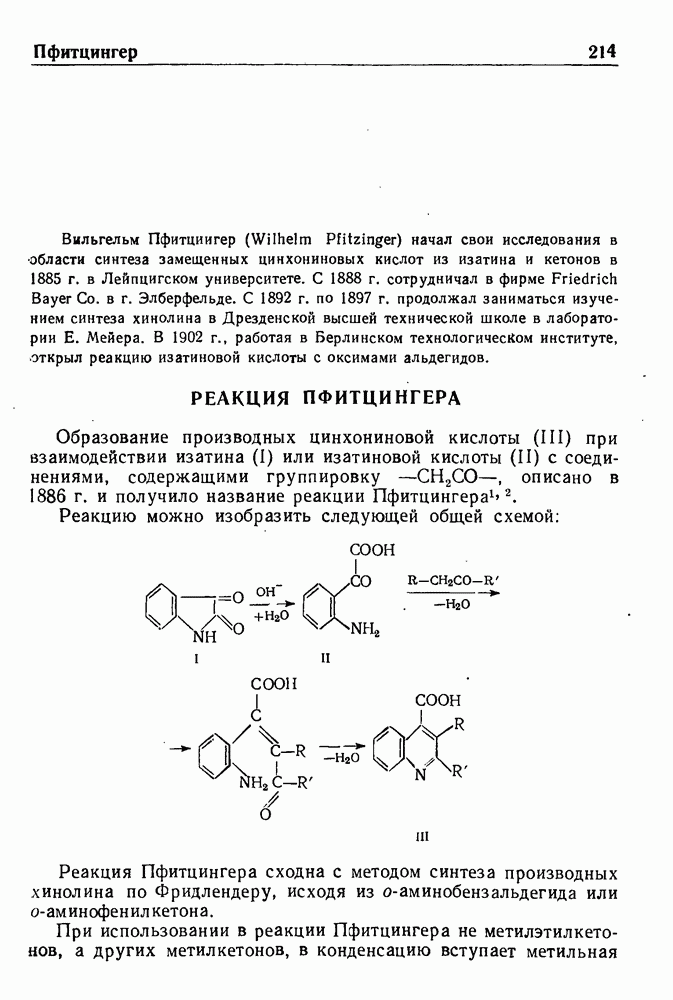
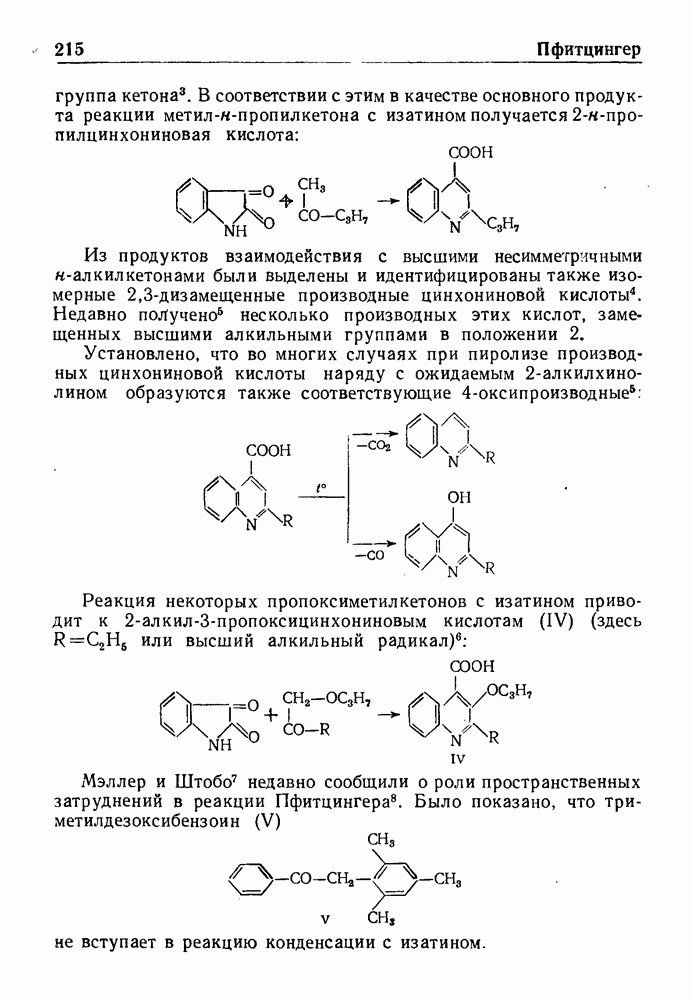
- РЕАКЦИЯ ПФИТЦИНГЕРА
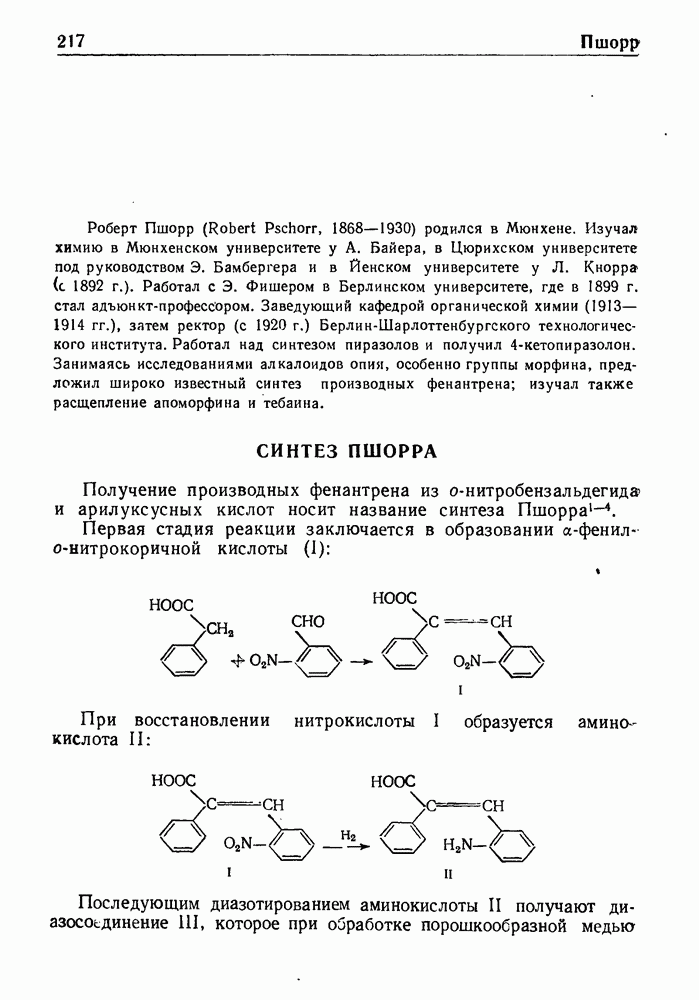
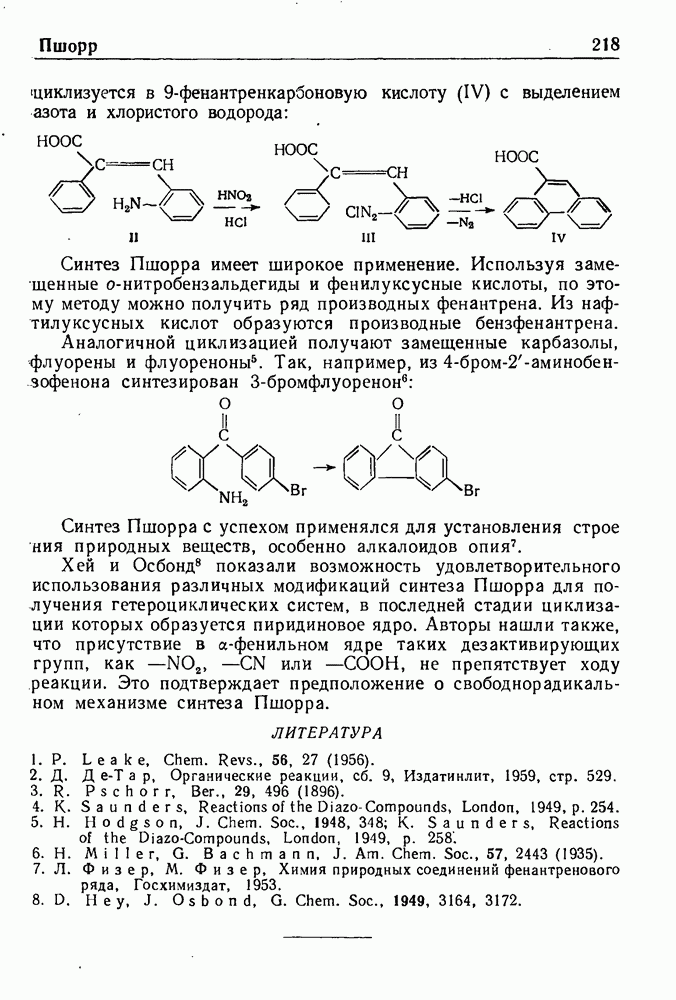
- СИНТЕЗ ПШОРРА
- РЕАКЦИЯ РЕЙМЕРА—ТИМАНА
- РЕАКЦИЯ РЕЙСЕРТА
- РЕАКЦИЯ РЕФОРМАТСКОГО
- РЕАКЦИЯ РОДИОНОВА
- ВОССТАНОВЛЕНИЕ ПО РОЗЕНМУНДУ
- РЕАКЦИЯ СКРАУПА
- РЕАКЦИЯ СОММЛЕ
- РЕАКЦИЯ СТЕФЕНА
- ПЕРЕГРУППИРОВКА СТИВЕНСА
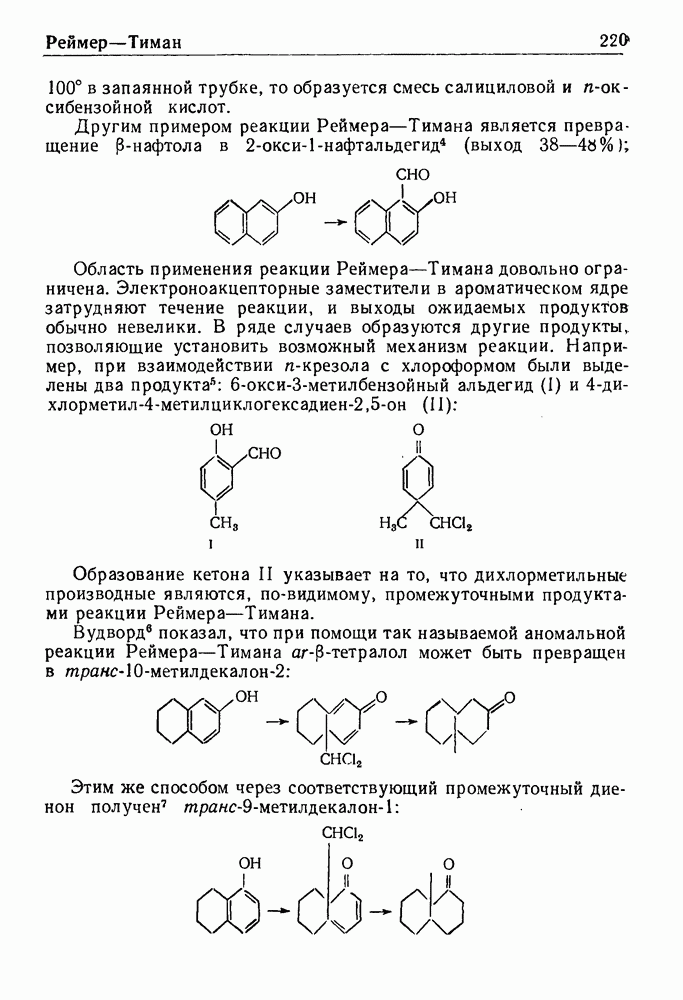
- РЕАКЦИЯ УЛЬМАНА
- КОНДЕНСАЦИЯ УЛЬМАНА
- ПЕРЕГРУППИРОВКА ФАВОРСКОГО
- СИНТЕЗ ИНДОЛА ПО ФИШЕРУ
- РЕАКЦИЯ ФРИДЕЛЯ—КРАФТСА
- СИНТЕЗ ФРИДЛЕНДЕРА
- РЕАКЦИЯ ФРИСА
- РЕАКЦИЯ ХУНСДИККЕРА
- РЕАКЦИЯ ЧИЧИБАБИНА
- РЕАКЦИЯ ЧУГАЕВА
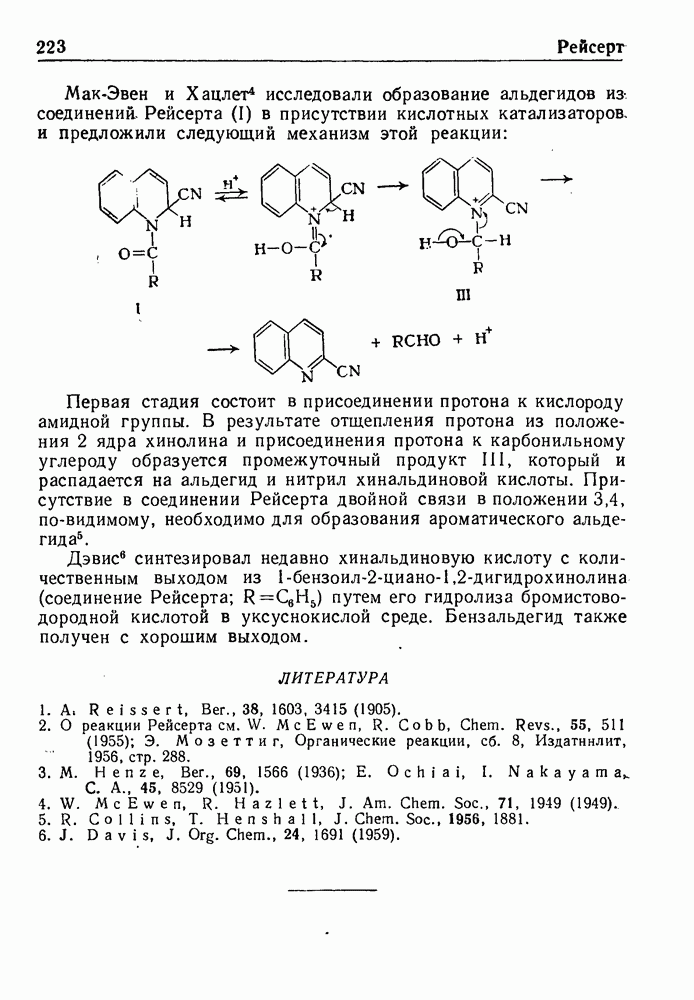
- РЕАКЦИЯ ШИМАНА
- РЕАКЦИИ ШМИДТА
- КОНДЕНСАЦИЯ ШТОББЕ
- РЕАКЦИЯ ШТОРКА
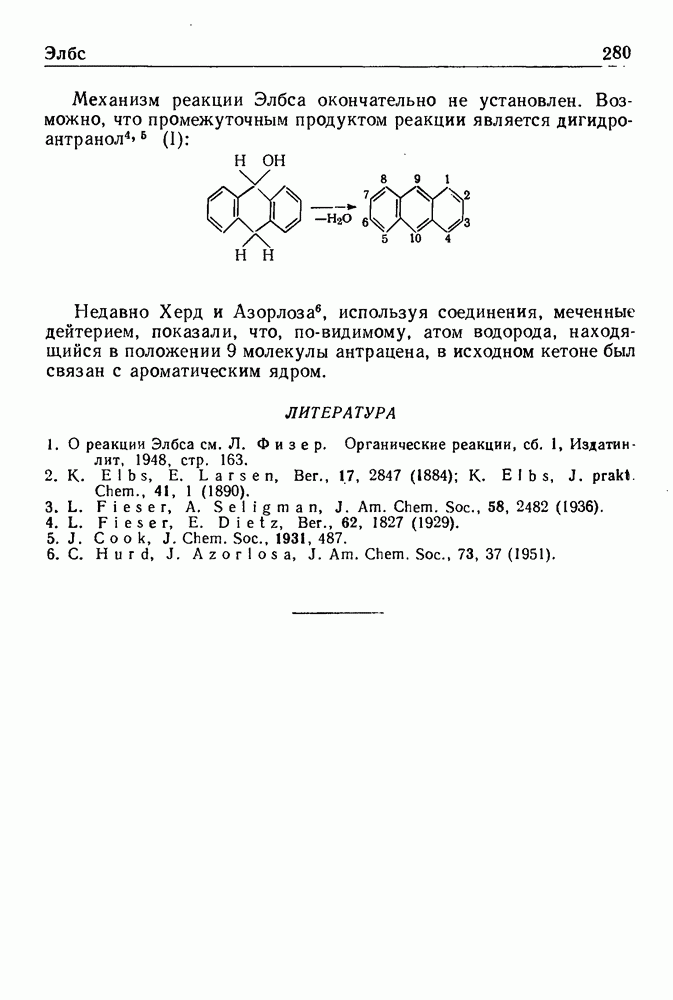
- РЕАКЦИЯ ЭЛБСА
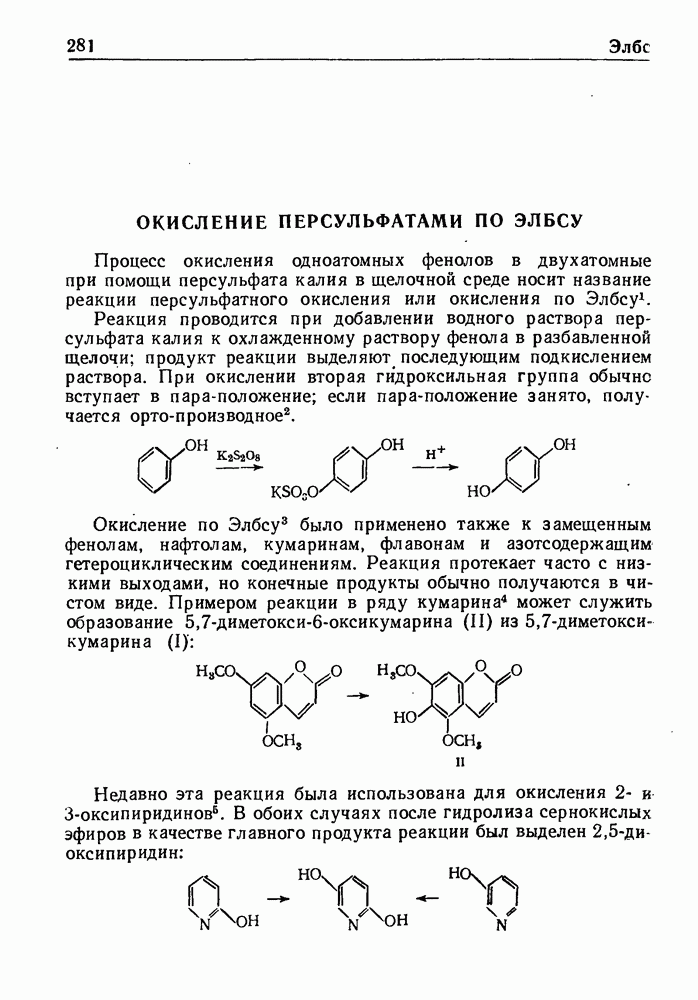
- ОКИСЛЕНИЕ ПЕРСУЛЬФАТАМИ ПО ЭЛБСУ
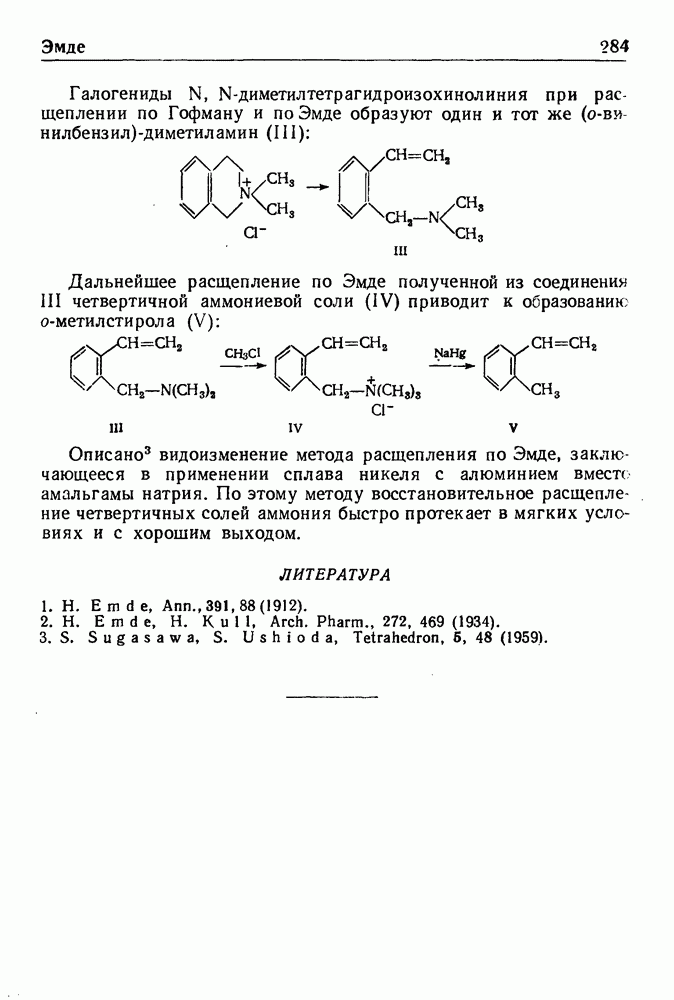
- РАСЩЕПЛЕНИЕ ПО ЭМДЕ
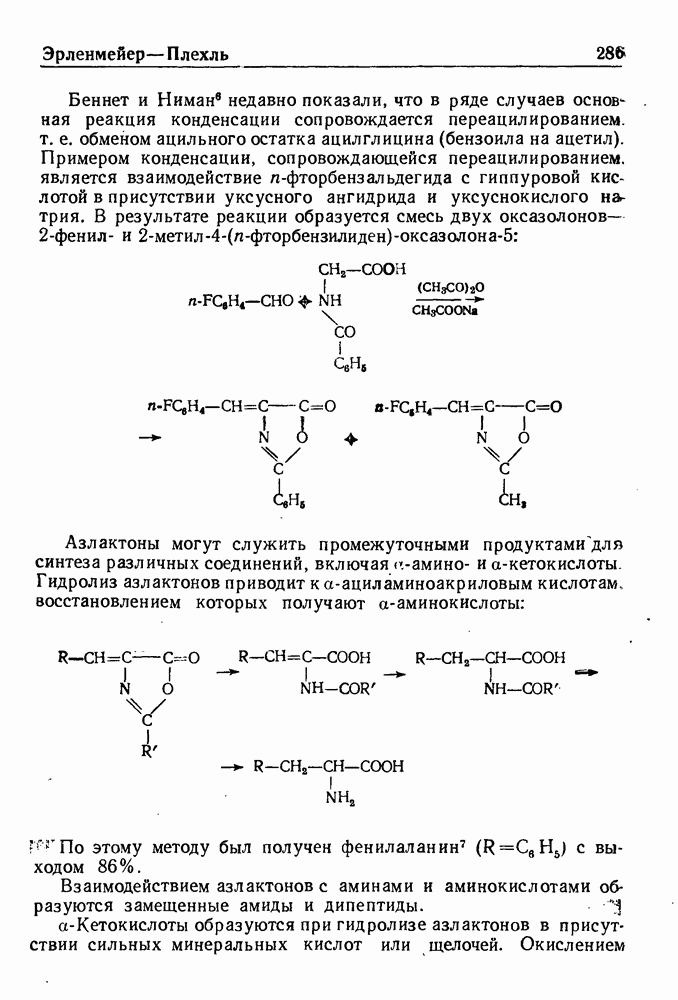
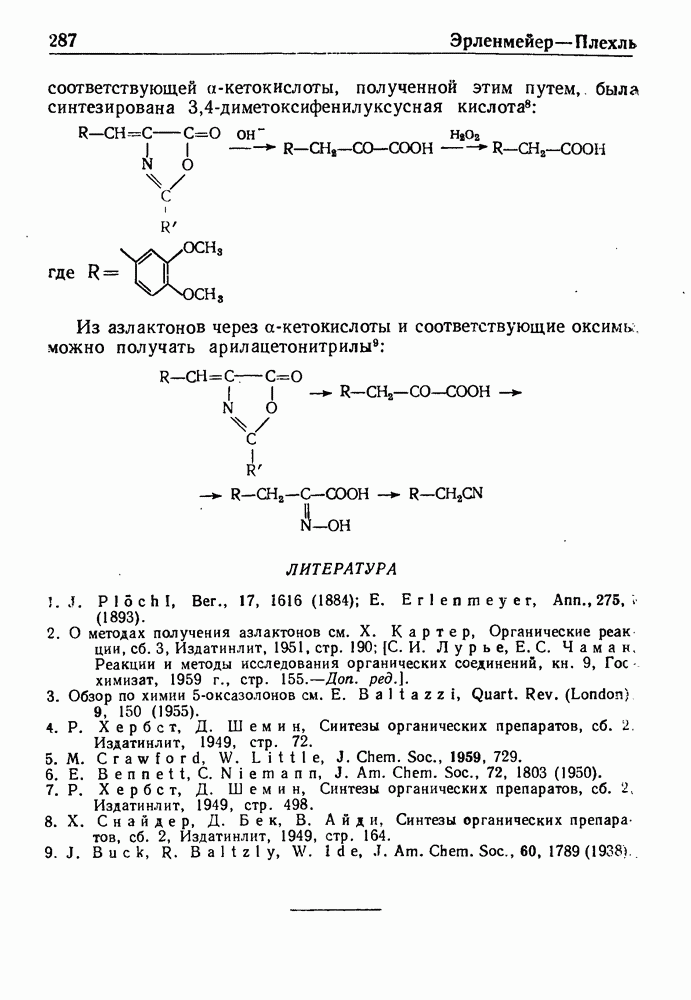
- СИНТЕЗ АЗЛАКТОНОВ ПО ЭРЛЕНМЕИЕРУ—ПЛЕХЛЮ
- РЕАКЦИЯ ЯКОБСЕНА