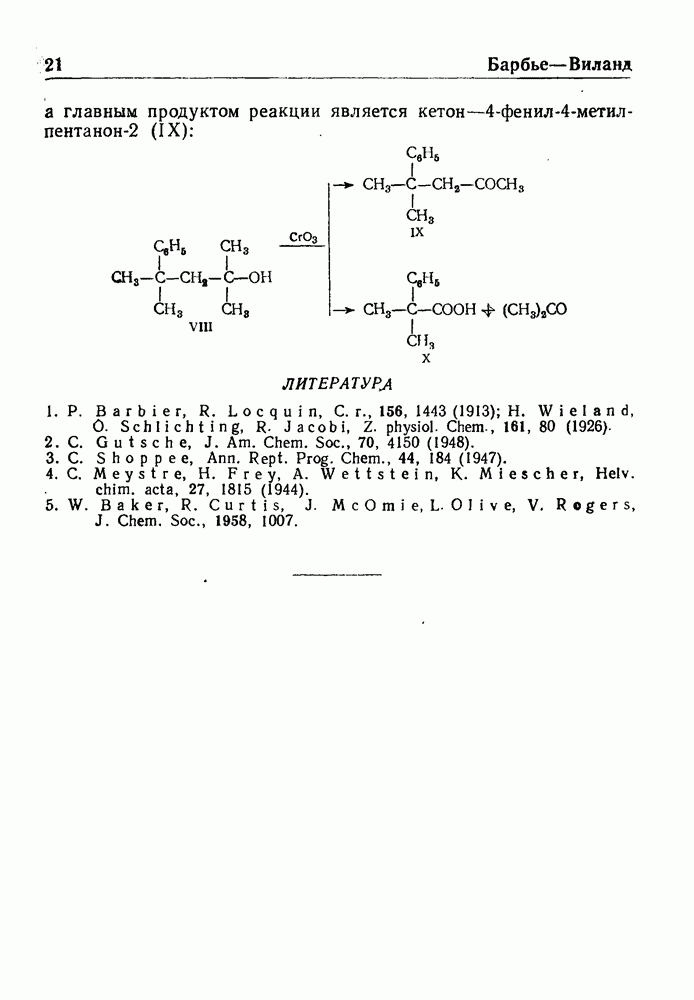
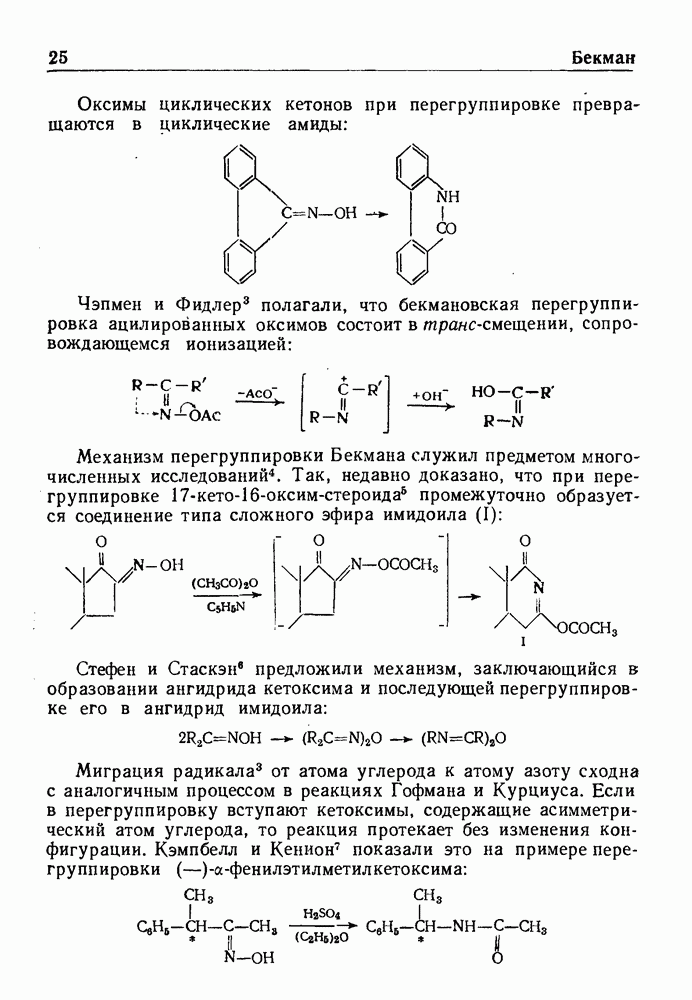
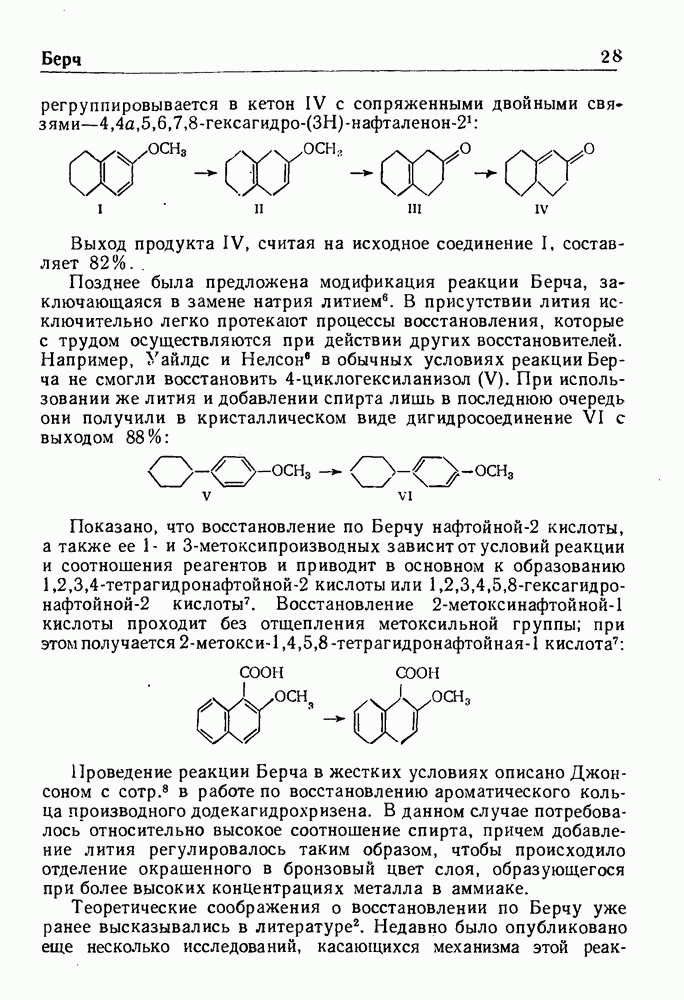
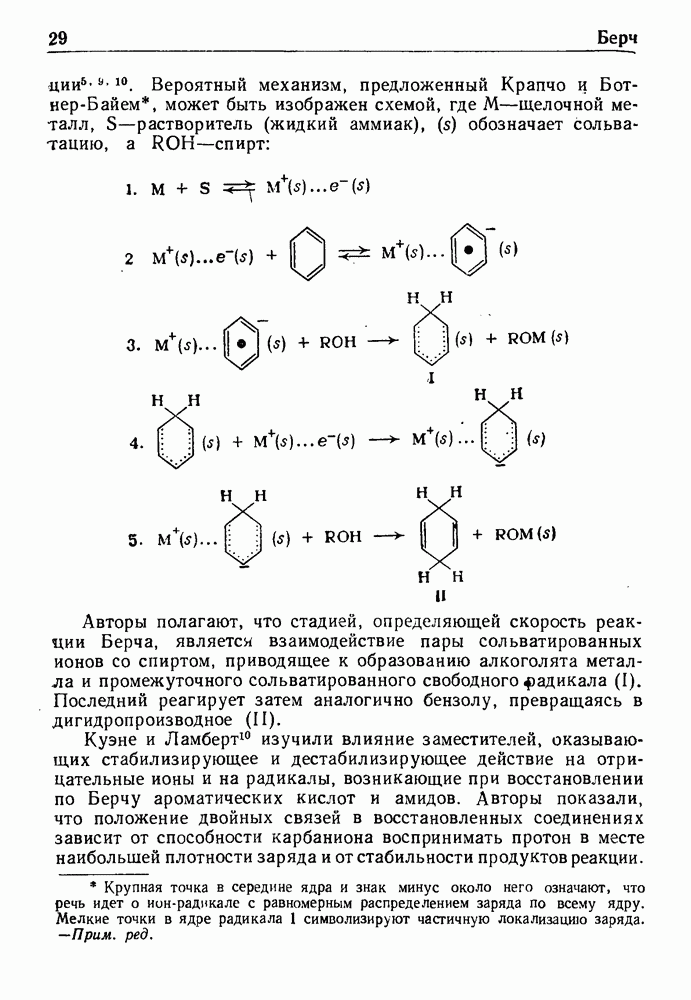
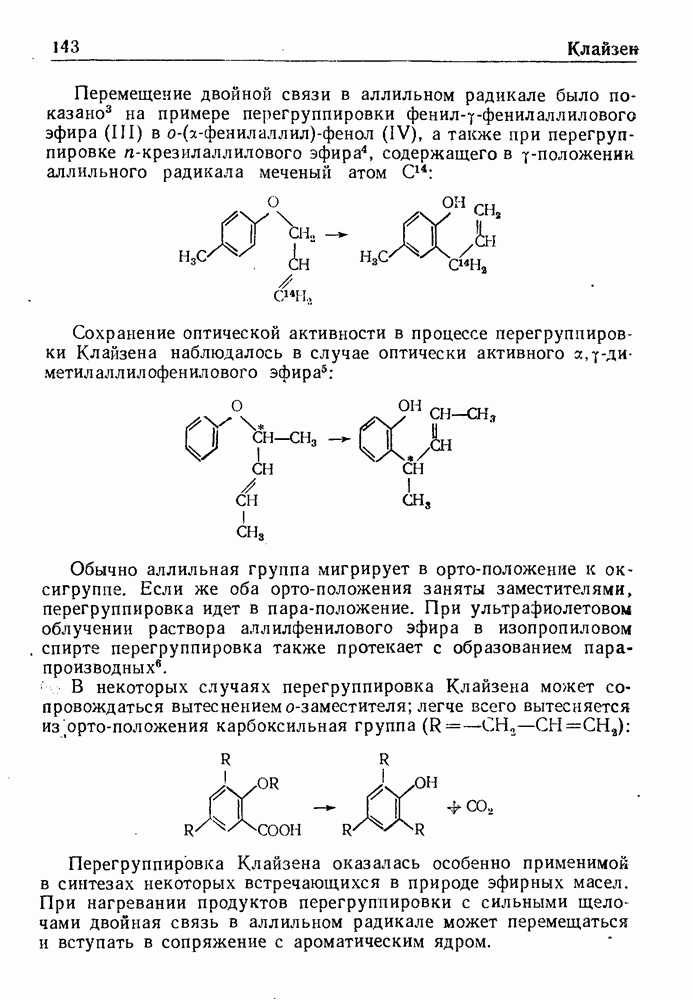
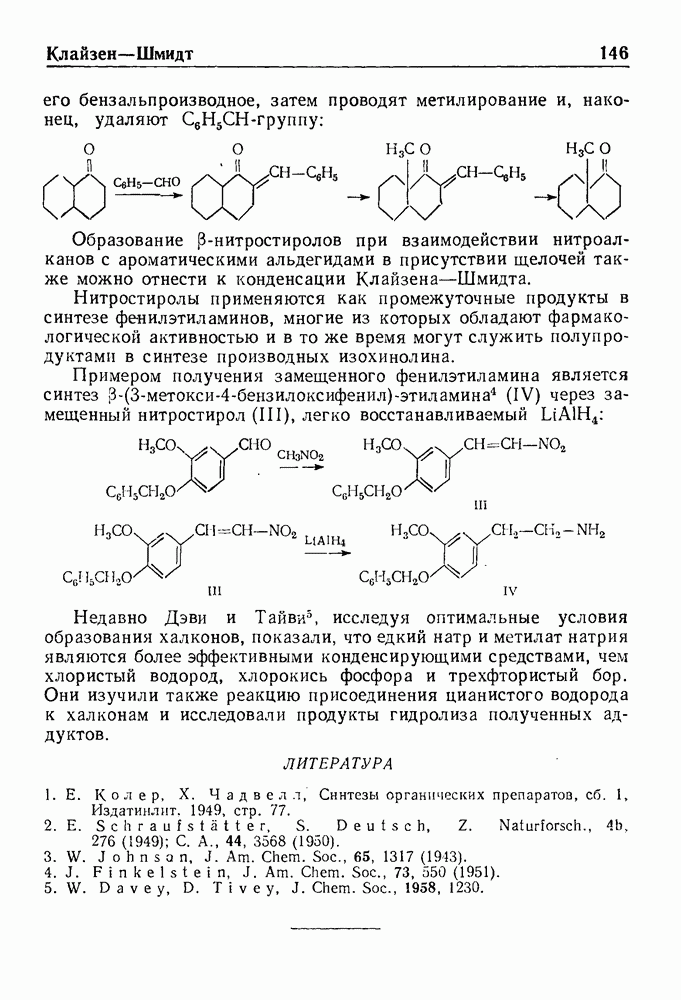
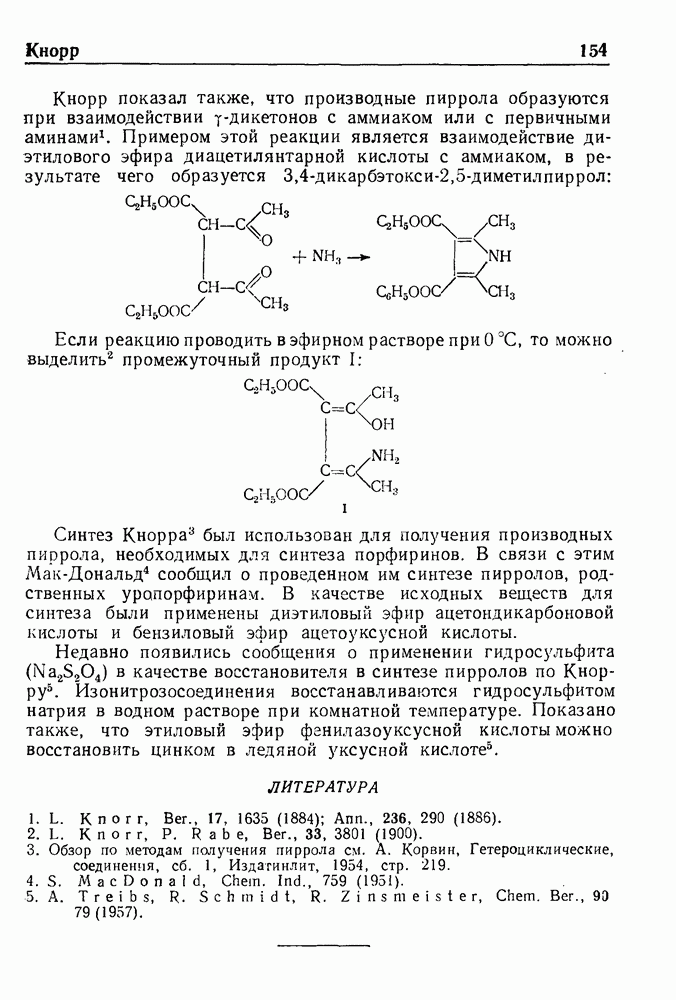
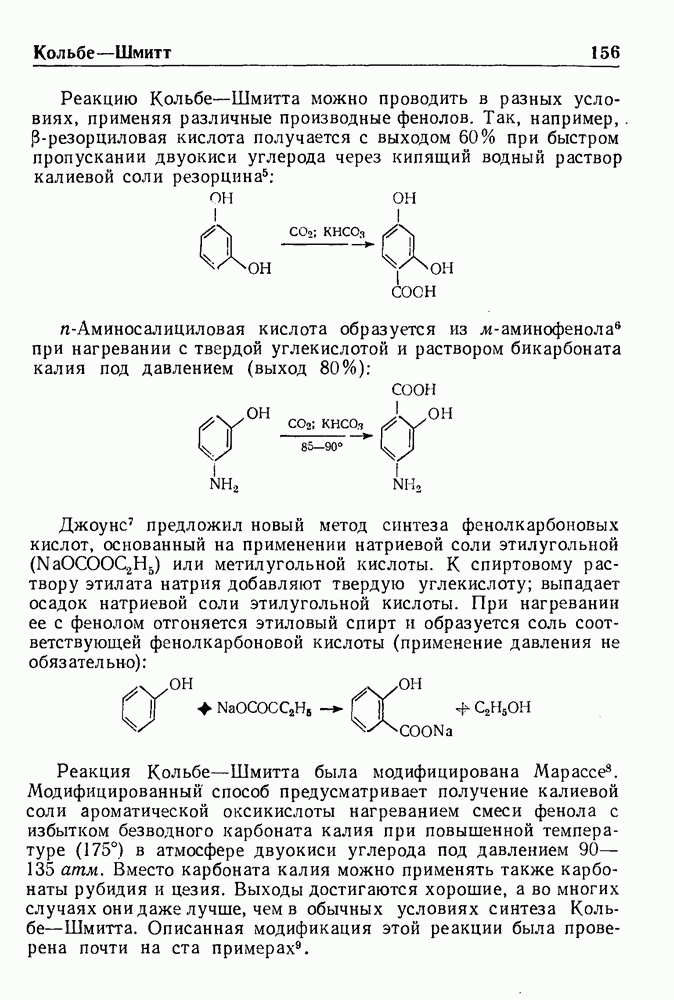
| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
РЕАКЦИЯ МАННИХА
Карл Ульрих Франц Манних (Carl (Jirich Franz Mannich, 1877-1947) родился в Бреслау (Германия). Учился в Марбургском, Берлинском и Базельском университетах- В 1903 г. получил степень доктора. Преподавал в Геттингенском и Франкфуртском университетах. С 1927 г. профессор и директор фармацевтического института в Берлине. Занимался главным образом синтезом органических веществ, применяемых в фармакологии. Он выделил в кристаллическом виде сердечные глюкознды из наперстянки и строфанта. Начиная с 1917 г., в течение почти 30 лет, изучал реакцию, носящую его имя, и возможности ее практического применения. Установил, что при взаимодействии метиламина с формальдегидом и ацетоном образуется производное пиперидина и получил из него метилареколин. Синтезировал большое число аминокетонов и аминоспиртов, использовал аминоспирты для приготовления эфиров  -аминобензойной кислоты, исследовал возможность применения этих эфиров в качестве местных анестезирующих средств.
-аминобензойной кислоты, исследовал возможность применения этих эфиров в качестве местных анестезирующих средств.
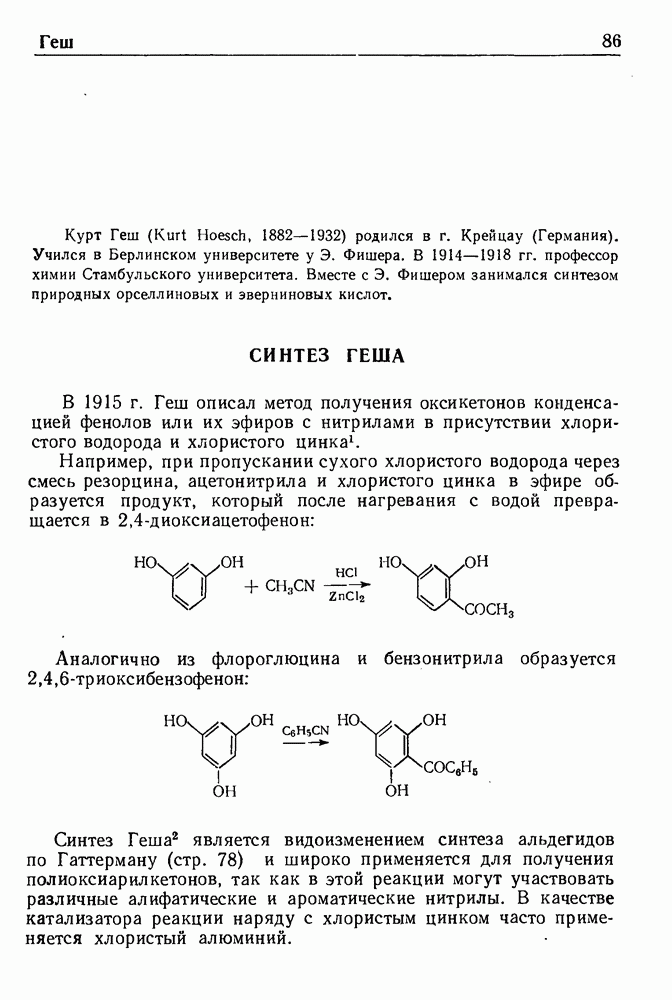
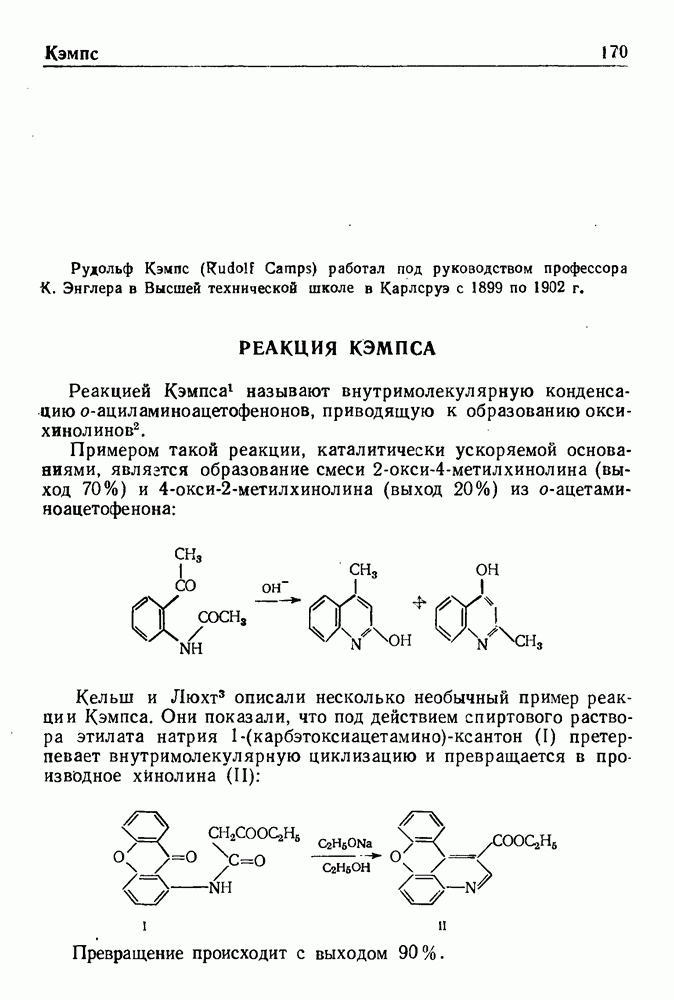
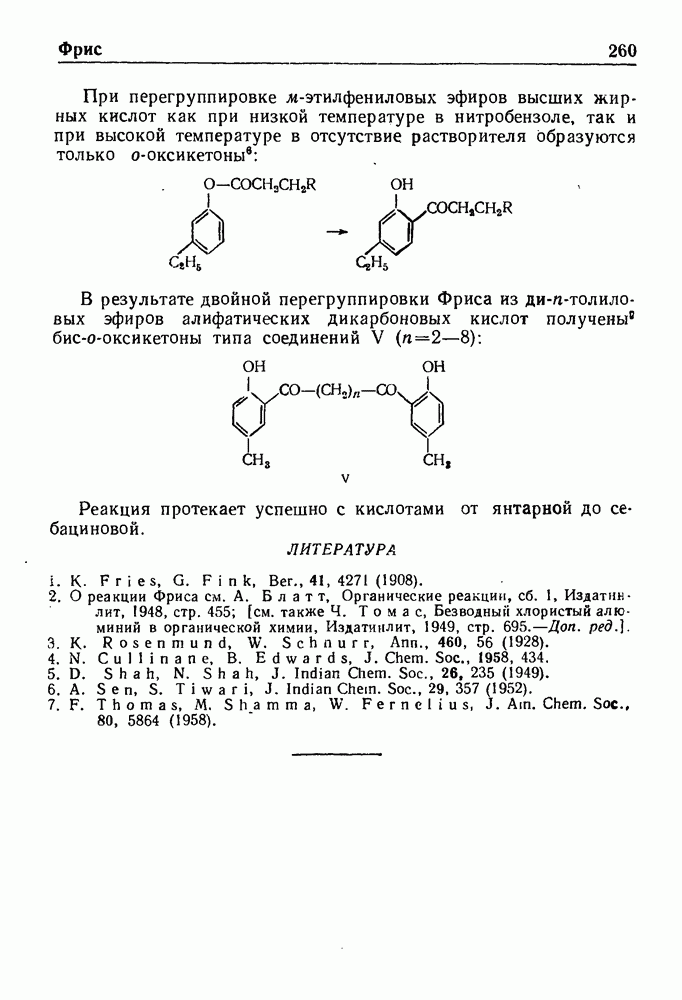
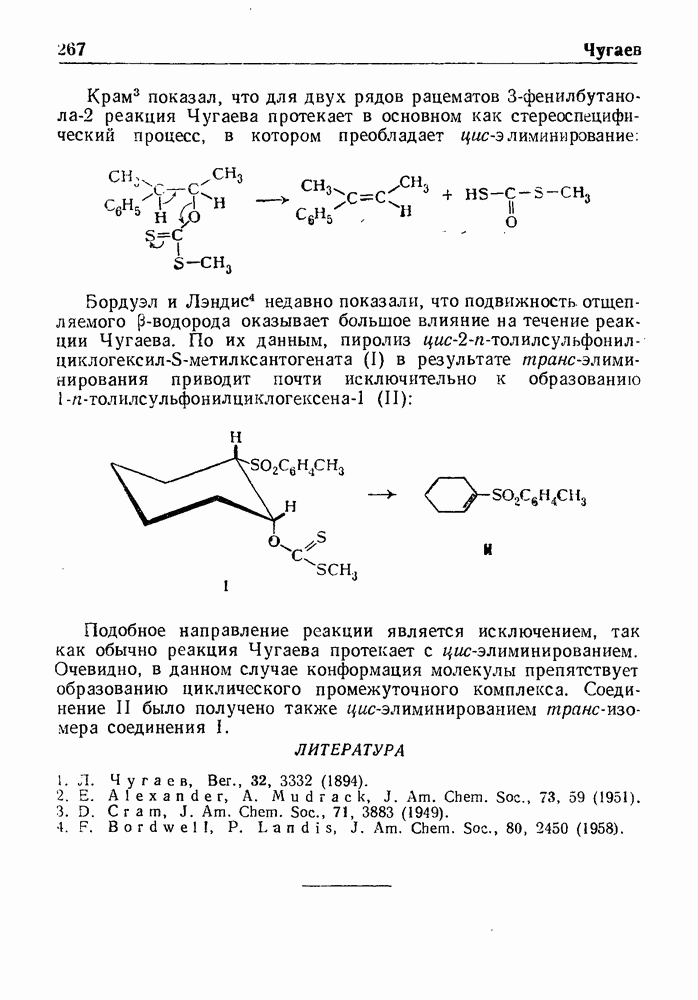
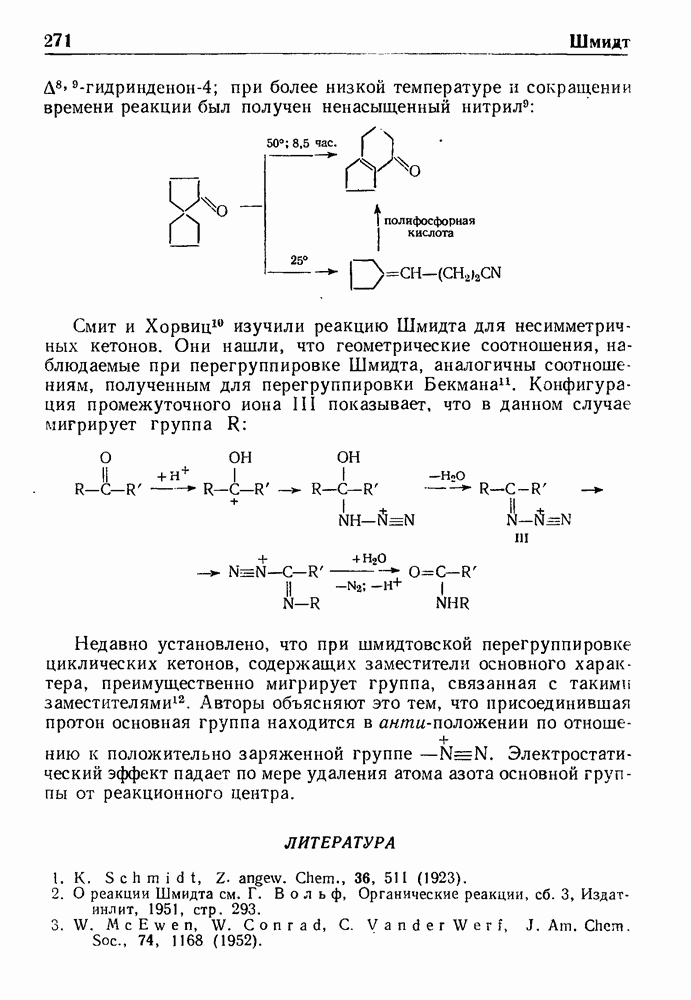
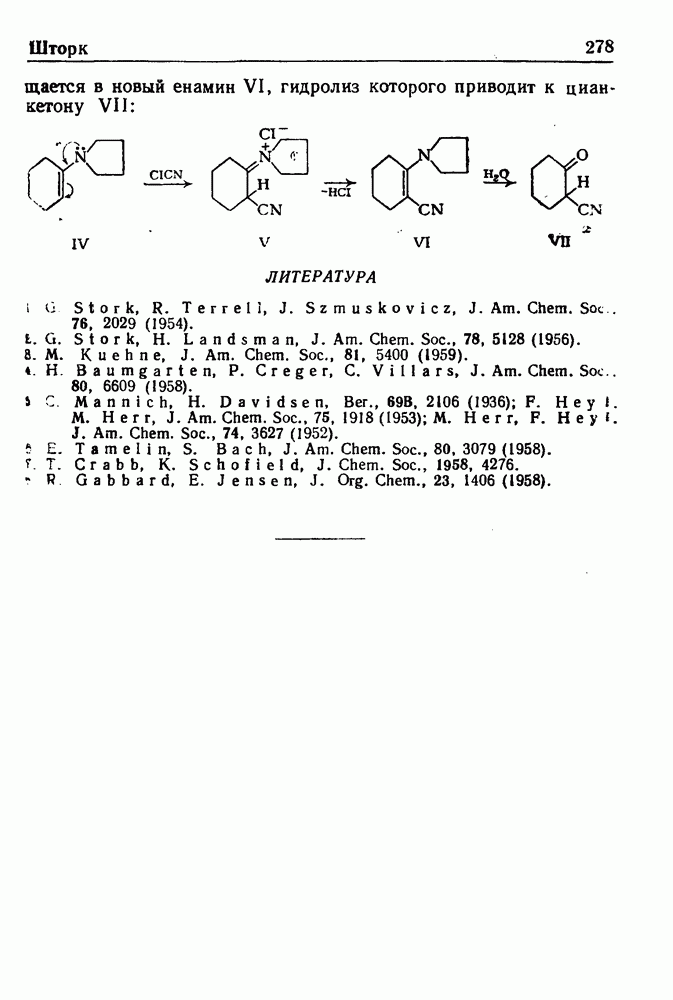
Реакцией Манииха называют конденсацию соединений, содержащих один или несколько подвижных атомов водорода, с формальдегидом и аммиаком или аминами (первичными или вторичными); при этом атомы водорода замещаются на аминометильную группу.
Примером реакции может служить синтез хлоргидрата 4(-ди-этиламино)-бутанона-2 из ацетона, формальдегида и солянокислого диэтиламина:

Поскольку в молекуле ацетона имеется несколько подвижных атомов водорода, их также можно заменить на диэтиламинометилькые группы.
Отдельные примеры конденсации подобного типа были известны и до Манниха, но он первый показал общий характер этой реакции и ее значение в органическом синтезе.
В реакции Манниха успешно используется большое число различных соединений, включая кетоны, альдегиды, сложные
эфиры и фенолы. Аминосоставляющие реакции также могут быть самыми разнообразными.
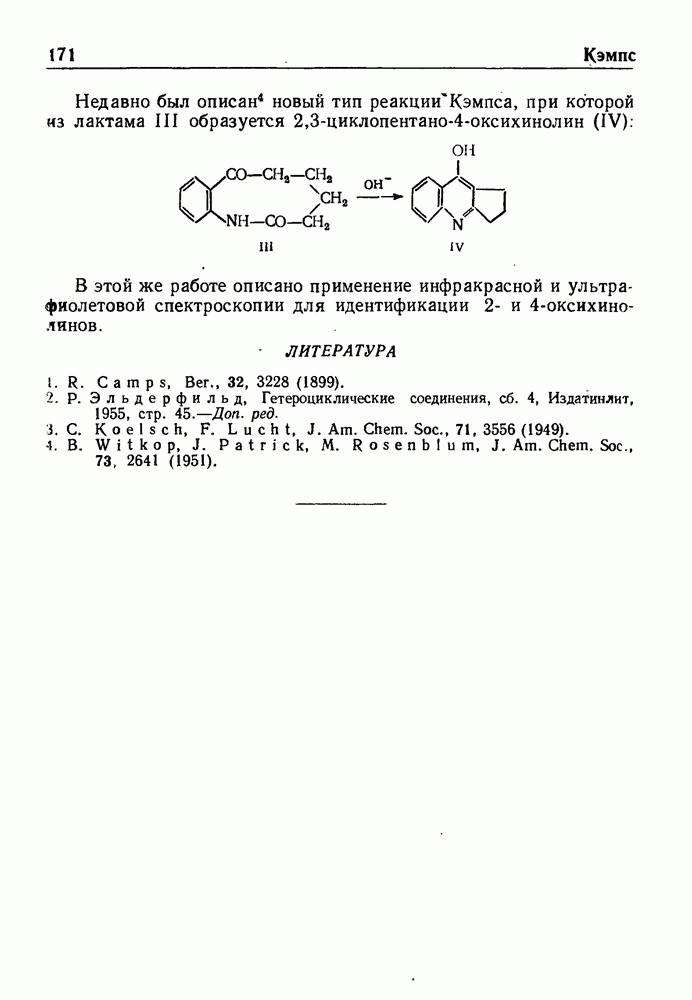
Иллюстрацией применения ароматических оксисоединений для получения оснований Манниха является конденсация 5-хлор-8-оксихинолина с диэтиламином и параформальдегидом; при этом образуется активный химиотерапевтический (амебоцидный) препарат-5-хлор-7-диэтиламинометил-8-оксихинолин:

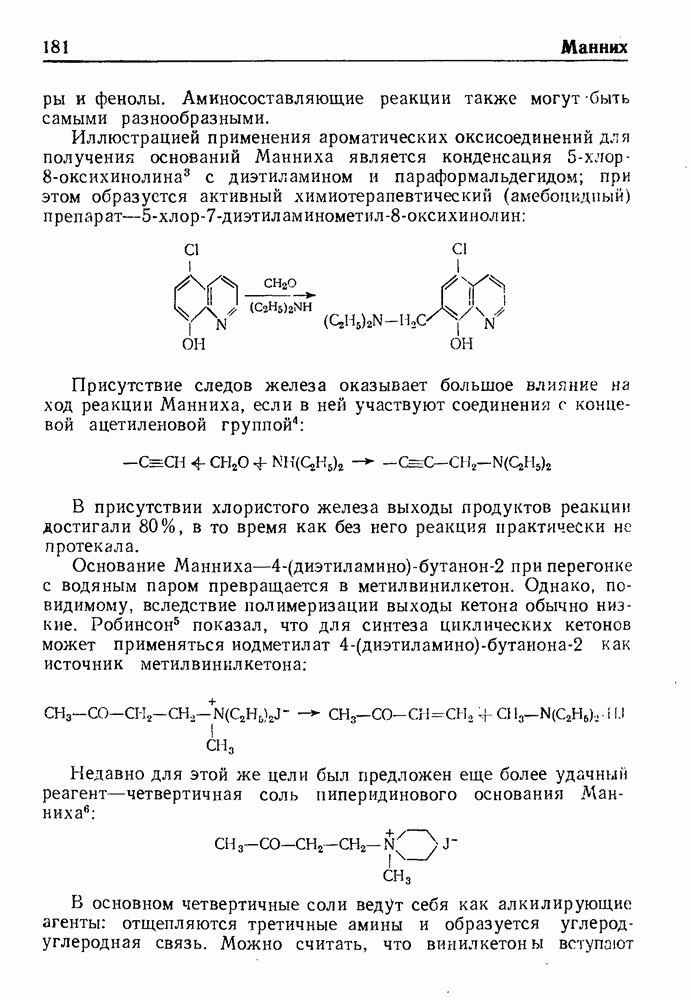
Присутствие следов железа оказывает большое влияние на ход реакции Манниха, если в ней участвуют соединения с концевой ацетиленовой группой:

В присутствии хлористого железа выходы продуктов реакции достигали 80%, в то время как без него реакция практически не протекала.
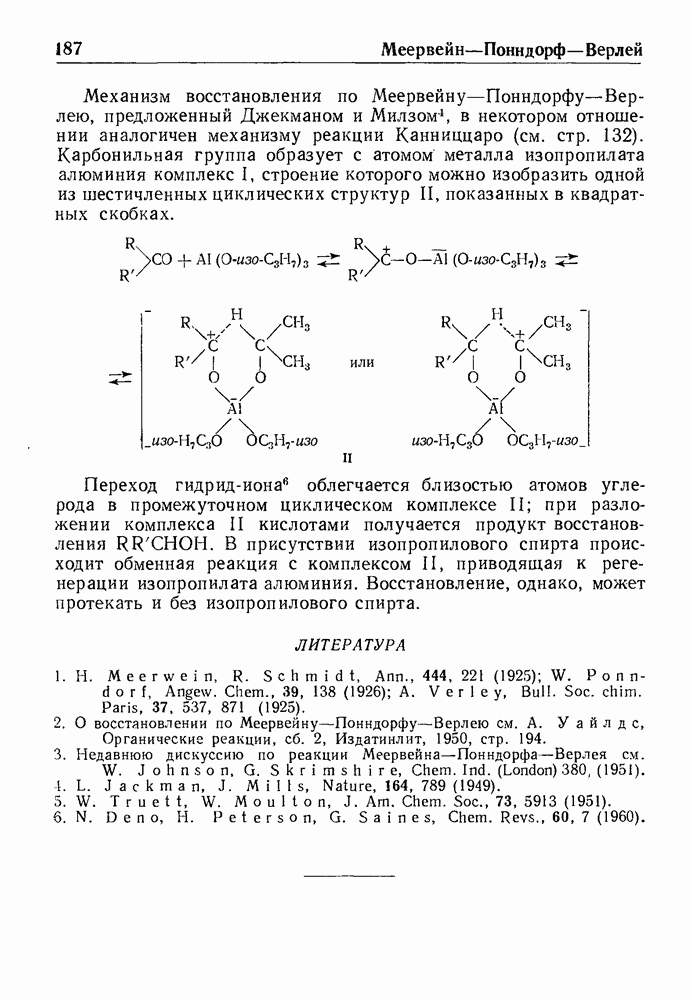
Основание Манниха-4-(диэтиламино)-бутанон-2 при перегонке с водяным паром превращается в метилвинилкетон. Однако, по-видимому, вследствие полимеризации выходы кетона обычно низкие. Робинсон показал, что для синтеза циклических кетонов может применяться иодметилат 4-(диэтиламино)-бутаиона-2 как источник метилвинил кетона:

Недавно для этой же цели был предложен еще более удачный реагент—четвертичная соль пиперидинового основания Манниха:

В основном четвертичные соли ведут себя как алкилирующие агенты: отщепляются третичные амины и образуется углерод-углеродная связь. Можно считать, что винилкетоны вступают
при этом в конденсацию по Михаэлю. Реакция этого типа была использована для синтеза триптофана, причем алкилирование ацетаминомалонового эфира проводили иодметилатом грамина:

Показано, что иодметилаты и окиси оснований Манниха, полученных из фенолов, легко реагируют в щелочной среде с различными нуклеофильными реагентами. Так, например, при взаимодействии с ионом метоксила происходит замена четвертичного лтома азота на метоксигруппу.
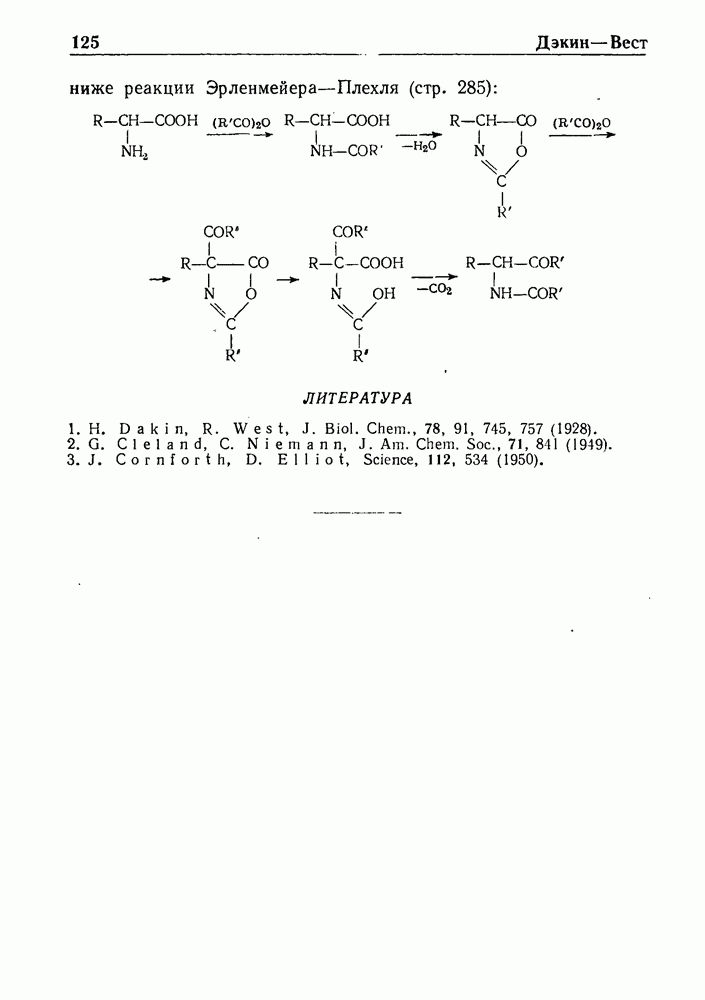
Применение основания Манниха как алкилирующего агента подробно описано Додсоном и Солменом. Авторы показали, что продукт конденсации 6-(диметиламино)-4-кетокапроновой кислоты (основание Манниха, образованное левулиновой кислотой) с этиловым эфиром малоновой кислоты при последующем гидролизе и декарбоксилировании превращается в у-кетосубериновую кислоту:

Механизм реакции Манниха не установлен; возможно, что промежуточным продуктом реакции является аминометанол, образующийся из амина и формальдегида:

Предполагают также, что в качестве промежуточных продуктов получаются метилен-бис-амины, которые в условиях реакции способны конденсироваться с соединениями, содержащими активную группу  в основания Манниха.
в основания Манниха.
ЛИТЕРАТУРА
(см. скан)
(см. скан)
| << Предыдущий параграф | Следующий параграф >> |
- ОТ РЕДАКТОРА
- ПЕРЕГРУППИРОВКА АРБУЗОВА
- СИНТЕЗ АРНДТА—ЭЙСТЕРТА
- ОКИСЛЕНИЕ ПО БАЙЕРУ—ВИЛЛИГЕРУ
- РАСЩЕПЛЕНИЕ ПО БАРБЬЕ—ВИЛАНДУ
- РЕАКЦИЯ БАРТА
- ПЕРЕГРУППИРОВКА БЕКМАНА
- ВОССТАНОВЛЕНИЕ ПО БЕРНУ
- ВОССТАНОВЛЕНИЕ ПО БЕШАНУ
- РЕАКЦИЯ БИШЛЕРА—НАПИРАЛЬСКОГО
- ХЛОРМЕТИЛИРОВАНИЕ ПО БЛАНУ
- РЕАКЦИЯ БРАУНА
- РАСЩЕПЛЕНИЕ АМИНОВ ПО БРАУНУ
- ВОССТАНОВЛЕНИЕ ПО БУВО—БЛАНУ
- СИНТЕЗ АЛЬДЕГИДОВ ПО БУВО
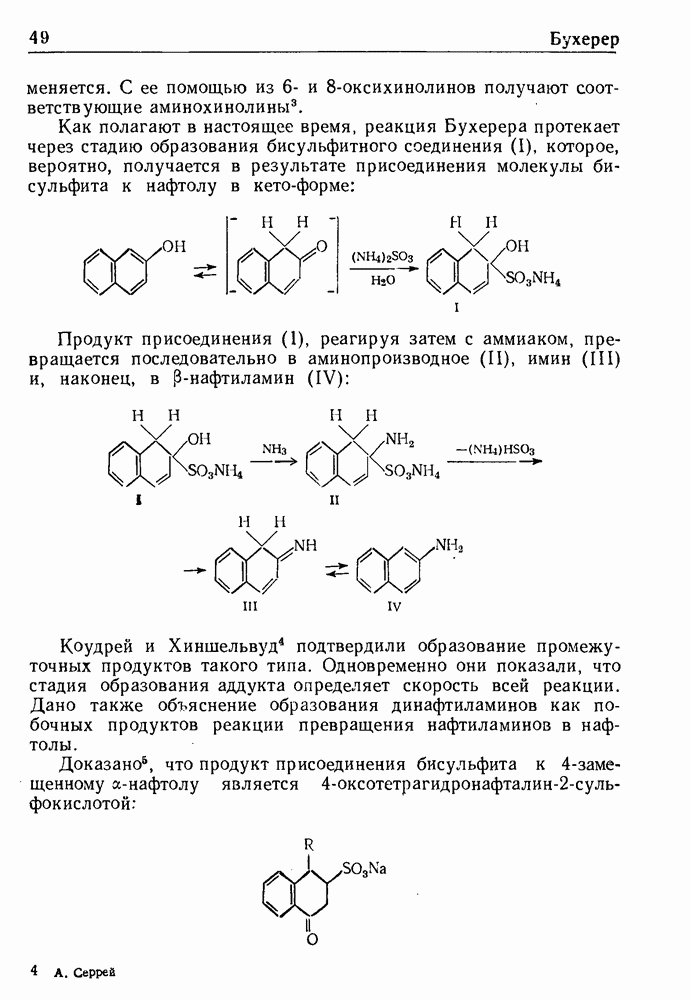
- РЕАКЦИЯ БУХЕРЕРА
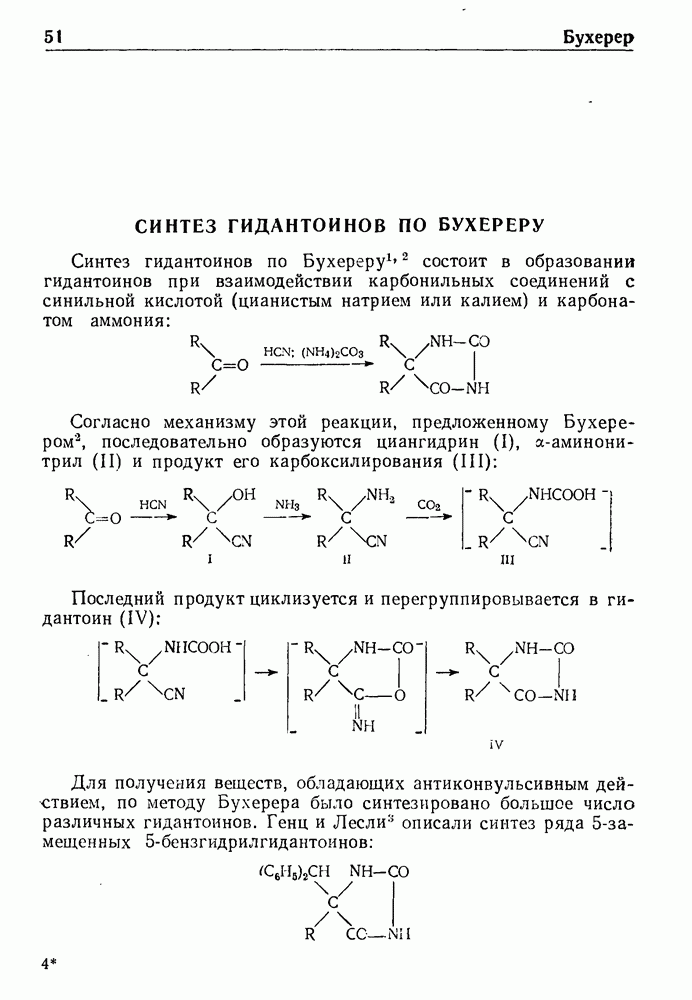
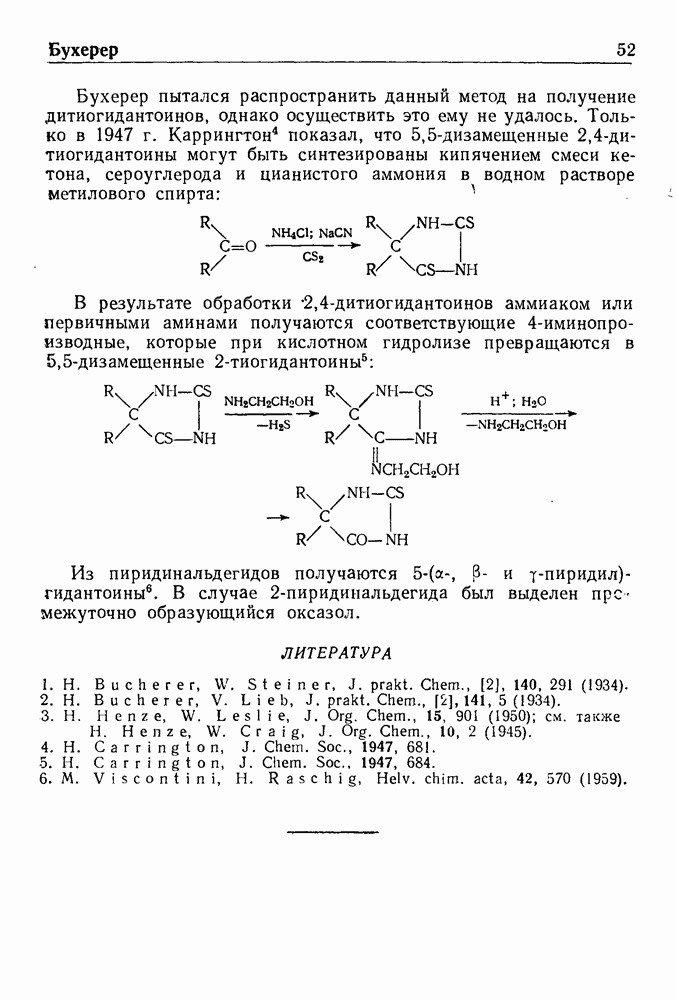
- СИНТЕЗ ГИДАНТОИНОВ ПО БУХЕРЕРУ
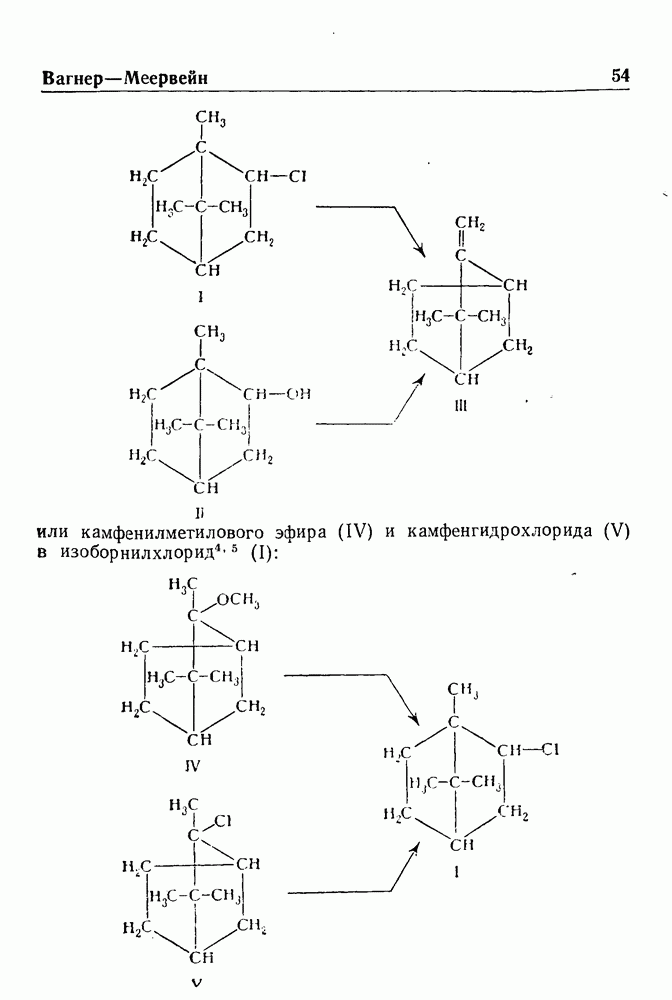
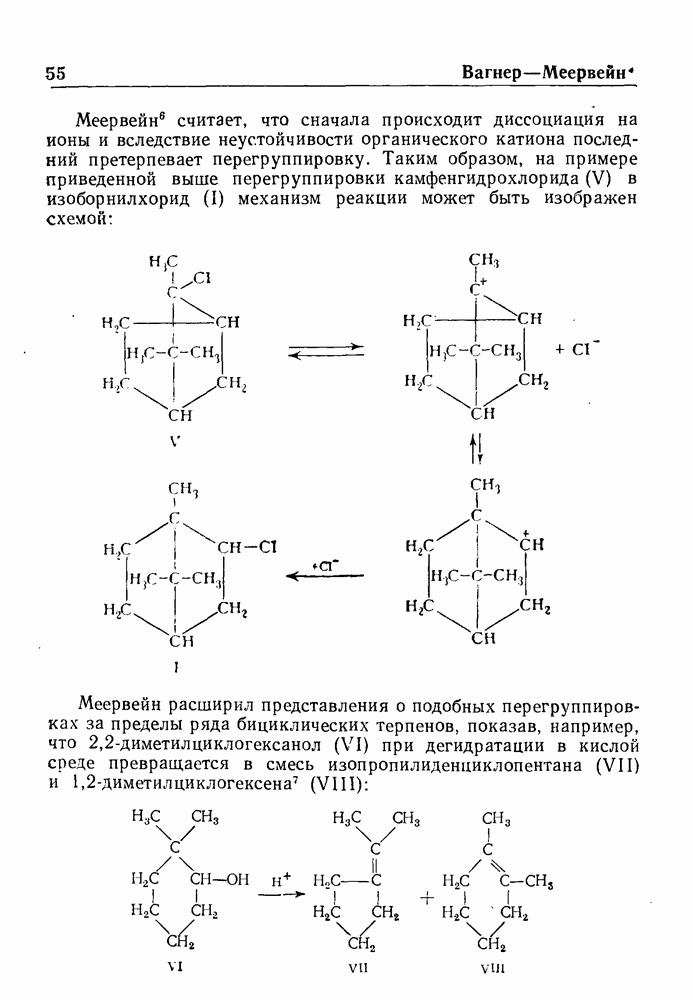
- ПЕРЕГРУППИРОВКА ВАГНЕРА—МЕЕРВЕЙНА
- РЕАКЦИЯ ВАЛЛАХА
- РЕАКЦИЯ ВИЛЬГЕРОДТА
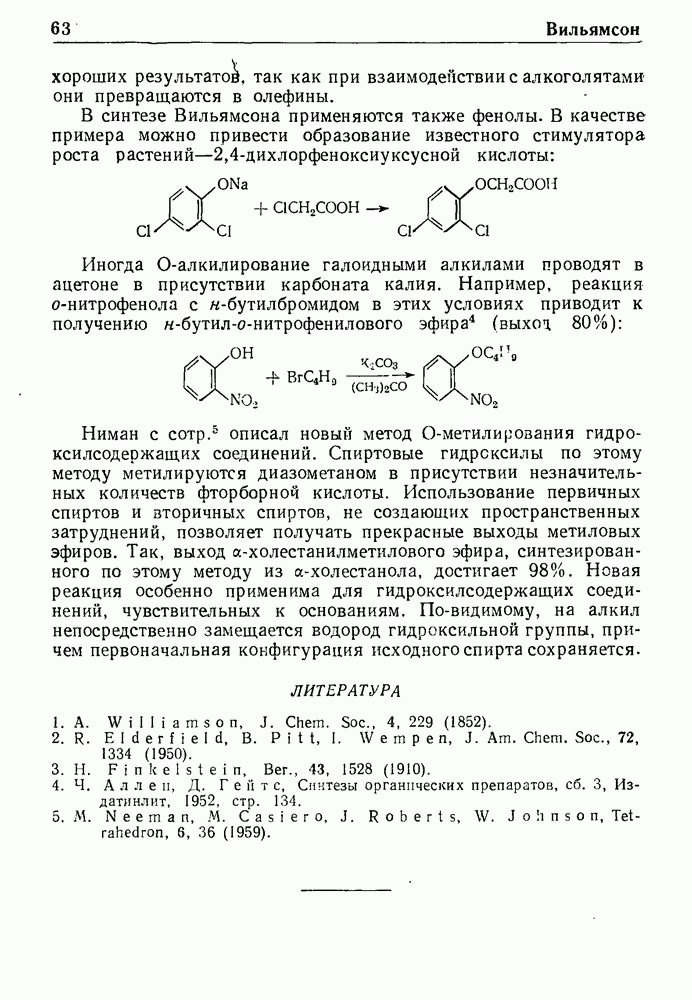
- СИНТЕЗ ВИЛЬЯМСОНА
- РЕАКЦИЯ ВИТТИГА
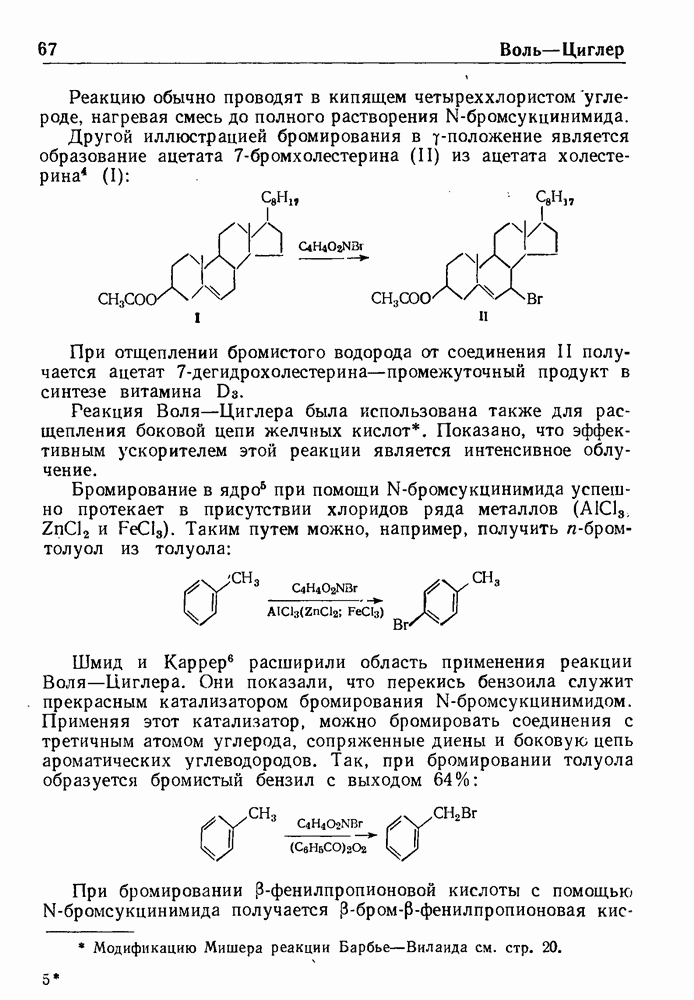
- РЕАКЦИЯ ВОЛЯ-ЦИГЛЕРА
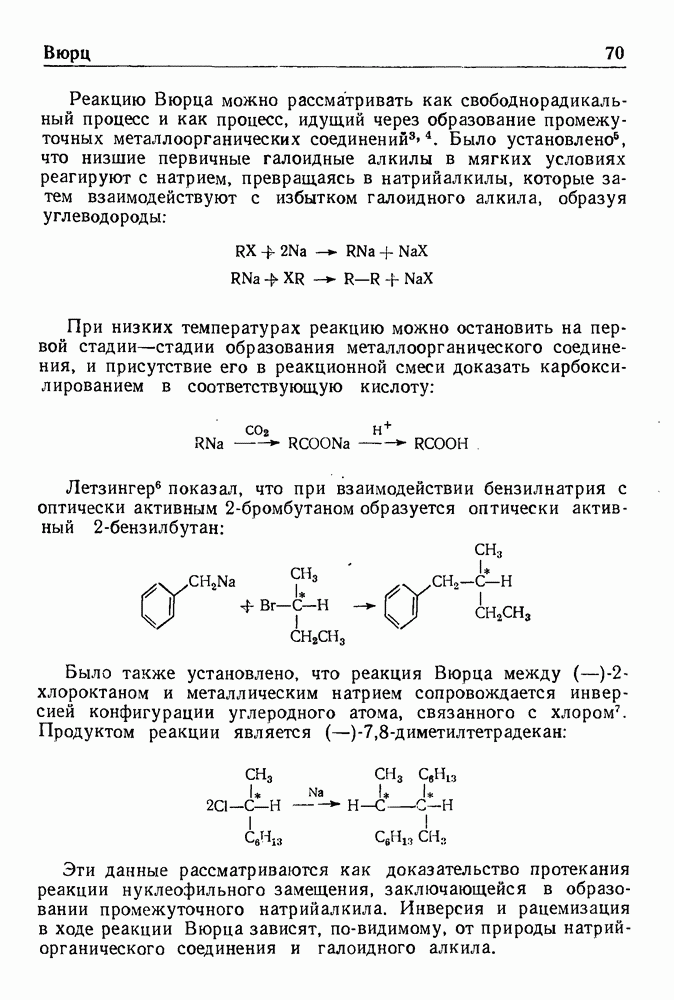
- РЕАКЦИЯ ВЮРЦА
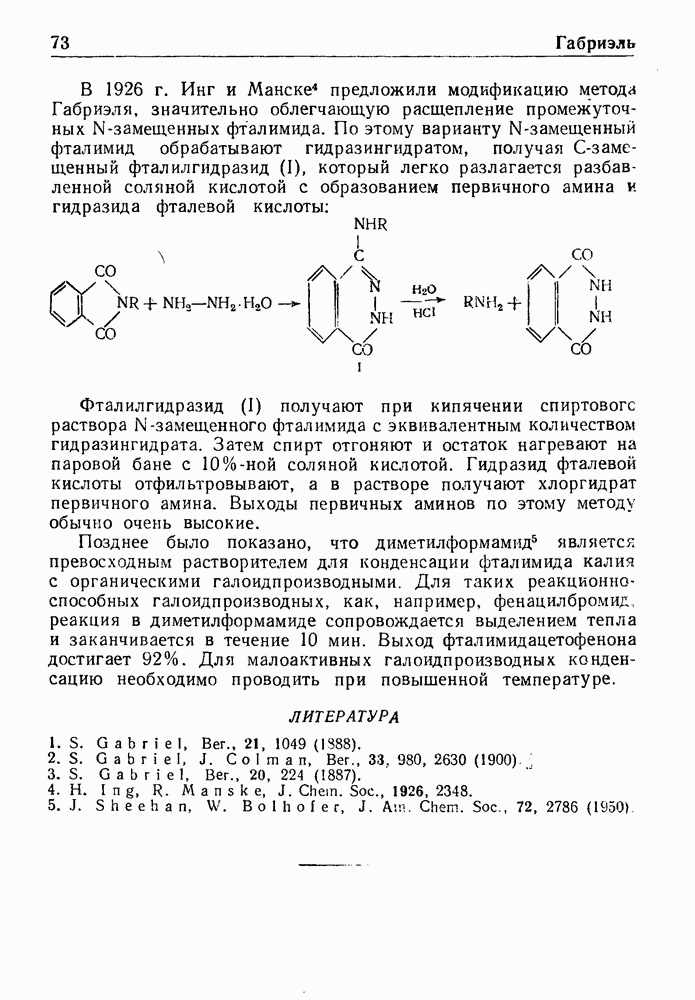
- СИНТЕЗ ГАБРИЭЛЯ
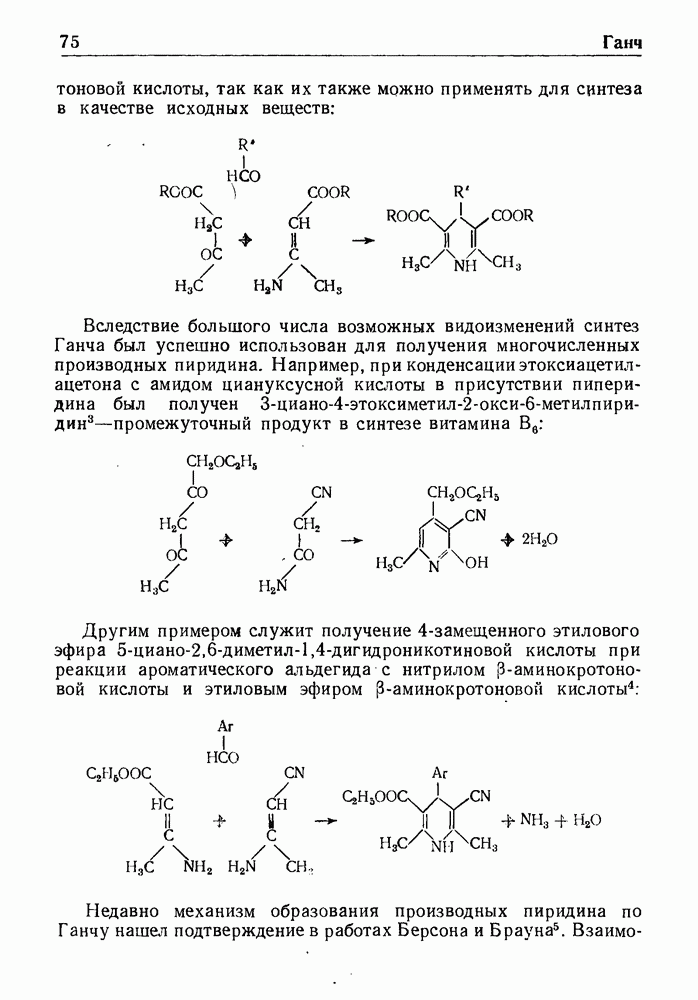
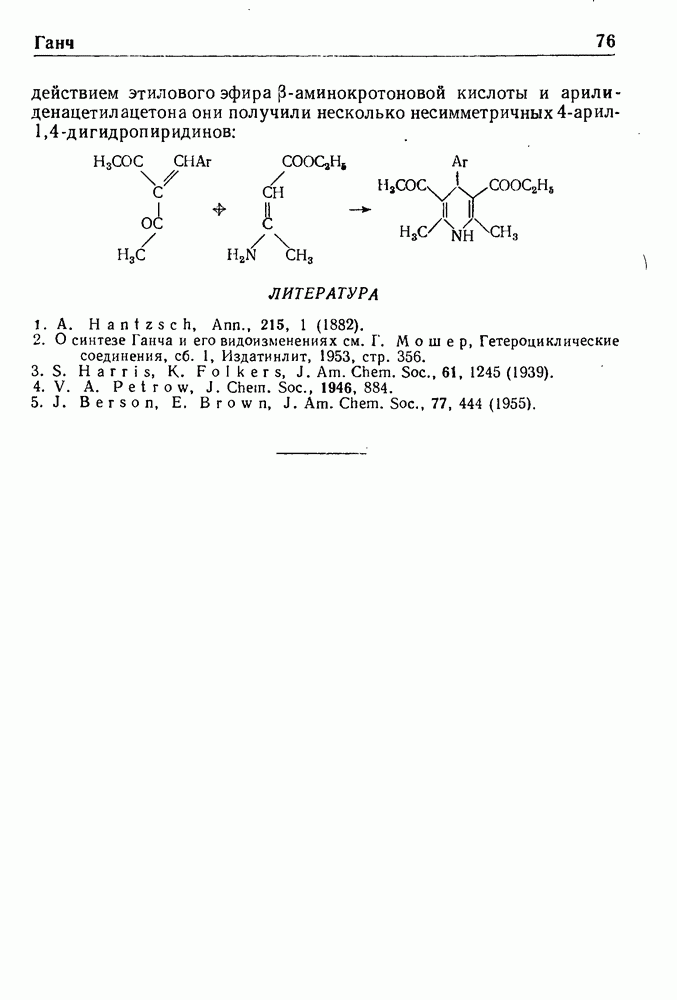
- СИНТЕЗ ГАНЧА
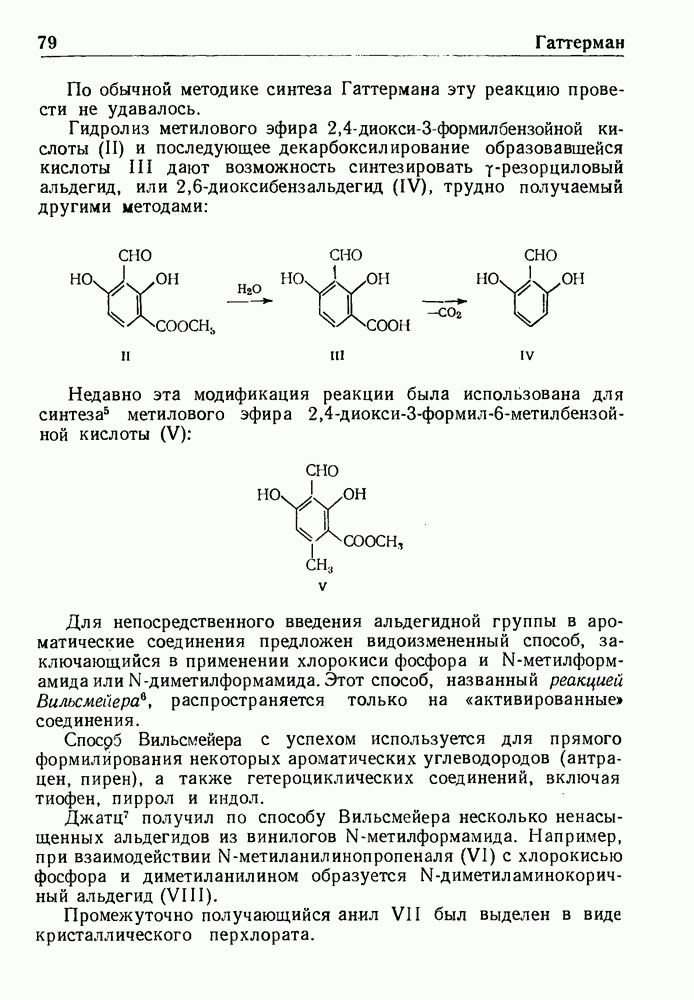
- РЕАКЦИЯ ГАТТЕРМАНА
- СИНТЕЗ АЛЬДЕГИДОВ ПО ГАТТЕРМАНУ
- РЕАКЦИЯ ГАТТЕРМАНА—КОХА
- РЕАКЦИЯ ГЕЛЛЯ—ФОЛЬГАРДА—ЗЕЛИНСКОГО
- СИНТЕЗ ГЕША
- РЕАКЦИЯ ГОМБЕРГА—БАХМАНА—ХЕЯ
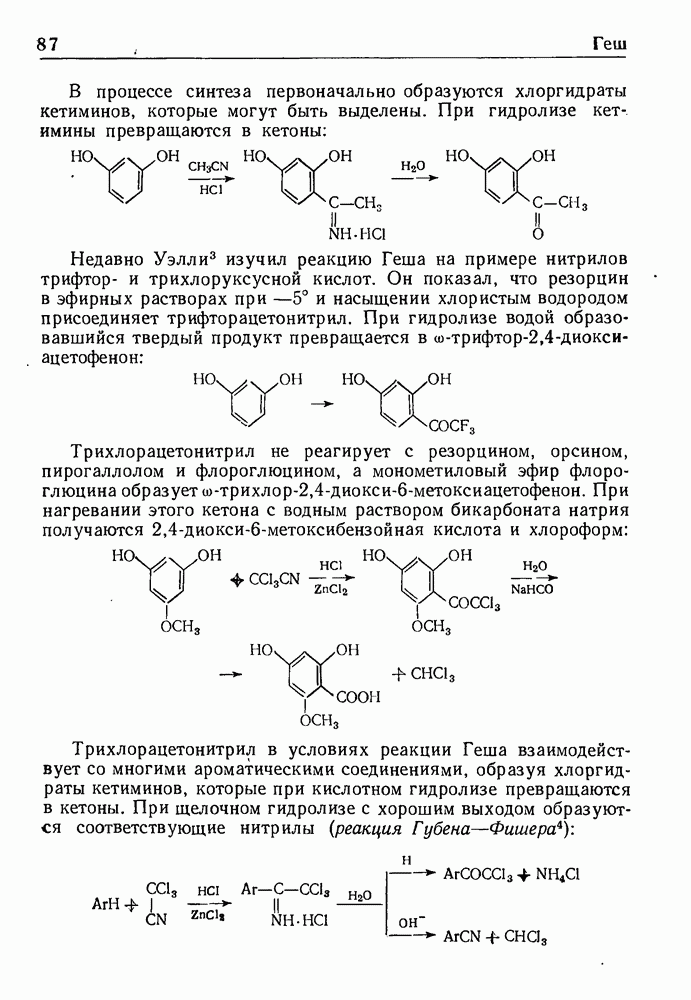
- РЕАКЦИЯ ГОУЛДА—ДЖЕКОБСА
- ПЕРЕГРУППИРОВКА ГОФМАНА
- РАСЩЕПЛЕНИЕ ПО ГОФМАНУ
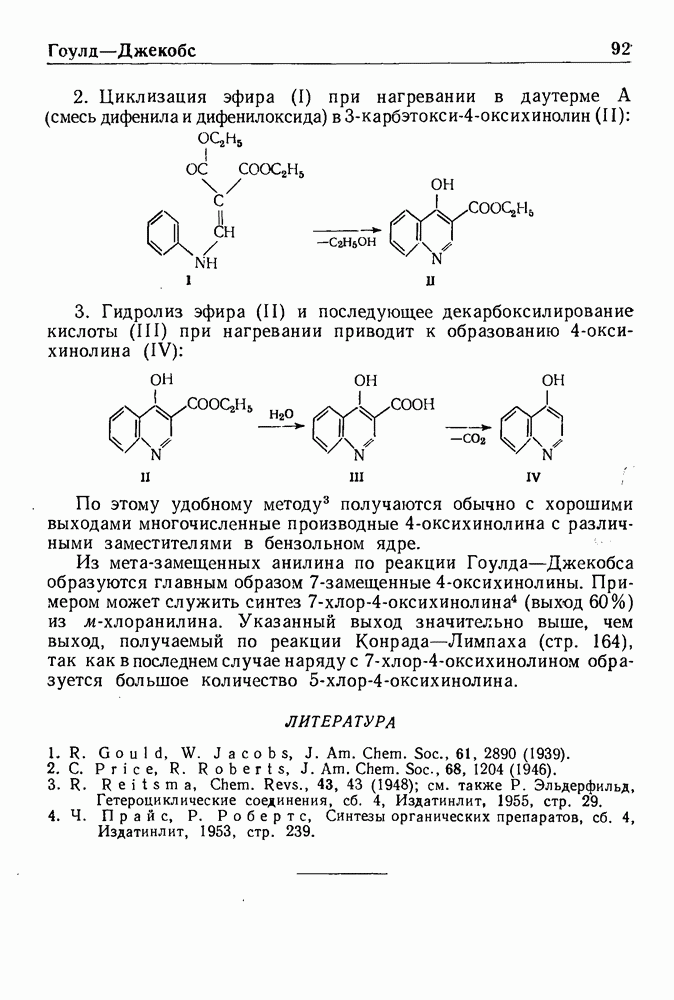
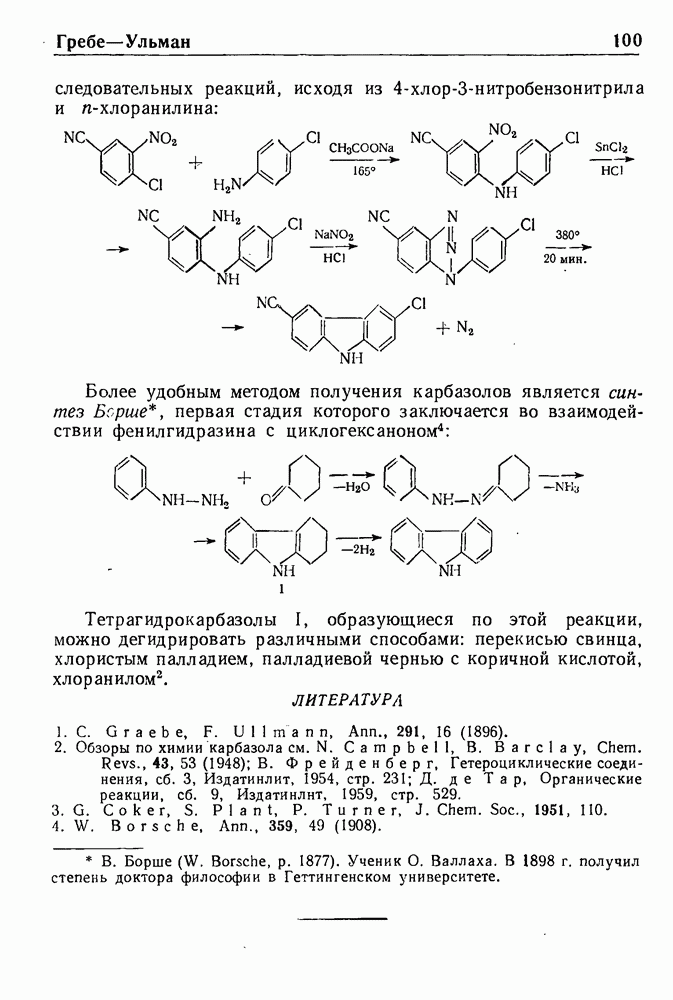
- СИНТЕЗ ГРЕБЕ—УЛЬМАНА
- РЕАКЦИЯ ГРИНЬЯРА
- СИНТЕЗ ГЛИЦИДНЫХ ЭФИРОВ ПО ДАРЗАНУ
- СИНТЕЗ НЕПРЕДЕЛЬНЫХ КЕТОНОВ ПО ДАРЗАНУ
- РЕАКЦИЯ ДАФФА
- СИНТЕЗ ДЕБНЕРА
- СИНТЕЗ ДЕБНЕРА—МИЛЛЕРА
- РЕАКЦИЯ ДЕЛЕПИНА
- РЕАКЦИЯ ДИКМАНА
- РЕАКЦИЯ ДИЛЬСА-АЛЬДЕРА
- РЕАКЦИЯ ДЭКИНА
- РЕАКЦИЯ ДЭКИНА—ВЕСТА
- РЕАКЦИЯ ЗАНДМЕЙЕРА
- РЕАКЦИЯ ИВАНОВА
- РЕАКЦИЯ ИОЦИЧА
- РЕАКЦИЯ КАННИЦЦАРО
- РЕАКЦИЯ КИЖНЕРА
- КОНДЕНСАЦИЯ КЛАЙЗЕНА
- ПЕРЕГРУППИРОВКА КЛАЙЗЕНА
- КОНДЕНСАЦИЯ КЛАЙЗЕНА—ШМИДТА
- ВОССТАНОВЛЕНИЕ ПО КЛЕММЕНСЕНУ
- РЕАКЦИЯ КНЕВЕНАГЕЛЯ
- СИНТЕЗ КНОРРА
- РЕАКЦИЯ КОЛЬБЕ—ШМИТТА
- ЭЛЕКТРОХИМИЧЕСКАЯ РЕАКЦИЯ КОЛЬБЕ
- СИНТЕЗ ХИНОЛИНА ПО КОМБУ
- РЕАКЦИЯ КОНОВАЛОВА
- СИНТЕЗ ХИНОЛИНА ПО КОНРАДУ—ЛИМПАХУ
- РЕАКЦИЯ КУРЦИУСА
- РЕАКЦИЯ КУЧЕРОВА
- РЕАКЦИЯ КЭМПСА
- РЕАКЦИЯ ЛЕЙКАРТА
- РЕАКЦИЯ ЛОССЕНА
- ВОССТАНОВЛЕНИЕ ПО МАК ФАДИЕНУ—СТИВЕНСУ
- РЕАКЦИЯ МАННИХА
- КОНДЕНСАЦИЯ МЕЕРВЕЙНА
- ВОССТАНОВЛЕНИЕ ПО МЕЕРВЕЙНУ-ПОННДОРФУ-ВЕРЛЕЮ
- РЕАКЦИЯ МИХАЭЛЯ
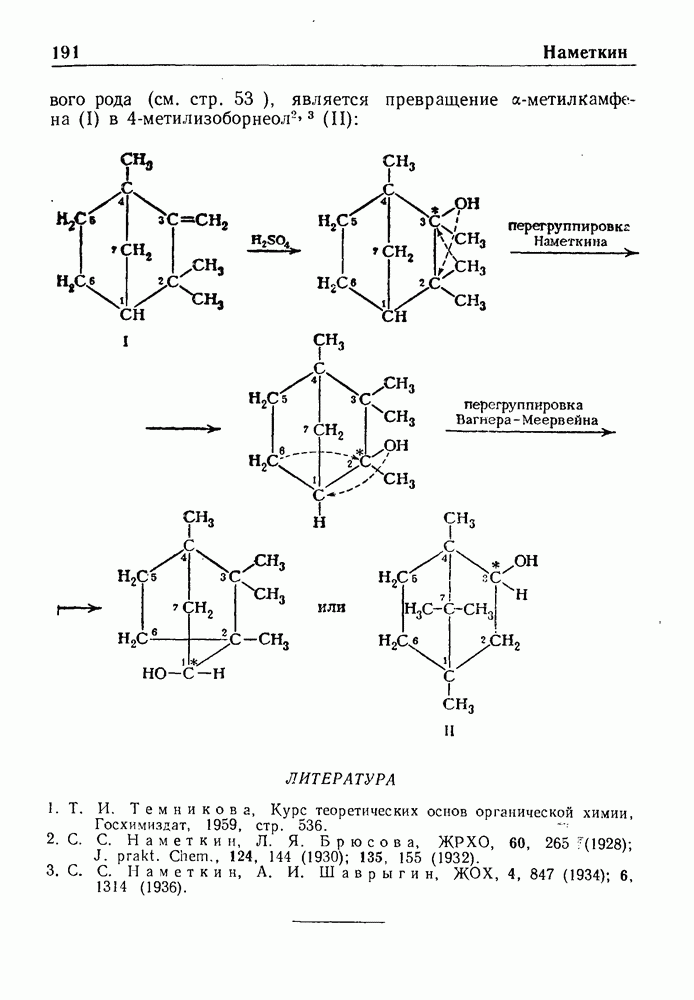
- ПЕРЕГРУППИРОВКА НАМЕТКИНА
- РЕАКЦИЯ НЕСМЕЯНОВА
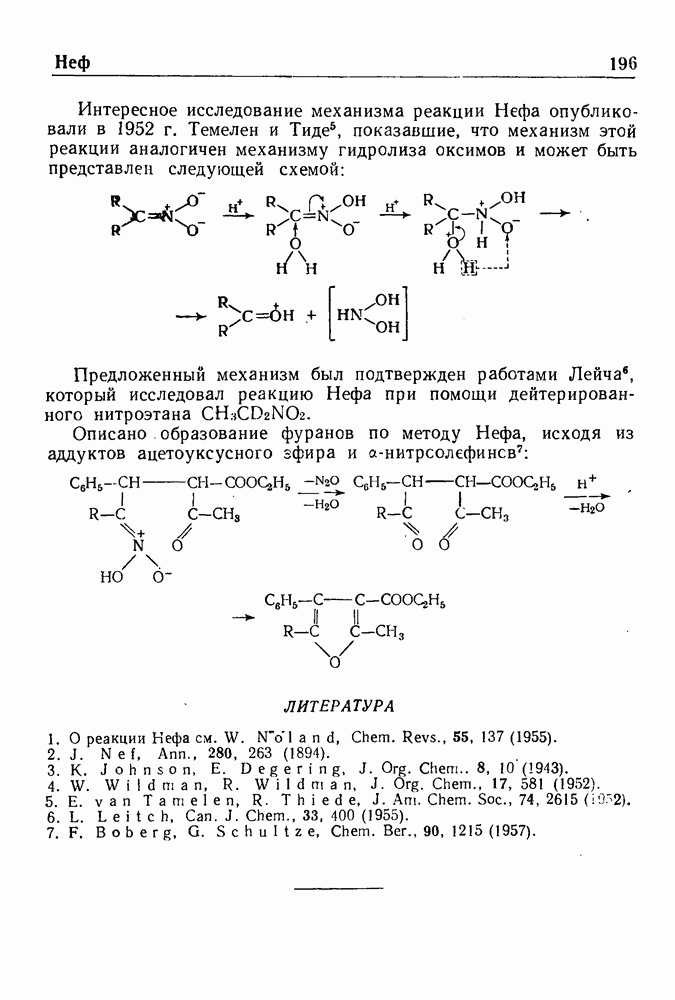
- РЕАКЦИЯ НЕФА
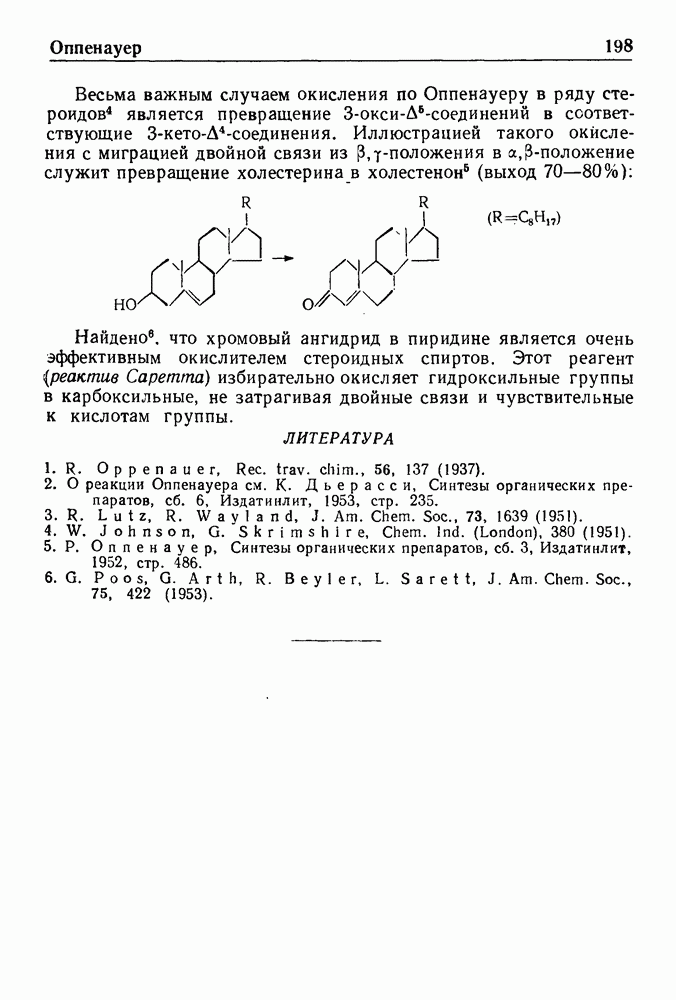
- ОКИСЛЕНИЕ ПО ОППЕНАУЕРУ
- РЕАКЦИЯ ПАССЕРИНИ
- РЕАКЦИЯ ПЕРКИНА
- КОНДЕНСАЦИЯ ПЕХМАНА
- РЕАКЦИЯ ПИКТЭ—ШПЕНГЛЕРА
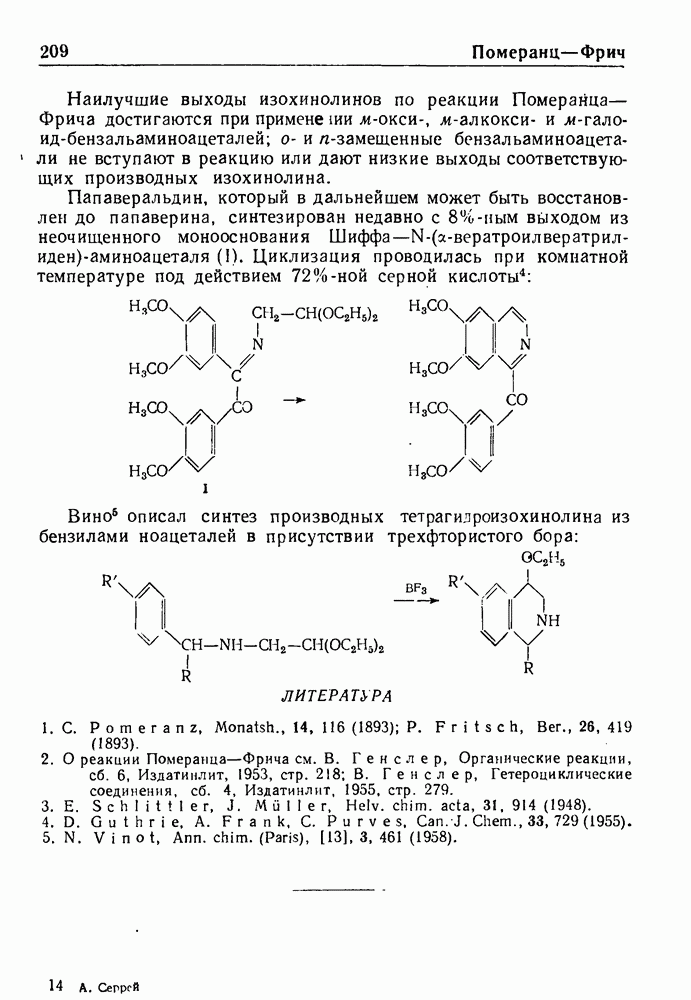
- РЕАКЦИЯ ПОМЕРАНЦА—ФРИЧА
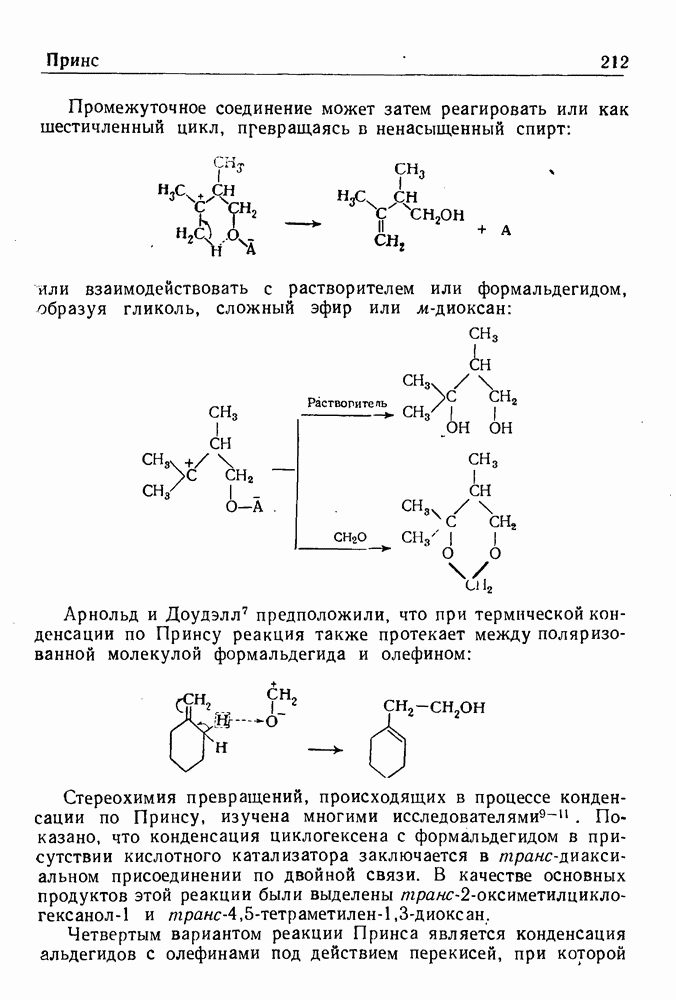
- РЕАКЦИЯ ПРИНСА
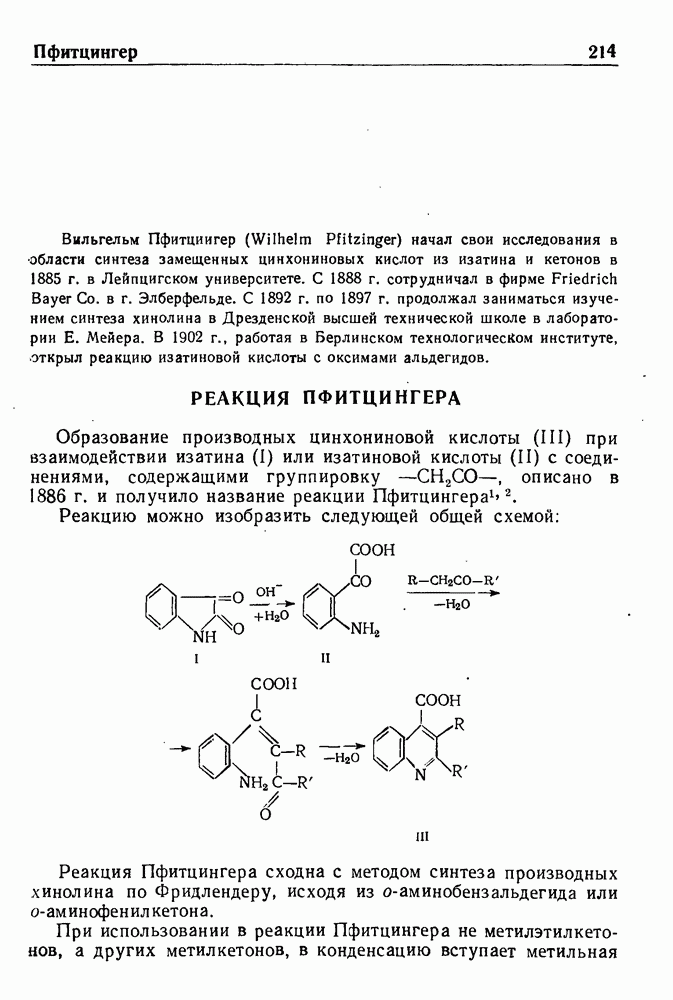
- РЕАКЦИЯ ПФИТЦИНГЕРА
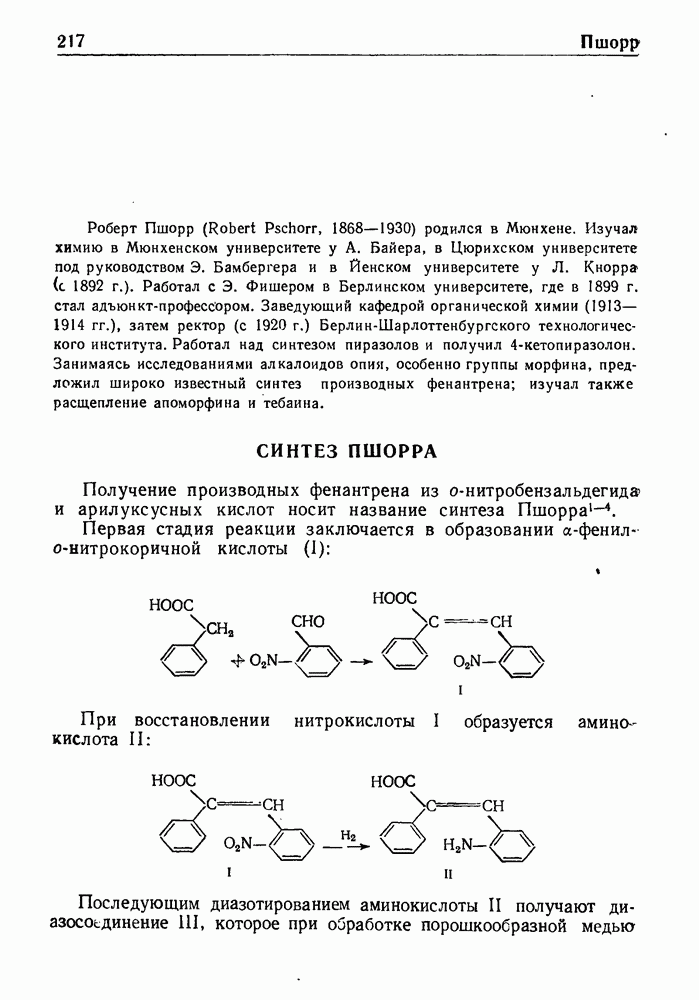
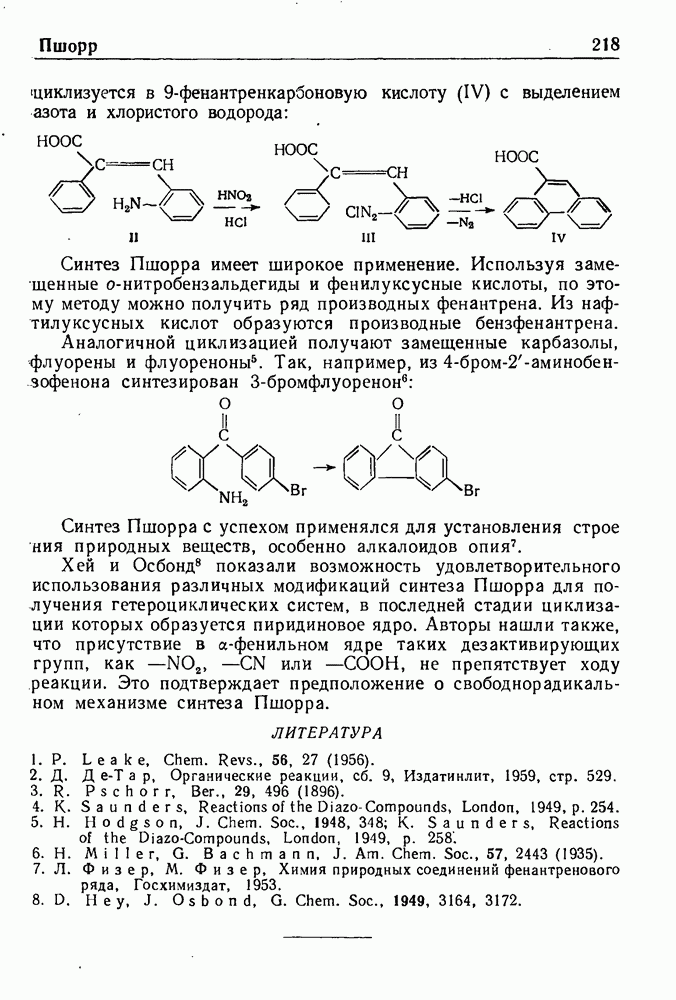
- СИНТЕЗ ПШОРРА
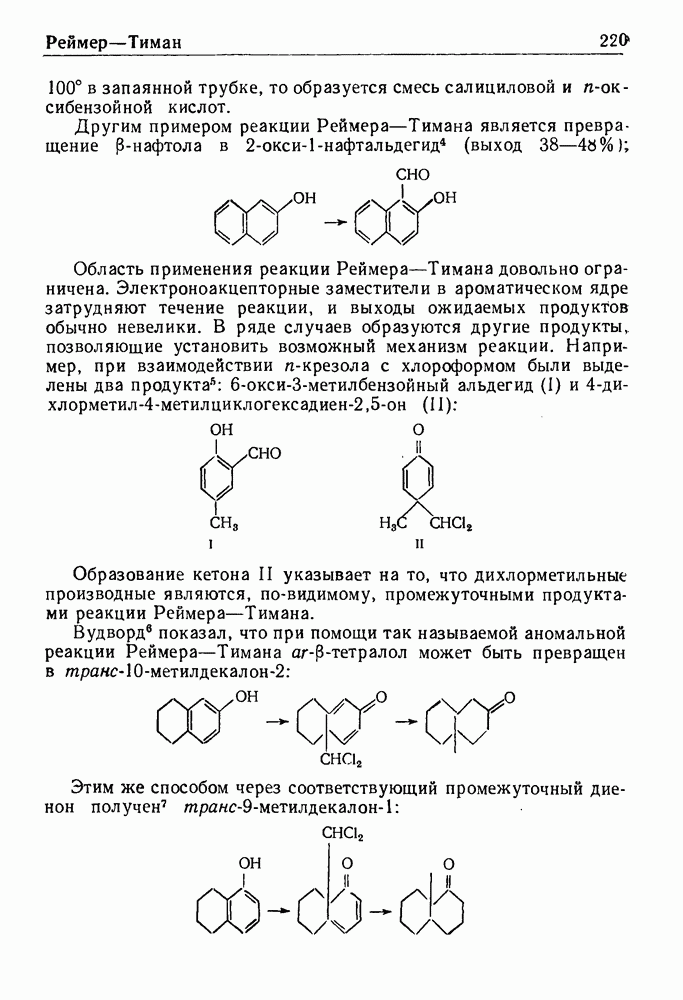
- РЕАКЦИЯ РЕЙМЕРА—ТИМАНА
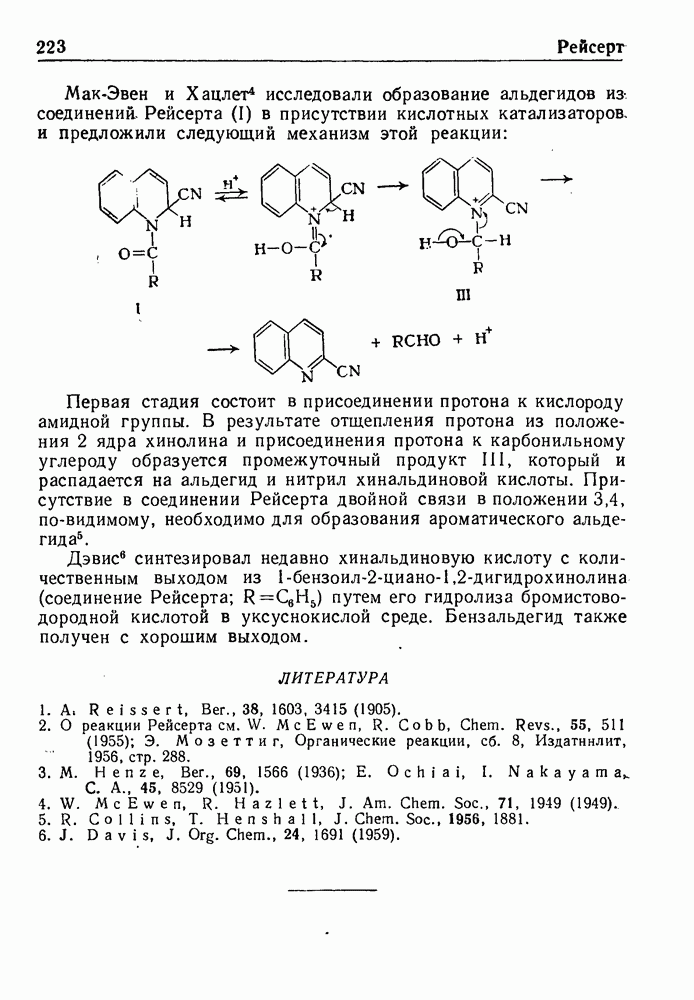
- РЕАКЦИЯ РЕЙСЕРТА
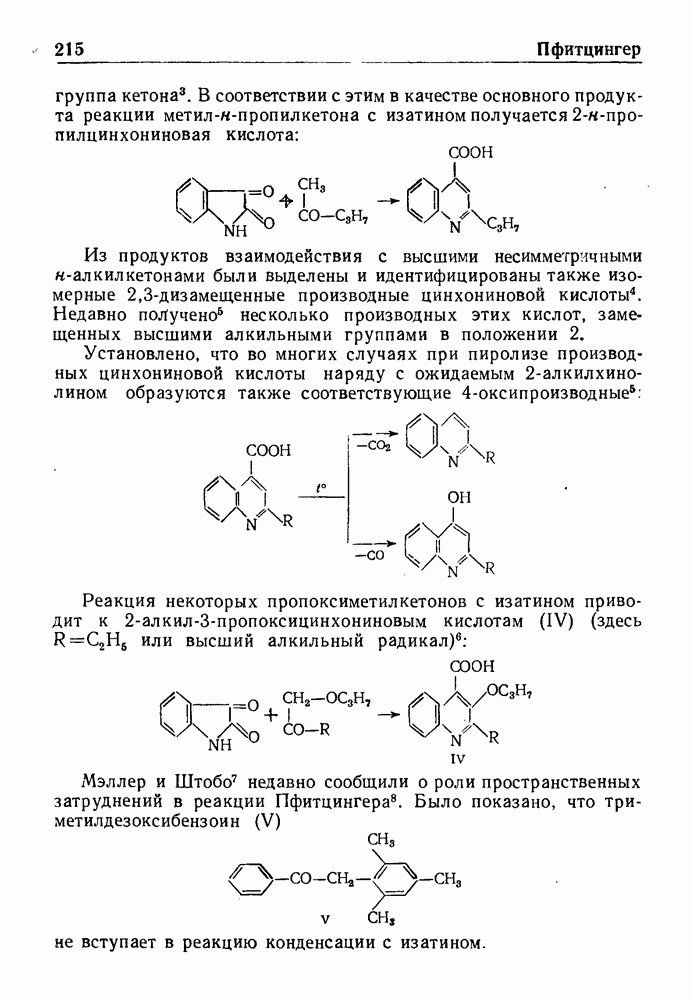
- РЕАКЦИЯ РЕФОРМАТСКОГО
- РЕАКЦИЯ РОДИОНОВА
- ВОССТАНОВЛЕНИЕ ПО РОЗЕНМУНДУ
- РЕАКЦИЯ СКРАУПА
- РЕАКЦИЯ СОММЛЕ
- РЕАКЦИЯ СТЕФЕНА
- ПЕРЕГРУППИРОВКА СТИВЕНСА
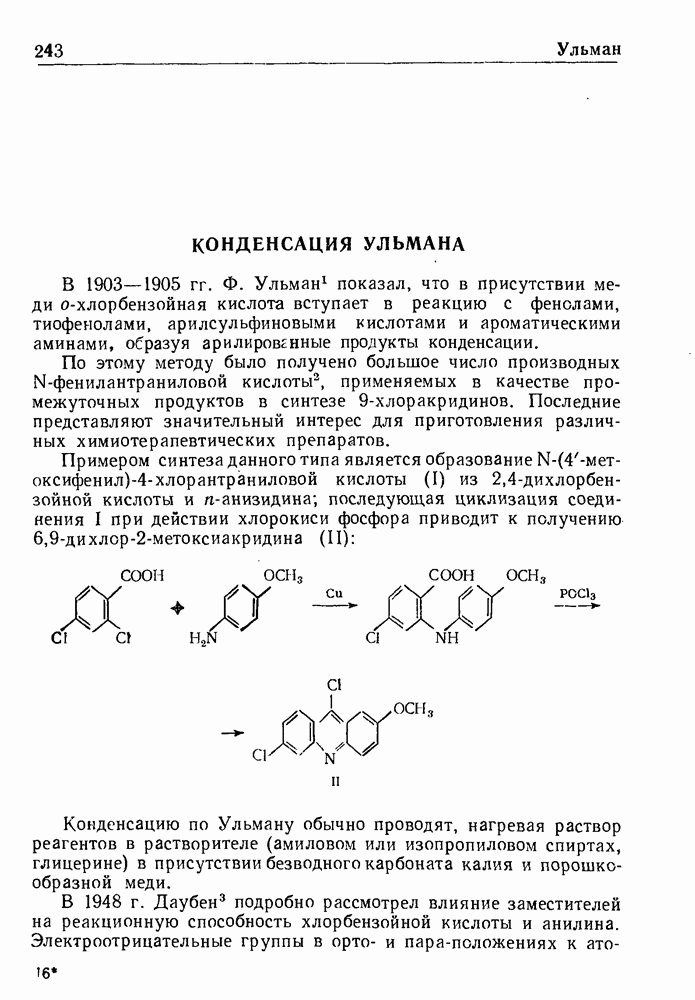
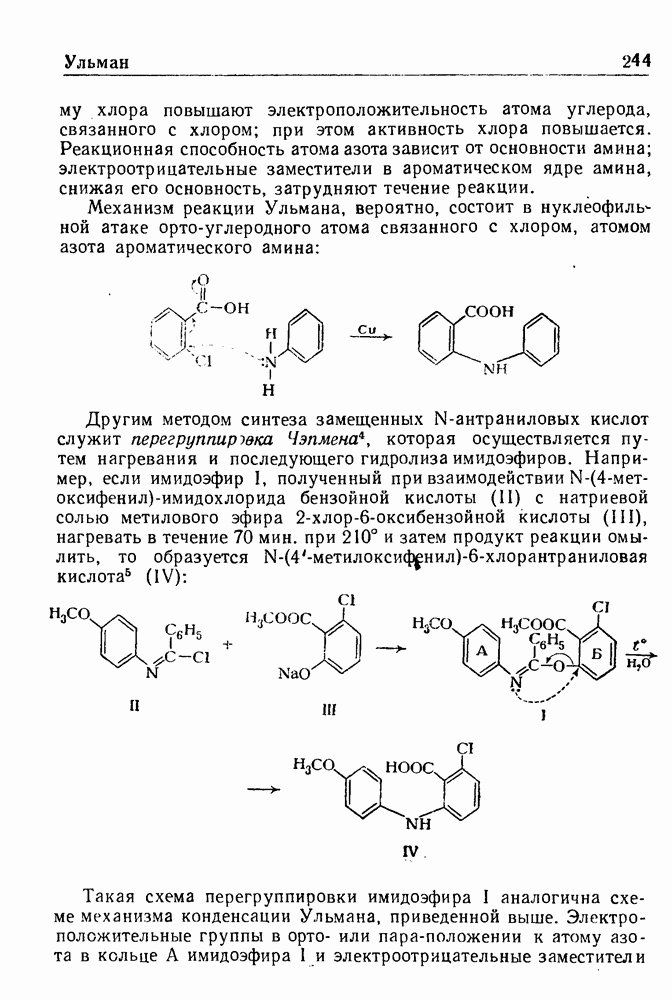
- РЕАКЦИЯ УЛЬМАНА
- КОНДЕНСАЦИЯ УЛЬМАНА
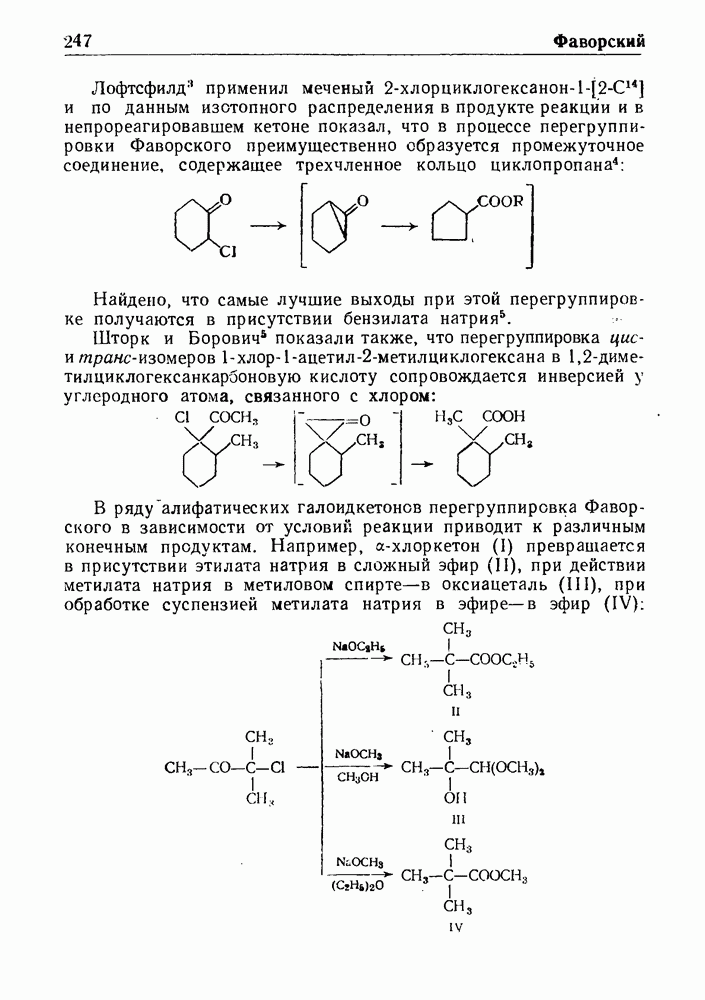
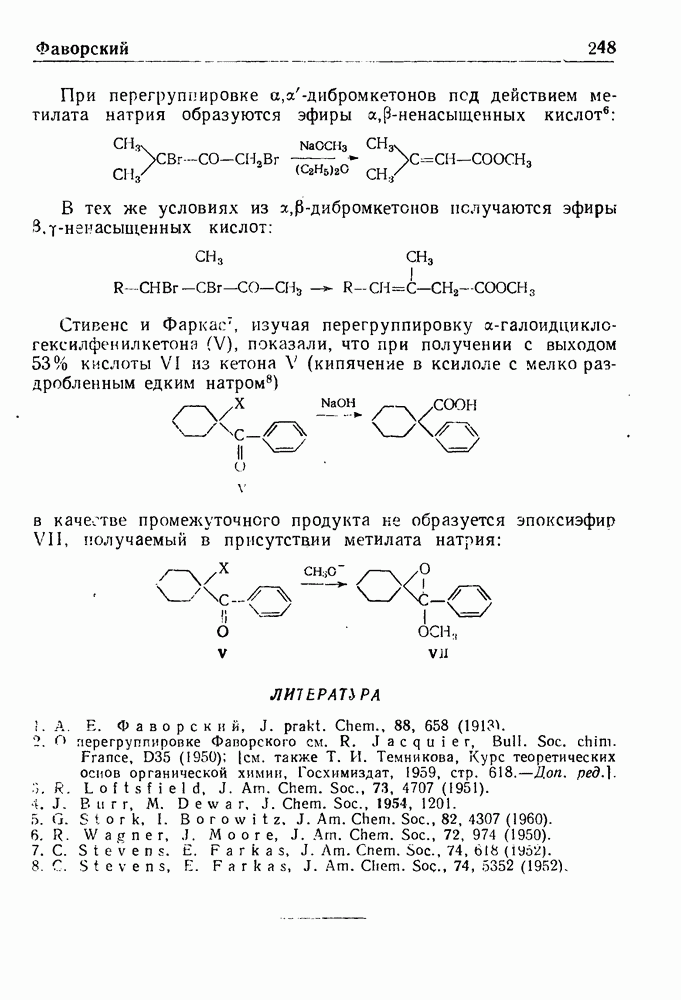
- ПЕРЕГРУППИРОВКА ФАВОРСКОГО
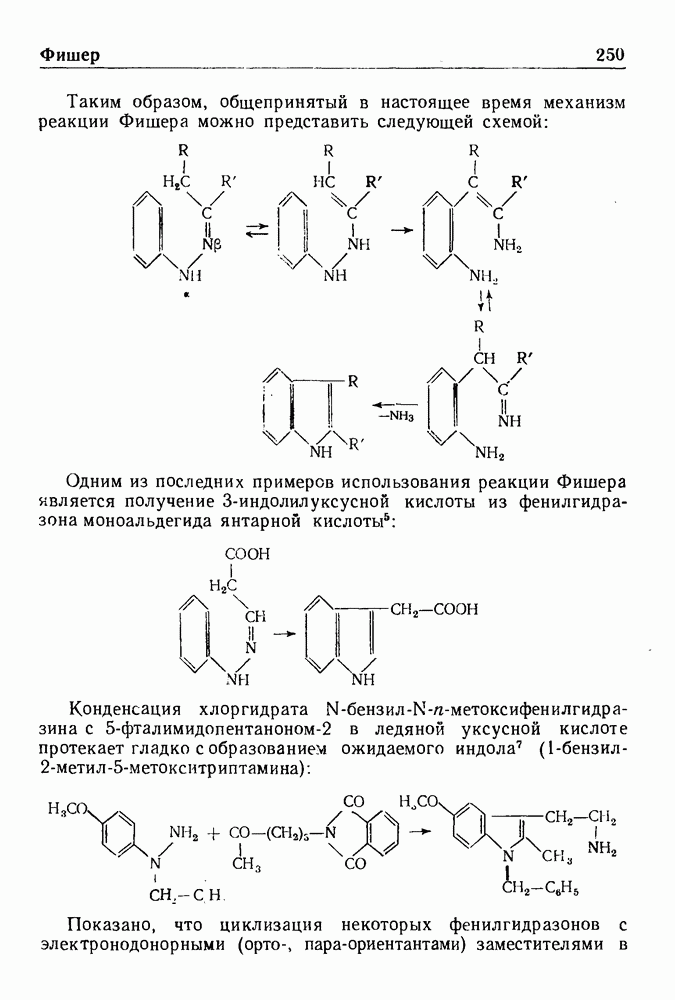
- СИНТЕЗ ИНДОЛА ПО ФИШЕРУ
- РЕАКЦИЯ ФРИДЕЛЯ—КРАФТСА
- СИНТЕЗ ФРИДЛЕНДЕРА
- РЕАКЦИЯ ФРИСА
- РЕАКЦИЯ ХУНСДИККЕРА
- РЕАКЦИЯ ЧИЧИБАБИНА
- РЕАКЦИЯ ЧУГАЕВА
- РЕАКЦИЯ ШИМАНА
- РЕАКЦИИ ШМИДТА
- КОНДЕНСАЦИЯ ШТОББЕ
- РЕАКЦИЯ ШТОРКА
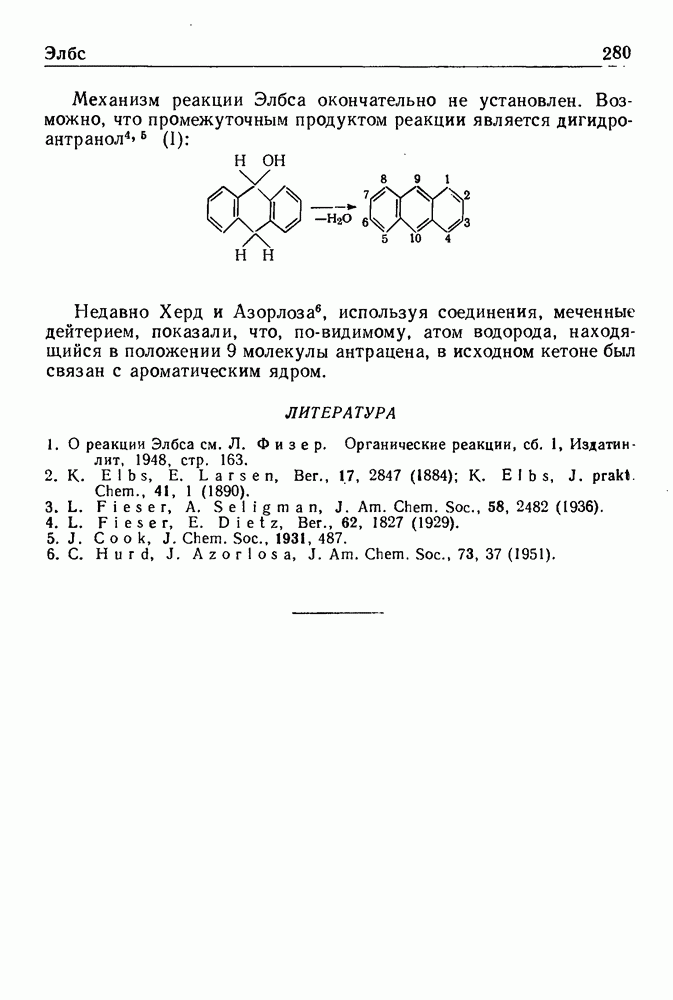
- РЕАКЦИЯ ЭЛБСА
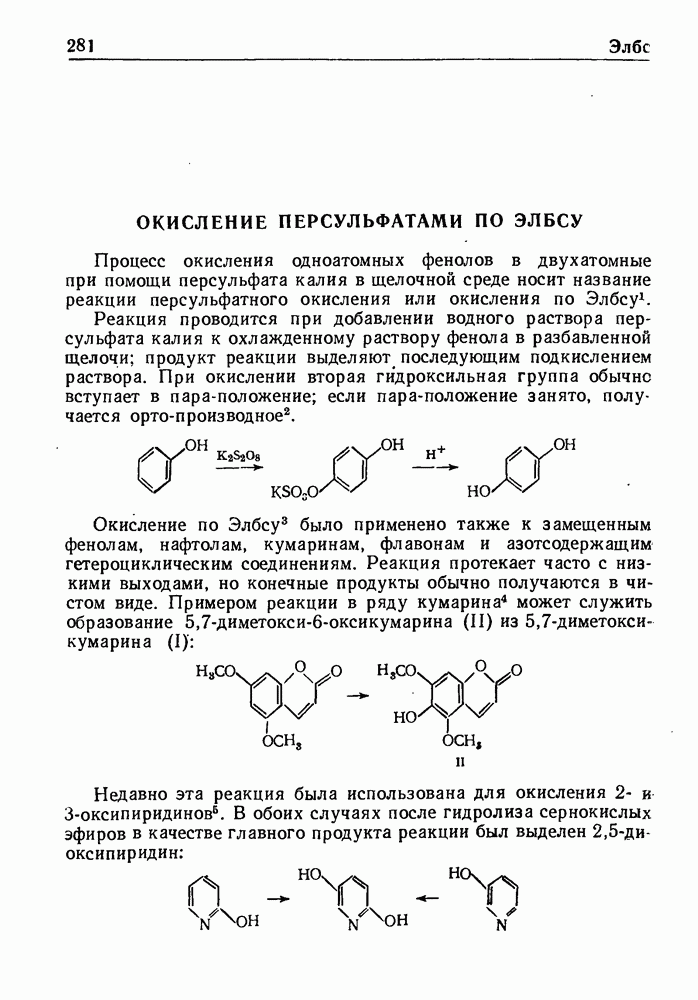
- ОКИСЛЕНИЕ ПЕРСУЛЬФАТАМИ ПО ЭЛБСУ
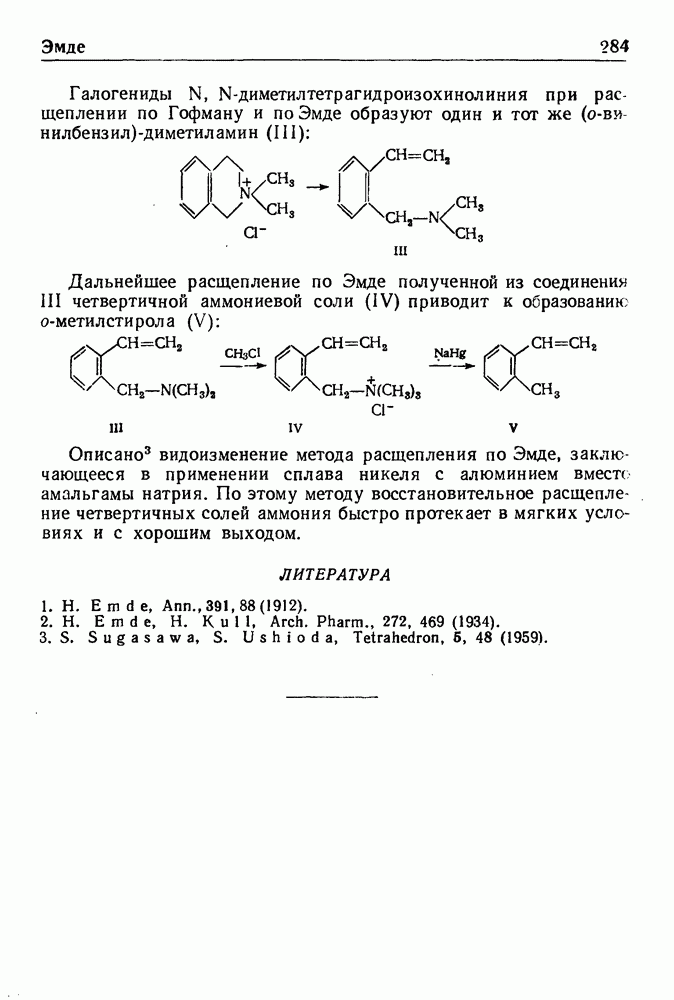
- РАСЩЕПЛЕНИЕ ПО ЭМДЕ
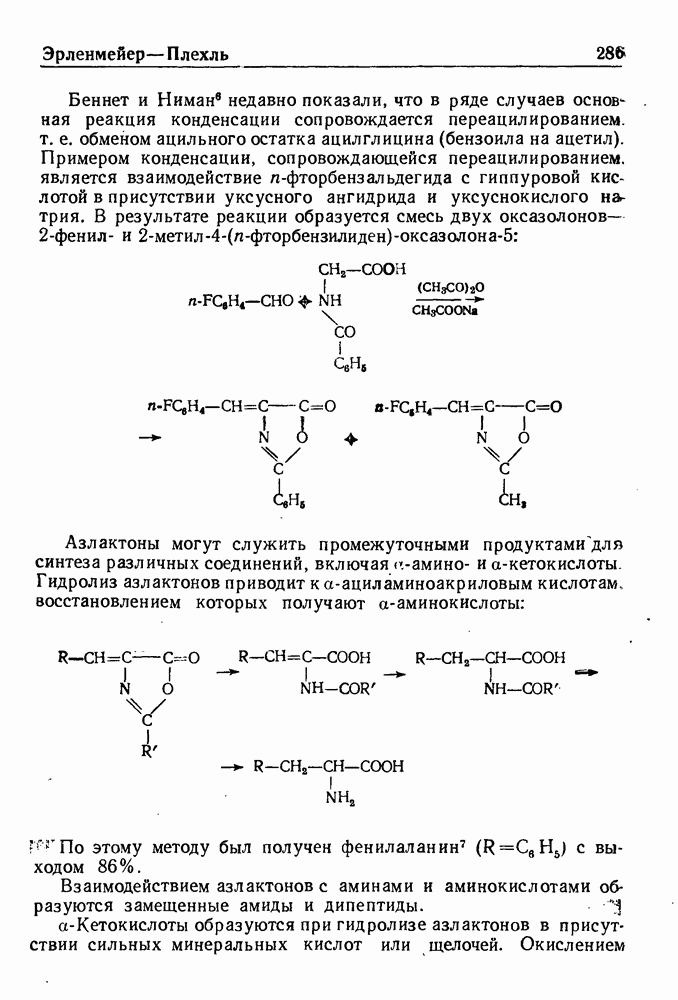
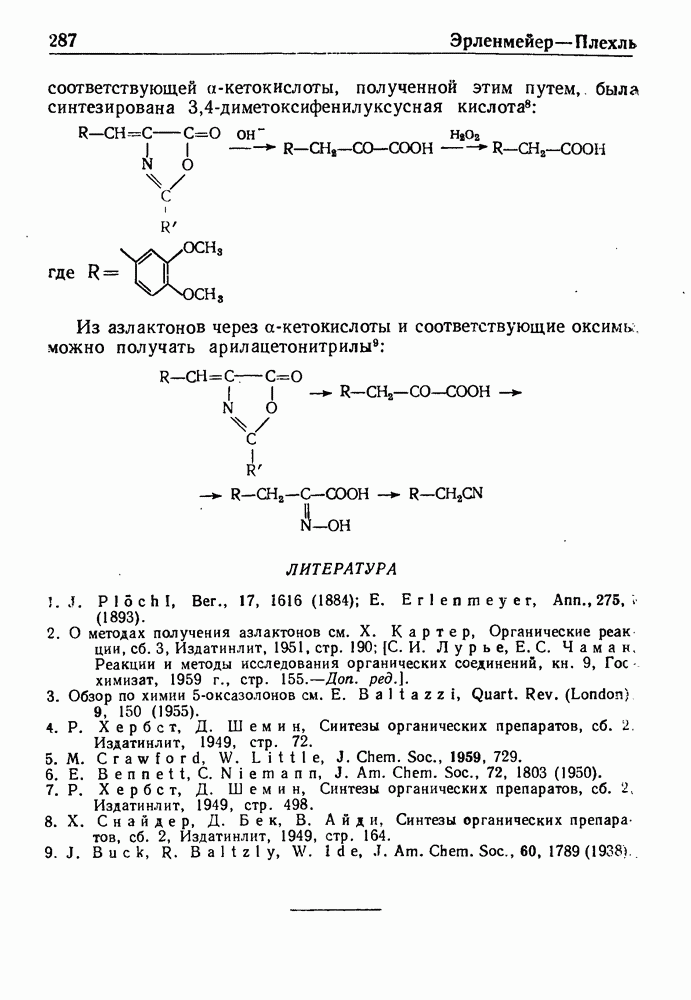
- СИНТЕЗ АЗЛАКТОНОВ ПО ЭРЛЕНМЕИЕРУ—ПЛЕХЛЮ
- РЕАКЦИЯ ЯКОБСЕНА