| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ВОССТАНОВЛЕНИЕ ПО БЕРНУ
А. Дж. Берч (A. J. Birch) родился в 1915 г. в Сиднее (Австралия). Учился а университете в Сиднее, а затем в Оксфордском университете, где под руководством Р. Робинсона в 1938 г. защитил докторскую диссертацию. В 1949 г. получил от Английского королевского общества стипендию Смитсона и приехал в Кембридж, где работал у А. Тодда. В 1952-1957 гг. профессор органической химии в Сиднее, а с 1958 г.—профессор Манчестерского университета. В 1954 г. он был избран членом Академии наук Австралии, а в 1958 г. стал членом Английского королевского общества. Основными направлениями его исследований являются: восстановление с помощью растворов металлов в жидком аммиаке, синтезы аналогов стероидов, биосинтез и установление строения природных соединений.
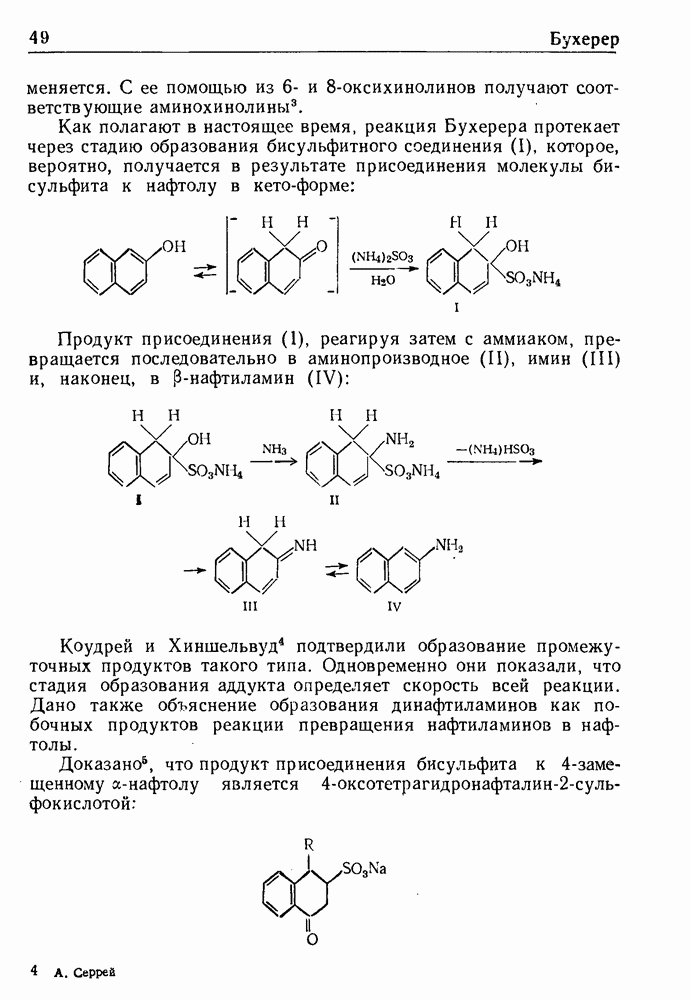
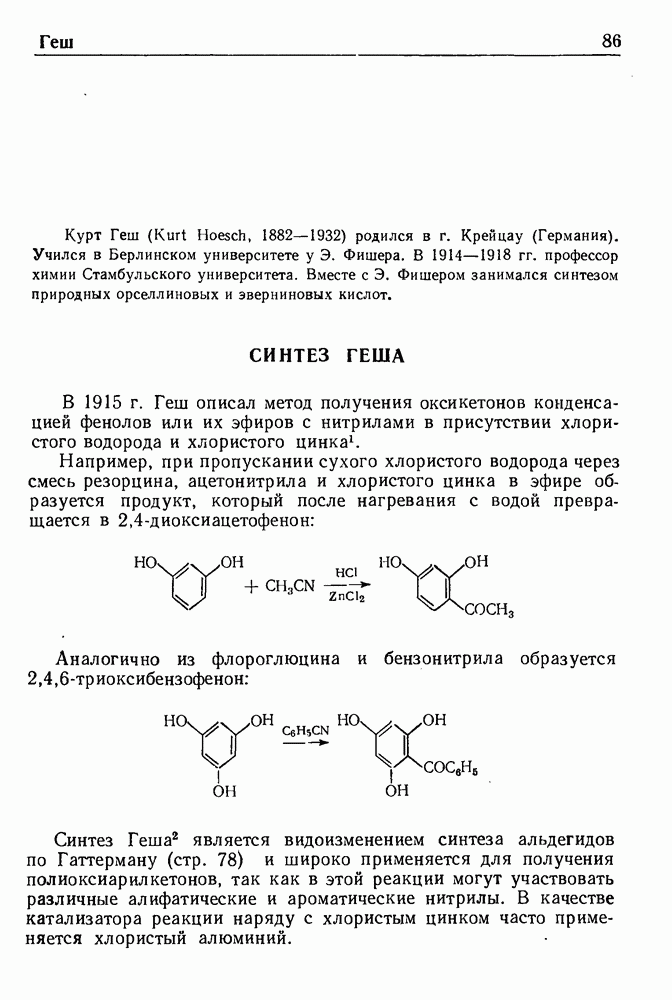
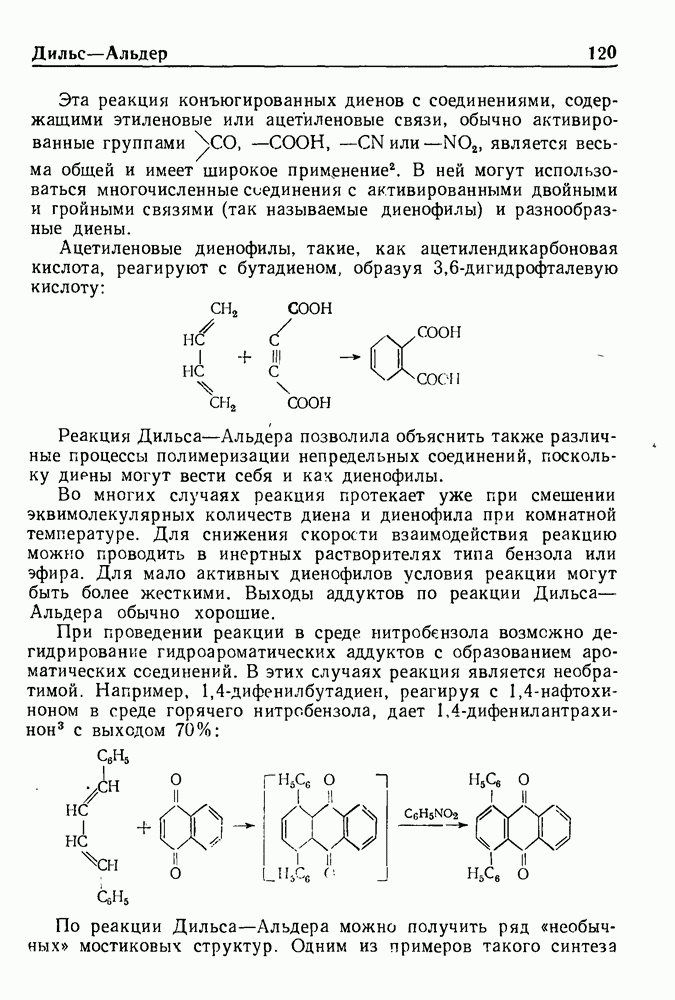
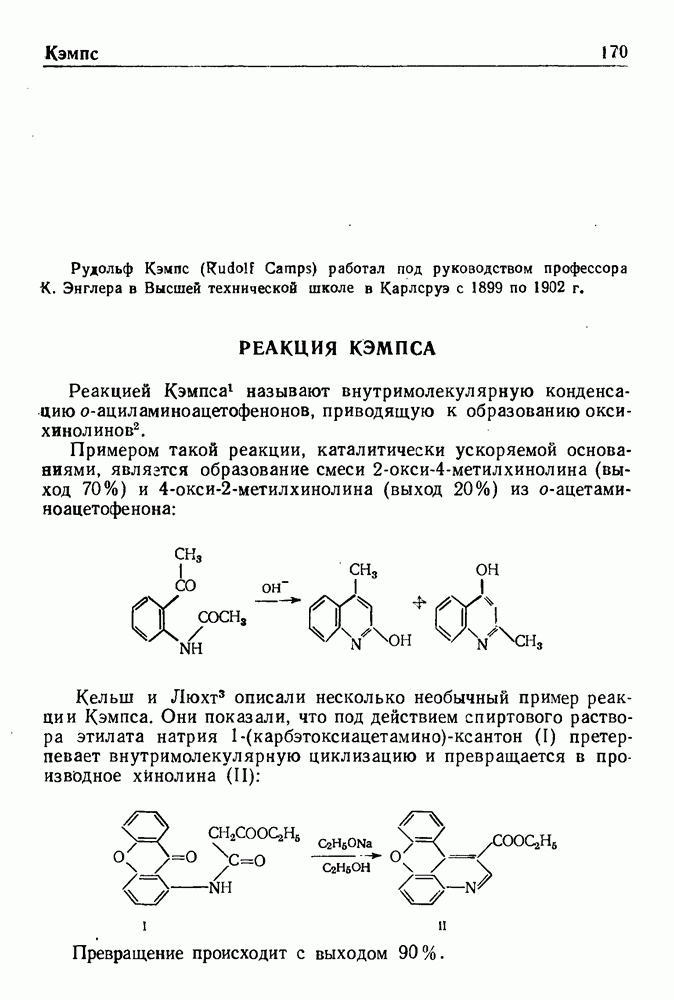
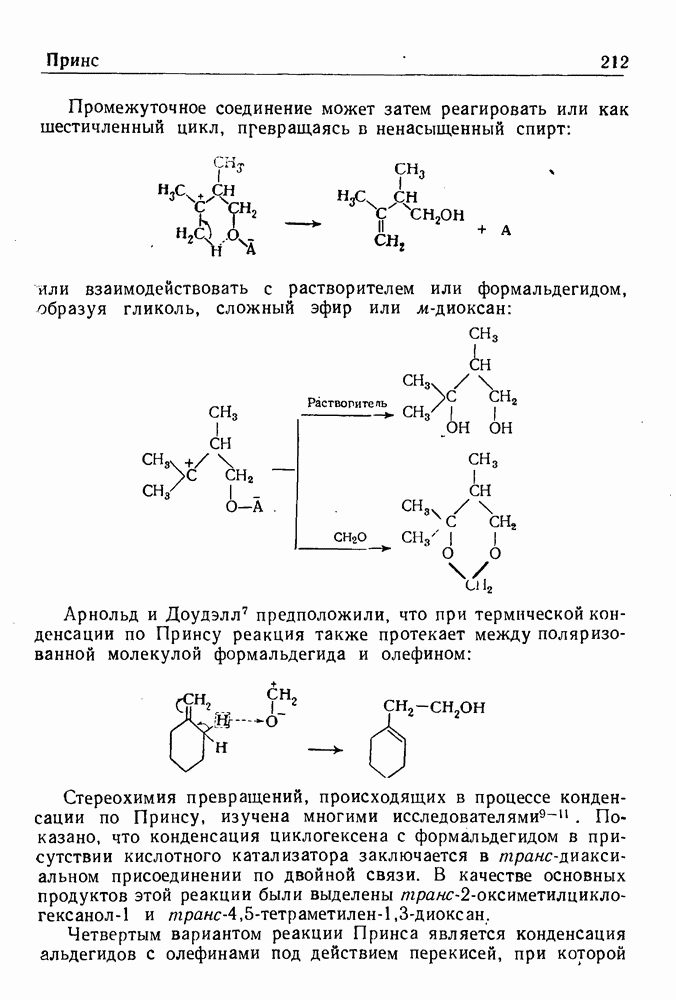
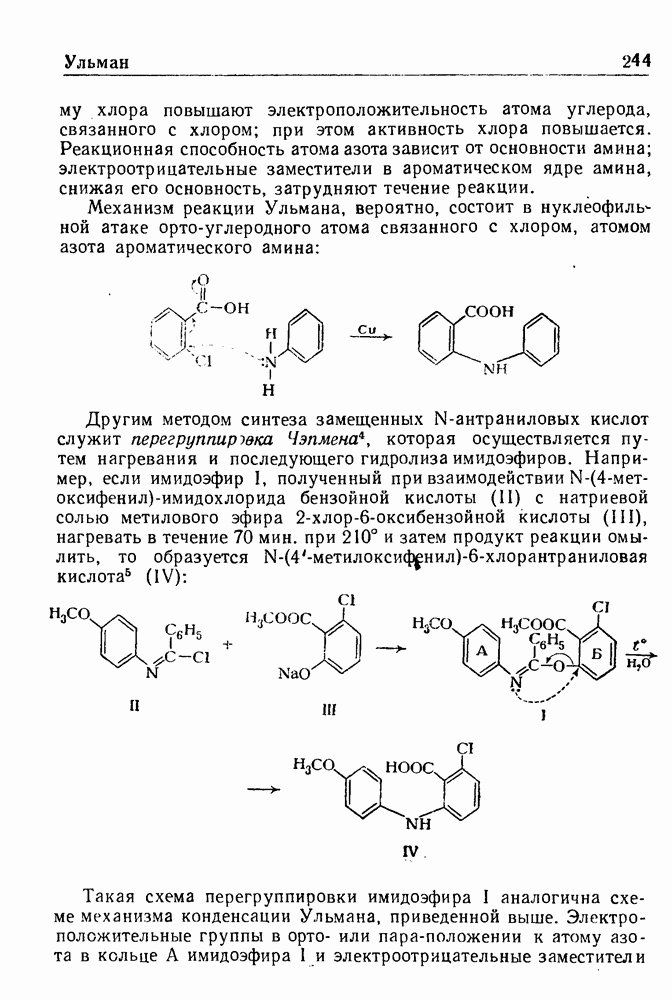
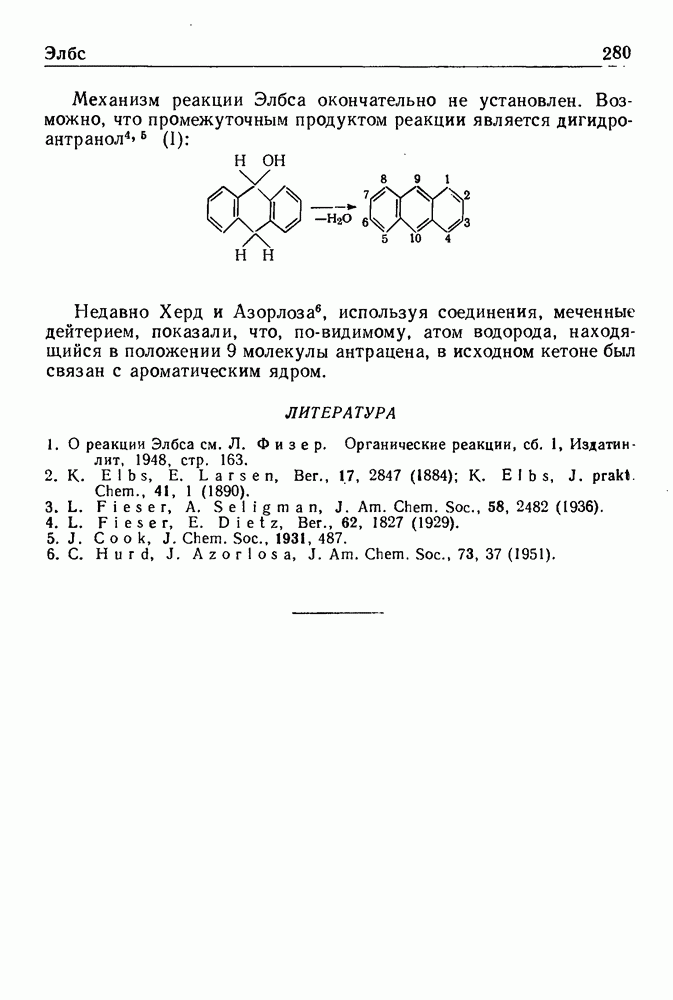
Восстановление ароматических соединений в жидком аммиаке при действии щелочного металла и спирта с образованием на первой стадии циклогексадиенов-1,4 обычно называют восстановлением по Верчу.
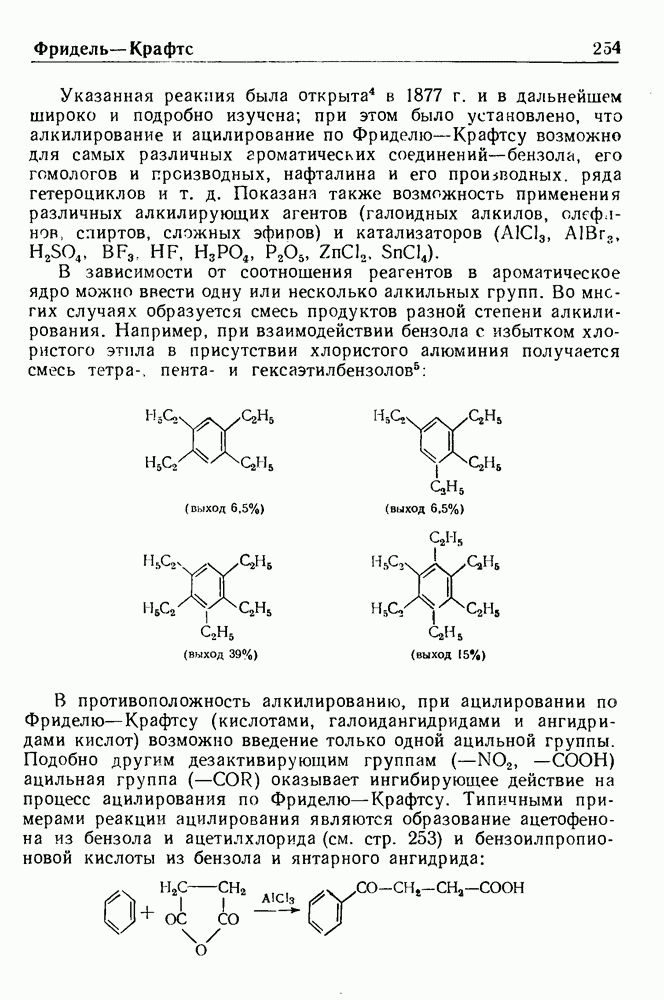
Значение этой реакции, впервые открытой Вустером, а позднее исследованной и развитой Берчем, заключается в широте ее применения и простоте эксперимента, а также в том, что получаемые соединения очень сложно синтезировать другими методами. Восстановлению по Берчу были подвергнуты органические соединения различных классов, включая метоксипроизводные ряда бензола, бензойные кислоты, нафтойные кислоты, нафтолы, гетероциклические соединения, амидины, имидазолы и стероиды.
Эту реакцию обычно проводят, прибавляя металлический натрий к реакционной смеси, состоящей из восстанавливаемого соединения, жидкого аммиака и абсолютного спирта. Для повышения растворимости исходного вещества часто добавляют эфир, тетрагидрофуран или 1,2-диметоксиэтан; иногда, в случае необходимости, спирт приливают последним.
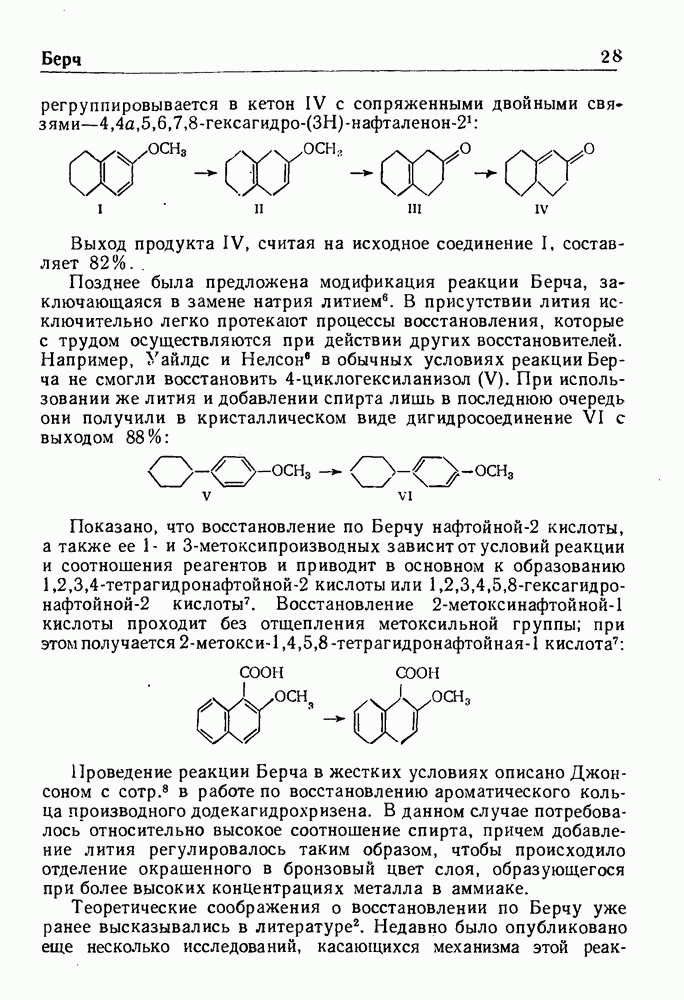
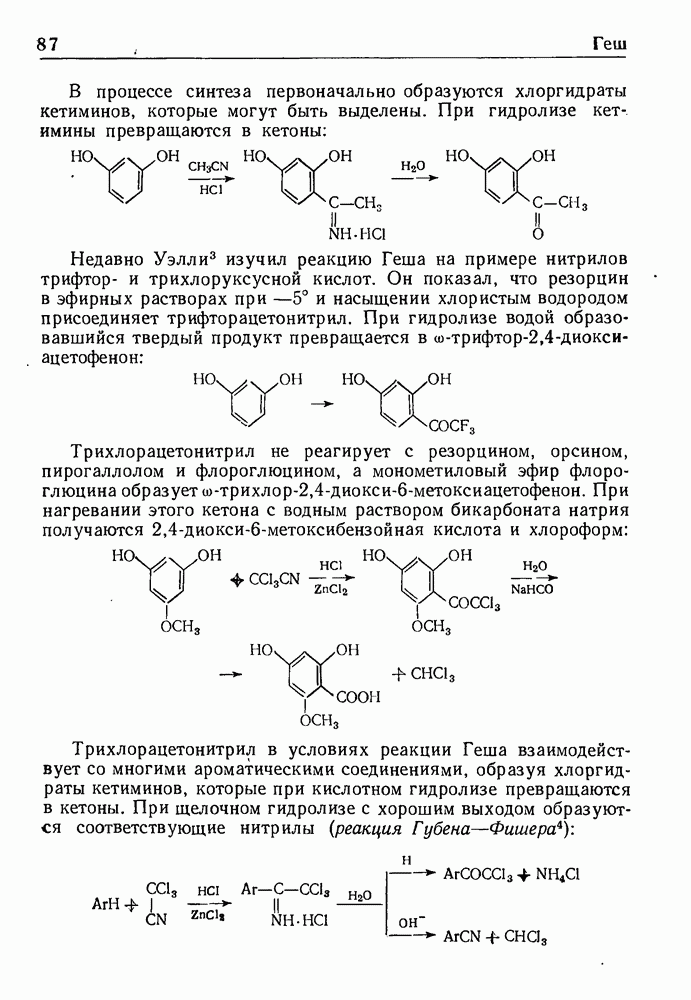
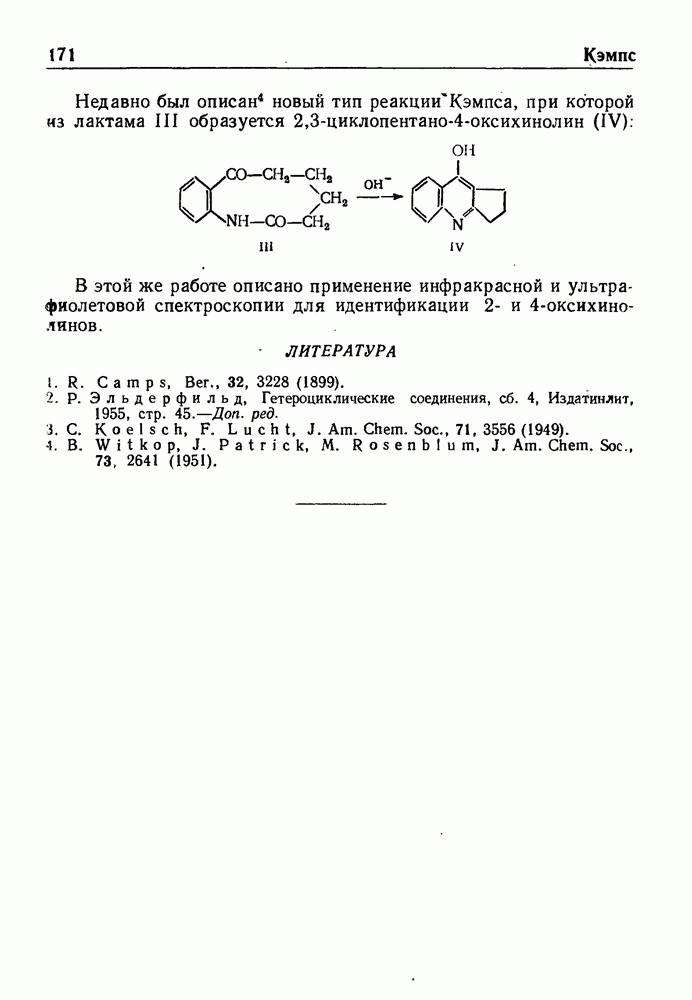
Примером реакции может служить восстановление 2-метокси-5,6,7,8-тетрагидронафталина (I) до эфира енола II, который гидролизуют в мягких условиях и получают кетон III с несопряженными связями; при действии кислот или оснований кетон III
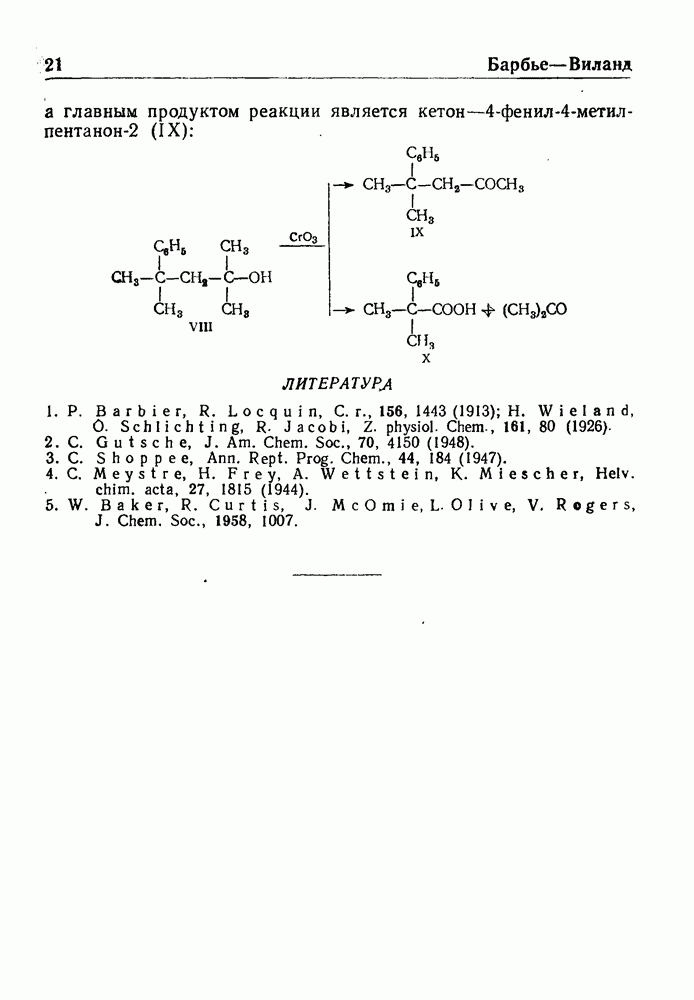
перегруппировывается в кетон IV с сопряженными двойными связями  :
:

Выход продукта IV, считая на исходное соединение I, составляет 82%.
Позднее была предложена модификация реакции Берча, заключающаяся в замене натрия литием. В присутствии лития исключительно легко протекают процессы восстановления, которые с трудом осуществляются при действии других восстановителей. Например, Уайлдс и Нелсон в обычных условиях реакции Берча не смогли восстановить 4-циклогексиланизол (V). При использовании же лития и добавлении спирта лишь в последнюю очередь они получили в кристаллическом виде дигидросоединение VI с выходом 88%:

Показано, что восстановление по Берчу нафтойной-2 кислоты, а также ее 1- и 3-метоксипроизводных зависит от условий реакции и соотношения реагентов и приводит в основном к образованию 1,2,3,4-тетрагидронафтойной-2 кислоты или 1,2,3,4,5,8-гексагидро-нафтойной-2 кислоты. Восстановление 2-метоксинафтойной-1 кислоты проходит без отщепления метоксильной группы; при этом получается 2-метокси-1,4,5,8-тетрагидронафтойная-1 кислота:

Проведение реакции Берча в жестких условиях описано Джонсоном с сотр. в работе по восстановлению ароматического кольца производного додекагидрохризена. В данном случае потребовалось относительно высокое соотношение спирта, причем добавление лития регулировалось таким образом, чтобы происходило отделение окрашенного в бронзовый цвет слоя, образующегося при более высоких концентрациях металла в аммиаке.
Теоретические соображения о восстановлении по Берчу уже ранее высказывались в литературе. Недавно было опубликовано еще несколько исследований, касающихся механизма этой
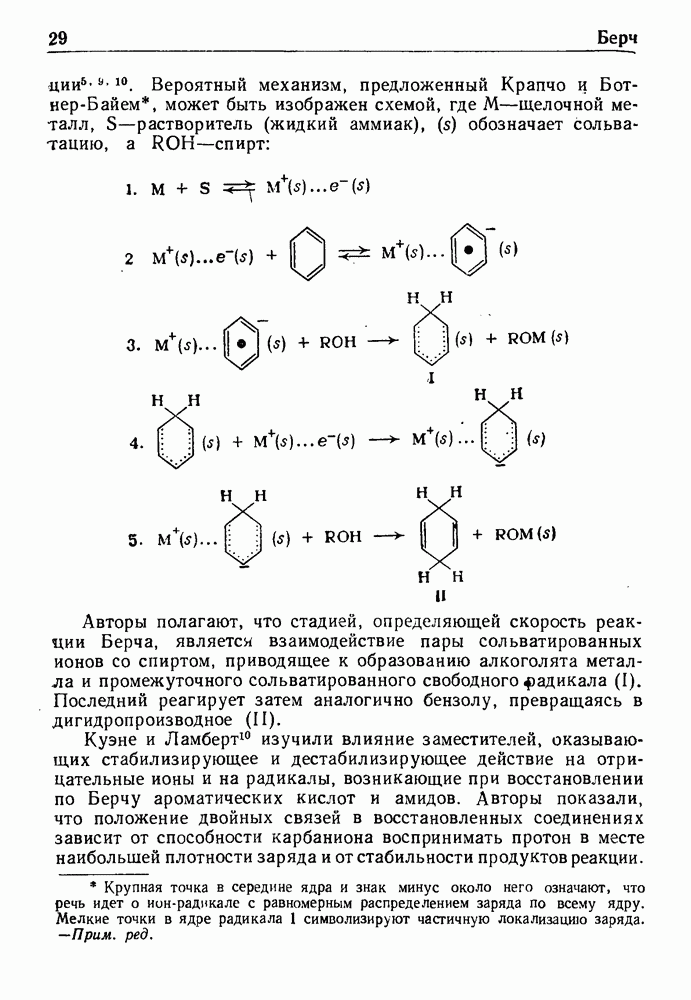
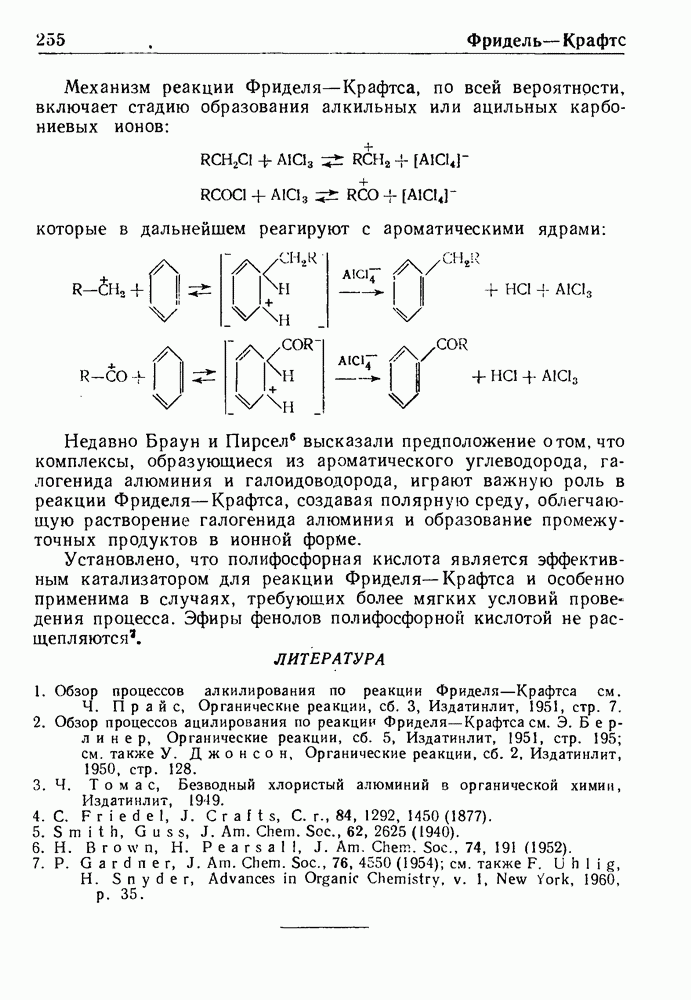
реакции. Вероятный механизм, предложенный Крапчо и Ботнер-Байем, может быть изображен схемой, где  —щелочной металл,
—щелочной металл,  -растворитель (жидкий аммиак), (5) обозначает сольватацию,
-растворитель (жидкий аммиак), (5) обозначает сольватацию, 

Авторы полагают, что стадией, определяющей скорость реакции Берча, является взаимодействие пары сольватированных ионов со спиртом, приводящее к образованию алкоголята металла и промежуточного сольватированного свободного радикала (I). Последний реагирует затем аналогично бензолу, превращаясь в дигидропроизводное (II).
Куэне и Ламберт изучили влияние заместителей, оказывающих стабилизирующее и дестабилизирующее действие на отрицательные ионы и на радикалы, возникающие при восстановлении по Берчу ароматических кислот и амидов. Авторы показали, что положение двойных связей в восстановленных соединениях зависит от способности карбаниона воспринимать протон в месте наибольшей плотности заряда и от стабильности продуктов реакции.
ЛИТЕРАТУРА
(см. скан)
| << Предыдущий параграф | Следующий параграф >> |
- ОТ РЕДАКТОРА
- ПЕРЕГРУППИРОВКА АРБУЗОВА
- СИНТЕЗ АРНДТА—ЭЙСТЕРТА
- ОКИСЛЕНИЕ ПО БАЙЕРУ—ВИЛЛИГЕРУ
- РАСЩЕПЛЕНИЕ ПО БАРБЬЕ—ВИЛАНДУ
- РЕАКЦИЯ БАРТА
- ПЕРЕГРУППИРОВКА БЕКМАНА
- ВОССТАНОВЛЕНИЕ ПО БЕРНУ
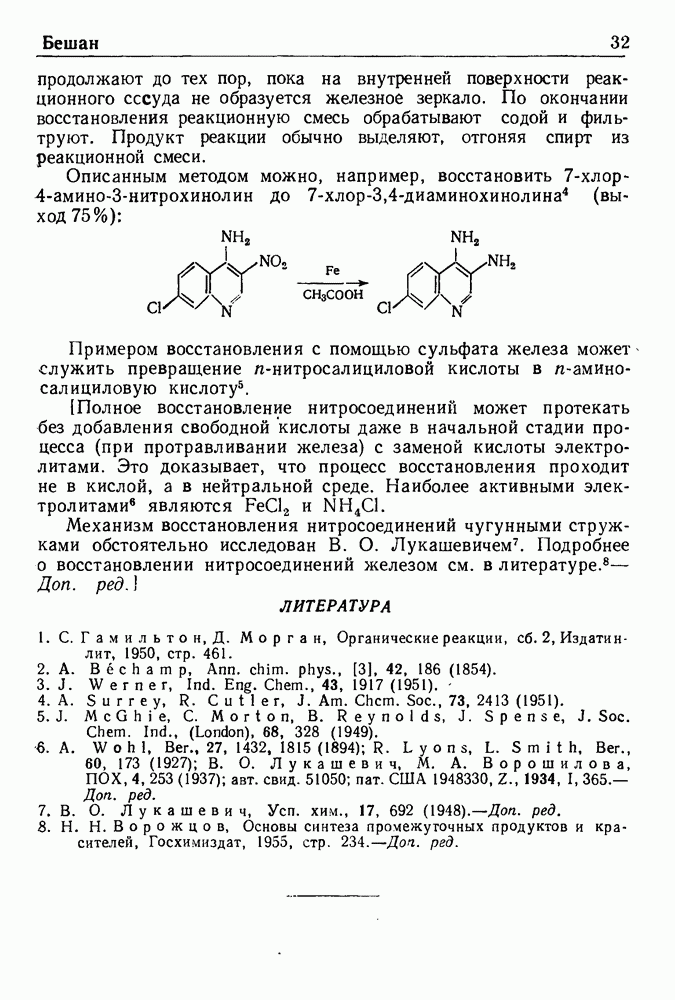
- ВОССТАНОВЛЕНИЕ ПО БЕШАНУ
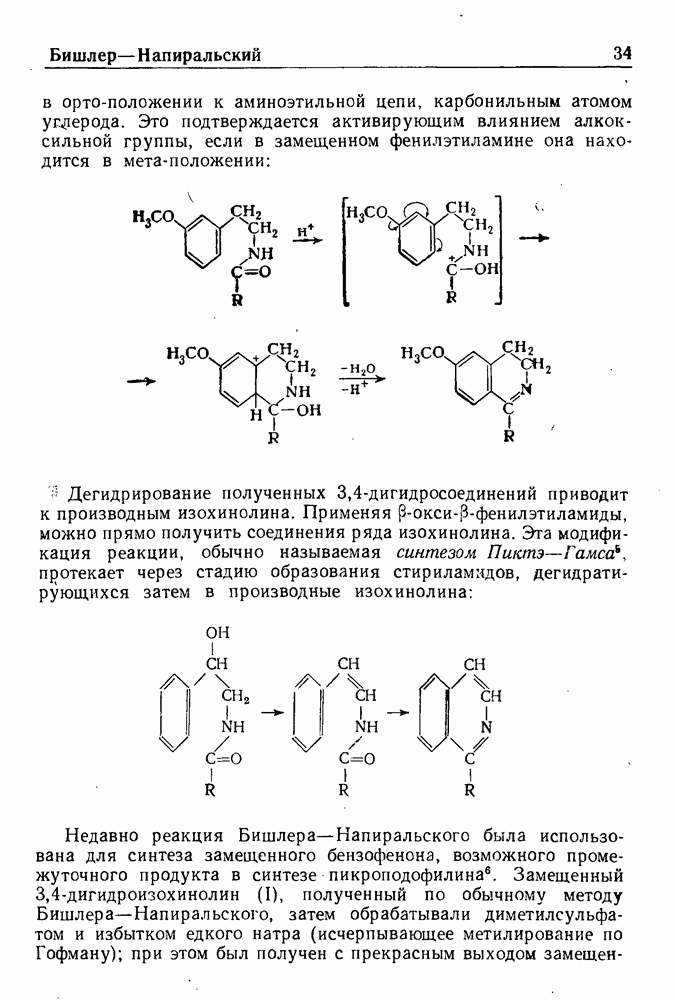
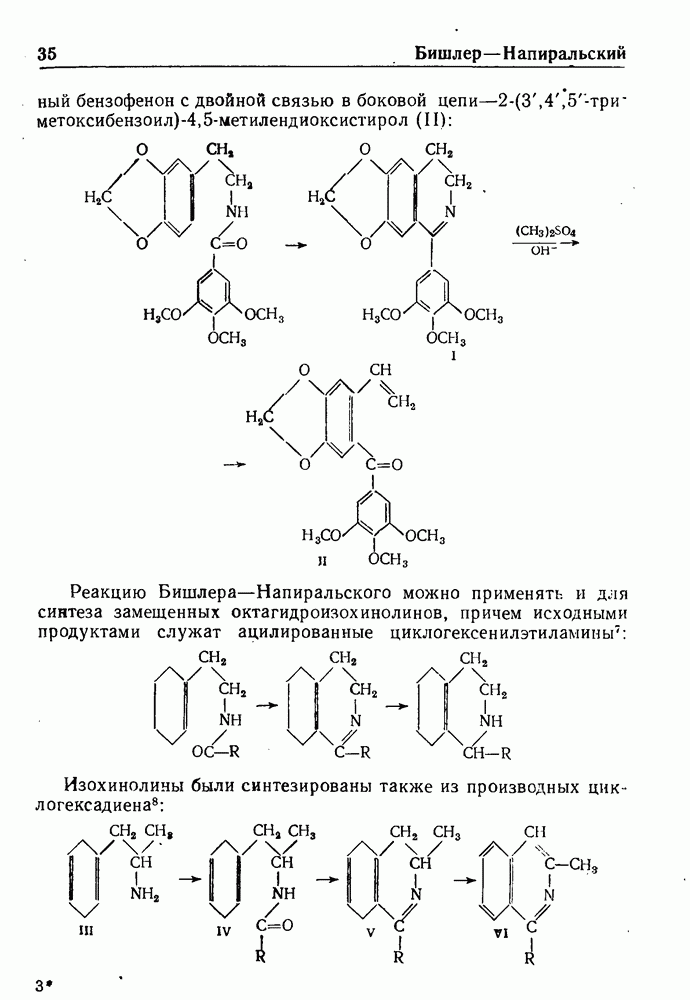
- РЕАКЦИЯ БИШЛЕРА—НАПИРАЛЬСКОГО
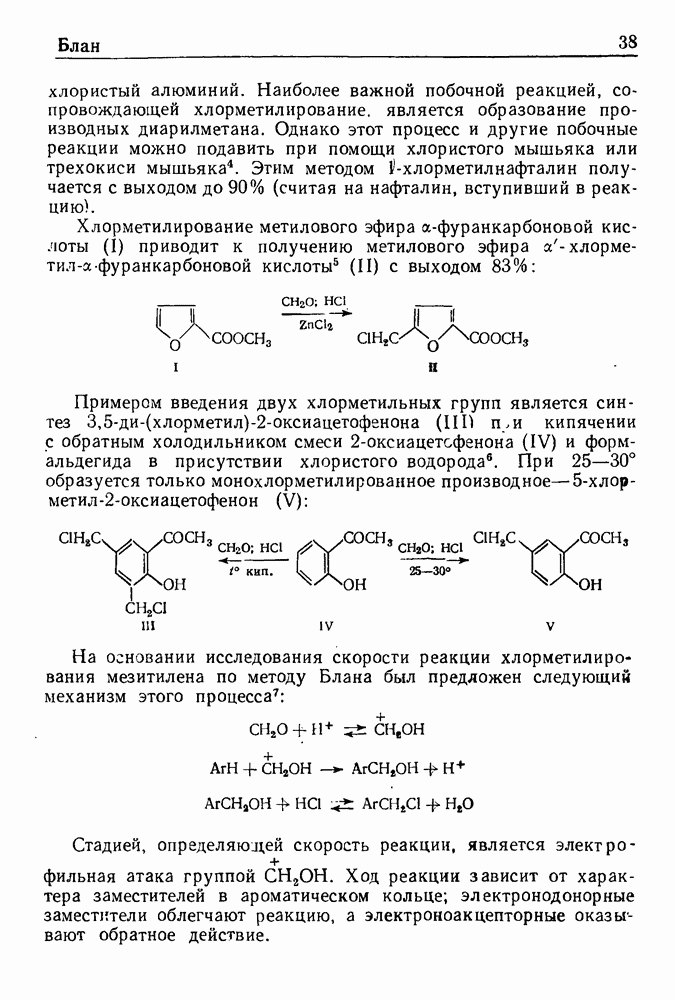
- ХЛОРМЕТИЛИРОВАНИЕ ПО БЛАНУ
- РЕАКЦИЯ БРАУНА
- РАСЩЕПЛЕНИЕ АМИНОВ ПО БРАУНУ
- ВОССТАНОВЛЕНИЕ ПО БУВО—БЛАНУ
- СИНТЕЗ АЛЬДЕГИДОВ ПО БУВО
- РЕАКЦИЯ БУХЕРЕРА
- СИНТЕЗ ГИДАНТОИНОВ ПО БУХЕРЕРУ
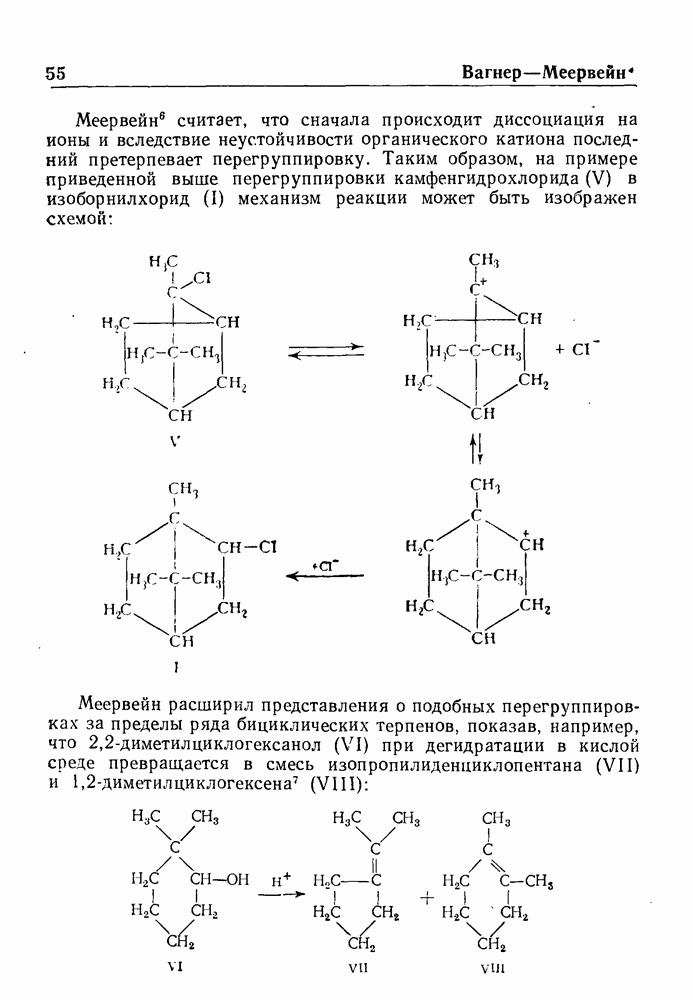
- ПЕРЕГРУППИРОВКА ВАГНЕРА—МЕЕРВЕЙНА
- РЕАКЦИЯ ВАЛЛАХА
- РЕАКЦИЯ ВИЛЬГЕРОДТА
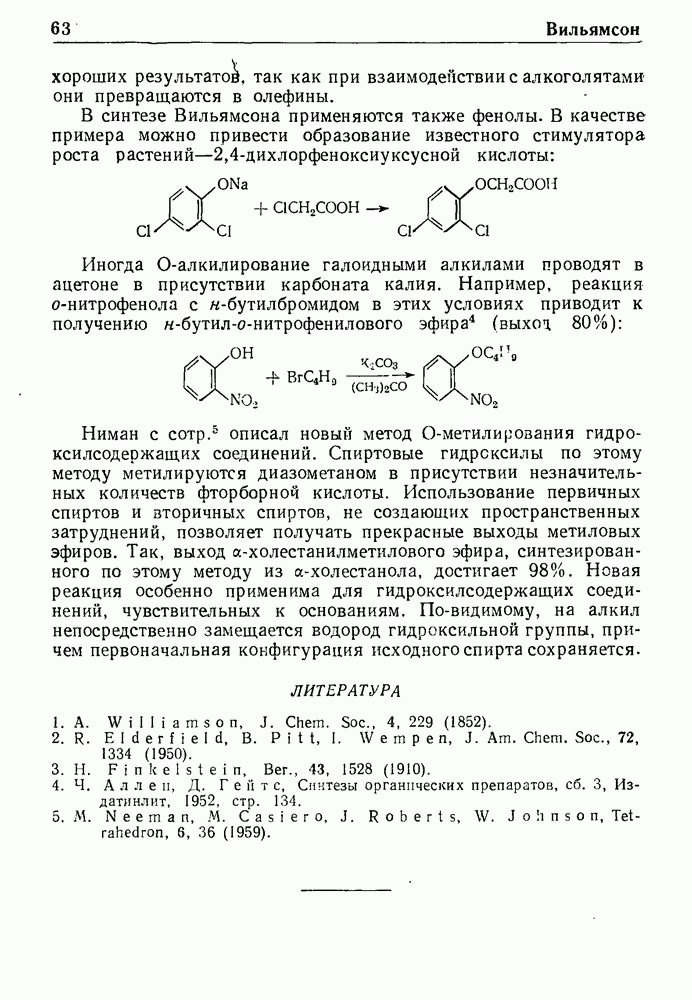
- СИНТЕЗ ВИЛЬЯМСОНА
- РЕАКЦИЯ ВИТТИГА
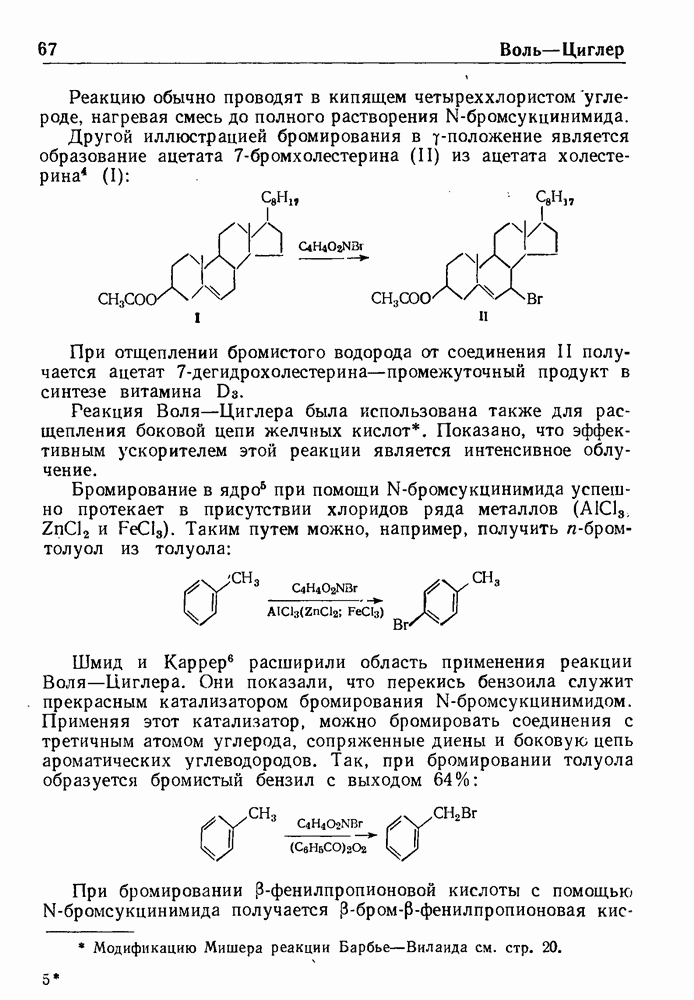
- РЕАКЦИЯ ВОЛЯ-ЦИГЛЕРА
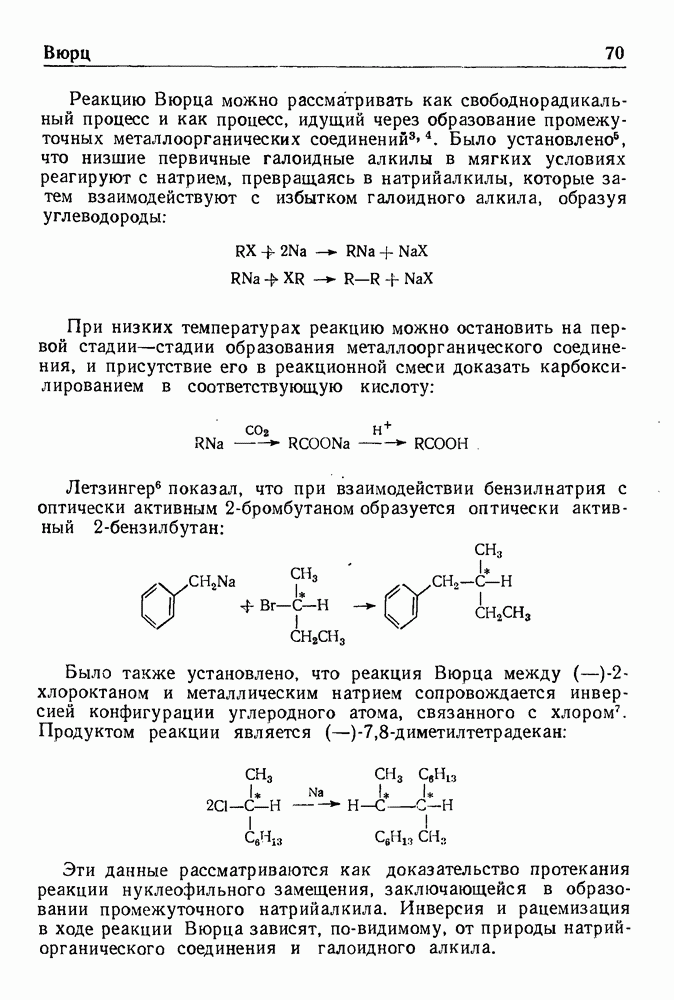
- РЕАКЦИЯ ВЮРЦА
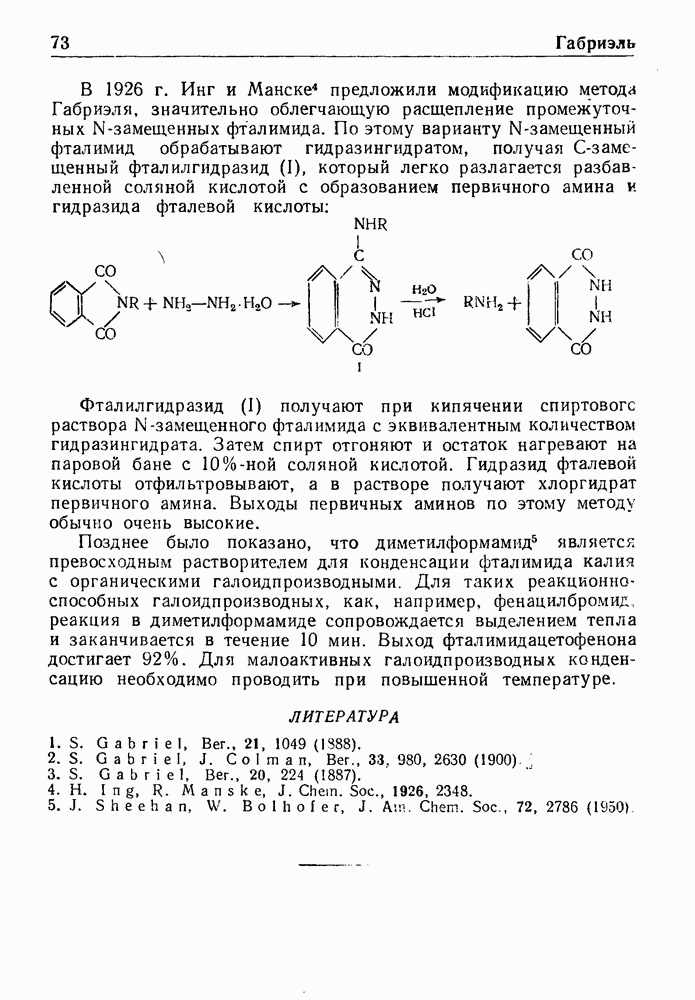
- СИНТЕЗ ГАБРИЭЛЯ
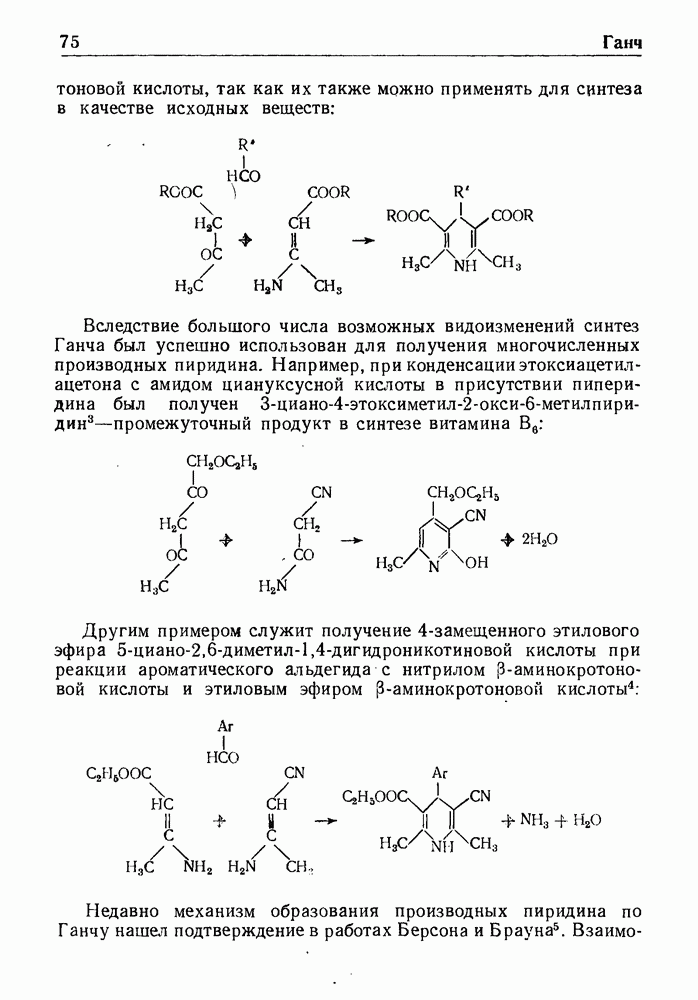
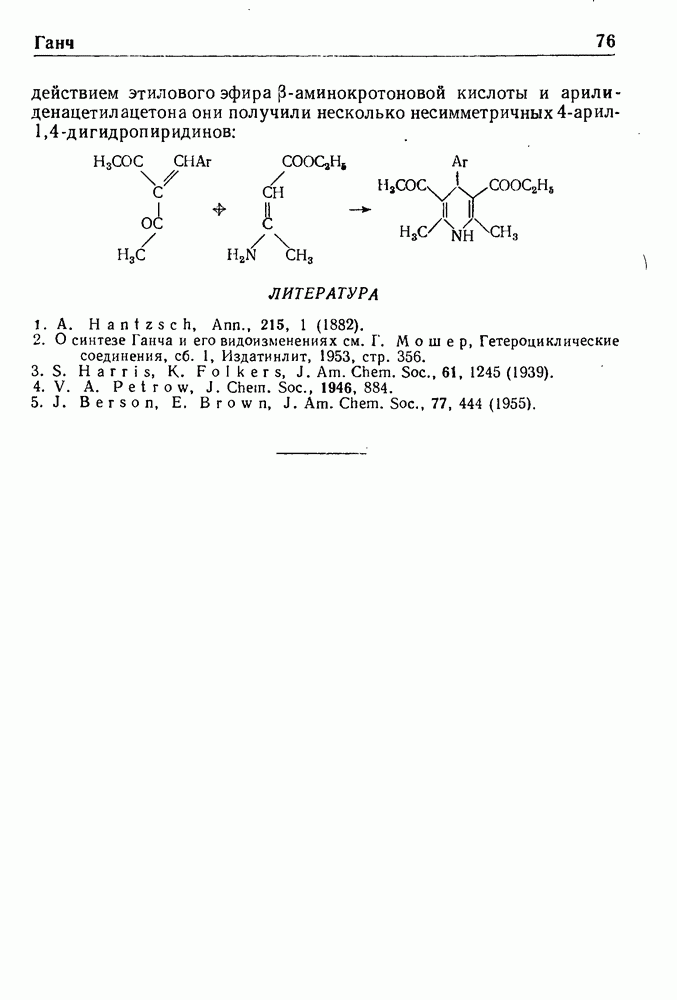
- СИНТЕЗ ГАНЧА
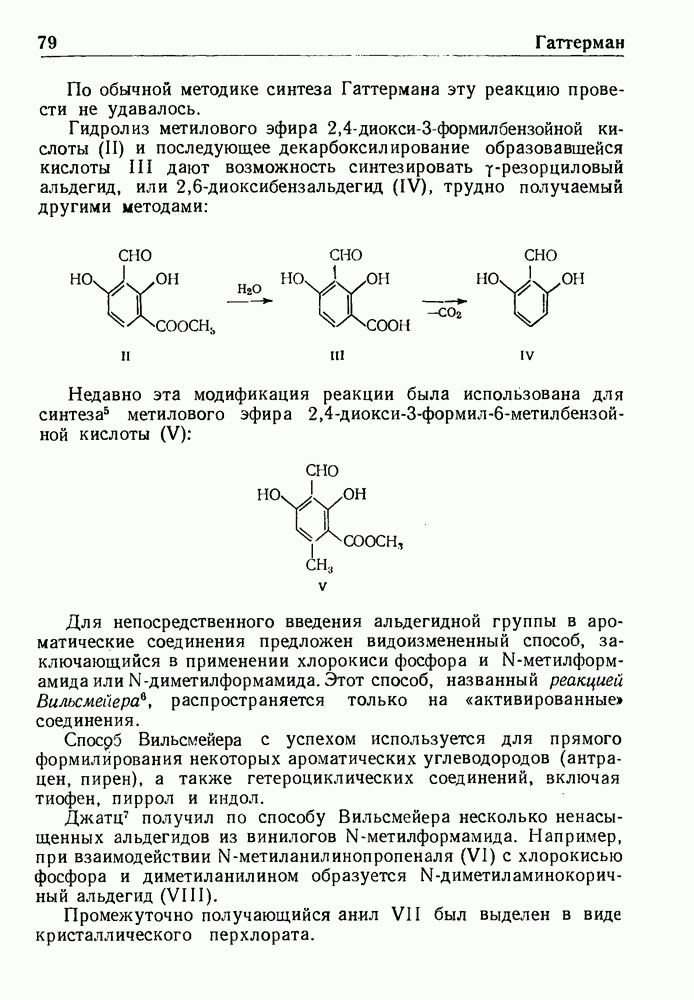
- РЕАКЦИЯ ГАТТЕРМАНА
- СИНТЕЗ АЛЬДЕГИДОВ ПО ГАТТЕРМАНУ
- РЕАКЦИЯ ГАТТЕРМАНА—КОХА
- РЕАКЦИЯ ГЕЛЛЯ—ФОЛЬГАРДА—ЗЕЛИНСКОГО
- СИНТЕЗ ГЕША
- РЕАКЦИЯ ГОМБЕРГА—БАХМАНА—ХЕЯ
- РЕАКЦИЯ ГОУЛДА—ДЖЕКОБСА
- ПЕРЕГРУППИРОВКА ГОФМАНА
- РАСЩЕПЛЕНИЕ ПО ГОФМАНУ
- СИНТЕЗ ГРЕБЕ—УЛЬМАНА
- РЕАКЦИЯ ГРИНЬЯРА
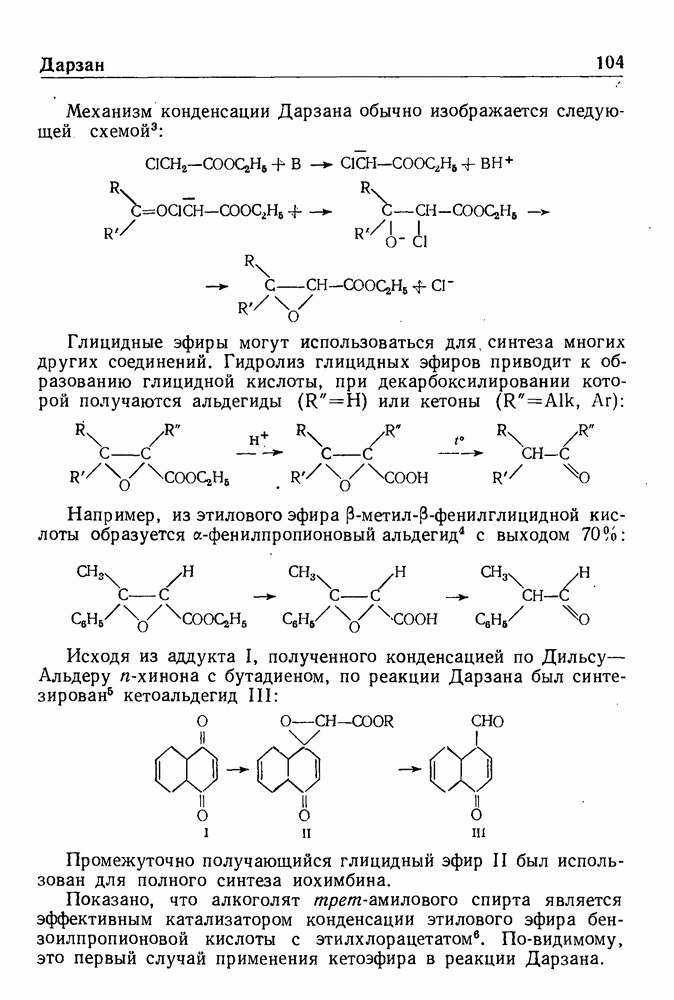
- СИНТЕЗ ГЛИЦИДНЫХ ЭФИРОВ ПО ДАРЗАНУ
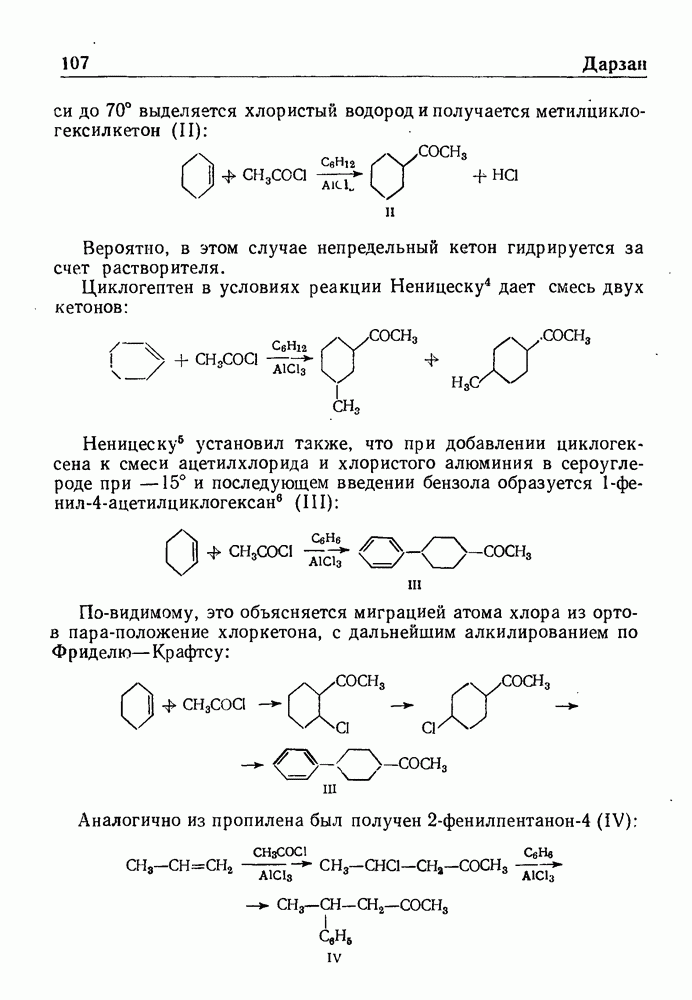
- СИНТЕЗ НЕПРЕДЕЛЬНЫХ КЕТОНОВ ПО ДАРЗАНУ
- РЕАКЦИЯ ДАФФА
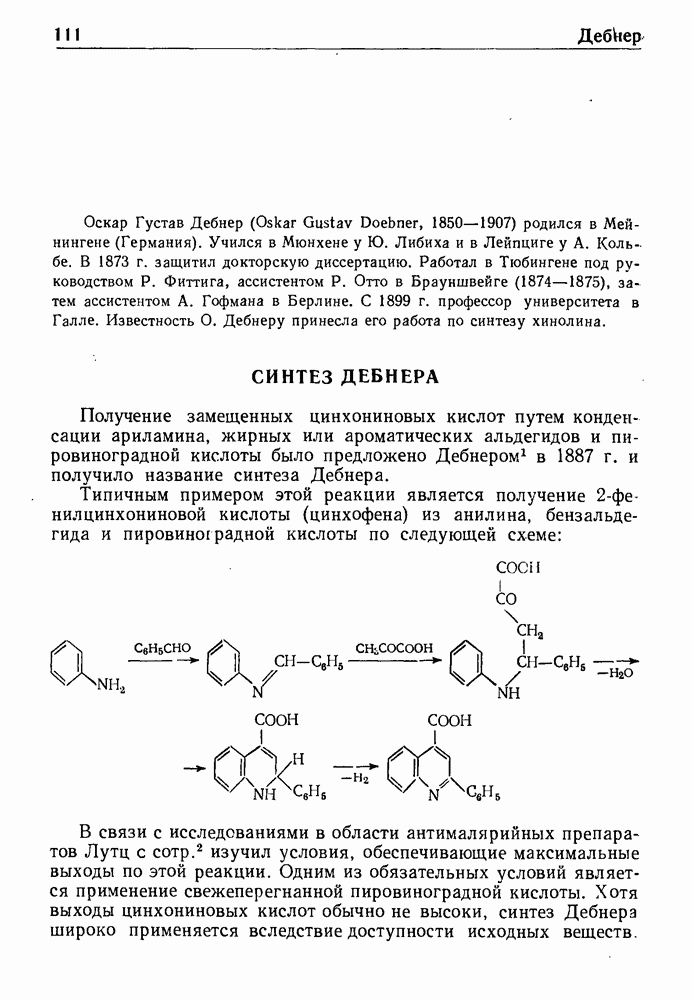
- СИНТЕЗ ДЕБНЕРА
- СИНТЕЗ ДЕБНЕРА—МИЛЛЕРА
- РЕАКЦИЯ ДЕЛЕПИНА
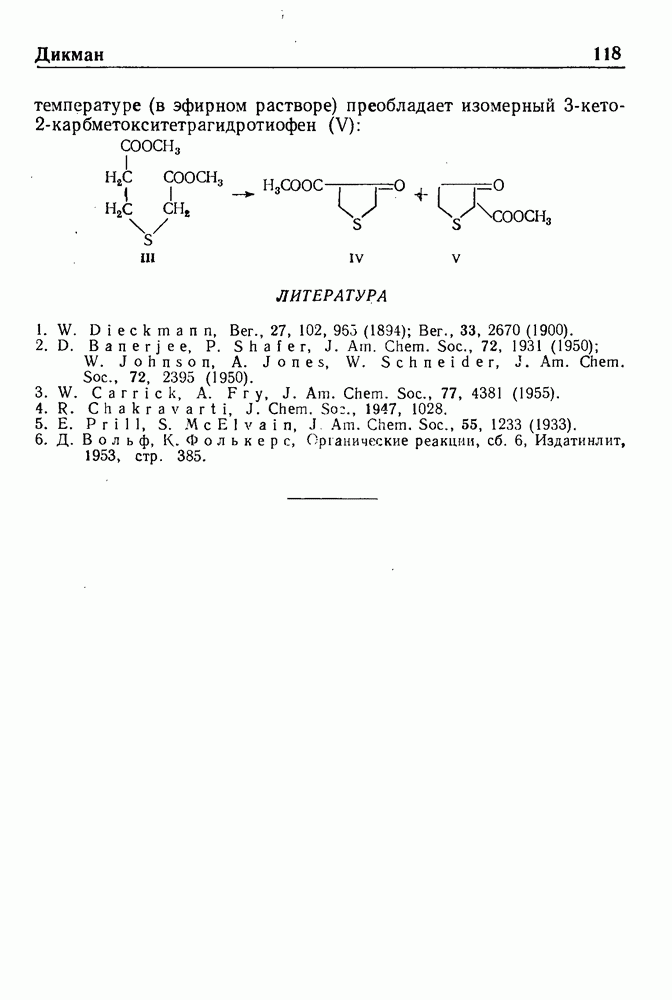
- РЕАКЦИЯ ДИКМАНА
- РЕАКЦИЯ ДИЛЬСА-АЛЬДЕРА
- РЕАКЦИЯ ДЭКИНА
- РЕАКЦИЯ ДЭКИНА—ВЕСТА
- РЕАКЦИЯ ЗАНДМЕЙЕРА
- РЕАКЦИЯ ИВАНОВА
- РЕАКЦИЯ ИОЦИЧА
- РЕАКЦИЯ КАННИЦЦАРО
- РЕАКЦИЯ КИЖНЕРА
- КОНДЕНСАЦИЯ КЛАЙЗЕНА
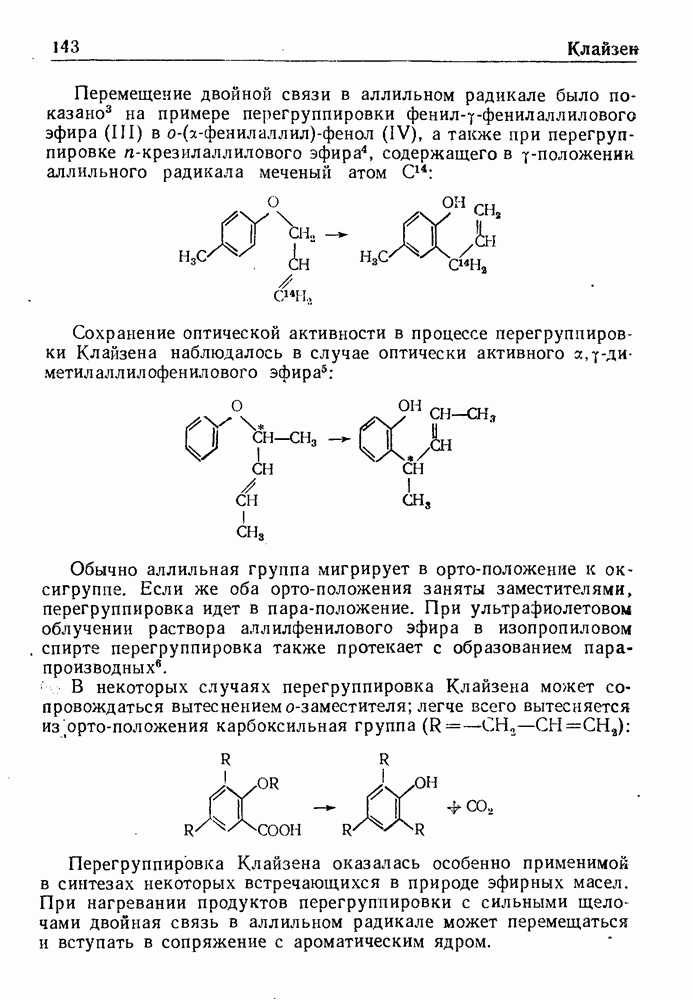
- ПЕРЕГРУППИРОВКА КЛАЙЗЕНА
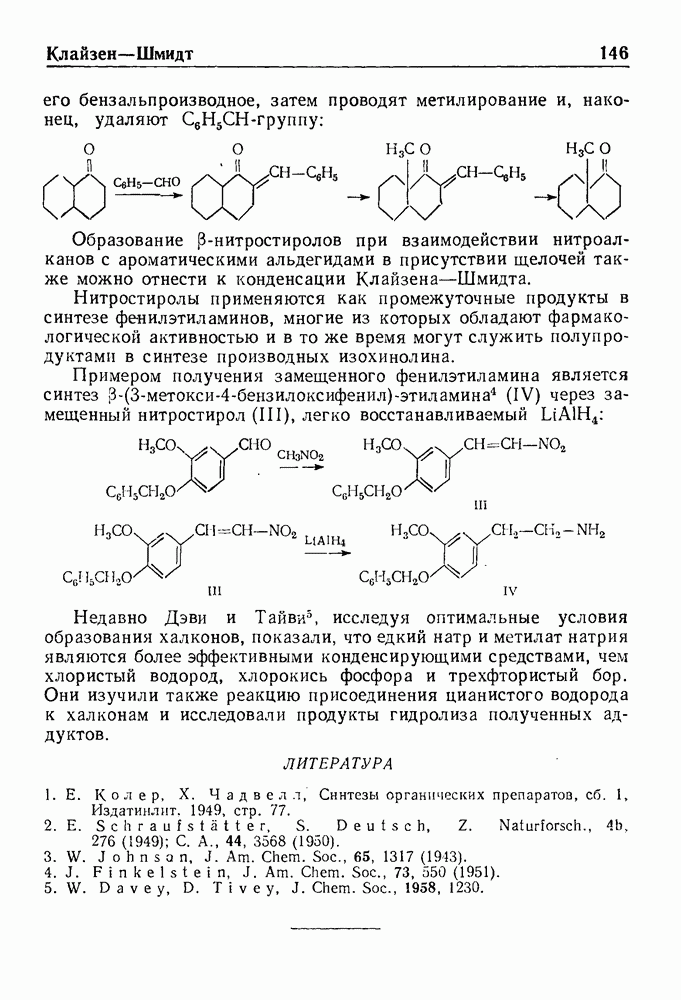
- КОНДЕНСАЦИЯ КЛАЙЗЕНА—ШМИДТА
- ВОССТАНОВЛЕНИЕ ПО КЛЕММЕНСЕНУ
- РЕАКЦИЯ КНЕВЕНАГЕЛЯ
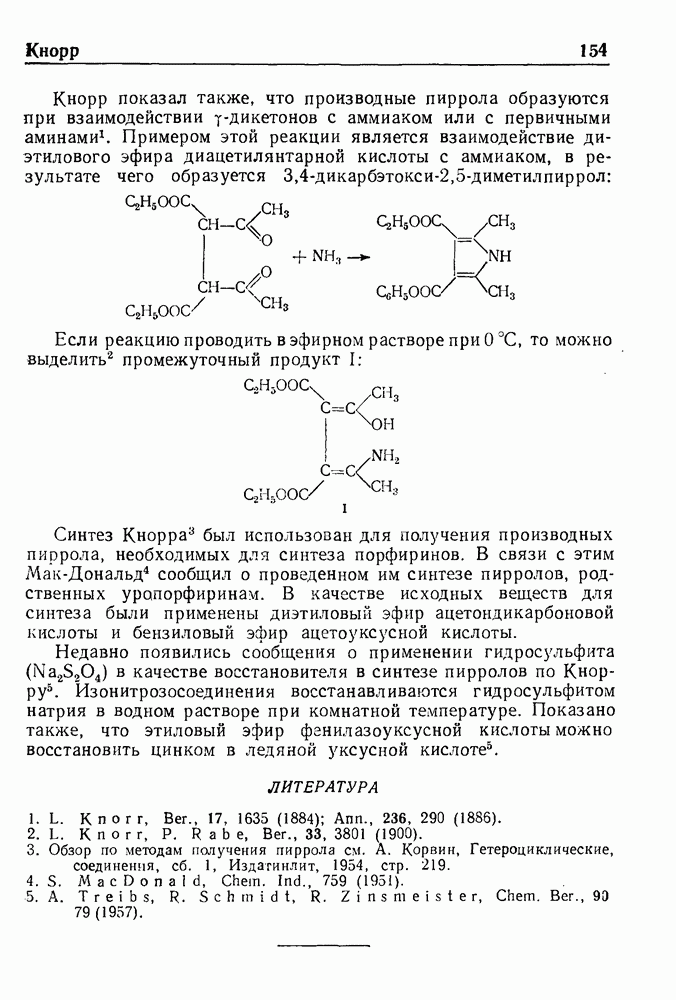
- СИНТЕЗ КНОРРА
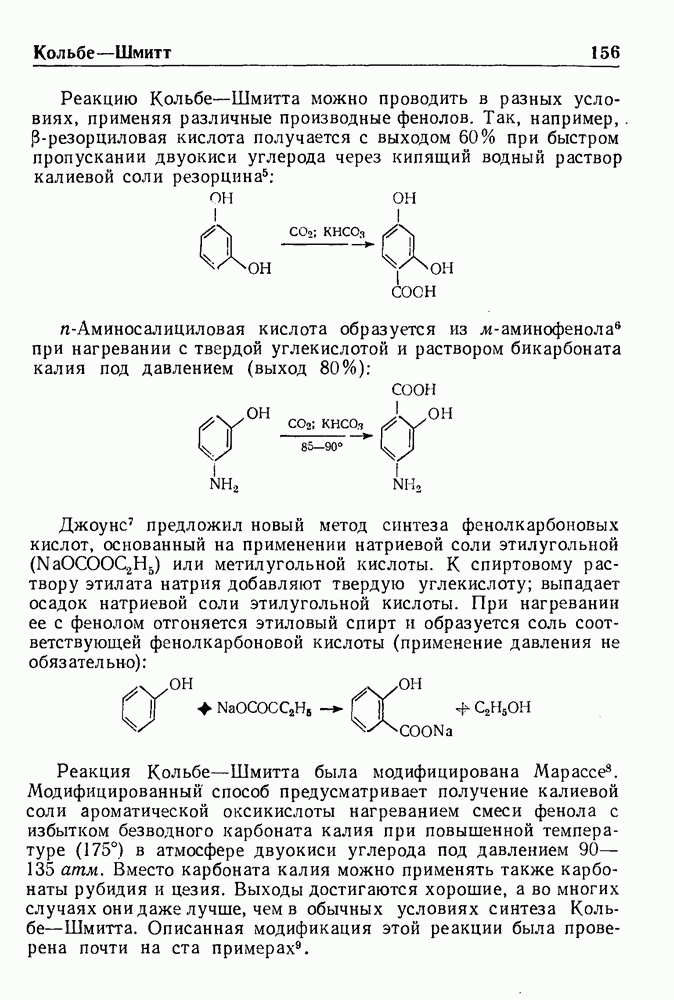
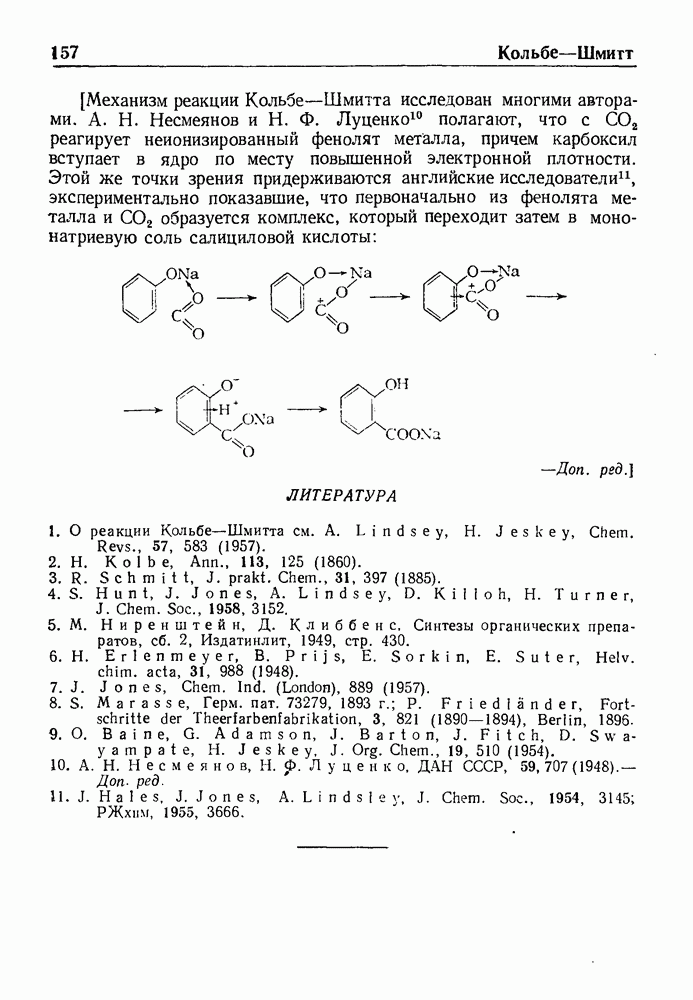
- РЕАКЦИЯ КОЛЬБЕ—ШМИТТА
- ЭЛЕКТРОХИМИЧЕСКАЯ РЕАКЦИЯ КОЛЬБЕ
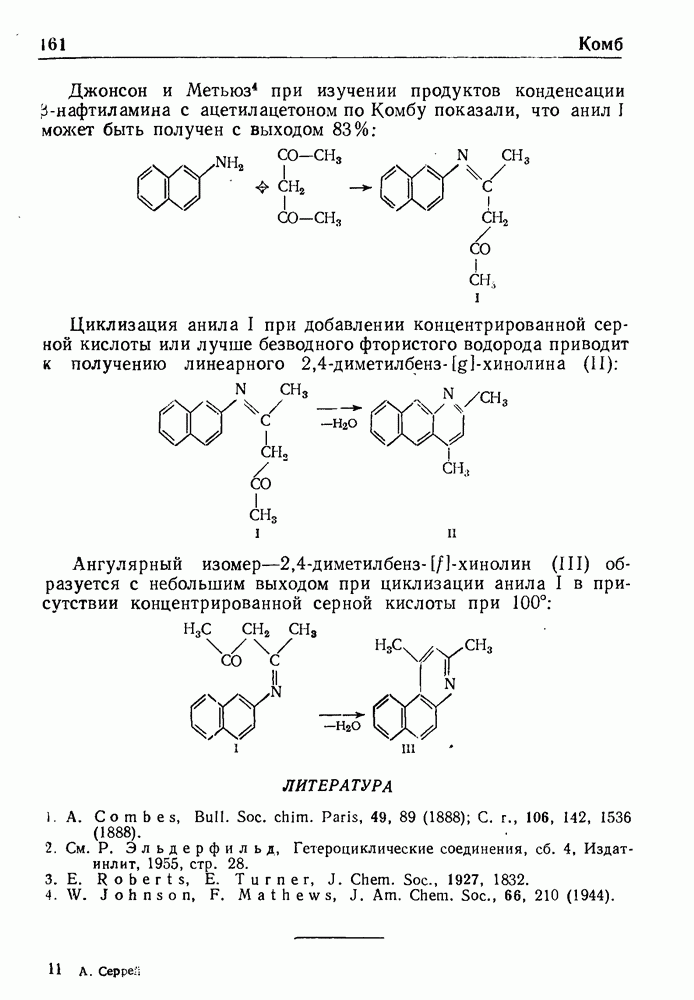
- СИНТЕЗ ХИНОЛИНА ПО КОМБУ
- РЕАКЦИЯ КОНОВАЛОВА
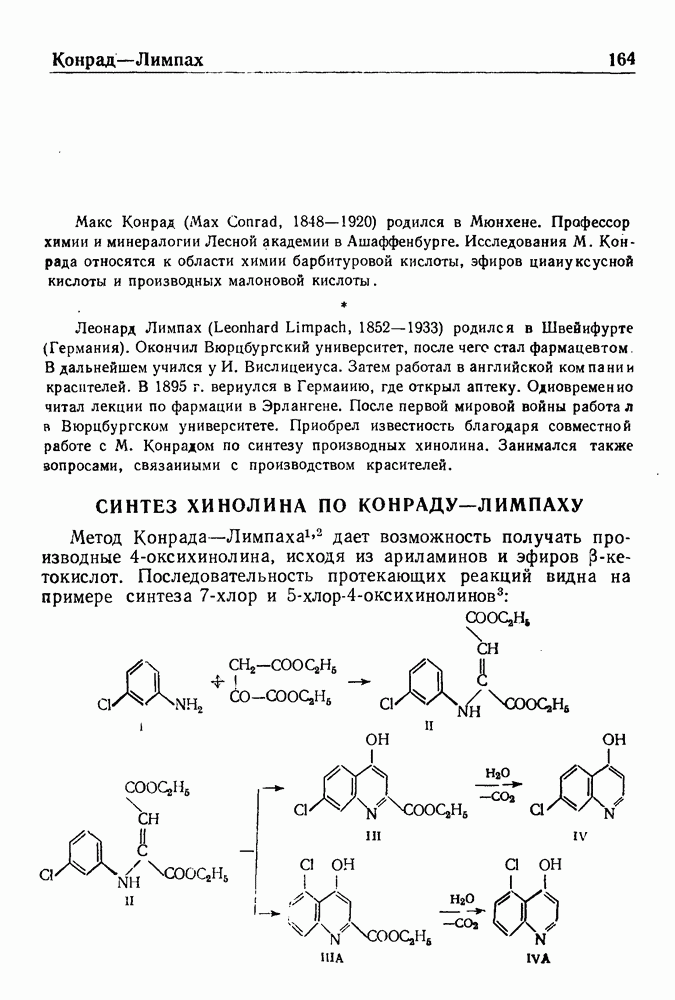
- СИНТЕЗ ХИНОЛИНА ПО КОНРАДУ—ЛИМПАХУ
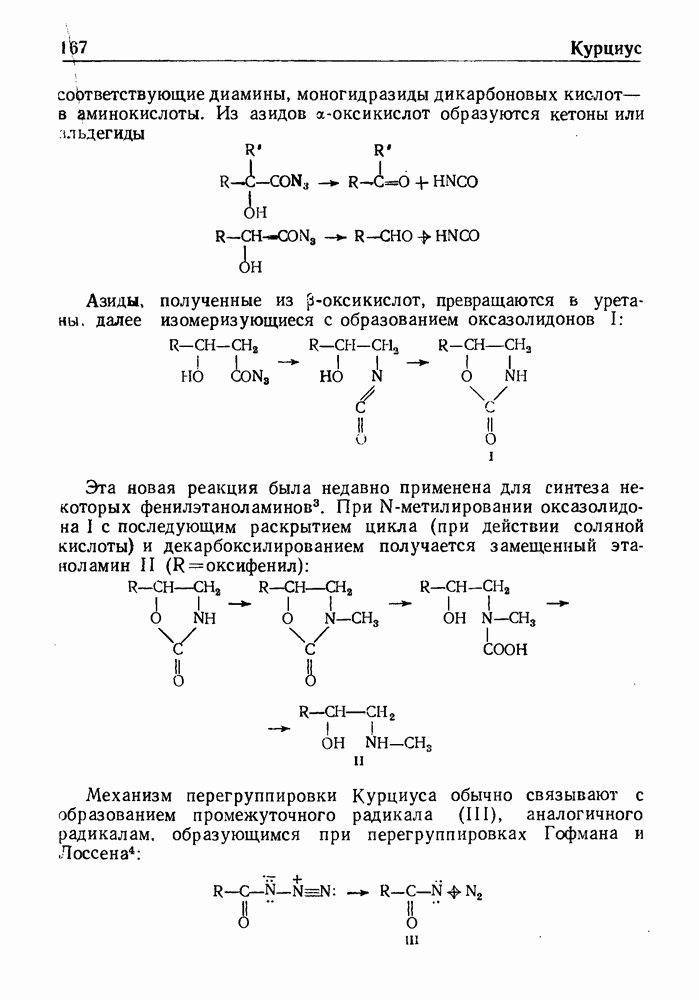
- РЕАКЦИЯ КУРЦИУСА
- РЕАКЦИЯ КУЧЕРОВА
- РЕАКЦИЯ КЭМПСА
- РЕАКЦИЯ ЛЕЙКАРТА
- РЕАКЦИЯ ЛОССЕНА
- ВОССТАНОВЛЕНИЕ ПО МАК ФАДИЕНУ—СТИВЕНСУ
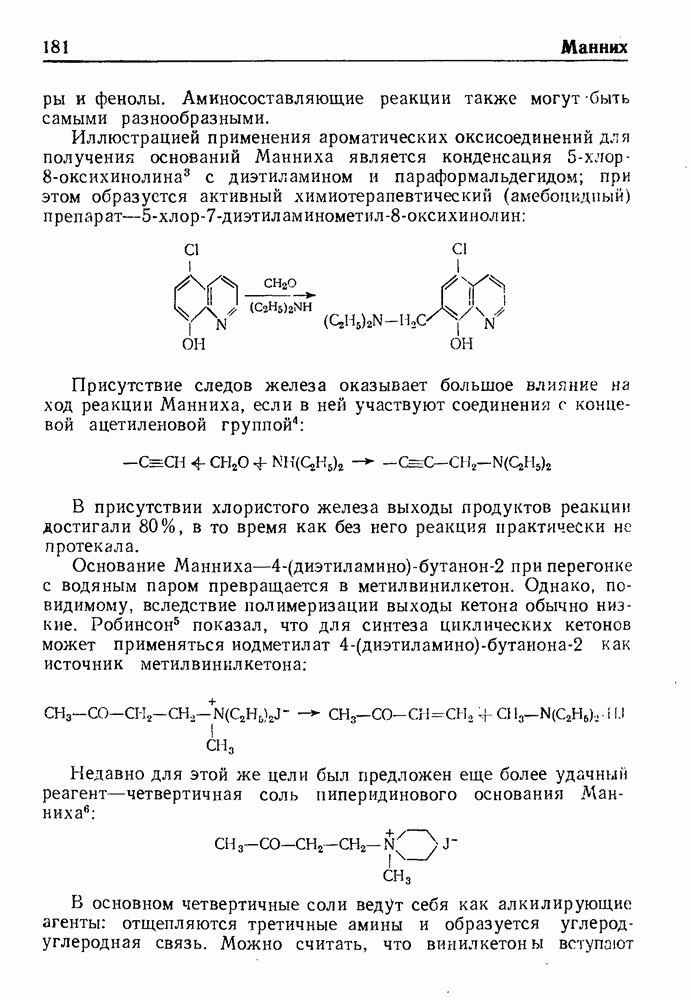
- РЕАКЦИЯ МАННИХА
- КОНДЕНСАЦИЯ МЕЕРВЕЙНА
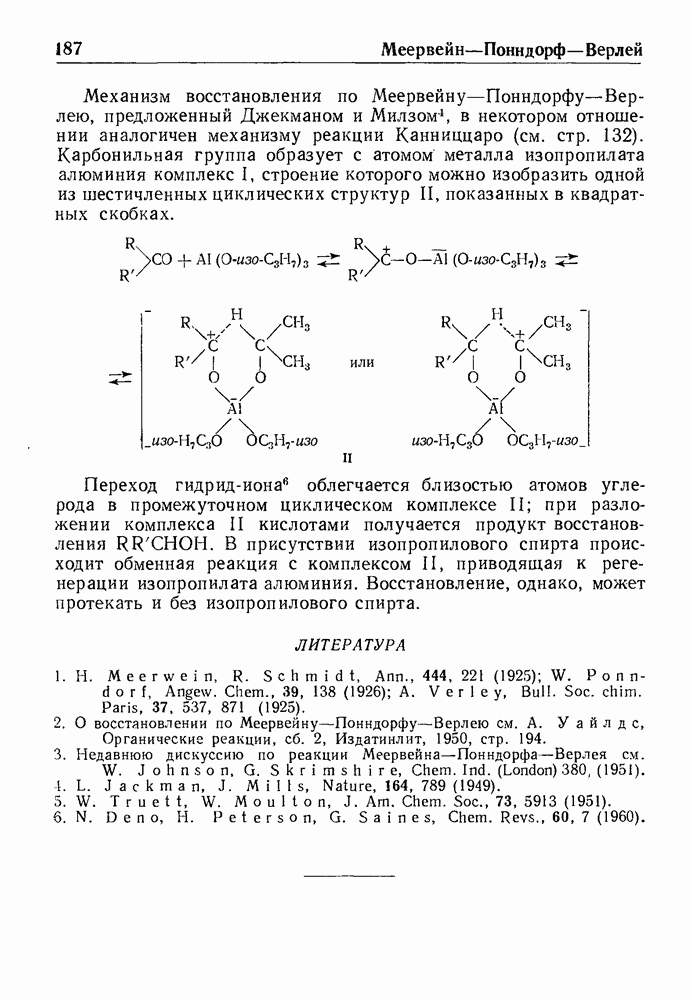
- ВОССТАНОВЛЕНИЕ ПО МЕЕРВЕЙНУ-ПОННДОРФУ-ВЕРЛЕЮ
- РЕАКЦИЯ МИХАЭЛЯ
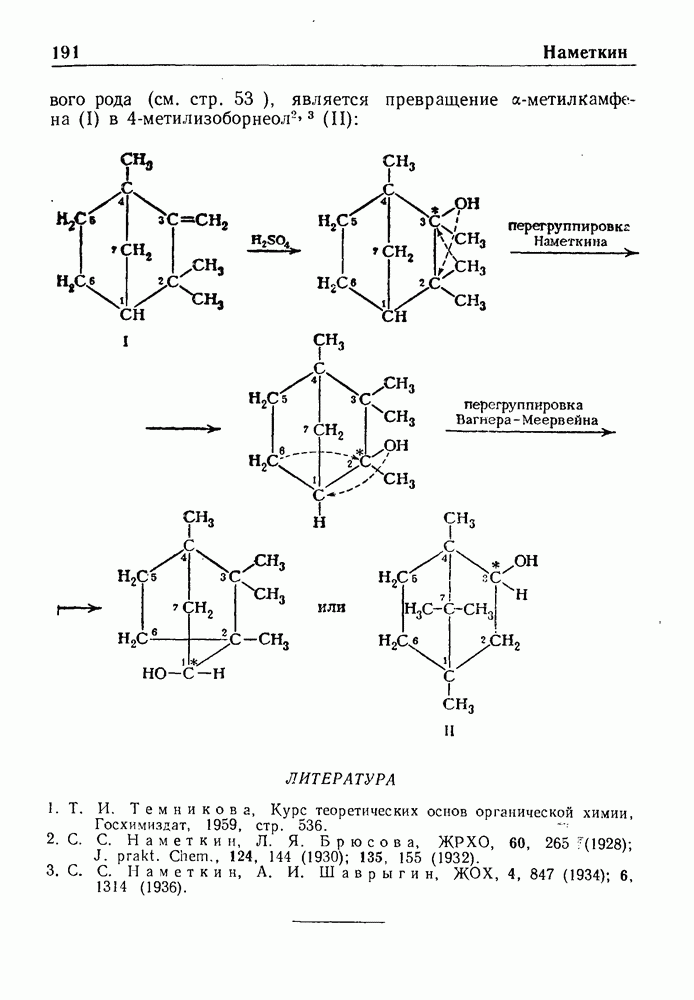
- ПЕРЕГРУППИРОВКА НАМЕТКИНА
- РЕАКЦИЯ НЕСМЕЯНОВА
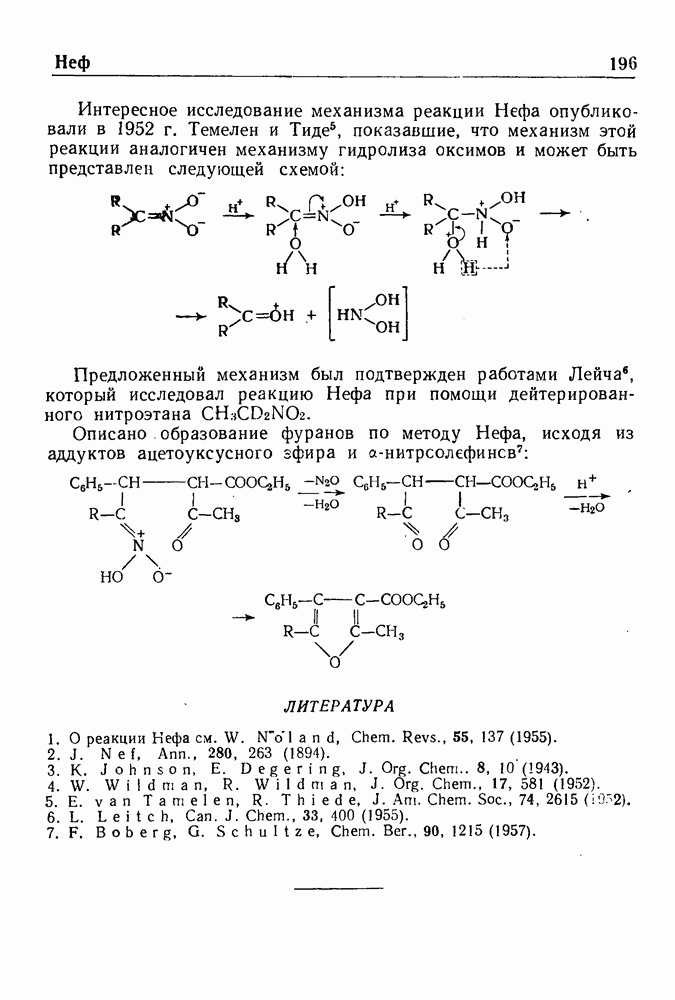
- РЕАКЦИЯ НЕФА
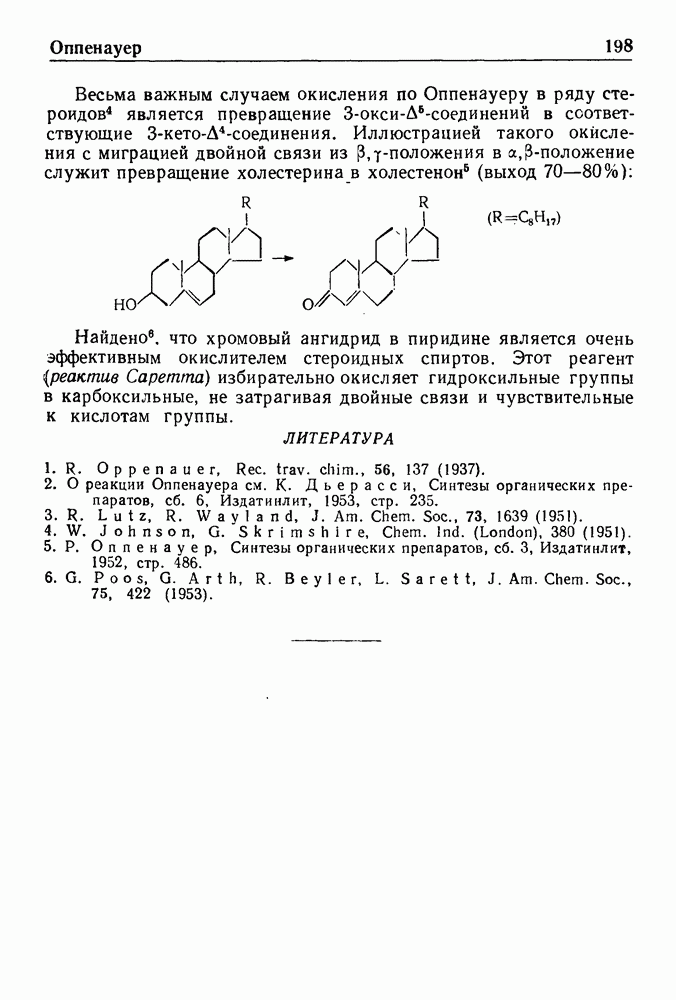
- ОКИСЛЕНИЕ ПО ОППЕНАУЕРУ
- РЕАКЦИЯ ПАССЕРИНИ
- РЕАКЦИЯ ПЕРКИНА
- КОНДЕНСАЦИЯ ПЕХМАНА
- РЕАКЦИЯ ПИКТЭ—ШПЕНГЛЕРА
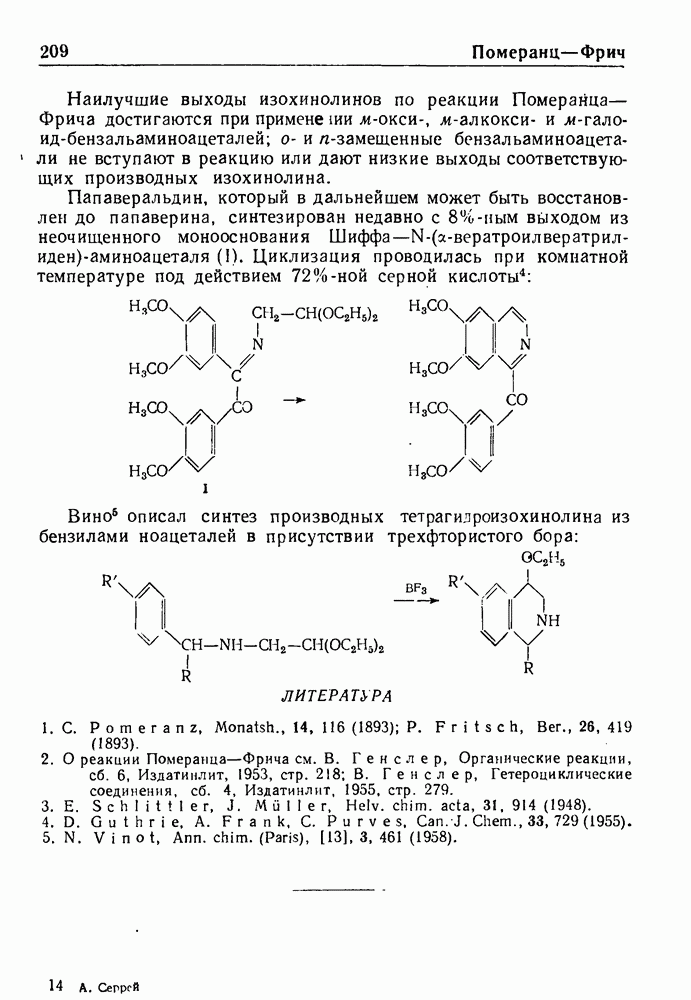
- РЕАКЦИЯ ПОМЕРАНЦА—ФРИЧА
- РЕАКЦИЯ ПРИНСА
- РЕАКЦИЯ ПФИТЦИНГЕРА
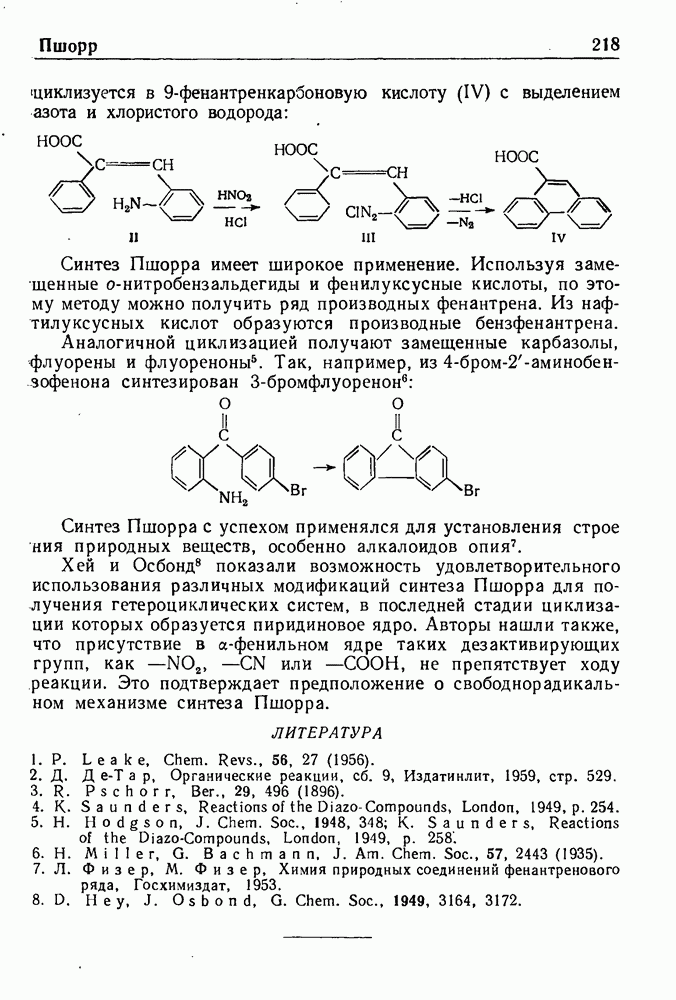
- СИНТЕЗ ПШОРРА
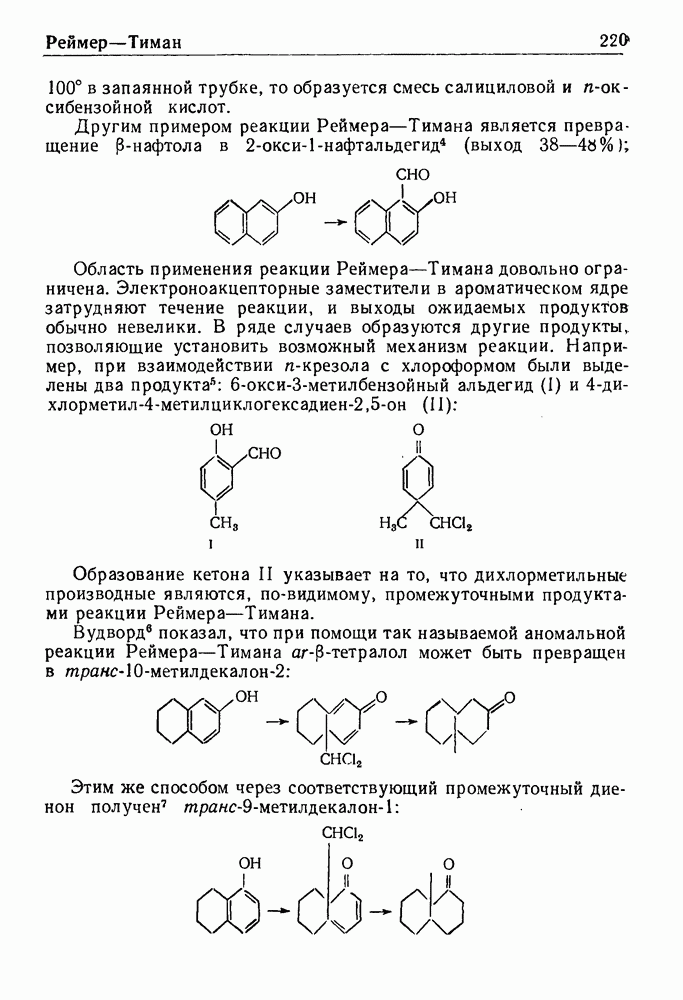
- РЕАКЦИЯ РЕЙМЕРА—ТИМАНА
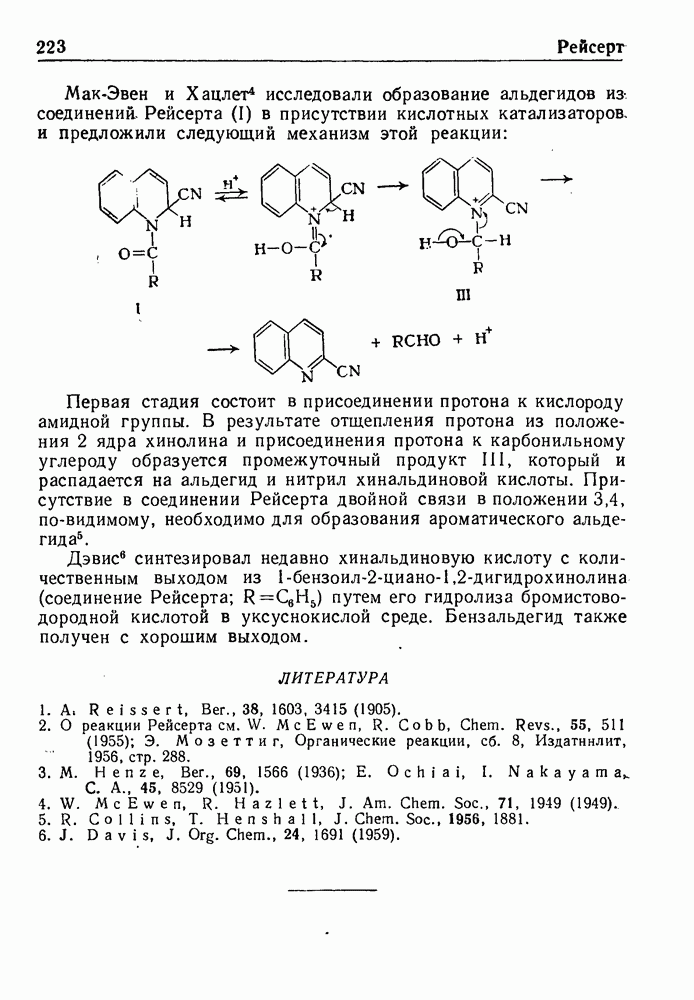
- РЕАКЦИЯ РЕЙСЕРТА
- РЕАКЦИЯ РЕФОРМАТСКОГО
- РЕАКЦИЯ РОДИОНОВА
- ВОССТАНОВЛЕНИЕ ПО РОЗЕНМУНДУ
- РЕАКЦИЯ СКРАУПА
- РЕАКЦИЯ СОММЛЕ
- РЕАКЦИЯ СТЕФЕНА
- ПЕРЕГРУППИРОВКА СТИВЕНСА
- РЕАКЦИЯ УЛЬМАНА
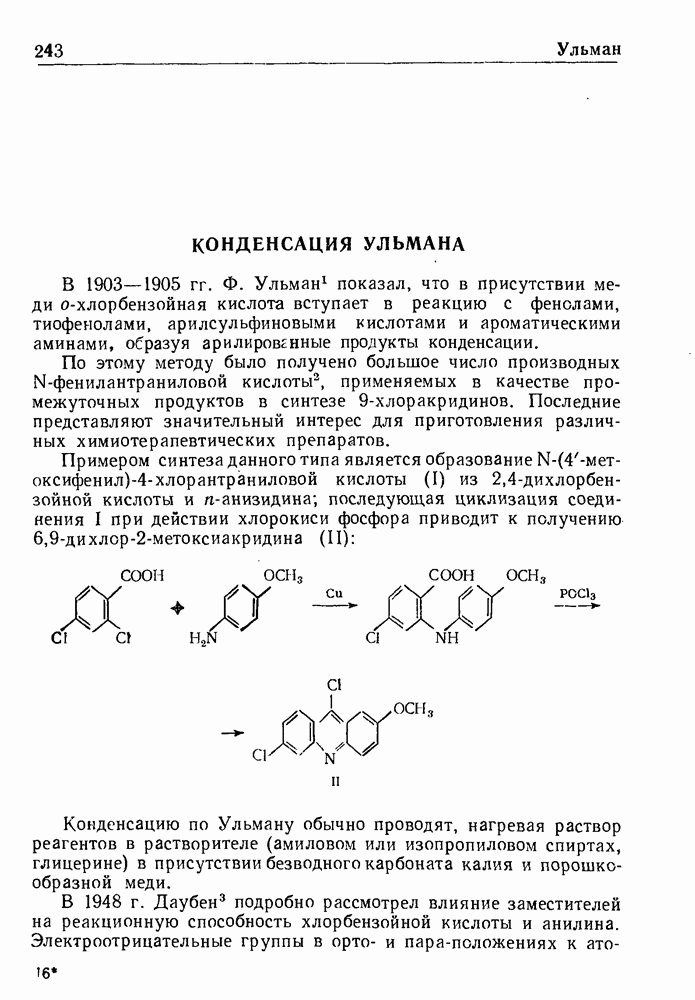
- КОНДЕНСАЦИЯ УЛЬМАНА
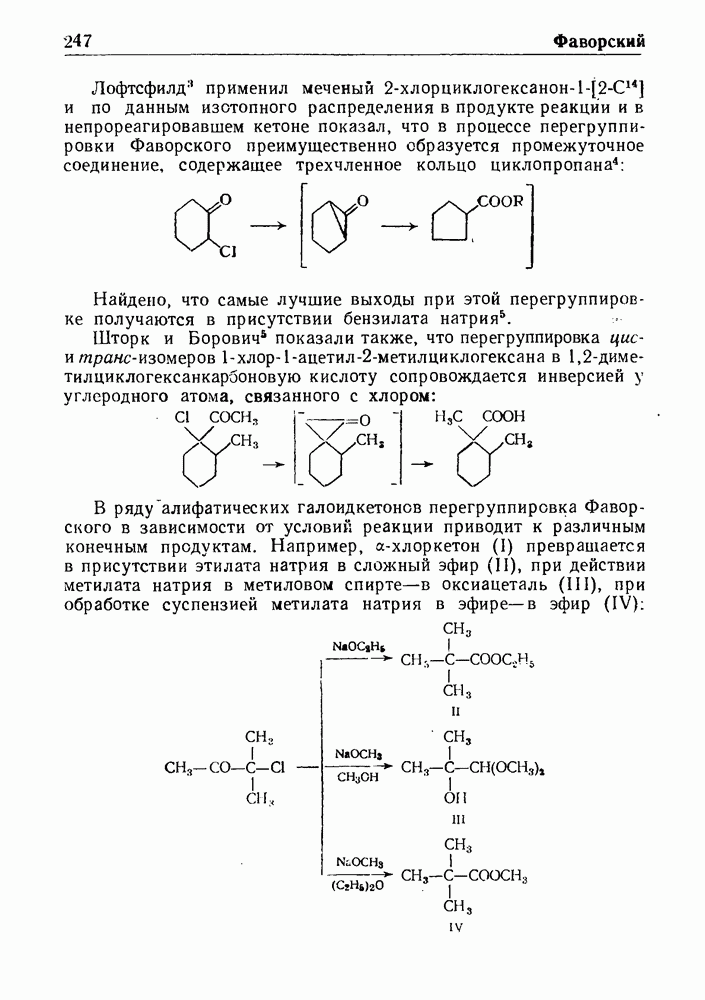
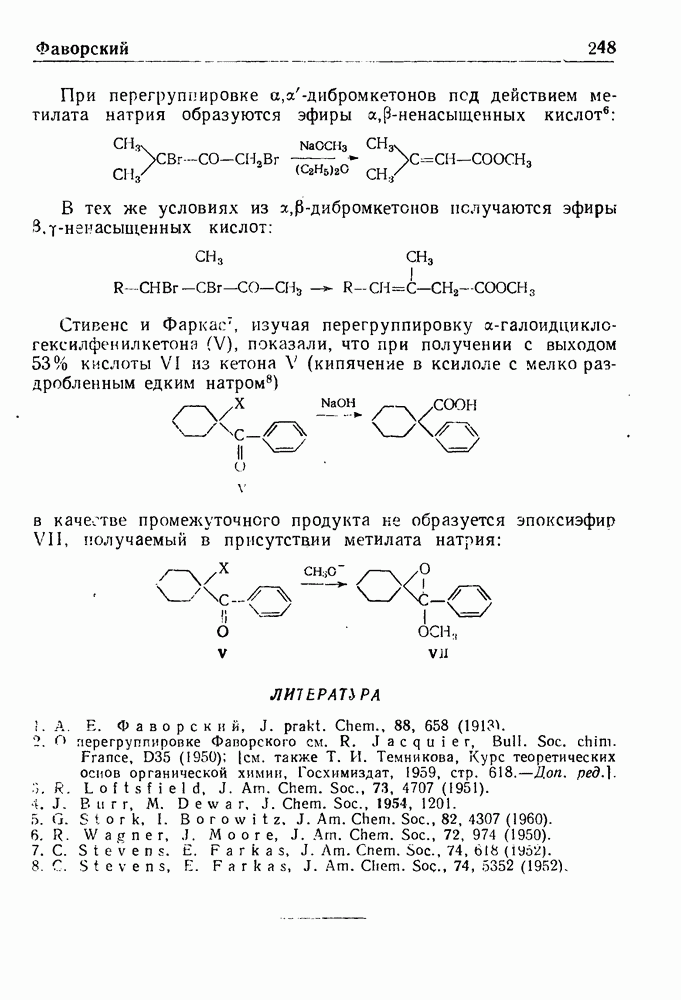
- ПЕРЕГРУППИРОВКА ФАВОРСКОГО
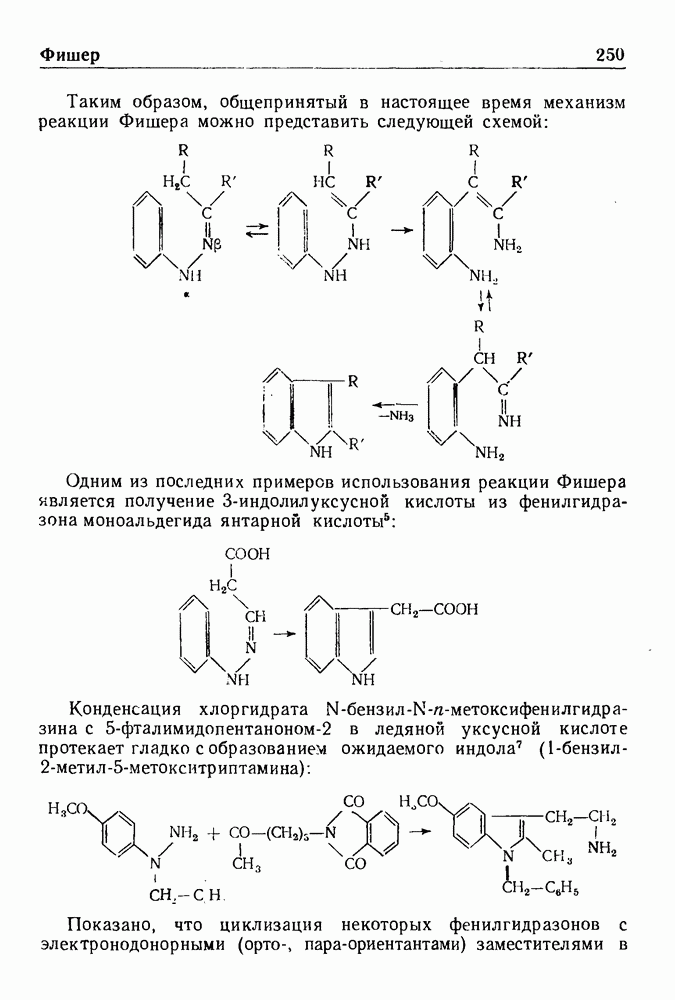
- СИНТЕЗ ИНДОЛА ПО ФИШЕРУ
- РЕАКЦИЯ ФРИДЕЛЯ—КРАФТСА
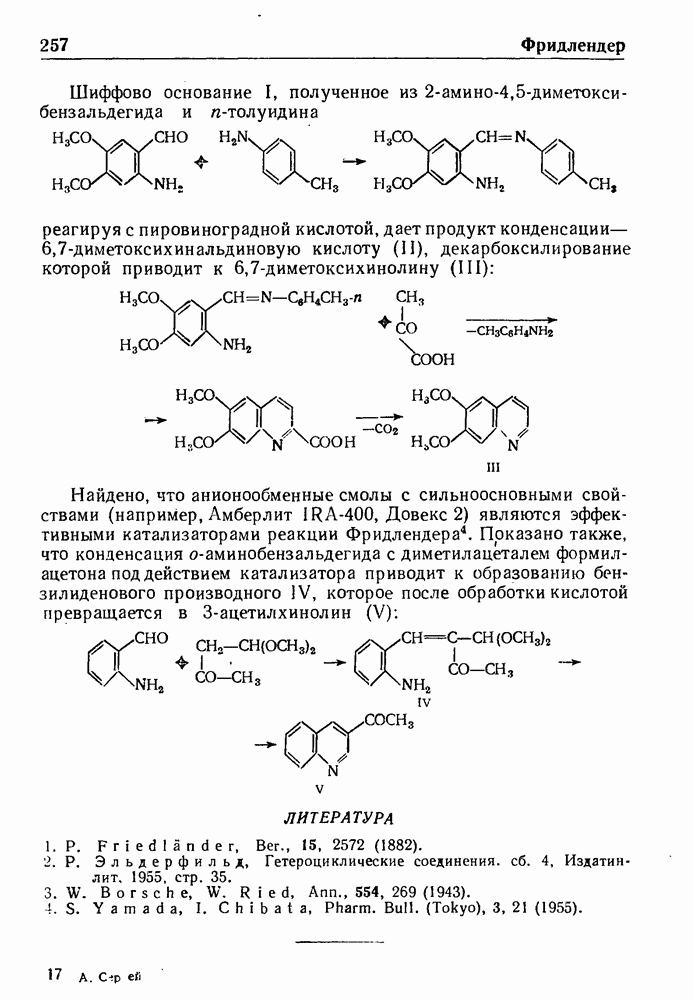
- СИНТЕЗ ФРИДЛЕНДЕРА
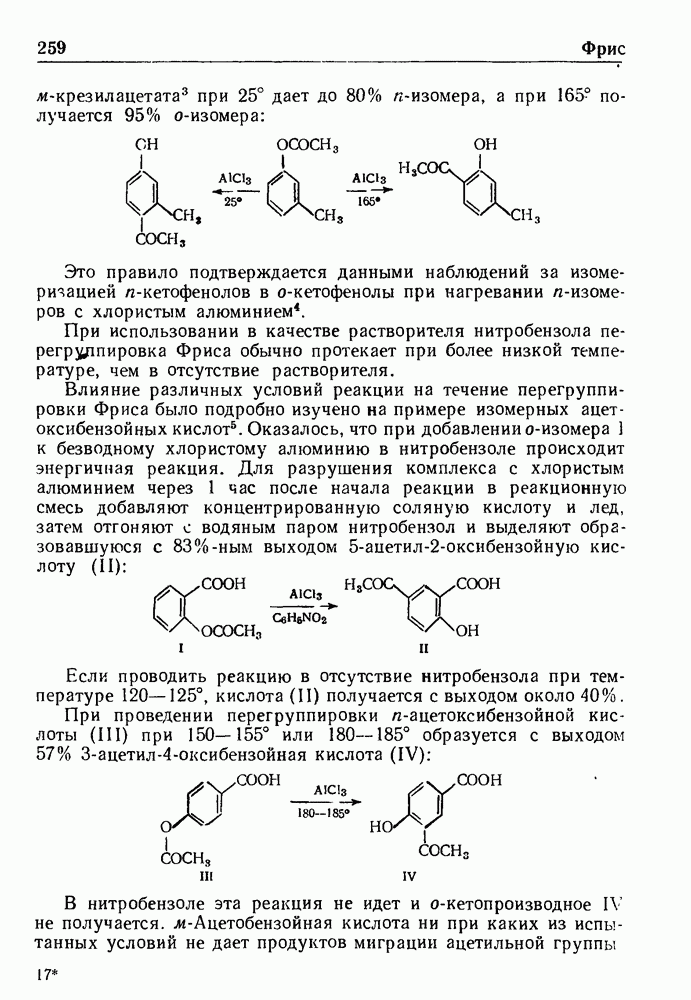
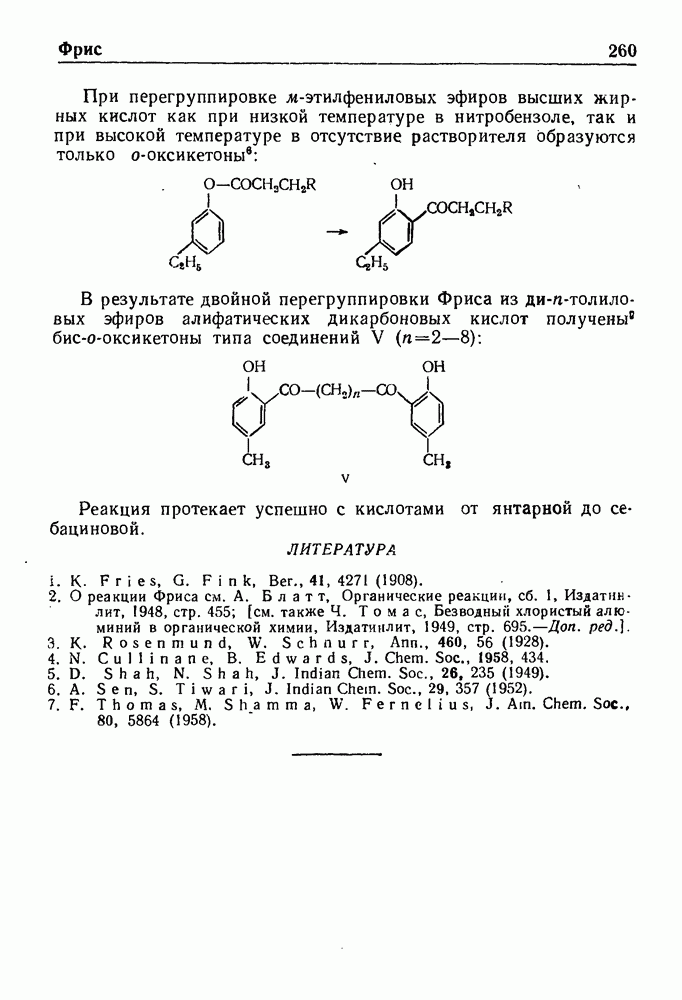
- РЕАКЦИЯ ФРИСА
- РЕАКЦИЯ ХУНСДИККЕРА
- РЕАКЦИЯ ЧИЧИБАБИНА
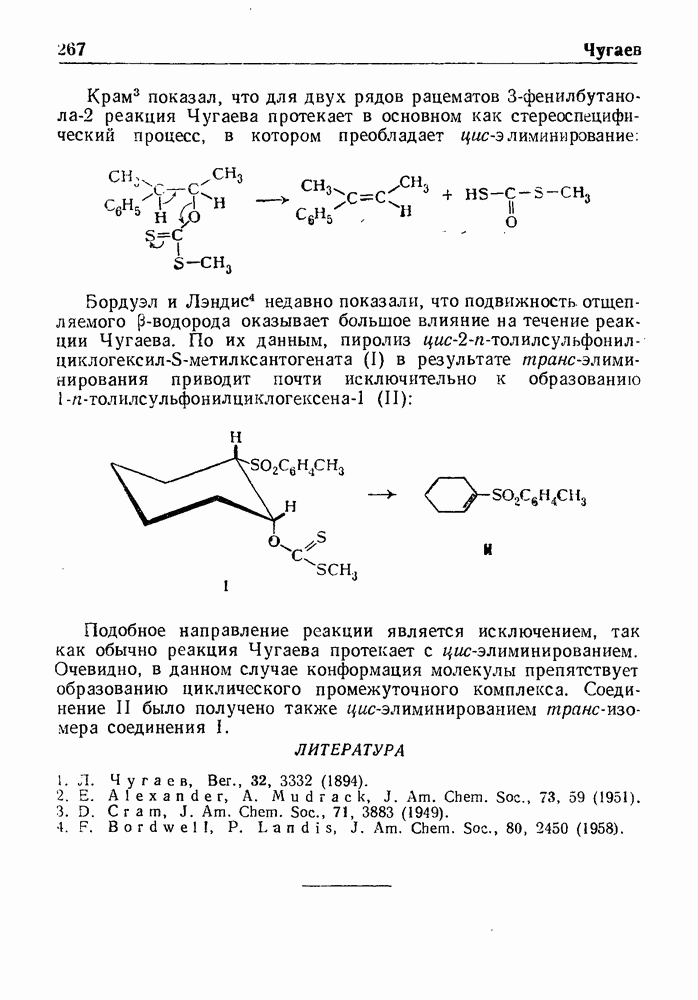
- РЕАКЦИЯ ЧУГАЕВА
- РЕАКЦИЯ ШИМАНА
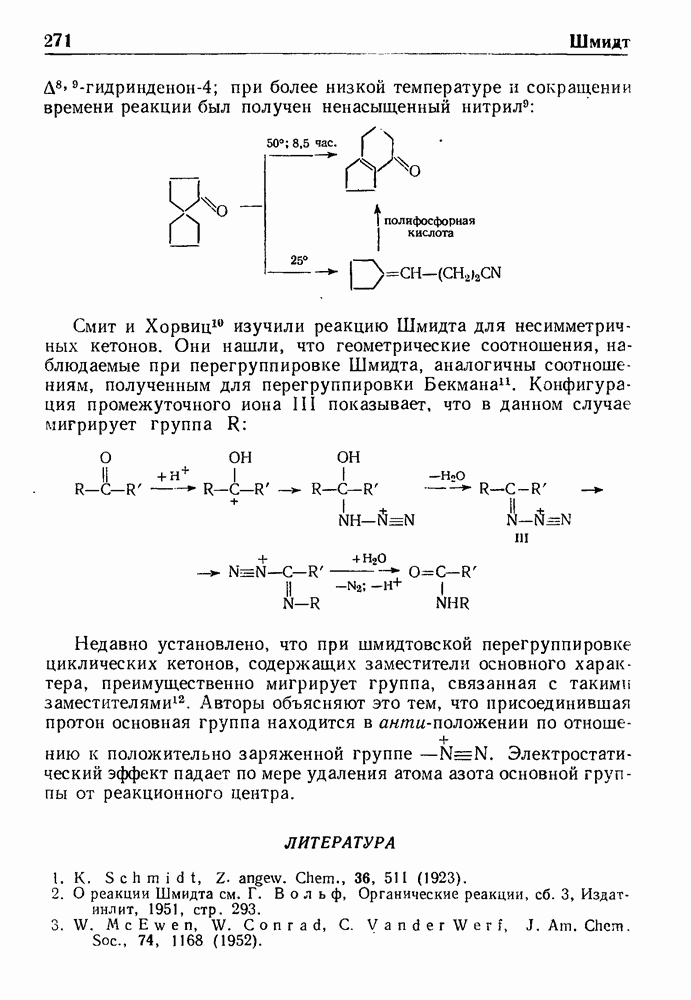
- РЕАКЦИИ ШМИДТА
- КОНДЕНСАЦИЯ ШТОББЕ
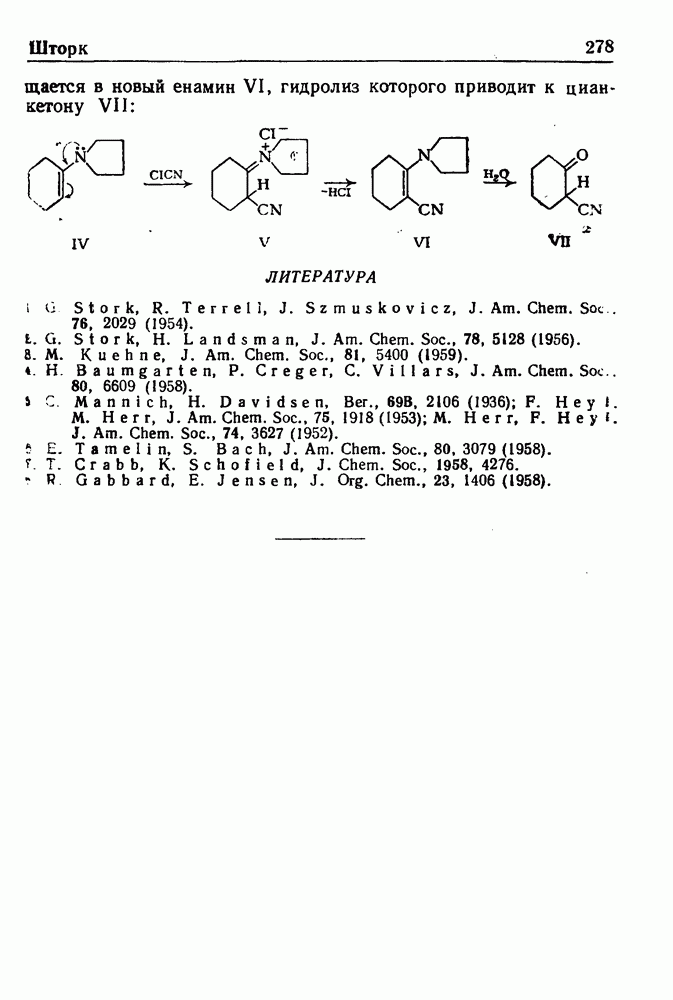
- РЕАКЦИЯ ШТОРКА
- РЕАКЦИЯ ЭЛБСА
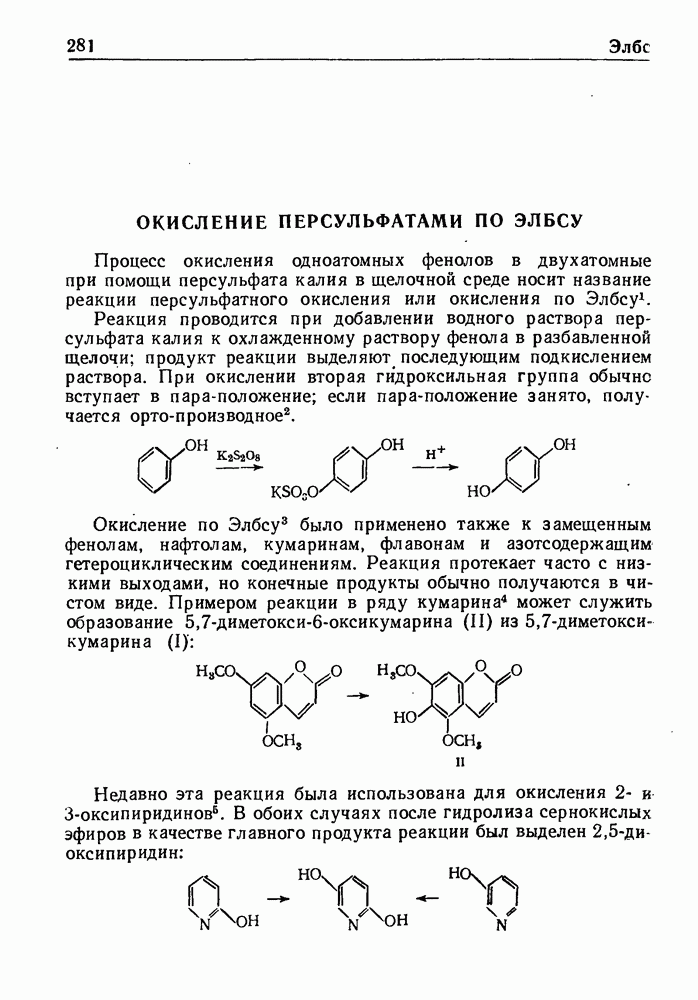
- ОКИСЛЕНИЕ ПЕРСУЛЬФАТАМИ ПО ЭЛБСУ
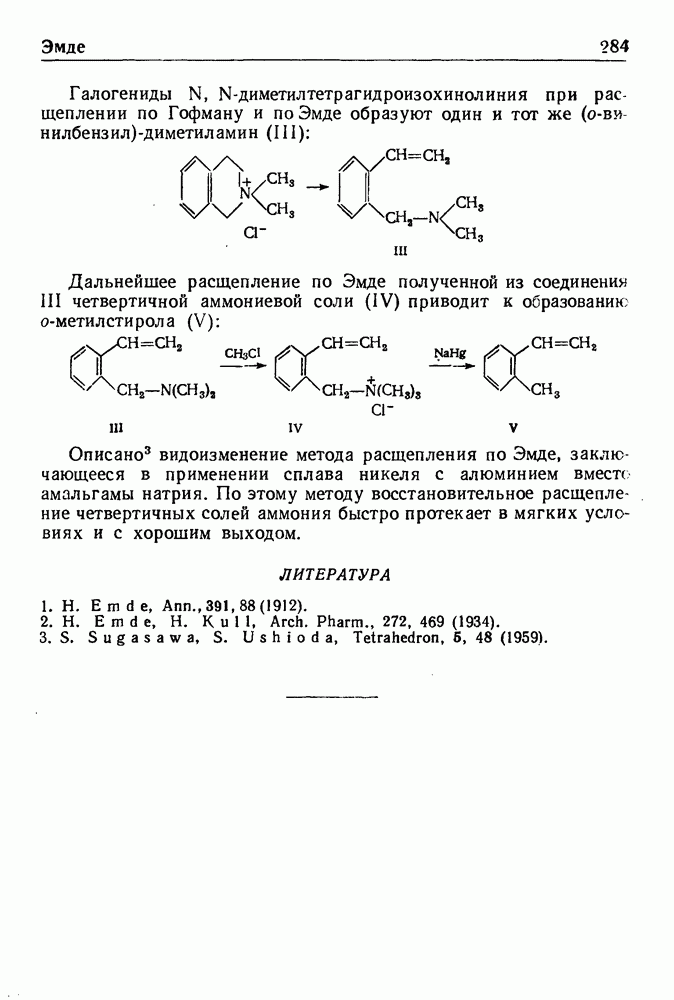
- РАСЩЕПЛЕНИЕ ПО ЭМДЕ
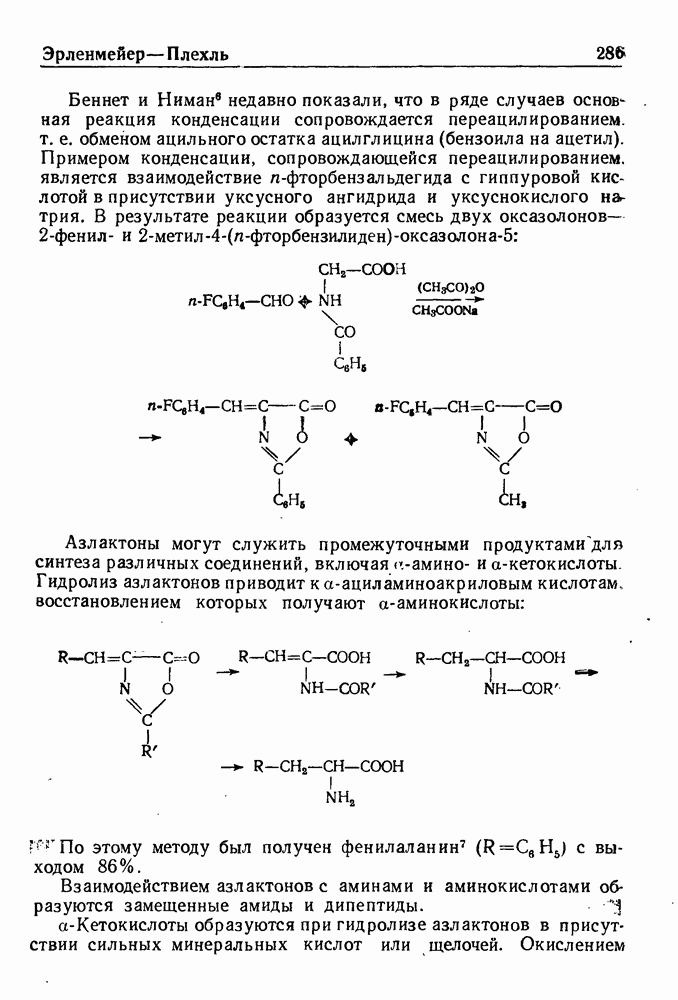
- СИНТЕЗ АЗЛАКТОНОВ ПО ЭРЛЕНМЕИЕРУ—ПЛЕХЛЮ
- РЕАКЦИЯ ЯКОБСЕНА