| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
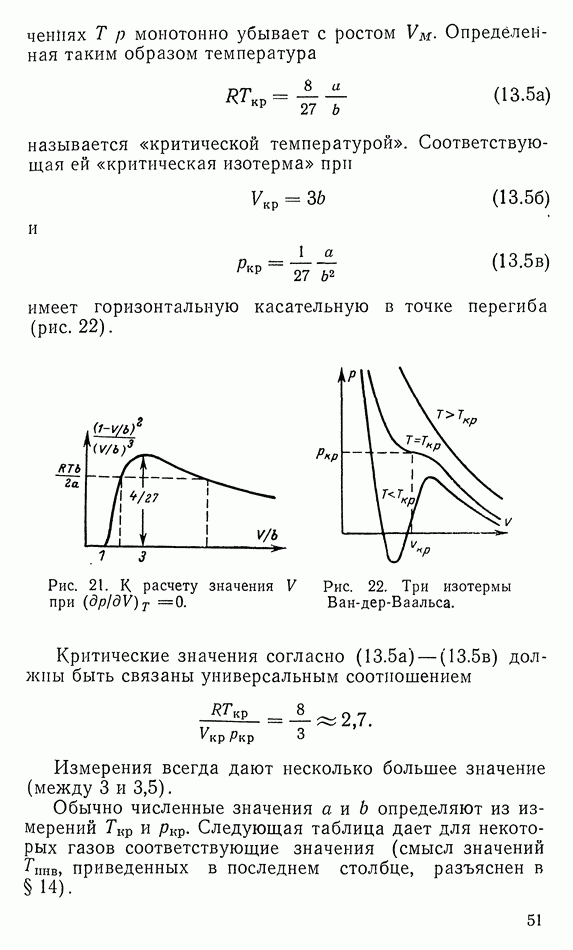
9. РОСТ ЭНТРОПИИ В ИЗОЛИРОВАННОЙ СИСТЕМЕ
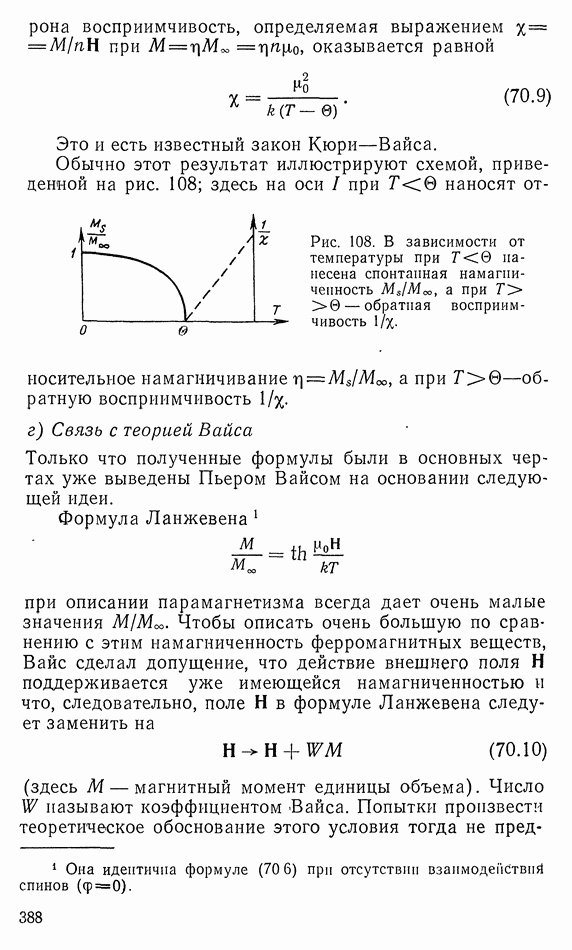
Из второго закона термодинамики вытекает фундаментальный закон: энтропия изолированной системы никогда не может уменьшаться. Она возрастает при всех реальных, протекающих с конечной скоростью процессах. Она остается постоянной в идеальном случае бесконечно медленного (обратимого) процесса.
Этот закон был бы доказан, если бы мы смогли показать, что протекание в изолированной системе процесса, связанного с уменьшением энтропии, равносильно возможности создания перпетуум мобиле второго рода.
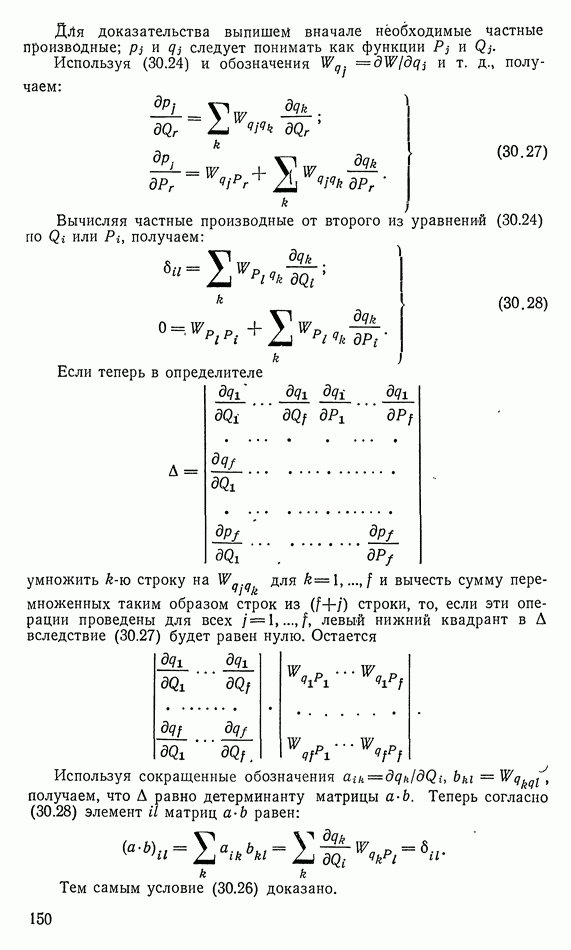
Иллюстрацию вышеприведенного закона полезно начать со специального примера, а именно с выравнивания температуры между Двумя соприкасающимися телами. Рассмотрим, например, два металлических тела равных размеров, изготовленных из одинакового материала (рис. 14). Пусть каждое из них имеет теплоемкость С. Изменениями объема пренебрегаем. Пусть вначале они будут изолированы друг от друга; одно из них имеет температуру  а другое
а другое  (при этом
(при этом  ). Приведем теперь оба в
). Приведем теперь оба в
соприкосновение, после чего их температуры станут выравниваться. В конце концов оба они примут температуру  С этим процессом связано возрастание энтропии изолированной системы, состоящей из обоих тел, которое мы рассчитаем согласно уравнению (8.5) из выражения
С этим процессом связано возрастание энтропии изолированной системы, состоящей из обоих тел, которое мы рассчитаем согласно уравнению (8.5) из выражения

При заданной теплоемкости  Следовательно, с точностью до несущественной для данного случая аддитивной постоянной
Следовательно, с точностью до несущественной для данного случая аддитивной постоянной  Обозначим индексами а не значения 5 в начале и конце выравнивания, получим перед контактом:
Обозначим индексами а не значения 5 в начале и конце выравнивания, получим перед контактом:

после выравнивания


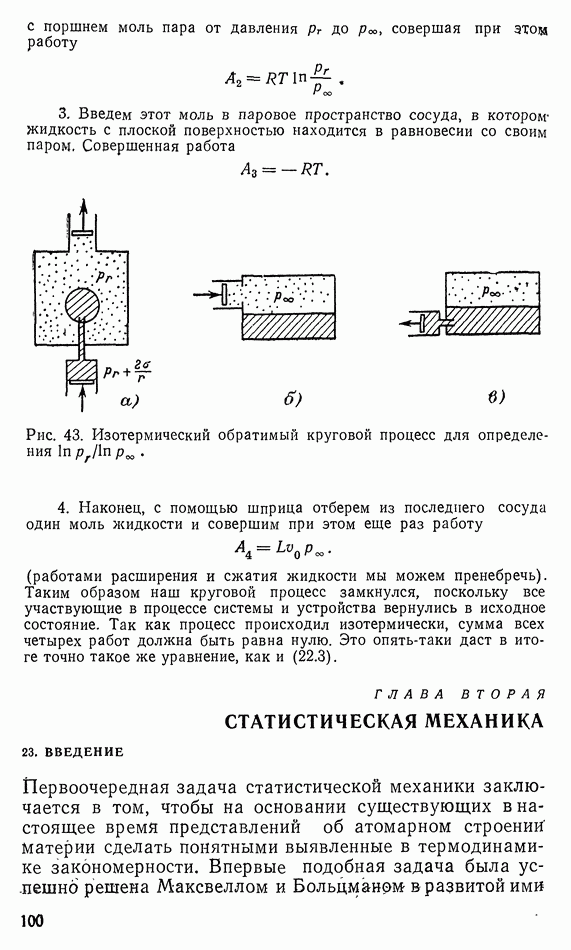
Рис. 14. Теплообмен между более нагретым  и более холодным
и более холодным  телом.
телом.
Приращение этропин  равно
равно  Для удобства записи обозначим через
Для удобства записи обозначим через  начальную разность температур обоих тел и выразим соответственно
начальную разность температур обоих тел и выразим соответственно

Тогда

Как утверждалось ранее, для всех возможных  положительно. Для
положительно. Для 

То
Необратимое выравнивание температуры, следовательно, связано с возрастанием энтропии, определяемым с помощью уравнения (9.1). Исследуем теперь возможность обратимого выравнивания разности температур  При таком выравнивании энтропия всех частей системы не должна изменяться. Так как, однако, энтропия одних только рассмотренных металлических тел возрастает на величину
При таком выравнивании энтропия всех частей системы не должна изменяться. Так как, однако, энтропия одних только рассмотренных металлических тел возрастает на величину  то мы должны обязательно включить в рассматриваемую систему дополнительные тела, с тем чтобы энтропия такой расширенной системы могла оставаться постоянной. Для расширения системы возьмем источник тепла с температурой
то мы должны обязательно включить в рассматриваемую систему дополнительные тела, с тем чтобы энтропия такой расширенной системы могла оставаться постоянной. Для расширения системы возьмем источник тепла с температурой  (Сейчас мы познакомимся с механизмом осуществления обратимого выравнивания температуры.) Энтропия этого источника тепла должна, следовательно, снизиться на величину
(Сейчас мы познакомимся с механизмом осуществления обратимого выравнивания температуры.) Энтропия этого источника тепла должна, следовательно, снизиться на величину  т. е. этот источник тепла должен отдать тепло
т. е. этот источник тепла должен отдать тепло  Однако энергия обоих металлических стержней до и после выравнивания температуры остается неизменной; таким образом, отнятое от источника тепла тепло
Однако энергия обоих металлических стержней до и после выравнивания температуры остается неизменной; таким образом, отнятое от источника тепла тепло  согласно первому основному закону может проявиться лишь в виде совершенной работы.
согласно первому основному закону может проявиться лишь в виде совершенной работы.
Следовательно, если удастся произвести обратимое выравнивание температуры, то при этом должна быть совершена механическая работа

за счет одного только источника тепла с температурой 
Рассмотрим такой обратимый процесс детально. Пусть имеются два изолированных друг от друга металлических тела с температурами  Вместо того, чтобы приводить их в контакт друг с другом, приведем каждый из них обратимым способом к конечной температуре
Вместо того, чтобы приводить их в контакт друг с другом, приведем каждый из них обратимым способом к конечной температуре 

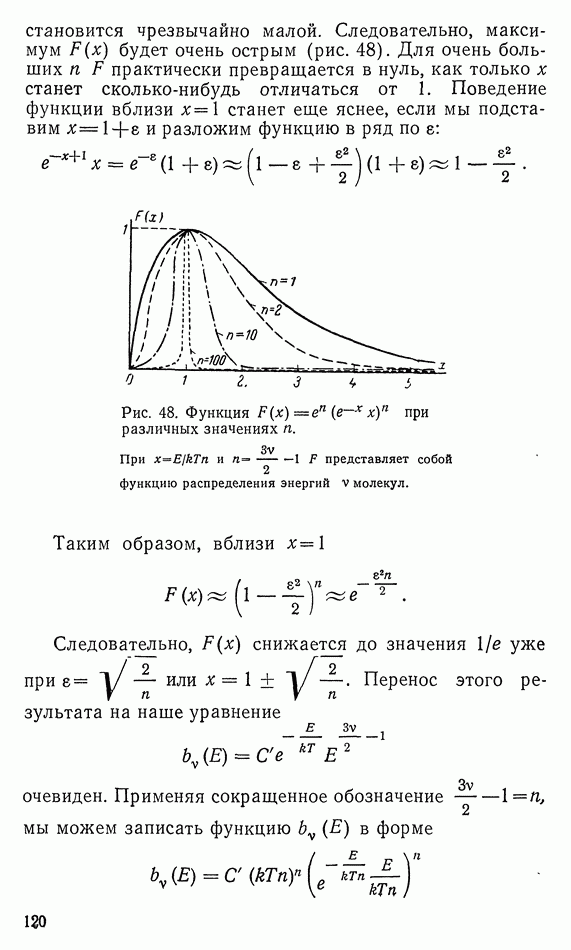
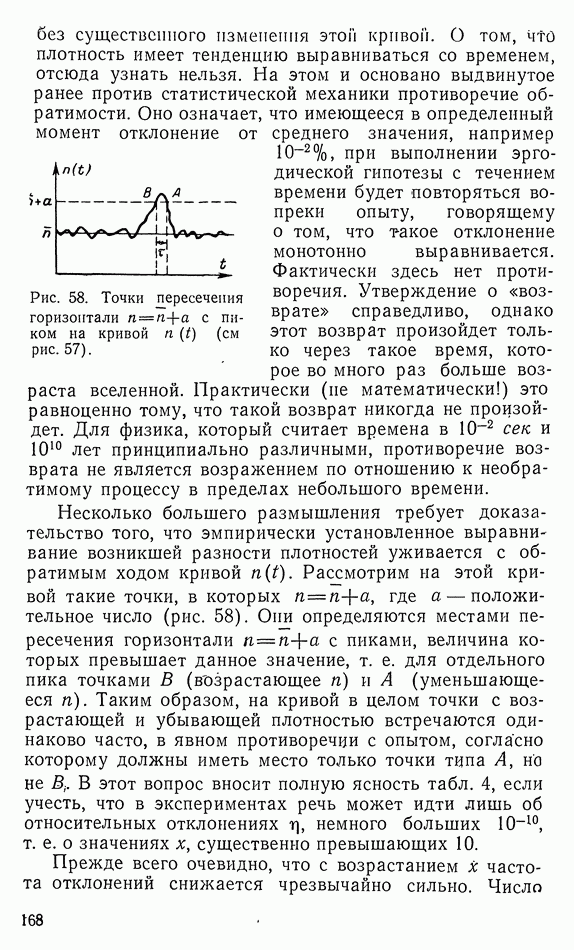
Рис. 15. Устройство для обратимого охлаждения (контакт с расширяющимся газом).
В начале первое тело должно охладиться от температуры  до
до  Для этой цели приведем его в контакт с цилиндром, с поршнем, содержащим 1 моль идеального газа с температурой
Для этой цели приведем его в контакт с цилиндром, с поршнем, содержащим 1 моль идеального газа с температурой  (рис. 15). Если мы теперь будем медленно выдвигать поршень, то при увеличении объема на
(рис. 15). Если мы теперь будем медленно выдвигать поршень, то при увеличении объема на  получим работу
получим работу  за счет энергоемкости металлического тела (с теплоемкостью
за счет энергоемкости металлического тела (с теплоемкостью  Следовательно,
Следовательно,

Если обозначить через  и
и  объемы газа в начале
объемы газа в начале  конце
конце  этого расширения, то совершенная при этом работа будет равна:
этого расширения, то совершенная при этом работа будет равна:

При  далее из (9.3) следует:
далее из (9.3) следует:

Для того чтобы энергия использованного газа не входила в баланс энергии, поставим теперь задачу привести газ обратимо в начальное состояние  оставив, однако, металлическое тело в только что достигнутом состоянии
оставив, однако, металлическое тело в только что достигнутом состоянии  Для этого будем использовать источник тепла
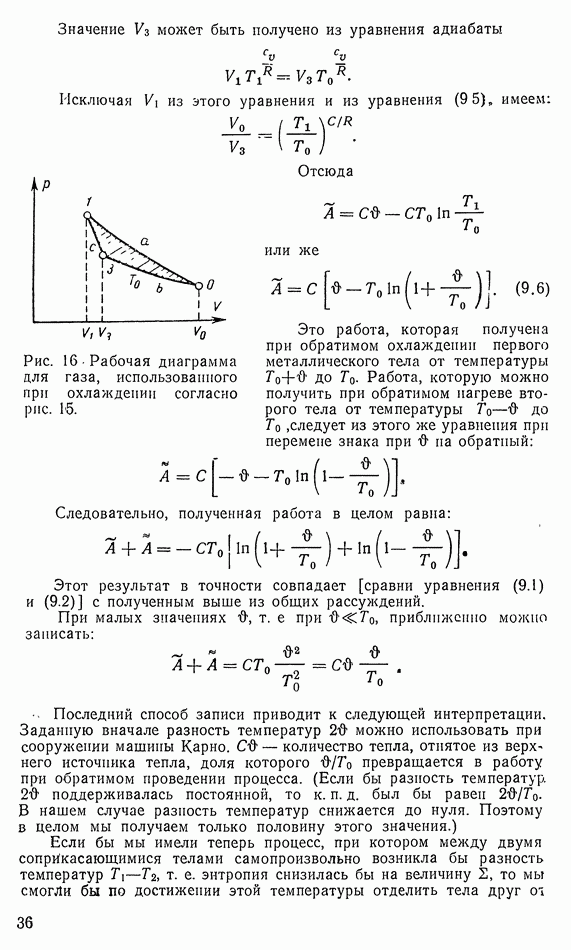
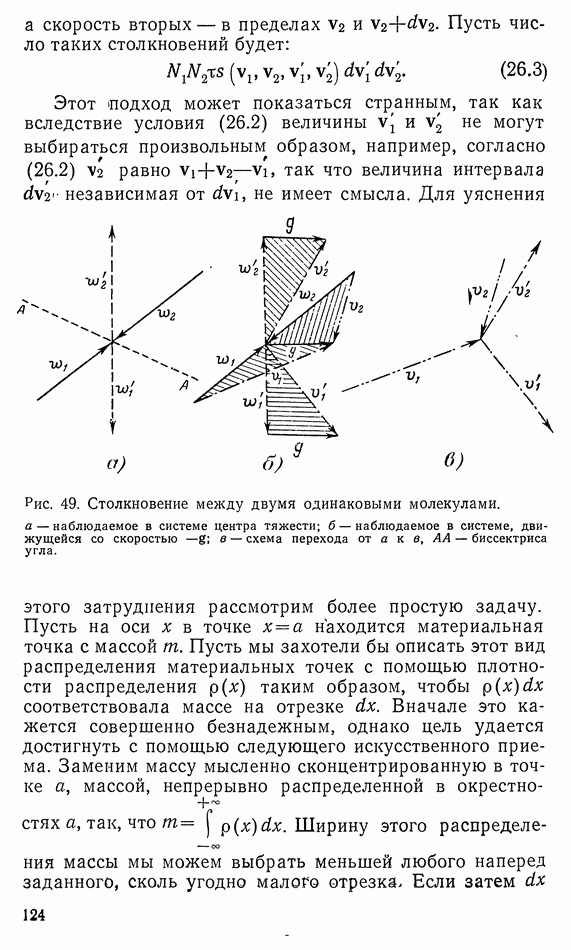
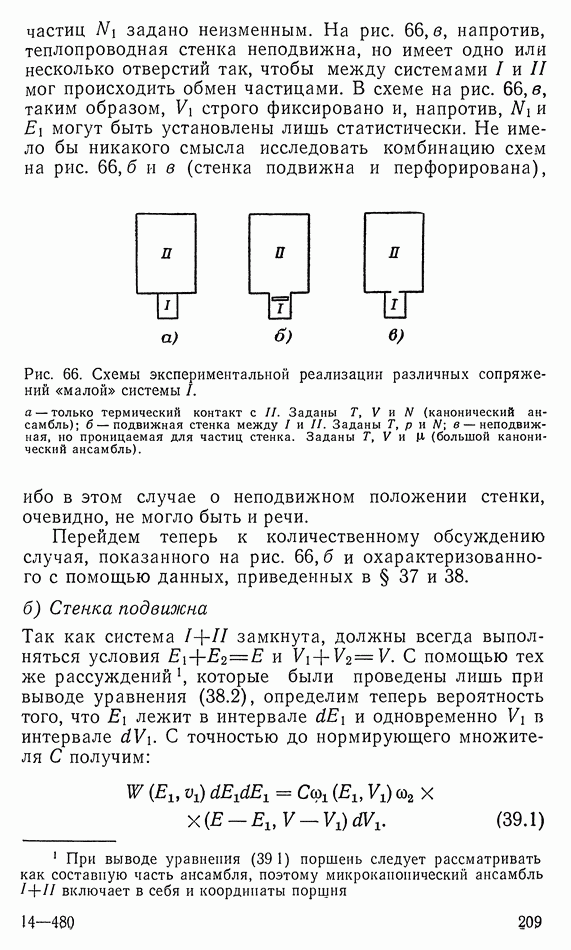
Для этого будем использовать источник тепла  применяя способ, показанный на диаграмме рис. 16. На этой диаграмме 1 — начальное состояние
применяя способ, показанный на диаграмме рис. 16. На этой диаграмме 1 — начальное состояние  только что достигнутое и описанное с помощью уравнения (9.5) состояние
только что достигнутое и описанное с помощью уравнения (9.5) состояние  Теперь отделим газ от металлического тела, приведем его в соприкосновение с источником тепла
Теперь отделим газ от металлического тела, приведем его в соприкосновение с источником тепла  и будем изотермически сжимать до объема
и будем изотермически сжимать до объема  (путь
(путь  на диаграмме). Объем
на диаграмме). Объем  выбран таким образом, чтобы начавшееся при
выбран таким образом, чтобы начавшееся при  адиабатное сжатие (путь с) привело к состоянию 1. На пути
адиабатное сжатие (путь с) привело к состоянию 1. На пути  мы должны затратить работу
мы должны затратить работу  Работа при адиабатном сжатии с равна росту энергии газа, т. е.
Работа при адиабатном сжатии с равна росту энергии газа, т. е. 
Полученная работа в целом (заштрихованная на диаграмме площадь), следовательно, равна:

Значение  может быть получено из уравнения адиабаты
может быть получено из уравнения адиабаты

Исключая  из этого уравнения и из уравнения (9 5), имеем:
из этого уравнения и из уравнения (9 5), имеем:

Отсюда

или


Рис. 16 Рабочая диаграмма для газа, использованного при охлаждении согласно рис. 15.
Это работа, которая получена при обратимом охлаждении первого металлического тела от температуры  до
до  Работа, которую можно получить при обратимом нагреве второго тела от температуры
Работа, которую можно получить при обратимом нагреве второго тела от температуры  до
до  следует из этого же уравнения при перемене знака при
следует из этого же уравнения при перемене знака при  на обратный:
на обратный:

Следовательно, полученная работа в целом равна:

Этот результат в точности совпадает [сравни уравнения (9.1) и (9.2)] с полученным выше из общих рассуждений.
При малых значениях  при
при  приближенно можно записать:
приближенно можно записать:

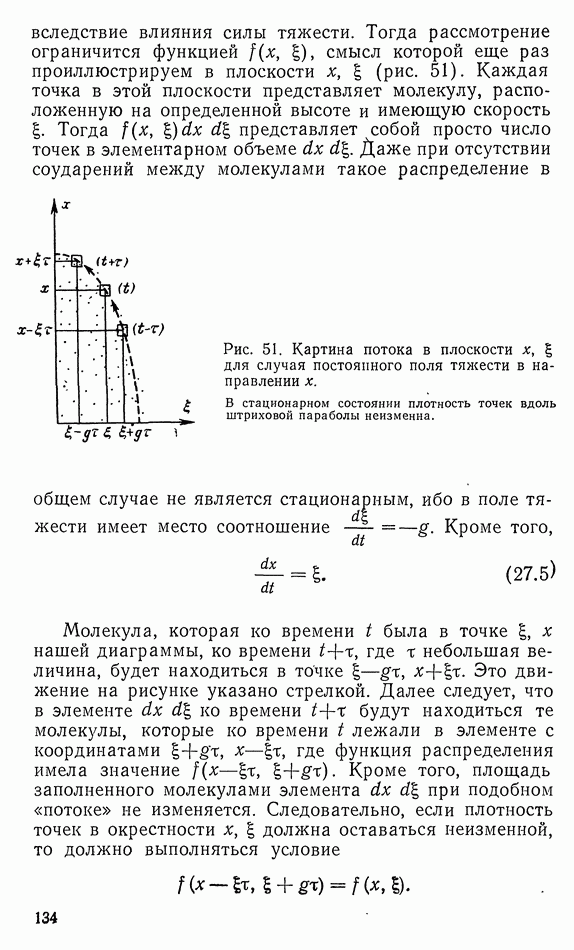
Последний способ записи приводит к следующей интерпретации. Заданную вначале разность температур  можно использовать при сооружении машины Карно.
можно использовать при сооружении машины Карно.  количество тепла, отнятое из верх него источника тепла, доля которого
количество тепла, отнятое из верх него источника тепла, доля которого  превращается в работу при обратимом проведении процесса. (Если бы разность температур.
превращается в работу при обратимом проведении процесса. (Если бы разность температур.  поддерживалась постоянной, то k.
поддерживалась постоянной, то k.  был бы равен
был бы равен  нашем случае разность температур снижается до нуля. Поэтому в целом мы получаем только половину этого значения.)
нашем случае разность температур снижается до нуля. Поэтому в целом мы получаем только половину этого значения.)
Если бы мы имели теперь процесс, при котором между двумя соприкасающимися телами самопроизвольно возникла бы разность температур  т. е. энтропия снизилась бы на величину
т. е. энтропия снизилась бы на величину  то мы смогли бы по достижении этой температуры отделить тела друг
то мы смогли бы по достижении этой температуры отделить тела друг 
друга и с помощью описанного процесса обратимым образом вновь выровнять температуры обоих тел  для обоих тел). При этом была бы совершена работа
для обоих тел). При этом была бы совершена работа  за счет теплового источника
за счет теплового источника  Если бы вновь самопроизвольно появилась разность температур, то эту операцию можно было бы повторить снова и т. д. Следовательно, налицо был бы перпетуум мобиле.
Если бы вновь самопроизвольно появилась разность температур, то эту операцию можно было бы повторить снова и т. д. Следовательно, налицо был бы перпетуум мобиле.
После рассмотрения этих частных необратимых процессов можно кратко изложить закон приращения энтропии в общем случае. В соответствии с основным уравнением  Здесь
Здесь  представляет собой тепло, подведенное к системе с помощью обратимого процесса,
представляет собой тепло, подведенное к системе с помощью обратимого процесса,  совершенную над системой работу;
совершенную над системой работу;  является, следовательно, работой, отданной системой в окружающую среду, иначе говоря, полученной работой. Если, таким образом, при обратимом процессе энергия
является, следовательно, работой, отданной системой в окружающую среду, иначе говоря, полученной работой. Если, таким образом, при обратимом процессе энергия  остается постоянной, то с ростом энтропии
остается постоянной, то с ростом энтропии  связано получение работы
связано получение работы  При этом процессе система должна быть в контакте с источником тепла, от которого она отнимает тепло, так как в противном случае ее энергия снижалась бы на величину совершенной работы. Полученная работа, следовательно, в энергетическом смысле черпается из источника тепла. Напротив, при необратимом приращении энтропии изолированной системы О и несмотря на это
При этом процессе система должна быть в контакте с источником тепла, от которого она отнимает тепло, так как в противном случае ее энергия снижалась бы на величину совершенной работы. Полученная работа, следовательно, в энергетическом смысле черпается из источника тепла. Напротив, при необратимом приращении энтропии изолированной системы О и несмотря на это  Доказательство поставленного в заголовок этого параграфа закона вытекает из следующего рассуждения. Если предположить, что в изолированной системе произошел связанный со снижением энтропии
Доказательство поставленного в заголовок этого параграфа закона вытекает из следующего рассуждения. Если предположить, что в изолированной системе произошел связанный со снижением энтропии  процесс, то вслед за ним можно было бы осуществить обратимый процесс с возрастанием энтропии
процесс, то вслед за ним можно было бы осуществить обратимый процесс с возрастанием энтропии  при котором совершалась бы работа
при котором совершалась бы работа  за счет примыкающего к системе теплового источника.
за счет примыкающего к системе теплового источника.
Закон возрастания энтропии для всех естественных процессов образует фундамент других разделов учения о теплоте. Среди них нужно отметить:
1. Учение о равновесии. В изолированной системе не могут протекать такие процессы, как, например, испарение или химическая реакция, если бы эти процессы были связаны с уменьшением энтропии. Следовательно, система находится в равновесии, если ее энтропия имеет самое большое соответствующее заданным условиям (например, постоянство общей энергии, общего объема, общего числа частиц) значение. В разделе  (стр. 82) мы детально остановимся на этом пункте.
(стр. 82) мы детально остановимся на этом пункте.
2. Термодинамика необратимых процессов. Эта интенсивно развивающаяся в последнее время область основывается на другом способе записи закона приращения энтропии. Утверждение, что при каждом необратимом процессе энтропия возрастает, изменяется следующим образом. Тенденция энтропии к приращению является «первопричиной» необратимого процесса. Связанное с каким-либо процессом возрастание энтропии может рассматриваться как «сила», которая приводит в действие процесс. Детальные рассуждения об этом мы проведем в гл. 7.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА РУССКОГО ПЕРЕВОДА
- ГЛАВА ПЕРВАЯ. ТЕРМОДИНАМИКА
- 1. ПОНЯТИЕ ТЕМПЕРАТУРЫ И УРАВНЕНИЕ СОСТОЯНИЯ ИДЕАЛЬНОГО ГАЗА
- 2. ПАРАМЕТРЫ СОСТОЯНИЯ
- 3. ПЕРВЫЙ ОСНОВНОЙ ЗАКОН
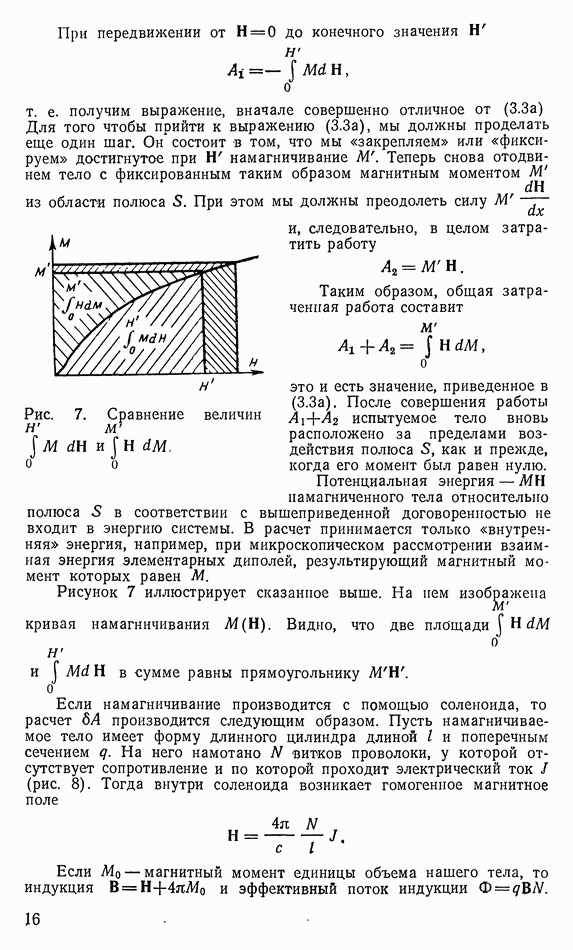
- б) Намагничивание
- в) Энергия идеального газа
- 4. УДЕЛЬНАЯ ТЕПЛОЕМКОСТЬ
- б) Адиабатный процесс
- в) Применение для расчета скорости звука
- г) Энергия и удельная теплоемкость идеального газа
- 5. ВТОРОЙ ОСНОВНОЙ ЗАКОН
- 6. КОЭФФИЦИЕНТ ПОЛЕЗНОГО ДЕЙСТВИЯ КАРНО
- 7. ОБЩИЙ СЛУЧАЙ МАШИНЫ КАРНО И ОПРЕДЕЛЕНИЕ АБСОЛЮТНОЙ ТЕМПЕРАТУРЫ
- Б. ЭНТРОПИЯ
- 8. ЭНТРОПИЯ КАК ФУНКЦИЯ СОСТОЯНИЯ
- 9. РОСТ ЭНТРОПИИ В ИЗОЛИРОВАННОЙ СИСТЕМЕ
- 10. ЭНТРОПИЯ ИДЕАЛЬНОГО ГАЗА
- В. НЕКОТОРЫЕ ПРИМЕНЕНИЯ
- 11. СВОБОДНАЯ ЭНЕРГИЯ
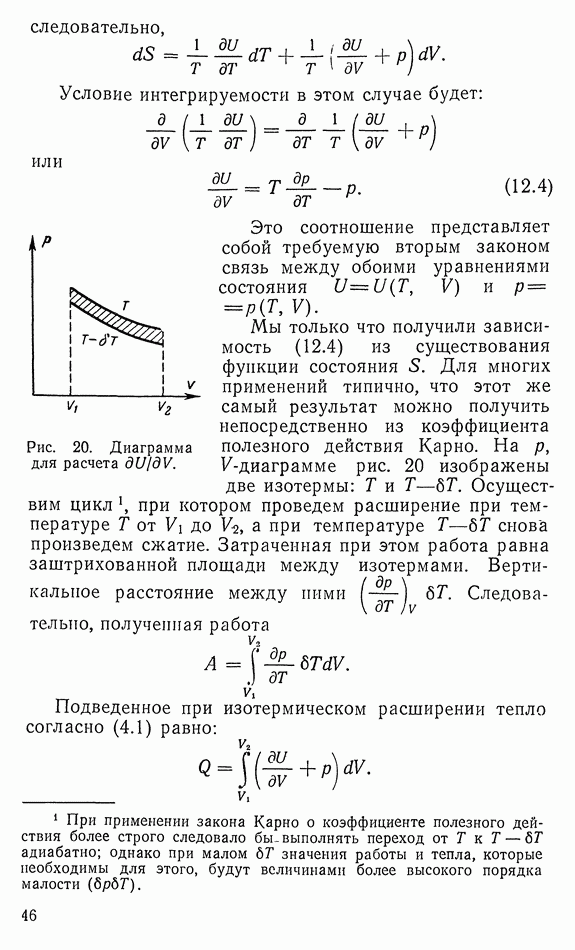
- 12. УРАВНЕНИЕ СОСТОЯНИЯ И УСЛОВИЕ ИНТЕГРИРУЕМОСТИ
- 13. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА
- 14. ЭФФЕКТ ДЖОУЛЯ — ТОМСОНА
- Г. МЕТОД КРУГОВЫХ ПРОЦЕССОВ
- 15. ДАВЛЕНИЕ ПАРА (ФОРМУЛА КЛАУЗИУСА — КЛАПЕЙРОНА)
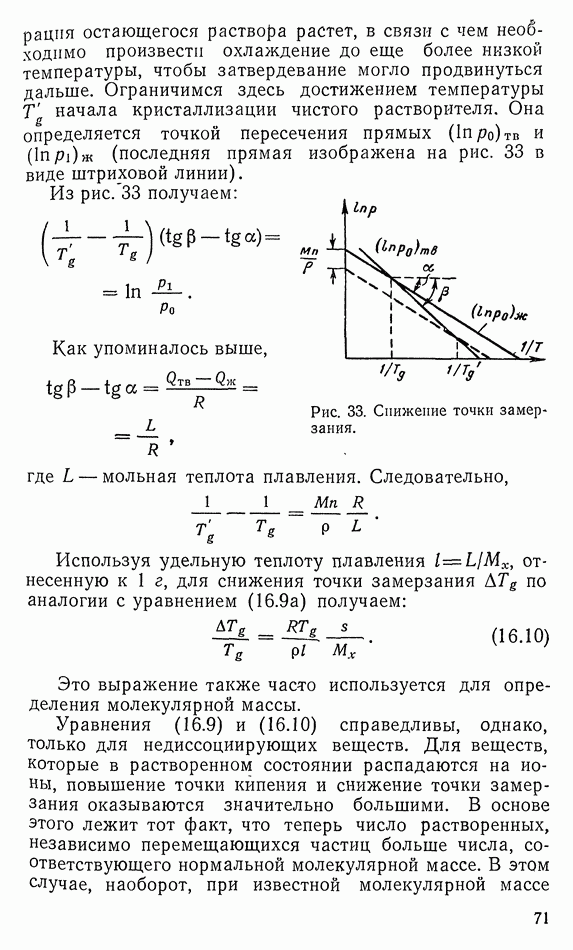
- 16. РАСТВОРЫ
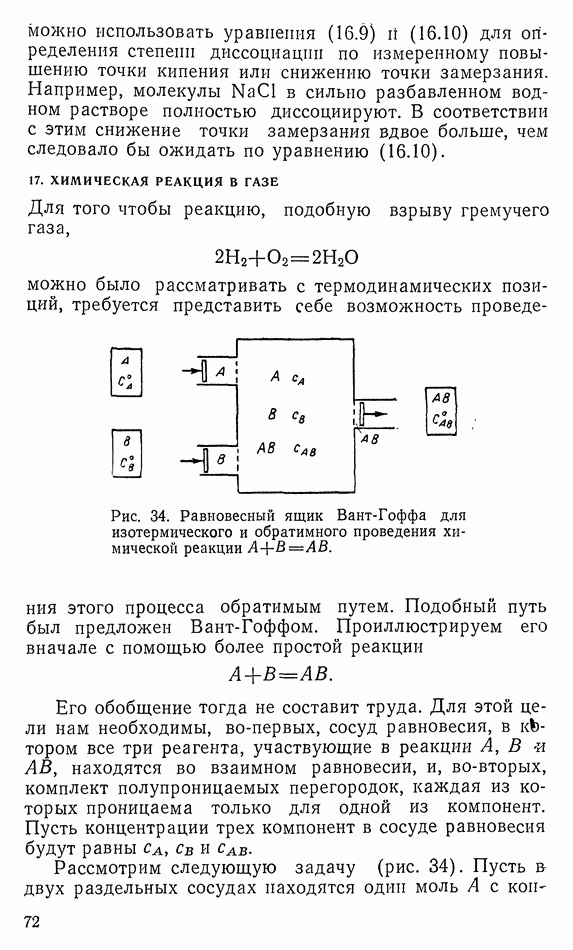
- 17. ХИМИЧЕСКАЯ РЕАКЦИЯ В ГАЗЕ
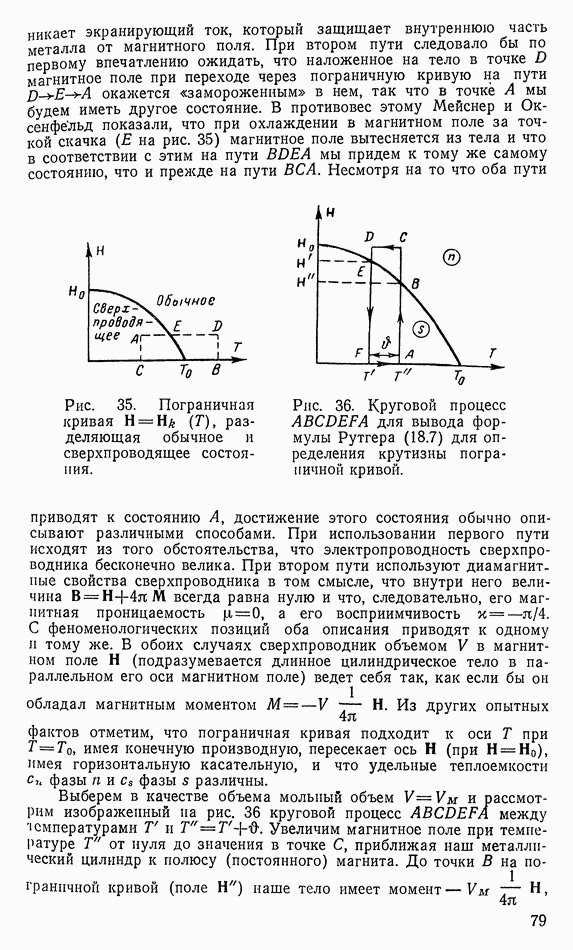
- 18. ПРИМЕР ИЗ СВЕРХПРОВОДИМОСТИ
- Д. ТЕРМОДИНАМИЧЕСКИЕ ФУНКЦИИ И ОБЩЕЕ РАВНОВЕСИЕ
- 19. ТЕРМОДИНАМИЧЕСКИЕ ФУНКЦИИ И ИХ ПРИМЕНЕНИЕ К ГОМОГЕННЫМ ФАЗАМ
- 20. ТЕРМОДИНАМИЧЕСКОЕ РАВНОВЕСИЕ
- 21. ХИМИЧЕСКИЙ ПОТЕНЦИАЛ ИДЕАЛЬНОГО ГАЗА
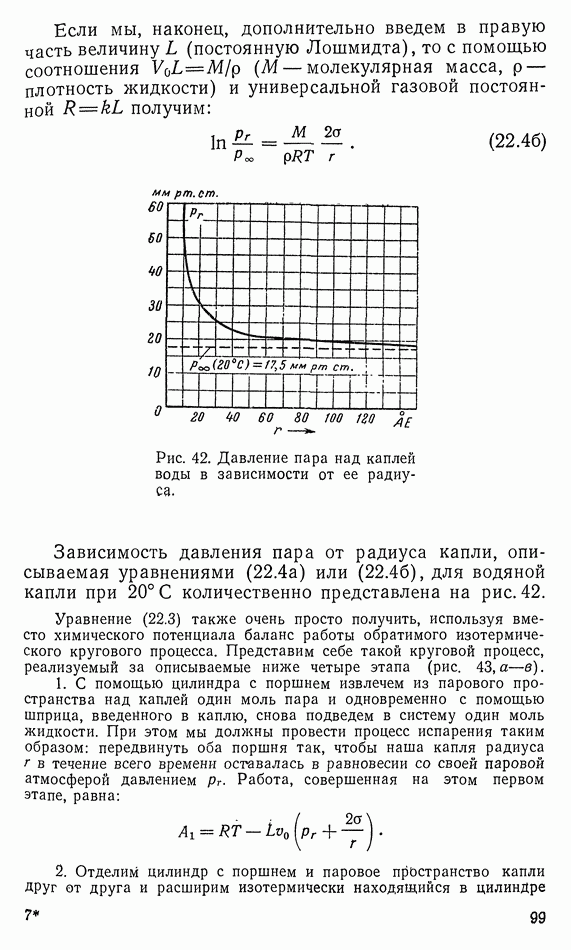
- 22. ДАВЛЕНИЕ ПАРА НАД НЕБОЛЬШОЙ КАПЛЕЙ
- ГЛАВА ВТОРАЯ. СТАТИСТИЧЕСКАЯ МЕХАНИКА
- А. КИНЕТИЧЕСКАЯ ТЕОРИЯ ГАЗОВ
- 24. УРАВНЕНИЕ СОСТОЯНИЯ ИДЕАЛЬНОГО ГАЗА
- 25. МАКСВЕЛЛОВСКОЕ РАСПРЕДЕЛЕНИЕ СКОРОСТЕЙ
- 26. ОБОСНОВАНИЕ БОЛЬЦМАНОМ РАСПРЕДЕЛЕНИЯ СКОРОСТЕЙ МАКСВЕЛЛА И Н-TEOPEMA
- 27. БАРОМЕТРИЧЕСКАЯ ФОРМУЛА
- 28. ТЕОРЕМА О ВИРИАЛЕ
- 29. РАЗРЕЖЕННЫЙ НЕИДЕАЛЬНЫЙ ГАЗ
- Б. НЕКОТОРЫЕ ОСНОВНЫЕ ПОНЯТИЯ МЕХАНИКИ
- 30. УРАВНЕНИЯ ДВИЖЕНЙЯ ГАМИЛЬТОНА
- 31. Г-ПРОСТРАНСТВО
- В. МИКРОКАНОНИЧЕСКИЙ АНСАМБЛЬ
- 32. УСРЕДНЕНИЕ ПО ВРЕМЕНИ И ПО АНСАМБЛЮ
- 33. ПРОСТЕЙШИЕ ПРИМЕНЕНИЯ
- 34. ЭНТРОПИЯ
- 35. ДЕЛЕНИЕ НА N1 И ДЕЙСТВИТЕЛЬНЫЙ ФАЗОВЫЙ ОБЪЕМ
- Г. КАНОНИЧЕСКИЙ АНСАМБЛЬ
- 37. КАНОНИЧЕСКИЙ АНСАМБЛЬ
- 38. МАКРОСКОПИЧЕСКОЕ ТЕЛО
- Д. ДВА ДРУГИХ АНСАМБЛЯ
- 39. СВОБОДНАЯ ЭНТАЛЬПИЯ
- 40. БОЛЬШОЙ КАНОНИЧЕСКИЙ АНСАМБЛЬ (T, V, «мю» ЗАДАНЫ)
- 41. ЗАКЛЮЧЕНИЕ
- ГЛАВА ТРЕТЬЯ. КВАНТОВАЯ СТАТИСТИКА
- 42. ПРЕДВАРИТЕЛЬНОЕ РАССМОТРЕНИЕ НЕКОТОРЫХ РЕЗУЛЬТАТОВ
- 43. НЕКОТОРЫЕ СВЕДЕНИЯ ИЗ КВАНТОВОЙ ТЕОРИИ
- 44. АНСАМБЛЬ ИЛИ СТАТИСТИЧЕСКАЯ СОВОКУПНОСТЬ
- 45. ЭНТРОПИЯ ТЕРМИЧЕСКИ ИЗОЛИРОВАННОЙ СИСТЕМЫ
- 46. КАНОНИЧЕСКИЙ АНСАМБЛЬ
- ГЛАВА ЧЕТВЕРТАЯ. ИДЕАЛЬНЫЕ И РЕАЛЬНЫЕ ГАЗЫ А. ИДЕАЛЬНЫЙ ГАЗ И ВЫРОЖДЕНИЕ ГАЗА
- 47. СТАТИСТИЧЕСКИЙ ИНТЕГРАЛ И СТАТИСТИЧЕСКАЯ СУММА ДЛЯ ЧАСТИЦ
- 48. N ОДИНАКОВЫХ НЕВЗАИМОДЕЙСТВУЮЩИХ ЧАСТИЦ
- 49. СИСТЕМА ИЗОЛИРОВАНА
- 50. СИСТЕМА НАХОДИТСЯ В ТЕРМОСТАТЕ
- 51. БОЛЬШОЙ КАНОНИЧЕСКИЙ АНСАМБЛЬ
- 52. ПРЕДЕЛЬНЫЙ СЛУЧАЙ СИЛЬНОГО РАЗРЕЖЕНИЯ
- 53. ГАЗ ФЕРМИ
- 54. ГАЗ БОЗЕ
- Б. РЕАЛЬНЫЕ ГАЗЫ И КОНДЕНСАЦИЯ
- 56. ОБЛАСТЬ НЕНАСЫЩЕННОГО ПАРА
- 57. КОНДЕНСАЦИЯ
- 58. ЖИДКАЯ ФАЗА
- 59. АНАЛОГИЯ МЕЖДУ ИДЕАЛЬНЫМ ГАЗОМ БОЗЕ И РЕАЛЬНЫМ ГАЗОМ
- 60. ОБРАЗОВАНИЕ ЗАРОДЫШЕЙ
- ГЛАВА ПЯТАЯ. ТВЕРДОЕ ТЕЛО
- 62. КВАНТОВОМЕХАНИЧЕСКОЕ РАССМОТРЕНИЕ И ОБЩИЙ ОБЗОР
- 63. ЛИНЕЙНАЯ ЦЕПЬ
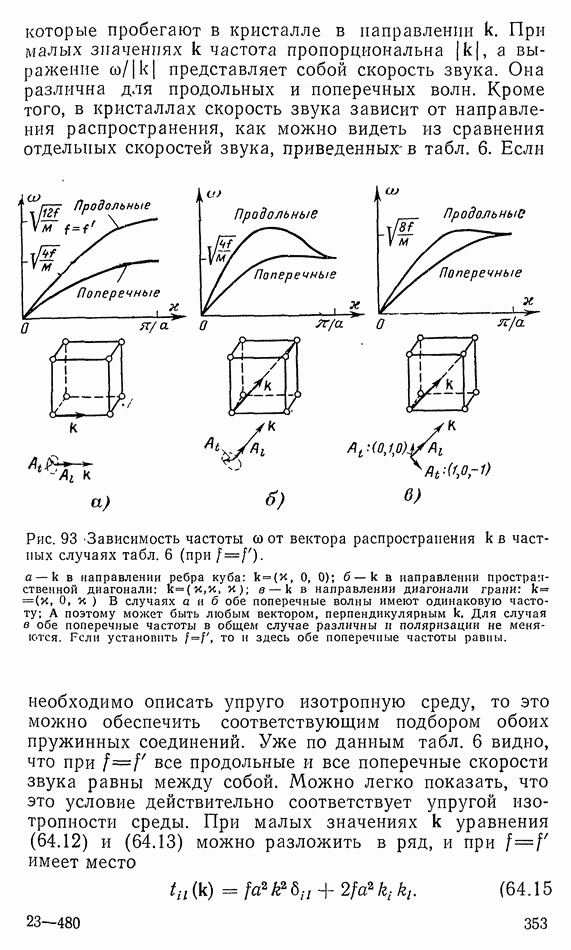
- 64. КОЛЕБАНИЯ ПРОСТРАНСТВЕННОЙ РЕШЕТКИ
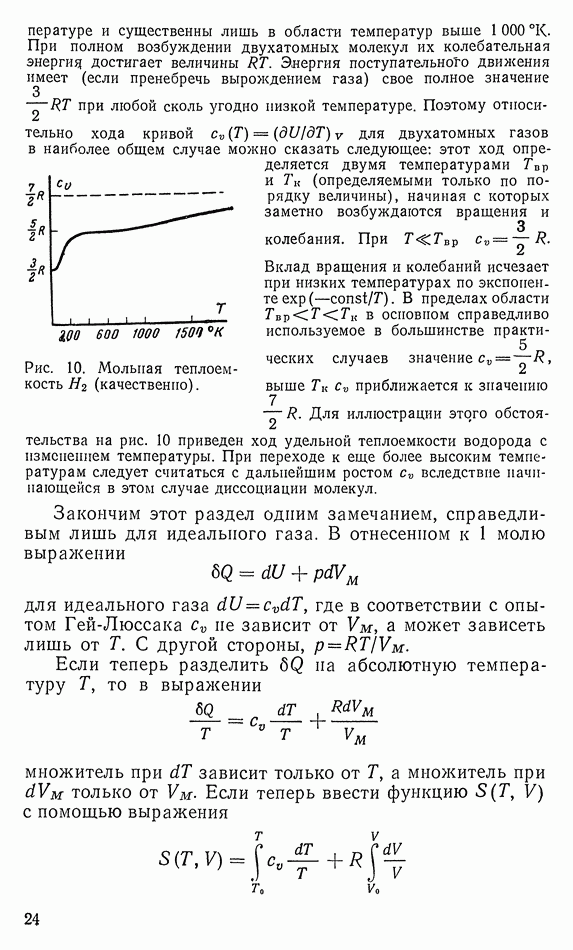
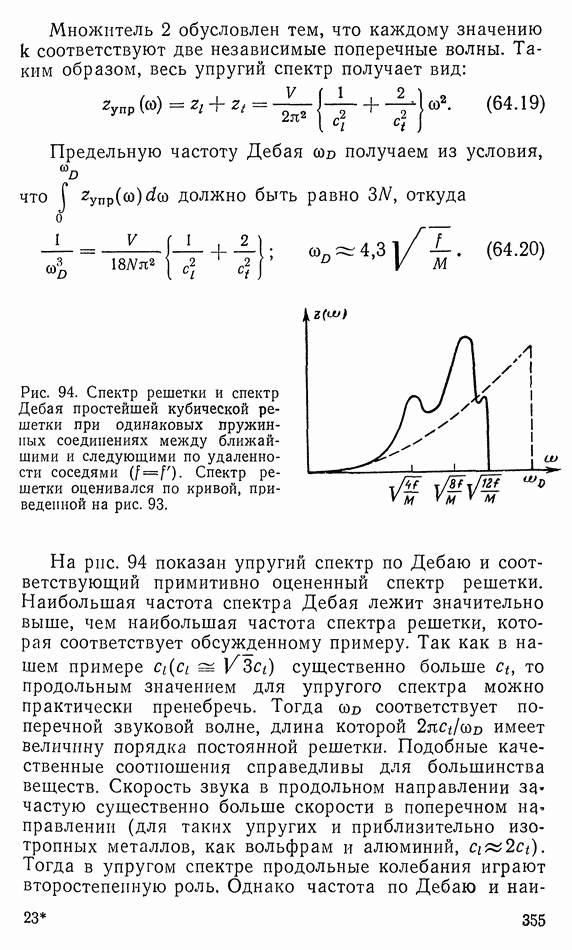
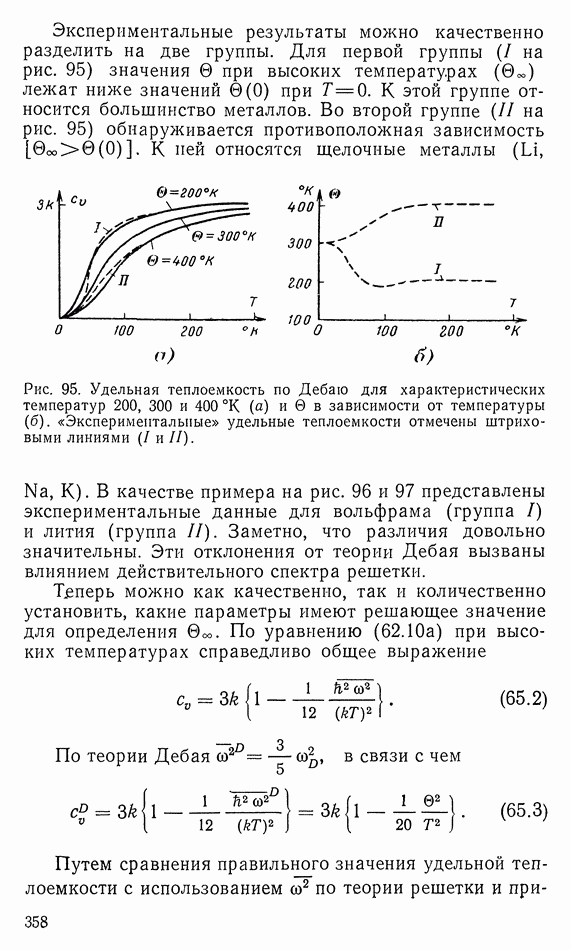
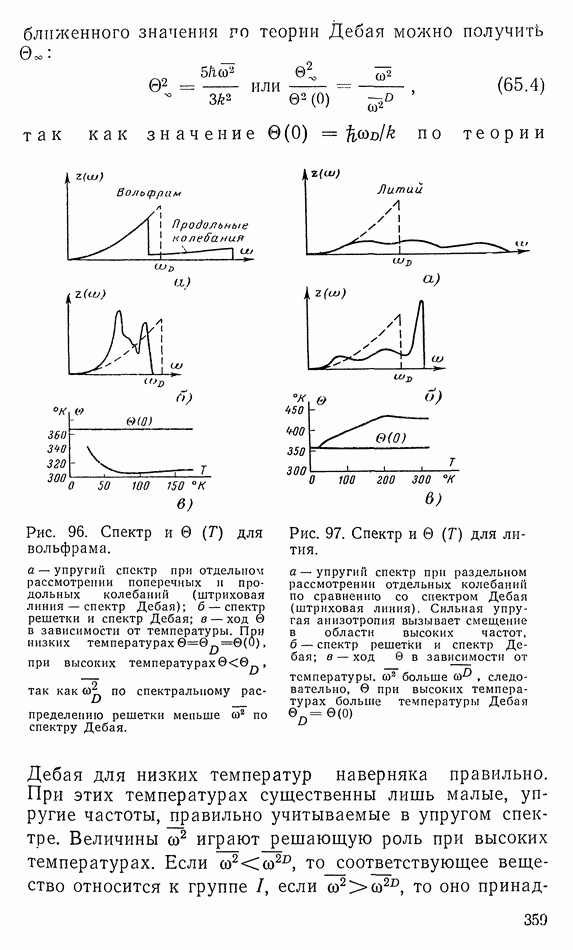
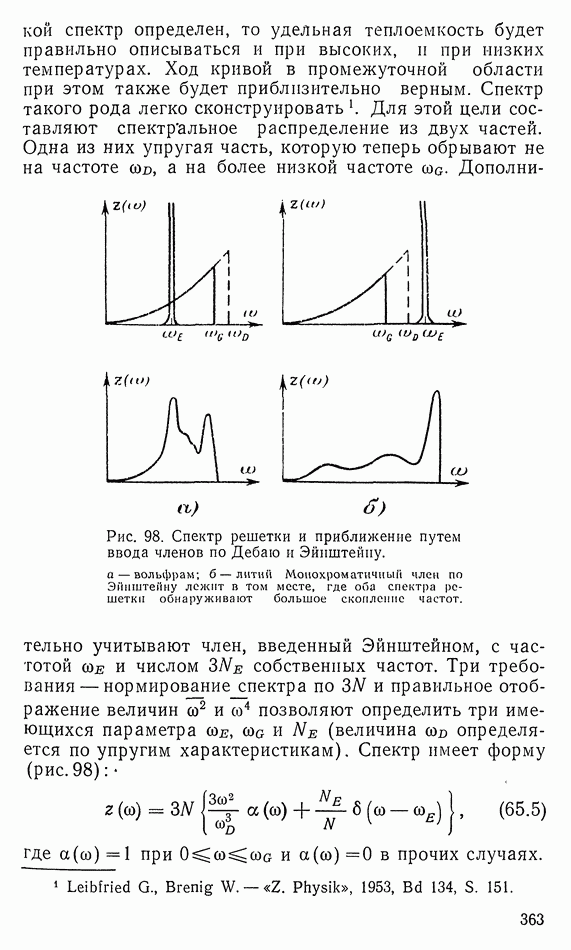
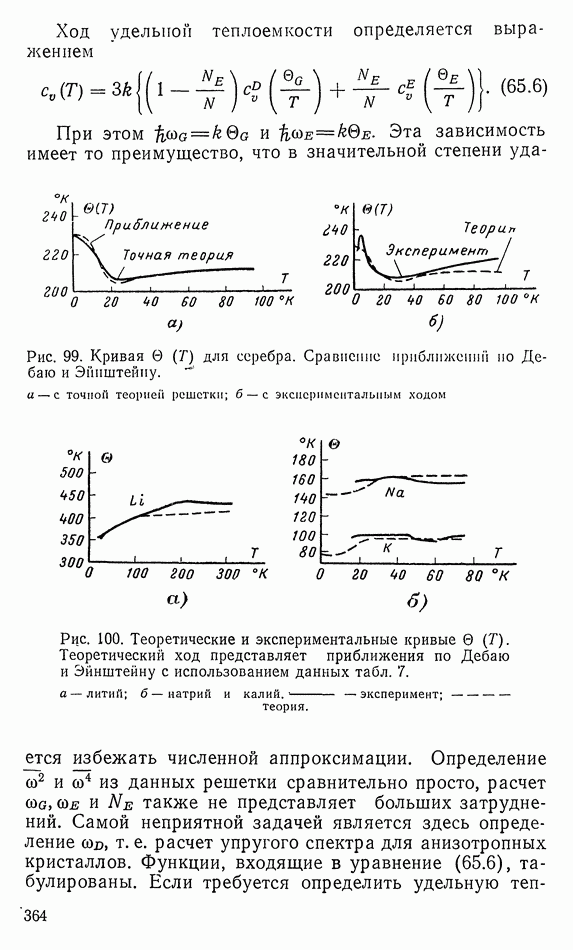
- 65. ОБСУЖДЕНИЕ ХОДА УДЕЛЬНОЙ ТЕПЛОЕМКОСТИ
- Б. УПОРЯДОЧЕННАЯ И НЕУПОРЯДОЧЕННАЯ КРИСТАЛЛИЧЕСКАЯ РЕШЕТКА
- 67. СТАТИСТИЧЕСКИЙ МЕТОД
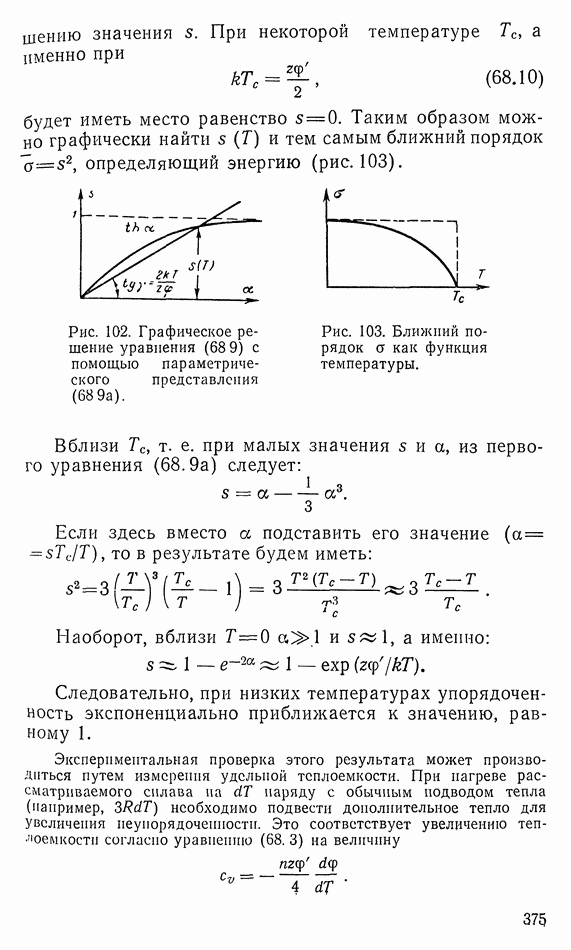
- 68. СВЕРХСТРУКТУРА
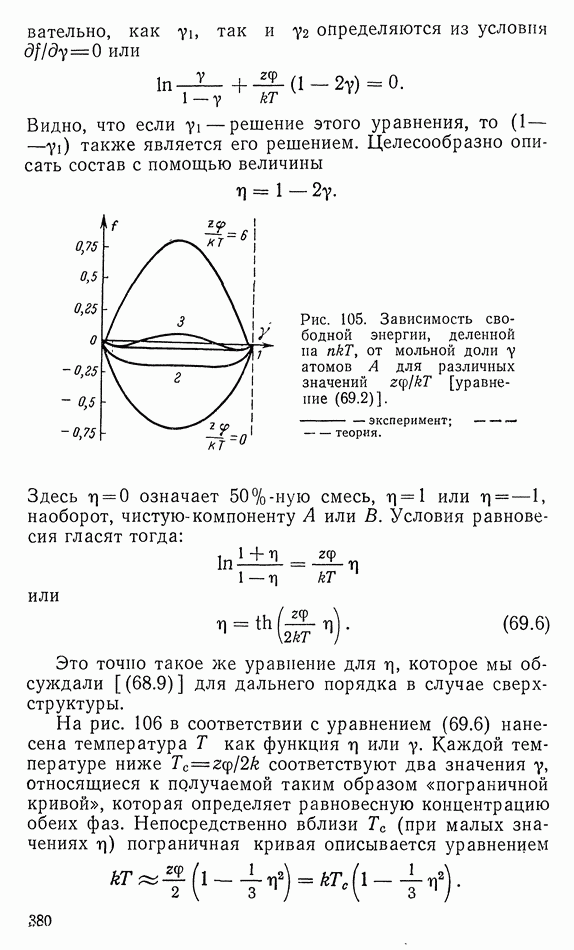
- 60. РАЗДЕЛЕНИЕ ФАЗ («фи» ПОЛОЖИТЕЛЬНО)
- 70. ФЕРРОМАГНЕТИЗМ
- 71. ПРИБЛИЖЕНИЕ БЭТЕ ДЛЯ МОДЕЛИ ИЗИНГА
- 72. ЛИНЕИНАЯ И ПЛОСКАЯ РЕШЕТКИ ПО МЕТОДУ МАТРИЦ
- ГЛАВА ШЕСТАЯ. ФЛУКТУАЦИИ И БРОУНОВСКОЕ ДВИЖЕНИЕ
- 74. ЯВЛЕНИЯ ФЛУКТУАЦИЙ
- Б. БРОУНОВСКОЕ ДВИЖЕНИЕ
- 76. ПОДВИЖНОСТЬ И ДИФФУЗИЯ
- 77. УРАВНЕНИЕ ЛАНЖЕВЕНА
- 78. МЕТОД ЭЙНШТЕЙНА И ХОПФА
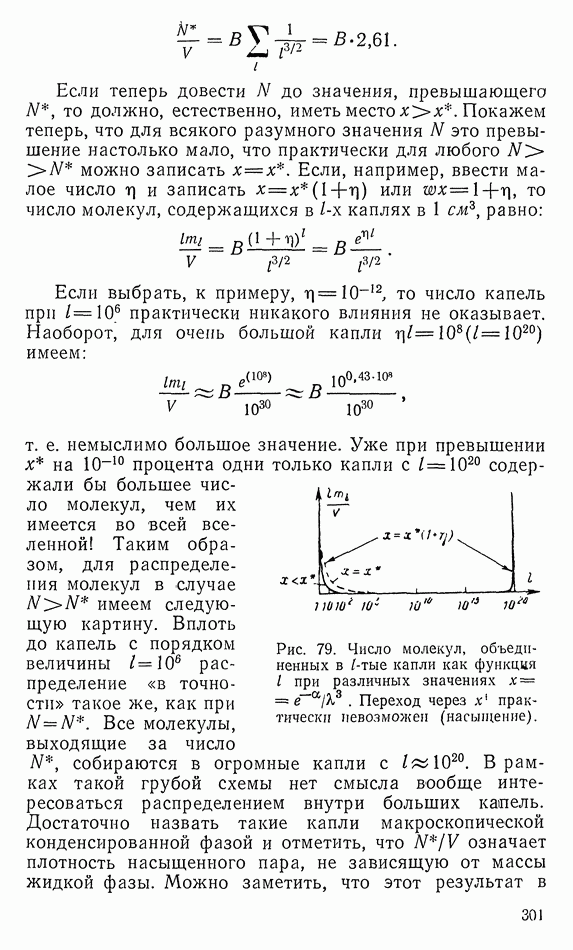
- 79. УСТАНОВЛЕНИЕ РАСПРЕДЕЛЕНИЯ МАКСВЕЛЛА
- 80. НЕКОТОРЫЕ СВЕДЕНИЯ О СЛУЧАЙНОМ ДВИЖЕНИИ
- 81. КОРРЕЛЯЦИЯ ДЛЯ СТАТИСТИЧЕСКИ ИЗМЕНЯЮЩЕЙСЯ ФУНКЦИИ
- 82. ДИФФЕРЕНЦИАЛЬНОЕ УРАВНЕНИЕ ФОККЕРА — ПЛАНКА
- 83. СПЕКТРАЛЬНОЕ РАЗЛОЖЕНИЕ СТАТИСТИЧЕСКОЙ ФУНКЦИИ
- 84. СЛАБО ДЕМПФИРОВАННЫЙ ОСЦИЛЛЯТОР С ЗАТУХАНИЕМ, ЗАВИСЯЩИМ ОТ ЧАСТОТЫ
- 85. ФОРМУЛА НАЙКВИСТА
- 86. ДРОБОВОЙ ЭФФЕКТ
- ГЛАВА СЕДЬМАЯ. ТЕРМОДИНАМИКА НЕОБРАТИМЫХ ПРОЦЕССОВ
- 88. НЕОБРАТИМЫЕ ПРОЦЕССЫ В СТАТИСТИЧЕСКОЙ МЕХАНИКЕ
- 89. ОДНОВРЕМЕННОЕ НАБЛЮДЕНИЕ НЕСКОЛЬКИХ МАКРОСКОПИЧЕСКИХ ВЕЛИЧИН
- 90. МЕТОД КОКСА
- 91. ОБМЕН ТЕПЛОМ И ЧАСТИЦАМИ
- 92. НЕКОТОРЫЕ ПРИМЕНЕНИЯ
- 93. МЕТОД ТОМСОНА И ЕГО ПОДТВЕРЖДЕНИЕ СООТНОШЕНИЯМИ ОНЗАГЕРА
- 94. ТЕРМОЭЛЕКТРИЧЕСКИЕ ЯВЛЕНИЯ. ВЫВОД ТОМСОНА
- 95. ТЕРМОЭЛЕКТРИЧЕСКИЕ ЯВЛЕНИЯ. ОБСУЖДЕНИЕ С ПОМОЩЬЮ СООТНОШЕНИЯ ВЗАИМНОСТИ ОНЗАГЕРА