| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
21. ХИМИЧЕСКИЙ ПОТЕНЦИАЛ ИДЕАЛЬНОГО ГАЗА
Для того чтобы для газа, состоящего из компонент  с числами молекул
с числами молекул  рассчитать соответствующие химические потенциалы
рассчитать соответствующие химические потенциалы  определим вначале в соответствии с уравнением (19.5) свободную энергию
определим вначале в соответствии с уравнением (19.5) свободную энергию  Для энтропии в § 10 мы нашли:
Для энтропии в § 10 мы нашли:

 представляет собой вклад вращательных и колебательных степеней свободы в удельную теплоемкость,
представляет собой вклад вращательных и колебательных степеней свободы в удельную теплоемкость,  энтропийную постоянную компоненты
энтропийную постоянную компоненты  При определении энергии мы должны установить единообразный нулевой уровень энергии. В качестве такового мы принимаем: «находящийся в покое, изолированный, простой атом имеет энергию, равную нулю». Если теперь
При определении энергии мы должны установить единообразный нулевой уровень энергии. В качестве такового мы принимаем: «находящийся в покое, изолированный, простой атом имеет энергию, равную нулю». Если теперь  сложная молекула, то при
сложная молекула, то при  мы должны приписать ей энергию —
мы должны приписать ей энергию —  причем
причем  означает энергию, необходимую для разложения молекулы на отдельные свободные атомы (энергия диссоциации).
означает энергию, необходимую для разложения молекулы на отдельные свободные атомы (энергия диссоциации).
Следовательно, для отдельного атома (согласно определению)  После такого выбора
После такого выбора

Таким образом,

Частная производная  по
по  представляет собой искомый химический потенциал
представляет собой искомый химический потенциал  Если ввести парциальное давление
Если ввести парциальное давление  компоненты
компоненты

то получим:

Если нас интересует зависимость  только от давления, то можно воспользоваться сокращенной формой записи
только от давления, то можно воспользоваться сокращенной формой записи

где  функция только температуры.
функция только температуры.
Используя общее выражение (21.3), мы можем расшифровать условие равновесия  для химической реакции
для химической реакции  При этом учтем, что величина
При этом учтем, что величина 

представляет собой константу равновесия, отнесенную к парциальному давлению, и что величина  означает тепловой эффект, экстраполированный на случай
означает тепловой эффект, экстраполированный на случай 
Вначале из уравнения (21.3) получаем:

Таким образом, константа равновесия будет равна: 

Тем самым мы снова пришли точно к выражению (17.11), полученному выше с помощью метода круговых процессов. Сверх того мы привели оставшуюся там не определенной постоянную интегрирования К к энтропийным постоянным  компонент, принимающих участие в реакции. Величина
компонент, принимающих участие в реакции. Величина

также уже известна нам: в § 15 мы определили ее как «постоянную давления пара».
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ РЕДАКТОРА РУССКОГО ПЕРЕВОДА
- ГЛАВА ПЕРВАЯ. ТЕРМОДИНАМИКА
- 1. ПОНЯТИЕ ТЕМПЕРАТУРЫ И УРАВНЕНИЕ СОСТОЯНИЯ ИДЕАЛЬНОГО ГАЗА
- 2. ПАРАМЕТРЫ СОСТОЯНИЯ
- 3. ПЕРВЫЙ ОСНОВНОЙ ЗАКОН
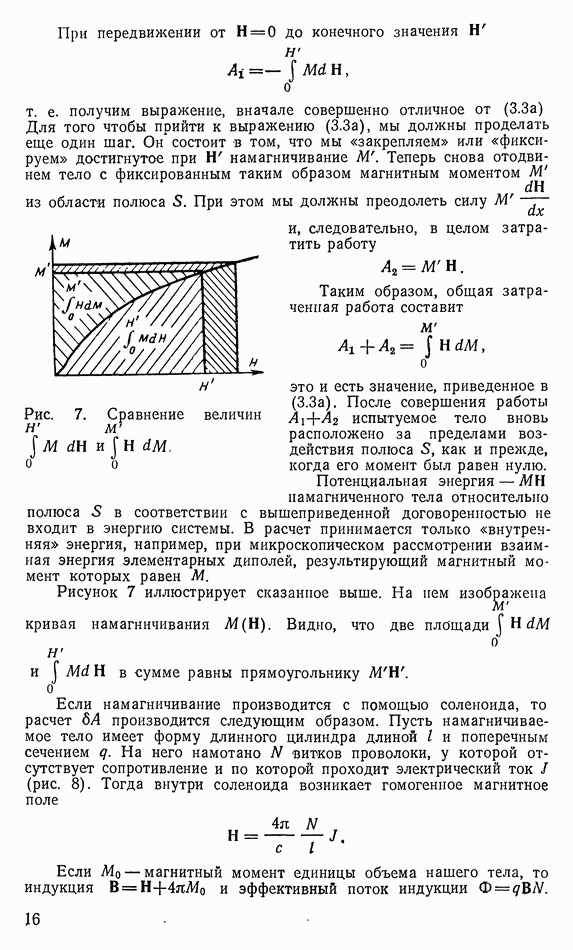
- б) Намагничивание
- в) Энергия идеального газа
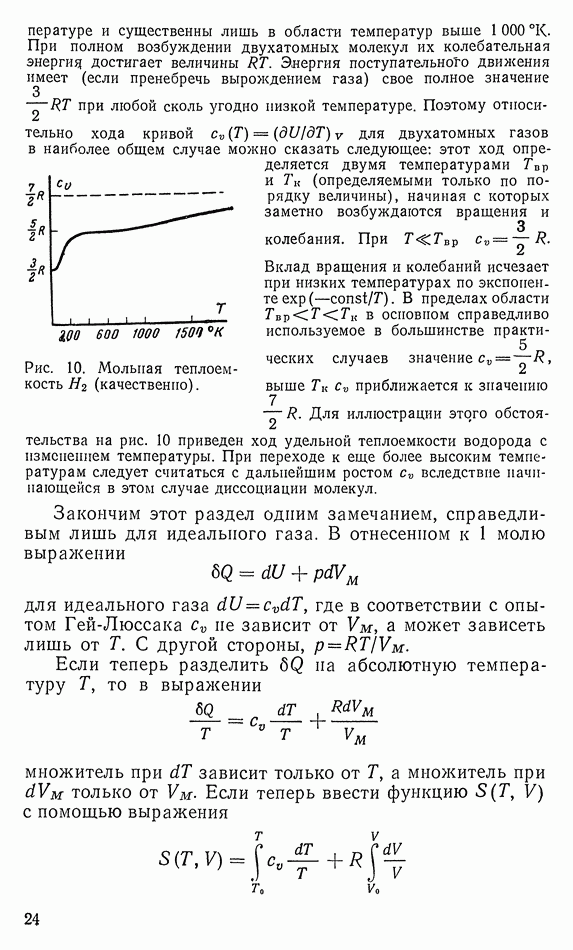
- 4. УДЕЛЬНАЯ ТЕПЛОЕМКОСТЬ
- б) Адиабатный процесс
- в) Применение для расчета скорости звука
- г) Энергия и удельная теплоемкость идеального газа
- 5. ВТОРОЙ ОСНОВНОЙ ЗАКОН
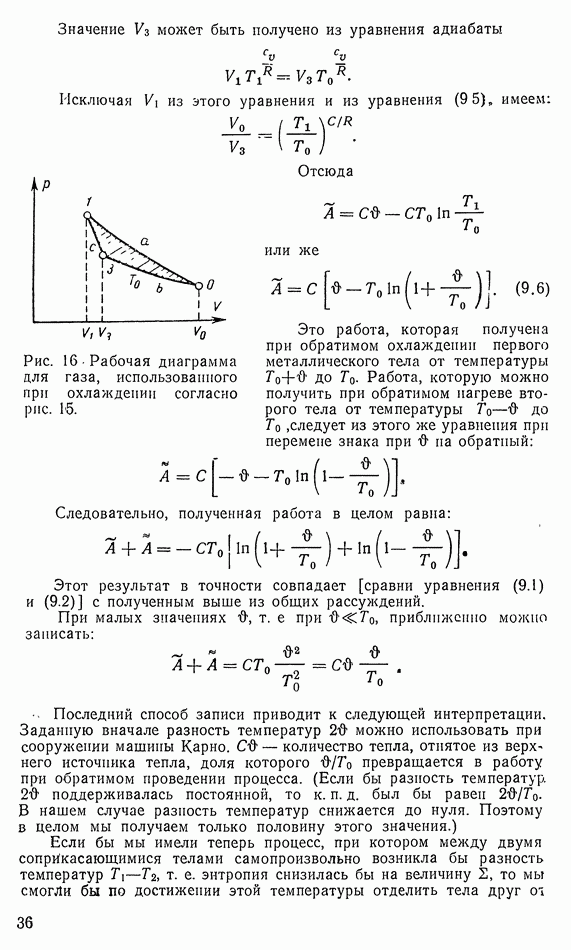
- 6. КОЭФФИЦИЕНТ ПОЛЕЗНОГО ДЕЙСТВИЯ КАРНО
- 7. ОБЩИЙ СЛУЧАЙ МАШИНЫ КАРНО И ОПРЕДЕЛЕНИЕ АБСОЛЮТНОЙ ТЕМПЕРАТУРЫ
- Б. ЭНТРОПИЯ
- 8. ЭНТРОПИЯ КАК ФУНКЦИЯ СОСТОЯНИЯ
- 9. РОСТ ЭНТРОПИИ В ИЗОЛИРОВАННОЙ СИСТЕМЕ
- 10. ЭНТРОПИЯ ИДЕАЛЬНОГО ГАЗА
- В. НЕКОТОРЫЕ ПРИМЕНЕНИЯ
- 11. СВОБОДНАЯ ЭНЕРГИЯ
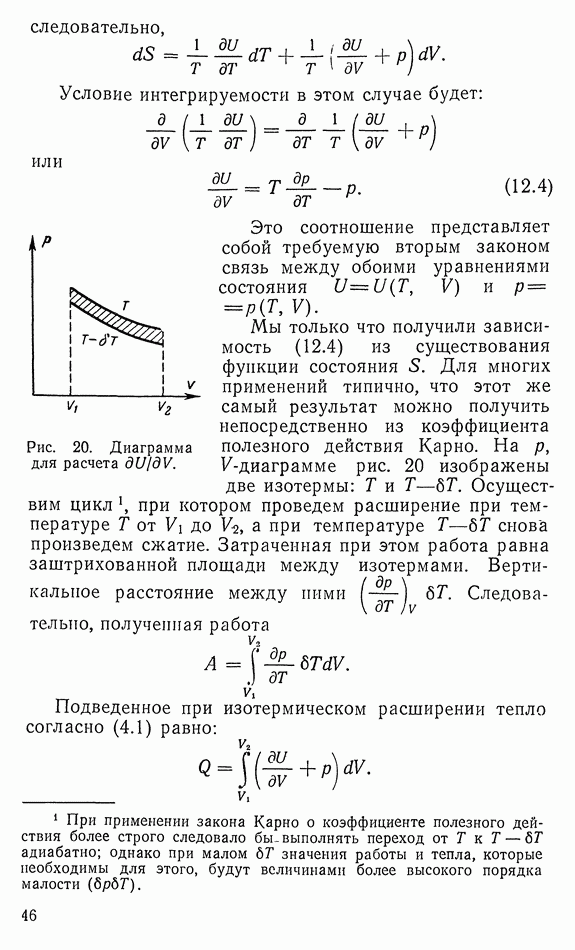
- 12. УРАВНЕНИЕ СОСТОЯНИЯ И УСЛОВИЕ ИНТЕГРИРУЕМОСТИ
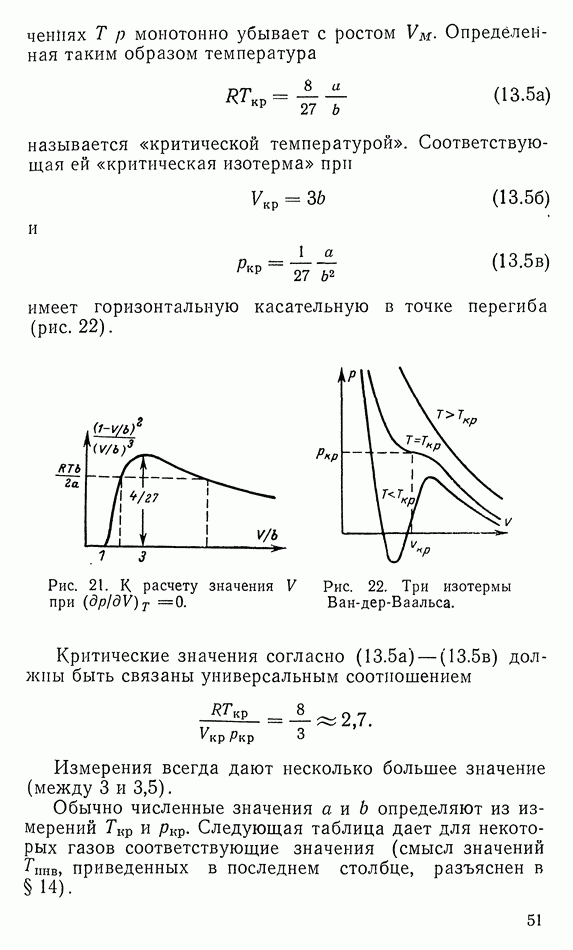
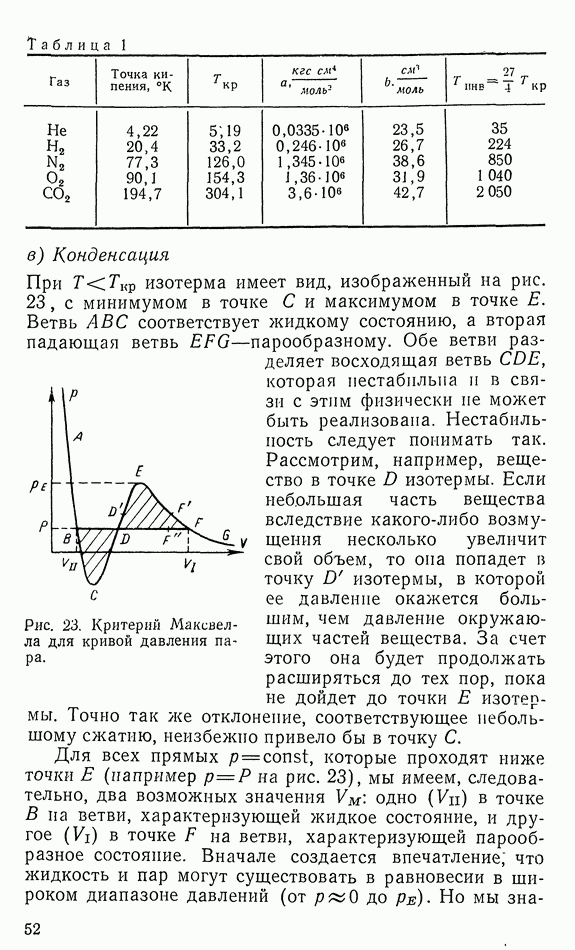
- 13. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА
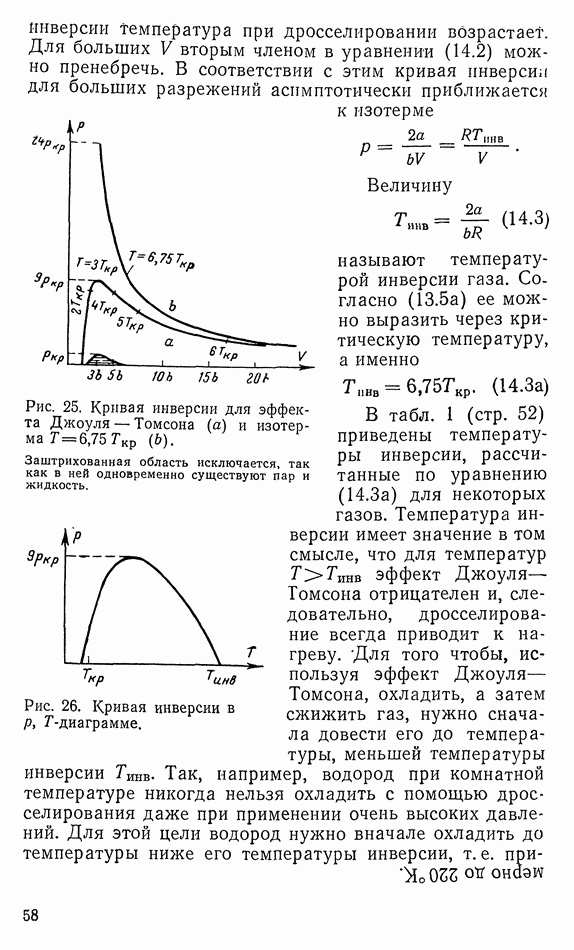
- 14. ЭФФЕКТ ДЖОУЛЯ — ТОМСОНА
- Г. МЕТОД КРУГОВЫХ ПРОЦЕССОВ
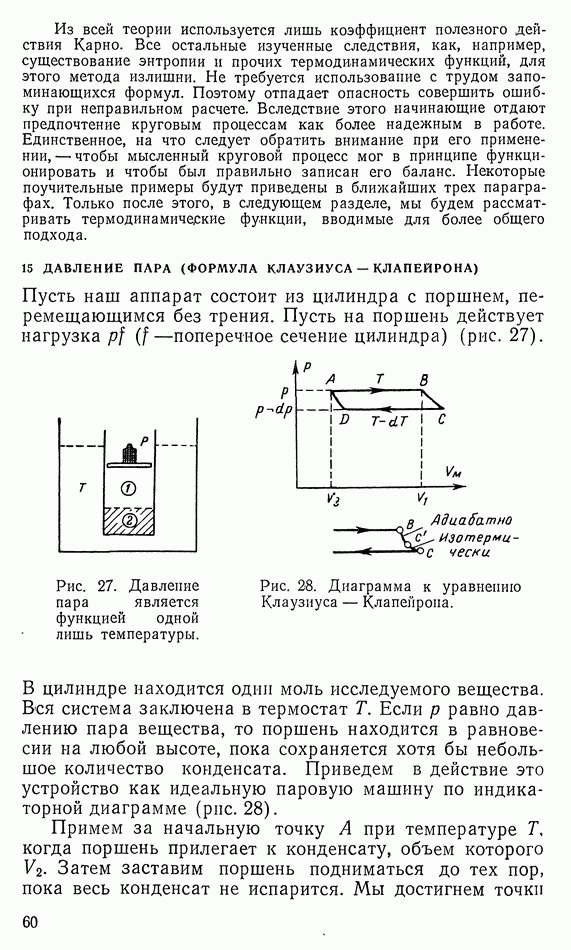
- 15. ДАВЛЕНИЕ ПАРА (ФОРМУЛА КЛАУЗИУСА — КЛАПЕЙРОНА)
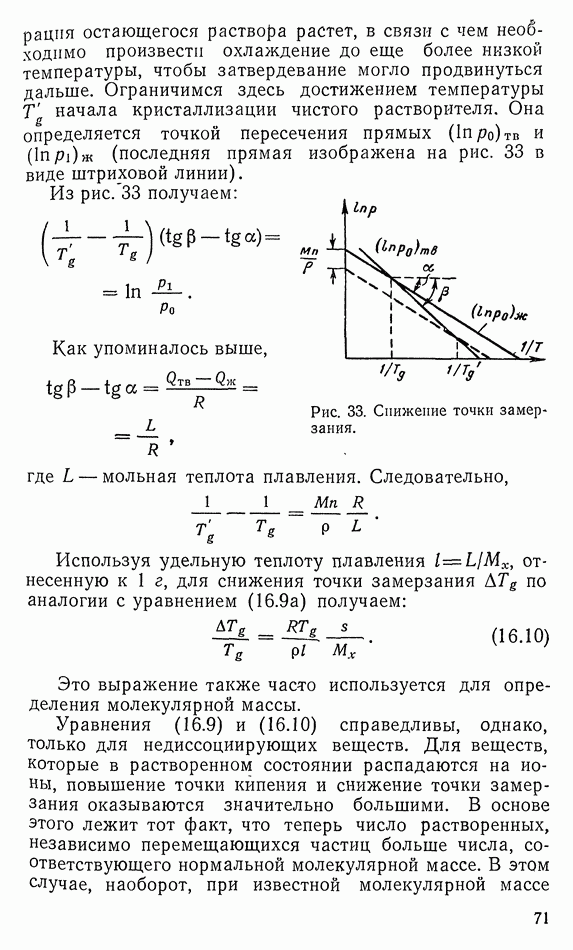
- 16. РАСТВОРЫ
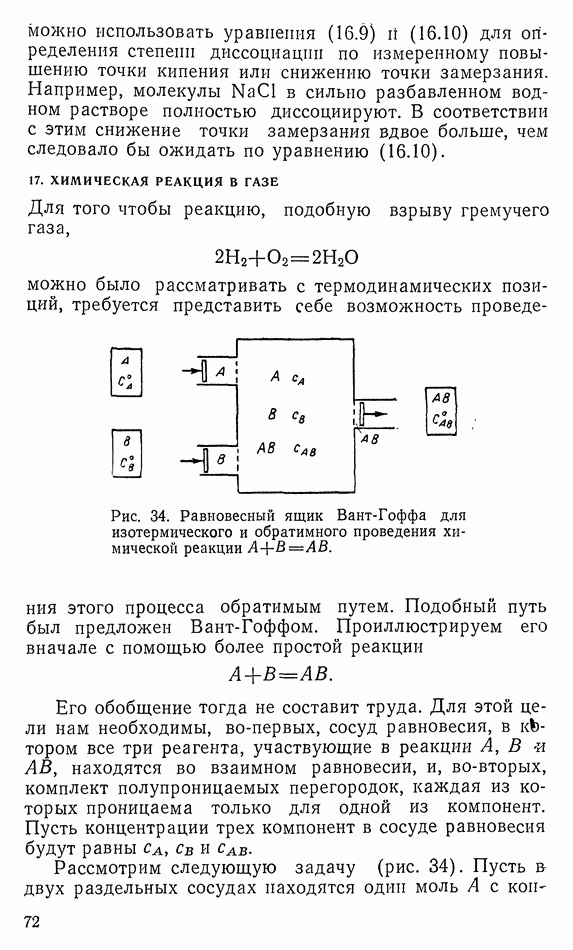
- 17. ХИМИЧЕСКАЯ РЕАКЦИЯ В ГАЗЕ
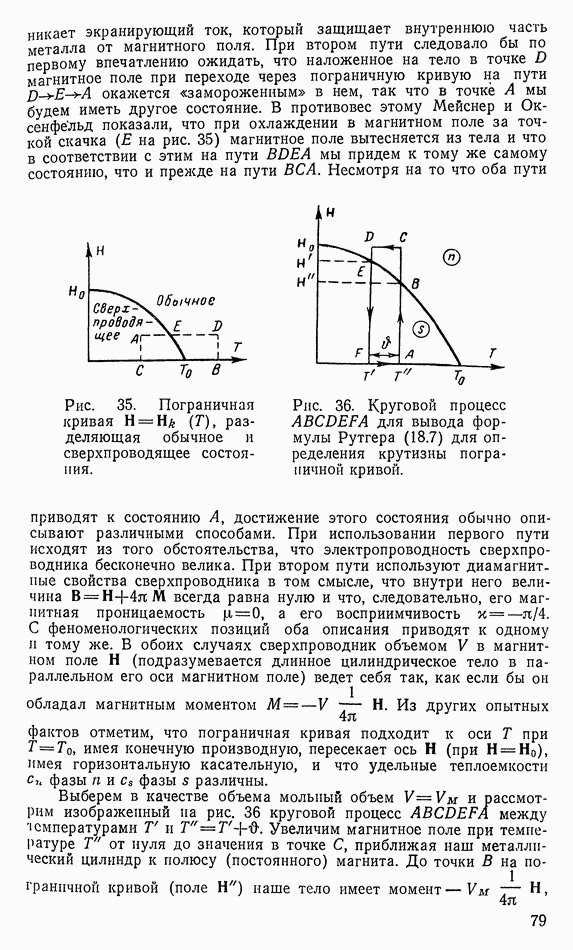
- 18. ПРИМЕР ИЗ СВЕРХПРОВОДИМОСТИ
- Д. ТЕРМОДИНАМИЧЕСКИЕ ФУНКЦИИ И ОБЩЕЕ РАВНОВЕСИЕ
- 19. ТЕРМОДИНАМИЧЕСКИЕ ФУНКЦИИ И ИХ ПРИМЕНЕНИЕ К ГОМОГЕННЫМ ФАЗАМ
- 20. ТЕРМОДИНАМИЧЕСКОЕ РАВНОВЕСИЕ
- 21. ХИМИЧЕСКИЙ ПОТЕНЦИАЛ ИДЕАЛЬНОГО ГАЗА
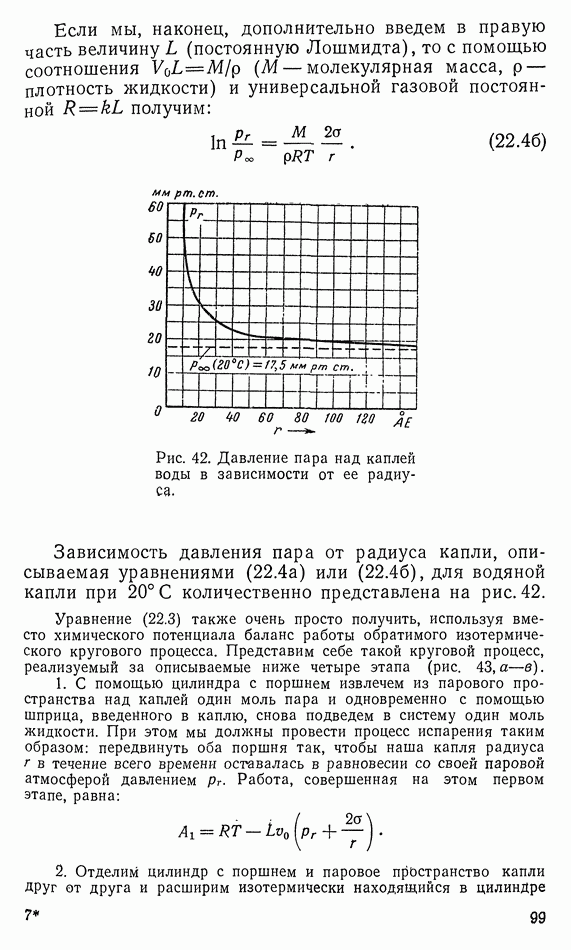
- 22. ДАВЛЕНИЕ ПАРА НАД НЕБОЛЬШОЙ КАПЛЕЙ
- ГЛАВА ВТОРАЯ. СТАТИСТИЧЕСКАЯ МЕХАНИКА
- А. КИНЕТИЧЕСКАЯ ТЕОРИЯ ГАЗОВ
- 24. УРАВНЕНИЕ СОСТОЯНИЯ ИДЕАЛЬНОГО ГАЗА
- 25. МАКСВЕЛЛОВСКОЕ РАСПРЕДЕЛЕНИЕ СКОРОСТЕЙ
- 26. ОБОСНОВАНИЕ БОЛЬЦМАНОМ РАСПРЕДЕЛЕНИЯ СКОРОСТЕЙ МАКСВЕЛЛА И Н-TEOPEMA
- 27. БАРОМЕТРИЧЕСКАЯ ФОРМУЛА
- 28. ТЕОРЕМА О ВИРИАЛЕ
- 29. РАЗРЕЖЕННЫЙ НЕИДЕАЛЬНЫЙ ГАЗ
- Б. НЕКОТОРЫЕ ОСНОВНЫЕ ПОНЯТИЯ МЕХАНИКИ
- 30. УРАВНЕНИЯ ДВИЖЕНЙЯ ГАМИЛЬТОНА
- 31. Г-ПРОСТРАНСТВО
- В. МИКРОКАНОНИЧЕСКИЙ АНСАМБЛЬ
- 32. УСРЕДНЕНИЕ ПО ВРЕМЕНИ И ПО АНСАМБЛЮ
- 33. ПРОСТЕЙШИЕ ПРИМЕНЕНИЯ
- 34. ЭНТРОПИЯ
- 35. ДЕЛЕНИЕ НА N1 И ДЕЙСТВИТЕЛЬНЫЙ ФАЗОВЫЙ ОБЪЕМ
- Г. КАНОНИЧЕСКИЙ АНСАМБЛЬ
- 37. КАНОНИЧЕСКИЙ АНСАМБЛЬ
- 38. МАКРОСКОПИЧЕСКОЕ ТЕЛО
- Д. ДВА ДРУГИХ АНСАМБЛЯ
- 39. СВОБОДНАЯ ЭНТАЛЬПИЯ
- 40. БОЛЬШОЙ КАНОНИЧЕСКИЙ АНСАМБЛЬ (T, V, «мю» ЗАДАНЫ)
- 41. ЗАКЛЮЧЕНИЕ
- ГЛАВА ТРЕТЬЯ. КВАНТОВАЯ СТАТИСТИКА
- 42. ПРЕДВАРИТЕЛЬНОЕ РАССМОТРЕНИЕ НЕКОТОРЫХ РЕЗУЛЬТАТОВ
- 43. НЕКОТОРЫЕ СВЕДЕНИЯ ИЗ КВАНТОВОЙ ТЕОРИИ
- 44. АНСАМБЛЬ ИЛИ СТАТИСТИЧЕСКАЯ СОВОКУПНОСТЬ
- 45. ЭНТРОПИЯ ТЕРМИЧЕСКИ ИЗОЛИРОВАННОЙ СИСТЕМЫ
- 46. КАНОНИЧЕСКИЙ АНСАМБЛЬ
- ГЛАВА ЧЕТВЕРТАЯ. ИДЕАЛЬНЫЕ И РЕАЛЬНЫЕ ГАЗЫ А. ИДЕАЛЬНЫЙ ГАЗ И ВЫРОЖДЕНИЕ ГАЗА
- 47. СТАТИСТИЧЕСКИЙ ИНТЕГРАЛ И СТАТИСТИЧЕСКАЯ СУММА ДЛЯ ЧАСТИЦ
- 48. N ОДИНАКОВЫХ НЕВЗАИМОДЕЙСТВУЮЩИХ ЧАСТИЦ
- 49. СИСТЕМА ИЗОЛИРОВАНА
- 50. СИСТЕМА НАХОДИТСЯ В ТЕРМОСТАТЕ
- 51. БОЛЬШОЙ КАНОНИЧЕСКИЙ АНСАМБЛЬ
- 52. ПРЕДЕЛЬНЫЙ СЛУЧАЙ СИЛЬНОГО РАЗРЕЖЕНИЯ
- 53. ГАЗ ФЕРМИ
- 54. ГАЗ БОЗЕ
- Б. РЕАЛЬНЫЕ ГАЗЫ И КОНДЕНСАЦИЯ
- 56. ОБЛАСТЬ НЕНАСЫЩЕННОГО ПАРА
- 57. КОНДЕНСАЦИЯ
- 58. ЖИДКАЯ ФАЗА
- 59. АНАЛОГИЯ МЕЖДУ ИДЕАЛЬНЫМ ГАЗОМ БОЗЕ И РЕАЛЬНЫМ ГАЗОМ
- 60. ОБРАЗОВАНИЕ ЗАРОДЫШЕЙ
- ГЛАВА ПЯТАЯ. ТВЕРДОЕ ТЕЛО
- 62. КВАНТОВОМЕХАНИЧЕСКОЕ РАССМОТРЕНИЕ И ОБЩИЙ ОБЗОР
- 63. ЛИНЕЙНАЯ ЦЕПЬ
- 64. КОЛЕБАНИЯ ПРОСТРАНСТВЕННОЙ РЕШЕТКИ
- 65. ОБСУЖДЕНИЕ ХОДА УДЕЛЬНОЙ ТЕПЛОЕМКОСТИ
- Б. УПОРЯДОЧЕННАЯ И НЕУПОРЯДОЧЕННАЯ КРИСТАЛЛИЧЕСКАЯ РЕШЕТКА
- 67. СТАТИСТИЧЕСКИЙ МЕТОД
- 68. СВЕРХСТРУКТУРА
- 60. РАЗДЕЛЕНИЕ ФАЗ («фи» ПОЛОЖИТЕЛЬНО)
- 70. ФЕРРОМАГНЕТИЗМ
- 71. ПРИБЛИЖЕНИЕ БЭТЕ ДЛЯ МОДЕЛИ ИЗИНГА
- 72. ЛИНЕИНАЯ И ПЛОСКАЯ РЕШЕТКИ ПО МЕТОДУ МАТРИЦ
- ГЛАВА ШЕСТАЯ. ФЛУКТУАЦИИ И БРОУНОВСКОЕ ДВИЖЕНИЕ
- 74. ЯВЛЕНИЯ ФЛУКТУАЦИЙ
- Б. БРОУНОВСКОЕ ДВИЖЕНИЕ
- 76. ПОДВИЖНОСТЬ И ДИФФУЗИЯ
- 77. УРАВНЕНИЕ ЛАНЖЕВЕНА
- 78. МЕТОД ЭЙНШТЕЙНА И ХОПФА
- 79. УСТАНОВЛЕНИЕ РАСПРЕДЕЛЕНИЯ МАКСВЕЛЛА
- 80. НЕКОТОРЫЕ СВЕДЕНИЯ О СЛУЧАЙНОМ ДВИЖЕНИИ
- 81. КОРРЕЛЯЦИЯ ДЛЯ СТАТИСТИЧЕСКИ ИЗМЕНЯЮЩЕЙСЯ ФУНКЦИИ
- 82. ДИФФЕРЕНЦИАЛЬНОЕ УРАВНЕНИЕ ФОККЕРА — ПЛАНКА
- 83. СПЕКТРАЛЬНОЕ РАЗЛОЖЕНИЕ СТАТИСТИЧЕСКОЙ ФУНКЦИИ
- 84. СЛАБО ДЕМПФИРОВАННЫЙ ОСЦИЛЛЯТОР С ЗАТУХАНИЕМ, ЗАВИСЯЩИМ ОТ ЧАСТОТЫ
- 85. ФОРМУЛА НАЙКВИСТА
- 86. ДРОБОВОЙ ЭФФЕКТ
- ГЛАВА СЕДЬМАЯ. ТЕРМОДИНАМИКА НЕОБРАТИМЫХ ПРОЦЕССОВ
- 88. НЕОБРАТИМЫЕ ПРОЦЕССЫ В СТАТИСТИЧЕСКОЙ МЕХАНИКЕ
- 89. ОДНОВРЕМЕННОЕ НАБЛЮДЕНИЕ НЕСКОЛЬКИХ МАКРОСКОПИЧЕСКИХ ВЕЛИЧИН
- 90. МЕТОД КОКСА
- 91. ОБМЕН ТЕПЛОМ И ЧАСТИЦАМИ
- 92. НЕКОТОРЫЕ ПРИМЕНЕНИЯ
- 93. МЕТОД ТОМСОНА И ЕГО ПОДТВЕРЖДЕНИЕ СООТНОШЕНИЯМИ ОНЗАГЕРА
- 94. ТЕРМОЭЛЕКТРИЧЕСКИЕ ЯВЛЕНИЯ. ВЫВОД ТОМСОНА
- 95. ТЕРМОЭЛЕКТРИЧЕСКИЕ ЯВЛЕНИЯ. ОБСУЖДЕНИЕ С ПОМОЩЬЮ СООТНОШЕНИЯ ВЗАИМНОСТИ ОНЗАГЕРА