| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
в) Энергия идеального газа
Если в качестве параметров состояния рассматриваются температура  и объем V, то
и объем V, то  т. е.
т. е.

Если в частном случае  равно нулю, то согласно уравнению (3.2а) над системой не производится работа. Следовательно, прирост энергии
равно нулю, то согласно уравнению (3.2а) над системой не производится работа. Следовательно, прирост энергии  в соответствии с уравнением (3.1) равен подведенному теплу
в соответствии с уравнением (3.1) равен подведенному теплу  Поэтому величину
Поэтому величину  называют «теплоемкостью». Если мы разделим эту величину на массу или
называют «теплоемкостью». Если мы разделим эту величину на массу или
число молей тела, то получится «удельная теплоемкость» или «мольная теплоемкость»  Смысл производной
Смысл производной  мы еще неоднократно будем выяснять. В данном случае ограничимся основополагающим опытом Гей-Люссака для измерения этой величины в газах (рис. 9). Пусть сосуд объемом
мы еще неоднократно будем выяснять. В данном случае ограничимся основополагающим опытом Гей-Люссака для измерения этой величины в газах (рис. 9). Пусть сосуд объемом  разделен на две части
разделен на две части  с помощью перегородки
с помощью перегородки  Часть А первоначально заполнена газом (объем
Часть А первоначально заполнена газом (объем  , температура
, температура  часть В, напротив, вакуумирована. Уберем теперь перегородку. Газ мгновенно расширится благодаря вакууму В. После этого — теперь уже в объеме
часть В, напротив, вакуумирована. Уберем теперь перегородку. Газ мгновенно расширится благодаря вакууму В. После этого — теперь уже в объеме  когда газ придет в стационарное состояние, вновь измерим его температуру
когда газ придет в стационарное состояние, вновь измерим его температуру  Так как вся система во время этого процесса была изолированной, ее энергия не могла измениться, следовательно, должно быть
Так как вся система во время этого процесса была изолированной, ее энергия не могла измениться, следовательно, должно быть


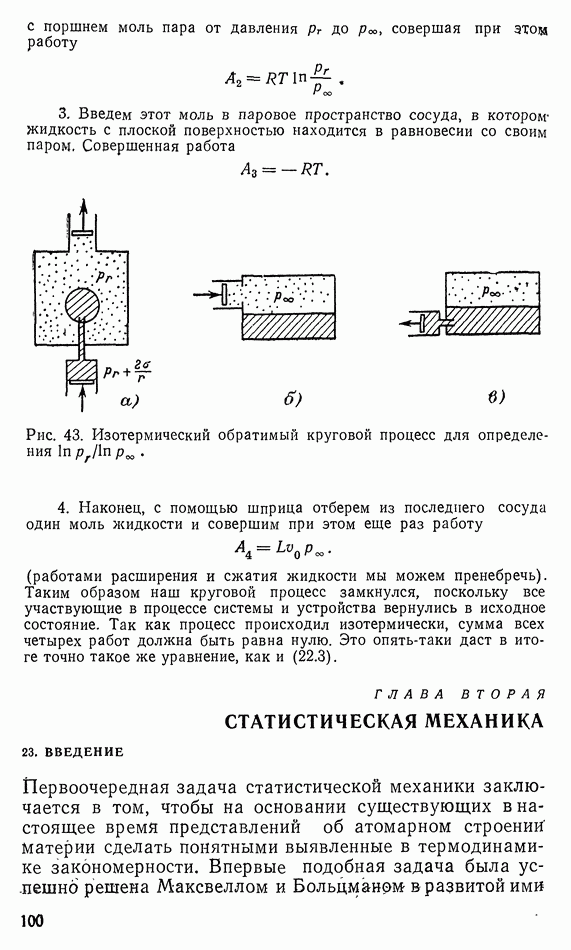
Рис. 9. Опыт Гей-Люссака (расширение без совершения работы).
Далее экспериментально было установлено, что  т. е. что газ при таком расширении не меняет свою температуру. В пределах точности эксперимента отсюда вытекает, что для газов энергия
т. е. что газ при таком расширении не меняет свою температуру. В пределах точности эксперимента отсюда вытекает, что для газов энергия  не зависит от объема, а является функцией одной лишь температуры. Следовательно, для идеальных газов
не зависит от объема, а является функцией одной лишь температуры. Следовательно, для идеальных газов

мы добавили слово «идеальных», поскольку для реальных газов при расширении все же происходит небольшое, однако не улавливаемое в пределах точности экспериментов Гей-Люссака изменение  Позднее мы к этому еще вернемся (§ 13 и 14).
Позднее мы к этому еще вернемся (§ 13 и 14).
Если принять энергию идеального газа при  также равной нулю и обозначить через
также равной нулю и обозначить через  мольную теплоемкость этого газа, то его уравнения состояния будут иметь вид:
мольную теплоемкость этого газа, то его уравнения состояния будут иметь вид:

Уравнение (3.6а) называют калорическим,  термическим уравнением состояния.
термическим уравнением состояния.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ РЕДАКТОРА РУССКОГО ПЕРЕВОДА
- ГЛАВА ПЕРВАЯ. ТЕРМОДИНАМИКА
- 1. ПОНЯТИЕ ТЕМПЕРАТУРЫ И УРАВНЕНИЕ СОСТОЯНИЯ ИДЕАЛЬНОГО ГАЗА
- 2. ПАРАМЕТРЫ СОСТОЯНИЯ
- 3. ПЕРВЫЙ ОСНОВНОЙ ЗАКОН
- б) Намагничивание
- в) Энергия идеального газа
- 4. УДЕЛЬНАЯ ТЕПЛОЕМКОСТЬ
- б) Адиабатный процесс
- в) Применение для расчета скорости звука
- г) Энергия и удельная теплоемкость идеального газа
- 5. ВТОРОЙ ОСНОВНОЙ ЗАКОН
- 6. КОЭФФИЦИЕНТ ПОЛЕЗНОГО ДЕЙСТВИЯ КАРНО
- 7. ОБЩИЙ СЛУЧАЙ МАШИНЫ КАРНО И ОПРЕДЕЛЕНИЕ АБСОЛЮТНОЙ ТЕМПЕРАТУРЫ
- Б. ЭНТРОПИЯ
- 8. ЭНТРОПИЯ КАК ФУНКЦИЯ СОСТОЯНИЯ
- 9. РОСТ ЭНТРОПИИ В ИЗОЛИРОВАННОЙ СИСТЕМЕ
- 10. ЭНТРОПИЯ ИДЕАЛЬНОГО ГАЗА
- В. НЕКОТОРЫЕ ПРИМЕНЕНИЯ
- 11. СВОБОДНАЯ ЭНЕРГИЯ
- 12. УРАВНЕНИЕ СОСТОЯНИЯ И УСЛОВИЕ ИНТЕГРИРУЕМОСТИ
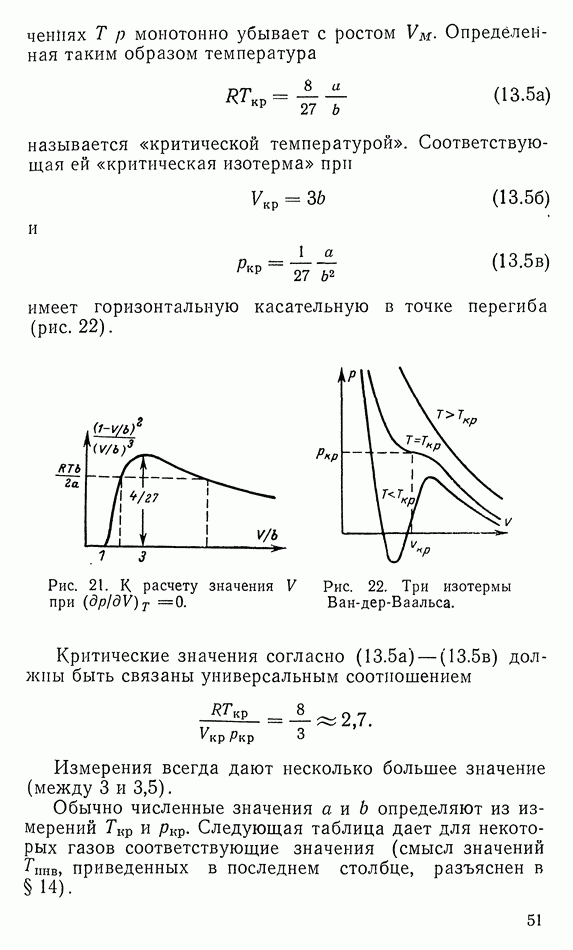
- 13. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА
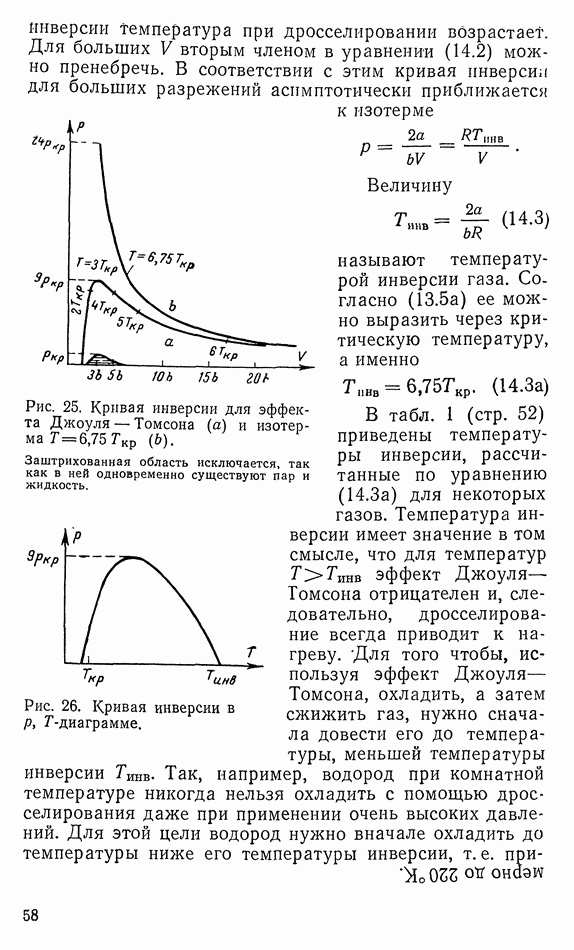
- 14. ЭФФЕКТ ДЖОУЛЯ — ТОМСОНА
- Г. МЕТОД КРУГОВЫХ ПРОЦЕССОВ
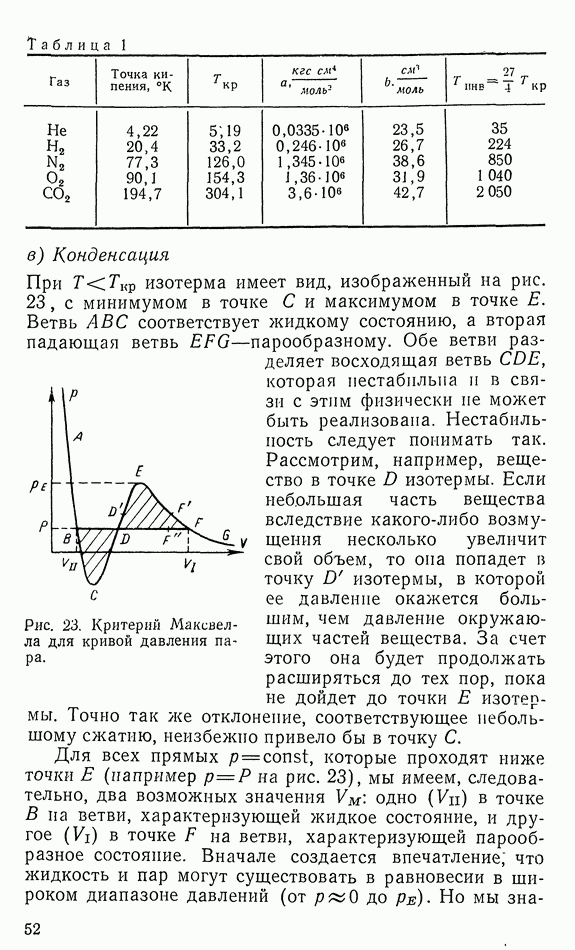
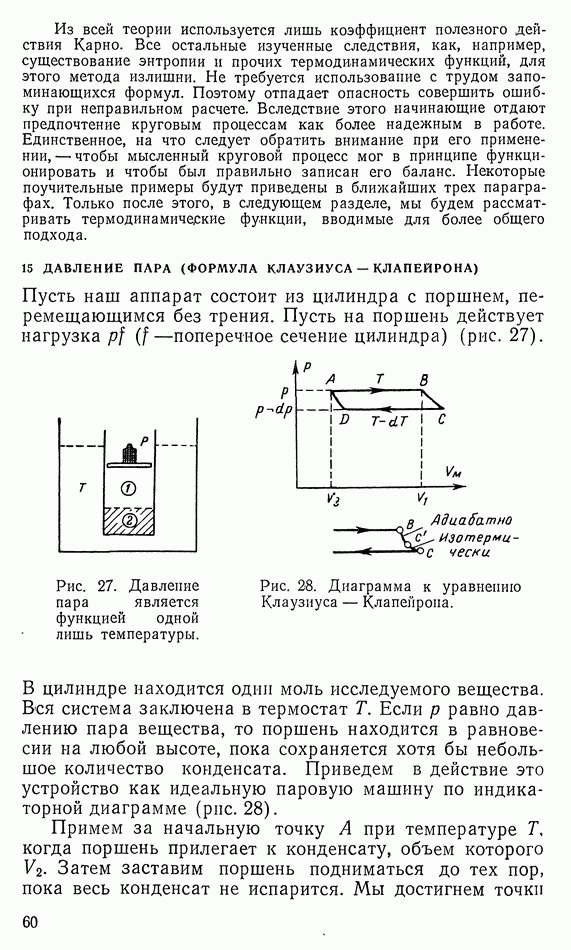
- 15. ДАВЛЕНИЕ ПАРА (ФОРМУЛА КЛАУЗИУСА — КЛАПЕЙРОНА)
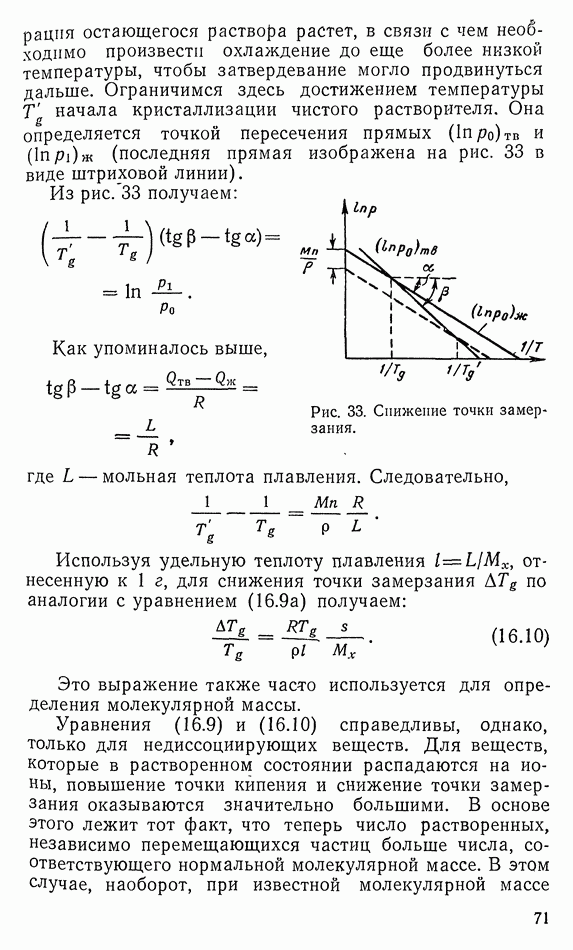
- 16. РАСТВОРЫ
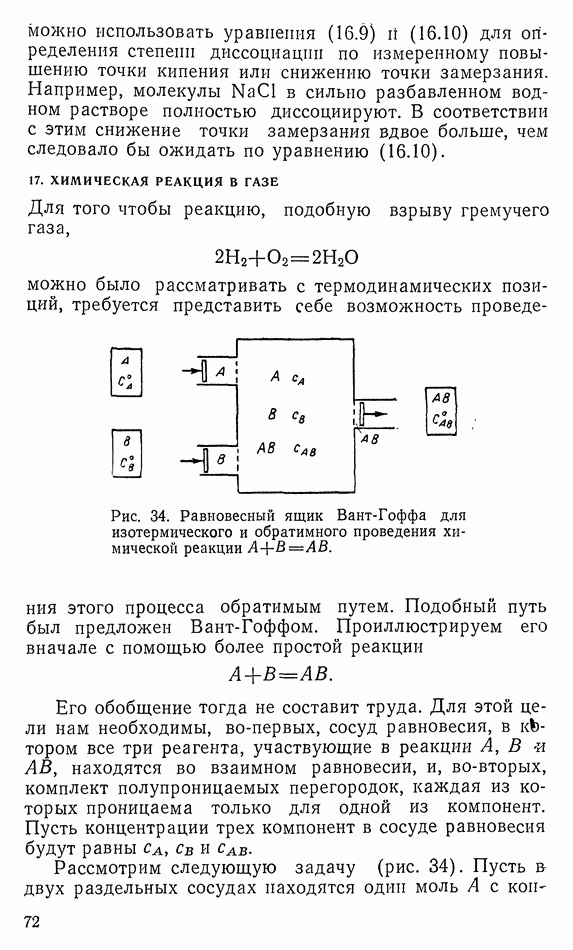
- 17. ХИМИЧЕСКАЯ РЕАКЦИЯ В ГАЗЕ
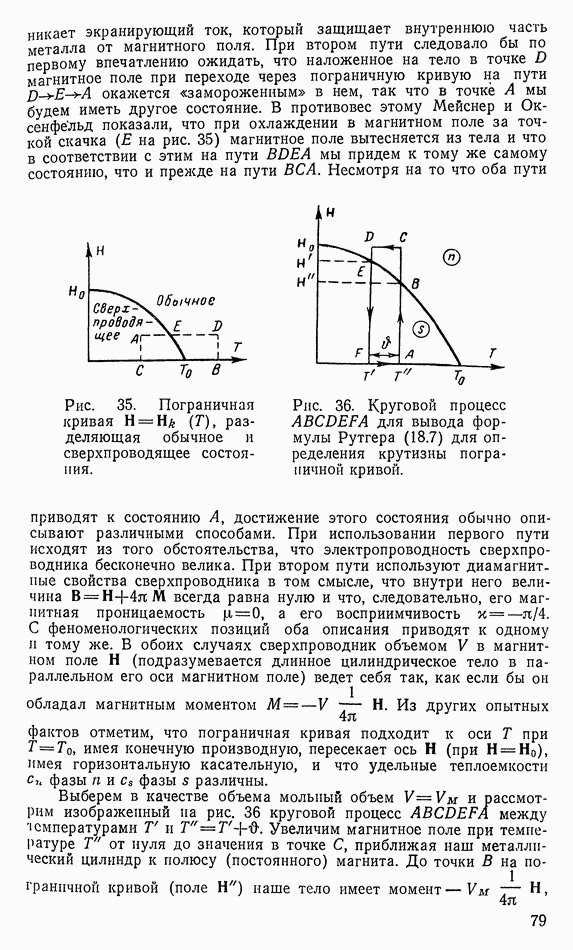
- 18. ПРИМЕР ИЗ СВЕРХПРОВОДИМОСТИ
- Д. ТЕРМОДИНАМИЧЕСКИЕ ФУНКЦИИ И ОБЩЕЕ РАВНОВЕСИЕ
- 19. ТЕРМОДИНАМИЧЕСКИЕ ФУНКЦИИ И ИХ ПРИМЕНЕНИЕ К ГОМОГЕННЫМ ФАЗАМ
- 20. ТЕРМОДИНАМИЧЕСКОЕ РАВНОВЕСИЕ
- 21. ХИМИЧЕСКИЙ ПОТЕНЦИАЛ ИДЕАЛЬНОГО ГАЗА
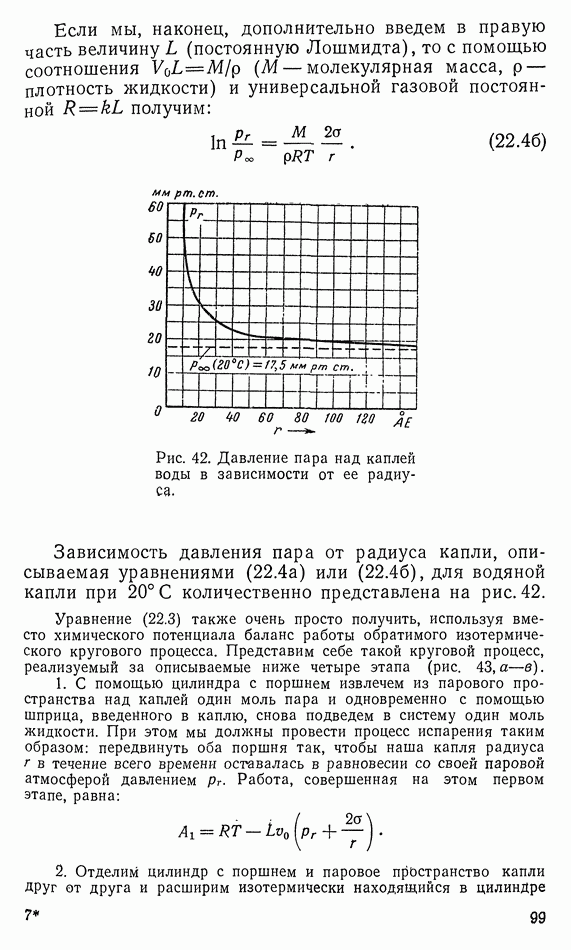
- 22. ДАВЛЕНИЕ ПАРА НАД НЕБОЛЬШОЙ КАПЛЕЙ
- ГЛАВА ВТОРАЯ. СТАТИСТИЧЕСКАЯ МЕХАНИКА
- А. КИНЕТИЧЕСКАЯ ТЕОРИЯ ГАЗОВ
- 24. УРАВНЕНИЕ СОСТОЯНИЯ ИДЕАЛЬНОГО ГАЗА
- 25. МАКСВЕЛЛОВСКОЕ РАСПРЕДЕЛЕНИЕ СКОРОСТЕЙ
- 26. ОБОСНОВАНИЕ БОЛЬЦМАНОМ РАСПРЕДЕЛЕНИЯ СКОРОСТЕЙ МАКСВЕЛЛА И Н-TEOPEMA
- 27. БАРОМЕТРИЧЕСКАЯ ФОРМУЛА
- 28. ТЕОРЕМА О ВИРИАЛЕ
- 29. РАЗРЕЖЕННЫЙ НЕИДЕАЛЬНЫЙ ГАЗ
- Б. НЕКОТОРЫЕ ОСНОВНЫЕ ПОНЯТИЯ МЕХАНИКИ
- 30. УРАВНЕНИЯ ДВИЖЕНЙЯ ГАМИЛЬТОНА
- 31. Г-ПРОСТРАНСТВО
- В. МИКРОКАНОНИЧЕСКИЙ АНСАМБЛЬ
- 32. УСРЕДНЕНИЕ ПО ВРЕМЕНИ И ПО АНСАМБЛЮ
- 33. ПРОСТЕЙШИЕ ПРИМЕНЕНИЯ
- 34. ЭНТРОПИЯ
- 35. ДЕЛЕНИЕ НА N1 И ДЕЙСТВИТЕЛЬНЫЙ ФАЗОВЫЙ ОБЪЕМ
- Г. КАНОНИЧЕСКИЙ АНСАМБЛЬ
- 37. КАНОНИЧЕСКИЙ АНСАМБЛЬ
- 38. МАКРОСКОПИЧЕСКОЕ ТЕЛО
- Д. ДВА ДРУГИХ АНСАМБЛЯ
- 39. СВОБОДНАЯ ЭНТАЛЬПИЯ
- 40. БОЛЬШОЙ КАНОНИЧЕСКИЙ АНСАМБЛЬ (T, V, «мю» ЗАДАНЫ)
- 41. ЗАКЛЮЧЕНИЕ
- ГЛАВА ТРЕТЬЯ. КВАНТОВАЯ СТАТИСТИКА
- 42. ПРЕДВАРИТЕЛЬНОЕ РАССМОТРЕНИЕ НЕКОТОРЫХ РЕЗУЛЬТАТОВ
- 43. НЕКОТОРЫЕ СВЕДЕНИЯ ИЗ КВАНТОВОЙ ТЕОРИИ
- 44. АНСАМБЛЬ ИЛИ СТАТИСТИЧЕСКАЯ СОВОКУПНОСТЬ
- 45. ЭНТРОПИЯ ТЕРМИЧЕСКИ ИЗОЛИРОВАННОЙ СИСТЕМЫ
- 46. КАНОНИЧЕСКИЙ АНСАМБЛЬ
- ГЛАВА ЧЕТВЕРТАЯ. ИДЕАЛЬНЫЕ И РЕАЛЬНЫЕ ГАЗЫ А. ИДЕАЛЬНЫЙ ГАЗ И ВЫРОЖДЕНИЕ ГАЗА
- 47. СТАТИСТИЧЕСКИЙ ИНТЕГРАЛ И СТАТИСТИЧЕСКАЯ СУММА ДЛЯ ЧАСТИЦ
- 48. N ОДИНАКОВЫХ НЕВЗАИМОДЕЙСТВУЮЩИХ ЧАСТИЦ
- 49. СИСТЕМА ИЗОЛИРОВАНА
- 50. СИСТЕМА НАХОДИТСЯ В ТЕРМОСТАТЕ
- 51. БОЛЬШОЙ КАНОНИЧЕСКИЙ АНСАМБЛЬ
- 52. ПРЕДЕЛЬНЫЙ СЛУЧАЙ СИЛЬНОГО РАЗРЕЖЕНИЯ
- 53. ГАЗ ФЕРМИ
- 54. ГАЗ БОЗЕ
- Б. РЕАЛЬНЫЕ ГАЗЫ И КОНДЕНСАЦИЯ
- 56. ОБЛАСТЬ НЕНАСЫЩЕННОГО ПАРА
- 57. КОНДЕНСАЦИЯ
- 58. ЖИДКАЯ ФАЗА
- 59. АНАЛОГИЯ МЕЖДУ ИДЕАЛЬНЫМ ГАЗОМ БОЗЕ И РЕАЛЬНЫМ ГАЗОМ
- 60. ОБРАЗОВАНИЕ ЗАРОДЫШЕЙ
- ГЛАВА ПЯТАЯ. ТВЕРДОЕ ТЕЛО
- 62. КВАНТОВОМЕХАНИЧЕСКОЕ РАССМОТРЕНИЕ И ОБЩИЙ ОБЗОР
- 63. ЛИНЕЙНАЯ ЦЕПЬ
- 64. КОЛЕБАНИЯ ПРОСТРАНСТВЕННОЙ РЕШЕТКИ
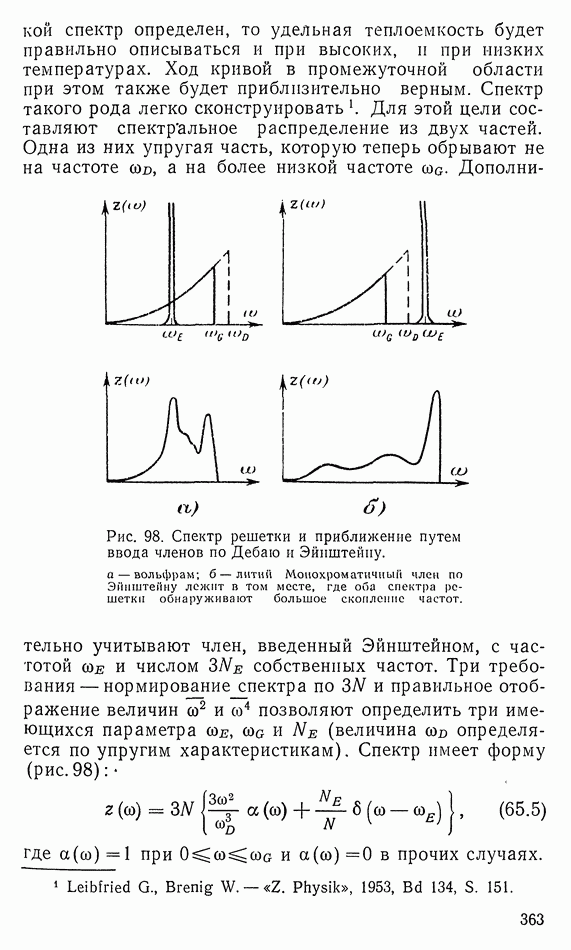
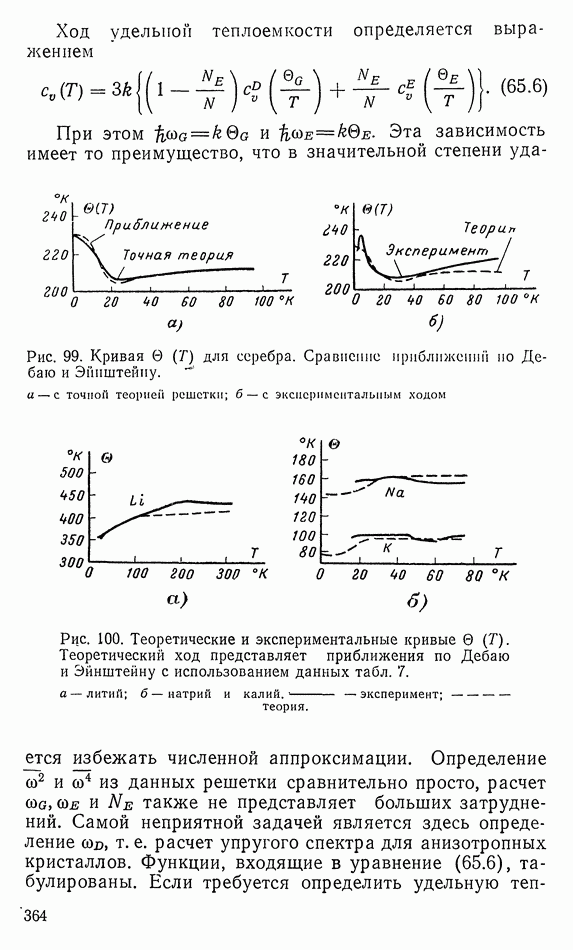
- 65. ОБСУЖДЕНИЕ ХОДА УДЕЛЬНОЙ ТЕПЛОЕМКОСТИ
- Б. УПОРЯДОЧЕННАЯ И НЕУПОРЯДОЧЕННАЯ КРИСТАЛЛИЧЕСКАЯ РЕШЕТКА
- 67. СТАТИСТИЧЕСКИЙ МЕТОД
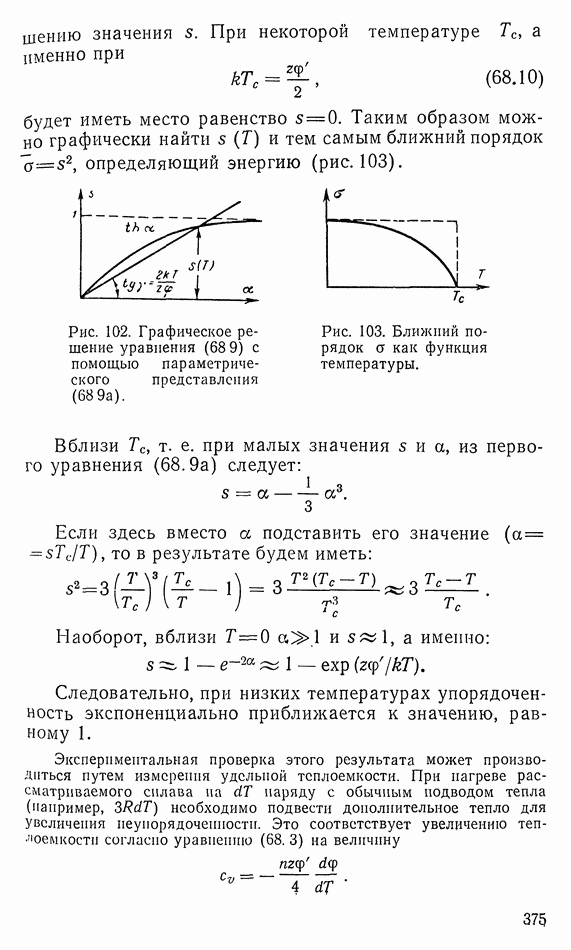
- 68. СВЕРХСТРУКТУРА
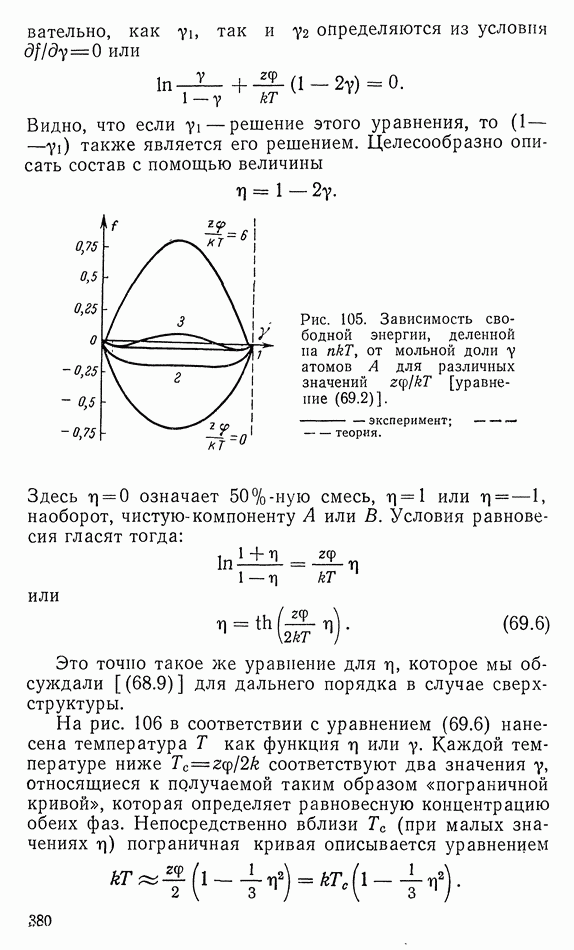
- 60. РАЗДЕЛЕНИЕ ФАЗ («фи» ПОЛОЖИТЕЛЬНО)
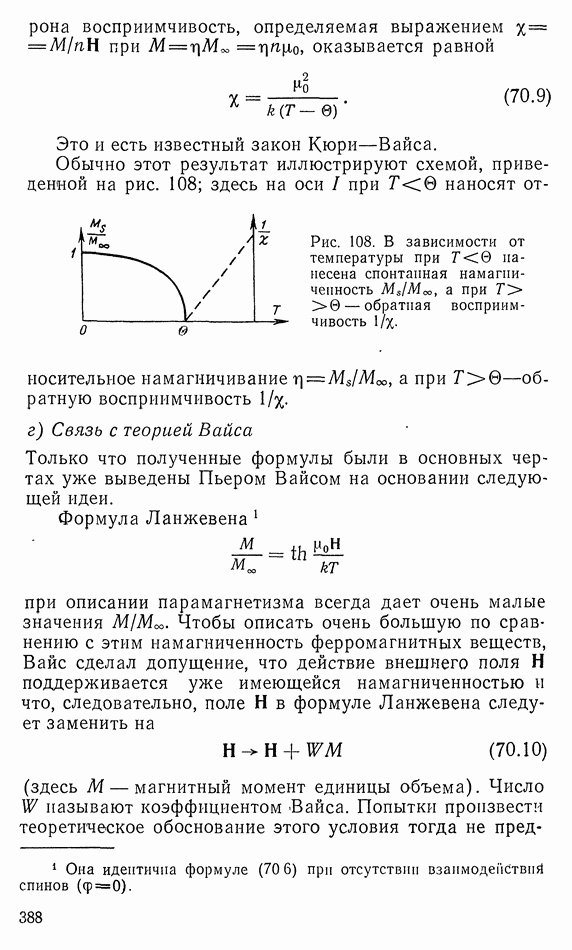
- 70. ФЕРРОМАГНЕТИЗМ
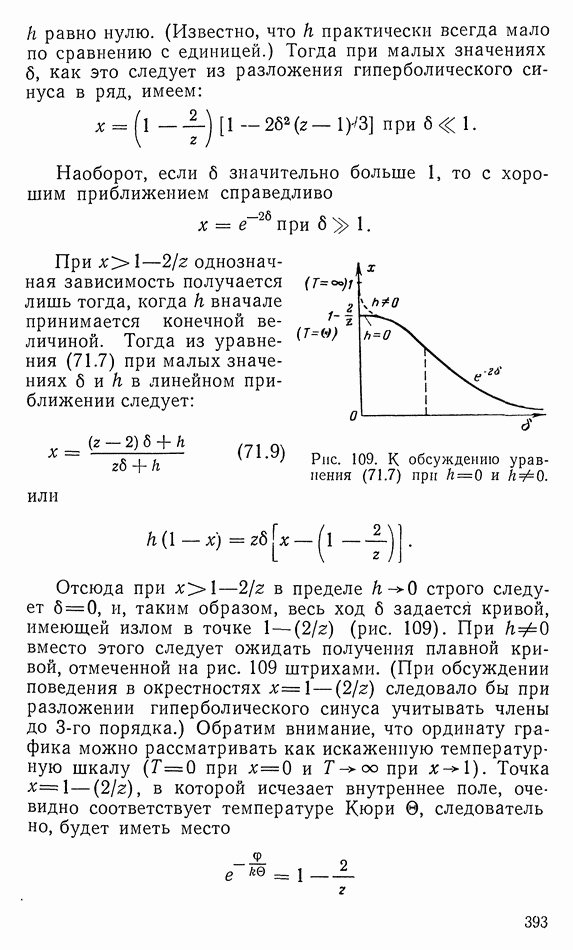
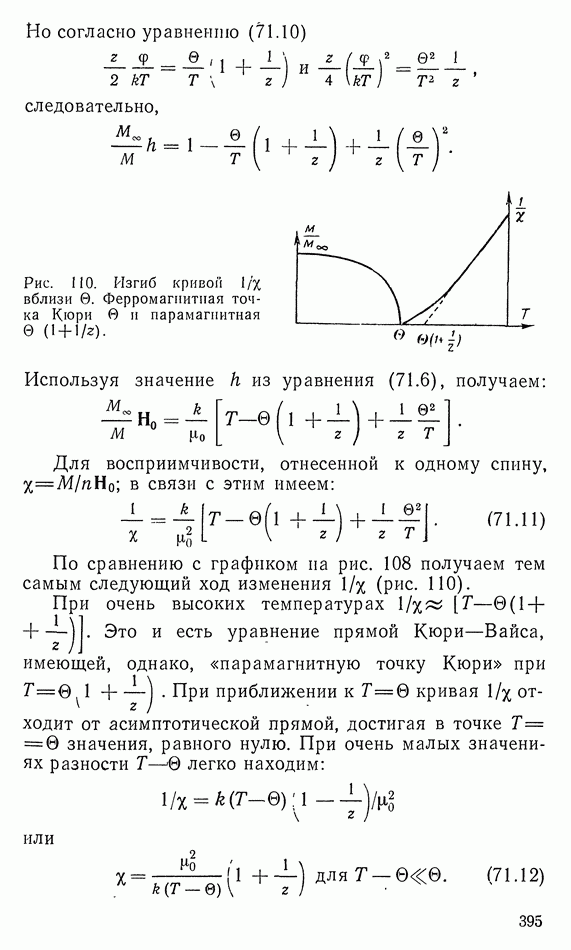
- 71. ПРИБЛИЖЕНИЕ БЭТЕ ДЛЯ МОДЕЛИ ИЗИНГА
- 72. ЛИНЕИНАЯ И ПЛОСКАЯ РЕШЕТКИ ПО МЕТОДУ МАТРИЦ
- ГЛАВА ШЕСТАЯ. ФЛУКТУАЦИИ И БРОУНОВСКОЕ ДВИЖЕНИЕ
- 74. ЯВЛЕНИЯ ФЛУКТУАЦИЙ
- Б. БРОУНОВСКОЕ ДВИЖЕНИЕ
- 76. ПОДВИЖНОСТЬ И ДИФФУЗИЯ
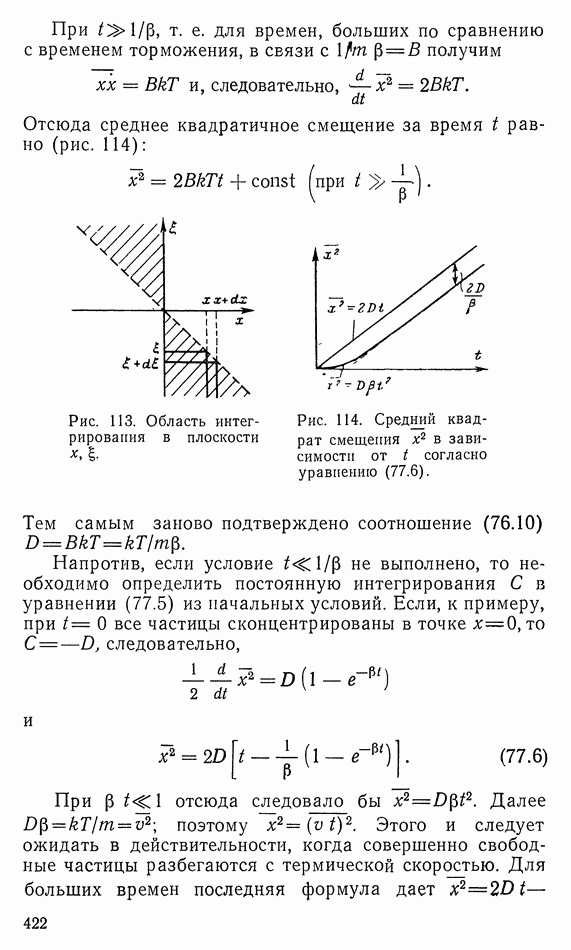
- 77. УРАВНЕНИЕ ЛАНЖЕВЕНА
- 78. МЕТОД ЭЙНШТЕЙНА И ХОПФА
- 79. УСТАНОВЛЕНИЕ РАСПРЕДЕЛЕНИЯ МАКСВЕЛЛА
- 80. НЕКОТОРЫЕ СВЕДЕНИЯ О СЛУЧАЙНОМ ДВИЖЕНИИ
- 81. КОРРЕЛЯЦИЯ ДЛЯ СТАТИСТИЧЕСКИ ИЗМЕНЯЮЩЕЙСЯ ФУНКЦИИ
- 82. ДИФФЕРЕНЦИАЛЬНОЕ УРАВНЕНИЕ ФОККЕРА — ПЛАНКА
- 83. СПЕКТРАЛЬНОЕ РАЗЛОЖЕНИЕ СТАТИСТИЧЕСКОЙ ФУНКЦИИ
- 84. СЛАБО ДЕМПФИРОВАННЫЙ ОСЦИЛЛЯТОР С ЗАТУХАНИЕМ, ЗАВИСЯЩИМ ОТ ЧАСТОТЫ
- 85. ФОРМУЛА НАЙКВИСТА
- 86. ДРОБОВОЙ ЭФФЕКТ
- ГЛАВА СЕДЬМАЯ. ТЕРМОДИНАМИКА НЕОБРАТИМЫХ ПРОЦЕССОВ
- 88. НЕОБРАТИМЫЕ ПРОЦЕССЫ В СТАТИСТИЧЕСКОЙ МЕХАНИКЕ
- 89. ОДНОВРЕМЕННОЕ НАБЛЮДЕНИЕ НЕСКОЛЬКИХ МАКРОСКОПИЧЕСКИХ ВЕЛИЧИН
- 90. МЕТОД КОКСА
- 91. ОБМЕН ТЕПЛОМ И ЧАСТИЦАМИ
- 92. НЕКОТОРЫЕ ПРИМЕНЕНИЯ
- 93. МЕТОД ТОМСОНА И ЕГО ПОДТВЕРЖДЕНИЕ СООТНОШЕНИЯМИ ОНЗАГЕРА
- 94. ТЕРМОЭЛЕКТРИЧЕСКИЕ ЯВЛЕНИЯ. ВЫВОД ТОМСОНА
- 95. ТЕРМОЭЛЕКТРИЧЕСКИЕ ЯВЛЕНИЯ. ОБСУЖДЕНИЕ С ПОМОЩЬЮ СООТНОШЕНИЯ ВЗАИМНОСТИ ОНЗАГЕРА