| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
§ 24. Зависимость термодинамических величин от числа частиц
Наряду с энергией и энтропией свойством аддитивности обладают также и такие термодинамические величины, как F, Ф, W (как это следует непосредственно из их определения, если учесть, что давление и температура постоянны вдоль находящегося в равновесии тела). Это свойство позволяет сделать определенные заключения о характере зависимости всех этих величин от числа частиц в теле. Мы будем рассматривать здесь тела, состоящие из одинаковых частиц (молекул); все результаты могут быть непосредственно обобщены на тела, состоящие из различных частиц смеси (см. § 85).
Аддитивность величины означает, что при изменении количества вещества (а с ним и числа частиц N) в некоторое число раз эта величина меняется во столько же раз. Другими словами, можно сказать, что аддитивная термодинамическая величина должна быть однородной функцией первого порядка относительно аддитивных переменных.
Выразим энергию тела в виде функции энтропии и объема, а также числа частиц.
Поскольку S и V сами по себе тоже аддитивны, эта функция должна иметь вид

что является наиболее общим видом однородной функции первого порядка от N, S и V. Свободная энергия F есть функция от N, Т и V. Поскольку температура постоянна вдоль тела, а объем аддитивен, то из тех же соображений можно написать

Совершенно аналогично для тепловой функции W, выраженной в виде функции от N, S и давления Р, получим

Наконец, для термодинамического потенциала как функции от N, Р, Т имеем

В предыдущем изложении мы по существу рассматривали число частиц как параметр, имеющий для каждого тела заданное постоянное значение. Будем теперь формально рассматривать N как еще одну независимую переменную. Тогда в выражения дифференциалов термодинамических потенциалов должны быть добавлены члены, пропорциональные dN. Например, для полного дифференциала энергии будем писать:

где посредством  мы обозначили частную производную
мы обозначили частную производную

Величина  называется химическим потенциалом тела. Аналогично имеем теперь
называется химическим потенциалом тела. Аналогично имеем теперь

с тем же  Из этих формул следует, что
Из этих формул следует, что
 (24,10)
(24,10)
т. е. химический потенциал можно получить дифференцированием любой из величин Е, W, F, Ф по числу частиц, однако при этом он окажется выраженным через различные переменные.
Дифференцируя Ф, написанное в виде (24,4), найдем, что  , т. е.
, т. е.
 (24,11)
(24,11)
Таким образом, химический потенциал тела (состоящего из одинаковых частиц) есть не что иное, как его термодинамический потенциал, отнесенный к одной молекуле. Будучи выражен в функции от Р и Т, химический потенциал не зависит от N. Для дифференциала химического потенциала можно, следовательно, сразу написать следующее выражение:
 (24,12)
(24,12)
где s и v - энтропия и объем, отнесенные к одной молекуле.
Если рассматривать (как мы до сих пор обычно делали) определенное количество вещества, то число частиц в нем есть заданная постоянная величина, а его объем — величина переменная. Выделим теперь внутри тела некоторый определенный объем и будем рассматривать то вещество, которое заключено в этом объеме; при этом переменной величиной будет число частиц N, а объем V будет постоянным. Тогда, например, равенство (24,8) сведется к

Здесь независимыми переменными являются Т и N; введем такой термодинамический потенциал, для которого второй независимой переменной было бы не N, а  Для этого подставляем
Для этого подставляем  и получаем
и получаем

Но  . Таким образом, новый термодинамический потенциал (который мы обозначим буквой
. Таким образом, новый термодинамический потенциал (который мы обозначим буквой  ) равен просто
) равен просто
 (24,13)
(24,13)
причем
 (24,14)
(24,14)
Число частиц получается дифференцированием Q по химическому потенциалу при постоянных температуре и объеме:

Подобно тому, как было доказано равенство между собой небольших изменений Е, W, F и Ф (при постоянных соответствующих парах величин) легко показать, что изменение  , при постоянных
, при постоянных  , обладает тем же свойством. Иными словами,
, обладает тем же свойством. Иными словами,
 (24,16)
(24,16)
Эти равенства уточняют и расширяют теорему о малых добавках (15,12).
Наконец, аналогично тому, как это было сделано в §§ 15 и 20 для свободной энергии и термодинамического потенциала, можно показать, что работа при обратимом процессе, происходящем при постоянных Т, V и  равна изменению потенциала
равна изменению потенциала  . В состоянии же теплового равновесия потенциал
. В состоянии же теплового равновесия потенциал  имеет минимальное значение по отношению ко всякому изменению состояния при постоянных
имеет минимальное значение по отношению ко всякому изменению состояния при постоянных 
Задача
Получить выражение для теплоемкости  в переменных
в переменных  .
.
Решение. Преобразуем производную  к переменным
к переменным  для чего пишем (рассматривая V все время как постоянную):
для чего пишем (рассматривая V все время как постоянную):

Ho  : поэтому
: поэтому

| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ
- НЕКОТОРЫЕ ОБОЗНАЧЕНИЯ
- ГЛАВА I. ОСНОВНЫЕ ПРИНЦИПЫ СТАТИСТИКИ
- § 1. Статистическое распределение
- § 2. Статистическая независимость
- § 3. Теорема Лиувилля
- § 4. Роль энергии
- § 5. Статистическая матрица
- § 6. Статистическое распределение в квантовой статистике
- § 7. Энтропия
- § 8. Закон возрастания энтропии
- ГЛАВА II. ТЕРМОДИНАМИЧЕСКИЕ ВЕЛИЧИНЫ
- § 9. Температура
- § 10. Макроскопическое движение
- § 11. Адиабатический процесс
- § 12. Давление
- § 13. Работа и количество тепла
- § 14. Тепловая функция
- § 15. Свободная энергия и термодинамический потенциал
- § 16. Соотношения между производными термодинамических величин
- § 17. Термодинамическая шкала температуры
- § 18. Процесс Джоуля — Томсона
- § 19. Максимальная работа
- § 20. Максимальная работа, производимая телом, находящимся во внешней среде
- § 21. Термодинамические неравенства
- § 22. Принцип Ле-Шателье
- § 23. Теорема Нериста
- § 24. Зависимость термодинамических величин от числа частиц
- § 25. Равновесие тела во внешнем поле
- § 26. Вращающиеся тела
- § 27. Термодинамические соотношения в релятивистской области
- ГЛАВА III. РАСПРЕДЕЛЕНИЕ ГИББСА
- § 28. Распределение Гиббса
- § 29. Распределение Максвелла
- Задачи
- § 30. Распределение вероятностей для осциллятора
- § 31. Свободная энергия в распределении Гиббса
- Задачи
- § 32. Термодинамическая теория возмущений
- § 33. Разложение по степеням h
- § 34. Распределение Гиббса для вращающихся тел
- § 35. Распределение Гиббса с переменным числом частиц
- § 36. Вывод термодинамических соотношений из распределения Гиббса
- ГЛАВА IV. ИДЕАЛЬНЫЙ ГАЗ
- § 37. Распределение Больцмана
- § 38. Распределение Больцмана в классической статистике
- Задачи
- § 39. Столкновения молекул
- Задачи
- § 40. Неравновесный идеальный газ
- § 41. Свободная энергия больцмановского идеального газа
- § 42. Уравнение состояния идеального газа
- Задачи
- § 43. Идеальный газ с постоянной теплоемкостью
- Задачи
- § 44. Закон равнораспределения
- § 43. Одноатомный идеальный газ
- § 46. Одноатомный газ. Влияние электронного момента
- § 47. Двухатомный газ с молекулами из различных атомов. Вращение молекул
- § 48. Двухатомный газ с молекулами из одинаковых атомов. Вращение молекул
- § 49. Двухатомный газ. Колебания атомов
- § 50. Двухатомный газ. Влияние электронного момента
- § 51. Многоатомный газ
- § 52. Магнетизм газов
- Задачи
- ГЛАВА V. РАСПРЕДЕЛЕНИЯ ФЕРМИ И БОЗЕ
- § 53. Распределение Ферми
- § 54. Распределение Бозе
- § 55. Неравновесные ферми- и бозе-газы
- § 56. Ферми- и бозе-газы элементарных частиц
- § 57. Вырожденный электронный газ
- § 58. Теплоемкость вырожденного электронного газа
- § 60. Магнетизм электронного газа. Сильные поля
- § 61. Релятивистский вырожденный электронный газ
- Задачи
- § 62. Вырожденный бозе-газ
- Задача
- § 63. Черное излучение
- ГЛАВА VI. ТВЕРДЫЕ ТЕЛА
- § 64. Твердые тела при низких температурах
- § 65. Твердые тела при высоких температурах
- § 66. Интерполяционная формула Дебая
- § 67. Тепловое расширение твердых тел
- § 68. Сильно анизотропные кристаллы
- § 69. Колебания кристаллической решетки
- § 70. Плотность числа колебаний
- § 71. Фононы.
- § 72. Операторы рождения и уничтожения фононов
- § 73. Отрицательные температуры
- ГЛАВА VII. НЕИДЕАЛЬНЫЕ ГАЗЫ
- § 74. Отклонение газов от идеальности
- § 75. Разложение по степеням плотности
- § 76. Формула ван-дер-Ваальса
- § 77. Связь вириального коэффициента с амплитудой рассеяния
- § 78. Термодинамические величины классической плазмы
- § 79. Метод корреляционных функций
- § 80. Термодинамические величины вырожденной плазмы
- ГЛАВА VIII. РАВНОВЕСИЕ ФАЗ
- § 81. Условия равновесия фаз
- § 82. Формула Клапейрона — Клаузиуса
- § 83. Критическая точка
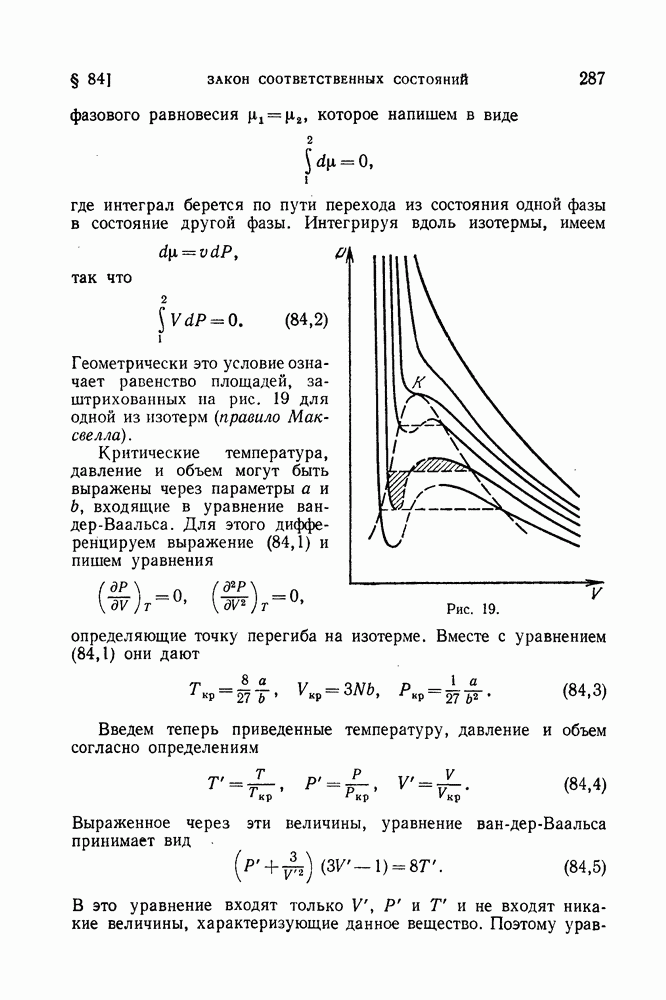
- § 84. Закон соответственных состояний
- ГЛАВА IX. РАСТВОРЫ
- § 85. Системы с различными частицами
- § 86. Правило фаз
- § 87. Слабые растворы
- § 88. Осмотическое давление
- § 89. Соприкосновение фаз растворителя
- § 90. Равновесие по отношению к растворенному веществу
- Задачи
- § 91. Выделение тепла и изменение объема при растворении
- § 92. Растворы сильных электролитов
- § 93. Смесь идеальных газов
- § 94. Смесь изотопов
- § 95. Давление пара над концентрированным раствором
- § 96. Термодинамические неравенства в растворах
- § 97. Кривые равновесия
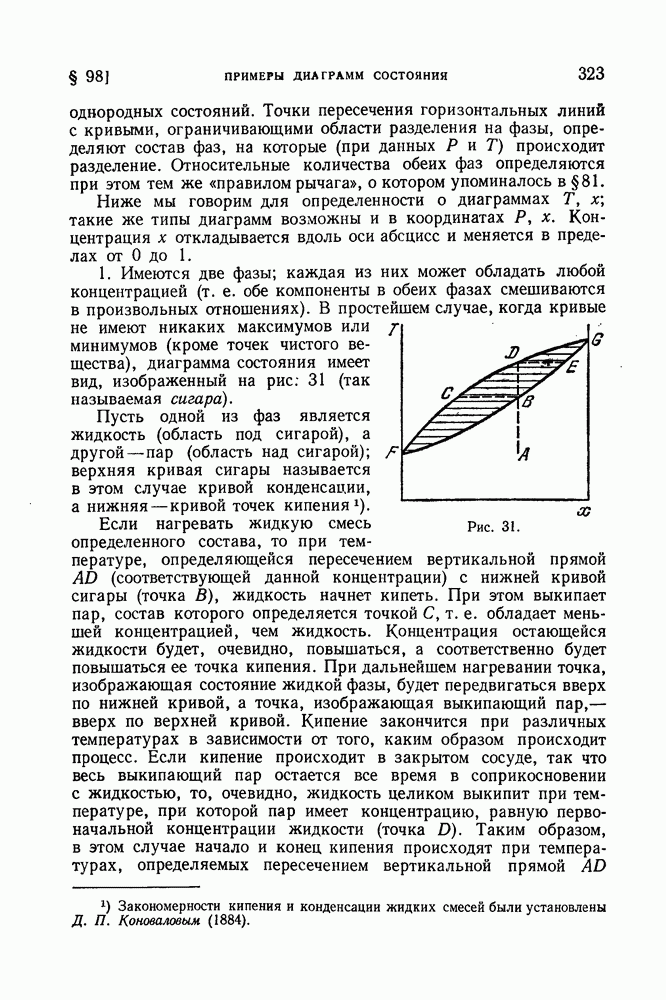
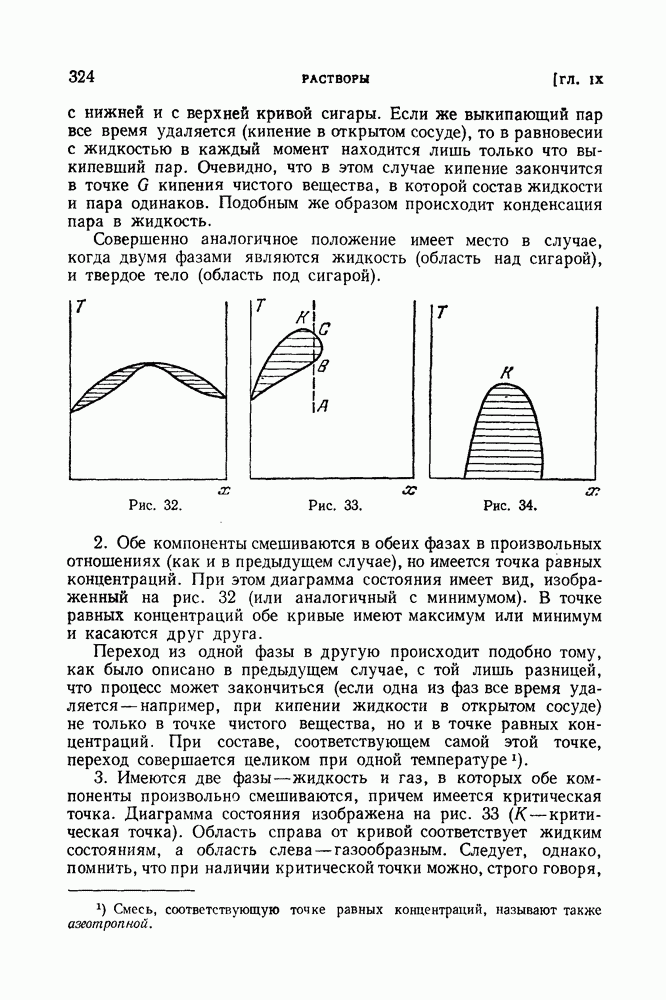
- § 98. Примеры диаграмм состояния
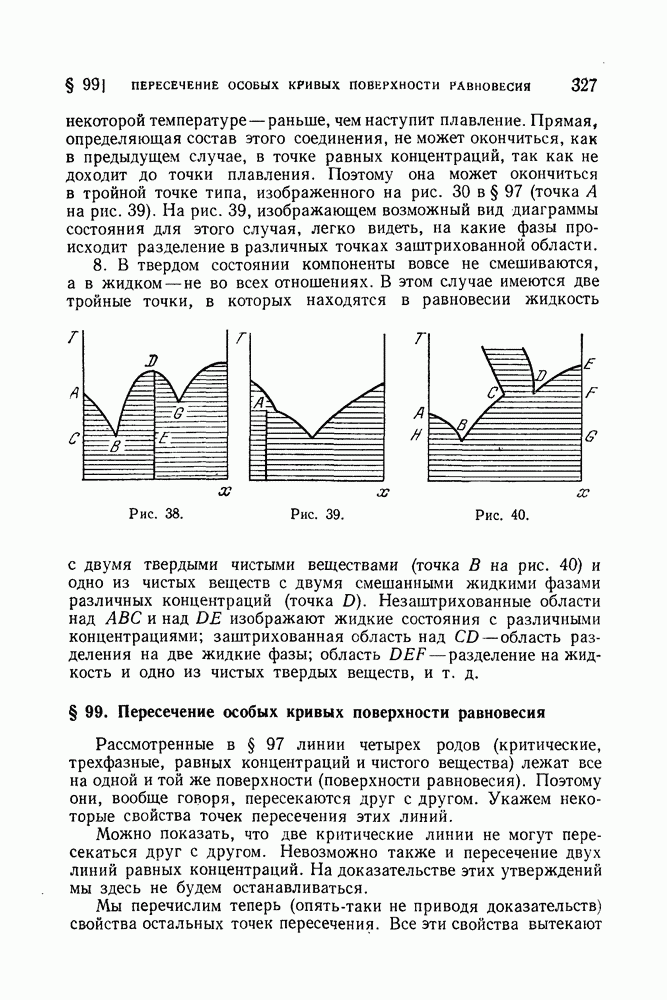
- § 99. Пересечение особых кривых поверхности равновесия
- § 100. Газ и жидкость
- ГЛАВА X. ХИМИЧЕСКИЕ РЕАКЦИИ
- § 101. Условие химического равновесия
- § 102. Закон действующих масс
- Задачи
- § 103. Теплота реакции
- § 104. Ионизационное равновесие
- § 105. Равновесие по отношению к образованию пар
- ГЛАВА XI. СВОЙСТВА ВЕЩЕСТВА ПРИ ОЧЕНЬ БОЛЬШИХ ПЛОТНОСТЯХ
- § 106. Уравнение состояния вещества при больших плотностях
- § 107. Равновесие тел с большой массой
- § 108. Энергия гравитирующего тела
- § 109. Равновесие нейтронной сферы
- ГЛАВА XII. ФЛУКТУАЦИИ
- § 110. Распределение Гаусса
- § 111. Распределение Гаусса для нескольких величин
- § 112. Флуктуации основных термодинамических величин
- Задачи
- § 113. Флуктуации в идеальном газе
- § 114. Формула Пуассона
- § 115. Флуктуации в растворах
- § 116. Пространственная корреляция флуктуаций плотности
- § 117. Корреляция флуктуаций плотности в вырожденном газе
- Задачи
- § 118. Корреляция флуктуаций во времени
- § 119. Временная корреляция флуктуаций нескольких величин
- § 120. Симметрия кинетических коэффициентов
- § 121. Диссипативная функция
- § 122. Спектральное разложение флуктуаций
- § 123. Обобщенная восприимчивость
- § 124. Флуктуационно-диссипационная теорема
- § 125. Флуктуационно-диссипационная теорема для нескольких величин
- § 126. Операторное выражение обобщенной восприимчивости
- § 127. Флуктуации изгиба длинных молекул
- ГЛАВА XIII. СИММЕТРИЯ КРИСТАЛЛОВ
- § 128. Элементы симметрии кристаллической решетки
- § 129. Решетка Бравэ
- § 130. Кристаллические системы
- § 131. Кристаллические классы
- § 132. Пространственные группы
- § 133. Обратная решетка
- § 134. Неприводимые представления пространственных групп
- § 135. Симметрия относительно обращения времени
- § 136. Свойства симметрии нормальных колебаний кристаллической решетки
- § 137. Структуры с одно- и двумерной периодичностью
- § 138. Корреляционная функция в двумерных системах
- § 139. Симметрия по ориентации молекул
- § 140. Нематические и холестерические жидкие кристаллы
- § 141. Флуктуации в жидких кристаллах
- ГЛАВА XIV. ФАЗОВЫЕ ПЕРЕХОДЫ ВТОРОГО РОДА И КРИТИЧЕСКИЕ ЯВЛЕНИЯ
- § 142. Фазовые переходы второго рода
- § 143. Скачок теплоемкости
- § 144. Влияние внешнего поля на фазовый переход
- § 145. Изменение симметрии при фазовом переходе второго рода
- § 146. Флуктуации параметра порядка
- § 147. Эффективный гамильтониан
- § 148. Критические индексы
- § 149. Масштабная инвариантность
- § 150. Изолированные и критические точки непрерывного перехода
- § 151. Фазовый переход второго рода в двумерной решетке
- § 152. Ван-дер-ваальсова теория критической точки
- § 153. Флуктуационная теория критической точки
- ГЛАВА XV. ПОВЕРХНОСТИ
- § 154. Поверхностное натяжение
- § 155. Поверхностное натяжение кристаллов
- § 156. Поверхностное давление
- § 157. Поверхностное натяжение растворов
- § 158. Поверхностное натяжение растворов сильных электролитов
- § 159. Адсорбция
- § 160. Смачивание
- § 161. Краевой угол
- § 162. Образование зародышей при фазовых переходах
- § 163. Невозможность существования фаз в одномерных системах