| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
§ 83. Критическая точка
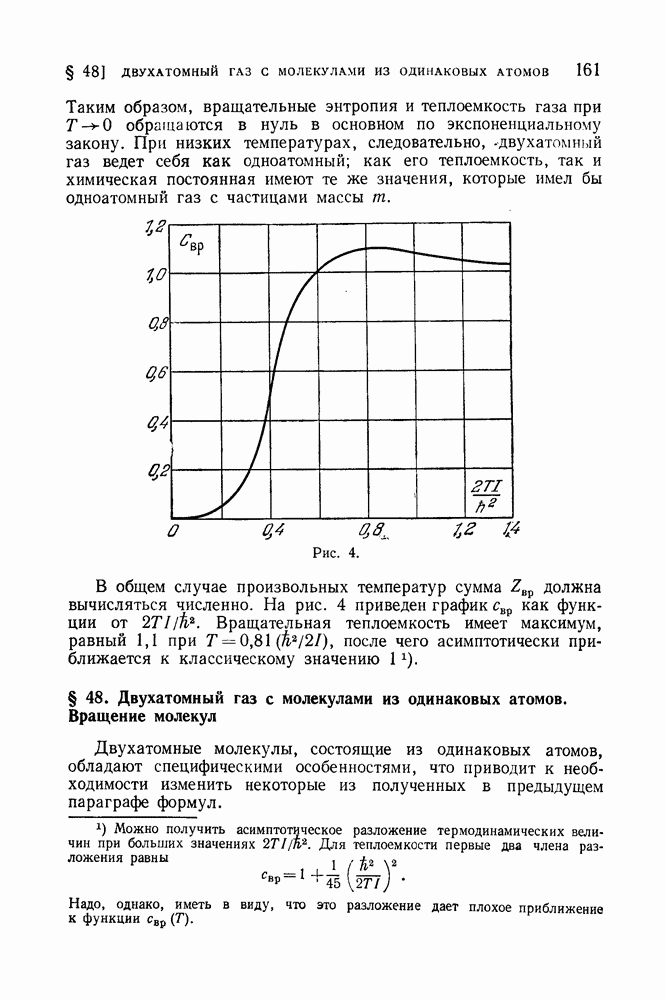
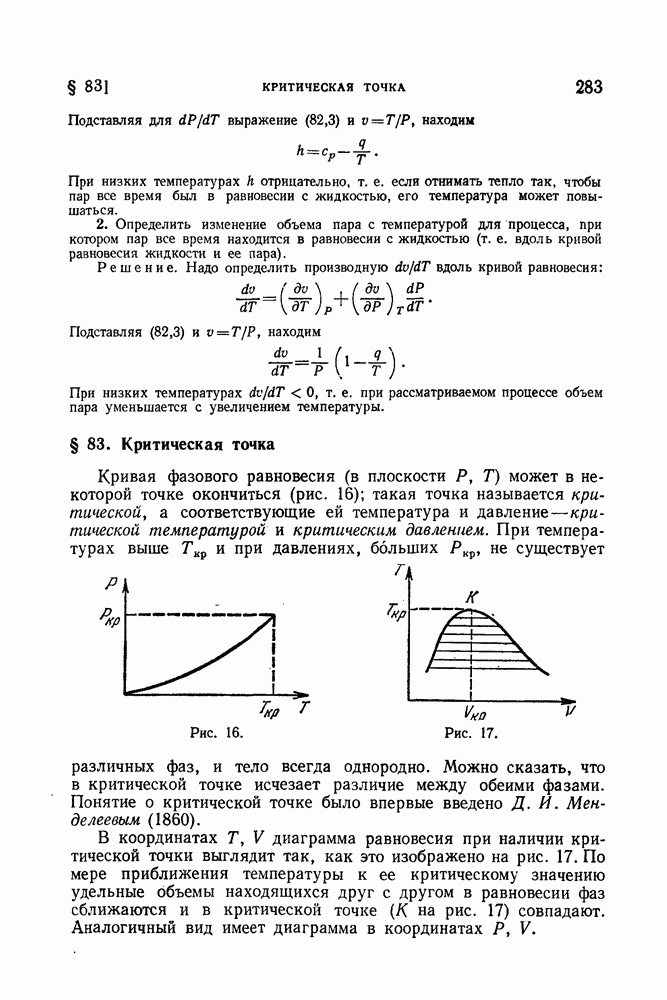
Кривая фазового равновесия (в плоскости Р, Т) может в некоторой точке окончиться (рис. 16); такая точка называется критической, а соответствующие ей температура и давление — критической температурой и критическим давлением. При температурах выше  и при давлениях, больших
и при давлениях, больших  не существует различных фаз, и тело всегда однородно.
не существует различных фаз, и тело всегда однородно.

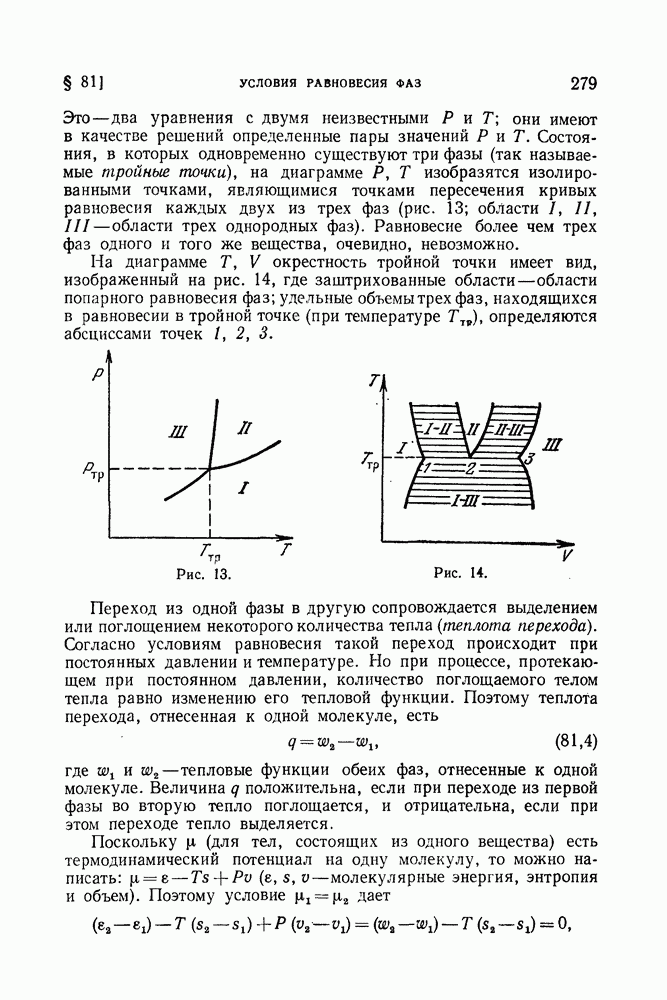
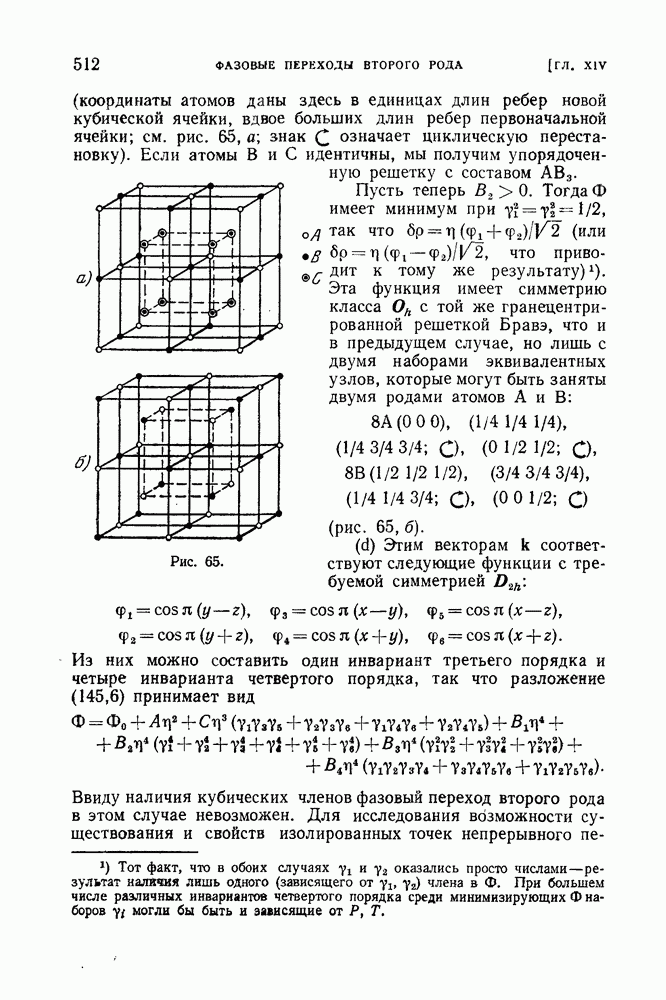
Рис. 16.

Рис. 17.
Можно сказать, что в критической точке исчезает различие между обеими фазами. Понятие о критической точке было впервые введено Д. И. Менделеевым (1860).
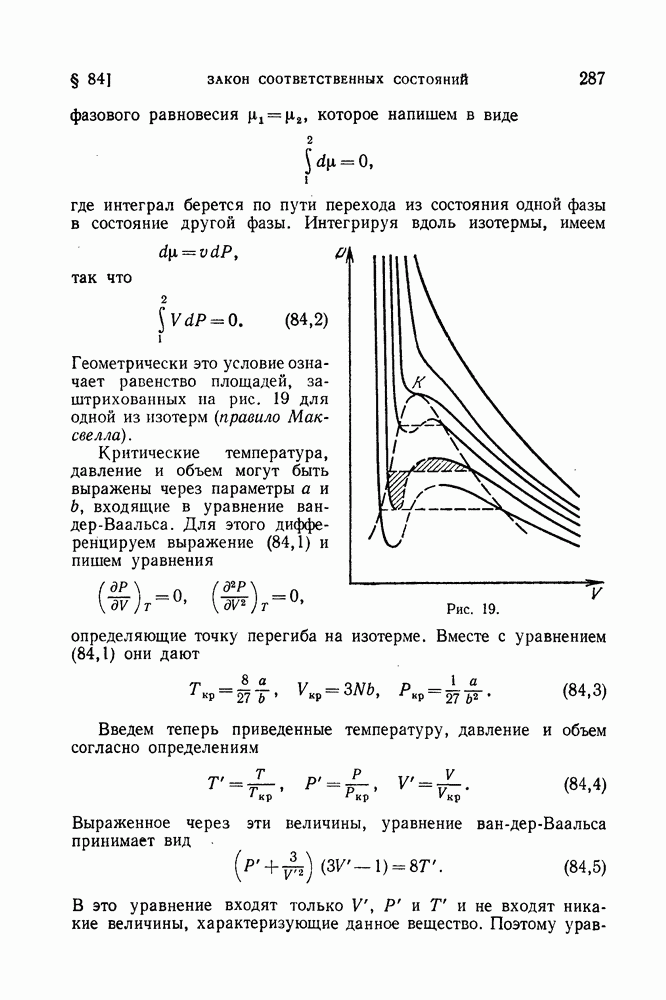
В координатах Т, V диаграмма равновесия при наличии критической точки выглядит так, как это изображено на рис. 17. По мере приближения температуры к ее критическому значению удельные объемы находящихся друг с другом в равновесии фаз сближаются и в критической точке (К на рис. 17) совпадают. Аналогичный вид имеет диаграмма в координатах Р, V.
При наличии критической точки между всякими двумя состояниями вещества может быть произведен непрерывный переход, при котором ни в какой момент не происходит расслоения на две фазы — для этого надо менять состояние вдоль какой-либо кривой, огибающей критическую точку и нигде не пересекающей кривую равновесия. В этом смысле при наличии критической точки становится условным самое понятие о различных фазах, и невозможно во всех случаях указать, какие состояния являются одной фазой, а какие — другой. Строго говоря, можно говорить о двух фазах лишь тогда, когда они существуют обе одновременно, соприкасаясь друг с другом, т. е. в точках, лежащих на кривой равновесия.
Ясно, что критическая точка может существовать лишь для таких фаз, различие между которыми имеет лишь чисто количественный характер. Таковы жидкость и газ, отличающиеся друг от друга лишь большей или меньшей ролью взаимодействия между молекулами.
Такие же фазы, как жидкость и твердое тело (кристалл) или различные кристаллические модификации вещества, качественно различны между собой, так как отличаются своей внутренней симметрией. Ясно, что о всяком свойстве (элементе) симметрии можно сказать только либо, что оно есть, либо, что его нет; оно может появиться или исчезнуть лишь сразу, скачком, а не постепенно. В каждом состоянии тело будет обладать либо одной, либо другой симметрией, и потому всегда можно указать, к которой из двух фаз оно относится. Критическая точка, следовательно, для таких фаз не может существовать, и кривая равновесия должна либо уходить на бесконечность, либо заканчиваться, пересекаясь с кривыми равновесия других фаз.
Обычная точка фазового перехода не представляет собой в математическом отношении особенности для термодинамических величин вещества. Действительно, каждая из фаз может существовать (хотя бы как метастабильная) и по другую сторону от точки перехода; термодинамические неравенства в этой точке не нарушаются. В точке перехода химические потенциалы обеих фаз равны друг другу:  ; для каждой же из функций
; для каждой же из функций  эта точка ничем не замечательна.
эта точка ничем не замечательна.
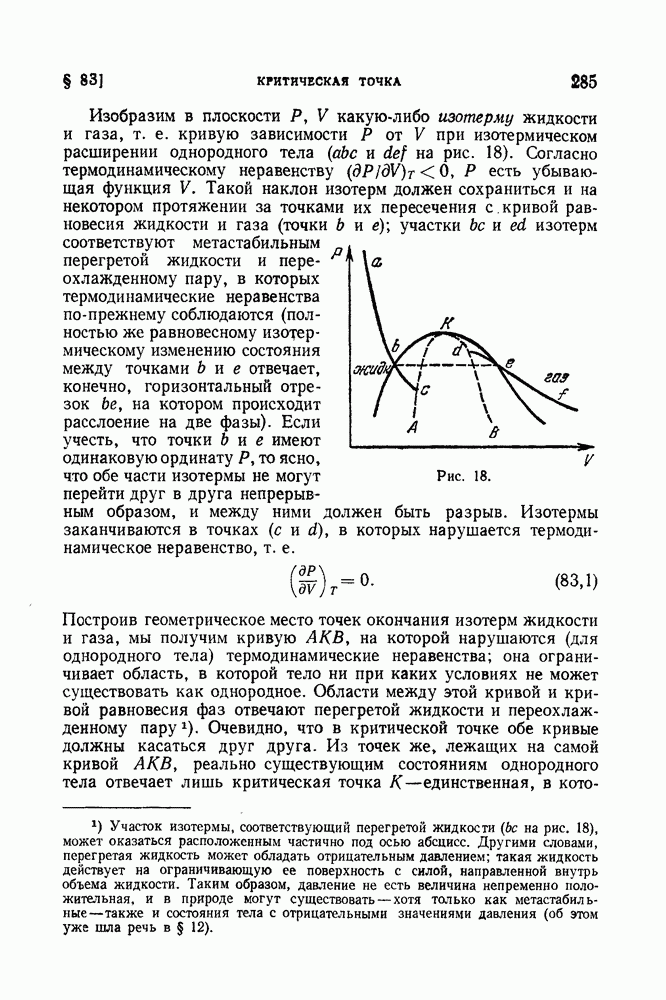
Изобразим в плоскости Р, V какую-либо изотерму жидкости и газа, т. е. кривую зависимости Р от V при изотермическом расширении однородного тела  на рис. 18). Согласно термодинамическому неравенству
на рис. 18). Согласно термодинамическому неравенству  есть убывающая функция V. Такой наклон изотерм должен сохраниться и на некотором протяжении за точками их пересечения с кривой равновесия жидкости и газа (точки b и
есть убывающая функция V. Такой наклон изотерм должен сохраниться и на некотором протяжении за точками их пересечения с кривой равновесия жидкости и газа (точки b и  участки
участки  изотерм соответствуют метастабильным перегретой жидкости и переохлажденному пару, в которых термодинамические неравенства по-прежнему соблюдаются (полностью же равновесному изотермическому изменению состояния между точками b не отвечает, конечно, горизонтальный отрезок
изотерм соответствуют метастабильным перегретой жидкости и переохлажденному пару, в которых термодинамические неравенства по-прежнему соблюдаются (полностью же равновесному изотермическому изменению состояния между точками b не отвечает, конечно, горизонтальный отрезок  на котором происходит расслоение на две фазы).
на котором происходит расслоение на две фазы).

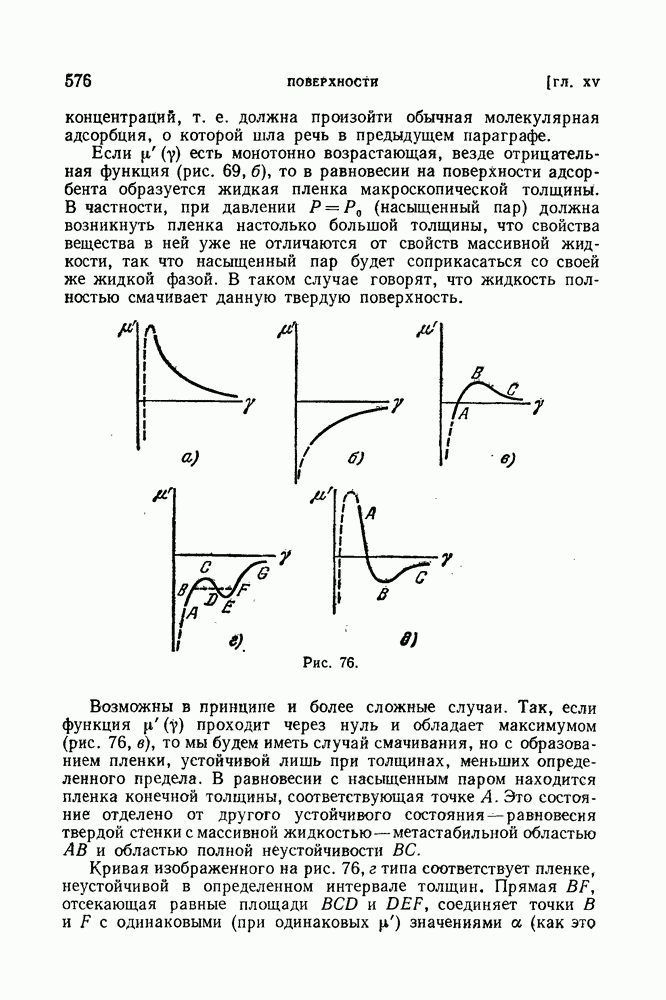
Рис. 18.
Если учесть, что точки  имеют одинаковую ординату Р, то ясно, что обе части изотермы не могут перейти друг в друга непрерывным образом, и между ними должен быть разрыв. Изотермы заканчиваются в точках (с и d), в которых нарушается термодинамическое неравенство, т. е.
имеют одинаковую ординату Р, то ясно, что обе части изотермы не могут перейти друг в друга непрерывным образом, и между ними должен быть разрыв. Изотермы заканчиваются в точках (с и d), в которых нарушается термодинамическое неравенство, т. е.

Построив геометрическое место точек окончания изотерм жидкости и газа, мы получим кривую АКБ, на которой нарушаются (для однородного тела) термодинамические неравенства; она ограничивает область, в которой тело ни при каких условиях не может существовать как однородное. Области между этой кривой и кривой равновесия фаз отвечают перегретой жидкости и переохлажденному пару. Очевидно, что в критической точке обе кривые должны касаться друг друга. Из точек же, лежащих на самой кривой АКБ, реально существующим состояниям однородного тела отвечает лишь критическая точка К — единственная, в которой эта кривая соприкасается с областью устойчивых однородных состояний.
Полезно указать, что условие (83,1) в критической точке может быть получено из следующих простых соображений. Вблизи критической точки удельные объемы жидкости и пара близки друг к другу. Обозначив их посредством  напишем условие равенства давлений обеих фаз в виде
напишем условие равенства давлений обеих фаз в виде

Разложив правую сторону равенства по степеням  и разделив на малую, но конечную величину
и разделив на малую, но конечную величину  , найдем
, найдем

Отсюда видно, что при стремлении  к нулю, т. е. в критической точке,
к нулю, т. е. в критической точке,  во всяком случае должно обратиться в нуль.
во всяком случае должно обратиться в нуль.
В противоположность обычным точкам фазового равновесия критическая точка является в математическом отношении особой точкой для термодинамических функций вещества (то же самое относится ко всей кривой АКВ, ограничивающей область существования однородных состояний тела). Характер этой особенности и поведение вещества вблизи критической точки будут рассмотрены в § 153.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ
- НЕКОТОРЫЕ ОБОЗНАЧЕНИЯ
- ГЛАВА I. ОСНОВНЫЕ ПРИНЦИПЫ СТАТИСТИКИ
- § 1. Статистическое распределение
- § 2. Статистическая независимость
- § 3. Теорема Лиувилля
- § 4. Роль энергии
- § 5. Статистическая матрица
- § 6. Статистическое распределение в квантовой статистике
- § 7. Энтропия
- § 8. Закон возрастания энтропии
- ГЛАВА II. ТЕРМОДИНАМИЧЕСКИЕ ВЕЛИЧИНЫ
- § 9. Температура
- § 10. Макроскопическое движение
- § 11. Адиабатический процесс
- § 12. Давление
- § 13. Работа и количество тепла
- § 14. Тепловая функция
- § 15. Свободная энергия и термодинамический потенциал
- § 16. Соотношения между производными термодинамических величин
- § 17. Термодинамическая шкала температуры
- § 18. Процесс Джоуля — Томсона
- § 19. Максимальная работа
- § 20. Максимальная работа, производимая телом, находящимся во внешней среде
- § 21. Термодинамические неравенства
- § 22. Принцип Ле-Шателье
- § 23. Теорема Нериста
- § 24. Зависимость термодинамических величин от числа частиц
- § 25. Равновесие тела во внешнем поле
- § 26. Вращающиеся тела
- § 27. Термодинамические соотношения в релятивистской области
- ГЛАВА III. РАСПРЕДЕЛЕНИЕ ГИББСА
- § 28. Распределение Гиббса
- § 29. Распределение Максвелла
- Задачи
- § 30. Распределение вероятностей для осциллятора
- § 31. Свободная энергия в распределении Гиббса
- Задачи
- § 32. Термодинамическая теория возмущений
- § 33. Разложение по степеням h
- § 34. Распределение Гиббса для вращающихся тел
- § 35. Распределение Гиббса с переменным числом частиц
- § 36. Вывод термодинамических соотношений из распределения Гиббса
- ГЛАВА IV. ИДЕАЛЬНЫЙ ГАЗ
- § 37. Распределение Больцмана
- § 38. Распределение Больцмана в классической статистике
- Задачи
- § 39. Столкновения молекул
- Задачи
- § 40. Неравновесный идеальный газ
- § 41. Свободная энергия больцмановского идеального газа
- § 42. Уравнение состояния идеального газа
- Задачи
- § 43. Идеальный газ с постоянной теплоемкостью
- Задачи
- § 44. Закон равнораспределения
- § 43. Одноатомный идеальный газ
- § 46. Одноатомный газ. Влияние электронного момента
- § 47. Двухатомный газ с молекулами из различных атомов. Вращение молекул
- § 48. Двухатомный газ с молекулами из одинаковых атомов. Вращение молекул
- § 49. Двухатомный газ. Колебания атомов
- § 50. Двухатомный газ. Влияние электронного момента
- § 51. Многоатомный газ
- § 52. Магнетизм газов
- Задачи
- ГЛАВА V. РАСПРЕДЕЛЕНИЯ ФЕРМИ И БОЗЕ
- § 53. Распределение Ферми
- § 54. Распределение Бозе
- § 55. Неравновесные ферми- и бозе-газы
- § 56. Ферми- и бозе-газы элементарных частиц
- § 57. Вырожденный электронный газ
- § 58. Теплоемкость вырожденного электронного газа
- § 60. Магнетизм электронного газа. Сильные поля
- § 61. Релятивистский вырожденный электронный газ
- Задачи
- § 62. Вырожденный бозе-газ
- Задача
- § 63. Черное излучение
- ГЛАВА VI. ТВЕРДЫЕ ТЕЛА
- § 64. Твердые тела при низких температурах
- § 65. Твердые тела при высоких температурах
- § 66. Интерполяционная формула Дебая
- § 67. Тепловое расширение твердых тел
- § 68. Сильно анизотропные кристаллы
- § 69. Колебания кристаллической решетки
- § 70. Плотность числа колебаний
- § 71. Фононы.
- § 72. Операторы рождения и уничтожения фононов
- § 73. Отрицательные температуры
- ГЛАВА VII. НЕИДЕАЛЬНЫЕ ГАЗЫ
- § 74. Отклонение газов от идеальности
- § 75. Разложение по степеням плотности
- § 76. Формула ван-дер-Ваальса
- § 77. Связь вириального коэффициента с амплитудой рассеяния
- § 78. Термодинамические величины классической плазмы
- § 79. Метод корреляционных функций
- § 80. Термодинамические величины вырожденной плазмы
- ГЛАВА VIII. РАВНОВЕСИЕ ФАЗ
- § 81. Условия равновесия фаз
- § 82. Формула Клапейрона — Клаузиуса
- § 83. Критическая точка
- § 84. Закон соответственных состояний
- ГЛАВА IX. РАСТВОРЫ
- § 85. Системы с различными частицами
- § 86. Правило фаз
- § 87. Слабые растворы
- § 88. Осмотическое давление
- § 89. Соприкосновение фаз растворителя
- § 90. Равновесие по отношению к растворенному веществу
- Задачи
- § 91. Выделение тепла и изменение объема при растворении
- § 92. Растворы сильных электролитов
- § 93. Смесь идеальных газов
- § 94. Смесь изотопов
- § 95. Давление пара над концентрированным раствором
- § 96. Термодинамические неравенства в растворах
- § 97. Кривые равновесия
- § 98. Примеры диаграмм состояния
- § 99. Пересечение особых кривых поверхности равновесия
- § 100. Газ и жидкость
- ГЛАВА X. ХИМИЧЕСКИЕ РЕАКЦИИ
- § 101. Условие химического равновесия
- § 102. Закон действующих масс
- Задачи
- § 103. Теплота реакции
- § 104. Ионизационное равновесие
- § 105. Равновесие по отношению к образованию пар
- ГЛАВА XI. СВОЙСТВА ВЕЩЕСТВА ПРИ ОЧЕНЬ БОЛЬШИХ ПЛОТНОСТЯХ
- § 106. Уравнение состояния вещества при больших плотностях
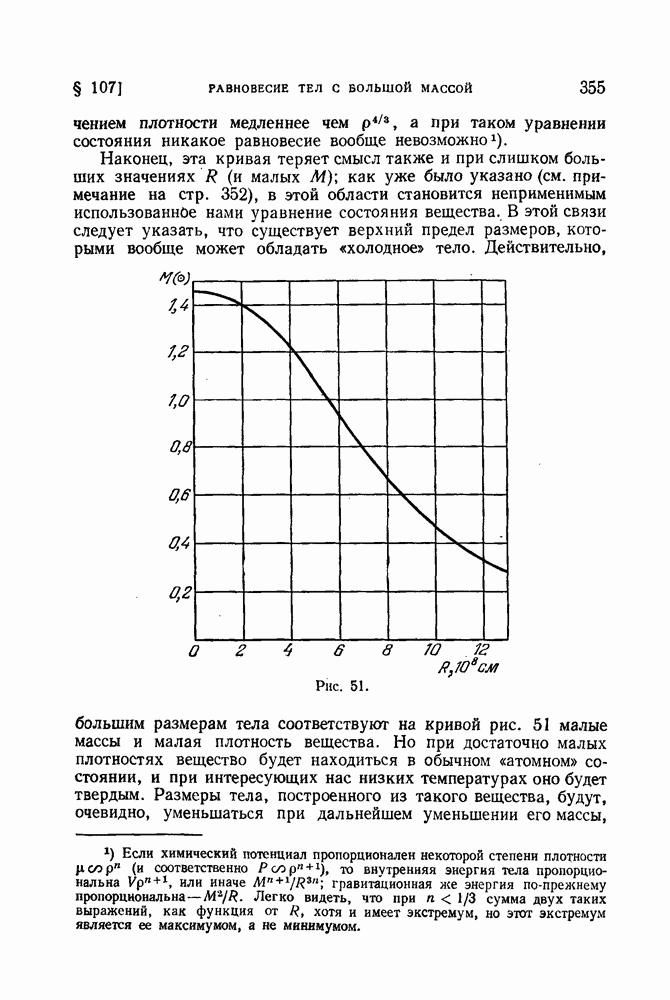
- § 107. Равновесие тел с большой массой
- § 108. Энергия гравитирующего тела
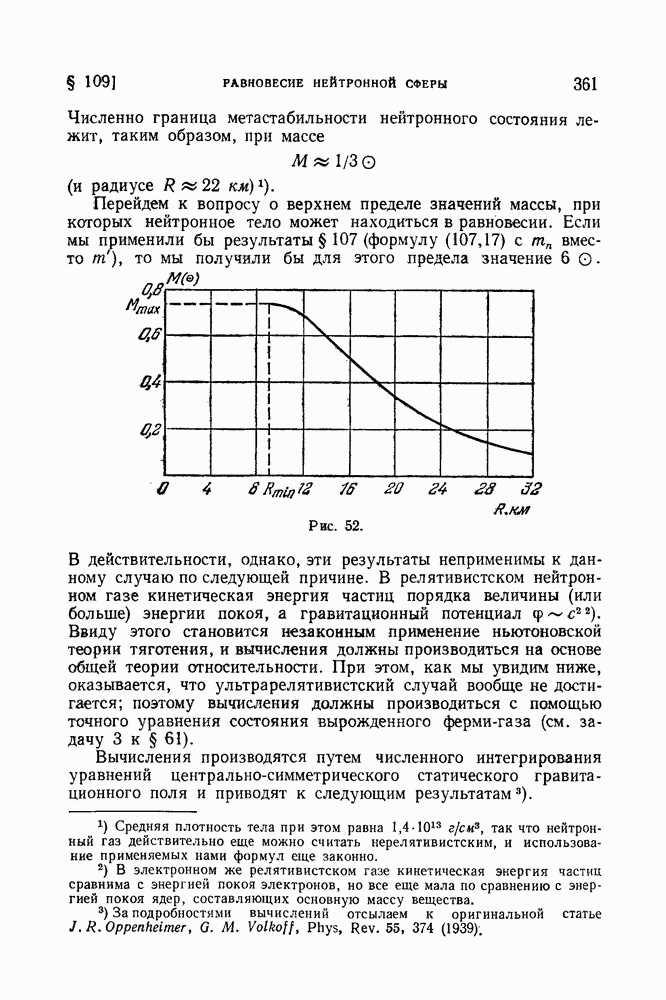
- § 109. Равновесие нейтронной сферы
- ГЛАВА XII. ФЛУКТУАЦИИ
- § 110. Распределение Гаусса
- § 111. Распределение Гаусса для нескольких величин
- § 112. Флуктуации основных термодинамических величин
- Задачи
- § 113. Флуктуации в идеальном газе
- § 114. Формула Пуассона
- § 115. Флуктуации в растворах
- § 116. Пространственная корреляция флуктуаций плотности
- § 117. Корреляция флуктуаций плотности в вырожденном газе
- Задачи
- § 118. Корреляция флуктуаций во времени
- § 119. Временная корреляция флуктуаций нескольких величин
- § 120. Симметрия кинетических коэффициентов
- § 121. Диссипативная функция
- § 122. Спектральное разложение флуктуаций
- § 123. Обобщенная восприимчивость
- § 124. Флуктуационно-диссипационная теорема
- § 125. Флуктуационно-диссипационная теорема для нескольких величин
- § 126. Операторное выражение обобщенной восприимчивости
- § 127. Флуктуации изгиба длинных молекул
- ГЛАВА XIII. СИММЕТРИЯ КРИСТАЛЛОВ
- § 128. Элементы симметрии кристаллической решетки
- § 129. Решетка Бравэ
- § 130. Кристаллические системы
- § 131. Кристаллические классы
- § 132. Пространственные группы
- § 133. Обратная решетка
- § 134. Неприводимые представления пространственных групп
- § 135. Симметрия относительно обращения времени
- § 136. Свойства симметрии нормальных колебаний кристаллической решетки
- § 137. Структуры с одно- и двумерной периодичностью
- § 138. Корреляционная функция в двумерных системах
- § 139. Симметрия по ориентации молекул
- § 140. Нематические и холестерические жидкие кристаллы
- § 141. Флуктуации в жидких кристаллах
- ГЛАВА XIV. ФАЗОВЫЕ ПЕРЕХОДЫ ВТОРОГО РОДА И КРИТИЧЕСКИЕ ЯВЛЕНИЯ
- § 142. Фазовые переходы второго рода
- § 143. Скачок теплоемкости
- § 144. Влияние внешнего поля на фазовый переход
- § 145. Изменение симметрии при фазовом переходе второго рода
- § 146. Флуктуации параметра порядка
- § 147. Эффективный гамильтониан
- § 148. Критические индексы
- § 149. Масштабная инвариантность
- § 150. Изолированные и критические точки непрерывного перехода
- § 151. Фазовый переход второго рода в двумерной решетке
- § 152. Ван-дер-ваальсова теория критической точки
- § 153. Флуктуационная теория критической точки
- ГЛАВА XV. ПОВЕРХНОСТИ
- § 154. Поверхностное натяжение
- § 155. Поверхностное натяжение кристаллов
- § 156. Поверхностное давление
- § 157. Поверхностное натяжение растворов
- § 158. Поверхностное натяжение растворов сильных электролитов
- § 159. Адсорбция
- § 160. Смачивание
- § 161. Краевой угол
- § 162. Образование зародышей при фазовых переходах
- § 163. Невозможность существования фаз в одномерных системах