| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
ГЛАВА IV. ИДЕАЛЬНЫЙ ГАЗ
§ 37. Распределение Больцмана
Одним из важнейших объектов изучения статистической физики является так называемый идеальный газ. Под этим названием подразумевают газ, взаимодействие между частицами (молекулами) которого настолько слабо, что им можно пренебречь. Физически допустимость такого пренебрежения может быть обеспечена либо малостью взаимодействия частиц при любых расстояниях между ними, либо достаточной разреженностью газа. В последнем, наиболее важном случае разреженность газа приводит к тому, что его молекулы почти всегда находятся на значительных расстояниях друг от друга, на которых силы взаимодействия уже достаточно малы.
Отсутствие взаимодействия между молекулами позволяет свести квантовомеханическую задачу об определении уровней энергии  всего газа в целом к задаче об определении уровней энергии отдельной молекулы. Эти уровни мы будем обозначать посредством
всего газа в целом к задаче об определении уровней энергии отдельной молекулы. Эти уровни мы будем обозначать посредством  , где индекс k представляет собой совокупность квантовых чисел, определяющих состояние молекулы. Энергии
, где индекс k представляет собой совокупность квантовых чисел, определяющих состояние молекулы. Энергии  выразятся тогда в виде сумм энергий каждой из молекул.
выразятся тогда в виде сумм энергий каждой из молекул.
Надо, однако, иметь в виду, что даже при отсутствии непосредственного силового взаимодействия в квантовой механике имеет место своеобразное взаимное влияние частиц, находящихся в одинаковом квантовом состоянии (так называемые обменные эффекты). Так, если частицы подчиняются статистике Ферми, то это влияние проявляется в том, что в каждом квантовом состоянии может находиться одновременно не более одной частицы); аналогичное влияние, проявляющееся иным образом, имеет место и для частиц, подчиняющихся статистике Бозе.
Обозначим посредством  число частиц в газе, находящихся в k-м квантовом состоянии; числа
число частиц в газе, находящихся в k-м квантовом состоянии; числа  называют числами заполнения различных квантовых состояний.
называют числами заполнения различных квантовых состояний.
Поставим задачу о вычислении средних значений  этих чисел, причем обратимся к подробному изучению чрезвычайно важного случая, когда все числа
этих чисел, причем обратимся к подробному изучению чрезвычайно важного случая, когда все числа

Физически этот случай соответствует достаточно разреженному газу. В дальнейшем будет установлен критерий, обеспечивающий выполнение этого условия, но уже сейчас укажем, что фактически оно выполняется для всех обычных молекулярных или атомных газов. Это условие нарушилось бы лишь при таких больших плотностях, при которых вещество фактически уже ни в какой мере нельзя было бы рассматривать как идеальный газ.
Условие  для средних чисел заполнения означает, что в каждый момент времени в каждом квантовом состоянии фактически находится не более одной частицы. В связи с этим можно пренебрегать не только непосредственным силовым взаимодействием частиц, но и их косвенным квантовомеханическим взаимным влиянием, упомянутым выше. Это обстоятельство в свою очередь позволяет применить к отдельным молекулам формулу распределения Гиббса.
для средних чисел заполнения означает, что в каждый момент времени в каждом квантовом состоянии фактически находится не более одной частицы. В связи с этим можно пренебрегать не только непосредственным силовым взаимодействием частиц, но и их косвенным квантовомеханическим взаимным влиянием, упомянутым выше. Это обстоятельство в свою очередь позволяет применить к отдельным молекулам формулу распределения Гиббса.
Действительно, распределение Гиббса было выведено нами для тел, являющихся относительно малыми, но в то же время макроскопическими частями каких-либо больших замкнутцх систем. Макроскопичность тел давала возможность считать их квазизамкнутыми, т. е. в известном смысле пренебречь их взаимодействием с другими частями системы. В рассматриваемом случае квазизамкнутыми являются отдельные молекулы газа, хотя они отнюдь не представляют собой макроскопических тел.
Применив к молекулам газа формулу распределения Гиббса, мы можем утверждать, что вероятность молекуле находиться в  состоянии, а потому и среднее число
состоянии, а потому и среднее число  молекул в этом состоянии, пропорциональны
молекул в этом состоянии, пропорциональны  :
:

где а — постоянная, определяющаяся условием нормировки

(N — полное число частиц в газе). Распределение молекул идеального газа по различным состояниям, определяемое формулой (37,2), называется распределением Больцмана (оно было открыто Больцманом для классической статистики в 1877 г.).
Постоянный коэффициент в (37,2) может быть выражен через термодинамические величины газа. Для этого дадим еще один вывод этой формулы, основанный на применении распределения Гиббса к совокупности всех частиц газа, находящихся в данном квантовом состоянии.
Мы имеем право сделать это (даже если числа  не малы), поскольку непосредственного силового взаимодействия между этими и остальными частицами (как и между всеми вообще частицами идеального газа) нет, а квантовомеханические обменные эффекты имеют место лишь для частиц, находящихся в одном и том же состоянии. Полагая в общей формуле распределения Гиббса с переменным числом частиц
не малы), поскольку непосредственного силового взаимодействия между этими и остальными частицами (как и между всеми вообще частицами идеального газа) нет, а квантовомеханические обменные эффекты имеют место лишь для частиц, находящихся в одном и том же состоянии. Полагая в общей формуле распределения Гиббса с переменным числом частиц  и приписывая индекс k величине
и приписывая индекс k величине  получим распределение вероятностей различных значений
получим распределение вероятностей различных значений  в виде
в виде

В частности,  есть вероятность полного отсутствия частиц в данном состоянии. В интересующем нас здесь случае, когда
есть вероятность полного отсутствия частиц в данном состоянии. В интересующем нас здесь случае, когда  вероятность
вероятность  близка к единице; поэтому в выражении
близка к единице; поэтому в выражении  для вероятности наличия одной частицы в
для вероятности наличия одной частицы в  состоянии можно положить, опуская члены высшего порядка малости,
состоянии можно положить, опуская члены высшего порядка малости,  . Тогда
. Тогда

Что же касается вероятностей значений  , то они в том же приближении должны быть положены равными нулю. Поэтому
, то они в том же приближении должны быть положены равными нулю. Поэтому

и мы получаем распределение Больцмана в виде

Таким образом, коэффициент в формуле (37,2) оказываете» выраженным через химический потенциал газа.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ
- НЕКОТОРЫЕ ОБОЗНАЧЕНИЯ
- ГЛАВА I. ОСНОВНЫЕ ПРИНЦИПЫ СТАТИСТИКИ
- § 1. Статистическое распределение
- § 2. Статистическая независимость
- § 3. Теорема Лиувилля
- § 4. Роль энергии
- § 5. Статистическая матрица
- § 6. Статистическое распределение в квантовой статистике
- § 7. Энтропия
- § 8. Закон возрастания энтропии
- ГЛАВА II. ТЕРМОДИНАМИЧЕСКИЕ ВЕЛИЧИНЫ
- § 9. Температура
- § 10. Макроскопическое движение
- § 11. Адиабатический процесс
- § 12. Давление
- § 13. Работа и количество тепла
- § 14. Тепловая функция
- § 15. Свободная энергия и термодинамический потенциал
- § 16. Соотношения между производными термодинамических величин
- § 17. Термодинамическая шкала температуры
- § 18. Процесс Джоуля — Томсона
- § 19. Максимальная работа
- § 20. Максимальная работа, производимая телом, находящимся во внешней среде
- § 21. Термодинамические неравенства
- § 22. Принцип Ле-Шателье
- § 23. Теорема Нериста
- § 24. Зависимость термодинамических величин от числа частиц
- § 25. Равновесие тела во внешнем поле
- § 26. Вращающиеся тела
- § 27. Термодинамические соотношения в релятивистской области
- ГЛАВА III. РАСПРЕДЕЛЕНИЕ ГИББСА
- § 28. Распределение Гиббса
- § 29. Распределение Максвелла
- Задачи
- § 30. Распределение вероятностей для осциллятора
- § 31. Свободная энергия в распределении Гиббса
- Задачи
- § 32. Термодинамическая теория возмущений
- § 33. Разложение по степеням h
- § 34. Распределение Гиббса для вращающихся тел
- § 35. Распределение Гиббса с переменным числом частиц
- § 36. Вывод термодинамических соотношений из распределения Гиббса
- ГЛАВА IV. ИДЕАЛЬНЫЙ ГАЗ
- § 37. Распределение Больцмана
- § 38. Распределение Больцмана в классической статистике
- Задачи
- § 39. Столкновения молекул
- Задачи
- § 40. Неравновесный идеальный газ
- § 41. Свободная энергия больцмановского идеального газа
- § 42. Уравнение состояния идеального газа
- Задачи
- § 43. Идеальный газ с постоянной теплоемкостью
- Задачи
- § 44. Закон равнораспределения
- § 43. Одноатомный идеальный газ
- § 46. Одноатомный газ. Влияние электронного момента
- § 47. Двухатомный газ с молекулами из различных атомов. Вращение молекул
- § 48. Двухатомный газ с молекулами из одинаковых атомов. Вращение молекул
- § 49. Двухатомный газ. Колебания атомов
- § 50. Двухатомный газ. Влияние электронного момента
- § 51. Многоатомный газ
- § 52. Магнетизм газов
- Задачи
- ГЛАВА V. РАСПРЕДЕЛЕНИЯ ФЕРМИ И БОЗЕ
- § 53. Распределение Ферми
- § 54. Распределение Бозе
- § 55. Неравновесные ферми- и бозе-газы
- § 56. Ферми- и бозе-газы элементарных частиц
- § 57. Вырожденный электронный газ
- § 58. Теплоемкость вырожденного электронного газа
- § 60. Магнетизм электронного газа. Сильные поля
- § 61. Релятивистский вырожденный электронный газ
- Задачи
- § 62. Вырожденный бозе-газ
- Задача
- § 63. Черное излучение
- ГЛАВА VI. ТВЕРДЫЕ ТЕЛА
- § 64. Твердые тела при низких температурах
- § 65. Твердые тела при высоких температурах
- § 66. Интерполяционная формула Дебая
- § 67. Тепловое расширение твердых тел
- § 68. Сильно анизотропные кристаллы
- § 69. Колебания кристаллической решетки
- § 70. Плотность числа колебаний
- § 71. Фононы.
- § 72. Операторы рождения и уничтожения фононов
- § 73. Отрицательные температуры
- ГЛАВА VII. НЕИДЕАЛЬНЫЕ ГАЗЫ
- § 74. Отклонение газов от идеальности
- § 75. Разложение по степеням плотности
- § 76. Формула ван-дер-Ваальса
- § 77. Связь вириального коэффициента с амплитудой рассеяния
- § 78. Термодинамические величины классической плазмы
- § 79. Метод корреляционных функций
- § 80. Термодинамические величины вырожденной плазмы
- ГЛАВА VIII. РАВНОВЕСИЕ ФАЗ
- § 81. Условия равновесия фаз
- § 82. Формула Клапейрона — Клаузиуса
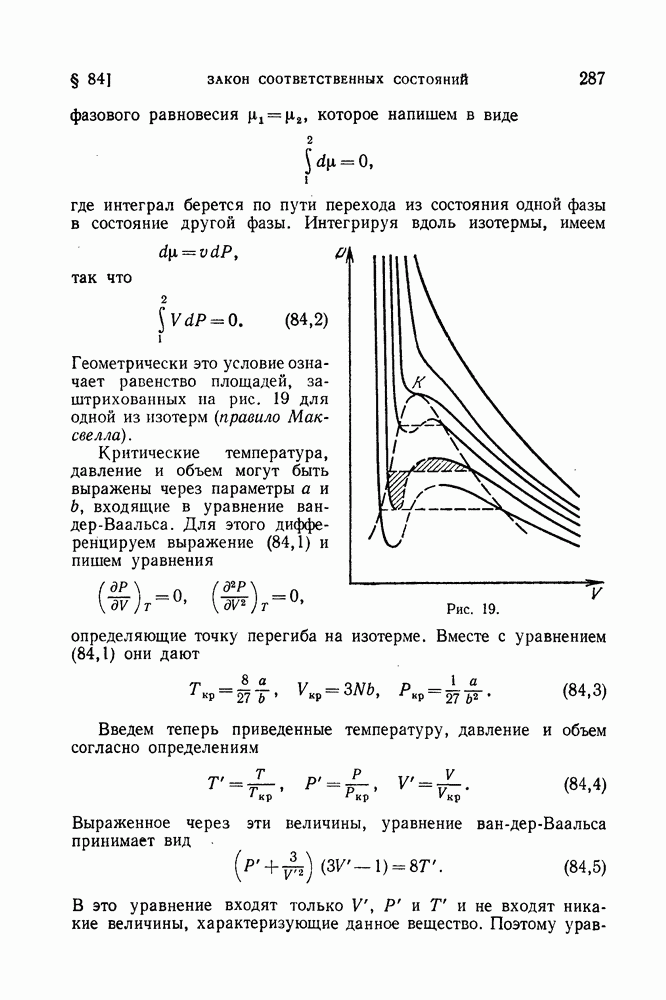
- § 83. Критическая точка
- § 84. Закон соответственных состояний
- ГЛАВА IX. РАСТВОРЫ
- § 85. Системы с различными частицами
- § 86. Правило фаз
- § 87. Слабые растворы
- § 88. Осмотическое давление
- § 89. Соприкосновение фаз растворителя
- § 90. Равновесие по отношению к растворенному веществу
- Задачи
- § 91. Выделение тепла и изменение объема при растворении
- § 92. Растворы сильных электролитов
- § 93. Смесь идеальных газов
- § 94. Смесь изотопов
- § 95. Давление пара над концентрированным раствором
- § 96. Термодинамические неравенства в растворах
- § 97. Кривые равновесия
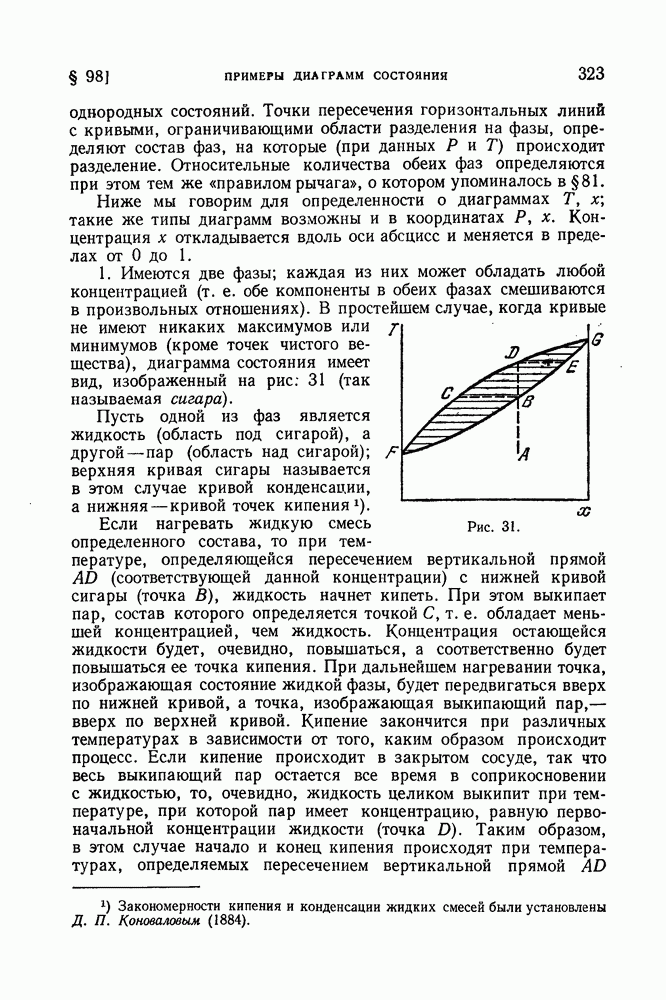
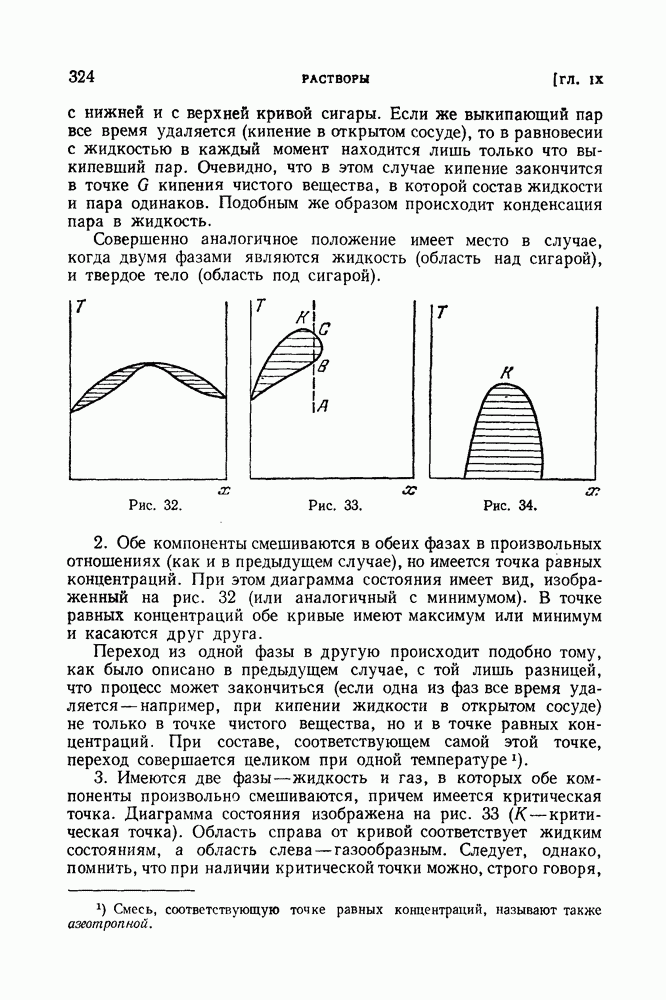
- § 98. Примеры диаграмм состояния
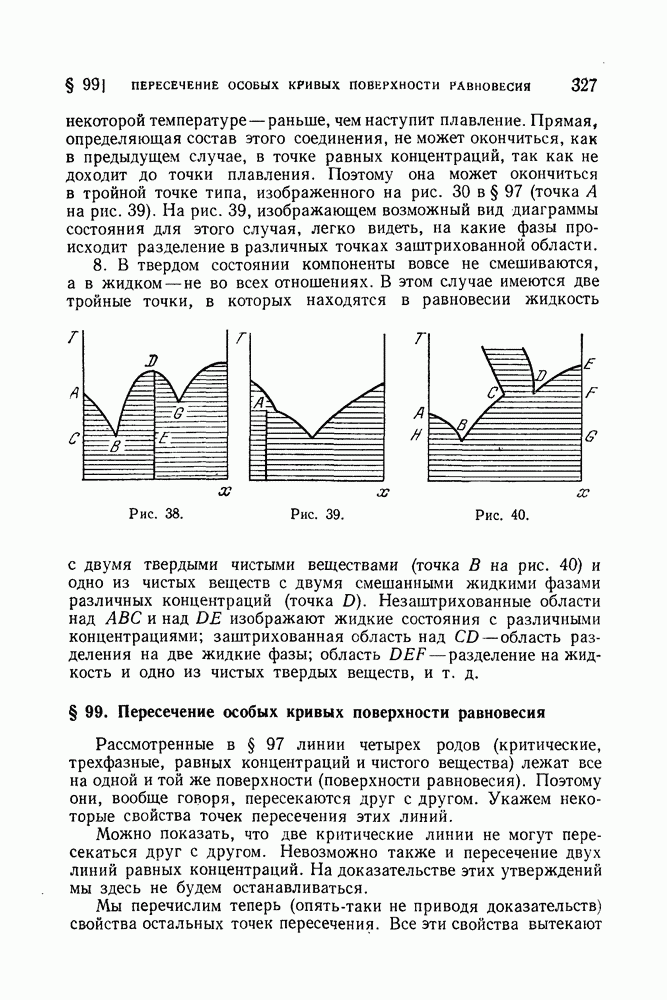
- § 99. Пересечение особых кривых поверхности равновесия
- § 100. Газ и жидкость
- ГЛАВА X. ХИМИЧЕСКИЕ РЕАКЦИИ
- § 101. Условие химического равновесия
- § 102. Закон действующих масс
- Задачи
- § 103. Теплота реакции
- § 104. Ионизационное равновесие
- § 105. Равновесие по отношению к образованию пар
- ГЛАВА XI. СВОЙСТВА ВЕЩЕСТВА ПРИ ОЧЕНЬ БОЛЬШИХ ПЛОТНОСТЯХ
- § 106. Уравнение состояния вещества при больших плотностях
- § 107. Равновесие тел с большой массой
- § 108. Энергия гравитирующего тела
- § 109. Равновесие нейтронной сферы
- ГЛАВА XII. ФЛУКТУАЦИИ
- § 110. Распределение Гаусса
- § 111. Распределение Гаусса для нескольких величин
- § 112. Флуктуации основных термодинамических величин
- Задачи
- § 113. Флуктуации в идеальном газе
- § 114. Формула Пуассона
- § 115. Флуктуации в растворах
- § 116. Пространственная корреляция флуктуаций плотности
- § 117. Корреляция флуктуаций плотности в вырожденном газе
- Задачи
- § 118. Корреляция флуктуаций во времени
- § 119. Временная корреляция флуктуаций нескольких величин
- § 120. Симметрия кинетических коэффициентов
- § 121. Диссипативная функция
- § 122. Спектральное разложение флуктуаций
- § 123. Обобщенная восприимчивость
- § 124. Флуктуационно-диссипационная теорема
- § 125. Флуктуационно-диссипационная теорема для нескольких величин
- § 126. Операторное выражение обобщенной восприимчивости
- § 127. Флуктуации изгиба длинных молекул
- ГЛАВА XIII. СИММЕТРИЯ КРИСТАЛЛОВ
- § 128. Элементы симметрии кристаллической решетки
- § 129. Решетка Бравэ
- § 130. Кристаллические системы
- § 131. Кристаллические классы
- § 132. Пространственные группы
- § 133. Обратная решетка
- § 134. Неприводимые представления пространственных групп
- § 135. Симметрия относительно обращения времени
- § 136. Свойства симметрии нормальных колебаний кристаллической решетки
- § 137. Структуры с одно- и двумерной периодичностью
- § 138. Корреляционная функция в двумерных системах
- § 139. Симметрия по ориентации молекул
- § 140. Нематические и холестерические жидкие кристаллы
- § 141. Флуктуации в жидких кристаллах
- ГЛАВА XIV. ФАЗОВЫЕ ПЕРЕХОДЫ ВТОРОГО РОДА И КРИТИЧЕСКИЕ ЯВЛЕНИЯ
- § 142. Фазовые переходы второго рода
- § 143. Скачок теплоемкости
- § 144. Влияние внешнего поля на фазовый переход
- § 145. Изменение симметрии при фазовом переходе второго рода
- § 146. Флуктуации параметра порядка
- § 147. Эффективный гамильтониан
- § 148. Критические индексы
- § 149. Масштабная инвариантность
- § 150. Изолированные и критические точки непрерывного перехода
- § 151. Фазовый переход второго рода в двумерной решетке
- § 152. Ван-дер-ваальсова теория критической точки
- § 153. Флуктуационная теория критической точки
- ГЛАВА XV. ПОВЕРХНОСТИ
- § 154. Поверхностное натяжение
- § 155. Поверхностное натяжение кристаллов
- § 156. Поверхностное давление
- § 157. Поверхностное натяжение растворов
- § 158. Поверхностное натяжение растворов сильных электролитов
- § 159. Адсорбция
- § 160. Смачивание
- § 161. Краевой угол
- § 162. Образование зародышей при фазовых переходах
- § 163. Невозможность существования фаз в одномерных системах