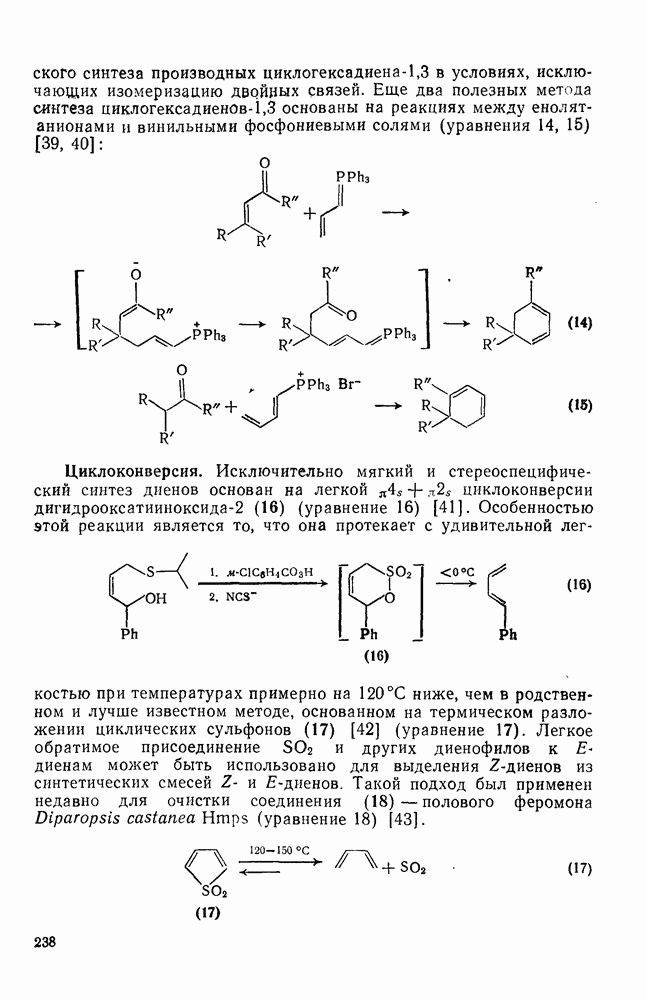
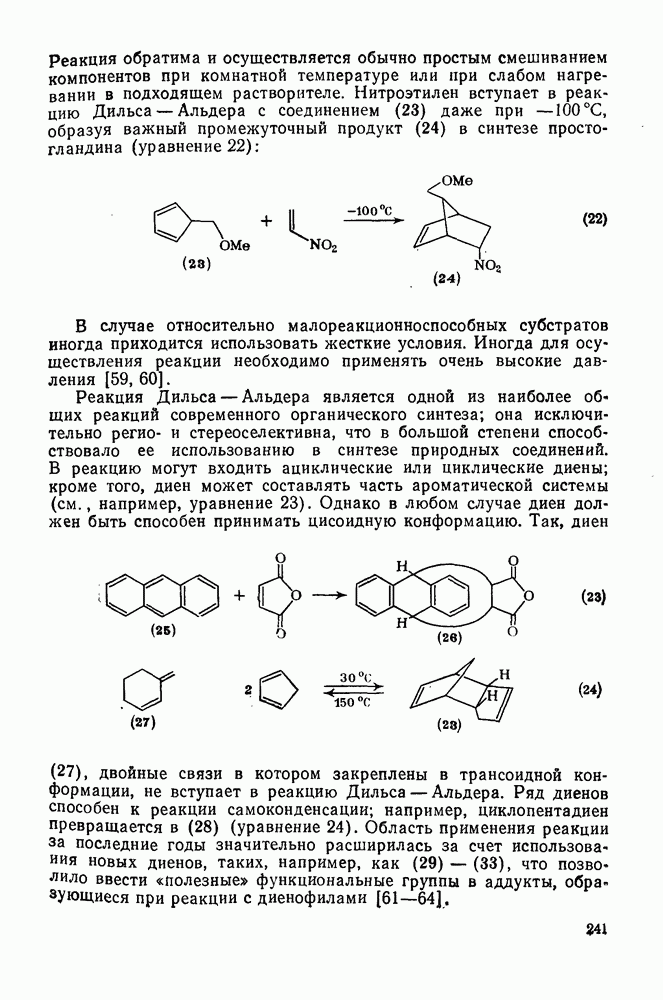
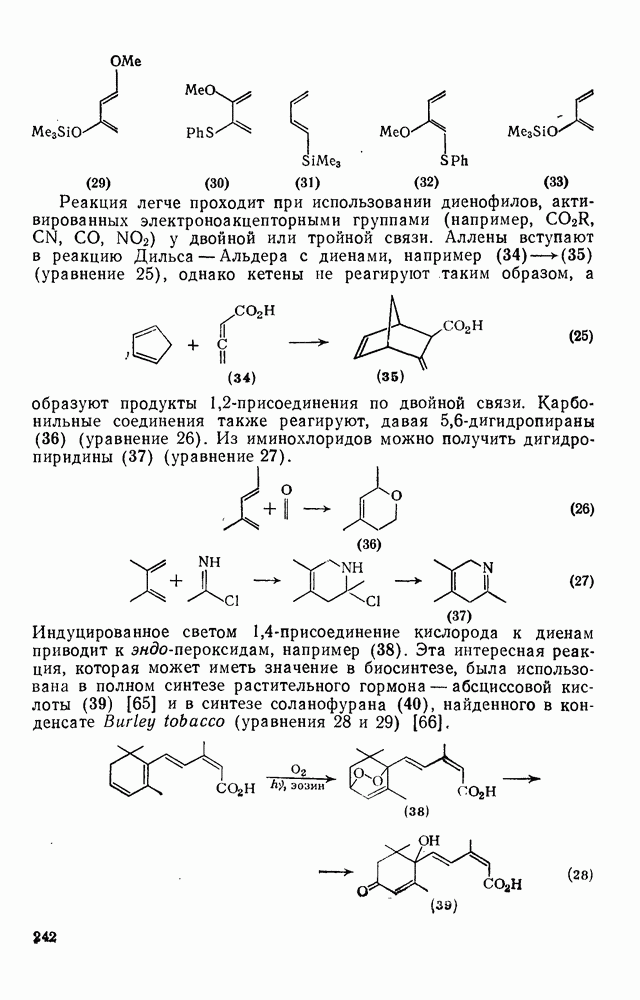
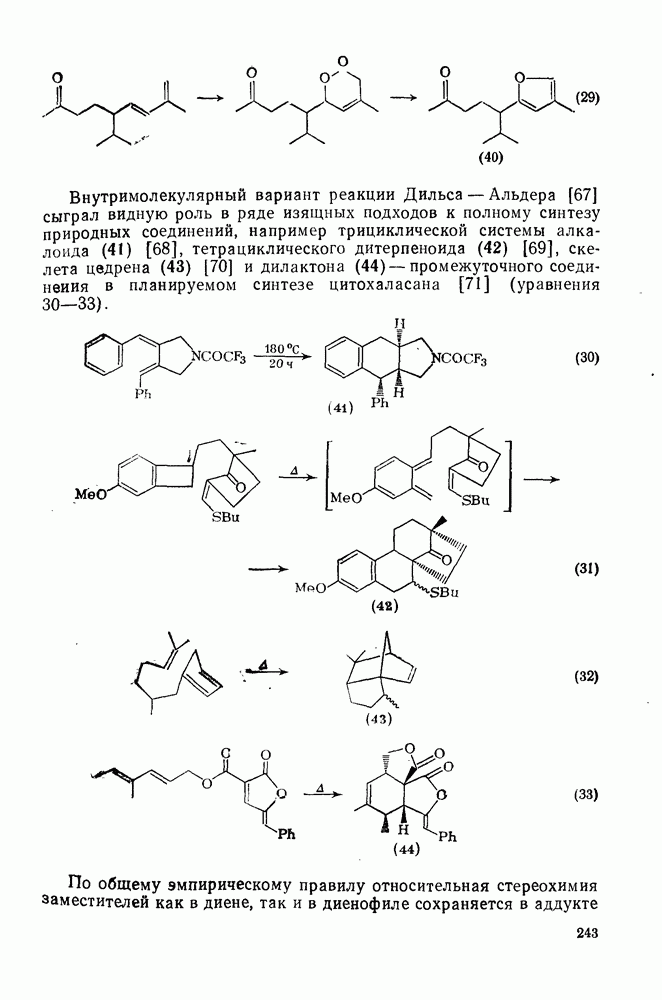
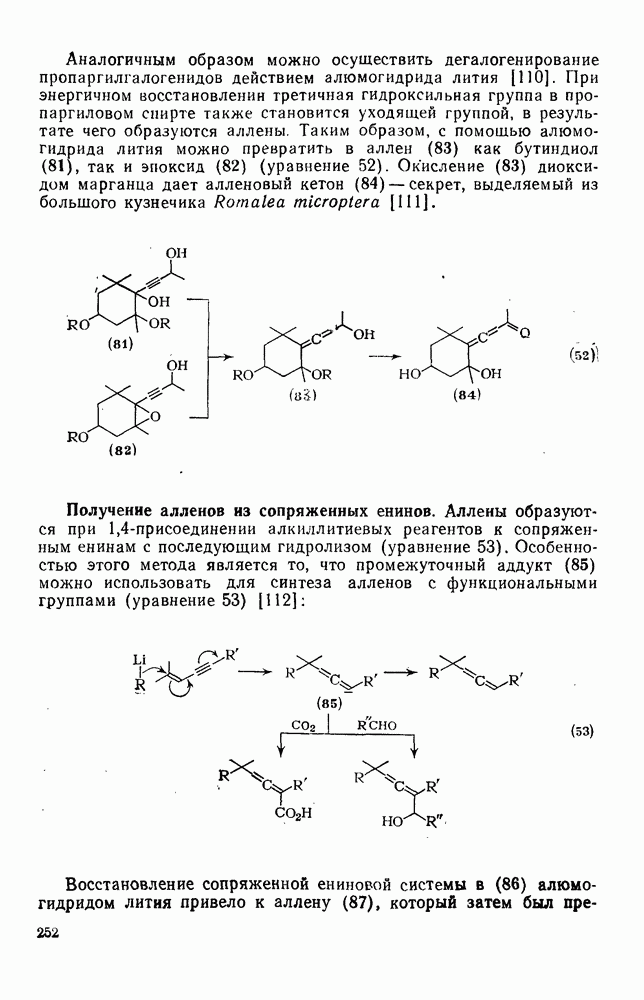
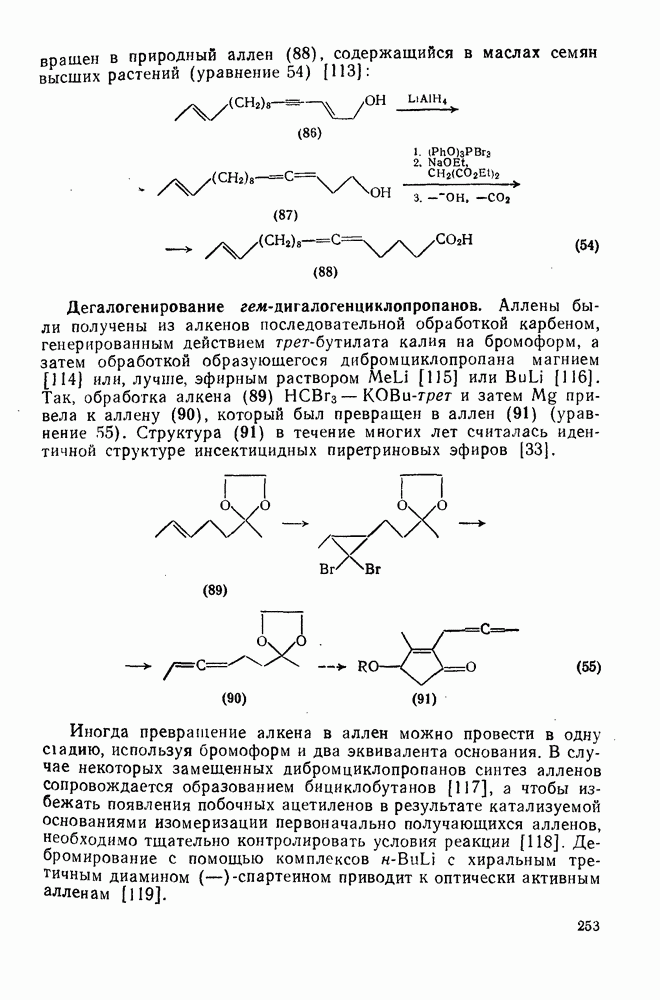
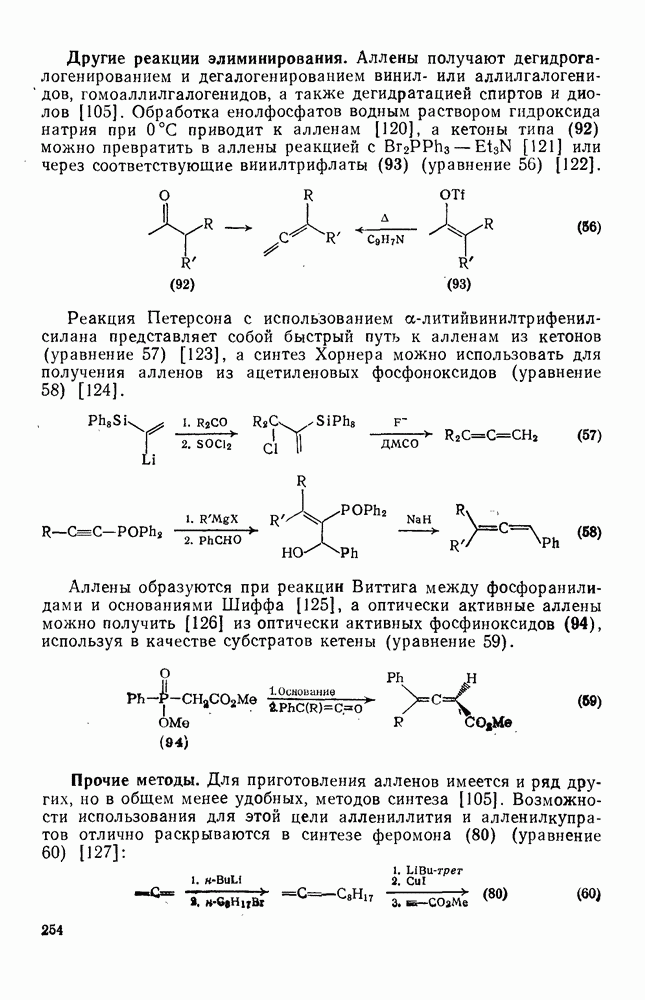
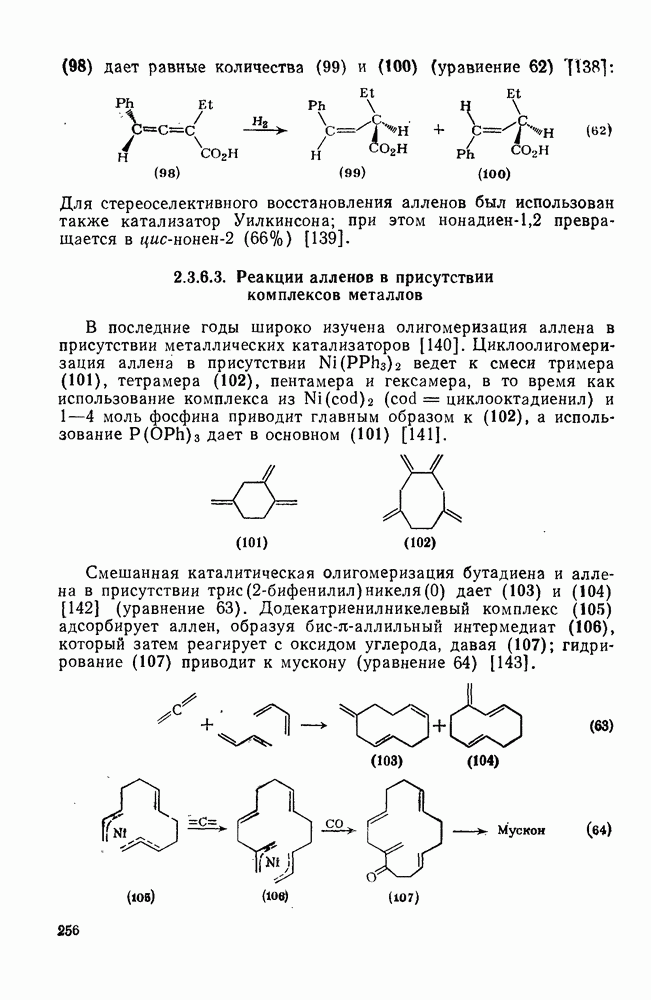
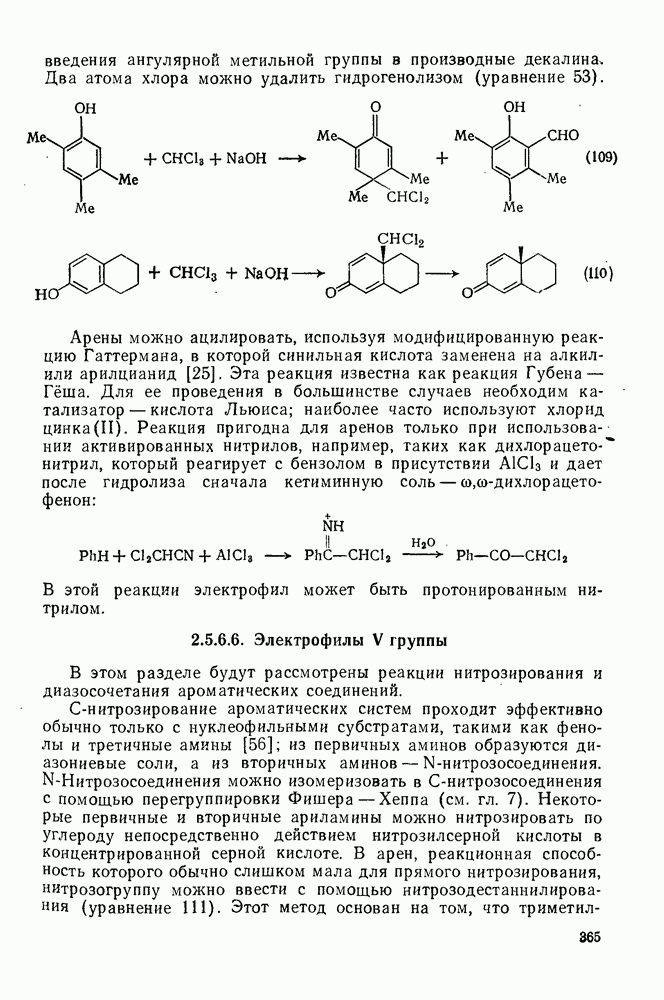
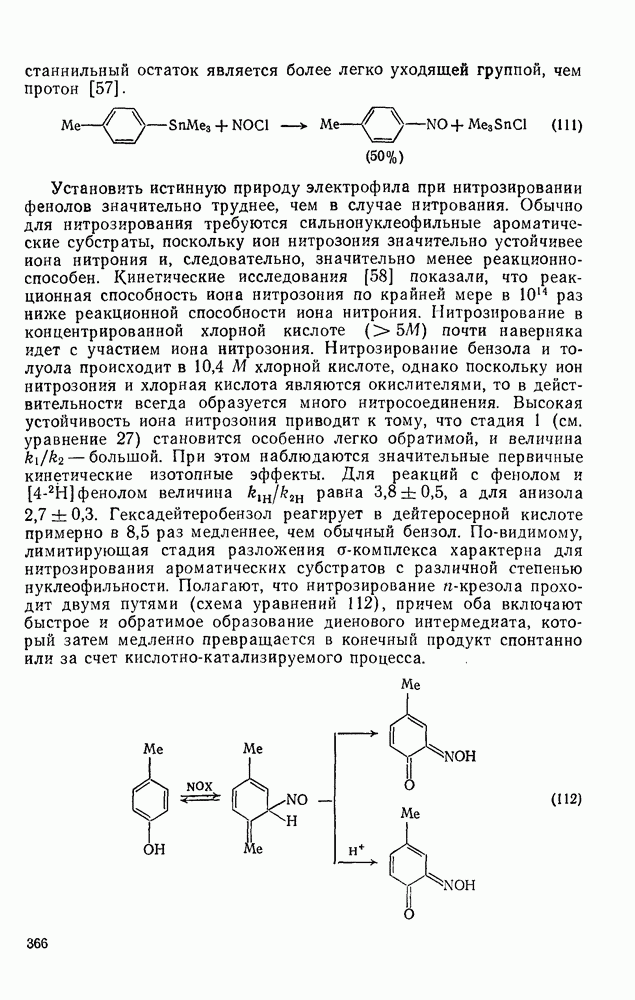
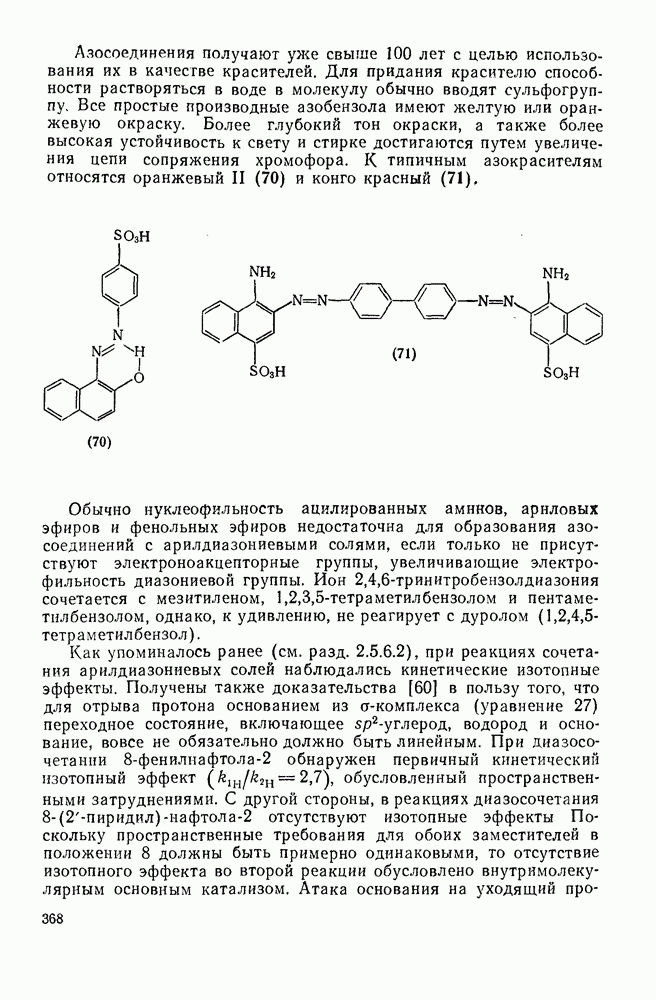
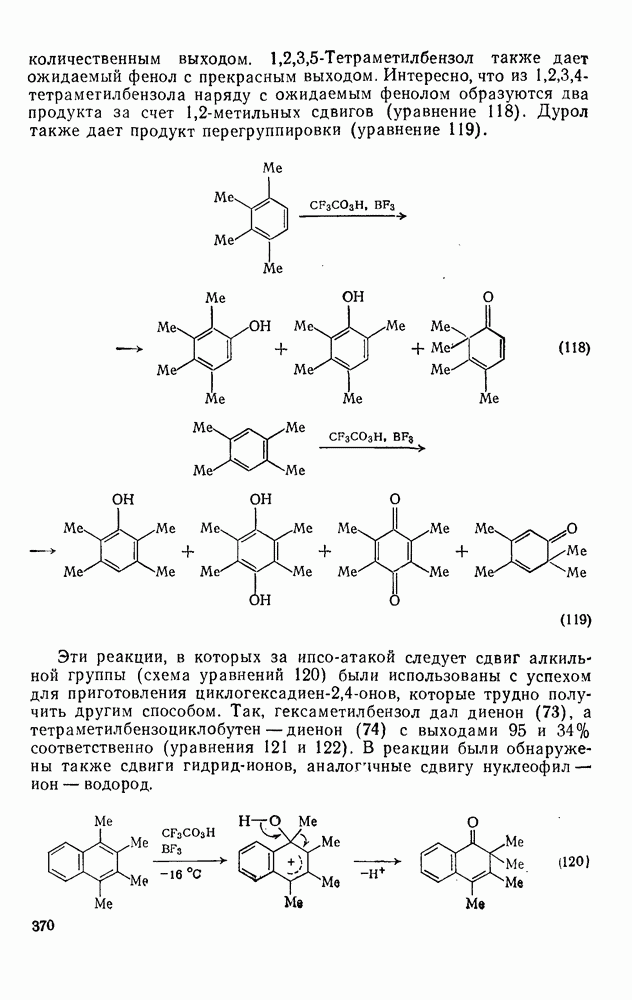
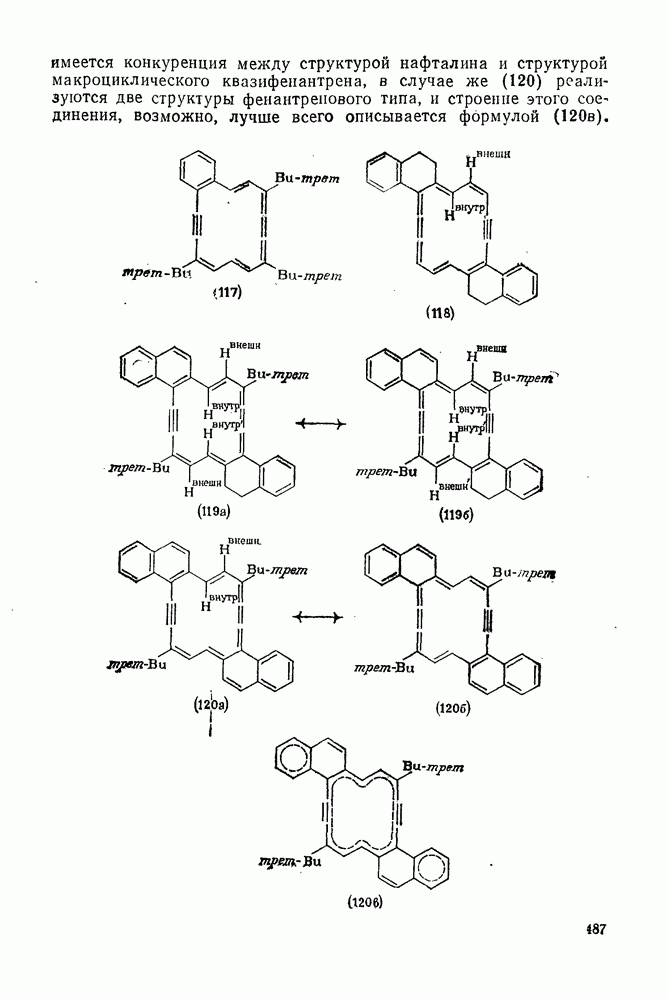
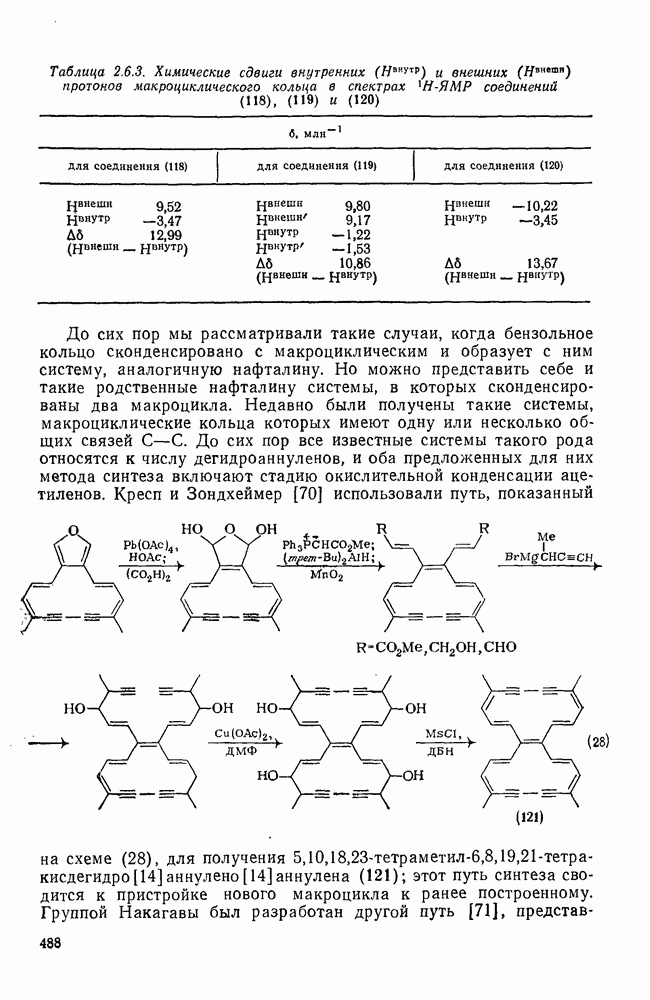
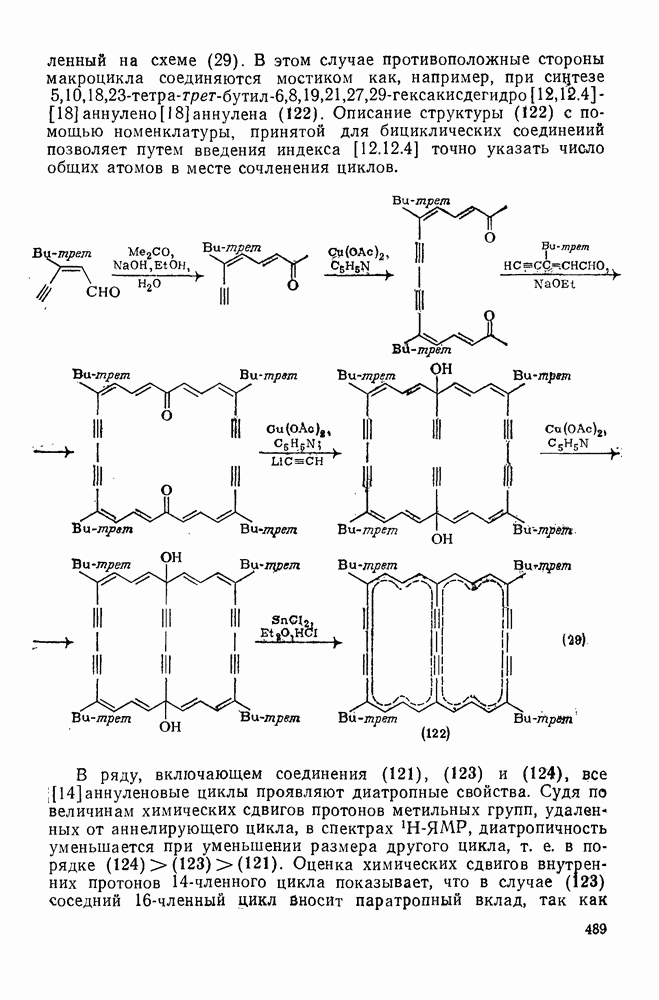
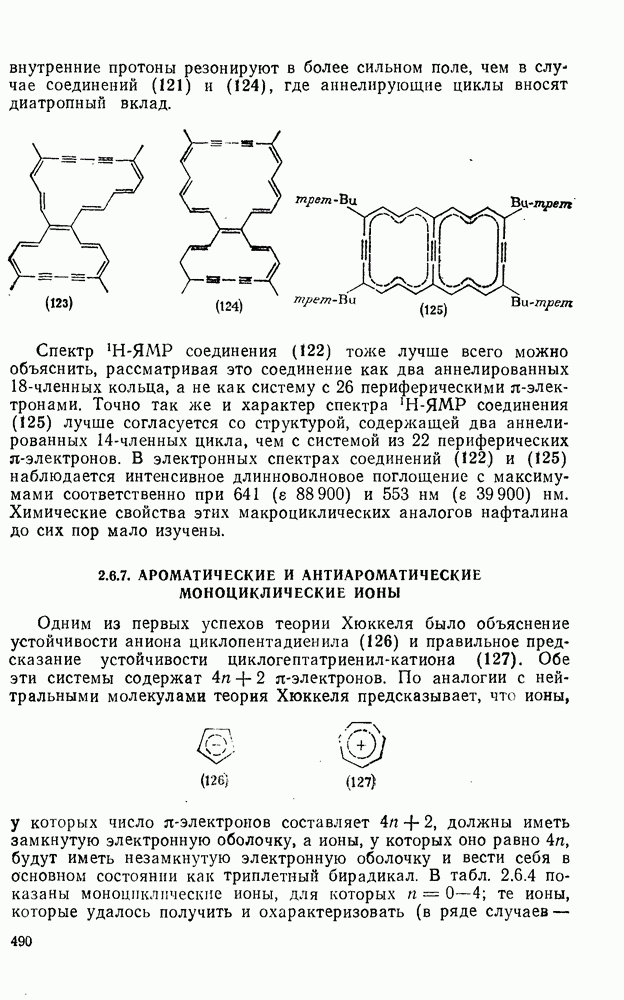
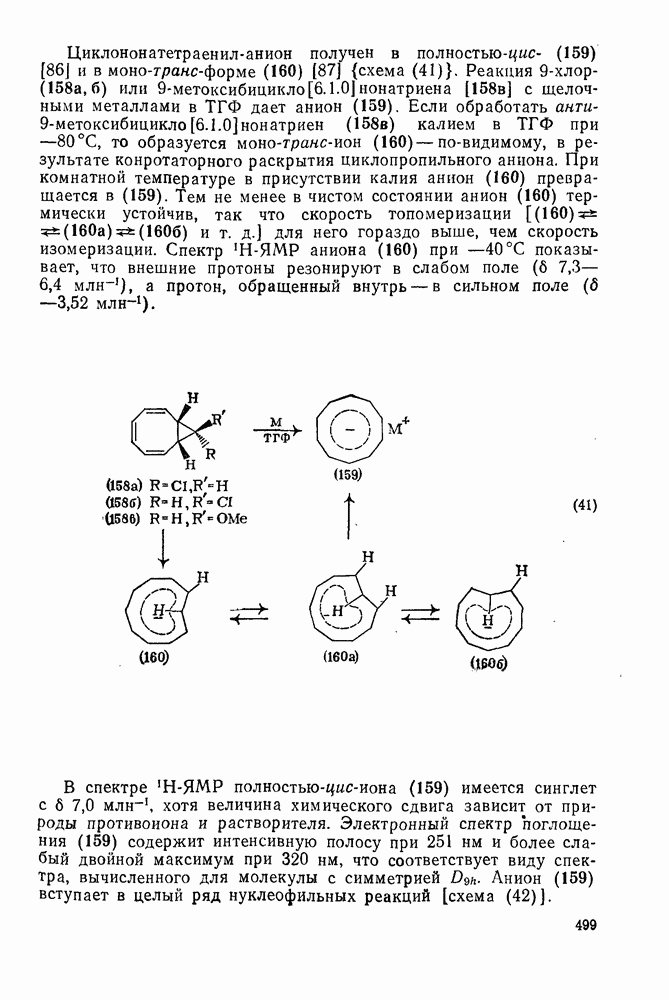
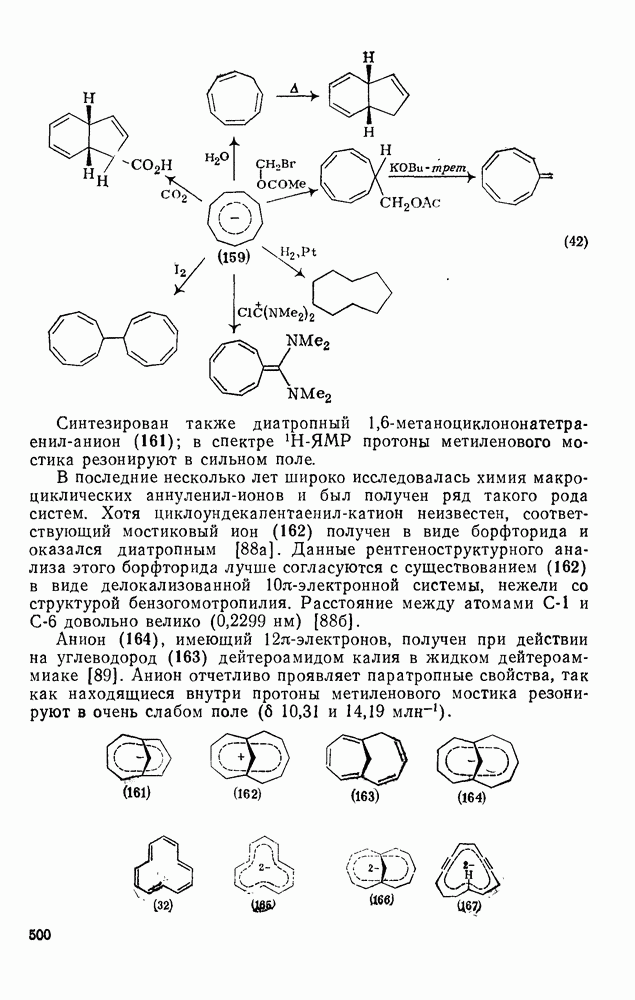
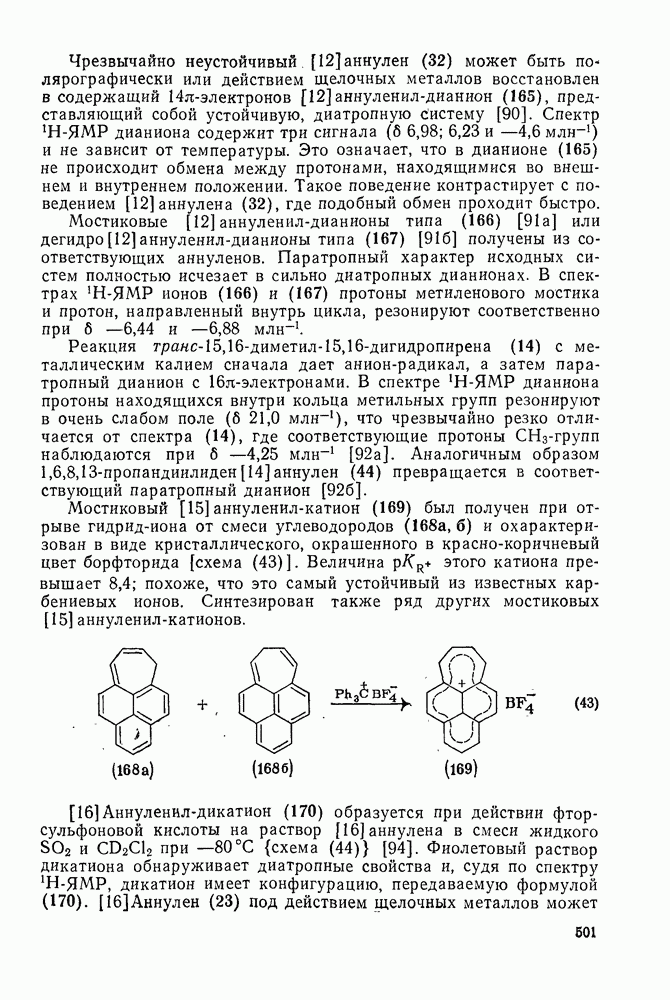
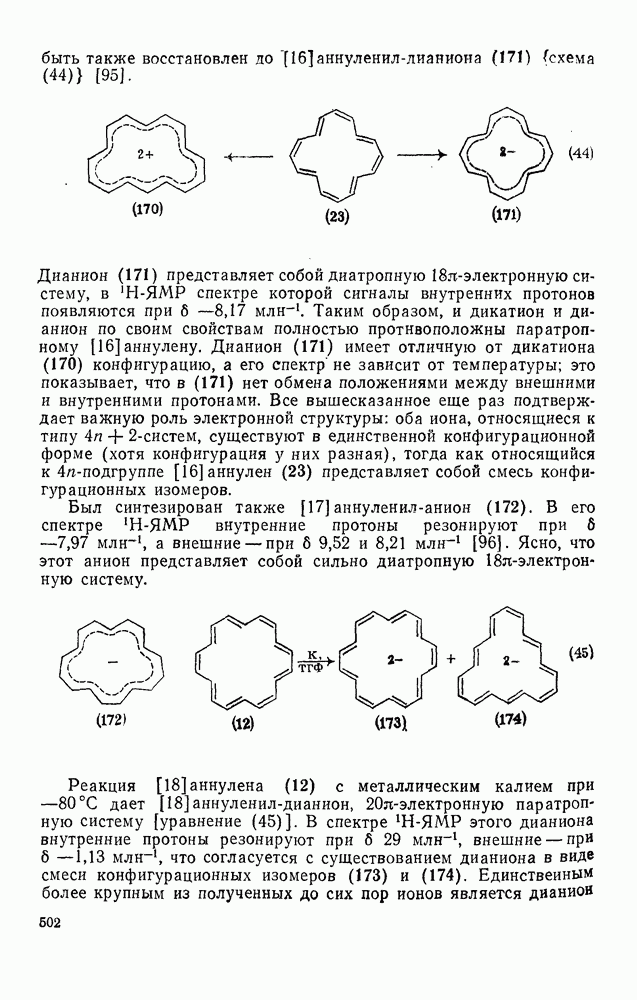
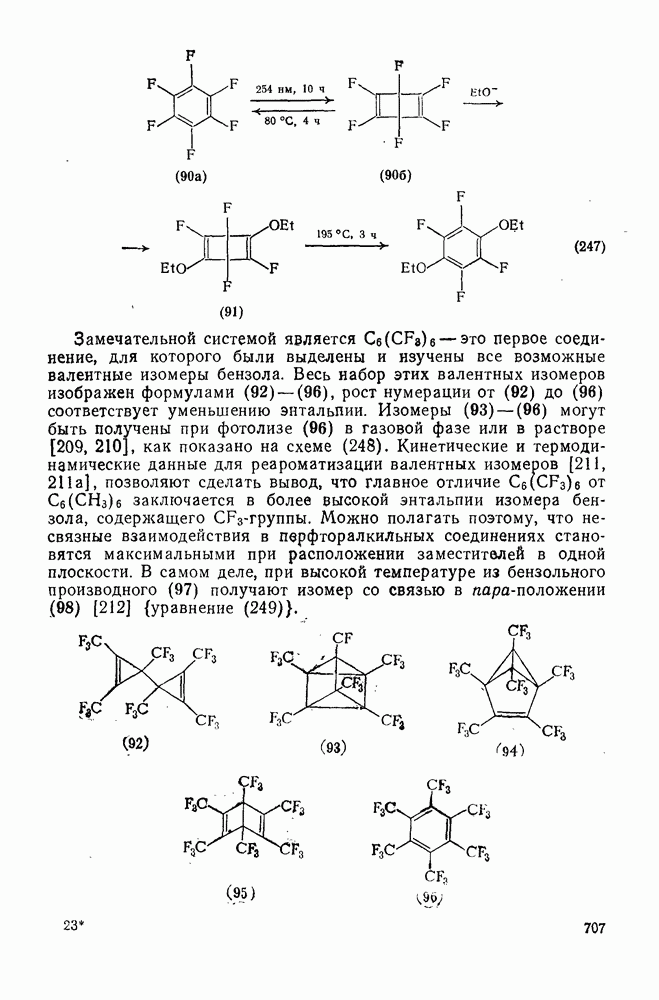
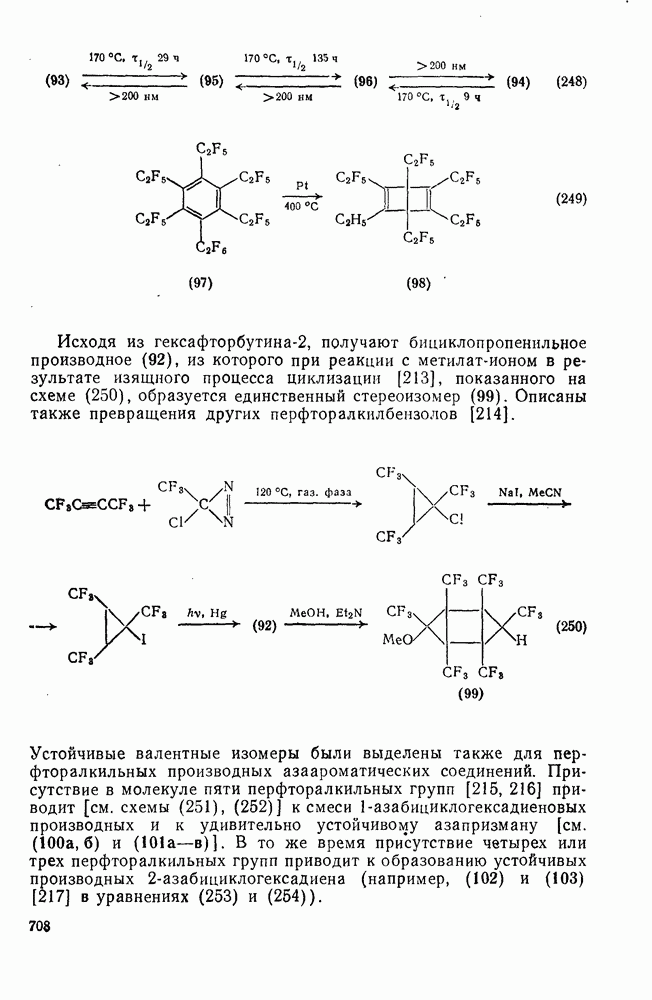
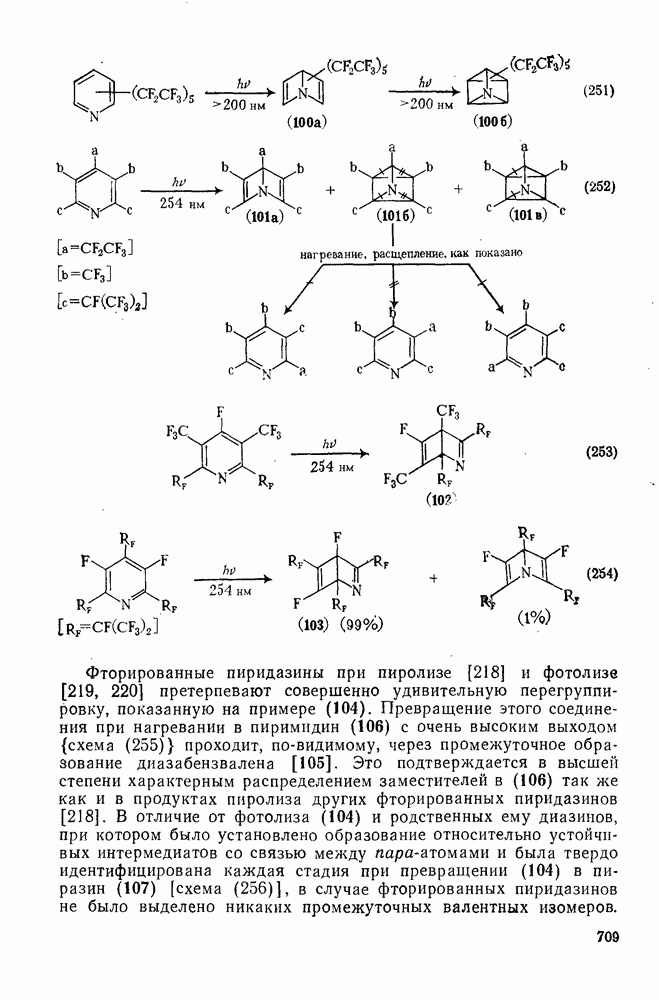
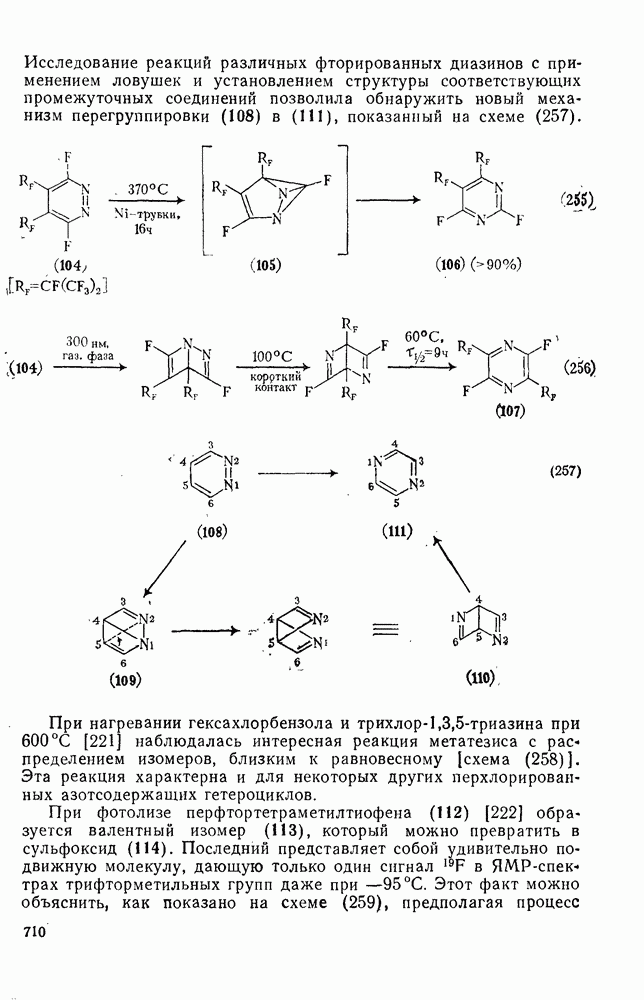
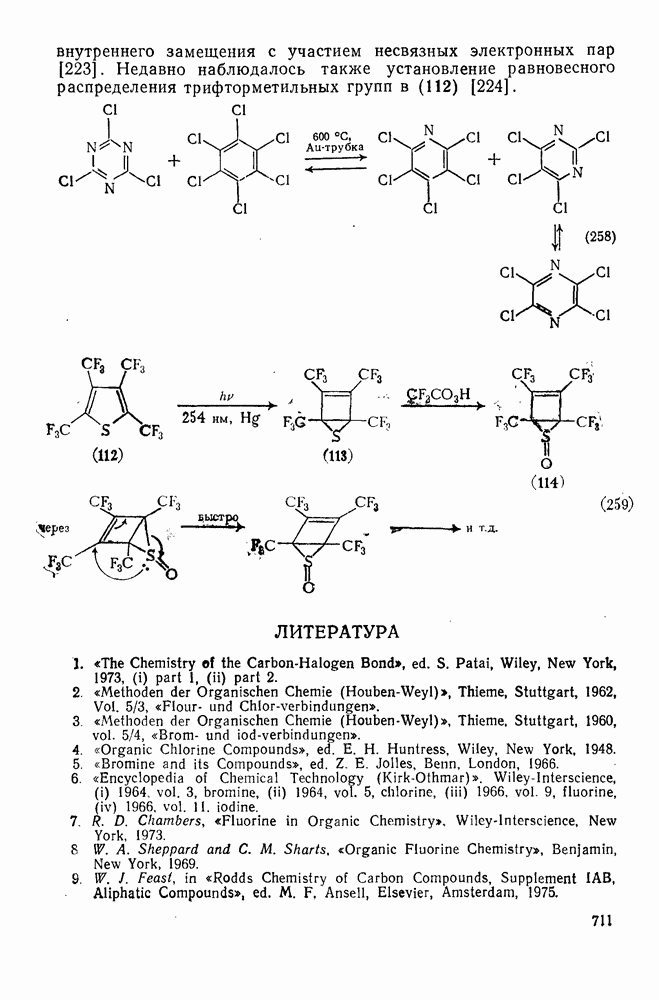
| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
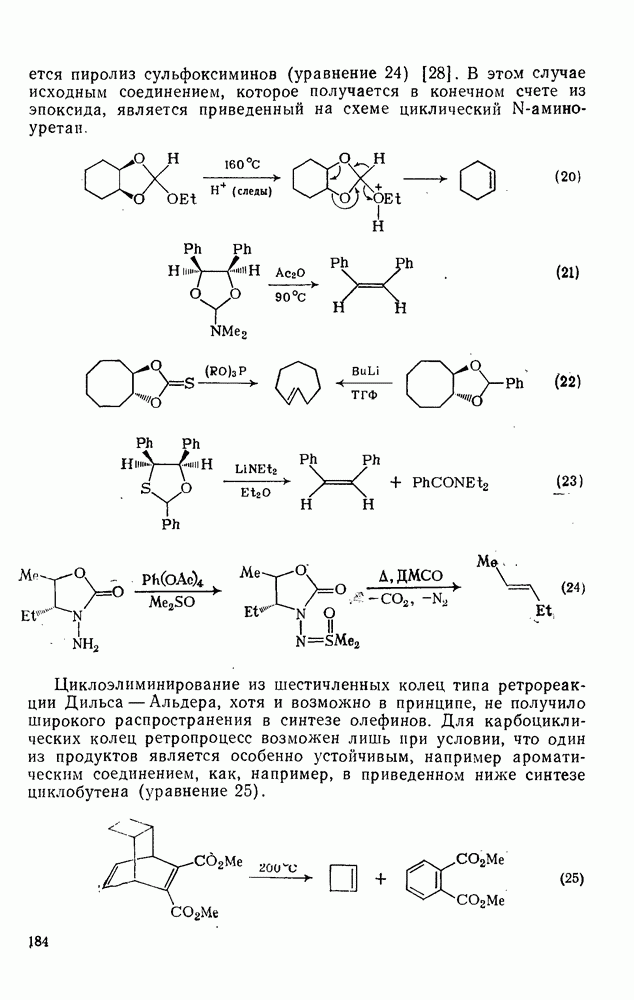
2.5.9.3. Фотоциклоприсоединение к моноциклическим аренам [126]
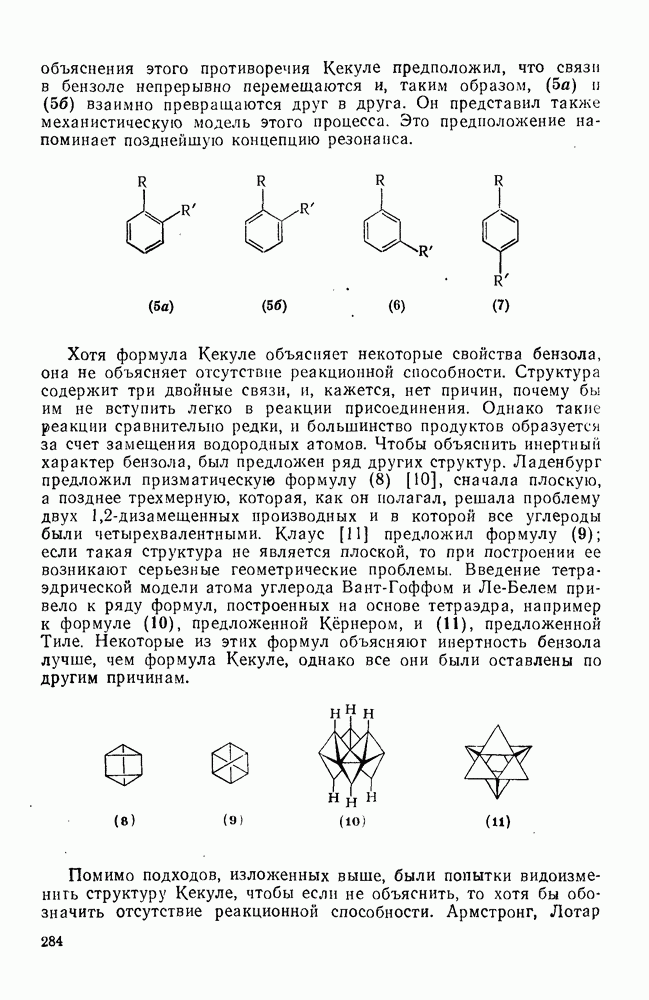
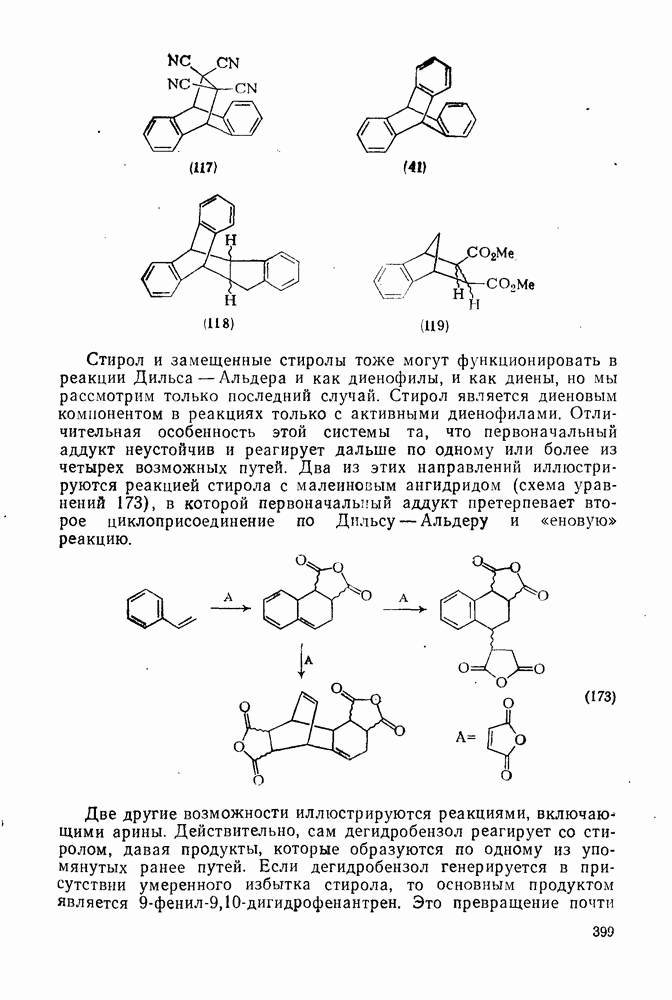
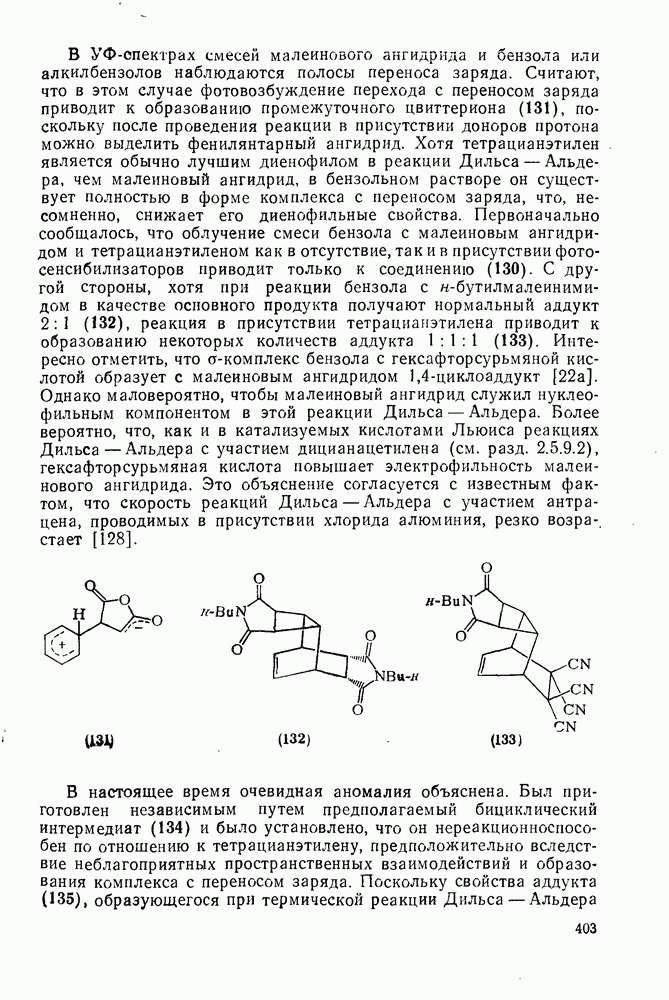
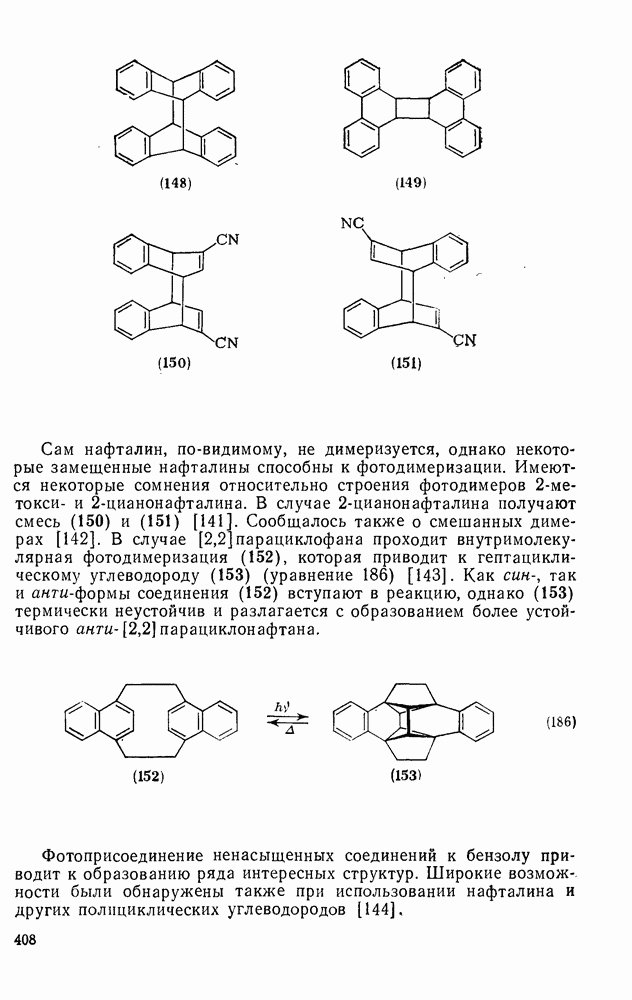
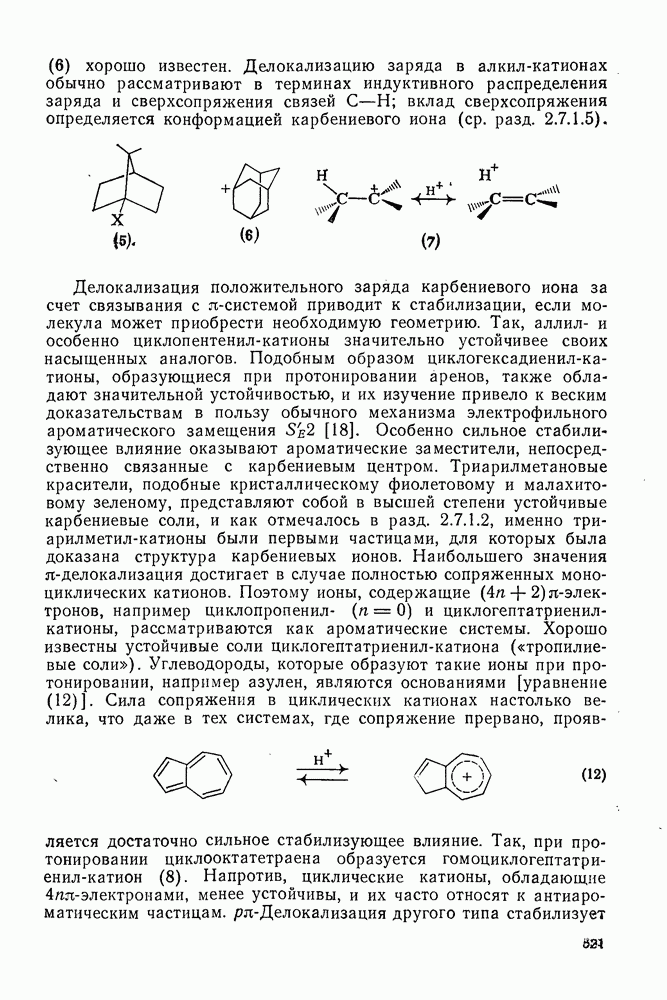
Хотя первая фотохимическая реакция арена — фотодимериза-ция антрацена — была описана свыше 100 лет назад, только за последние 20 лет фотоприсоединение и фотоизомеризация аренов были изучены подробно. После сообщения об образовании аддукта  между малеиновым ангидридом и бензолом (уравнение 178) [127] были открыты многие типы реакции фотоприсоединения с участием аренов. Формально структура продукта (130) такова, как будто он образовался за счет фотохимического
между малеиновым ангидридом и бензолом (уравнение 178) [127] были открыты многие типы реакции фотоприсоединения с участием аренов. Формально структура продукта (130) такова, как будто он образовался за счет фотохимического  -циклоприсоединения с последующей термической реакцией Дильса — Альдера. Однако в настоящее время точно установлено, что в данном примере синхронное
-циклоприсоединения с последующей термической реакцией Дильса — Альдера. Однако в настоящее время точно установлено, что в данном примере синхронное  -циклоприсоединение не имеет места.
-циклоприсоединение не имеет места.

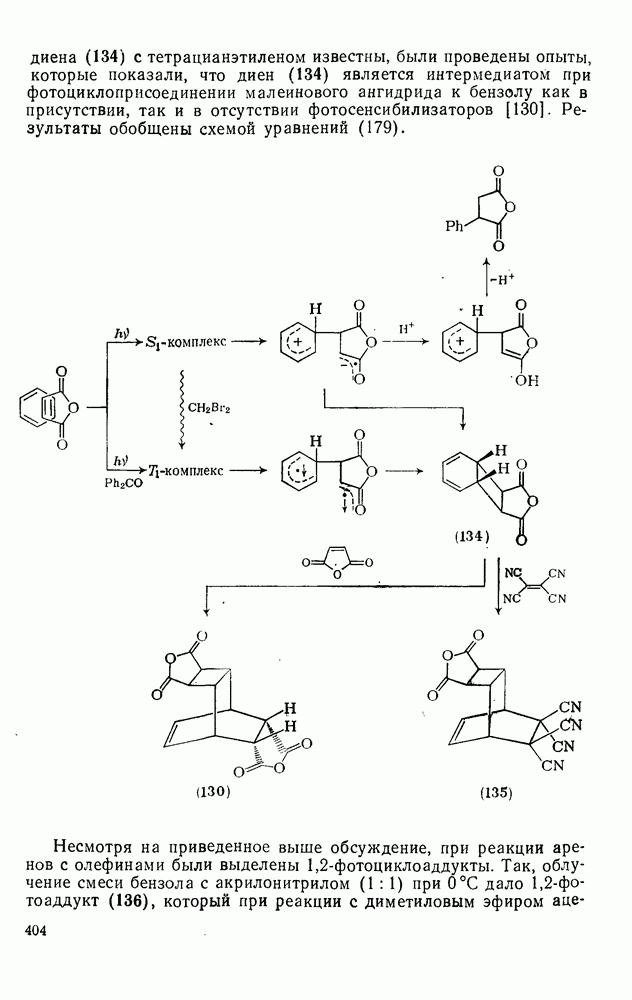
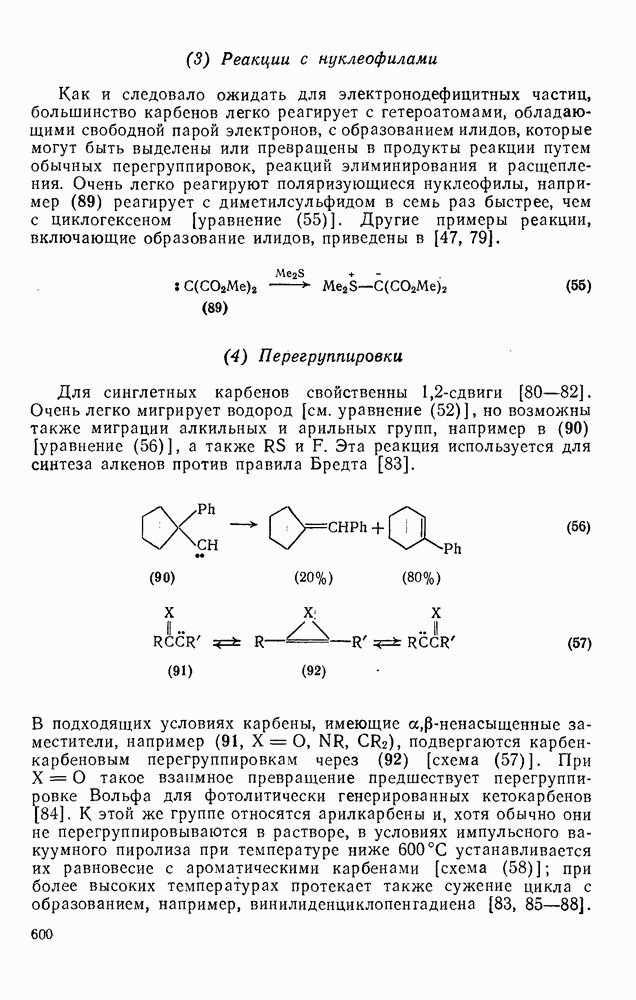
В УФ-епектрах смесей малеинового ангидрида и бензола или алкилбензолов наблюдаются полосы переноса заряда. Считают, что в этом случае фотовозбуждение перехода с переносом заряда приводит к образованию промежуточного цвиттериона (131), поскольку после проведения реакции в присутствии доноров протона можно выделить фенилянтарный ангидрид. Хотя тетрацианзтилен является обычно лучшим диенофилом в реакции Дильса — Альдера, чем малеиновый ангидрид, в бензольном растворе он существует полностью в форме комплекса с переносом заряда, что, несомненно, снижает его диенофильные свойства. Первоначально сообщалось, что облучение смеси бензола с малеиновым ангидридом и тетрацианэтиленом как в отсутствие, так и в присутствии фотосенсибилизаторов приводит только к соединению (130). С другой стороны, хотя при реакции бензола с н-бутилмалеинимидом в качестве основного продукта получают нормальный аддукт  (132), реакция в присутствии тетрацианэтилена приводит к образованию некоторых количеств аддукта
(132), реакция в присутствии тетрацианэтилена приводит к образованию некоторых количеств аддукта  (133). Интересно отметить, что
(133). Интересно отметить, что  -комплекс бензола с гексафторсурьмяной кислотой образует с малеиновым ангидридом
-комплекс бензола с гексафторсурьмяной кислотой образует с малеиновым ангидридом  -циклоаддукт [22а]. Однако маловероятно, чтобы малеиновый ангидрид служил нуклеофильным компонентом в этой реакции Дильса — Альдера. Более вероятно, что, как и в катализуемых кислотами Льюиса реакциях Дильса—Альдера с участием дицианацетилена (см. разд. 2.5.9.2), гексафторсурьмяная кислота повышает электрофильность малеинового ангидрида. Это объяснение согласуется с известным фактом, что скорость реакций Дильса — Альдера с участием антрацена, проводимых в присутствии хлорида алюминия, резко возрастает [128].
-циклоаддукт [22а]. Однако маловероятно, чтобы малеиновый ангидрид служил нуклеофильным компонентом в этой реакции Дильса — Альдера. Более вероятно, что, как и в катализуемых кислотами Льюиса реакциях Дильса—Альдера с участием дицианацетилена (см. разд. 2.5.9.2), гексафторсурьмяная кислота повышает электрофильность малеинового ангидрида. Это объяснение согласуется с известным фактом, что скорость реакций Дильса — Альдера с участием антрацена, проводимых в присутствии хлорида алюминия, резко возрастает [128].

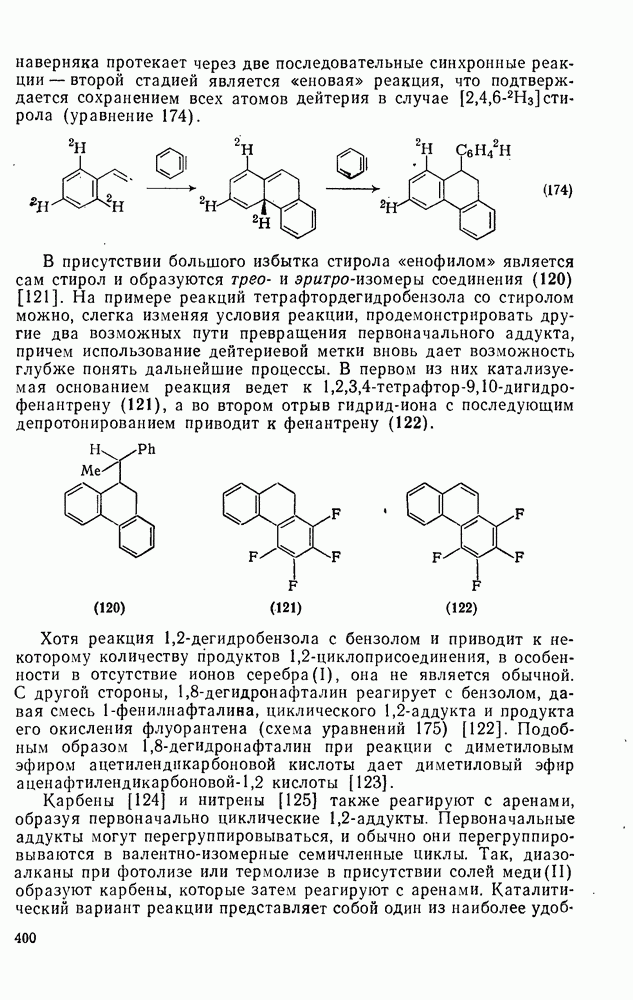
В настоящее время очевидная аномалия объяснена. Был приготовлен независимым путем предполагаемый бициклический интермедиат (134) и было установлено, что он нереакционноспособен по отношению к тетрацианэтилену, предположительно вследствие неблагоприятных пространственных взаимодействий и образования комплекса с переносом заряда.
Поскольку свойства аддукта (135), образующегося при термической реакции Дильса—Альдера диена (134) с тетрацианэтиленом известны, были проведены опыты, которые показали, что диен (134) является интермедиатом при фотоциклоприсоединении малеинового ангидрида к бензолу как в присутствии, так и в отсутствии фотосенсибилизаторов [130]. Результаты обобщены схемой уравнений (179).

Несмотря на приведенное выше обсуждение, при реакции аренов с олефинами были выделены  -фотоциклоаддукты. Так, облучение смеси бензола с акрилонитрилом
-фотоциклоаддукты. Так, облучение смеси бензола с акрилонитрилом  : 1) при
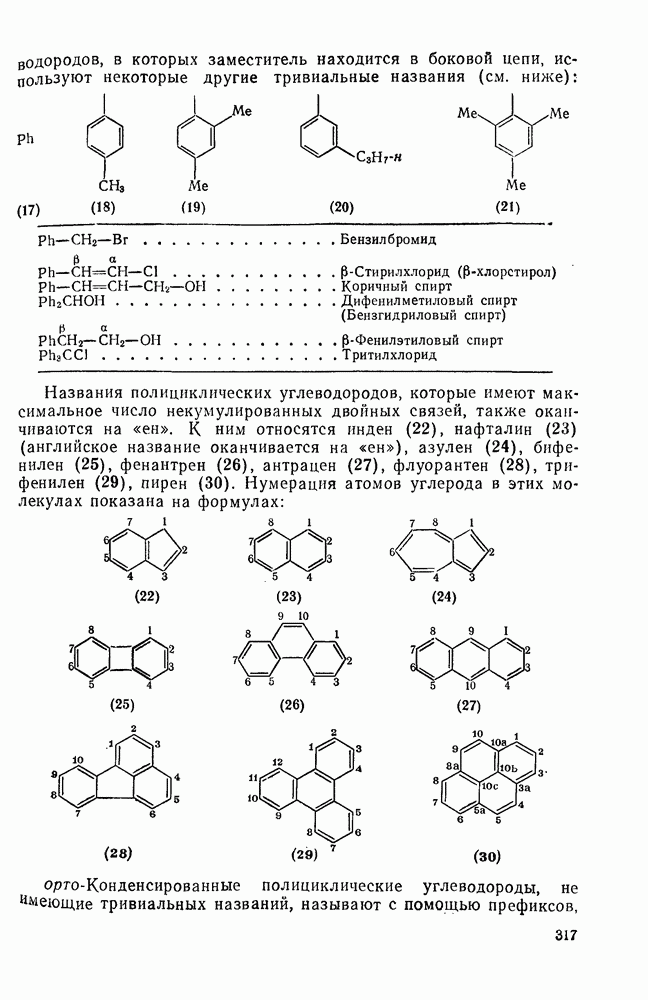
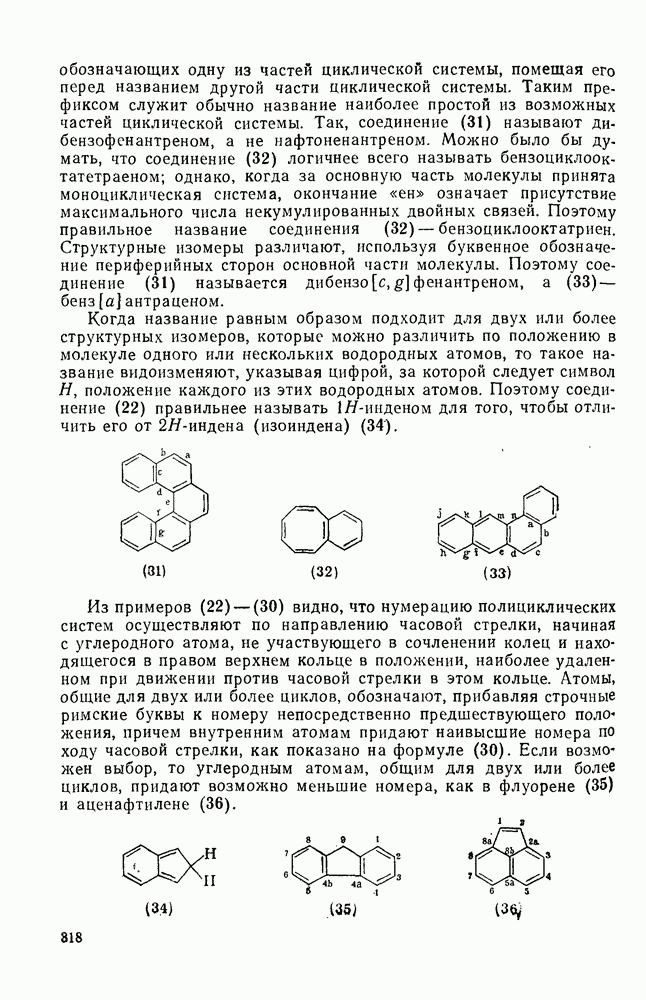
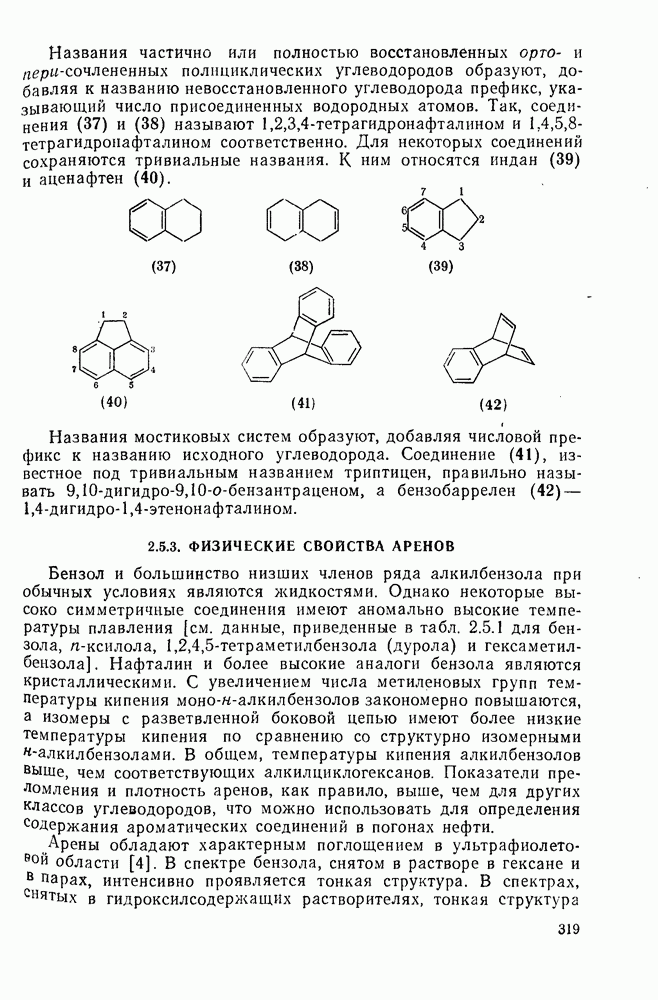
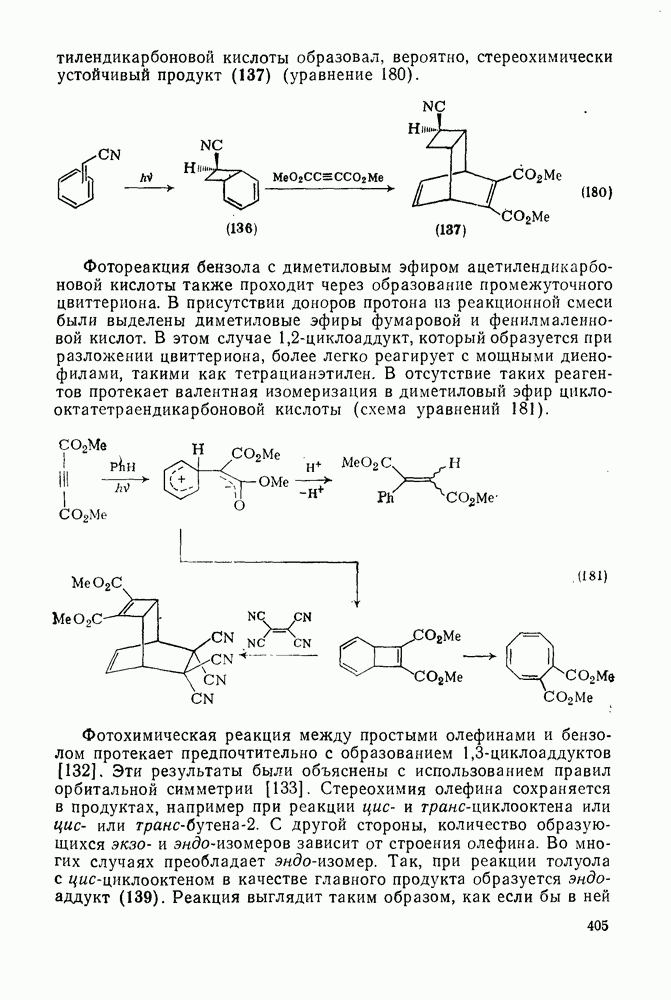
: 1) при  дало
дало  -фотоаддукт (136), который при реакции с диметиловым эфиром ацетилендикарбоновой кислоты образовал, вероятно, стереохимически устойчивый продукт (137) (уравнение 180).
-фотоаддукт (136), который при реакции с диметиловым эфиром ацетилендикарбоновой кислоты образовал, вероятно, стереохимически устойчивый продукт (137) (уравнение 180).

Фотореакция бензола с диметиловым эфиром ацетилендикарбоновой кислоты также проходит через образование промежуточного цвиттериона. В присутствии доноров протона из реакционной смеси были выделены диметиловые эфиры фумаровой и фенилмалеиновой кислот. В этом случае  -циклоаддукт, который образуется при разложении цвиттериона, более легко реагирует с мощными диено-филами, такими как тетрацианэтилен. В отсутствие таких реагентов протекает валентная изомеризация в диметиловый эфир циклооктатетраендикарбоновой кислоты (схема уравнений 181).
-циклоаддукт, который образуется при разложении цвиттериона, более легко реагирует с мощными диено-филами, такими как тетрацианэтилен. В отсутствие таких реагентов протекает валентная изомеризация в диметиловый эфир циклооктатетраендикарбоновой кислоты (схема уравнений 181).

Фотохимическая реакция между простыми олефинами и бензолом протекает предпочтительно с образованием  -циклоаддуктов [132]. Эти результаты были объяснены с использованием правил орбитальной симметрии [133]. Стереохимия олефина сохраняется в продуктах, например при реакции
-циклоаддуктов [132]. Эти результаты были объяснены с использованием правил орбитальной симметрии [133]. Стереохимия олефина сохраняется в продуктах, например при реакции  и транс-циклооктена или
и транс-циклооктена или  или
или  . С другой стороны, количество образующихся экзо- и эндо-изомеров зависит от строения олефина. Во многих случаях преобладает эндо-изомер. Так, при реакции толуола с
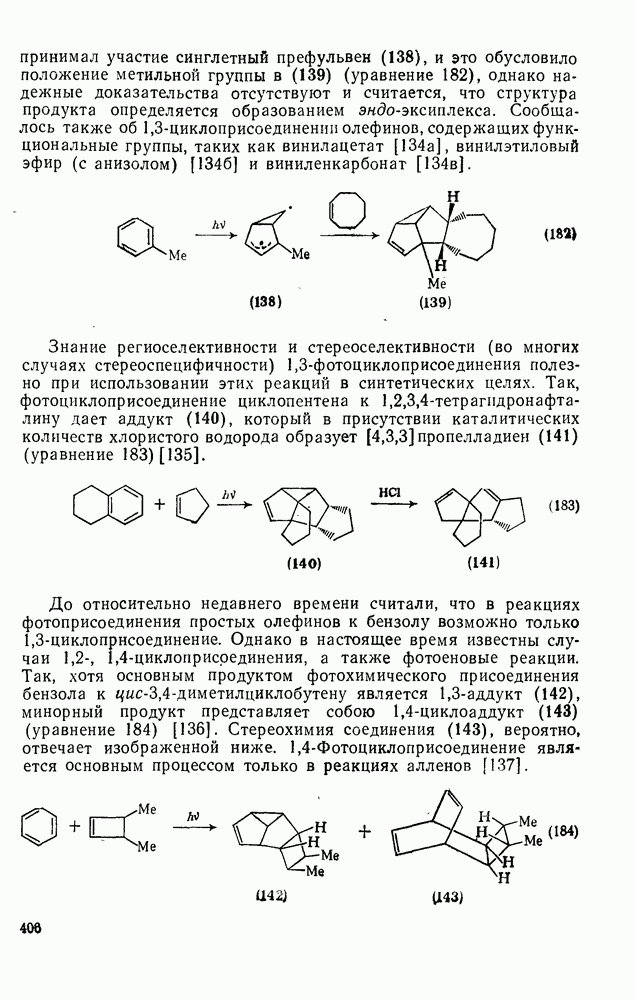
. С другой стороны, количество образующихся экзо- и эндо-изомеров зависит от строения олефина. Во многих случаях преобладает эндо-изомер. Так, при реакции толуола с  -циклооктеном в качестве главного продукта образуется эндо-аддукт (139). Реакция выглядит таким образом, как если бы в ней принимал участие синглетный префульвен (138), и это обусловило положение метальной группы в (139) (уравнение 182), однако надежные доказательства отсутствуют и считается, что структура продукта определяется образованием эндо-эксиплекса.
-циклооктеном в качестве главного продукта образуется эндо-аддукт (139). Реакция выглядит таким образом, как если бы в ней принимал участие синглетный префульвен (138), и это обусловило положение метальной группы в (139) (уравнение 182), однако надежные доказательства отсутствуют и считается, что структура продукта определяется образованием эндо-эксиплекса.
Сообщалось также об  -циклоприсоединении олефинов, содержащих функциональные группы, таких как винилацетат [134а], винилэтиловый эфир (с анизолом) [1346] и виниленкарбонат [134в].
-циклоприсоединении олефинов, содержащих функциональные группы, таких как винилацетат [134а], винилэтиловый эфир (с анизолом) [1346] и виниленкарбонат [134в].

Знание региоселективности и стереоселективности (во многих случаях стереоспецифичности)  -фотоциклоприсоединения полезно при использовании этих реакций в синтетических целях. Так, фотоциклоприсоединение циклопентена к
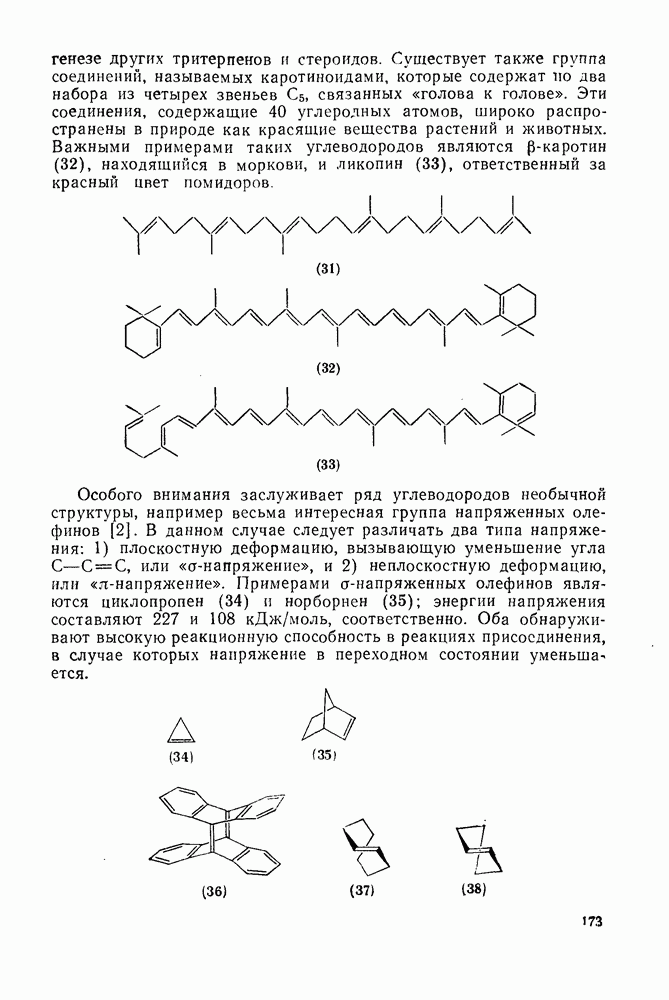
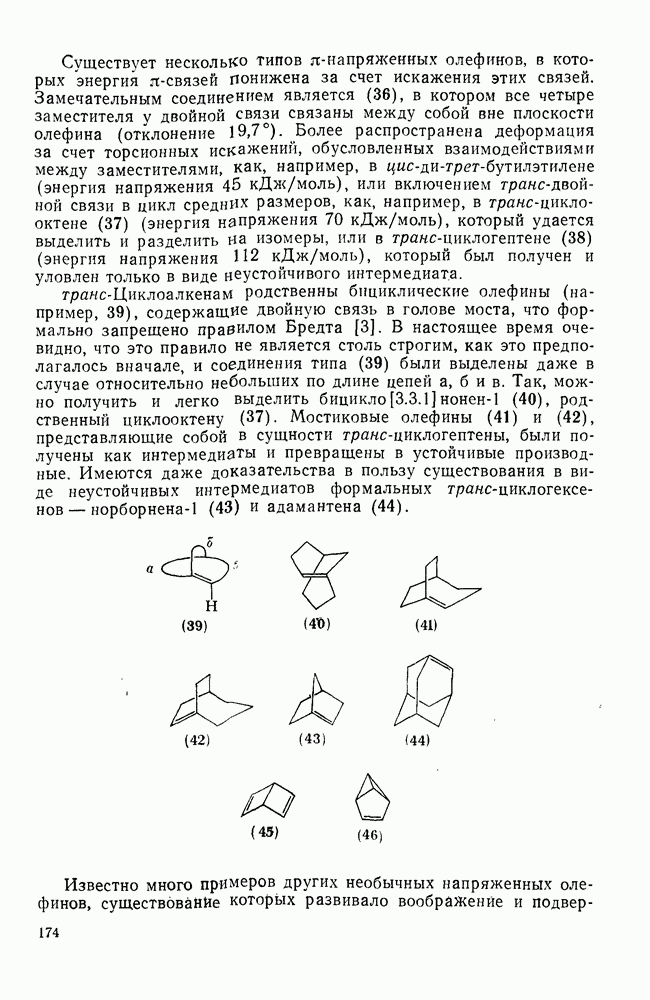
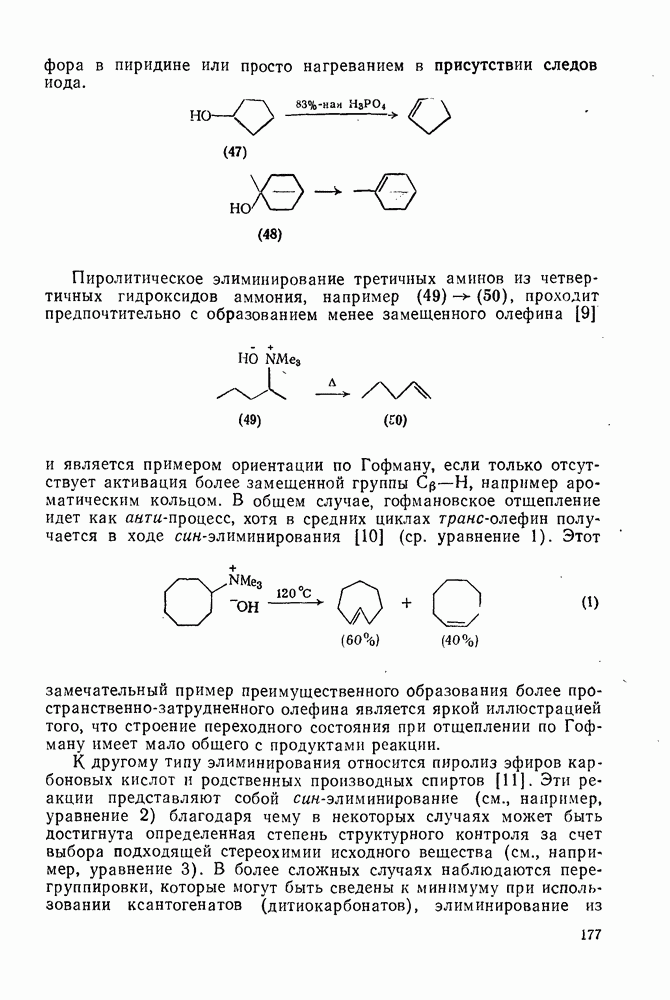
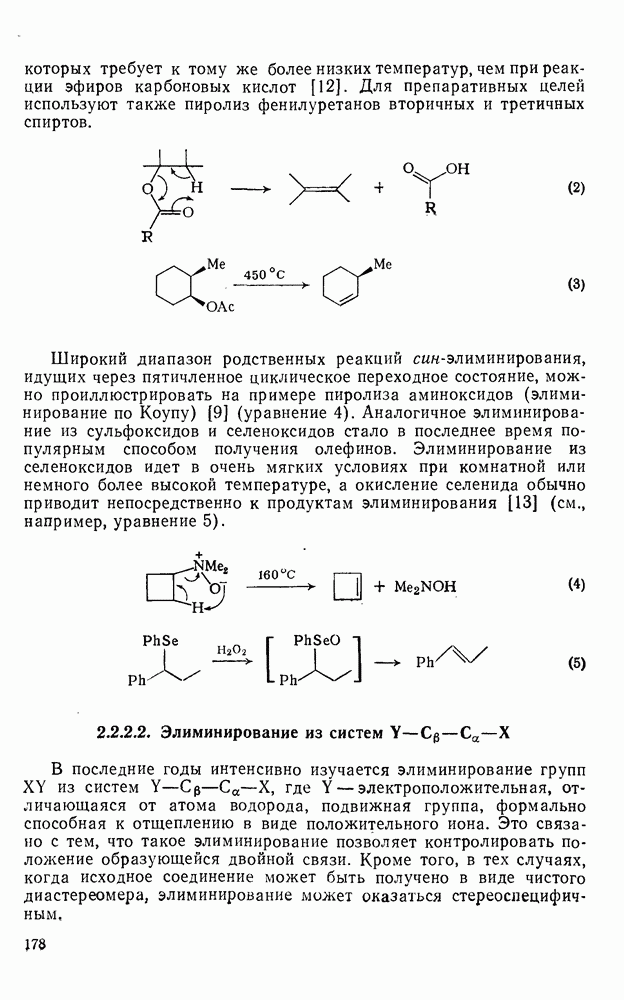
-фотоциклоприсоединения полезно при использовании этих реакций в синтетических целях. Так, фотоциклоприсоединение циклопентена к  -тетрагидронафталину дает аддукт (140), который в присутствии каталитических количеств хлористого водорода образует [4,3,3] пропелладиен (141) (уравнение
-тетрагидронафталину дает аддукт (140), который в присутствии каталитических количеств хлористого водорода образует [4,3,3] пропелладиен (141) (уравнение  .
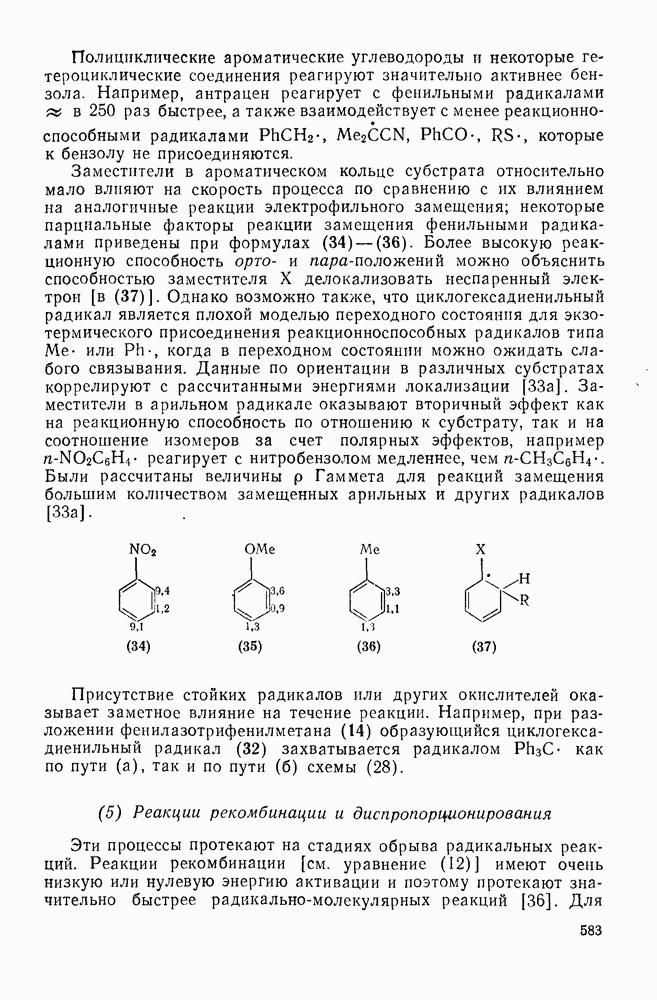
.

До относительно недавнего времени считали, что в реакциях фотоприсоединения простых олефинов к бензолу возможно только  -циклопрнсоединение. Однако в настоящее время известны случаи
-циклопрнсоединение. Однако в настоящее время известны случаи  ,
,  -циклоприсоединения, а также фотоеновые реакции. Так, хотя основным продуктом фотохимического присоединения бензола к
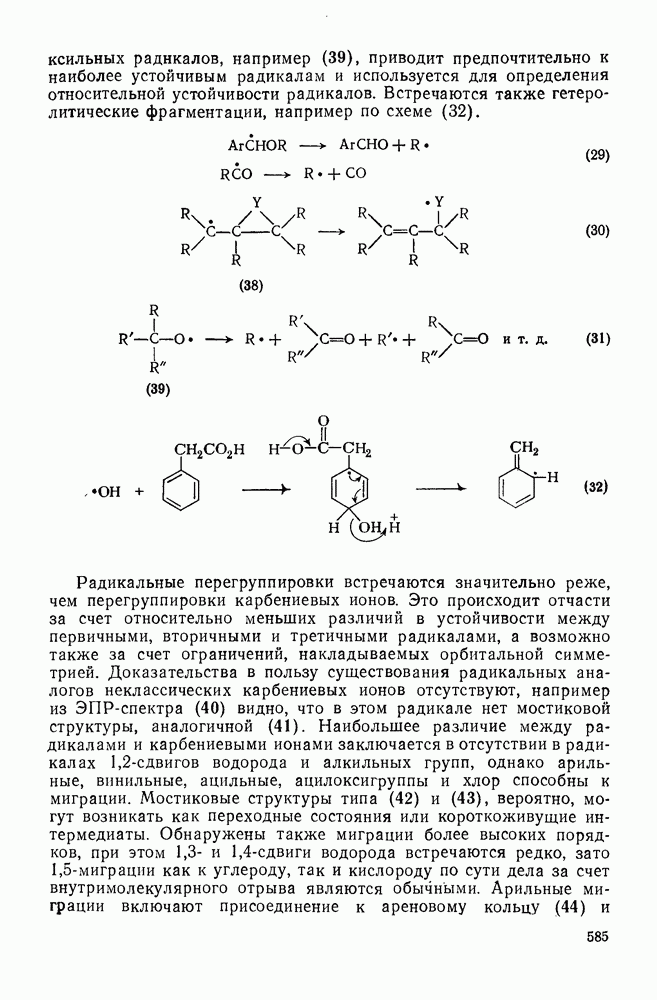
-циклоприсоединения, а также фотоеновые реакции. Так, хотя основным продуктом фотохимического присоединения бензола к  является
является  -аддукт (142), минорный продукт представляет собою
-аддукт (142), минорный продукт представляет собою  -циклоаддукт (143) (уравнение 184) [136]. Стереохимия соединения (143), вероятно, отвечает изображенной ниже.
-циклоаддукт (143) (уравнение 184) [136]. Стереохимия соединения (143), вероятно, отвечает изображенной ниже.  -Фотоциклоприсоединение является основным процессом только в реакциях алленов [137].
-Фотоциклоприсоединение является основным процессом только в реакциях алленов [137].

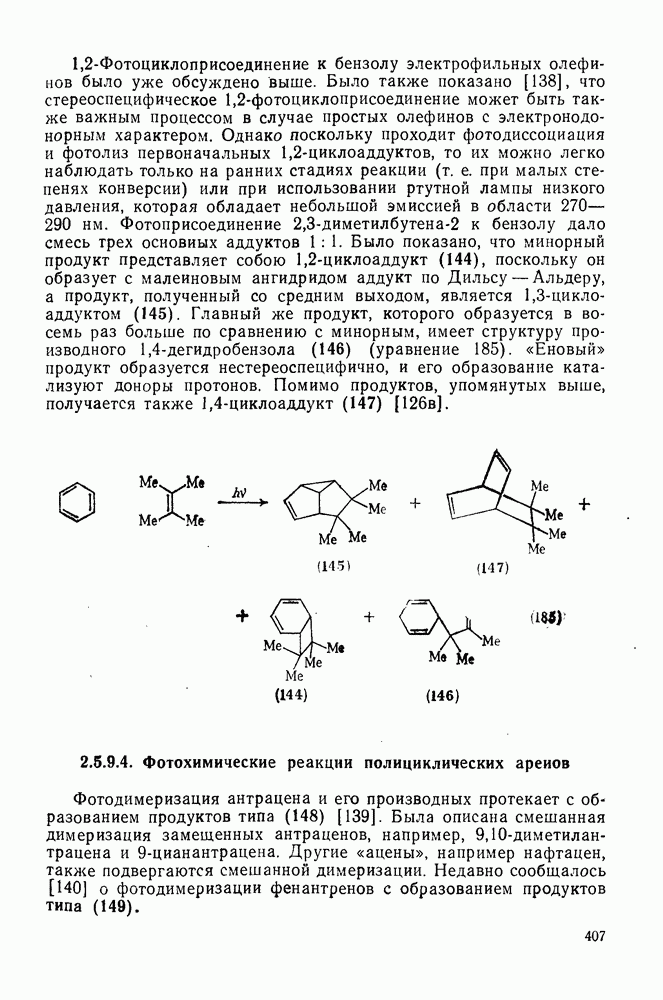
1,2-Фотоциклоприсоединение к бензолу электрофильных олефинов было уже обсуждено выше. Было также показано [138], что стереоспецифическое 1,2-фотоциклоприсоединение может быть также важным процессом в случае простых олефинов с электронодонорным характером. Однако поскольку проходит фотодиссоциация и фотолиз первоначальных 1,2-циклоаддуктов, то их можно легко наблюдать только на ранних стадиях реакции (т. е. при малых степенях конверсии) или при использовании ртутной лампы низкого давления, которая обладает небольшой эмиссией в области 270— 290 нм. Фотоприсоединение  к бензолу дало смесь трех основных аддуктов
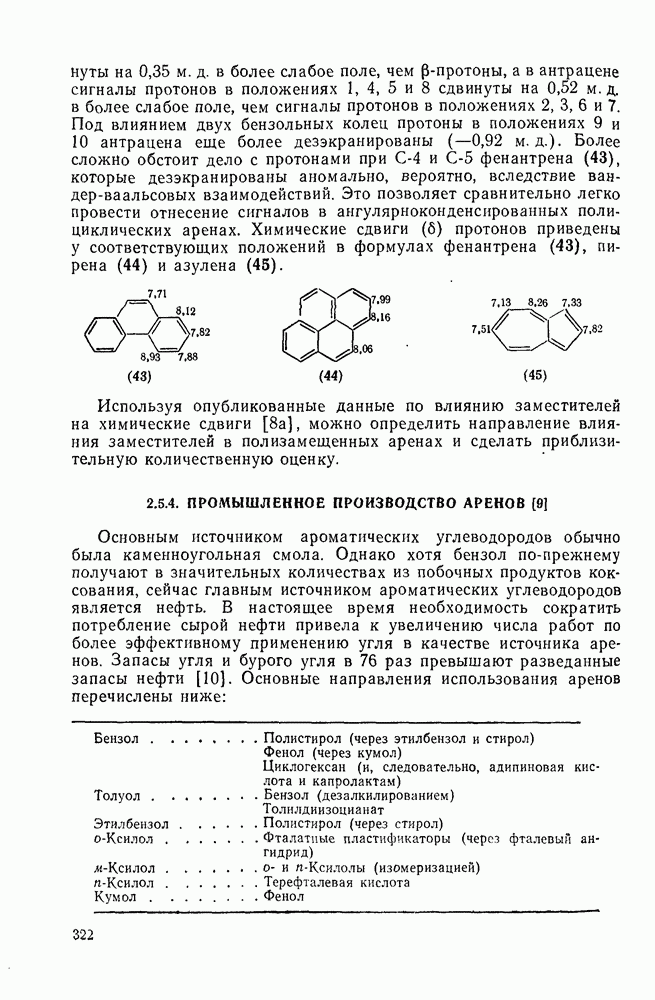
к бензолу дало смесь трех основных аддуктов  . Было показано, что минорный продукт представляет собою
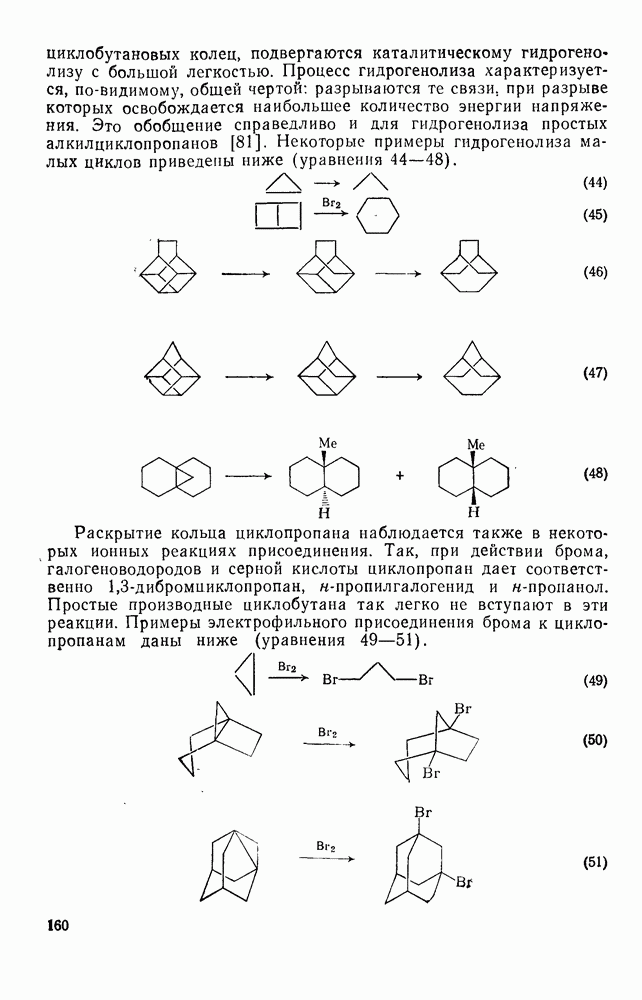
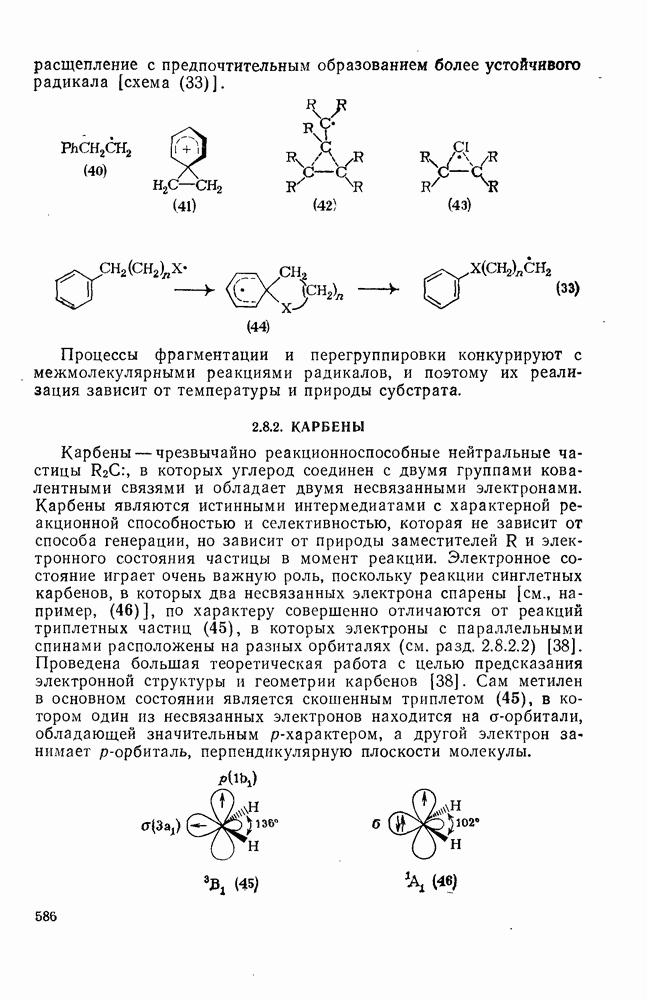
. Было показано, что минорный продукт представляет собою  -циклоаддукт (144), поскольку он образует с малеиновым ангидридом аддукт по Дильсу — Альдеру, а продукт, полученный со средним выходом, является
-циклоаддукт (144), поскольку он образует с малеиновым ангидридом аддукт по Дильсу — Альдеру, а продукт, полученный со средним выходом, является  -циклоаддуктом (145). Главный же продукт, которого образуется в восемь раз больше по сравнению с минорным, имеет структуру производного
-циклоаддуктом (145). Главный же продукт, которого образуется в восемь раз больше по сравнению с минорным, имеет структуру производного  -дегидробензола (146) (уравнение 185). «Еновый» продукт образуется нестереоспецифично, и его образование ката-лизуют доноры протонов. Помимо продуктов, упомянутых выше, получается также
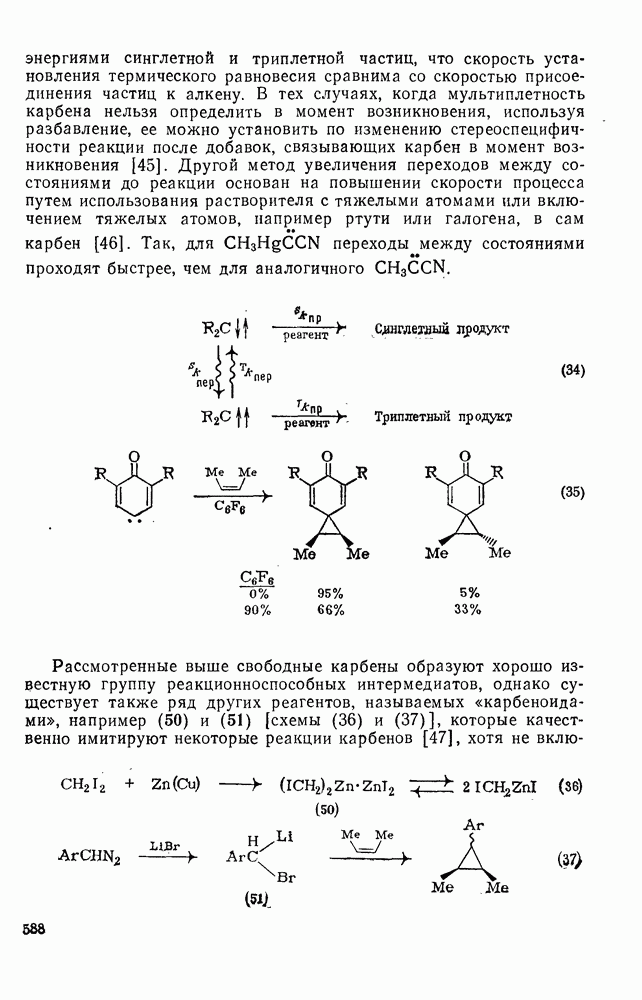
-дегидробензола (146) (уравнение 185). «Еновый» продукт образуется нестереоспецифично, и его образование ката-лизуют доноры протонов. Помимо продуктов, упомянутых выше, получается также  -циклоаддукт (147) [126в].
-циклоаддукт (147) [126в].

| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- ПРЕДИСЛОВИЕ
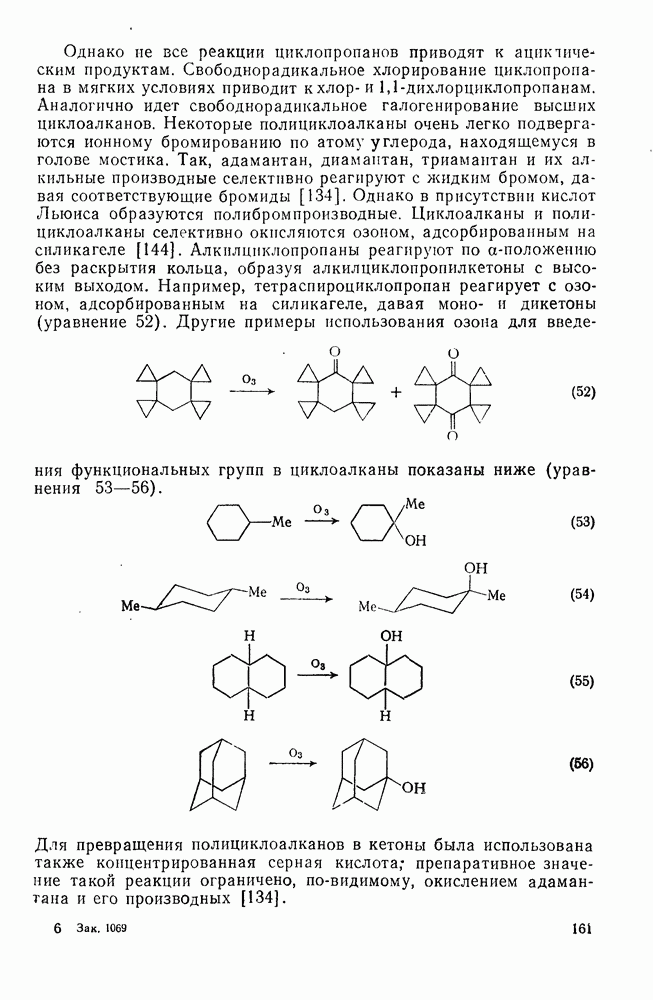
- ИЗ ПРЕДИСЛОВИЯ К ТОМУ 1 АНГЛИЙСКОГО ИЗДАНИЯ
- ЧАСТЬ I. НОМЕНКЛАТУРА И СТЕРЕОХИМИЯ
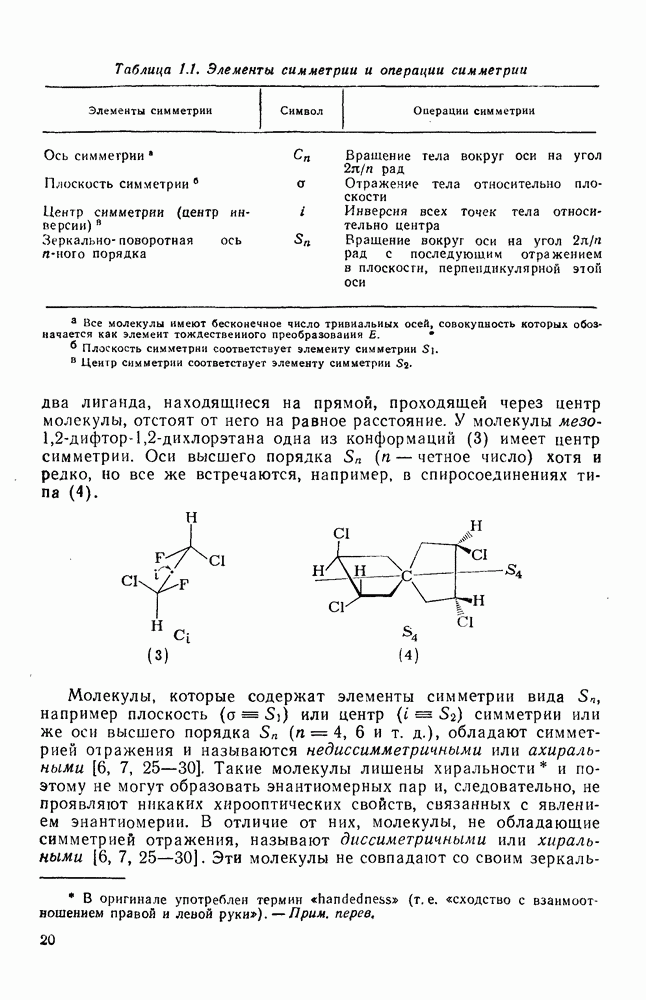
- 1.1. ВВЕДЕНИЕ И СТЕРЕОХИМИЯ
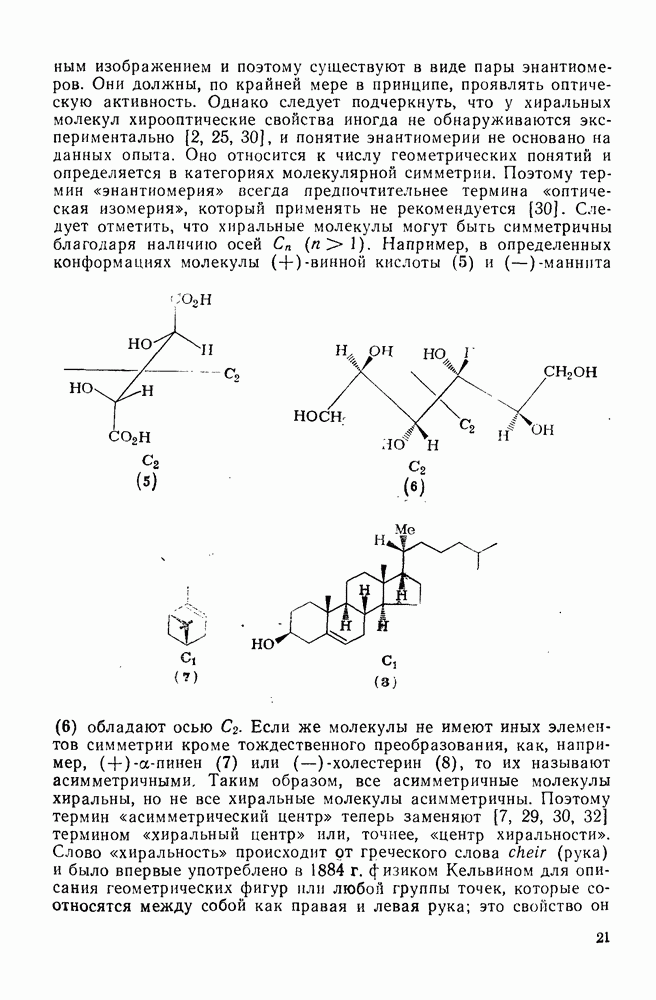
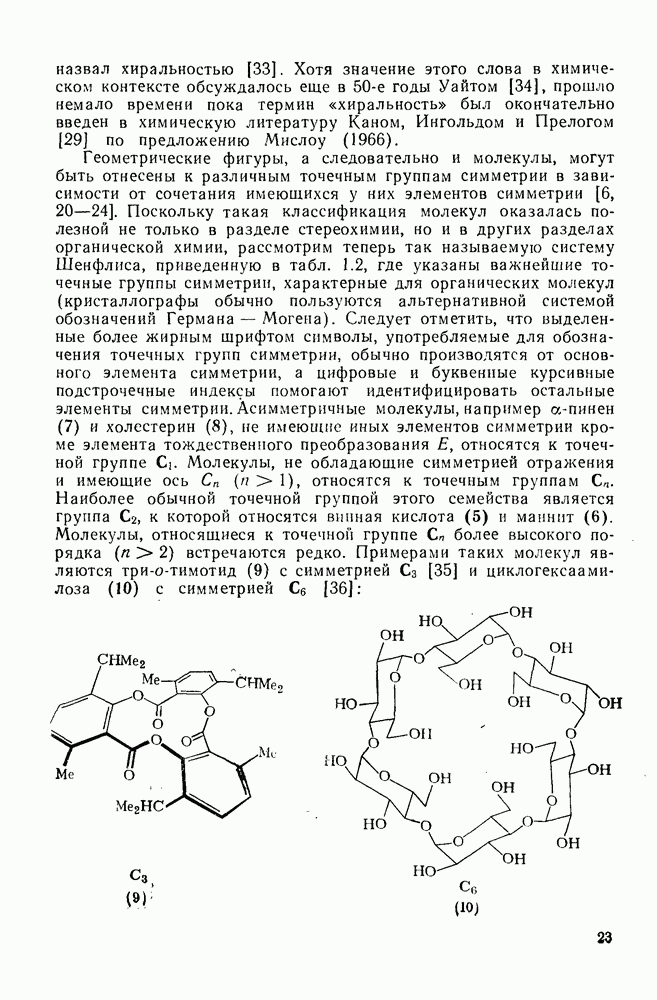
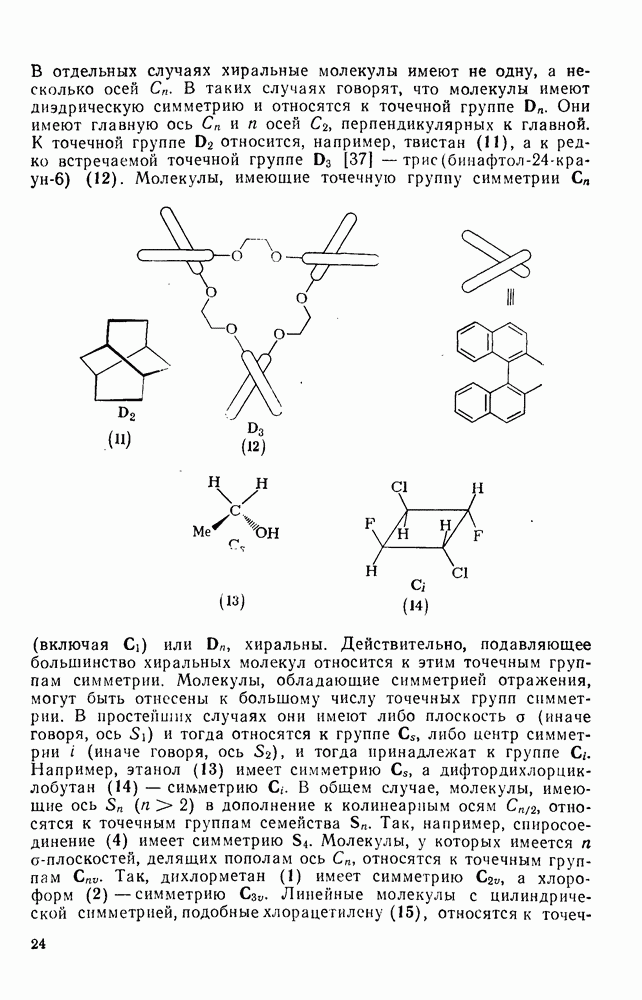
- 1.1.2. СИММЕТРИЯ И ХИРАЛЬНОСТЬ
- 1.1.3. ХИМИЧЕСКАЯ ТОПОЛОГИЯ
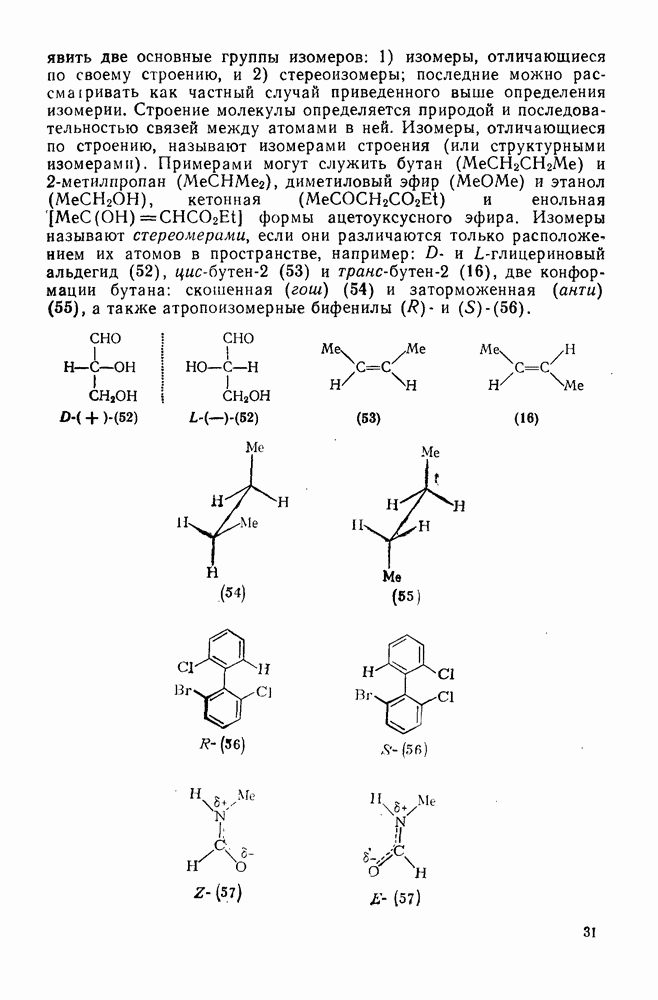
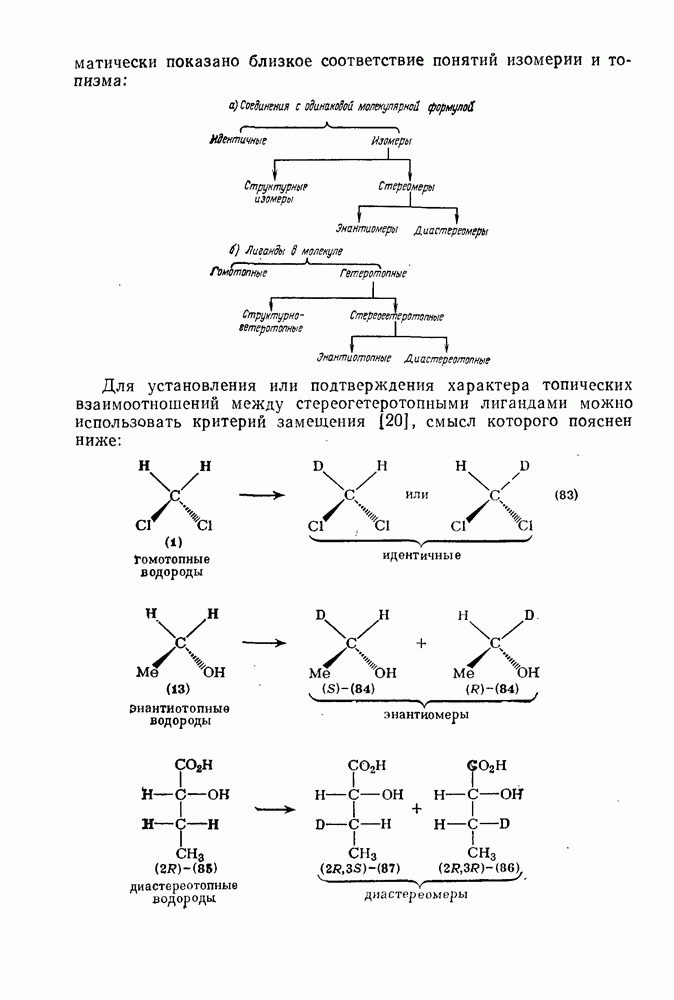
- 1.1.4. ИЗОМЕРИЯ
- 1.1.4.2. Строение
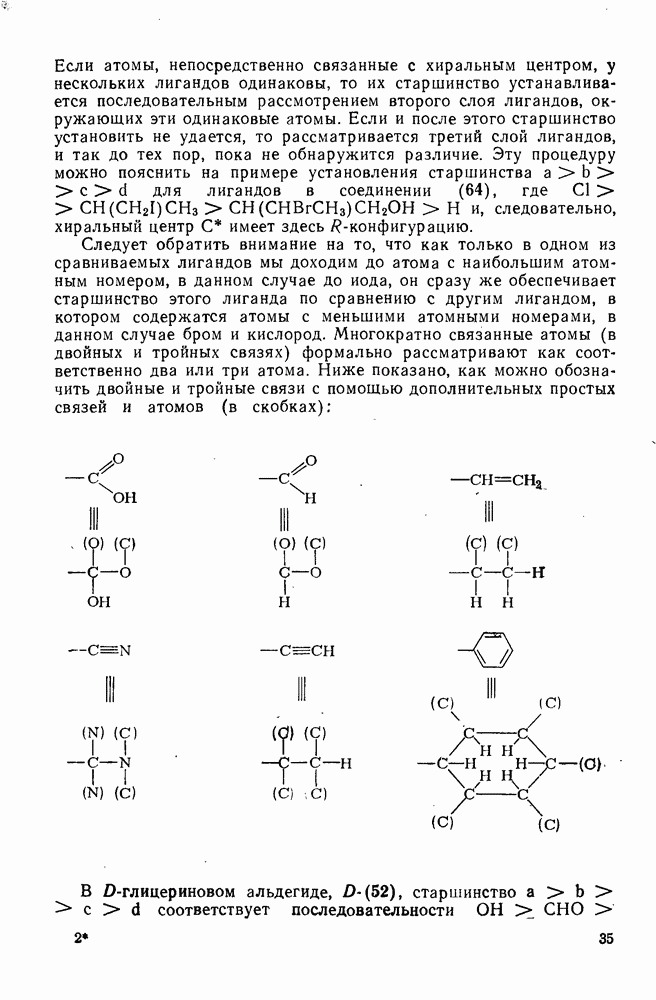
- 1.1.4.3. Абсолютная конфигурация
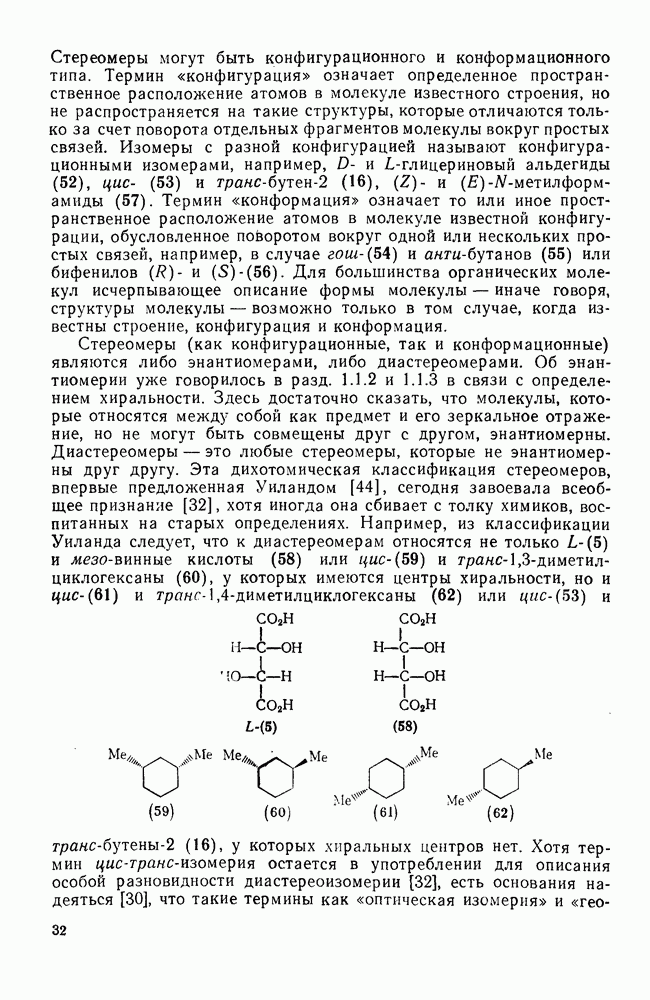
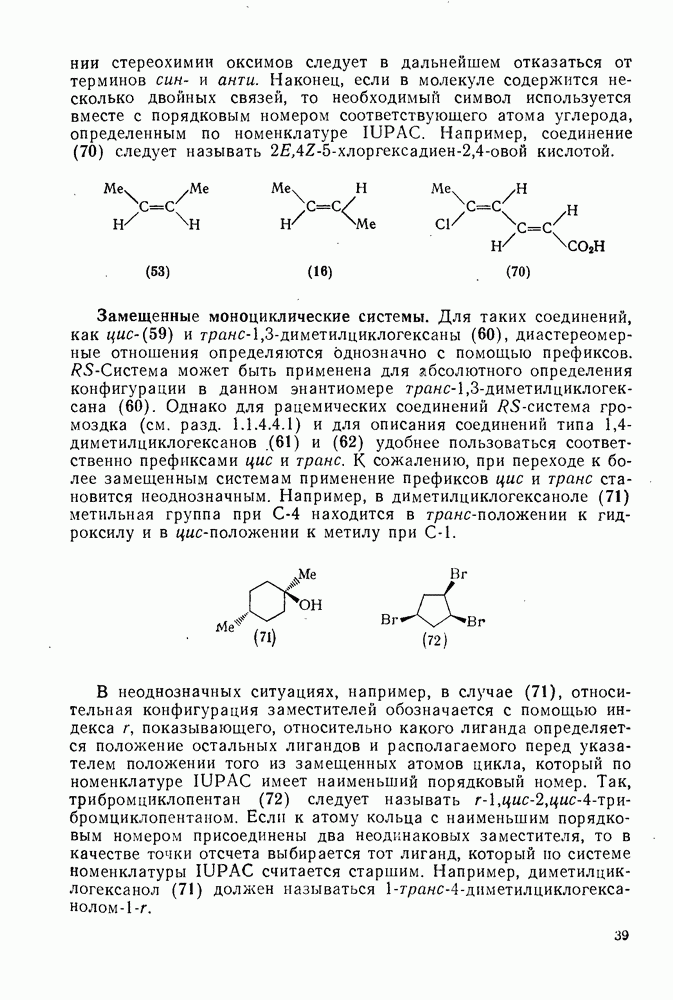
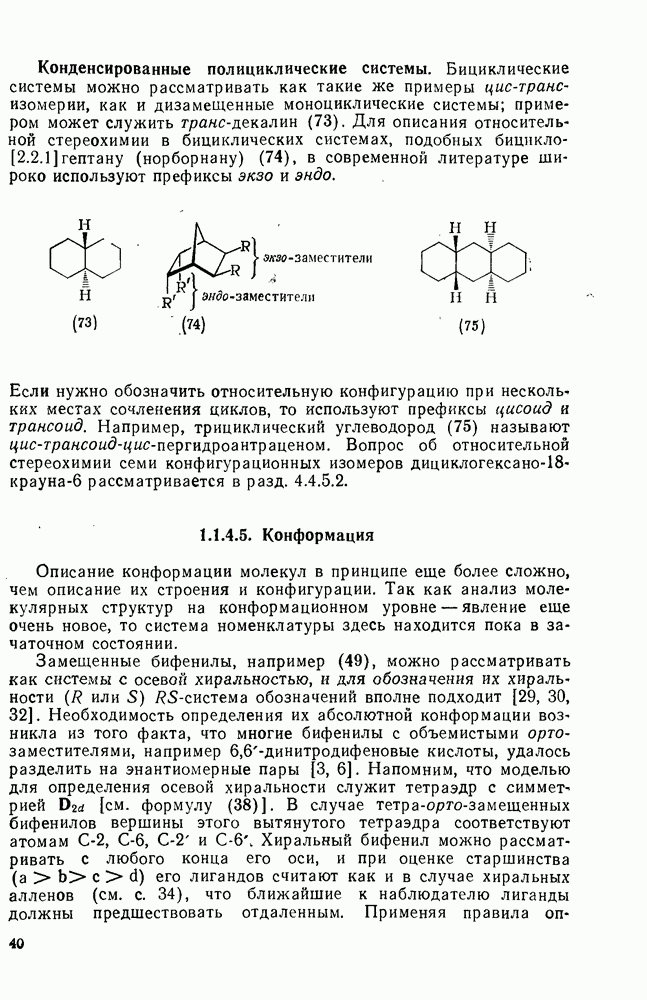
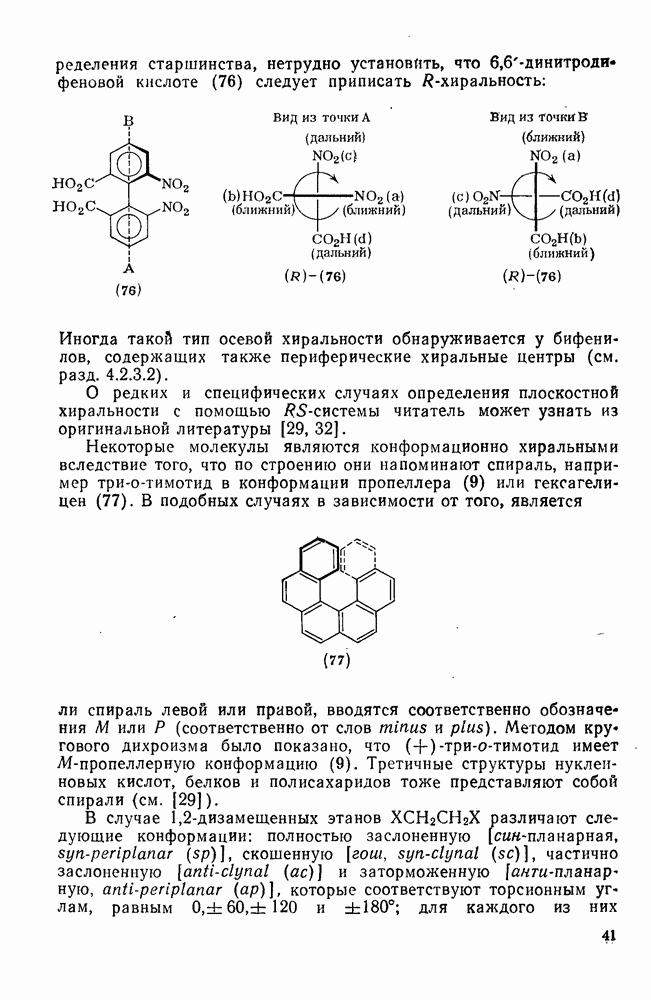
- 1.1.4.4. Относительная конфигурация
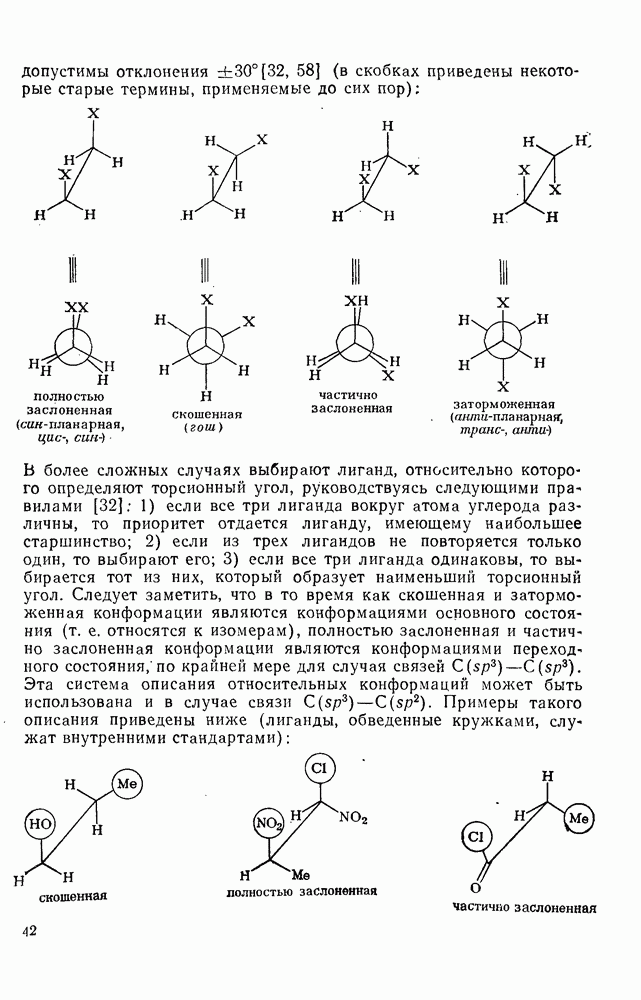
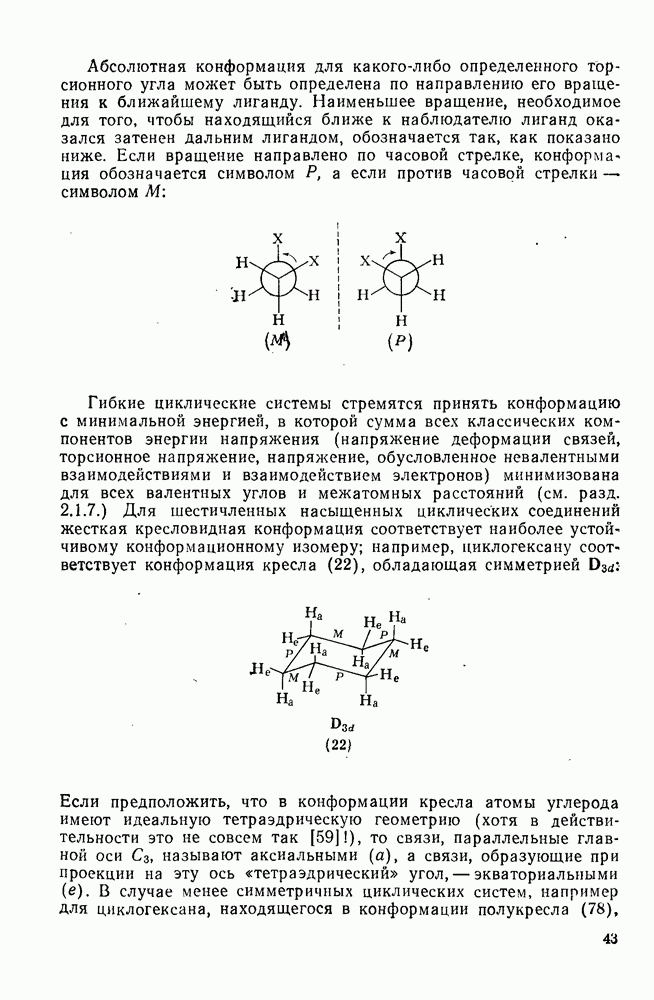
- 1.1.4.5. Конформация
- 1.1.4.6. Концепция изомерии
- 1.1.5. ТОПИЗМ
- 1.1.5.2. Прохиральность
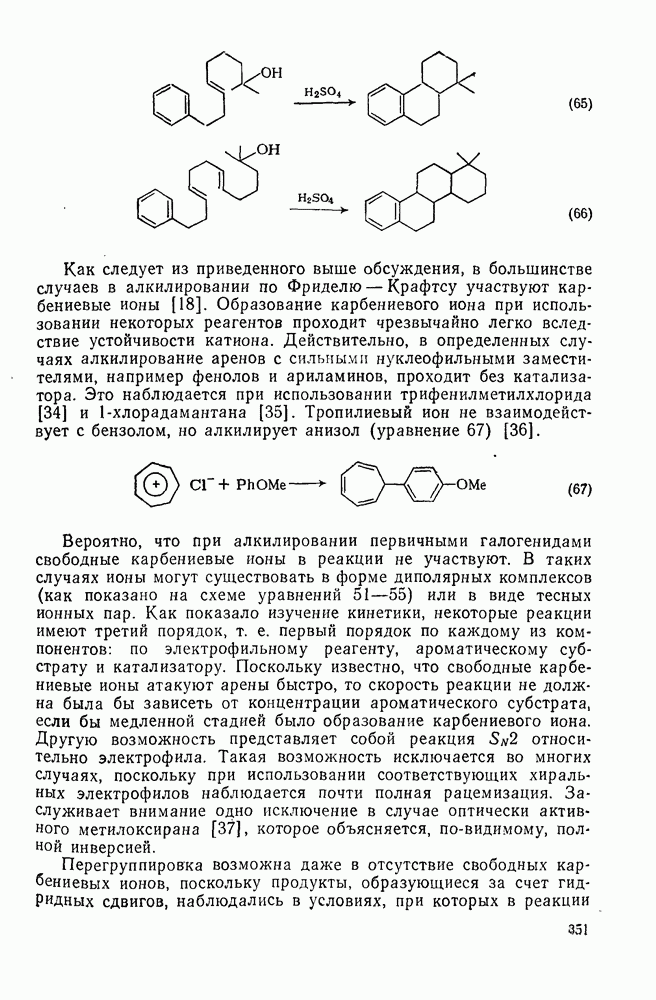
- 1.1.5.3. Псевдоасимметрия (псевдохиральность)
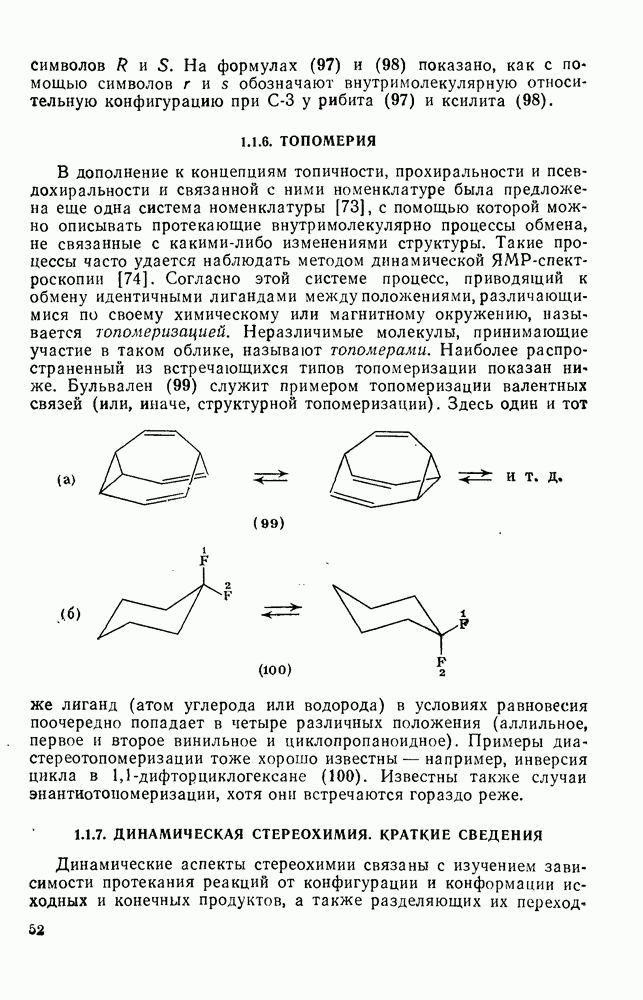
- 1.1.6. ТОПОМЕРИЯ
- 1.1.7. ДИНАМИЧЕСКАЯ СТЕРЕОХИМИЯ. КРАТКИЕ СВЕДЕНИЯ
- ЧАСТЬ 2. УГЛЕВОДОРОДЫ
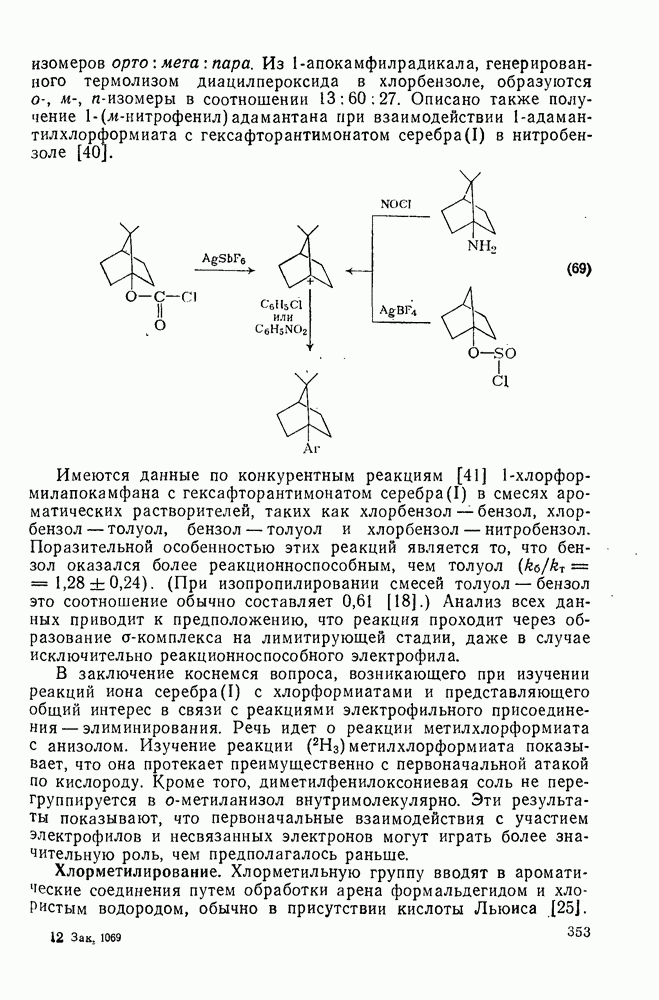
- 2.1. НАСЫЩЕННЫЕ УГЛЕВОДОРОДЫ
- 2.1.2. Строение и номенклатура
- 2.1.2.1. Номенклатура IUPAC
- 2.1.2.2. Алициклические алканы
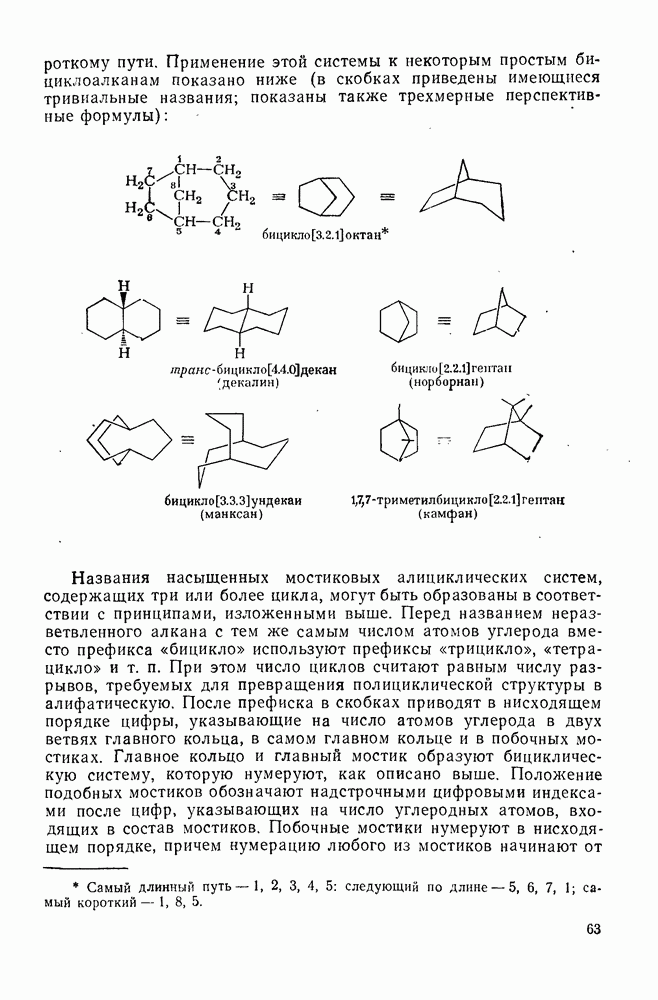
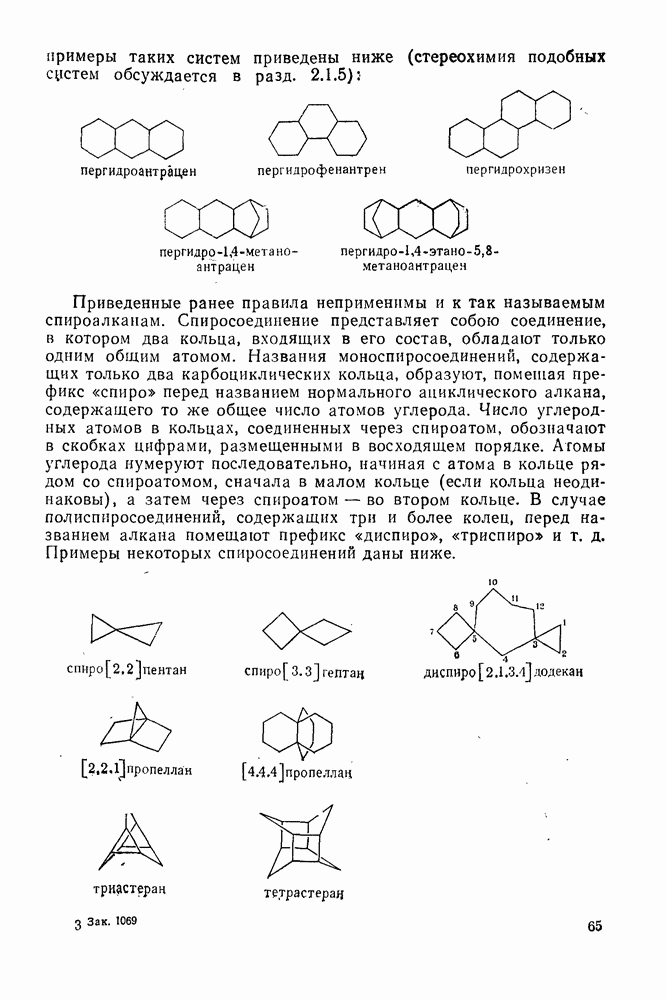
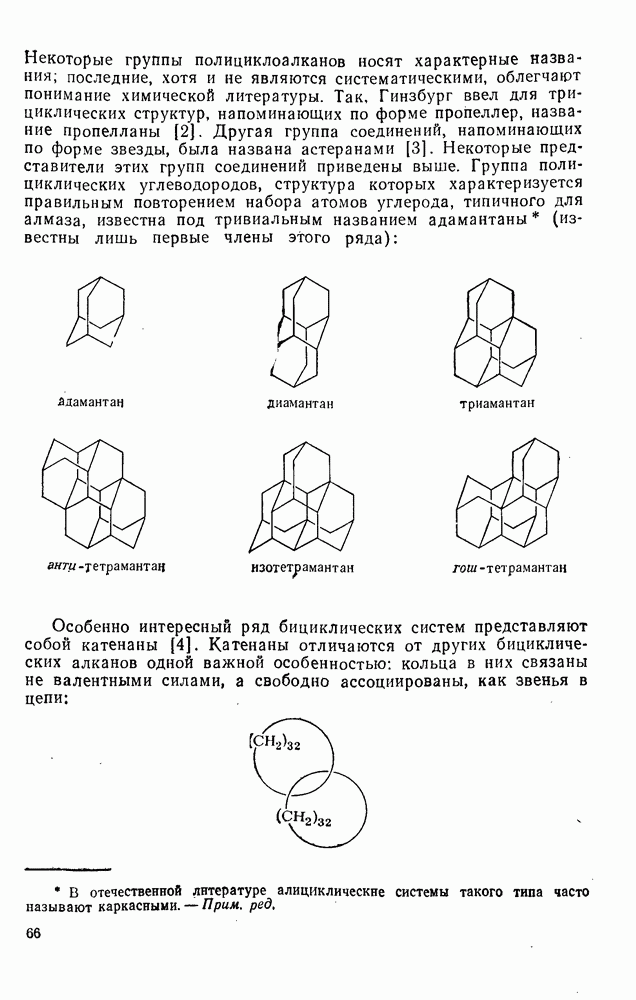
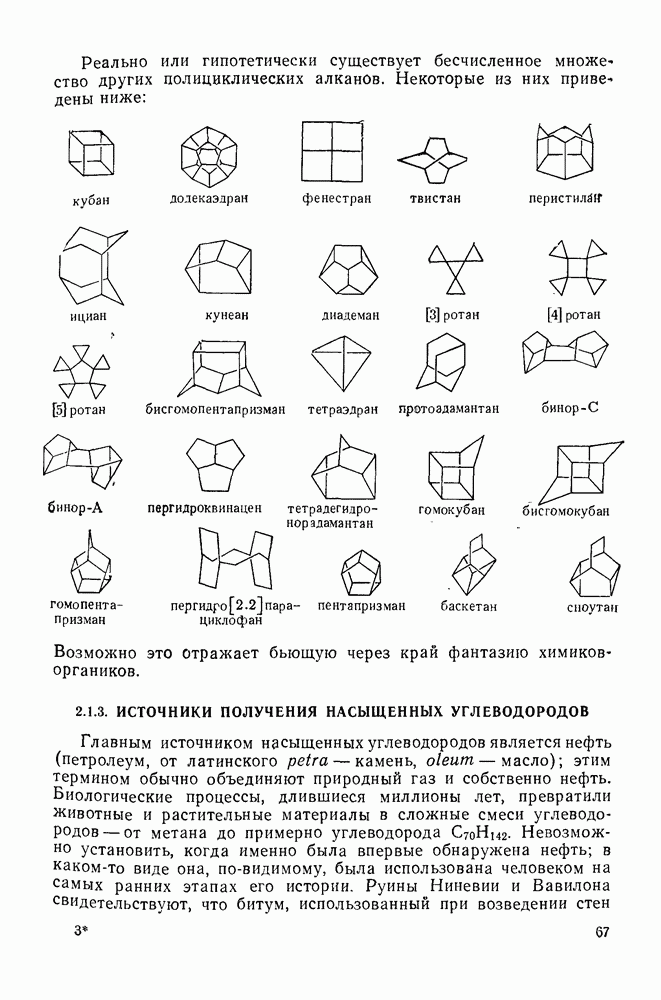
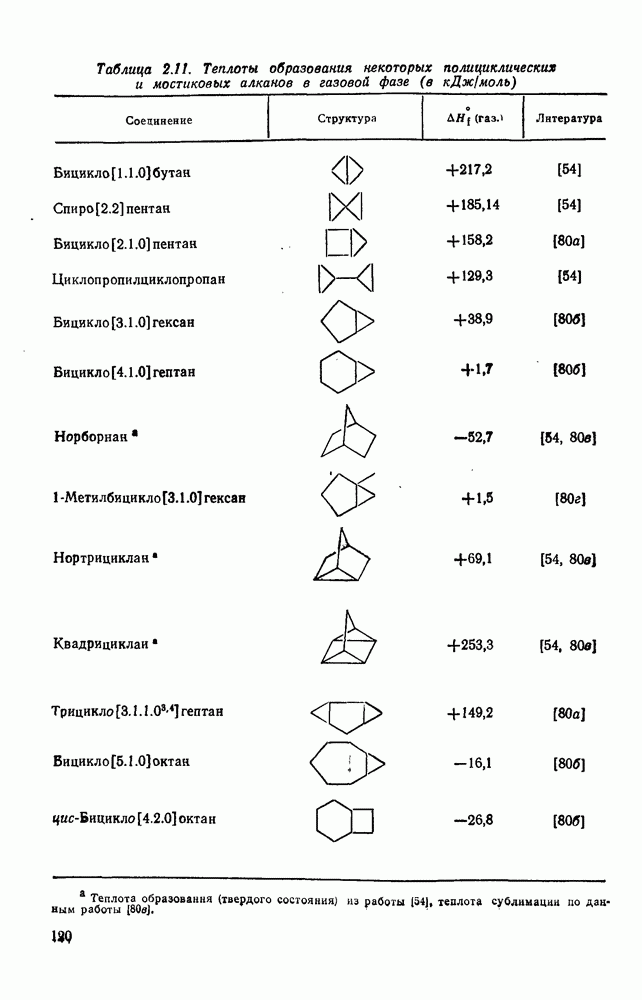
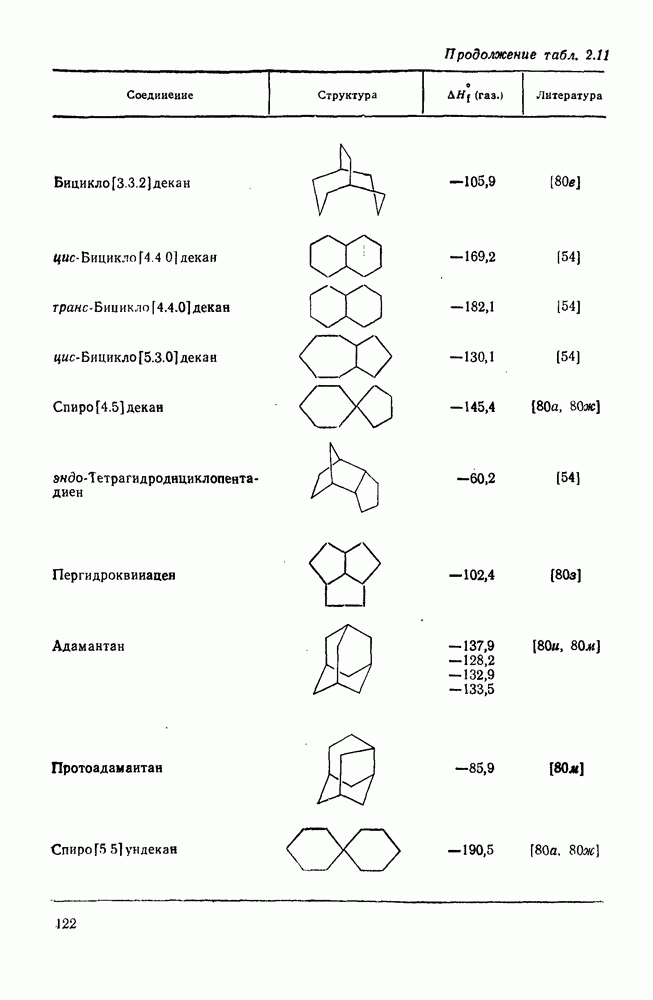
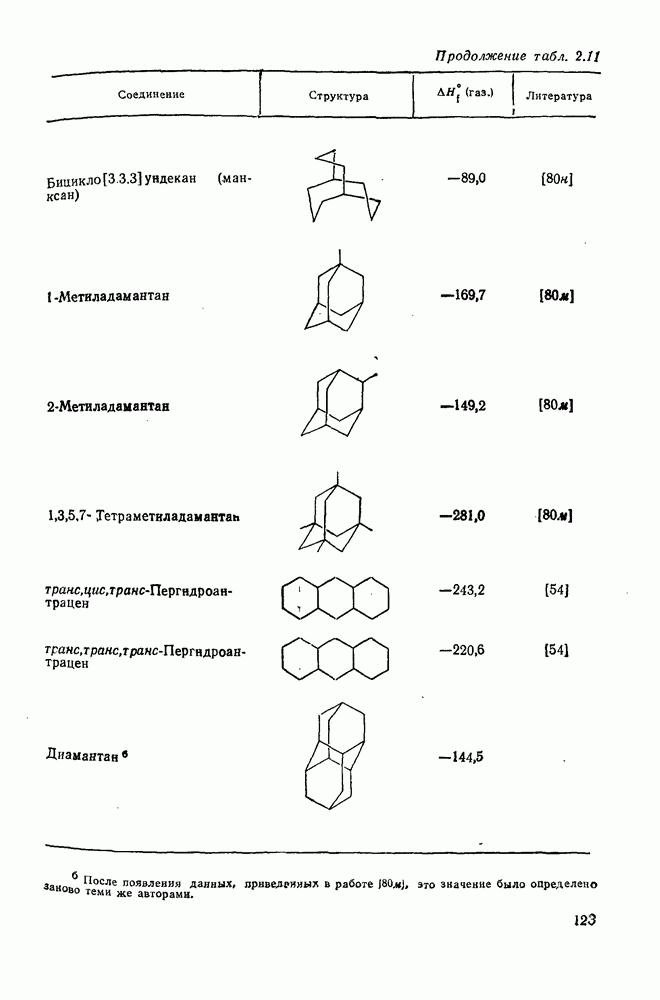
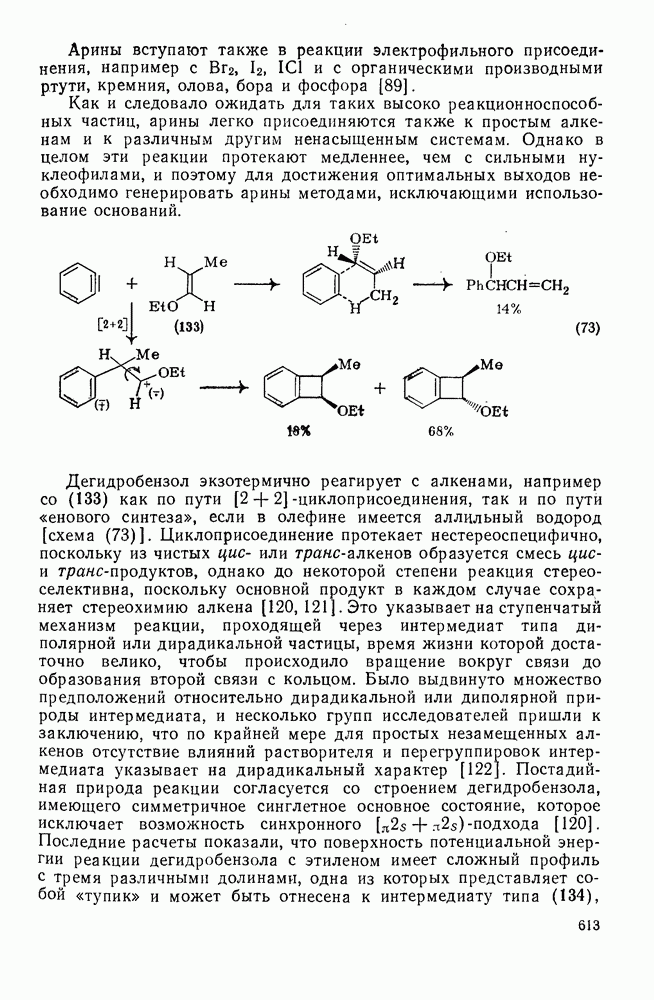
- 2.1.2.3. Полициклоалканы
- 2.1.3. ИСТОЧНИКИ ПОЛУЧЕНИЯ НАСЫЩЕННЫХ УГЛЕВОДОРОДОВ
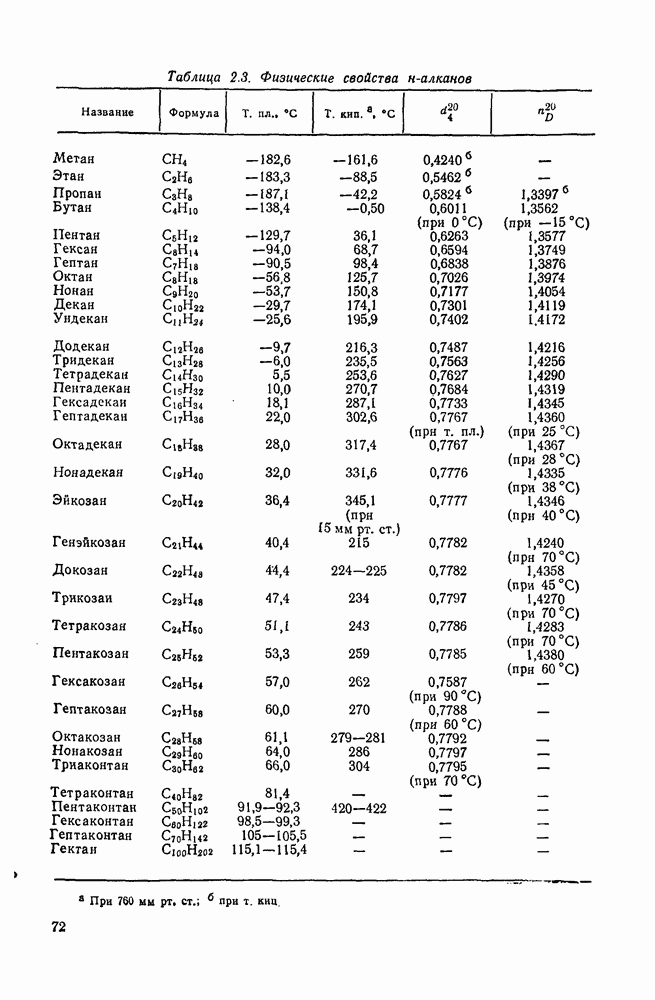
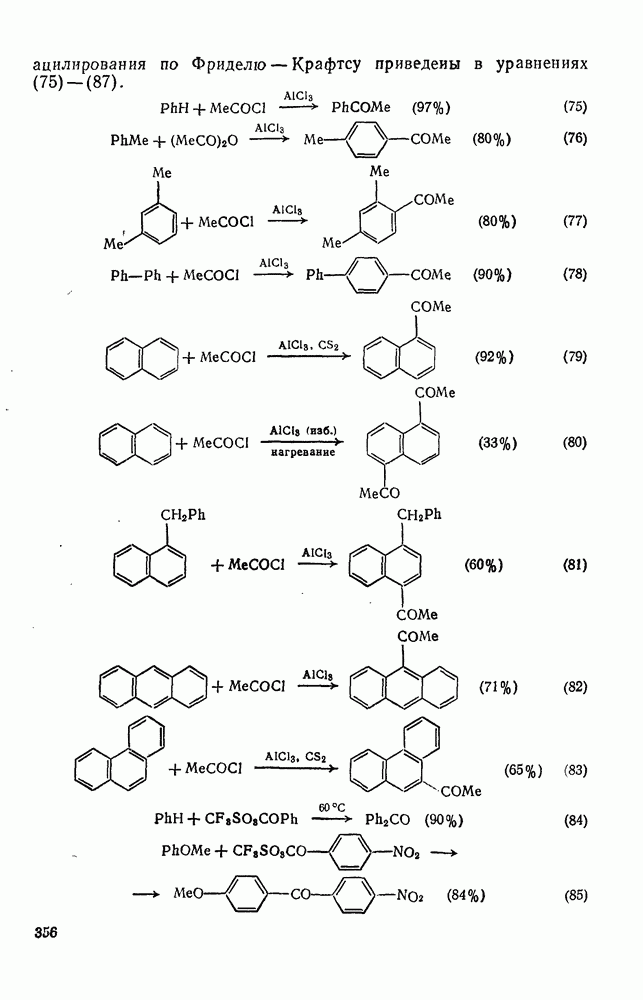
- 2.1.4. ФИЗИЧЕСКИЕ СВОЙСТВА
- 2.1.4.1. Ациклические алканы
- 2.1.4.2. Моно- и полициклоалканы
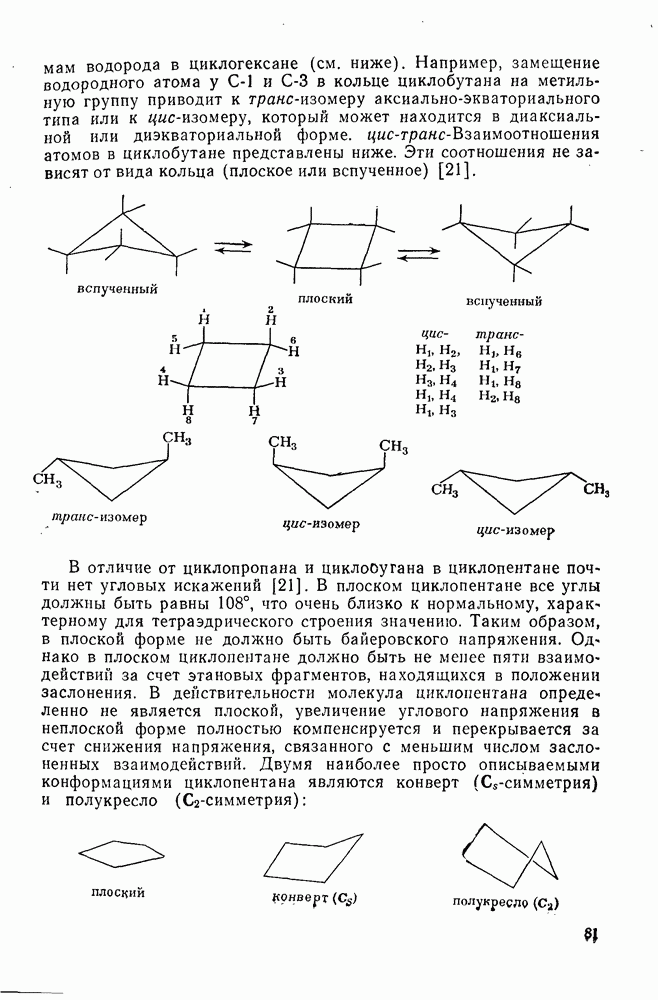
- 2.1.5. СТЕРЕОХИМИЯ И КОНФОРМАЦИОННЫЙ АНАЛИЗ
- 2.1.5.1. Углы и длины связей
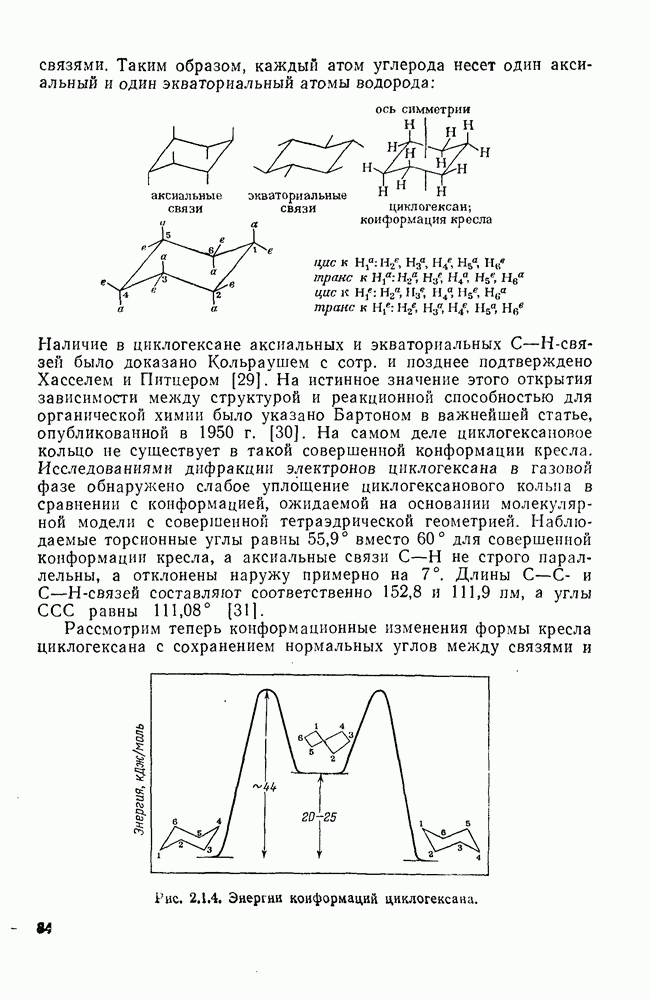
- 2.1.5.2. Алкил- и полиалкилциклогексаны
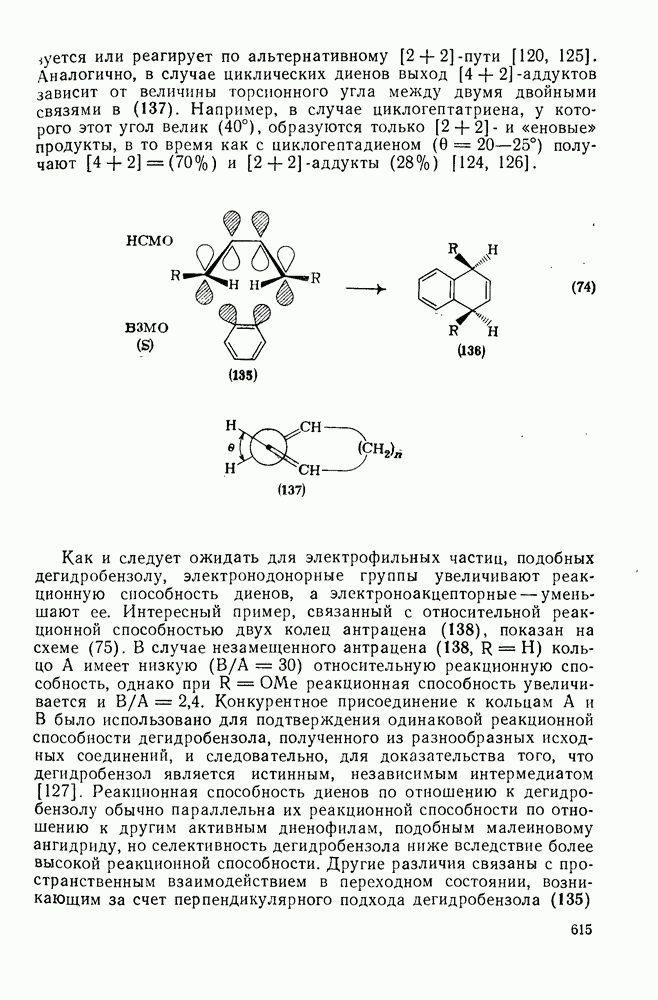
- 2.1.5.3. Конформация карбоциклических колец, больших, чем циклогексан
- 2.1.6. ТЕРМОХИМИЧЕСКИЕ СВОЙСТВА
- 2.1.6.1. Горение. Алканы и циклоалканы как топливо
- 2.1.6.2. Определение теплот сгорания и термохимические свойства
- 2.1.6.3. Эмпирические методы оценки теплот образования алканов
- 2.1.6.4. Оценка теплот образования алканов на основе энергии связей
- 2.1.6.5. Оценка теплот образования алканов на основе инкрементов групп
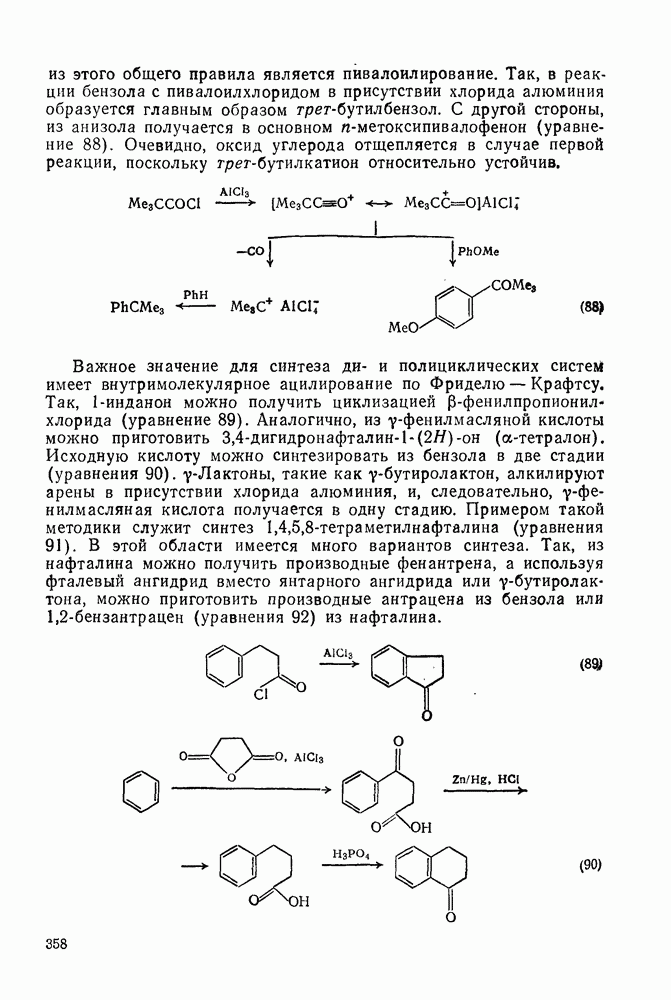
- 2.1.6.6. Оценка теплот образования циклических, полициклических и мостиковых алканов на основе инкрементов «скошенных разобщенных» групп и «единственных» наиболее устойчивых конформаций
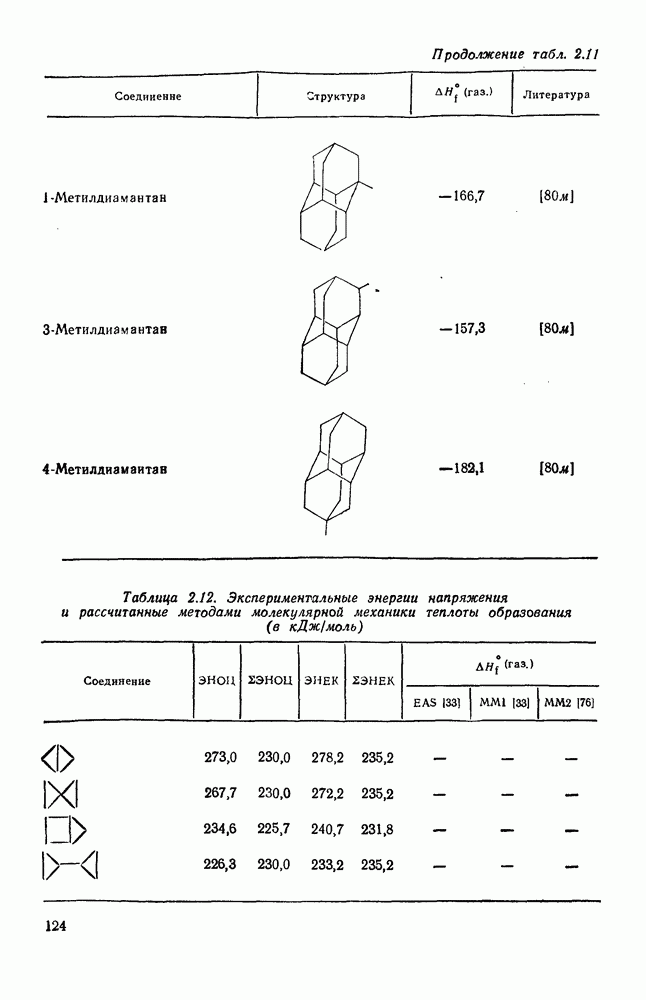
- 2.1.6.7. Молекулярно-механические расчеты теплот образования и энергии напряжения
- 2.1.6.8. Моно- и полициклоалкаиы
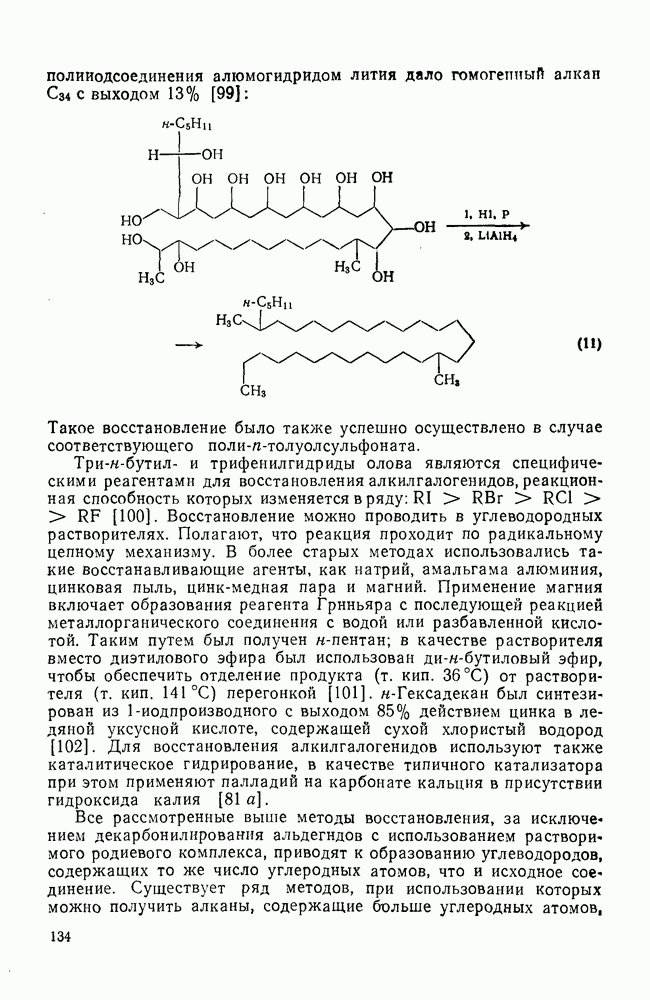
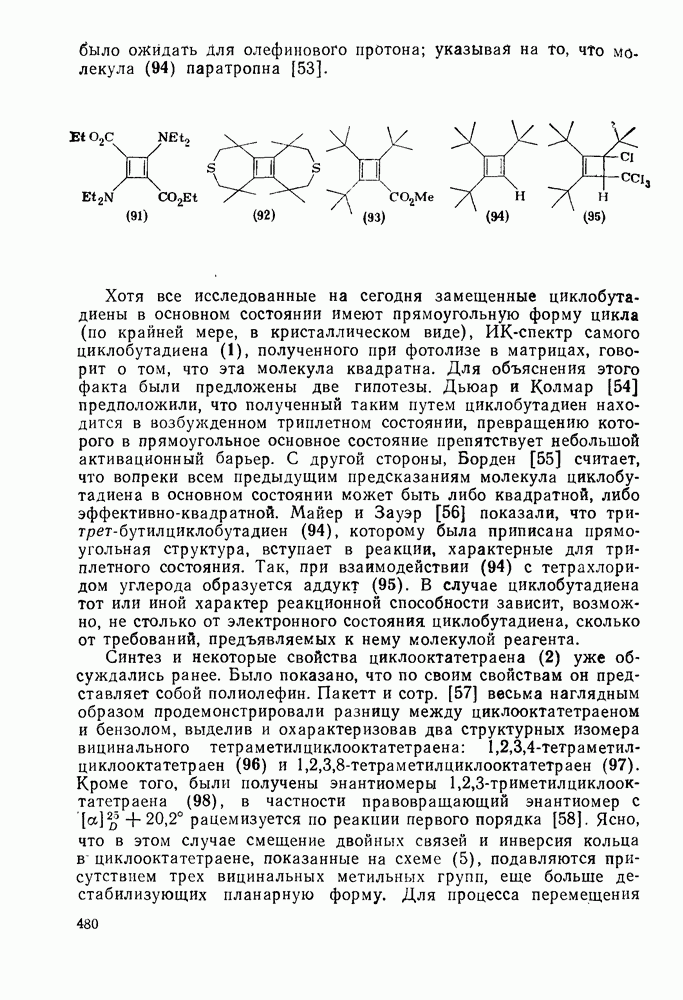
- 2.1.7. ПОЛУЧЕНИЕ АЦИКЛИЧЕСКИХ АЛКАНОВ
- 2.1.7.1. Получение алканов восстановлением олефинов
- 2.1.7.2. Получение алканов из альдегидов и кетонов
- 2.1.7.3. Получение алканов из спиртов и алкилгалогенидов
- 2.1.7.4. Получение алканов из карбоновых кислот
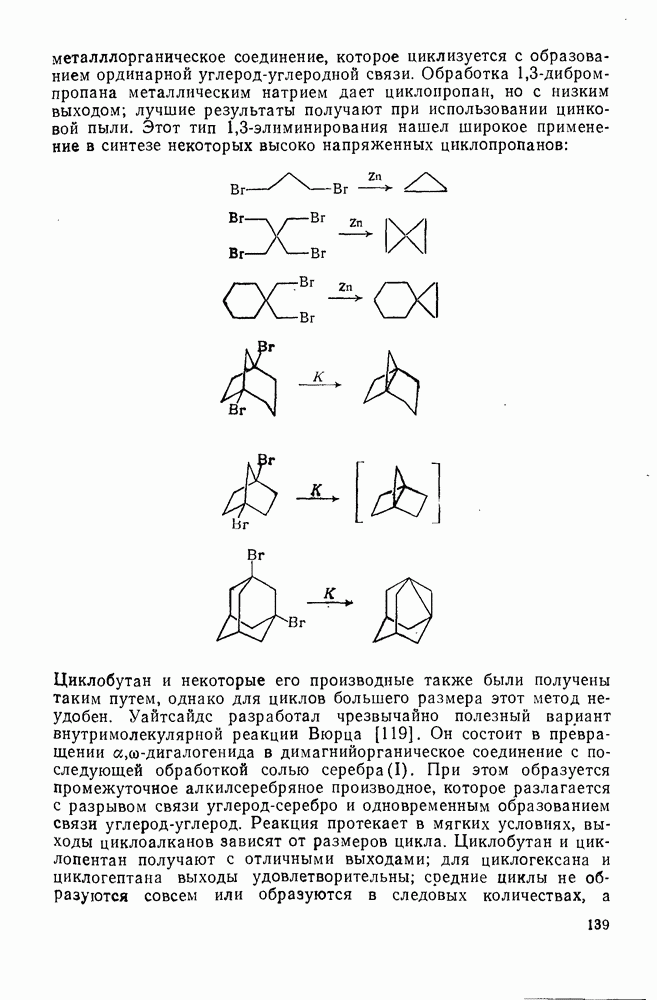
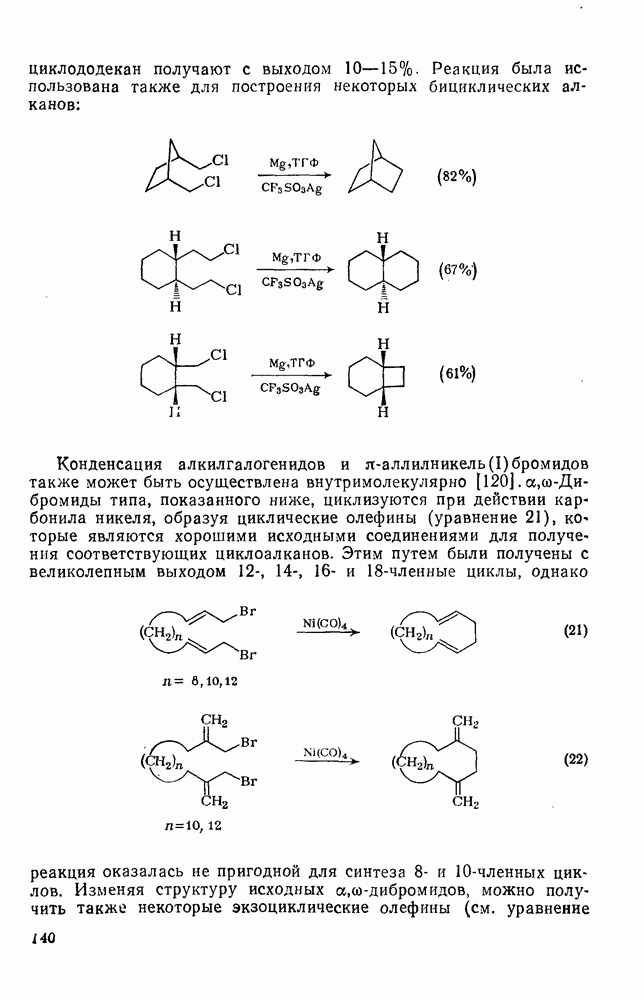
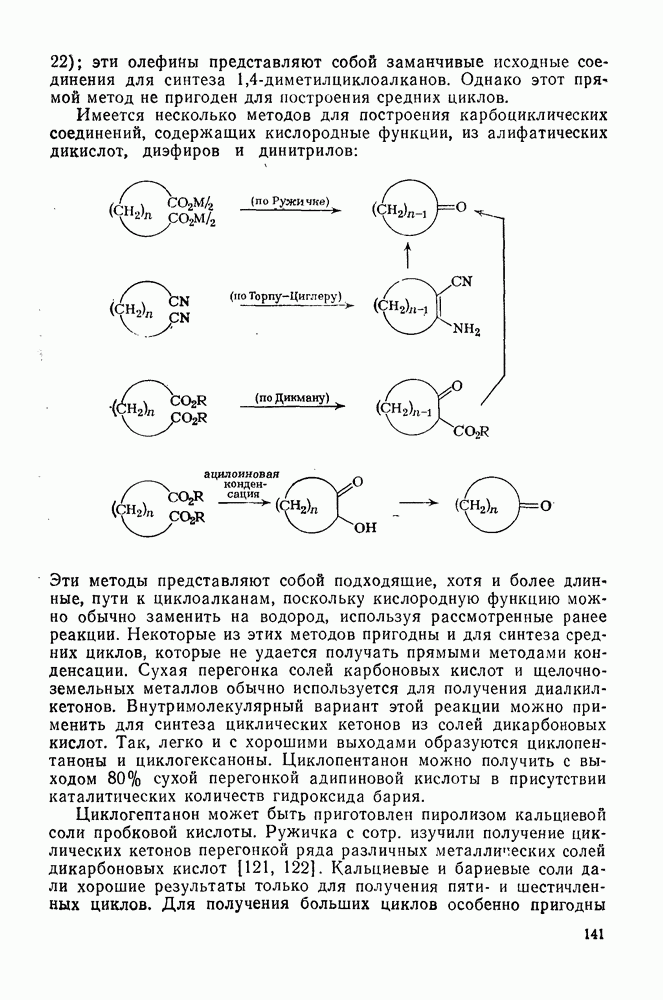
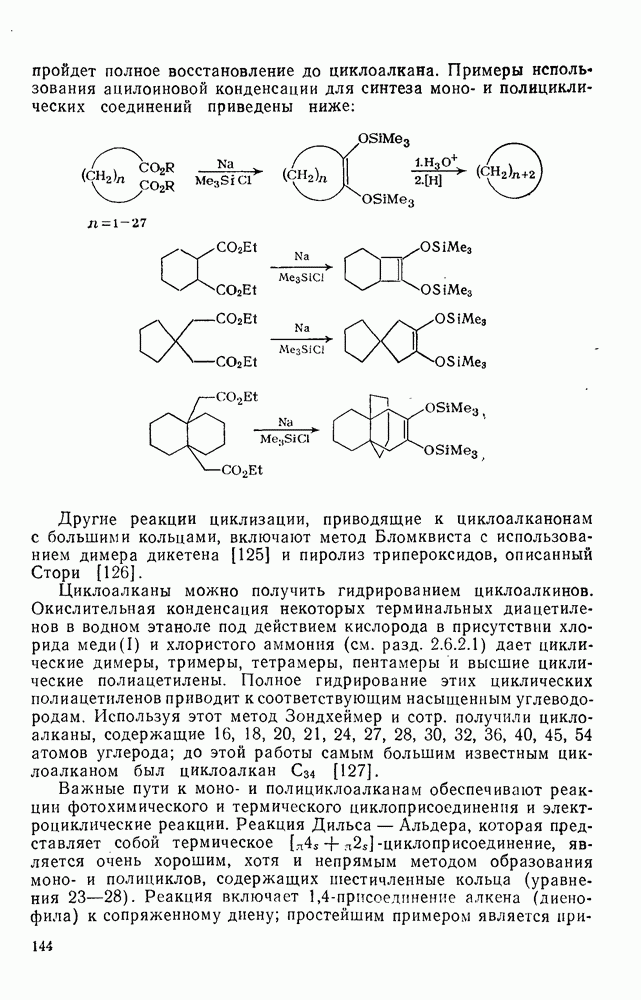
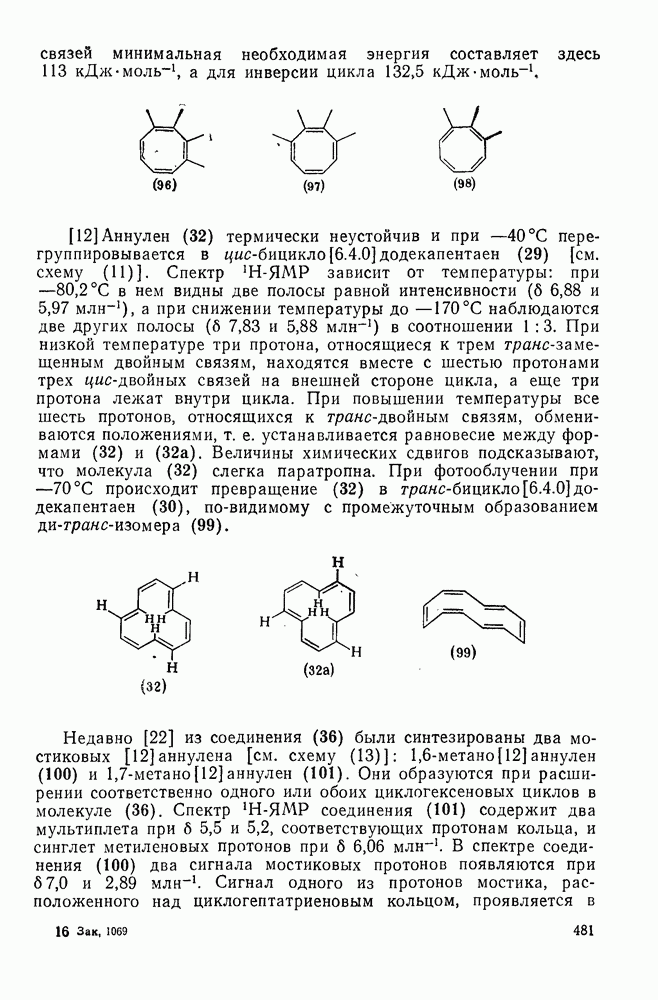
- 2.1.8. СИНТЕЗ МОНО- И ПОЛИЦИКЛОАЛКАНОВ
- 2.1.9. РЕАКЦИИ АЦИКЛИЧЕСКИХ АЛКАНОВ
- 2.1.9.1. Галогенирование
- 2.1.9.2. Нитрование
- 2.1.9.3. Окисление
- 2.1.9.4. Каталитическая изомеризация алканов
- 2.1.9.5. Каталитическое алкилирование алканов
- 2.1.9.6. Реакции крекинга алканов
- 2.1.9.7. Термический крекинг
- 2.1.9.8. Каталитический крекинг
- 2.1.9.9. Каталитический риформинг и дегидроциклизация алканов
- 2.1.10. РЕАКЦИИ ЦИКЛОАЛКАНОВ И ПОЛИЦИКЛОАЛКАНОВ
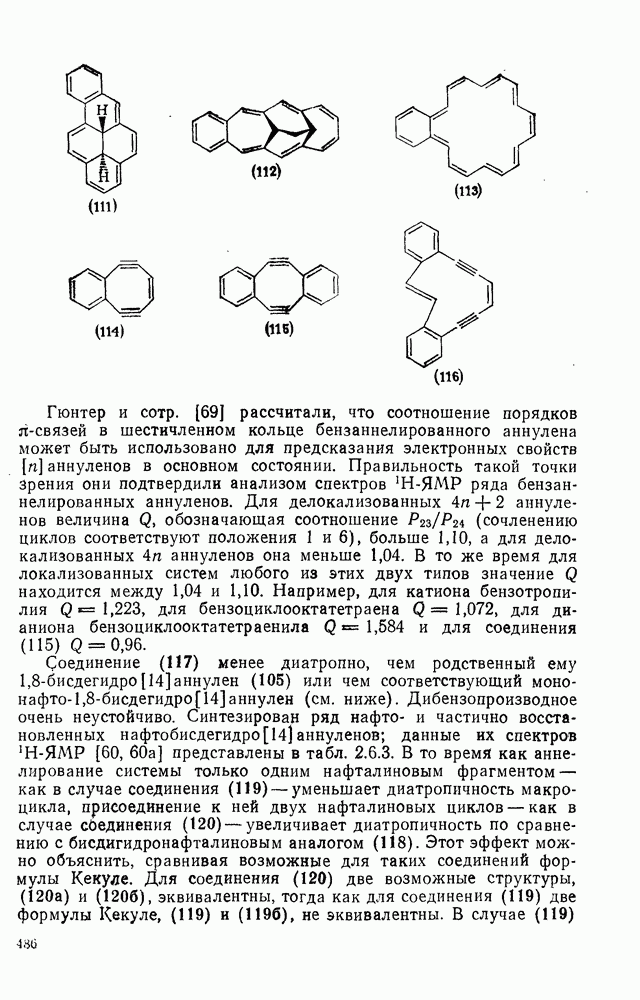
- 2.2. ОЛЕФИНОВЫЕ И АЦЕТИЛЕНОВЫЕ УГЛЕВОДОРОДЫ
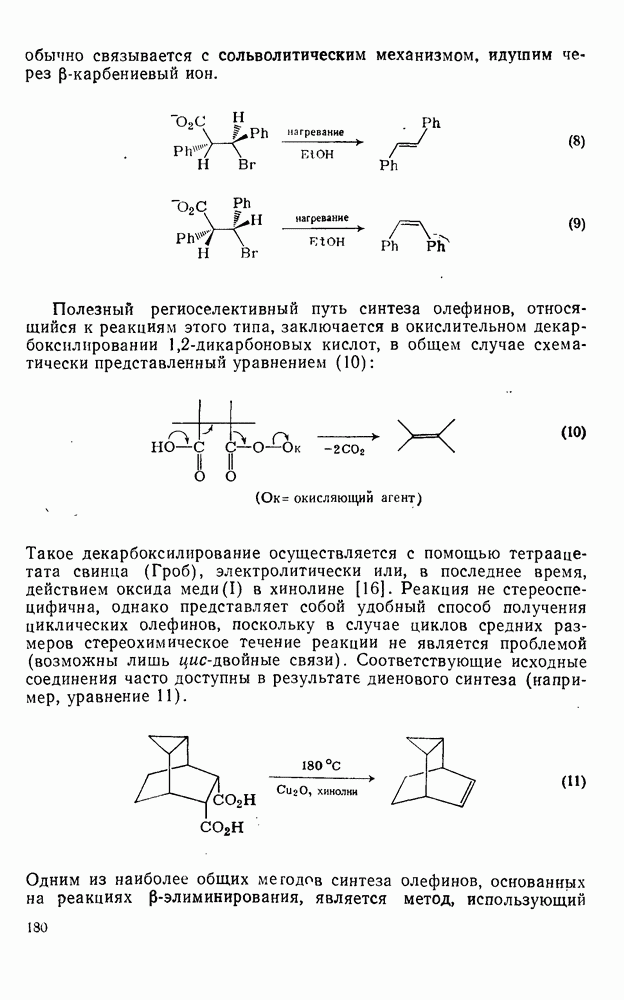
- 2.2.2. ПОЛУЧЕНИЕ ОЛЕФИНОВ
- 2.2.2.1. Элиминирование в системах
- 2.2.2.2. Элиминирование из систем
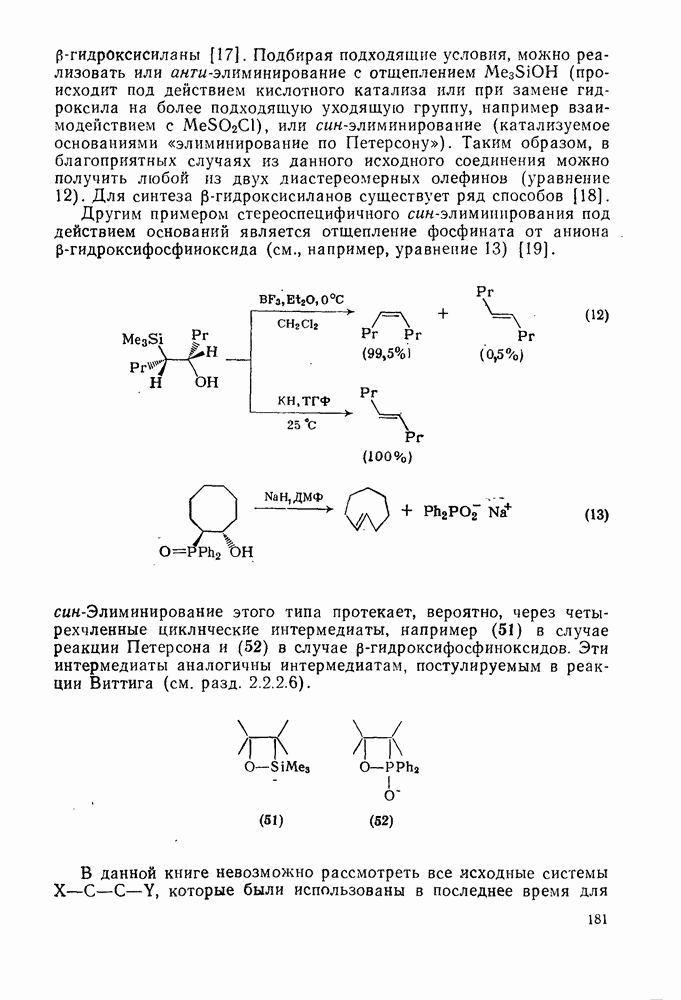
- 2.2.2.3. Циклоэлиминирование
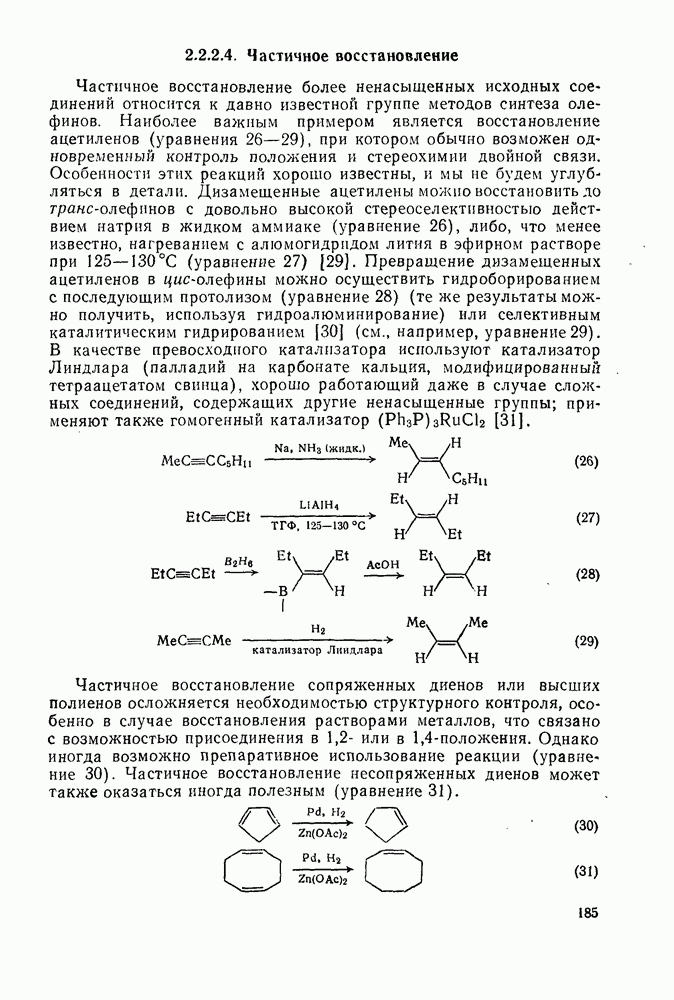
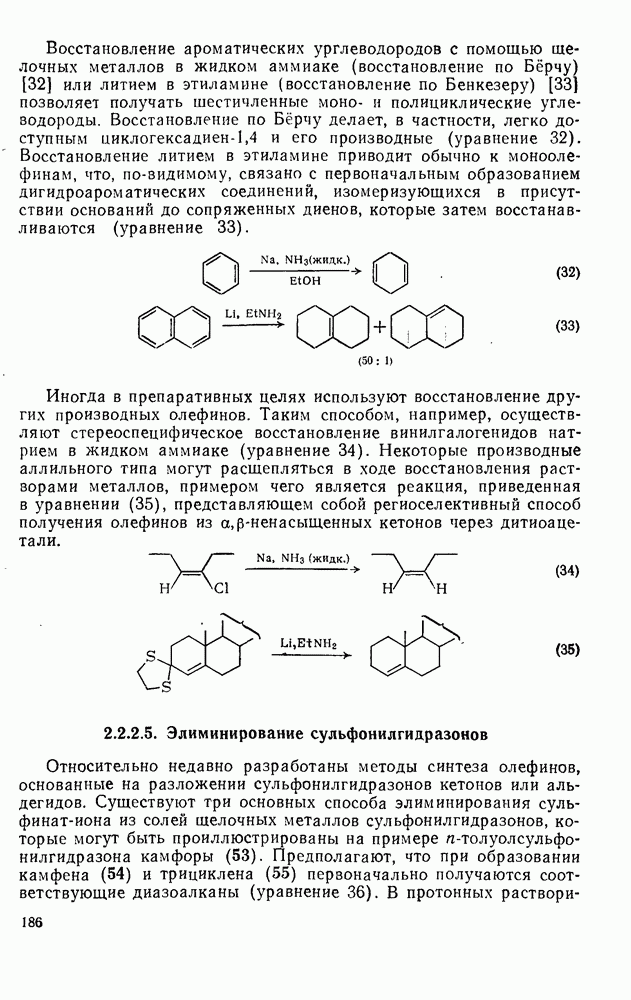
- 2.2.2.4. Частичное восстановление
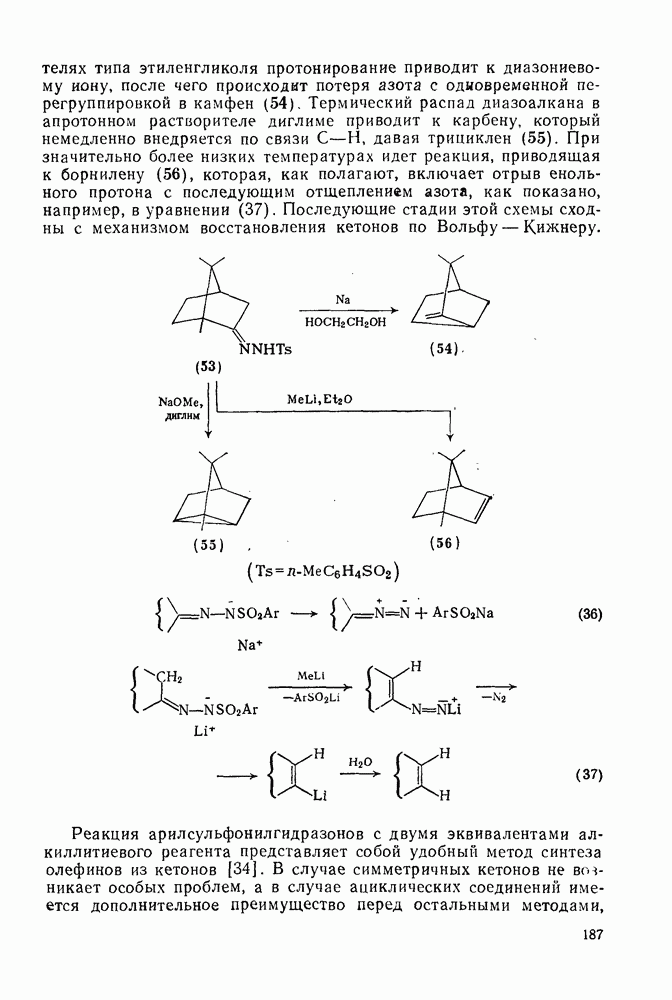
- 2.2.2.5. Элиминирование сульфонилгидразонов
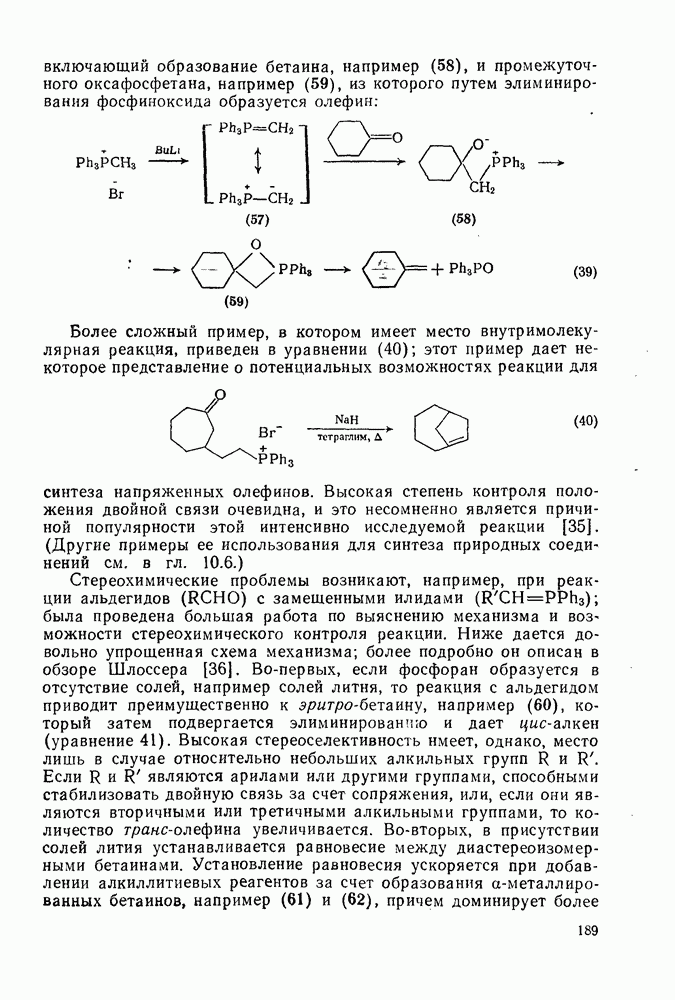
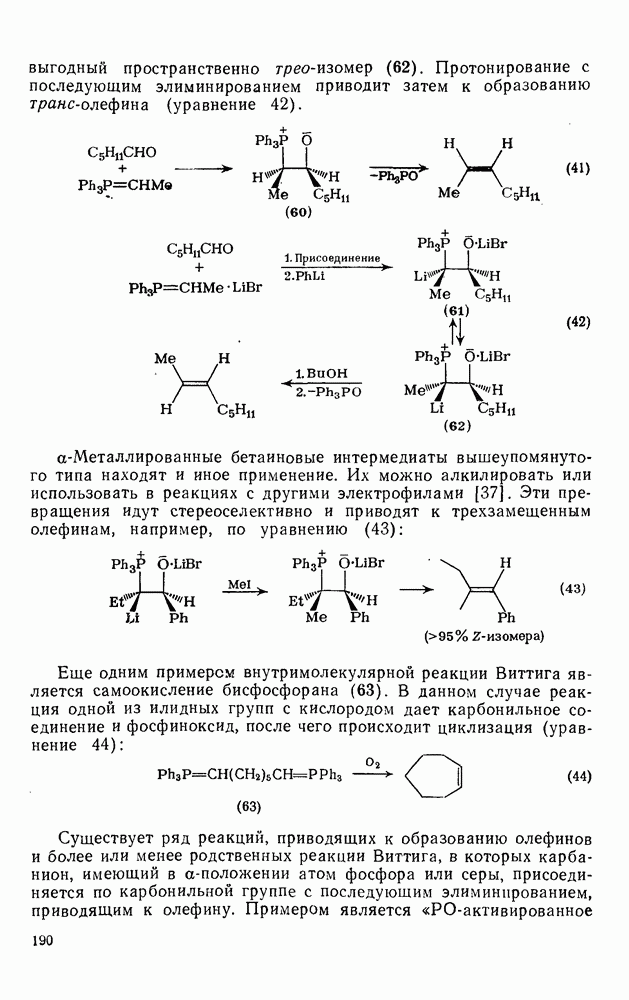
- 2.2.2.6. Реакция Виттига и родственные ей реакции
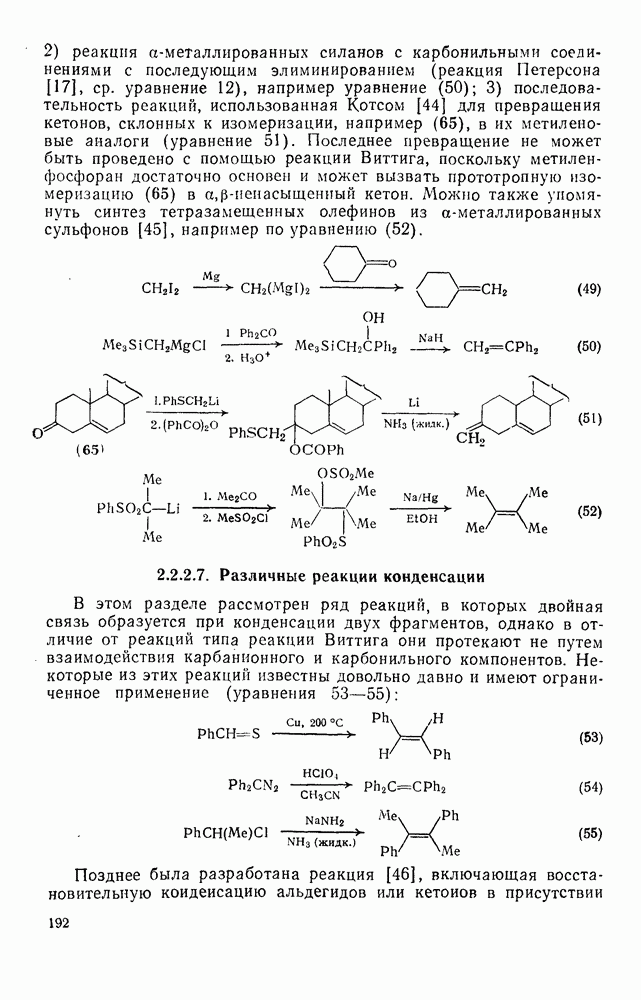
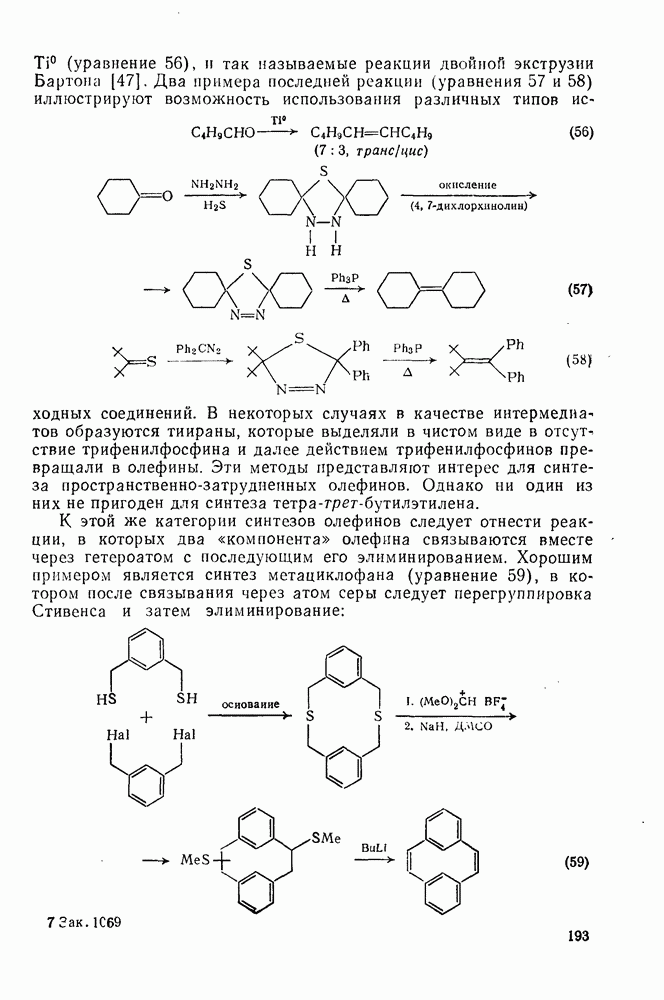
- 2.2.2.7. Различные реакции конденсации
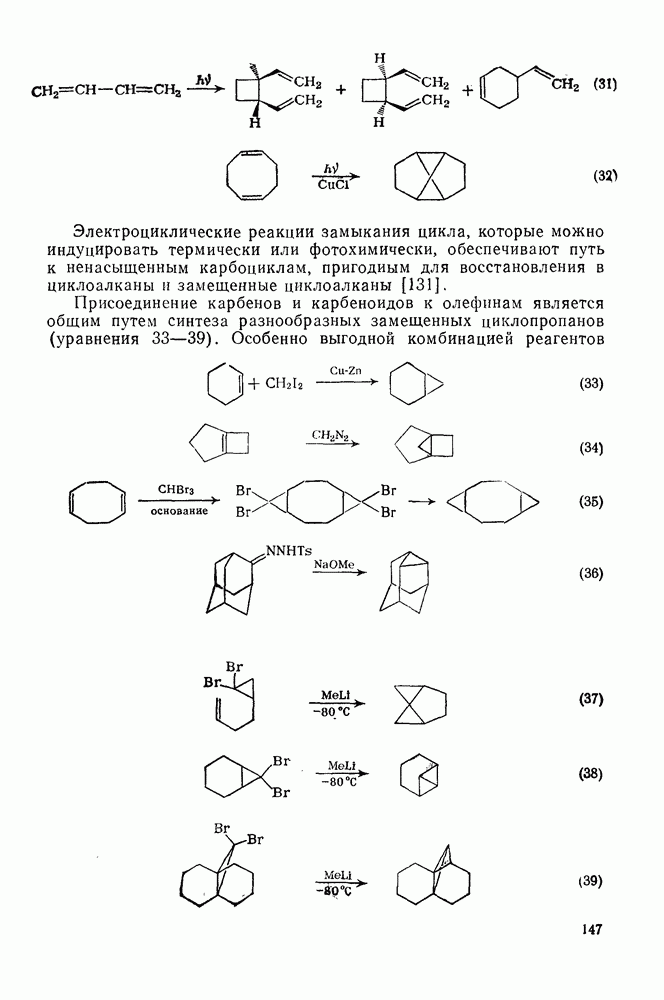
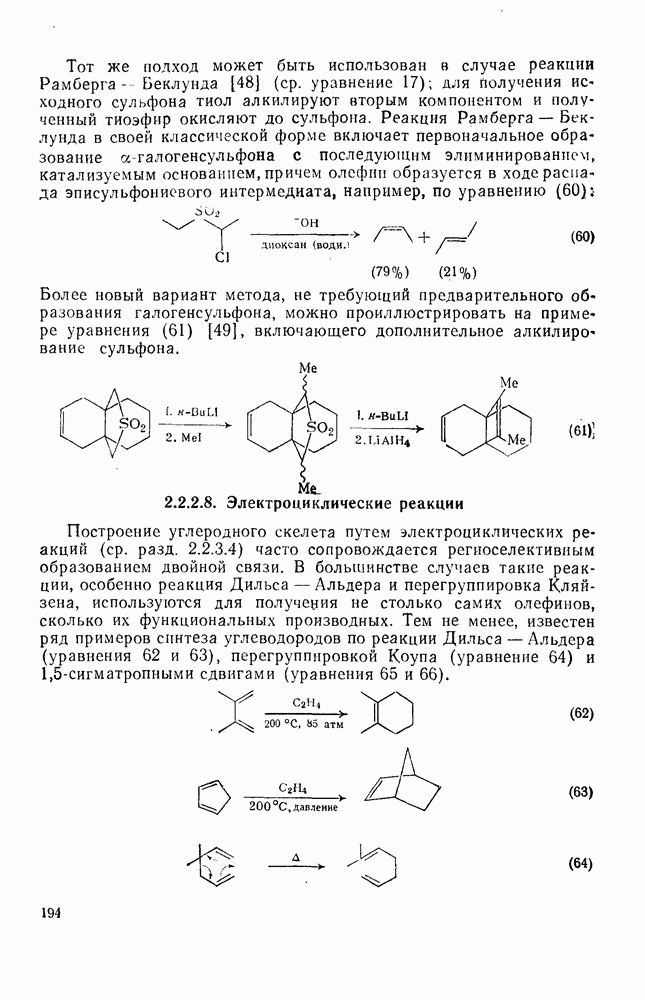
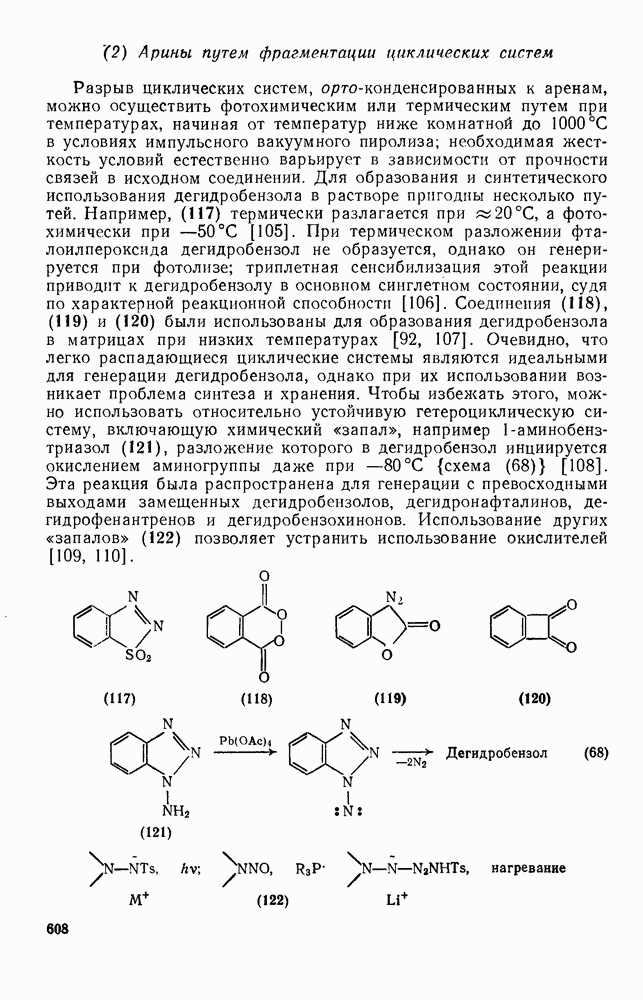
- 2.2.2.8. Электроциклические реакции
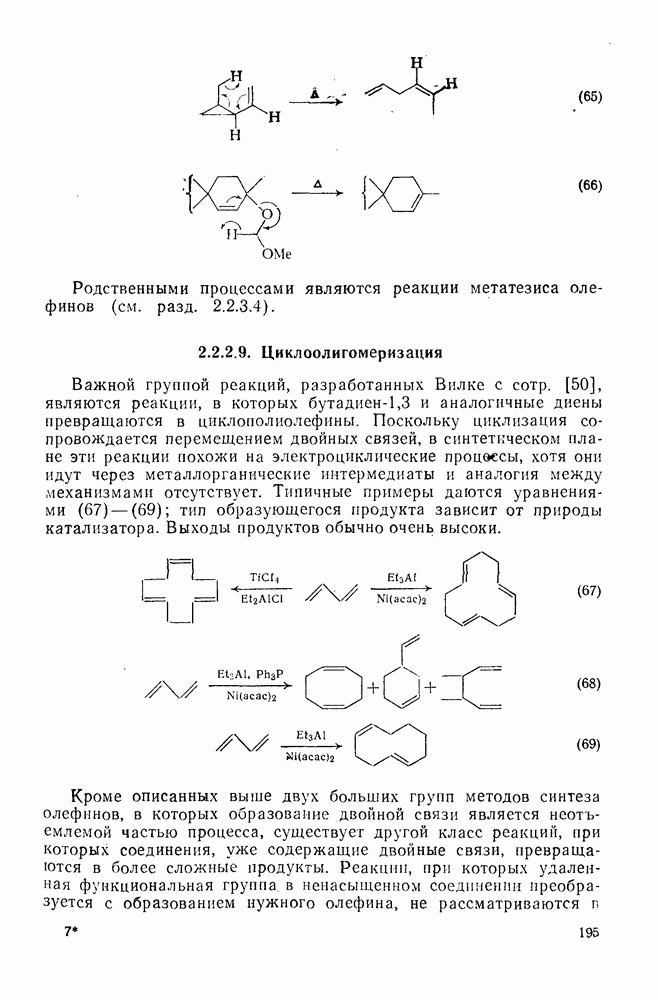
- 2.2.2.9. Циклоолигомеризация
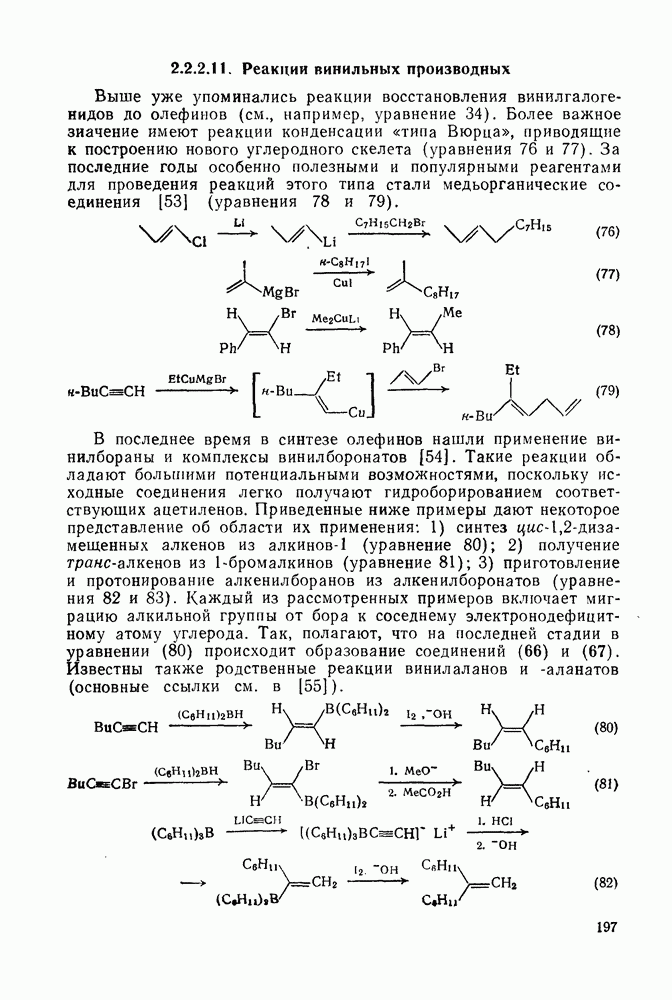
- 2.2.2.11. Реакции винильных производных
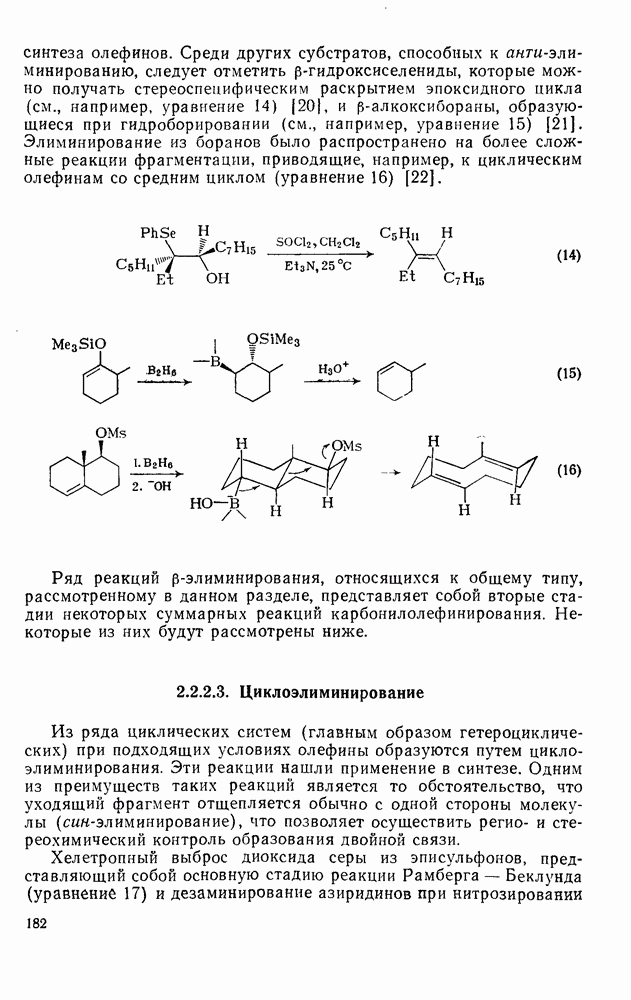
- 2.2.3. РЕАКЦИИ ОЛЕФИНОВ
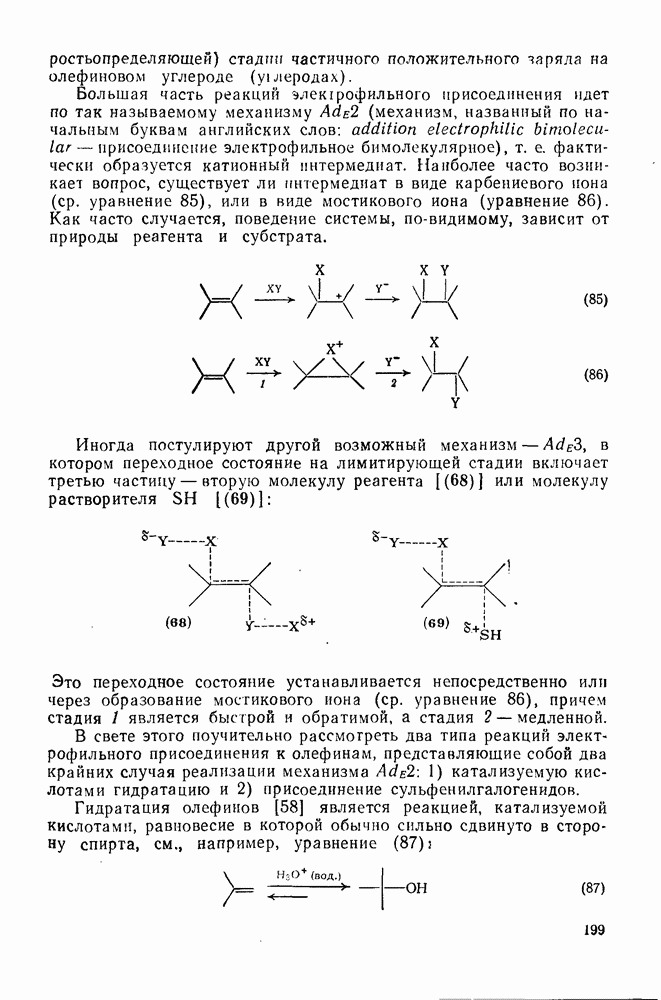
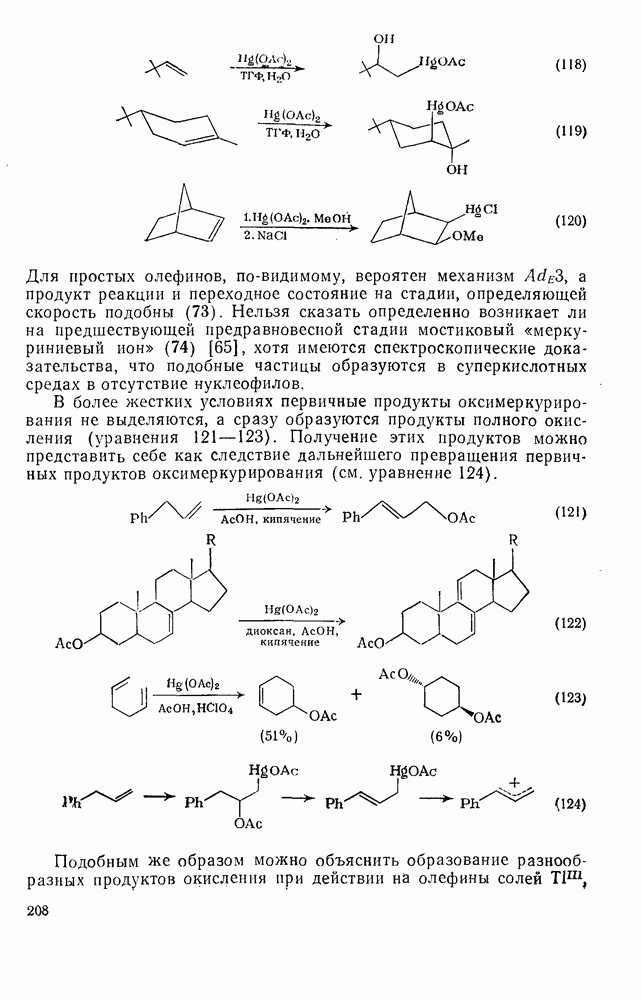
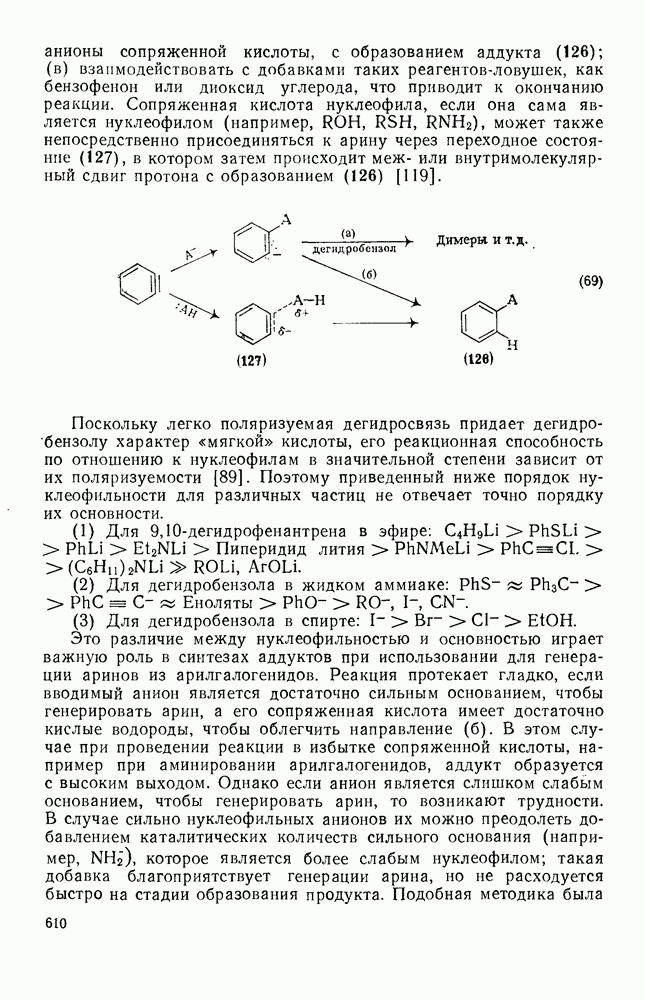
- 2.2.3.1. Электрофильное присоединение
- 2.2.3.2. Нуклеофильное присоединение
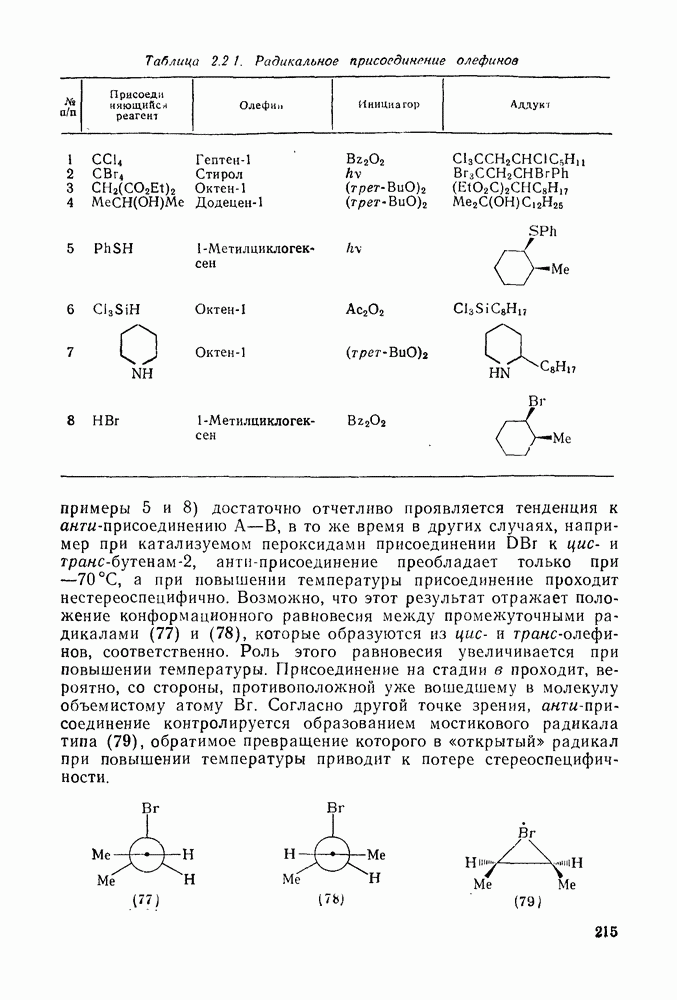
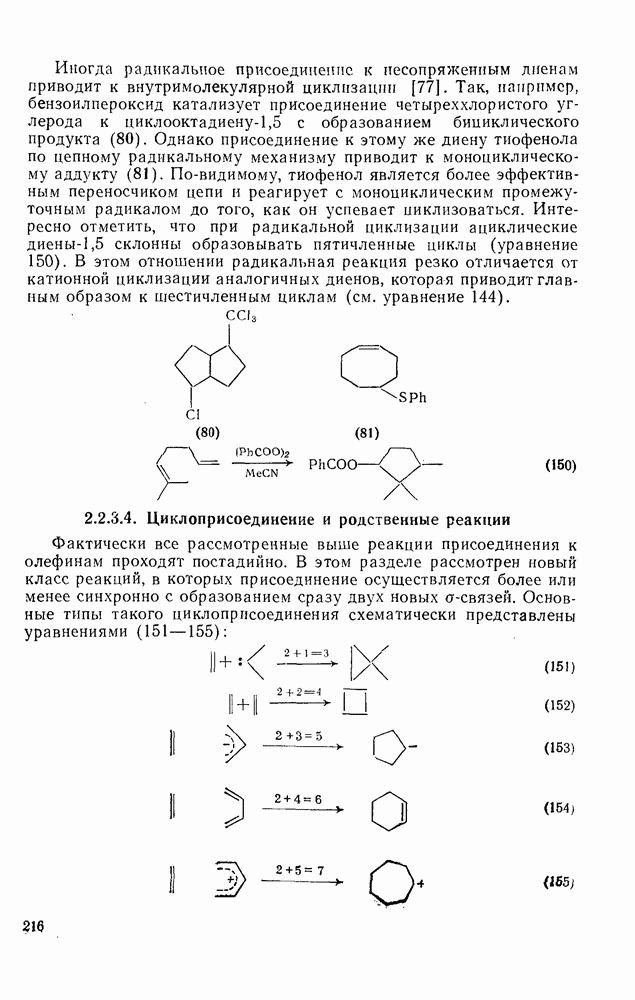
- 2.2.3.3. Радикальное присоединение
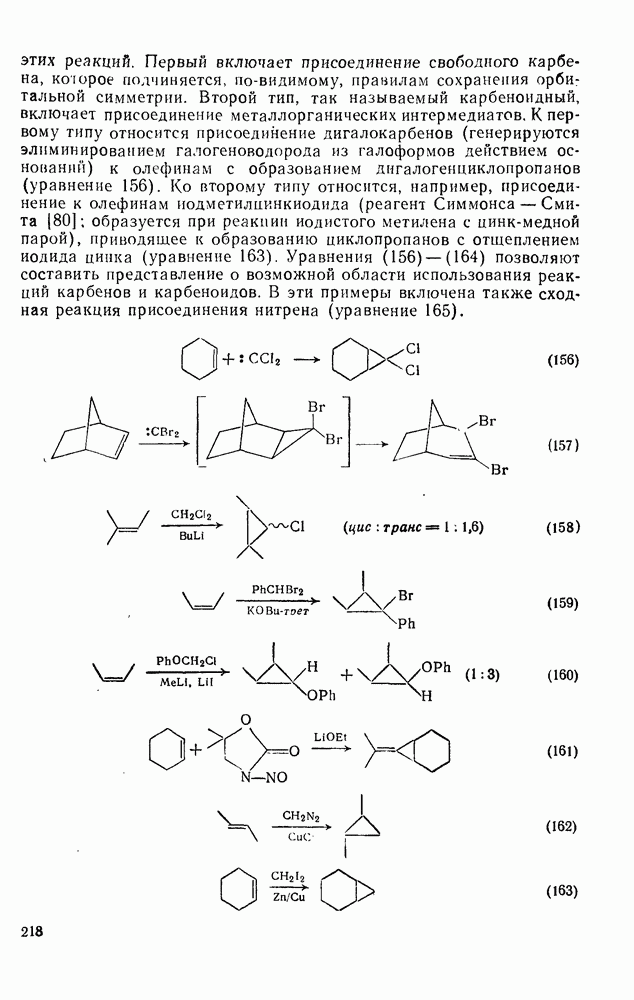
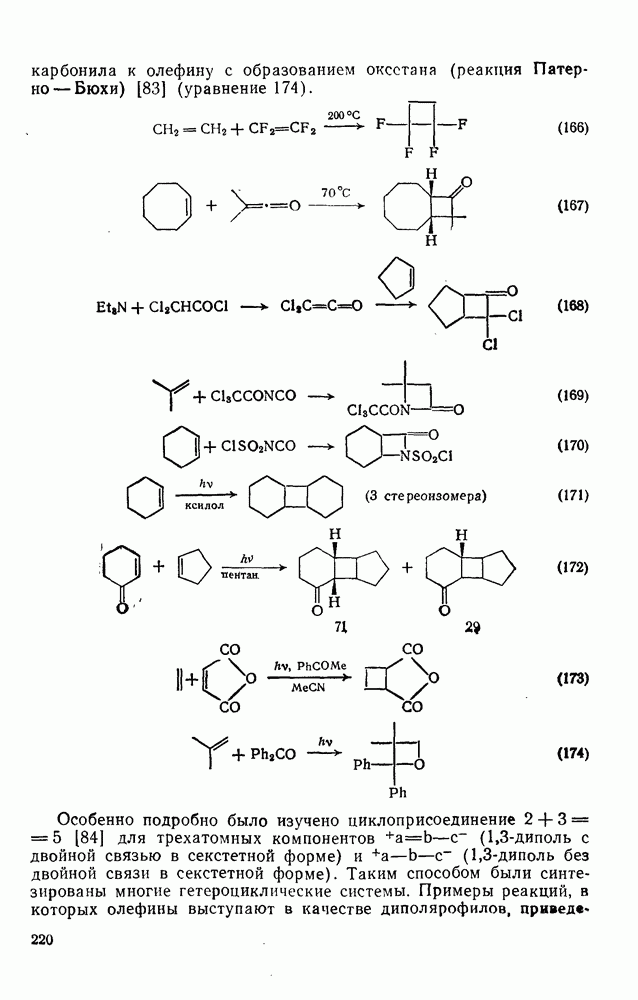
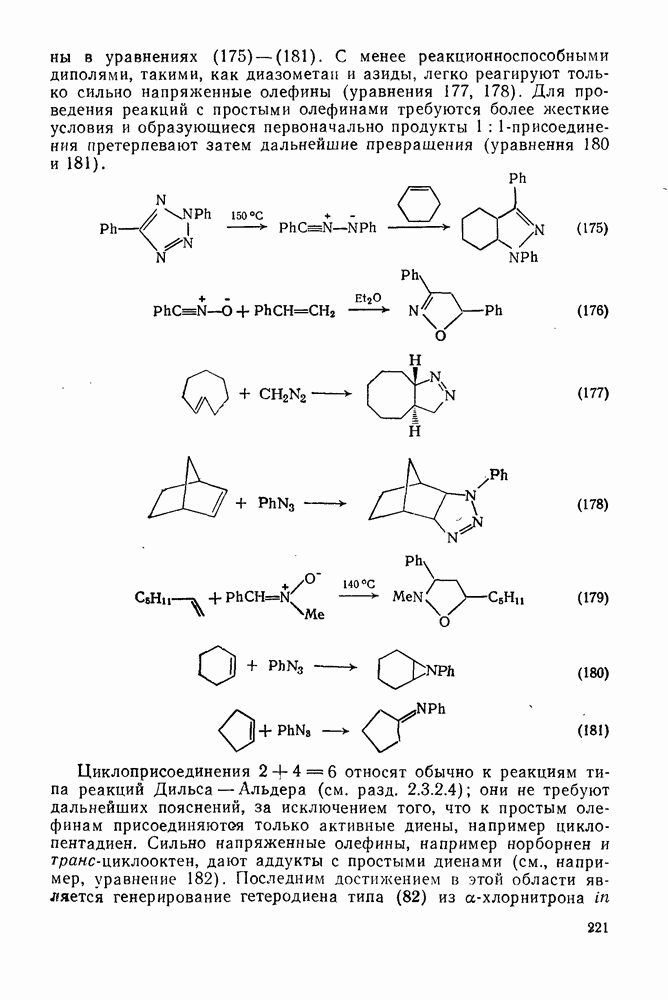
- 2.2.3.4. Циклоприсоединение и родственные реакции
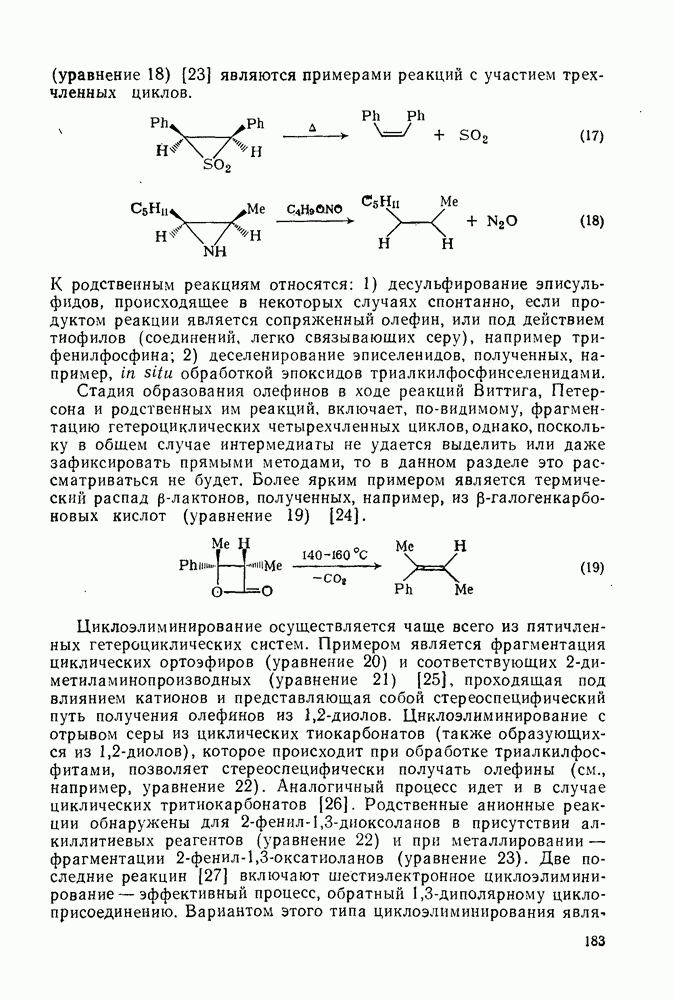
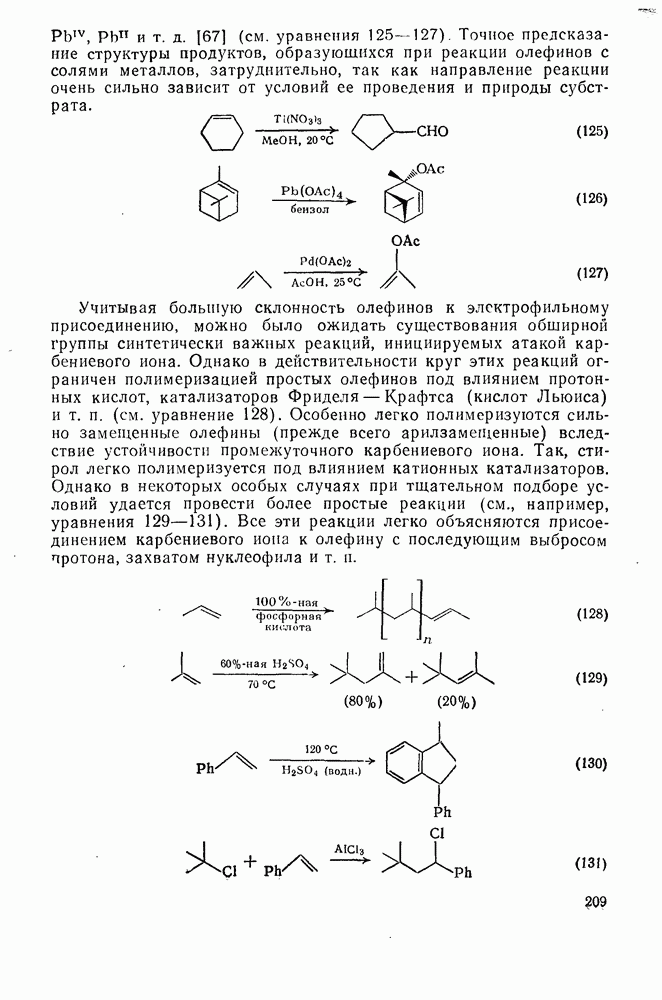
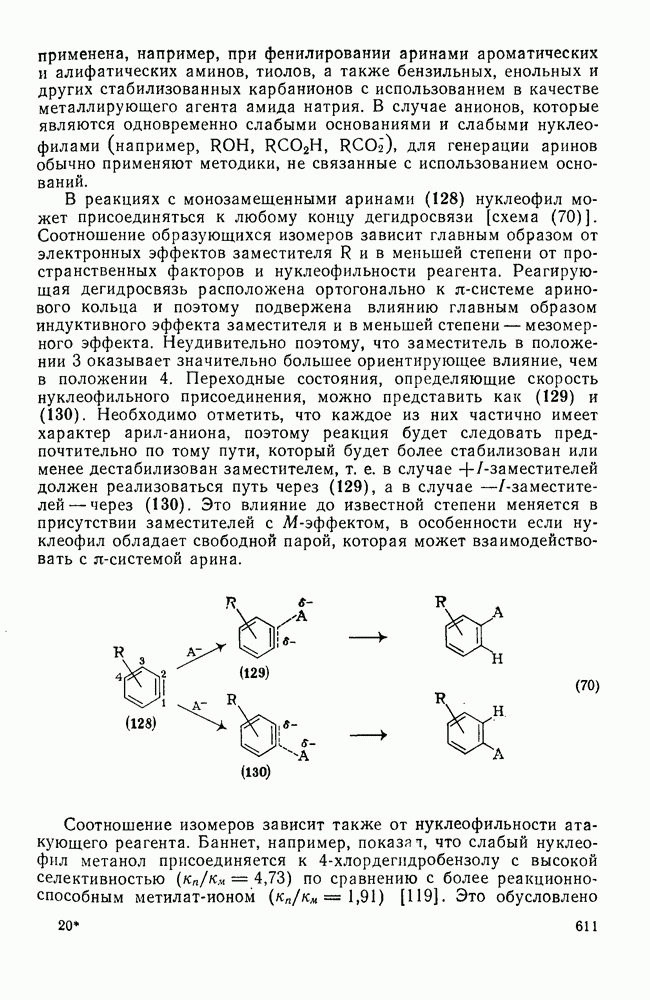
- 2.2.3.5. Окисление
- 2.2.3.6. Восстановление
- 2.2.3.7. Перегруппировки
- 2.2.3.8. Фотохимические реакции
- 2.2.3.9. Прочие реакции
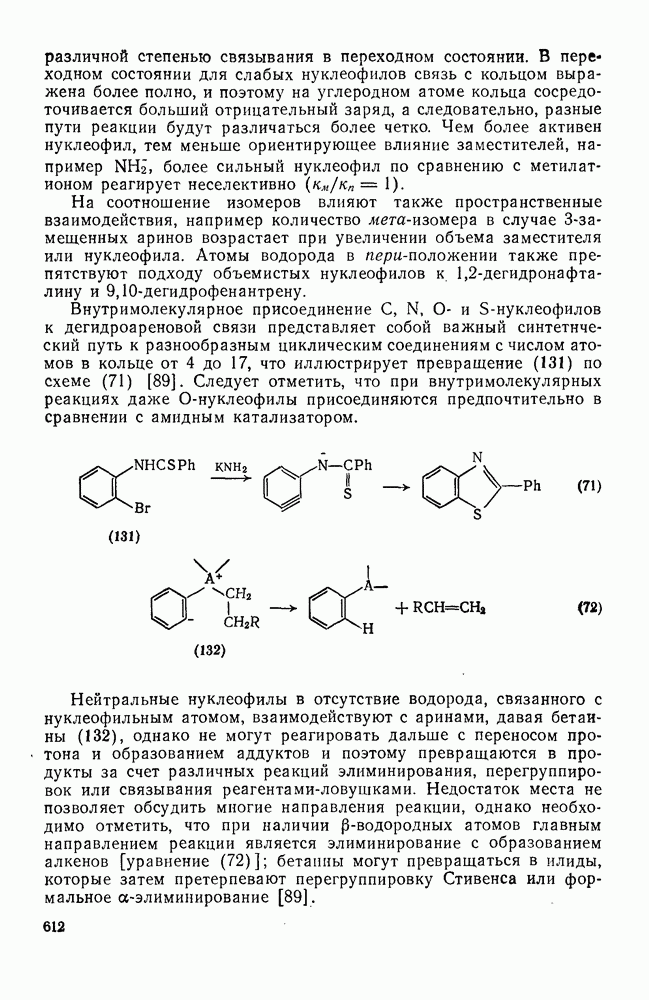
- 2.3. ДИЕНЫ, ПОЛНЕНЫ И АЦЕТИЛЕНОВЫЕ УГЛЕВОДОРОДЫ
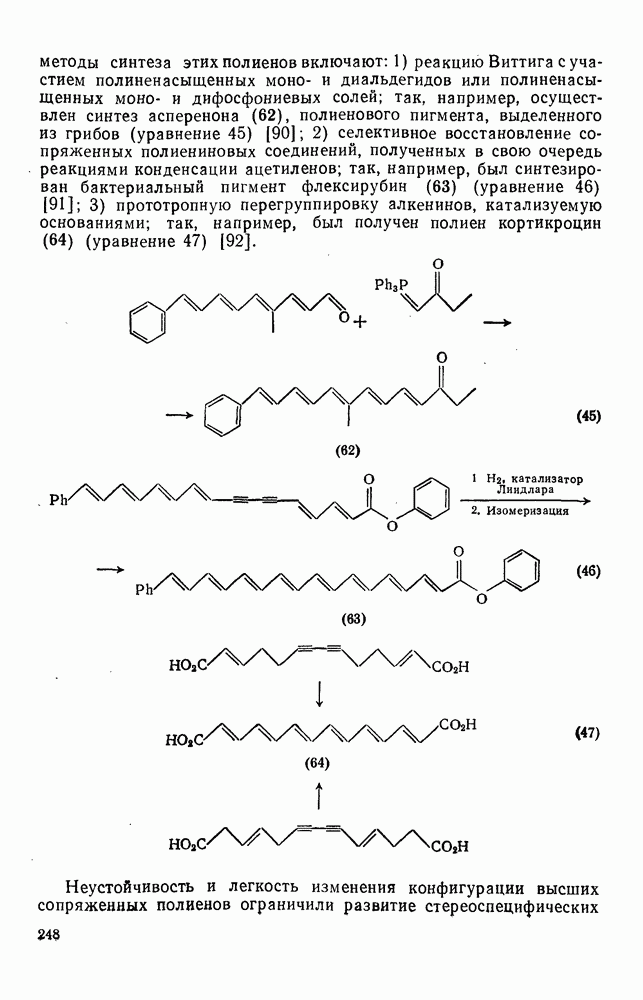
- 2.3.1. СОПРЯЖЕННЫЕ ДИЕНЫ И ПОЛНЕНЫ
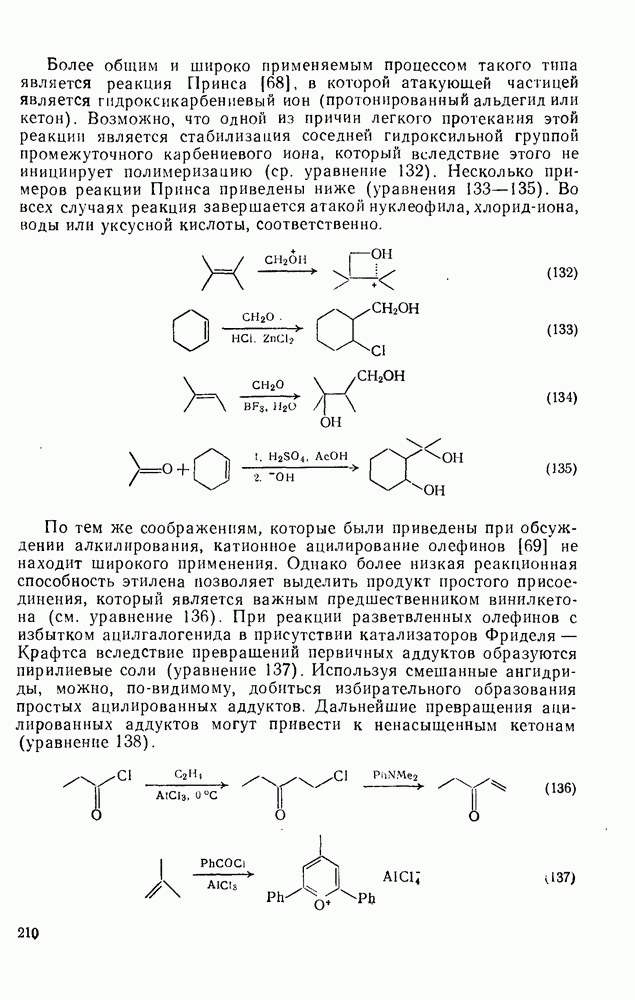
- 2.3.1.2. Получение сопряженных диенов
- 2.3.2. РЕАКЦИИ СОПРЯЖЕННЫХ ДИЕНОВ
- 2.3.2.2. Восстановление
- 2.3.2.3. Гидроборирование
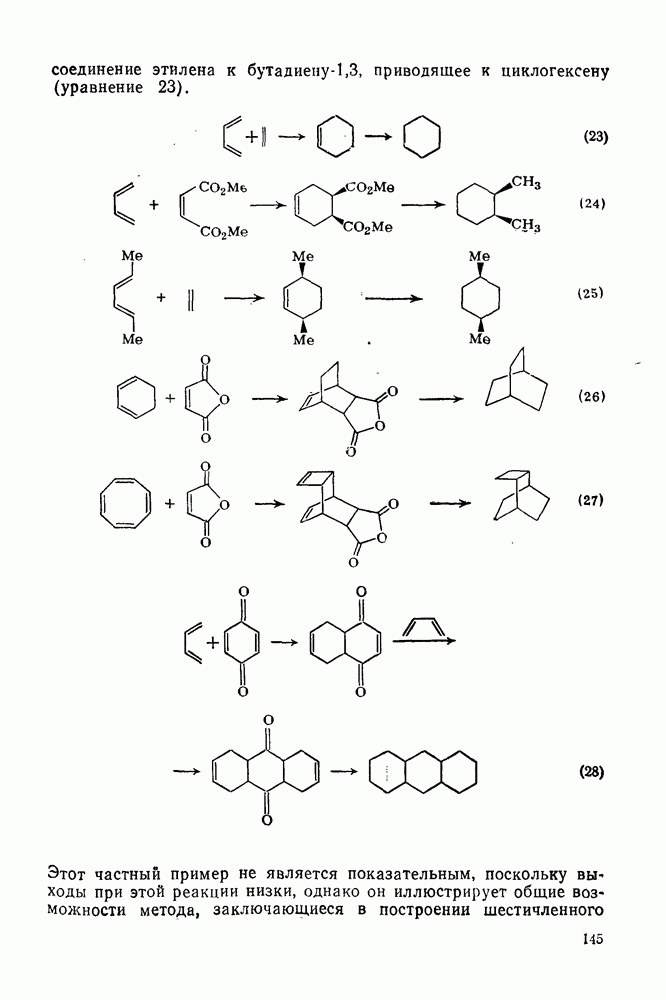
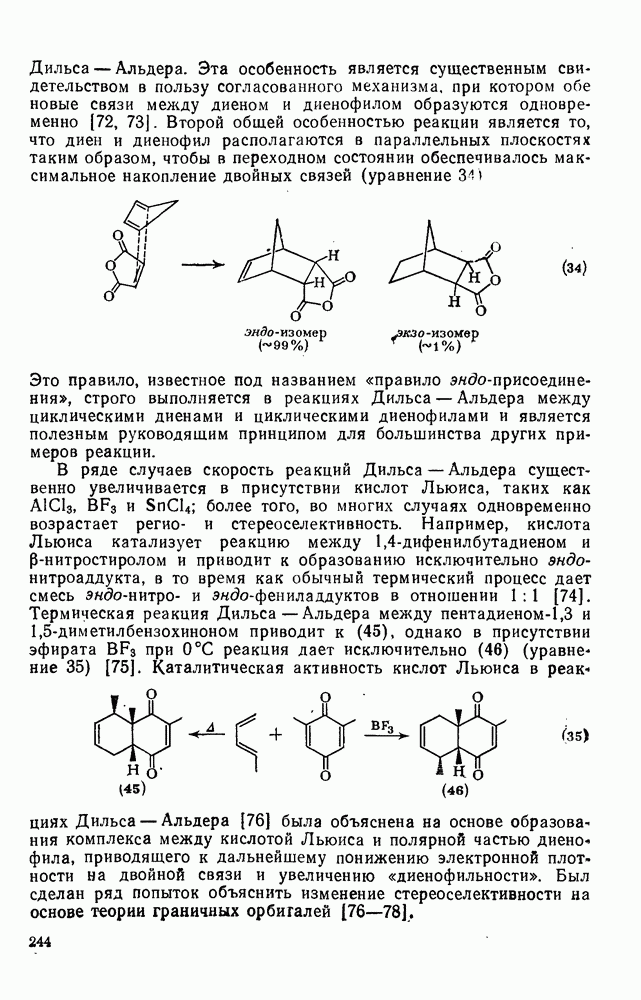
- 2.3.2.4. Реакция Дильса — Альдера
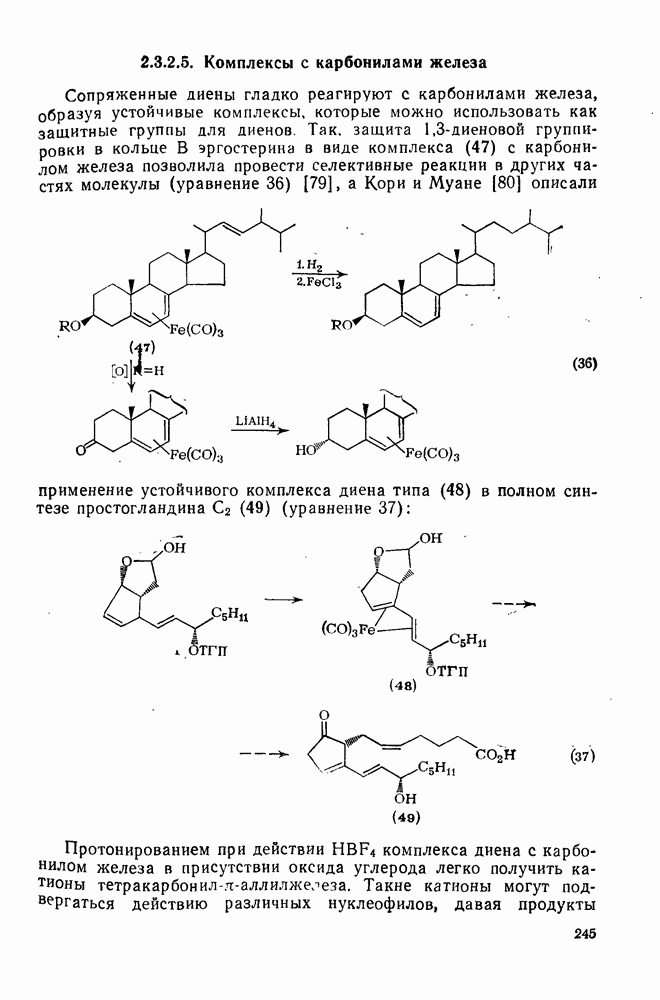
- 2.3.2.5. Комплексы с карбонилами железа
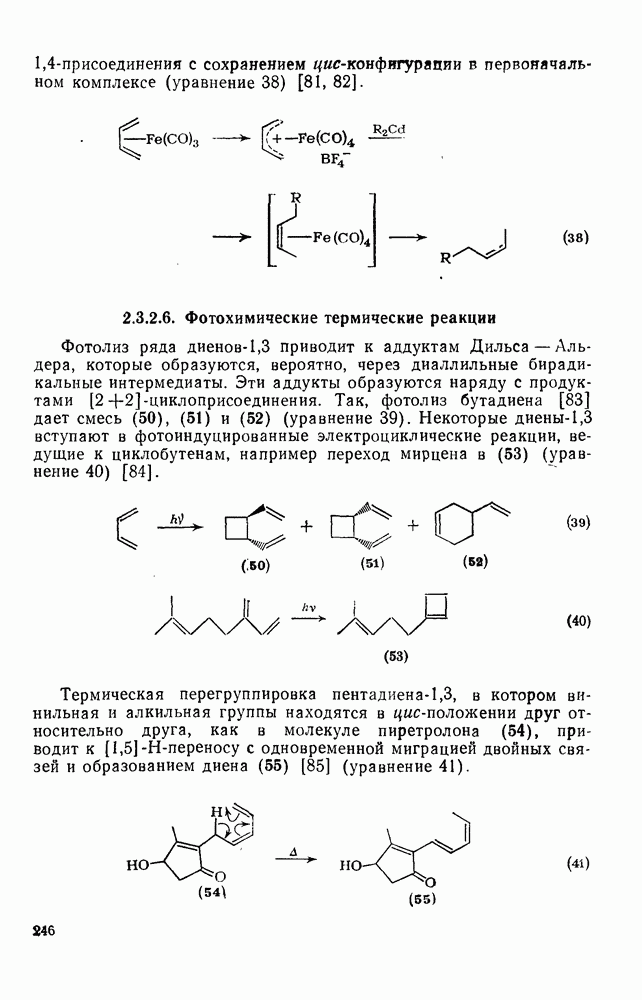
- 2.3.2.6. Фотохимические термические реакции
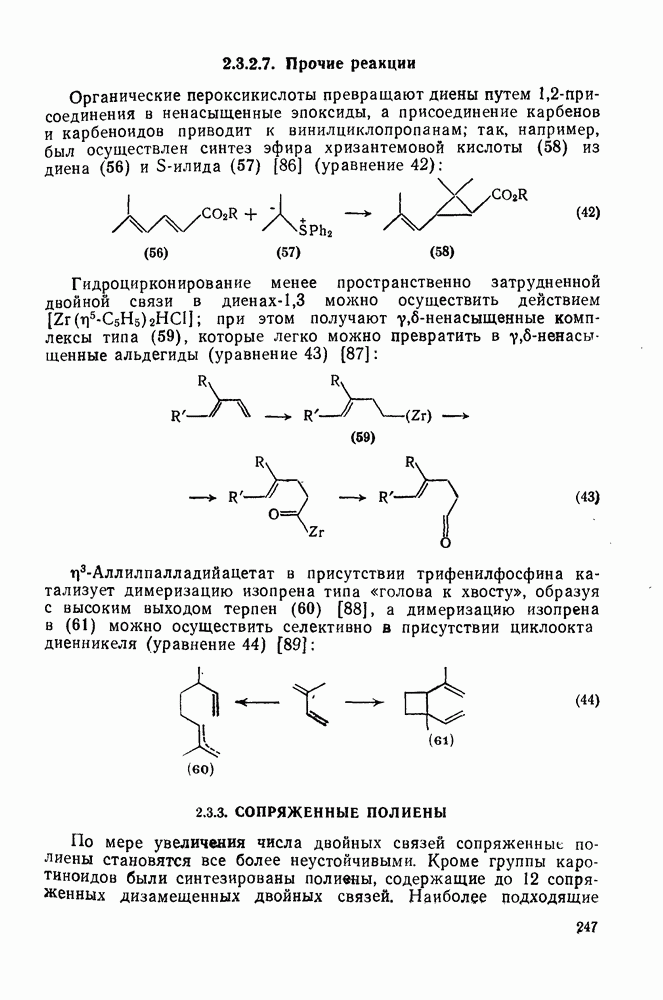
- 2.3.2.7. Прочие реакции
- 2.3.3. СОПРЯЖЕННЫЕ ПОЛИЕНЫ
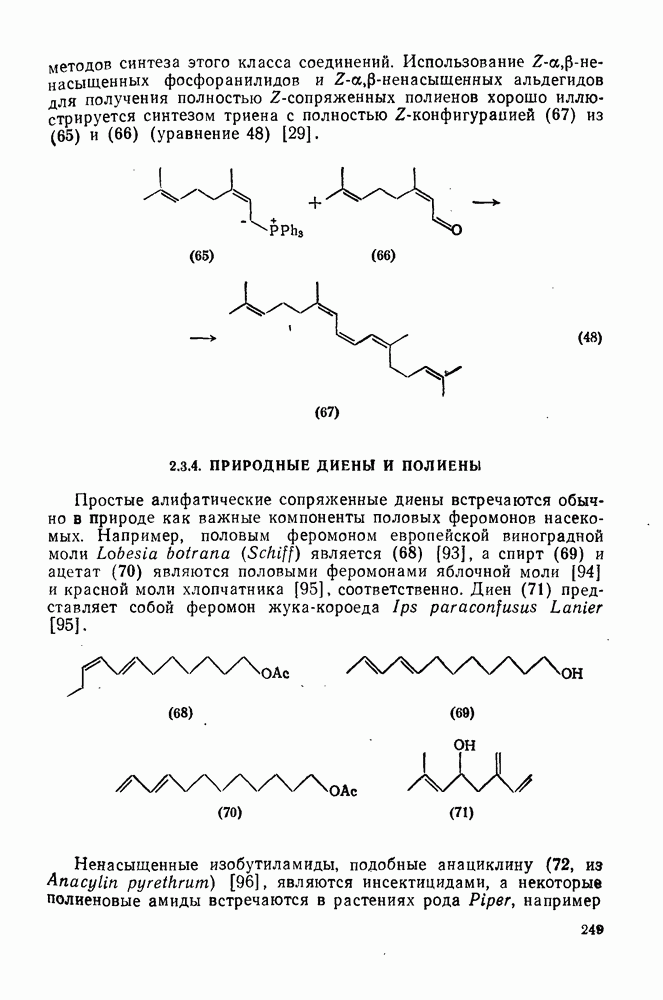
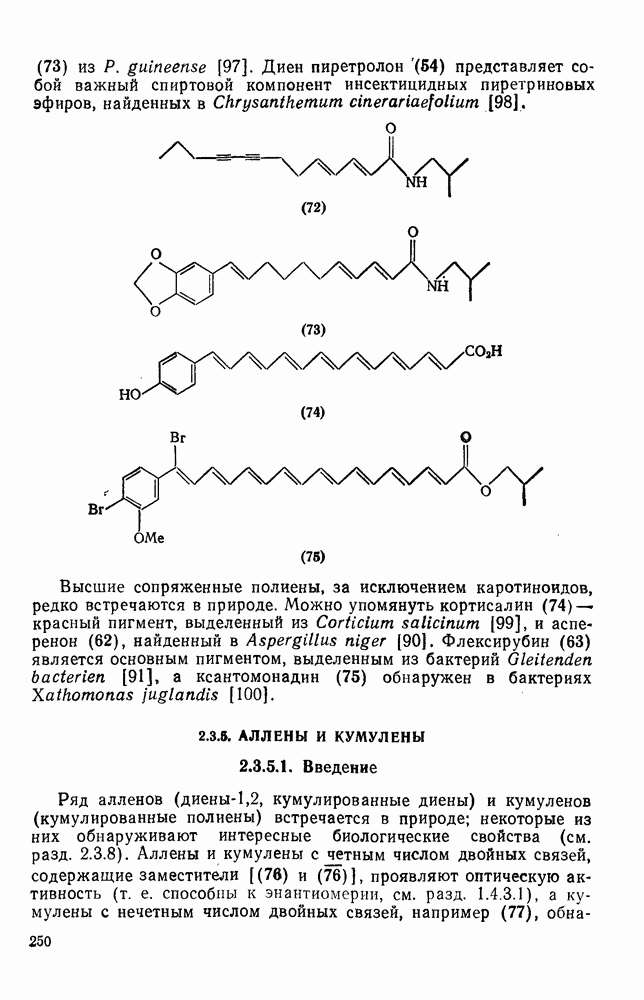
- 2.3.4. ПРИРОДНЫЕ ДИЕНЫ И ПОЛНЕНЫ
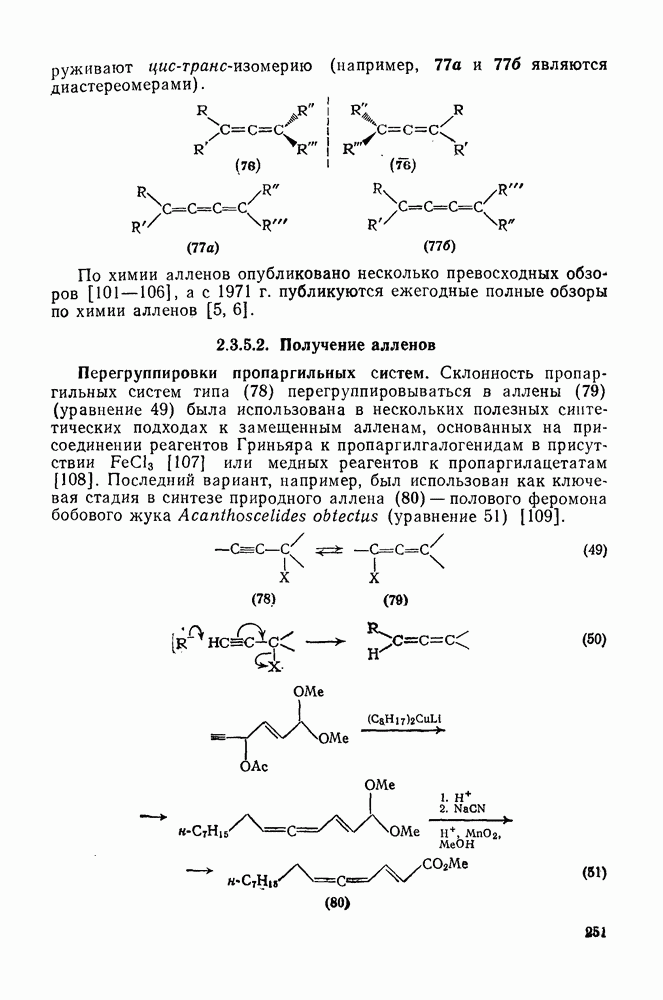
- 2.3.5. АЛЛЕНЫ И КУМУЛЕНЫ
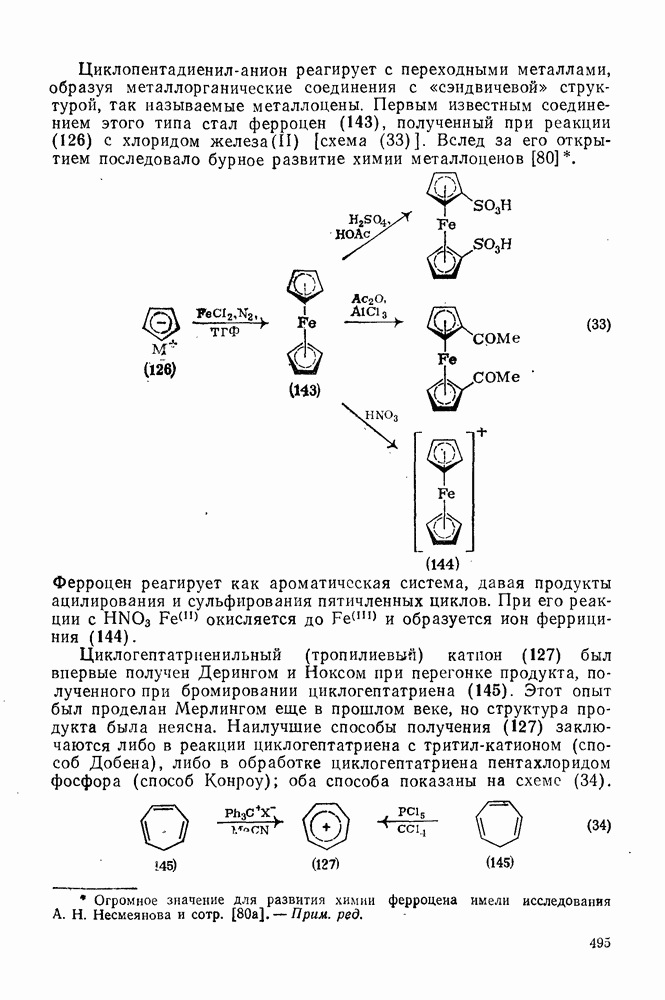
- 2.3.5.2. Получение алленов
- 2.3.6. РЕАКЦИИ АЛЛЕНОВ
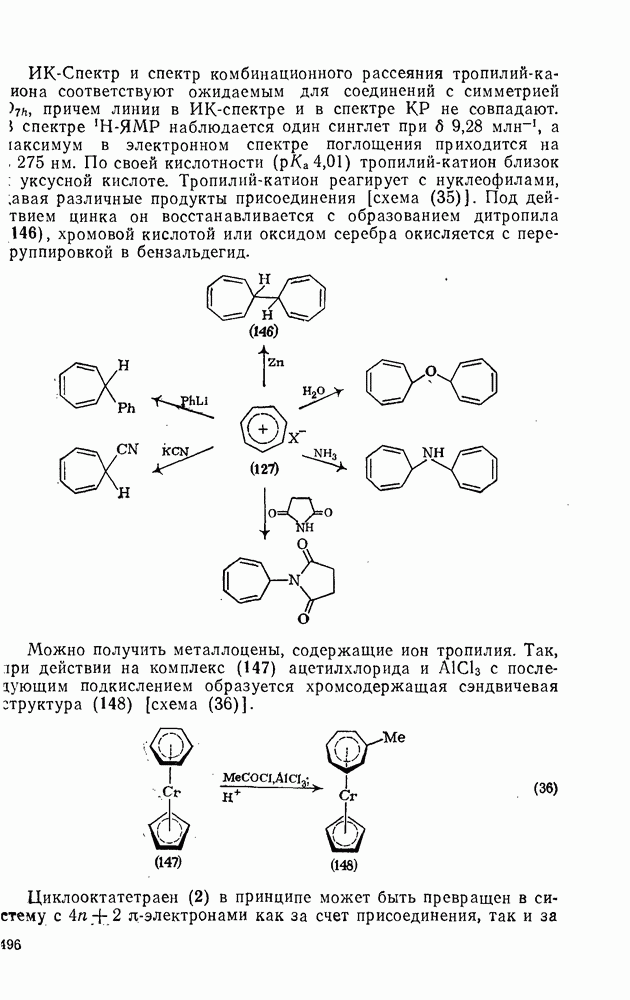
- 2.3.6.2. Гидрирование
- 2.3.6.3. Реакции алленов в присутствии комплексов металлов
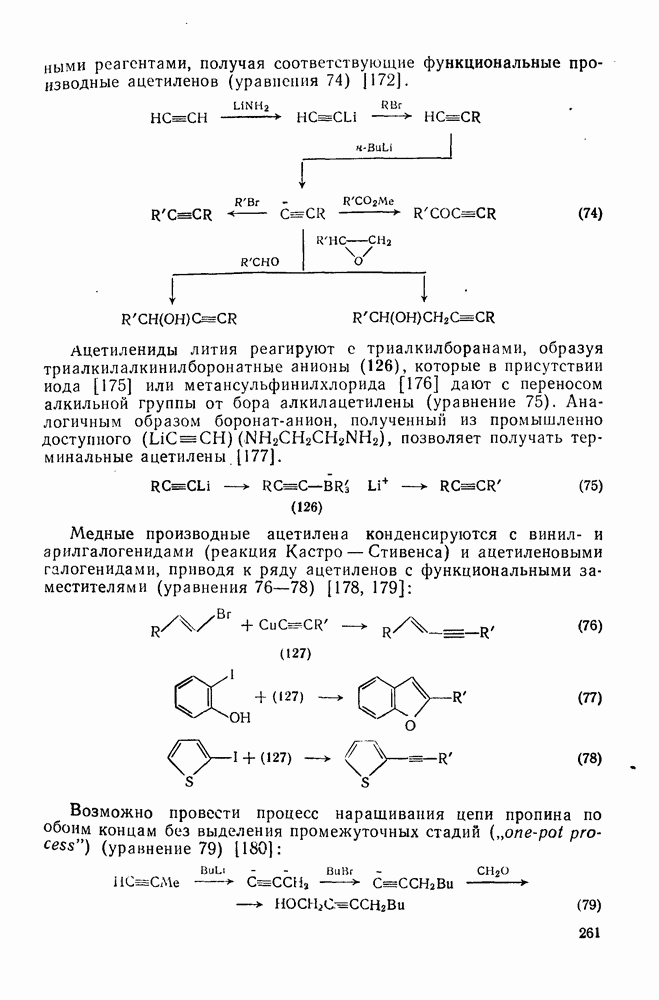
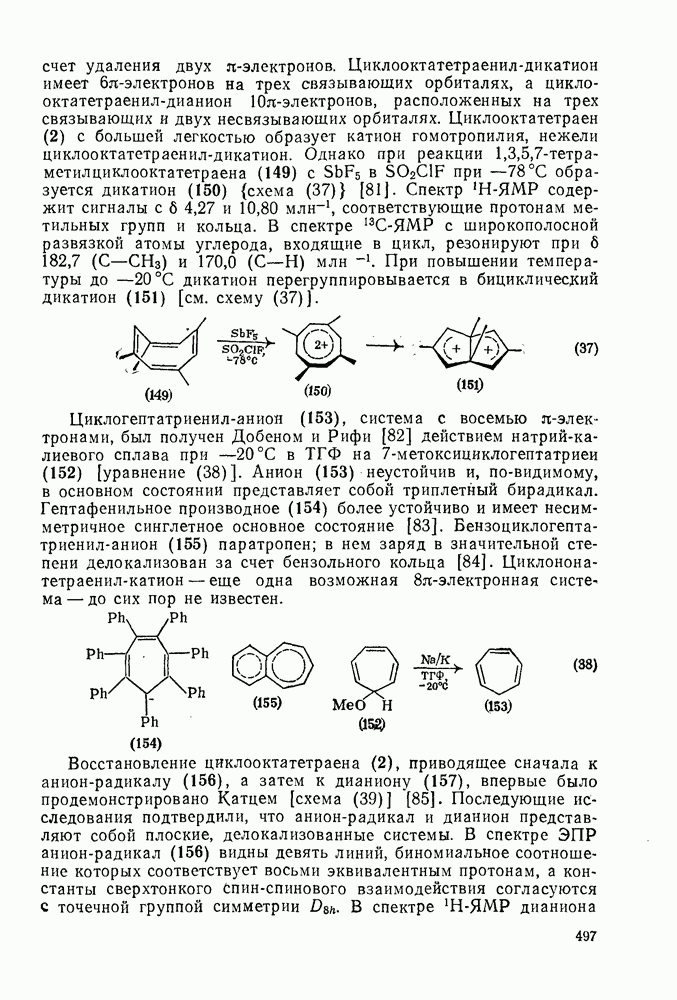
- 2.3.7. КУМУЛЕНЫ
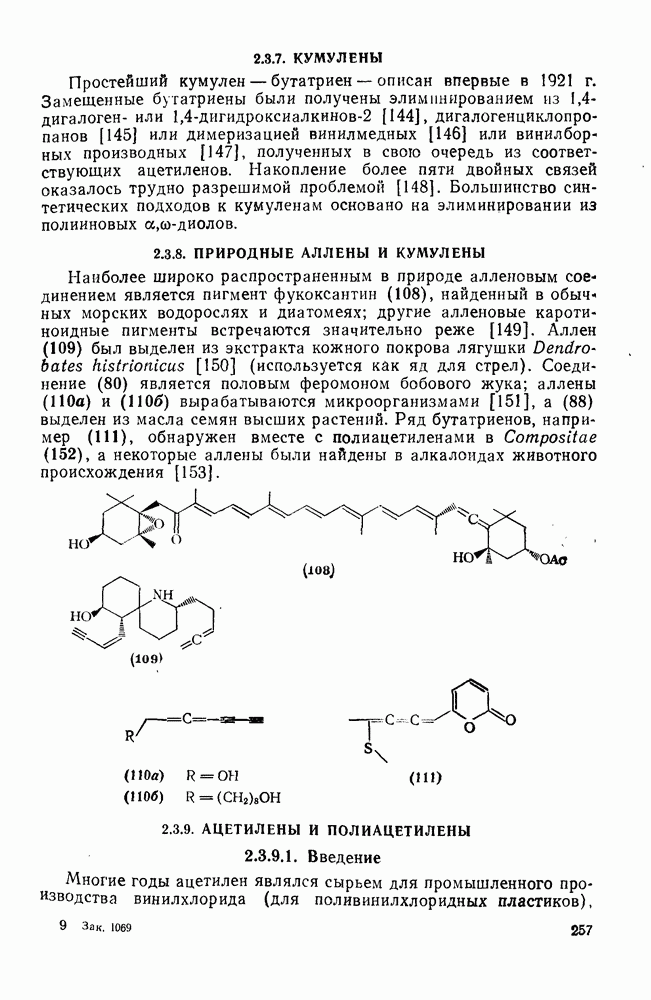
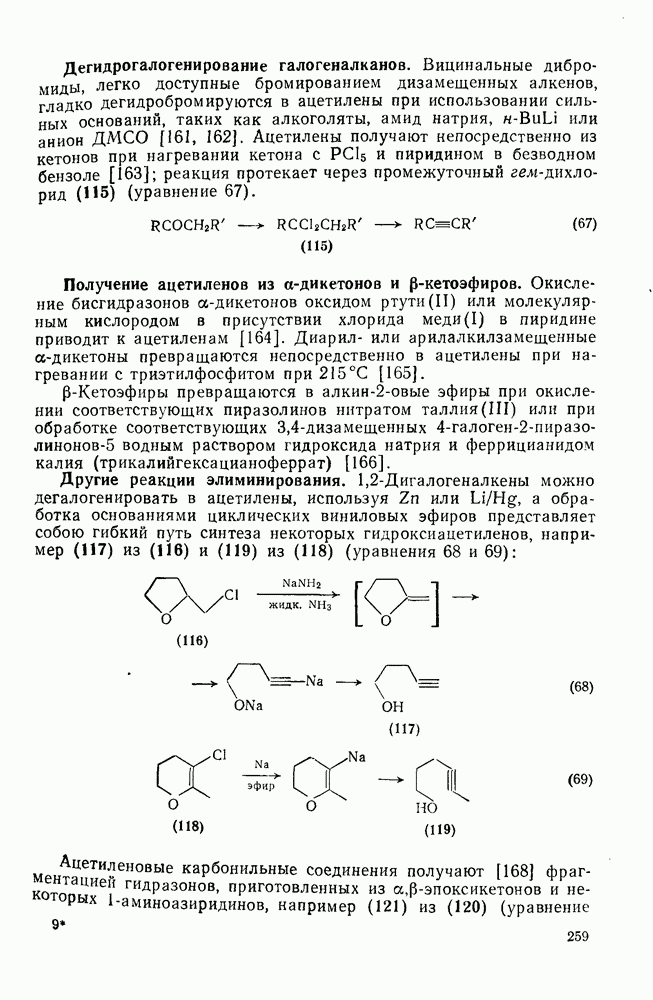
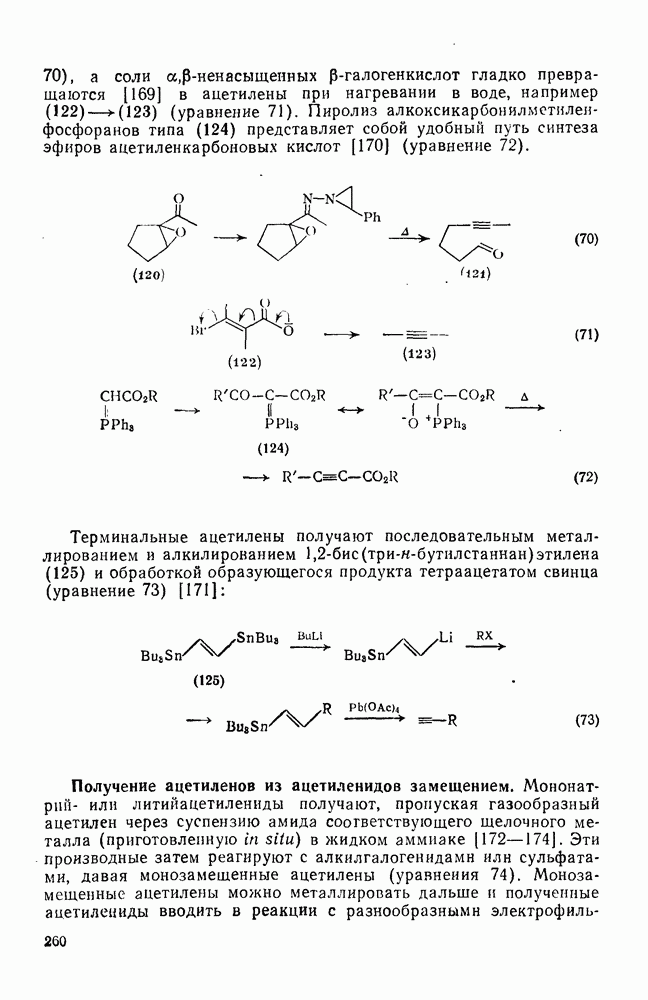
- 2.3.8. ПРИРОДНЫЕ АЛЛЕНЫ И КУМУЛЕНЫ
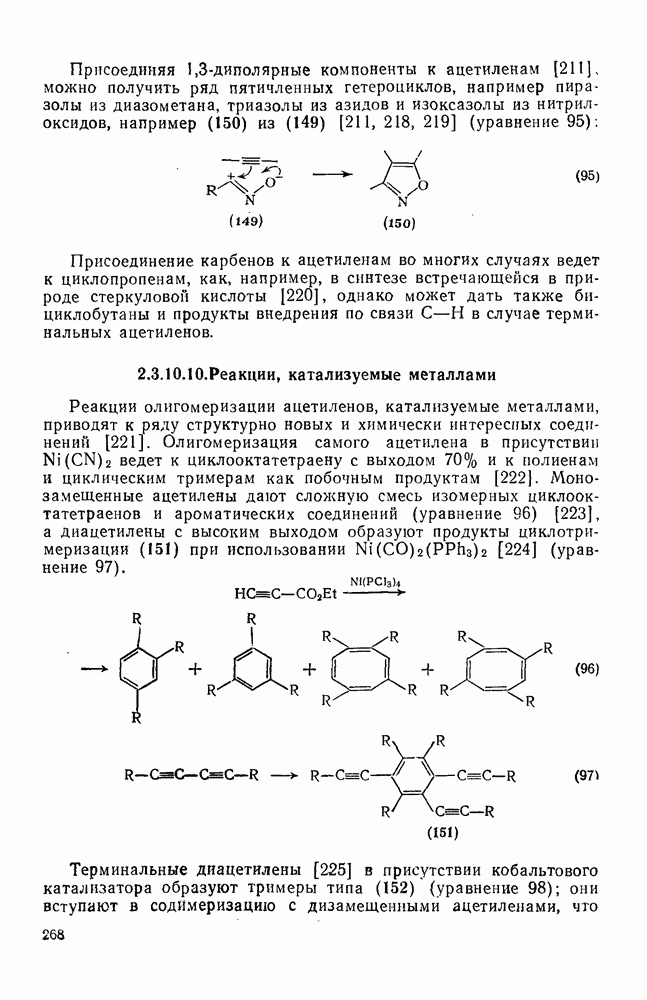
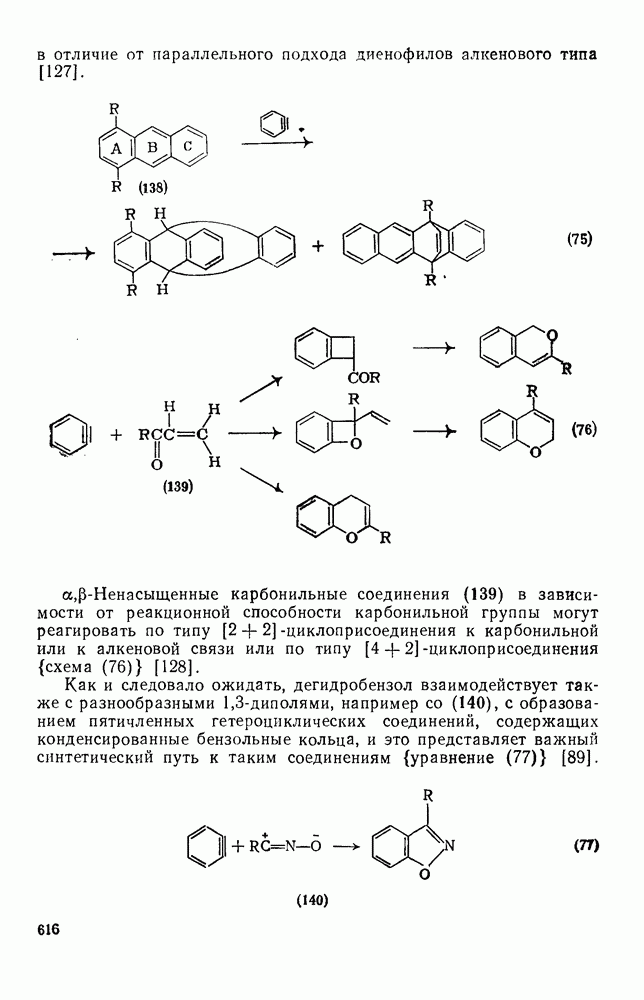
- 2.3.9. АЦЕТИЛЕНЫ И ПОЛИАЦЕТИЛЕНЫ
- 2.3.9.2. Получение ацетиленов
- 2.3.10. РЕАКЦИИ АЦЕТИЛЕНОВ
- 2.3.10.2. Изомеризация
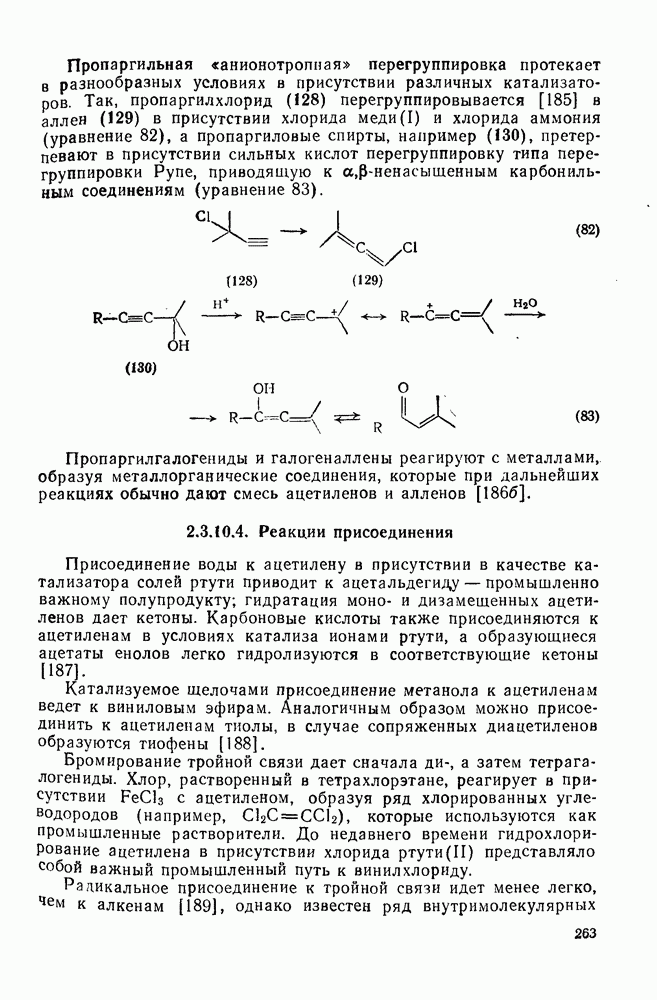
- 2.3.10.3. Пропаргильные перегруппировки
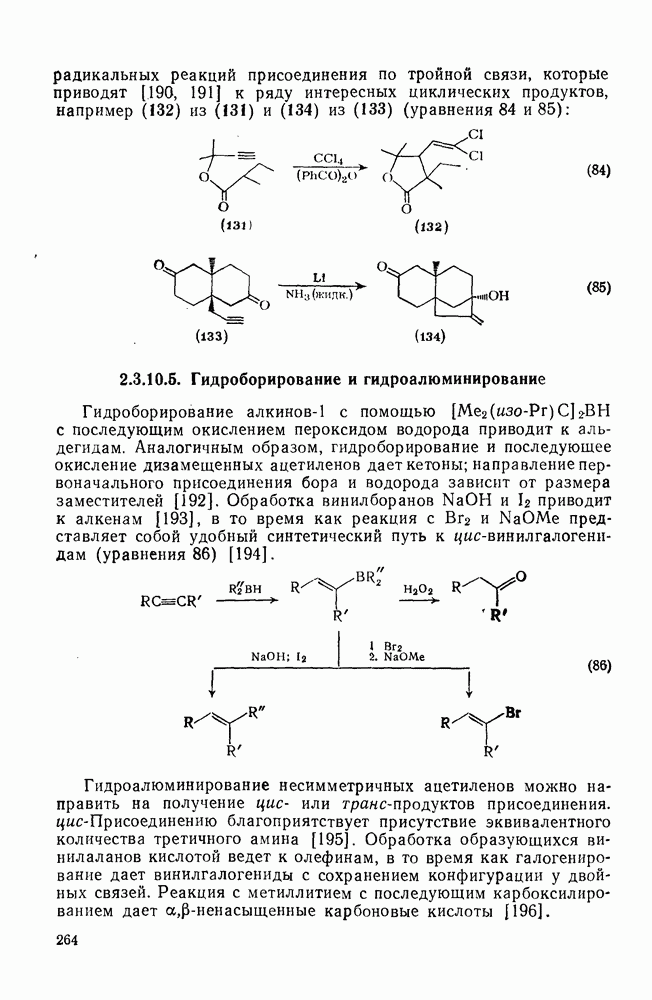
- 2.3.10.4. Реакции присоединения
- 2.3.10.5. Гидроборирование и гидроалюминирование
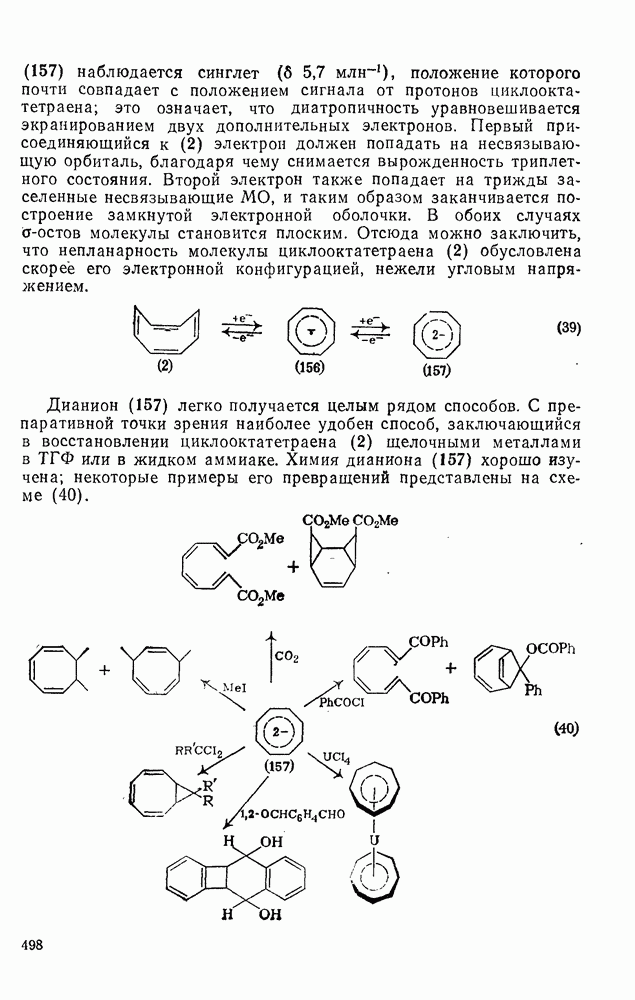
- 2.3.10.6. Реакции замещения
- 2.3.10.7. Восстановление
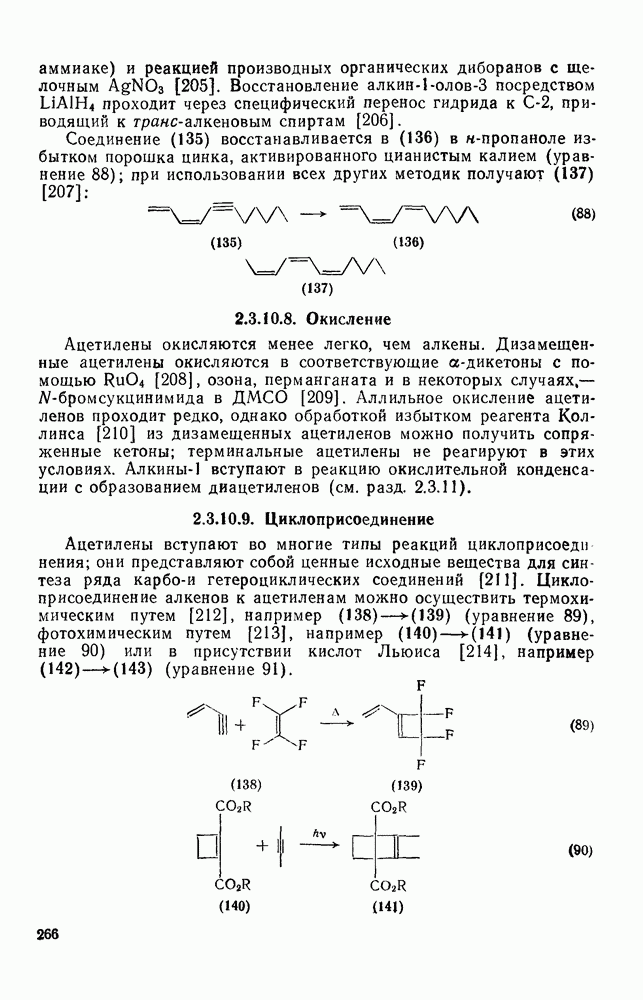
- 2.3.10.8. Окисление
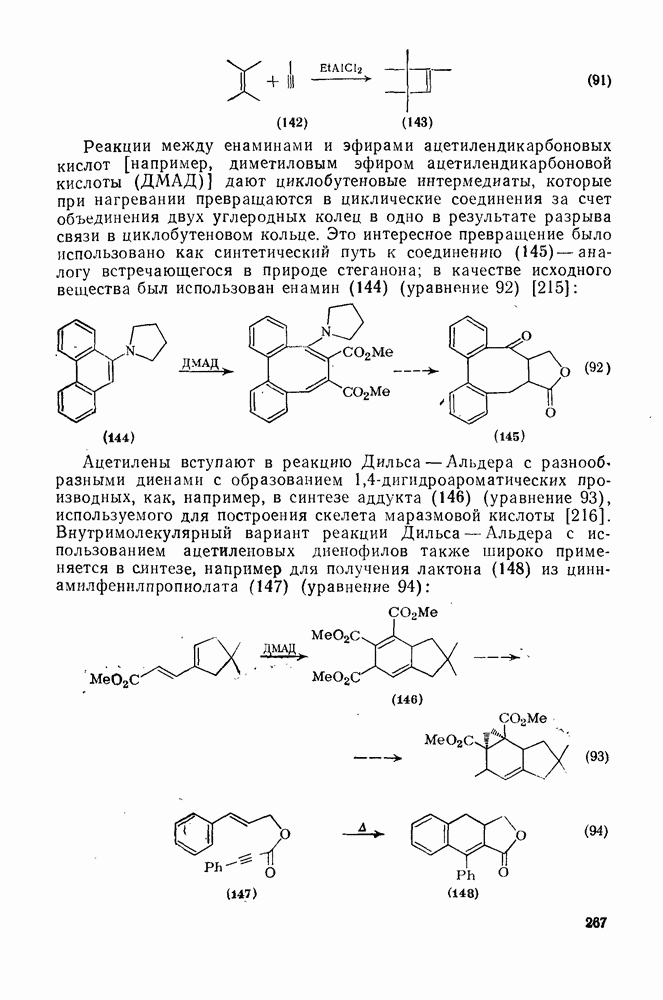
- 2.3.10.9. Циклоприсоединение
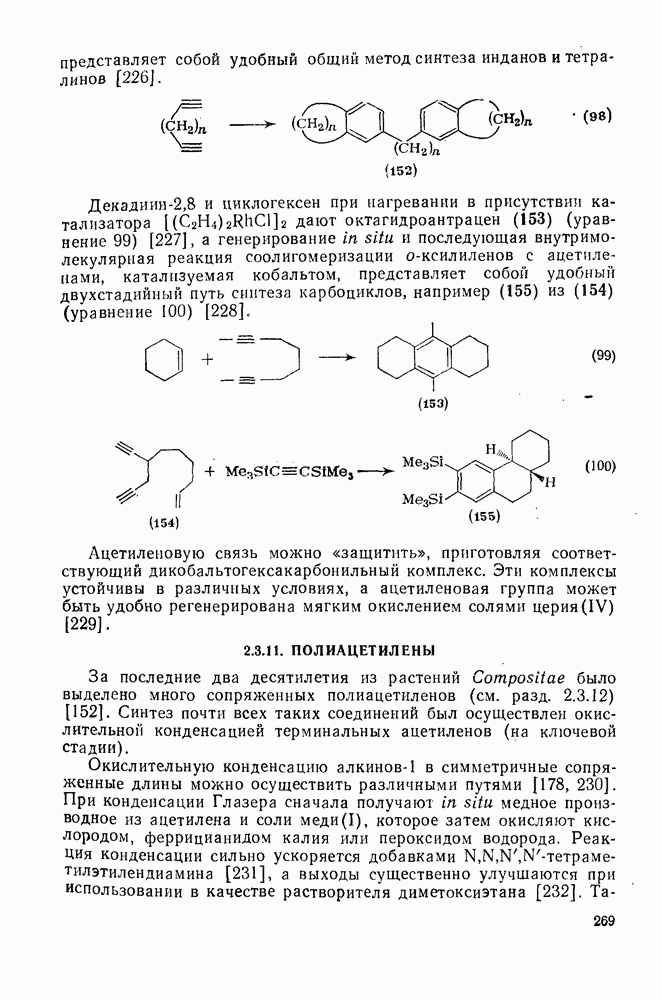
- 2.3.10.10. Реакции катализуемые металлами
- 2.3.11. ПОЛИАЦЕТИЛЕНЫ
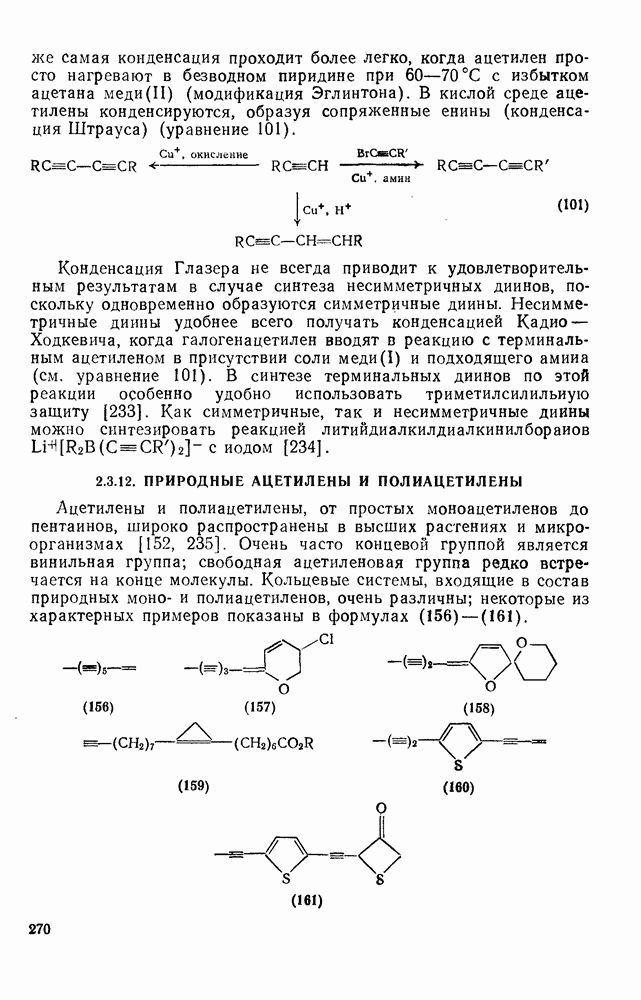
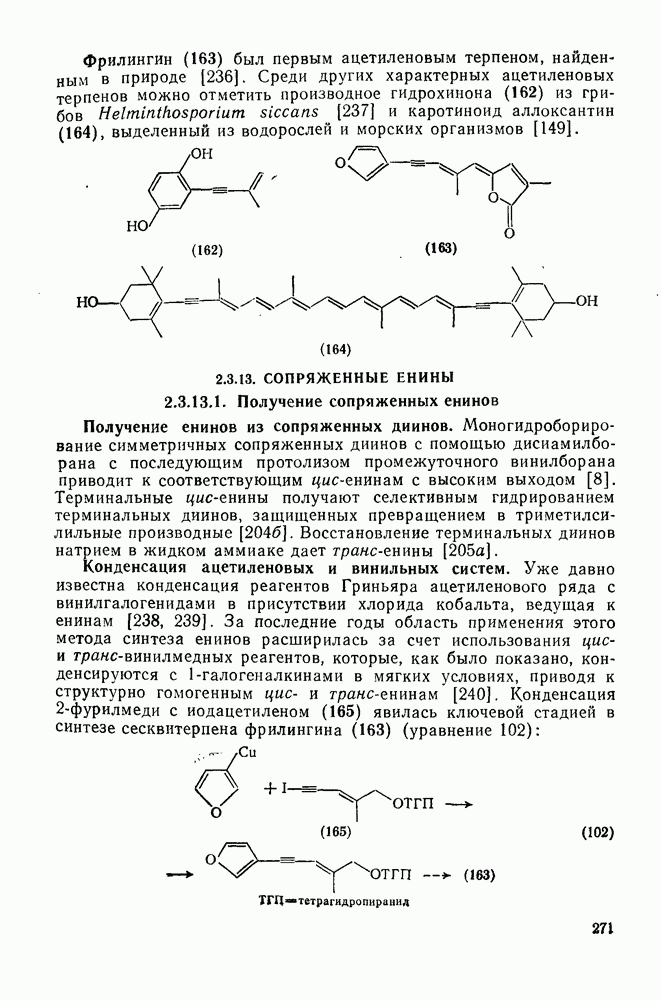
- 2.3.12. ПРИРОДНЫЕ АЦЕТИЛЕНЫ И ПОЛИАЦЕТИЛЕНЫ
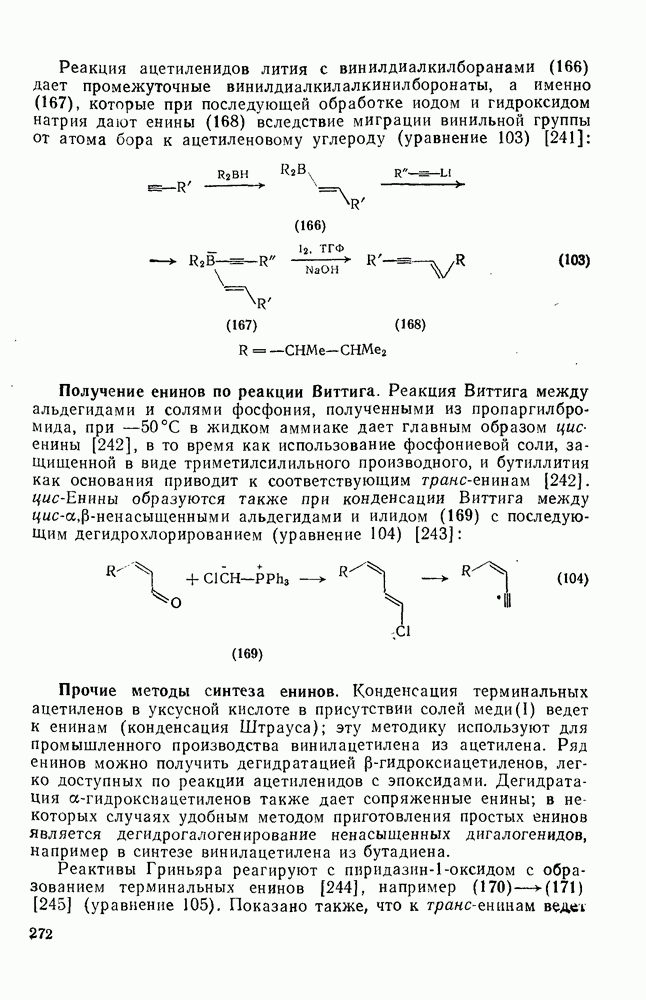
- 2.3.13. СОПРЯЖЕННЫЕ ЕНИНЫ
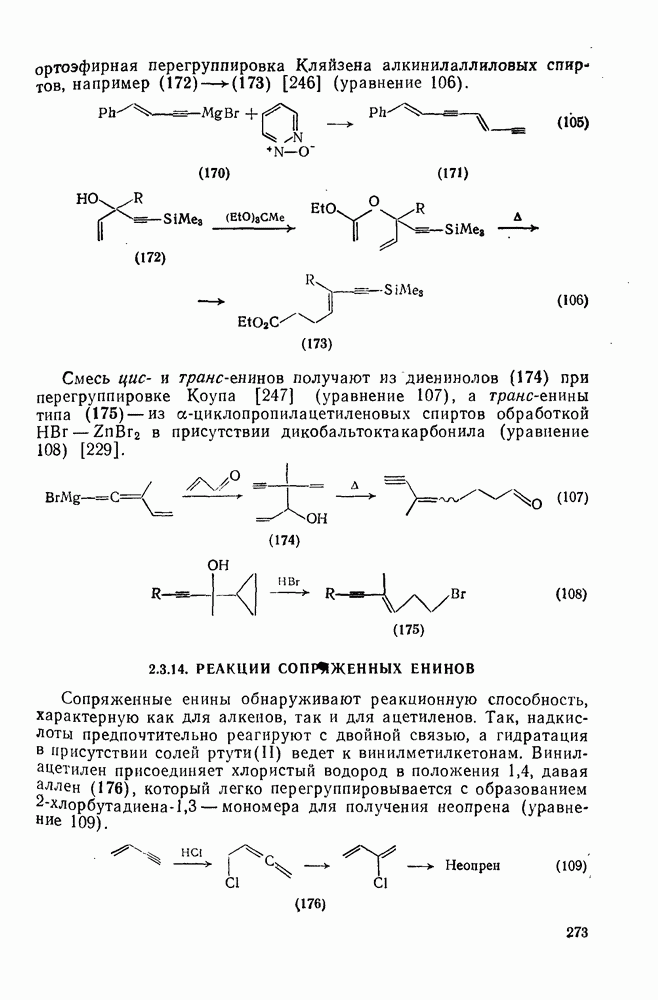
- 2.3.13.1. Получение сопряженных енинов
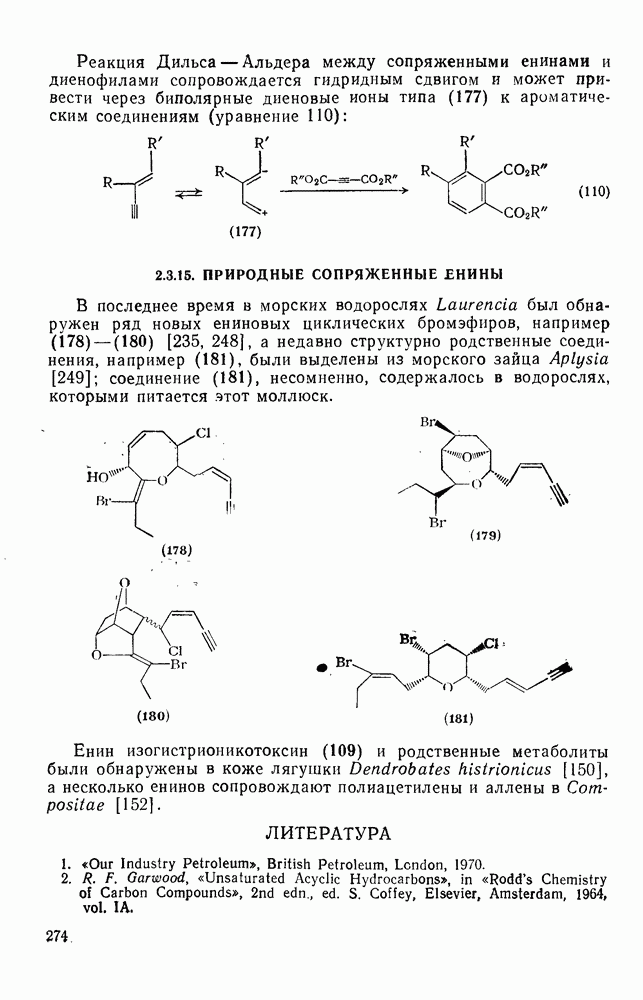
- 2.3.14. РЕАКЦИИ СОПРЯЖЕННЫХ ЕНИНОВ
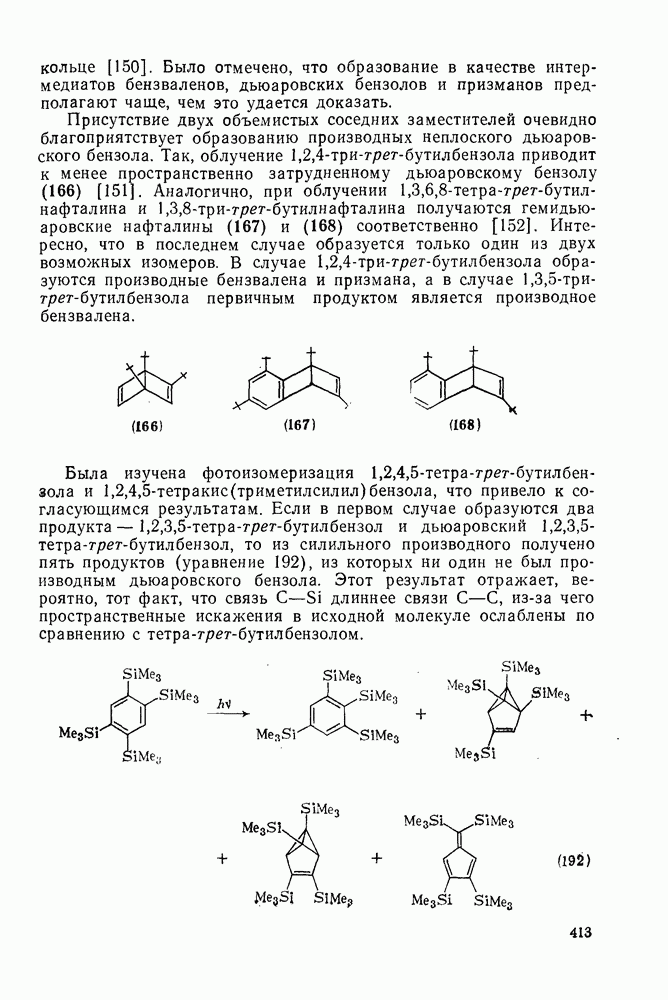
- 2.3.15. ПРИРОДНЫЕ СОПРЯЖЕННЫЕ ЕНИНЫ
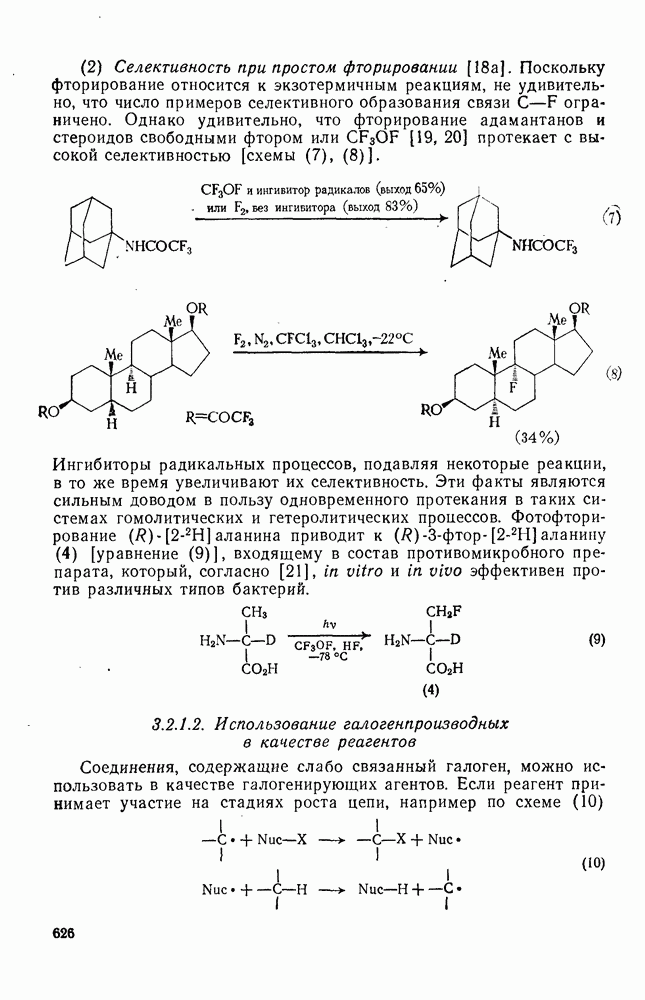
- 2.4. АРОМАТИЧНОСТЬ
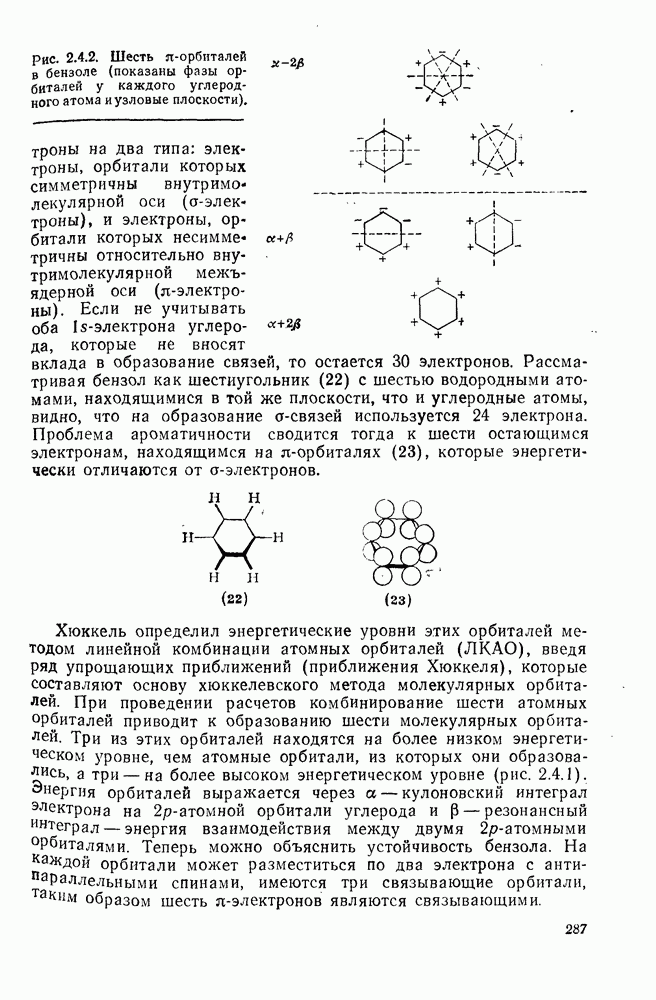
- 2.4.2. ЭЛЕКТРОННЫЕ ТЕОРИИ СТРОЕНИЯ БЕНЗОЛА
- 2.4.3. КРИТЕРИИ АРОМАТИЧНОСТИ
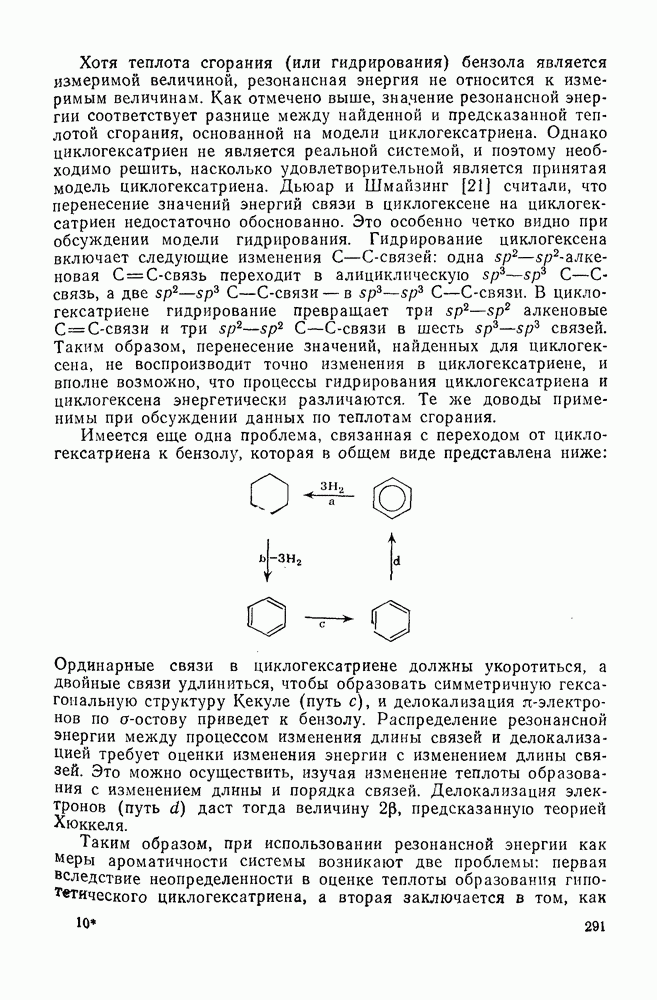
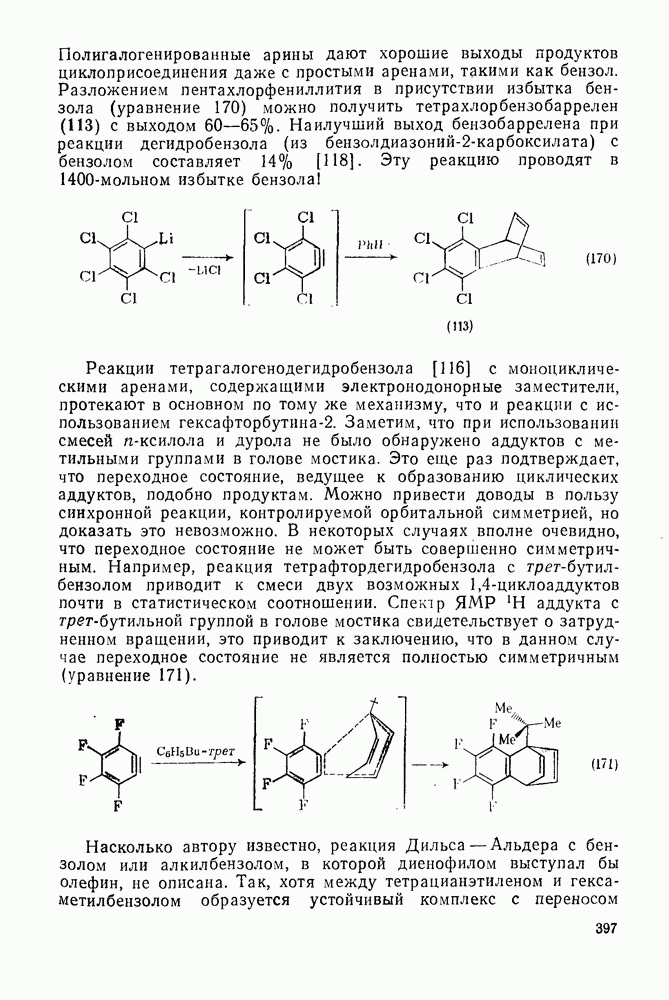
- 2.4.3.1. Термодинамические свойства
- 2.4.3.2. Структурные особенности
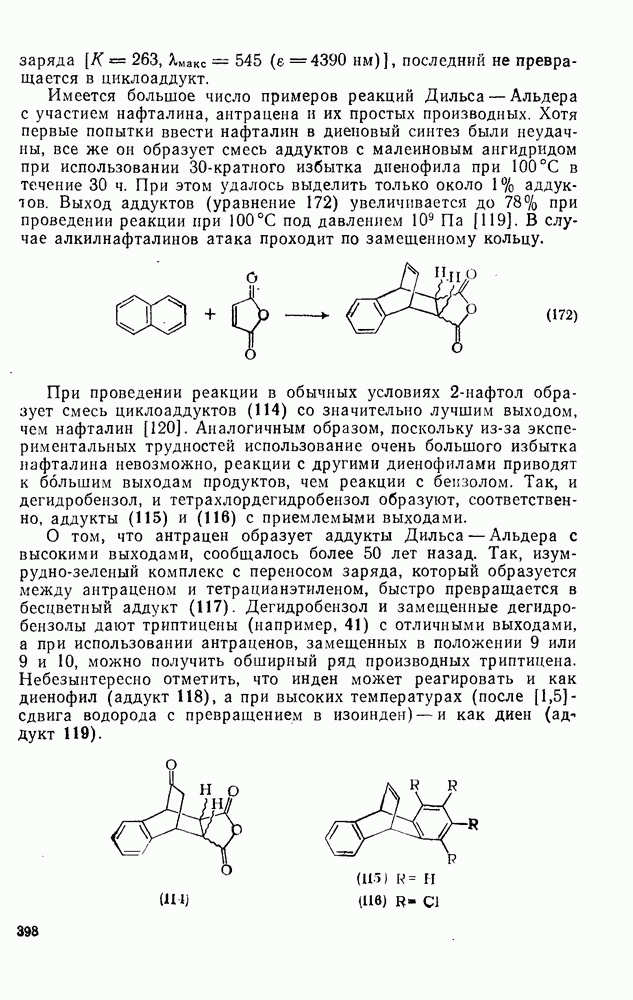
- 2.4.3.3. Магнитные свойства
- 2.4.3.4. Прочие критерии
- 2.4.4. АНТИАРОМАТИЧНОСТЬ
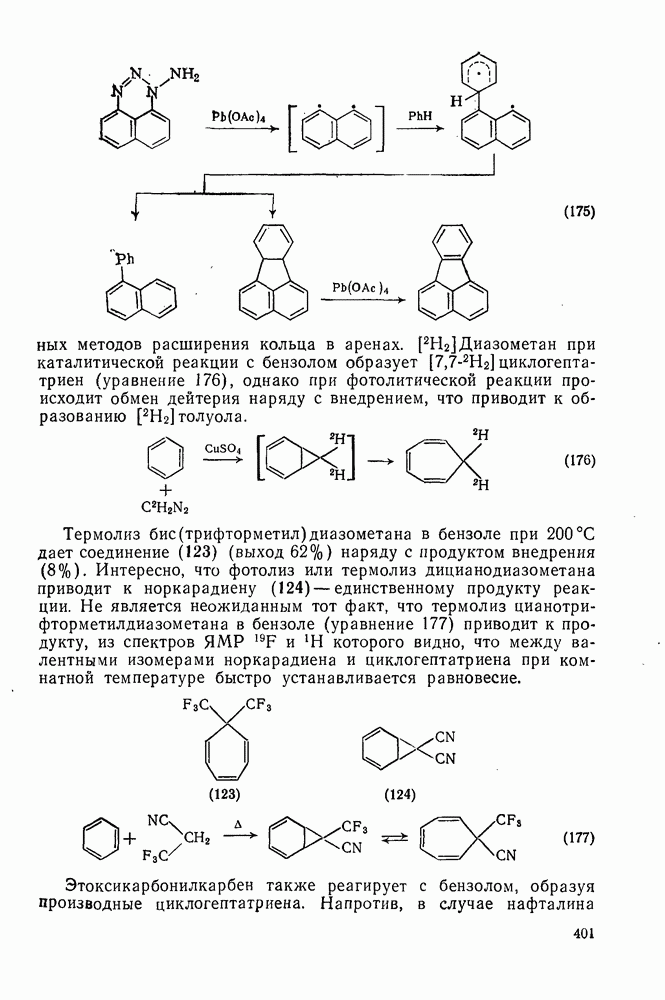
- 2.4.4.1. Термодинамические свойства
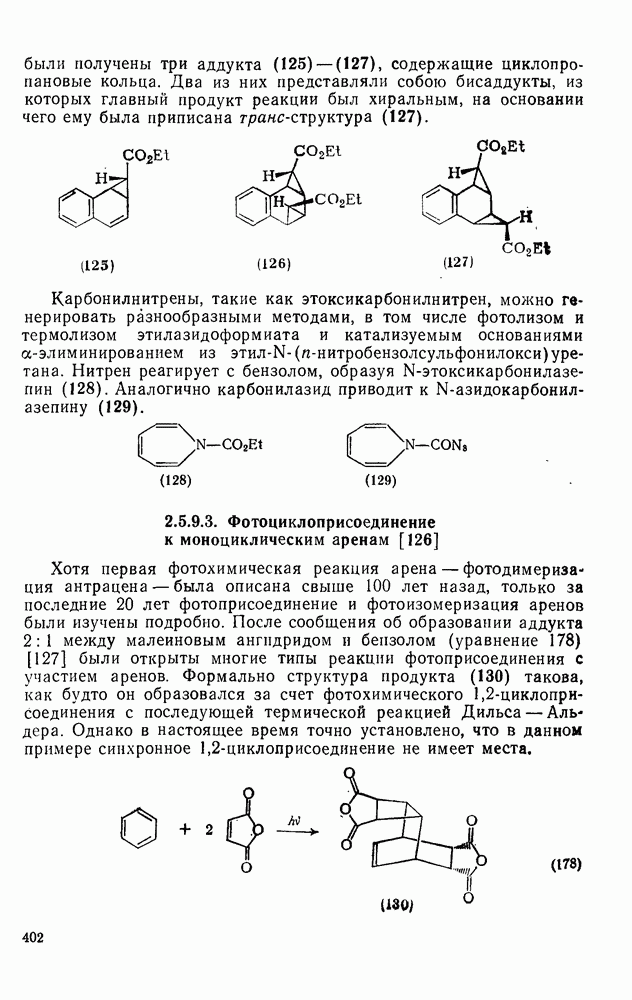
- 2.4.4.2. Структурные особенности
- 2.4.4.3. Магнитные свойства
- 2.4.4.4. Прочие свойства
- 2.4.5. ТЕОРЕТИЧЕСКИЕ ОПРЕДЕЛЕНИЯ АРОМАТИЧНОСТИ
- 2.4.5.1. Полуэмпирические расчеты и дьюаровская резонансная энергия
- 2.4.5.2. Расчеты по методу валентных пар и применение резонансного метода
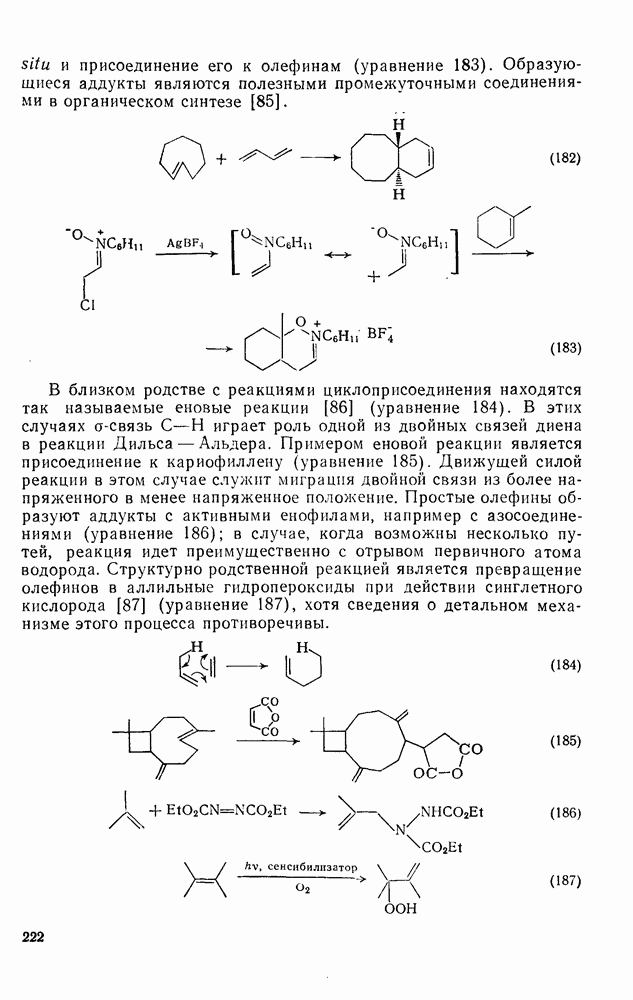
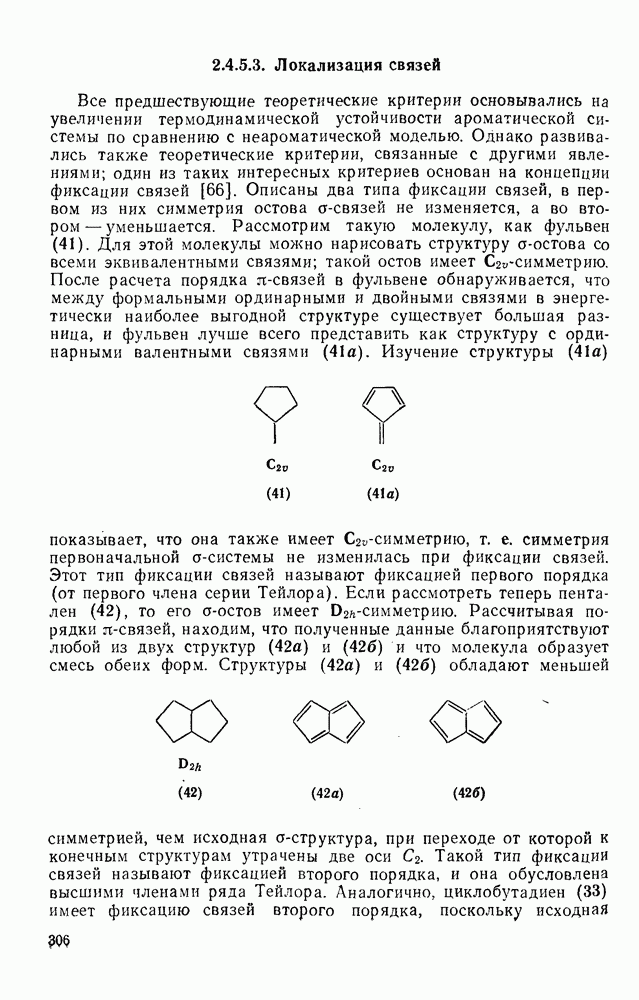
- 2.4.5.3. Локализация связей
- 2.4.5.4. Связь энергетических критериев с критериями локализации связей
- 2.4.6. АРОМАТИЧЕСКИЕ ПЕРЕХОДНЫЕ СОСТОЯНИЯ
- 2.5. АРЕНЫ И ИХ РЕАКЦИИ
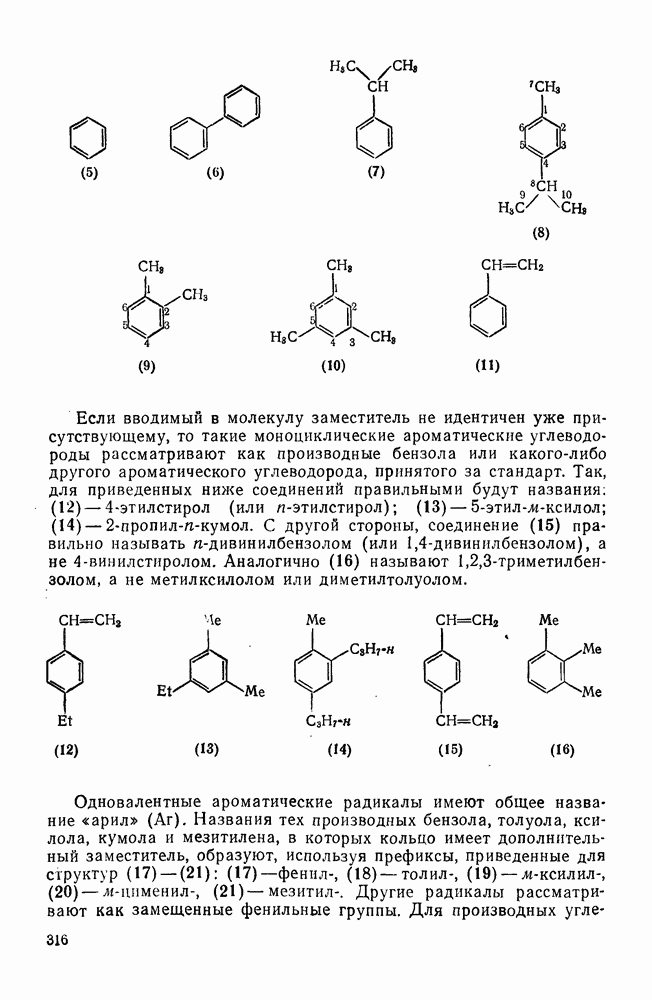
- 2.5.2. НОМЕНКЛАТУРА
- 2.5.3. ФИЗИЧЕСКИЕ СВОЙСТВА АРЕНОВ
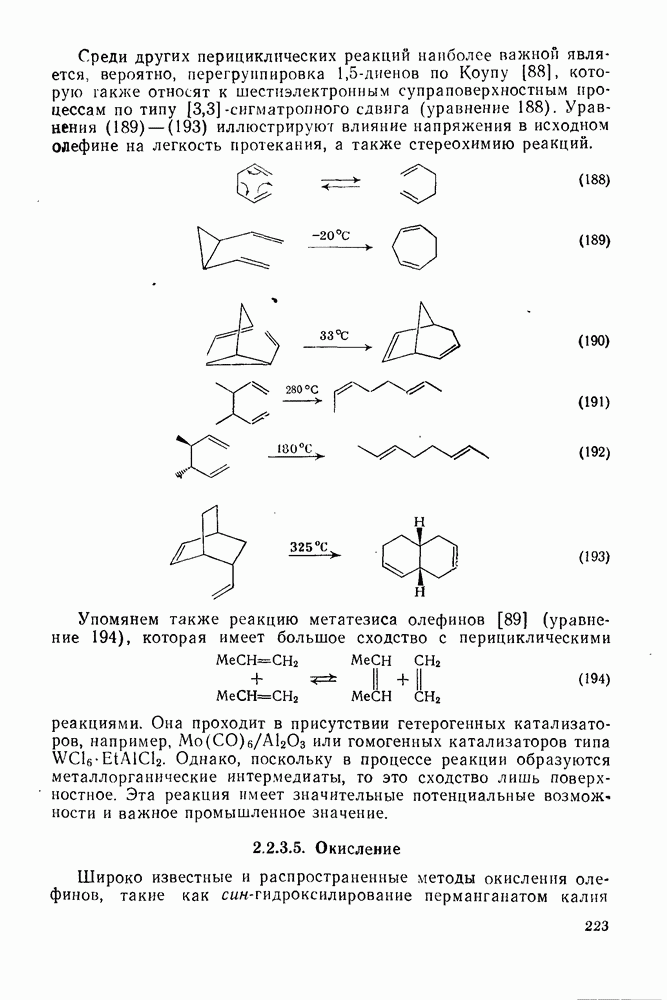
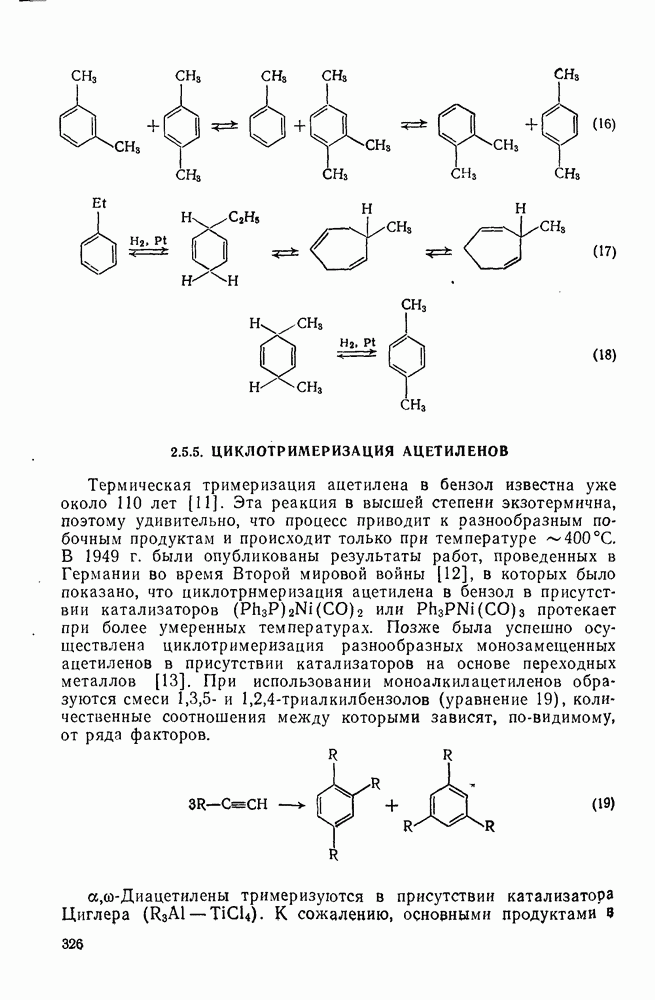
- 2.5.4. ПРОМЫШЛЕННОЕ ПРОИЗВОДСТВО АРЕНОВ
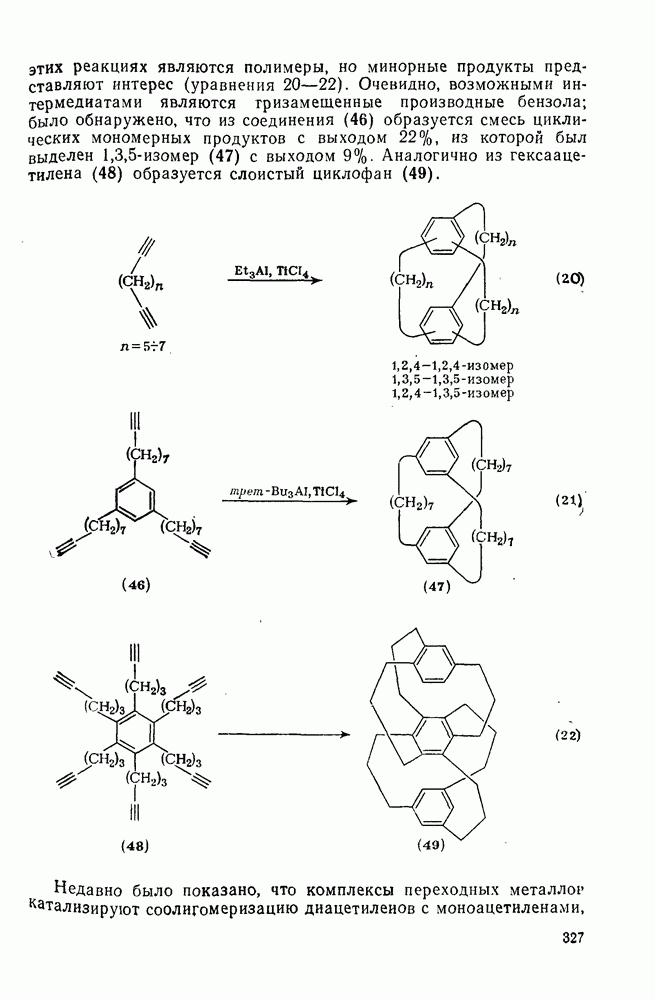
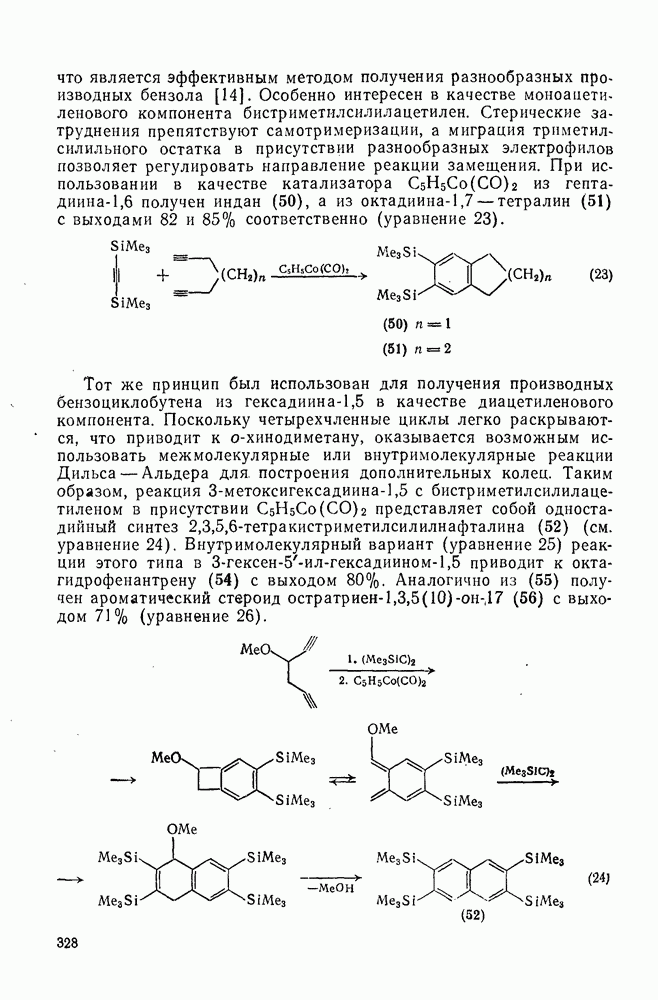
- 2.5.5. ЦИКЛОТРИМЕРИЗАЦИЯ АЦЕТИЛЕНОВ
- 2.5.6. РЕАКЦИИ ЭЛЕКТРОФИЛЬНОГО ПРИСОЕДИНЕНИЯ — ЭЛИМИНИРОВАНИЯ АРЕНОВ
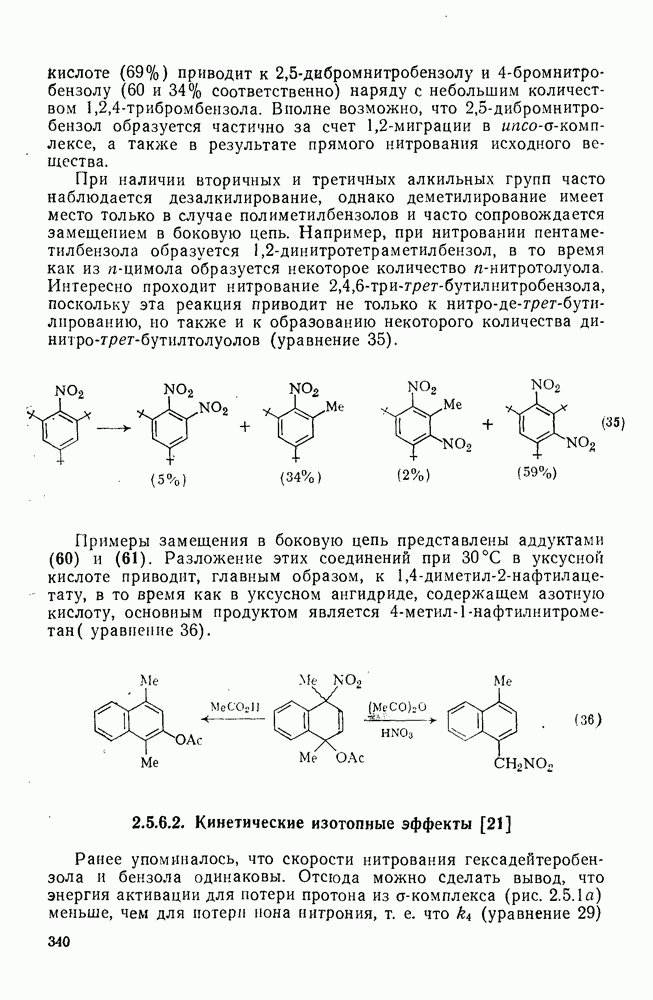
- 2.5.6.1. Механизм ароматического нитрования [15]
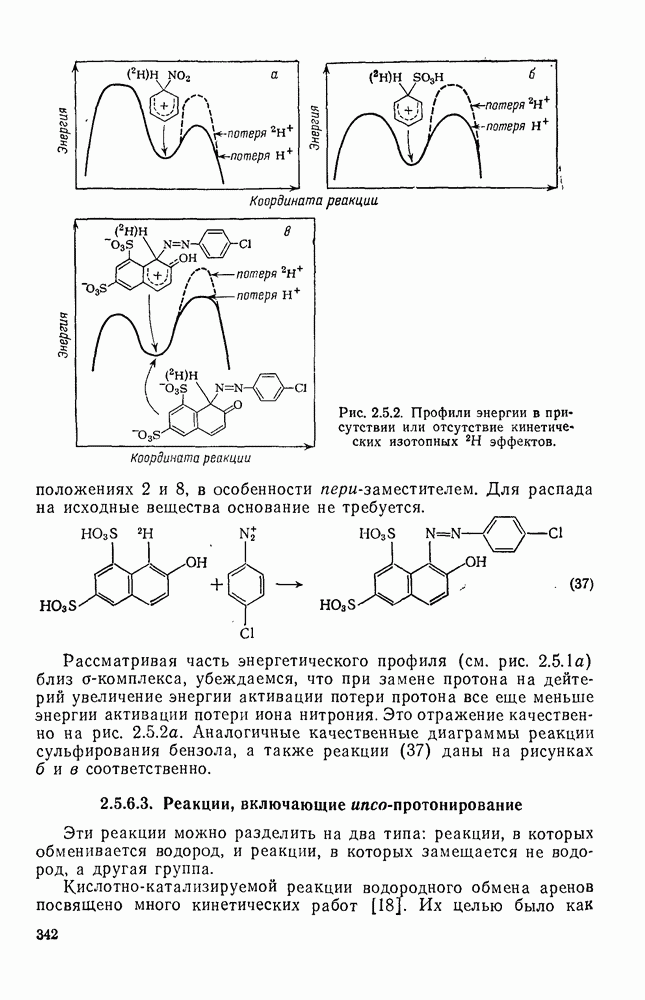
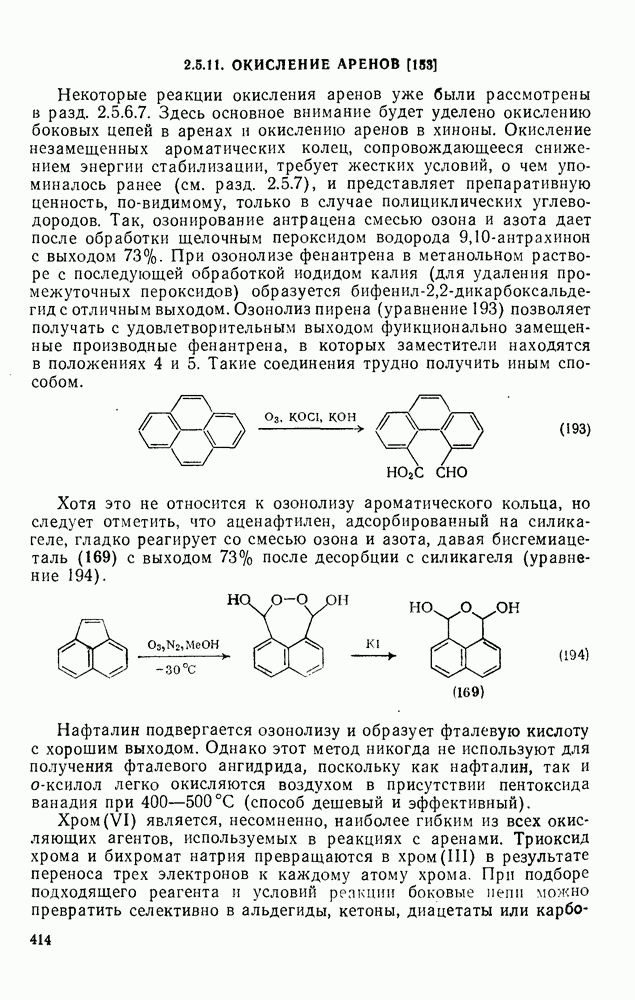
- 2.5.6.2. Кинетические изотопные эффекты [21]
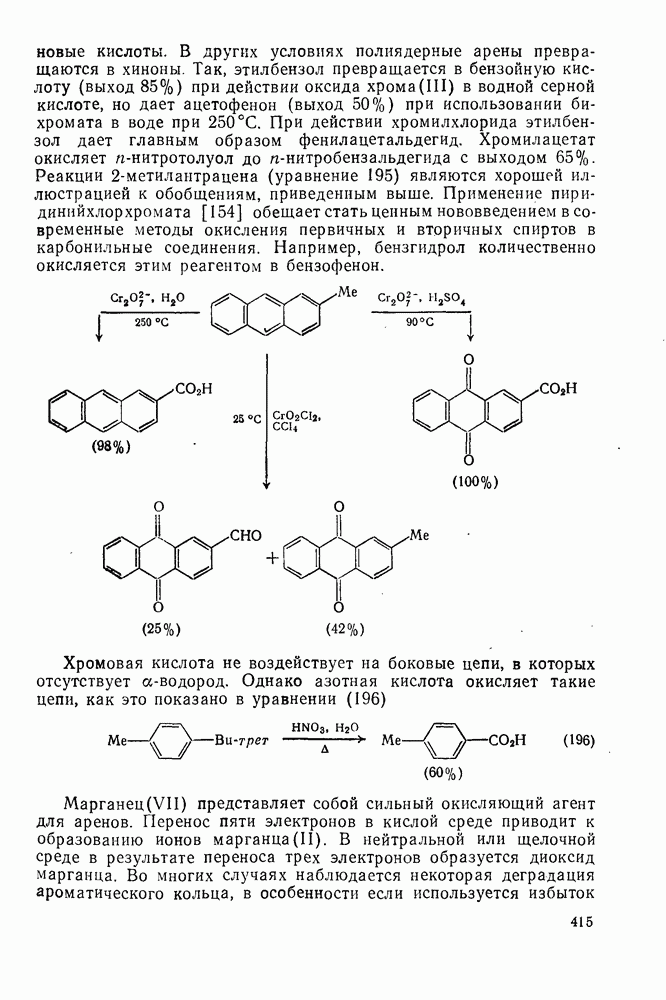
- 2.5.6.3. Реакции, включающие ипсо-протонирование
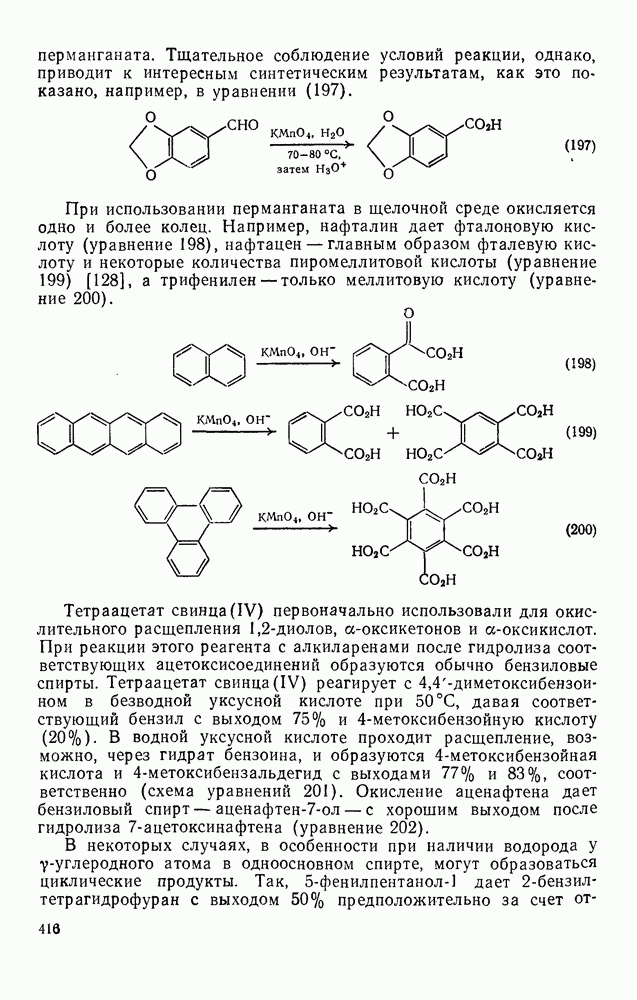
- 2.5.6.4. Металлирование
- 2.5.6.5. Электрофилы IV группы
- 2.5.6.6. Электрофилы V группы
- 2.5.6.7. Электрофилы VI группы [18, 56]
- 2.5.6.8. Электрофилы VII группы [18, 25а, 56]
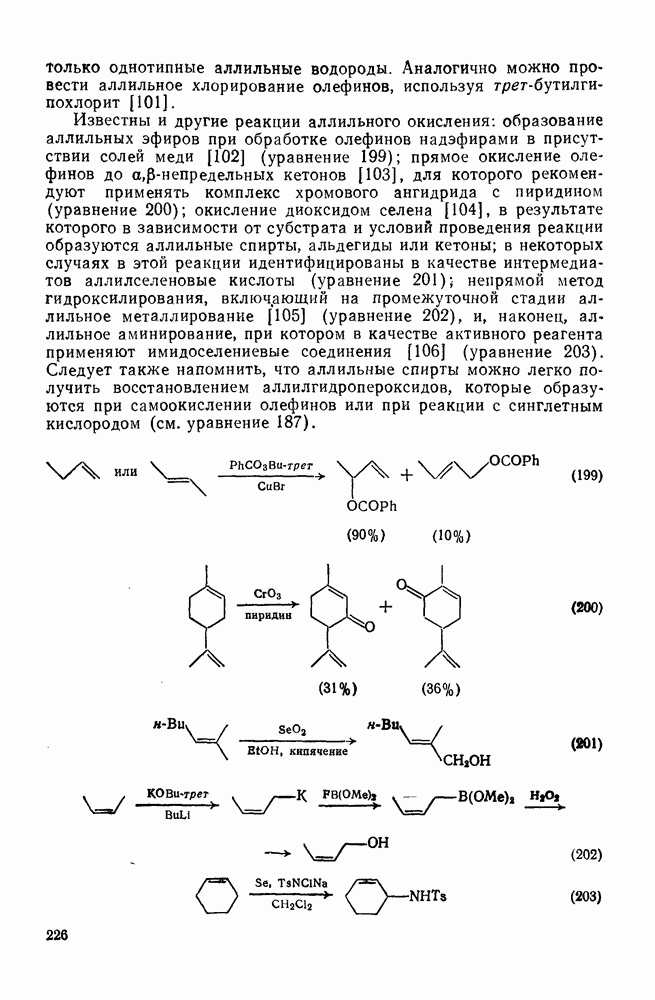
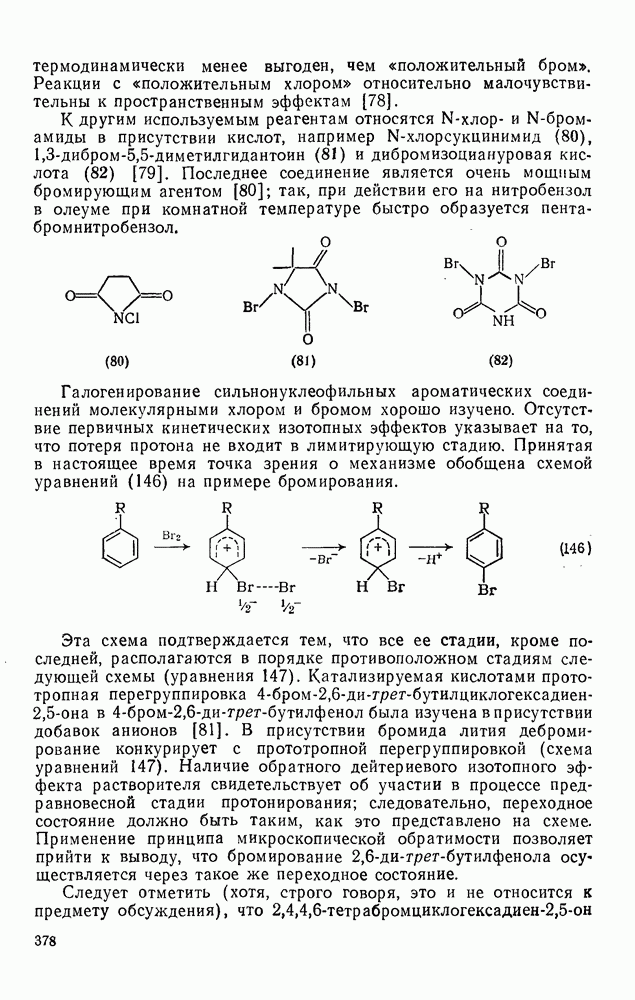
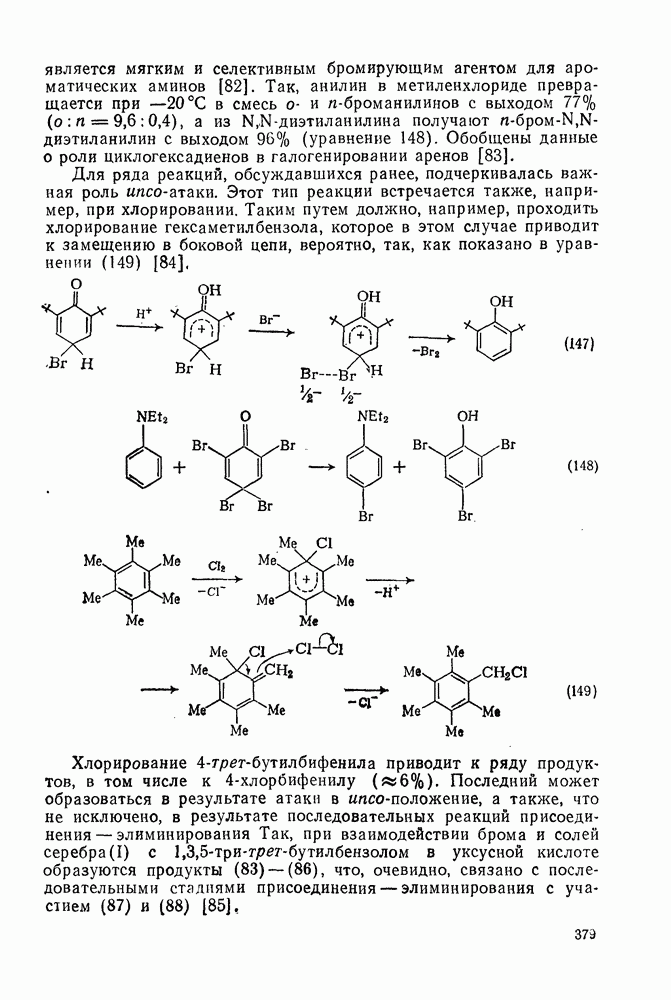
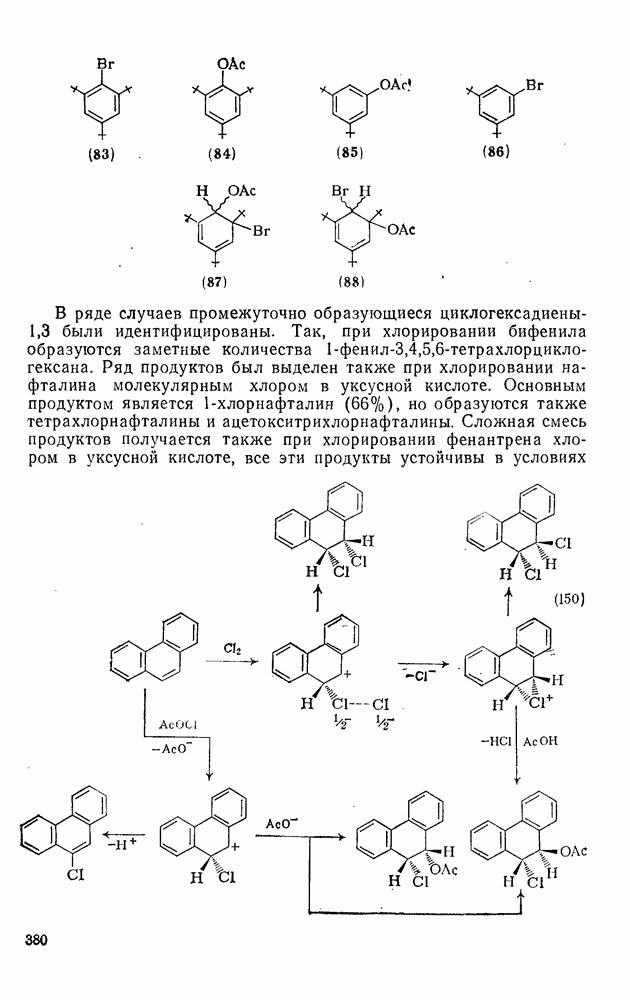
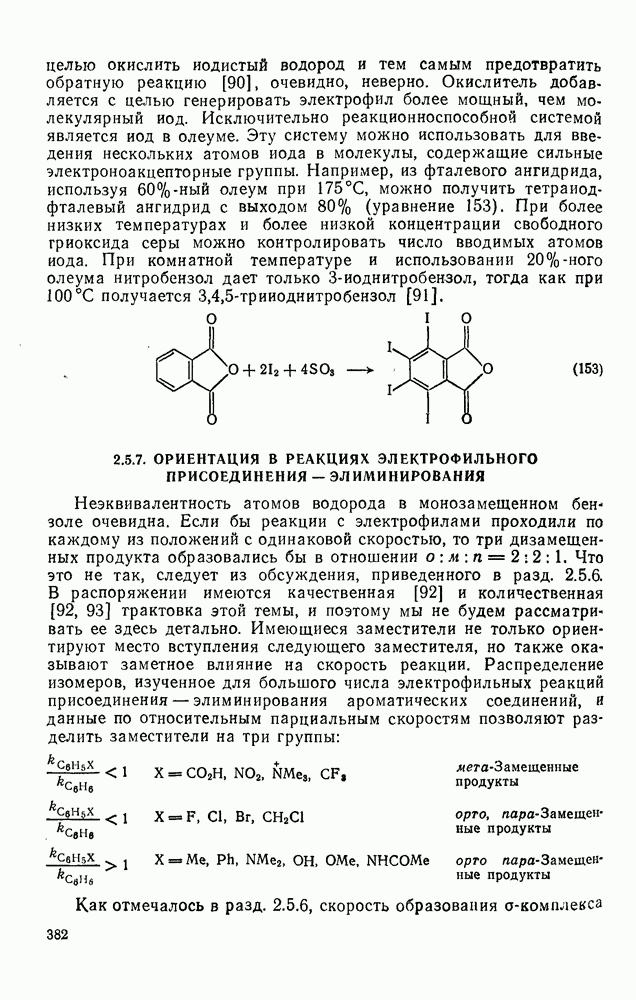
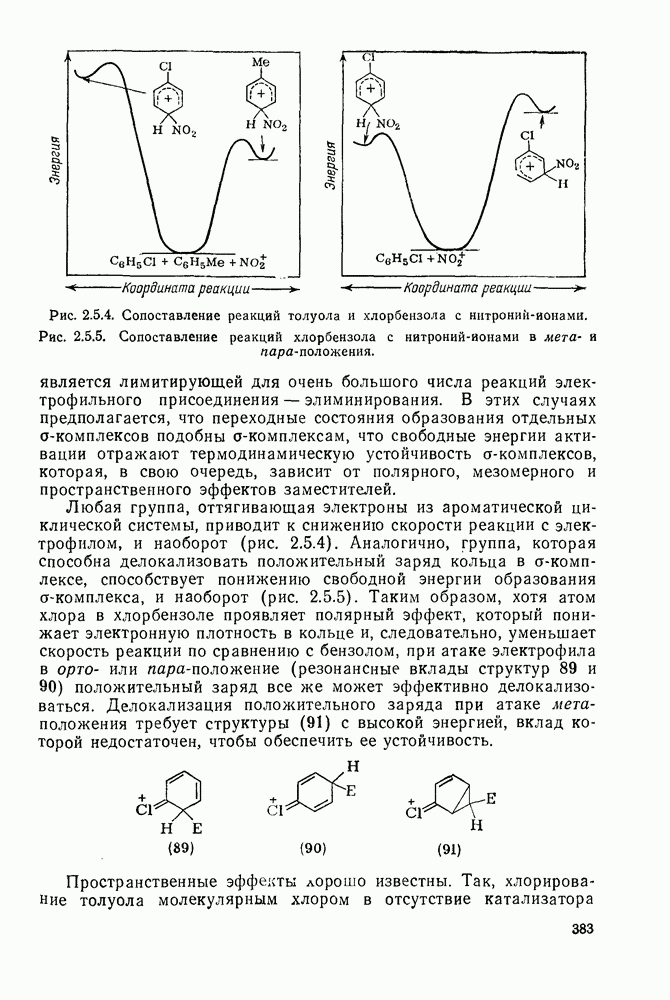
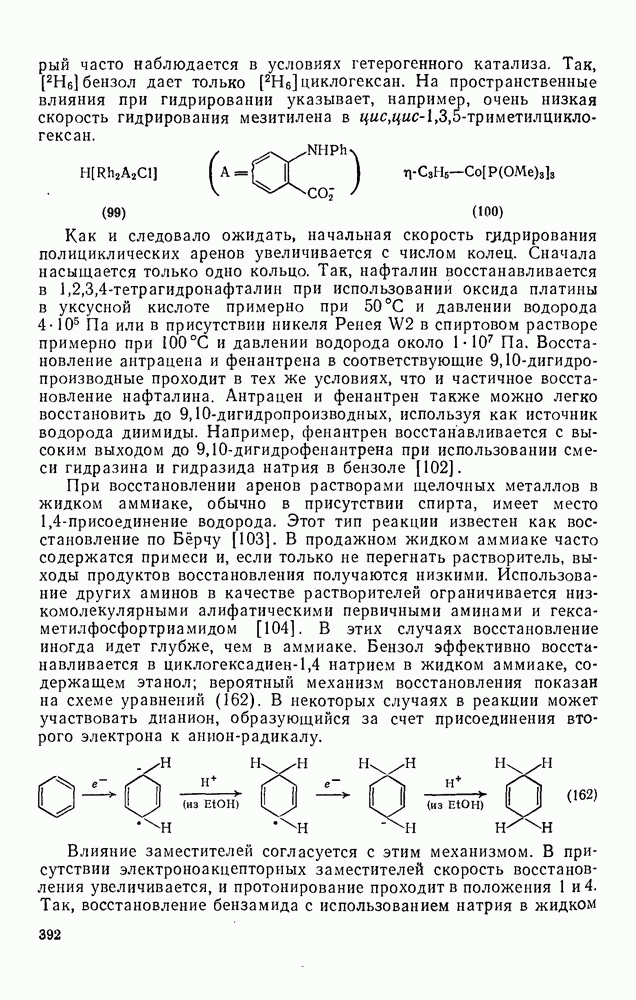
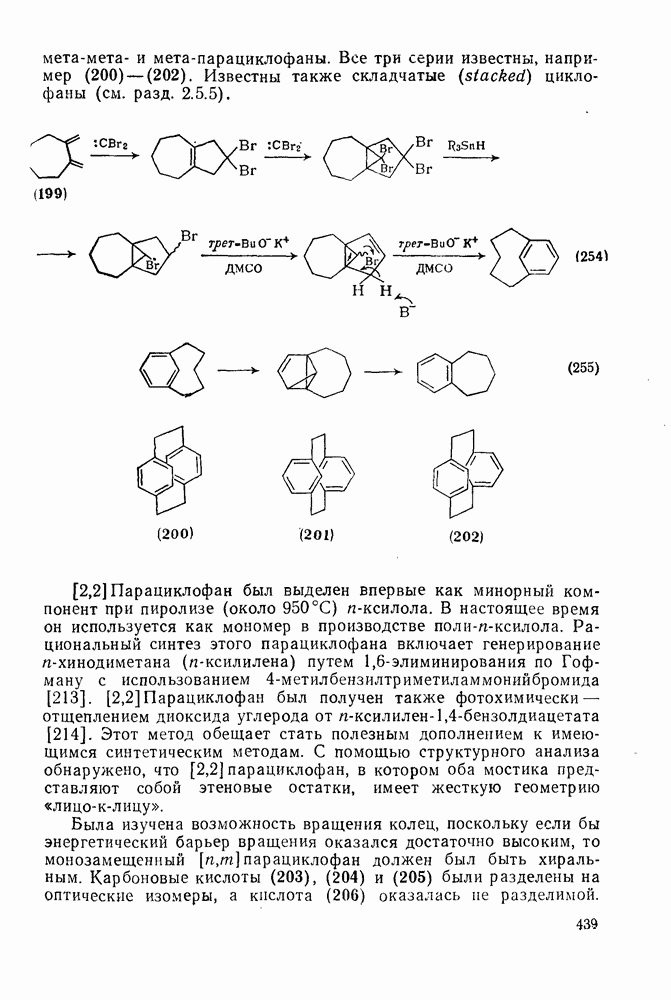
- 2.5.7. ОРИЕНТАЦИЯ В РЕАКЦИЯХ ЭЛЕКТРОФИЛЬНОГО ПРИСОЕДИНЕНИЯ — ЭЛИМИНИРОВАНИЯ
- 2.5.8. РАДИКАЛЬНОЕ ГАЛОГЕНИРОВАНИЕ АРЕНОВ В БОКОВУЮ ЦЕПЬ [96]
- 2.5.9. РЕАКЦИИ ПРИСОЕДИНЕНИЯ К АРЕНАМ
- 2.5.9.1. Восстановление аренов
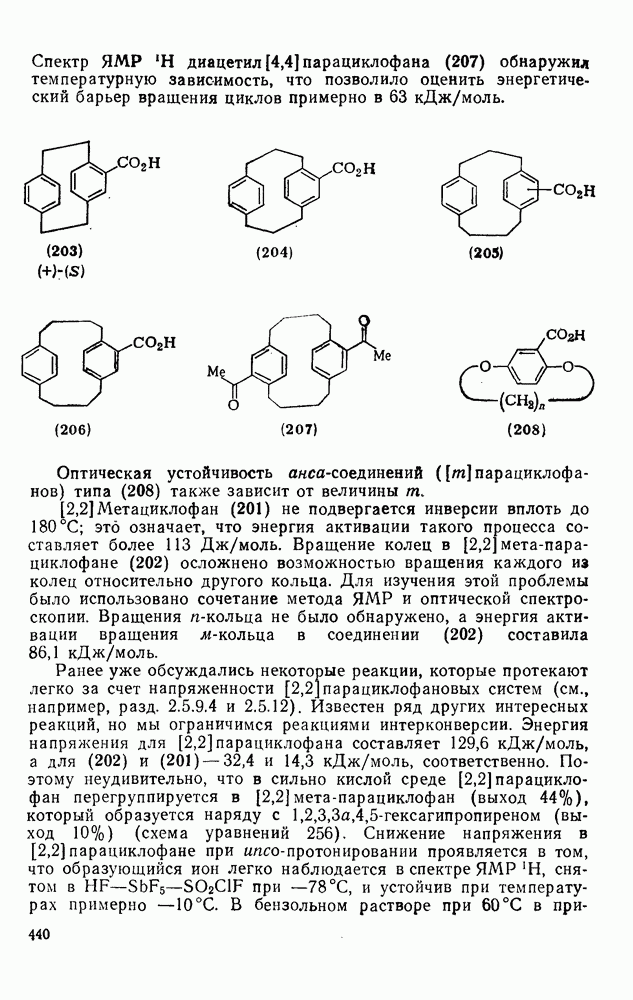
- 2.5.9.2. Термическое циклоприсоединение к аренам
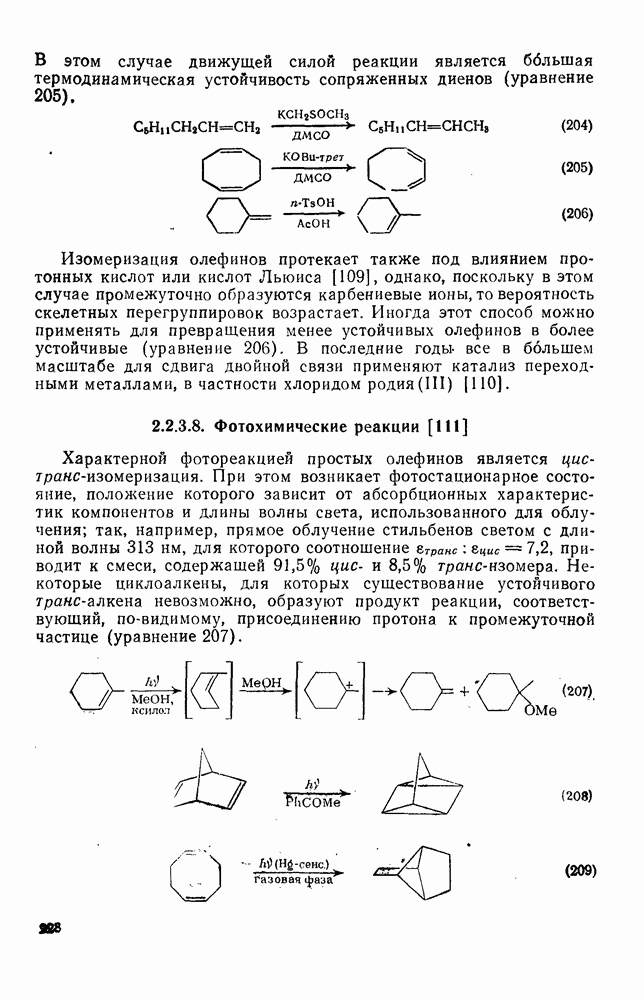
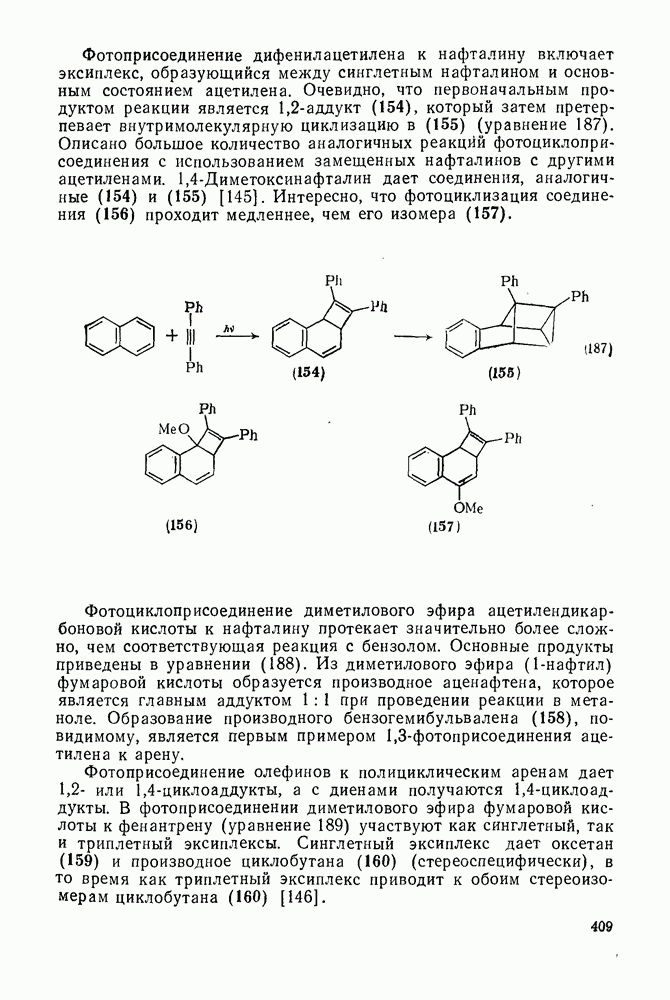
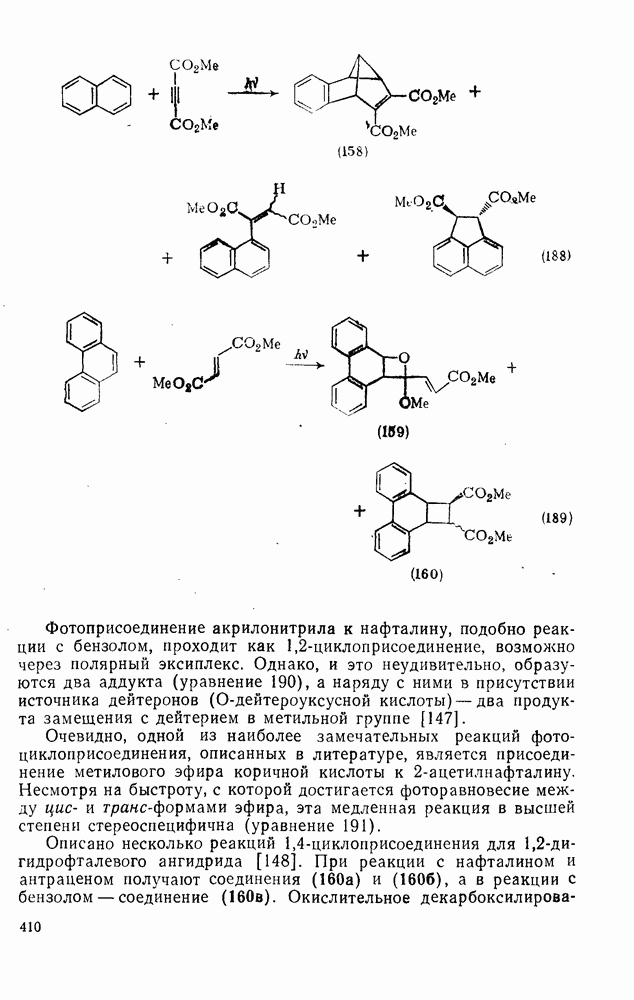
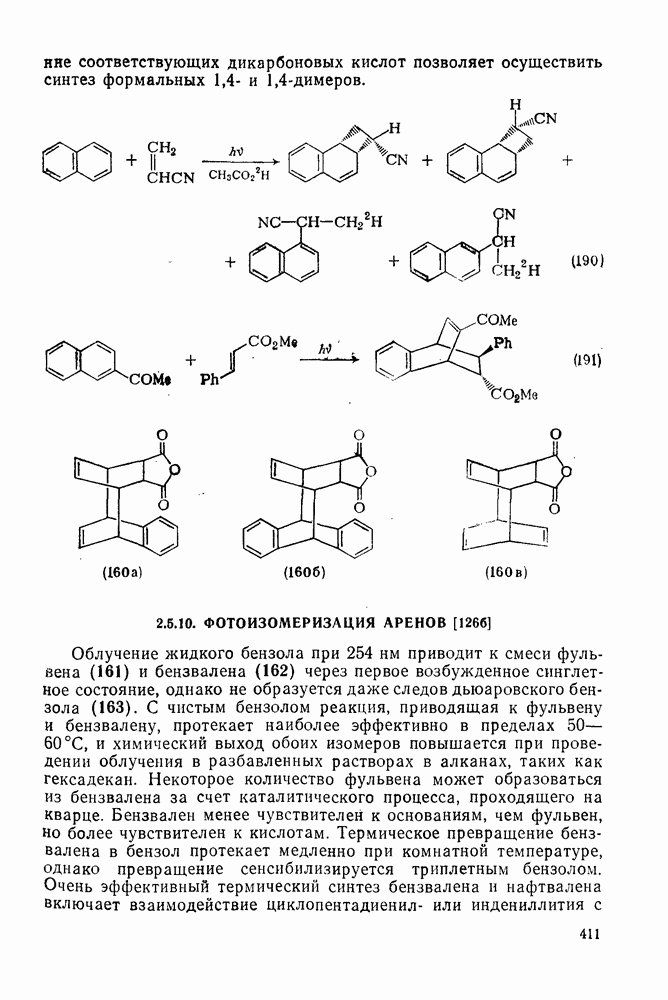
- 2.5.9.3. Фотоциклоприсоединение к моноциклическим аренам [126]
- 2.5.9.4. Фотохимические реакции полициклических аренов
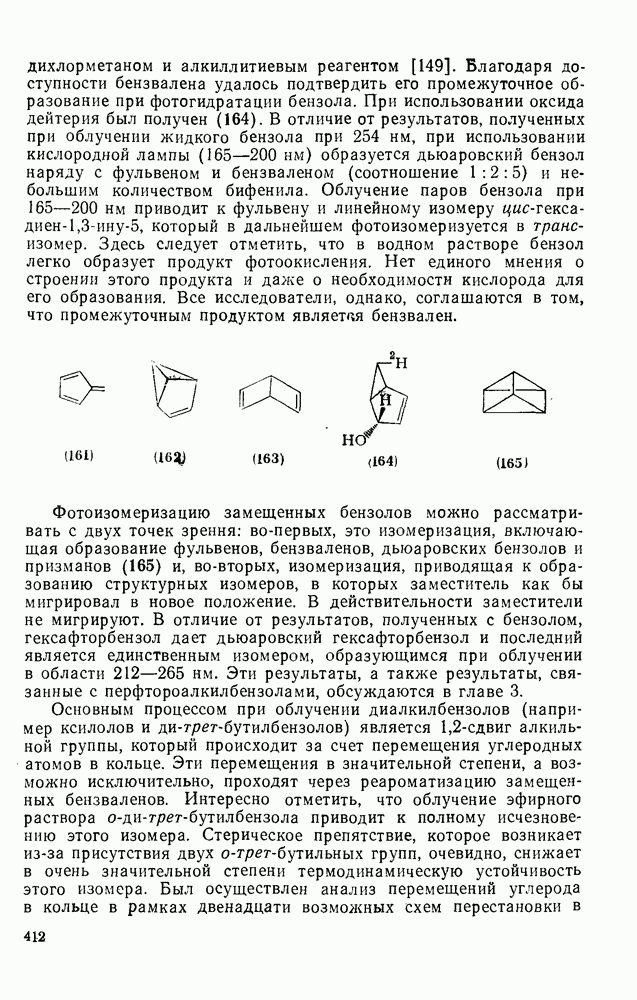
- 2.6.10. ФОТОИЗОМЕРИЗАЦИЯ АРЕНОВ [126б]
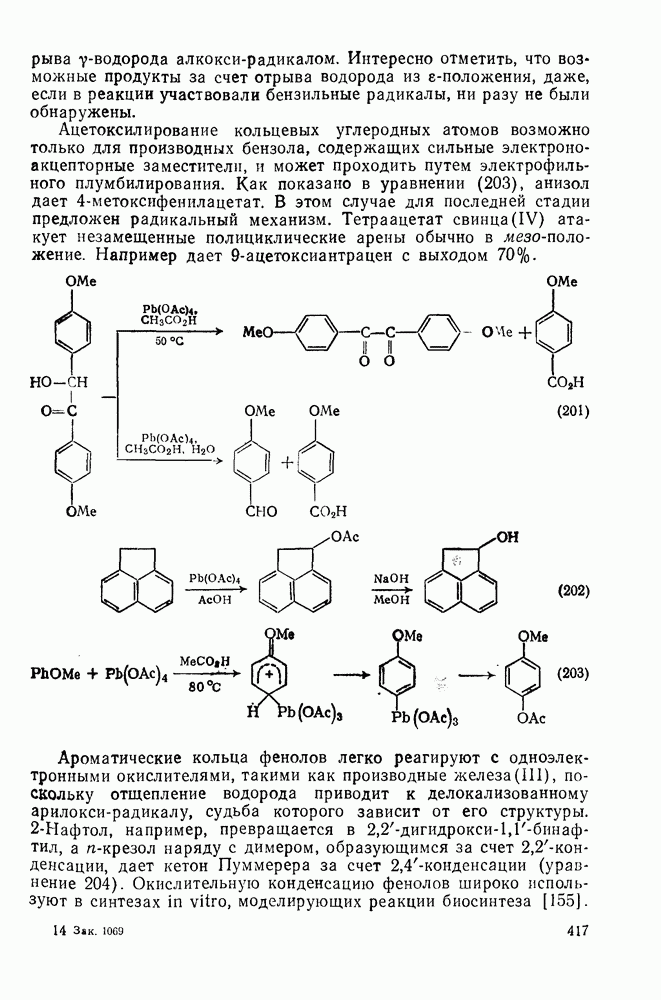
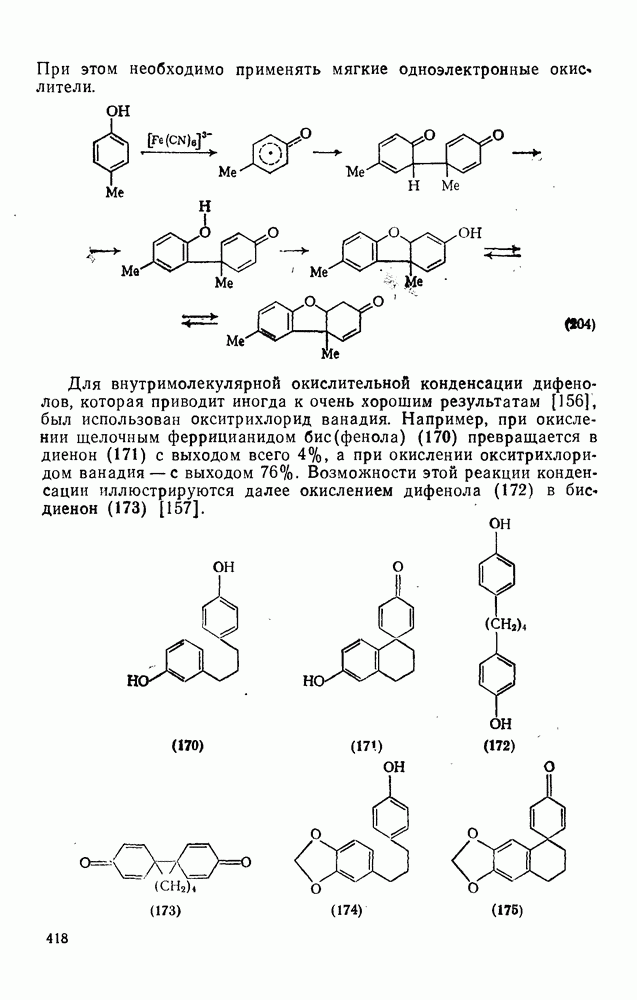
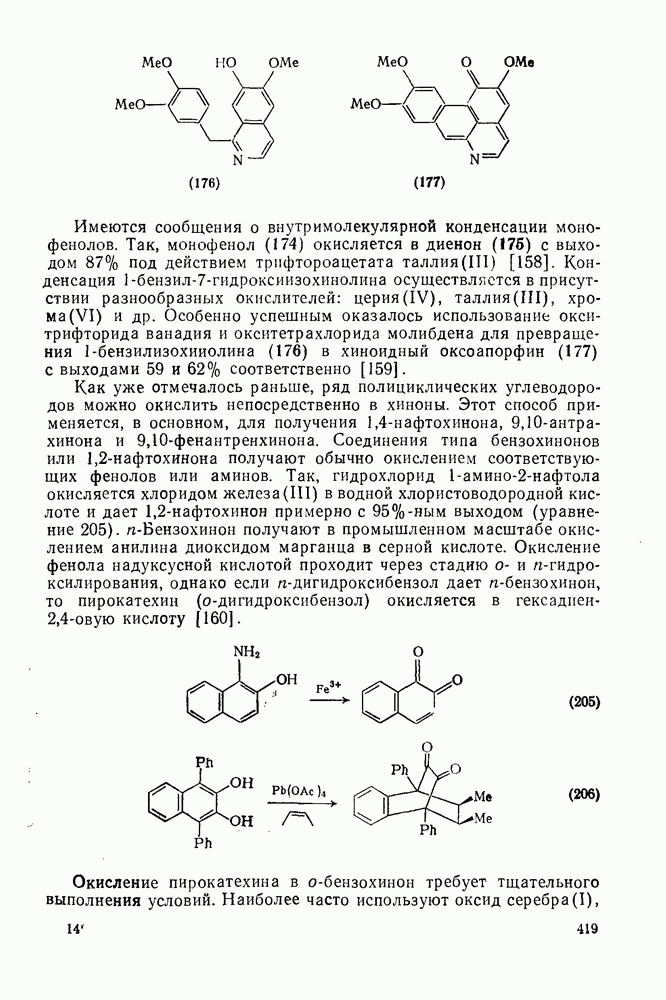
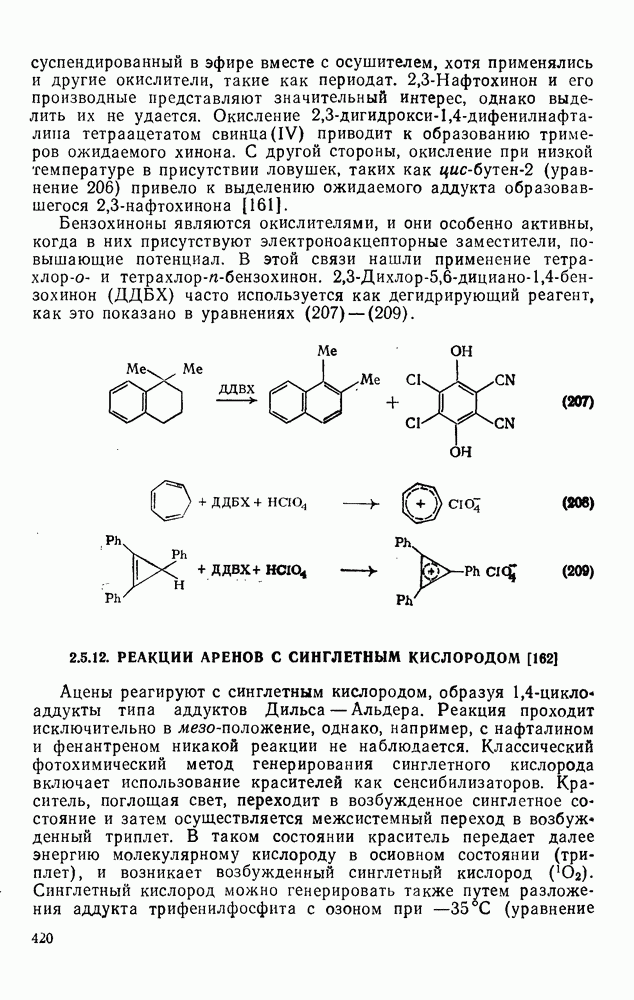
- 2.5.11. ОКИСЛЕНИЕ АРЕНОВ [153]
- 2.5.12. РЕАКЦИИ АРЕНОВ С СИНГЛЕТНЫМ КИСЛОРОДОМ [162]
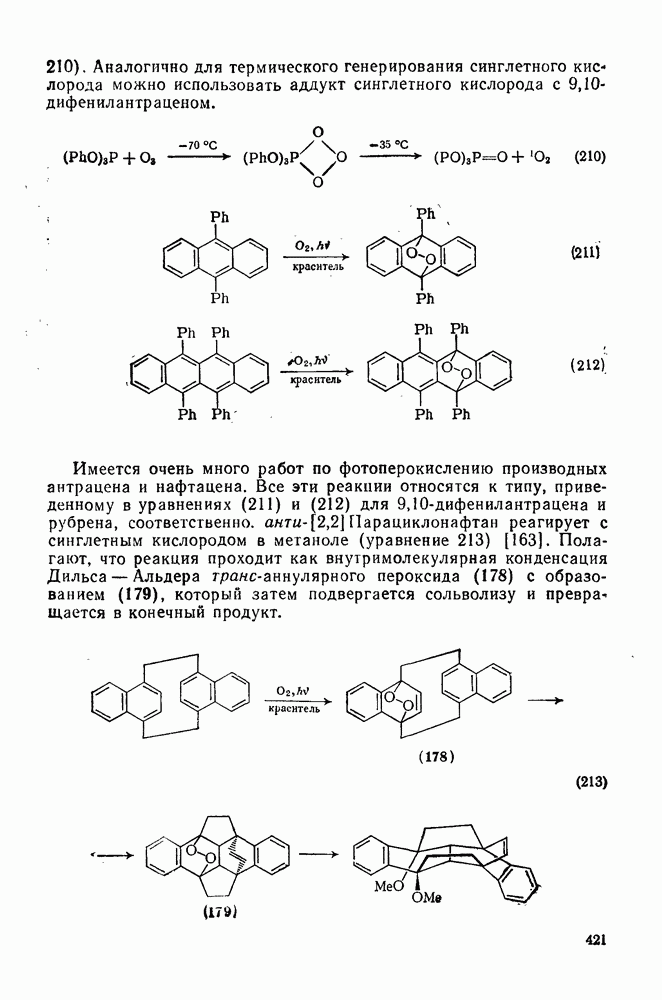
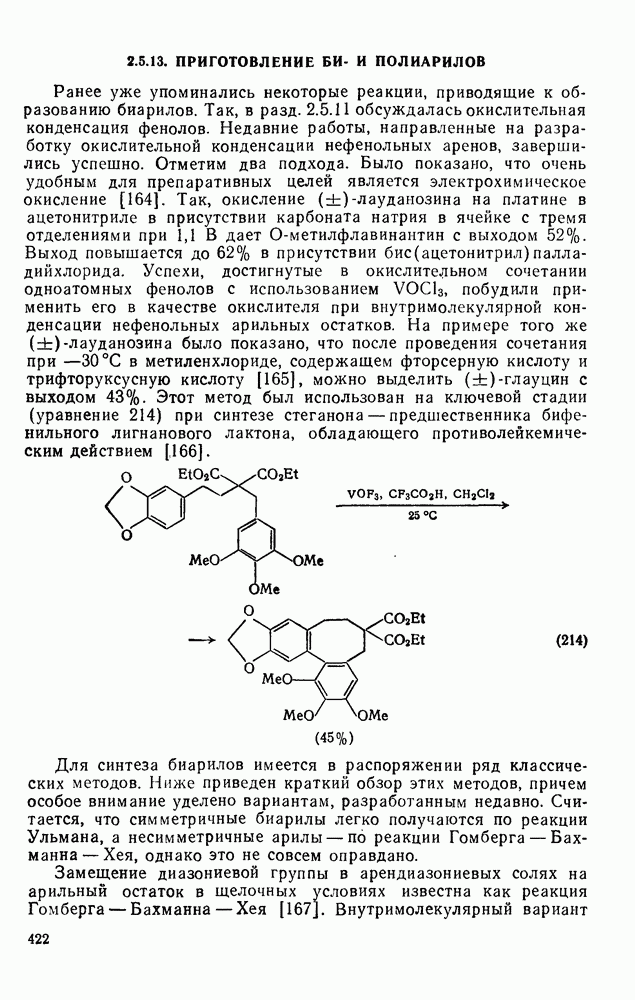
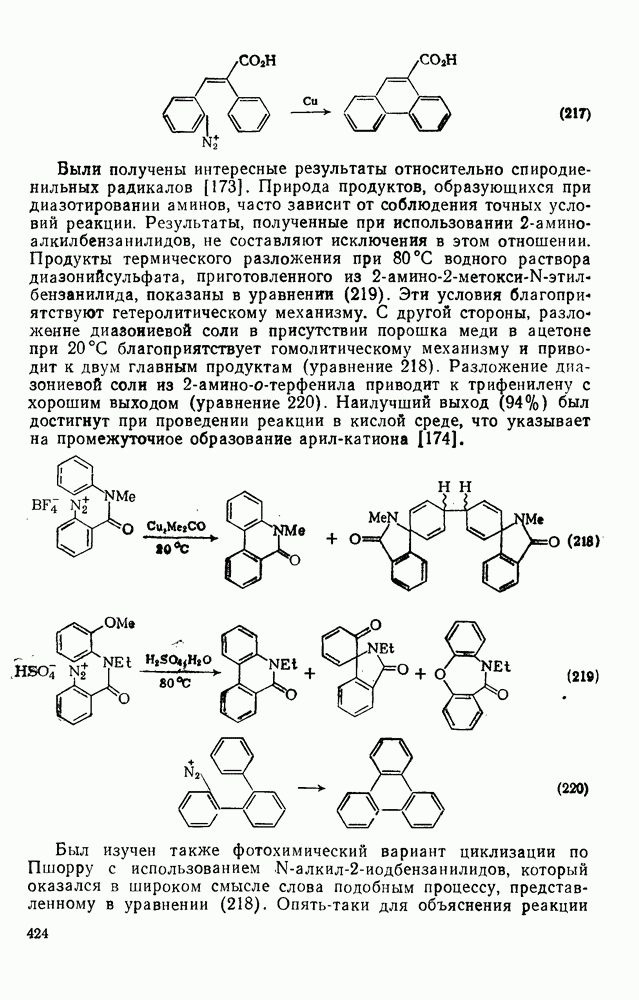
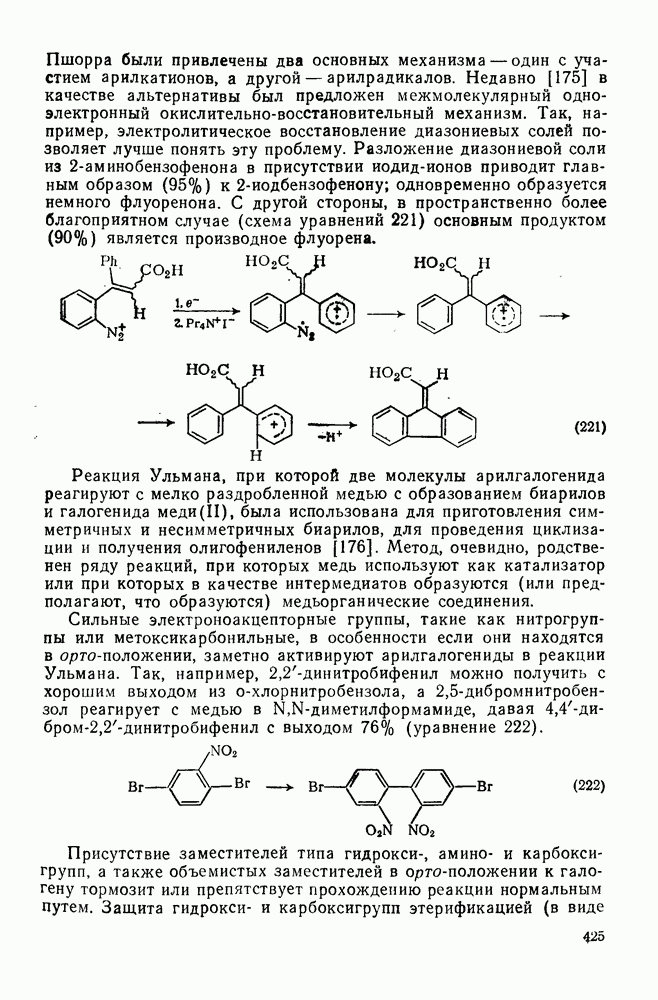
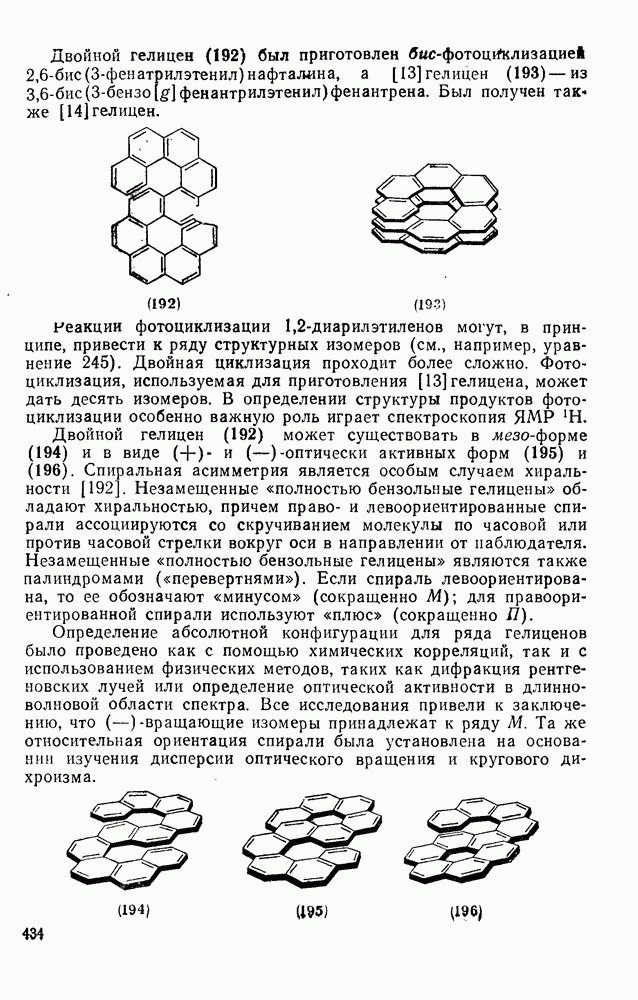
- 2.5.13. ПРИГОТОВЛЕНИЕ БИ- И ПОЛИАРИЛОВ
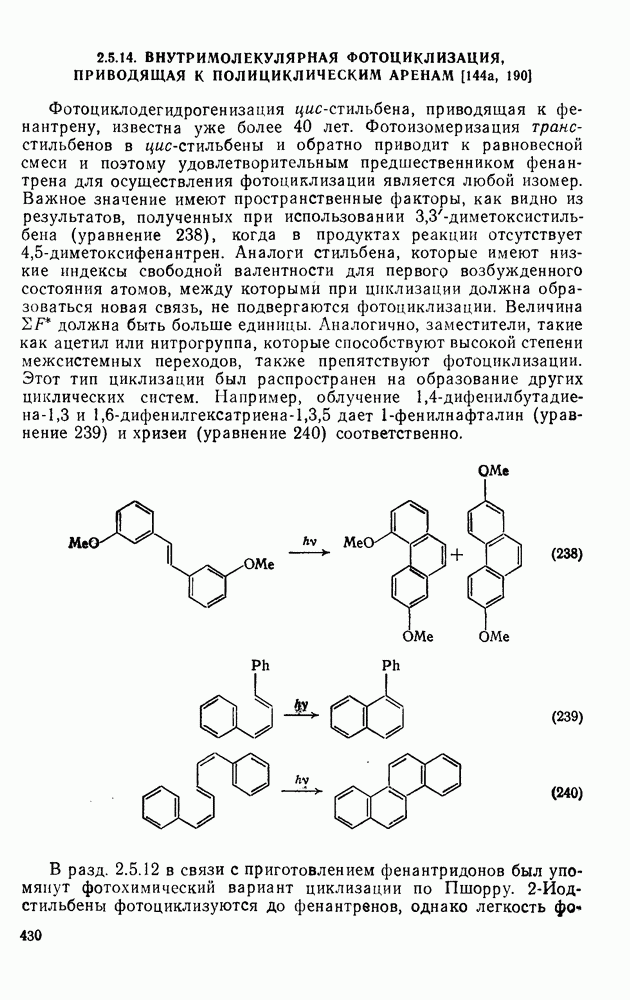
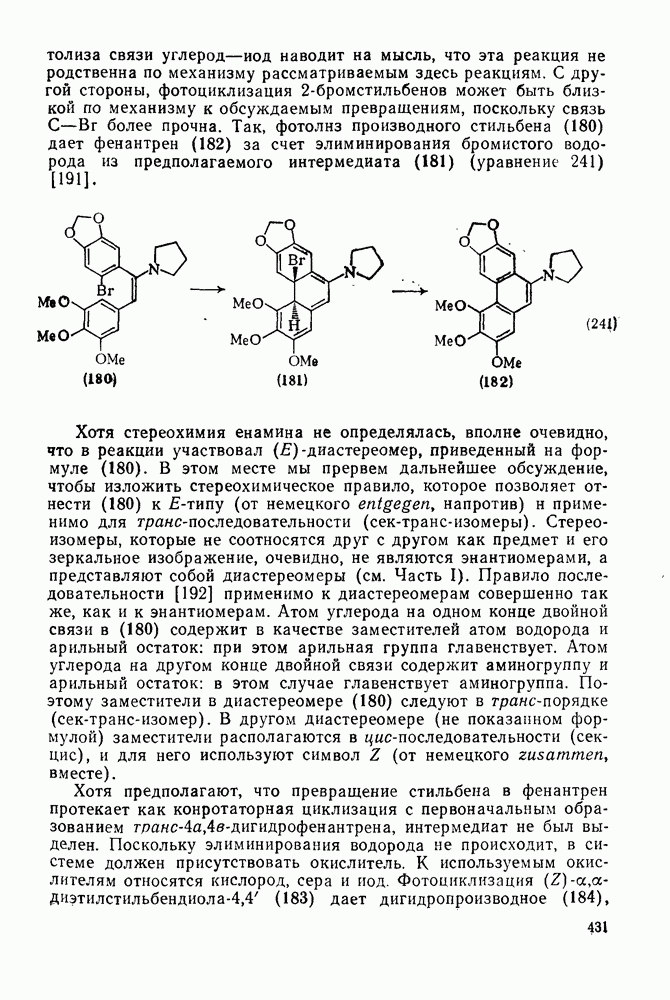
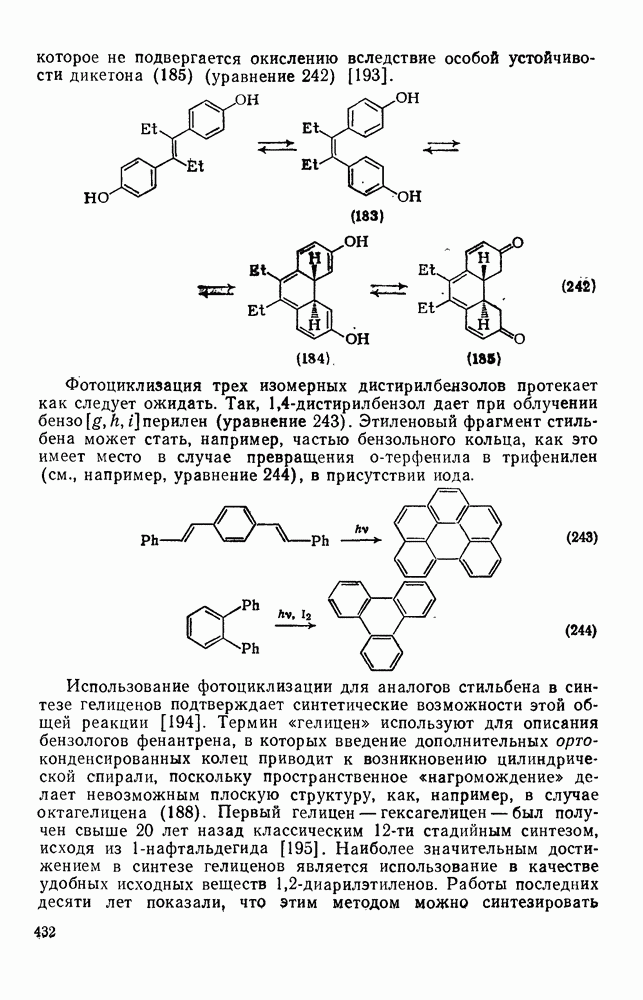
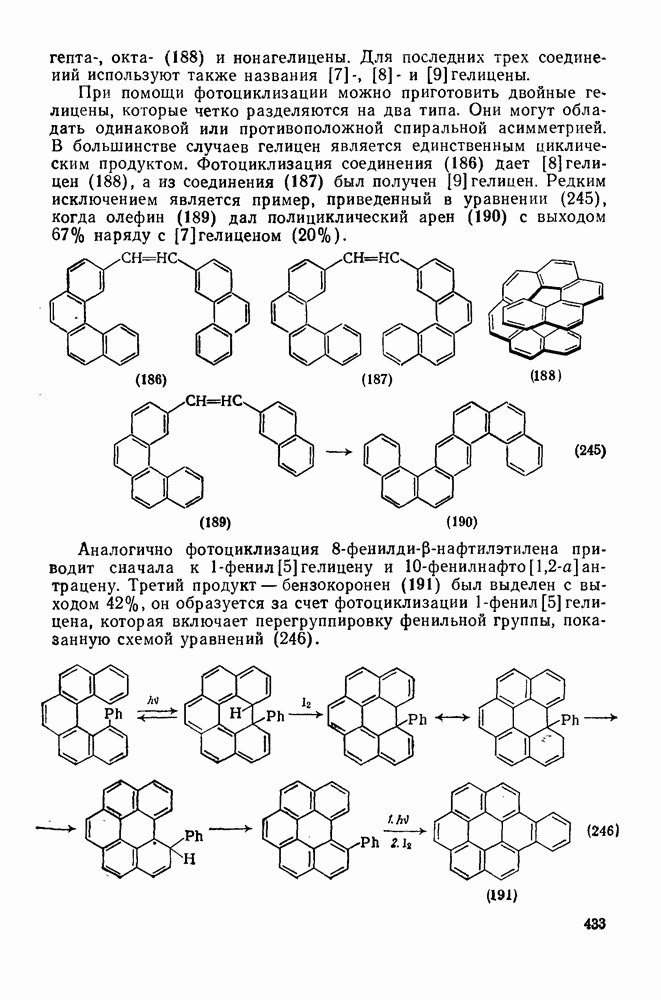
- 2.5.14. ВНУТРИМОЛЕКУЛЯРНАЯ ФОТОЦИКЛИЗАЦИЯ, ПРИВОДЯЩАЯ К ПОЛИЦИКЛИЧЕСКИМ АРЕНАМ
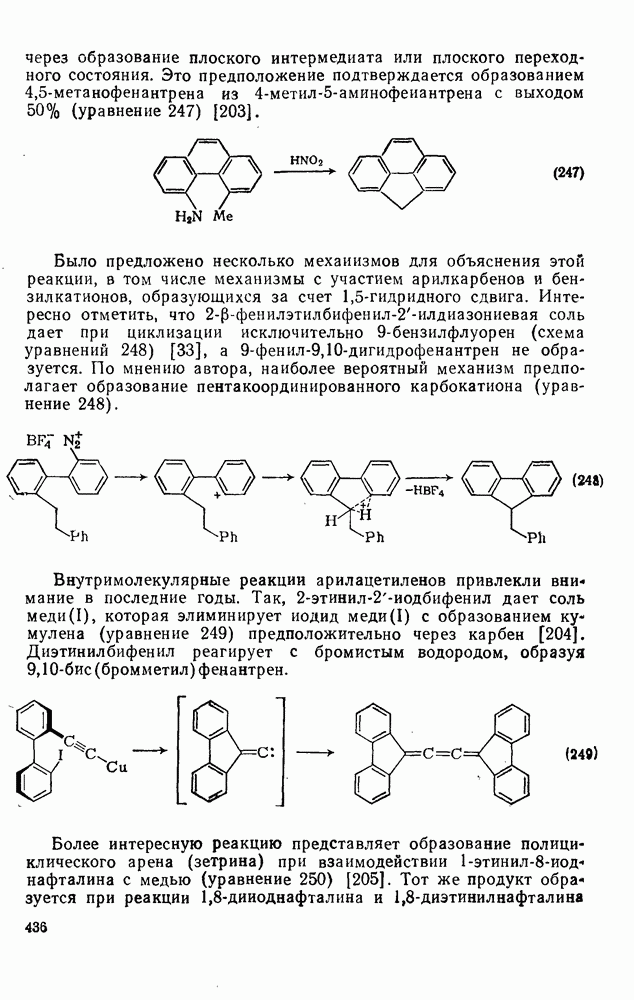
- 2.5.15. ВНУТРИМОЛЕКУЛЯРНАЯ ЦИКЛИЗАЦИЯ ДИЗАМЕЩЕННЫХ АРЕНОВ
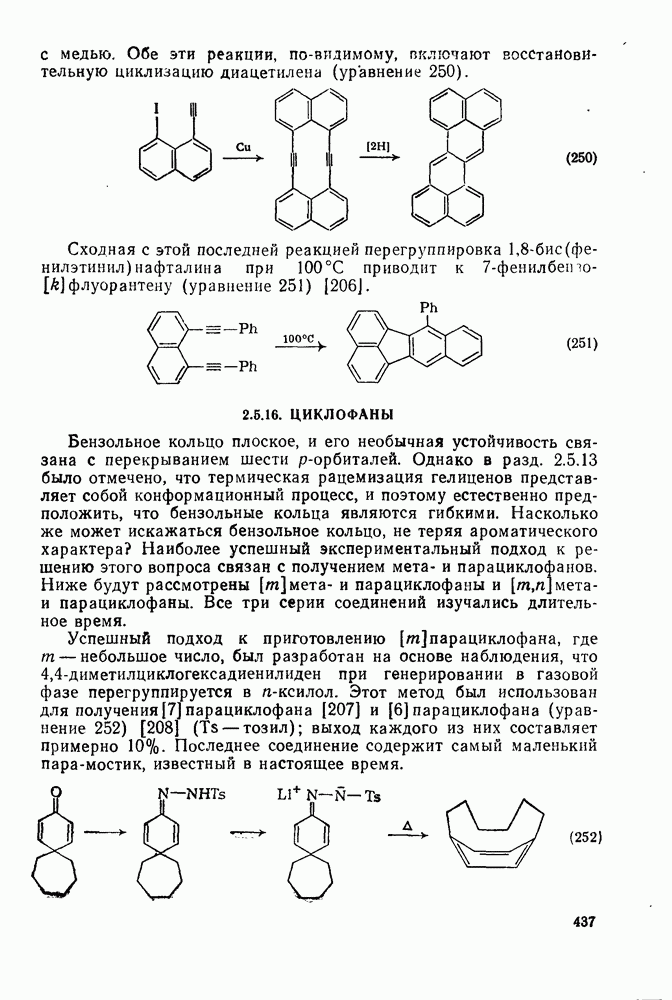
- 2.5.16. ЦИКЛОФАНЫ
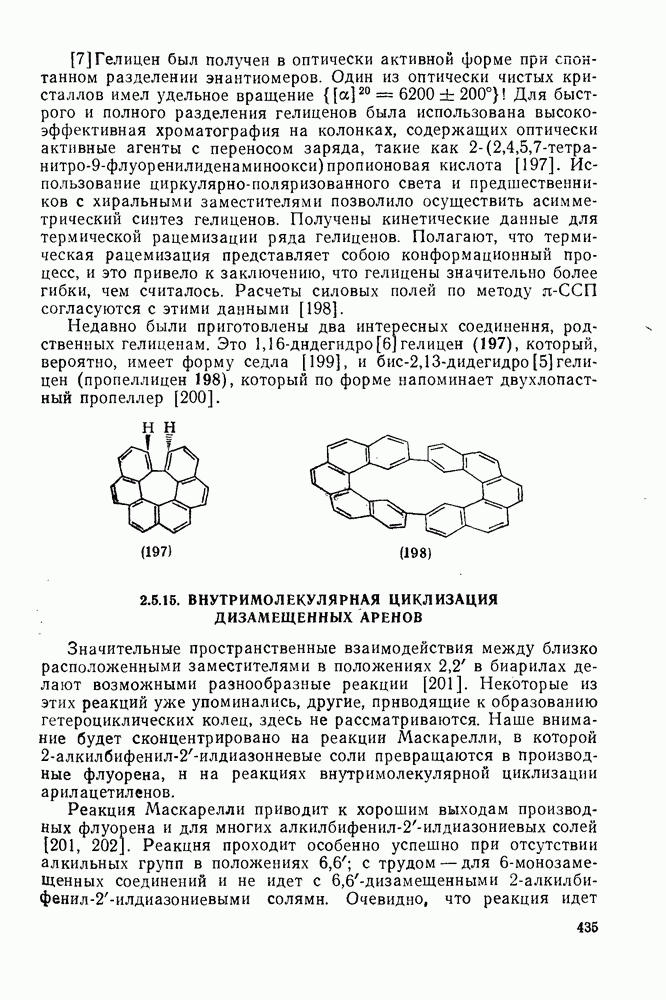
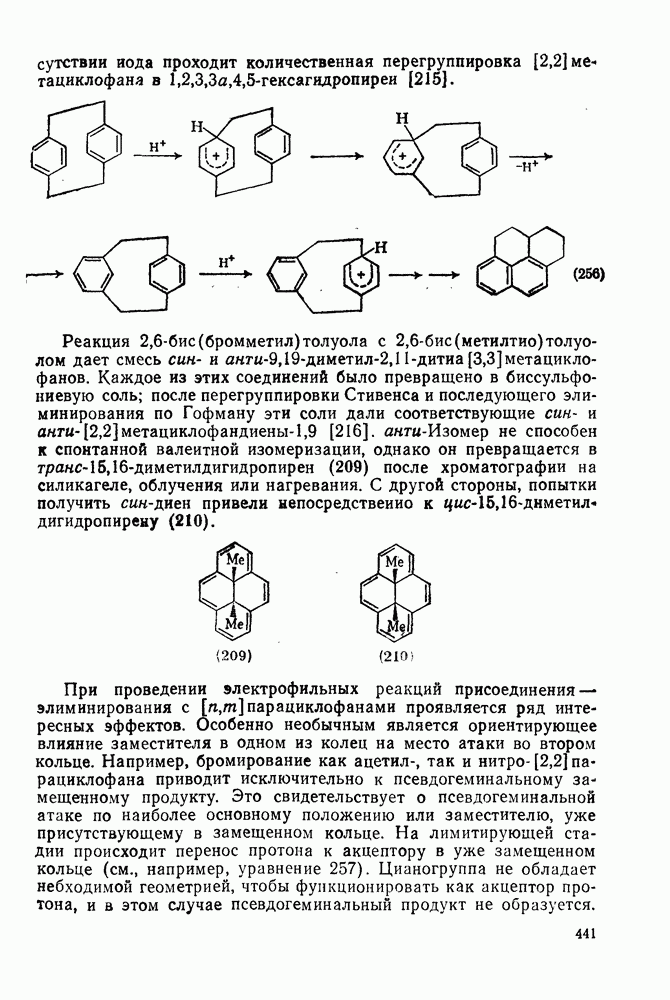
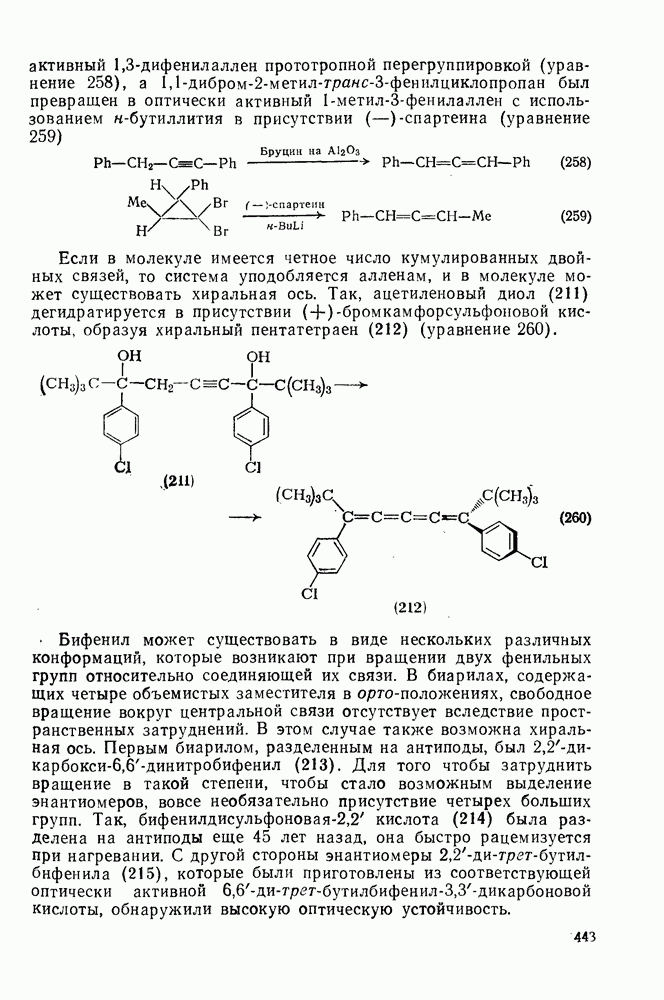
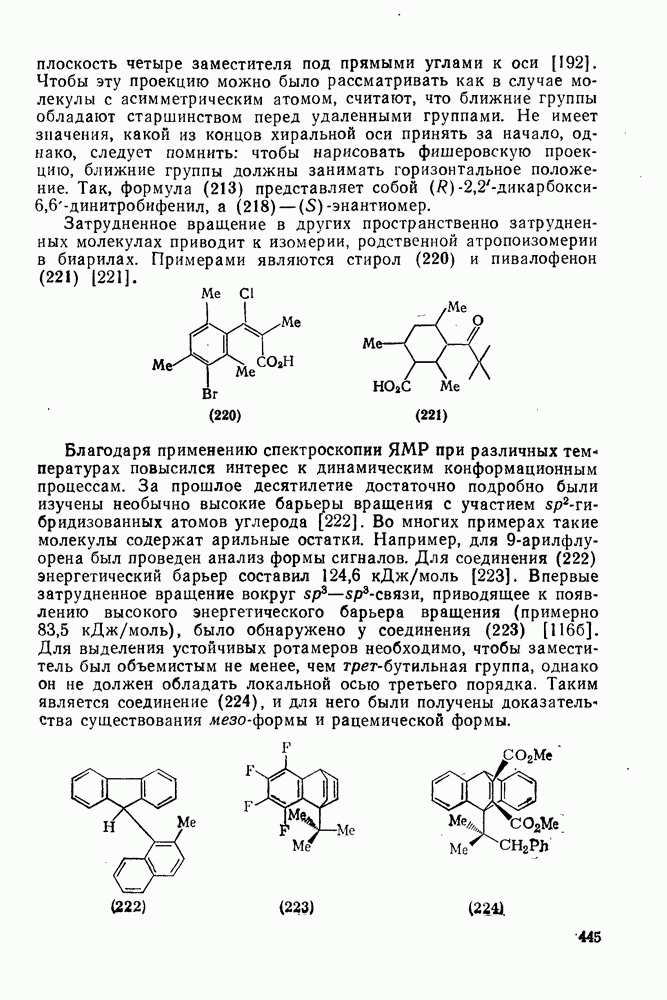
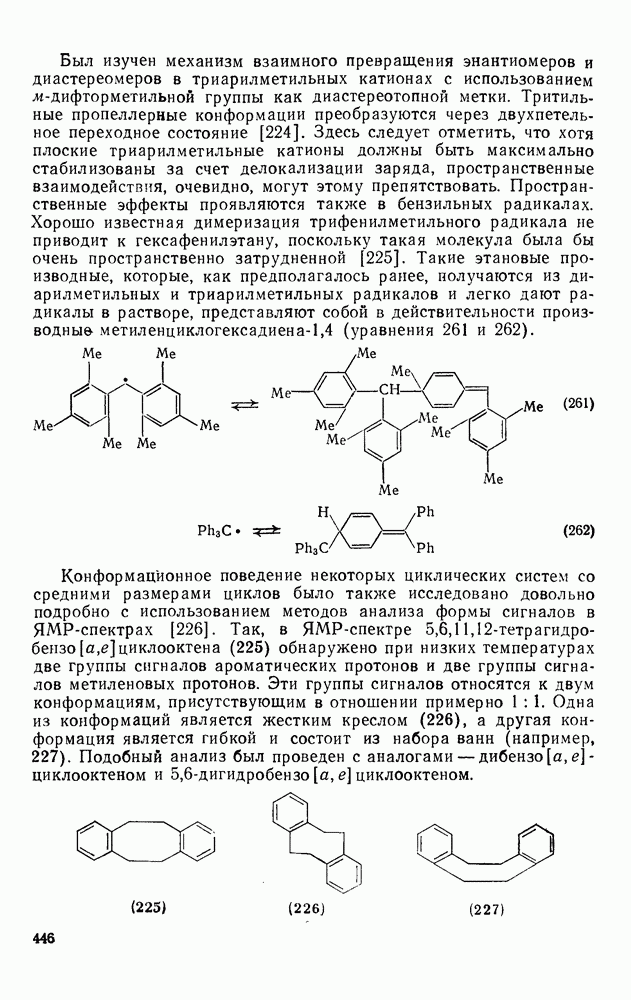
- 2.5.17. КОНФОРМАЦИЯ И ХИРАЛЬНОСТЬ АРЕНОВ
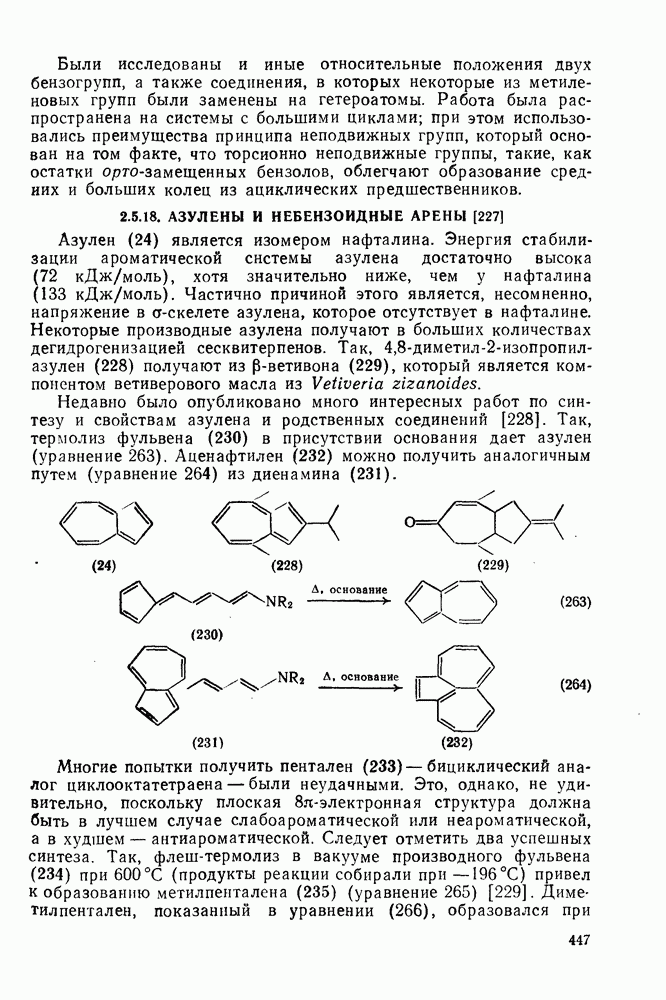
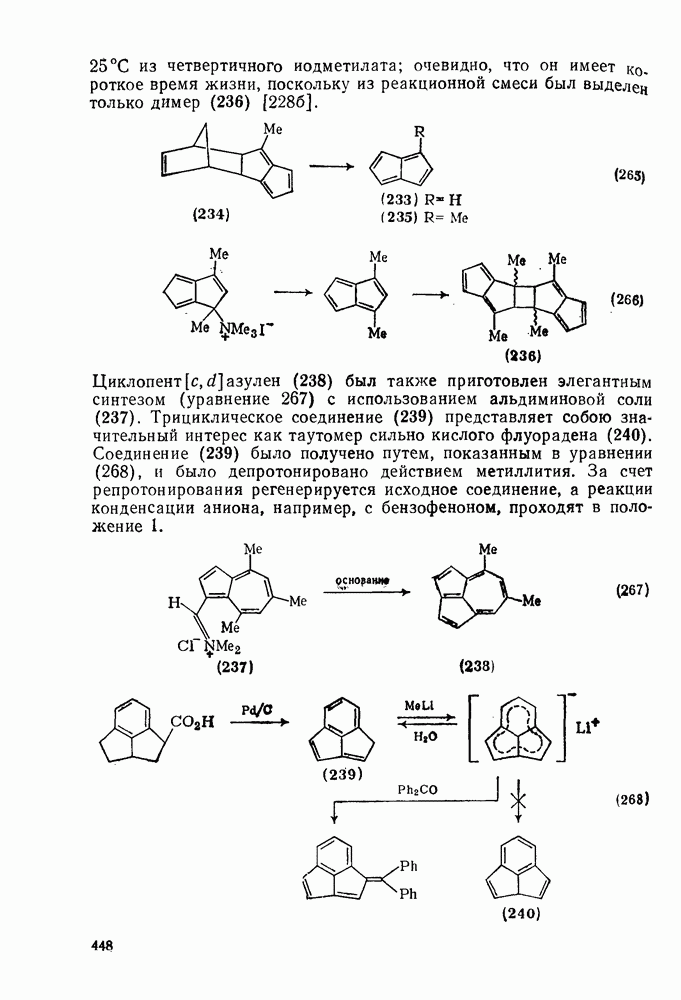
- 2.5.18. АЗУЛЕНЫ И НЕБЕНЗОИДНЫЕ АРЕНЫ
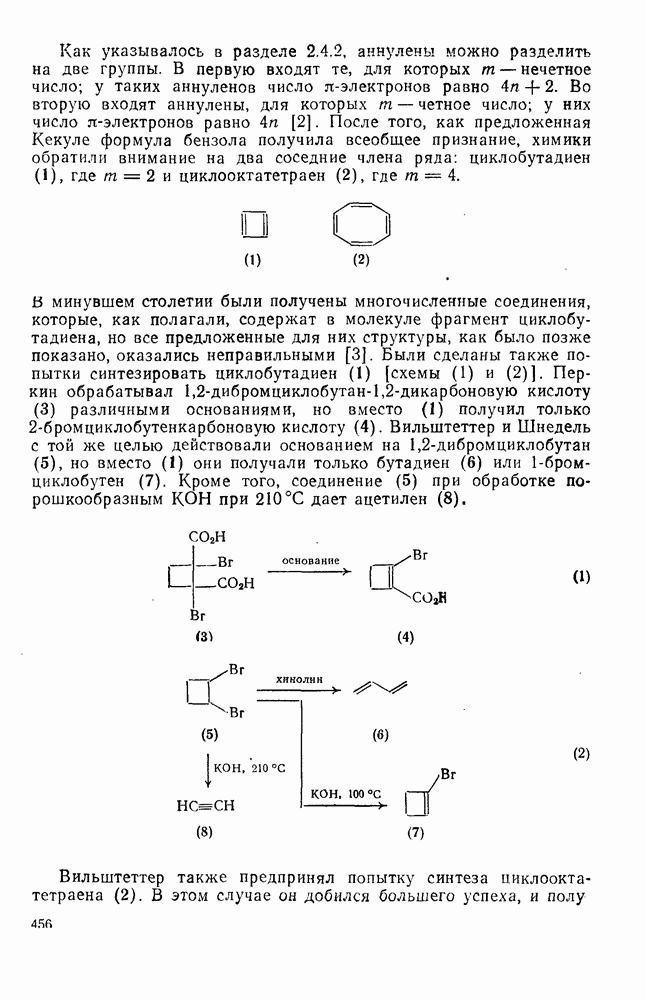
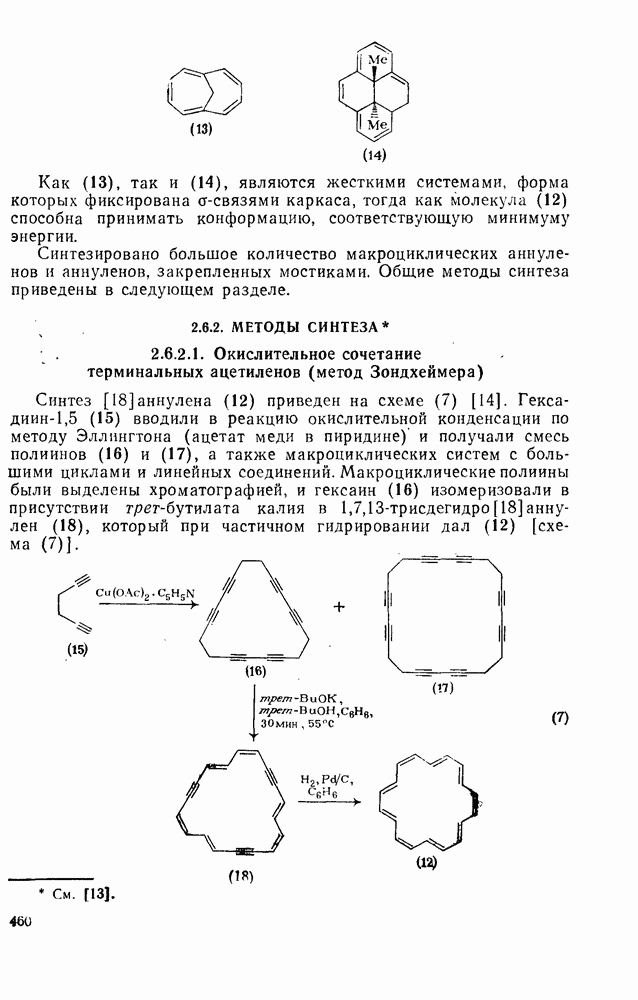
- 2.6. АННУЛЕНЫ И РОДСТВЕННЫЕ СИСТЕМЫ
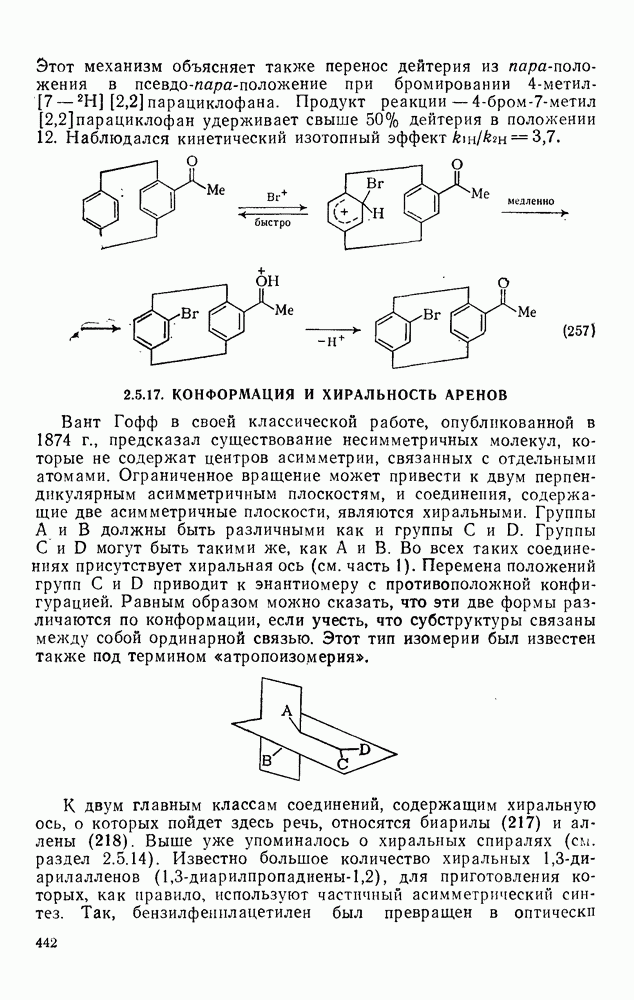
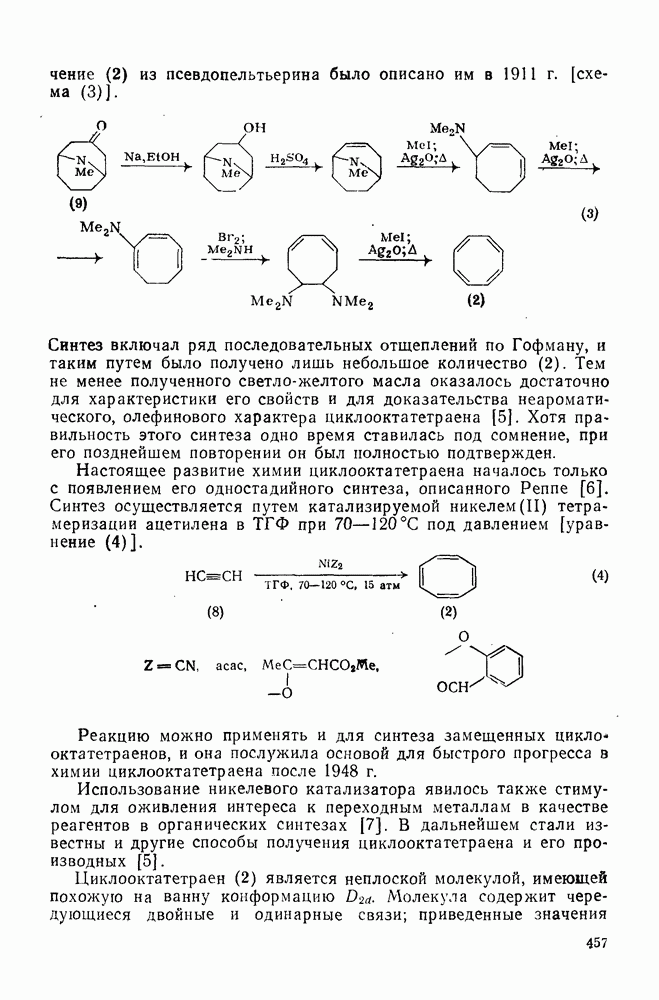
- 2.6.2. МЕТОДЫ СИНТЕЗА
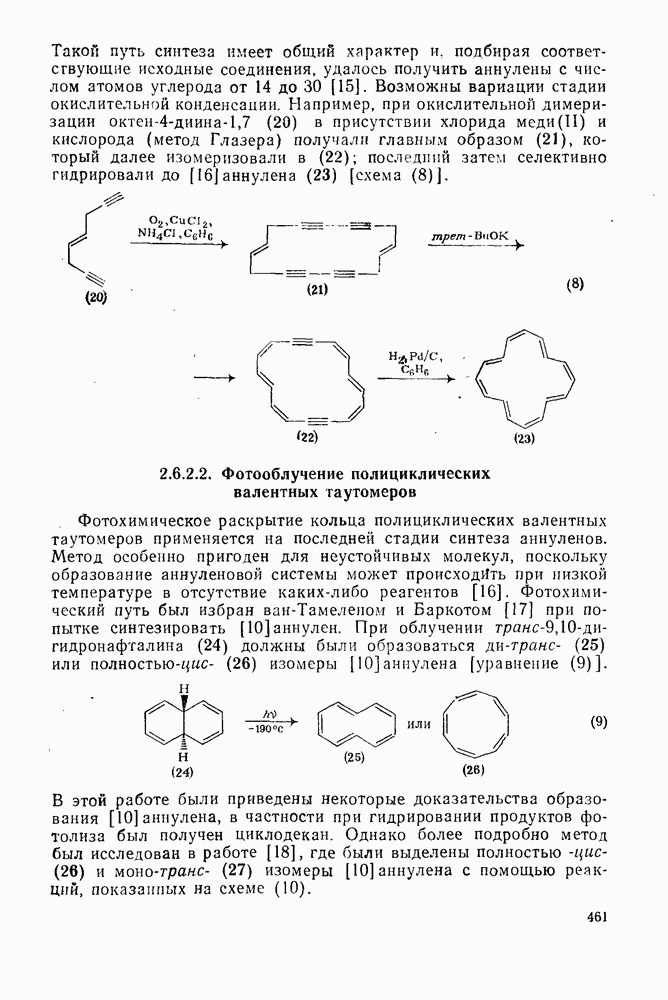
- 2.6.2.1. Окислительное сочетание терминальных ацетиленов (метод Зондхеймера)
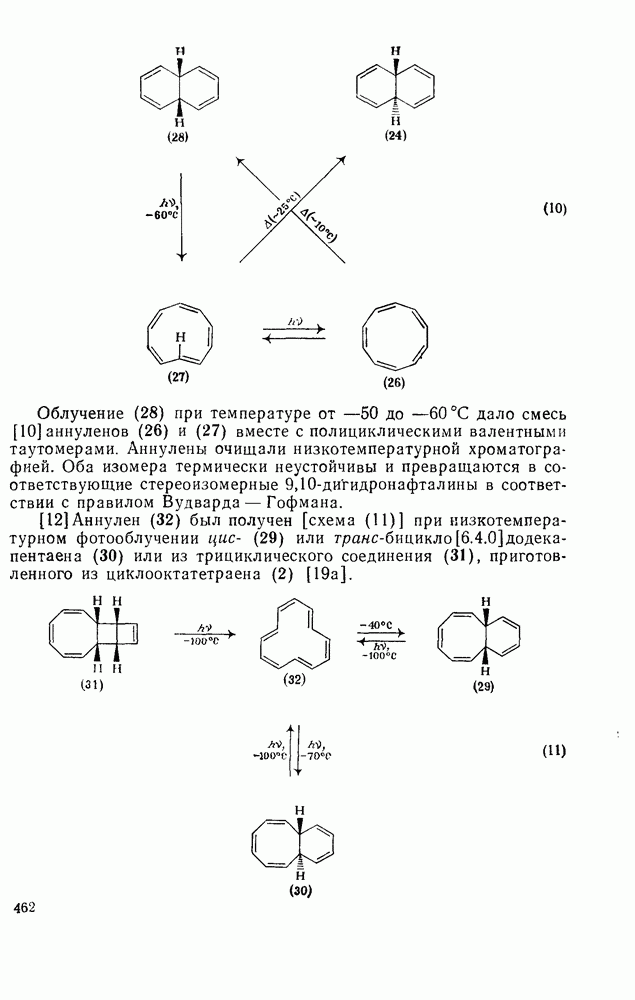
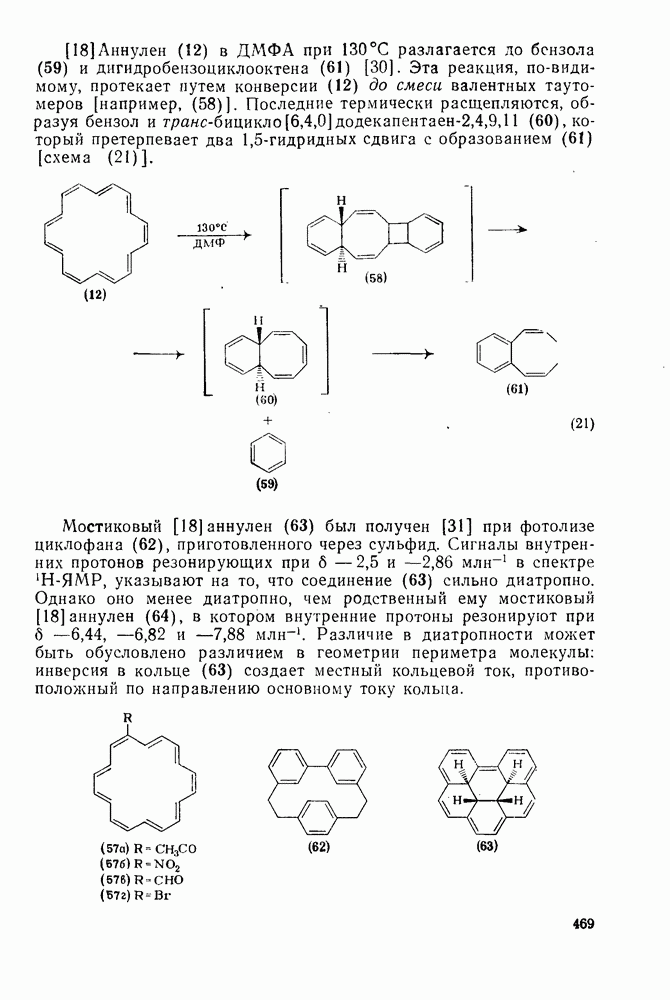
- 2.6.2.2. Фотооблучение полициклических валентных таутомеров
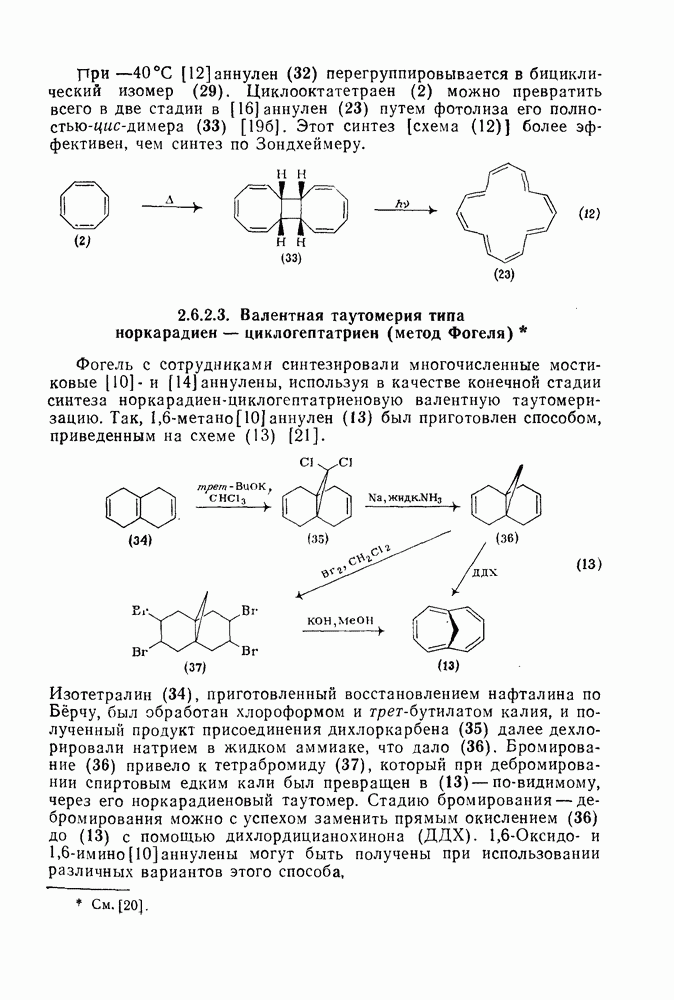
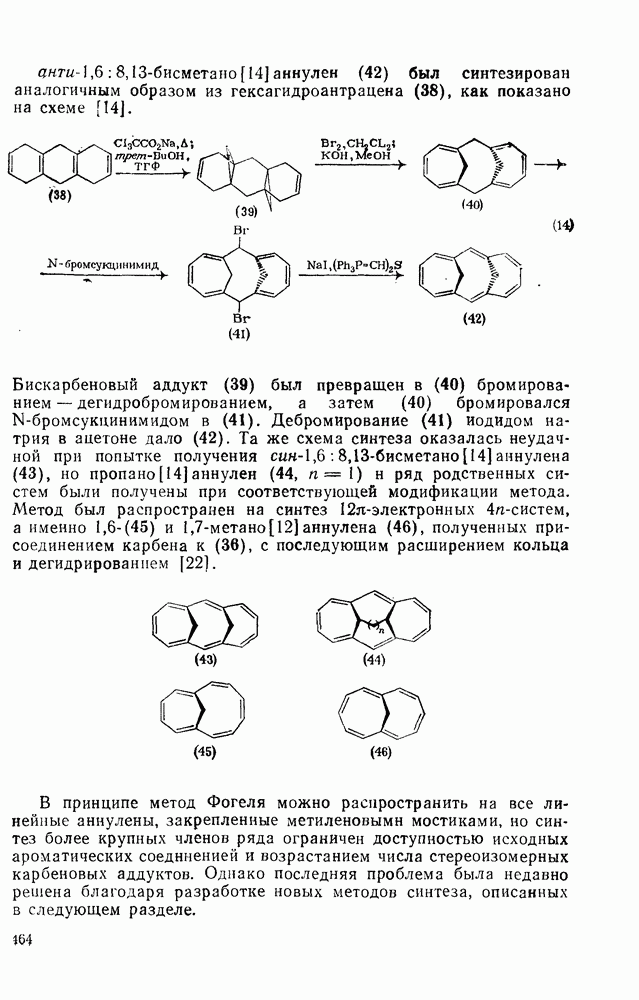
- 2.6.2.3. Валентная таутомерия типа норкарадиен — циклогептатриен (метод Фогеля)
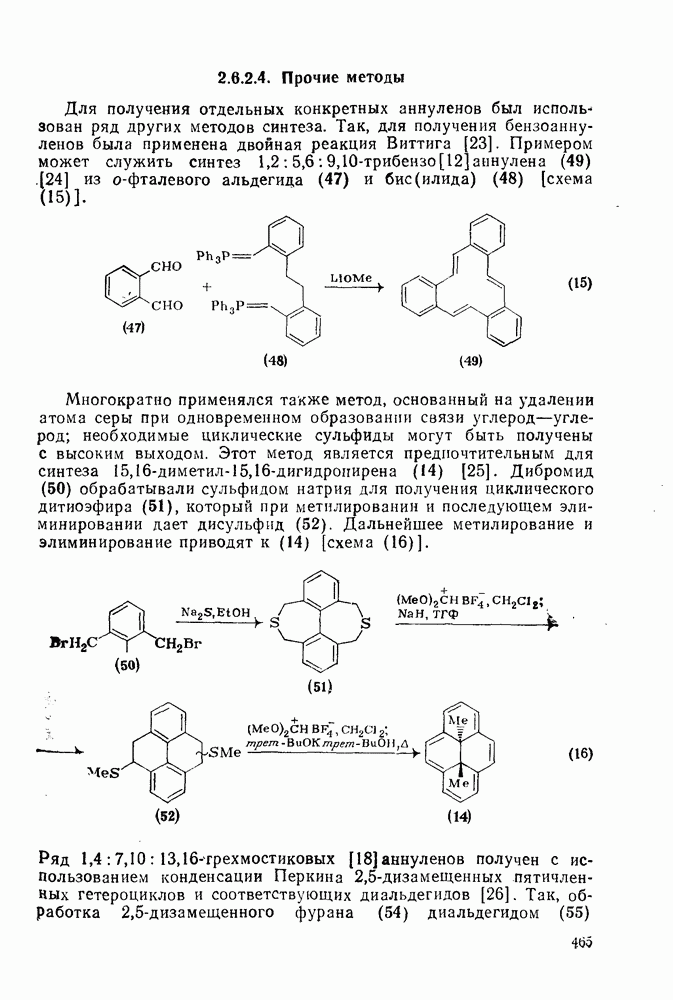
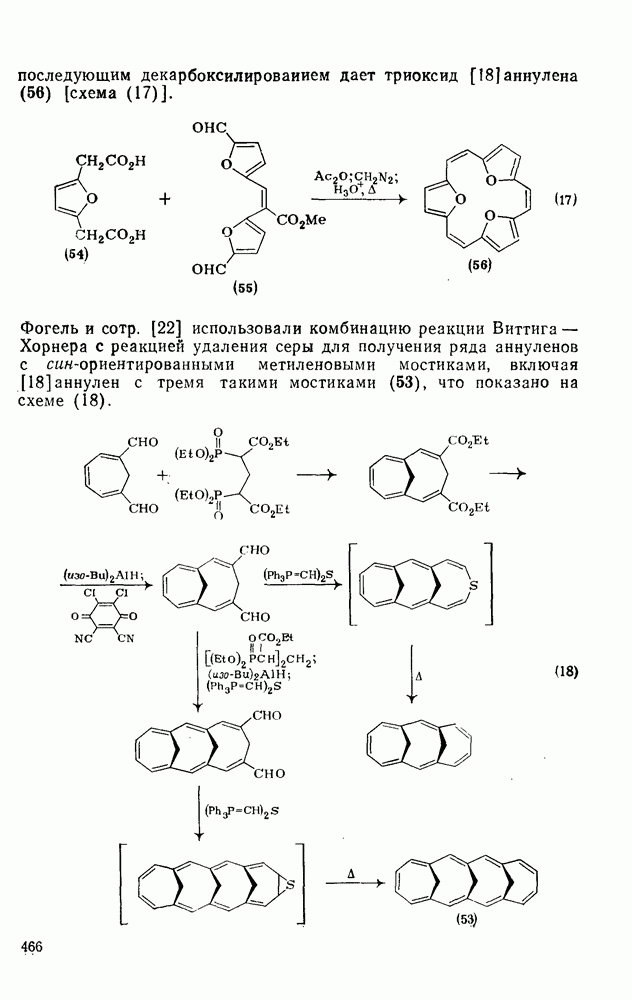
- 2.6.2.4. Прочие методы
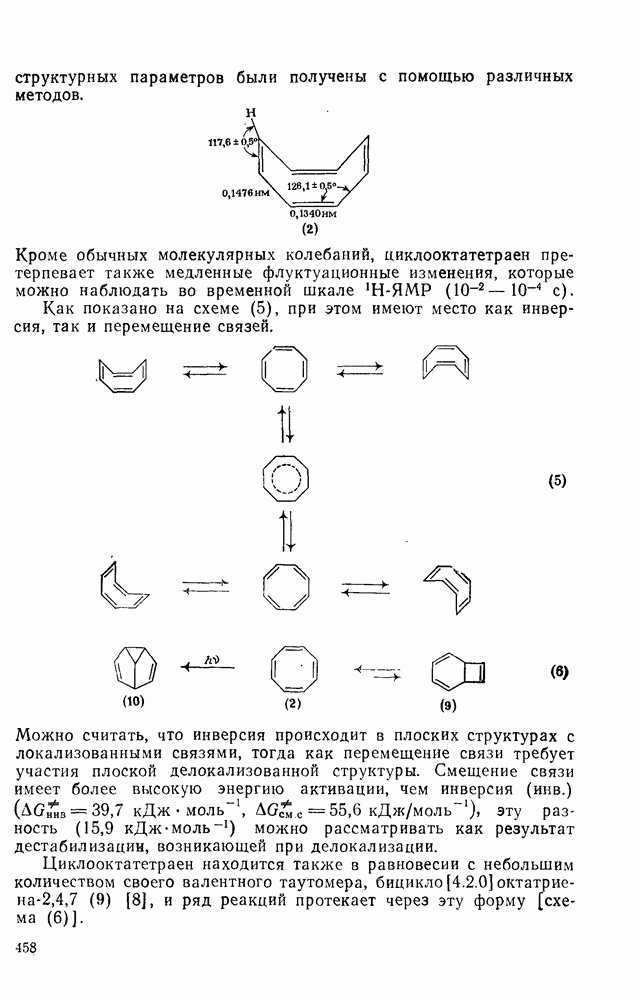
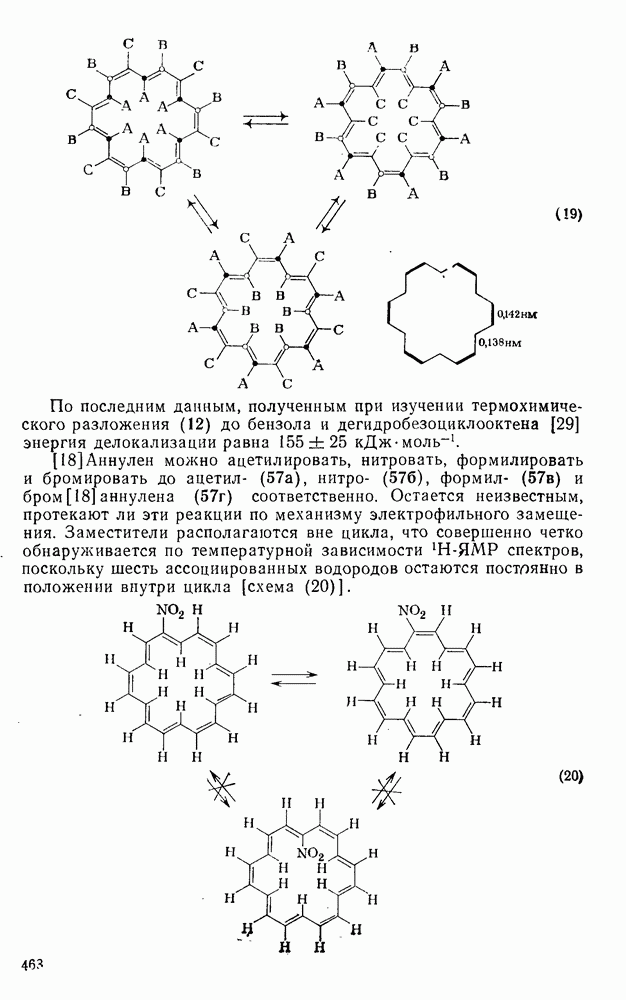
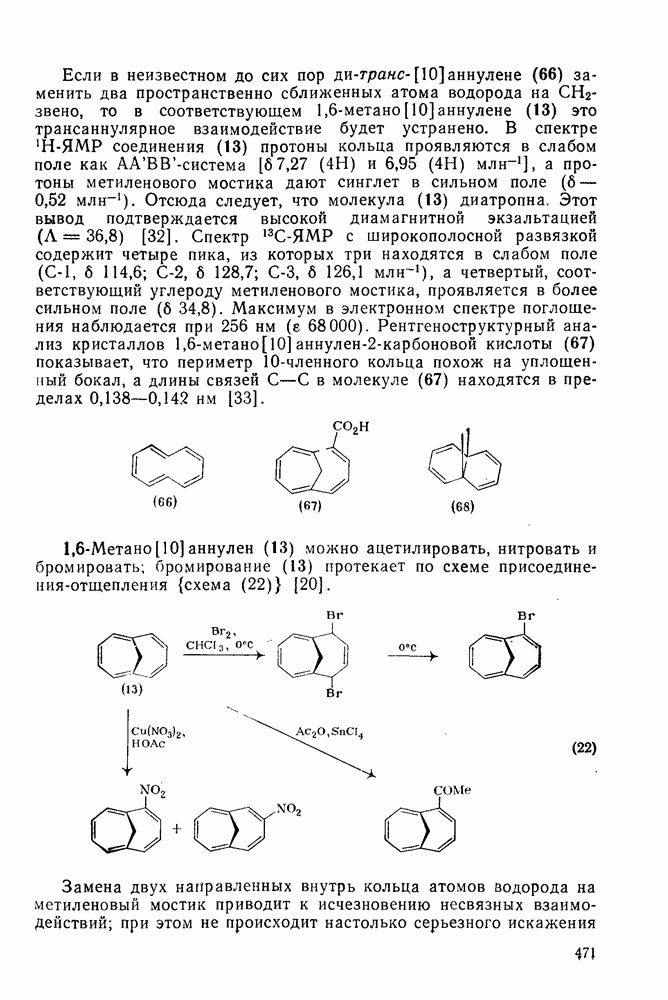
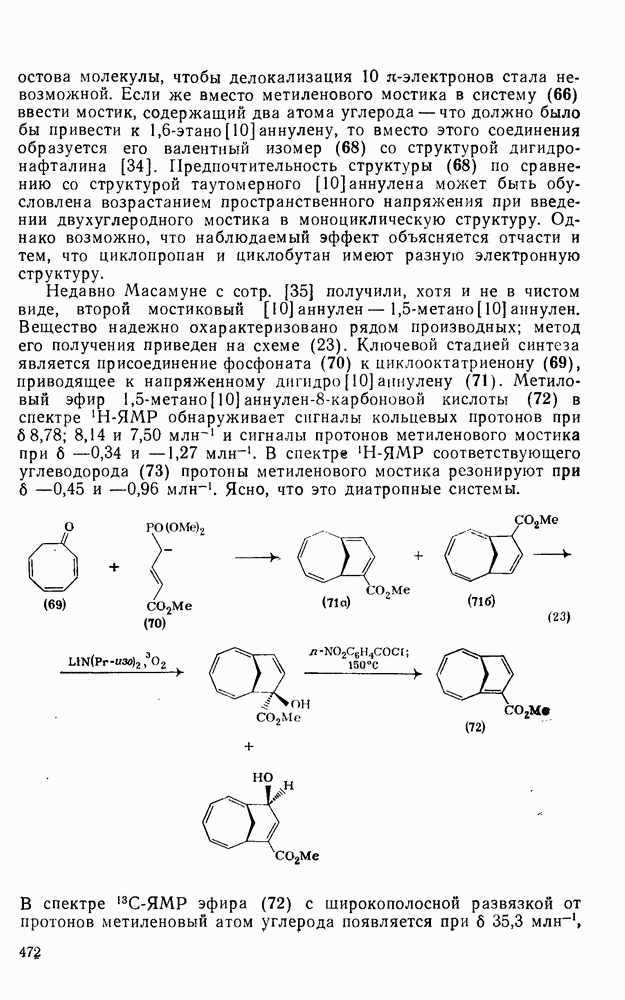
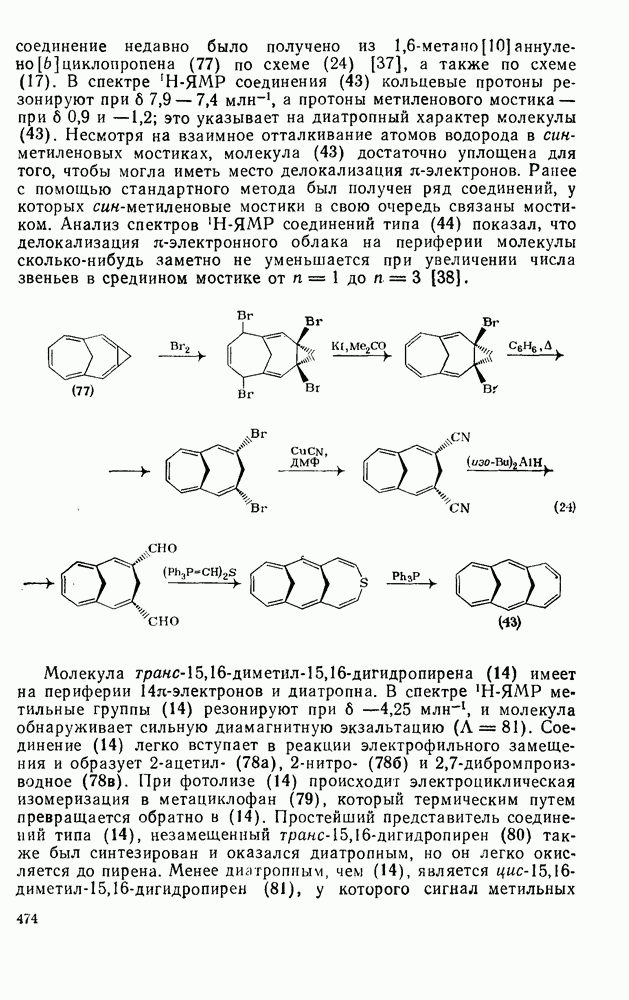
- 2.6.3. СВОЙСТВА АННУЛЕНОВ
- 2.6.4. СВОЙСТВА 4n-АННУЛЕНОВ
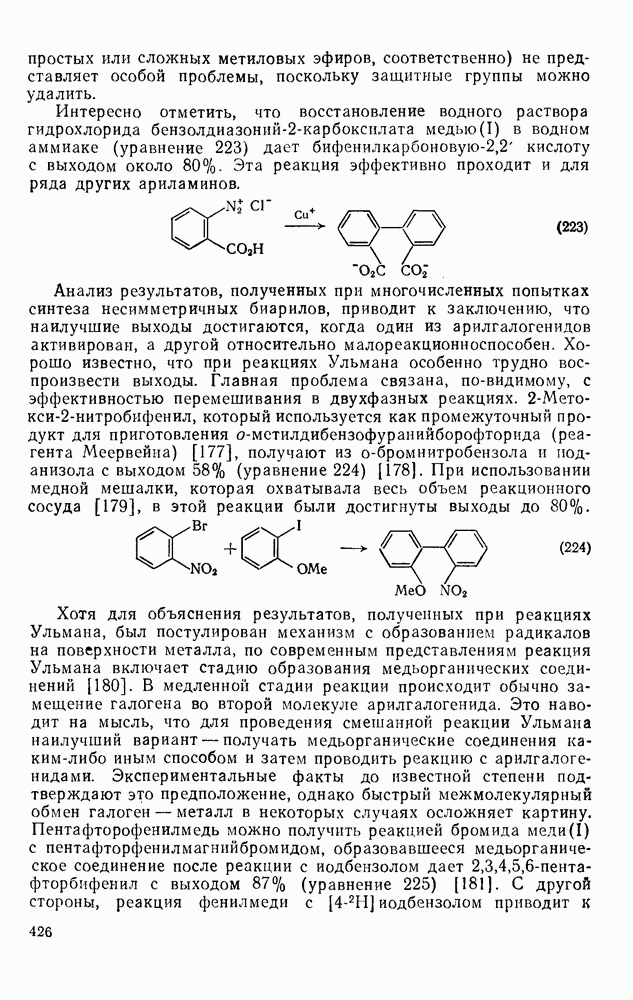
- 2.6.5. ДЕГИДРОАННУЛЕНЫ
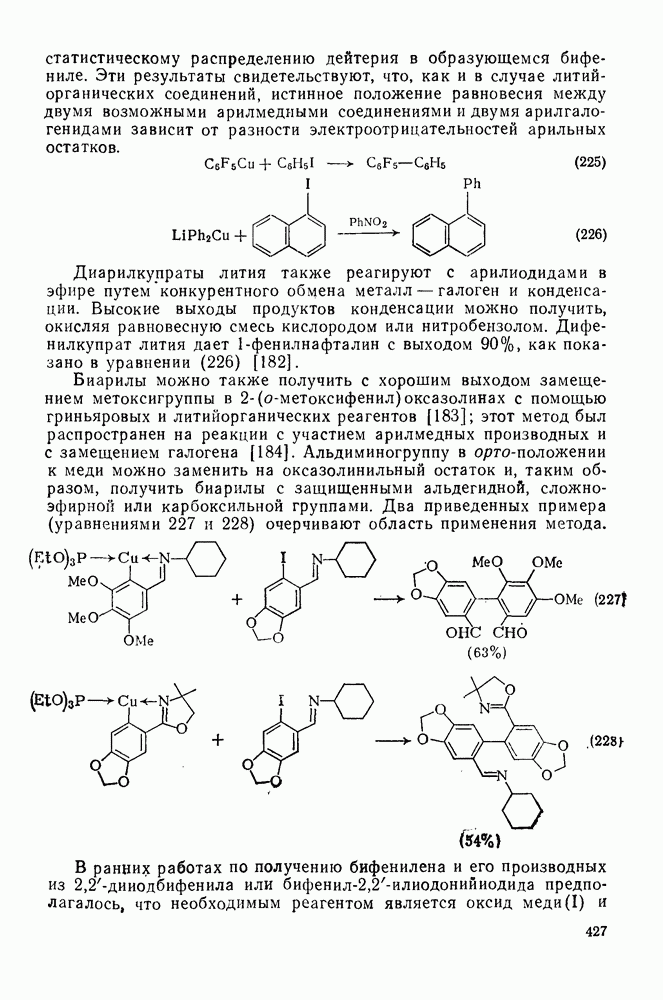
- 2.6.6. АННЕЛИРОВАННЫЕ АННУЛЕНЫ
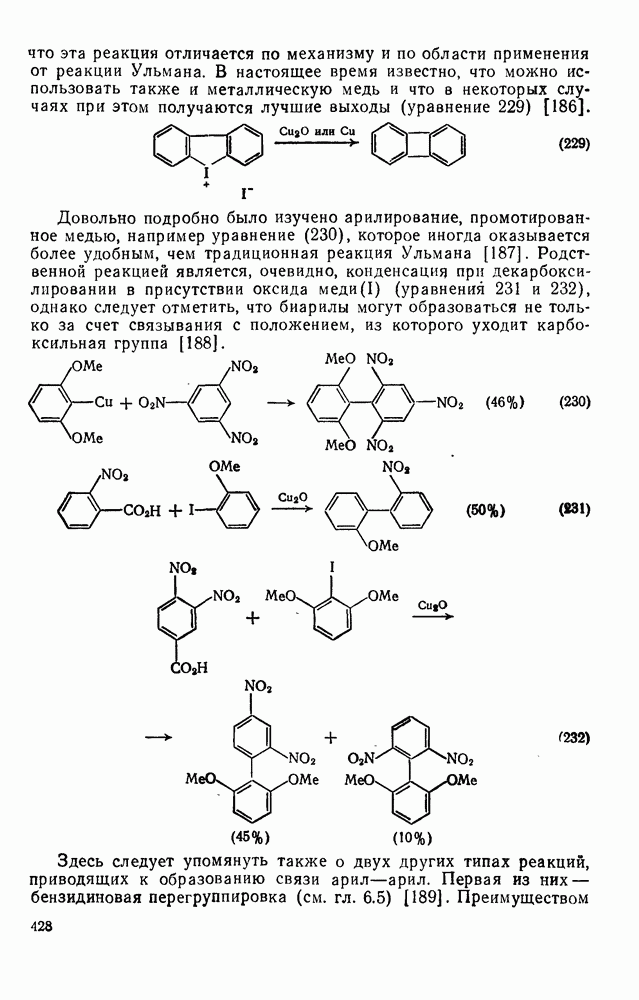
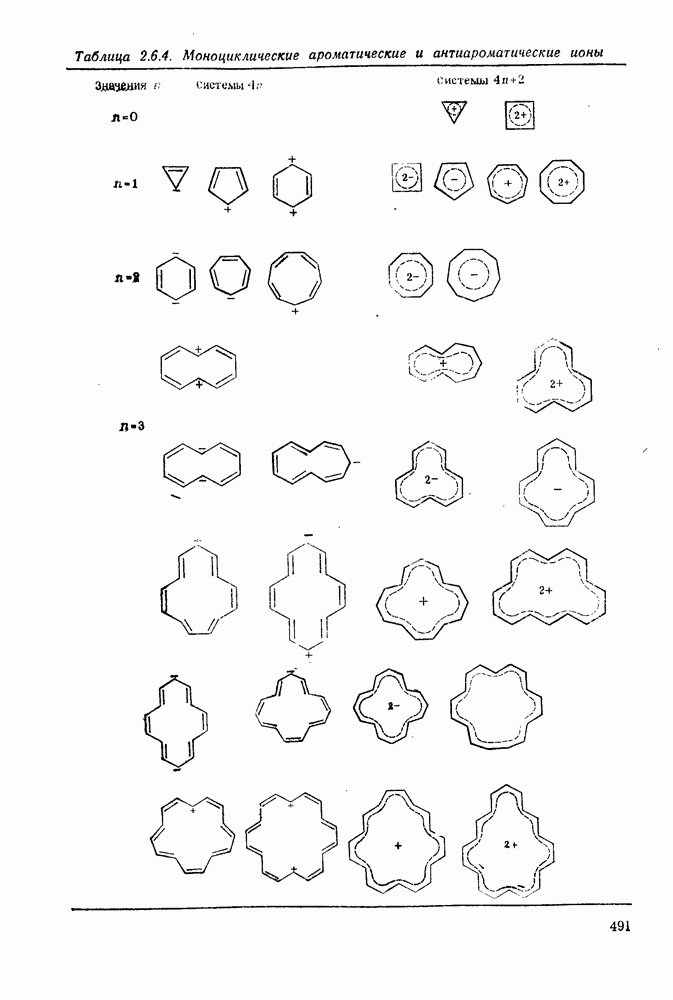
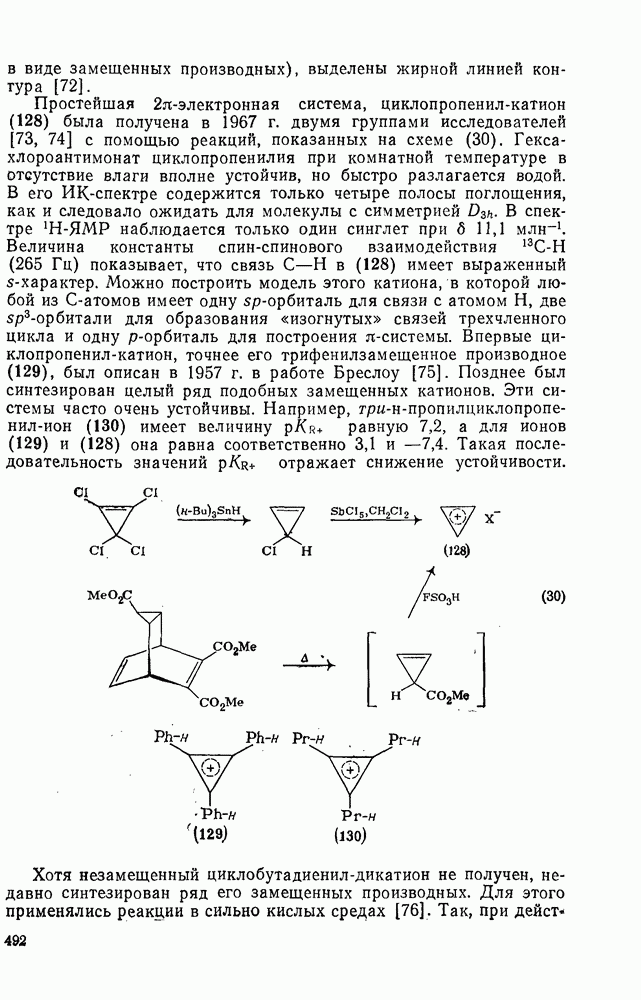
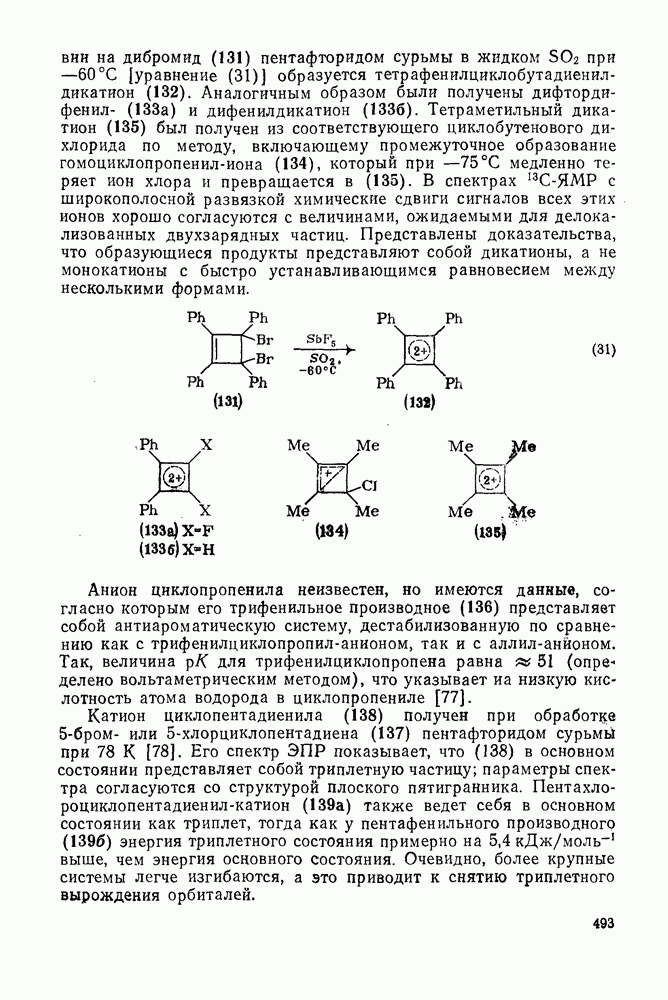
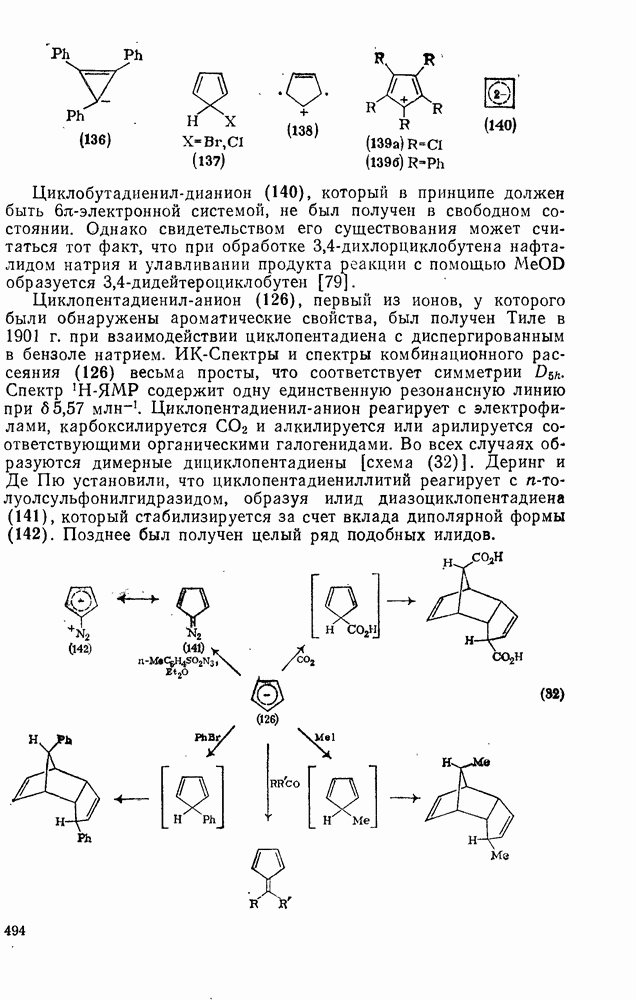
- 2.6.7. АРОМАТИЧЕСКИЕ И АНТИАРОМАТИЧЕСКИЕ МОНОЦИКЛИЧЕСКИЕ ИОНЫ
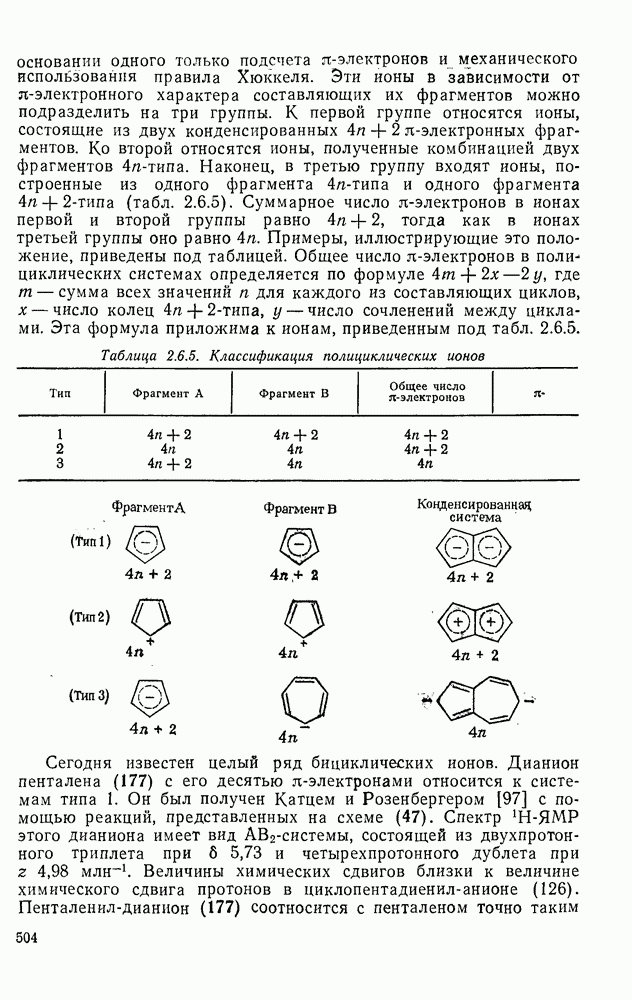
- 2.6.8. АРОМАТИЧЕСКИЕ И АНТИАРОМАТИЧЕСКИЕ ПОЛИЦИКЛИЧЕСКИЕ ИОНЫ
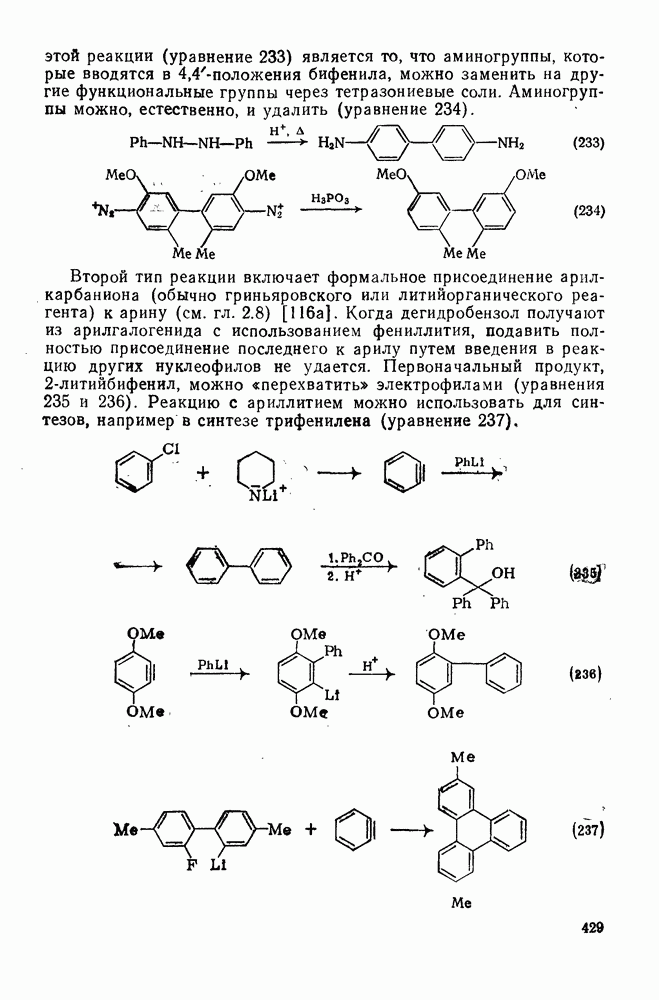
- 2.6.9. ГОМОАРОМАТИЧЕСКИЕ СИСТЕМЫ
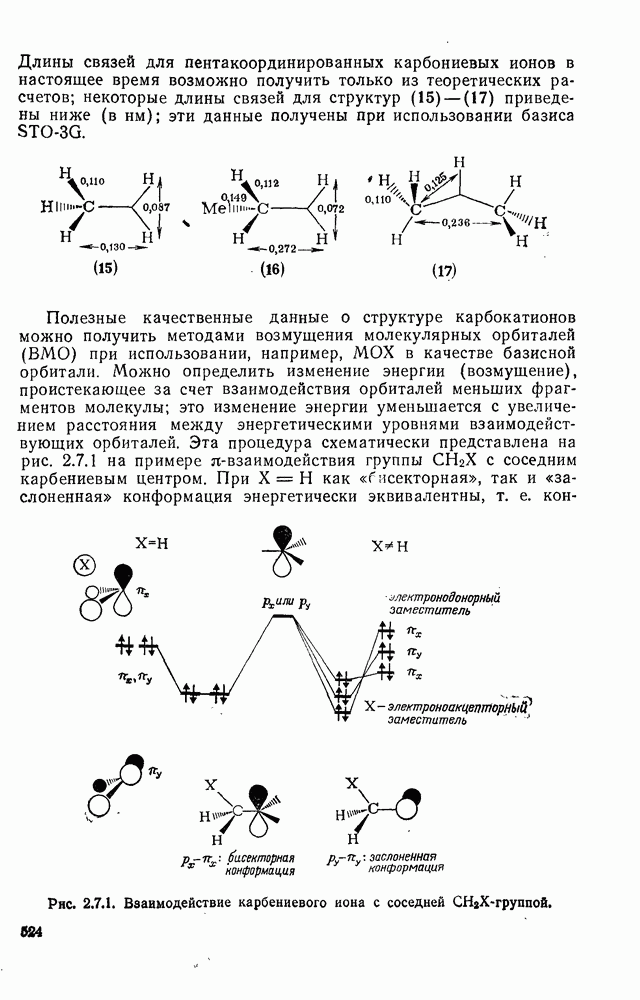
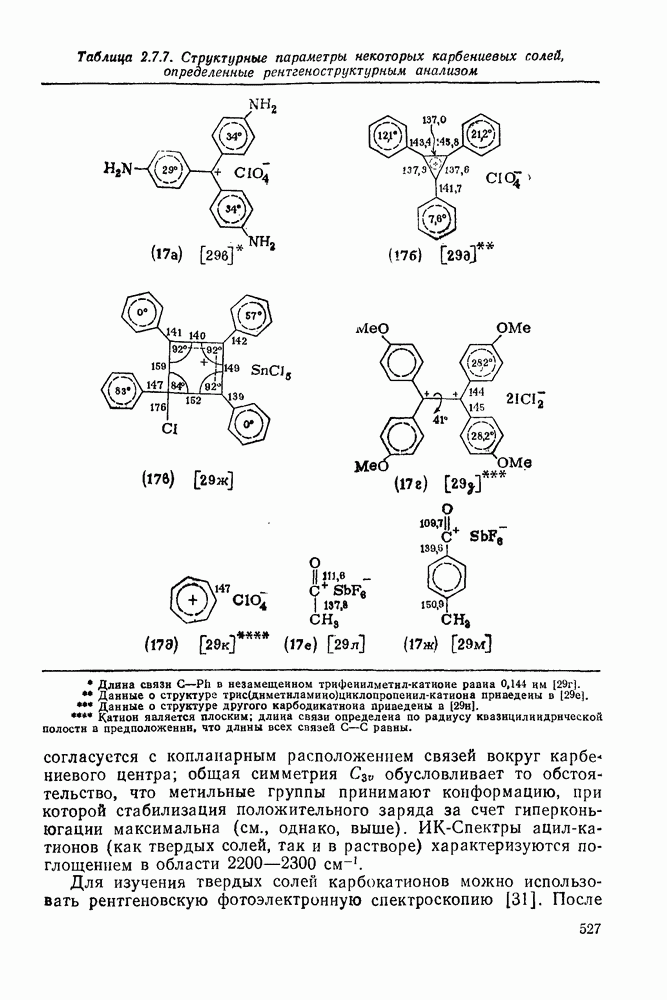
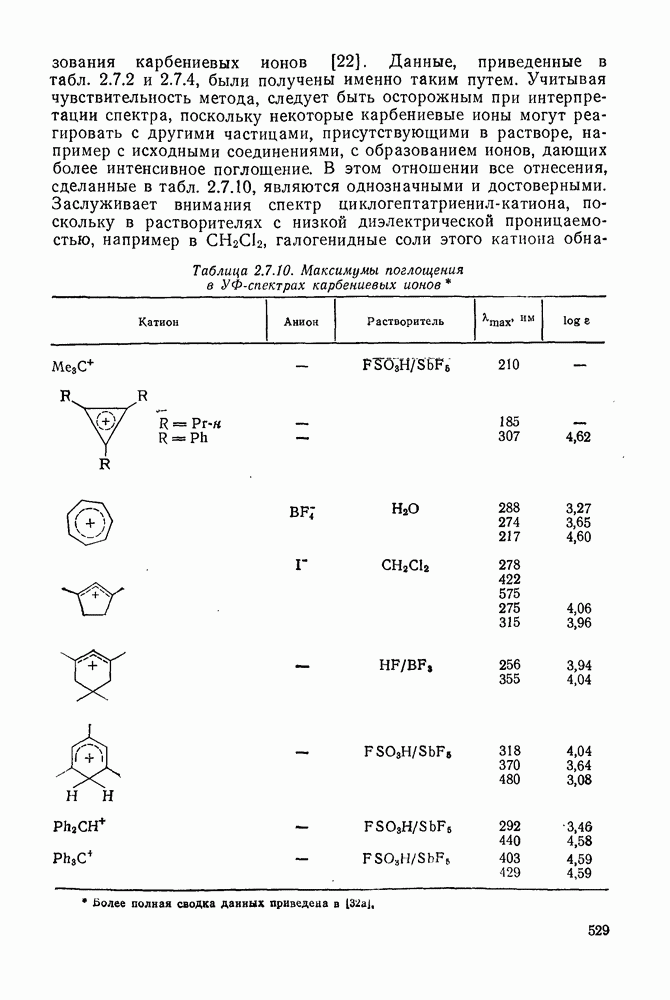
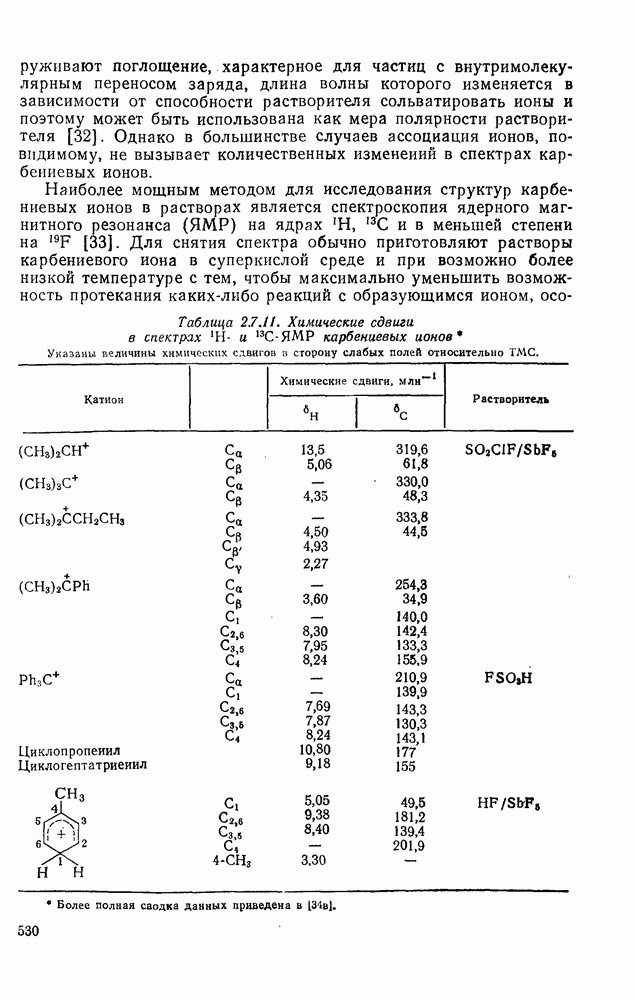
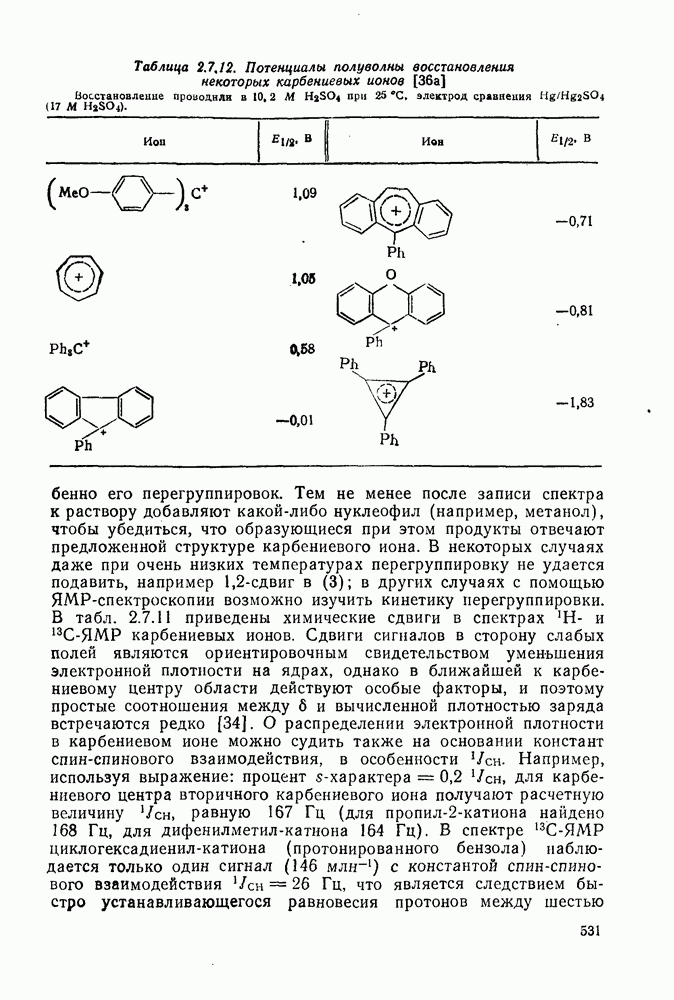
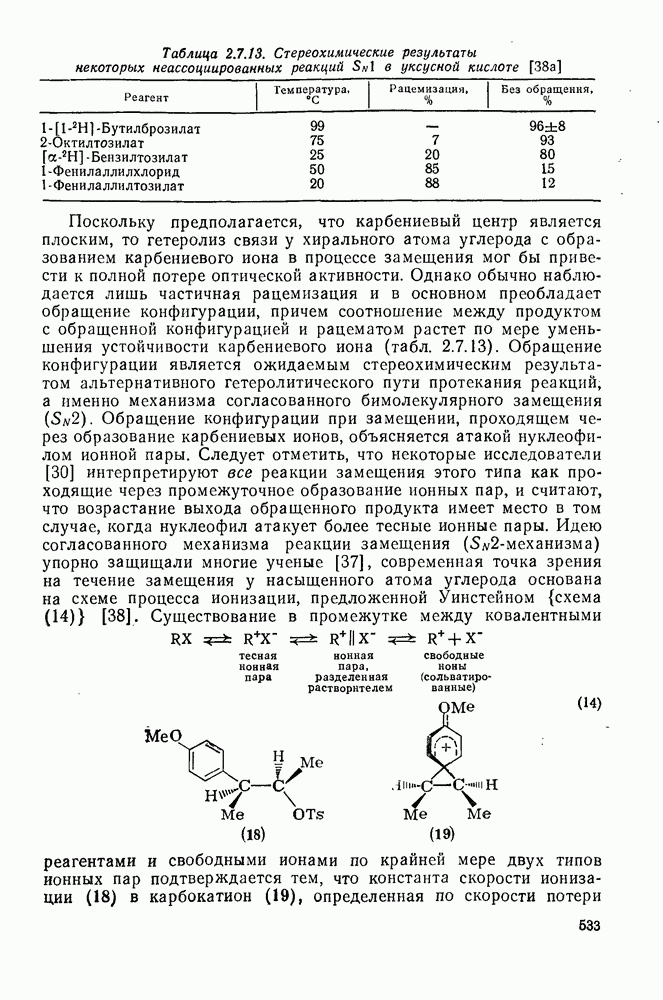
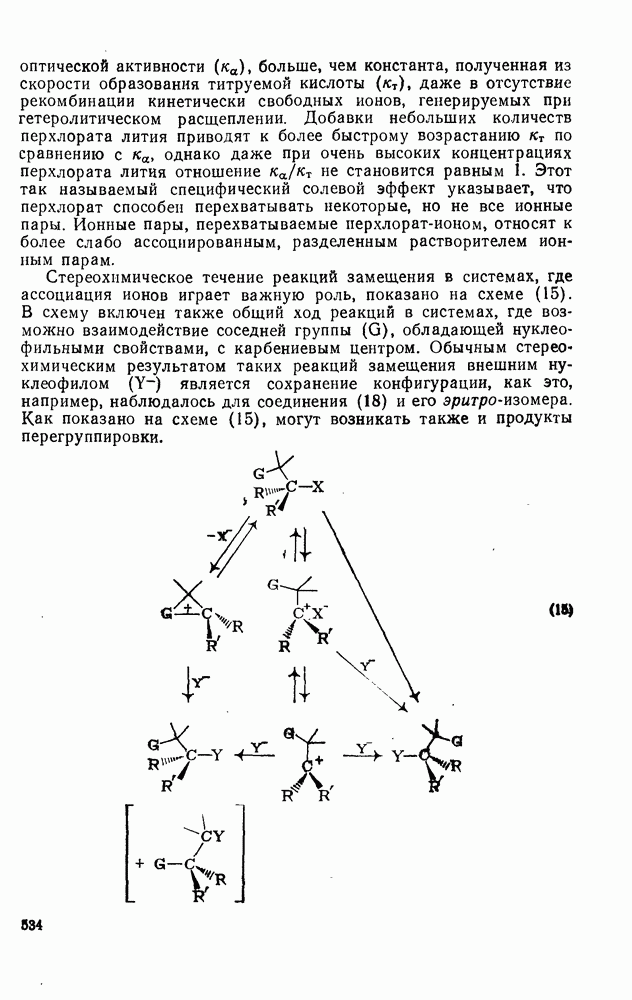
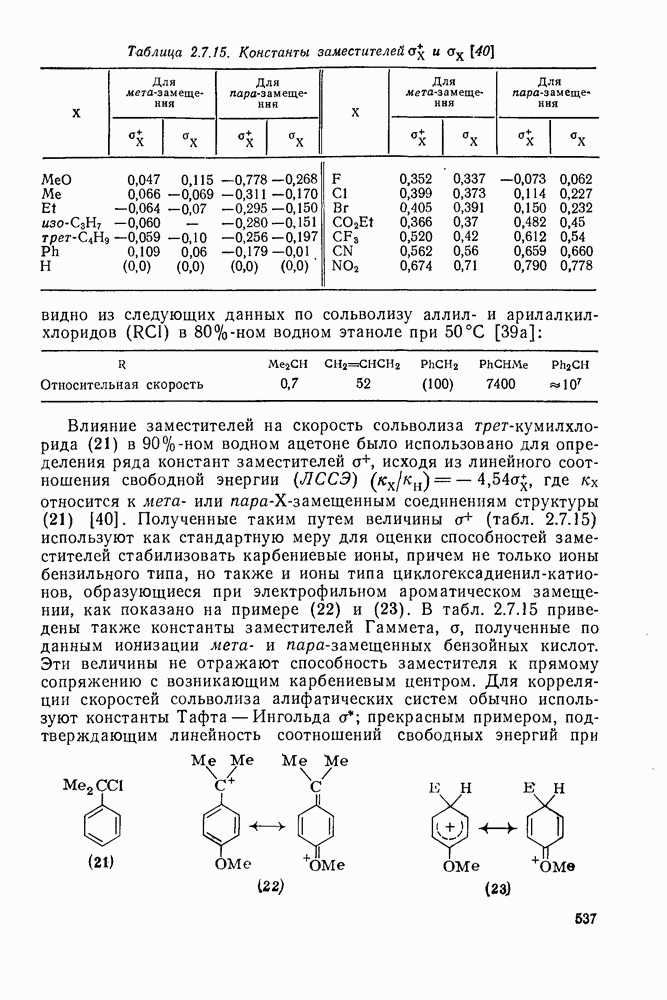
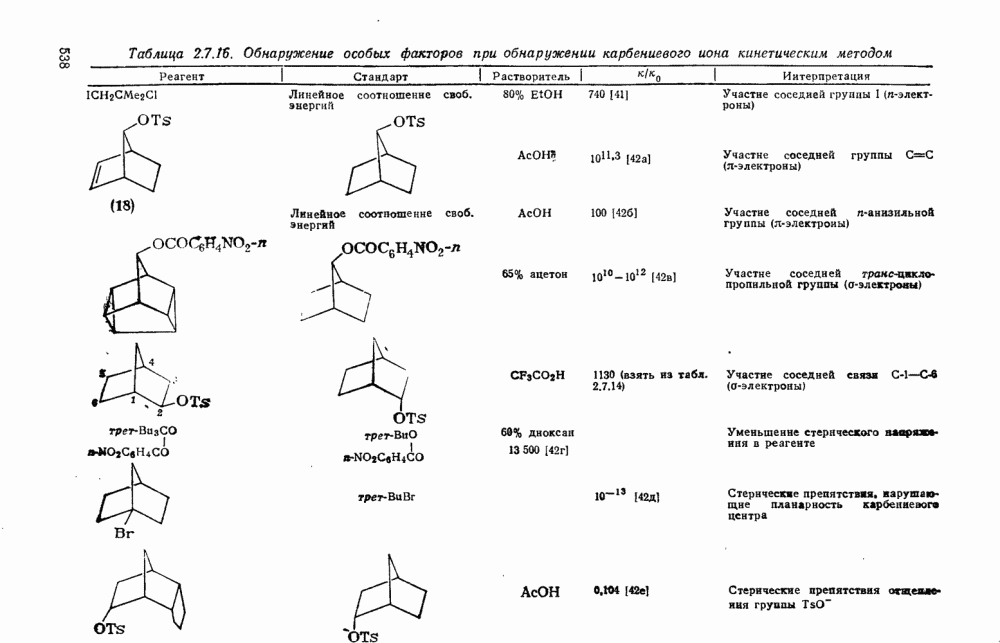
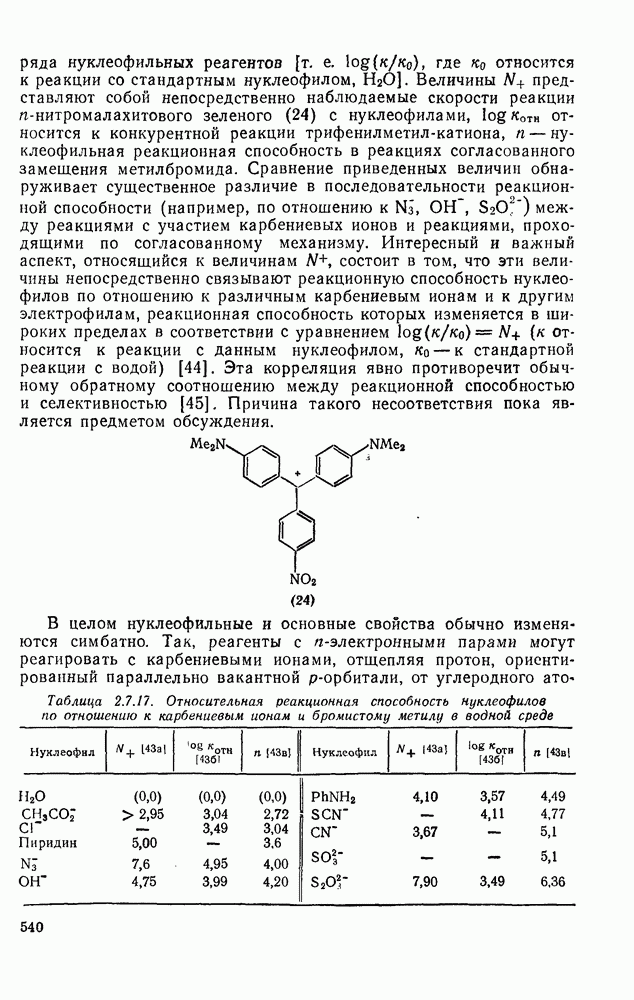
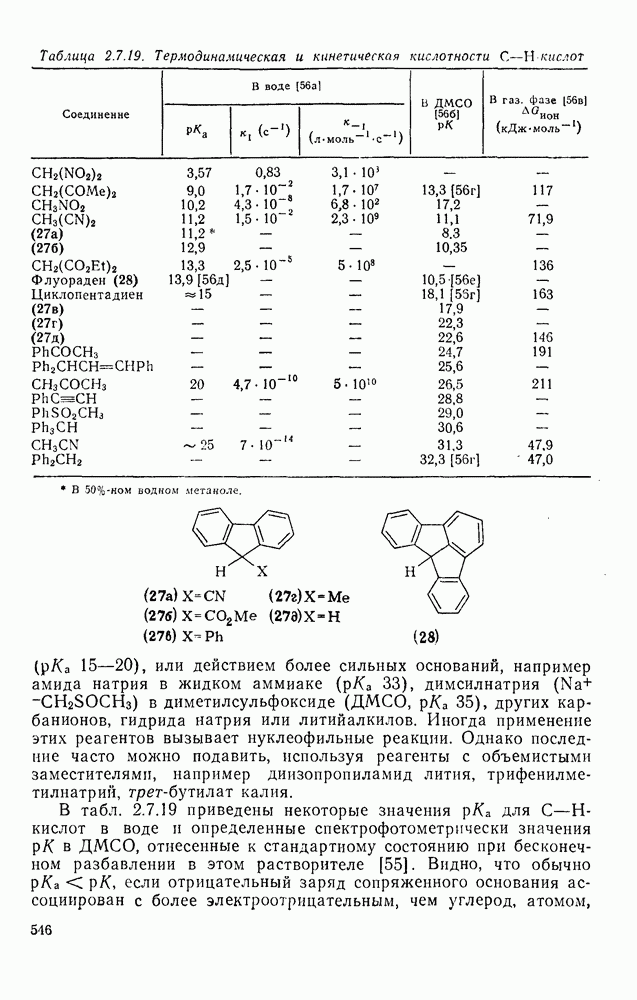
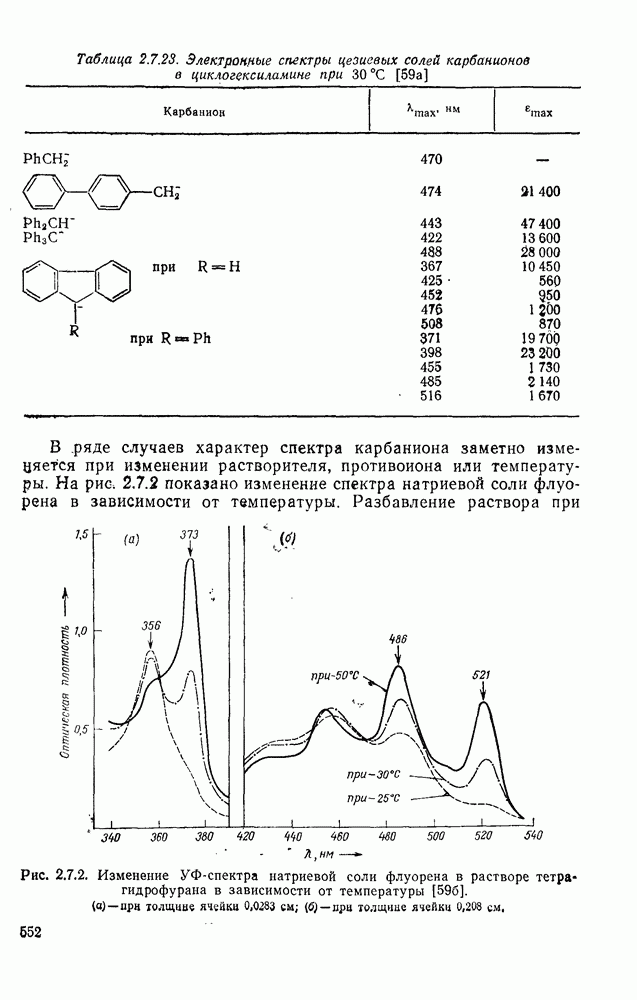
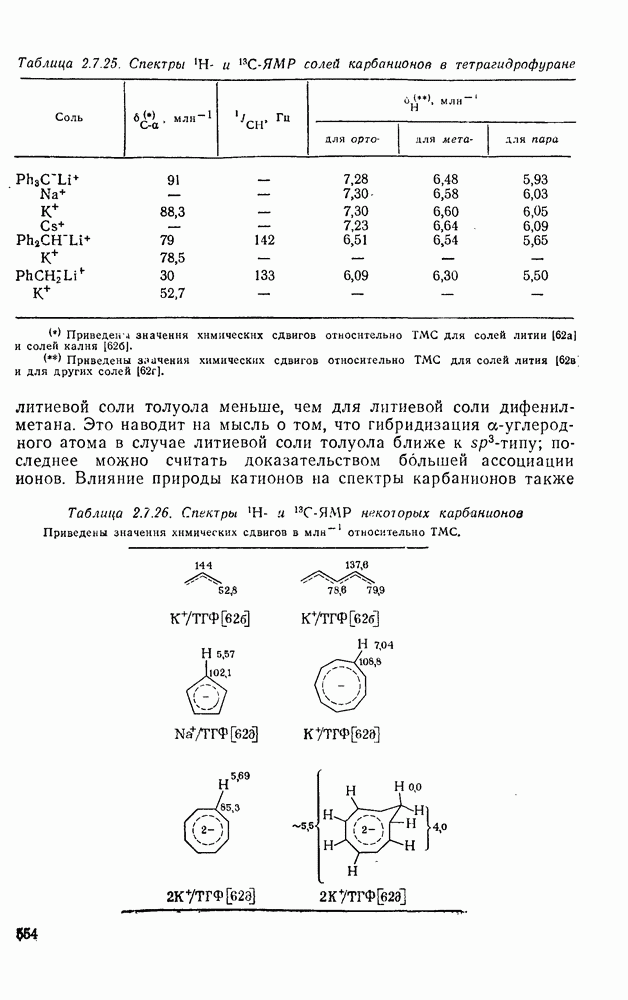
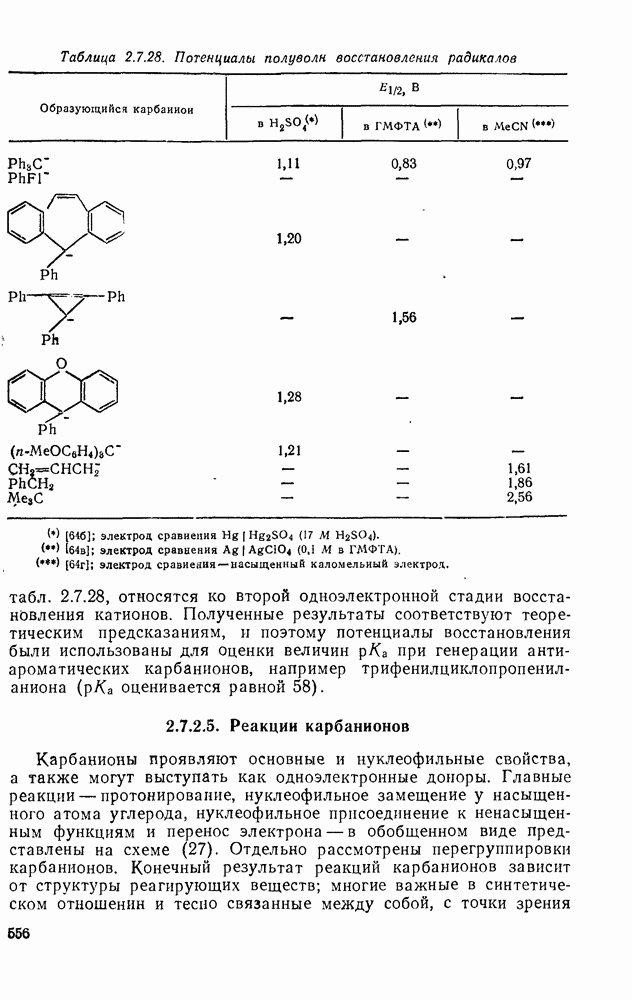
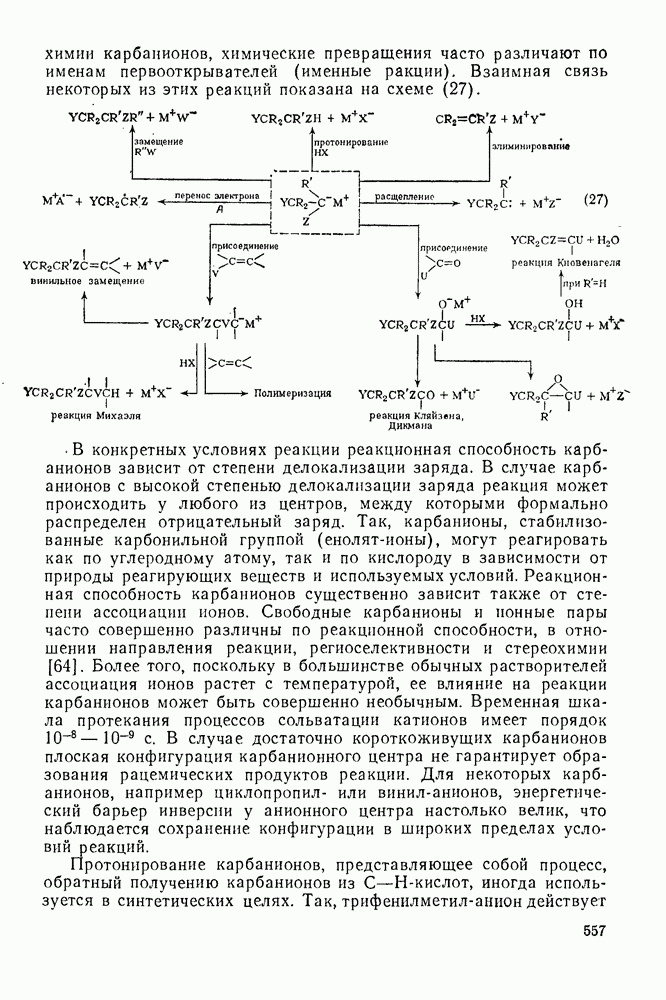
- 2.7. КАРБОКАТИОНЫ И КАРБАНИОНЫ
- 2.7.1.2. Краткий исторический очерк развития химии карбокатионов
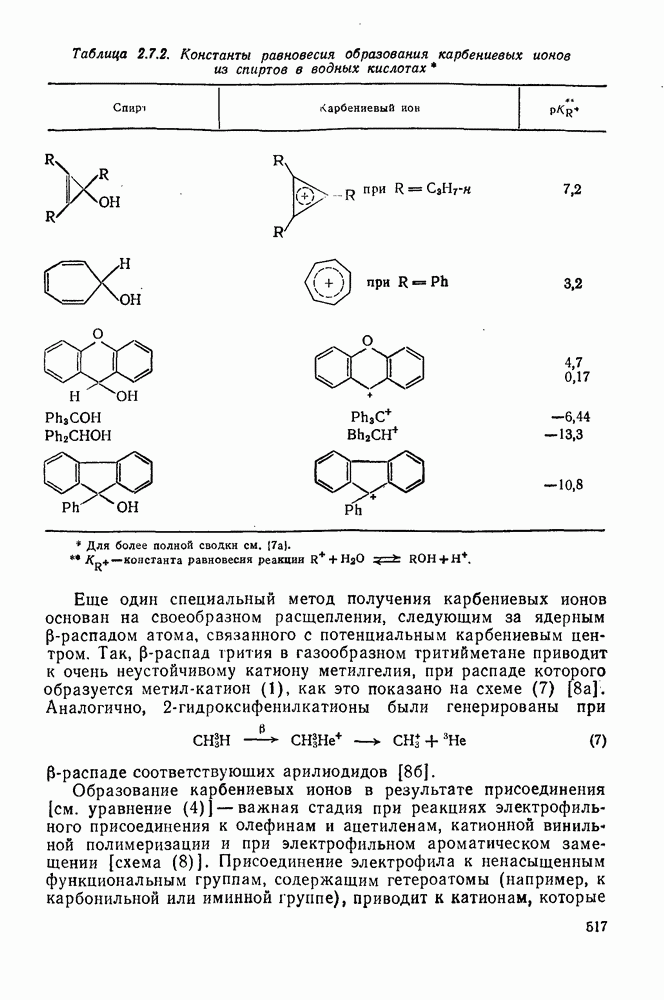
- 2.7.1.3. Методы генерации карбокатионов
- 2.7.1.4. Типы карбокатионов
- 2.7.1.5. Изучение карбокатионов: методы и результаты
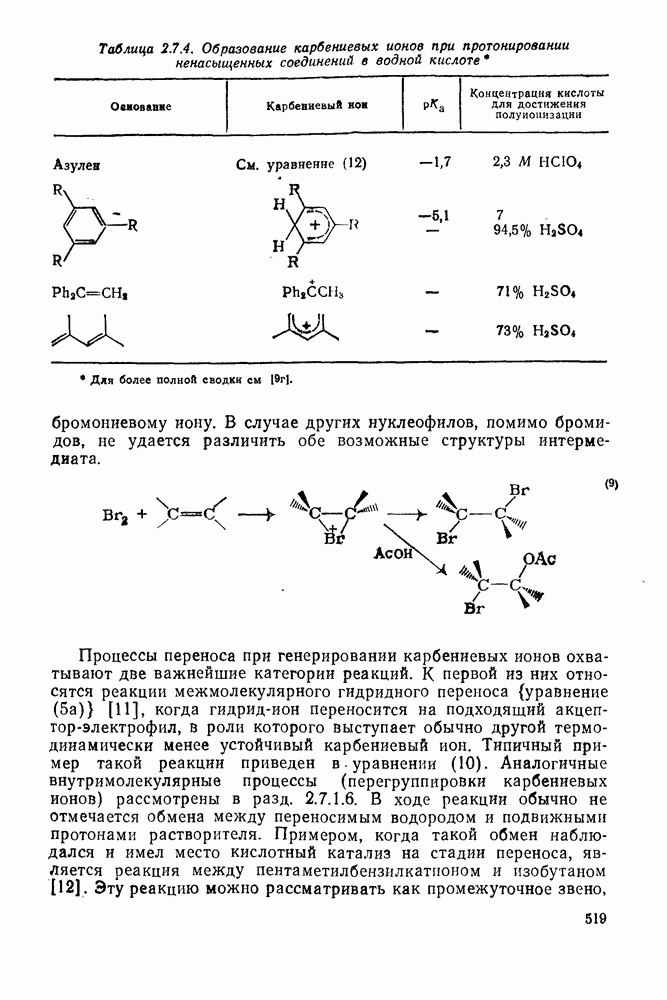
- 2.7.1.6. Реакции карбокатионов
- 2.7.2. КАРБАНИОНЫ
- 2.7.2.2. Методы генерации карбанионов
- 2.7.2.3. Типы карбанионов
- 2.7.2.4. Физические свойства карбанионов
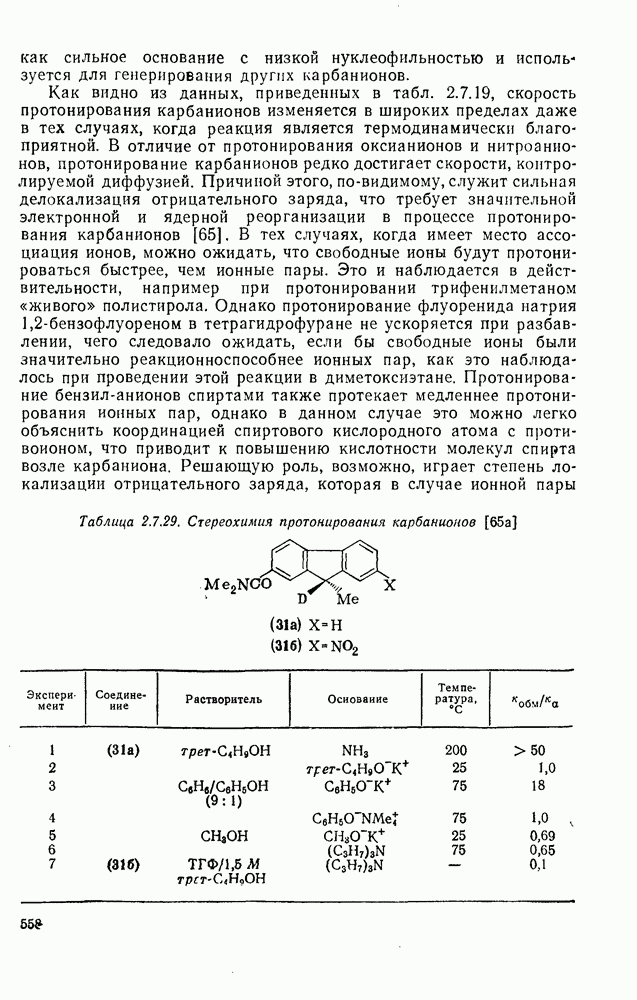
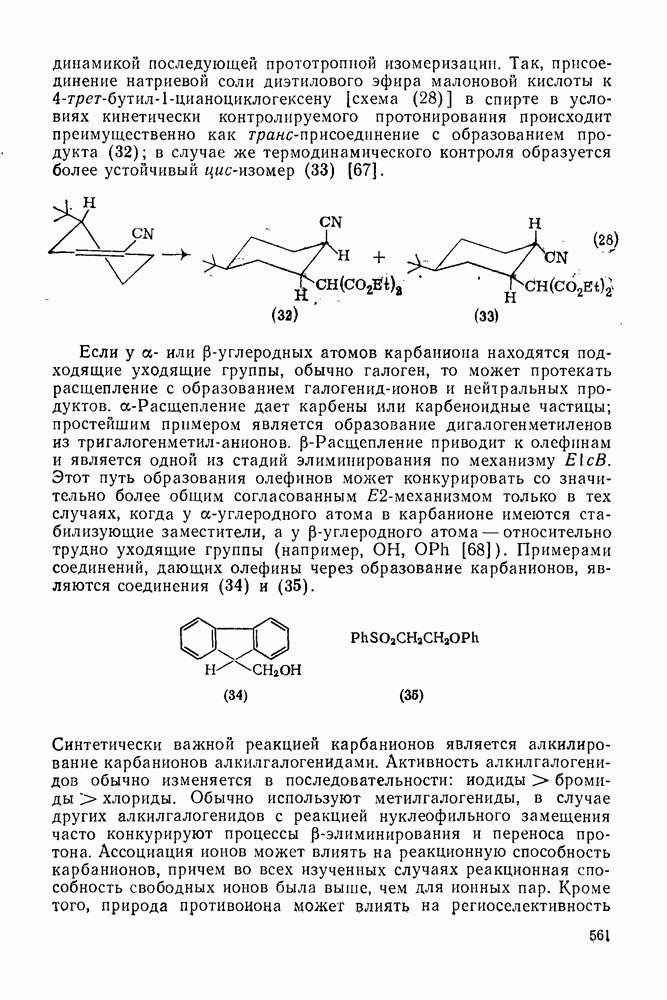
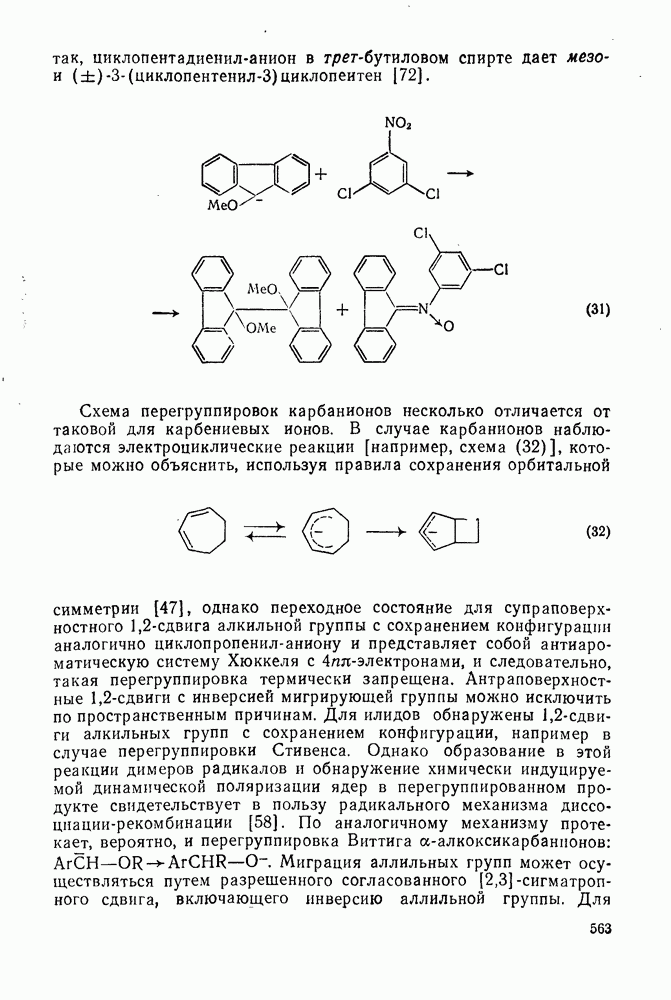
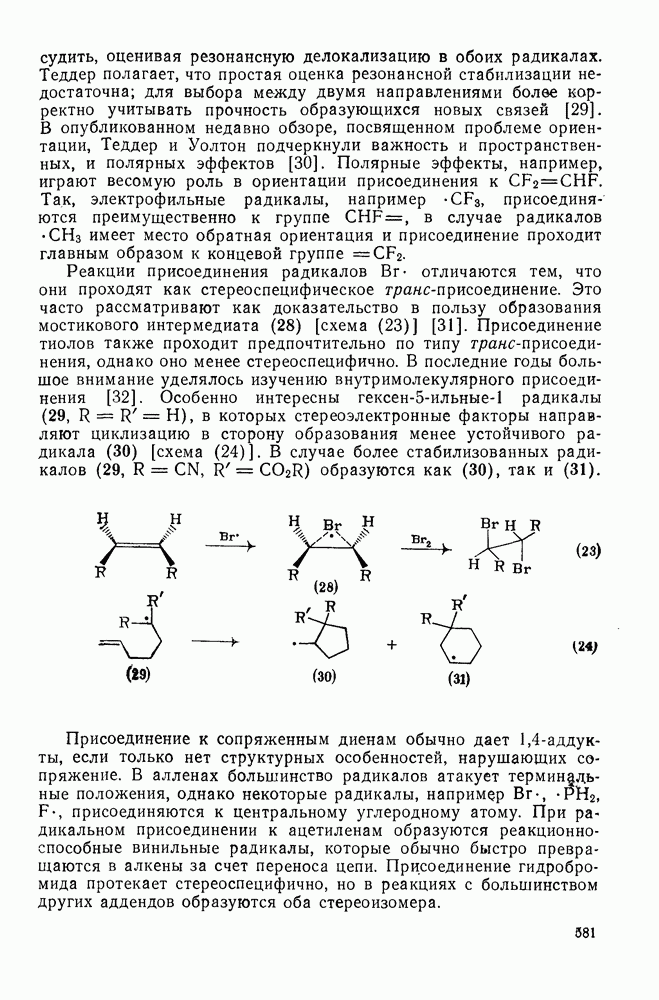
- 2.7.5.2. Реакции карбанионов
- 2.8. РАДИКАЛЫ, КАРБЕНЫ, АРИНЫ
- 2.8.1. РАДИКАЛЫ
- 2.8.1.1. Структура, устойчивость и реакционная способность радикалов
- 2.8.1.2. Методы генерации и реакции радикалов
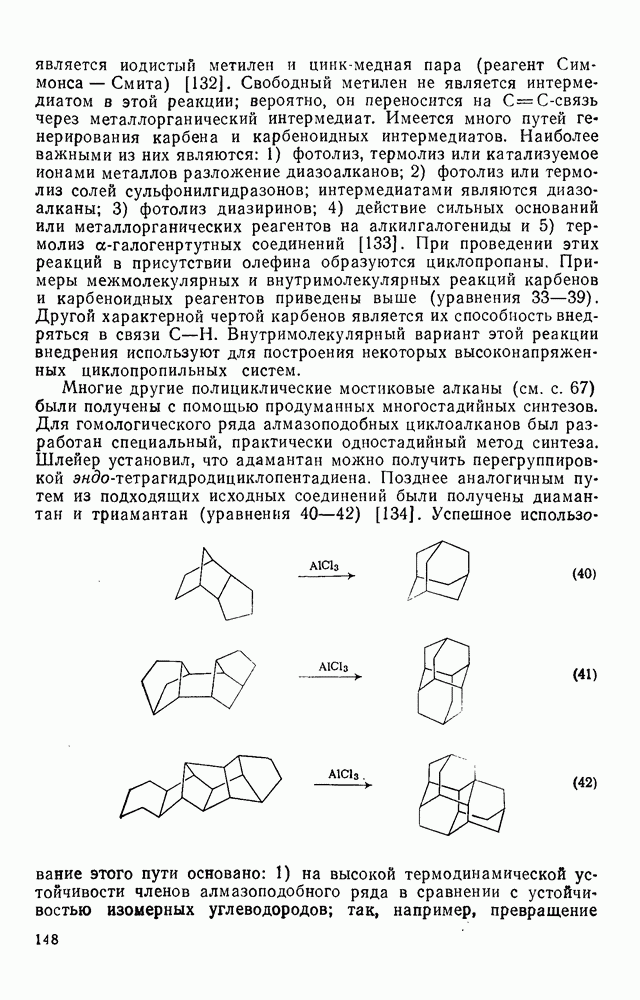
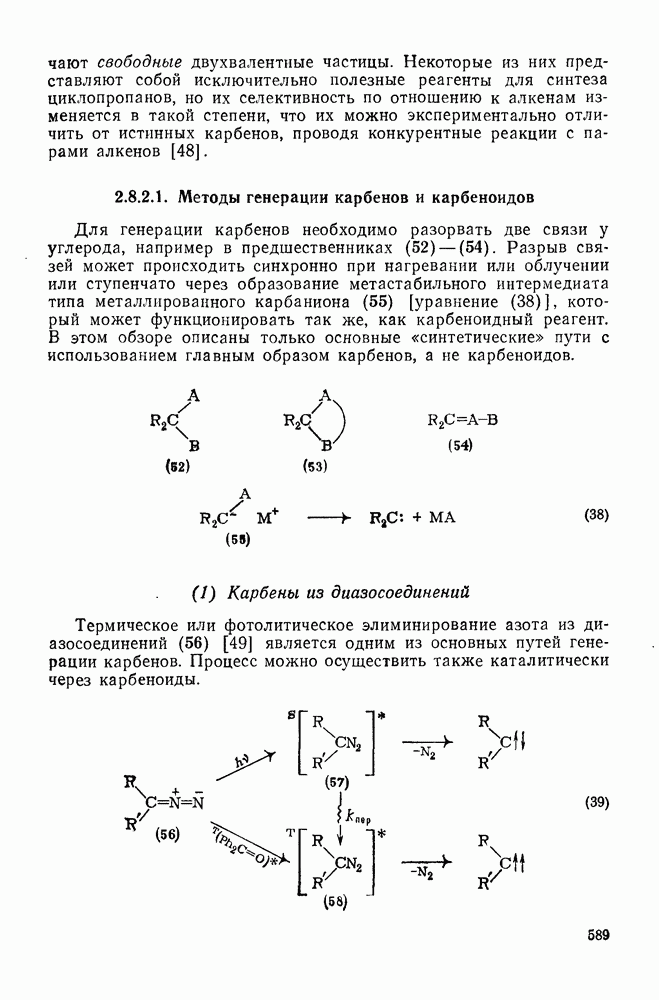
- 2.8.2. КАРБЕНЫ
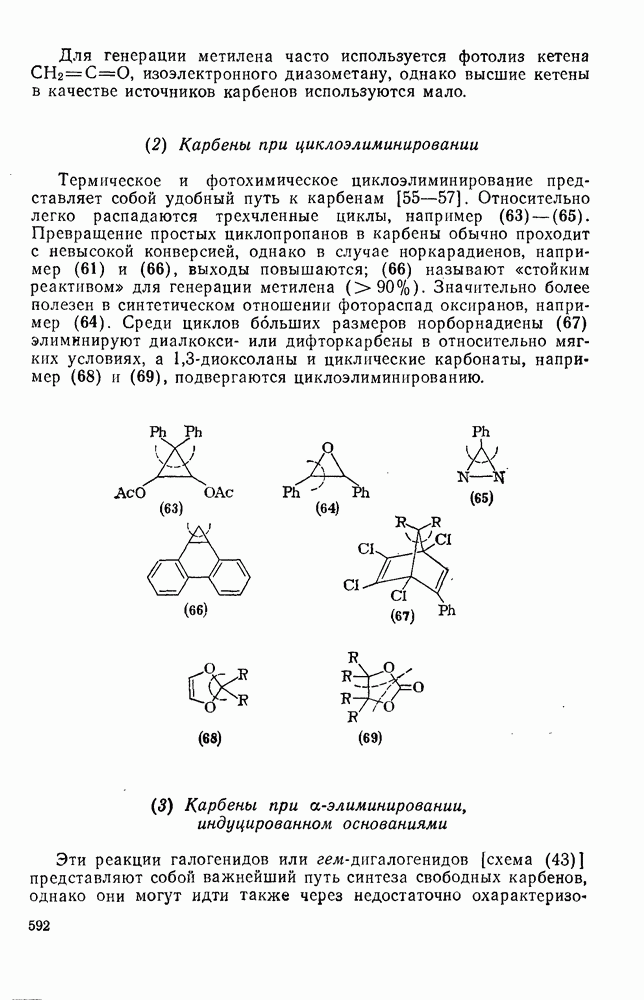
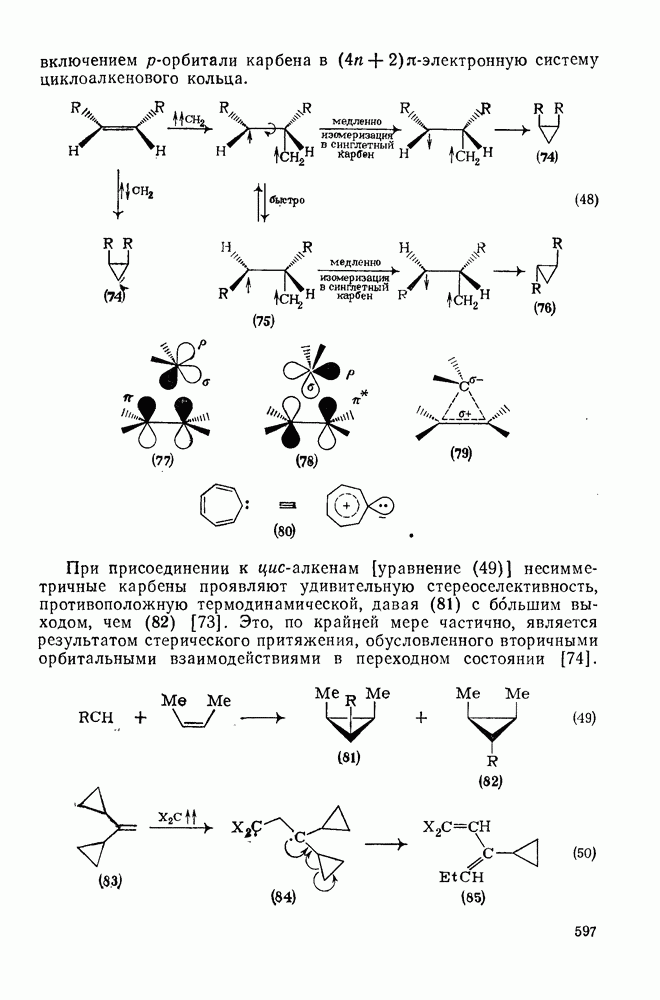
- 2.8.2.1. Методы генерации карбенов и карбеноидов
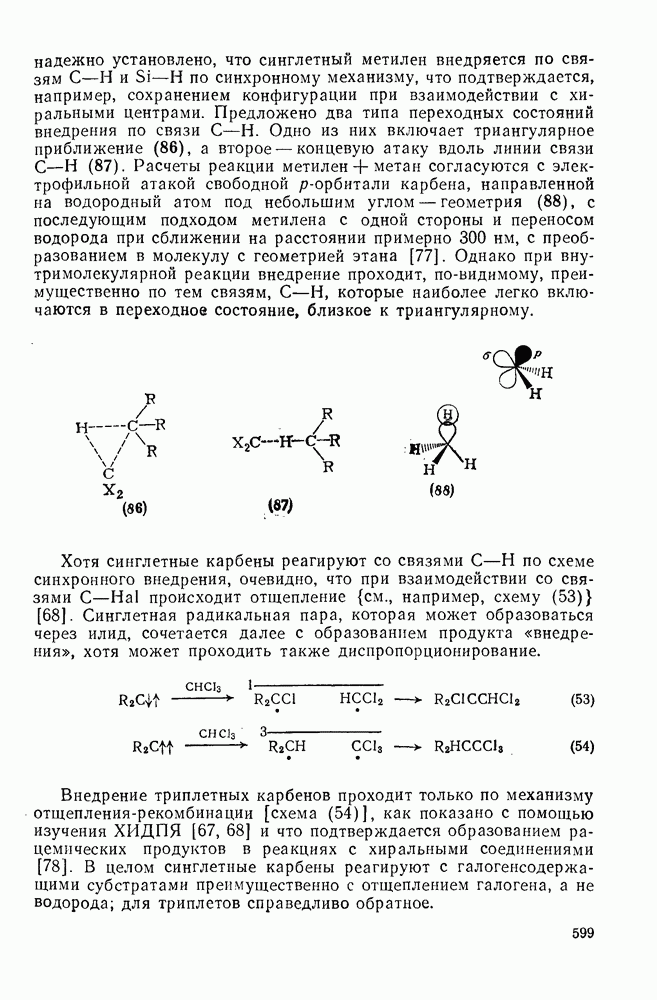
- 2.8.2.2. Реакции карбенов
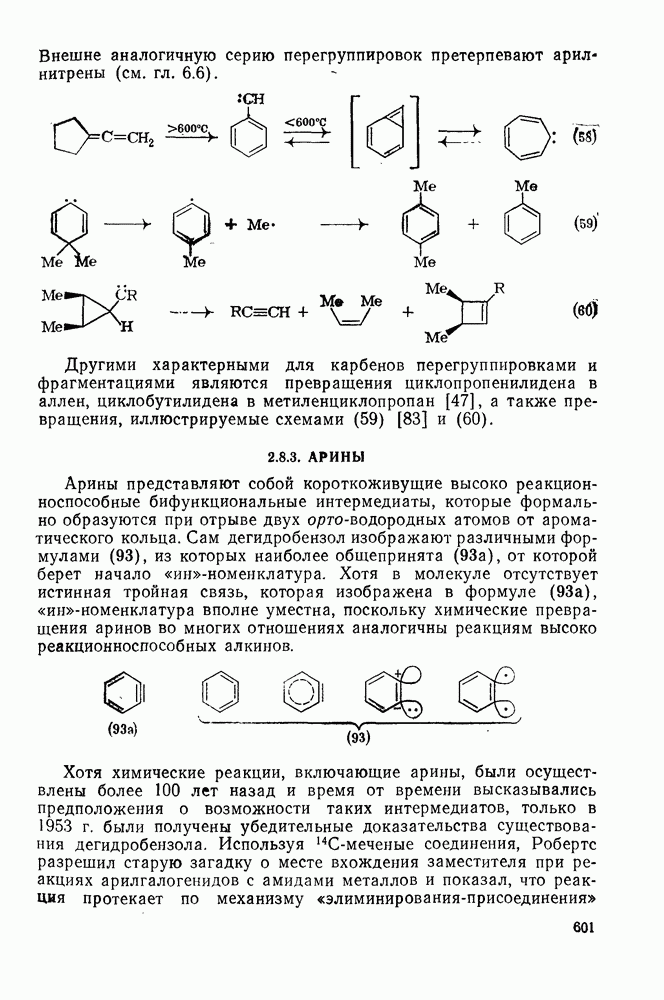
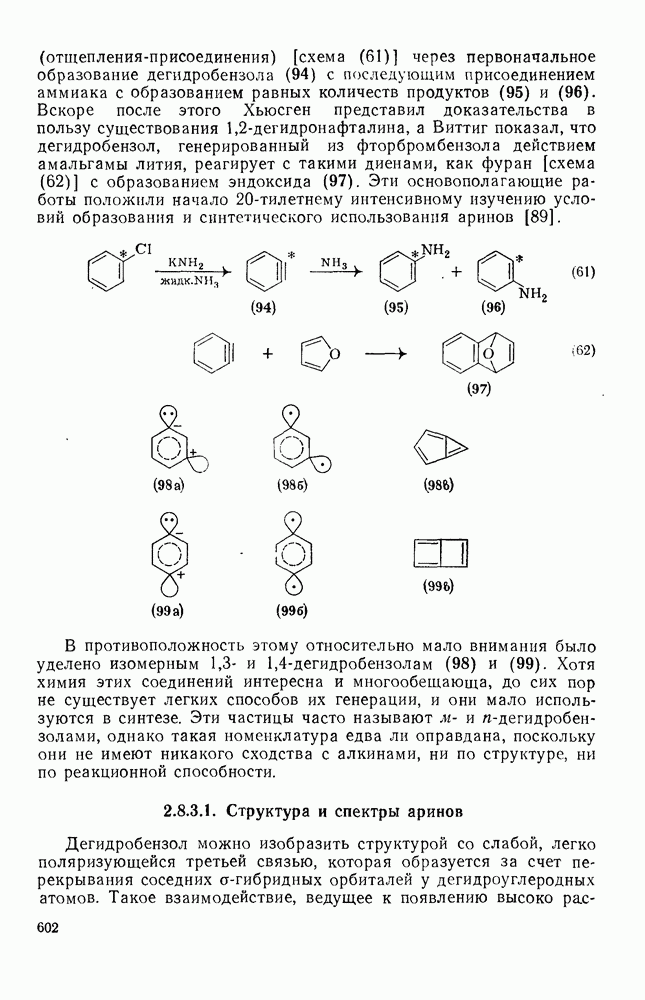
- 2.8.3. АРИНЫ
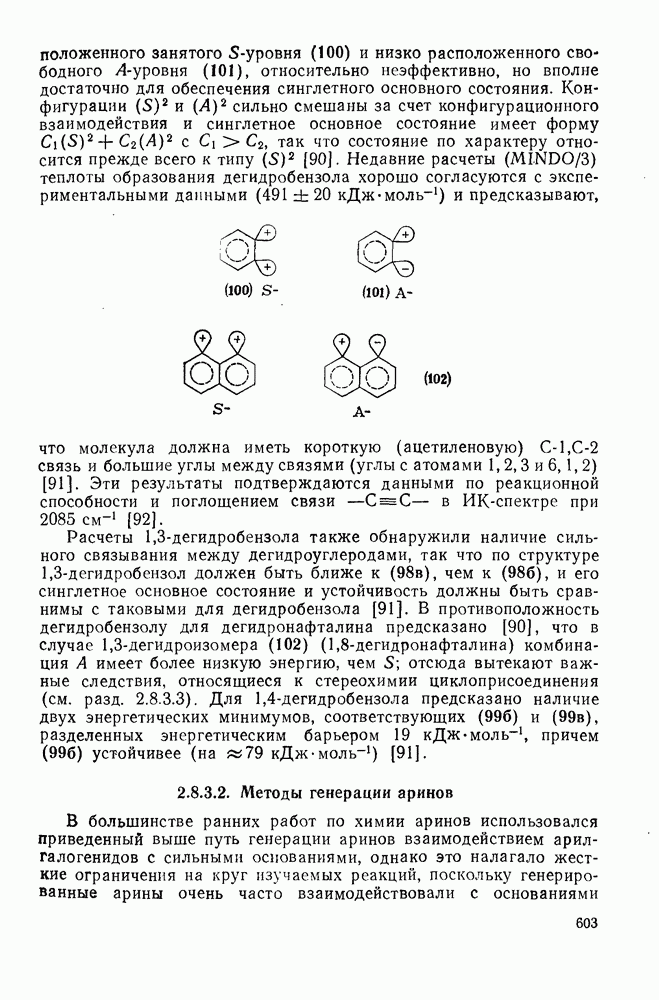
- 2.8.3.1. Структура и спектры аринов
- 2.8.3.2. Методы генерации аринов
- 2.8.3.3. Реакции аринов
- ЧАСТЬ 3. ГАЛОГЕНСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
- 3.2. МЕТОДЫ ГАЛОГЕНИРОВАНИЯ
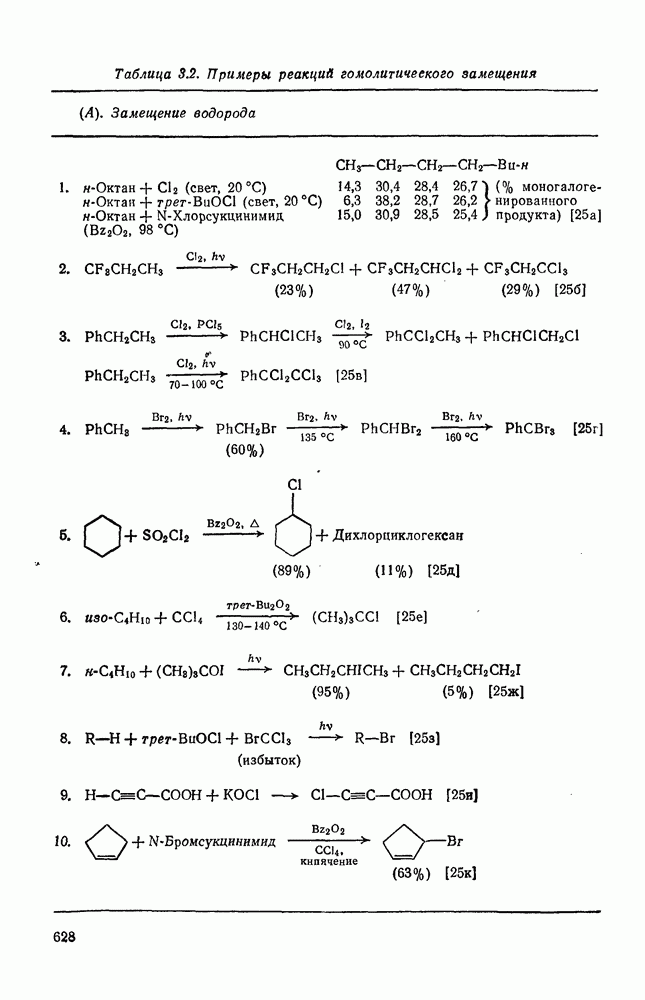
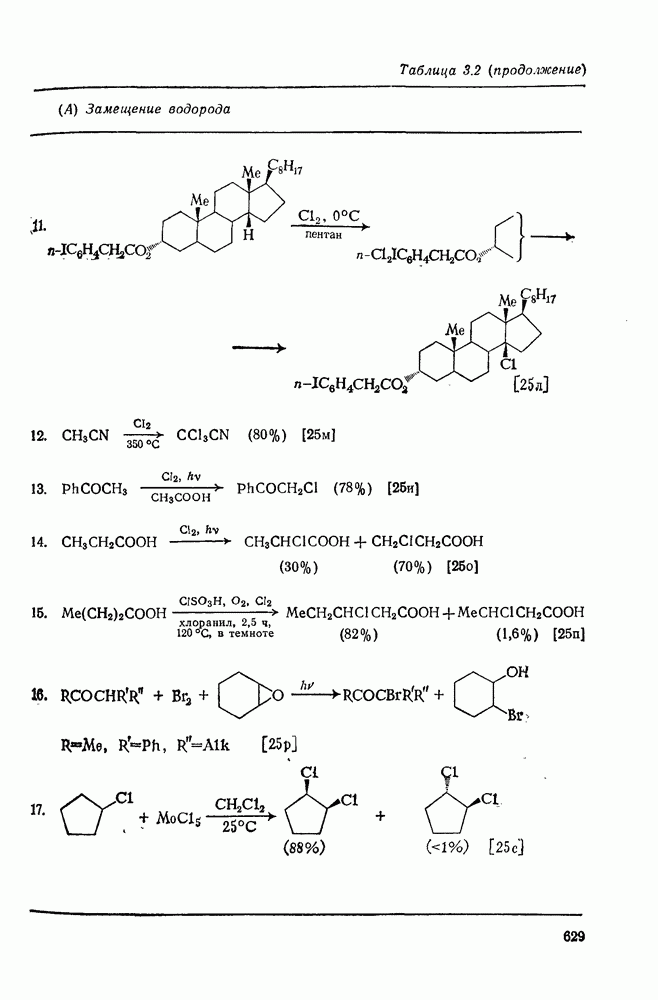
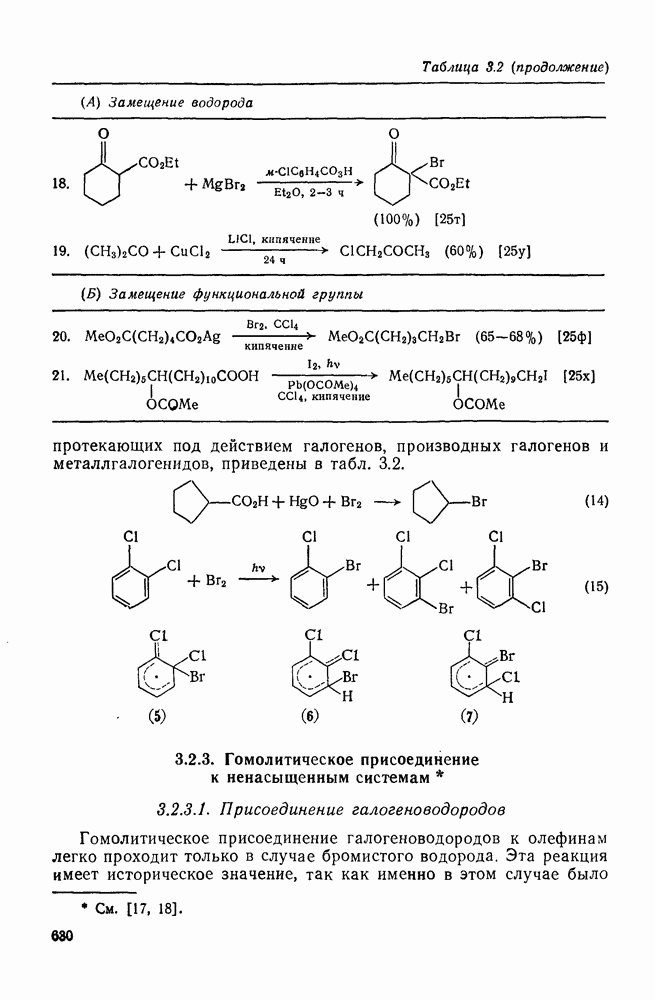
- 3.2.1. Гомолитическое замещение водорода
- 3.2.1.2. Использование галогенпроизводных в качестве реагентов
- 3.2.2. Гомолитическое замещение функциональных групп
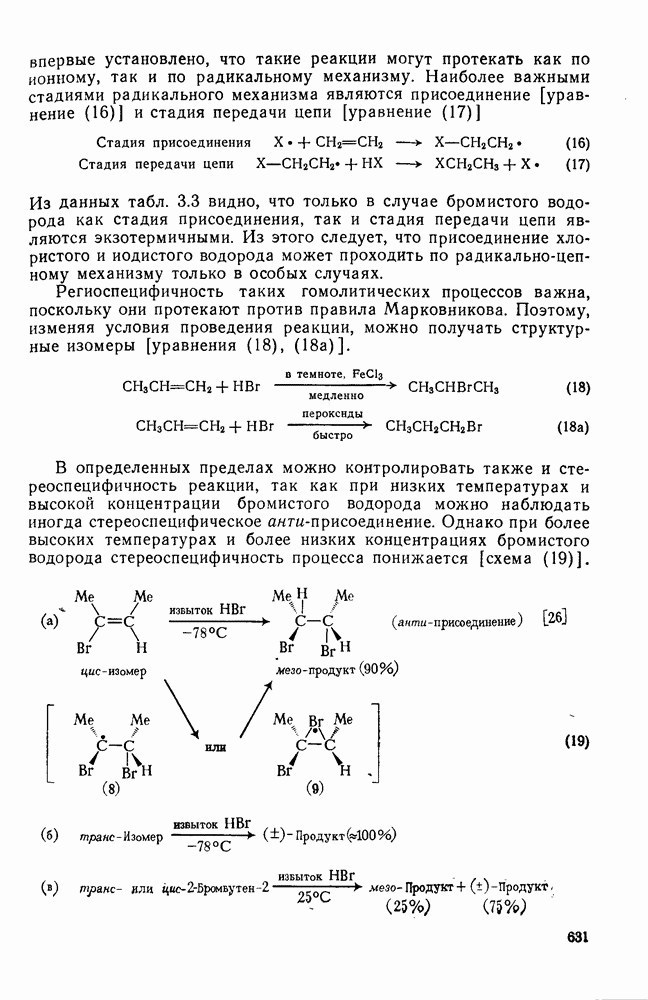
- 3.2.3. Гомолитическое присоединение к ненасыщенным системам
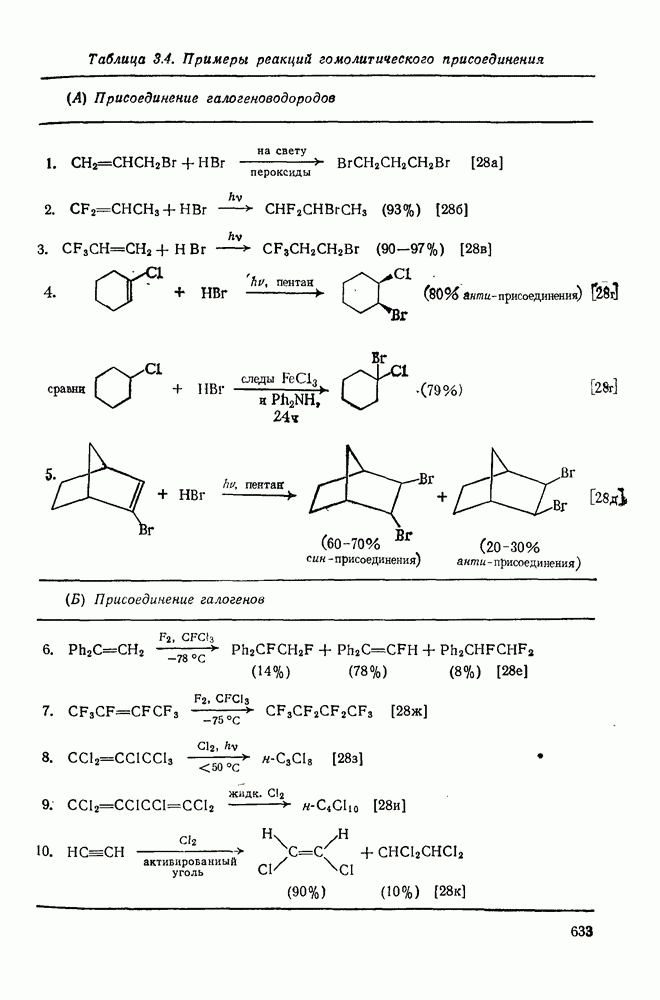
- 3.2.3.1. Присоединение галогеноводородов
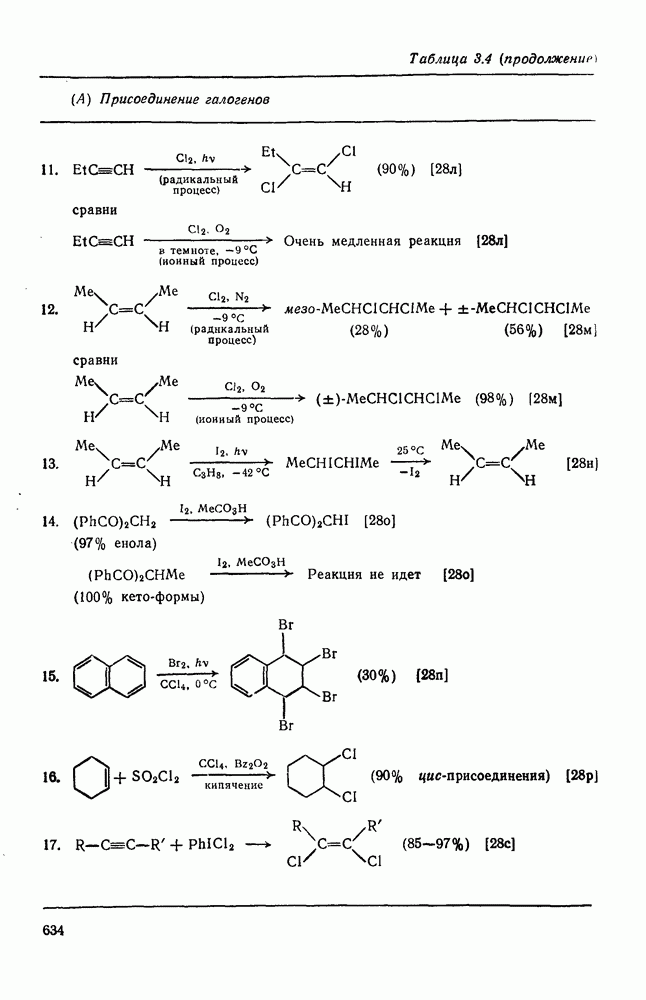
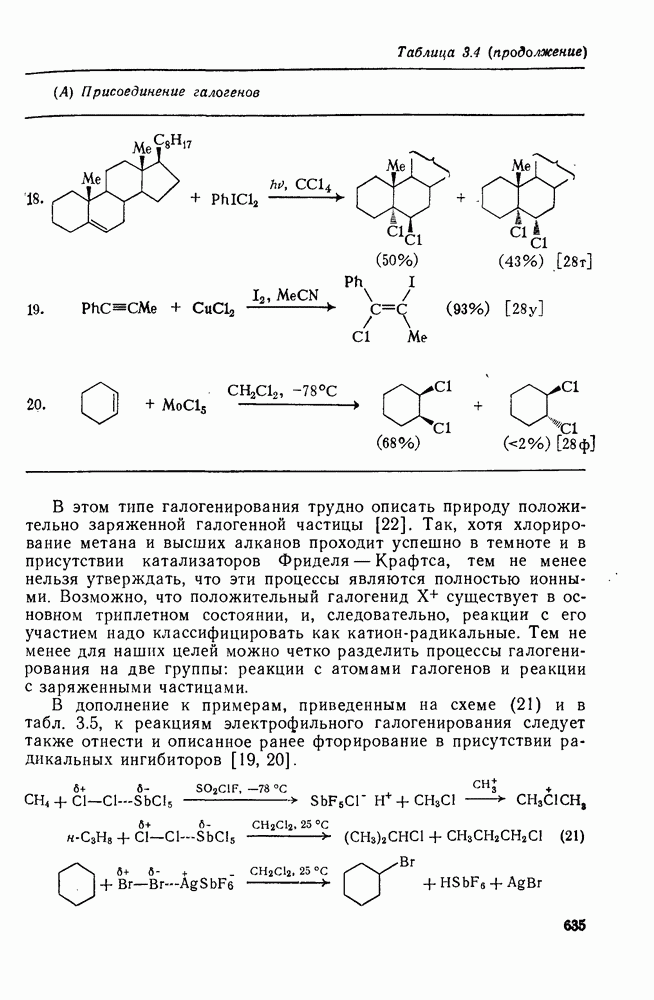
- 3.2.3.2. Присоединение галогенов
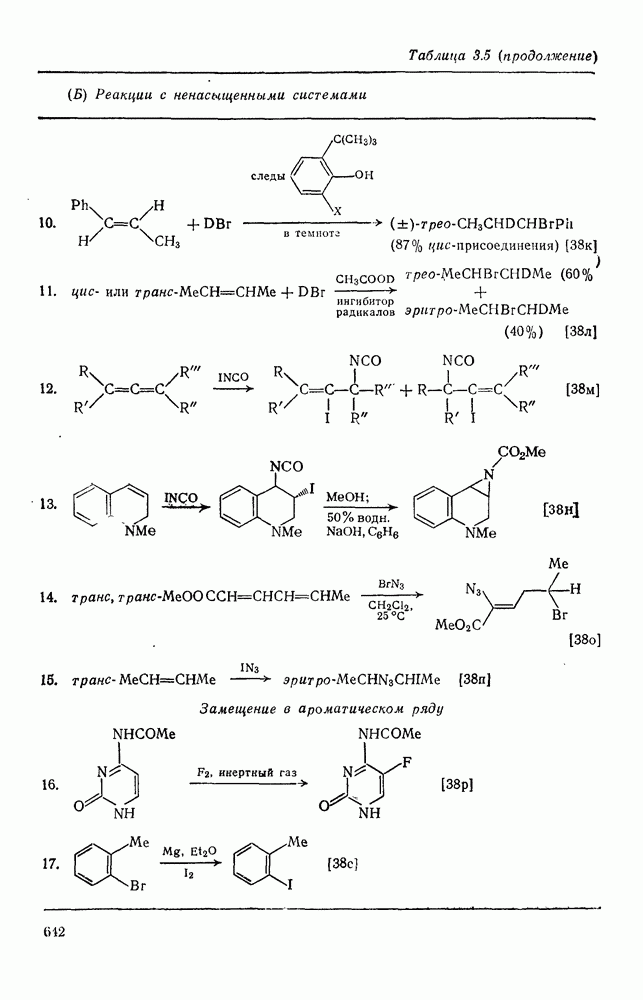
- 3.2.4. Электрофильное галогенирование
- 3.2.4.1. Замещение у насыщенной связи С-Н
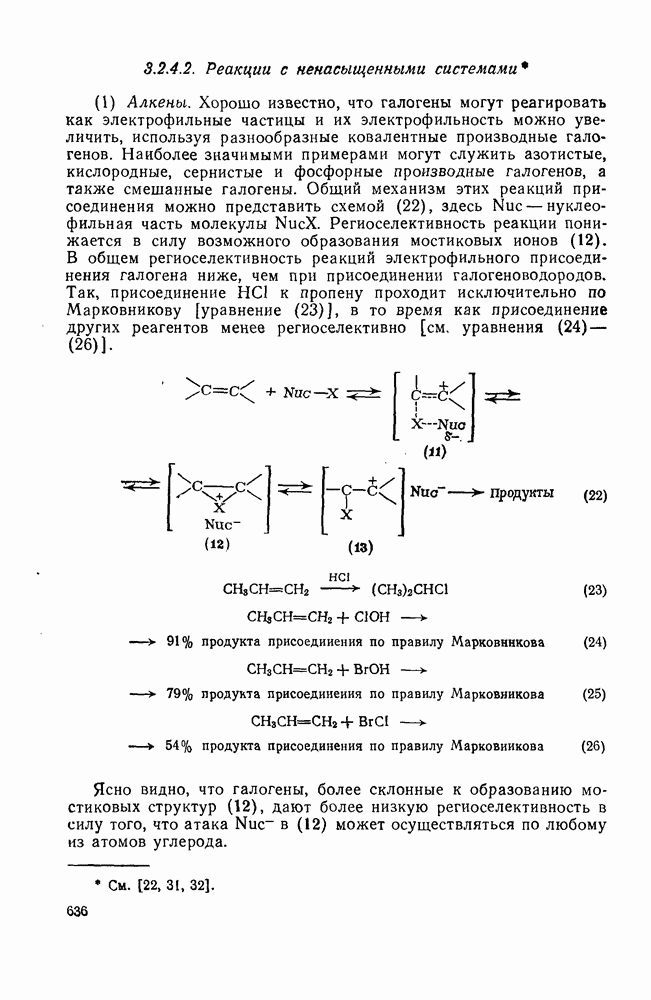
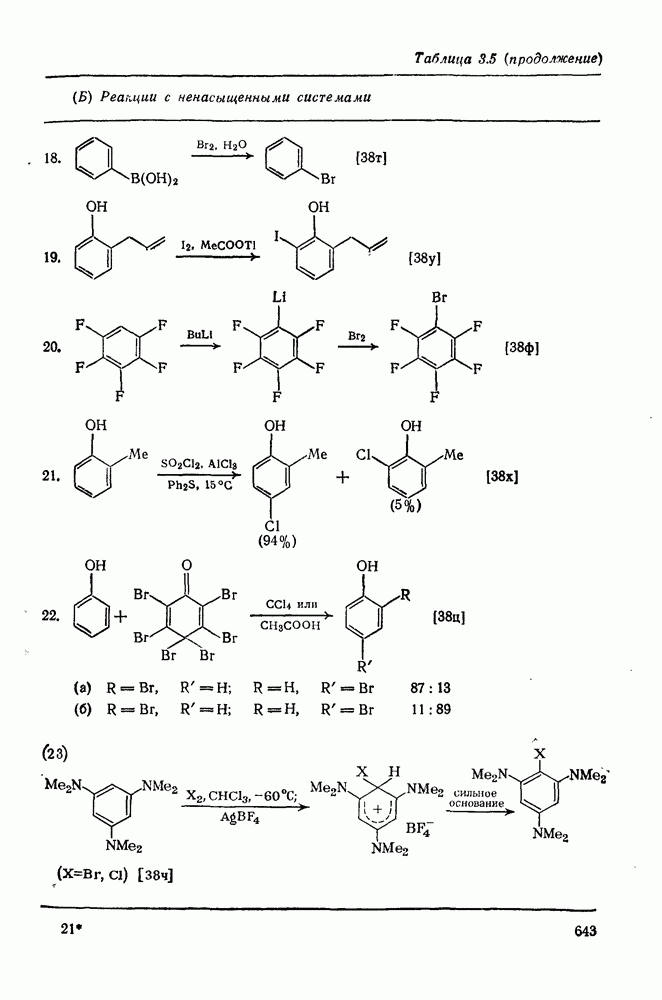
- 3.2.4.2. Реакции с ненасыщенными системами
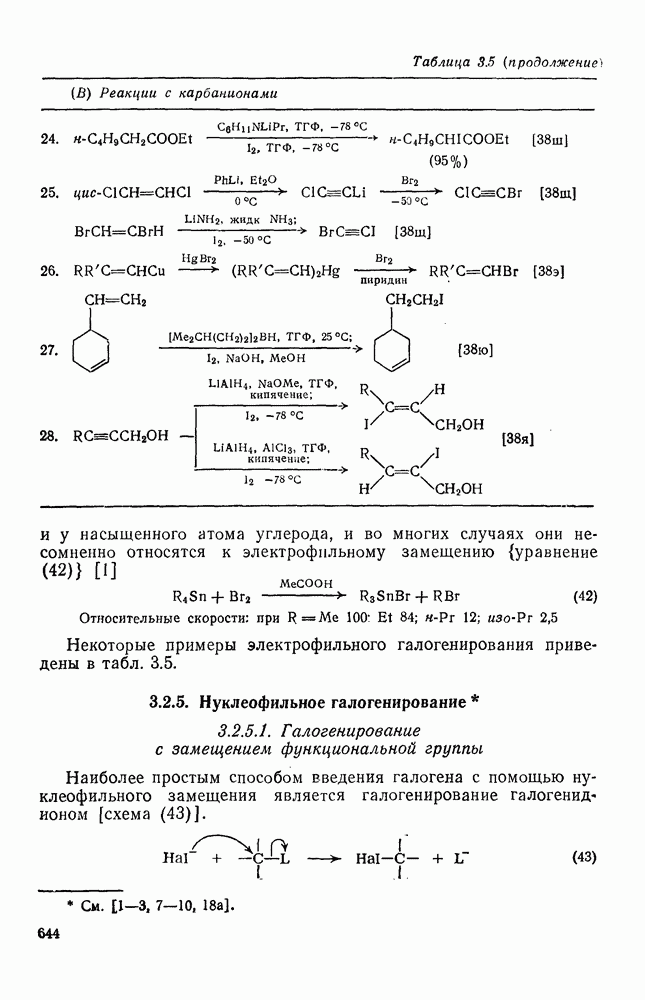
- 3.2.4.3. Реакции с карбанионами
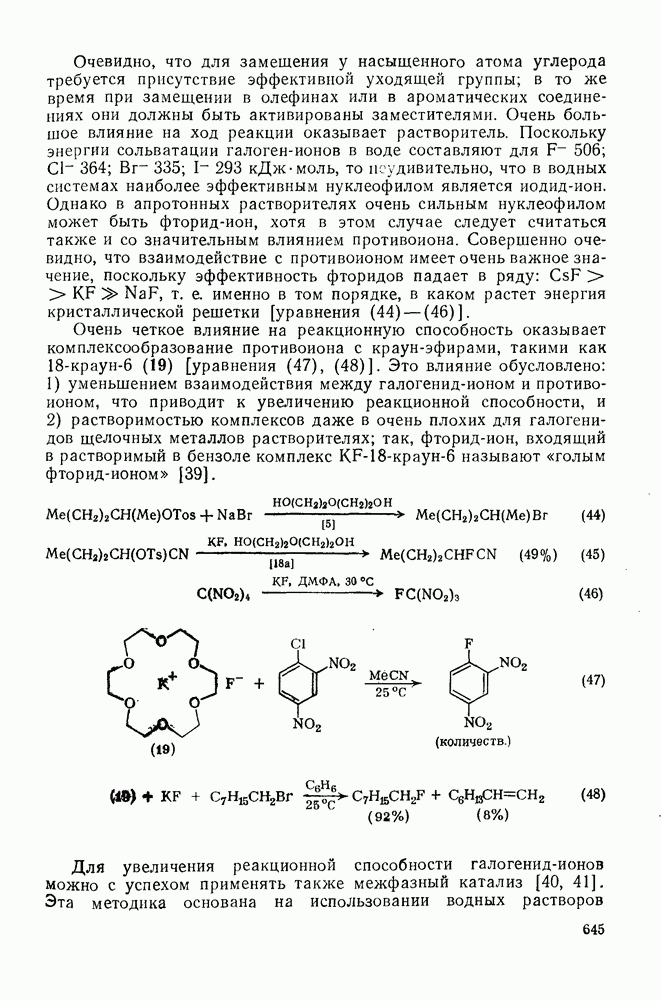
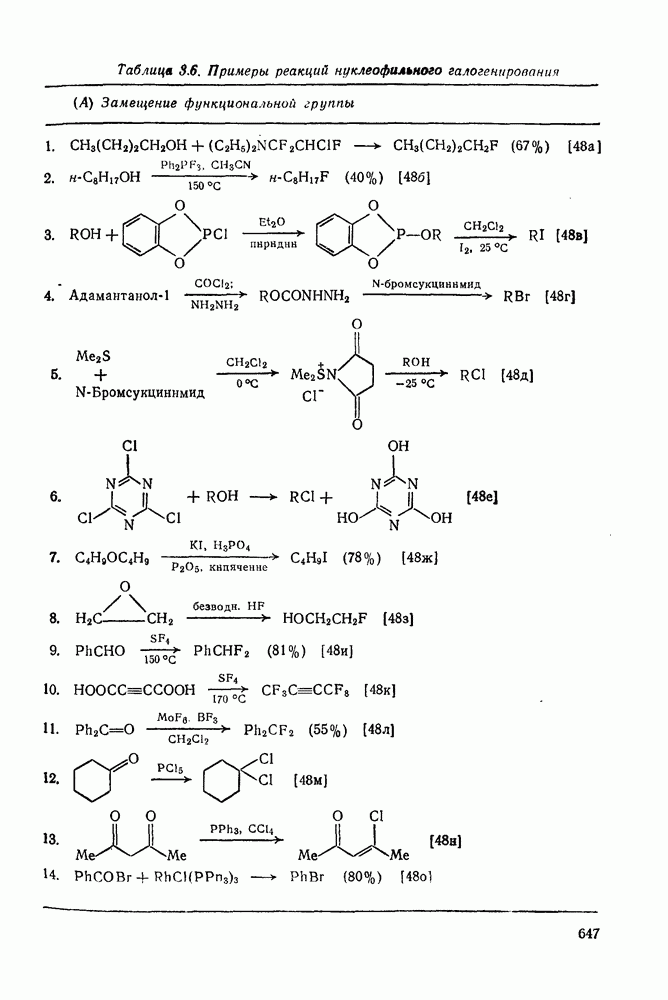
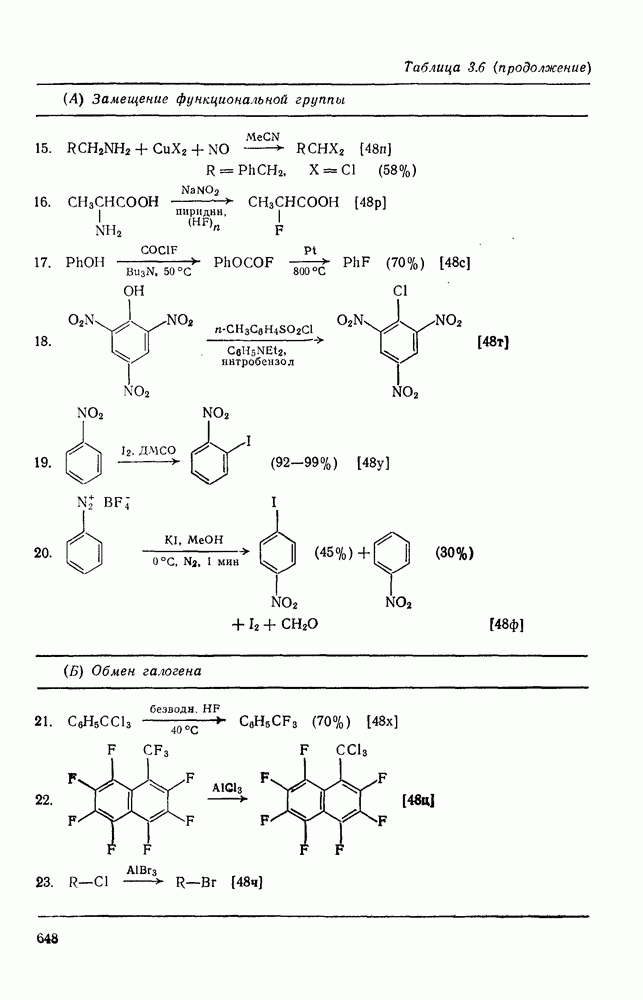
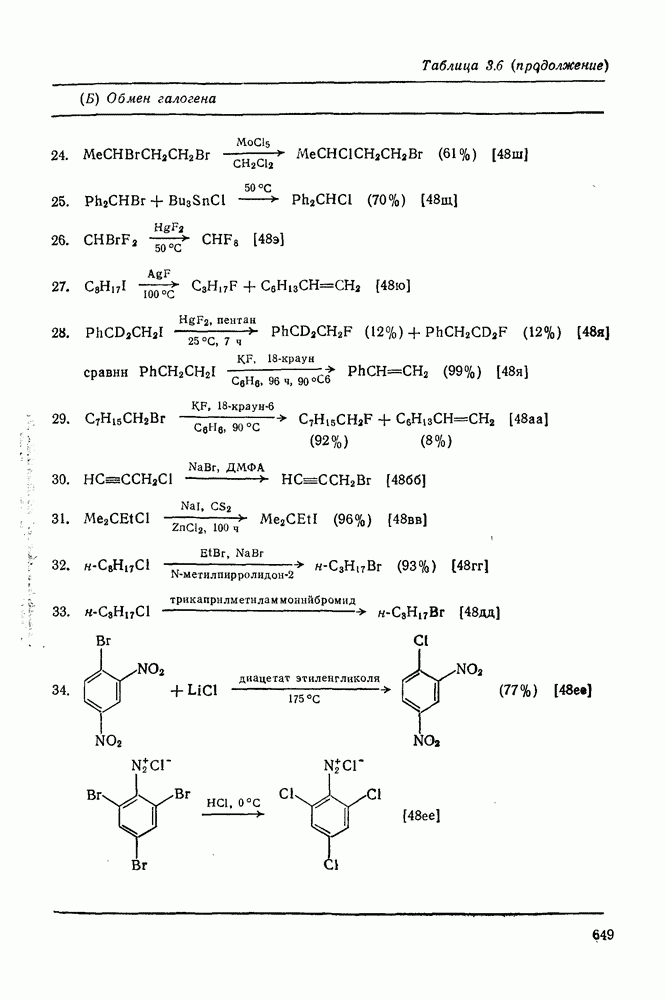
- 3.2.5. Нуклеофильное галогенирование
- 3.2.5.1. Галогенирование с замещением функциональной группы
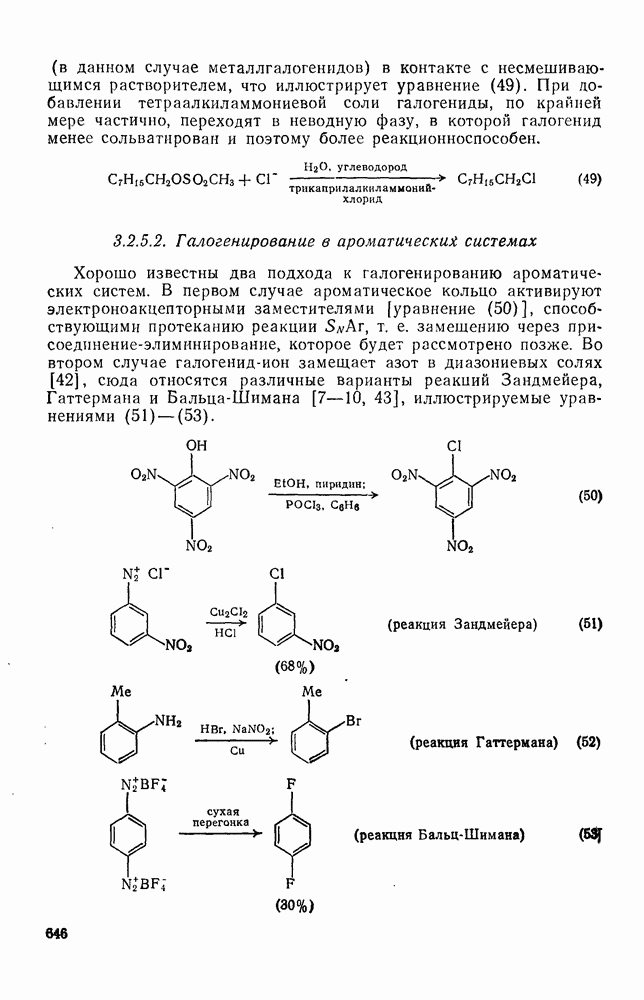
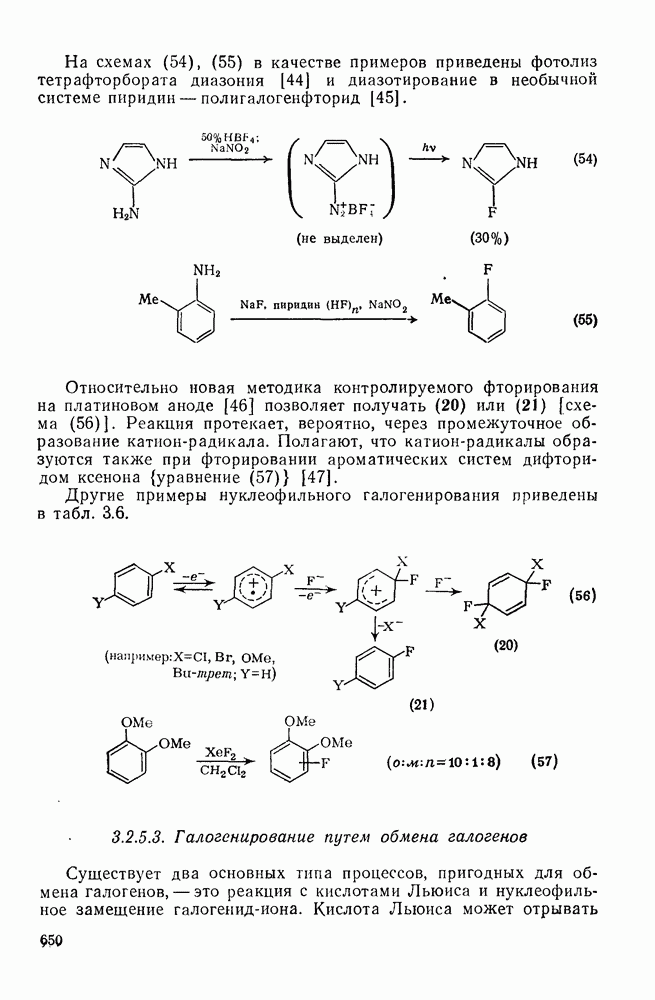
- 3.2.5.2. Галогенирование в ароматических системах
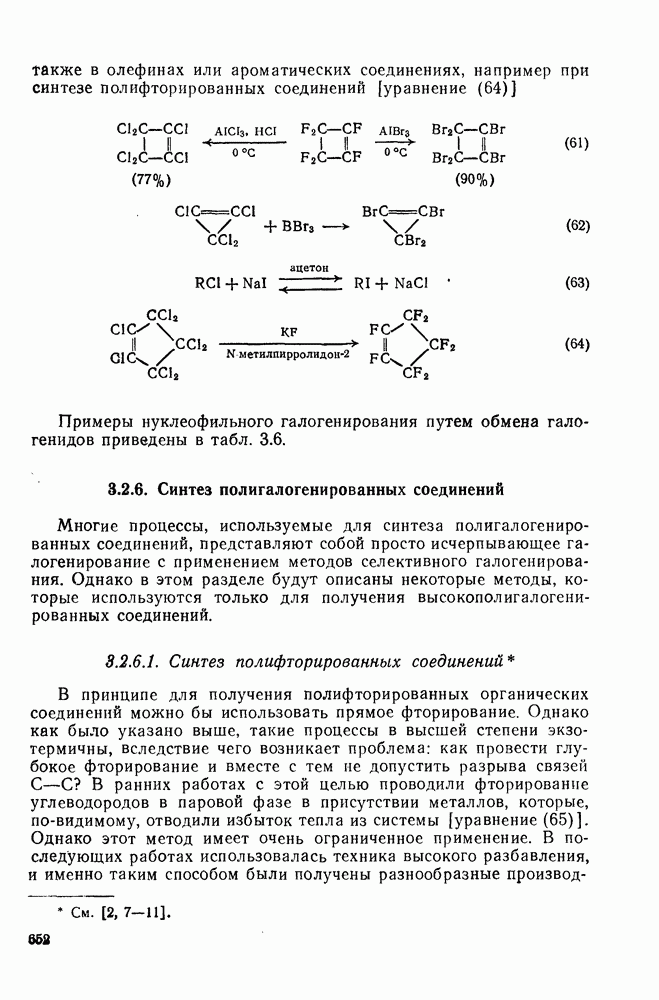
- 3.2.5.3. Галогенирование путем обмена галогенов
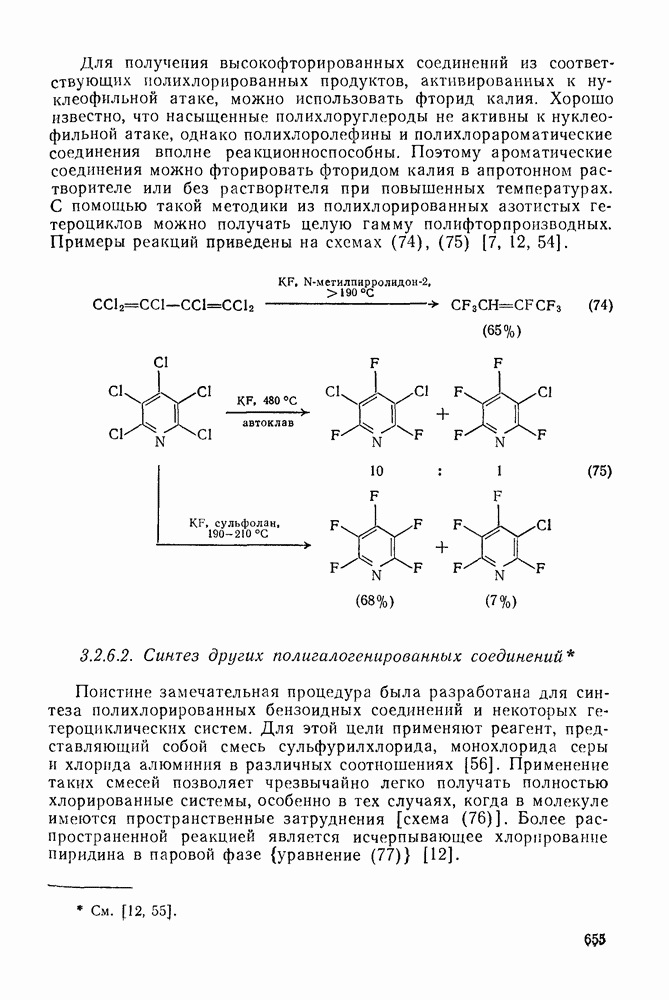
- 3.2.6. Синтез полигалогенированных соединений
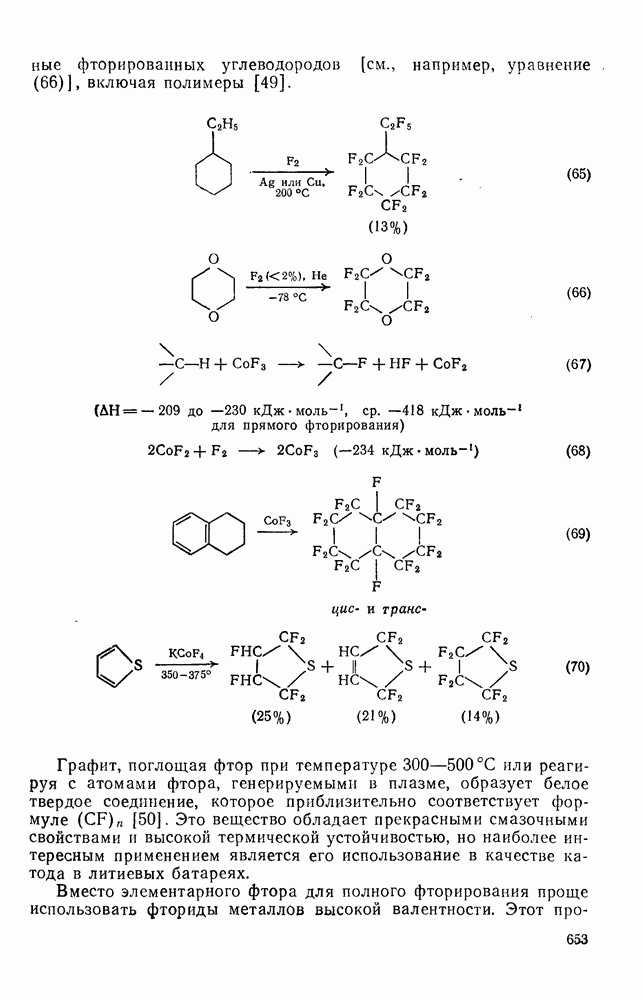
- 3.2.6.1. Синтез полифторированных соединений
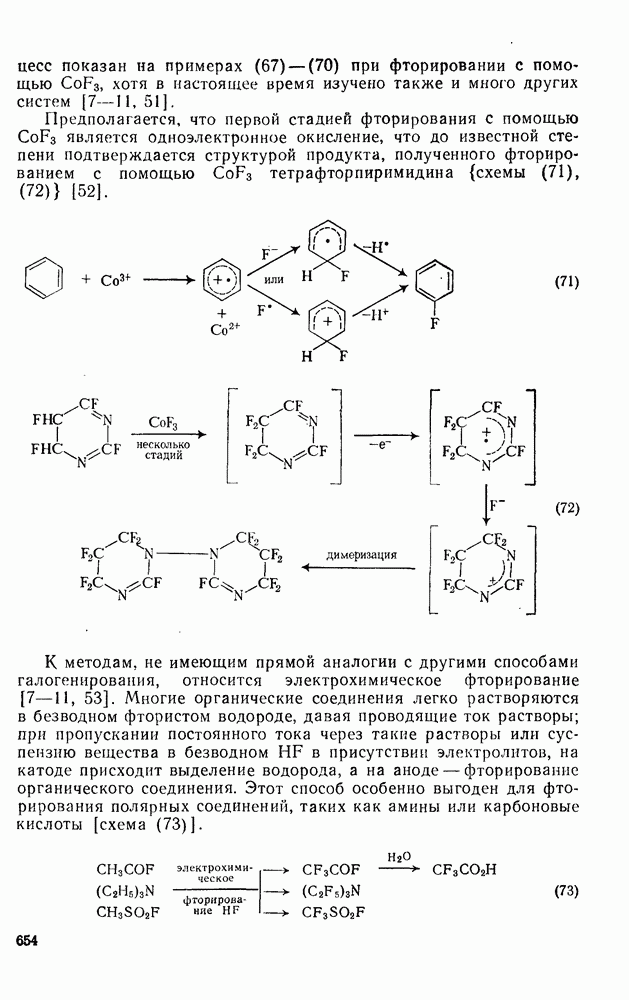
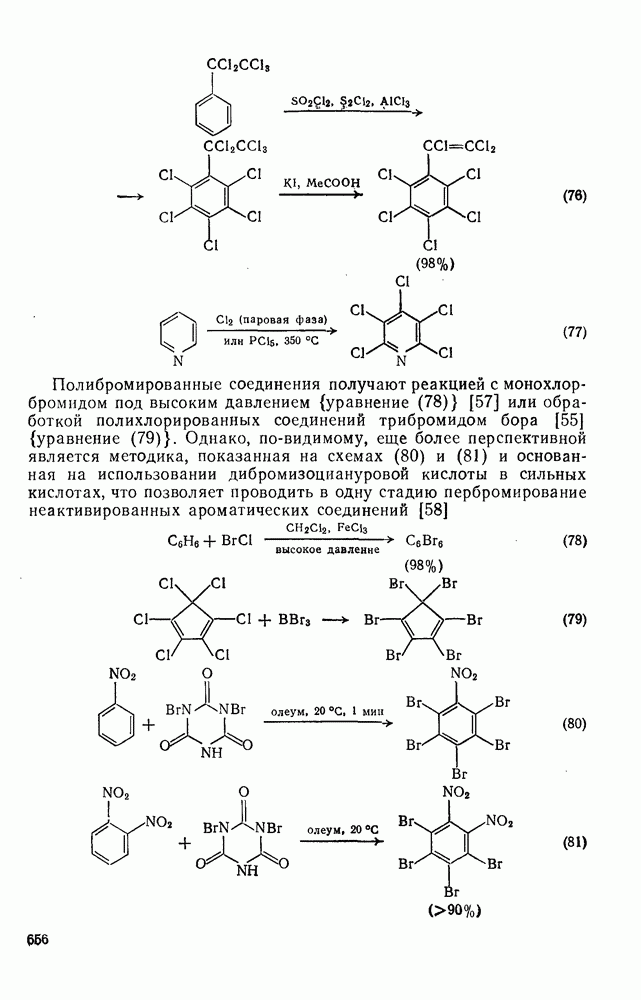
- 3.2.6.2. Синтез других полигалогенированных соединений
- 3.3. ГАЛОГЕНАЛКАНЫ
- 3.3.1. Характеристика связей углерод-галоген
- 3.3.2. Промышленное применение
- 3.3.3. Нуклеофильное замещение галогена
- 3.3.3.1. Реакции SN2 и родственные процессы
- 3.3.3.2. Соучастие соседних групп
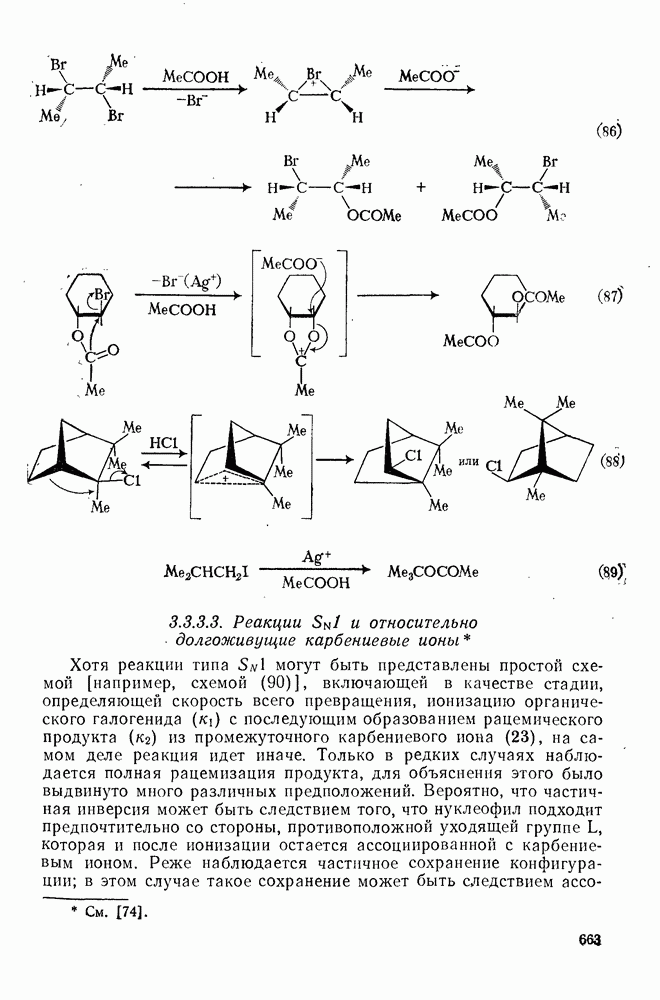
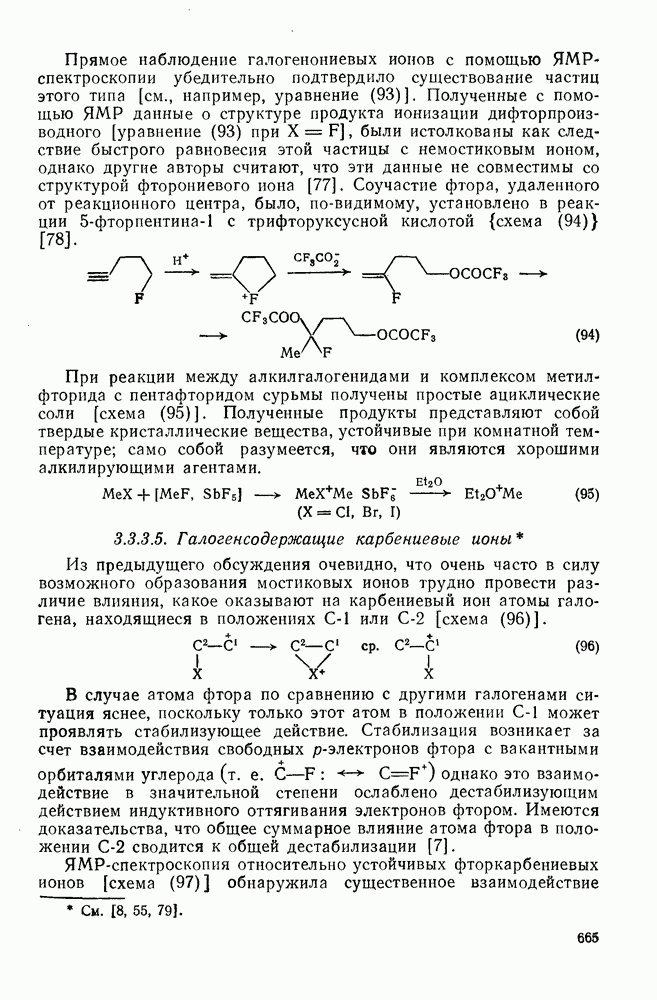
- 3.3.3.3. Реакции SN1 и относительно долгоживущие карбениевые ионы
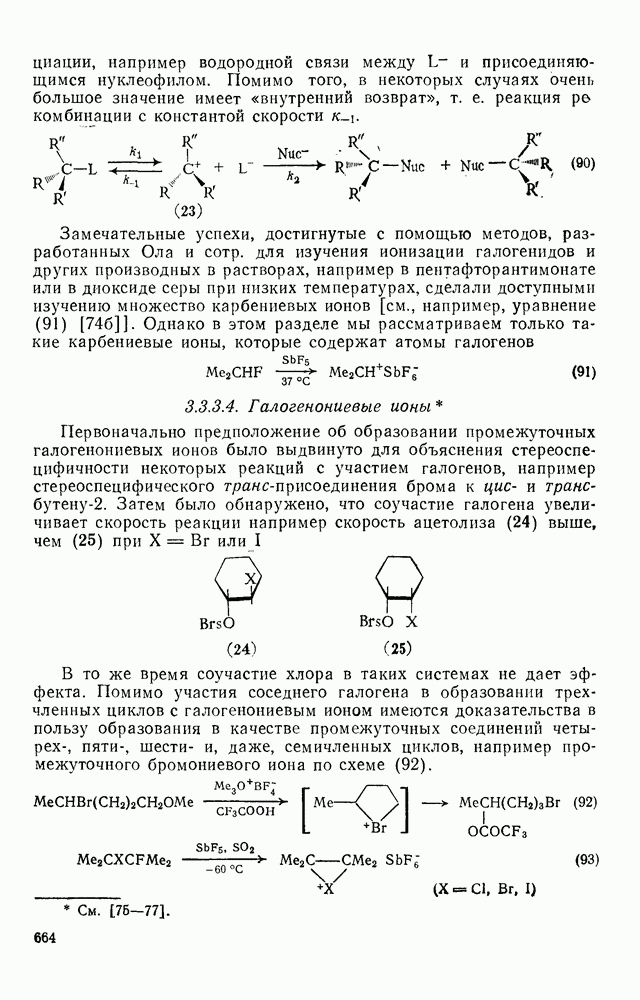
- 3.3.3.4. Галогенониевые ионы
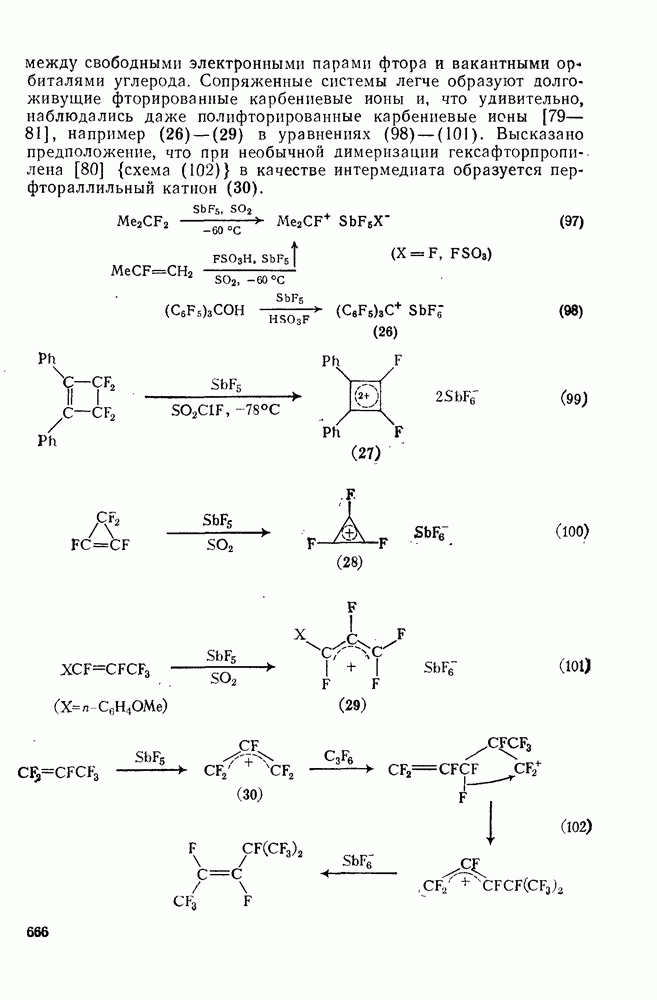
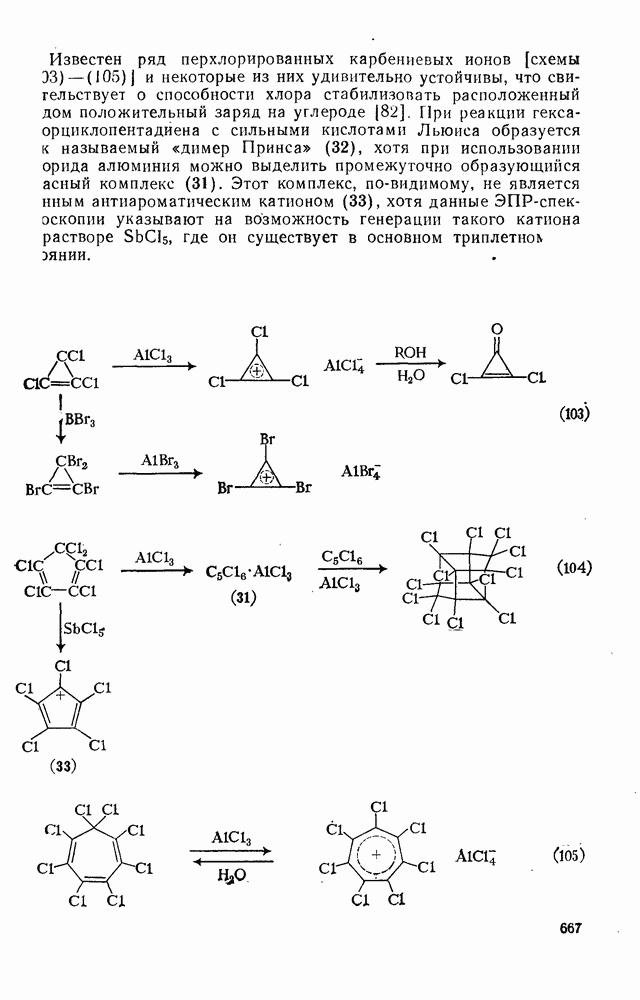
- 3.3.3.5. Галогенсодержащие карбениевые ионы
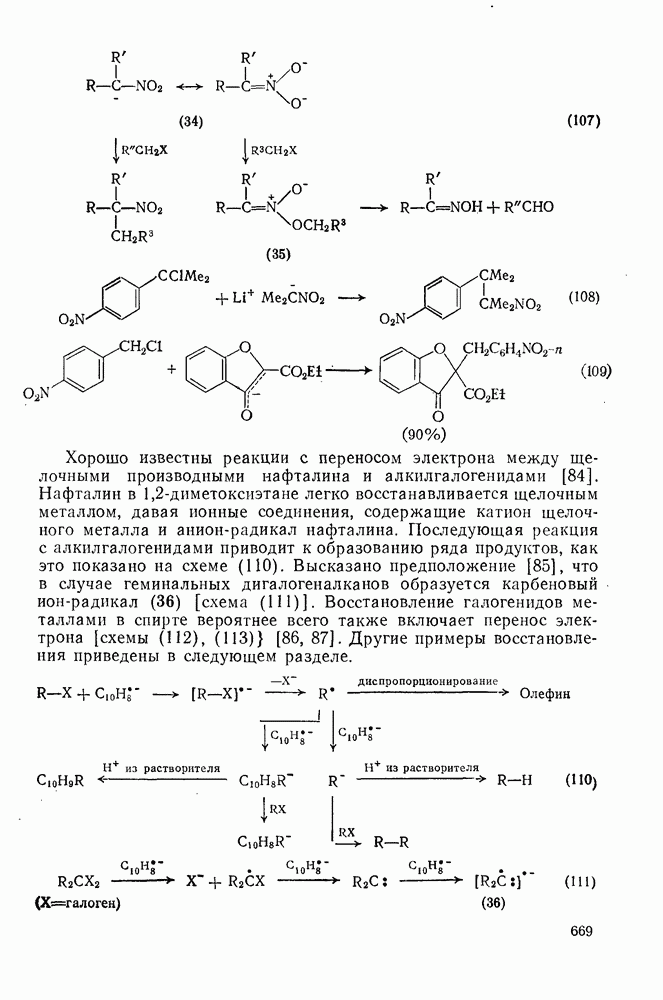
- 3.3.3.6. Механизм замещения с переносом электрона
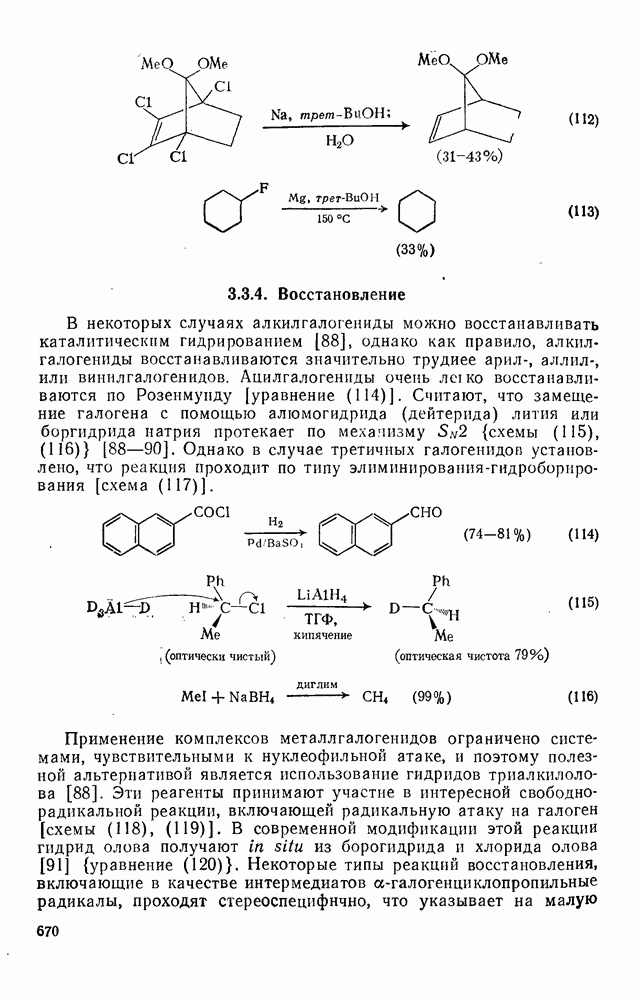
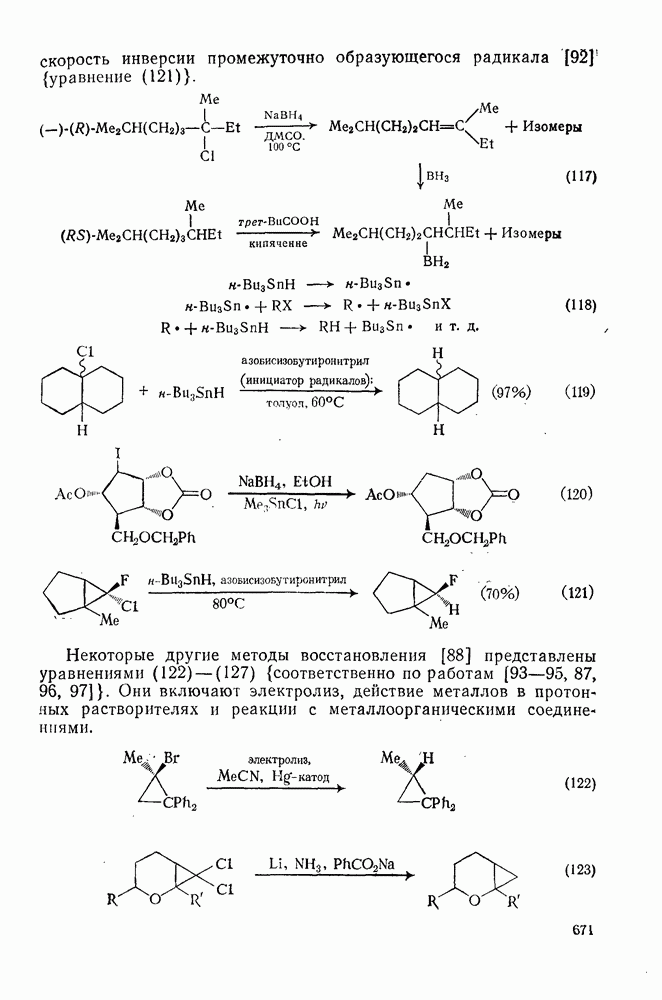
- 3.3.4. Восстановление
- 3.3.5. Замещение на металлы
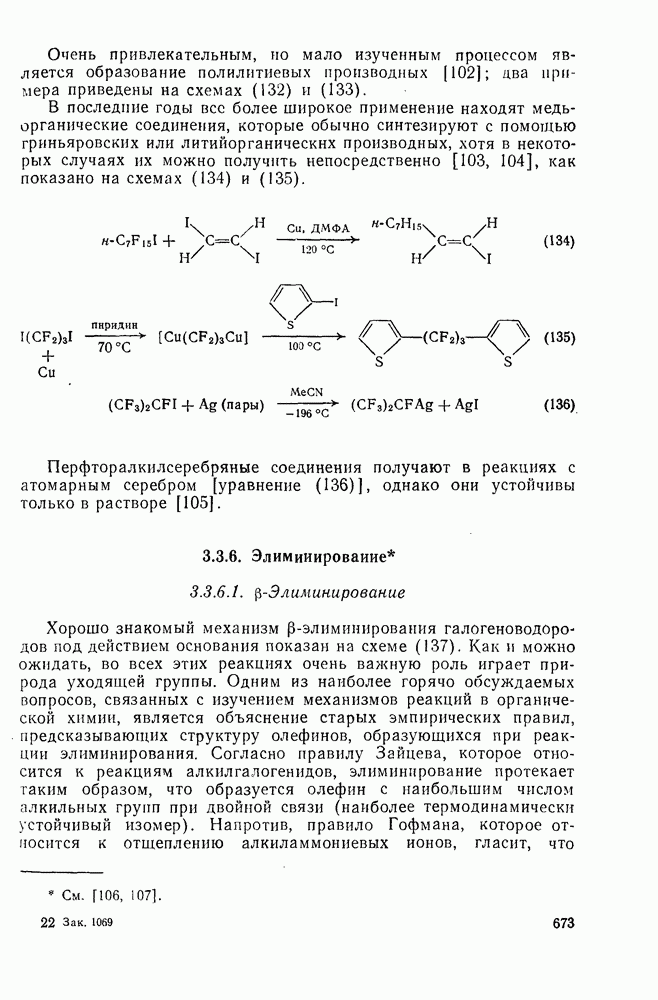
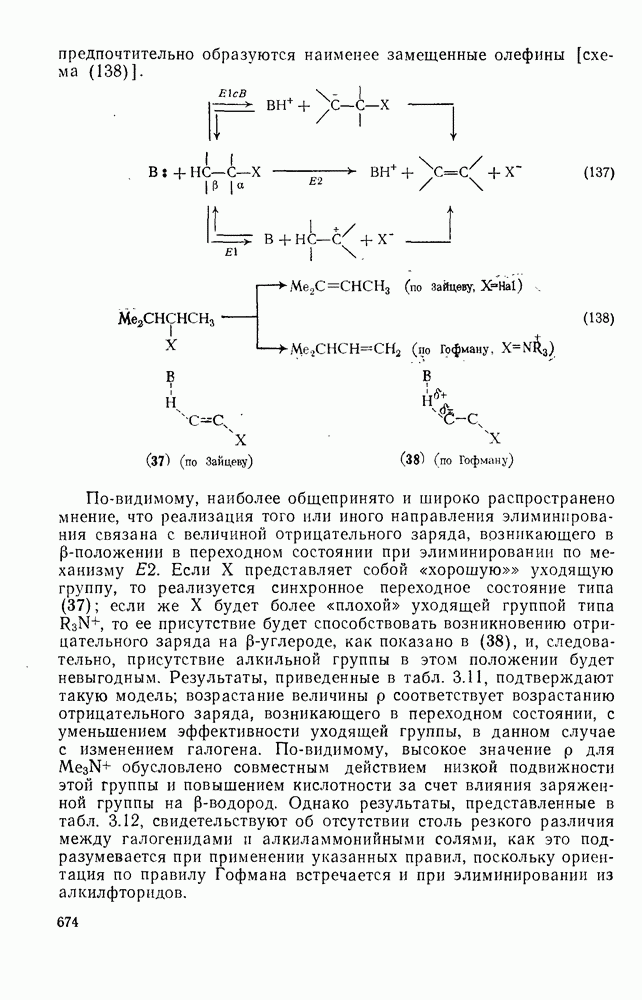
- 3.3.6. Элиминирование
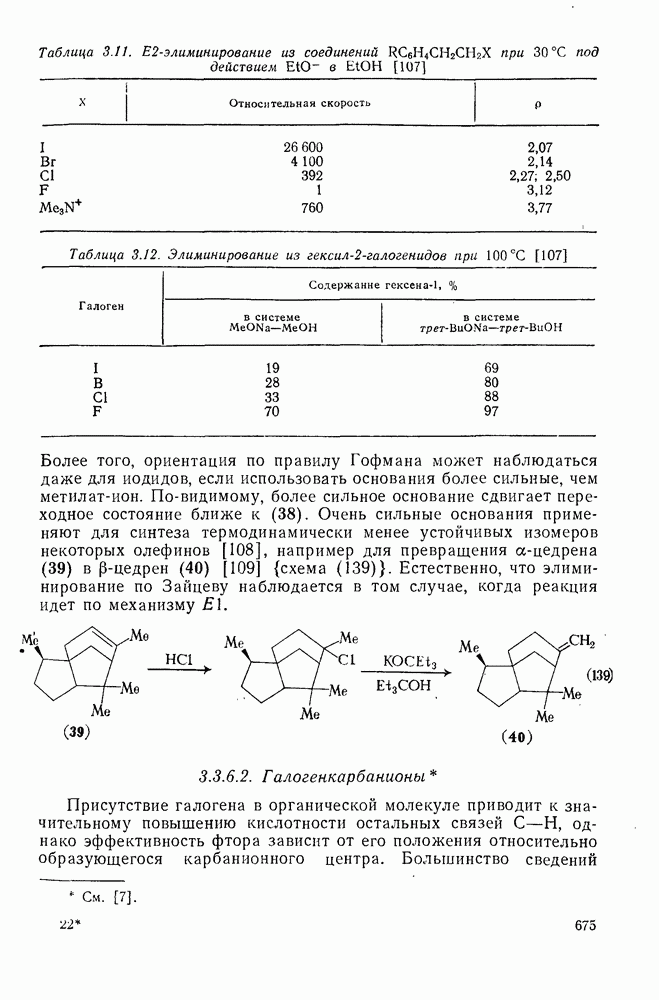
- 3.3.6.1. b-Элиминирование
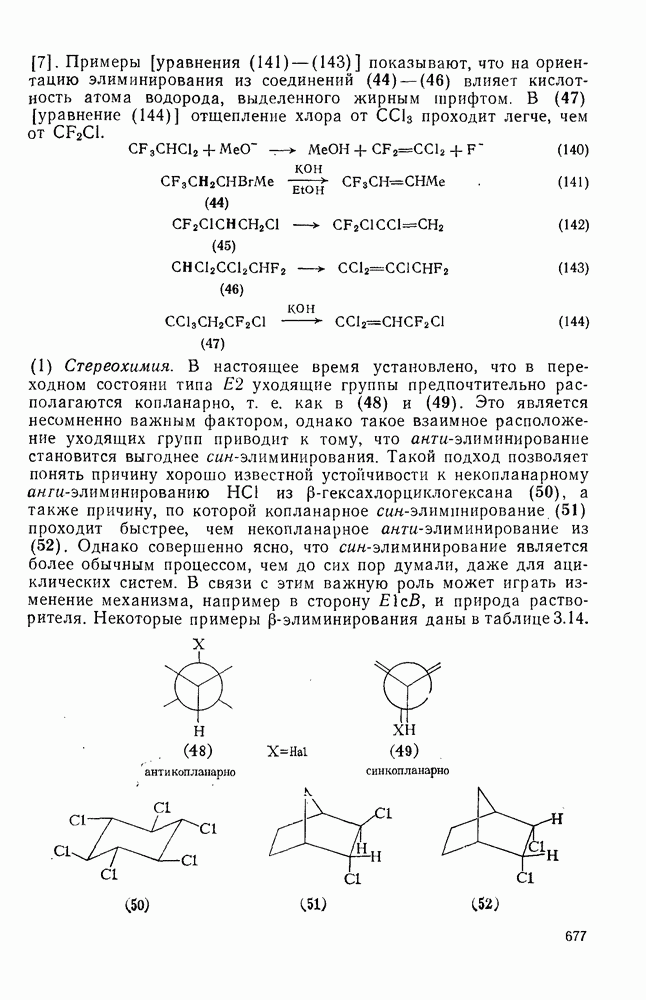
- 3.3.6.2. Галогенкарбанионы
- 3.3.6.3. Элиминирование через карбанионы
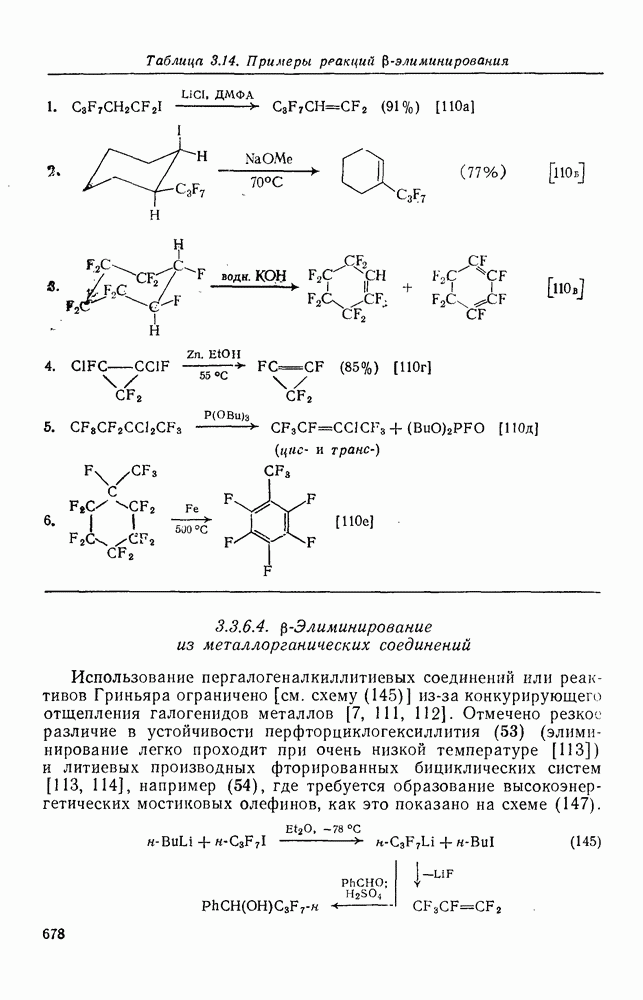
- 3.3.6.4. b-Элиминирование из металлорганических соединений
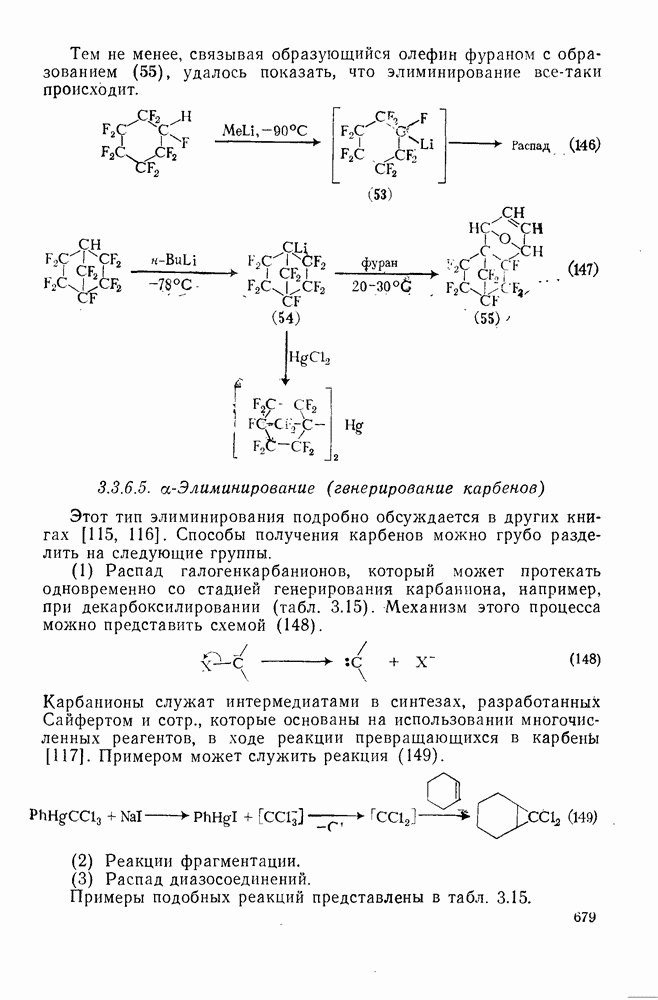
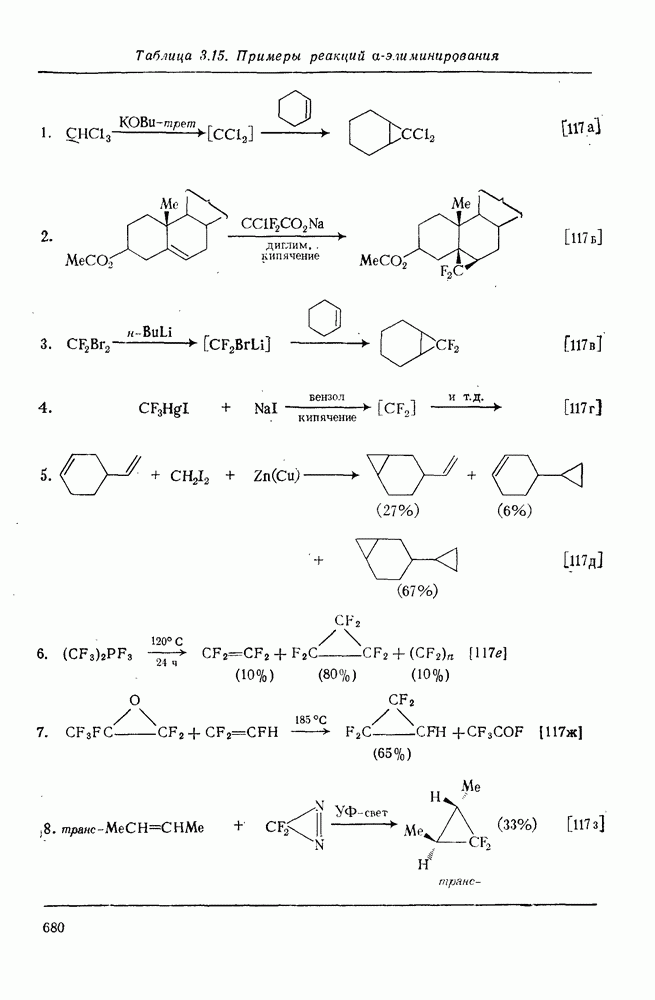
- 3.3.6.5. a-Элиминирование (генерирование карбенов)
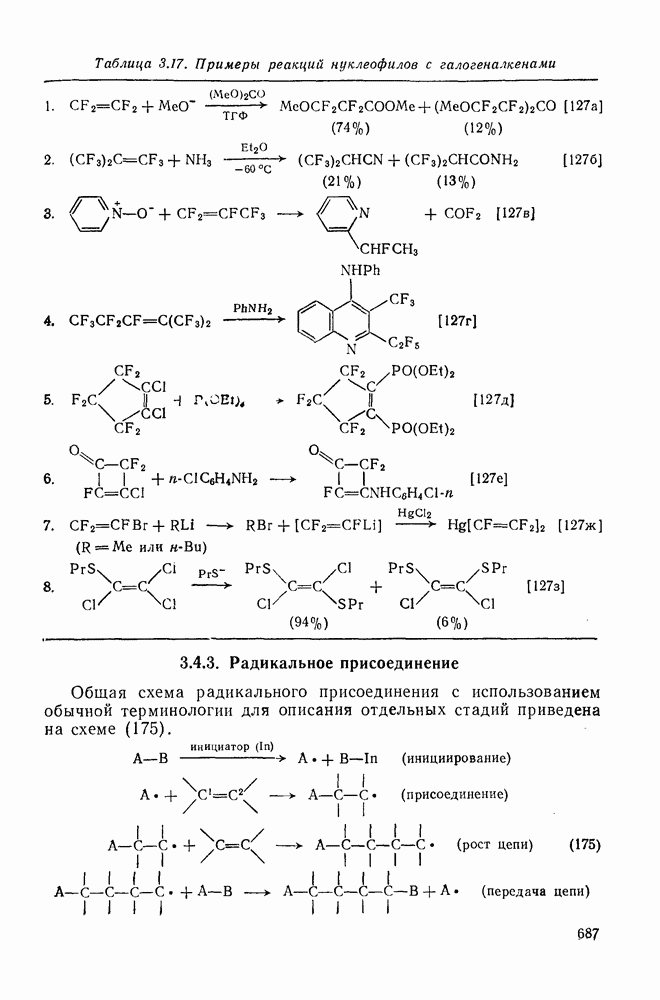
- 3.4. ГАЛОГЕНАЛКЕНЫ
- 3.4.1. Синтез галогеналкенов
- 3.4.2. Нуклеофильная атака
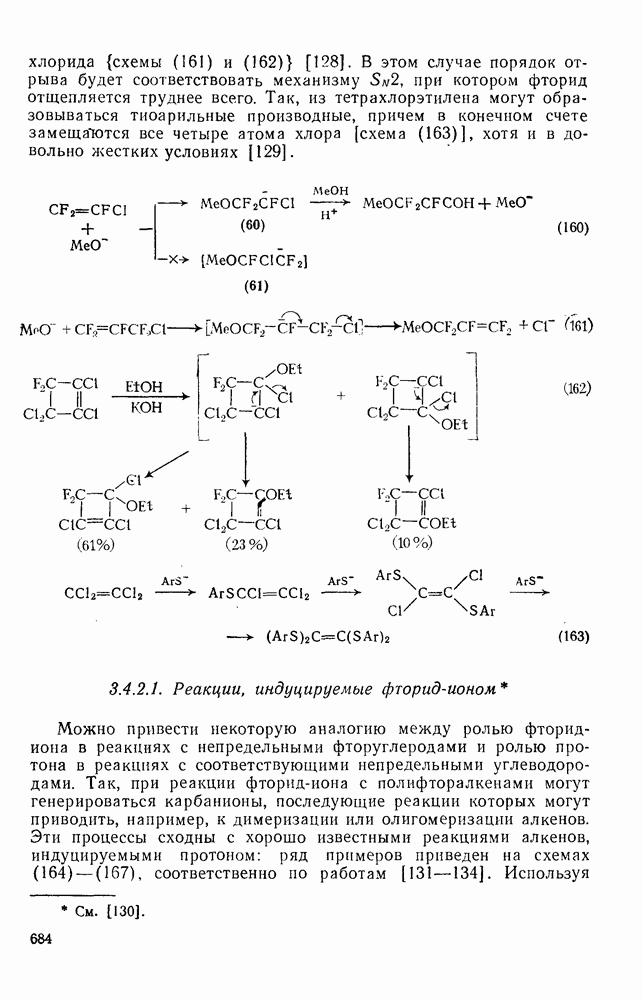
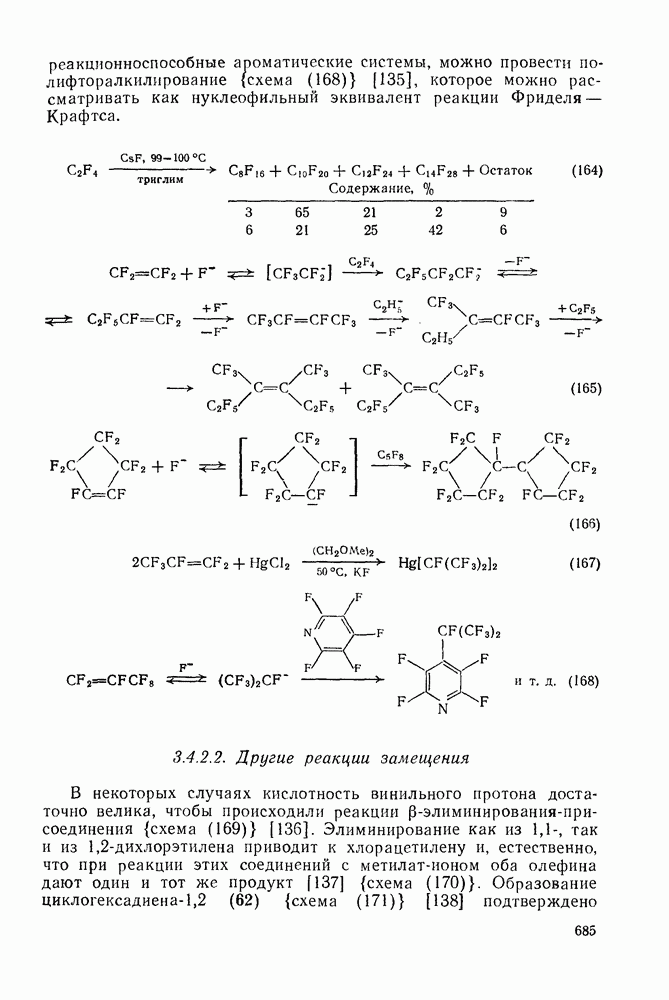
- 3.4.2.1. Реакции, индуцируемые фторид-ионом
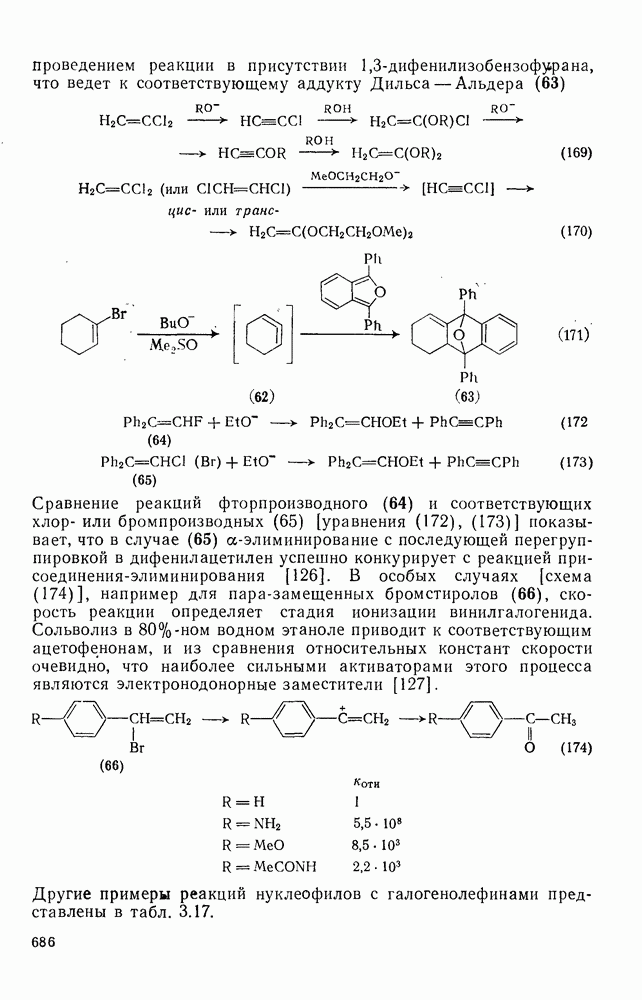
- 3.4.2.2. Другие реакции замещения
- 3.4.3. Радикальное присоединение
- 3.4.4. Электрофильное присоединение
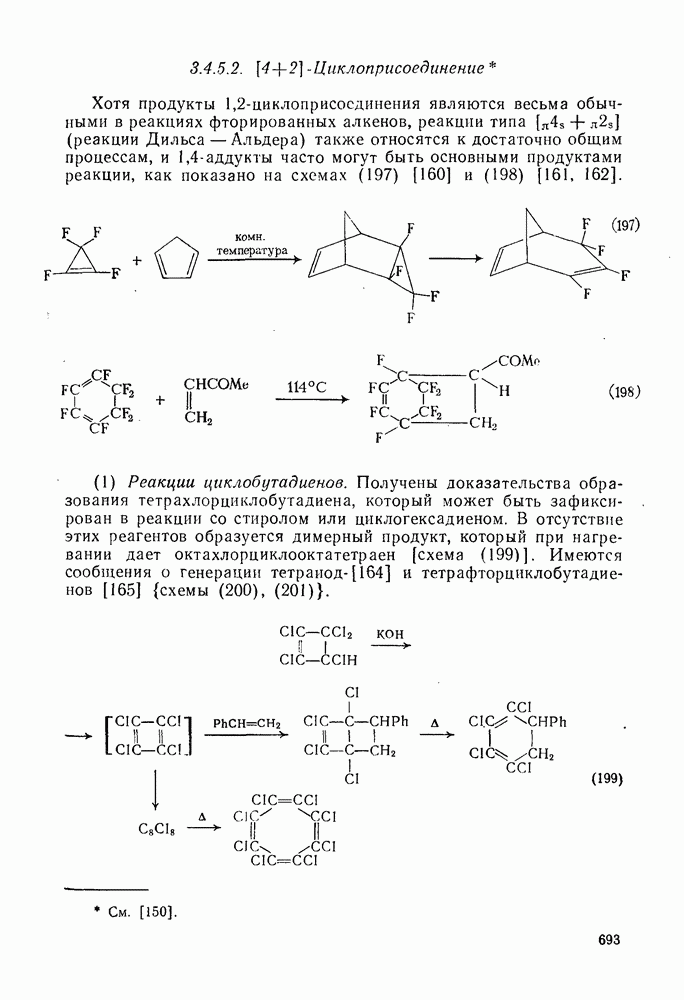
- 3.4.5. Циклоприсоединение
- 3.4.5.1. [2+2]-Циклоприсоединение
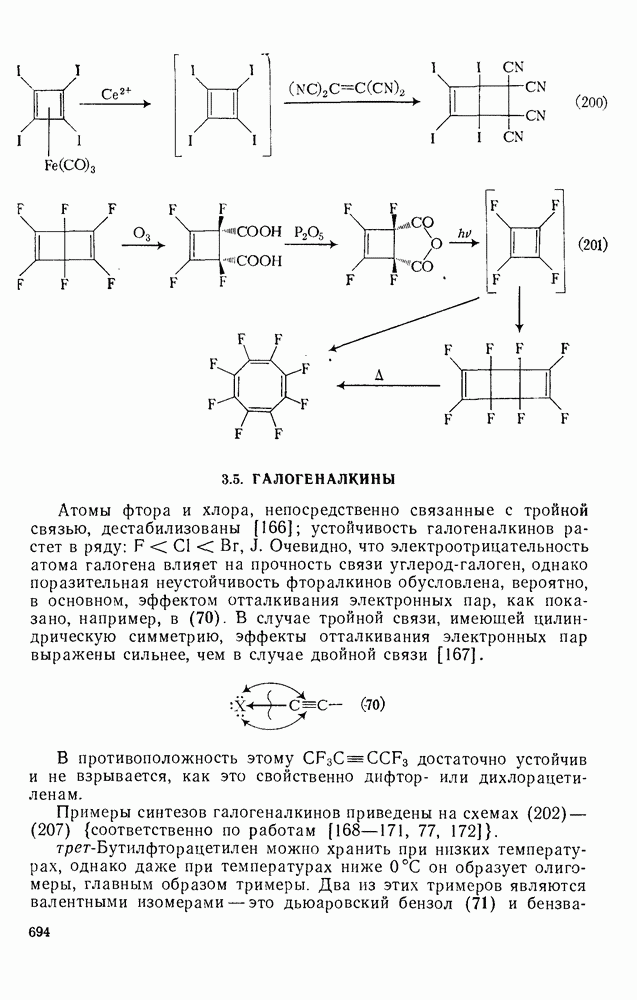
- 3.4.5.2. [4+2]-Циклоприсоединение
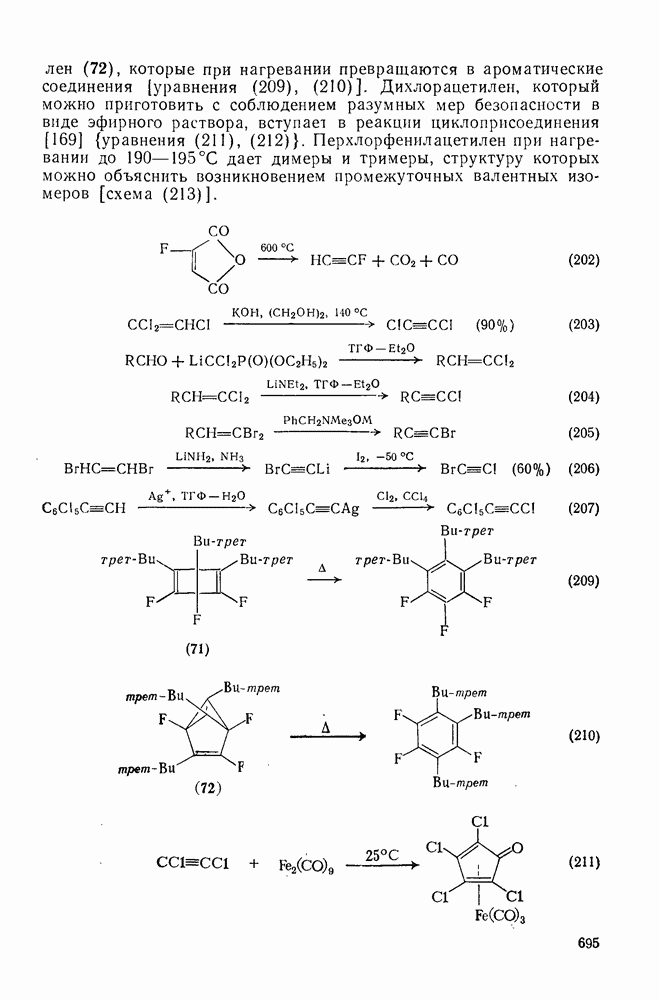
- 3.5. ГАЛОГЕНАЛКИНЫ
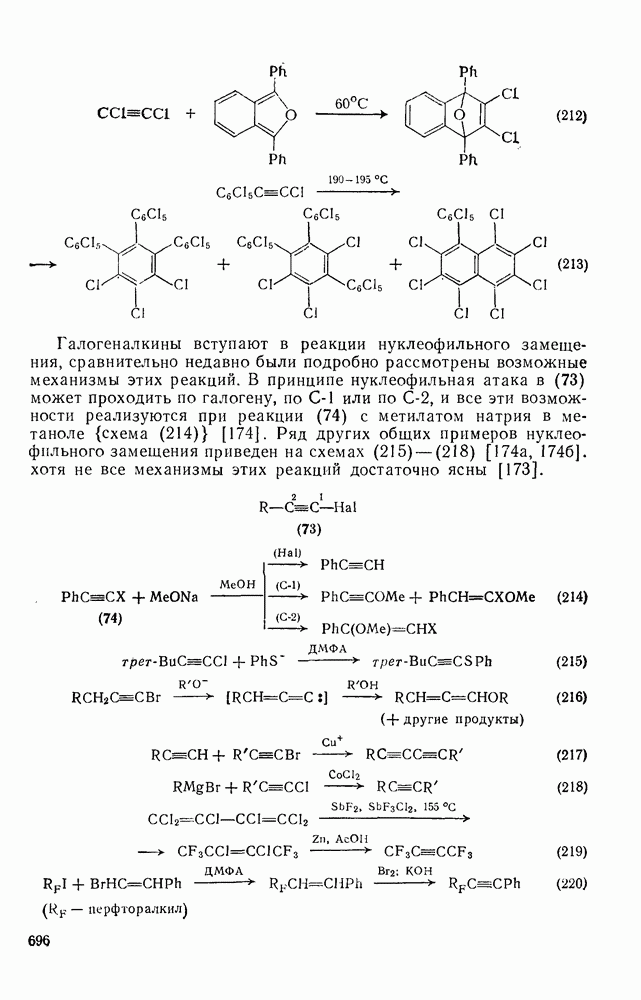
- 3.6. ГАЛОГЕНАРЕНЫ
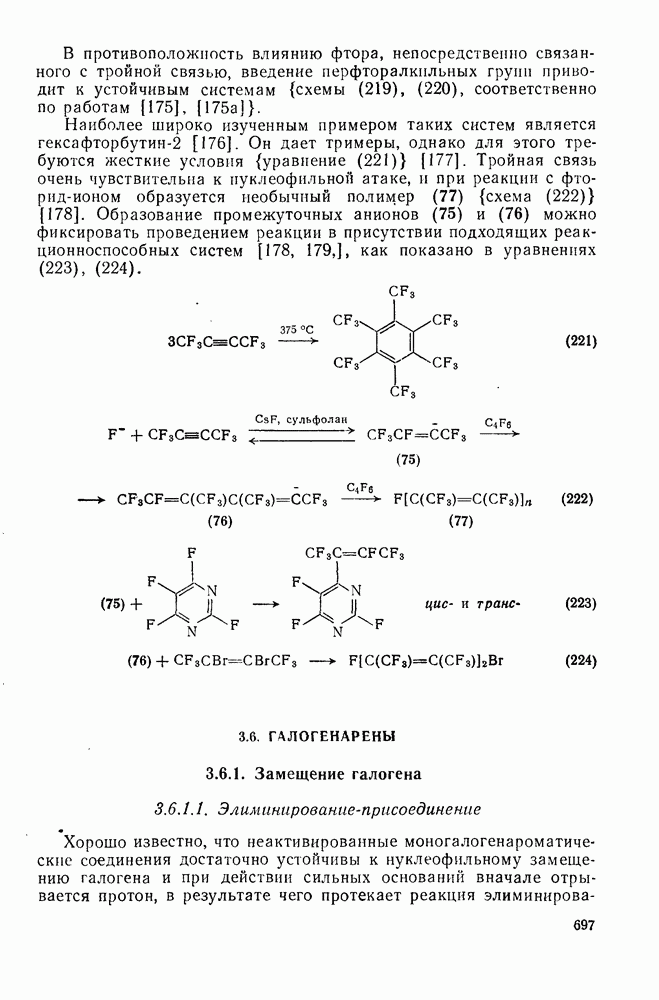
- 3.6.1. Замещение галогена
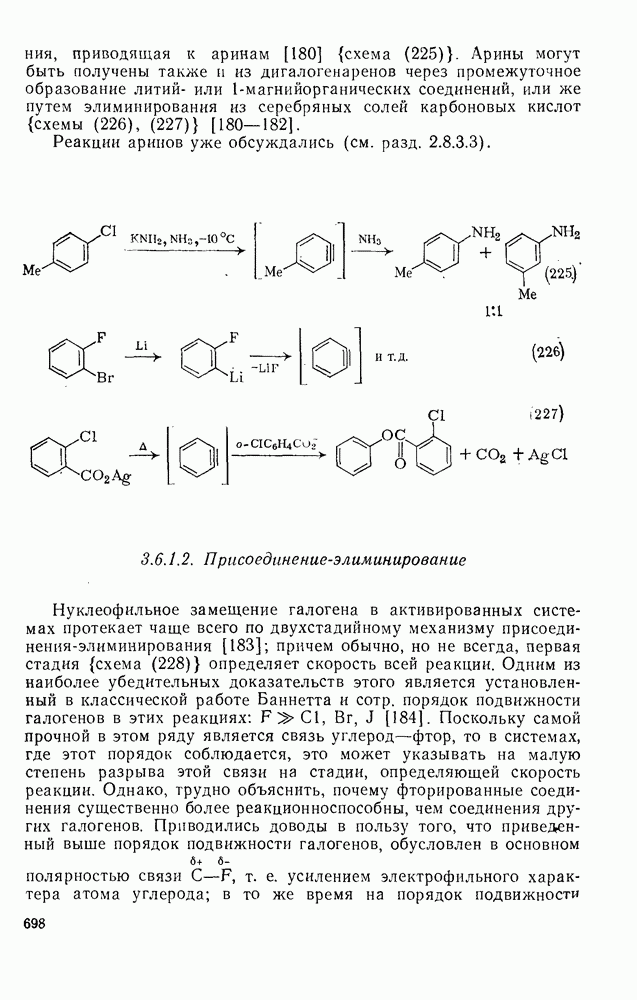
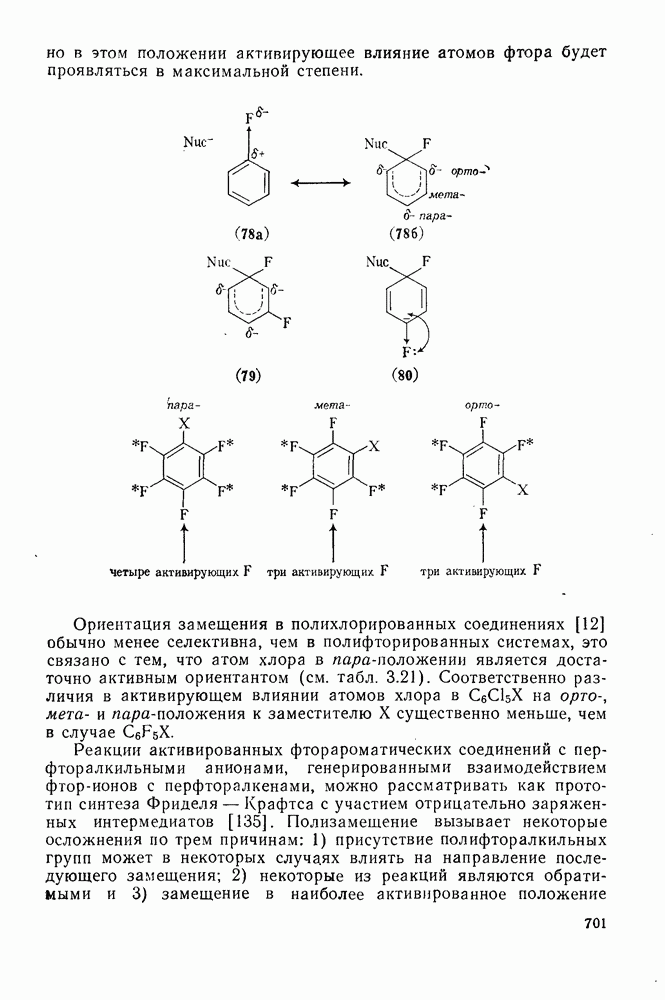
- 3.6.1.2. Присоединение-элиминирование
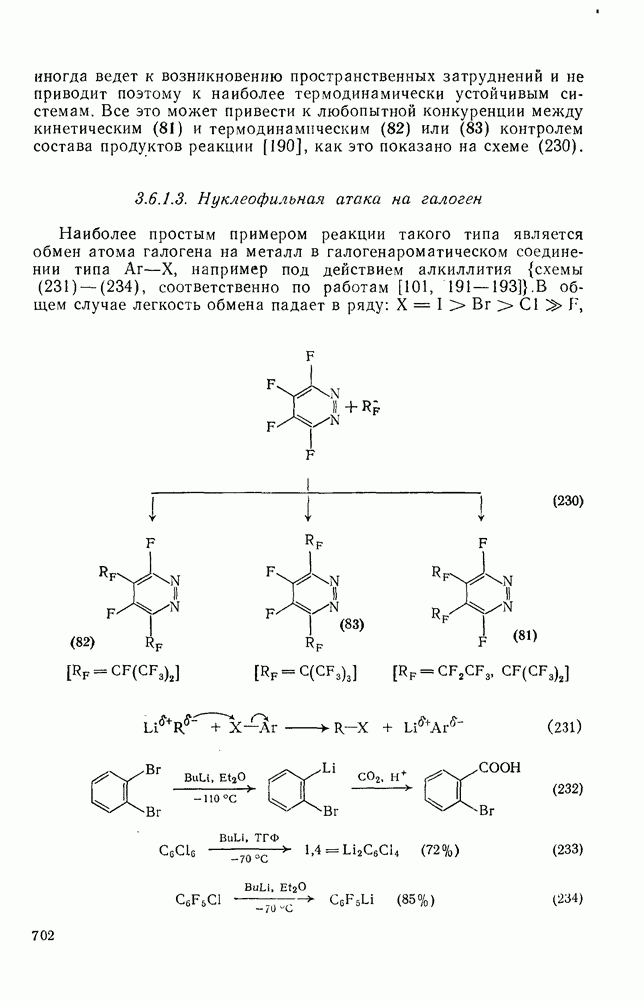
- 3.6.1.3. Нуклеофильная атака на галоген
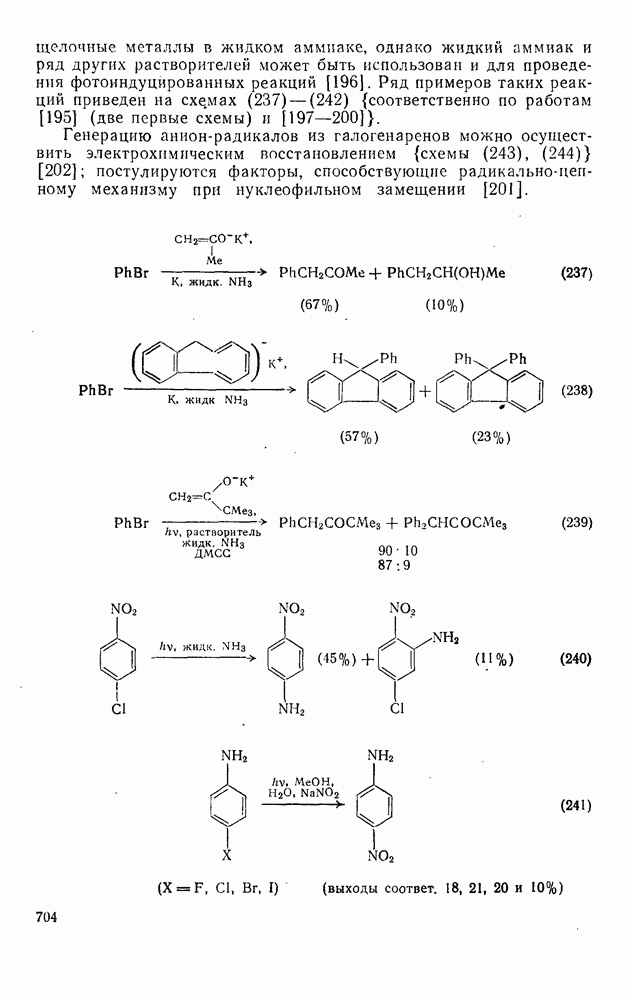
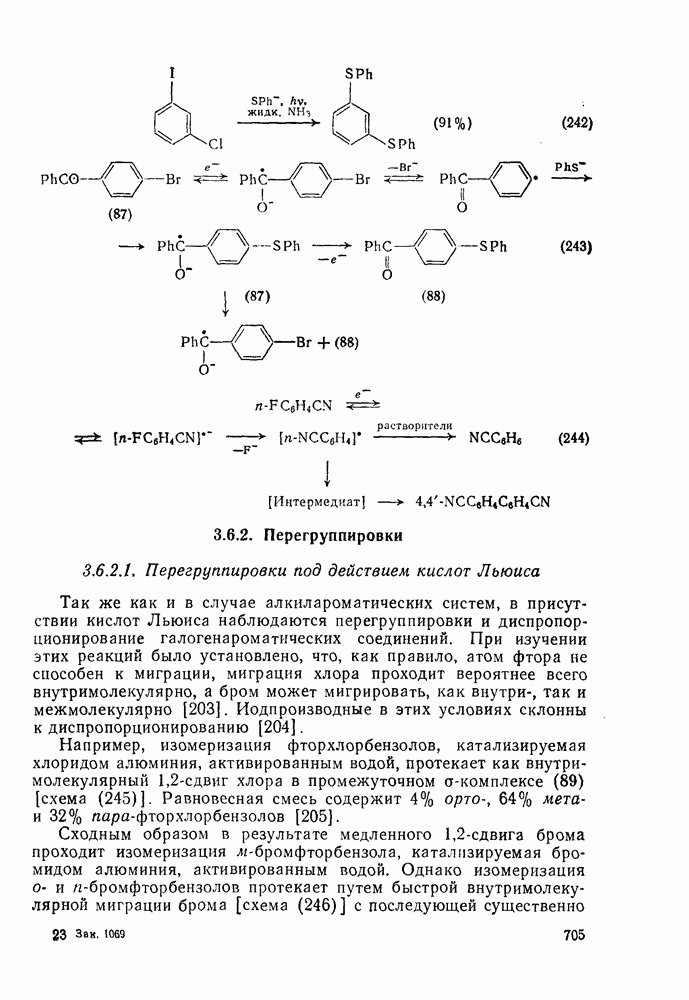
- 3.6.1.4. Перенос электрона
- 3.6.2. Перегруппировки
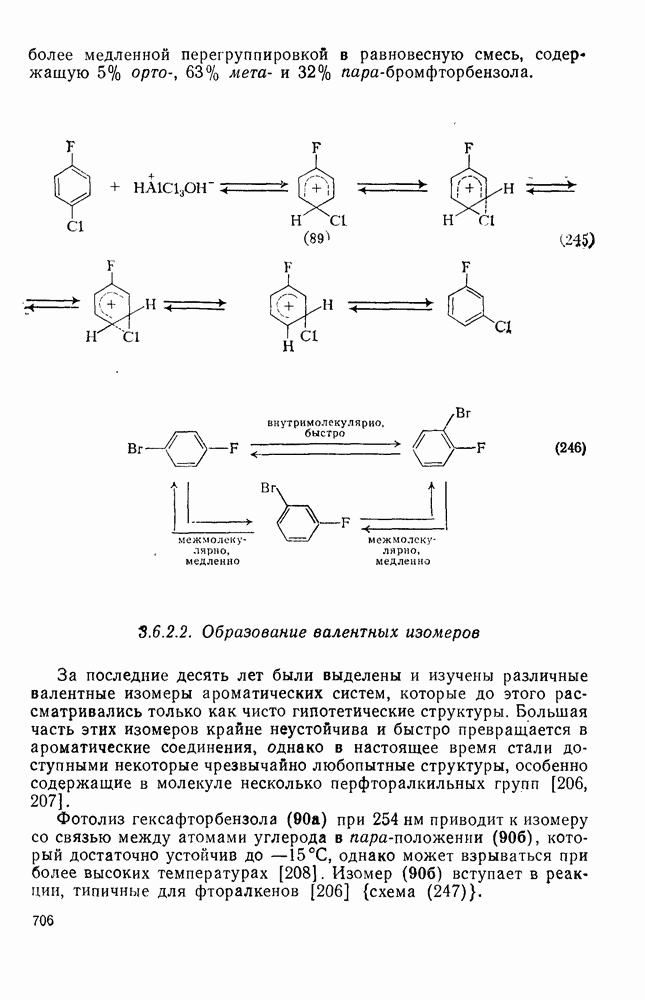
- 3.6.2.1. Перегруппировки под действием кислот Льюиса
- 3.6.2.2. Образование валентных изомеров