| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
2.8.2.2. Реакции карбенов
Наше знание химии карбенов в значительной мере стало возможным благодаря применению физических методов, таких как химически индуцнроваиная динамическая поляризация ядер, электронный парамагнитный резонанс и импульсный фотолиз для изучения реакций карбенов в растворе [66]. Обсуждение этих методов выходит за рамки данного раздела, поэтому мы отсылаем читателей к существующим превосходным обзорам [67, 68].
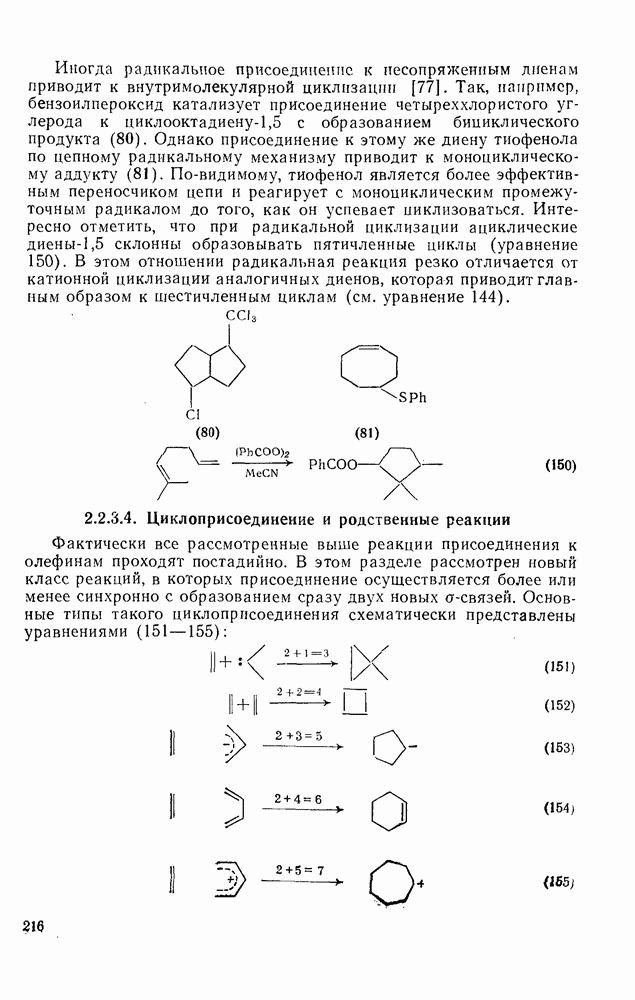
(1) Циклоприсоединение
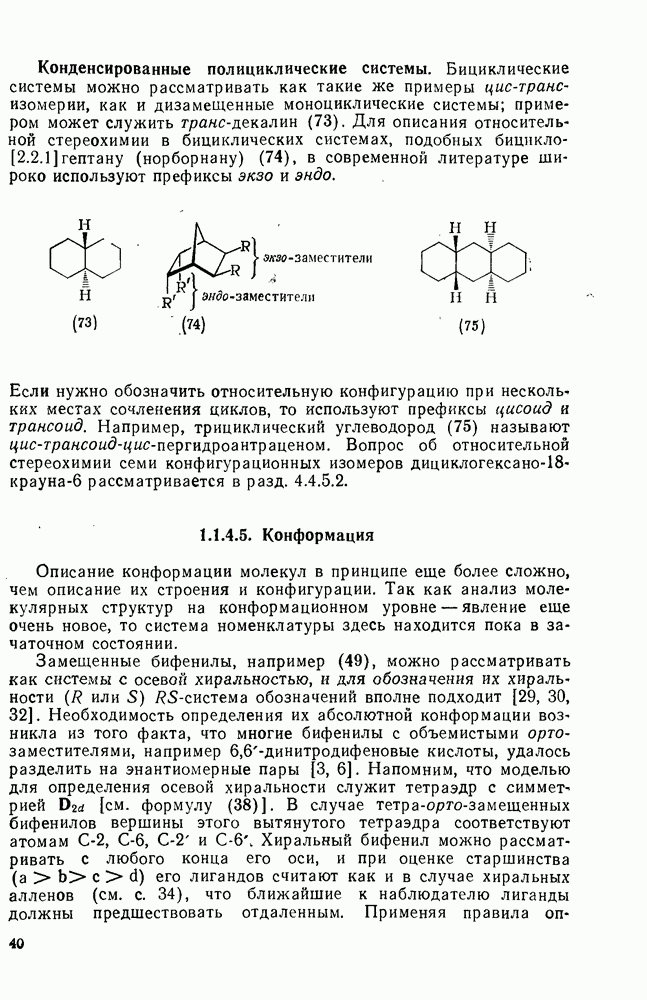
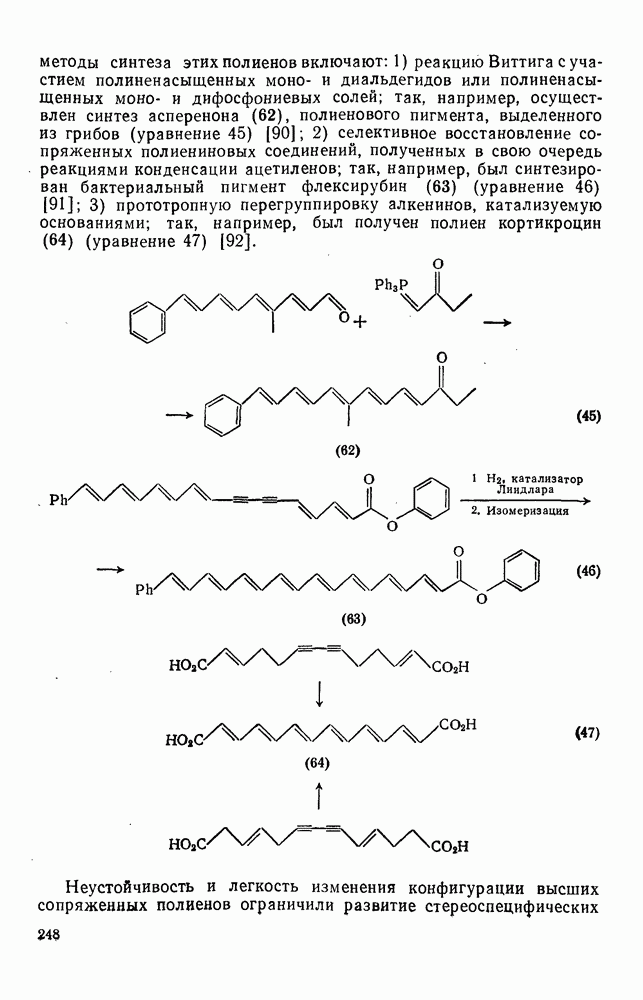
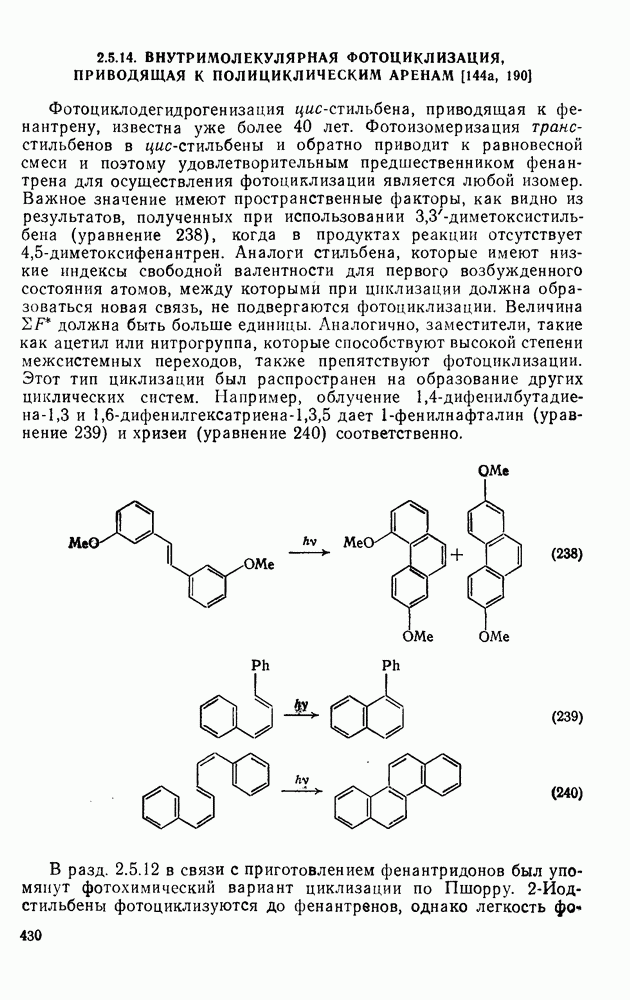
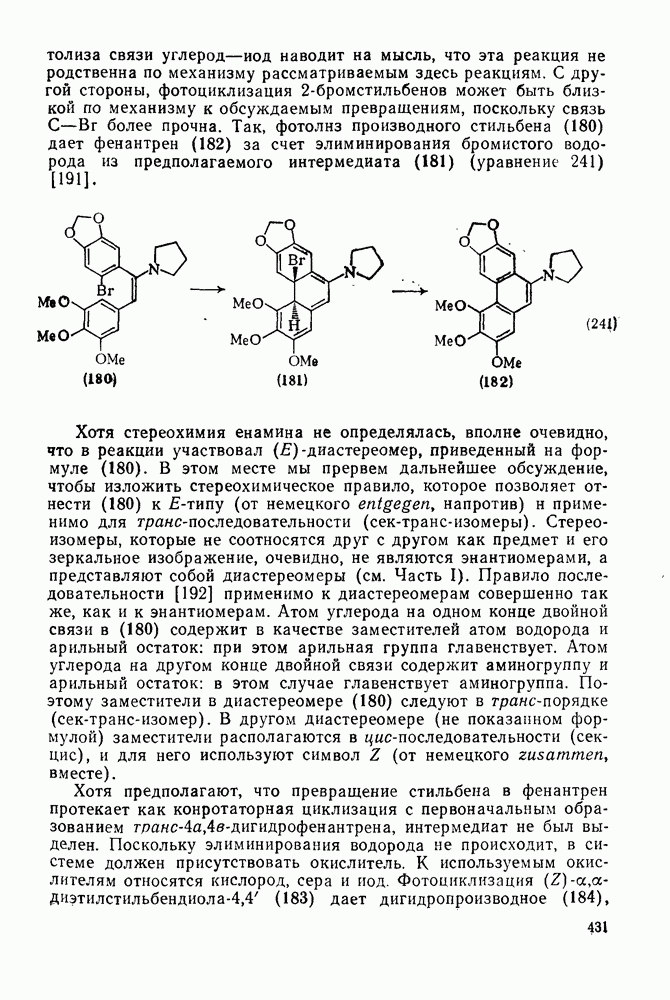
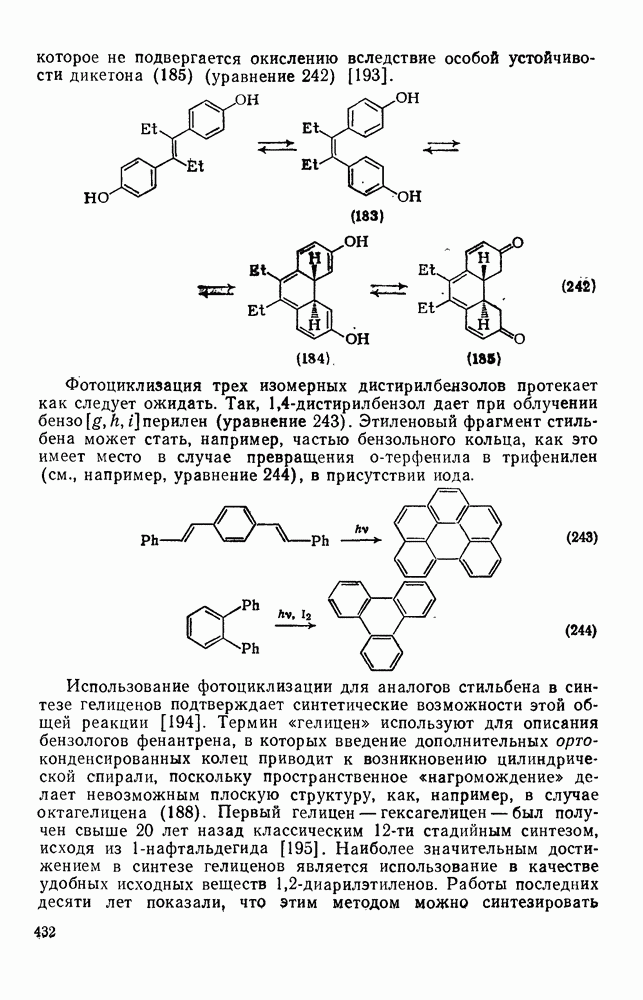
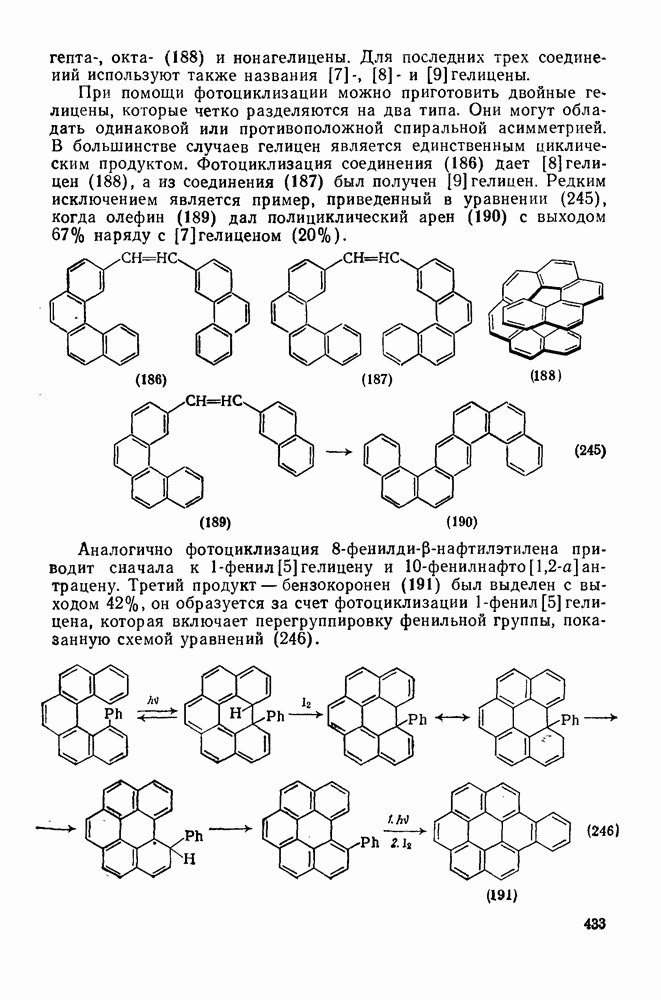
Присоединение карбенов к алкенам с образованием циклопропанов [схемы (35), (42) и (46)] является одной из наиболее характерных и синтетически полезных реакций [69]. Часто возможно успешно осуществить внутримолекулярные варианты этой реакции [см., например, уравнение  ], однако они зачастую проходят с низкими выходами и осложняются водородными сдвигами и другими конкурирующими реакциями. Расчеты молекул, аналогичных (73), в которых внутримолекулярное образование циклопропана стереохимически невозможно, показывают, что в таких соединениях электронное взаимодействие с двойной связью вполне достаточно для стабилизации синглетного основного состояния карбена. Такие карбены называют «листовидными» метиленами, и было затрачено много сил, чтобы обнаружить экспериментально влияние такой неклассической стабилизации на свойства карбена [69].
], однако они зачастую проходят с низкими выходами и осложняются водородными сдвигами и другими конкурирующими реакциями. Расчеты молекул, аналогичных (73), в которых внутримолекулярное образование циклопропана стереохимически невозможно, показывают, что в таких соединениях электронное взаимодействие с двойной связью вполне достаточно для стабилизации синглетного основного состояния карбена. Такие карбены называют «листовидными» метиленами, и было затрачено много сил, чтобы обнаружить экспериментально влияние такой неклассической стабилизации на свойства карбена [69].

Механизм межмолекулярного присоединения карбенов к алкенам широко обсуждался в течение многих лет. С поразительной химической интуицией Скелл в 1956 г. предположил, что механизм и стереохимия реакции зависят от спинового состояния карбена.
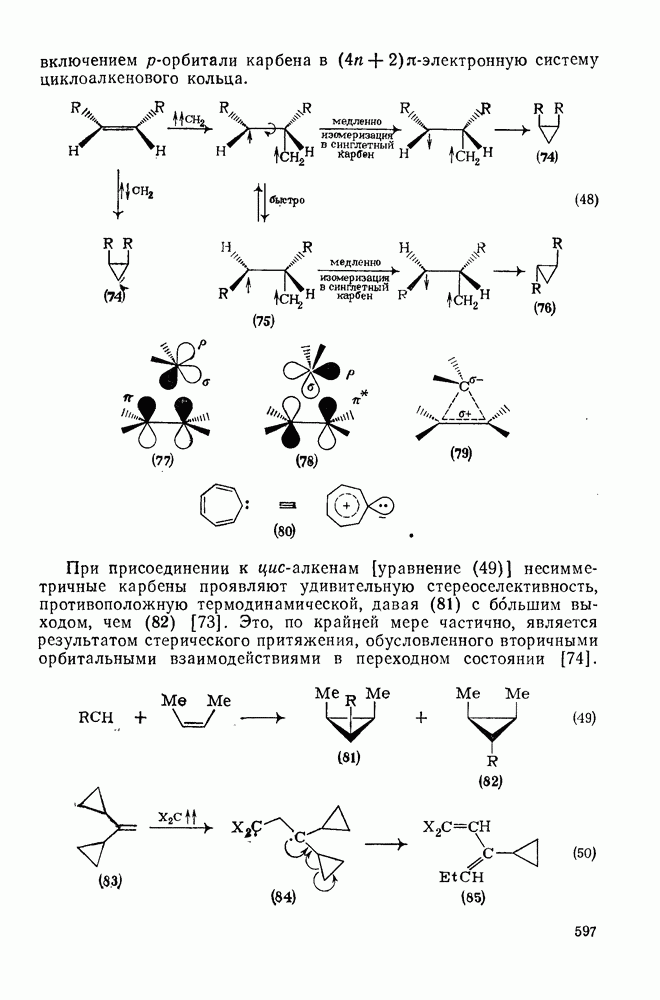
Он привел доводы в пользу того, что синглетные карбены присоединяются путем синхронного образования обоих новых  -связей, давая только (74) и сохраняя таким образом стереохимию исходного алкена, в то время как триплетные карбены присоединяются по радикальному двухстадийному механизму с образованием в первую очередь бирадикала (75), в котором может происходить вращение вокруг связи до инверсии спина и замыкания кольца, что приводит к обоим диастереомерам (74) и (76). Несмотря на широкое обсуждение справедливости теоретических предпосылок, правило Скелла исключительно успешно объясняет многие экспериментальные данные, полученные для этих реакций присоединения. Однако при использовании правила следует соблюдать определенную осторожность, так как в его основе лежат некоторые предположения об относительных скоростях стадий схемы (48), которые могут соблюдаться не во всех случаях [38]. Таким образом, прежде чем однозначно приписать определенную реакционную способность одному из спиновых состояний карбена, следует выяснить свойства обоих состояний. В ряде случаев, когда это требование было точно соблюдено, например в случае метилена, бисметоксикарбонилкарбена, флуоренилидена и др., результаты всегда соответствовали предсказаниям Скелла. Расчет поверхности потенциальной энергии присоединения синглетного метилена к этилену [40, 70] подтверждает синхронность реакции и свидетельствует, что она осуществляется по принципу наименьшего движения через разрешенный орбитальной симметрией подход (77), при котором вакантная р-орбиталь (НСМО) карбена взаимодействует с занятой
-связей, давая только (74) и сохраняя таким образом стереохимию исходного алкена, в то время как триплетные карбены присоединяются по радикальному двухстадийному механизму с образованием в первую очередь бирадикала (75), в котором может происходить вращение вокруг связи до инверсии спина и замыкания кольца, что приводит к обоим диастереомерам (74) и (76). Несмотря на широкое обсуждение справедливости теоретических предпосылок, правило Скелла исключительно успешно объясняет многие экспериментальные данные, полученные для этих реакций присоединения. Однако при использовании правила следует соблюдать определенную осторожность, так как в его основе лежат некоторые предположения об относительных скоростях стадий схемы (48), которые могут соблюдаться не во всех случаях [38]. Таким образом, прежде чем однозначно приписать определенную реакционную способность одному из спиновых состояний карбена, следует выяснить свойства обоих состояний. В ряде случаев, когда это требование было точно соблюдено, например в случае метилена, бисметоксикарбонилкарбена, флуоренилидена и др., результаты всегда соответствовали предсказаниям Скелла. Расчет поверхности потенциальной энергии присоединения синглетного метилена к этилену [40, 70] подтверждает синхронность реакции и свидетельствует, что она осуществляется по принципу наименьшего движения через разрешенный орбитальной симметрией подход (77), при котором вакантная р-орбиталь (НСМО) карбена взаимодействует с занятой  -молекулярной орбиталью алкена, причем карбен расположен так, чтобы перекрывание было максимальным, а пространственные взаимодействия минимальны. Более симметричный подход (78), когда занятая
-молекулярной орбиталью алкена, причем карбен расположен так, чтобы перекрывание было максимальным, а пространственные взаимодействия минимальны. Более симметричный подход (78), когда занятая  -орбиталь карбена взаимодействует с
-орбиталь карбена взаимодействует с  -системой, запрещен орбитальной симметрией и по расчету обладает более высокой энергией, чем (77). Расчеты (77) указывают на наличие
-системой, запрещен орбитальной симметрией и по расчету обладает более высокой энергией, чем (77). Расчеты (77) указывают на наличие  -переноса заряда в переходном состоянии (79), что согласуется с экспериментально наблюдаемым ускорением присоединения большинства карбенов к алкенам, содержащим электронодонорные заместители, и свидетельствует об электрофильной атаке карбена. Многочисленные исследования относительной реакционной способности карбенов с целью выяснения влияния пространственных и электронных эффектов различных заместителей в алкенах и карбенах критически оценены Моссом [48], который показал недавно, что селективность многих карбенов типа
-переноса заряда в переходном состоянии (79), что согласуется с экспериментально наблюдаемым ускорением присоединения большинства карбенов к алкенам, содержащим электронодонорные заместители, и свидетельствует об электрофильной атаке карбена. Многочисленные исследования относительной реакционной способности карбенов с целью выяснения влияния пространственных и электронных эффектов различных заместителей в алкенах и карбенах критически оценены Моссом [48], который показал недавно, что селективность многих карбенов типа  при реакции с олефинами коррелирует как с резонансными, так и с индуктивными параметрами X и Y [71]. Большинство карбенов, в том числе сильно
при реакции с олефинами коррелирует как с резонансными, так и с индуктивными параметрами X и Y [71]. Большинство карбенов, в том числе сильно  -стабилизованный
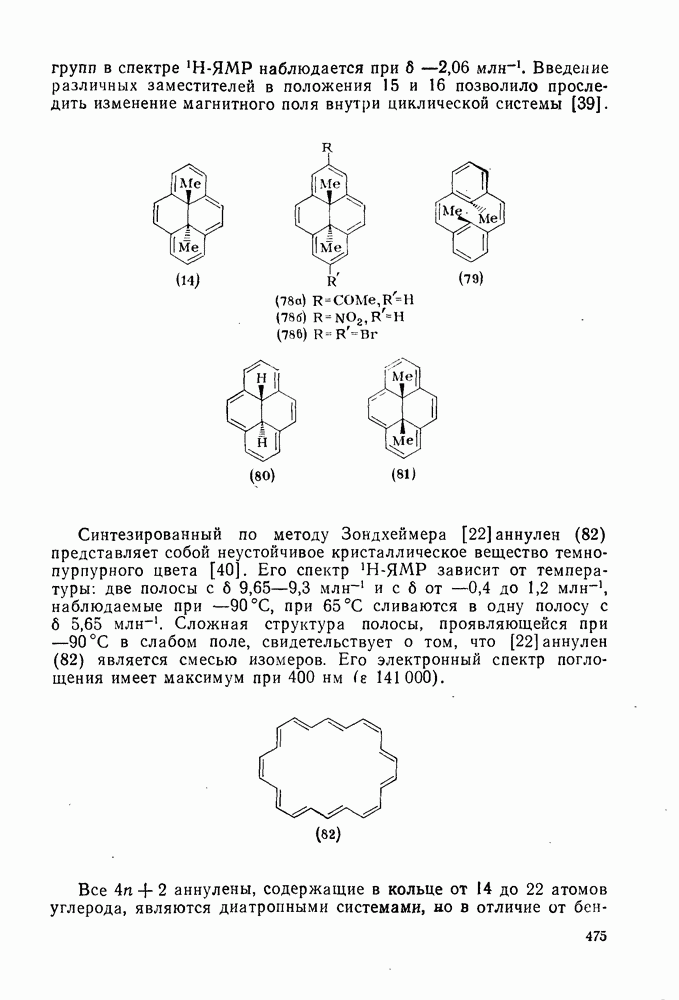
-стабилизованный  (49), ведут себя как типичные электрофилы, однако «ароматические» карбены, такие как (80) и (47), проявляют нуклеофильные свойства, например (80) присоединяется через переходное состояние, поляризованное противоположно (79) [72].
(49), ведут себя как типичные электрофилы, однако «ароматические» карбены, такие как (80) и (47), проявляют нуклеофильные свойства, например (80) присоединяется через переходное состояние, поляризованное противоположно (79) [72].
Полагают, что это обусловлено включением р-орбитали карбена в  -электронную систему циклоалкенового кольца.
-электронную систему циклоалкенового кольца.

При присоединении к цис-алкенам [уравнение (49)] несимметричные карбены проявляют удивительную стереоселективность, противоположную термодинамической, давая (81) с большим выходом, чем (82) [73]. Это, по крайней мере частично, является результатом стерического притяжения, обусловленного вторичными орбитальными взаимодействиями в переходном состоянии [74].

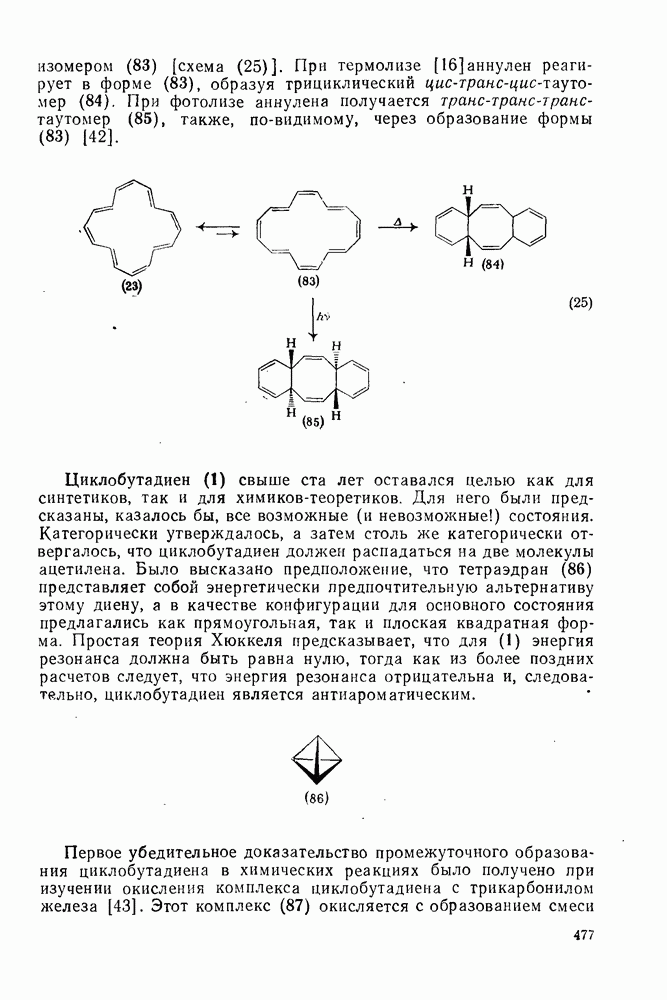
Расчеты присоединения триплетного метилена к этилену указывают на первоначально  -подобный подход с последующим связыванием карбена с одной стороны с образованием триплетного триметиленового бирадикала [50]. Триплетные карбены обычно реагируют с алкенами медленнее синглетных, для диенов справедливо обратное соотношение. Алкен (83) служит полезным индикатором мультиплетности карбена, поскольку синглетные карбены присоединяются к нему без перегруппировки, в то время как присоединение триплета приводит к (84), который быстро перегруппировывается с образованием (85) [50], как показано на схеме (50). Правила орбитальной симметрии разрешают как
-подобный подход с последующим связыванием карбена с одной стороны с образованием триплетного триметиленового бирадикала [50]. Триплетные карбены обычно реагируют с алкенами медленнее синглетных, для диенов справедливо обратное соотношение. Алкен (83) служит полезным индикатором мультиплетности карбена, поскольку синглетные карбены присоединяются к нему без перегруппировки, в то время как присоединение триплета приводит к (84), который быстро перегруппировывается с образованием (85) [50], как показано на схеме (50). Правила орбитальной симметрии разрешают как  , так и
, так и  -присоединение к сопряженным диенам, однако отталкивание за счет замкнутой оболочки делает невыгодным
-присоединение к сопряженным диенам, однако отталкивание за счет замкнутой оболочки делает невыгодным  -присоединение, и оно наблюдается очень редко [75]. Однако цикло-пропенилиден присоединяется в положение 1,4 к тетрациклонам, а дифторкарбен присоединяется к норборнадиену в
-присоединение, и оно наблюдается очень редко [75]. Однако цикло-пропенилиден присоединяется в положение 1,4 к тетрациклонам, а дифторкарбен присоединяется к норборнадиену в  [76].
[76].
Карбены присоединяются также к алкинам, аренам, гетероаренам и различным другим ненасыщенным группам, таким как  и
и  [69].
[69].
(2) Реакции внедрения и отщепления
Характерные межмолекулярные и внутримолекулярные реакции внедрения по связи [см., например, уравнения (51) и (52)], присущи большинству карбенов и многим типам связей, например  [47]. При внедрении самого метилена по связи
[47]. При внедрении самого метилена по связи  в растворе фактически не обнаруживается различий между первичными, вторичными и третичными связями; в газофазных реакциях такие различия не слишком велики, например в случае изопентана относительная скорость внедрения следующая: первичная связь 1,0; вторичная связь 1,2; третичная связь 1,4. При наличии в карбене арильных групп, галогенов или электроноакцепторных заместителей селективность возрастает. Пр и взаимодействии с алкенами основной реакцией является присоединение по двойной связи; внедрение по связи
в растворе фактически не обнаруживается различий между первичными, вторичными и третичными связями; в газофазных реакциях такие различия не слишком велики, например в случае изопентана относительная скорость внедрения следующая: первичная связь 1,0; вторичная связь 1,2; третичная связь 1,4. При наличии в карбене арильных групп, галогенов или электроноакцепторных заместителей селективность возрастает. Пр и взаимодействии с алкенами основной реакцией является присоединение по двойной связи; внедрение по связи  лишь слабо конкурирует с ним и только в случае более реакционноспособных карбенов.
лишь слабо конкурирует с ним и только в случае более реакционноспособных карбенов.

Как и в случае реакции присоединения, возможен одностадийный синхронный или двухстадийный механизмы [38].
Достаточно надежно установлено, что синглетный метилен внедряется по связям  и
и  по синхронному механизму, что подтверждается, например, сохранением конфигурации при взаимодействии с хиральными центрами. Предложено два типа переходных состояний внедрения по связи
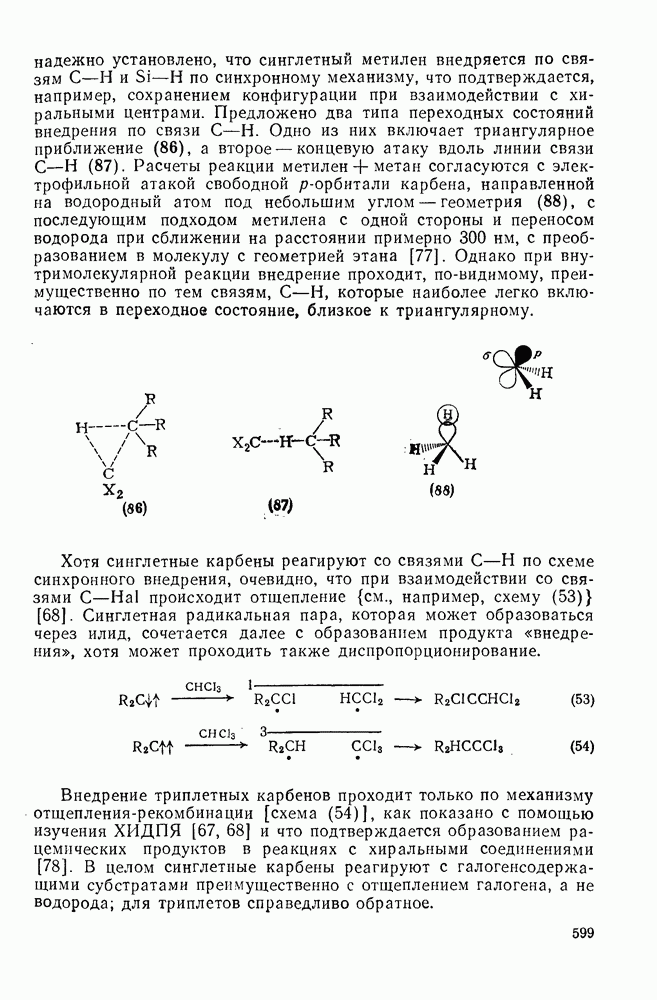
по синхронному механизму, что подтверждается, например, сохранением конфигурации при взаимодействии с хиральными центрами. Предложено два типа переходных состояний внедрения по связи  . Одно из них включает триангулярное приближение (86), а второе — концевую атаку вдоль линии связи
. Одно из них включает триангулярное приближение (86), а второе — концевую атаку вдоль линии связи  (87). Расчеты реакции метилен+метан согласуются с электрофильной атакой свободной р-орбитали карбена, направленной на водородный атом под небольшим углом — геометрия (88), с последующим подходом метилена с одной стороны и переносом водорода при сближении на расстоянии примерно 300 нм, с преобразованием в молекулу с геометрией этана [77]. Однако при внутримолекулярной реакции внедрение проходит, по-видимому, преимущественно по тем связям,
(87). Расчеты реакции метилен+метан согласуются с электрофильной атакой свободной р-орбитали карбена, направленной на водородный атом под небольшим углом — геометрия (88), с последующим подходом метилена с одной стороны и переносом водорода при сближении на расстоянии примерно 300 нм, с преобразованием в молекулу с геометрией этана [77]. Однако при внутримолекулярной реакции внедрение проходит, по-видимому, преимущественно по тем связям,  , которые наиболее легко включаются в переходное состояние, близкое к триангулярному.
, которые наиболее легко включаются в переходное состояние, близкое к триангулярному.

Хотя синглетные карбены реагируют со связями  по схеме синхронного внедрения, очевидно, что при взаимодействии со связями
по схеме синхронного внедрения, очевидно, что при взаимодействии со связями  происходит отщепление {см., например, схему
происходит отщепление {см., например, схему  ] [68]. Синглетная радикальная пара, которая может образоваться через илид, сочетается далее с образованием продукта «внедрения», хотя может проходить также диспропорционирование.
] [68]. Синглетная радикальная пара, которая может образоваться через илид, сочетается далее с образованием продукта «внедрения», хотя может проходить также диспропорционирование.

Внедрение триплетных карбенов проходит только по механизму отщепления-рекомбинации [схема  ], как показано с помощью изучения ХИДПЯ [67, 68] и что подтверждается образованием рацемических продуктов в реакциях с хиральными соединениями [78]. В целом синглетные карбены реагируют с галогенсодержащими субстратами преимущественно с отщеплением галогена, а не водорода; для триплетов справедливо обратное.
], как показано с помощью изучения ХИДПЯ [67, 68] и что подтверждается образованием рацемических продуктов в реакциях с хиральными соединениями [78]. В целом синглетные карбены реагируют с галогенсодержащими субстратами преимущественно с отщеплением галогена, а не водорода; для триплетов справедливо обратное.
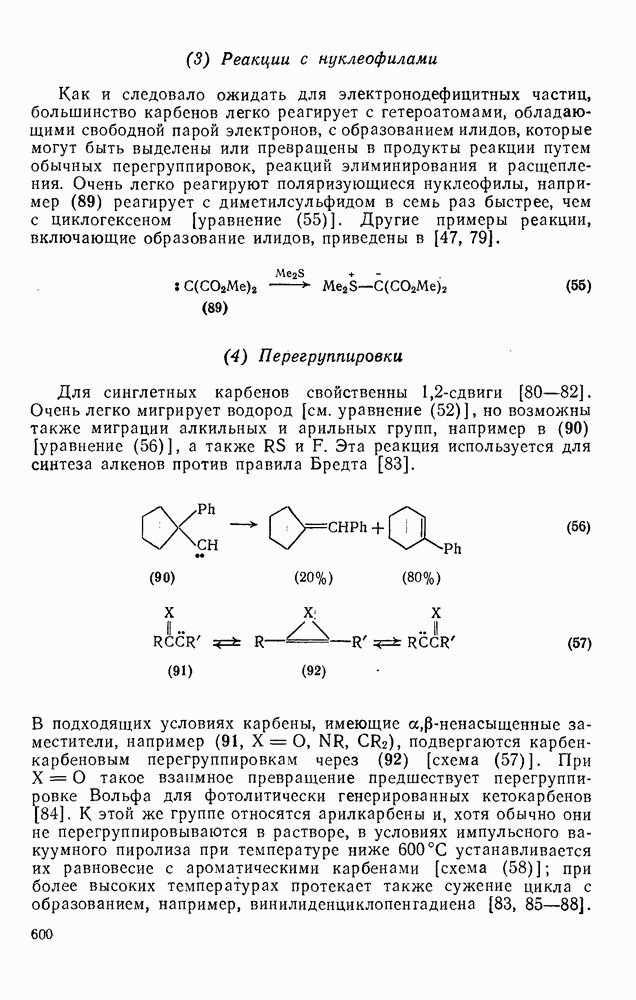
(3) Реакции с нуклеофилами
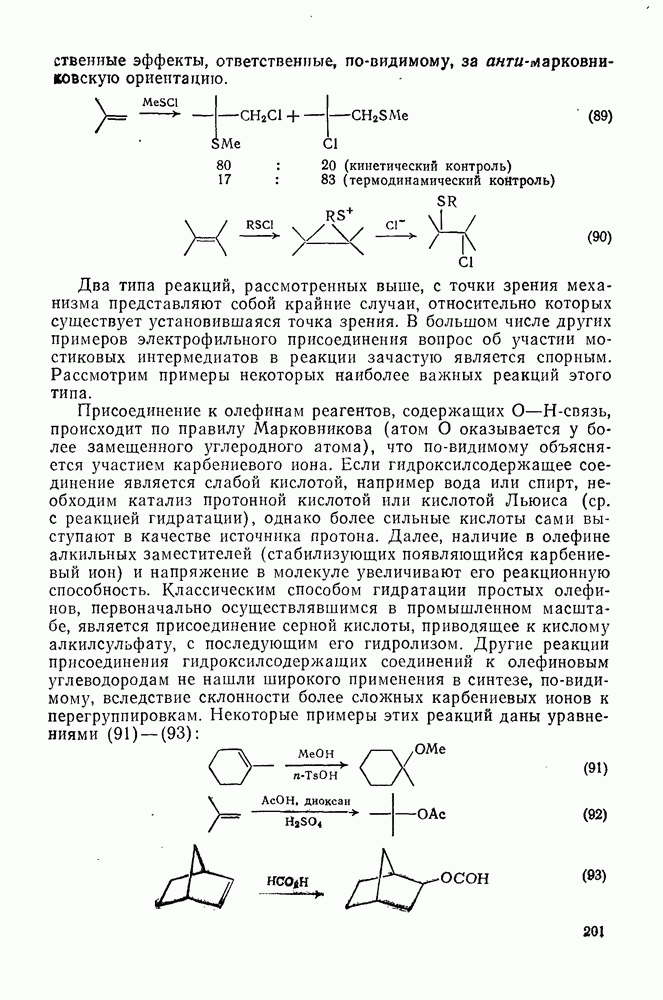
Как и следовало ожидать для электронодефицитных частиц, большинство карбенов легко реагирует с гетероатомами, обладающими свободной парой электронов, с образованием илидов, которые могут быть выделены или превращены в продукты реакции путем обычных перегруппировок, реакций элиминирования и расщепления. Очень легко реагируют поляризующиеся нуклеофилы, например (89) реагирует с диметилсульфидом в семь раз быстрее, чем с циклогексеном [уравнение (55)]. Другие примеры реакции, включающие образование илидов, приведены в [47, 79].

(4) Перегруппировки
Для синглетных карбенов свойственны  -сдвиги [80—82]. Очень легко мигрирует водород [см. уравнение
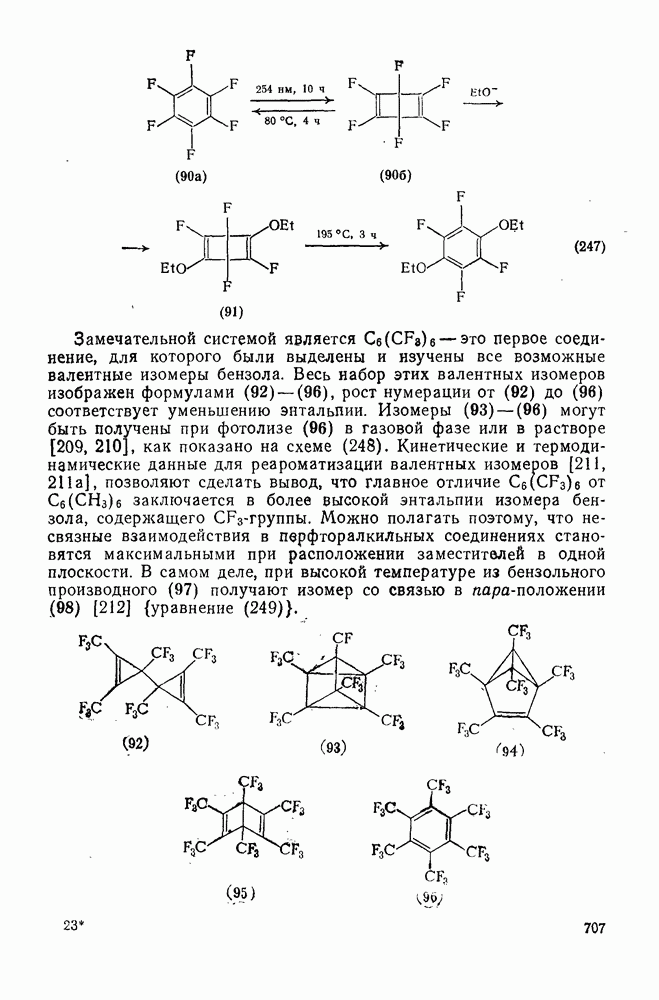
-сдвиги [80—82]. Очень легко мигрирует водород [см. уравнение  ], но возможны также миграции алкильных и арильных групп, например в (90) [уравнение
], но возможны также миграции алкильных и арильных групп, например в (90) [уравнение  ], а также RS и F. Эта реакция используется для синтеза алкенов против правила Бредта [83].
], а также RS и F. Эта реакция используется для синтеза алкенов против правила Бредта [83].

В подходящих условиях карбены, имеющие  -ненасыщенные заместители, например (
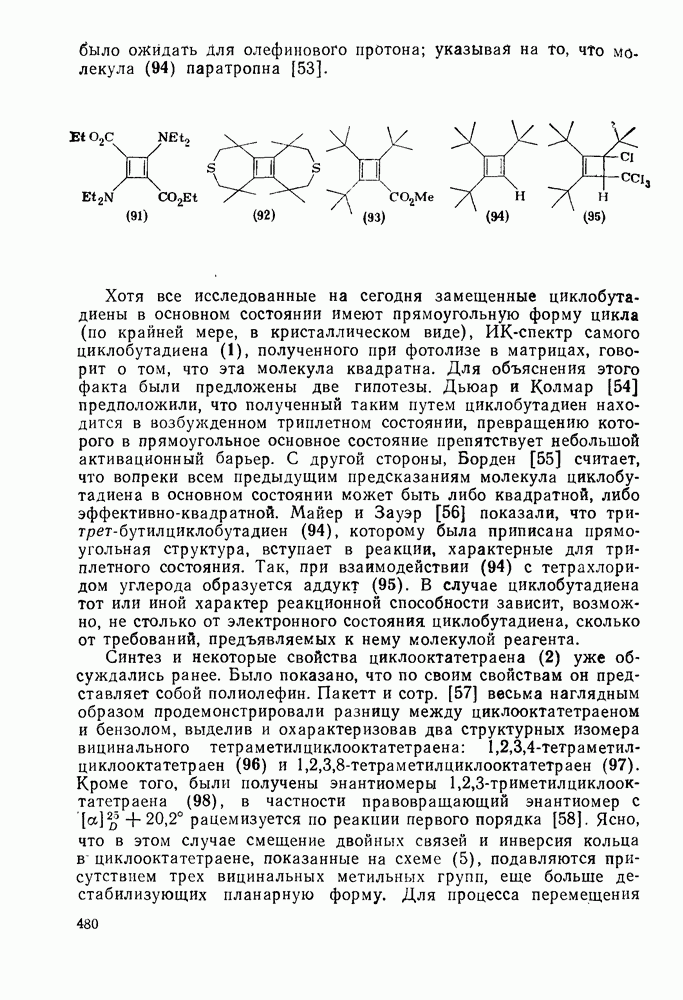
-ненасыщенные заместители, например ( ), подвергаются карбен-карбеновым перегруппировкам через (92) [схема (57)]. При X=0 такое взаимное превращение предшествует перегруппировке Вольфа для фотолитически генерированных кетокарбенов [84]. К этой же группе относятся арилкарбены и, хотя обычно они не перегруппировываются в растворе, в условиях импульсного вакуумного пиролиза при температуре ниже
), подвергаются карбен-карбеновым перегруппировкам через (92) [схема (57)]. При X=0 такое взаимное превращение предшествует перегруппировке Вольфа для фотолитически генерированных кетокарбенов [84]. К этой же группе относятся арилкарбены и, хотя обычно они не перегруппировываются в растворе, в условиях импульсного вакуумного пиролиза при температуре ниже  устанавливается их равновесие с ароматическими карбенами [схема
устанавливается их равновесие с ароматическими карбенами [схема  ] при более высоких температурах протекает также сужение цикла с образованием, например, винилиденциклопенгадиена [83, 85—88].
] при более высоких температурах протекает также сужение цикла с образованием, например, винилиденциклопенгадиена [83, 85—88].
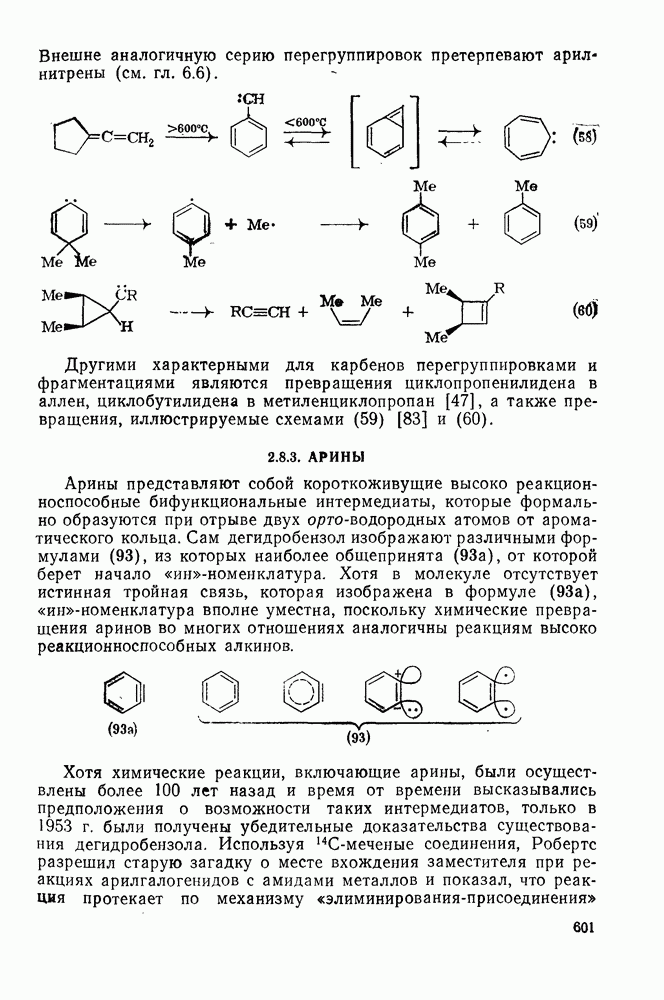
Внешне аналогичную серию перегруппировок претерпевают арил-нитрены (см. гл. 6.6).

Другими характерными для карбенов перегруппировками и фрагментациями являются превращения циклопропенилидена в аллен, циклобутилидена в метиленциклопропан [47], а также превращения, иллюстрируемые схемами (59) [83] и (60).
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- ПРЕДИСЛОВИЕ
- ИЗ ПРЕДИСЛОВИЯ К ТОМУ 1 АНГЛИЙСКОГО ИЗДАНИЯ
- ЧАСТЬ I. НОМЕНКЛАТУРА И СТЕРЕОХИМИЯ
- 1.1. ВВЕДЕНИЕ И СТЕРЕОХИМИЯ
- 1.1.2. СИММЕТРИЯ И ХИРАЛЬНОСТЬ
- 1.1.3. ХИМИЧЕСКАЯ ТОПОЛОГИЯ
- 1.1.4. ИЗОМЕРИЯ
- 1.1.4.2. Строение
- 1.1.4.3. Абсолютная конфигурация
- 1.1.4.4. Относительная конфигурация
- 1.1.4.5. Конформация
- 1.1.4.6. Концепция изомерии
- 1.1.5. ТОПИЗМ
- 1.1.5.2. Прохиральность
- 1.1.5.3. Псевдоасимметрия (псевдохиральность)
- 1.1.6. ТОПОМЕРИЯ
- 1.1.7. ДИНАМИЧЕСКАЯ СТЕРЕОХИМИЯ. КРАТКИЕ СВЕДЕНИЯ
- ЧАСТЬ 2. УГЛЕВОДОРОДЫ
- 2.1. НАСЫЩЕННЫЕ УГЛЕВОДОРОДЫ
- 2.1.2. Строение и номенклатура
- 2.1.2.1. Номенклатура IUPAC
- 2.1.2.2. Алициклические алканы
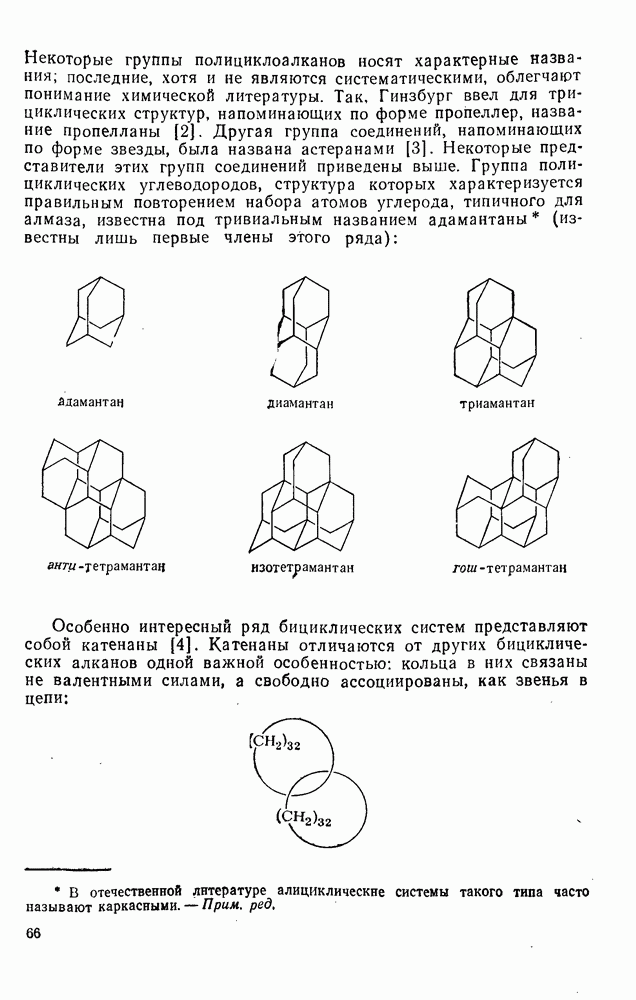
- 2.1.2.3. Полициклоалканы
- 2.1.3. ИСТОЧНИКИ ПОЛУЧЕНИЯ НАСЫЩЕННЫХ УГЛЕВОДОРОДОВ
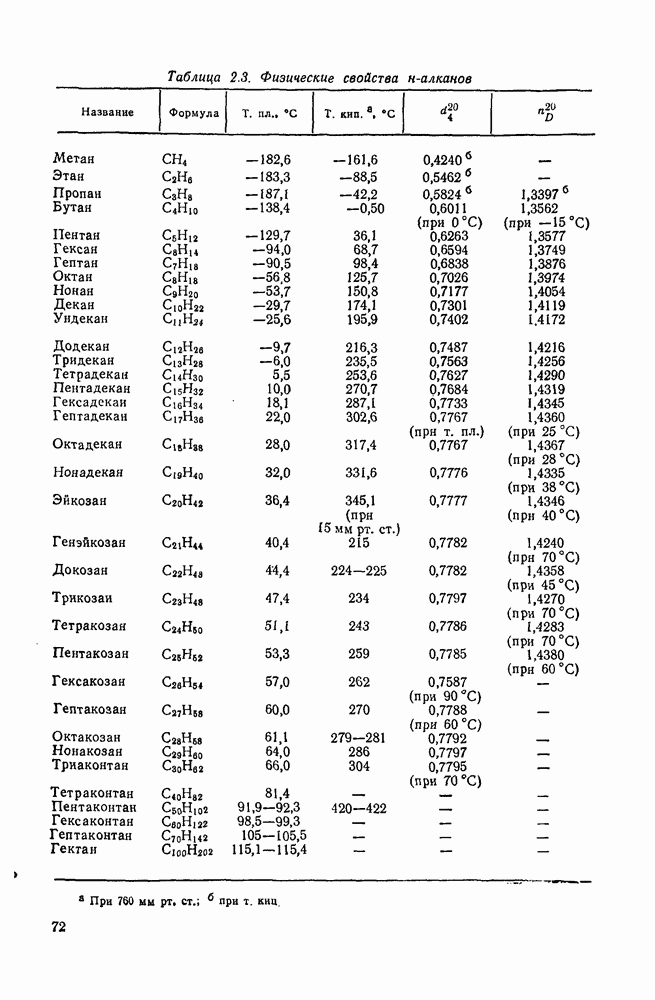
- 2.1.4. ФИЗИЧЕСКИЕ СВОЙСТВА
- 2.1.4.1. Ациклические алканы
- 2.1.4.2. Моно- и полициклоалканы
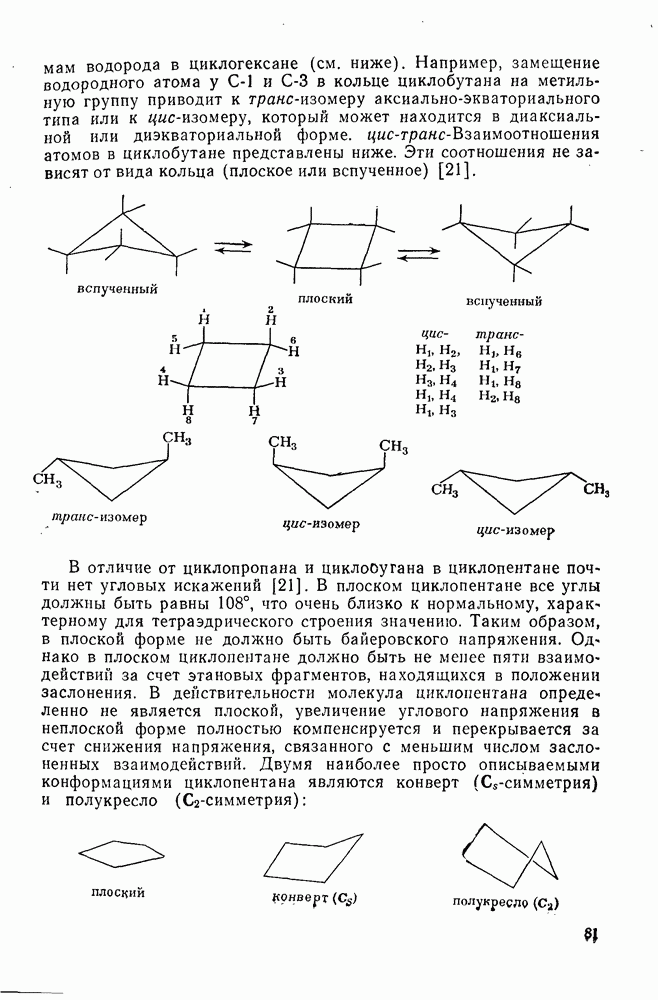
- 2.1.5. СТЕРЕОХИМИЯ И КОНФОРМАЦИОННЫЙ АНАЛИЗ
- 2.1.5.1. Углы и длины связей
- 2.1.5.2. Алкил- и полиалкилциклогексаны
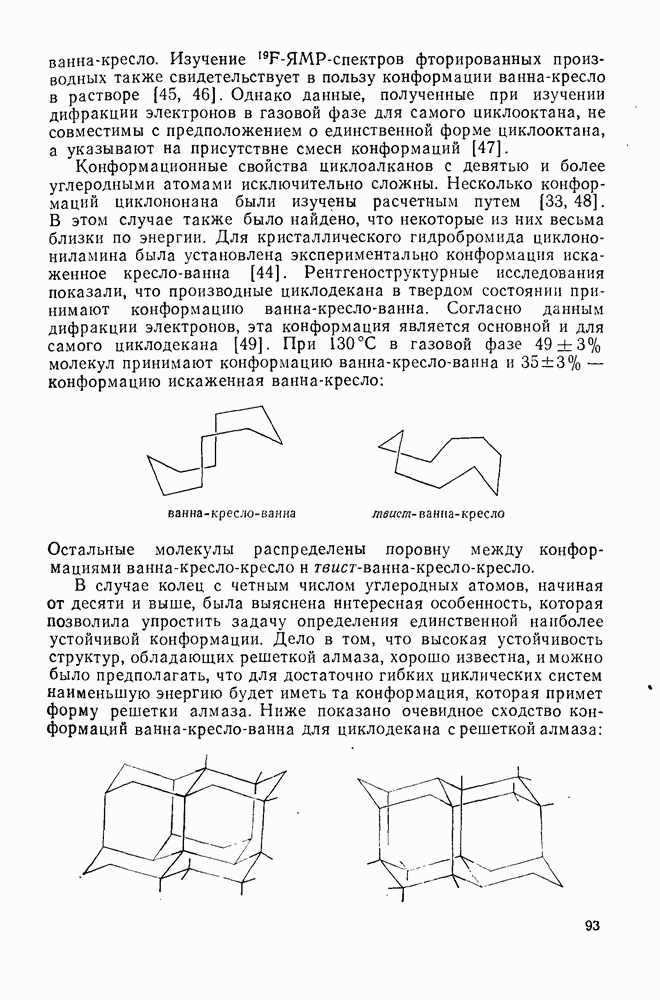
- 2.1.5.3. Конформация карбоциклических колец, больших, чем циклогексан
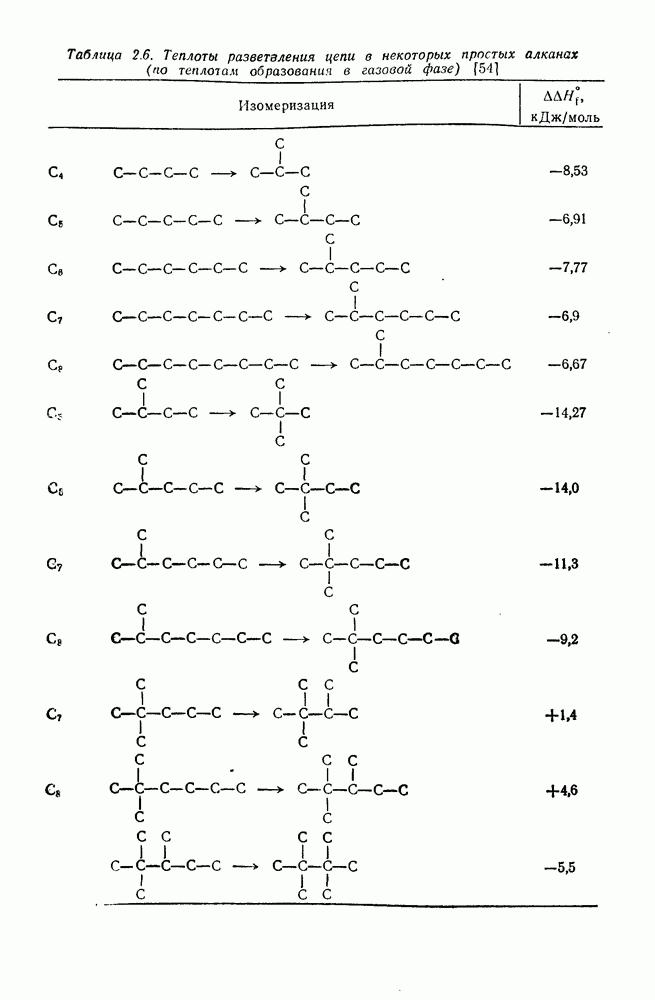
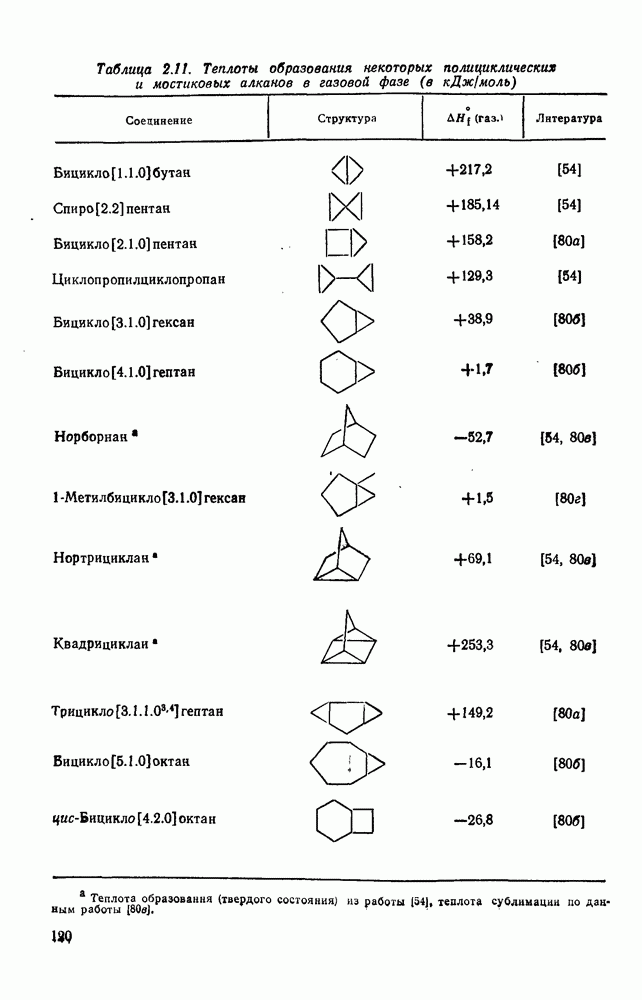
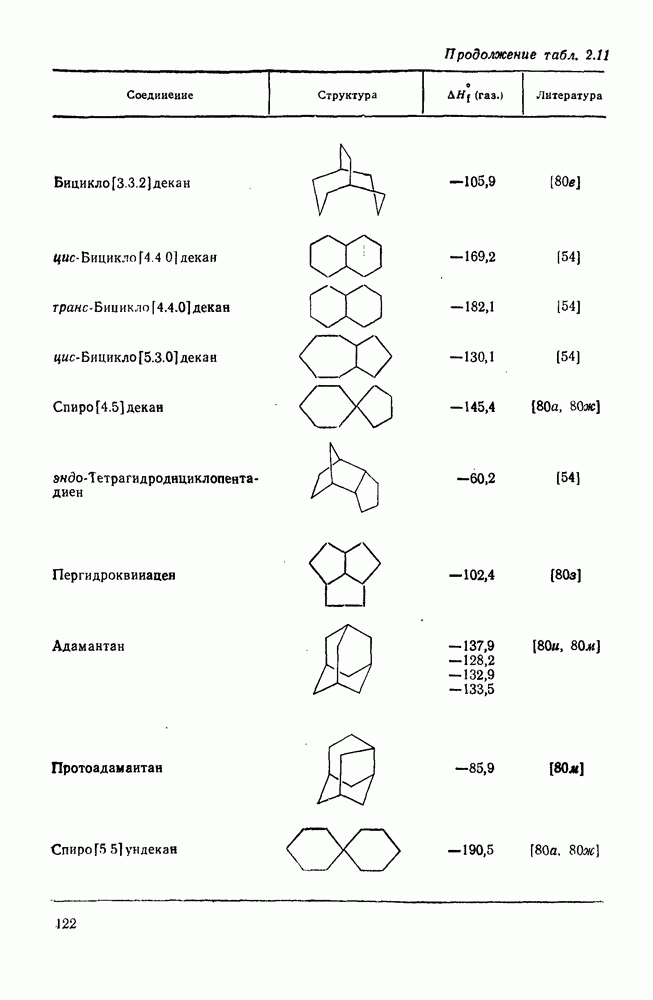
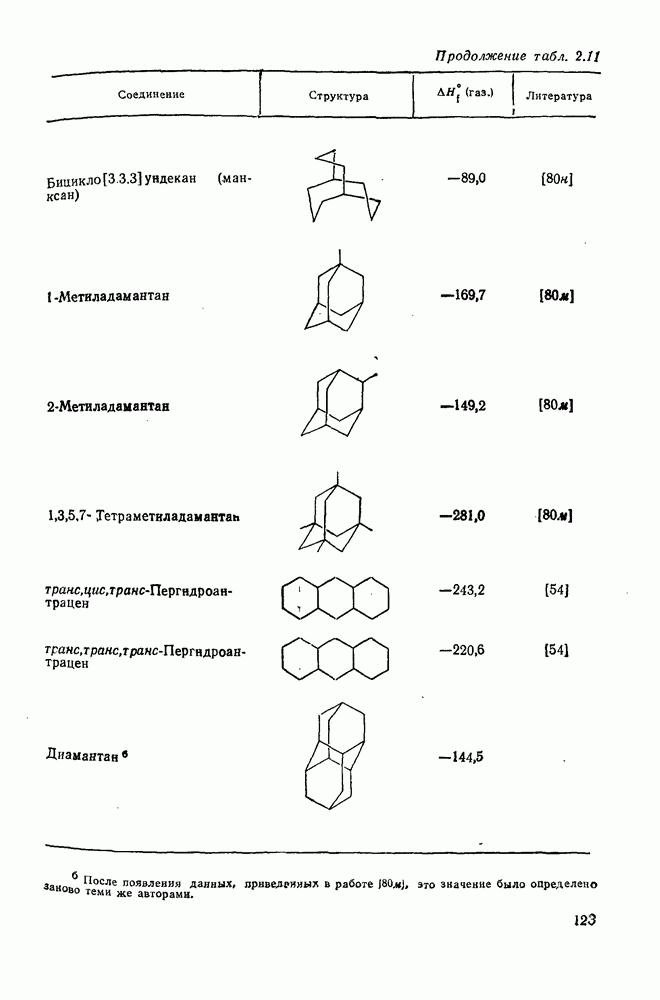
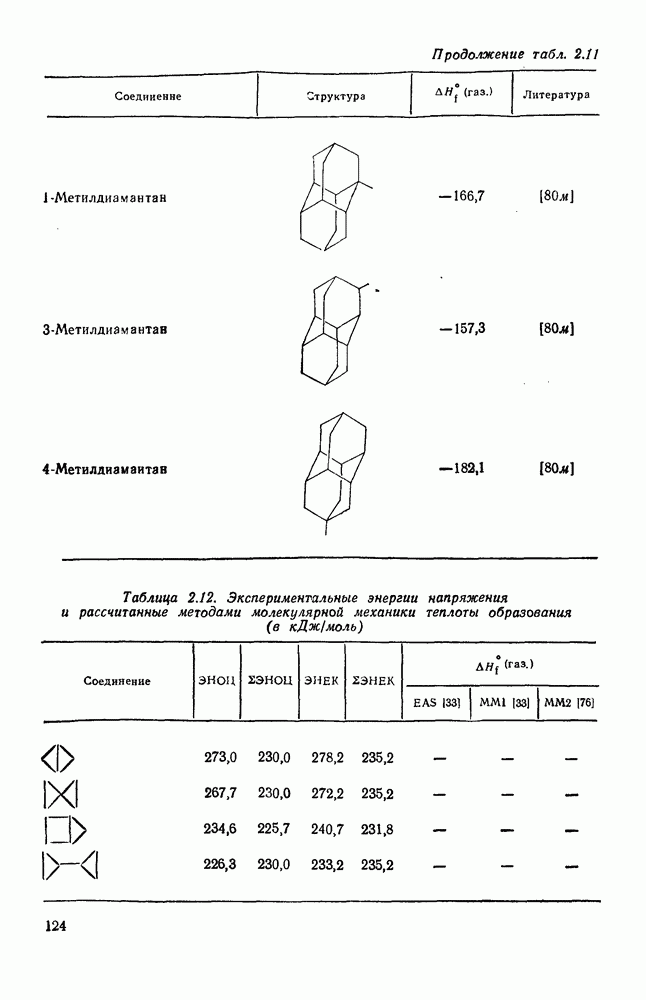
- 2.1.6. ТЕРМОХИМИЧЕСКИЕ СВОЙСТВА
- 2.1.6.1. Горение. Алканы и циклоалканы как топливо
- 2.1.6.2. Определение теплот сгорания и термохимические свойства
- 2.1.6.3. Эмпирические методы оценки теплот образования алканов
- 2.1.6.4. Оценка теплот образования алканов на основе энергии связей
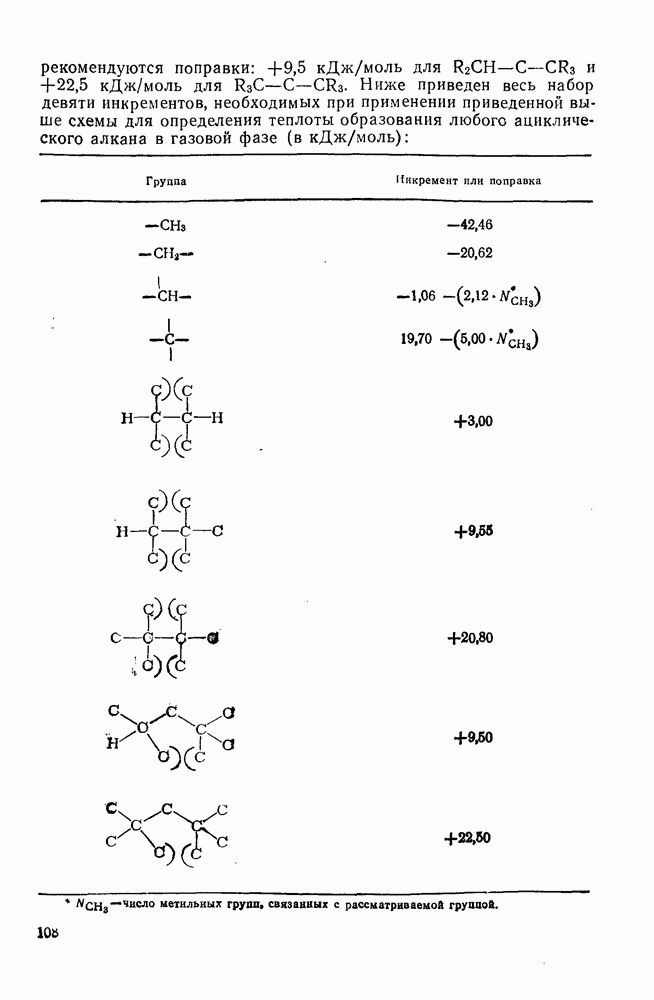
- 2.1.6.5. Оценка теплот образования алканов на основе инкрементов групп
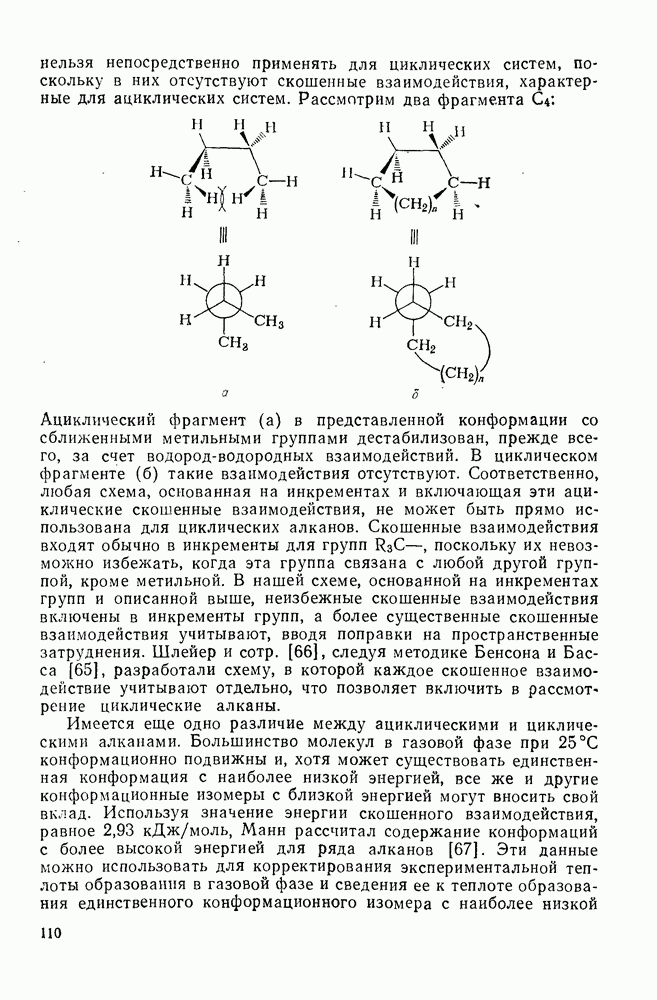
- 2.1.6.6. Оценка теплот образования циклических, полициклических и мостиковых алканов на основе инкрементов «скошенных разобщенных» групп и «единственных» наиболее устойчивых конформаций
- 2.1.6.7. Молекулярно-механические расчеты теплот образования и энергии напряжения
- 2.1.6.8. Моно- и полициклоалкаиы
- 2.1.7. ПОЛУЧЕНИЕ АЦИКЛИЧЕСКИХ АЛКАНОВ
- 2.1.7.1. Получение алканов восстановлением олефинов
- 2.1.7.2. Получение алканов из альдегидов и кетонов
- 2.1.7.3. Получение алканов из спиртов и алкилгалогенидов
- 2.1.7.4. Получение алканов из карбоновых кислот
- 2.1.8. СИНТЕЗ МОНО- И ПОЛИЦИКЛОАЛКАНОВ
- 2.1.9. РЕАКЦИИ АЦИКЛИЧЕСКИХ АЛКАНОВ
- 2.1.9.1. Галогенирование
- 2.1.9.2. Нитрование
- 2.1.9.3. Окисление
- 2.1.9.4. Каталитическая изомеризация алканов
- 2.1.9.5. Каталитическое алкилирование алканов
- 2.1.9.6. Реакции крекинга алканов
- 2.1.9.7. Термический крекинг
- 2.1.9.8. Каталитический крекинг
- 2.1.9.9. Каталитический риформинг и дегидроциклизация алканов
- 2.1.10. РЕАКЦИИ ЦИКЛОАЛКАНОВ И ПОЛИЦИКЛОАЛКАНОВ
- 2.2. ОЛЕФИНОВЫЕ И АЦЕТИЛЕНОВЫЕ УГЛЕВОДОРОДЫ
- 2.2.2. ПОЛУЧЕНИЕ ОЛЕФИНОВ
- 2.2.2.1. Элиминирование в системах
- 2.2.2.2. Элиминирование из систем
- 2.2.2.3. Циклоэлиминирование
- 2.2.2.4. Частичное восстановление
- 2.2.2.5. Элиминирование сульфонилгидразонов
- 2.2.2.6. Реакция Виттига и родственные ей реакции
- 2.2.2.7. Различные реакции конденсации
- 2.2.2.8. Электроциклические реакции
- 2.2.2.9. Циклоолигомеризация
- 2.2.2.11. Реакции винильных производных
- 2.2.3. РЕАКЦИИ ОЛЕФИНОВ
- 2.2.3.1. Электрофильное присоединение
- 2.2.3.2. Нуклеофильное присоединение
- 2.2.3.3. Радикальное присоединение
- 2.2.3.4. Циклоприсоединение и родственные реакции
- 2.2.3.5. Окисление
- 2.2.3.6. Восстановление
- 2.2.3.7. Перегруппировки
- 2.2.3.8. Фотохимические реакции
- 2.2.3.9. Прочие реакции
- 2.3. ДИЕНЫ, ПОЛНЕНЫ И АЦЕТИЛЕНОВЫЕ УГЛЕВОДОРОДЫ
- 2.3.1. СОПРЯЖЕННЫЕ ДИЕНЫ И ПОЛНЕНЫ
- 2.3.1.2. Получение сопряженных диенов
- 2.3.2. РЕАКЦИИ СОПРЯЖЕННЫХ ДИЕНОВ
- 2.3.2.2. Восстановление
- 2.3.2.3. Гидроборирование
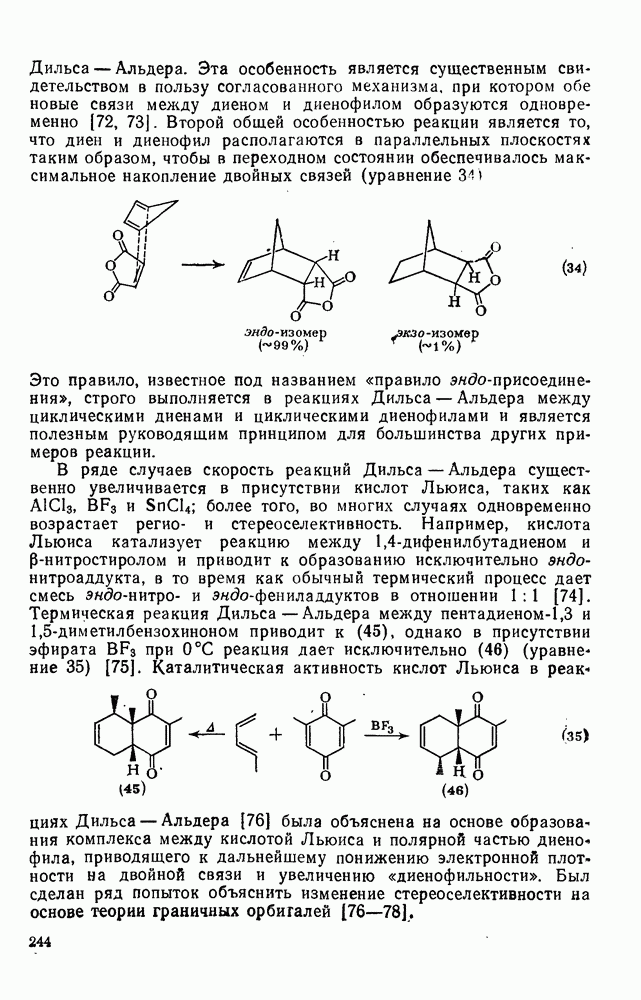
- 2.3.2.4. Реакция Дильса — Альдера
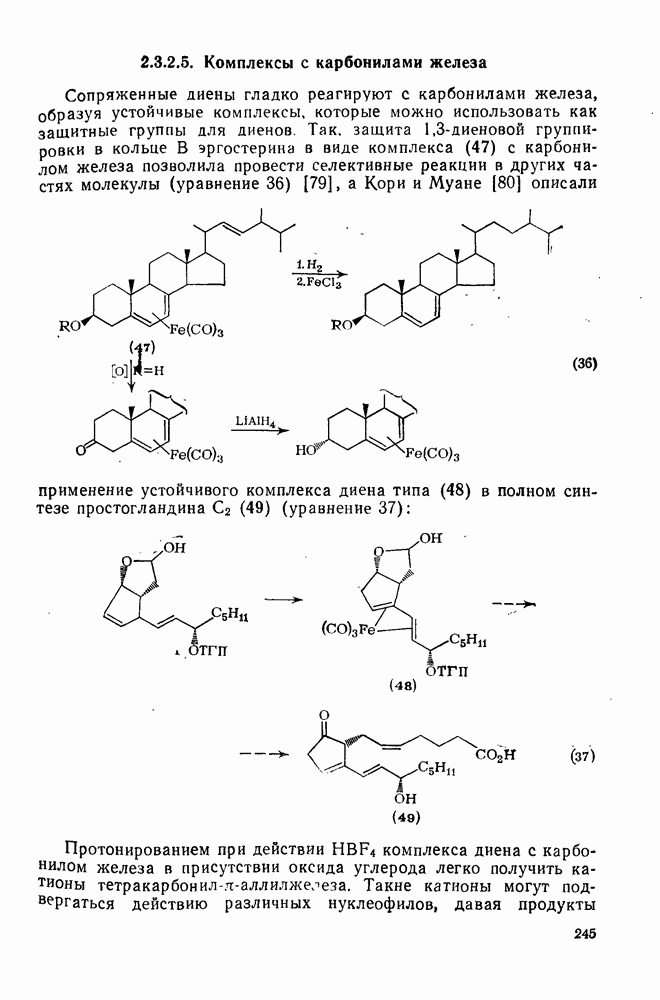
- 2.3.2.5. Комплексы с карбонилами железа
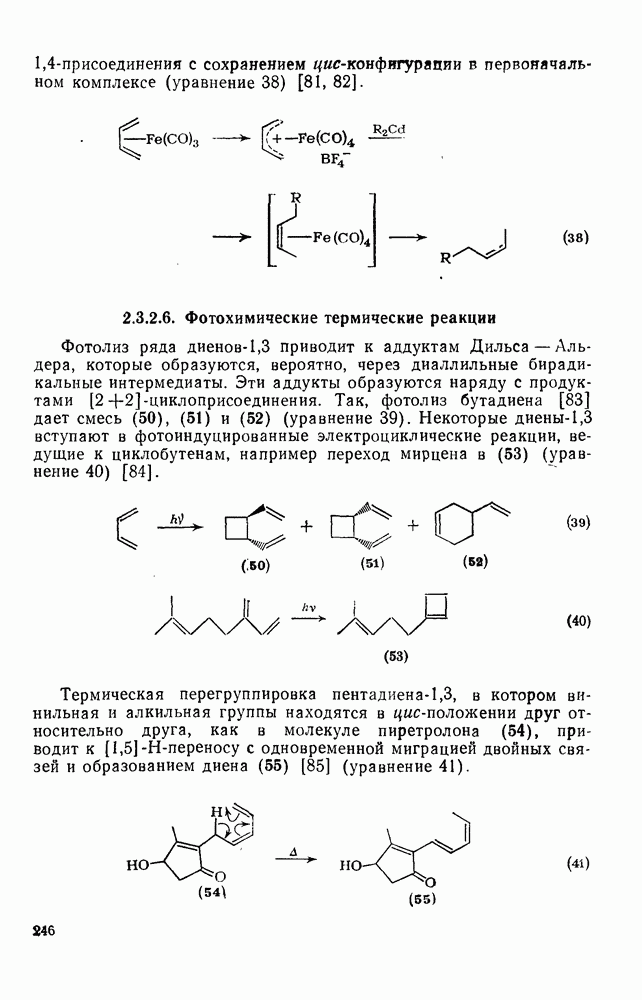
- 2.3.2.6. Фотохимические термические реакции
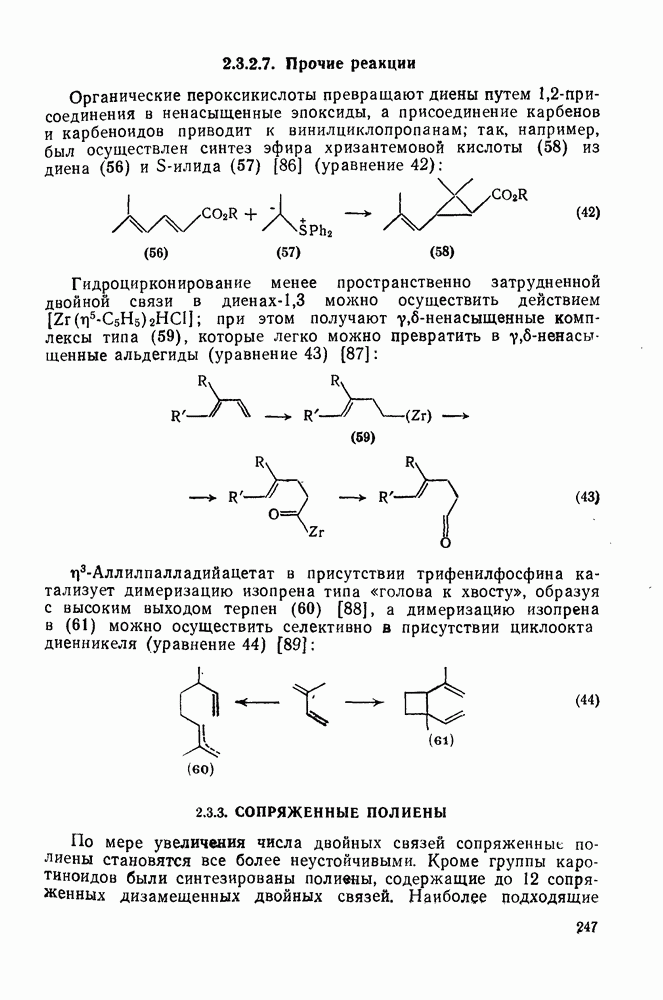
- 2.3.2.7. Прочие реакции
- 2.3.3. СОПРЯЖЕННЫЕ ПОЛИЕНЫ
- 2.3.4. ПРИРОДНЫЕ ДИЕНЫ И ПОЛНЕНЫ
- 2.3.5. АЛЛЕНЫ И КУМУЛЕНЫ
- 2.3.5.2. Получение алленов
- 2.3.6. РЕАКЦИИ АЛЛЕНОВ
- 2.3.6.2. Гидрирование
- 2.3.6.3. Реакции алленов в присутствии комплексов металлов
- 2.3.7. КУМУЛЕНЫ
- 2.3.8. ПРИРОДНЫЕ АЛЛЕНЫ И КУМУЛЕНЫ
- 2.3.9. АЦЕТИЛЕНЫ И ПОЛИАЦЕТИЛЕНЫ
- 2.3.9.2. Получение ацетиленов
- 2.3.10. РЕАКЦИИ АЦЕТИЛЕНОВ
- 2.3.10.2. Изомеризация
- 2.3.10.3. Пропаргильные перегруппировки
- 2.3.10.4. Реакции присоединения
- 2.3.10.5. Гидроборирование и гидроалюминирование
- 2.3.10.6. Реакции замещения
- 2.3.10.7. Восстановление
- 2.3.10.8. Окисление
- 2.3.10.9. Циклоприсоединение
- 2.3.10.10. Реакции катализуемые металлами
- 2.3.11. ПОЛИАЦЕТИЛЕНЫ
- 2.3.12. ПРИРОДНЫЕ АЦЕТИЛЕНЫ И ПОЛИАЦЕТИЛЕНЫ
- 2.3.13. СОПРЯЖЕННЫЕ ЕНИНЫ
- 2.3.13.1. Получение сопряженных енинов
- 2.3.14. РЕАКЦИИ СОПРЯЖЕННЫХ ЕНИНОВ
- 2.3.15. ПРИРОДНЫЕ СОПРЯЖЕННЫЕ ЕНИНЫ
- 2.4. АРОМАТИЧНОСТЬ
- 2.4.2. ЭЛЕКТРОННЫЕ ТЕОРИИ СТРОЕНИЯ БЕНЗОЛА
- 2.4.3. КРИТЕРИИ АРОМАТИЧНОСТИ
- 2.4.3.1. Термодинамические свойства
- 2.4.3.2. Структурные особенности
- 2.4.3.3. Магнитные свойства
- 2.4.3.4. Прочие критерии
- 2.4.4. АНТИАРОМАТИЧНОСТЬ
- 2.4.4.1. Термодинамические свойства
- 2.4.4.2. Структурные особенности
- 2.4.4.3. Магнитные свойства
- 2.4.4.4. Прочие свойства
- 2.4.5. ТЕОРЕТИЧЕСКИЕ ОПРЕДЕЛЕНИЯ АРОМАТИЧНОСТИ
- 2.4.5.1. Полуэмпирические расчеты и дьюаровская резонансная энергия
- 2.4.5.2. Расчеты по методу валентных пар и применение резонансного метода
- 2.4.5.3. Локализация связей
- 2.4.5.4. Связь энергетических критериев с критериями локализации связей
- 2.4.6. АРОМАТИЧЕСКИЕ ПЕРЕХОДНЫЕ СОСТОЯНИЯ
- 2.5. АРЕНЫ И ИХ РЕАКЦИИ
- 2.5.2. НОМЕНКЛАТУРА
- 2.5.3. ФИЗИЧЕСКИЕ СВОЙСТВА АРЕНОВ
- 2.5.4. ПРОМЫШЛЕННОЕ ПРОИЗВОДСТВО АРЕНОВ
- 2.5.5. ЦИКЛОТРИМЕРИЗАЦИЯ АЦЕТИЛЕНОВ
- 2.5.6. РЕАКЦИИ ЭЛЕКТРОФИЛЬНОГО ПРИСОЕДИНЕНИЯ — ЭЛИМИНИРОВАНИЯ АРЕНОВ
- 2.5.6.1. Механизм ароматического нитрования [15]
- 2.5.6.2. Кинетические изотопные эффекты [21]
- 2.5.6.3. Реакции, включающие ипсо-протонирование
- 2.5.6.4. Металлирование
- 2.5.6.5. Электрофилы IV группы
- 2.5.6.6. Электрофилы V группы
- 2.5.6.7. Электрофилы VI группы [18, 56]
- 2.5.6.8. Электрофилы VII группы [18, 25а, 56]
- 2.5.7. ОРИЕНТАЦИЯ В РЕАКЦИЯХ ЭЛЕКТРОФИЛЬНОГО ПРИСОЕДИНЕНИЯ — ЭЛИМИНИРОВАНИЯ
- 2.5.8. РАДИКАЛЬНОЕ ГАЛОГЕНИРОВАНИЕ АРЕНОВ В БОКОВУЮ ЦЕПЬ [96]
- 2.5.9. РЕАКЦИИ ПРИСОЕДИНЕНИЯ К АРЕНАМ
- 2.5.9.1. Восстановление аренов
- 2.5.9.2. Термическое циклоприсоединение к аренам
- 2.5.9.3. Фотоциклоприсоединение к моноциклическим аренам [126]
- 2.5.9.4. Фотохимические реакции полициклических аренов
- 2.6.10. ФОТОИЗОМЕРИЗАЦИЯ АРЕНОВ [126б]
- 2.5.11. ОКИСЛЕНИЕ АРЕНОВ [153]
- 2.5.12. РЕАКЦИИ АРЕНОВ С СИНГЛЕТНЫМ КИСЛОРОДОМ [162]
- 2.5.13. ПРИГОТОВЛЕНИЕ БИ- И ПОЛИАРИЛОВ
- 2.5.14. ВНУТРИМОЛЕКУЛЯРНАЯ ФОТОЦИКЛИЗАЦИЯ, ПРИВОДЯЩАЯ К ПОЛИЦИКЛИЧЕСКИМ АРЕНАМ
- 2.5.15. ВНУТРИМОЛЕКУЛЯРНАЯ ЦИКЛИЗАЦИЯ ДИЗАМЕЩЕННЫХ АРЕНОВ
- 2.5.16. ЦИКЛОФАНЫ
- 2.5.17. КОНФОРМАЦИЯ И ХИРАЛЬНОСТЬ АРЕНОВ
- 2.5.18. АЗУЛЕНЫ И НЕБЕНЗОИДНЫЕ АРЕНЫ
- 2.6. АННУЛЕНЫ И РОДСТВЕННЫЕ СИСТЕМЫ
- 2.6.2. МЕТОДЫ СИНТЕЗА
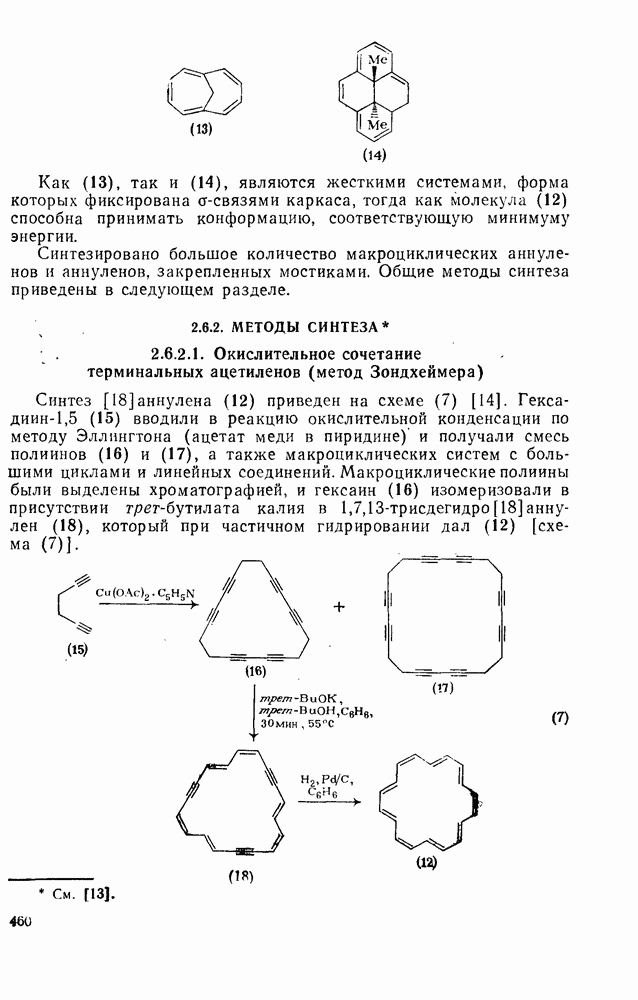
- 2.6.2.1. Окислительное сочетание терминальных ацетиленов (метод Зондхеймера)
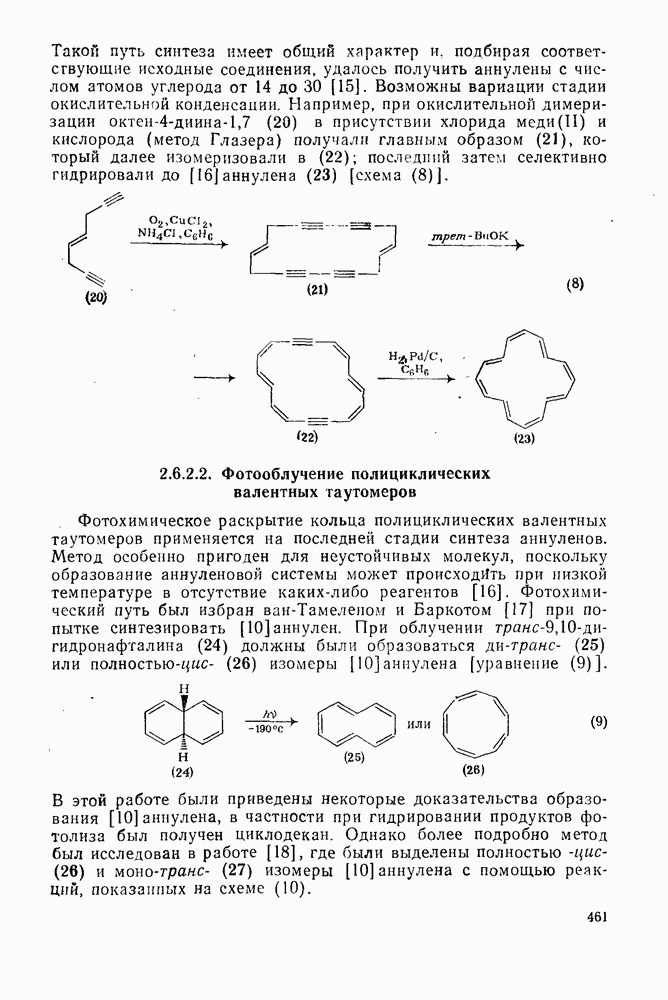
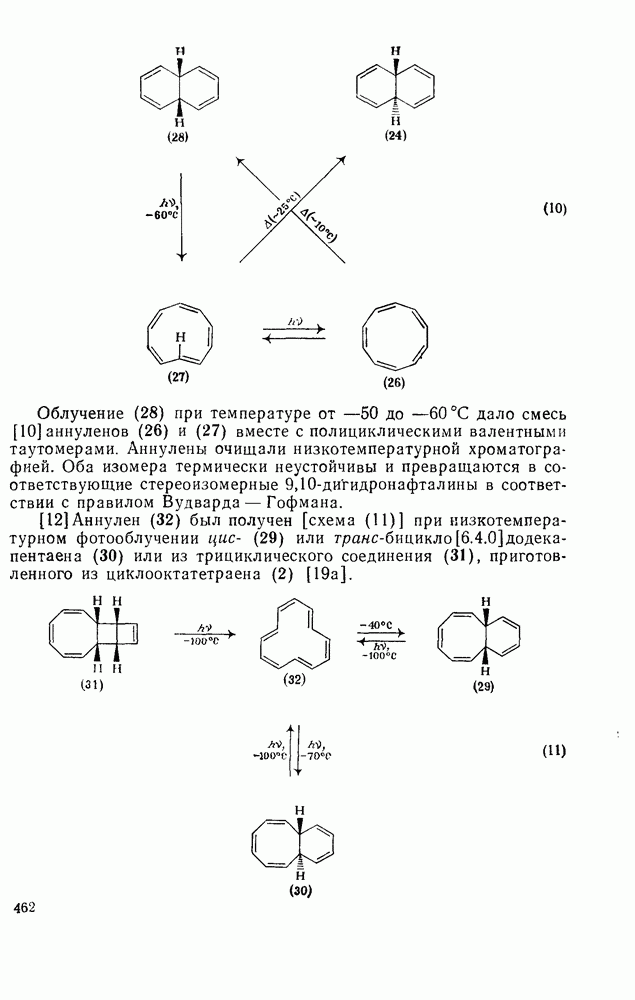
- 2.6.2.2. Фотооблучение полициклических валентных таутомеров
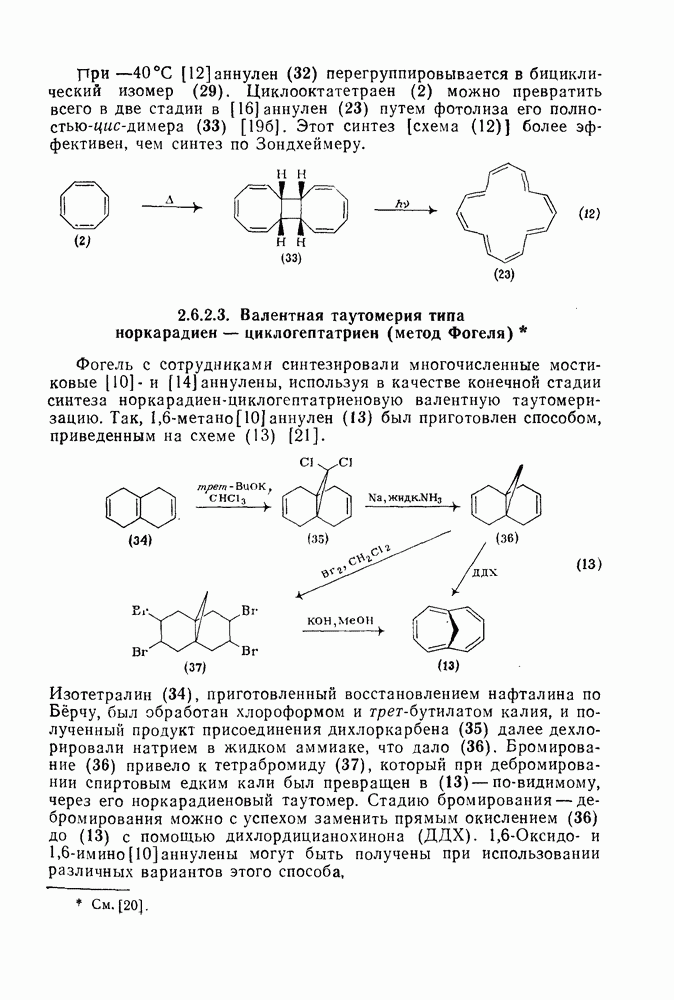
- 2.6.2.3. Валентная таутомерия типа норкарадиен — циклогептатриен (метод Фогеля)
- 2.6.2.4. Прочие методы
- 2.6.3. СВОЙСТВА АННУЛЕНОВ
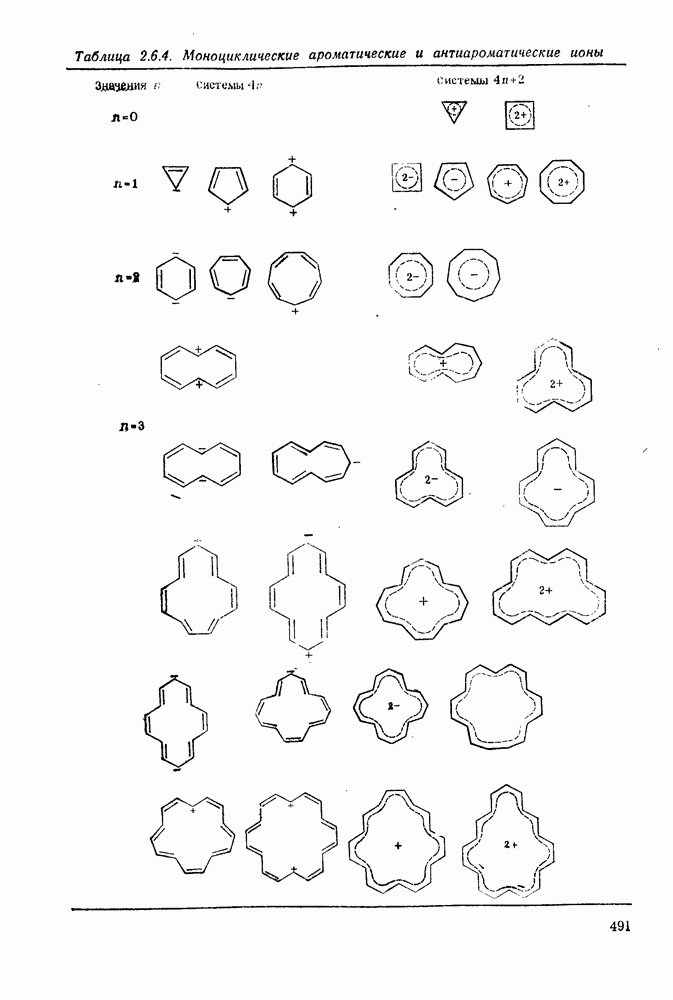
- 2.6.4. СВОЙСТВА 4n-АННУЛЕНОВ
- 2.6.5. ДЕГИДРОАННУЛЕНЫ
- 2.6.6. АННЕЛИРОВАННЫЕ АННУЛЕНЫ
- 2.6.7. АРОМАТИЧЕСКИЕ И АНТИАРОМАТИЧЕСКИЕ МОНОЦИКЛИЧЕСКИЕ ИОНЫ
- 2.6.8. АРОМАТИЧЕСКИЕ И АНТИАРОМАТИЧЕСКИЕ ПОЛИЦИКЛИЧЕСКИЕ ИОНЫ
- 2.6.9. ГОМОАРОМАТИЧЕСКИЕ СИСТЕМЫ
- 2.7. КАРБОКАТИОНЫ И КАРБАНИОНЫ
- 2.7.1.2. Краткий исторический очерк развития химии карбокатионов
- 2.7.1.3. Методы генерации карбокатионов
- 2.7.1.4. Типы карбокатионов
- 2.7.1.5. Изучение карбокатионов: методы и результаты
- 2.7.1.6. Реакции карбокатионов
- 2.7.2. КАРБАНИОНЫ
- 2.7.2.2. Методы генерации карбанионов
- 2.7.2.3. Типы карбанионов
- 2.7.2.4. Физические свойства карбанионов
- 2.7.5.2. Реакции карбанионов
- 2.8. РАДИКАЛЫ, КАРБЕНЫ, АРИНЫ
- 2.8.1. РАДИКАЛЫ
- 2.8.1.1. Структура, устойчивость и реакционная способность радикалов
- 2.8.1.2. Методы генерации и реакции радикалов
- 2.8.2. КАРБЕНЫ
- 2.8.2.1. Методы генерации карбенов и карбеноидов
- 2.8.2.2. Реакции карбенов
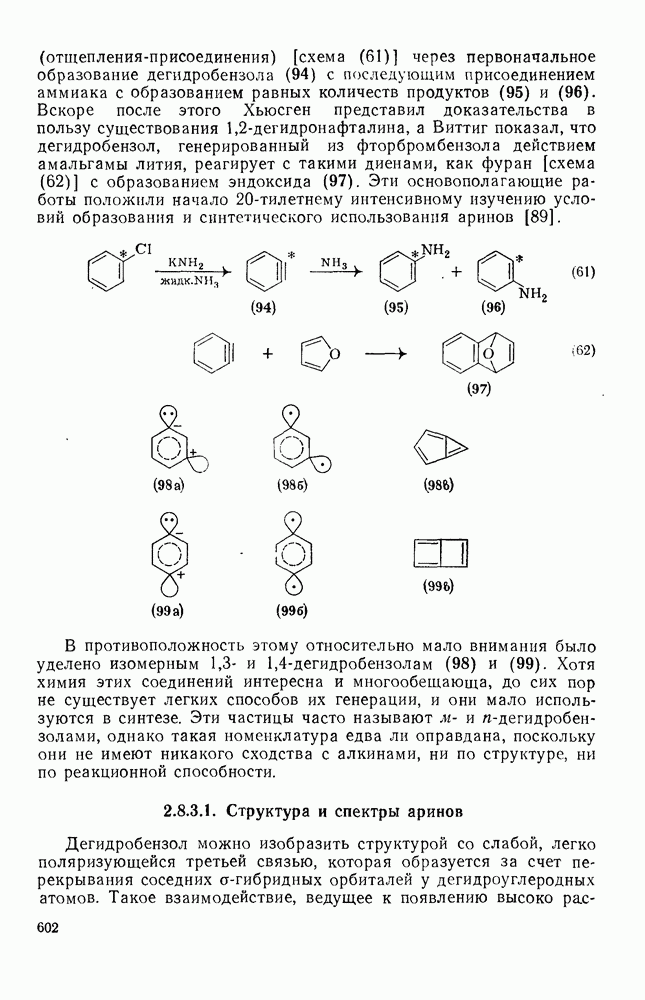
- 2.8.3. АРИНЫ
- 2.8.3.1. Структура и спектры аринов
- 2.8.3.2. Методы генерации аринов
- 2.8.3.3. Реакции аринов
- ЧАСТЬ 3. ГАЛОГЕНСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
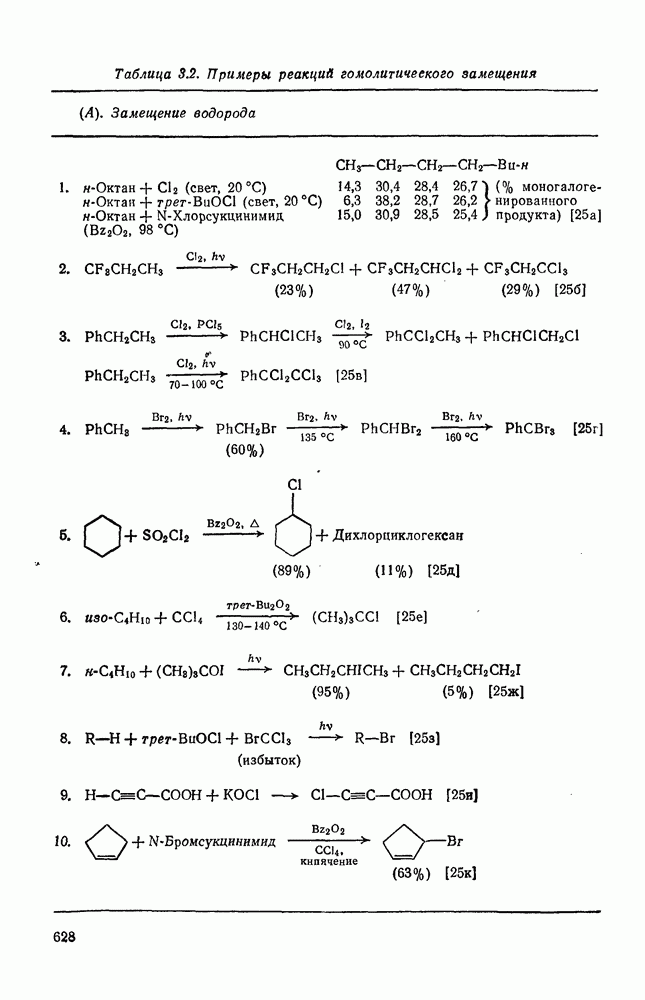
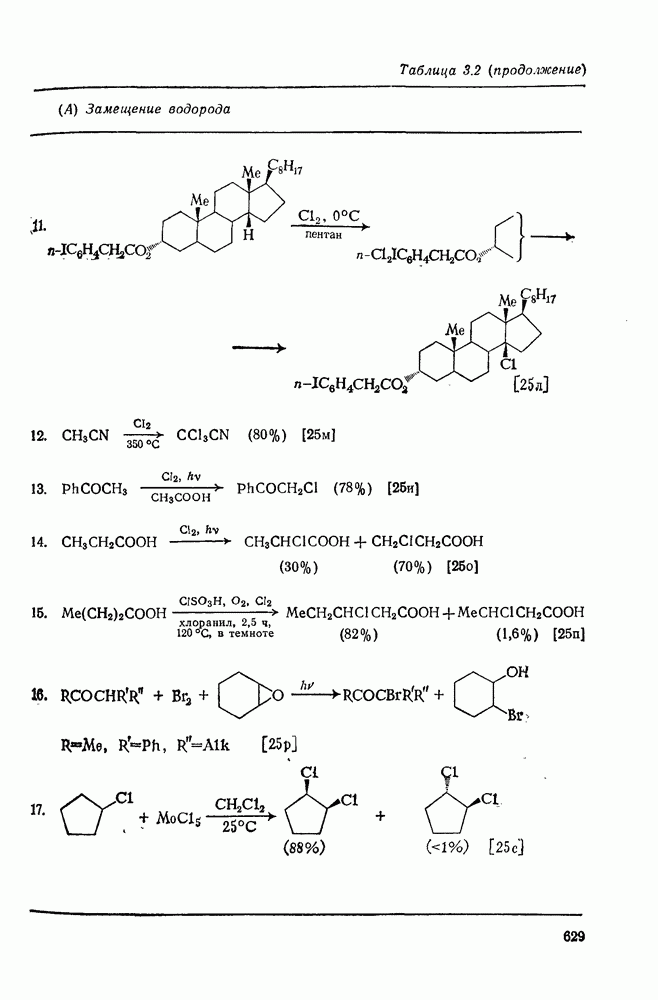
- 3.2. МЕТОДЫ ГАЛОГЕНИРОВАНИЯ
- 3.2.1. Гомолитическое замещение водорода
- 3.2.1.2. Использование галогенпроизводных в качестве реагентов
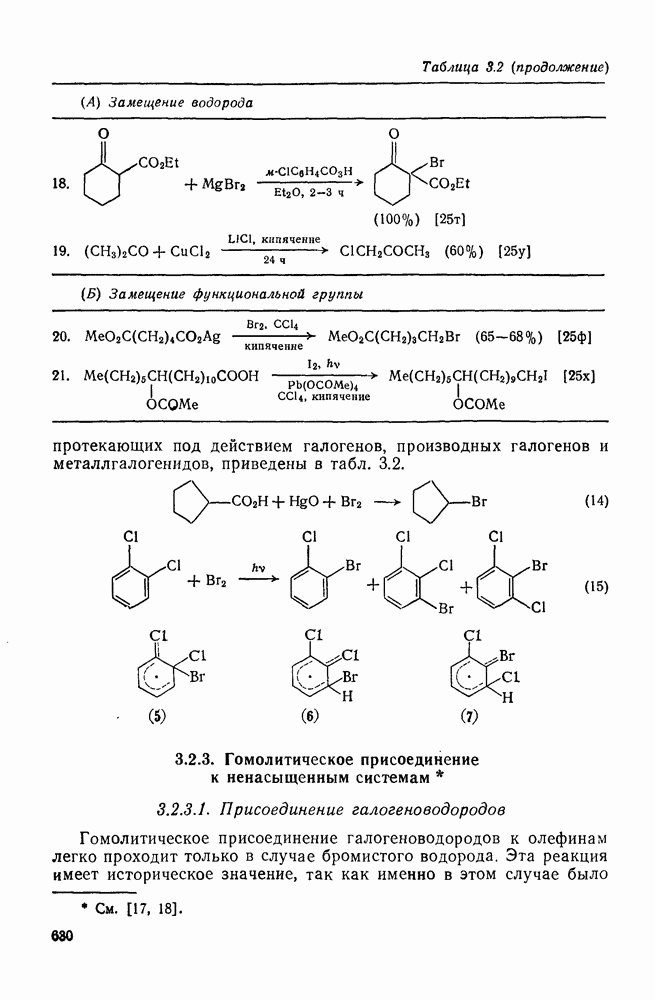
- 3.2.2. Гомолитическое замещение функциональных групп
- 3.2.3. Гомолитическое присоединение к ненасыщенным системам
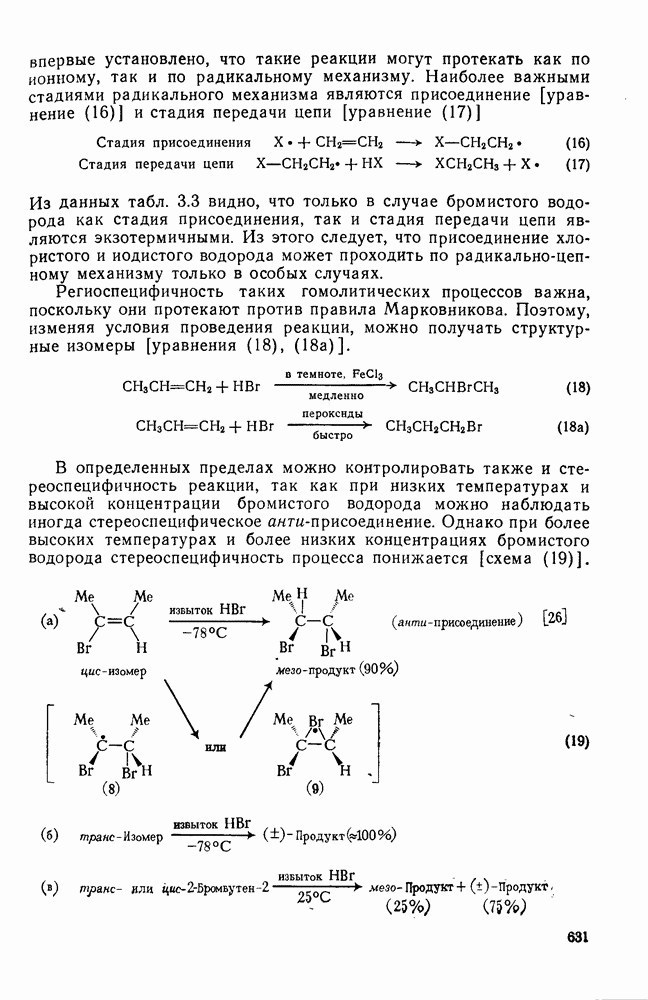
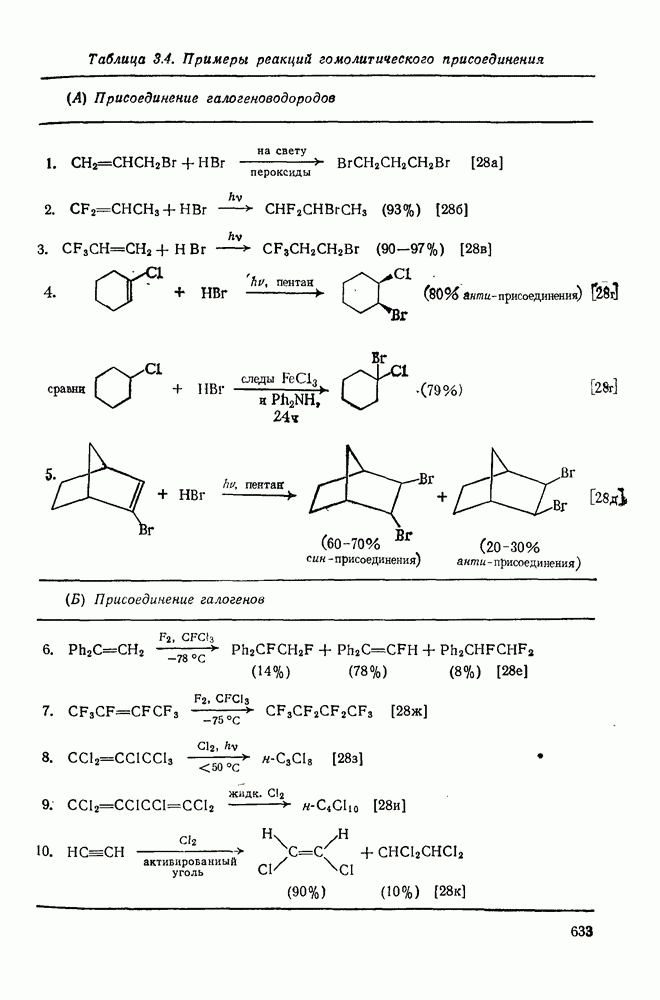
- 3.2.3.1. Присоединение галогеноводородов
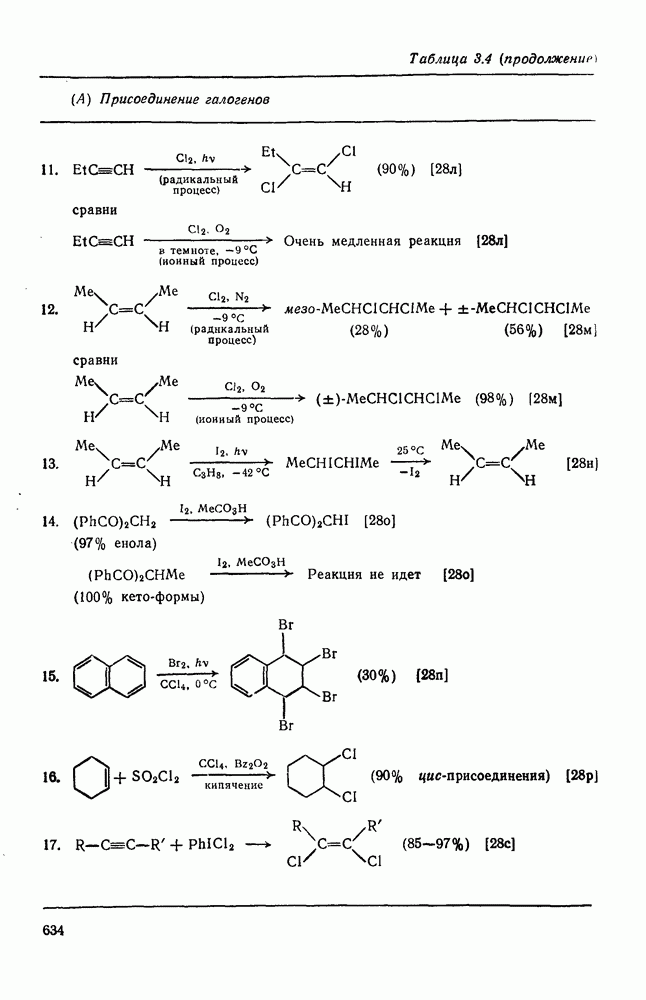
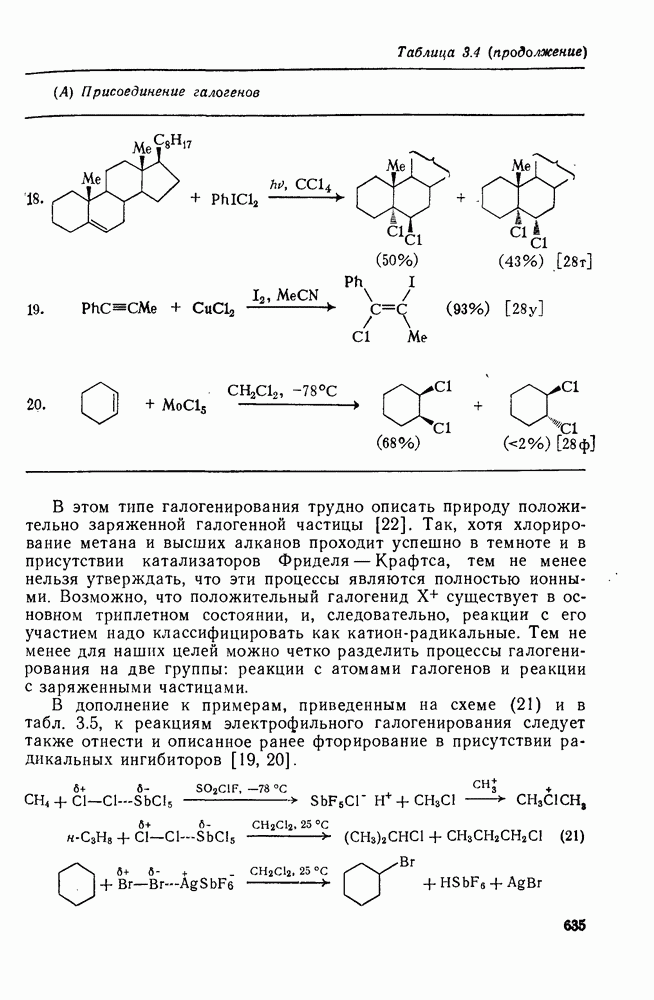
- 3.2.3.2. Присоединение галогенов
- 3.2.4. Электрофильное галогенирование
- 3.2.4.1. Замещение у насыщенной связи С-Н
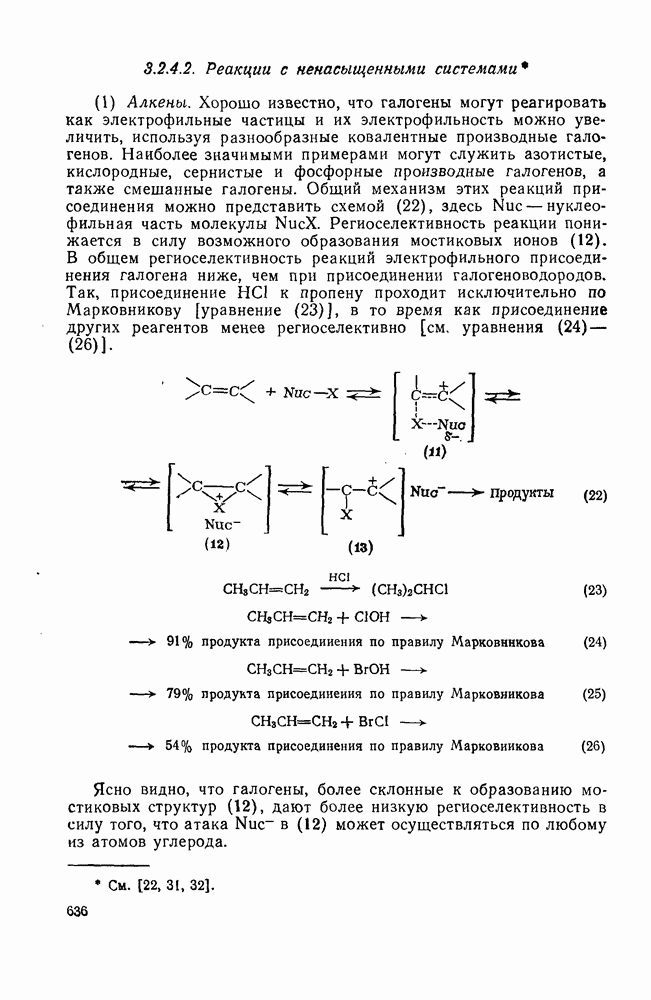
- 3.2.4.2. Реакции с ненасыщенными системами
- 3.2.4.3. Реакции с карбанионами
- 3.2.5. Нуклеофильное галогенирование
- 3.2.5.1. Галогенирование с замещением функциональной группы
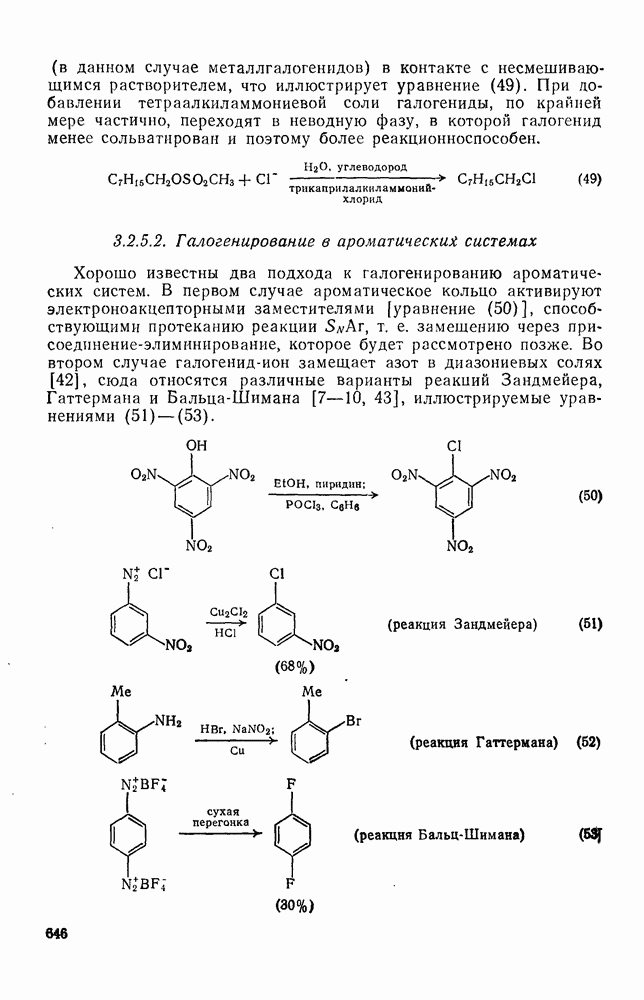
- 3.2.5.2. Галогенирование в ароматических системах
- 3.2.5.3. Галогенирование путем обмена галогенов
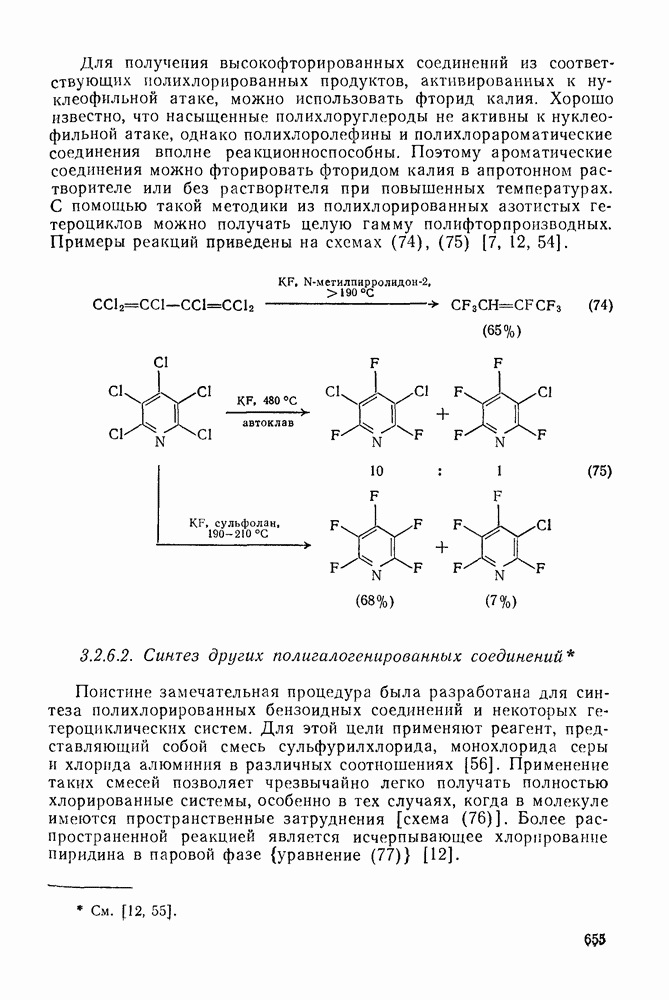
- 3.2.6. Синтез полигалогенированных соединений
- 3.2.6.1. Синтез полифторированных соединений
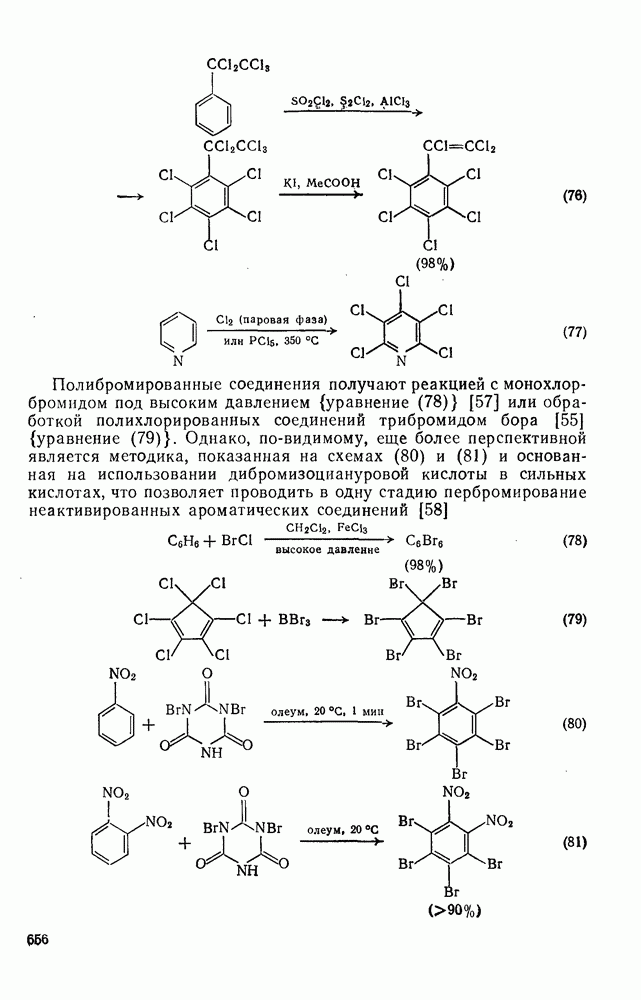
- 3.2.6.2. Синтез других полигалогенированных соединений
- 3.3. ГАЛОГЕНАЛКАНЫ
- 3.3.1. Характеристика связей углерод-галоген
- 3.3.2. Промышленное применение
- 3.3.3. Нуклеофильное замещение галогена
- 3.3.3.1. Реакции SN2 и родственные процессы
- 3.3.3.2. Соучастие соседних групп
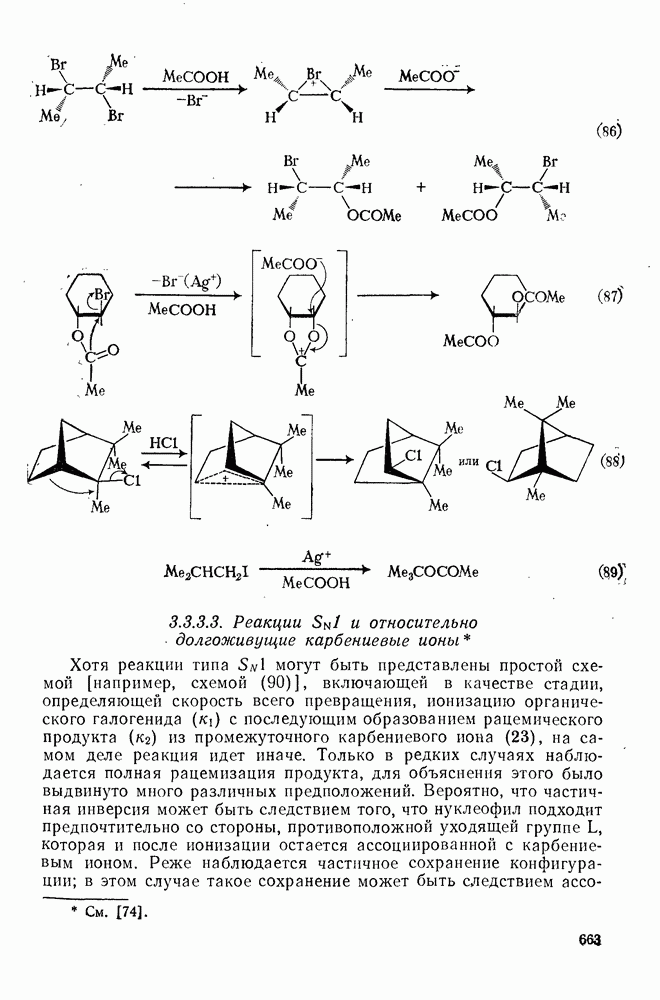
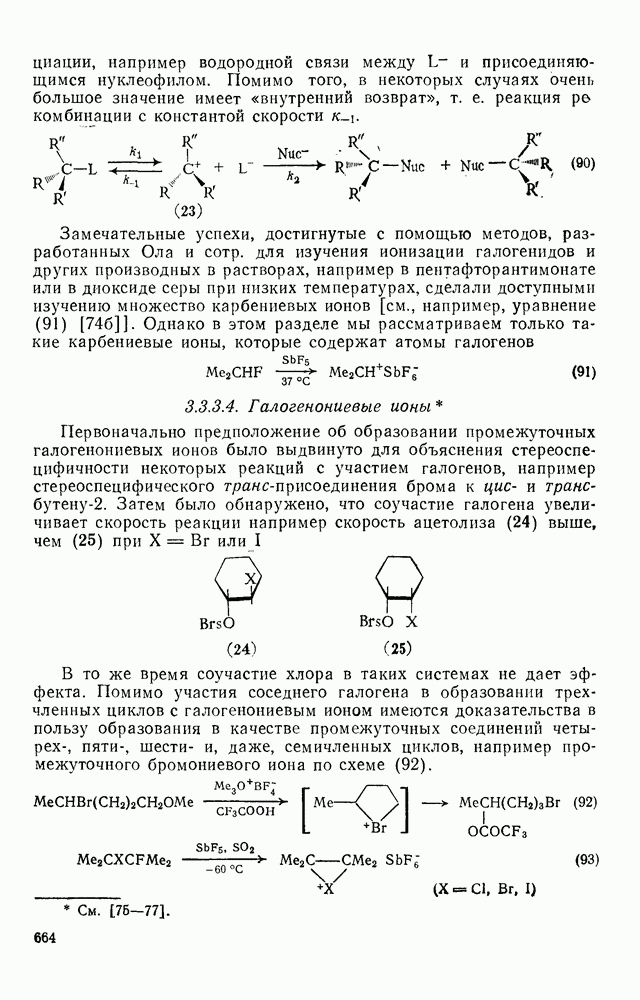
- 3.3.3.3. Реакции SN1 и относительно долгоживущие карбениевые ионы
- 3.3.3.4. Галогенониевые ионы
- 3.3.3.5. Галогенсодержащие карбениевые ионы
- 3.3.3.6. Механизм замещения с переносом электрона
- 3.3.4. Восстановление
- 3.3.5. Замещение на металлы
- 3.3.6. Элиминирование
- 3.3.6.1. b-Элиминирование
- 3.3.6.2. Галогенкарбанионы
- 3.3.6.3. Элиминирование через карбанионы
- 3.3.6.4. b-Элиминирование из металлорганических соединений
- 3.3.6.5. a-Элиминирование (генерирование карбенов)
- 3.4. ГАЛОГЕНАЛКЕНЫ
- 3.4.1. Синтез галогеналкенов
- 3.4.2. Нуклеофильная атака
- 3.4.2.1. Реакции, индуцируемые фторид-ионом
- 3.4.2.2. Другие реакции замещения
- 3.4.3. Радикальное присоединение
- 3.4.4. Электрофильное присоединение
- 3.4.5. Циклоприсоединение
- 3.4.5.1. [2+2]-Циклоприсоединение
- 3.4.5.2. [4+2]-Циклоприсоединение
- 3.5. ГАЛОГЕНАЛКИНЫ
- 3.6. ГАЛОГЕНАРЕНЫ
- 3.6.1. Замещение галогена
- 3.6.1.2. Присоединение-элиминирование
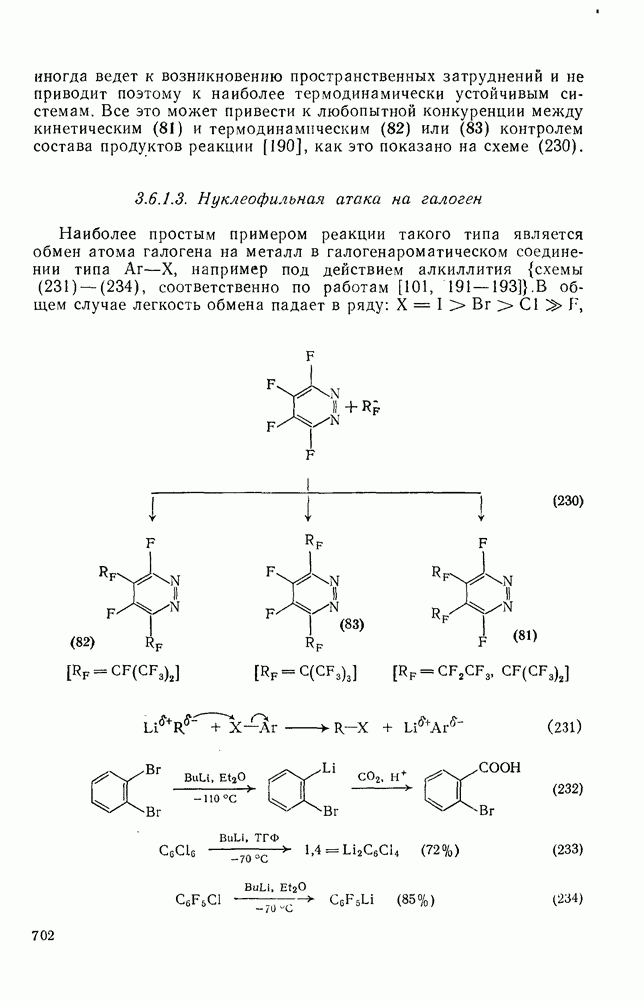
- 3.6.1.3. Нуклеофильная атака на галоген
- 3.6.1.4. Перенос электрона
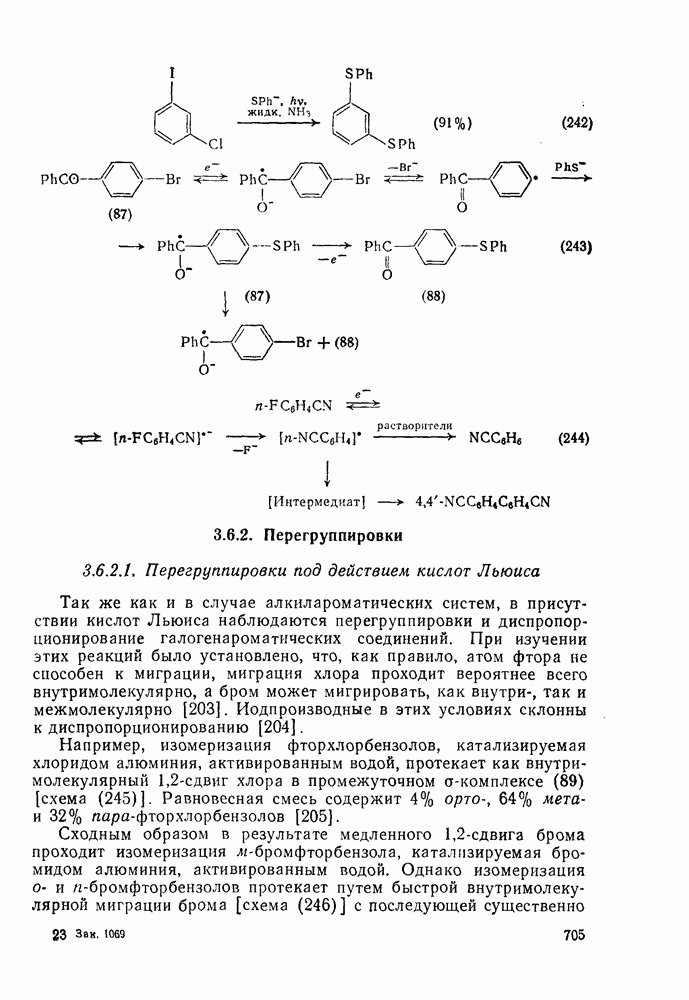
- 3.6.2. Перегруппировки
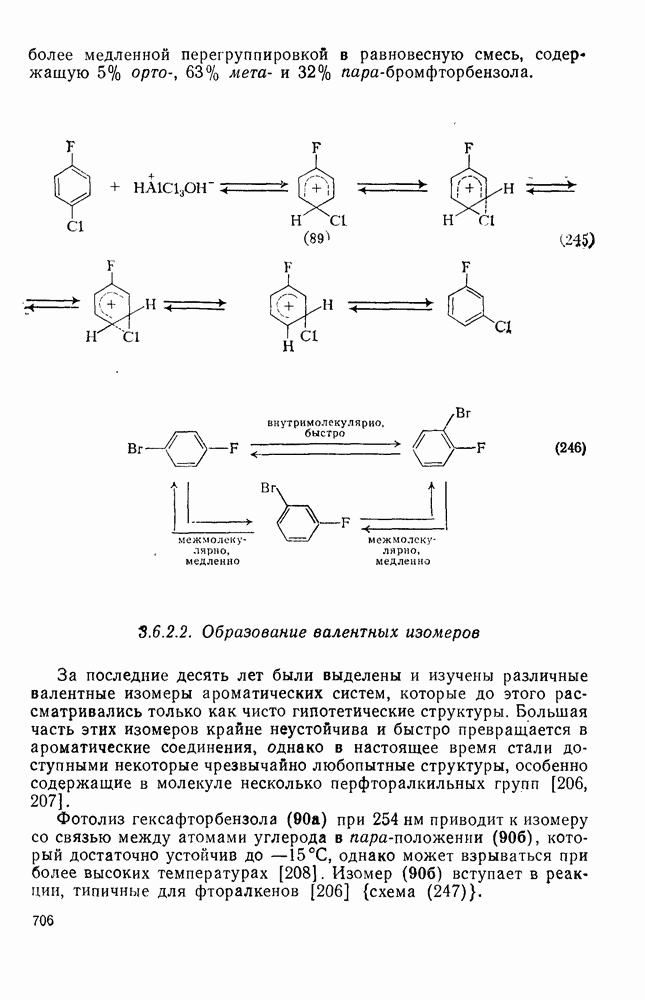
- 3.6.2.1. Перегруппировки под действием кислот Льюиса
- 3.6.2.2. Образование валентных изомеров