| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
2.6.3. СВОЙСТВА АННУЛЕНОВ
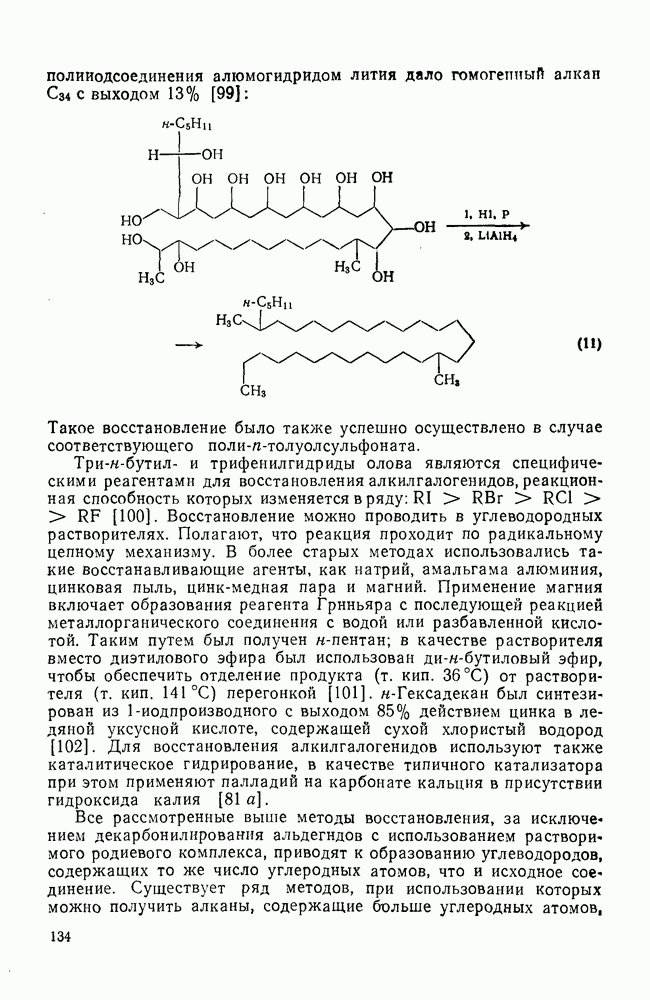
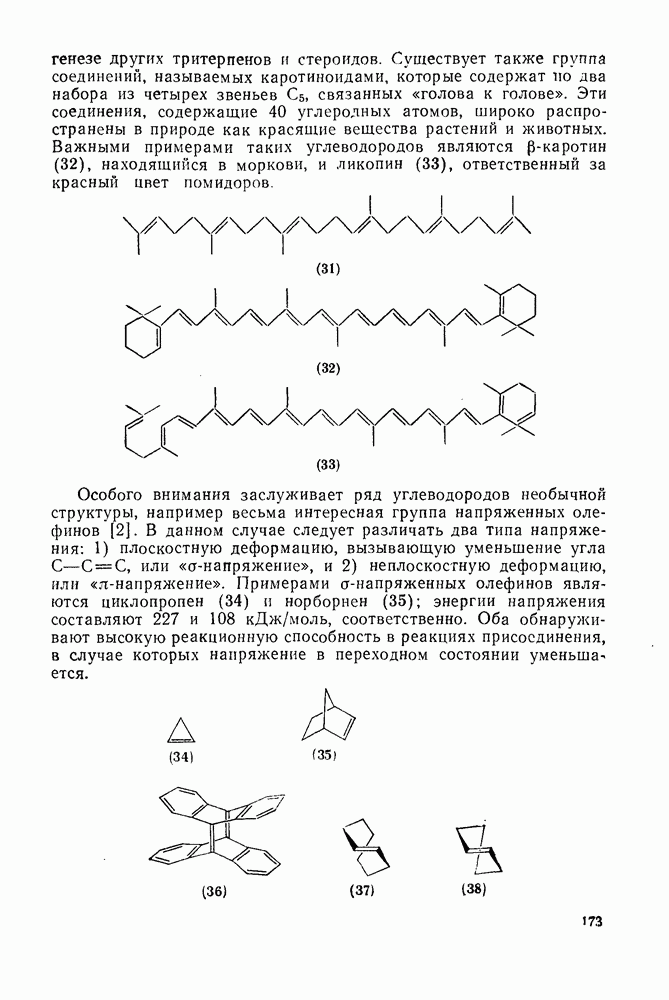
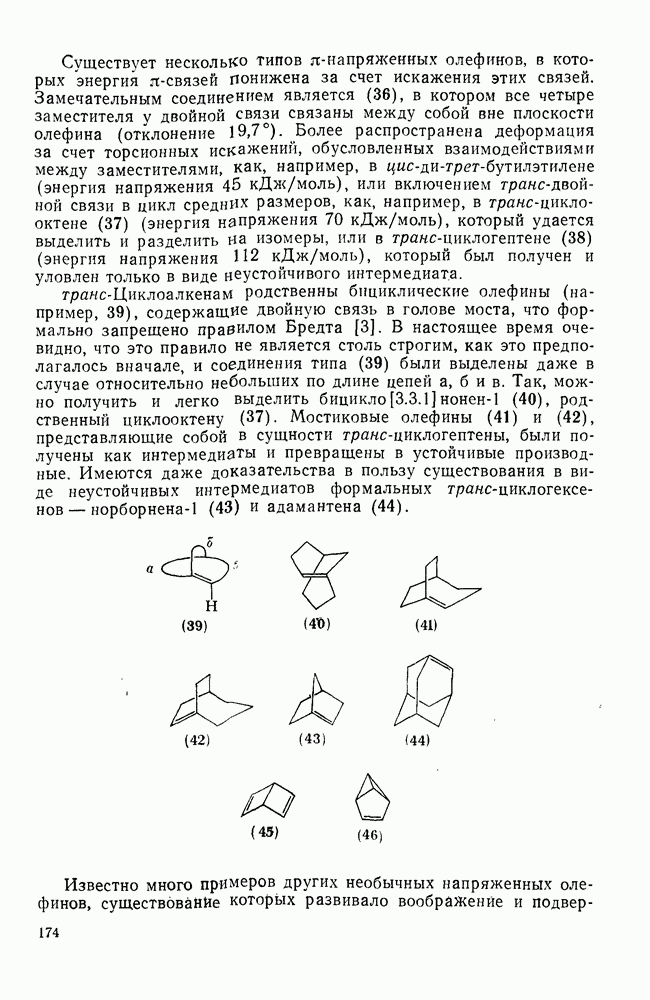
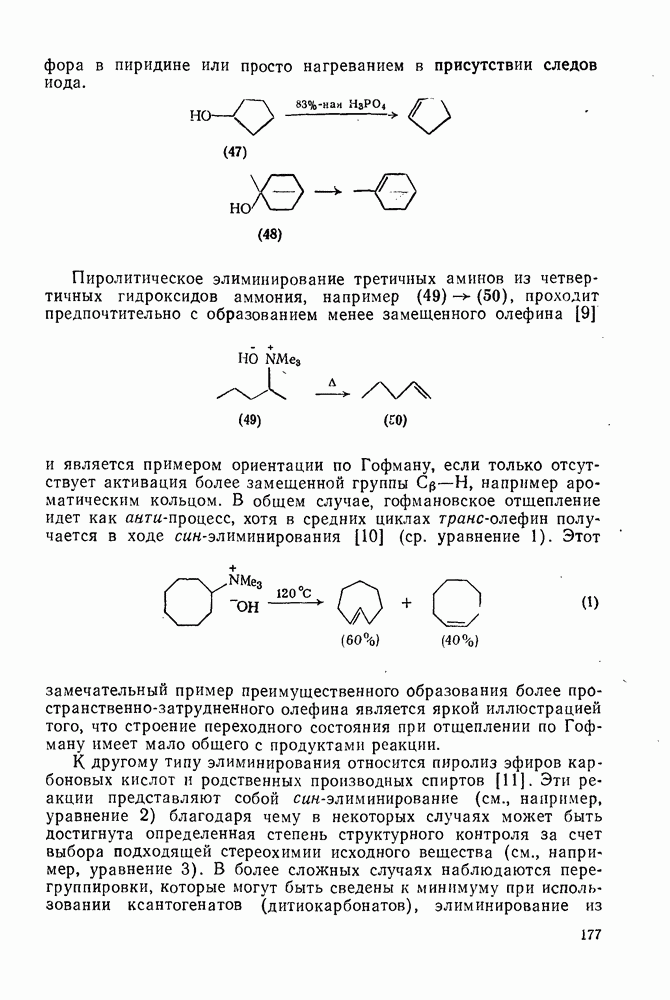
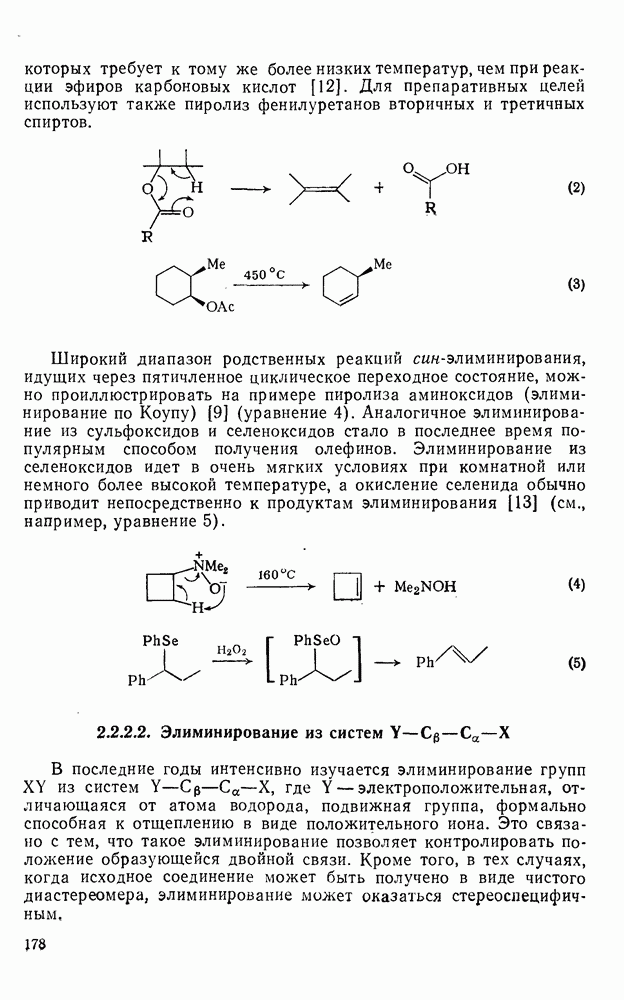
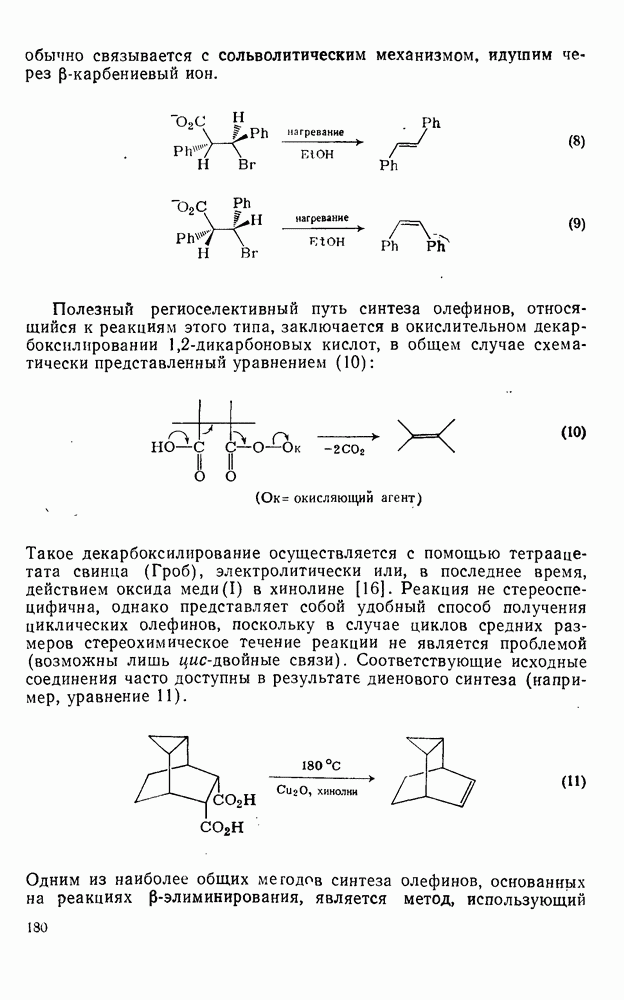
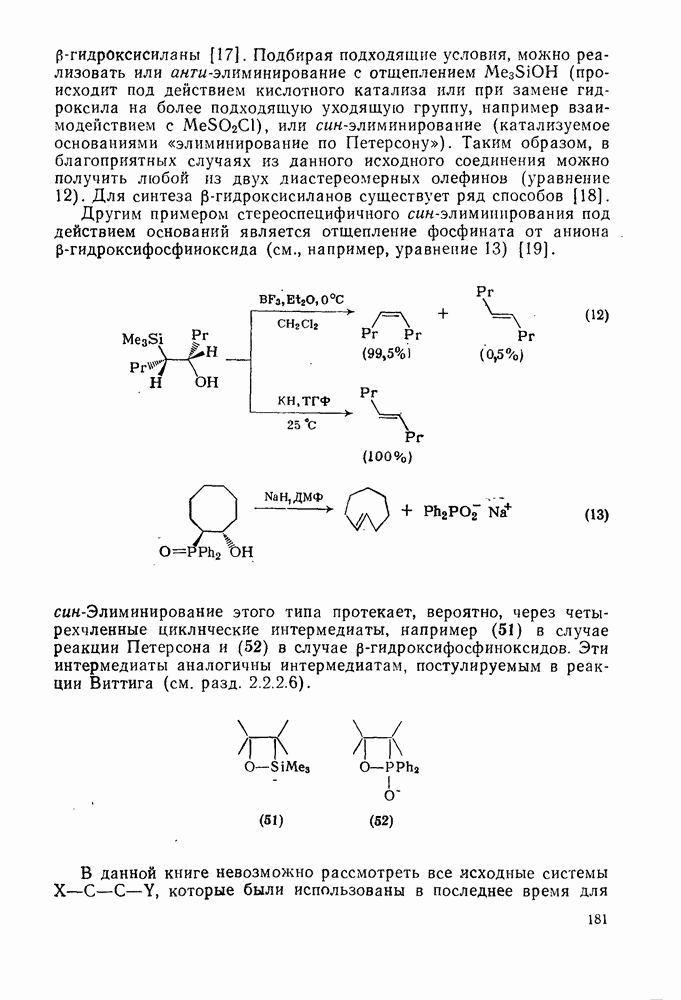
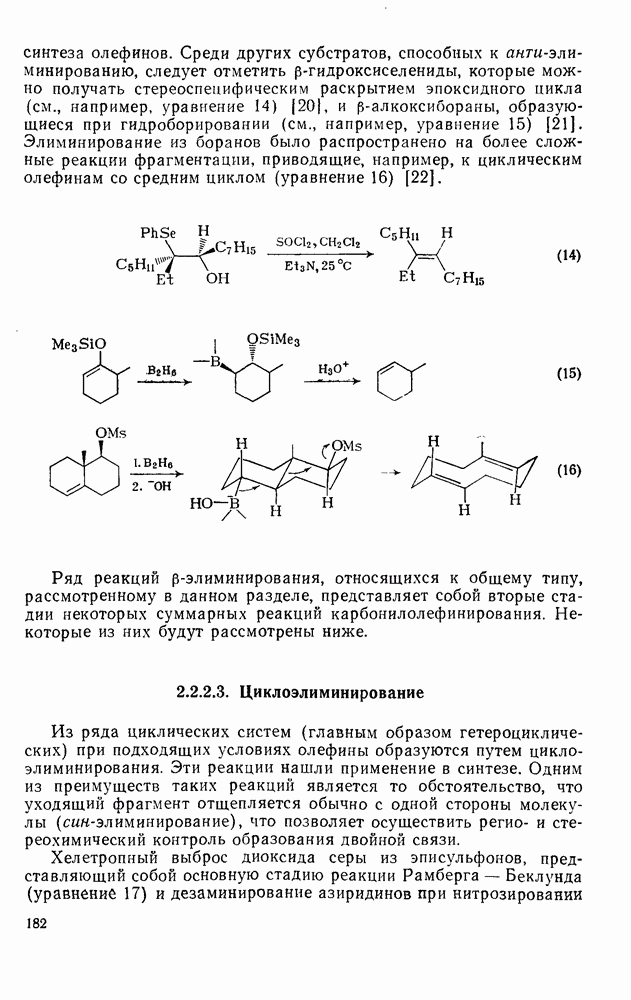
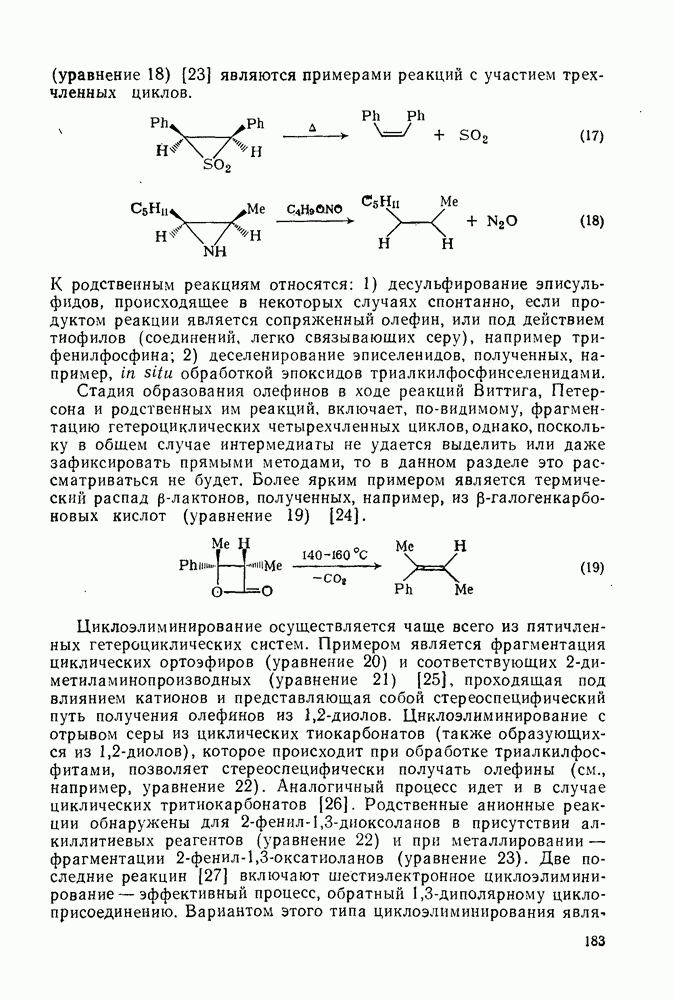
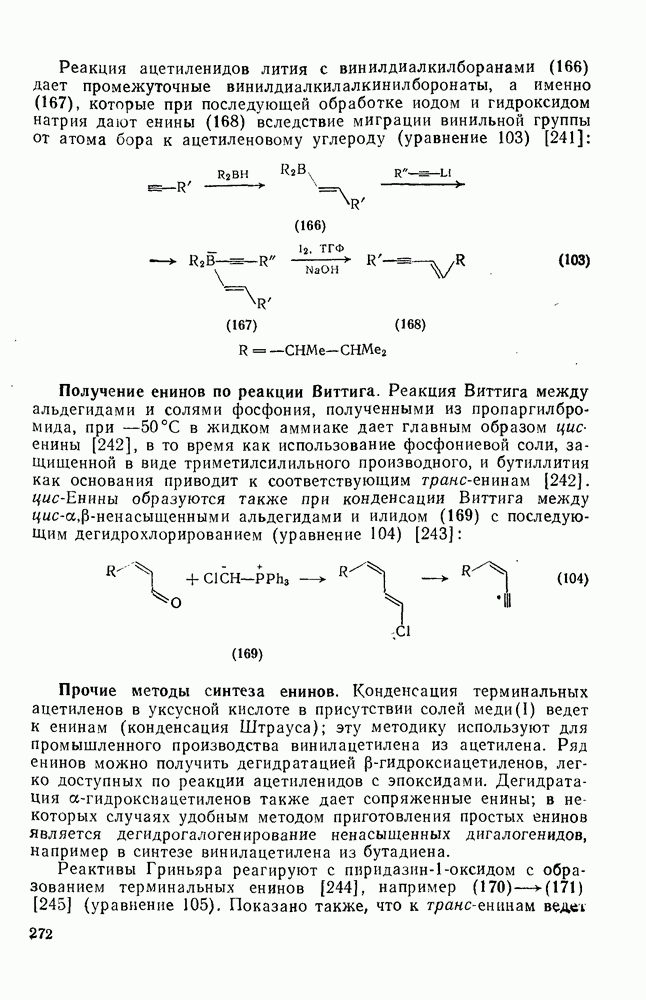
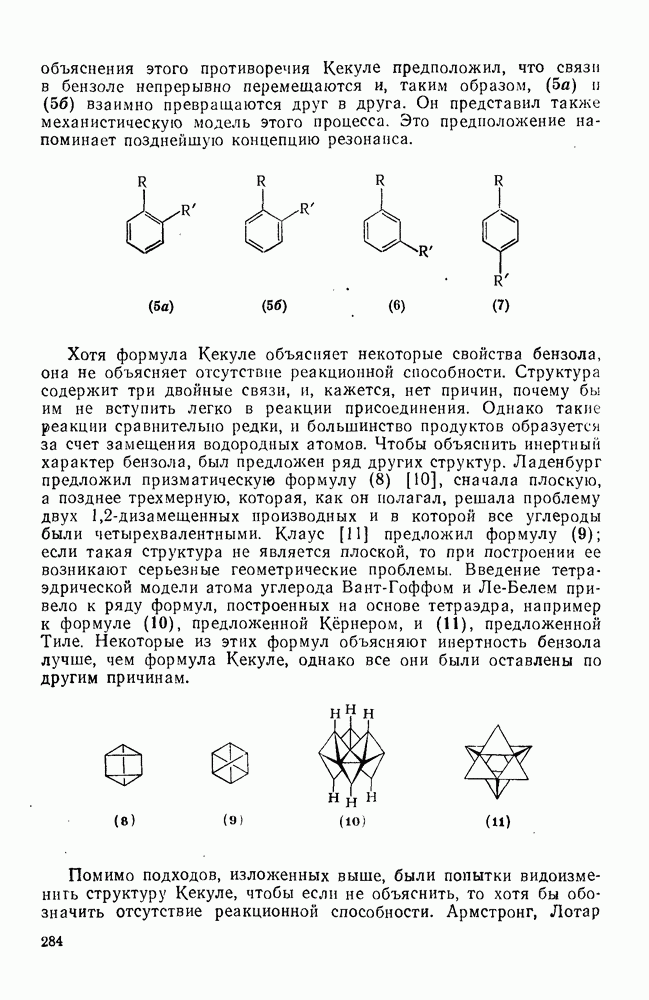
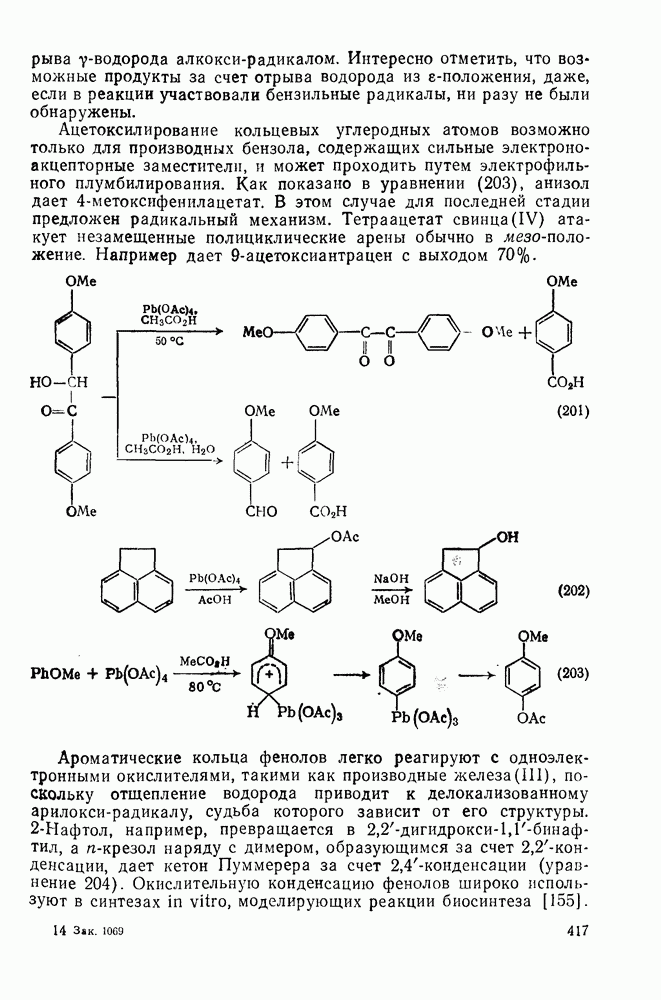
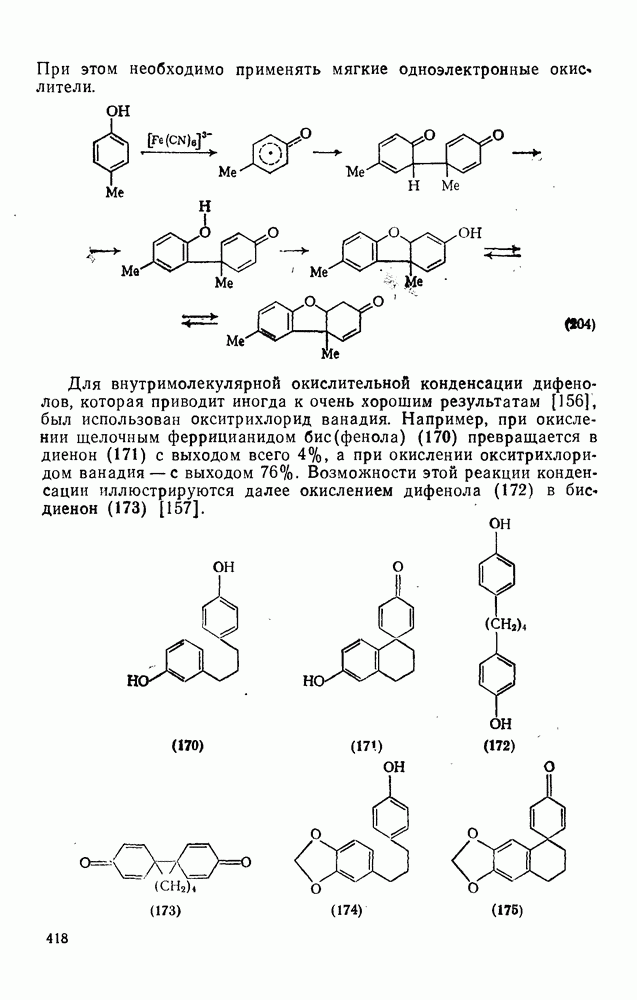
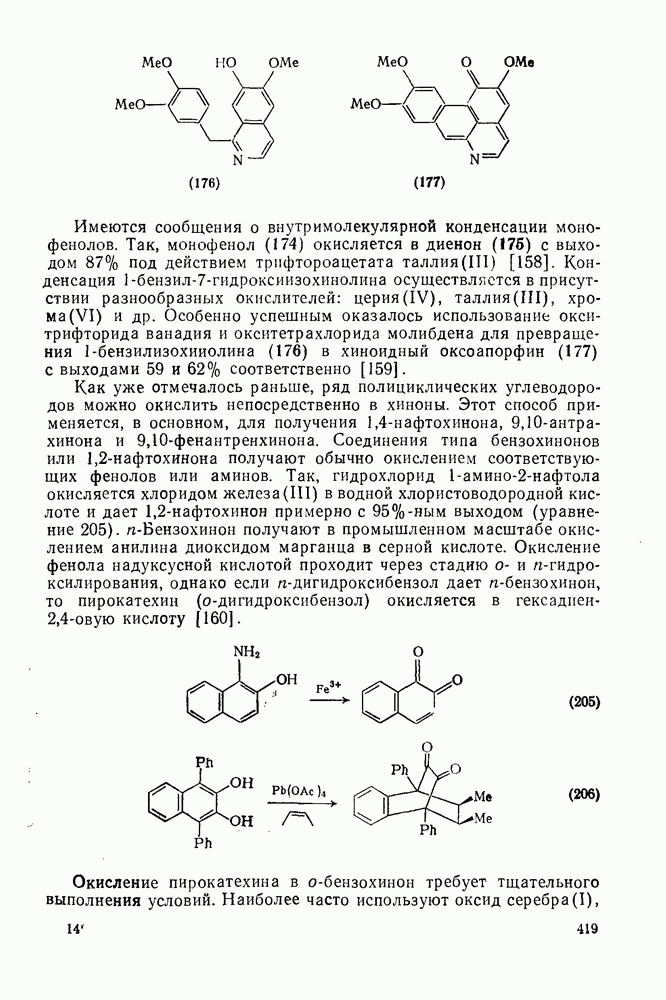
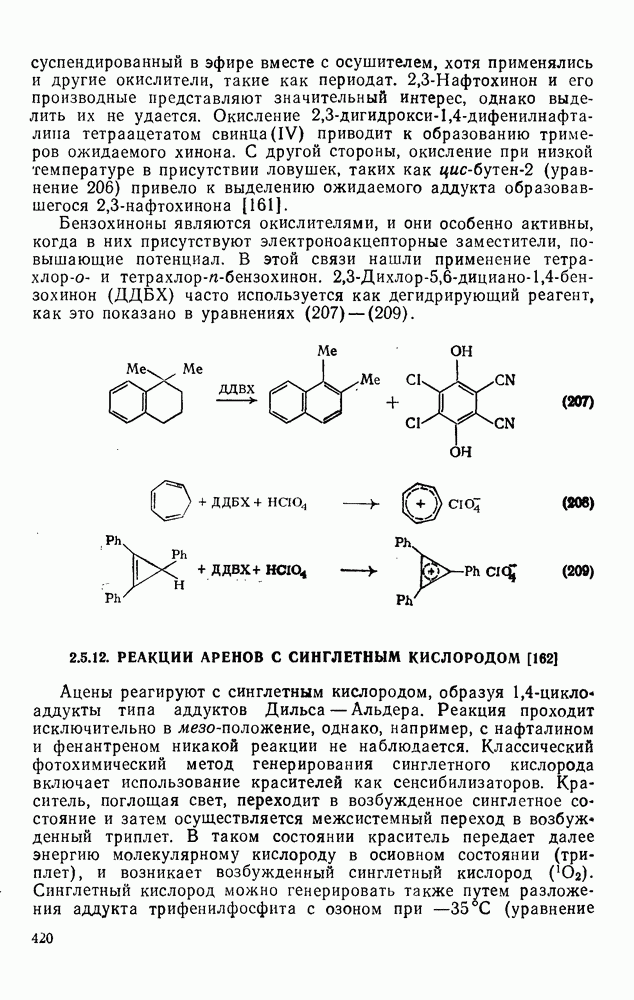
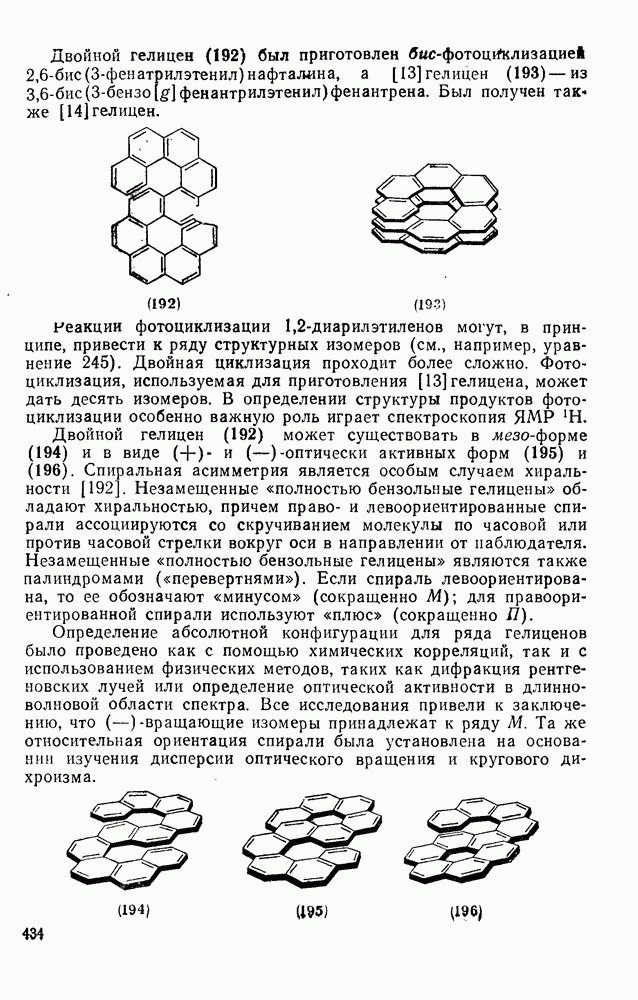
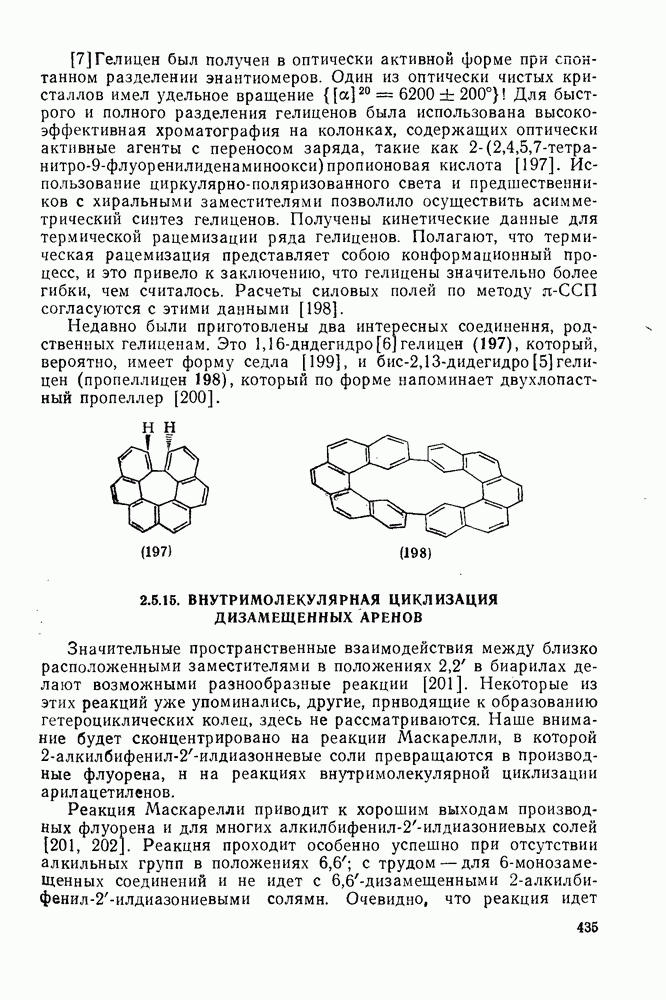
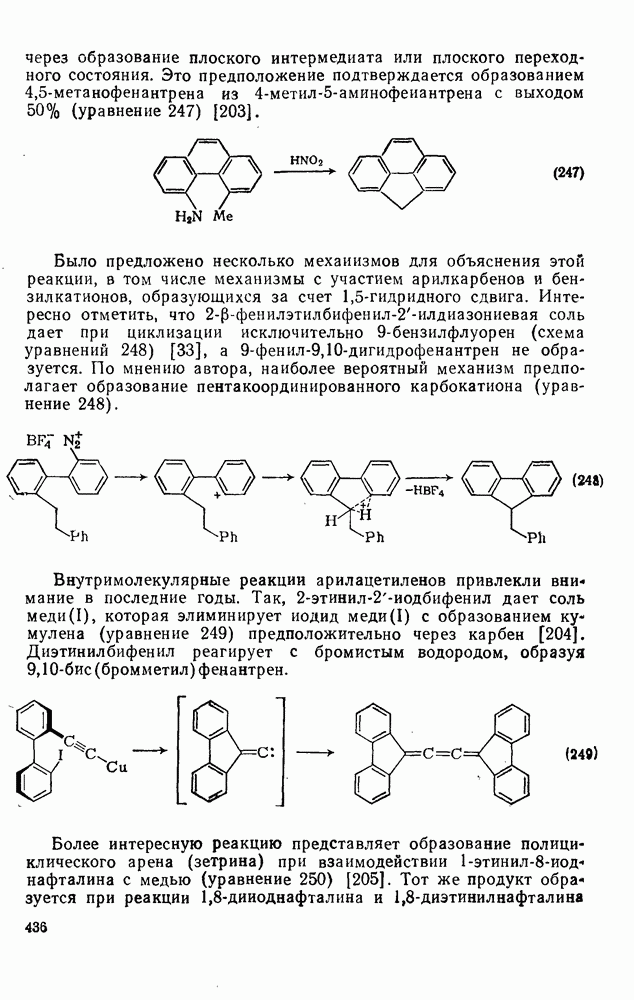
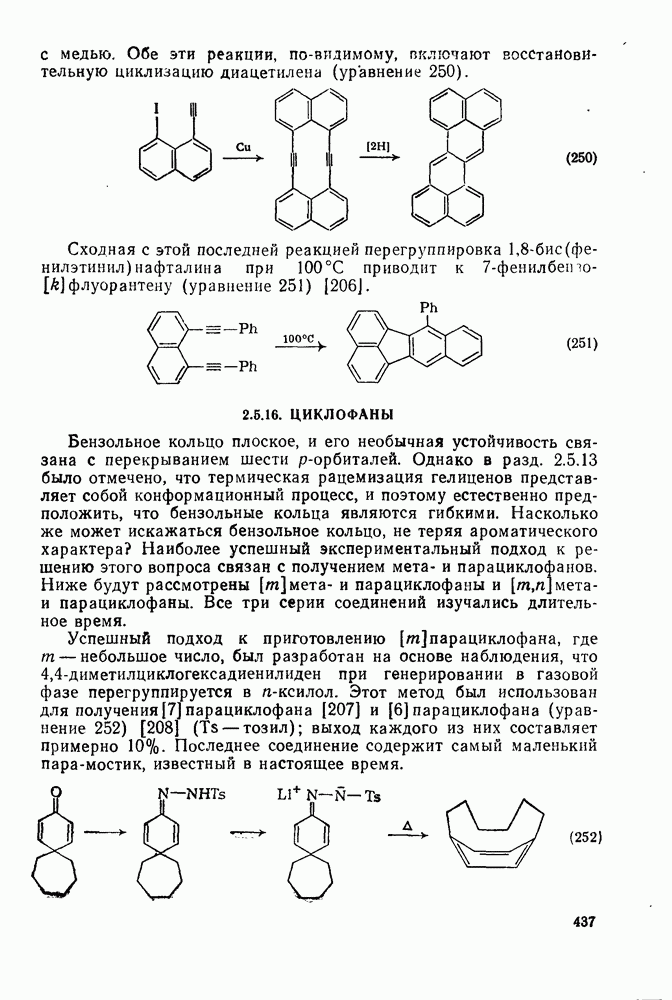
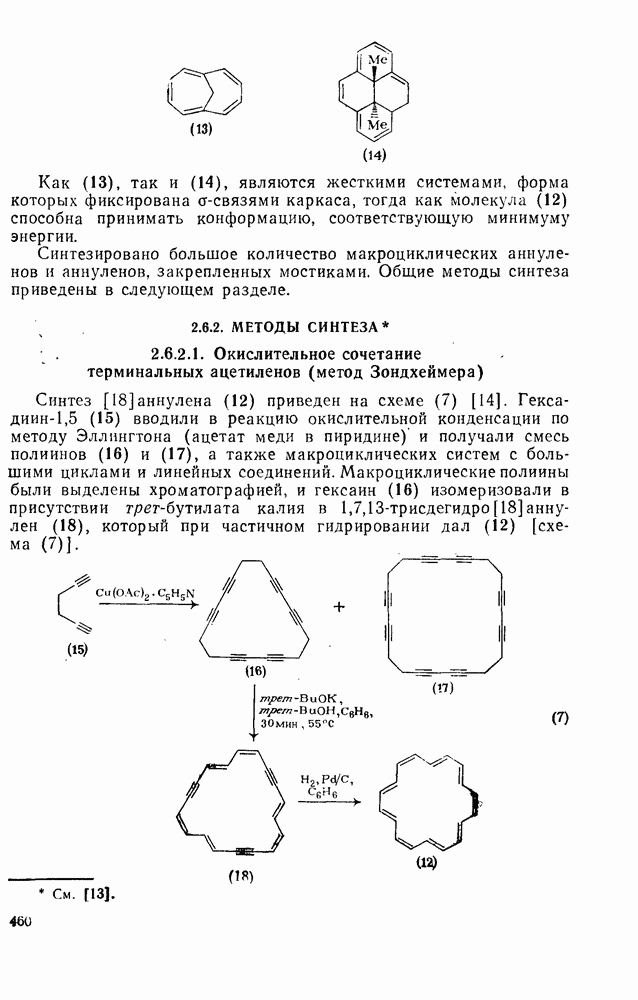
Свойства бензола, самой типичной ароматической системы детально описаны в гл. 2.5. Как соотносятся свойства большой группы аннуленов с  -электронами со свойствами бензола? Исторически первым макроциклическим аннуленом оказался
-электронами со свойствами бензола? Исторически первым макроциклическим аннуленом оказался  (12). В кристаллическом состоянии он устойчив, но разлагается в растворе при комнатной температуре, по-видимому, в результате окисления. Он имеет широкий электронный спектр с основным максимумом при 369 нм (
(12). В кристаллическом состоянии он устойчив, но разлагается в растворе при комнатной температуре, по-видимому, в результате окисления. Он имеет широкий электронный спектр с основным максимумом при 369 нм ( ) [13]. Спектр
) [13]. Спектр  -ЯМР зависит от температуры: при
-ЯМР зависит от температуры: при  в спектре видны два сигнала: мультиплет при
в спектре видны два сигнала: мультиплет при  и триплет при
и триплет при  , которые при нагревании расширяются, сливаются и, в конце концов, при
, которые при нагревании расширяются, сливаются и, в конце концов, при  дают острый синглет при
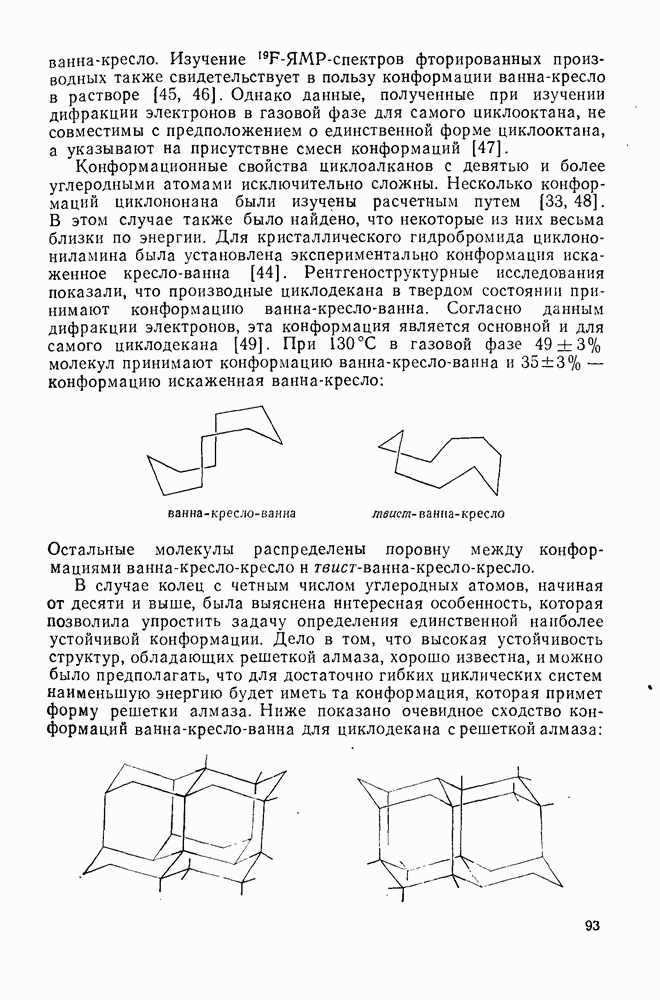
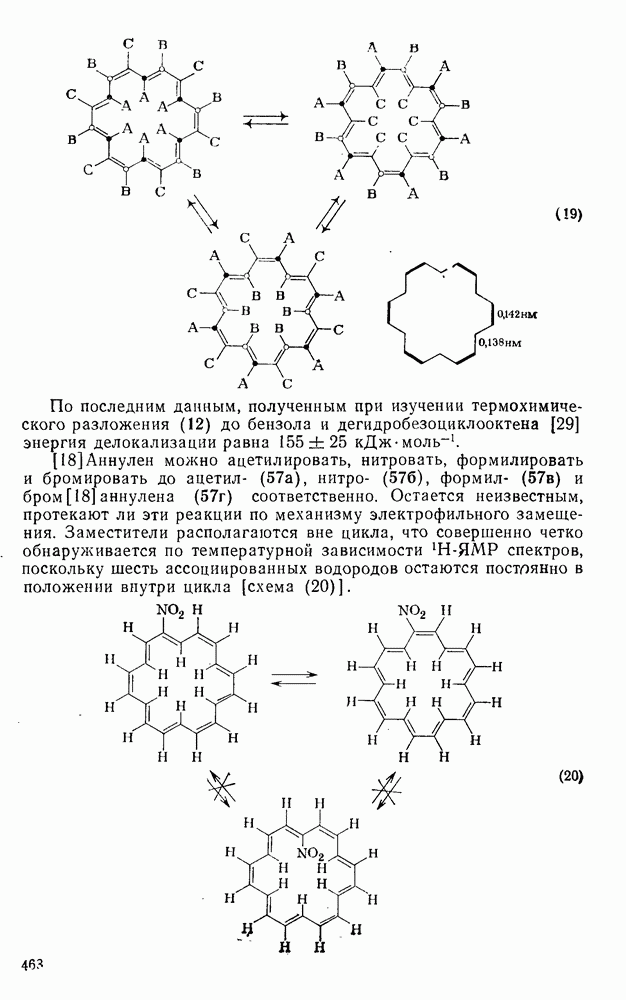
дают острый синглет при  [27]. Низкотемпературный спектр, как и следовало ожидать для соединения (12), соответствует двенадцати внешним, неэкранированным протонам и шести внутренним, экранированным протонам. Изменение спектра при повышении температуры указывает, что обмен протонов между внутренним и внешним положением происходит во временной шкале ЯМР достаточно быстро. Такое поведение можно интерпретировать как следствие инверсии трех эквивалентных структур, показанных на схеме (19). Установлено, что способность к флуктуациям структуры является общим свойством макроциклических аннуленов. Химические сдвиги внешних и внутренних протонов в низкотемпературном спектре
[27]. Низкотемпературный спектр, как и следовало ожидать для соединения (12), соответствует двенадцати внешним, неэкранированным протонам и шести внутренним, экранированным протонам. Изменение спектра при повышении температуры указывает, что обмен протонов между внутренним и внешним положением происходит во временной шкале ЯМР достаточно быстро. Такое поведение можно интерпретировать как следствие инверсии трех эквивалентных структур, показанных на схеме (19). Установлено, что способность к флуктуациям структуры является общим свойством макроциклических аннуленов. Химические сдвиги внешних и внутренних протонов в низкотемпературном спектре  указывают на то, что это диатропная молекула.
указывают на то, что это диатропная молекула.
Спектр  -ЯМР с широкополосной развязкой от протонов также зависит от температуры. При
-ЯМР с широкополосной развязкой от протонов также зависит от температуры. При  в нем содержатся два сигнала с
в нем содержатся два сигнала с  и
и  , а при
, а при  — только один сигнал с
— только один сигнал с  . Такое поведение возникает вследствие смены атомами углерода двух возможных положений [см. схему (19) на с. 468]. Трехмерный рентгенографический анализ кристаллической структуры
. Такое поведение возникает вследствие смены атомами углерода двух возможных положений [см. схему (19) на с. 468]. Трехмерный рентгенографический анализ кристаллической структуры  показал, что это почти плоская молекула с неальтернирующими связями двух типов: шестью «цисоидными» (0,142 нм) и двенадцатью «трансоидными» (0,138 нм) [28].
показал, что это почти плоская молекула с неальтернирующими связями двух типов: шестью «цисоидными» (0,142 нм) и двенадцатью «трансоидными» (0,138 нм) [28].

По последним данным, полученным при изучении термохимического разложения (12) до бензола и дегидробезоциклооктена [29] энергия делокализации равна  .
.
[18] Аннулен можно ацетилировать, нитровать, формилировать и бромировать до ацетил- (57а), нитро- (576), формил- (57в) и бром  аннулена (57г) соответственно. Остается неизвестным, протекают ли эти реакции по механизму электрофильного замещения. Заместители располагаются вне цикла, что совершенно четко обнаруживается по температурной зависимости
аннулена (57г) соответственно. Остается неизвестным, протекают ли эти реакции по механизму электрофильного замещения. Заместители располагаются вне цикла, что совершенно четко обнаруживается по температурной зависимости  -ЯМР спектров, поскольку шесть ассоциированных водородов остаются постоянно в положении внутри цикла [схема (20)].
-ЯМР спектров, поскольку шесть ассоциированных водородов остаются постоянно в положении внутри цикла [схема (20)].

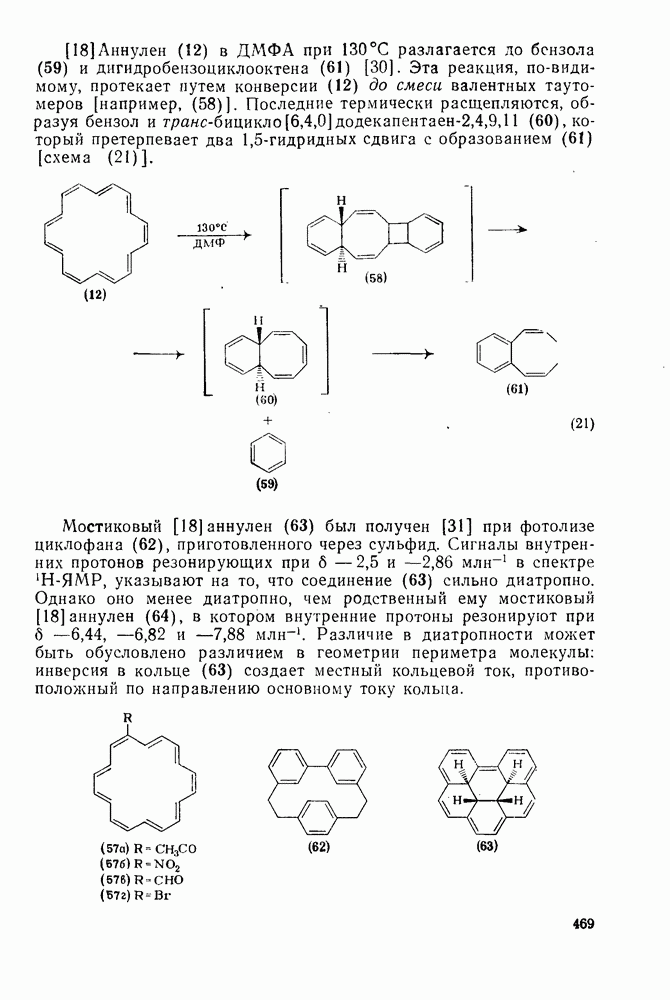
[18] Аннулен в ДМФА при  разлагается до бензола (59) и дигидробензоциклооктена (61) [30]. Эта реакция, по-видимому, протекает путем конверсии (12) до смеси валентных таутомеров [например, (58)]. Последние термически расщепляются, образуя бензол и гранс-бицикло
разлагается до бензола (59) и дигидробензоциклооктена (61) [30]. Эта реакция, по-видимому, протекает путем конверсии (12) до смеси валентных таутомеров [например, (58)]. Последние термически расщепляются, образуя бензол и гранс-бицикло  (60), который претерпевает два
(60), который претерпевает два  -гидридных сдвига с образованием (61) [схема (21)].
-гидридных сдвига с образованием (61) [схема (21)].

Мостиковый [18] аннулен (63) был получен [31] при фотолизе циклофана (62), приготовленного через сульфид. Сигналы внутренних протонов резонирующих при  и
и  в спектре
в спектре  -ЯМР, указывают на то, что соединение (63) сильно диатропно. Однако оно менее диатропно, чем родственный ему мостиковый
-ЯМР, указывают на то, что соединение (63) сильно диатропно. Однако оно менее диатропно, чем родственный ему мостиковый  (64), в котором внутренние протоны резонируют при
(64), в котором внутренние протоны резонируют при  . Различие в диатропности может быть обусловлено различием в геометрии периметра молекулы: инверсия в кольце (63) создает местный кольцевой ток, противоположный по направлению основному току кольца.
. Различие в диатропности может быть обусловлено различием в геометрии периметра молекулы: инверсия в кольце (63) создает местный кольцевой ток, противоположный по направлению основному току кольца.


Спектр  -ЯМР триоксида [18] аннулена (56) обнаруживает только сигналы в слабом поле
-ЯМР триоксида [18] аннулена (56) обнаруживает только сигналы в слабом поле  , и молекула явно диатропна. Если атомы кислорода последовательно замещать атомами серы, то в ряду соединений
, и молекула явно диатропна. Если атомы кислорода последовательно замещать атомами серы, то в ряду соединений  обнаруживаются изменения в спектрах
обнаруживаются изменения в спектрах  -ЯМР: молекула с двумя атомами кислорода и одним атомом серы (65а) еще диатропна, а молекула с двумя атомами серы и одним атомом кислорода (656) и трисульфид (
-ЯМР: молекула с двумя атомами кислорода и одним атомом серы (65а) еще диатропна, а молекула с двумя атомами серы и одним атомом кислорода (656) и трисульфид ( -атропны. Уменьшение циклической делокализапии может быть вызвано, во-первых, увеличением объема гетероатома и, во-вторых, склонностью тиофеновых систем к сохранению присущей им конъюгационной делокализации.
-атропны. Уменьшение циклической делокализапии может быть вызвано, во-первых, увеличением объема гетероатома и, во-вторых, склонностью тиофеновых систем к сохранению присущей им конъюгационной делокализации.
В отличие от  аннулена (12), полностью-цис- (26) и моно-транс- [10] -аннулен (27) не проявляют никаких ароматических свойств и устойчивы только при низкой температуре [17]. К термической интерконверсии эти изомеры не способны, но их можно превратить друг в друга фотохимическим путем.
аннулена (12), полностью-цис- (26) и моно-транс- [10] -аннулен (27) не проявляют никаких ароматических свойств и устойчивы только при низкой температуре [17]. К термической интерконверсии эти изомеры не способны, но их можно превратить друг в друга фотохимическим путем.

В спектре  -ЯМР соединения (26) виден только один синглет при
-ЯМР соединения (26) виден только один синглет при  , и в спектре
, и в спектре  -ЯМР с широкополосной развязкой также наблюдается только один пик при
-ЯМР с широкополосной развязкой также наблюдается только один пик при  оба спектра не зависят от температуры. Электронный спектр поглощения содержит малоинтенсивные максимумы при
оба спектра не зависят от температуры. Электронный спектр поглощения содержит малоинтенсивные максимумы при  и 265 нм. При
и 265 нм. При  претерпевает термическую изомеризацию в
претерпевает термическую изомеризацию в  (28). Спектр Н-ЯМР соединения (27) зависит от температуры: при
(28). Спектр Н-ЯМР соединения (27) зависит от температуры: при  в нем видны два сигнала, а при
в нем видны два сигнала, а при  — только синглет при
— только синглет при  . Это свидетельствует о перемещении транс-двойной связи по кольцу. В УФ-спектре (27) наблюдаются максимумы при 257 (
. Это свидетельствует о перемещении транс-двойной связи по кольцу. В УФ-спектре (27) наблюдаются максимумы при 257 ( ) и 265 (
) и 265 ( ) нм, от которых идет долгий спуск в длинноволновую область. При
) нм, от которых идет долгий спуск в длинноволновую область. При  соединение (27) изомеризуется в
соединение (27) изомеризуется в  [см. схему (8)]. Как (26), так и (27) являются неплоскими молекулами.
[см. схему (8)]. Как (26), так и (27) являются неплоскими молекулами.
Если в неизвестном до сих пор ди-транс- заменить два пространственно сближенных атома водорода на
заменить два пространственно сближенных атома водорода на  -звено, то в соответствующем 1,6-метано [10] аннулене (13) это трансаннулярное взаимодействие будет устранено. В спектре
-звено, то в соответствующем 1,6-метано [10] аннулене (13) это трансаннулярное взаимодействие будет устранено. В спектре  -ЯМР соединения (13) протоны кольца проявляются в слабом поле как
-ЯМР соединения (13) протоны кольца проявляются в слабом поле как  -система [
-система [ и
и  ], а протоны метиленового мостика дают синглет в сильном поле (
], а протоны метиленового мостика дают синглет в сильном поле ( ). Отсюда следует, что молекула (13) диатропна. Этот вывод подтверждается высокой диамагнитной экзальтацией (
). Отсюда следует, что молекула (13) диатропна. Этот вывод подтверждается высокой диамагнитной экзальтацией ( ) [32]. Спектр
) [32]. Спектр  -ЯМР с широкополосной развязкой содержит четыре пика, из которых три находятся в слабом поле
-ЯМР с широкополосной развязкой содержит четыре пика, из которых три находятся в слабом поле  , а четвертый, соответствующий углероду метиленового мостика, проявляется в более сильном поле (6 34,8). Максимум в электронном спектре поглощения наблюдается при 256 нм (
, а четвертый, соответствующий углероду метиленового мостика, проявляется в более сильном поле (6 34,8). Максимум в электронном спектре поглощения наблюдается при 256 нм ( 68 000). Рентгеноструктурный анализ кристаллов
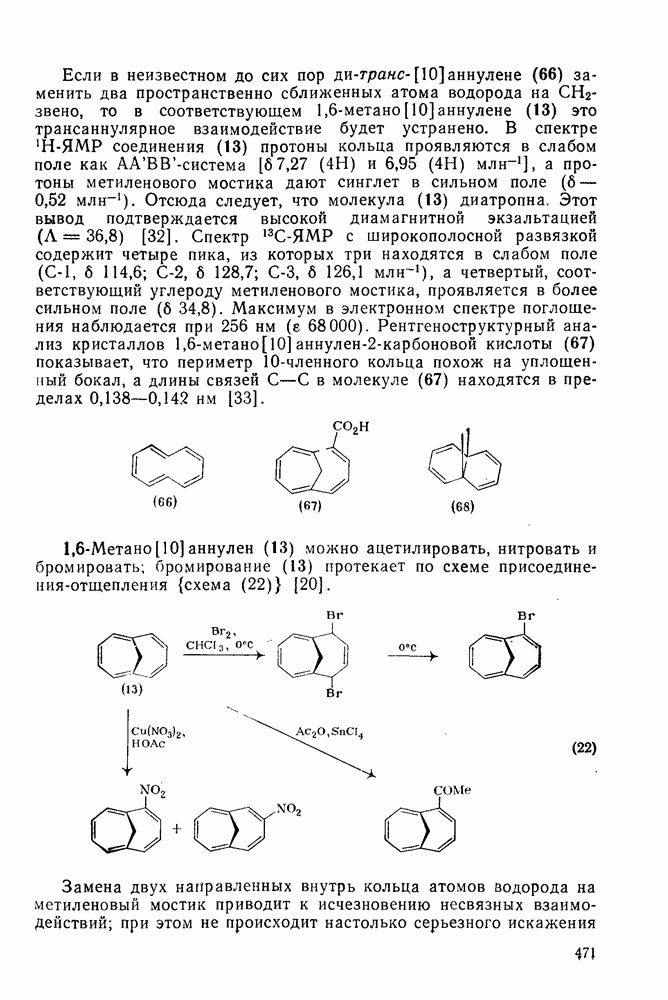
68 000). Рентгеноструктурный анализ кристаллов  кислоты (67) показывает, что периметр 10-членного кольца похож на уплощенный бокал, а длины связей
кислоты (67) показывает, что периметр 10-членного кольца похож на уплощенный бокал, а длины связей  в молекуле (67) находятся в пределах
в молекуле (67) находятся в пределах  нм [33].
нм [33].

1,6-Метано [10] аннулен (13) можно ацетилировать, нитровать и бромировать; бромирование (13) протекает по схеме присоединения-отщепления (схема (22))[20].

Замена двух направленных внутрь кольца атомов водорода на метиленовый мостик приводит к исчезновению несвязных взаимодействий; при этом не происходит настолько серьезного искажения остова молекулы, чтобы делокализация 10  -электронов стала невозможной.
-электронов стала невозможной.
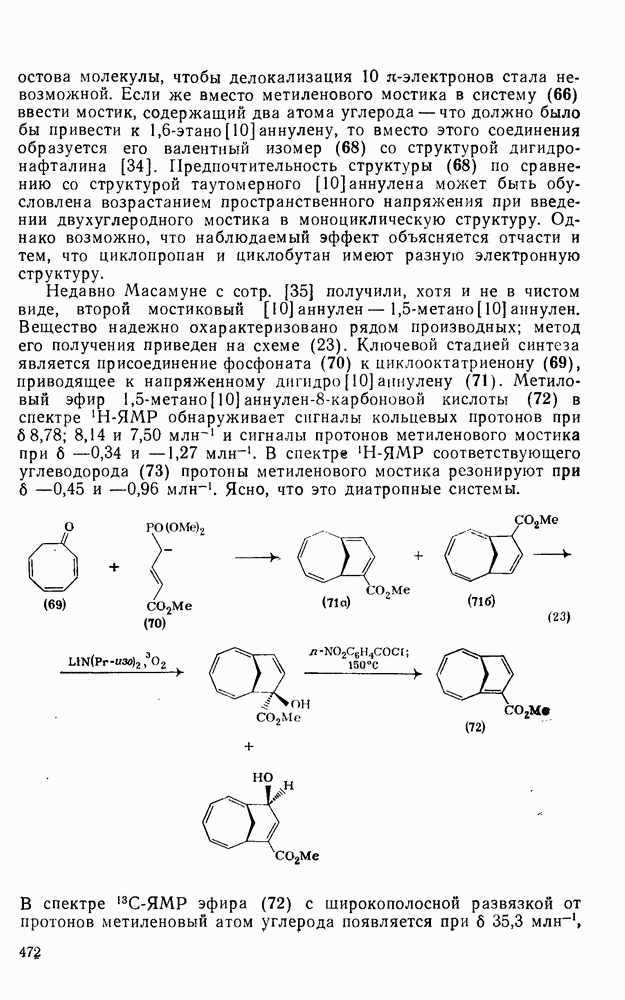
Если же вместо метиленового мостика в систему (66) ввести мостик, содержащий два атома углерода — что должно было бы привести к  аннулену, то вместо этого соединения образуется его валентный изомер (68) со структурой дигидронафталина [34]. Предпочтительность структуры (68) по сравнению со структурой таутомерного
аннулену, то вместо этого соединения образуется его валентный изомер (68) со структурой дигидронафталина [34]. Предпочтительность структуры (68) по сравнению со структурой таутомерного  может быть обусловлена возрастанием пространственного напряжения при введении двухуглеродного мостика в моноциклическую структуру. Однако возможно, что наблюдаемый эффект объясняется отчасти и тем, что циклопропан и циклобутан имеют разную электронную структуру.
может быть обусловлена возрастанием пространственного напряжения при введении двухуглеродного мостика в моноциклическую структуру. Однако возможно, что наблюдаемый эффект объясняется отчасти и тем, что циклопропан и циклобутан имеют разную электронную структуру.
Недавно Масамуне с сотр. [35] получили, хотя и не в чистом виде, второй мостиковый  -метано
-метано  аннулен. Вещество надежно охарактеризовано рядом производных; метод его получения приведен на схеме (23). Ключевой стадией синтеза является присоединение фосфоната (70) к циклооктатриенону (69), приводящее к напряженному дигидро [10] аннулену (71). Метиловый эфир
аннулен. Вещество надежно охарактеризовано рядом производных; метод его получения приведен на схеме (23). Ключевой стадией синтеза является присоединение фосфоната (70) к циклооктатриенону (69), приводящее к напряженному дигидро [10] аннулену (71). Метиловый эфир  -метано
-метано  карбоновой кислоты (72) в спектре
карбоновой кислоты (72) в спектре  -ЯМР обнаруживает сигналы кольцевых протонов при
-ЯМР обнаруживает сигналы кольцевых протонов при  и
и  и сигналы протонов метиленового мостика при
и сигналы протонов метиленового мостика при  . В спектре
. В спектре  -ЯМР соответствующего углеводорода (73) протоны метиленового мостика резонируют при
-ЯМР соответствующего углеводорода (73) протоны метиленового мостика резонируют при  и
и  . Ясно, что это диатропные системы.
. Ясно, что это диатропные системы.

В спектре  -ЯМР эфира (72) с широкополосной развязкой от протонов метиленовый атом углерода появляется при
-ЯМР эфира (72) с широкополосной развязкой от протонов метиленовый атом углерода появляется при  , а атомы углерода, входящие в цикл, резонируют в интервале
, а атомы углерода, входящие в цикл, резонируют в интервале  .
.
Спектры ЯМР (как  , так и
, так и  ) вплоть до температуры
) вплоть до температуры  не зависят от температуры, и если перемещение связей в цикле происходит, то оно должно быть очень быстрым. В электронном спектре максимумы приходятся на
не зависят от температуры, и если перемещение связей в цикле происходит, то оно должно быть очень быстрым. В электронном спектре максимумы приходятся на  266 (
266 ( 16 000), 295 (
16 000), 295 ( 25 000), 364 (
25 000), 364 ( 9000) и 480 (
9000) и 480 ( 600) нм. Смещение полос поглощения в длинноволновую область по сравнению со спектрами поглощения 1,6-метано [10] аннуленов напоминает различие в спектральных свойствах нафталина и азулена.
600) нм. Смещение полос поглощения в длинноволновую область по сравнению со спектрами поглощения 1,6-метано [10] аннуленов напоминает различие в спектральных свойствах нафталина и азулена.
[14] Аннулен (74) был получен Зондхеймером и сотр. из  по схеме, включавшей последовательно стадии окислительной конденсации, прототропной перегруппировки и частичного гидрирования. Это соединение существует в виде смеси двух конфигурационных изомеров. Для кристаллического компонента этой смеси методом рентгеноструктурного анализа была доказана конфигурация (74). Молекула значительно отклоняется от планарности, а длины связей
по схеме, включавшей последовательно стадии окислительной конденсации, прототропной перегруппировки и частичного гидрирования. Это соединение существует в виде смеси двух конфигурационных изомеров. Для кристаллического компонента этой смеси методом рентгеноструктурного анализа была доказана конфигурация (74). Молекула значительно отклоняется от планарности, а длины связей  лежат в интервале
лежат в интервале  нм [36]. Вид спектра
нм [36]. Вид спектра  -ЯМР изомера (74) зависит от температуры. Наблюдаемые при
-ЯМР изомера (74) зависит от температуры. Наблюдаемые при  два сигнала с
два сигнала с  и
и  при комнатной температуре сливаются, образуя синглет с
при комнатной температуре сливаются, образуя синглет с  . В спектре другого изомера появление двух сигналов наблюдается при гораздо более низкой температуре. [14]
. В спектре другого изомера появление двух сигналов наблюдается при гораздо более низкой температуре. [14] не так устойчив, как [18] аннулен, и для него получить продукты замещения не удается [15].
не так устойчив, как [18] аннулен, и для него получить продукты замещения не удается [15].

Описано получение различных  с двумя мостиками в положениях 1,6 и 8,13, содержащими как углерод, так и гетероатом. Например,
с двумя мостиками в положениях 1,6 и 8,13, содержащими как углерод, так и гетероатом. Например,  :
:  -бисоксидо [14] аннулен (75) представляет собой термически устойчивое кристаллическое вещество красного цвета, которое, судя по спектру
-бисоксидо [14] аннулен (75) представляет собой термически устойчивое кристаллическое вещество красного цвета, которое, судя по спектру  -ЯМР, диатропно. Рентгеноструктурный анализ показывает, что периферические связи
-ЯМР, диатропно. Рентгеноструктурный анализ показывает, что периферические связи  лежат приблизительно в одной плоскости и имеют примерно одинаковую длину (0,139 нм). Диатропна и система
лежат приблизительно в одной плоскости и имеют примерно одинаковую длину (0,139 нм). Диатропна и система  аннулена (76). В противоположность этому анти-
аннулена (76). В противоположность этому анти- :
:  -бисметано [14] аннулен (42) чрезвычайно реакционноспособный и атропный полиолефин желтого цвета. По-видимому, метиленовые мостики так искривляют
-бисметано [14] аннулен (42) чрезвычайно реакционноспособный и атропный полиолефин желтого цвета. По-видимому, метиленовые мостики так искривляют  -остов молекулы (42), что перекрывание
-остов молекулы (42), что перекрывание  -орбиталей становится невозможным. Хотя син-
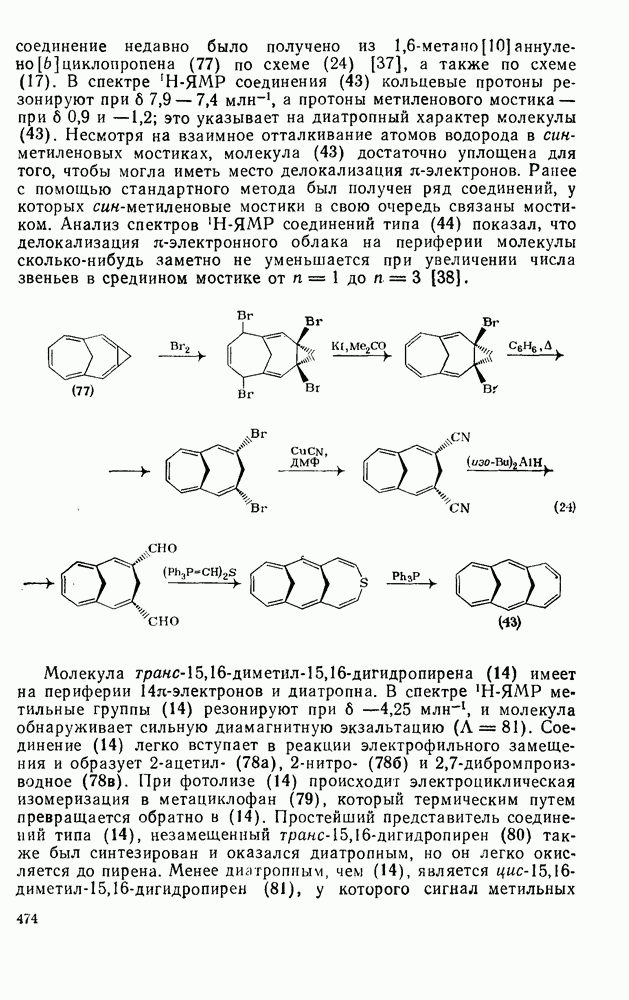
-орбиталей становится невозможным. Хотя син- не удалось синтезировать с помощью изомеризации типа норкарадиен-циклогептатриен, это соединение недавно было получено из 1,6-метано [10] аннулено
не удалось синтезировать с помощью изомеризации типа норкарадиен-циклогептатриен, это соединение недавно было получено из 1,6-метано [10] аннулено  по схеме (24) [37], а также по схеме (17).
по схеме (24) [37], а также по схеме (17).
В спектре  -ЯМР соединения (43) кольцевые протоны резонируют при
-ЯМР соединения (43) кольцевые протоны резонируют при  , а протоны метиленового мостика — при
, а протоны метиленового мостика — при  это указывает на диатропный характер молекулы (43). Несмотря на взаимное отталкивание атомов водорода в син-метиленовых мостиках, молекула (43) достаточно уплощена для того, чтобы могла иметь место делокализация
это указывает на диатропный характер молекулы (43). Несмотря на взаимное отталкивание атомов водорода в син-метиленовых мостиках, молекула (43) достаточно уплощена для того, чтобы могла иметь место делокализация  -электронов. Ранее с помощью стандартного метода был получен ряд соединений, у которых сим-метиленовые мостики в свою очередь связаны мостиком. Анализ спектров
-электронов. Ранее с помощью стандартного метода был получен ряд соединений, у которых сим-метиленовые мостики в свою очередь связаны мостиком. Анализ спектров  -ЯМР соединений типа (44) показал, что делокализация
-ЯМР соединений типа (44) показал, что делокализация  -электронного облака на периферии молекулы сколько-нибудь заметно не уменьшается при увеличении числа звеньев в срединном мостике от
-электронного облака на периферии молекулы сколько-нибудь заметно не уменьшается при увеличении числа звеньев в срединном мостике от  до
до  [38].
[38].

Молекула транс- имеет на периферии
имеет на периферии  -электронов и диатропна. В спектре
-электронов и диатропна. В спектре  -ЯМР метильные группы (14) резонируют при
-ЯМР метильные группы (14) резонируют при  , и молекула обнаруживает сильную диамагнитную экзальтацию (
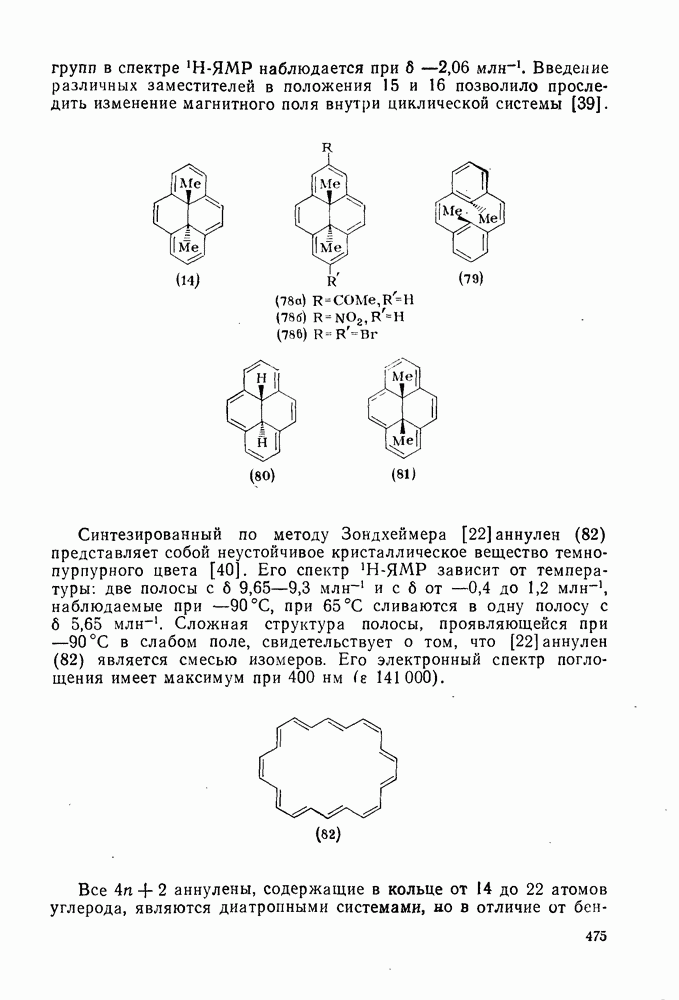
, и молекула обнаруживает сильную диамагнитную экзальтацию ( ). Соединение (14) легко вступает в реакции электрофильного замещения и образует
). Соединение (14) легко вступает в реакции электрофильного замещения и образует  -ацетил- (78а),
-ацетил- (78а),  -нитро- (786) и
-нитро- (786) и  -дибромпроизводное (78в). При фотолизе (14) происходит электроциклическая изомеризация в метациклофан (79), который термическим путем превращается обратно в (14). Простейший представитель соединений типа (Н), незамещенный
-дибромпроизводное (78в). При фотолизе (14) происходит электроциклическая изомеризация в метациклофан (79), который термическим путем превращается обратно в (14). Простейший представитель соединений типа (Н), незамещенный  также был синтезирован и оказался диатропным, но он легко окисляется до пирена. Менее диатропным, чем (14), является цис-
также был синтезирован и оказался диатропным, но он легко окисляется до пирена. Менее диатропным, чем (14), является цис- (81), у которого сигнал метильных групп в спектре
(81), у которого сигнал метильных групп в спектре  -ЯМР наблюдается при
-ЯМР наблюдается при  -
- .
.
Введение различных заместителей в положения 15 и 16 позволило проследить изменение магнитного поля внутри циклической системы [39].

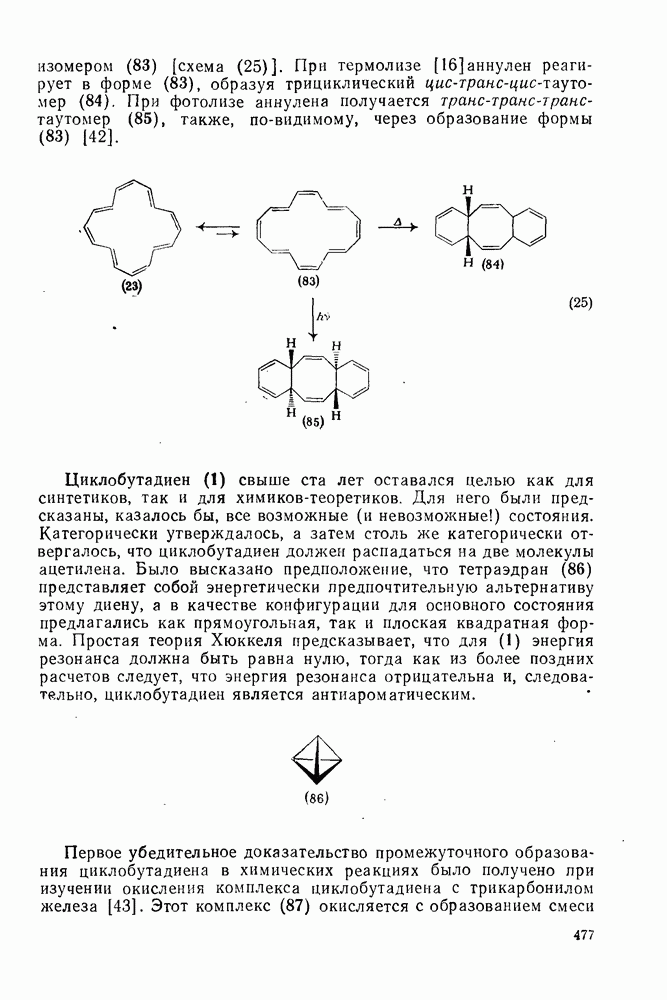
Синтезированный по методу Зондхеймера [22] аннулен (82) представляет собой неустойчивое кристаллическое вещество темнопурпурного цвета [40]. Его спектр  -ЯМР зависит от температуры: две полосы с
-ЯМР зависит от температуры: две полосы с  и с
и с  от —0,4 до
от —0,4 до  , наблюдаемые при
, наблюдаемые при  , при
, при  сливаются в одну полосу с
сливаются в одну полосу с  . Сложная структура полосы, проявляющейся при
. Сложная структура полосы, проявляющейся при  в слабом поле, свидетельствует о том, что [22] аннулен (82) является смесью изомеров. Его электронный спектр поглощения имеет максимум при 400 нм (
в слабом поле, свидетельствует о том, что [22] аннулен (82) является смесью изомеров. Его электронный спектр поглощения имеет максимум при 400 нм ( 141 000).
141 000).

Все  аннулены, содержащие в кольце от 14 до 22 атомов углерода, являются диатропными системами, но в отличие от бензола эти системы флуктуируют и для них характерны конформационные переходы с низкими барьерами инверсии для обмена протонами [40а].
аннулены, содержащие в кольце от 14 до 22 атомов углерода, являются диатропными системами, но в отличие от бензола эти системы флуктуируют и для них характерны конформационные переходы с низкими барьерами инверсии для обмена протонами [40а].

Термодинамические характеристики известны только для  . По последним оценкам энергии резонанса в
. По последним оценкам энергии резонанса в  -аннулене, величина РЭНЭ (резонансная энергия на
-аннулене, величина РЭНЭ (резонансная энергия на  -электрон) составляет здесь одну треть от соответствующей величины для бензола. [10] Аннулен явно не является ароматической системой, поскольку как полностью
-электрон) составляет здесь одну треть от соответствующей величины для бензола. [10] Аннулен явно не является ароматической системой, поскольку как полностью  (26), так и моно-транс- (27) формы принимают непланарные конформации. Введение мостиков приводит к большей устойчивости структур. В получающихся молекулах число несвязных взаимодействий уменьшается — но такие системы уже не являются больше макроциклическими.
(26), так и моно-транс- (27) формы принимают непланарные конформации. Введение мостиков приводит к большей устойчивости структур. В получающихся молекулах число несвязных взаимодействий уменьшается — но такие системы уже не являются больше макроциклическими.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- ПРЕДИСЛОВИЕ
- ИЗ ПРЕДИСЛОВИЯ К ТОМУ 1 АНГЛИЙСКОГО ИЗДАНИЯ
- ЧАСТЬ I. НОМЕНКЛАТУРА И СТЕРЕОХИМИЯ
- 1.1. ВВЕДЕНИЕ И СТЕРЕОХИМИЯ
- 1.1.2. СИММЕТРИЯ И ХИРАЛЬНОСТЬ
- 1.1.3. ХИМИЧЕСКАЯ ТОПОЛОГИЯ
- 1.1.4. ИЗОМЕРИЯ
- 1.1.4.2. Строение
- 1.1.4.3. Абсолютная конфигурация
- 1.1.4.4. Относительная конфигурация
- 1.1.4.5. Конформация
- 1.1.4.6. Концепция изомерии
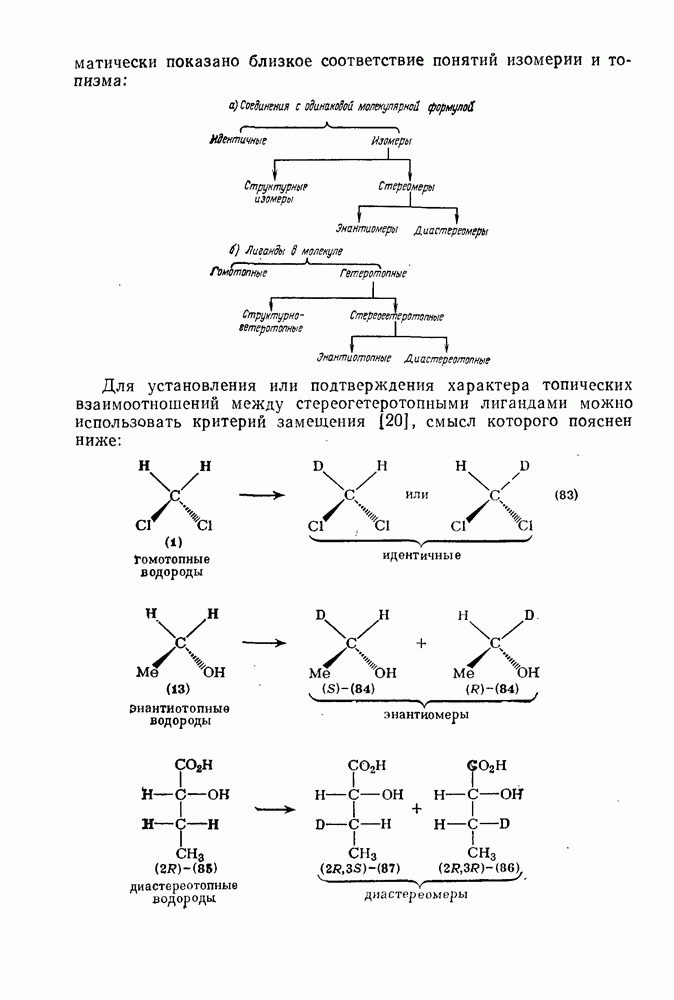
- 1.1.5. ТОПИЗМ
- 1.1.5.2. Прохиральность
- 1.1.5.3. Псевдоасимметрия (псевдохиральность)
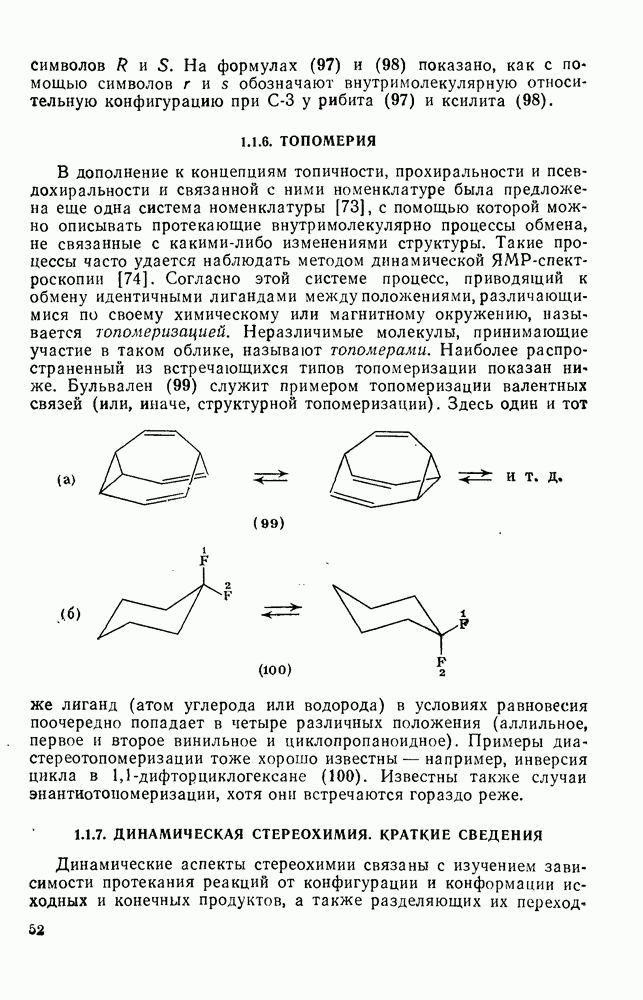
- 1.1.6. ТОПОМЕРИЯ
- 1.1.7. ДИНАМИЧЕСКАЯ СТЕРЕОХИМИЯ. КРАТКИЕ СВЕДЕНИЯ
- ЧАСТЬ 2. УГЛЕВОДОРОДЫ
- 2.1. НАСЫЩЕННЫЕ УГЛЕВОДОРОДЫ
- 2.1.2. Строение и номенклатура
- 2.1.2.1. Номенклатура IUPAC
- 2.1.2.2. Алициклические алканы
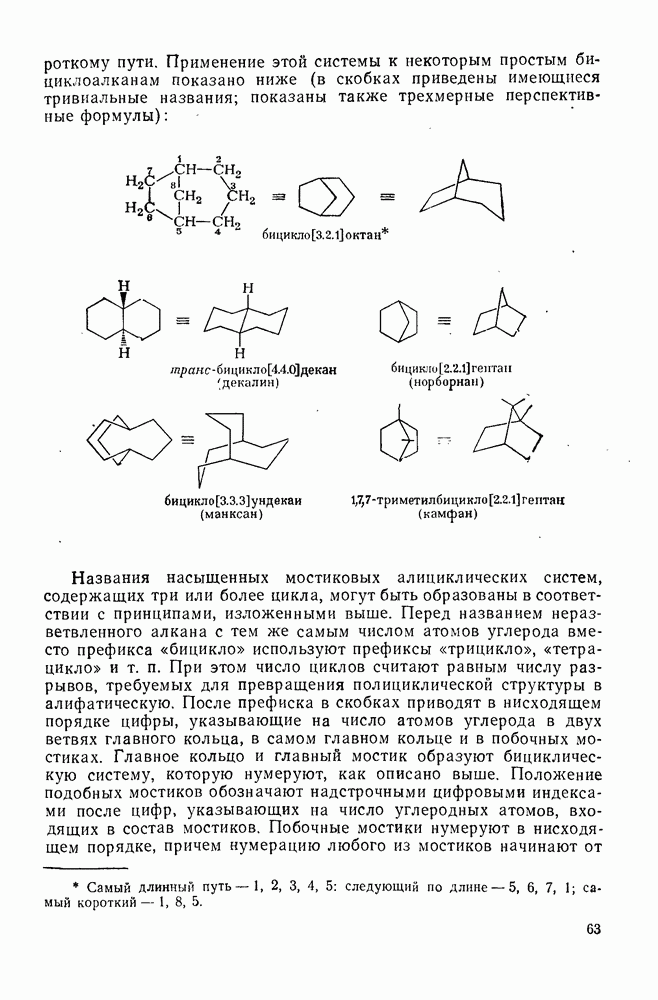
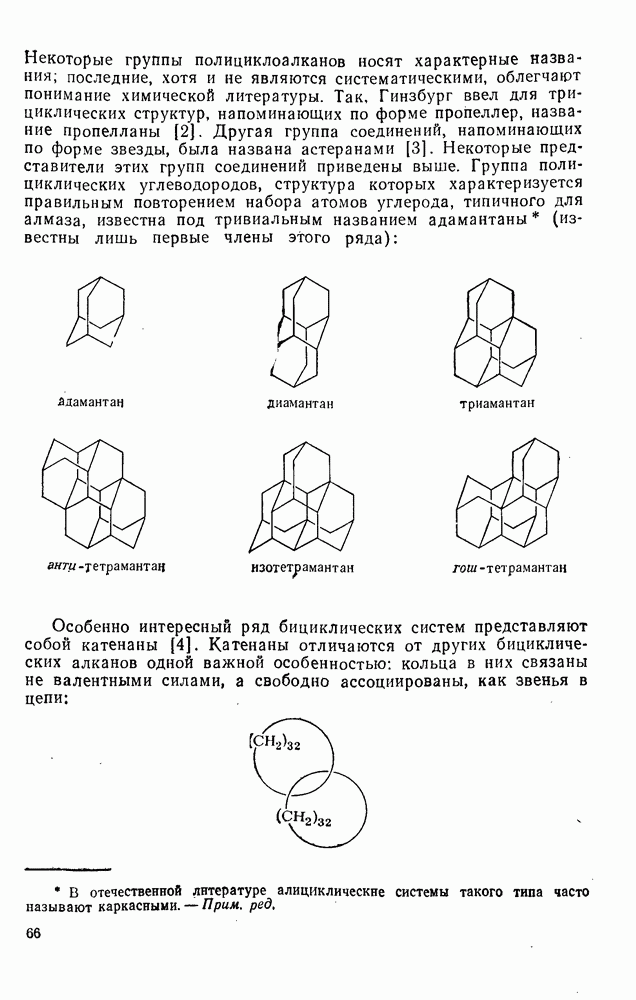
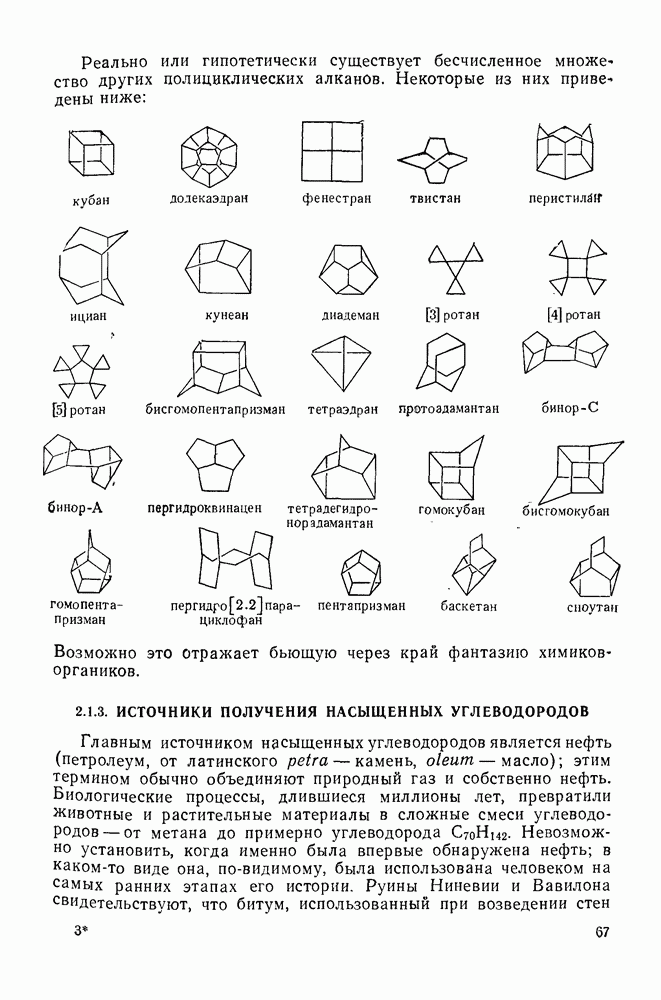
- 2.1.2.3. Полициклоалканы
- 2.1.3. ИСТОЧНИКИ ПОЛУЧЕНИЯ НАСЫЩЕННЫХ УГЛЕВОДОРОДОВ
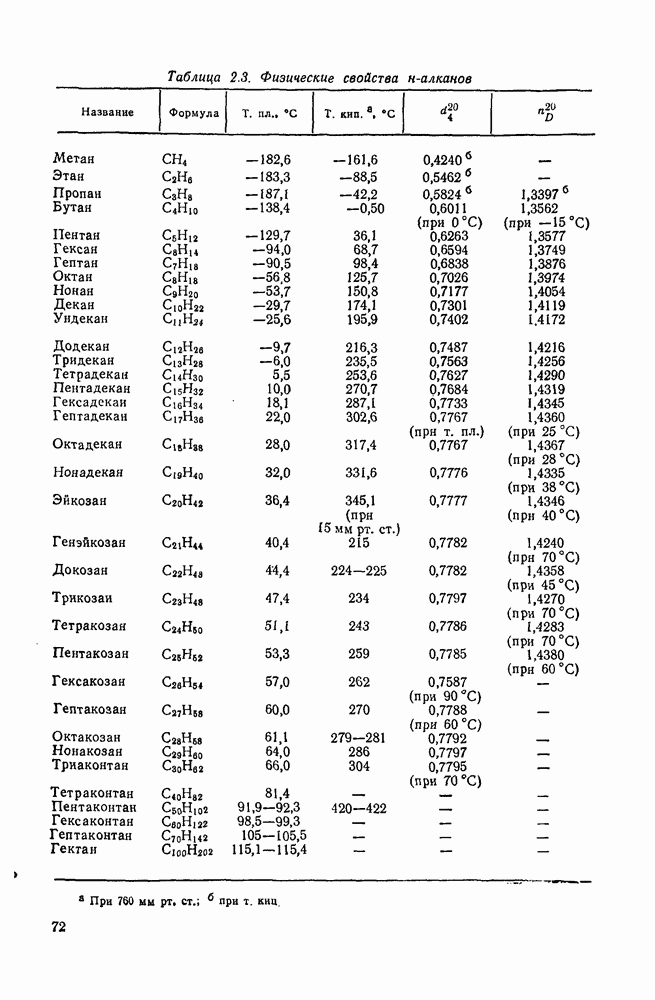
- 2.1.4. ФИЗИЧЕСКИЕ СВОЙСТВА
- 2.1.4.1. Ациклические алканы
- 2.1.4.2. Моно- и полициклоалканы
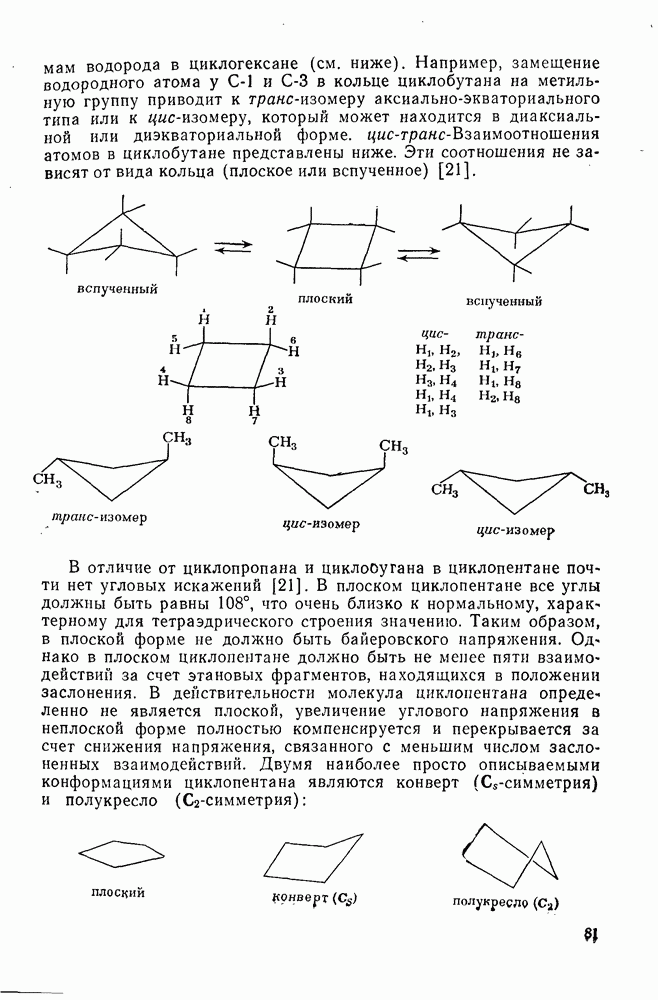
- 2.1.5. СТЕРЕОХИМИЯ И КОНФОРМАЦИОННЫЙ АНАЛИЗ
- 2.1.5.1. Углы и длины связей
- 2.1.5.2. Алкил- и полиалкилциклогексаны
- 2.1.5.3. Конформация карбоциклических колец, больших, чем циклогексан
- 2.1.6. ТЕРМОХИМИЧЕСКИЕ СВОЙСТВА
- 2.1.6.1. Горение. Алканы и циклоалканы как топливо
- 2.1.6.2. Определение теплот сгорания и термохимические свойства
- 2.1.6.3. Эмпирические методы оценки теплот образования алканов
- 2.1.6.4. Оценка теплот образования алканов на основе энергии связей
- 2.1.6.5. Оценка теплот образования алканов на основе инкрементов групп
- 2.1.6.6. Оценка теплот образования циклических, полициклических и мостиковых алканов на основе инкрементов «скошенных разобщенных» групп и «единственных» наиболее устойчивых конформаций
- 2.1.6.7. Молекулярно-механические расчеты теплот образования и энергии напряжения
- 2.1.6.8. Моно- и полициклоалкаиы
- 2.1.7. ПОЛУЧЕНИЕ АЦИКЛИЧЕСКИХ АЛКАНОВ
- 2.1.7.1. Получение алканов восстановлением олефинов
- 2.1.7.2. Получение алканов из альдегидов и кетонов
- 2.1.7.3. Получение алканов из спиртов и алкилгалогенидов
- 2.1.7.4. Получение алканов из карбоновых кислот
- 2.1.8. СИНТЕЗ МОНО- И ПОЛИЦИКЛОАЛКАНОВ
- 2.1.9. РЕАКЦИИ АЦИКЛИЧЕСКИХ АЛКАНОВ
- 2.1.9.1. Галогенирование
- 2.1.9.2. Нитрование
- 2.1.9.3. Окисление
- 2.1.9.4. Каталитическая изомеризация алканов
- 2.1.9.5. Каталитическое алкилирование алканов
- 2.1.9.6. Реакции крекинга алканов
- 2.1.9.7. Термический крекинг
- 2.1.9.8. Каталитический крекинг
- 2.1.9.9. Каталитический риформинг и дегидроциклизация алканов
- 2.1.10. РЕАКЦИИ ЦИКЛОАЛКАНОВ И ПОЛИЦИКЛОАЛКАНОВ
- 2.2. ОЛЕФИНОВЫЕ И АЦЕТИЛЕНОВЫЕ УГЛЕВОДОРОДЫ
- 2.2.2. ПОЛУЧЕНИЕ ОЛЕФИНОВ
- 2.2.2.1. Элиминирование в системах
- 2.2.2.2. Элиминирование из систем
- 2.2.2.3. Циклоэлиминирование
- 2.2.2.4. Частичное восстановление
- 2.2.2.5. Элиминирование сульфонилгидразонов
- 2.2.2.6. Реакция Виттига и родственные ей реакции
- 2.2.2.7. Различные реакции конденсации
- 2.2.2.8. Электроциклические реакции
- 2.2.2.9. Циклоолигомеризация
- 2.2.2.11. Реакции винильных производных
- 2.2.3. РЕАКЦИИ ОЛЕФИНОВ
- 2.2.3.1. Электрофильное присоединение
- 2.2.3.2. Нуклеофильное присоединение
- 2.2.3.3. Радикальное присоединение
- 2.2.3.4. Циклоприсоединение и родственные реакции
- 2.2.3.5. Окисление
- 2.2.3.6. Восстановление
- 2.2.3.7. Перегруппировки
- 2.2.3.8. Фотохимические реакции
- 2.2.3.9. Прочие реакции
- 2.3. ДИЕНЫ, ПОЛНЕНЫ И АЦЕТИЛЕНОВЫЕ УГЛЕВОДОРОДЫ
- 2.3.1. СОПРЯЖЕННЫЕ ДИЕНЫ И ПОЛНЕНЫ
- 2.3.1.2. Получение сопряженных диенов
- 2.3.2. РЕАКЦИИ СОПРЯЖЕННЫХ ДИЕНОВ
- 2.3.2.2. Восстановление
- 2.3.2.3. Гидроборирование
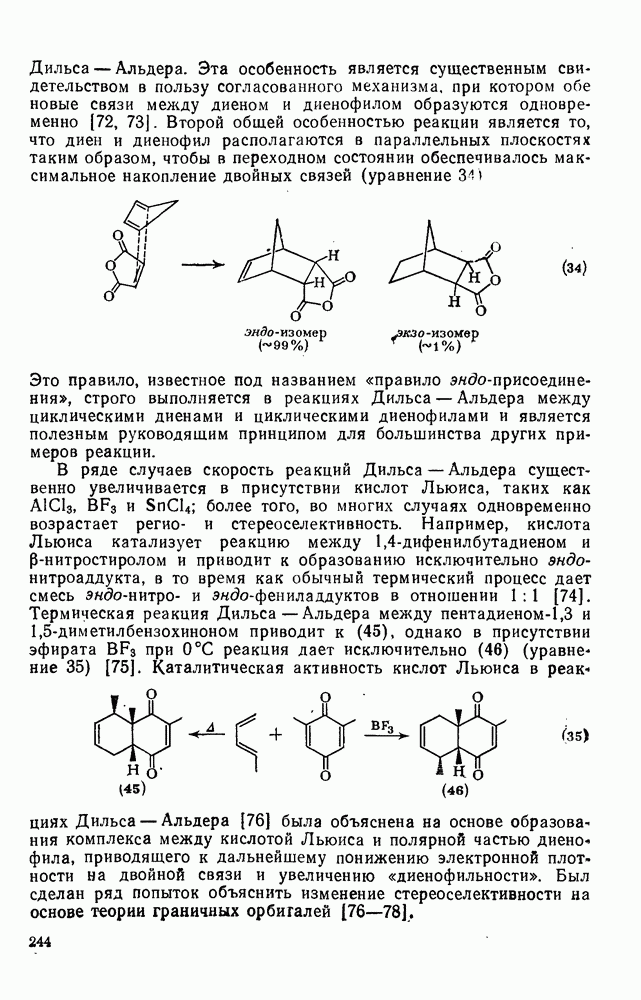
- 2.3.2.4. Реакция Дильса — Альдера
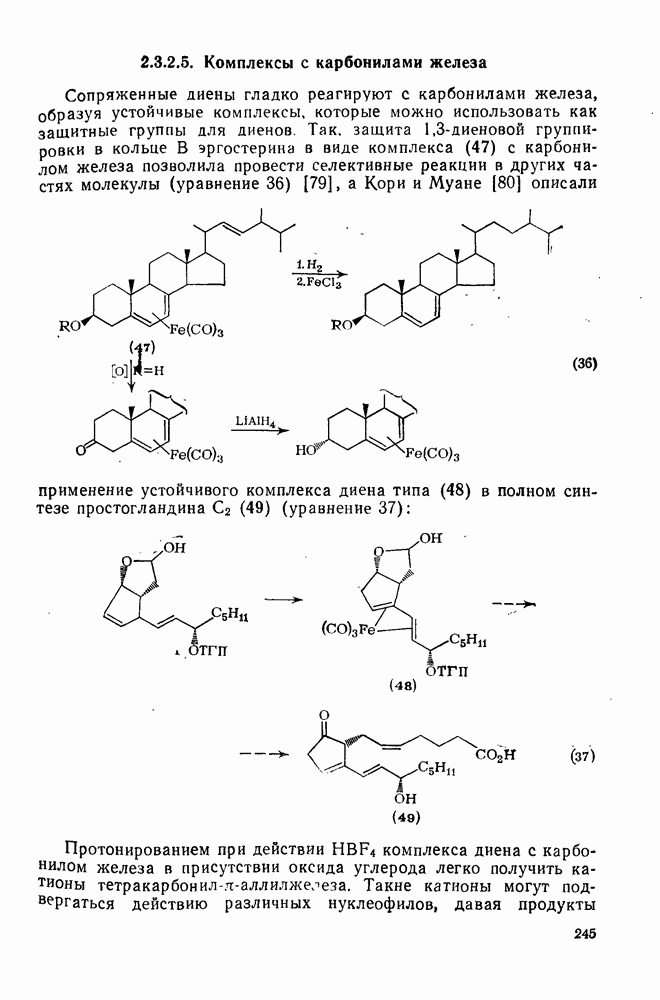
- 2.3.2.5. Комплексы с карбонилами железа
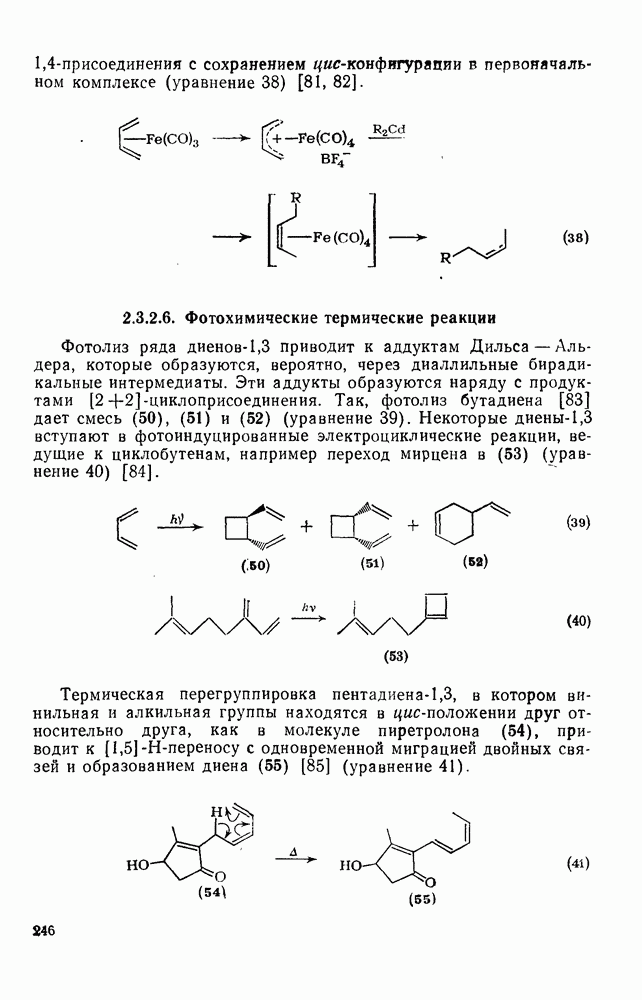
- 2.3.2.6. Фотохимические термические реакции
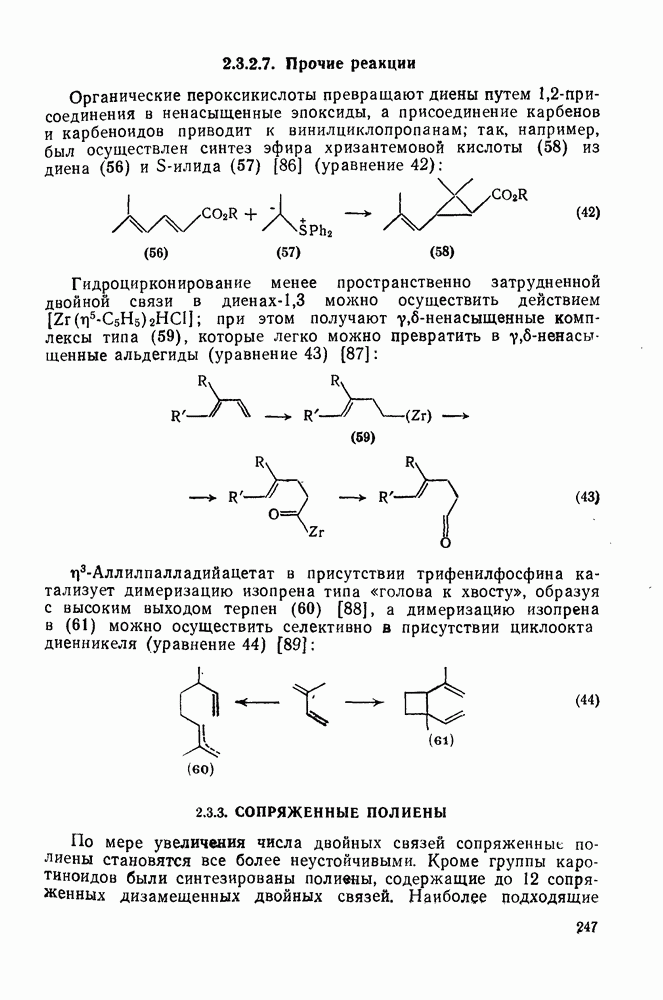
- 2.3.2.7. Прочие реакции
- 2.3.3. СОПРЯЖЕННЫЕ ПОЛИЕНЫ
- 2.3.4. ПРИРОДНЫЕ ДИЕНЫ И ПОЛНЕНЫ
- 2.3.5. АЛЛЕНЫ И КУМУЛЕНЫ
- 2.3.5.2. Получение алленов
- 2.3.6. РЕАКЦИИ АЛЛЕНОВ
- 2.3.6.2. Гидрирование
- 2.3.6.3. Реакции алленов в присутствии комплексов металлов
- 2.3.7. КУМУЛЕНЫ
- 2.3.8. ПРИРОДНЫЕ АЛЛЕНЫ И КУМУЛЕНЫ
- 2.3.9. АЦЕТИЛЕНЫ И ПОЛИАЦЕТИЛЕНЫ
- 2.3.9.2. Получение ацетиленов
- 2.3.10. РЕАКЦИИ АЦЕТИЛЕНОВ
- 2.3.10.2. Изомеризация
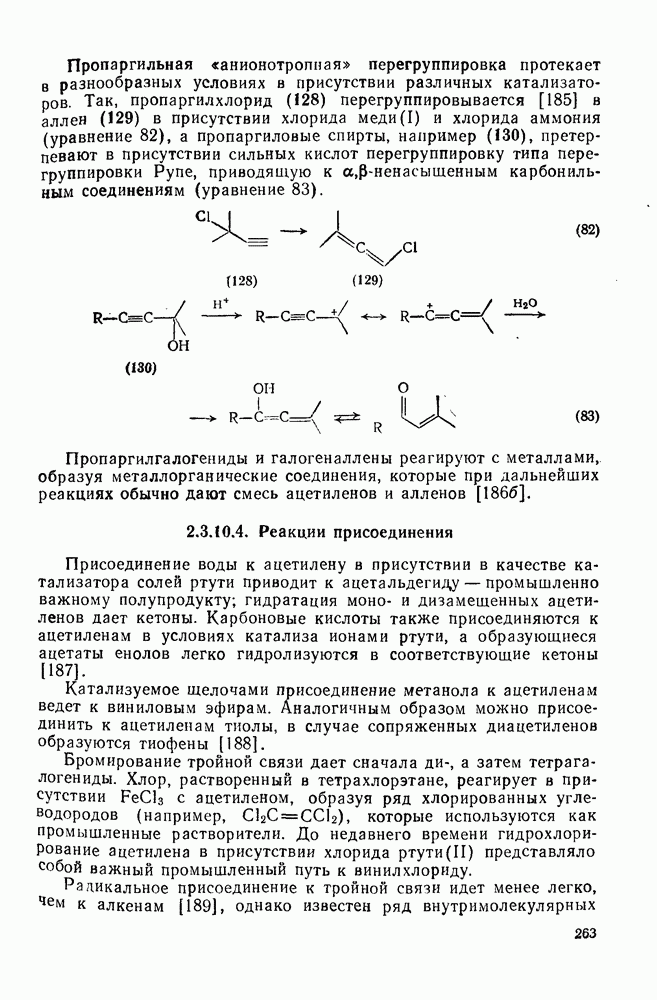
- 2.3.10.3. Пропаргильные перегруппировки
- 2.3.10.4. Реакции присоединения
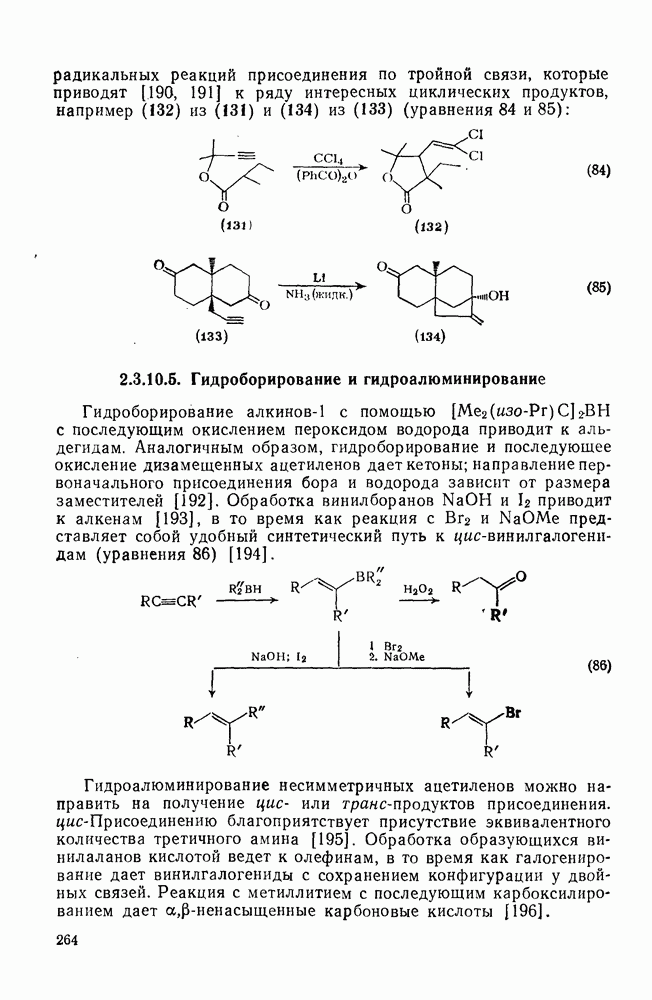
- 2.3.10.5. Гидроборирование и гидроалюминирование
- 2.3.10.6. Реакции замещения
- 2.3.10.7. Восстановление
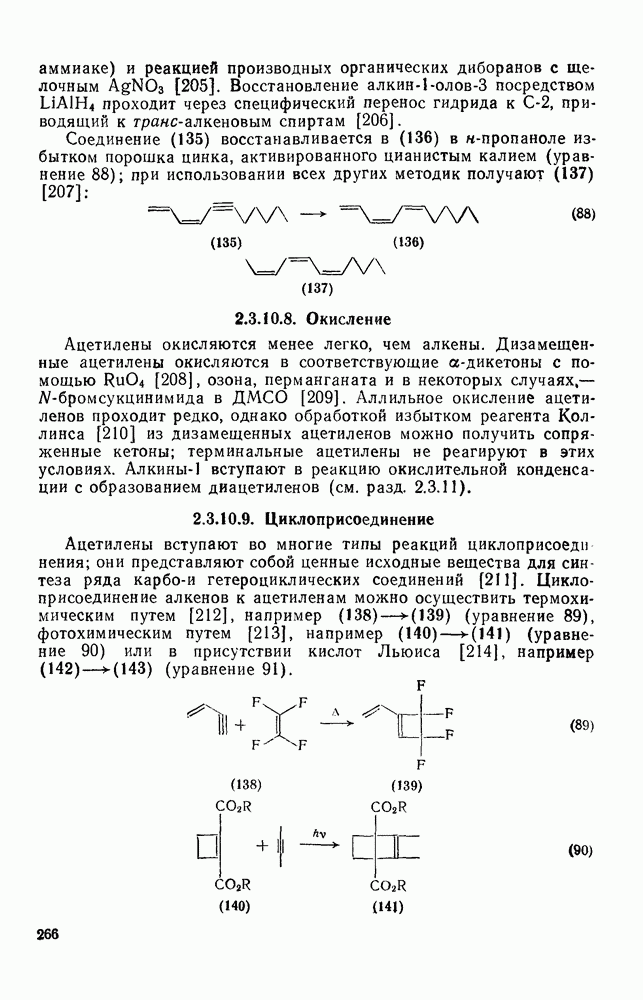
- 2.3.10.8. Окисление
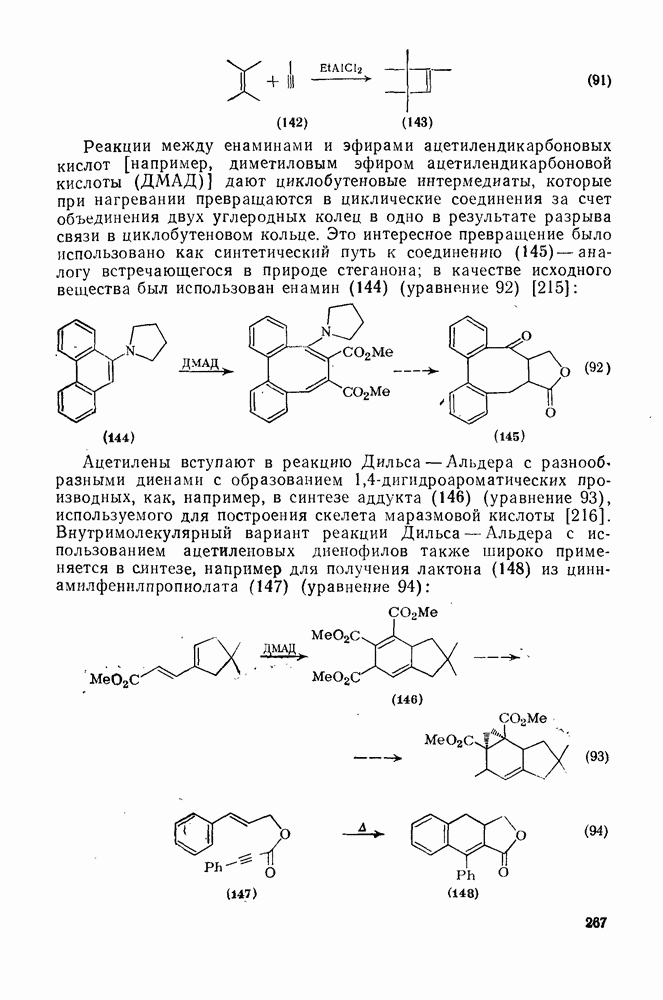
- 2.3.10.9. Циклоприсоединение
- 2.3.10.10. Реакции катализуемые металлами
- 2.3.11. ПОЛИАЦЕТИЛЕНЫ
- 2.3.12. ПРИРОДНЫЕ АЦЕТИЛЕНЫ И ПОЛИАЦЕТИЛЕНЫ
- 2.3.13. СОПРЯЖЕННЫЕ ЕНИНЫ
- 2.3.13.1. Получение сопряженных енинов
- 2.3.14. РЕАКЦИИ СОПРЯЖЕННЫХ ЕНИНОВ
- 2.3.15. ПРИРОДНЫЕ СОПРЯЖЕННЫЕ ЕНИНЫ
- 2.4. АРОМАТИЧНОСТЬ
- 2.4.2. ЭЛЕКТРОННЫЕ ТЕОРИИ СТРОЕНИЯ БЕНЗОЛА
- 2.4.3. КРИТЕРИИ АРОМАТИЧНОСТИ
- 2.4.3.1. Термодинамические свойства
- 2.4.3.2. Структурные особенности
- 2.4.3.3. Магнитные свойства
- 2.4.3.4. Прочие критерии
- 2.4.4. АНТИАРОМАТИЧНОСТЬ
- 2.4.4.1. Термодинамические свойства
- 2.4.4.2. Структурные особенности
- 2.4.4.3. Магнитные свойства
- 2.4.4.4. Прочие свойства
- 2.4.5. ТЕОРЕТИЧЕСКИЕ ОПРЕДЕЛЕНИЯ АРОМАТИЧНОСТИ
- 2.4.5.1. Полуэмпирические расчеты и дьюаровская резонансная энергия
- 2.4.5.2. Расчеты по методу валентных пар и применение резонансного метода
- 2.4.5.3. Локализация связей
- 2.4.5.4. Связь энергетических критериев с критериями локализации связей
- 2.4.6. АРОМАТИЧЕСКИЕ ПЕРЕХОДНЫЕ СОСТОЯНИЯ
- 2.5. АРЕНЫ И ИХ РЕАКЦИИ
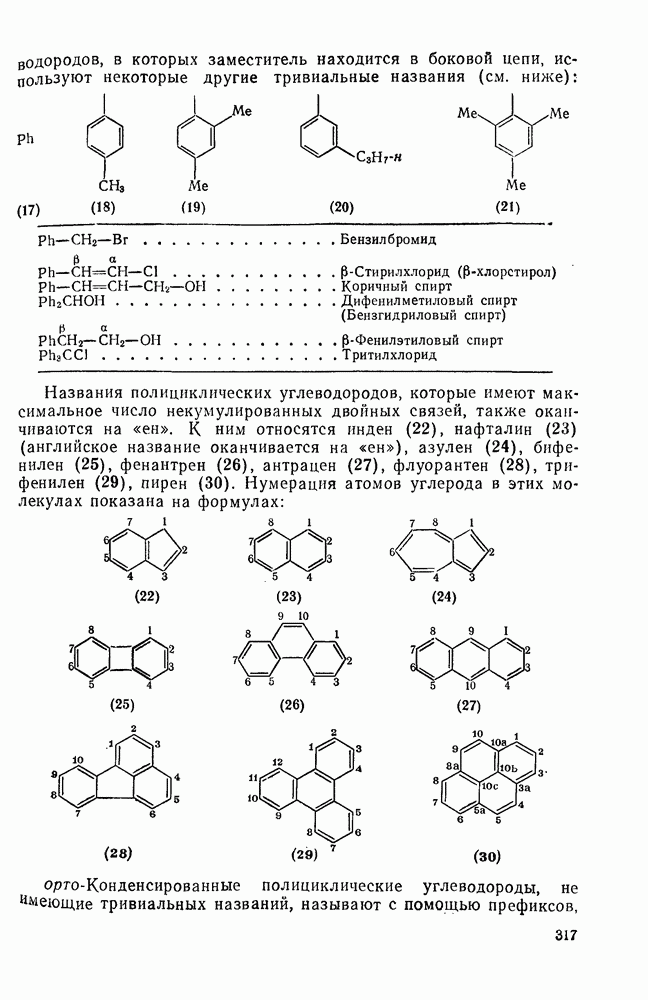
- 2.5.2. НОМЕНКЛАТУРА
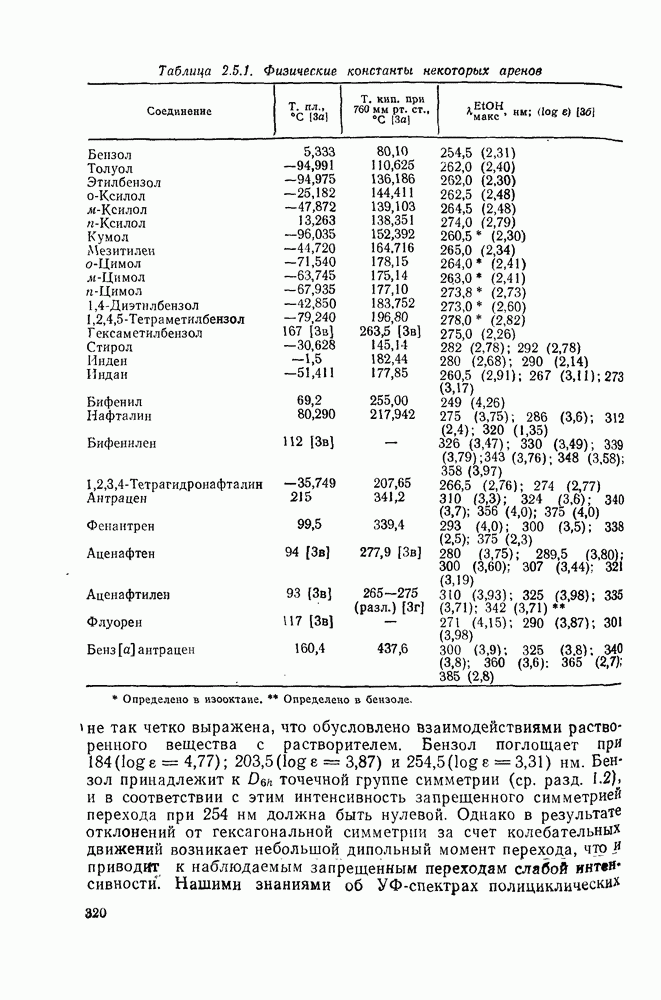
- 2.5.3. ФИЗИЧЕСКИЕ СВОЙСТВА АРЕНОВ
- 2.5.4. ПРОМЫШЛЕННОЕ ПРОИЗВОДСТВО АРЕНОВ
- 2.5.5. ЦИКЛОТРИМЕРИЗАЦИЯ АЦЕТИЛЕНОВ
- 2.5.6. РЕАКЦИИ ЭЛЕКТРОФИЛЬНОГО ПРИСОЕДИНЕНИЯ — ЭЛИМИНИРОВАНИЯ АРЕНОВ
- 2.5.6.1. Механизм ароматического нитрования [15]
- 2.5.6.2. Кинетические изотопные эффекты [21]
- 2.5.6.3. Реакции, включающие ипсо-протонирование
- 2.5.6.4. Металлирование
- 2.5.6.5. Электрофилы IV группы
- 2.5.6.6. Электрофилы V группы
- 2.5.6.7. Электрофилы VI группы [18, 56]
- 2.5.6.8. Электрофилы VII группы [18, 25а, 56]
- 2.5.7. ОРИЕНТАЦИЯ В РЕАКЦИЯХ ЭЛЕКТРОФИЛЬНОГО ПРИСОЕДИНЕНИЯ — ЭЛИМИНИРОВАНИЯ
- 2.5.8. РАДИКАЛЬНОЕ ГАЛОГЕНИРОВАНИЕ АРЕНОВ В БОКОВУЮ ЦЕПЬ [96]
- 2.5.9. РЕАКЦИИ ПРИСОЕДИНЕНИЯ К АРЕНАМ
- 2.5.9.1. Восстановление аренов
- 2.5.9.2. Термическое циклоприсоединение к аренам
- 2.5.9.3. Фотоциклоприсоединение к моноциклическим аренам [126]
- 2.5.9.4. Фотохимические реакции полициклических аренов
- 2.6.10. ФОТОИЗОМЕРИЗАЦИЯ АРЕНОВ [126б]
- 2.5.11. ОКИСЛЕНИЕ АРЕНОВ [153]
- 2.5.12. РЕАКЦИИ АРЕНОВ С СИНГЛЕТНЫМ КИСЛОРОДОМ [162]
- 2.5.13. ПРИГОТОВЛЕНИЕ БИ- И ПОЛИАРИЛОВ
- 2.5.14. ВНУТРИМОЛЕКУЛЯРНАЯ ФОТОЦИКЛИЗАЦИЯ, ПРИВОДЯЩАЯ К ПОЛИЦИКЛИЧЕСКИМ АРЕНАМ
- 2.5.15. ВНУТРИМОЛЕКУЛЯРНАЯ ЦИКЛИЗАЦИЯ ДИЗАМЕЩЕННЫХ АРЕНОВ
- 2.5.16. ЦИКЛОФАНЫ
- 2.5.17. КОНФОРМАЦИЯ И ХИРАЛЬНОСТЬ АРЕНОВ
- 2.5.18. АЗУЛЕНЫ И НЕБЕНЗОИДНЫЕ АРЕНЫ
- 2.6. АННУЛЕНЫ И РОДСТВЕННЫЕ СИСТЕМЫ
- 2.6.2. МЕТОДЫ СИНТЕЗА
- 2.6.2.1. Окислительное сочетание терминальных ацетиленов (метод Зондхеймера)
- 2.6.2.2. Фотооблучение полициклических валентных таутомеров
- 2.6.2.3. Валентная таутомерия типа норкарадиен — циклогептатриен (метод Фогеля)
- 2.6.2.4. Прочие методы
- 2.6.3. СВОЙСТВА АННУЛЕНОВ
- 2.6.4. СВОЙСТВА 4n-АННУЛЕНОВ
- 2.6.5. ДЕГИДРОАННУЛЕНЫ
- 2.6.6. АННЕЛИРОВАННЫЕ АННУЛЕНЫ
- 2.6.7. АРОМАТИЧЕСКИЕ И АНТИАРОМАТИЧЕСКИЕ МОНОЦИКЛИЧЕСКИЕ ИОНЫ
- 2.6.8. АРОМАТИЧЕСКИЕ И АНТИАРОМАТИЧЕСКИЕ ПОЛИЦИКЛИЧЕСКИЕ ИОНЫ
- 2.6.9. ГОМОАРОМАТИЧЕСКИЕ СИСТЕМЫ
- 2.7. КАРБОКАТИОНЫ И КАРБАНИОНЫ
- 2.7.1.2. Краткий исторический очерк развития химии карбокатионов
- 2.7.1.3. Методы генерации карбокатионов
- 2.7.1.4. Типы карбокатионов
- 2.7.1.5. Изучение карбокатионов: методы и результаты
- 2.7.1.6. Реакции карбокатионов
- 2.7.2. КАРБАНИОНЫ
- 2.7.2.2. Методы генерации карбанионов
- 2.7.2.3. Типы карбанионов
- 2.7.2.4. Физические свойства карбанионов
- 2.7.5.2. Реакции карбанионов
- 2.8. РАДИКАЛЫ, КАРБЕНЫ, АРИНЫ
- 2.8.1. РАДИКАЛЫ
- 2.8.1.1. Структура, устойчивость и реакционная способность радикалов
- 2.8.1.2. Методы генерации и реакции радикалов
- 2.8.2. КАРБЕНЫ
- 2.8.2.1. Методы генерации карбенов и карбеноидов
- 2.8.2.2. Реакции карбенов
- 2.8.3. АРИНЫ
- 2.8.3.1. Структура и спектры аринов
- 2.8.3.2. Методы генерации аринов
- 2.8.3.3. Реакции аринов
- ЧАСТЬ 3. ГАЛОГЕНСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
- 3.2. МЕТОДЫ ГАЛОГЕНИРОВАНИЯ
- 3.2.1. Гомолитическое замещение водорода
- 3.2.1.2. Использование галогенпроизводных в качестве реагентов
- 3.2.2. Гомолитическое замещение функциональных групп
- 3.2.3. Гомолитическое присоединение к ненасыщенным системам
- 3.2.3.1. Присоединение галогеноводородов
- 3.2.3.2. Присоединение галогенов
- 3.2.4. Электрофильное галогенирование
- 3.2.4.1. Замещение у насыщенной связи С-Н
- 3.2.4.2. Реакции с ненасыщенными системами
- 3.2.4.3. Реакции с карбанионами
- 3.2.5. Нуклеофильное галогенирование
- 3.2.5.1. Галогенирование с замещением функциональной группы
- 3.2.5.2. Галогенирование в ароматических системах
- 3.2.5.3. Галогенирование путем обмена галогенов
- 3.2.6. Синтез полигалогенированных соединений
- 3.2.6.1. Синтез полифторированных соединений
- 3.2.6.2. Синтез других полигалогенированных соединений
- 3.3. ГАЛОГЕНАЛКАНЫ
- 3.3.1. Характеристика связей углерод-галоген
- 3.3.2. Промышленное применение
- 3.3.3. Нуклеофильное замещение галогена
- 3.3.3.1. Реакции SN2 и родственные процессы
- 3.3.3.2. Соучастие соседних групп
- 3.3.3.3. Реакции SN1 и относительно долгоживущие карбениевые ионы
- 3.3.3.4. Галогенониевые ионы
- 3.3.3.5. Галогенсодержащие карбениевые ионы
- 3.3.3.6. Механизм замещения с переносом электрона
- 3.3.4. Восстановление
- 3.3.5. Замещение на металлы
- 3.3.6. Элиминирование
- 3.3.6.1. b-Элиминирование
- 3.3.6.2. Галогенкарбанионы
- 3.3.6.3. Элиминирование через карбанионы
- 3.3.6.4. b-Элиминирование из металлорганических соединений
- 3.3.6.5. a-Элиминирование (генерирование карбенов)
- 3.4. ГАЛОГЕНАЛКЕНЫ
- 3.4.1. Синтез галогеналкенов
- 3.4.2. Нуклеофильная атака
- 3.4.2.1. Реакции, индуцируемые фторид-ионом
- 3.4.2.2. Другие реакции замещения
- 3.4.3. Радикальное присоединение
- 3.4.4. Электрофильное присоединение
- 3.4.5. Циклоприсоединение
- 3.4.5.1. [2+2]-Циклоприсоединение
- 3.4.5.2. [4+2]-Циклоприсоединение
- 3.5. ГАЛОГЕНАЛКИНЫ
- 3.6. ГАЛОГЕНАРЕНЫ
- 3.6.1. Замещение галогена
- 3.6.1.2. Присоединение-элиминирование
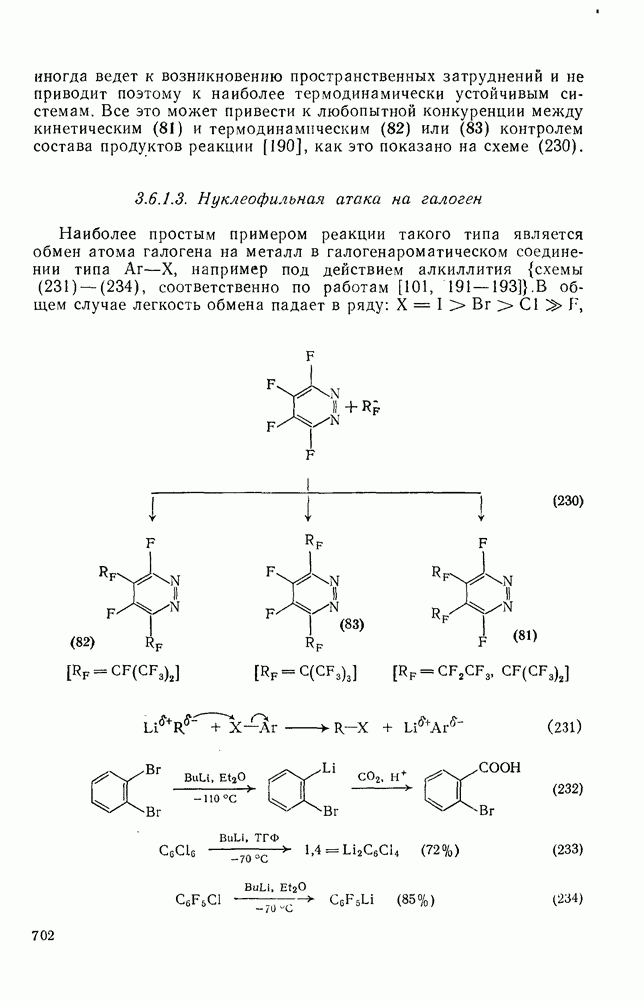
- 3.6.1.3. Нуклеофильная атака на галоген
- 3.6.1.4. Перенос электрона
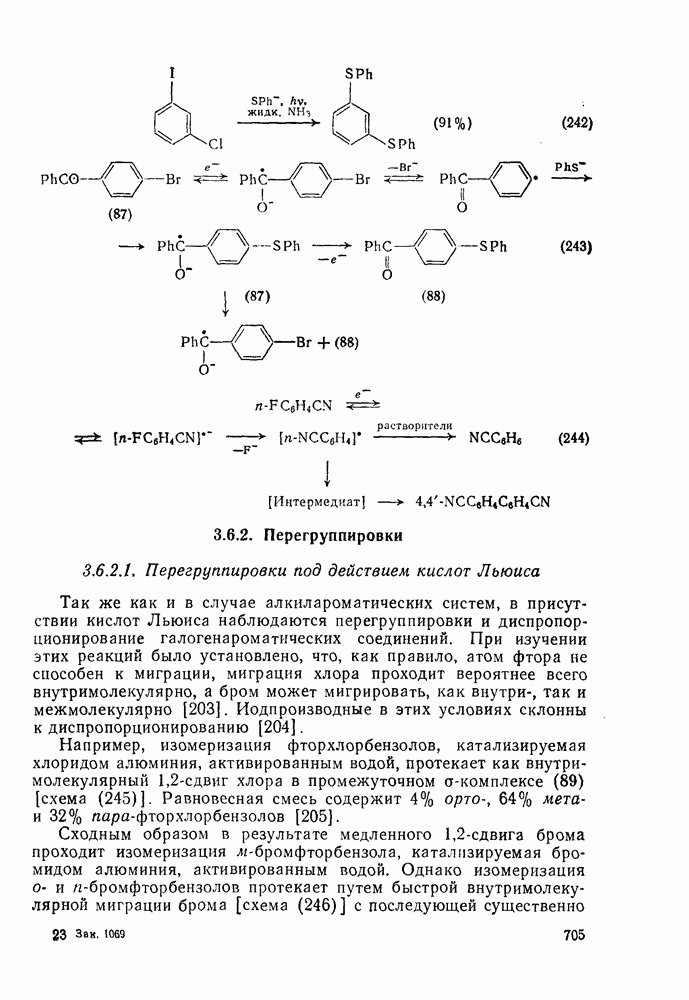
- 3.6.2. Перегруппировки
- 3.6.2.1. Перегруппировки под действием кислот Льюиса
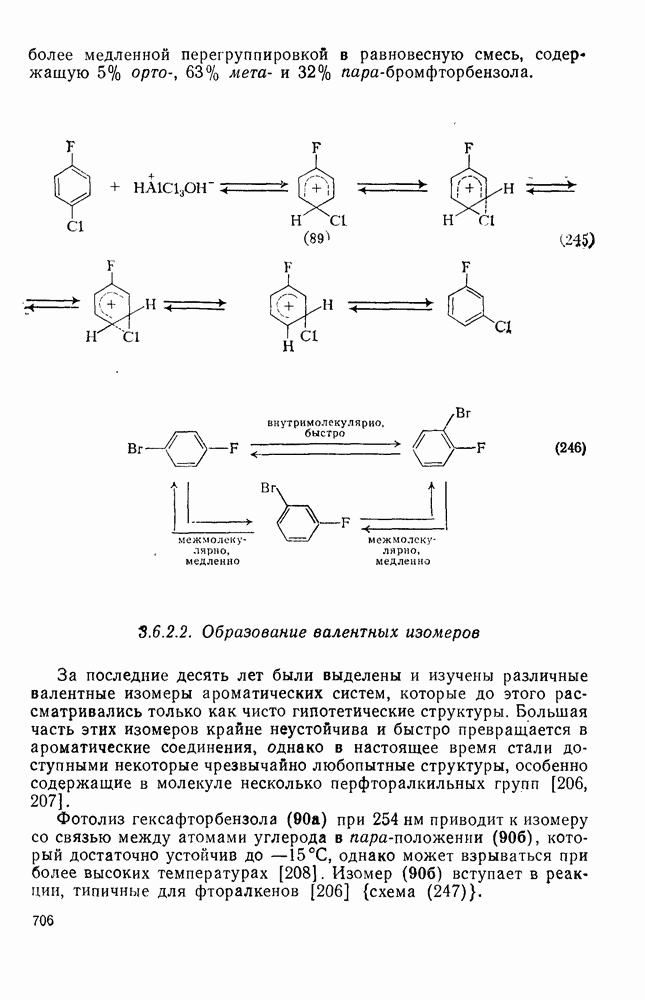
- 3.6.2.2. Образование валентных изомеров