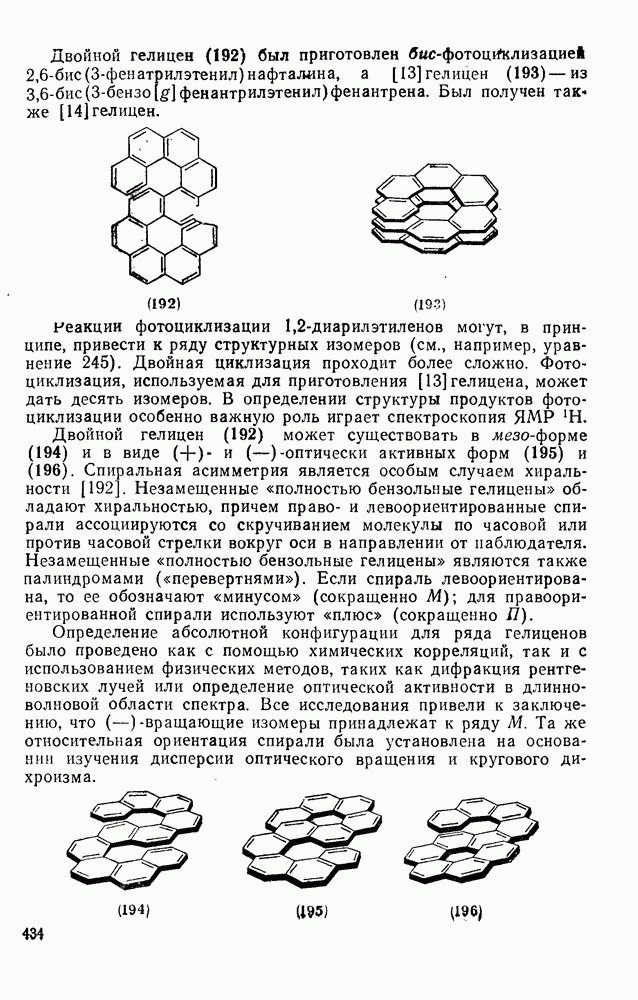
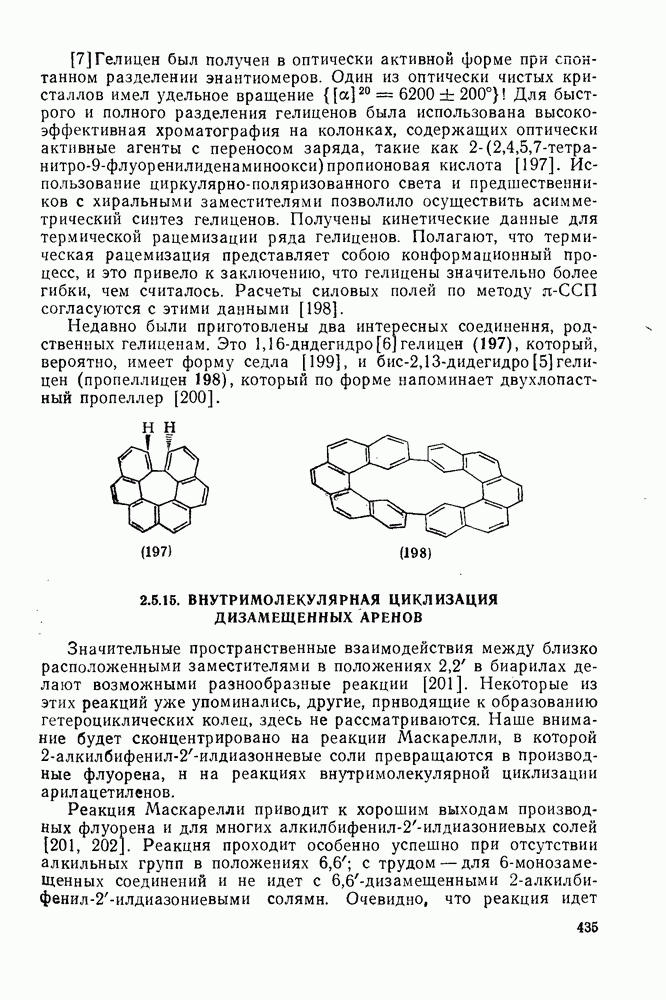
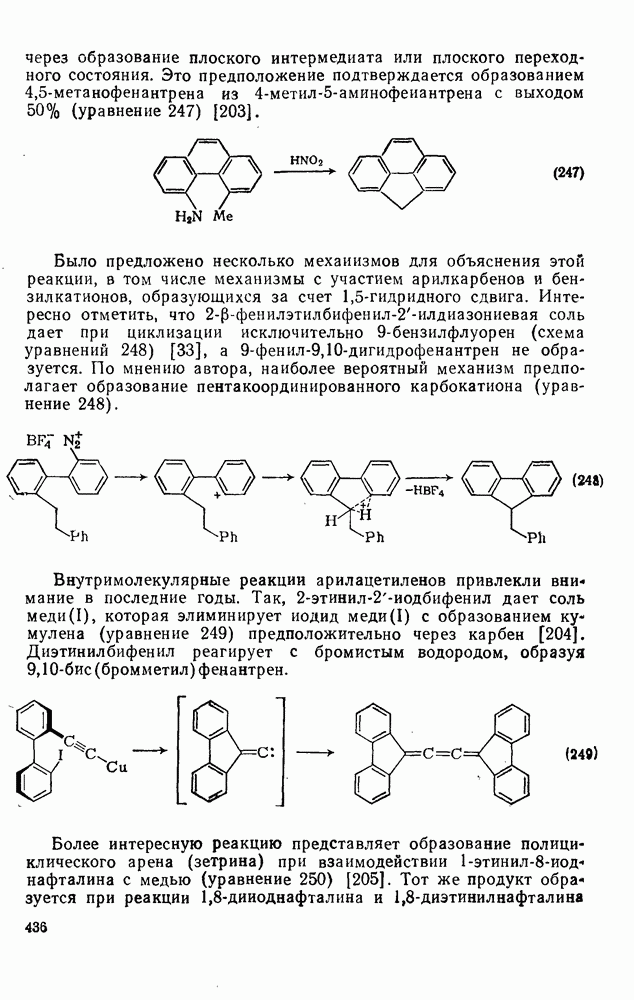
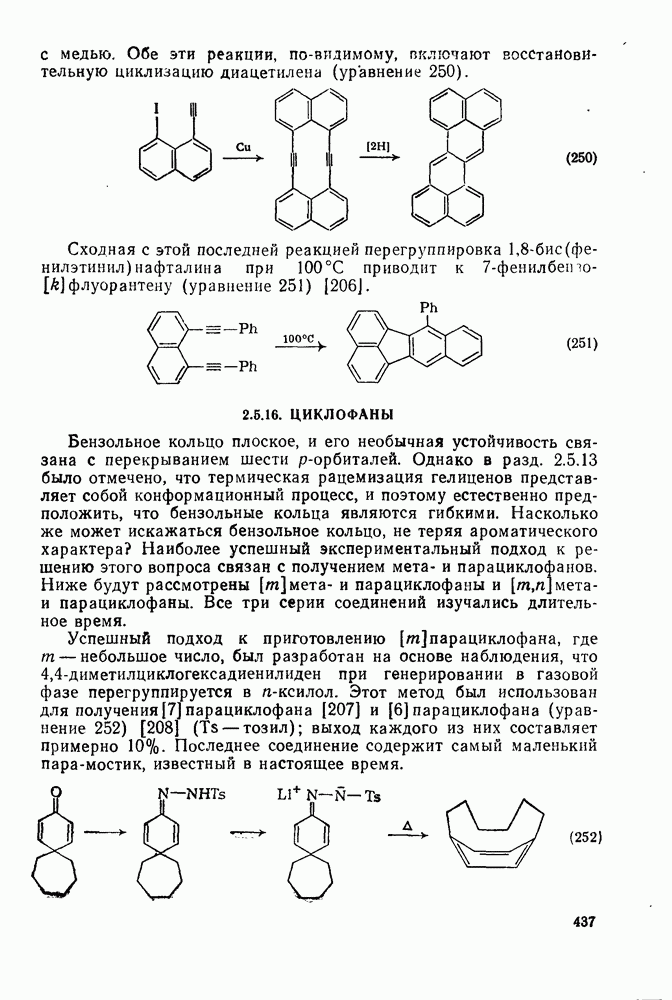
| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
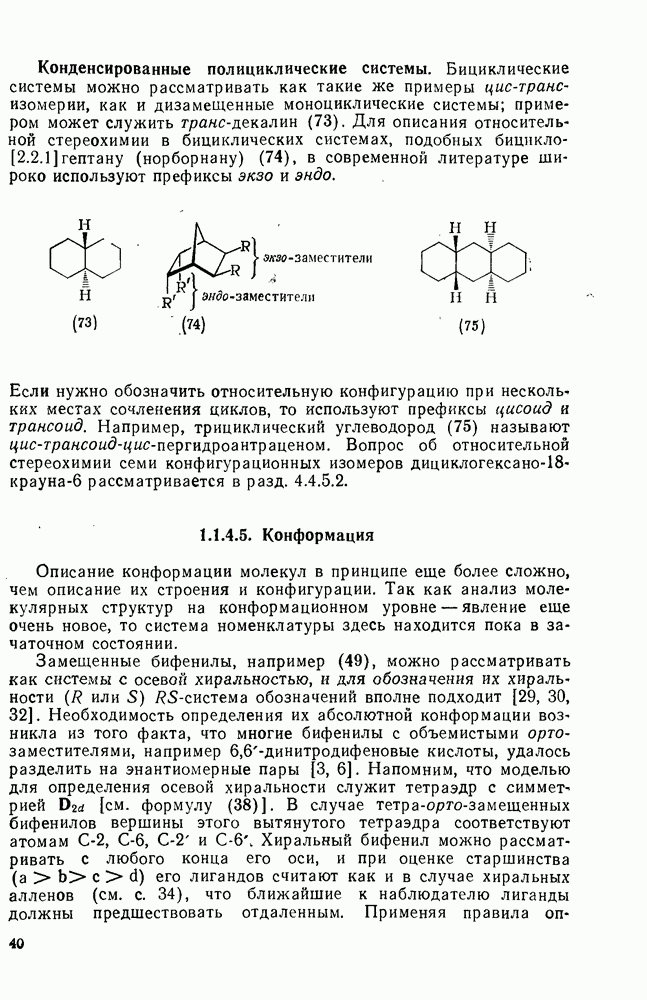
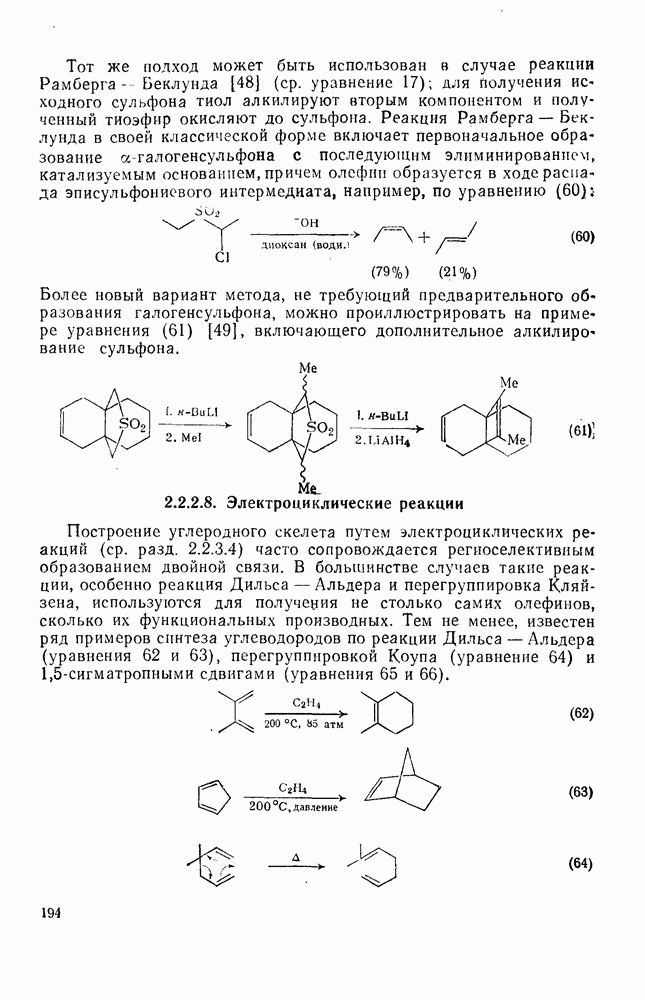
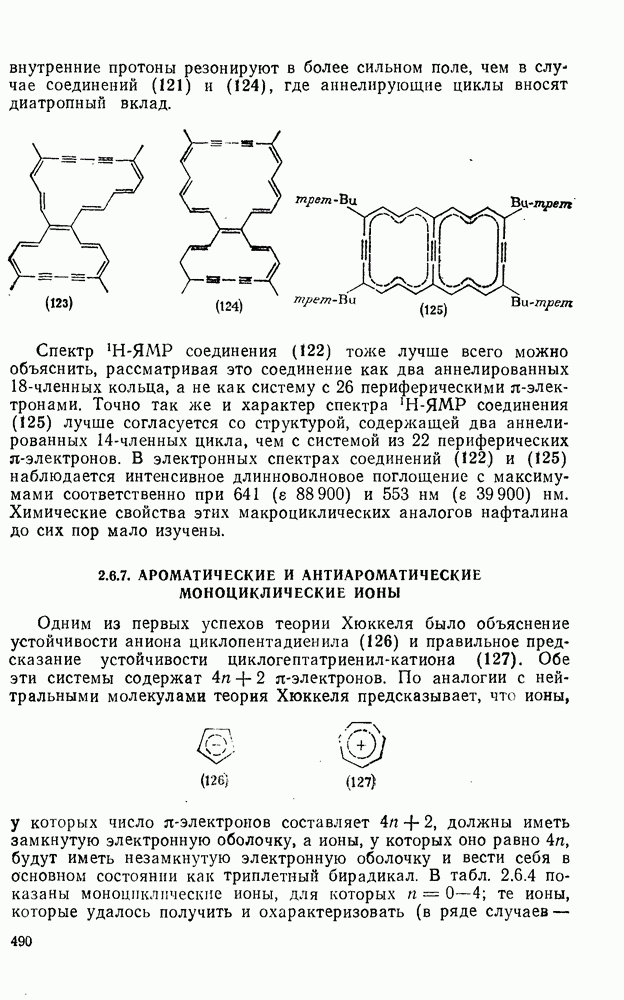
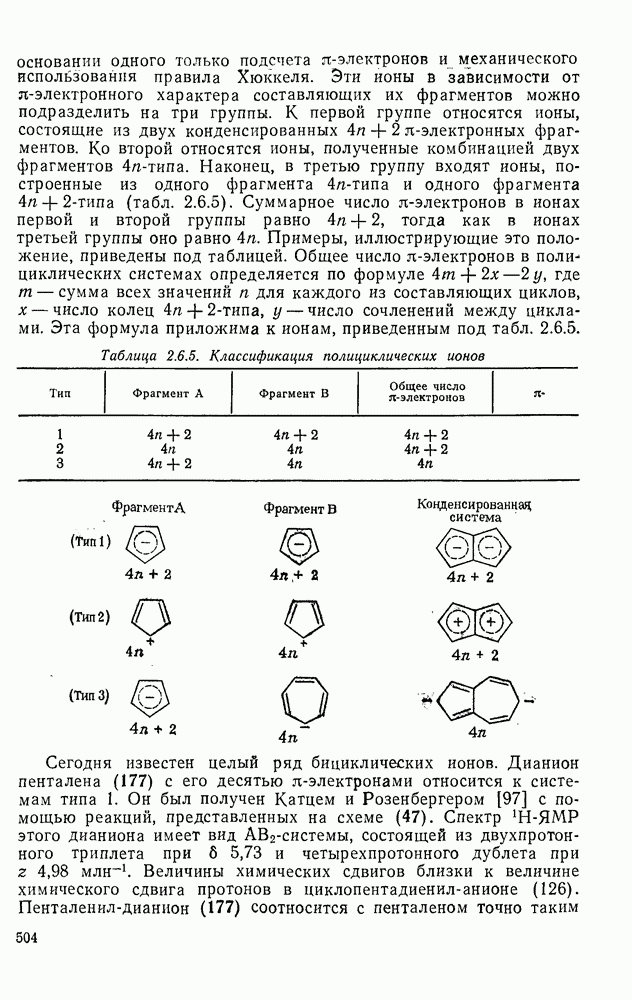
2.6.7. АРОМАТИЧЕСКИЕ И АНТИАРОМАТИЧЕСКИЕ МОНОЦИКЛИЧЕСКИЕ ИОНЫ
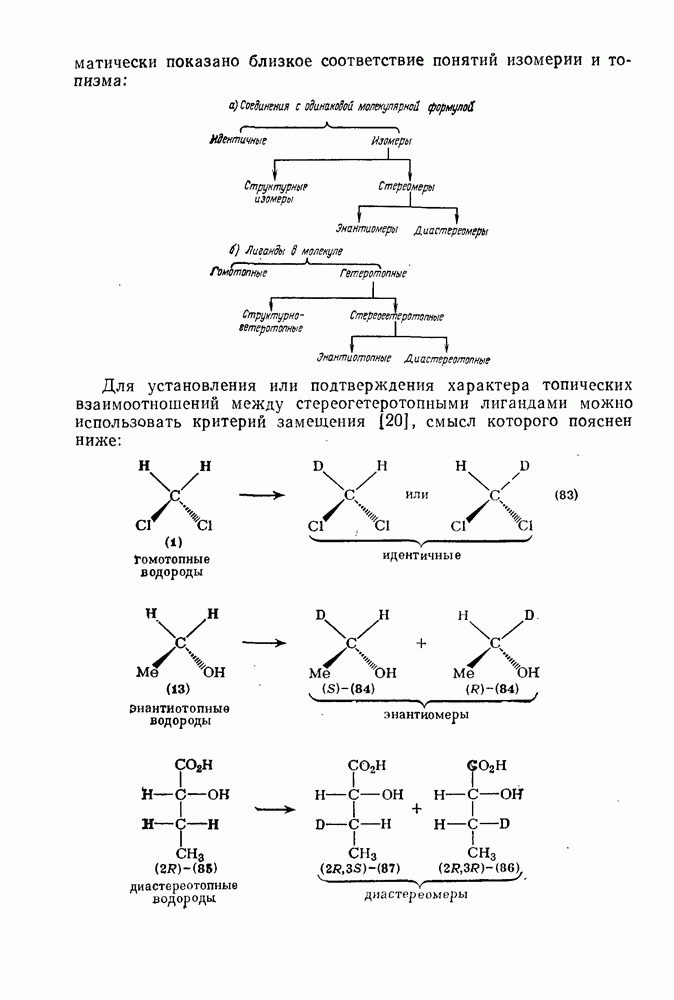
Одним из первых успехов теории Хюккеля было объяснение устойчивости аниона циклопентадиенила (126) и правильное предсказание устойчивости циклогептатриенил-катиона (127). Обе эти системы содержат  -электронов. По аналогии с нейтральными молекулами теория Хюккеля предсказывает, что ионы,
-электронов. По аналогии с нейтральными молекулами теория Хюккеля предсказывает, что ионы,

у которых число  -электронов составляет
-электронов составляет  должны иметь замкнутую электронную оболочку, а ионы, у которых оно равно
должны иметь замкнутую электронную оболочку, а ионы, у которых оно равно  , будут иметь незамкнутую электронную оболочку и вести себя в основном состоянии как триплетный бирадикал. В табл. 2.6.4 показаны моноцпклические ионы, для которых
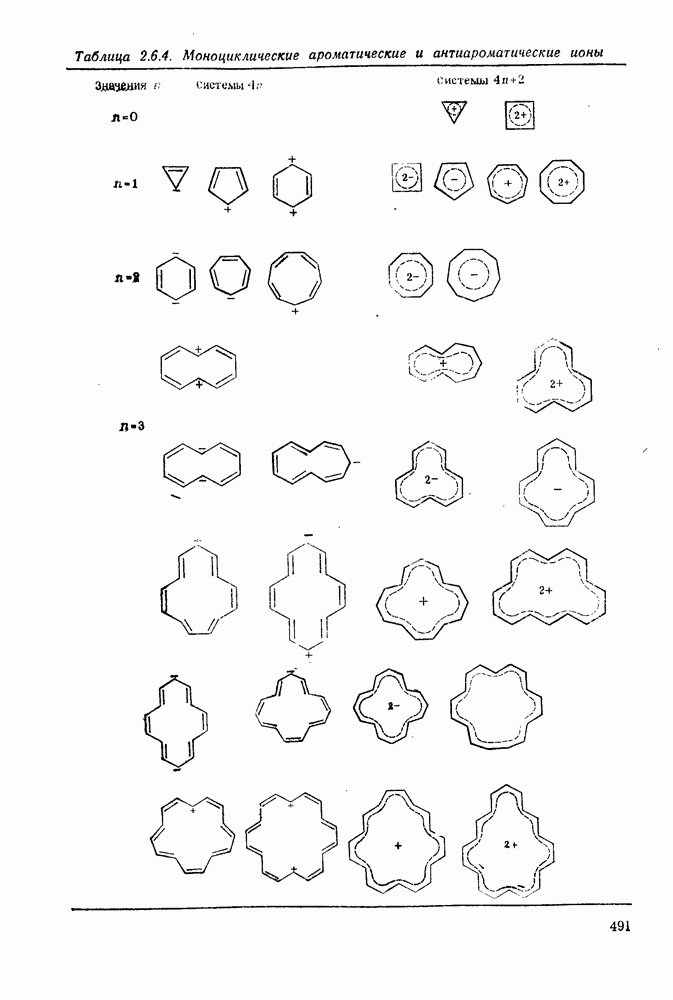
, будут иметь незамкнутую электронную оболочку и вести себя в основном состоянии как триплетный бирадикал. В табл. 2.6.4 показаны моноцпклические ионы, для которых  те ионы, которые удалось получить и охарактеризовать (в ряде случаев — в виде замещенных производных), выделены жирной линией контура [72].
те ионы, которые удалось получить и охарактеризовать (в ряде случаев — в виде замещенных производных), выделены жирной линией контура [72].
Таблица 2.6.4. Моноциклические ароматические и антиароматические ионы

Простейшая  -злектронная система, циклопропенил-катион
-злектронная система, циклопропенил-катион
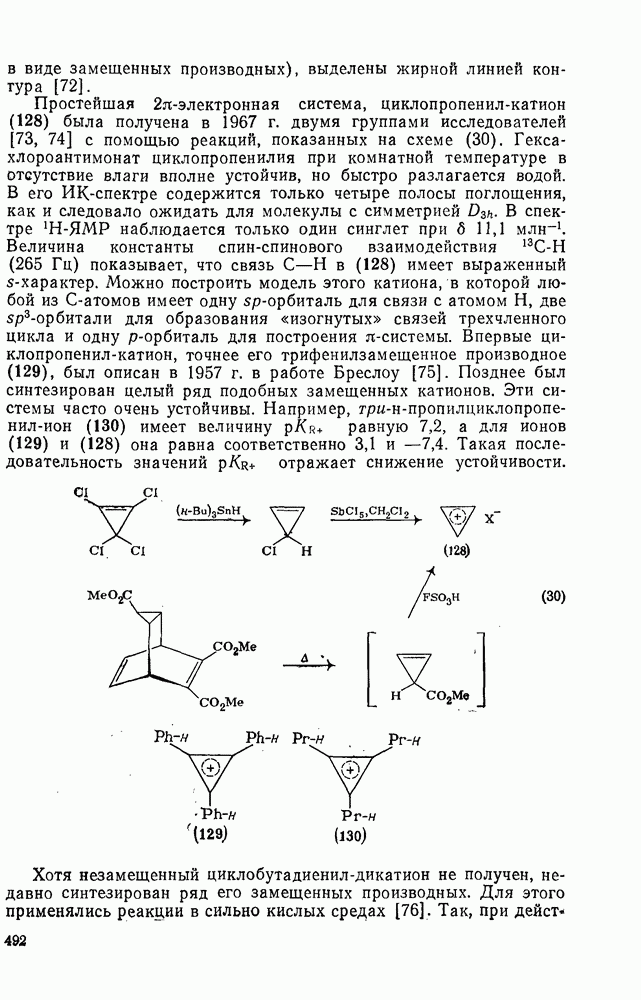
(128) была получена в 1967 г. двумя группами исследователей [73, 74] с помощью реакций, показанных на схеме (30). Гексахлороантимонат циклопропенилия при комнатной температуре в отсутствие влаги вполне устойчив, но быстро разлагается водой. В его ИК-спектре содержится только четыре полосы поглощения, как и следовало ожидать для молекулы с симметрией  . В спектре
. В спектре  -ЯМР наблюдается только один синглет при
-ЯМР наблюдается только один синглет при  . Величина константы спин-спинового взаимодействия
. Величина константы спин-спинового взаимодействия  показывает, что связь
показывает, что связь  в (128) имеет выраженный
в (128) имеет выраженный  -характер. Можно построить модель этого катиона, в которой любой из С-атомов имеет одну
-характер. Можно построить модель этого катиона, в которой любой из С-атомов имеет одну  -орбиталь для связи с атомом Н, две
-орбиталь для связи с атомом Н, две  -орбитали для образования «изогнутых» связей трехчленного цикла и одну р-орбиталь для построения
-орбитали для образования «изогнутых» связей трехчленного цикла и одну р-орбиталь для построения  -системы. Впервые циклопропенил-катион, точнее его трифенилзамещенное производное (129), был описан в 1957 г. в работе Бреслоу [75]. Позднее был синтезирован целый ряд подобных замещенных катионов. Эти системы часто очень устойчивы. Например, три-н-пропилциклопропенил-ион (130) имеет величину
-системы. Впервые циклопропенил-катион, точнее его трифенилзамещенное производное (129), был описан в 1957 г. в работе Бреслоу [75]. Позднее был синтезирован целый ряд подобных замещенных катионов. Эти системы часто очень устойчивы. Например, три-н-пропилциклопропенил-ион (130) имеет величину  равную 7,2, а для ионов (129) и (128) она равна соответственно 3,1
равную 7,2, а для ионов (129) и (128) она равна соответственно 3,1  . Такая последовательность значений
. Такая последовательность значений  отражает снижение устойчивости.
отражает снижение устойчивости.

Хотя незамещенный циклобутадиенил-дикатион не получен, недавно синтезирован ряд его замещенных производных. Для этого применялись реакции в сильно кислых средах  . Так, при действии на дибромид (131) пентафторидом сурьмы в жидком
. Так, при действии на дибромид (131) пентафторидом сурьмы в жидком  при
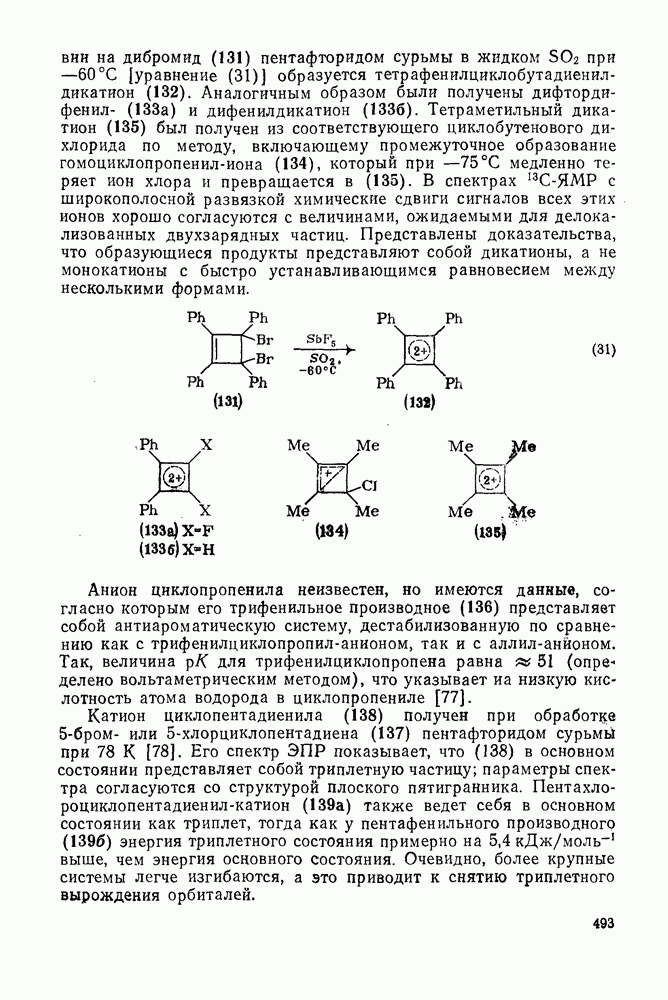
при  [уравнение (31)] образуется тетрафенилциклобутадиенил-дикатион (132).
[уравнение (31)] образуется тетрафенилциклобутадиенил-дикатион (132).
Аналогичным образом были получены дифторди-фенил- (133а) и дифенилдикатион (1336). Тетраметильный дикатион (135) был получен из соответствующего циклобутенового дихлорида по методу, включающему промежуточное образование гомоциклопропенил-иона (134), который при  медленно теряет ион хлора и превращается в (135). В спектрах
медленно теряет ион хлора и превращается в (135). В спектрах  -ЯМР с широкополосной развязкой химические сдвиги сигналов всех этих ионов хорошо согласуются с величинами, ожидаемыми для делока-лизованных двухзарядных частиц. Представлены доказательства, что образующиеся продукты представляют собой дикатионы, а не монокатионы с быстро устанавливающимся равновесием между несколькими формами.
-ЯМР с широкополосной развязкой химические сдвиги сигналов всех этих ионов хорошо согласуются с величинами, ожидаемыми для делока-лизованных двухзарядных частиц. Представлены доказательства, что образующиеся продукты представляют собой дикатионы, а не монокатионы с быстро устанавливающимся равновесием между несколькими формами.

Анион циклопропенила неизвестен, но имеются данные, согласно которым его трифенильное производное (136) представляет собой антиароматическую систему, дестабилизованную по сравнению как с трифенилциклопропил-анионом, так и с аллил-анионом. Так, величина  для трифенилциклопропена равна
для трифенилциклопропена равна  (определено вольтаметрическим методом), что указывает на низкую кислотность атома водорода в циклопропениле [77].
(определено вольтаметрическим методом), что указывает на низкую кислотность атома водорода в циклопропениле [77].
Катион циклопентадиенила (138) получен при обработке  -бром- или
-бром- или  -хлорциклопентадиена (137) пентафторидом сурьмк при 78 К [78]. Его спектр ЭПР показывает, что (138) в основном состоянии представляет собой триплетную частицу; параметры спектра согласуются со структурой плоского пятигранника. Пентахлороциклопентадиенил-катион (139а) также ведет себя в основном состоянии как триплет, тогда как у пентафен ильного производного (1396) энергия триплетного состояния примерно на
-хлорциклопентадиена (137) пентафторидом сурьмк при 78 К [78]. Его спектр ЭПР показывает, что (138) в основном состоянии представляет собой триплетную частицу; параметры спектра согласуются со структурой плоского пятигранника. Пентахлороциклопентадиенил-катион (139а) также ведет себя в основном состоянии как триплет, тогда как у пентафен ильного производного (1396) энергия триплетного состояния примерно на  выше, чем энергия основного состояния. Очевидно, более крупные системы легче изгибаются, а это приводит к снятию триплетного вырождения орбиталей.
выше, чем энергия основного состояния. Очевидно, более крупные системы легче изгибаются, а это приводит к снятию триплетного вырождения орбиталей.

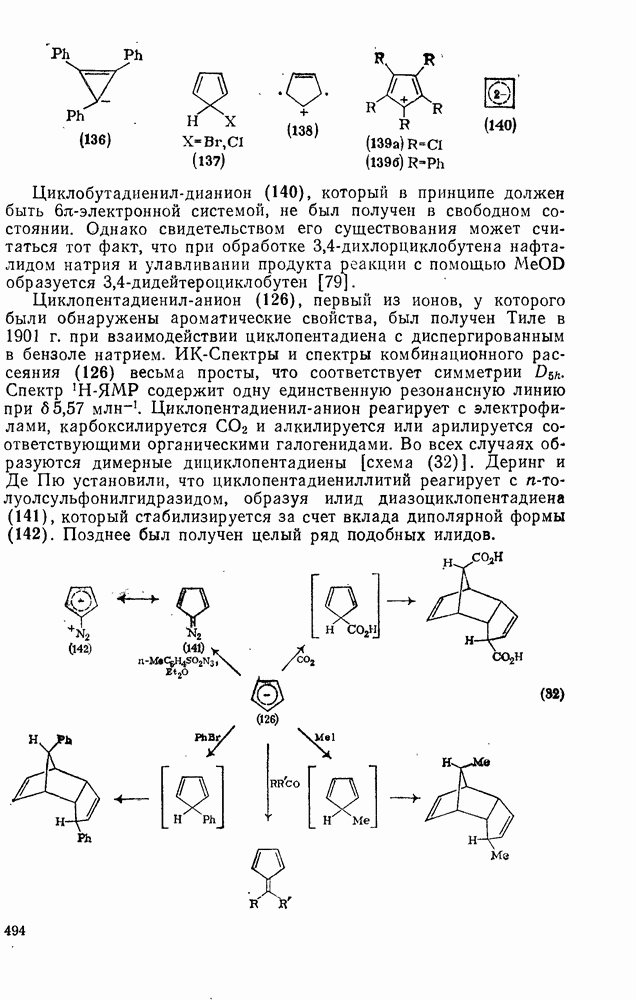
Циклобутадиенил-дианион (140), который в принципе должен быть  -электронной системой, не был получен в свободном состоянии. Однако свидетельством его существования может считаться тот факт, что при обработке
-электронной системой, не был получен в свободном состоянии. Однако свидетельством его существования может считаться тот факт, что при обработке  -дихлорциклобутена нафталидом натрия и улавливании продукта реакции с помощью
-дихлорциклобутена нафталидом натрия и улавливании продукта реакции с помощью  образуется
образуется  -дидейтероциклобутен [79].
-дидейтероциклобутен [79].
Циклопентадиенил-анион (126), первый из ионов, у которого были обнаружены ароматические свойства, был получен Тиле в 1901 г. при взаимодействии циклопентадиена с диспергированным в бензоле натрием. ИК-Спектры и спектры комбинационного рассеяния (126) весьма просты, что соответствует симметрии  . Спектр
. Спектр  -ЯМР содержит одну единственную резонансную линию при
-ЯМР содержит одну единственную резонансную линию при  . Циклопентадиенил-анион реагирует с электрофилами, карбоксилируется
. Циклопентадиенил-анион реагирует с электрофилами, карбоксилируется  и алкилируется или арилируется соответствующими органическими галогенидами. Во всех случаях образуются димерные дициклопентадиены [схема (32)]. Деринг и Де Пю установили, что циклопентадиениллитий реагирует с n-толуолсульфонилгидразидом, образуя илид диазоциклопентадиеиа (141), который стабилизируется за счет вклада диполярной формы (142). Позднее был получен целый ряд подобных илидов.
и алкилируется или арилируется соответствующими органическими галогенидами. Во всех случаях образуются димерные дициклопентадиены [схема (32)]. Деринг и Де Пю установили, что циклопентадиениллитий реагирует с n-толуолсульфонилгидразидом, образуя илид диазоциклопентадиеиа (141), который стабилизируется за счет вклада диполярной формы (142). Позднее был получен целый ряд подобных илидов.

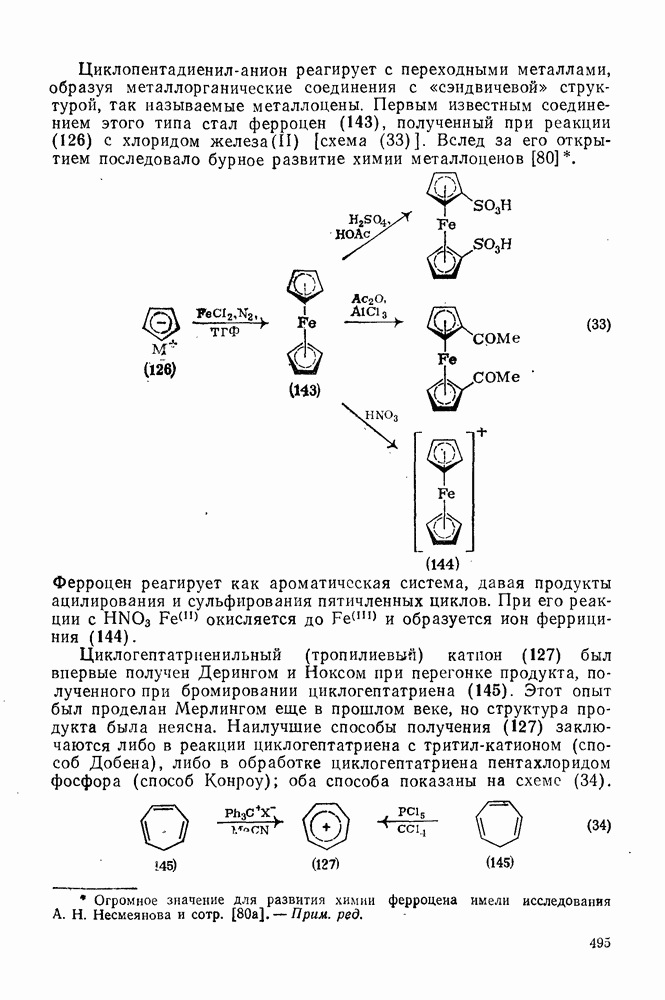
Циклопентадиенил-анион реагирует с переходными металлами, образуя металлорганические соединения с «сэндвичевой» структурой, так называемые металлоцены. Первым известным соединением этого типа стал ферроцен (143), полученный при реакции (126) с хлоридом железа(II) [схема (33)]. Вслед за его открытием последовало бурное развитие химии металлоценов  .
.

Ферроцен реагирует как ароматическая система, давая продукты ацилирования и сульфирования пятичленных циклов. При его реакции с  окисляется до
окисляется до  и образуется ион феррициния (144).
и образуется ион феррициния (144).
Циклогептатриенильный (тропилиевый) катион (127) был впервые получен Дерингом и Ноксом при перегонке продукта, полученного при бромировании циклогептатриена (145). Этот опыт был проделан Мерлингом еще в прошлом веке, но структура продукта была неясна. Наилучшие способы получения (127) заключаются либо в реакции циклогептатриена с тритилкатионом (способ Добена), либо в обработке циклогептатриена пентахлоридом фосфора (способ Конроу); оба способа показаны на схеме (34).

ИК-Спектр и спектр комбинационного рассеяния тропилий-катиона соответствуют ожидаемым для соединений с симметрией  , причем линии в ИК-спектре и в спектре КР не совпадают. В спектре
, причем линии в ИК-спектре и в спектре КР не совпадают. В спектре  -ЯМР наблюдается один синглет при
-ЯМР наблюдается один синглет при  , а максимум в электронном спектре поглощения приходится на 275 нм. По своей кислотности
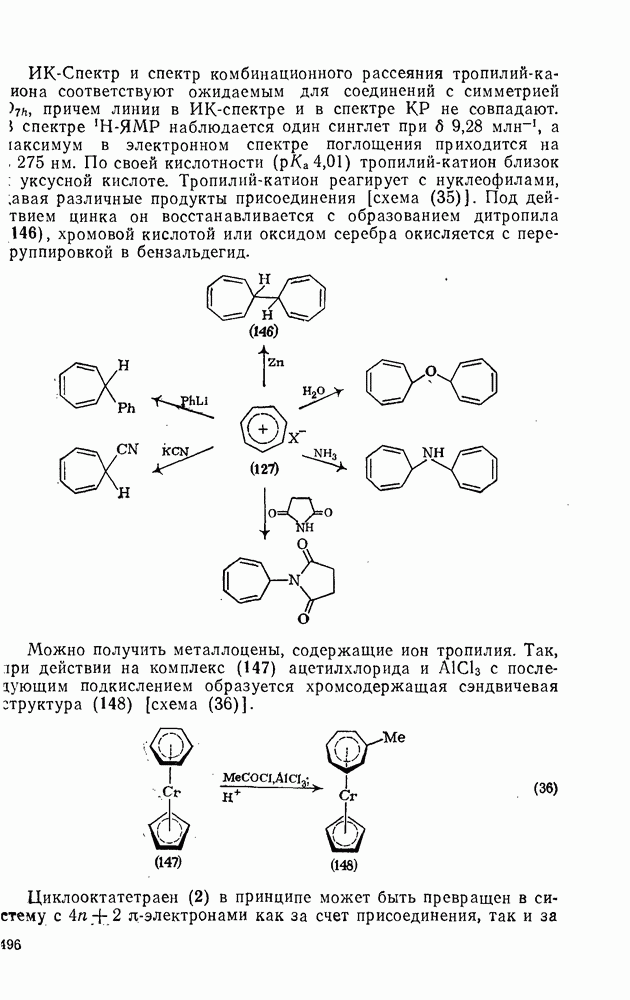
, а максимум в электронном спектре поглощения приходится на 275 нм. По своей кислотности  тропилий-катион близок к уксусной кислоте. Тропилий-катион реагирует с нуклеофилами, ,давая различные продукты присоединения [схема (35)]. Под действием цинка он восстанавливается с образованием дитропила (146), хромовой кислотой или оксидом серебра окисляется с перегруппировкой в бензальдегид.
тропилий-катион близок к уксусной кислоте. Тропилий-катион реагирует с нуклеофилами, ,давая различные продукты присоединения [схема (35)]. Под действием цинка он восстанавливается с образованием дитропила (146), хромовой кислотой или оксидом серебра окисляется с перегруппировкой в бензальдегид.

Можно получить металлоцены, содержащие ион тропилия. Так, при действии на комплекс (147) ацетилхлорида и  с последующим подкислением образуется хромсодержащая сэндвичевая структура (148) [схема (36)].
с последующим подкислением образуется хромсодержащая сэндвичевая структура (148) [схема (36)].

Циклооктатетраен (2) в принципе может быть превращен в систему с  -электронами как за счет присоединения, так и за счет удаления двух
-электронами как за счет присоединения, так и за счет удаления двух  -электронов.
-электронов.
Циклооктатетраенил-дикатион имеет  -электронов на трех связывающих орбиталях, а цикло-октатетраенилдианион
-электронов на трех связывающих орбиталях, а цикло-октатетраенилдианион  -электронов, расположенных на трех связывающих и двух несвязывающих орбиталях. Циклооктатетраен (2) с большей легкостью образует катион гомотропилия, нежели циклооктатетраенил-дикатион. Однако при реакции
-электронов, расположенных на трех связывающих и двух несвязывающих орбиталях. Циклооктатетраен (2) с большей легкостью образует катион гомотропилия, нежели циклооктатетраенил-дикатион. Однако при реакции  -тетра-метилциклооктатетраена (149) с
-тетра-метилциклооктатетраена (149) с  в
в  при
при  образуется дикатион
образуется дикатион  [81]. Спектр
[81]. Спектр  -ЯМР содержит сигналы с
-ЯМР содержит сигналы с  4,27 и
4,27 и  , соответствующие протонам метильных групп и кольца. В спектре
, соответствующие протонам метильных групп и кольца. В спектре  -ЯМР с широкополосной развязкой атомы углерода, входящие в цикл, резонируют при
-ЯМР с широкополосной развязкой атомы углерода, входящие в цикл, резонируют при  182,7 (
182,7 ( ) и
) и  . При повышении температуры до
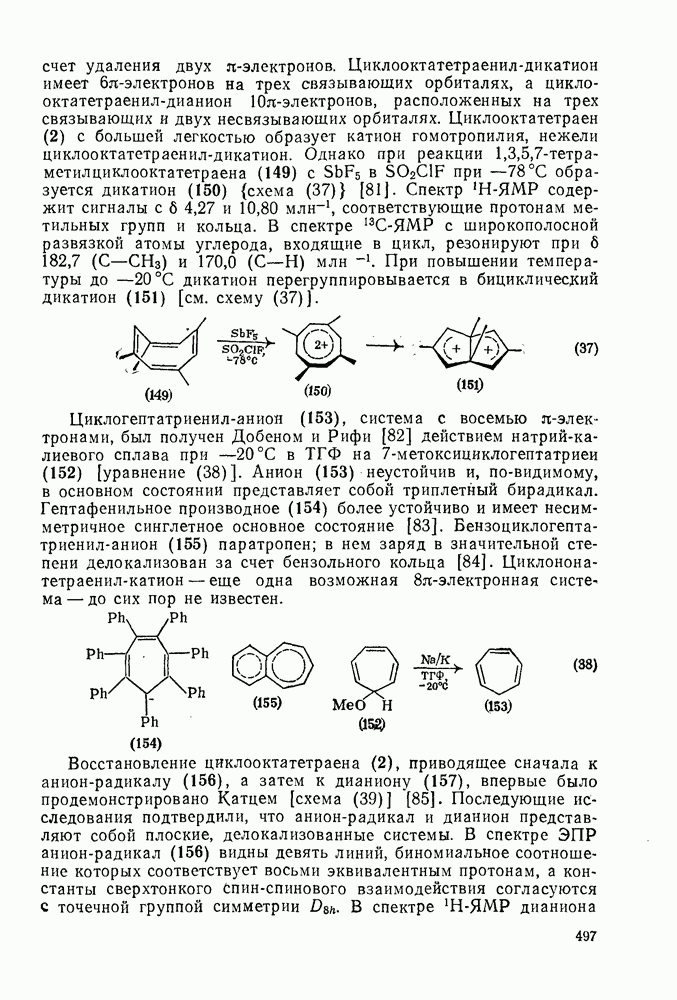
. При повышении температуры до  дикатион перегруппировывается в бицикличесдий дикатион (151) [см. схему (37)].
дикатион перегруппировывается в бицикличесдий дикатион (151) [см. схему (37)].

Циклогептатриенил-анион (153), система с восемью  -электронами, был получен Добеном и Рифи [82] действием натрий-калиевого сплава при
-электронами, был получен Добеном и Рифи [82] действием натрий-калиевого сплава при  в ТГФ на 7-метоксициклогептатриеи (152) [уравнение (38)]. Анион (153) неустойчив и, по-видимому, в основном состоянии представляет собой триплетный бирадикал. Гептафенильное производное (154) более устойчиво и имеет несимметричное синглетное основное состояние [83]. Бензоциклогептатриенил-анион (155) паратропен; в нем заряд в значительной степени делокализован за счет бензольного кольца [84]. Циклононатетраенил-катион — еще одна возможная
в ТГФ на 7-метоксициклогептатриеи (152) [уравнение (38)]. Анион (153) неустойчив и, по-видимому, в основном состоянии представляет собой триплетный бирадикал. Гептафенильное производное (154) более устойчиво и имеет несимметричное синглетное основное состояние [83]. Бензоциклогептатриенил-анион (155) паратропен; в нем заряд в значительной степени делокализован за счет бензольного кольца [84]. Циклононатетраенил-катион — еще одна возможная  -электронная система — до сих пор не известен.
-электронная система — до сих пор не известен.

Восстановление циклооктатетраена (2), приводящее сначала к анион-радикалу (156), а затем к дианиону (157), впервые было продемонстрировано Катцем [схема (39)] [85]. Последующие исследования подтвердили, что анион-радикал и дианион представляют собой плоские, делокализованные системы. В спектре ЭПР анион-радикал (156) видны девять линий, биномиальное соотношение которых соответствует восьми эквивалентным протонам, а константы сверхтонкого спин-спинового взаимодействия согласуются с точечной группой симметрии  .
.
В спектре  -ЯМР дианиона (157) наблюдается синглет (
-ЯМР дианиона (157) наблюдается синглет ( 5,7
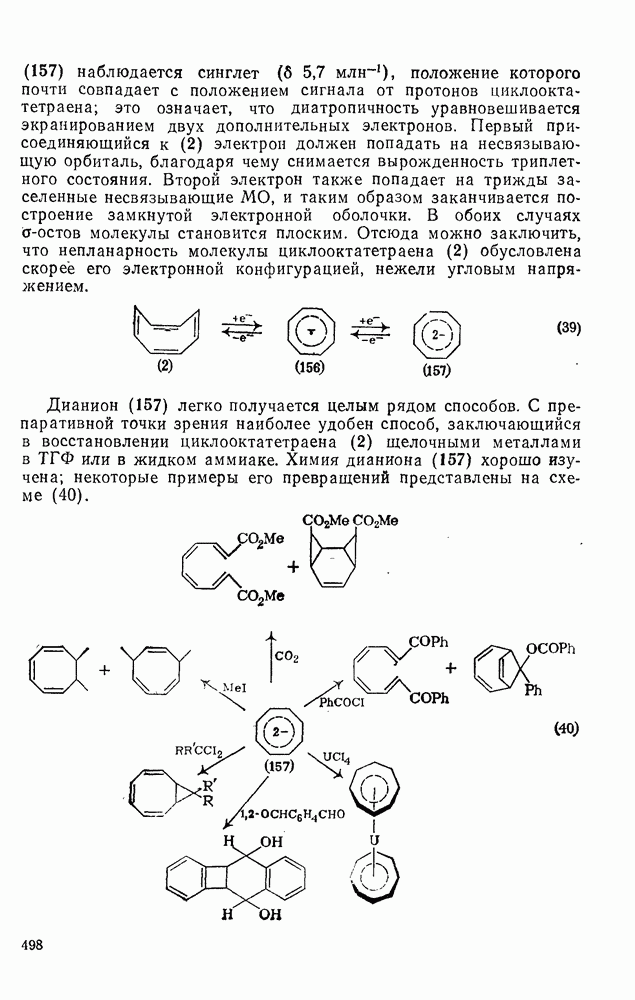
5,7  ), положение которого почти совпадает с положением сигнала от протонов циклооктатетраена; это означает, что диатропичность уравновешивается экранированием двух дополнительных электронов. Первый присоединяющийся к (2) электрон должен попадать на несвязывающую орбиталь, благодаря чему снимается вырожденность триплетного состояния. Второй электрон также попадает на трижды заселенные несвязывающие МО, и таким образом заканчивается построение замкнутой электронной оболочки. В обоих случаях
), положение которого почти совпадает с положением сигнала от протонов циклооктатетраена; это означает, что диатропичность уравновешивается экранированием двух дополнительных электронов. Первый присоединяющийся к (2) электрон должен попадать на несвязывающую орбиталь, благодаря чему снимается вырожденность триплетного состояния. Второй электрон также попадает на трижды заселенные несвязывающие МО, и таким образом заканчивается построение замкнутой электронной оболочки. В обоих случаях  -остов молекулы становится плоским. Отсюда можно заключить, что непланарность молекулы циклооктатетраена (2) обусловлена скорее его электронной конфигурацией, нежели угловым напряжением.
-остов молекулы становится плоским. Отсюда можно заключить, что непланарность молекулы циклооктатетраена (2) обусловлена скорее его электронной конфигурацией, нежели угловым напряжением.

Дианион (157) легко получается целым рядом способов. С препаративной точки зрения наиболее удобен способ, заключающийся в восстановлении циклооктатетраена (2) щелочными металлами в ТГФ или в жидком аммиаке. Химия дианиона (157) хорошо изучена; некоторые примеры его превращений представлены на схеме (40).

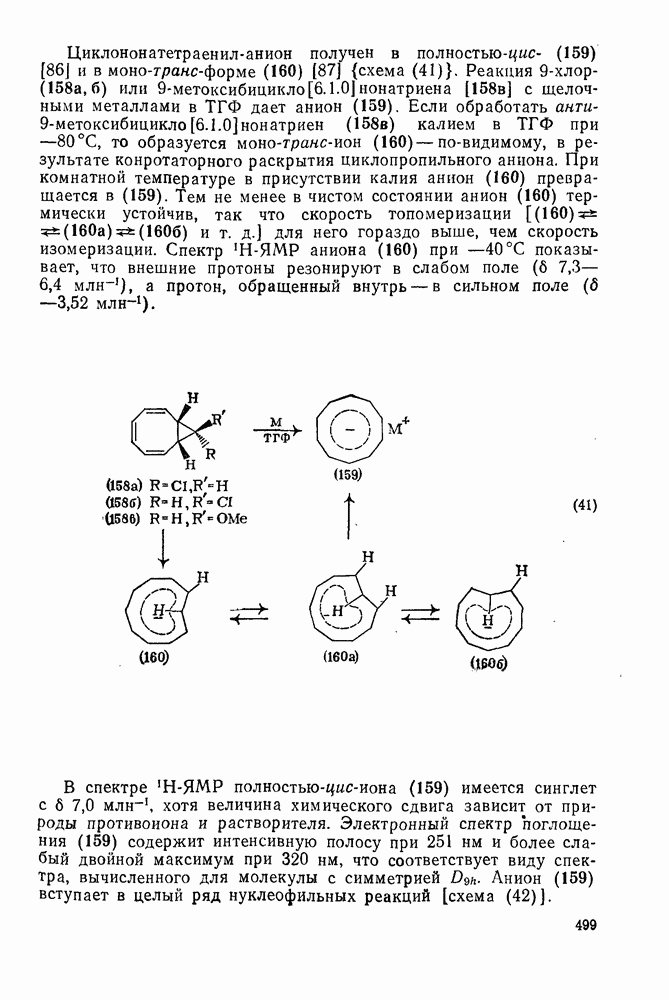
Циклононатетраенил-анион получен в  и в моно-транс-форме (160)
и в моно-транс-форме (160)  . Реакция
. Реакция  (158а,б) или
(158а,б) или  нонатриена [158в] с щелочными металлами в ТГФ дает анион (159). Если обработать
нонатриена [158в] с щелочными металлами в ТГФ дает анион (159). Если обработать  (158в) калием в ТГФ при
(158в) калием в ТГФ при  , то образуется моно-транс-ион (160) — по-видимому, в результате конротаторного раскрытия циклопропильного аниона. При комнатной температуре в присутствии калия анион (160) превращается в (159). Тем не менее в чистом состоянии анион (160) термически устойчив, так что скорость топомеризации ((160а) (160б) и т. д.) для него гораздо выше, чем скорость изомеризации. Спектр
, то образуется моно-транс-ион (160) — по-видимому, в результате конротаторного раскрытия циклопропильного аниона. При комнатной температуре в присутствии калия анион (160) превращается в (159). Тем не менее в чистом состоянии анион (160) термически устойчив, так что скорость топомеризации ((160а) (160б) и т. д.) для него гораздо выше, чем скорость изомеризации. Спектр  -ЯМР аниона (160) при
-ЯМР аниона (160) при  показывает, что внешние протоны резонируют в слабом поле (
показывает, что внешние протоны резонируют в слабом поле ( ), а протон, обращенный внутрь — в сильном поле (
), а протон, обращенный внутрь — в сильном поле ( —3,52
—3,52  ).
).

В спектре Н-ЯМР полностью цис-иона (159) имеется синглет  , хотя величина химического сдвига зависит от природы противоиона и растворителя. Электронный спектр поглощения (159) содержит интенсивную полосу при 251 нм и более слабый двойной максимум при 320 нм, что соответствует виду спектра, вычисленного для молекулы с симметрией
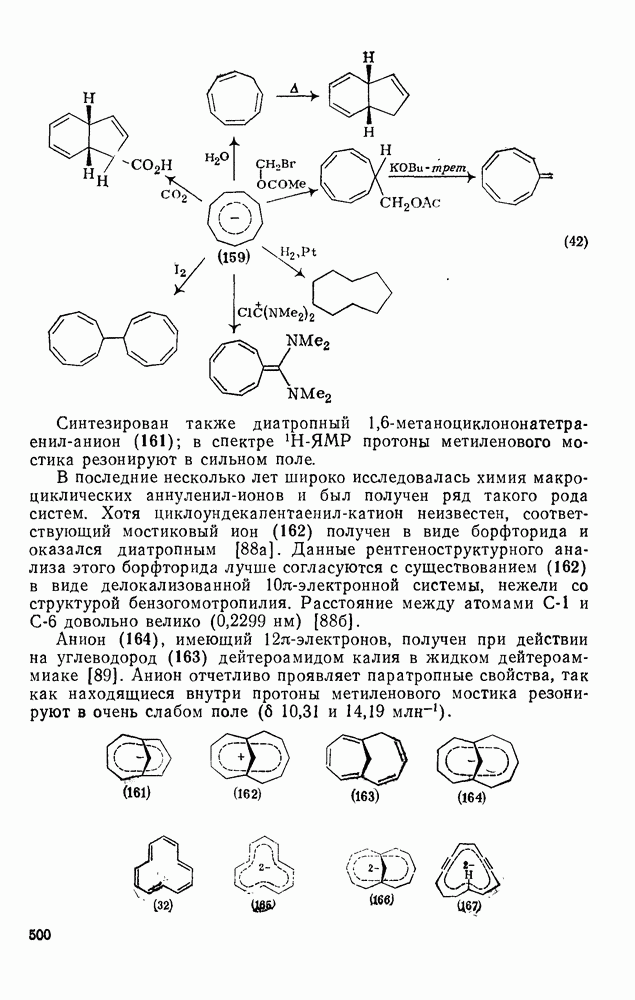
, хотя величина химического сдвига зависит от природы противоиона и растворителя. Электронный спектр поглощения (159) содержит интенсивную полосу при 251 нм и более слабый двойной максимум при 320 нм, что соответствует виду спектра, вычисленного для молекулы с симметрией  . Анион (159) вступает в целый ряд нуклеофильных реакций [схема (42)].
. Анион (159) вступает в целый ряд нуклеофильных реакций [схема (42)].

Синтезирован также диатропный 1,6-метаноциклононатетра-енил-анион (161); в спектре  -ЯМР протоны метиленового мостика резонируют в сильном поле.
-ЯМР протоны метиленового мостика резонируют в сильном поле.
В последние несколько лет широко исследовалась химия макроциклических аннуленил-ионов и был получен ряд такого рода систем. Хотя циклоундекапентаенил-катион неизвестен, соответствующий мостиковый ион (162) получен в виде борфторида и оказался диатропным [88а]. Данные рентгеноструктурного анализа этого борфторида лучше согласуются с существованием (162) в виде делокализованной  -электронной системы, нежели со структурой бензогомотропилия. Расстояние между атомами
-электронной системы, нежели со структурой бензогомотропилия. Расстояние между атомами  и
и  довольно велико (0,2299 нм) [886].
довольно велико (0,2299 нм) [886].
Анион (164), имеющий  -электронов, получен при действии на углеводород (163) дейтероамидом калия в жидком дейтероаммиаке [89]. Анион отчетливо проявляет паратропные свойства, так как находящиеся внутри протоны метиленового мостика резонируют в очень слабом поле (
-электронов, получен при действии на углеводород (163) дейтероамидом калия в жидком дейтероаммиаке [89]. Анион отчетливо проявляет паратропные свойства, так как находящиеся внутри протоны метиленового мостика резонируют в очень слабом поле ( 10,31 и 14,19
10,31 и 14,19  ).
).

Чрезвычайно неустойчивый [12] аннулен (32) может быть полярографически или действием щелочных металлов восстановлен в содержащий  -электронов
-электронов  -дианион (165), представляющий собой устойчивую, диатропную систему [90]. Спектр
-дианион (165), представляющий собой устойчивую, диатропную систему [90]. Спектр  -ЯМР дианиона содержит три сигнала (
-ЯМР дианиона содержит три сигнала ( 6,98; 6,23; -4,6
6,98; 6,23; -4,6  ) и не зависит от температуры. Это означает, что в дианионе (165) не происходит обмена между протонами, находящимися во внешнем и внутреннем положении. Такое поведение контрастирует с поведением [12] аннулена (32), где подобный обмен проходит быстро.
) и не зависит от температуры. Это означает, что в дианионе (165) не происходит обмена между протонами, находящимися во внешнем и внутреннем положении. Такое поведение контрастирует с поведением [12] аннулена (32), где подобный обмен проходит быстро.
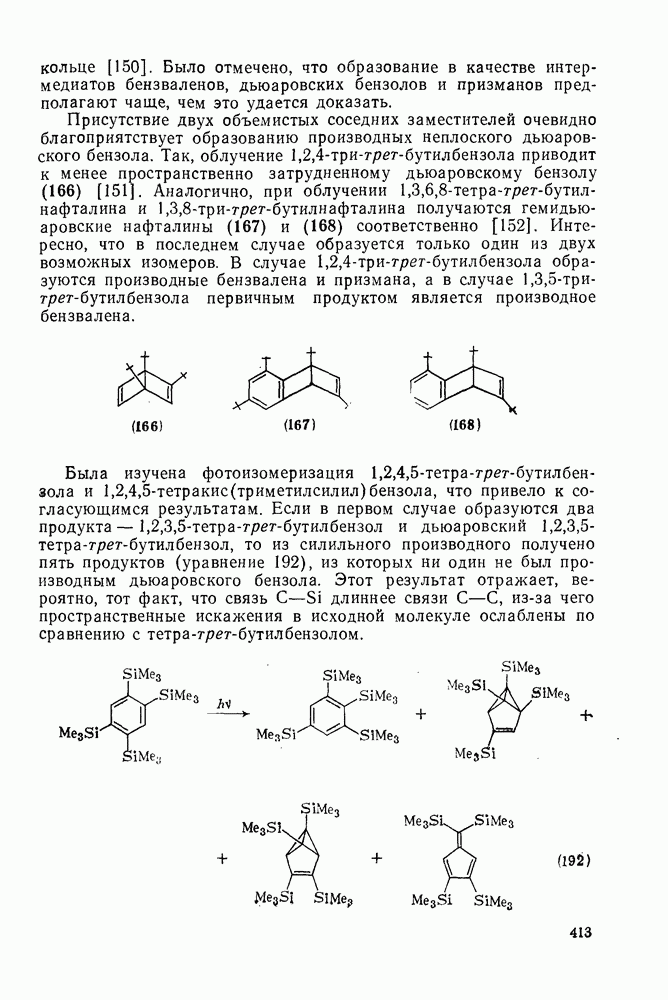
Мостиковые [12] аннуленил-дианионы типа (166) [91а] или дегидро [12] аннуленил-дианионы типа (167) [916] получены из соответствующих аннуленов. Паратропный характер исходных систем полностью исчезает в сильно диатропных дианионах. В спектрах  -ЯМР ионов (166) и (167) протоны метиленового мостика и протон, направленный внутрь цикла, резонируют соответственно при
-ЯМР ионов (166) и (167) протоны метиленового мостика и протон, направленный внутрь цикла, резонируют соответственно при  и
и  .
.
Реакция транс- с металлическим калием сначала дает анион-радикал, а затем паратропный дианион с
с металлическим калием сначала дает анион-радикал, а затем паратропный дианион с  -электронами. В спектре
-электронами. В спектре  -ЯМР дианиона протоны находящихся внутри кольца метальных групп резонируют в очень слабом поле (
-ЯМР дианиона протоны находящихся внутри кольца метальных групп резонируют в очень слабом поле ( 21,0
21,0  ), что чрезвычайно резко отличается от спектра (14), где соответствующие протоны
), что чрезвычайно резко отличается от спектра (14), где соответствующие протоны  -групп наблюдаются при
-групп наблюдаются при  [92а]. Аналогичным образом
[92а]. Аналогичным образом  -пропандиилиден [14] аннулен (44) превращается в соответствующий паратропный дианион [926].
-пропандиилиден [14] аннулен (44) превращается в соответствующий паратропный дианион [926].
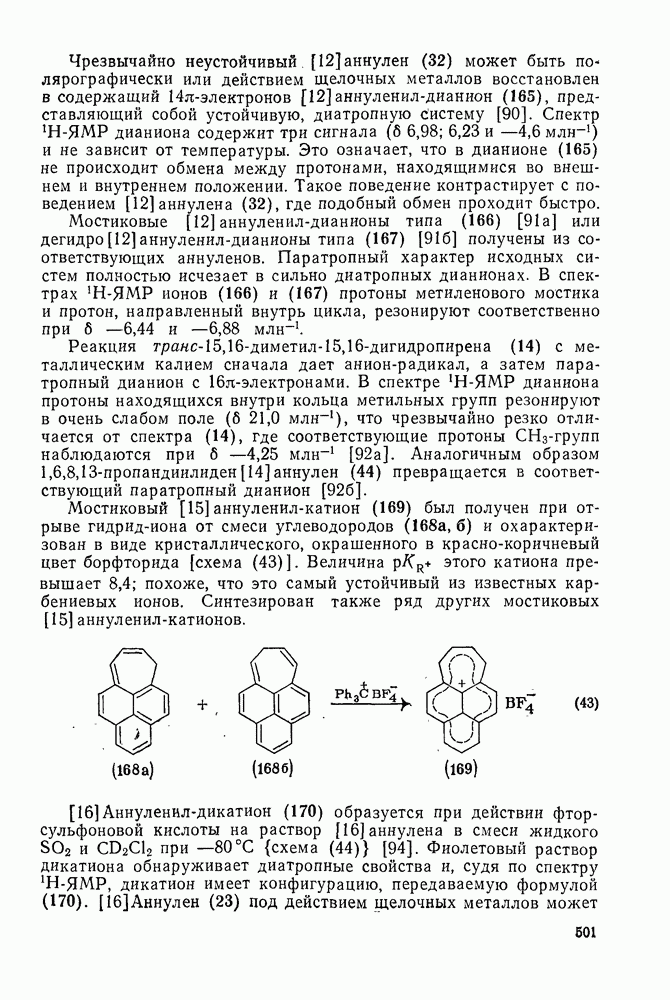
Мостиковый [15] аннуленил-катион (169) был получен при отрыве гидрид-иона от смеси углеводородов (168а, б) и охарактеризован в виде кристаллического, окрашенного в красно-коричневый цвет борфторида [схема (43)]. Величина рэтого катиона превышает 8,4; похоже, что это самый устойчивый из известных карбениевых ионов. Синтезирован также ряд других мостиковых

[16] Аннуленил-дикатион (170) образуется при действии фторсульфоновой кислоты на раствор [16] аннулена в смеси жидкого  и
и  при
при  [94]. Фиолетовый раствор дикатиона обнаруживает диатропные свойства и, судя по спектру
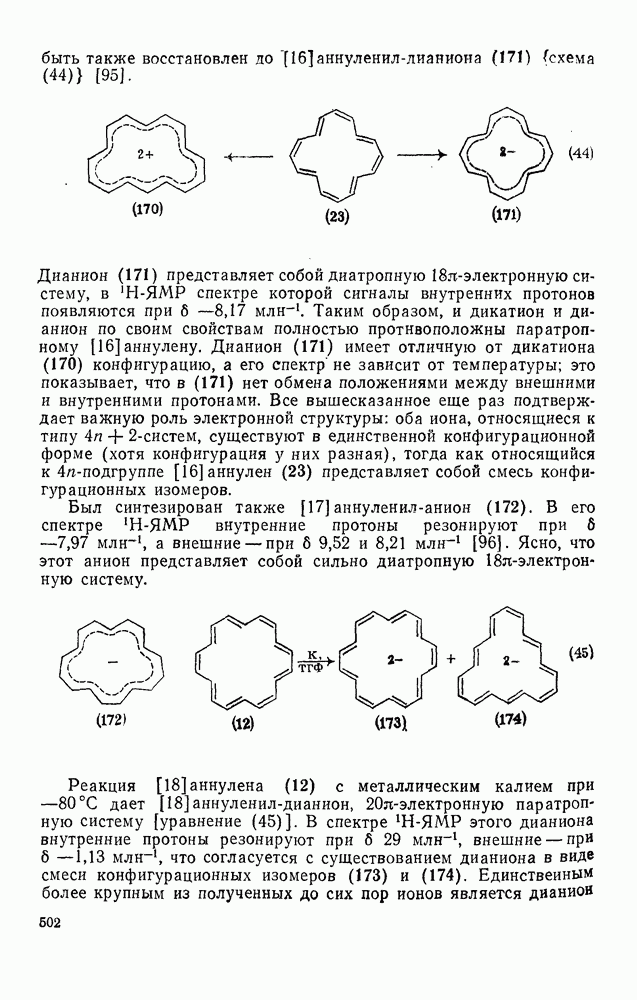
[94]. Фиолетовый раствор дикатиона обнаруживает диатропные свойства и, судя по спектру  -ЯМР, дикатион имеет конфигурацию, передаваемую формулой (170). [16] Аннулен (23) под действием щелочных металлов может быть также восстановлен до [16]-аннулен-лианиона (171) (схема 44) [95].
-ЯМР, дикатион имеет конфигурацию, передаваемую формулой (170). [16] Аннулен (23) под действием щелочных металлов может быть также восстановлен до [16]-аннулен-лианиона (171) (схема 44) [95].

Дианион (171) представляет собой диатропную  -электронную систему, в
-электронную систему, в  -ЯМР спектре которой сигналы внутренних протонов появляются при
-ЯМР спектре которой сигналы внутренних протонов появляются при  . Таким образом, и дикатион и дианион по своим свойствам полностью противоположны паратропному
. Таким образом, и дикатион и дианион по своим свойствам полностью противоположны паратропному  . Дианион (171) имеет отличную от дикатиона (170) конфигурацию, а его спектр не зависит от температуры; это показывает, что в (171) нет обмена положениями между внешними и внутренними протонами. Все вышесказанное еще раз подтверждает важную роль электронной структуры: оба иона, относящиеся к типу
. Дианион (171) имеет отличную от дикатиона (170) конфигурацию, а его спектр не зависит от температуры; это показывает, что в (171) нет обмена положениями между внешними и внутренними протонами. Все вышесказанное еще раз подтверждает важную роль электронной структуры: оба иона, относящиеся к типу 
 -систем, существуют в единственной конфигурационной форме (хотя конфигурация у них разная), тогда как относящийся к
-систем, существуют в единственной конфигурационной форме (хотя конфигурация у них разная), тогда как относящийся к  -подгруппе [16] аннулен (23) представляет собой смесь конфигурационных изомеров.
-подгруппе [16] аннулен (23) представляет собой смесь конфигурационных изомеров.
Был синтезирован также [17] аинуленил-анион (172). В его спектре  -ЯМР внутренние протоны резонируют при
-ЯМР внутренние протоны резонируют при  , а внешние — при
, а внешние — при  9,52 и
9,52 и  [96]. Ясно, что этот анион представляет собой сильно диатропную
[96]. Ясно, что этот анион представляет собой сильно диатропную  -электрон-ную систему.
-электрон-ную систему.

Реакция [18] аннулена (12) с металлическим калием при  дает [18] аннуленил-дианион,
дает [18] аннуленил-дианион,  -электронную паратропную систему [уравнение (45)]. В спектре
-электронную паратропную систему [уравнение (45)]. В спектре  -ЯМР этого дианиона внутренние протоны резонируют при
-ЯМР этого дианиона внутренние протоны резонируют при  , внешние — при
, внешние — при  , что согласуется с существованием дианиона в виде смеси конфигурационных изомеров (173) и (174). Единственным более крупным из полученных до сих пор ионов является дианион (176), полученный из октадегидро [24] аннулена (175) [уравнение (46)]; он, по-видимому, является 26
, что согласуется с существованием дианиона в виде смеси конфигурационных изомеров (173) и (174). Единственным более крупным из полученных до сих пор ионов является дианион (176), полученный из октадегидро [24] аннулена (175) [уравнение (46)]; он, по-видимому, является 26  -электронной системой.
-электронной системой.

В случае аннуленов с большим размером цикла  системы часто существуют в виде смеси конфигурационных изомеров, тогда как соответствующие
системы часто существуют в виде смеси конфигурационных изомеров, тогда как соответствующие  -системы имеют только одну конфигурацию. Это наглядно проявляется при переходе от нейтральной
-системы имеют только одну конфигурацию. Это наглядно проявляется при переходе от нейтральной  -системы к заряженной системе
-системы к заряженной системе  [уравнение (46)] или, наоборот, при переходе от нейтральной
[уравнение (46)] или, наоборот, при переходе от нейтральной  системы к заряженной
системы к заряженной  системе [см. уравнение (45)]. В ионах типа
системе [см. уравнение (45)]. В ионах типа  барьер интерконверсии для обмена положениями между протонами внутри и снаружи цикла выше, чем в нейтральных
барьер интерконверсии для обмена положениями между протонами внутри и снаружи цикла выше, чем в нейтральных  . Это, вероятно, является следствием неудобства локализации заряда в непланарном переходном состоянии. И наоборот, можно ожидать, что энергия планарных
. Это, вероятно, является следствием неудобства локализации заряда в непланарном переходном состоянии. И наоборот, можно ожидать, что энергия планарных  -ионов (которые можно рассматривать как переходные состояния между непланарными формами) должна понизиться за счет делокализации заряда.
-ионов (которые можно рассматривать как переходные состояния между непланарными формами) должна понизиться за счет делокализации заряда.
График зависимости химических сдвигов протонов в спектре  -ЯМР от плотности заряда на атомах углерода имеет линейный вид для всех рассмотренных значений n. Различие в линиях можно объяснить усилением кольцевого тока при увеличении n. Углы наклона прямых для значений n=1, 2, 4 приблизительно параллельны, как этого и следовало ожидать для эффекта, зависящего от плотности заряда. В противоположность этому химические сдвиги в спектрах
-ЯМР от плотности заряда на атомах углерода имеет линейный вид для всех рассмотренных значений n. Различие в линиях можно объяснить усилением кольцевого тока при увеличении n. Углы наклона прямых для значений n=1, 2, 4 приблизительно параллельны, как этого и следовало ожидать для эффекта, зависящего от плотности заряда. В противоположность этому химические сдвиги в спектрах  -ЯМР мало зависят от кольцевого тока. Химические сдвиги здесь отражают только изменение плотности заряда на каждом С-атоме, и потому все циклические ионы могут быть описаны одним общим линейным графиком [736].
-ЯМР мало зависят от кольцевого тока. Химические сдвиги здесь отражают только изменение плотности заряда на каждом С-атоме, и потому все циклические ионы могут быть описаны одним общим линейным графиком [736].
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- ПРЕДИСЛОВИЕ
- ИЗ ПРЕДИСЛОВИЯ К ТОМУ 1 АНГЛИЙСКОГО ИЗДАНИЯ
- ЧАСТЬ I. НОМЕНКЛАТУРА И СТЕРЕОХИМИЯ
- 1.1. ВВЕДЕНИЕ И СТЕРЕОХИМИЯ
- 1.1.2. СИММЕТРИЯ И ХИРАЛЬНОСТЬ
- 1.1.3. ХИМИЧЕСКАЯ ТОПОЛОГИЯ
- 1.1.4. ИЗОМЕРИЯ
- 1.1.4.2. Строение
- 1.1.4.3. Абсолютная конфигурация
- 1.1.4.4. Относительная конфигурация
- 1.1.4.5. Конформация
- 1.1.4.6. Концепция изомерии
- 1.1.5. ТОПИЗМ
- 1.1.5.2. Прохиральность
- 1.1.5.3. Псевдоасимметрия (псевдохиральность)
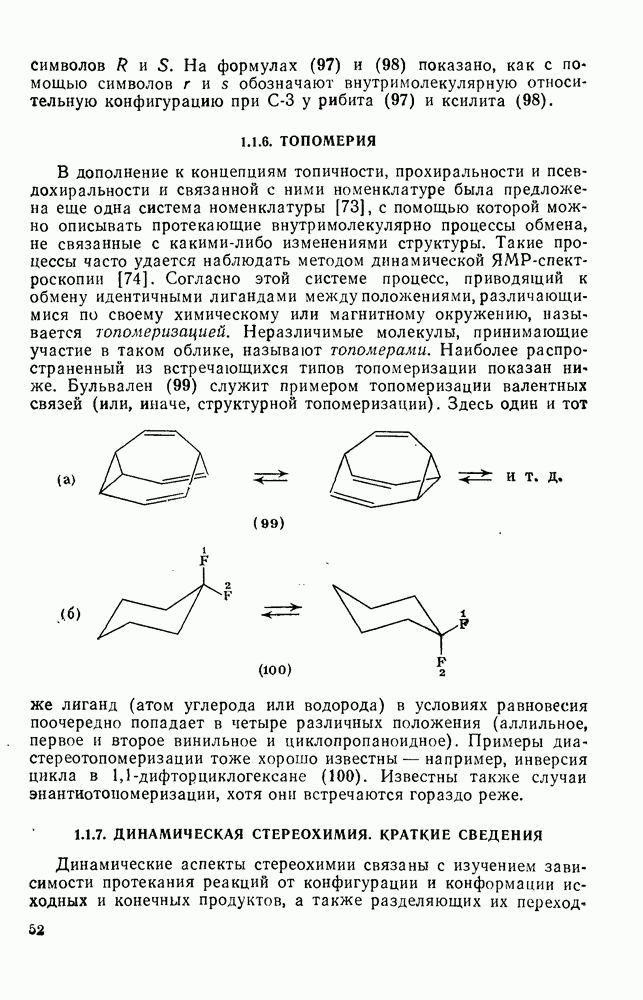
- 1.1.6. ТОПОМЕРИЯ
- 1.1.7. ДИНАМИЧЕСКАЯ СТЕРЕОХИМИЯ. КРАТКИЕ СВЕДЕНИЯ
- ЧАСТЬ 2. УГЛЕВОДОРОДЫ
- 2.1. НАСЫЩЕННЫЕ УГЛЕВОДОРОДЫ
- 2.1.2. Строение и номенклатура
- 2.1.2.1. Номенклатура IUPAC
- 2.1.2.2. Алициклические алканы
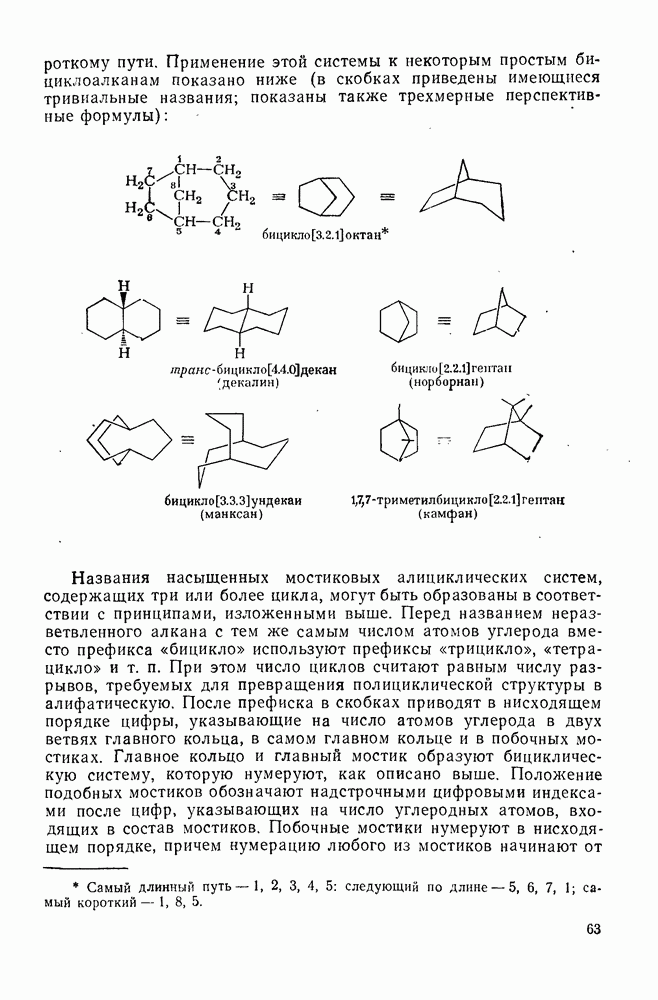
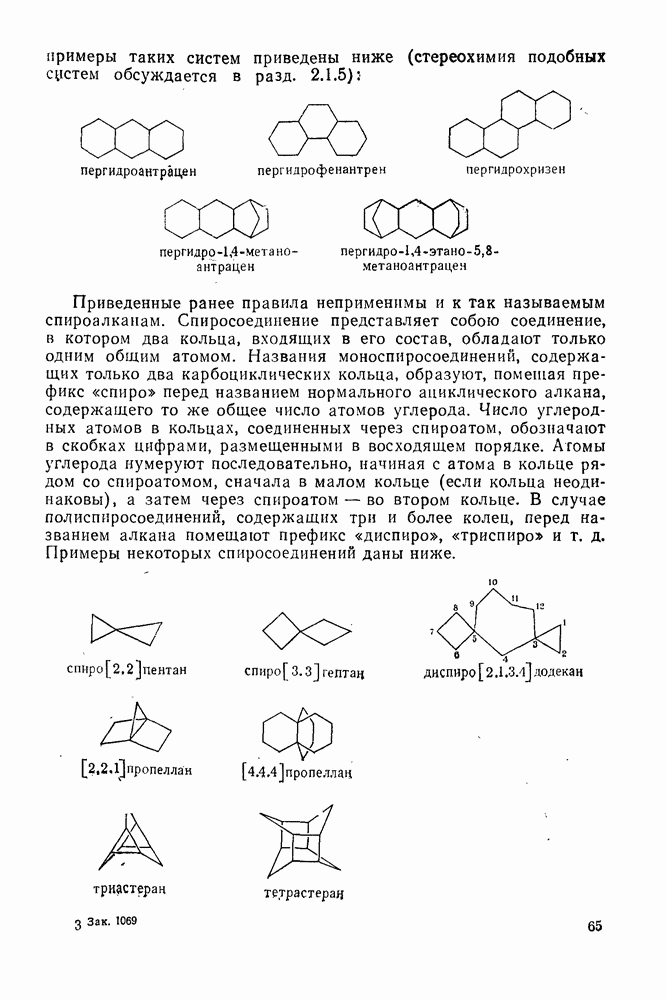
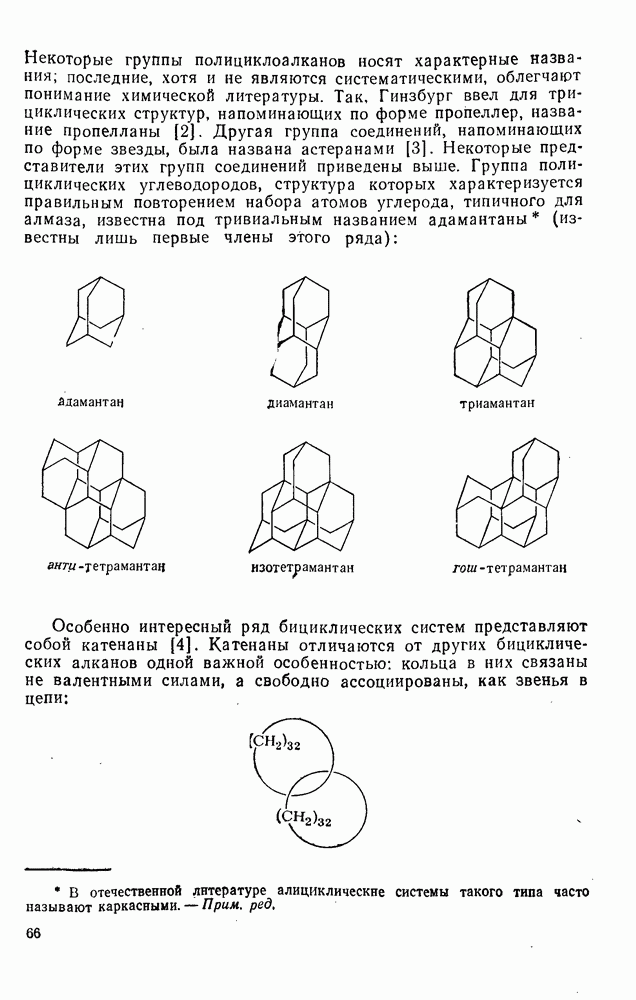
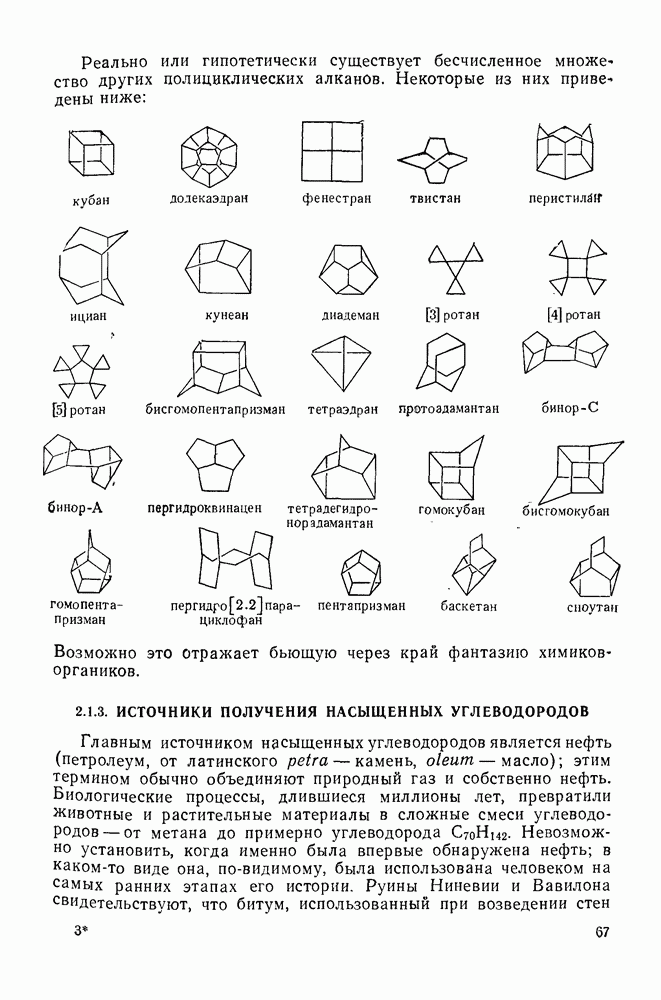
- 2.1.2.3. Полициклоалканы
- 2.1.3. ИСТОЧНИКИ ПОЛУЧЕНИЯ НАСЫЩЕННЫХ УГЛЕВОДОРОДОВ
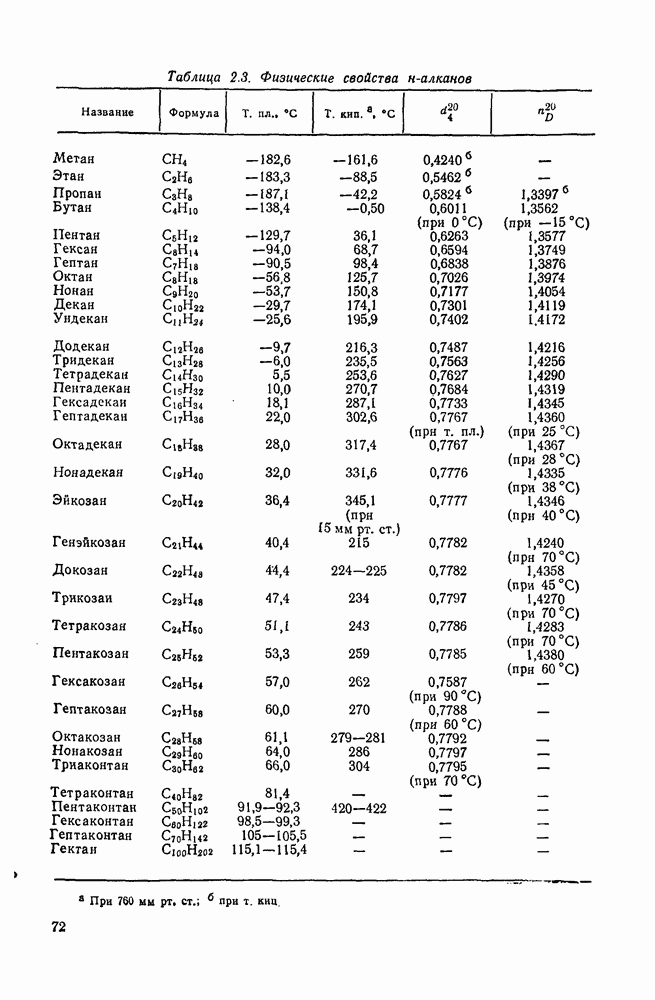
- 2.1.4. ФИЗИЧЕСКИЕ СВОЙСТВА
- 2.1.4.1. Ациклические алканы
- 2.1.4.2. Моно- и полициклоалканы
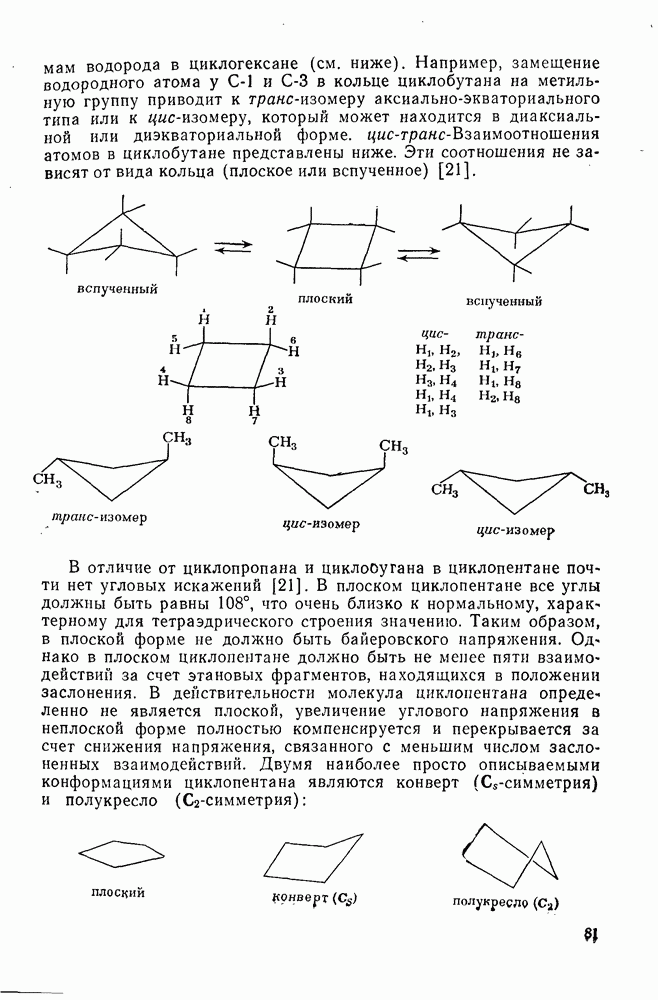
- 2.1.5. СТЕРЕОХИМИЯ И КОНФОРМАЦИОННЫЙ АНАЛИЗ
- 2.1.5.1. Углы и длины связей
- 2.1.5.2. Алкил- и полиалкилциклогексаны
- 2.1.5.3. Конформация карбоциклических колец, больших, чем циклогексан
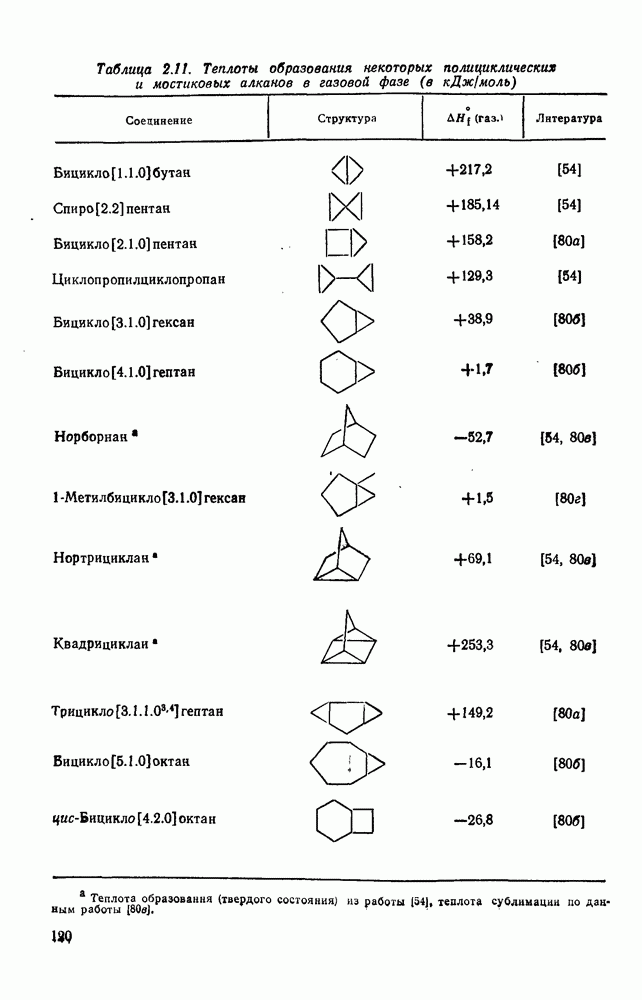
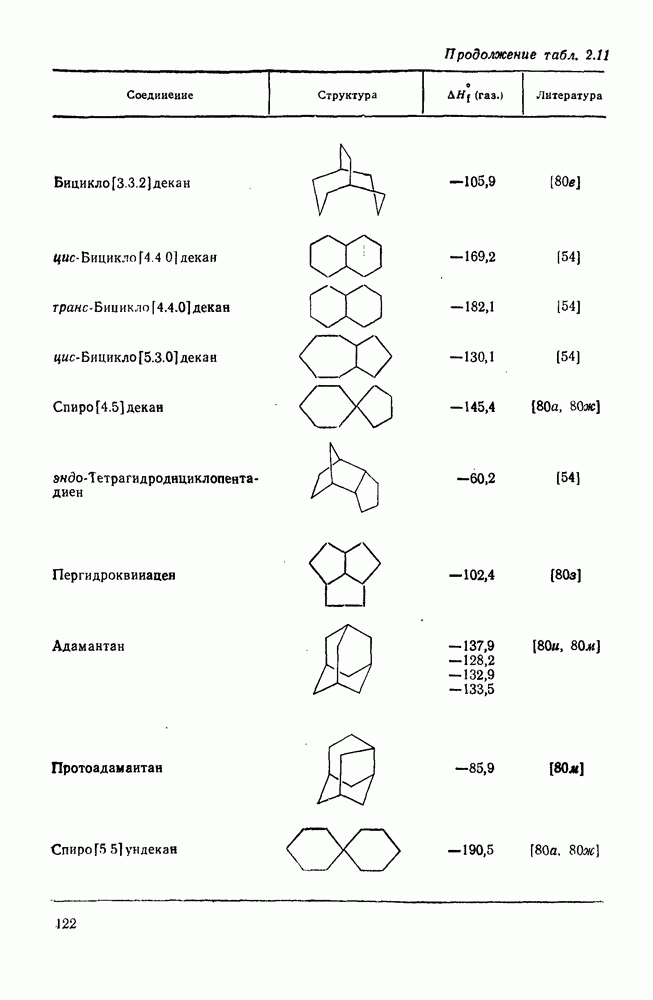
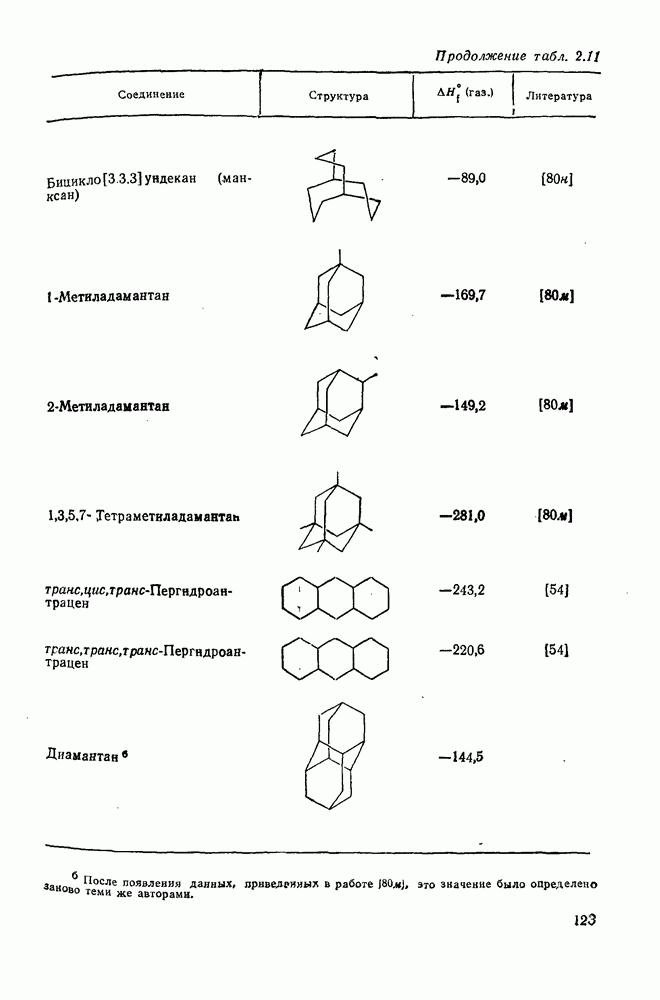
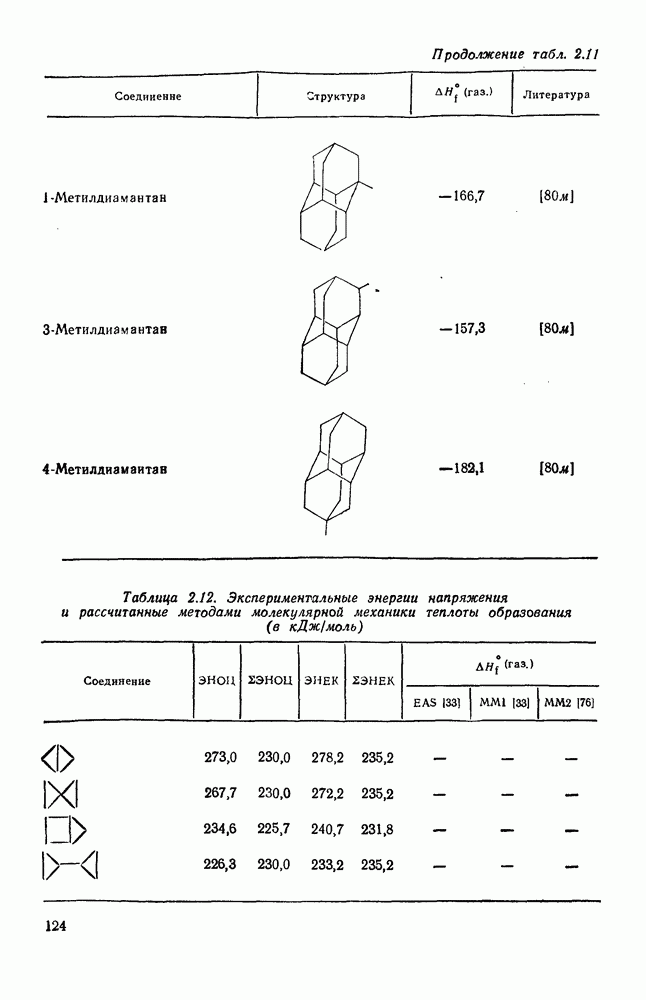
- 2.1.6. ТЕРМОХИМИЧЕСКИЕ СВОЙСТВА
- 2.1.6.1. Горение. Алканы и циклоалканы как топливо
- 2.1.6.2. Определение теплот сгорания и термохимические свойства
- 2.1.6.3. Эмпирические методы оценки теплот образования алканов
- 2.1.6.4. Оценка теплот образования алканов на основе энергии связей
- 2.1.6.5. Оценка теплот образования алканов на основе инкрементов групп
- 2.1.6.6. Оценка теплот образования циклических, полициклических и мостиковых алканов на основе инкрементов «скошенных разобщенных» групп и «единственных» наиболее устойчивых конформаций
- 2.1.6.7. Молекулярно-механические расчеты теплот образования и энергии напряжения
- 2.1.6.8. Моно- и полициклоалкаиы
- 2.1.7. ПОЛУЧЕНИЕ АЦИКЛИЧЕСКИХ АЛКАНОВ
- 2.1.7.1. Получение алканов восстановлением олефинов
- 2.1.7.2. Получение алканов из альдегидов и кетонов
- 2.1.7.3. Получение алканов из спиртов и алкилгалогенидов
- 2.1.7.4. Получение алканов из карбоновых кислот
- 2.1.8. СИНТЕЗ МОНО- И ПОЛИЦИКЛОАЛКАНОВ
- 2.1.9. РЕАКЦИИ АЦИКЛИЧЕСКИХ АЛКАНОВ
- 2.1.9.1. Галогенирование
- 2.1.9.2. Нитрование
- 2.1.9.3. Окисление
- 2.1.9.4. Каталитическая изомеризация алканов
- 2.1.9.5. Каталитическое алкилирование алканов
- 2.1.9.6. Реакции крекинга алканов
- 2.1.9.7. Термический крекинг
- 2.1.9.8. Каталитический крекинг
- 2.1.9.9. Каталитический риформинг и дегидроциклизация алканов
- 2.1.10. РЕАКЦИИ ЦИКЛОАЛКАНОВ И ПОЛИЦИКЛОАЛКАНОВ
- 2.2. ОЛЕФИНОВЫЕ И АЦЕТИЛЕНОВЫЕ УГЛЕВОДОРОДЫ
- 2.2.2. ПОЛУЧЕНИЕ ОЛЕФИНОВ
- 2.2.2.1. Элиминирование в системах
- 2.2.2.2. Элиминирование из систем
- 2.2.2.3. Циклоэлиминирование
- 2.2.2.4. Частичное восстановление
- 2.2.2.5. Элиминирование сульфонилгидразонов
- 2.2.2.6. Реакция Виттига и родственные ей реакции
- 2.2.2.7. Различные реакции конденсации
- 2.2.2.8. Электроциклические реакции
- 2.2.2.9. Циклоолигомеризация
- 2.2.2.11. Реакции винильных производных
- 2.2.3. РЕАКЦИИ ОЛЕФИНОВ
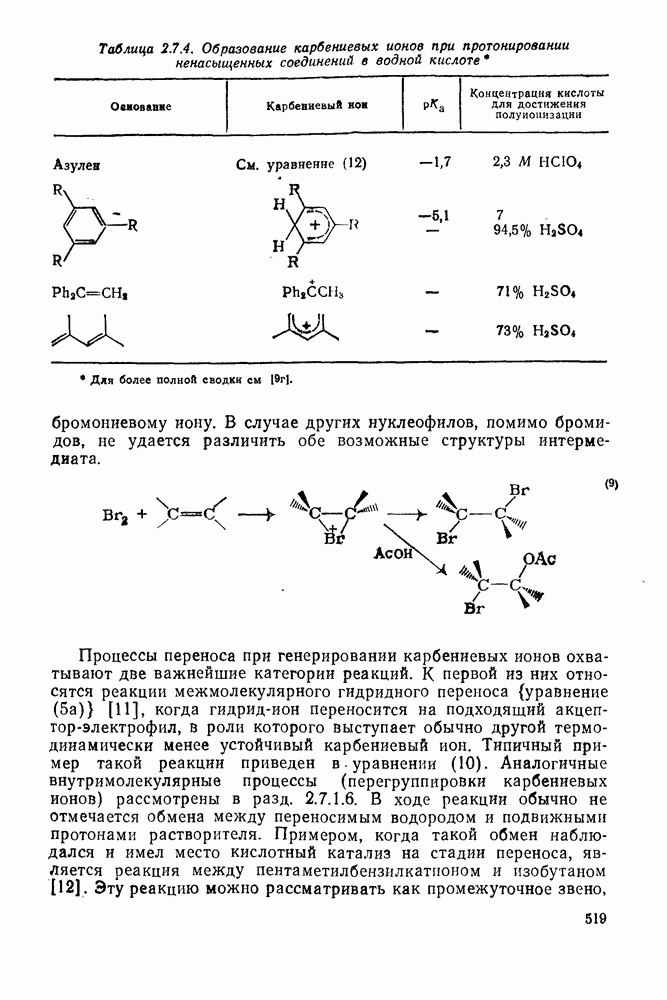
- 2.2.3.1. Электрофильное присоединение
- 2.2.3.2. Нуклеофильное присоединение
- 2.2.3.3. Радикальное присоединение
- 2.2.3.4. Циклоприсоединение и родственные реакции
- 2.2.3.5. Окисление
- 2.2.3.6. Восстановление
- 2.2.3.7. Перегруппировки
- 2.2.3.8. Фотохимические реакции
- 2.2.3.9. Прочие реакции
- 2.3. ДИЕНЫ, ПОЛНЕНЫ И АЦЕТИЛЕНОВЫЕ УГЛЕВОДОРОДЫ
- 2.3.1. СОПРЯЖЕННЫЕ ДИЕНЫ И ПОЛНЕНЫ
- 2.3.1.2. Получение сопряженных диенов
- 2.3.2. РЕАКЦИИ СОПРЯЖЕННЫХ ДИЕНОВ
- 2.3.2.2. Восстановление
- 2.3.2.3. Гидроборирование
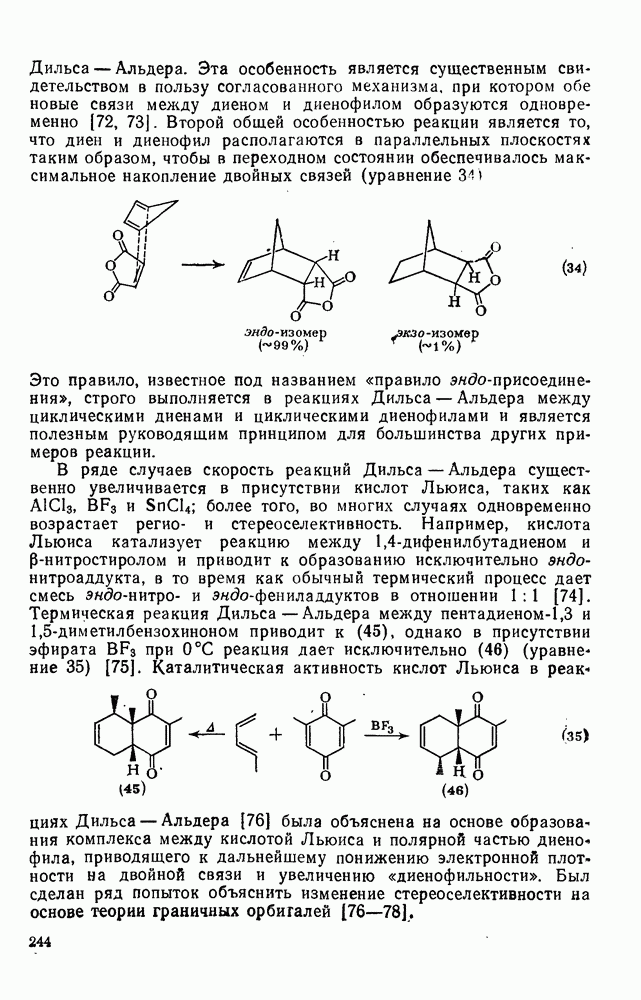
- 2.3.2.4. Реакция Дильса — Альдера
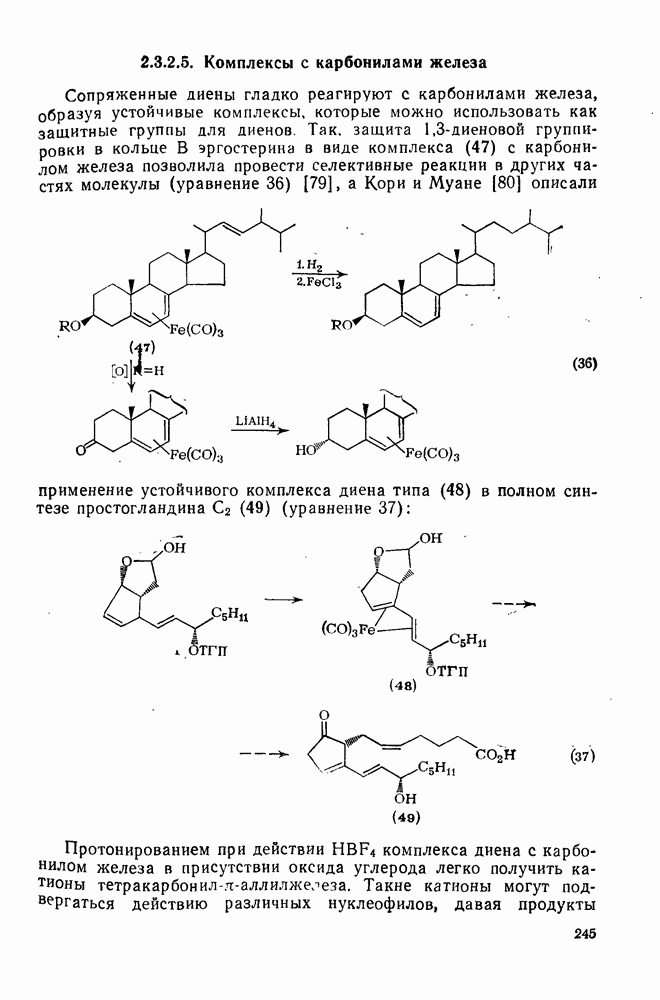
- 2.3.2.5. Комплексы с карбонилами железа
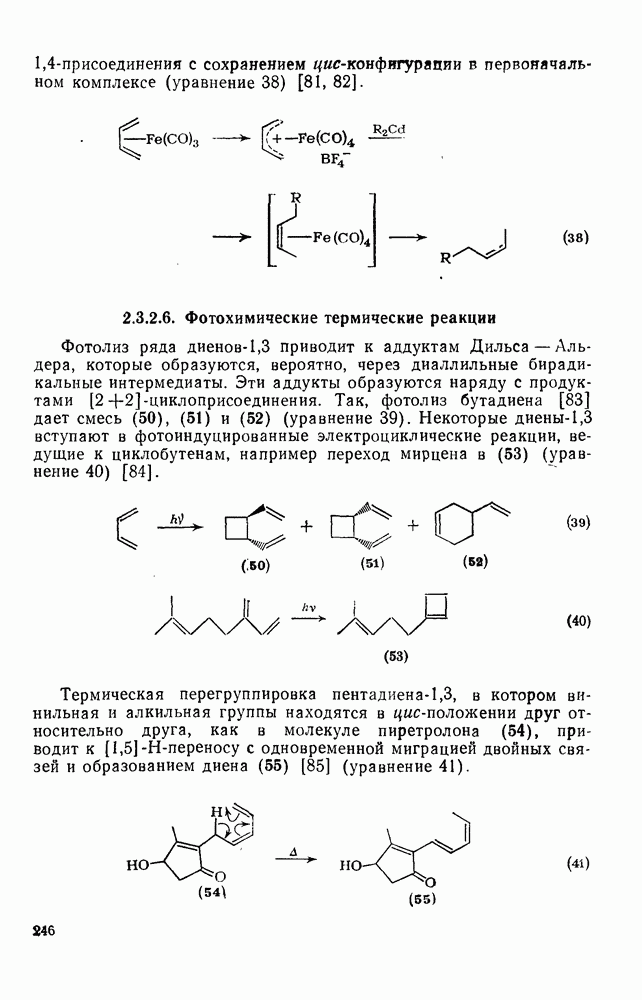
- 2.3.2.6. Фотохимические термические реакции
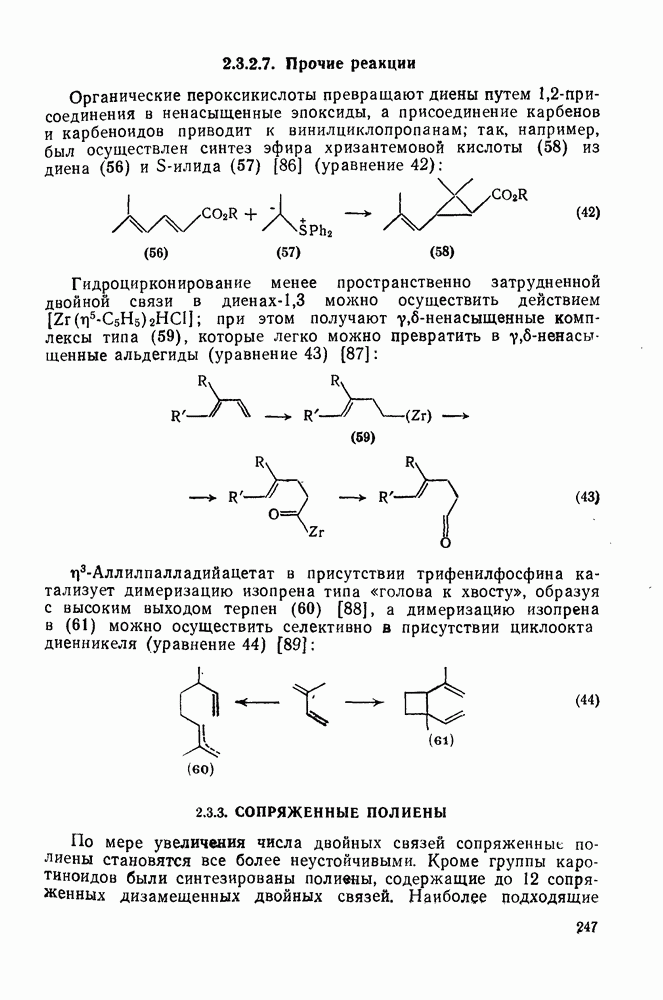
- 2.3.2.7. Прочие реакции
- 2.3.3. СОПРЯЖЕННЫЕ ПОЛИЕНЫ
- 2.3.4. ПРИРОДНЫЕ ДИЕНЫ И ПОЛНЕНЫ
- 2.3.5. АЛЛЕНЫ И КУМУЛЕНЫ
- 2.3.5.2. Получение алленов
- 2.3.6. РЕАКЦИИ АЛЛЕНОВ
- 2.3.6.2. Гидрирование
- 2.3.6.3. Реакции алленов в присутствии комплексов металлов
- 2.3.7. КУМУЛЕНЫ
- 2.3.8. ПРИРОДНЫЕ АЛЛЕНЫ И КУМУЛЕНЫ
- 2.3.9. АЦЕТИЛЕНЫ И ПОЛИАЦЕТИЛЕНЫ
- 2.3.9.2. Получение ацетиленов
- 2.3.10. РЕАКЦИИ АЦЕТИЛЕНОВ
- 2.3.10.2. Изомеризация
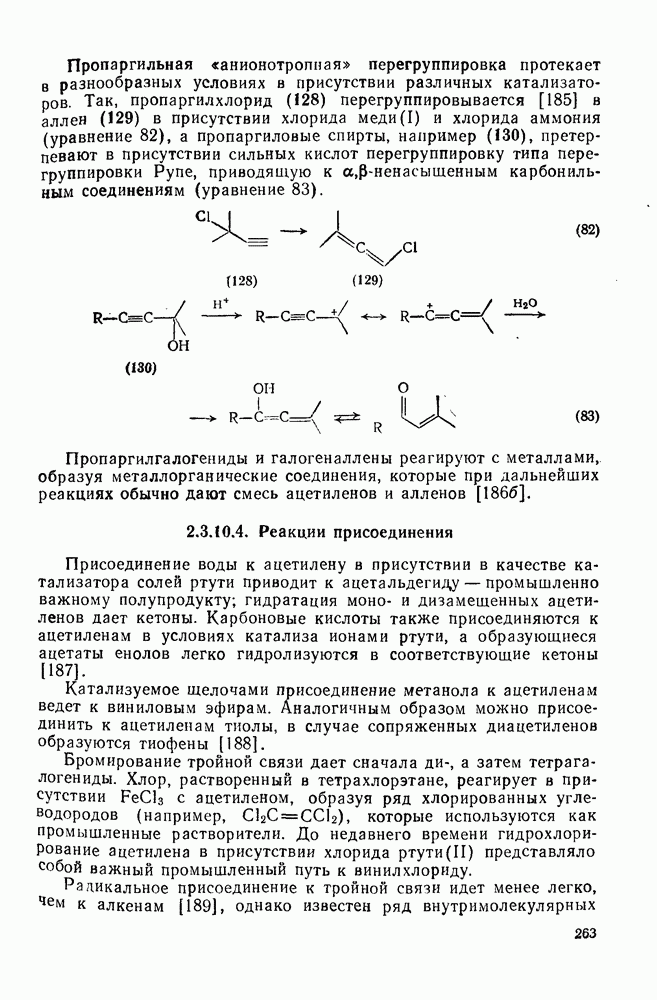
- 2.3.10.3. Пропаргильные перегруппировки
- 2.3.10.4. Реакции присоединения
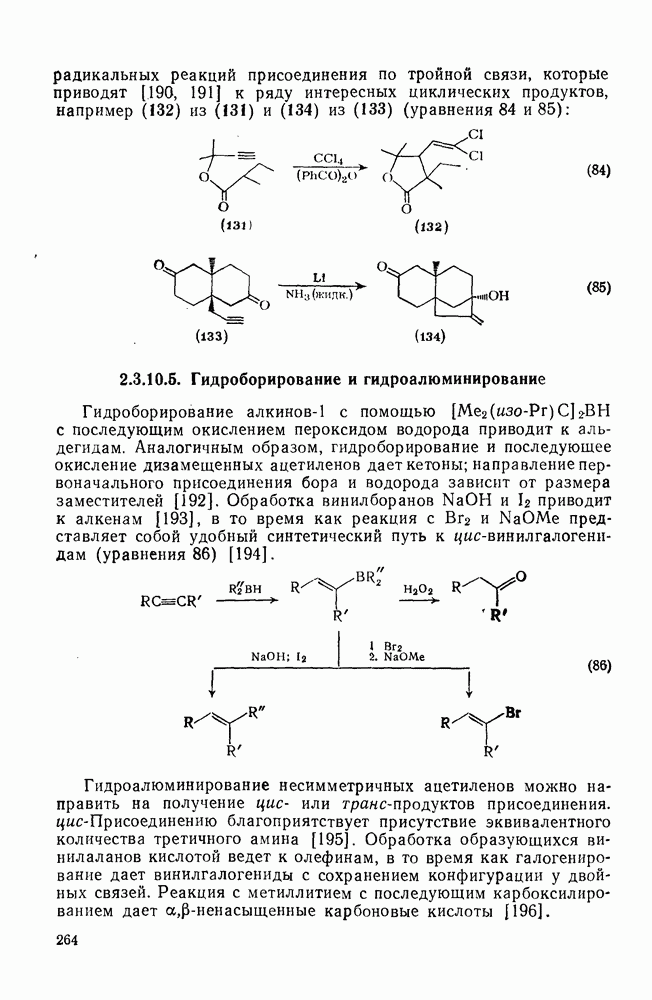
- 2.3.10.5. Гидроборирование и гидроалюминирование
- 2.3.10.6. Реакции замещения
- 2.3.10.7. Восстановление
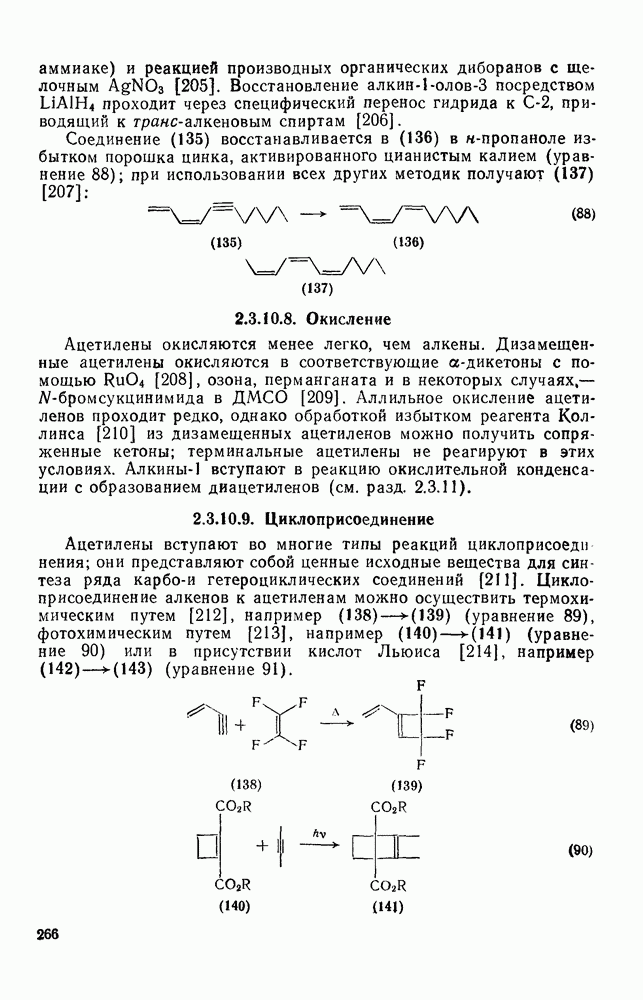
- 2.3.10.8. Окисление
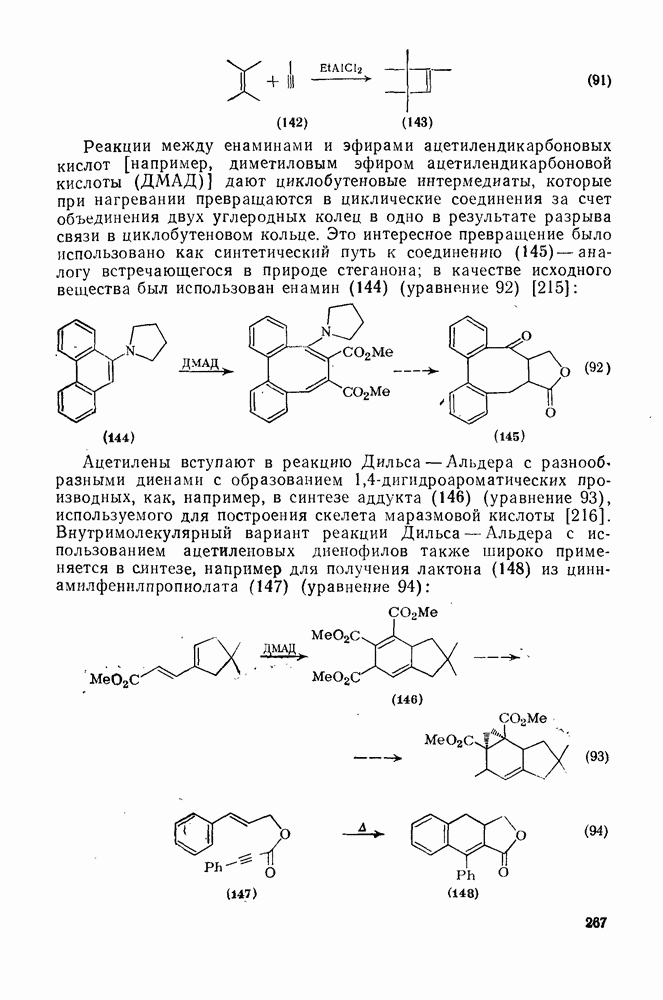
- 2.3.10.9. Циклоприсоединение
- 2.3.10.10. Реакции катализуемые металлами
- 2.3.11. ПОЛИАЦЕТИЛЕНЫ
- 2.3.12. ПРИРОДНЫЕ АЦЕТИЛЕНЫ И ПОЛИАЦЕТИЛЕНЫ
- 2.3.13. СОПРЯЖЕННЫЕ ЕНИНЫ
- 2.3.13.1. Получение сопряженных енинов
- 2.3.14. РЕАКЦИИ СОПРЯЖЕННЫХ ЕНИНОВ
- 2.3.15. ПРИРОДНЫЕ СОПРЯЖЕННЫЕ ЕНИНЫ
- 2.4. АРОМАТИЧНОСТЬ
- 2.4.2. ЭЛЕКТРОННЫЕ ТЕОРИИ СТРОЕНИЯ БЕНЗОЛА
- 2.4.3. КРИТЕРИИ АРОМАТИЧНОСТИ
- 2.4.3.1. Термодинамические свойства
- 2.4.3.2. Структурные особенности
- 2.4.3.3. Магнитные свойства
- 2.4.3.4. Прочие критерии
- 2.4.4. АНТИАРОМАТИЧНОСТЬ
- 2.4.4.1. Термодинамические свойства
- 2.4.4.2. Структурные особенности
- 2.4.4.3. Магнитные свойства
- 2.4.4.4. Прочие свойства
- 2.4.5. ТЕОРЕТИЧЕСКИЕ ОПРЕДЕЛЕНИЯ АРОМАТИЧНОСТИ
- 2.4.5.1. Полуэмпирические расчеты и дьюаровская резонансная энергия
- 2.4.5.2. Расчеты по методу валентных пар и применение резонансного метода
- 2.4.5.3. Локализация связей
- 2.4.5.4. Связь энергетических критериев с критериями локализации связей
- 2.4.6. АРОМАТИЧЕСКИЕ ПЕРЕХОДНЫЕ СОСТОЯНИЯ
- 2.5. АРЕНЫ И ИХ РЕАКЦИИ
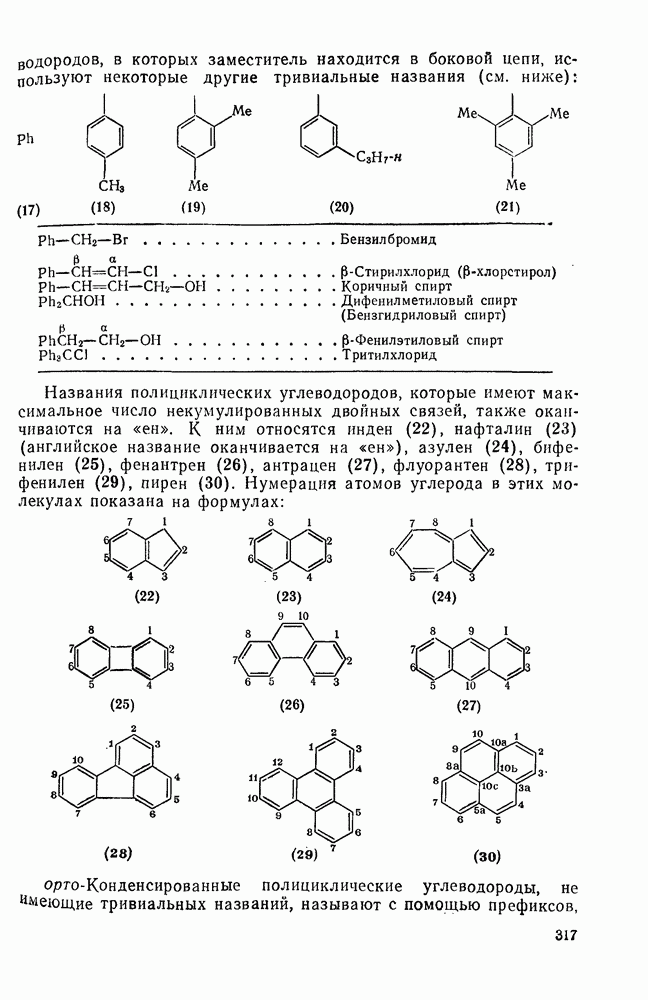
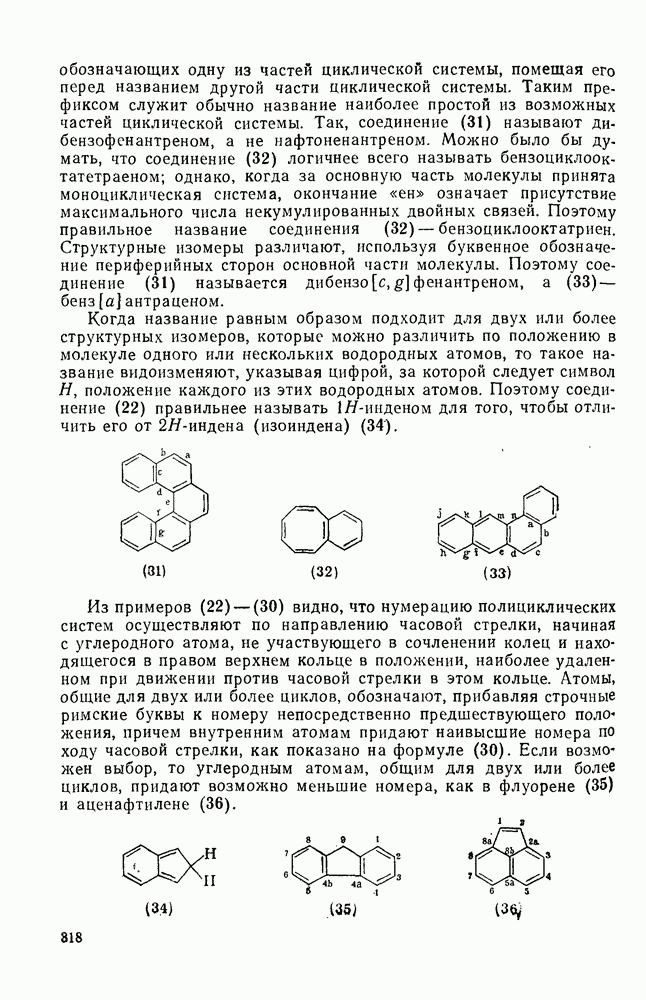
- 2.5.2. НОМЕНКЛАТУРА
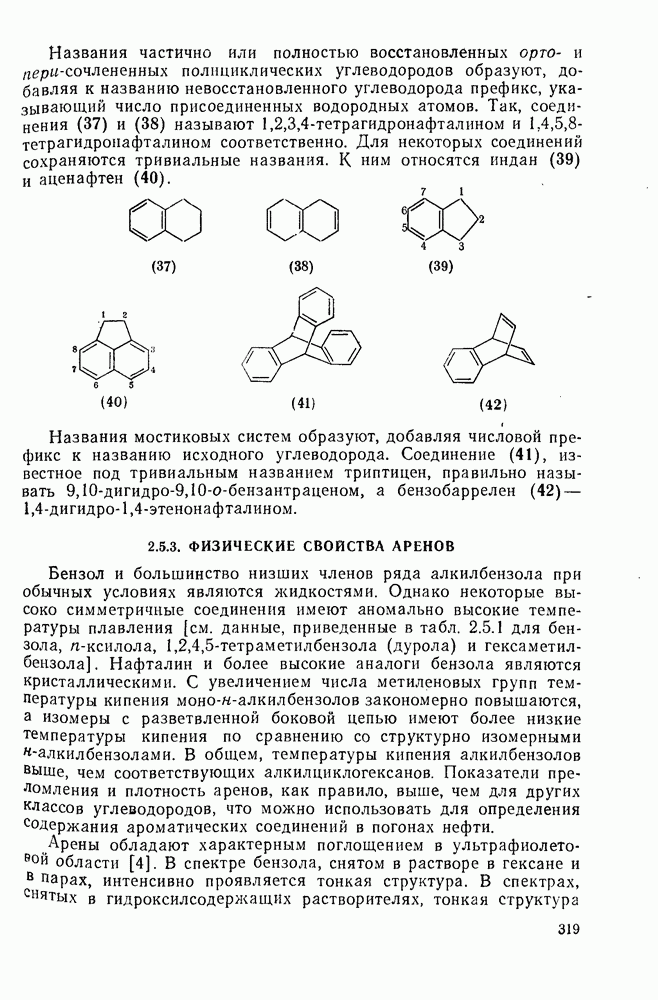
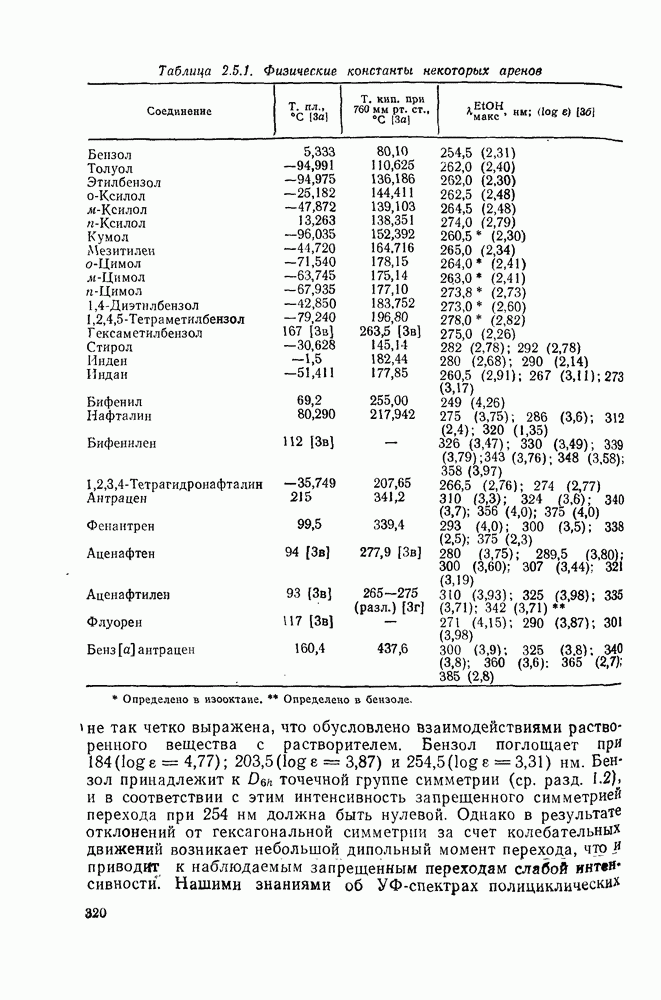
- 2.5.3. ФИЗИЧЕСКИЕ СВОЙСТВА АРЕНОВ
- 2.5.4. ПРОМЫШЛЕННОЕ ПРОИЗВОДСТВО АРЕНОВ
- 2.5.5. ЦИКЛОТРИМЕРИЗАЦИЯ АЦЕТИЛЕНОВ
- 2.5.6. РЕАКЦИИ ЭЛЕКТРОФИЛЬНОГО ПРИСОЕДИНЕНИЯ — ЭЛИМИНИРОВАНИЯ АРЕНОВ
- 2.5.6.1. Механизм ароматического нитрования [15]
- 2.5.6.2. Кинетические изотопные эффекты [21]
- 2.5.6.3. Реакции, включающие ипсо-протонирование
- 2.5.6.4. Металлирование
- 2.5.6.5. Электрофилы IV группы
- 2.5.6.6. Электрофилы V группы
- 2.5.6.7. Электрофилы VI группы [18, 56]
- 2.5.6.8. Электрофилы VII группы [18, 25а, 56]
- 2.5.7. ОРИЕНТАЦИЯ В РЕАКЦИЯХ ЭЛЕКТРОФИЛЬНОГО ПРИСОЕДИНЕНИЯ — ЭЛИМИНИРОВАНИЯ
- 2.5.8. РАДИКАЛЬНОЕ ГАЛОГЕНИРОВАНИЕ АРЕНОВ В БОКОВУЮ ЦЕПЬ [96]
- 2.5.9. РЕАКЦИИ ПРИСОЕДИНЕНИЯ К АРЕНАМ
- 2.5.9.1. Восстановление аренов
- 2.5.9.2. Термическое циклоприсоединение к аренам
- 2.5.9.3. Фотоциклоприсоединение к моноциклическим аренам [126]
- 2.5.9.4. Фотохимические реакции полициклических аренов
- 2.6.10. ФОТОИЗОМЕРИЗАЦИЯ АРЕНОВ [126б]
- 2.5.11. ОКИСЛЕНИЕ АРЕНОВ [153]
- 2.5.12. РЕАКЦИИ АРЕНОВ С СИНГЛЕТНЫМ КИСЛОРОДОМ [162]
- 2.5.13. ПРИГОТОВЛЕНИЕ БИ- И ПОЛИАРИЛОВ
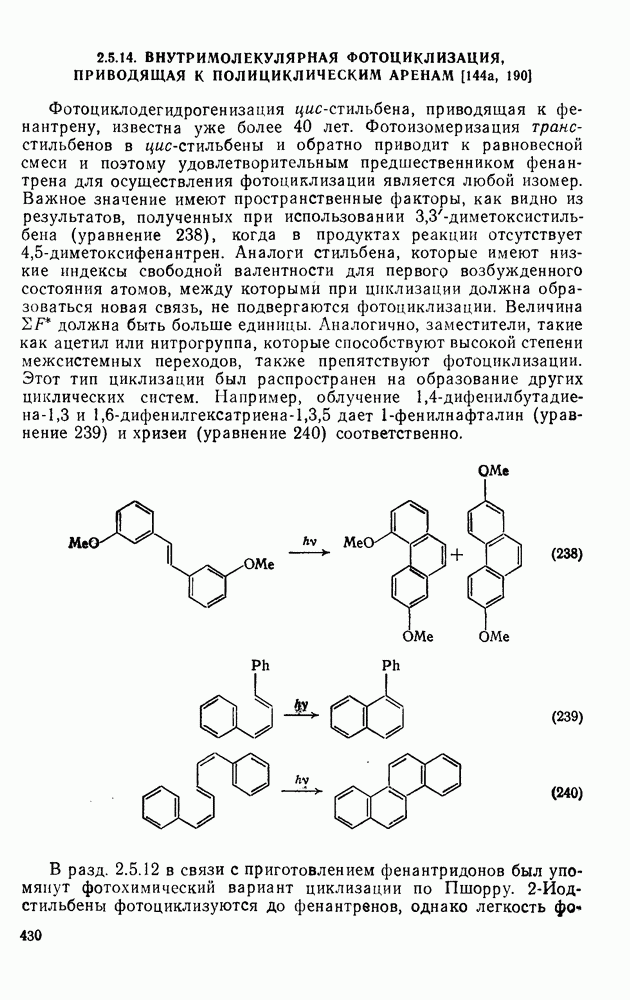
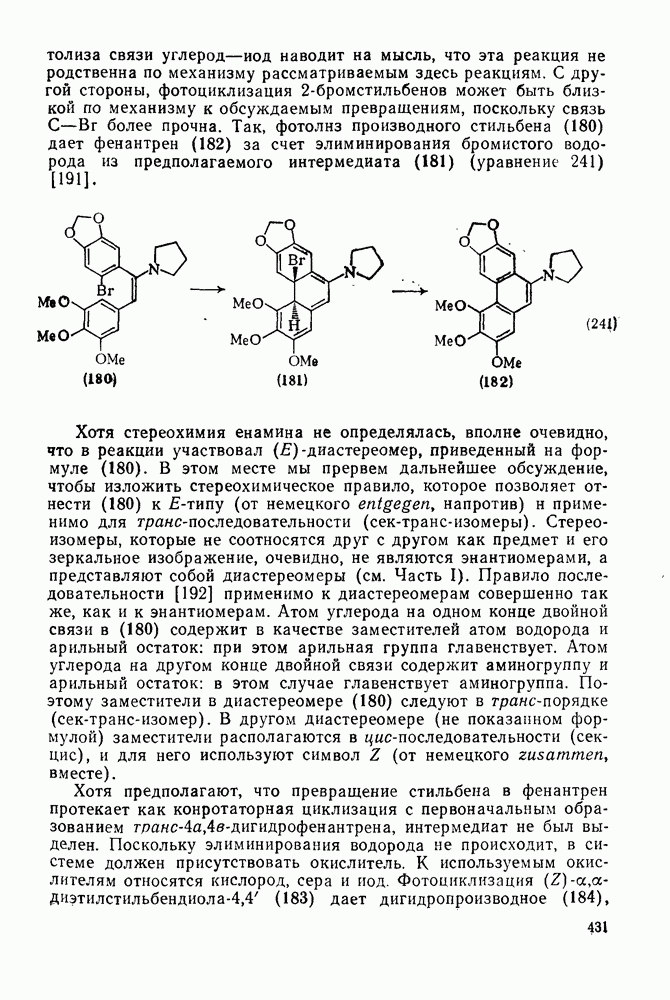
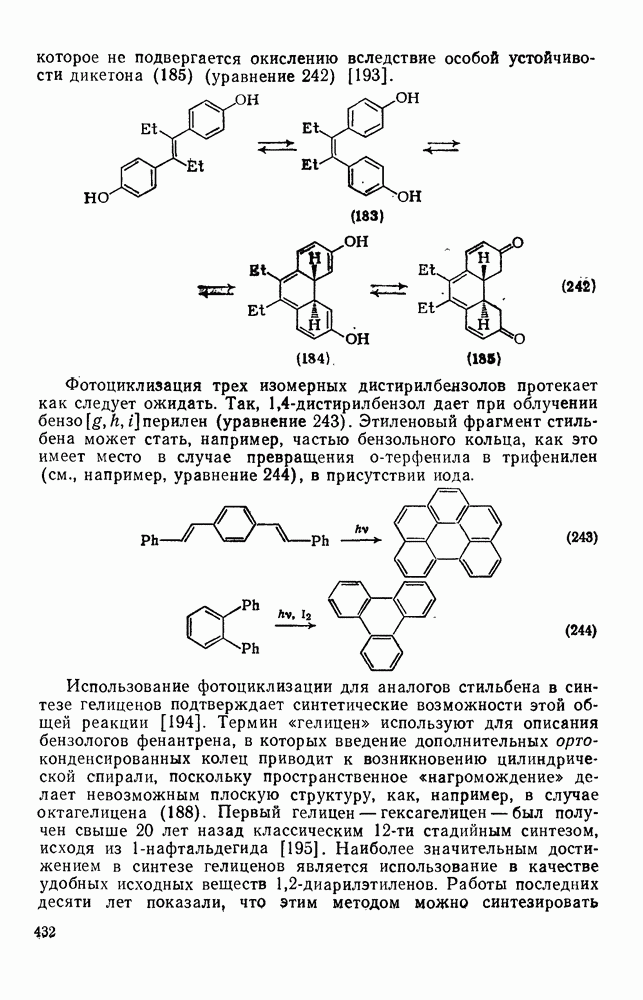
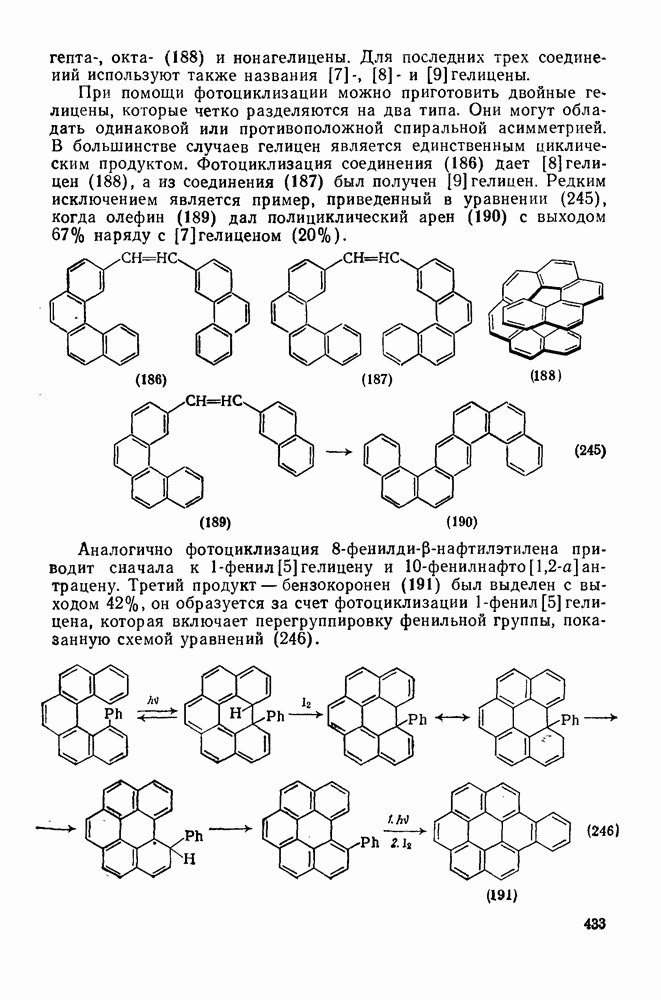
- 2.5.14. ВНУТРИМОЛЕКУЛЯРНАЯ ФОТОЦИКЛИЗАЦИЯ, ПРИВОДЯЩАЯ К ПОЛИЦИКЛИЧЕСКИМ АРЕНАМ
- 2.5.15. ВНУТРИМОЛЕКУЛЯРНАЯ ЦИКЛИЗАЦИЯ ДИЗАМЕЩЕННЫХ АРЕНОВ
- 2.5.16. ЦИКЛОФАНЫ
- 2.5.17. КОНФОРМАЦИЯ И ХИРАЛЬНОСТЬ АРЕНОВ
- 2.5.18. АЗУЛЕНЫ И НЕБЕНЗОИДНЫЕ АРЕНЫ
- 2.6. АННУЛЕНЫ И РОДСТВЕННЫЕ СИСТЕМЫ
- 2.6.2. МЕТОДЫ СИНТЕЗА
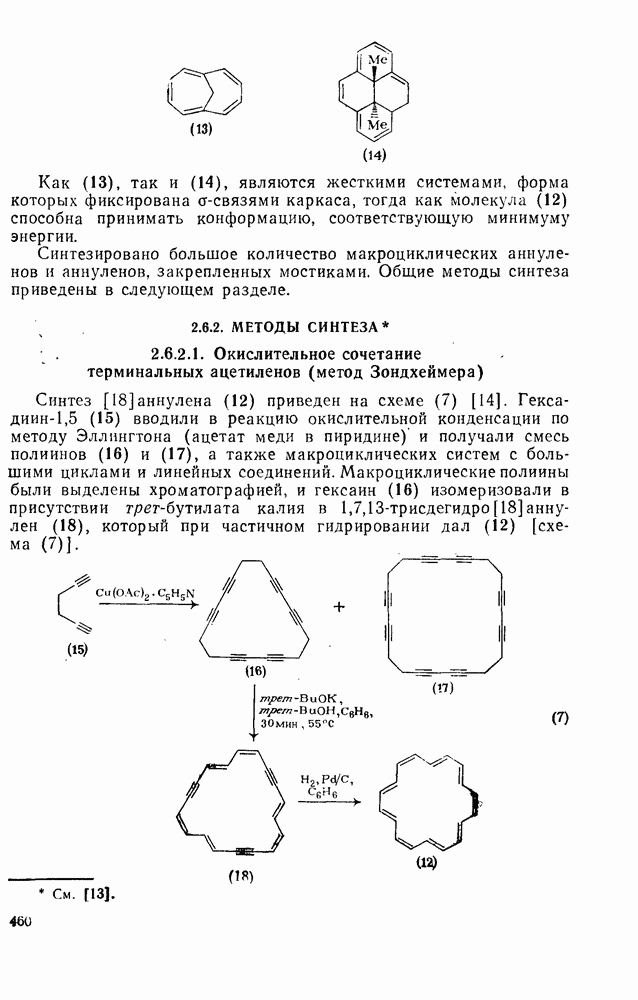
- 2.6.2.1. Окислительное сочетание терминальных ацетиленов (метод Зондхеймера)
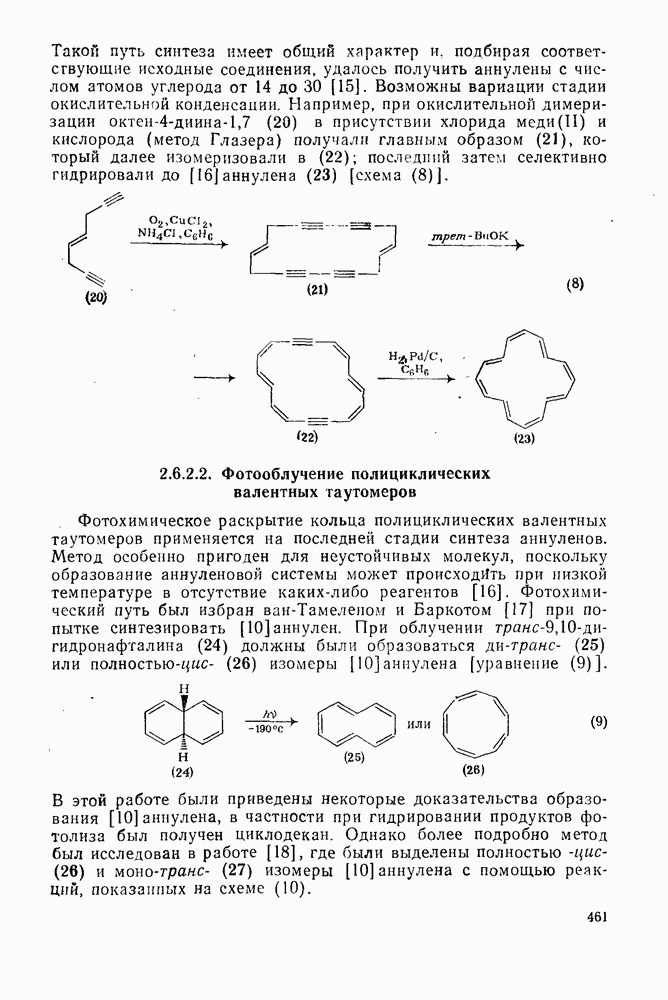
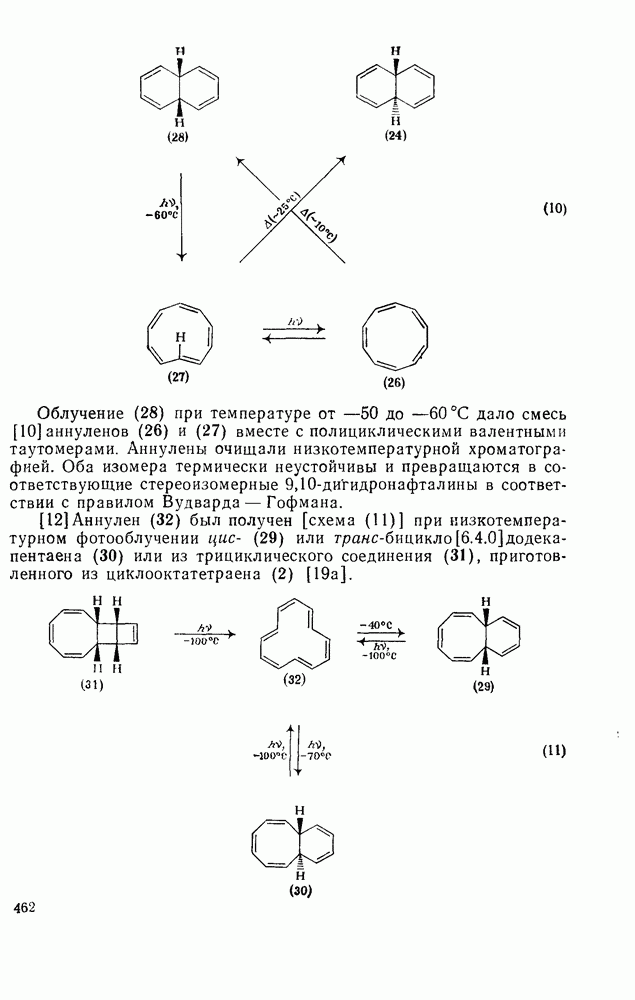
- 2.6.2.2. Фотооблучение полициклических валентных таутомеров
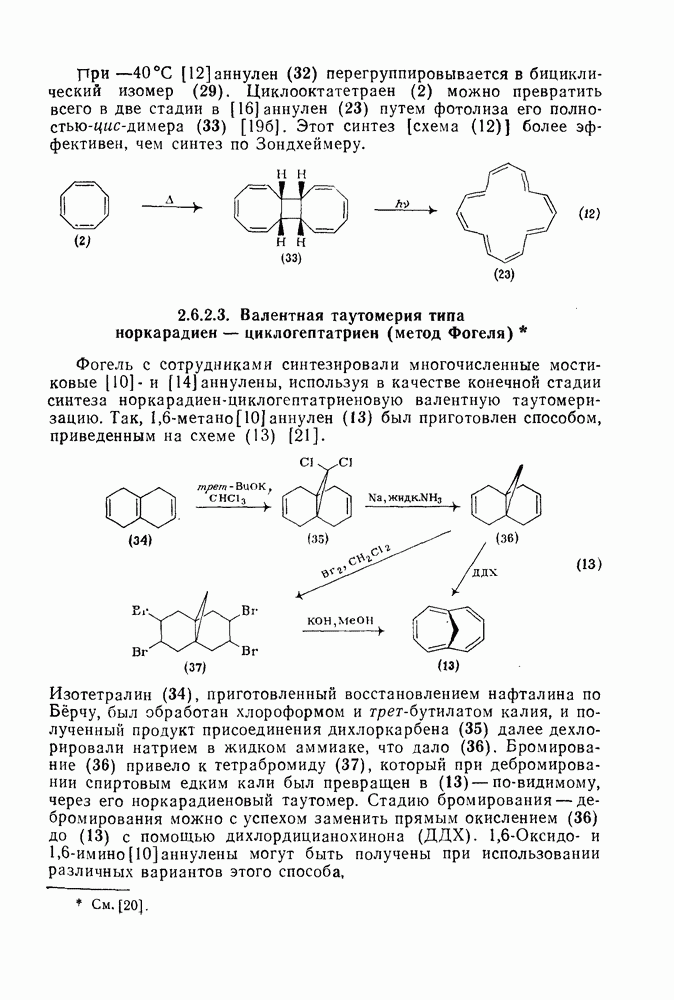
- 2.6.2.3. Валентная таутомерия типа норкарадиен — циклогептатриен (метод Фогеля)
- 2.6.2.4. Прочие методы
- 2.6.3. СВОЙСТВА АННУЛЕНОВ
- 2.6.4. СВОЙСТВА 4n-АННУЛЕНОВ
- 2.6.5. ДЕГИДРОАННУЛЕНЫ
- 2.6.6. АННЕЛИРОВАННЫЕ АННУЛЕНЫ
- 2.6.7. АРОМАТИЧЕСКИЕ И АНТИАРОМАТИЧЕСКИЕ МОНОЦИКЛИЧЕСКИЕ ИОНЫ
- 2.6.8. АРОМАТИЧЕСКИЕ И АНТИАРОМАТИЧЕСКИЕ ПОЛИЦИКЛИЧЕСКИЕ ИОНЫ
- 2.6.9. ГОМОАРОМАТИЧЕСКИЕ СИСТЕМЫ
- 2.7. КАРБОКАТИОНЫ И КАРБАНИОНЫ
- 2.7.1.2. Краткий исторический очерк развития химии карбокатионов
- 2.7.1.3. Методы генерации карбокатионов
- 2.7.1.4. Типы карбокатионов
- 2.7.1.5. Изучение карбокатионов: методы и результаты
- 2.7.1.6. Реакции карбокатионов
- 2.7.2. КАРБАНИОНЫ
- 2.7.2.2. Методы генерации карбанионов
- 2.7.2.3. Типы карбанионов
- 2.7.2.4. Физические свойства карбанионов
- 2.7.5.2. Реакции карбанионов
- 2.8. РАДИКАЛЫ, КАРБЕНЫ, АРИНЫ
- 2.8.1. РАДИКАЛЫ
- 2.8.1.1. Структура, устойчивость и реакционная способность радикалов
- 2.8.1.2. Методы генерации и реакции радикалов
- 2.8.2. КАРБЕНЫ
- 2.8.2.1. Методы генерации карбенов и карбеноидов
- 2.8.2.2. Реакции карбенов
- 2.8.3. АРИНЫ
- 2.8.3.1. Структура и спектры аринов
- 2.8.3.2. Методы генерации аринов
- 2.8.3.3. Реакции аринов
- ЧАСТЬ 3. ГАЛОГЕНСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
- 3.2. МЕТОДЫ ГАЛОГЕНИРОВАНИЯ
- 3.2.1. Гомолитическое замещение водорода
- 3.2.1.2. Использование галогенпроизводных в качестве реагентов
- 3.2.2. Гомолитическое замещение функциональных групп
- 3.2.3. Гомолитическое присоединение к ненасыщенным системам
- 3.2.3.1. Присоединение галогеноводородов
- 3.2.3.2. Присоединение галогенов
- 3.2.4. Электрофильное галогенирование
- 3.2.4.1. Замещение у насыщенной связи С-Н
- 3.2.4.2. Реакции с ненасыщенными системами
- 3.2.4.3. Реакции с карбанионами
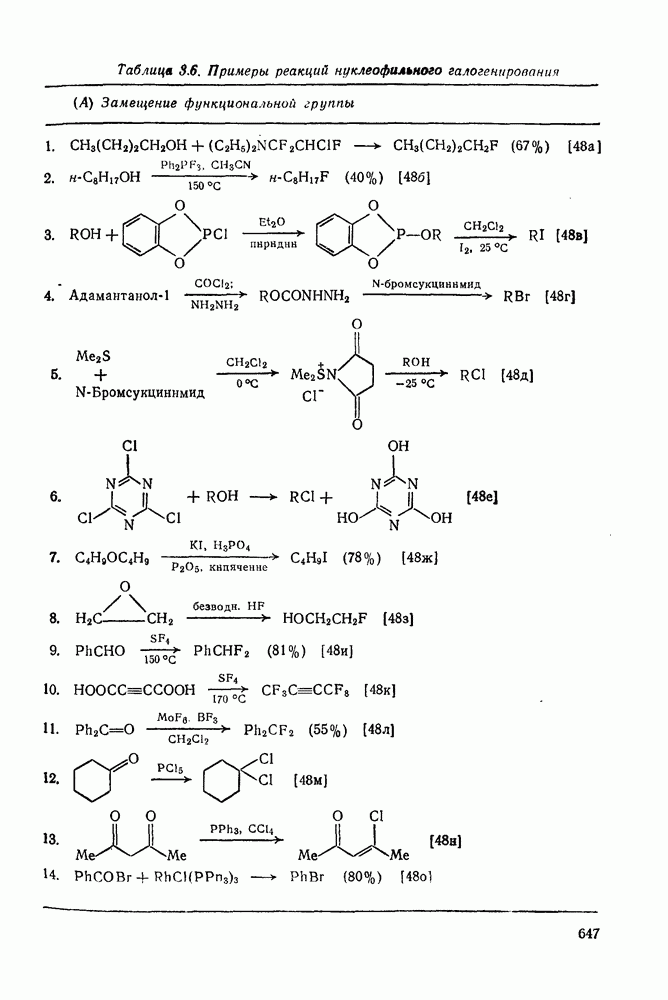
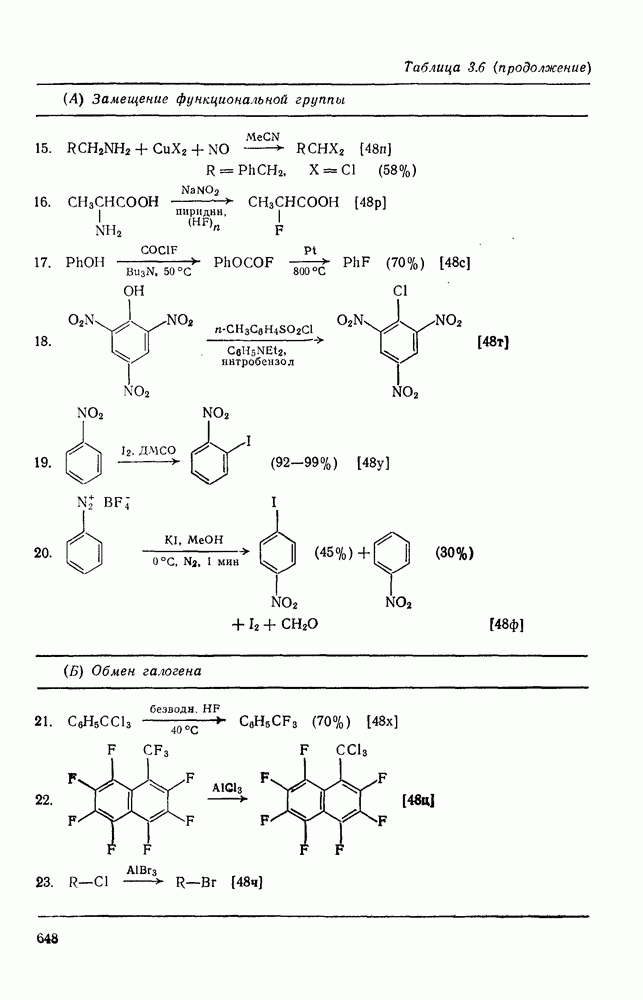
- 3.2.5. Нуклеофильное галогенирование
- 3.2.5.1. Галогенирование с замещением функциональной группы
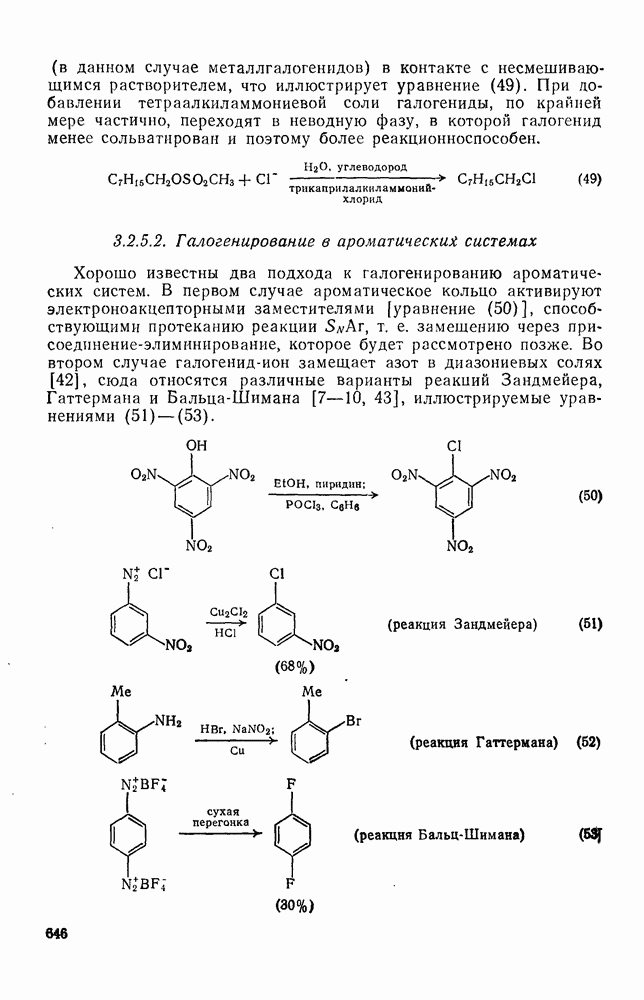
- 3.2.5.2. Галогенирование в ароматических системах
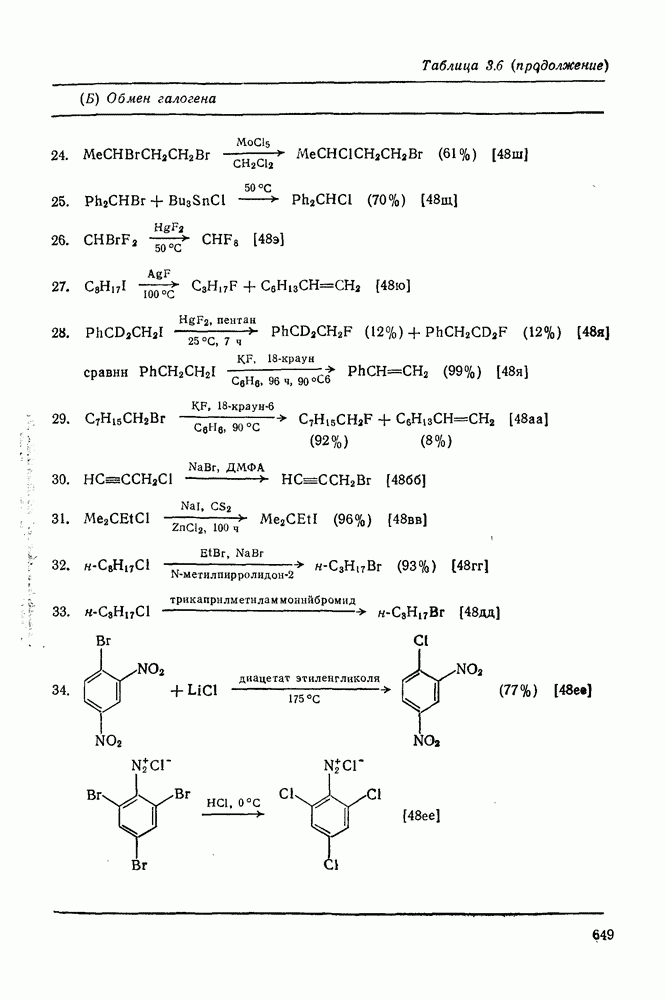
- 3.2.5.3. Галогенирование путем обмена галогенов
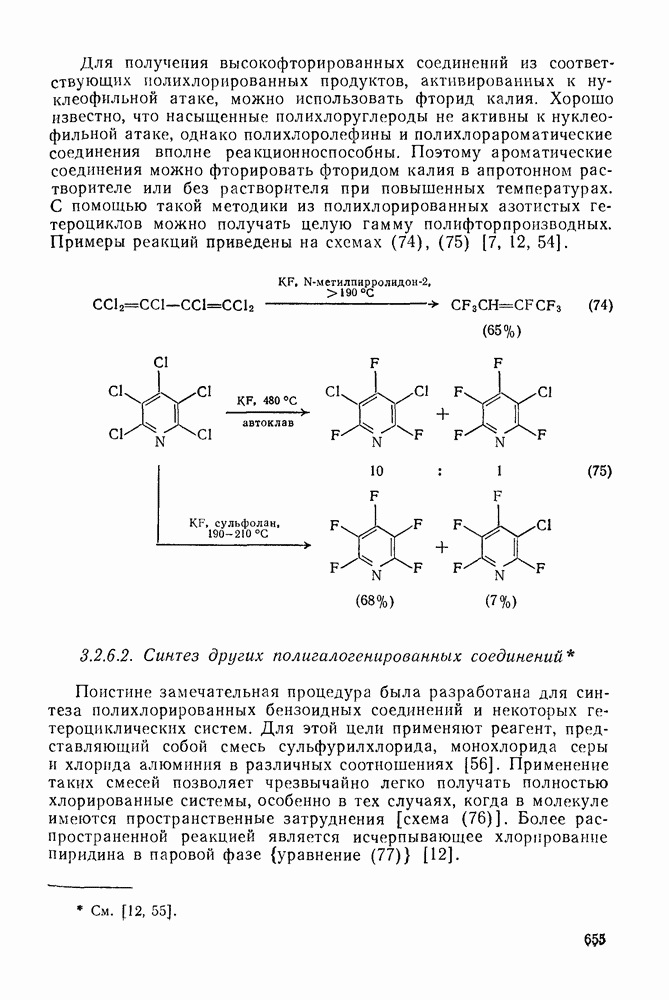
- 3.2.6. Синтез полигалогенированных соединений
- 3.2.6.1. Синтез полифторированных соединений
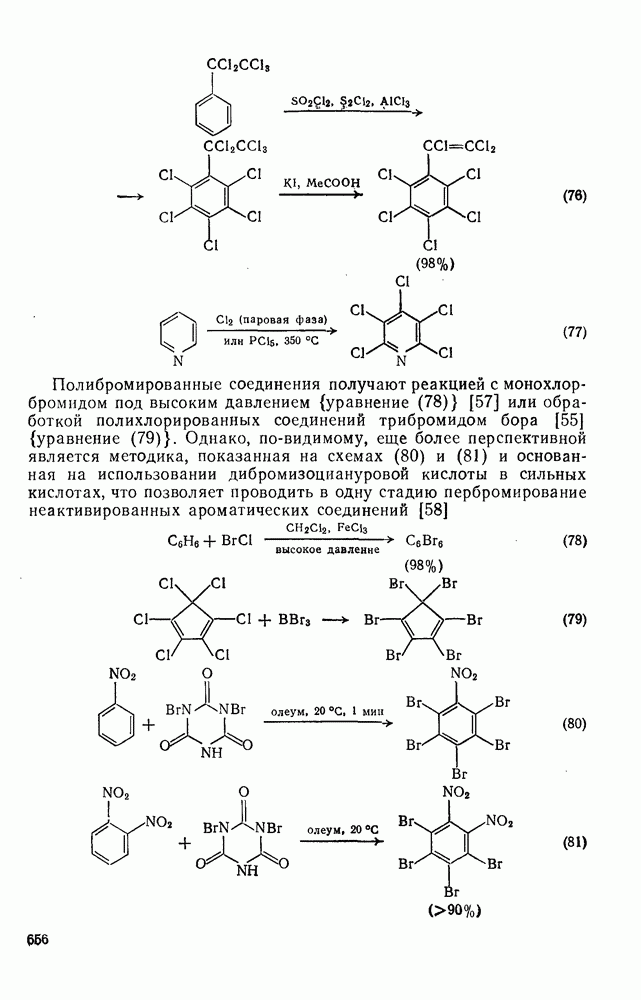
- 3.2.6.2. Синтез других полигалогенированных соединений
- 3.3. ГАЛОГЕНАЛКАНЫ
- 3.3.1. Характеристика связей углерод-галоген
- 3.3.2. Промышленное применение
- 3.3.3. Нуклеофильное замещение галогена
- 3.3.3.1. Реакции SN2 и родственные процессы
- 3.3.3.2. Соучастие соседних групп
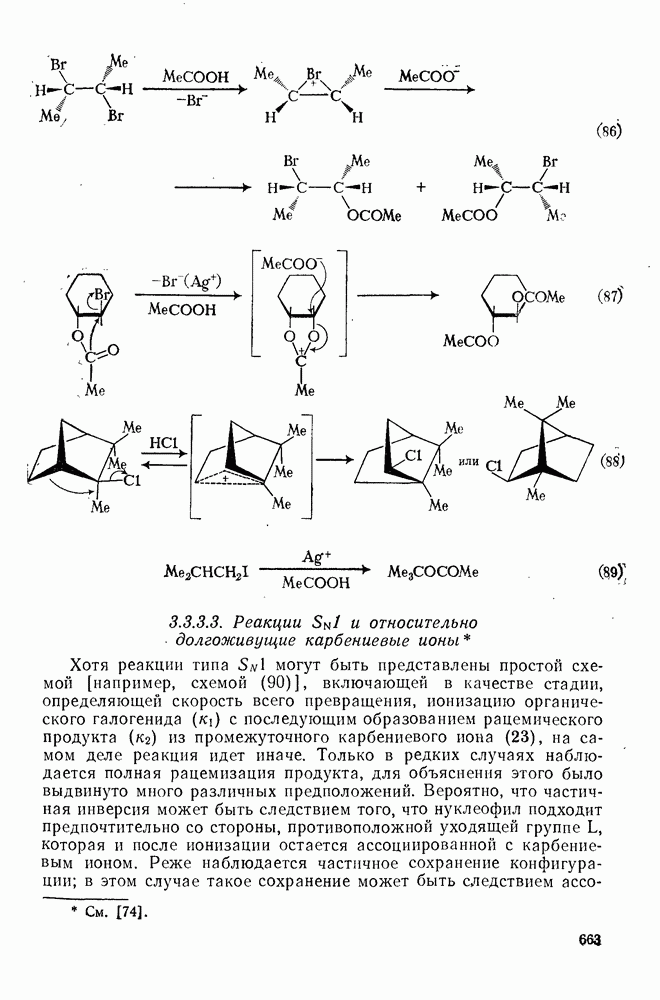
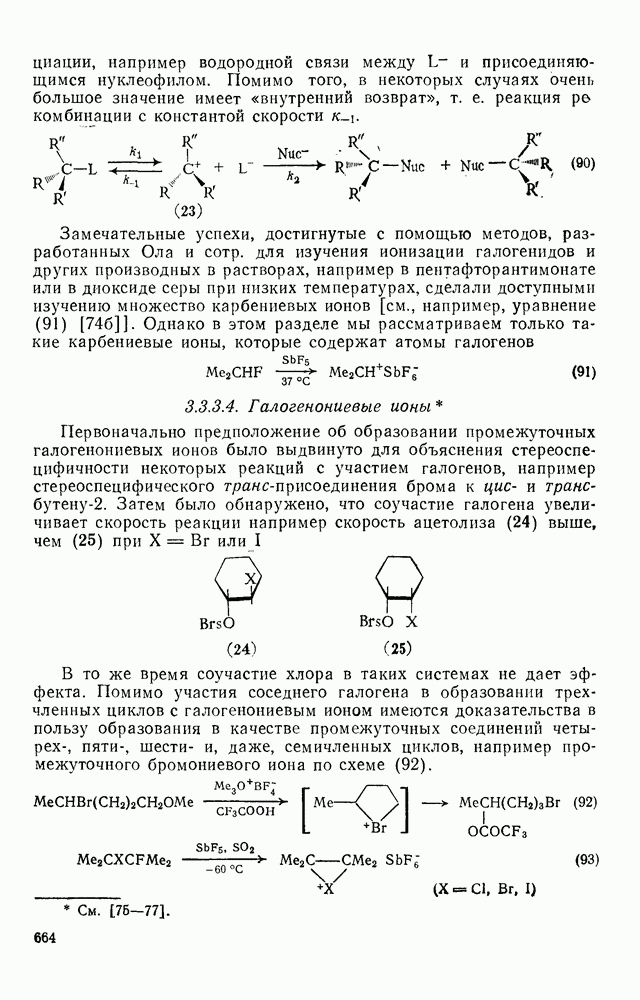
- 3.3.3.3. Реакции SN1 и относительно долгоживущие карбениевые ионы
- 3.3.3.4. Галогенониевые ионы
- 3.3.3.5. Галогенсодержащие карбениевые ионы
- 3.3.3.6. Механизм замещения с переносом электрона
- 3.3.4. Восстановление
- 3.3.5. Замещение на металлы
- 3.3.6. Элиминирование
- 3.3.6.1. b-Элиминирование
- 3.3.6.2. Галогенкарбанионы
- 3.3.6.3. Элиминирование через карбанионы
- 3.3.6.4. b-Элиминирование из металлорганических соединений
- 3.3.6.5. a-Элиминирование (генерирование карбенов)
- 3.4. ГАЛОГЕНАЛКЕНЫ
- 3.4.1. Синтез галогеналкенов
- 3.4.2. Нуклеофильная атака
- 3.4.2.1. Реакции, индуцируемые фторид-ионом
- 3.4.2.2. Другие реакции замещения
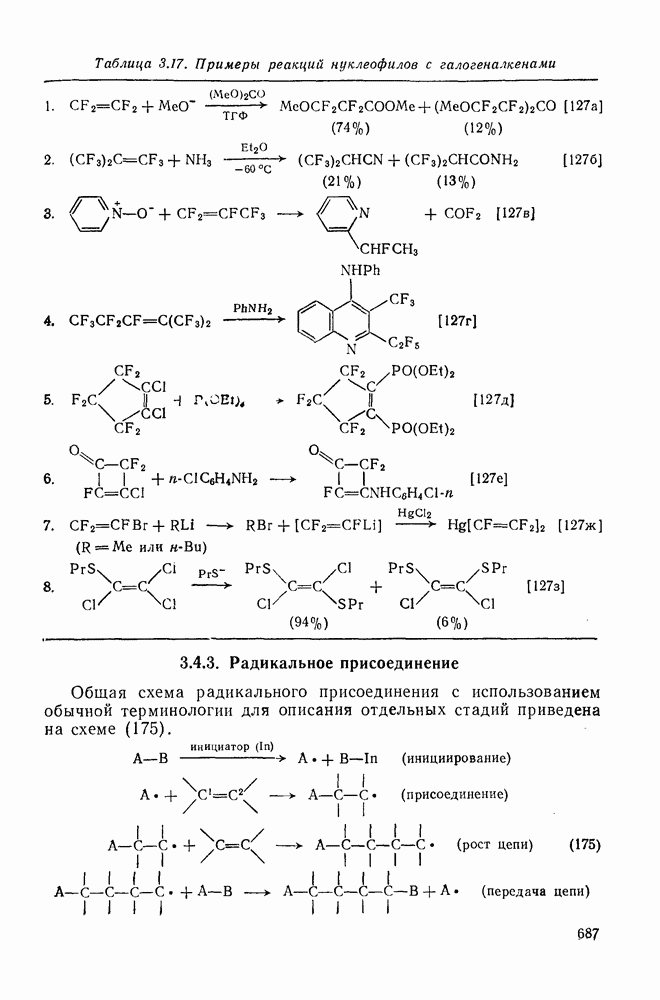
- 3.4.3. Радикальное присоединение
- 3.4.4. Электрофильное присоединение
- 3.4.5. Циклоприсоединение
- 3.4.5.1. [2+2]-Циклоприсоединение
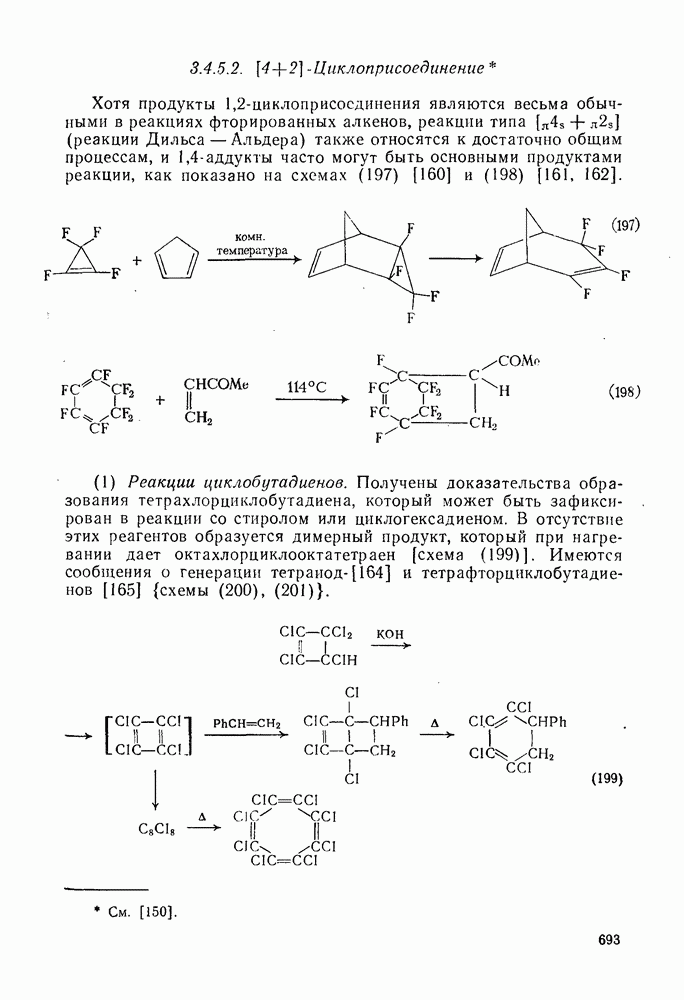
- 3.4.5.2. [4+2]-Циклоприсоединение
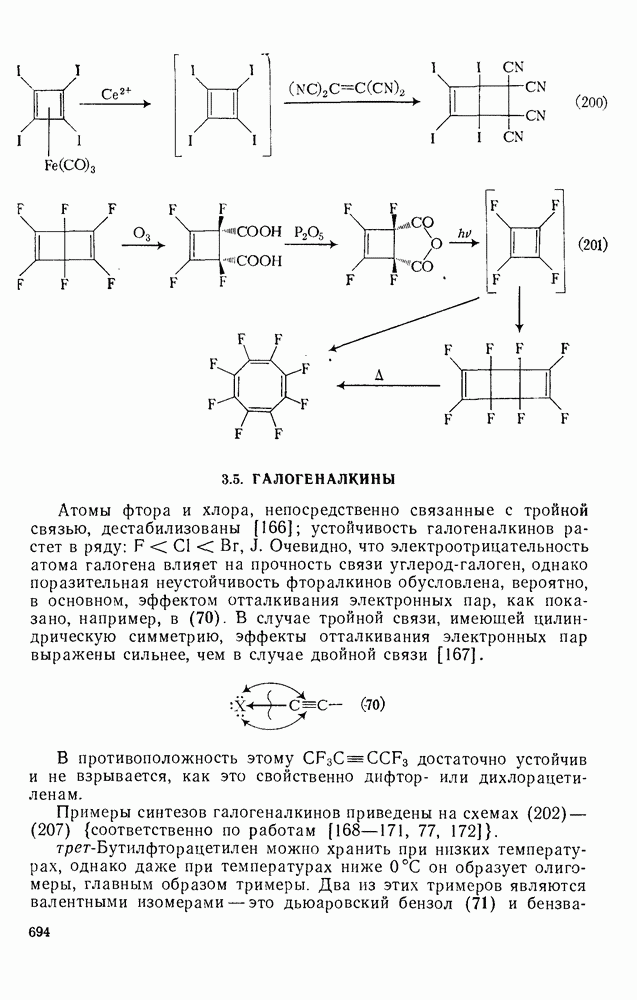
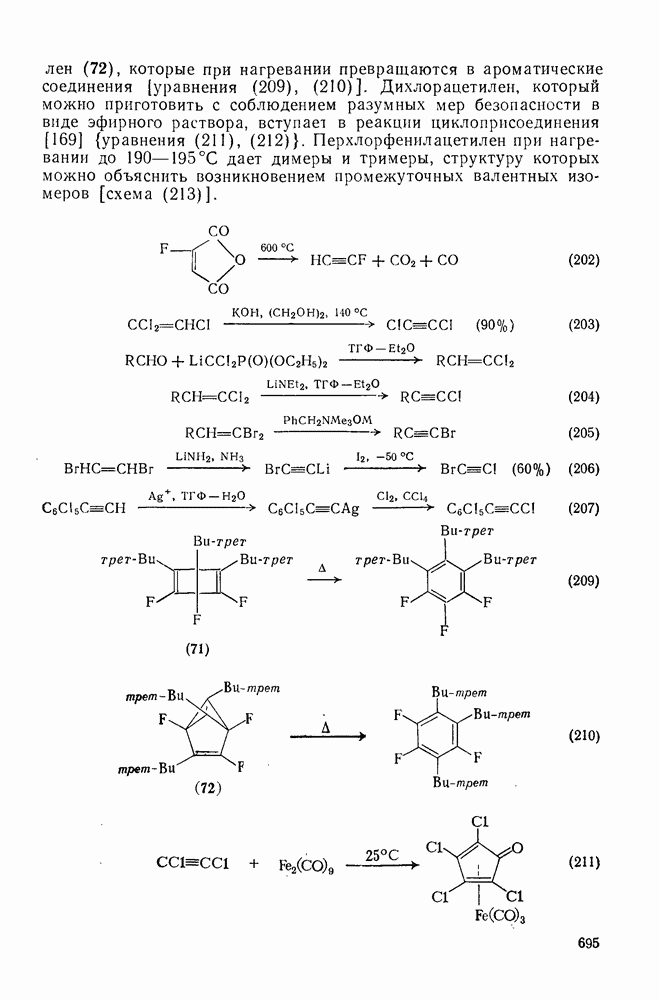
- 3.5. ГАЛОГЕНАЛКИНЫ
- 3.6. ГАЛОГЕНАРЕНЫ
- 3.6.1. Замещение галогена
- 3.6.1.2. Присоединение-элиминирование
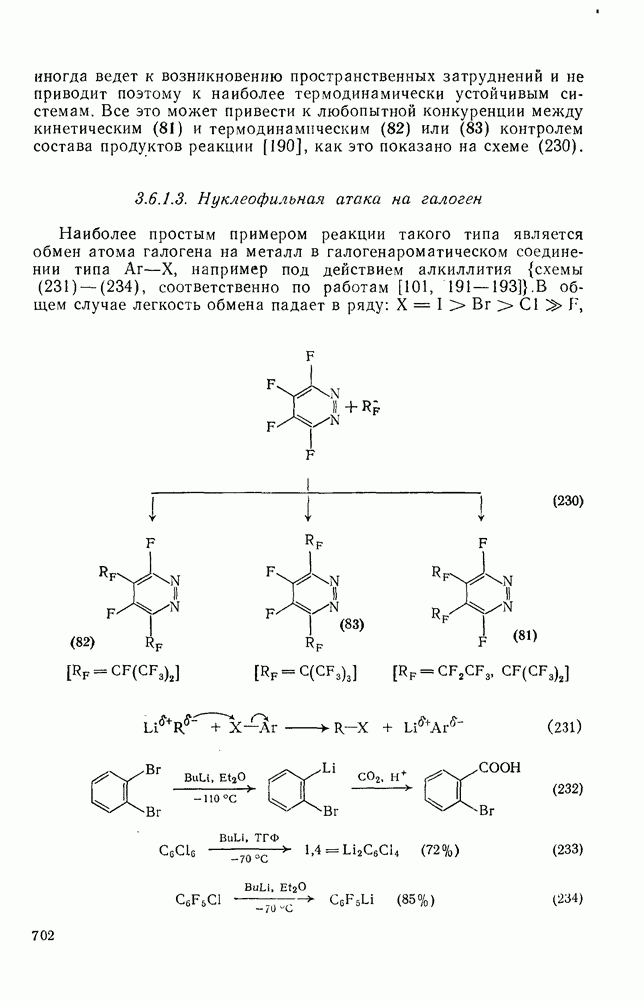
- 3.6.1.3. Нуклеофильная атака на галоген
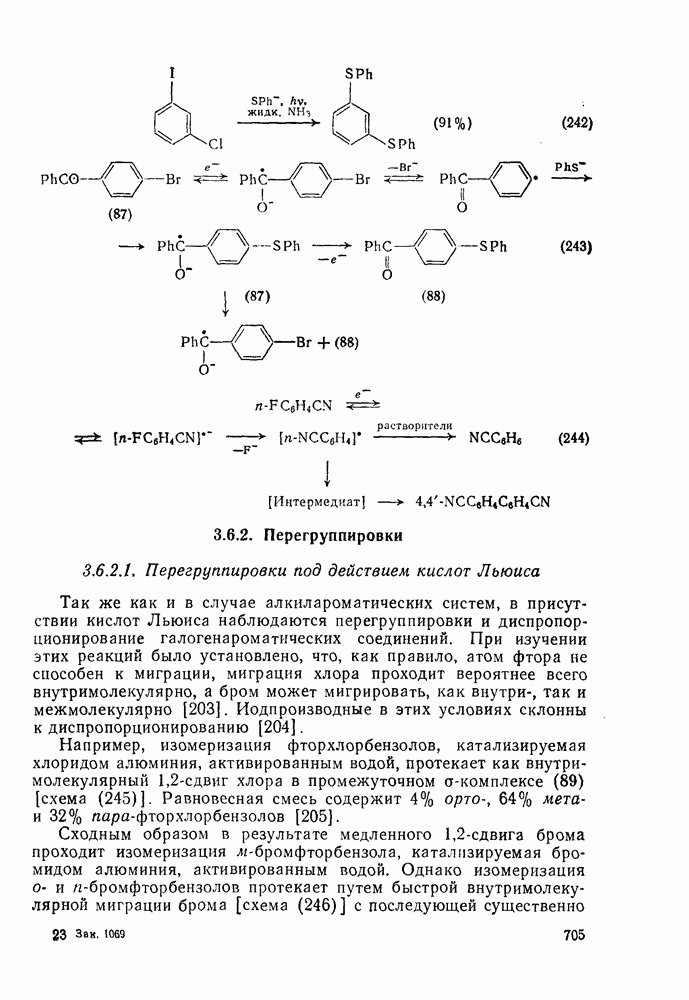
- 3.6.1.4. Перенос электрона
- 3.6.2. Перегруппировки
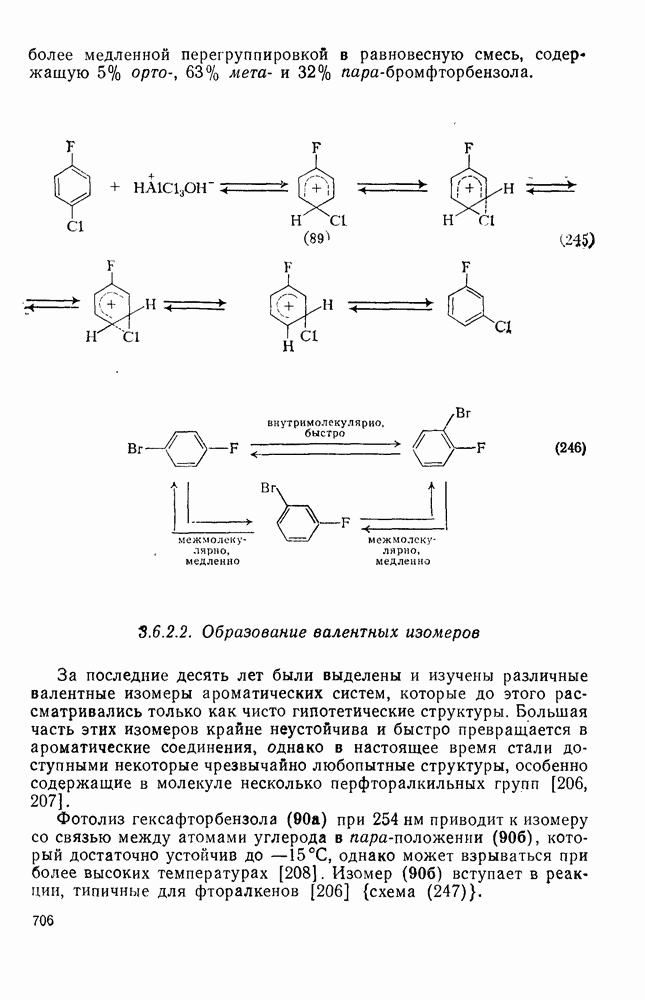
- 3.6.2.1. Перегруппировки под действием кислот Льюиса
- 3.6.2.2. Образование валентных изомеров