| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
2.5.11. ОКИСЛЕНИЕ АРЕНОВ [153]
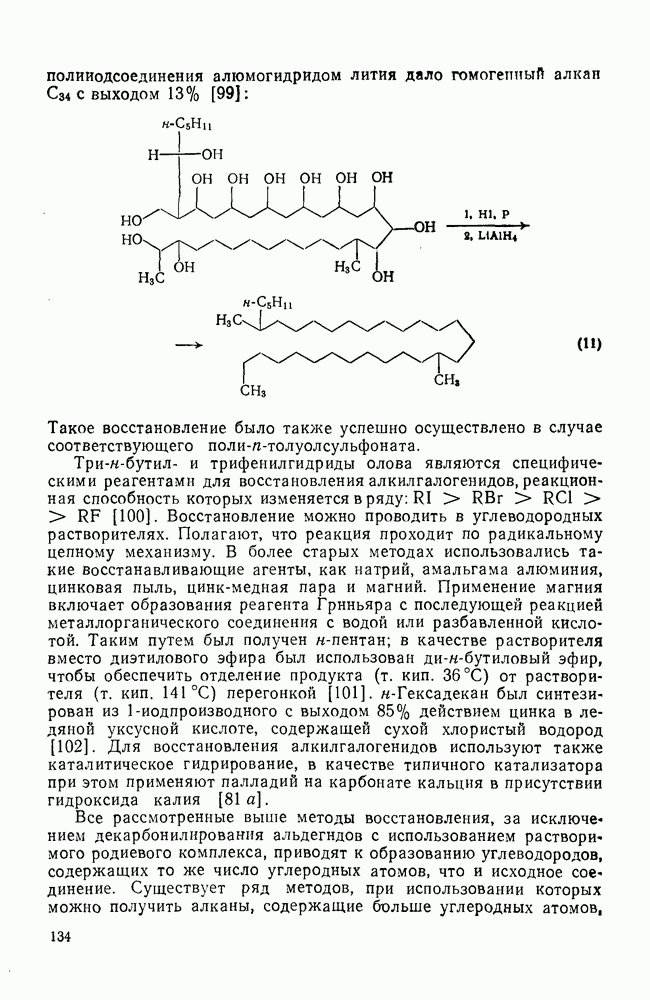
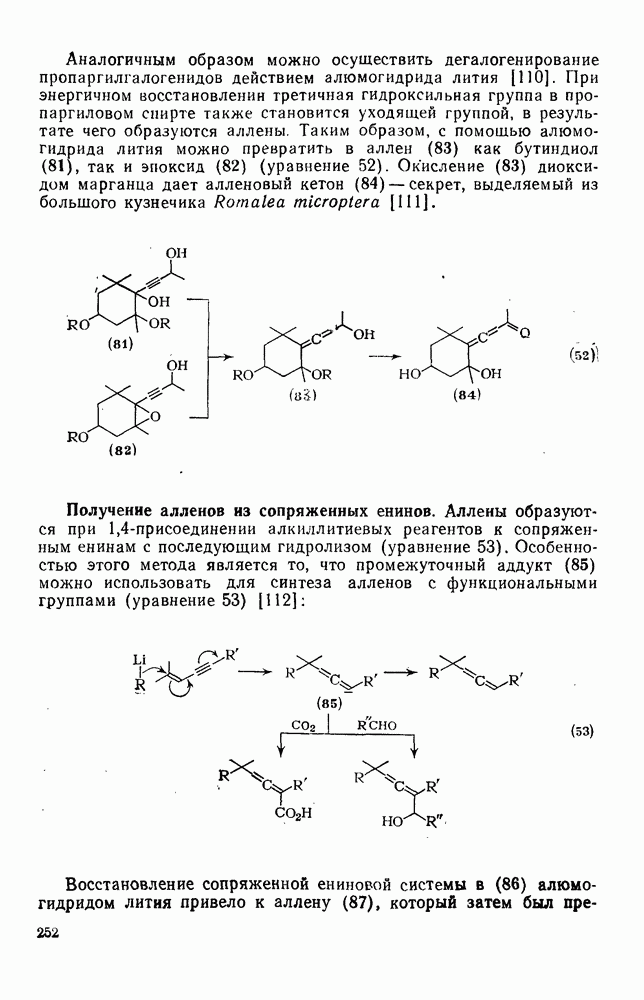
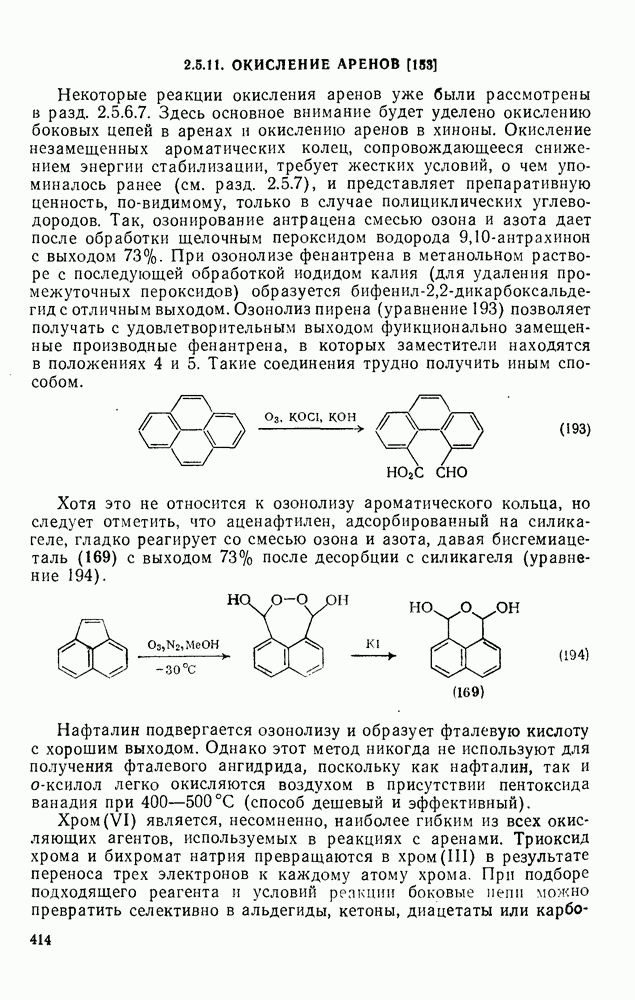
Некоторые реакции окисления аренов уже были рассмотрены в разд. 2.5.6.7. Здесь основное внимание будет уделено окислению боковых цепей в аренах и окислению аренов в хиноны. Окисление незамещенных ароматических колец, сопровождающееся снижением энергии стабилизации, требует жестких условий, о чем упоминалось ранее (см. разд. 2.5.7), и представляет препаративную ценность, по-видимому, только в случае полициклических углеводородов. Так, озонирование антрацена смесью озона и азота дает после обработки щелочным пероксидом водорода 9,10-антрахинон с выходом  . При озонолизе фенантрена в метанольном растворе с последующей обработкой иодидом калия (для удаления промежуточных пероксидов) образуется
. При озонолизе фенантрена в метанольном растворе с последующей обработкой иодидом калия (для удаления промежуточных пероксидов) образуется  с отличным выходом. Озонолиз пирена (уравнение 193) позволяет получать с удовлетворительным выходом функционально замещенные производные фенантрена, в которых заместители находятся в положениях 4 и 5. Такие соединения трудно получить иным способом.
с отличным выходом. Озонолиз пирена (уравнение 193) позволяет получать с удовлетворительным выходом функционально замещенные производные фенантрена, в которых заместители находятся в положениях 4 и 5. Такие соединения трудно получить иным способом.

Хотя это не относится к озонолизу ароматического кольца, но следует отметить, что аценафтилен, адсорбированный на силикагеле, гладко реагирует со смесью озона и азота, давая бисгемиацеталь (169) с выходом 73% после десорбции с силикагеля (уравнение 194).

Нафталин подвергается озонолизу и образует фталевую кислоту с хорошим выходом. Однако этот метод никогда не используют для получения фталевого ангидрида, поскольку как нафталин, так и  -ксилол легко окисляются воздухом в присутствии пентоксида ванадия при
-ксилол легко окисляются воздухом в присутствии пентоксида ванадия при  (способ дешевый и эффективный).
(способ дешевый и эффективный).
Хром(VI) является, несомненно, наиболее гибким из всех окисляющих агентов, используемых в реакциях с аренами. Триоксид хрома и бихромат натрия превращаются в хром(III) в результате переноса трех электронов к каждому атому хрома. При подборе подходящего реагента и условий реакции боковые цепи можно превратить селективно в альдегиды, кетоны, диацетаты или карбоновые кислоты.
В других условиях полиядерные арены превращаются в хиноны. Так, этилбензол превращается в бензойную кислоту (выход 85%) при действии оксида хрома(III) в водной серной кислоте, но дает ацетофенон (выход 50%) при использовании бихромата в воде при  . При действии хромилхлорида этилбензол дает главным образом фенилацетальдегид. Хромилацетат окисляет
. При действии хромилхлорида этилбензол дает главным образом фенилацетальдегид. Хромилацетат окисляет  -нитротолуол до
-нитротолуол до  -нитробензальдегида с выходом 65%. Реакции
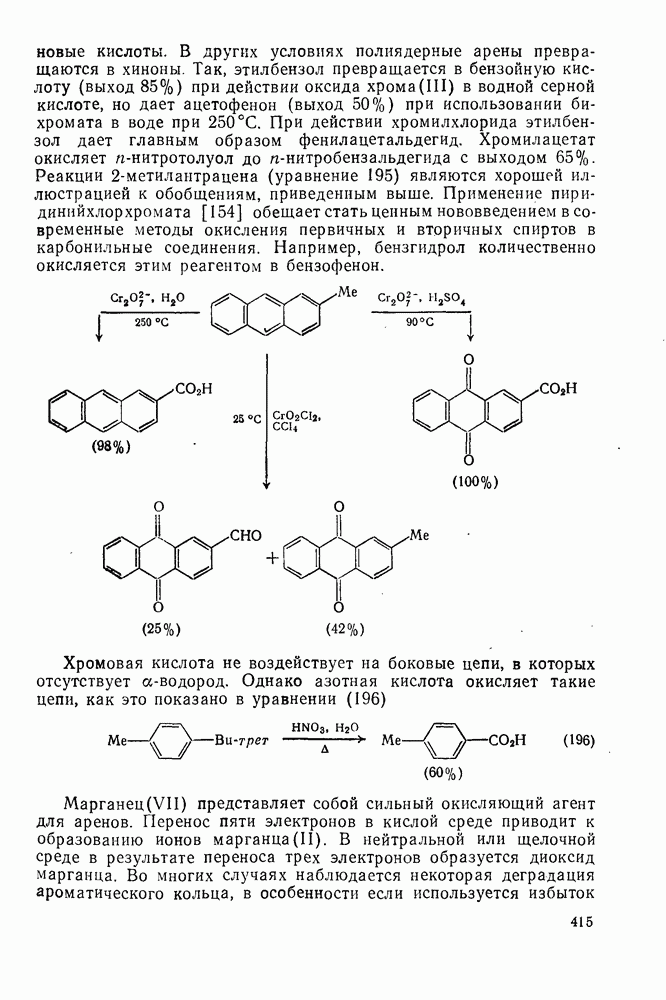
-нитробензальдегида с выходом 65%. Реакции  -метилантрацена (уравнение 195) являются хорошей иллюстрацией к обобщениям, приведенным выше. Применение пиридинийхлорхромата [154] обещает стать ценным нововведением в современные методы окисления первичных и вторичных спиртов в карбонильные соединения. Например, бензгидрол количественно окисляется этим реагентом в бензофенон.
-метилантрацена (уравнение 195) являются хорошей иллюстрацией к обобщениям, приведенным выше. Применение пиридинийхлорхромата [154] обещает стать ценным нововведением в современные методы окисления первичных и вторичных спиртов в карбонильные соединения. Например, бензгидрол количественно окисляется этим реагентом в бензофенон.

Хромовая кислота не воздействует на боковые цепи, в которых отсутствует  -водород. Однако азотная кислота окисляет такие цепи, как это показано в уравнении (196)
-водород. Однако азотная кислота окисляет такие цепи, как это показано в уравнении (196)

Марганец (VII) представляет собой сильный окисляющий агент для аренов. Перенос пяти электронов в кислой среде приводит к образованию ионов  . В нейтральной или щелочной среде в результате переноса трех электронов образуется диоксид марганца. Во многих случаях наблюдается некоторая деградация ароматического кольца, в особенности если используется избыток перманганата.
. В нейтральной или щелочной среде в результате переноса трех электронов образуется диоксид марганца. Во многих случаях наблюдается некоторая деградация ароматического кольца, в особенности если используется избыток перманганата.
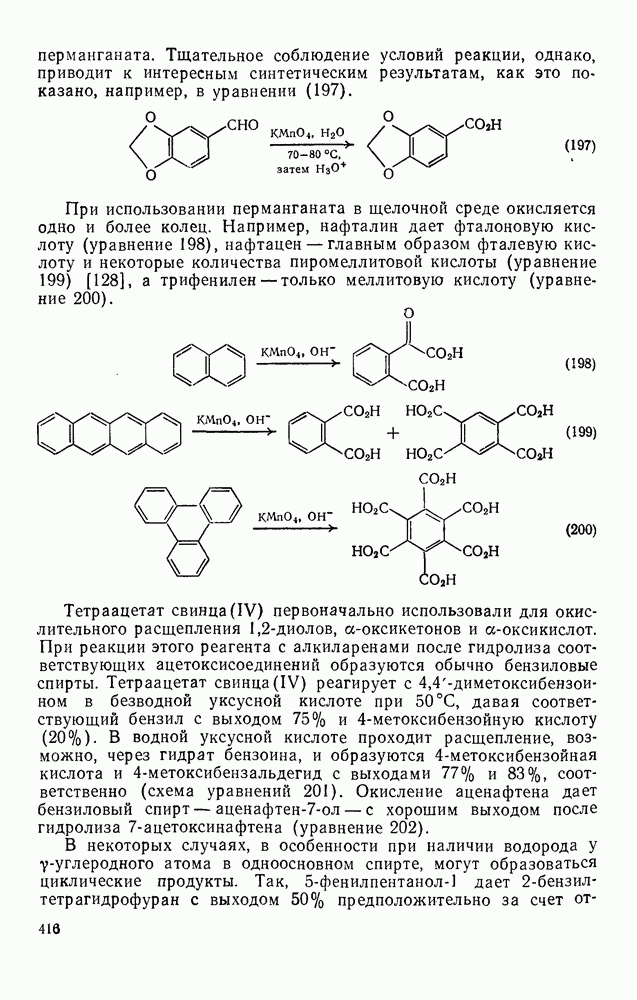
Тщательное соблюдение условий реакции, однако, приводит к интересным синтетическим результатам, как это показано, например, в уравнении (197).

При использовании перманганата в щелочной среде окисляется одно и более колец. Например, нафталин дает фталоновую кислоту (уравнение 198), нафтацен — главным образом фталевую кислоту и некоторые количества пиромеллитовой кислоты (уравнение 199) [128], а трифенилен — только меллитовую кислоту (уравнение 200).

Тетраацетат свинца(IV) первоначально использовали для окислительного расщепления 1,2-диолов,  -оксикетонов и
-оксикетонов и  -оксикислот. При реакции этого реагента с алкиларенами после гидролиза соответствующих ацетоксисоединений образуются обычно бензиловые спирты. Тетраацетат свинца(IV) реагирует с
-оксикислот. При реакции этого реагента с алкиларенами после гидролиза соответствующих ацетоксисоединений образуются обычно бензиловые спирты. Тетраацетат свинца(IV) реагирует с  -диметоксибензои-ном в безводной уксусной кислоте при
-диметоксибензои-ном в безводной уксусной кислоте при  , давая соответствующий бензил с выходом 75% и
, давая соответствующий бензил с выходом 75% и  -метоксибензойную кислоту
-метоксибензойную кислоту  . В водной уксусной кислоте проходит расщепление, возможно, через гидрат бензоина, и образуются
. В водной уксусной кислоте проходит расщепление, возможно, через гидрат бензоина, и образуются  -метоксибензойная кислота и
-метоксибензойная кислота и  -метоксибензальдегид с выходами 77% и 83%, соответственно (схема уравнений 201). Окисление аценафтена дает бензиловый
-метоксибензальдегид с выходами 77% и 83%, соответственно (схема уравнений 201). Окисление аценафтена дает бензиловый  — с хорошим выходом после гидролиза
— с хорошим выходом после гидролиза  -ацетоксинафтена (уравнение 202).
-ацетоксинафтена (уравнение 202).
В некоторых случаях, в особенности при наличии водорода у  -углеродного атома в одноосновном спирте, могут образоваться циклические продукты. Так,
-углеродного атома в одноосновном спирте, могут образоваться циклические продукты. Так,  дает 2-бензилтетрагидрофуран с выходом 50% предположительно за счет отрыва
дает 2-бензилтетрагидрофуран с выходом 50% предположительно за счет отрыва  -водорода алкоксирадикалом.
-водорода алкоксирадикалом.
Интересно отметить, что возможные продукты за счет отрыва водорода из  -положения, даже, если в реакции участвовали бензильные радикалы, ни разу не были обнаружены.
-положения, даже, если в реакции участвовали бензильные радикалы, ни разу не были обнаружены.
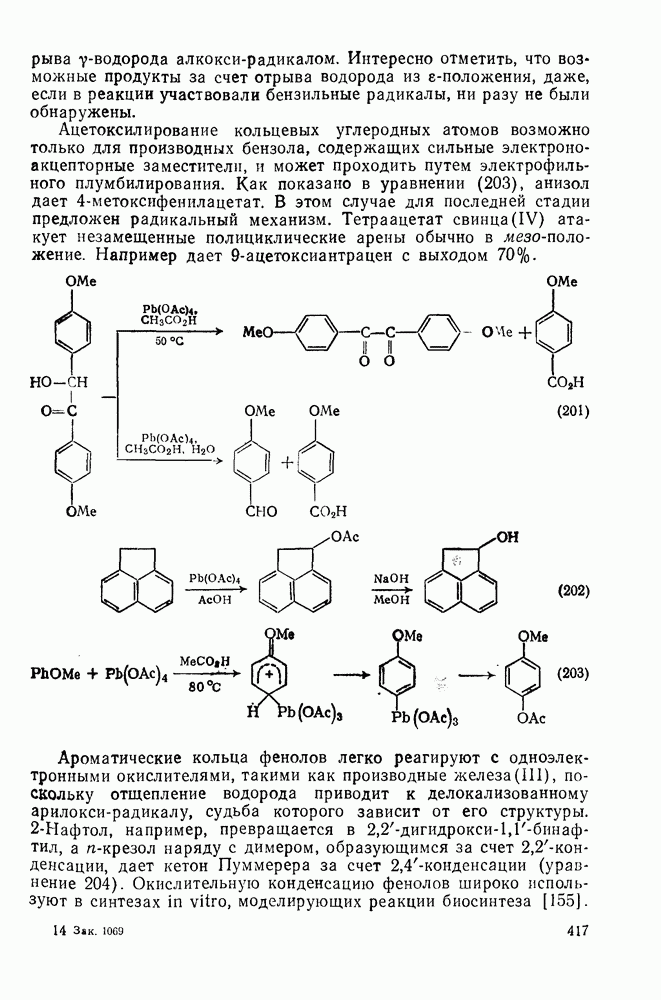
Ацетоксилирование кольцевых углеродных атомов возможно только для производных бензола, содержащих сильные электроноакцепторные заместители, и может проходить путем электрофильного плумбилирования. Как показано в уравнении (203), анизол дает  -метоксифенилацетат. В этом случае для последней стадии предложен радикальный механизм. Тетраацетат свинца(IV) атакует незамещенные полициклические арены обычно в мезо-положение. Например дает
-метоксифенилацетат. В этом случае для последней стадии предложен радикальный механизм. Тетраацетат свинца(IV) атакует незамещенные полициклические арены обычно в мезо-положение. Например дает  -ацетоксиантрацен с выходом 70%.
-ацетоксиантрацен с выходом 70%.

Ароматические кольца фенолов легко реагируют с одноэлектронными окислителями, такими как производные железа(III), поскольку отщепление водорода приводит к делокализованному арилокси-радикалу, судьба которого зависит от его структуры.  -Нафтол, например, превращается в
-Нафтол, например, превращается в  , а
, а  -крезол наряду с димером, образующимся за счет
-крезол наряду с димером, образующимся за счет  -кон-денсации, дает кетон Пуммерера за счет
-кон-денсации, дает кетон Пуммерера за счет  -конденсации (уравнение 204). Окислительную конденсацию фенолов широко используют в синтезах
-конденсации (уравнение 204). Окислительную конденсацию фенолов широко используют в синтезах  vitro, моделирующих реакции биосинтеза [155].
vitro, моделирующих реакции биосинтеза [155].
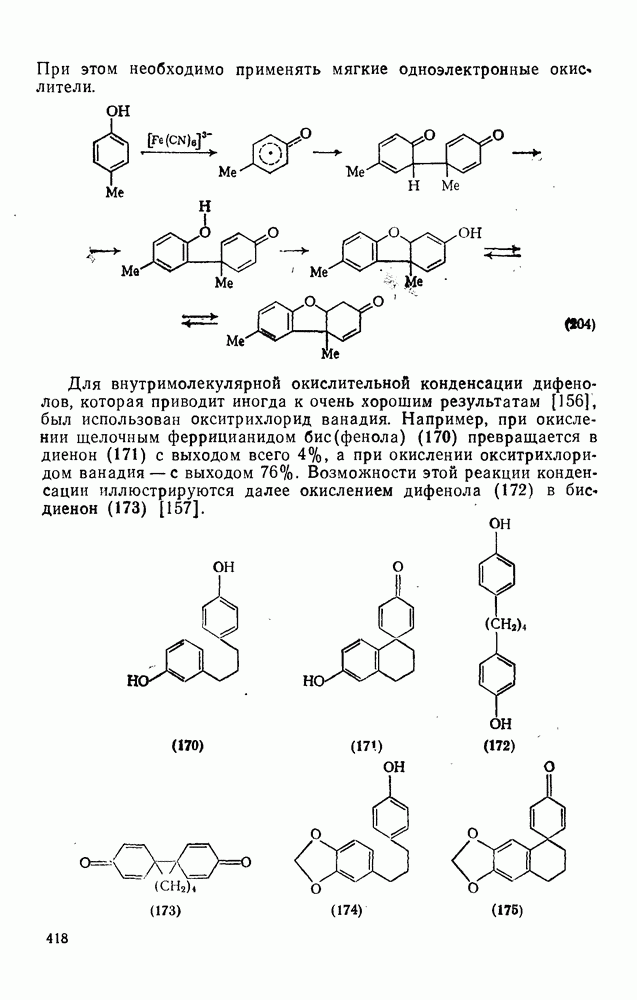
При этом необходимо применять мягкие одноэлектронные окислители.

Для внутримолекулярной окислительной конденсации дифенолов, которая приводит иногда к очень хорошим результатам [156], был использован окситрихлорид ванадия. Например, при окислении щелочным феррицианидом бис(фенола) превращается в диенон (171) с выходом всего 4%, а при окислении окситрихлоридом ванадия — с выходом 76%. Возможности этой реакции конденсации иллюстрируются далее окислением дифенола (172) в бис-диенон (173) [157].


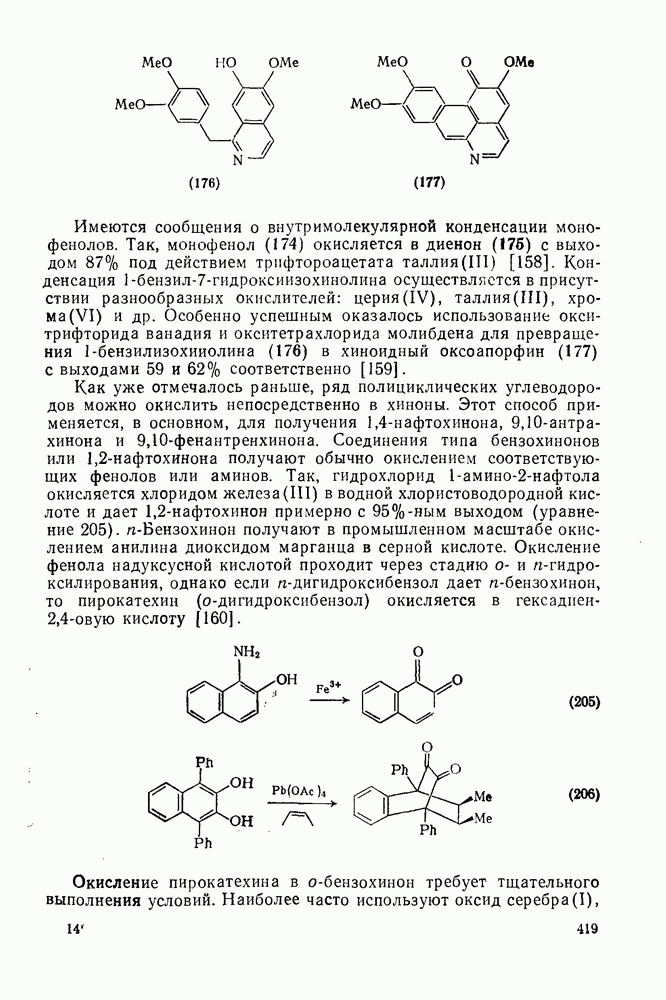
Имеются сообщения о внутримолекулярной конденсации монофенолов. Так, монофенол (174) окисляется в диенон (176) с выходом 87% под действием трифтороацетата  [158]. Конденсация
[158]. Конденсация  осуществляется в присутствии разнообразных окислителей: церия (IV), таллия(III), хрома (VI) и др. Особенно успешным оказалось использование окси-трифторида ванадия и окситетрахлорида молибдена для превращения
осуществляется в присутствии разнообразных окислителей: церия (IV), таллия(III), хрома (VI) и др. Особенно успешным оказалось использование окси-трифторида ванадия и окситетрахлорида молибдена для превращения  -бензилизохииолина (176) в хиноидный оксоапорфин (177) с выходами 59 и 62% соответственно [159].
-бензилизохииолина (176) в хиноидный оксоапорфин (177) с выходами 59 и 62% соответственно [159].
Как уже отмечалось раньше, ряд полициклических углеводородов можно окислить непосредственно в хиноны. Этот способ применяется, в основном, для получения  -нафтохинона,
-нафтохинона,  -антрахинона и
-антрахинона и  -фенантренхинона. Соединения типа бензохинонов или
-фенантренхинона. Соединения типа бензохинонов или  -нафтохинона получают обычно окислением соответствующих фенолов или аминов. Так, гидрохлорид
-нафтохинона получают обычно окислением соответствующих фенолов или аминов. Так, гидрохлорид  окисляется хлоридом железа(III) в водной хлористоводородной кислоте и дает
окисляется хлоридом железа(III) в водной хлористоводородной кислоте и дает  -нафтохинон примерно с
-нафтохинон примерно с  -ным выходом (уравнение 205).
-ным выходом (уравнение 205).  -Бензохинон получают в промышленном масштабе окислением анилина диоксидом марганца в серной кислоте. Окисление фенола надуксусной кислотой проходит через стадию
-Бензохинон получают в промышленном масштабе окислением анилина диоксидом марганца в серной кислоте. Окисление фенола надуксусной кислотой проходит через стадию  - и
- и  -гидроксилирования, однако если
-гидроксилирования, однако если  -дигидроксибензол дает п-бензохинон, то пирокатехин (о-дигидроксибензол) окисляется в
-дигидроксибензол дает п-бензохинон, то пирокатехин (о-дигидроксибензол) окисляется в  кислоту [160].
кислоту [160].

Окисление пирокатехина в  -бензохинон требует тщательного выполнения условий. Наиболее часто используют оксид серебра(I), суспендированный в эфире вместе с осушителем, хотя применялись и другие окислители, такие как периодат.
-бензохинон требует тщательного выполнения условий. Наиболее часто используют оксид серебра(I), суспендированный в эфире вместе с осушителем, хотя применялись и другие окислители, такие как периодат.
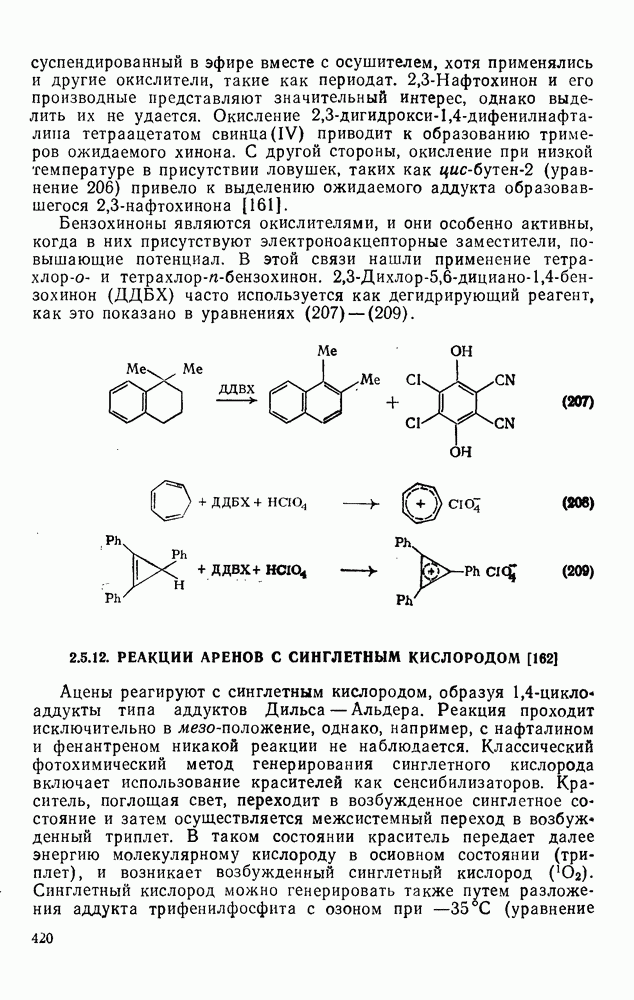
2,3-Нафтохинон и его производные представляют значительный интерес, однако выделить их не удается. Окисление  тетраацетатом свинца(IV) приводит к образованию тримеров ожидаемого хинона. С другой стороны, окисление при низкой температуре в присутствии ловушек, таких как цис-
тетраацетатом свинца(IV) приводит к образованию тримеров ожидаемого хинона. С другой стороны, окисление при низкой температуре в присутствии ловушек, таких как цис- (уравнение 206) привело к выделению ожидаемого аддукта образовавшегося
(уравнение 206) привело к выделению ожидаемого аддукта образовавшегося  -нафтохинона [161].
-нафтохинона [161].
Бензохиноны являются окислителями, и они особенно активны, когда в них присутствуют электроноакцепторные заместители, повышающие потенциал. В этой связи нашли применение тетра-хлор-о- и тетрахлор- -бензохинон.
-бензохинон.  (ДДБХ) часто используется как дегидрирующий реагент, как это показано в уравнениях
(ДДБХ) часто используется как дегидрирующий реагент, как это показано в уравнениях  .
.

| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- ПРЕДИСЛОВИЕ
- ИЗ ПРЕДИСЛОВИЯ К ТОМУ 1 АНГЛИЙСКОГО ИЗДАНИЯ
- ЧАСТЬ I. НОМЕНКЛАТУРА И СТЕРЕОХИМИЯ
- 1.1. ВВЕДЕНИЕ И СТЕРЕОХИМИЯ
- 1.1.2. СИММЕТРИЯ И ХИРАЛЬНОСТЬ
- 1.1.3. ХИМИЧЕСКАЯ ТОПОЛОГИЯ
- 1.1.4. ИЗОМЕРИЯ
- 1.1.4.2. Строение
- 1.1.4.3. Абсолютная конфигурация
- 1.1.4.4. Относительная конфигурация
- 1.1.4.5. Конформация
- 1.1.4.6. Концепция изомерии
- 1.1.5. ТОПИЗМ
- 1.1.5.2. Прохиральность
- 1.1.5.3. Псевдоасимметрия (псевдохиральность)
- 1.1.6. ТОПОМЕРИЯ
- 1.1.7. ДИНАМИЧЕСКАЯ СТЕРЕОХИМИЯ. КРАТКИЕ СВЕДЕНИЯ
- ЧАСТЬ 2. УГЛЕВОДОРОДЫ
- 2.1. НАСЫЩЕННЫЕ УГЛЕВОДОРОДЫ
- 2.1.2. Строение и номенклатура
- 2.1.2.1. Номенклатура IUPAC
- 2.1.2.2. Алициклические алканы
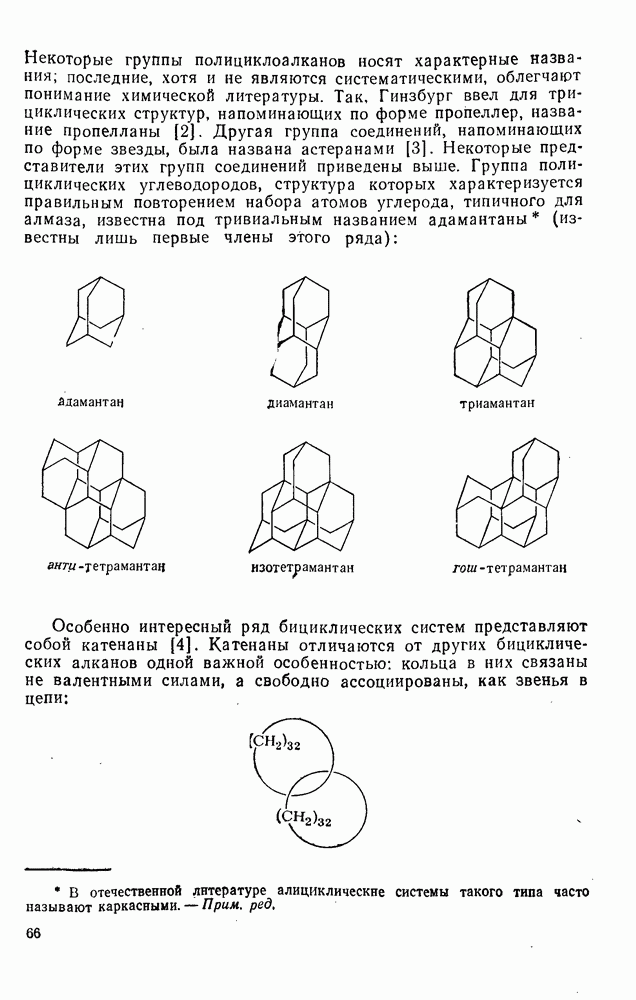
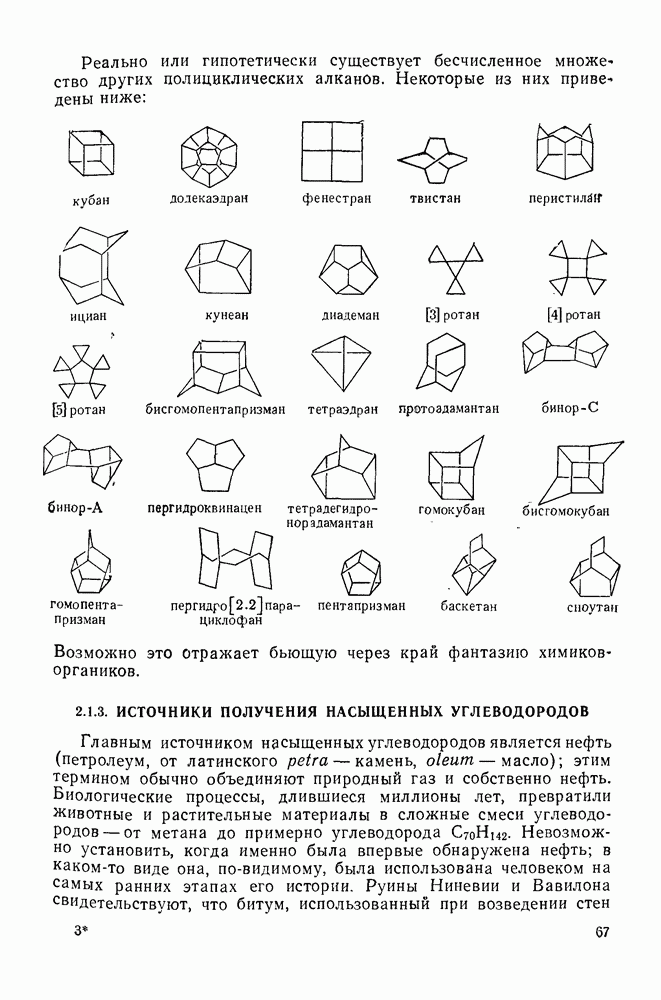
- 2.1.2.3. Полициклоалканы
- 2.1.3. ИСТОЧНИКИ ПОЛУЧЕНИЯ НАСЫЩЕННЫХ УГЛЕВОДОРОДОВ
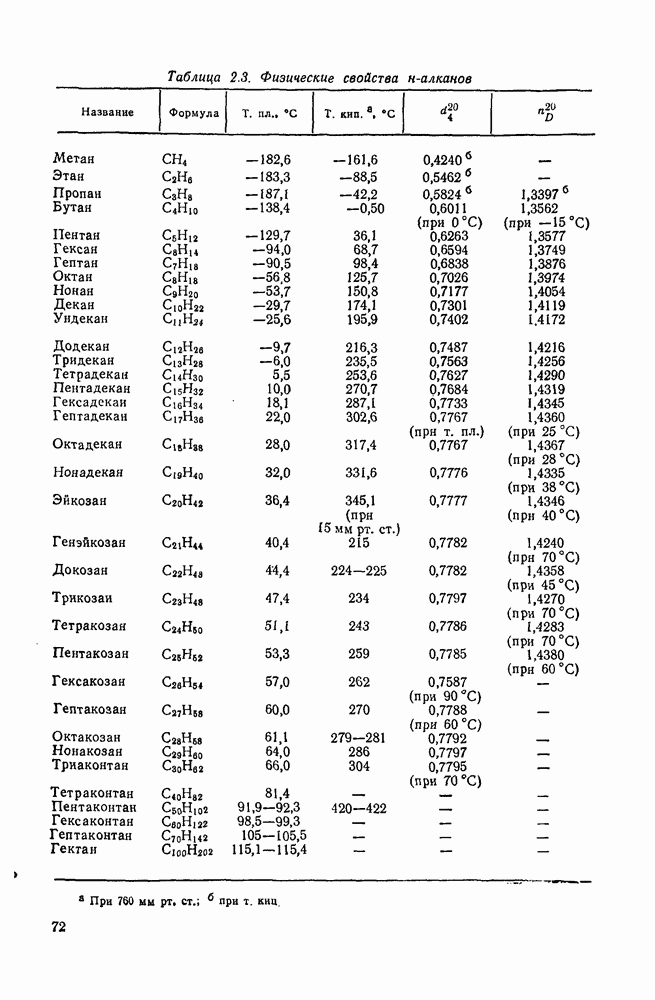
- 2.1.4. ФИЗИЧЕСКИЕ СВОЙСТВА
- 2.1.4.1. Ациклические алканы
- 2.1.4.2. Моно- и полициклоалканы
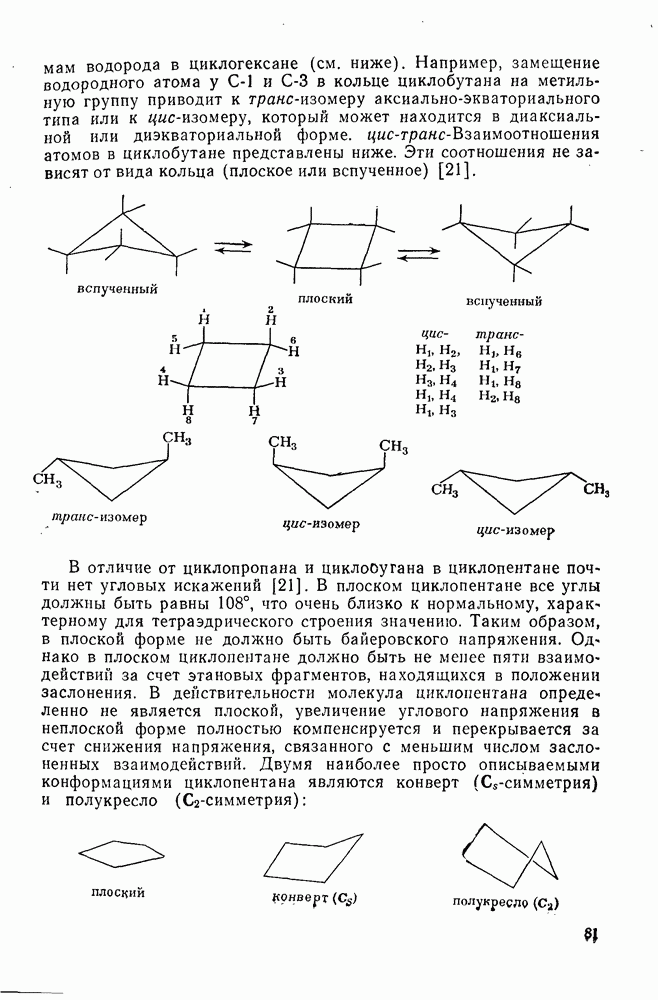
- 2.1.5. СТЕРЕОХИМИЯ И КОНФОРМАЦИОННЫЙ АНАЛИЗ
- 2.1.5.1. Углы и длины связей
- 2.1.5.2. Алкил- и полиалкилциклогексаны
- 2.1.5.3. Конформация карбоциклических колец, больших, чем циклогексан
- 2.1.6. ТЕРМОХИМИЧЕСКИЕ СВОЙСТВА
- 2.1.6.1. Горение. Алканы и циклоалканы как топливо
- 2.1.6.2. Определение теплот сгорания и термохимические свойства
- 2.1.6.3. Эмпирические методы оценки теплот образования алканов
- 2.1.6.4. Оценка теплот образования алканов на основе энергии связей
- 2.1.6.5. Оценка теплот образования алканов на основе инкрементов групп
- 2.1.6.6. Оценка теплот образования циклических, полициклических и мостиковых алканов на основе инкрементов «скошенных разобщенных» групп и «единственных» наиболее устойчивых конформаций
- 2.1.6.7. Молекулярно-механические расчеты теплот образования и энергии напряжения
- 2.1.6.8. Моно- и полициклоалкаиы
- 2.1.7. ПОЛУЧЕНИЕ АЦИКЛИЧЕСКИХ АЛКАНОВ
- 2.1.7.1. Получение алканов восстановлением олефинов
- 2.1.7.2. Получение алканов из альдегидов и кетонов
- 2.1.7.3. Получение алканов из спиртов и алкилгалогенидов
- 2.1.7.4. Получение алканов из карбоновых кислот
- 2.1.8. СИНТЕЗ МОНО- И ПОЛИЦИКЛОАЛКАНОВ
- 2.1.9. РЕАКЦИИ АЦИКЛИЧЕСКИХ АЛКАНОВ
- 2.1.9.1. Галогенирование
- 2.1.9.2. Нитрование
- 2.1.9.3. Окисление
- 2.1.9.4. Каталитическая изомеризация алканов
- 2.1.9.5. Каталитическое алкилирование алканов
- 2.1.9.6. Реакции крекинга алканов
- 2.1.9.7. Термический крекинг
- 2.1.9.8. Каталитический крекинг
- 2.1.9.9. Каталитический риформинг и дегидроциклизация алканов
- 2.1.10. РЕАКЦИИ ЦИКЛОАЛКАНОВ И ПОЛИЦИКЛОАЛКАНОВ
- 2.2. ОЛЕФИНОВЫЕ И АЦЕТИЛЕНОВЫЕ УГЛЕВОДОРОДЫ
- 2.2.2. ПОЛУЧЕНИЕ ОЛЕФИНОВ
- 2.2.2.1. Элиминирование в системах
- 2.2.2.2. Элиминирование из систем
- 2.2.2.3. Циклоэлиминирование
- 2.2.2.4. Частичное восстановление
- 2.2.2.5. Элиминирование сульфонилгидразонов
- 2.2.2.6. Реакция Виттига и родственные ей реакции
- 2.2.2.7. Различные реакции конденсации
- 2.2.2.8. Электроциклические реакции
- 2.2.2.9. Циклоолигомеризация
- 2.2.2.11. Реакции винильных производных
- 2.2.3. РЕАКЦИИ ОЛЕФИНОВ
- 2.2.3.1. Электрофильное присоединение
- 2.2.3.2. Нуклеофильное присоединение
- 2.2.3.3. Радикальное присоединение
- 2.2.3.4. Циклоприсоединение и родственные реакции
- 2.2.3.5. Окисление
- 2.2.3.6. Восстановление
- 2.2.3.7. Перегруппировки
- 2.2.3.8. Фотохимические реакции
- 2.2.3.9. Прочие реакции
- 2.3. ДИЕНЫ, ПОЛНЕНЫ И АЦЕТИЛЕНОВЫЕ УГЛЕВОДОРОДЫ
- 2.3.1. СОПРЯЖЕННЫЕ ДИЕНЫ И ПОЛНЕНЫ
- 2.3.1.2. Получение сопряженных диенов
- 2.3.2. РЕАКЦИИ СОПРЯЖЕННЫХ ДИЕНОВ
- 2.3.2.2. Восстановление
- 2.3.2.3. Гидроборирование
- 2.3.2.4. Реакция Дильса — Альдера
- 2.3.2.5. Комплексы с карбонилами железа
- 2.3.2.6. Фотохимические термические реакции
- 2.3.2.7. Прочие реакции
- 2.3.3. СОПРЯЖЕННЫЕ ПОЛИЕНЫ
- 2.3.4. ПРИРОДНЫЕ ДИЕНЫ И ПОЛНЕНЫ
- 2.3.5. АЛЛЕНЫ И КУМУЛЕНЫ
- 2.3.5.2. Получение алленов
- 2.3.6. РЕАКЦИИ АЛЛЕНОВ
- 2.3.6.2. Гидрирование
- 2.3.6.3. Реакции алленов в присутствии комплексов металлов
- 2.3.7. КУМУЛЕНЫ
- 2.3.8. ПРИРОДНЫЕ АЛЛЕНЫ И КУМУЛЕНЫ
- 2.3.9. АЦЕТИЛЕНЫ И ПОЛИАЦЕТИЛЕНЫ
- 2.3.9.2. Получение ацетиленов
- 2.3.10. РЕАКЦИИ АЦЕТИЛЕНОВ
- 2.3.10.2. Изомеризация
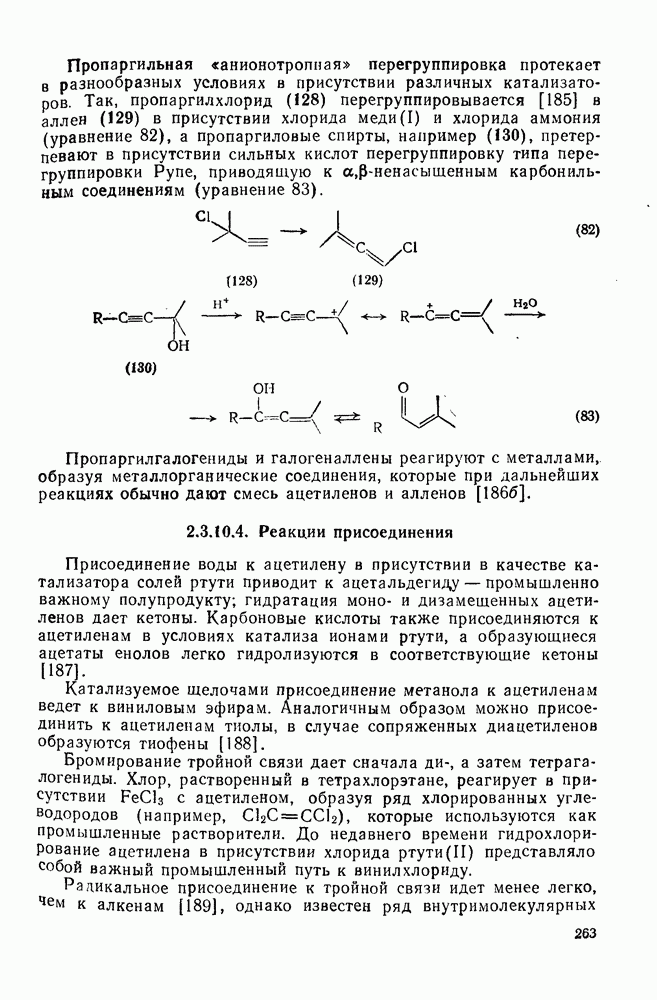
- 2.3.10.3. Пропаргильные перегруппировки
- 2.3.10.4. Реакции присоединения
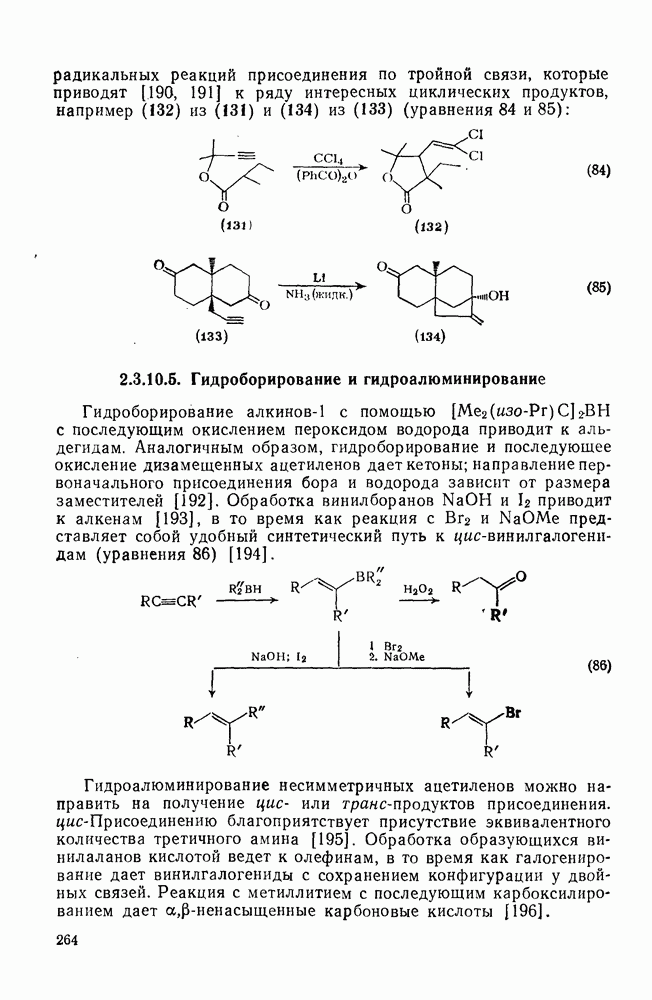
- 2.3.10.5. Гидроборирование и гидроалюминирование
- 2.3.10.6. Реакции замещения
- 2.3.10.7. Восстановление
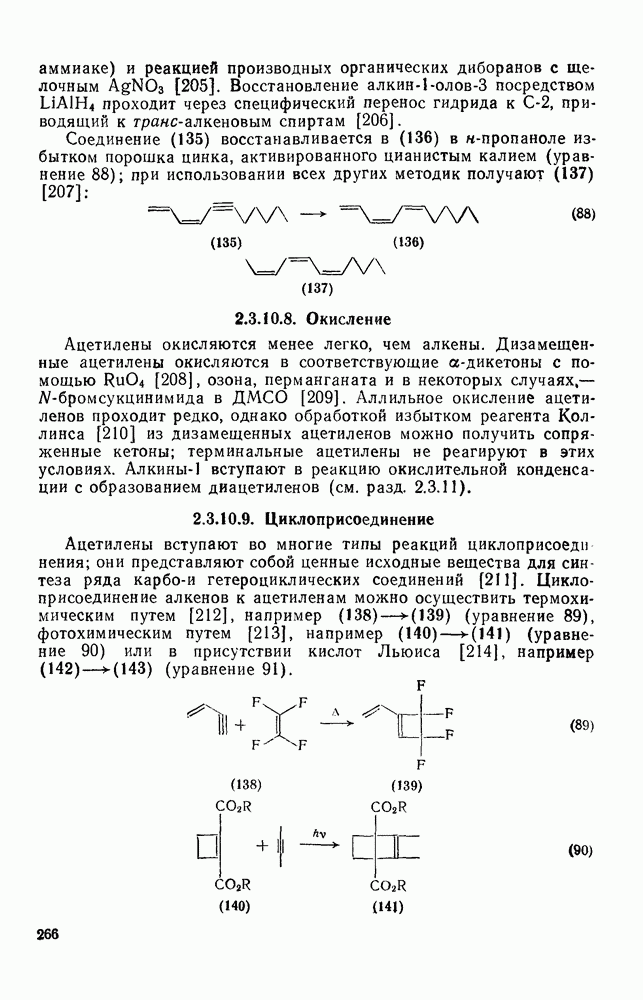
- 2.3.10.8. Окисление
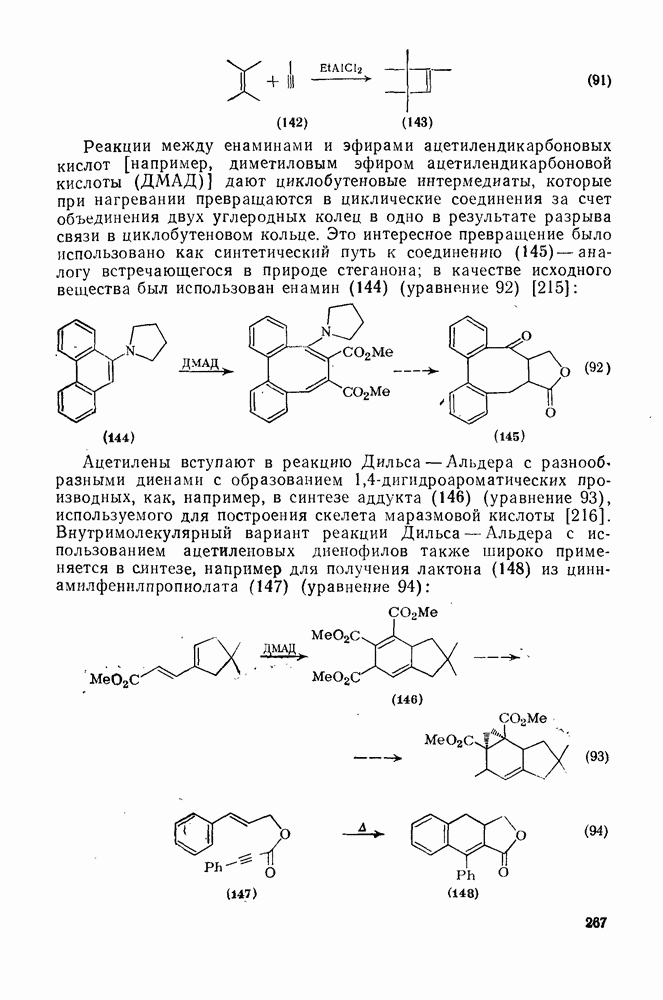
- 2.3.10.9. Циклоприсоединение
- 2.3.10.10. Реакции катализуемые металлами
- 2.3.11. ПОЛИАЦЕТИЛЕНЫ
- 2.3.12. ПРИРОДНЫЕ АЦЕТИЛЕНЫ И ПОЛИАЦЕТИЛЕНЫ
- 2.3.13. СОПРЯЖЕННЫЕ ЕНИНЫ
- 2.3.13.1. Получение сопряженных енинов
- 2.3.14. РЕАКЦИИ СОПРЯЖЕННЫХ ЕНИНОВ
- 2.3.15. ПРИРОДНЫЕ СОПРЯЖЕННЫЕ ЕНИНЫ
- 2.4. АРОМАТИЧНОСТЬ
- 2.4.2. ЭЛЕКТРОННЫЕ ТЕОРИИ СТРОЕНИЯ БЕНЗОЛА
- 2.4.3. КРИТЕРИИ АРОМАТИЧНОСТИ
- 2.4.3.1. Термодинамические свойства
- 2.4.3.2. Структурные особенности
- 2.4.3.3. Магнитные свойства
- 2.4.3.4. Прочие критерии
- 2.4.4. АНТИАРОМАТИЧНОСТЬ
- 2.4.4.1. Термодинамические свойства
- 2.4.4.2. Структурные особенности
- 2.4.4.3. Магнитные свойства
- 2.4.4.4. Прочие свойства
- 2.4.5. ТЕОРЕТИЧЕСКИЕ ОПРЕДЕЛЕНИЯ АРОМАТИЧНОСТИ
- 2.4.5.1. Полуэмпирические расчеты и дьюаровская резонансная энергия
- 2.4.5.2. Расчеты по методу валентных пар и применение резонансного метода
- 2.4.5.3. Локализация связей
- 2.4.5.4. Связь энергетических критериев с критериями локализации связей
- 2.4.6. АРОМАТИЧЕСКИЕ ПЕРЕХОДНЫЕ СОСТОЯНИЯ
- 2.5. АРЕНЫ И ИХ РЕАКЦИИ
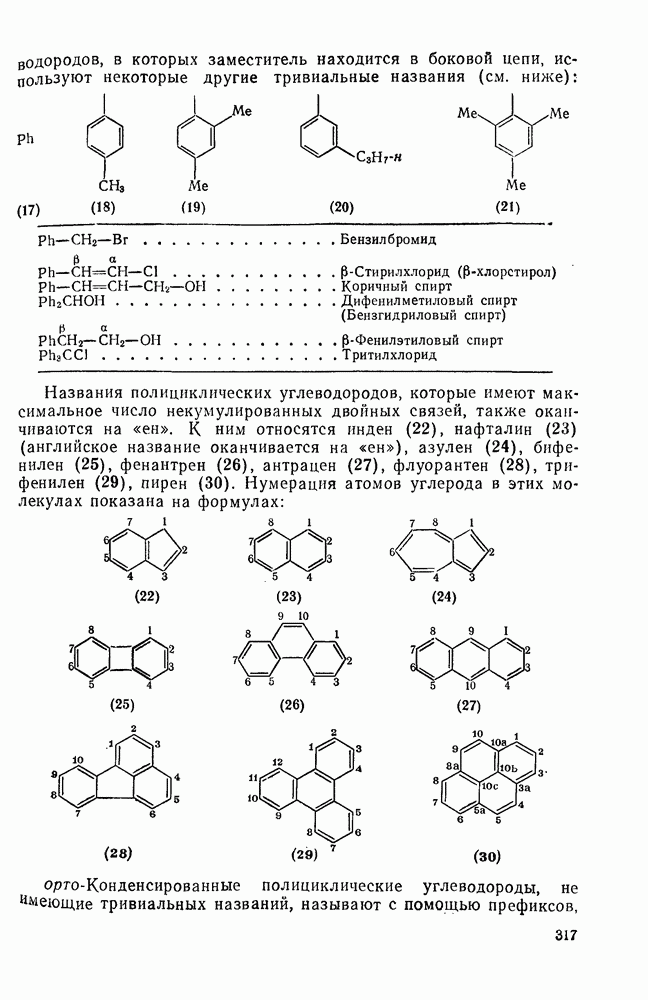
- 2.5.2. НОМЕНКЛАТУРА
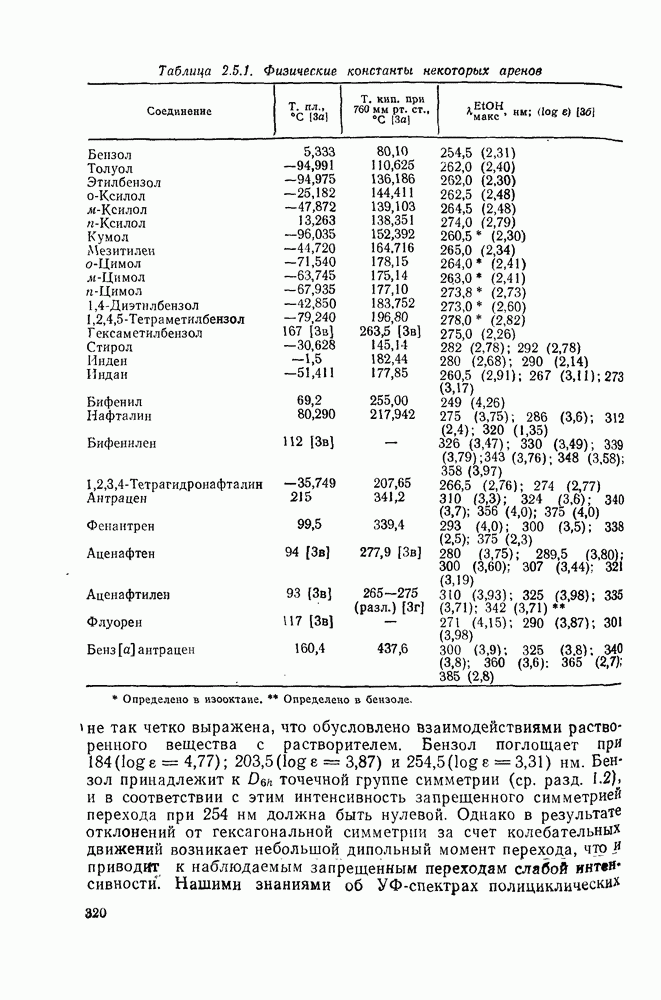
- 2.5.3. ФИЗИЧЕСКИЕ СВОЙСТВА АРЕНОВ
- 2.5.4. ПРОМЫШЛЕННОЕ ПРОИЗВОДСТВО АРЕНОВ
- 2.5.5. ЦИКЛОТРИМЕРИЗАЦИЯ АЦЕТИЛЕНОВ
- 2.5.6. РЕАКЦИИ ЭЛЕКТРОФИЛЬНОГО ПРИСОЕДИНЕНИЯ — ЭЛИМИНИРОВАНИЯ АРЕНОВ
- 2.5.6.1. Механизм ароматического нитрования [15]
- 2.5.6.2. Кинетические изотопные эффекты [21]
- 2.5.6.3. Реакции, включающие ипсо-протонирование
- 2.5.6.4. Металлирование
- 2.5.6.5. Электрофилы IV группы
- 2.5.6.6. Электрофилы V группы
- 2.5.6.7. Электрофилы VI группы [18, 56]
- 2.5.6.8. Электрофилы VII группы [18, 25а, 56]
- 2.5.7. ОРИЕНТАЦИЯ В РЕАКЦИЯХ ЭЛЕКТРОФИЛЬНОГО ПРИСОЕДИНЕНИЯ — ЭЛИМИНИРОВАНИЯ
- 2.5.8. РАДИКАЛЬНОЕ ГАЛОГЕНИРОВАНИЕ АРЕНОВ В БОКОВУЮ ЦЕПЬ [96]
- 2.5.9. РЕАКЦИИ ПРИСОЕДИНЕНИЯ К АРЕНАМ
- 2.5.9.1. Восстановление аренов
- 2.5.9.2. Термическое циклоприсоединение к аренам
- 2.5.9.3. Фотоциклоприсоединение к моноциклическим аренам [126]
- 2.5.9.4. Фотохимические реакции полициклических аренов
- 2.6.10. ФОТОИЗОМЕРИЗАЦИЯ АРЕНОВ [126б]
- 2.5.11. ОКИСЛЕНИЕ АРЕНОВ [153]
- 2.5.12. РЕАКЦИИ АРЕНОВ С СИНГЛЕТНЫМ КИСЛОРОДОМ [162]
- 2.5.13. ПРИГОТОВЛЕНИЕ БИ- И ПОЛИАРИЛОВ
- 2.5.14. ВНУТРИМОЛЕКУЛЯРНАЯ ФОТОЦИКЛИЗАЦИЯ, ПРИВОДЯЩАЯ К ПОЛИЦИКЛИЧЕСКИМ АРЕНАМ
- 2.5.15. ВНУТРИМОЛЕКУЛЯРНАЯ ЦИКЛИЗАЦИЯ ДИЗАМЕЩЕННЫХ АРЕНОВ
- 2.5.16. ЦИКЛОФАНЫ
- 2.5.17. КОНФОРМАЦИЯ И ХИРАЛЬНОСТЬ АРЕНОВ
- 2.5.18. АЗУЛЕНЫ И НЕБЕНЗОИДНЫЕ АРЕНЫ
- 2.6. АННУЛЕНЫ И РОДСТВЕННЫЕ СИСТЕМЫ
- 2.6.2. МЕТОДЫ СИНТЕЗА
- 2.6.2.1. Окислительное сочетание терминальных ацетиленов (метод Зондхеймера)
- 2.6.2.2. Фотооблучение полициклических валентных таутомеров
- 2.6.2.3. Валентная таутомерия типа норкарадиен — циклогептатриен (метод Фогеля)
- 2.6.2.4. Прочие методы
- 2.6.3. СВОЙСТВА АННУЛЕНОВ
- 2.6.4. СВОЙСТВА 4n-АННУЛЕНОВ
- 2.6.5. ДЕГИДРОАННУЛЕНЫ
- 2.6.6. АННЕЛИРОВАННЫЕ АННУЛЕНЫ
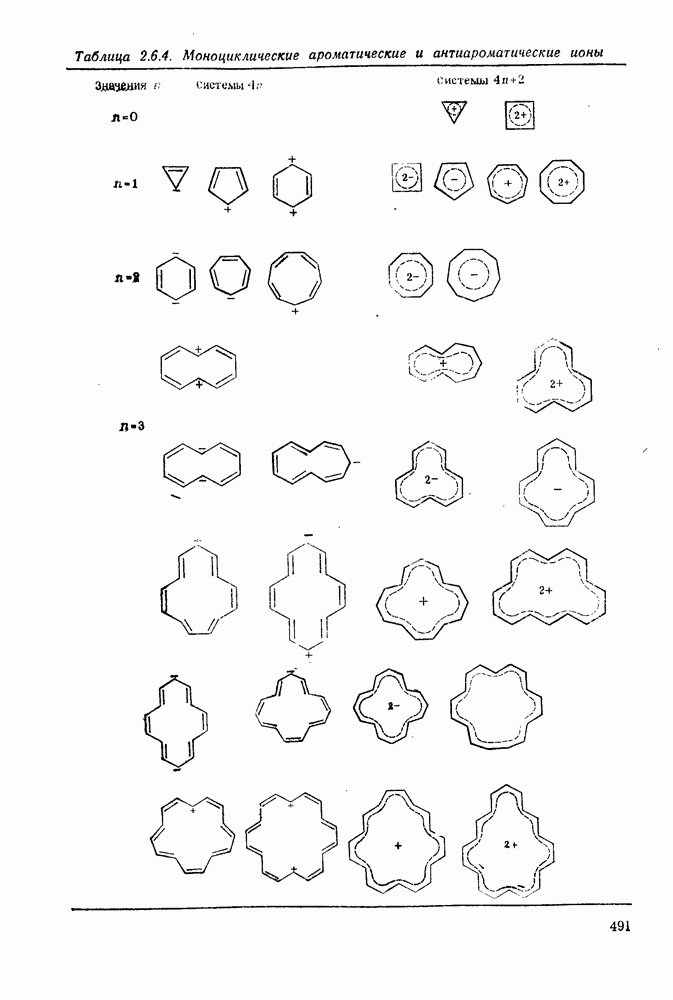
- 2.6.7. АРОМАТИЧЕСКИЕ И АНТИАРОМАТИЧЕСКИЕ МОНОЦИКЛИЧЕСКИЕ ИОНЫ
- 2.6.8. АРОМАТИЧЕСКИЕ И АНТИАРОМАТИЧЕСКИЕ ПОЛИЦИКЛИЧЕСКИЕ ИОНЫ
- 2.6.9. ГОМОАРОМАТИЧЕСКИЕ СИСТЕМЫ
- 2.7. КАРБОКАТИОНЫ И КАРБАНИОНЫ
- 2.7.1.2. Краткий исторический очерк развития химии карбокатионов
- 2.7.1.3. Методы генерации карбокатионов
- 2.7.1.4. Типы карбокатионов
- 2.7.1.5. Изучение карбокатионов: методы и результаты
- 2.7.1.6. Реакции карбокатионов
- 2.7.2. КАРБАНИОНЫ
- 2.7.2.2. Методы генерации карбанионов
- 2.7.2.3. Типы карбанионов
- 2.7.2.4. Физические свойства карбанионов
- 2.7.5.2. Реакции карбанионов
- 2.8. РАДИКАЛЫ, КАРБЕНЫ, АРИНЫ
- 2.8.1. РАДИКАЛЫ
- 2.8.1.1. Структура, устойчивость и реакционная способность радикалов
- 2.8.1.2. Методы генерации и реакции радикалов
- 2.8.2. КАРБЕНЫ
- 2.8.2.1. Методы генерации карбенов и карбеноидов
- 2.8.2.2. Реакции карбенов
- 2.8.3. АРИНЫ
- 2.8.3.1. Структура и спектры аринов
- 2.8.3.2. Методы генерации аринов
- 2.8.3.3. Реакции аринов
- ЧАСТЬ 3. ГАЛОГЕНСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
- 3.2. МЕТОДЫ ГАЛОГЕНИРОВАНИЯ
- 3.2.1. Гомолитическое замещение водорода
- 3.2.1.2. Использование галогенпроизводных в качестве реагентов
- 3.2.2. Гомолитическое замещение функциональных групп
- 3.2.3. Гомолитическое присоединение к ненасыщенным системам
- 3.2.3.1. Присоединение галогеноводородов
- 3.2.3.2. Присоединение галогенов
- 3.2.4. Электрофильное галогенирование
- 3.2.4.1. Замещение у насыщенной связи С-Н
- 3.2.4.2. Реакции с ненасыщенными системами
- 3.2.4.3. Реакции с карбанионами
- 3.2.5. Нуклеофильное галогенирование
- 3.2.5.1. Галогенирование с замещением функциональной группы
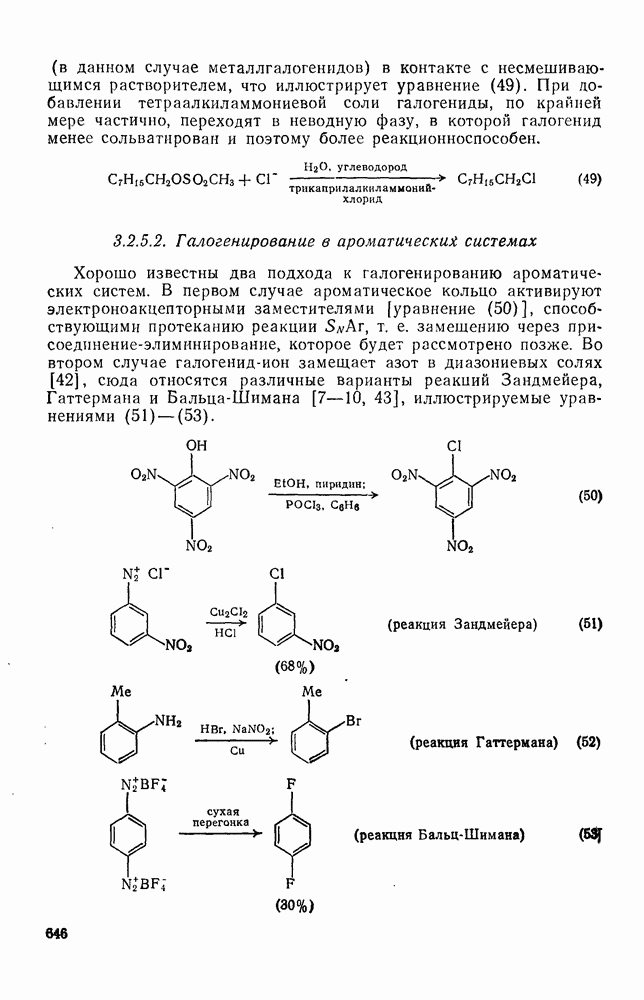
- 3.2.5.2. Галогенирование в ароматических системах
- 3.2.5.3. Галогенирование путем обмена галогенов
- 3.2.6. Синтез полигалогенированных соединений
- 3.2.6.1. Синтез полифторированных соединений
- 3.2.6.2. Синтез других полигалогенированных соединений
- 3.3. ГАЛОГЕНАЛКАНЫ
- 3.3.1. Характеристика связей углерод-галоген
- 3.3.2. Промышленное применение
- 3.3.3. Нуклеофильное замещение галогена
- 3.3.3.1. Реакции SN2 и родственные процессы
- 3.3.3.2. Соучастие соседних групп
- 3.3.3.3. Реакции SN1 и относительно долгоживущие карбениевые ионы
- 3.3.3.4. Галогенониевые ионы
- 3.3.3.5. Галогенсодержащие карбениевые ионы
- 3.3.3.6. Механизм замещения с переносом электрона
- 3.3.4. Восстановление
- 3.3.5. Замещение на металлы
- 3.3.6. Элиминирование
- 3.3.6.1. b-Элиминирование
- 3.3.6.2. Галогенкарбанионы
- 3.3.6.3. Элиминирование через карбанионы
- 3.3.6.4. b-Элиминирование из металлорганических соединений
- 3.3.6.5. a-Элиминирование (генерирование карбенов)
- 3.4. ГАЛОГЕНАЛКЕНЫ
- 3.4.1. Синтез галогеналкенов
- 3.4.2. Нуклеофильная атака
- 3.4.2.1. Реакции, индуцируемые фторид-ионом
- 3.4.2.2. Другие реакции замещения
- 3.4.3. Радикальное присоединение
- 3.4.4. Электрофильное присоединение
- 3.4.5. Циклоприсоединение
- 3.4.5.1. [2+2]-Циклоприсоединение
- 3.4.5.2. [4+2]-Циклоприсоединение
- 3.5. ГАЛОГЕНАЛКИНЫ
- 3.6. ГАЛОГЕНАРЕНЫ
- 3.6.1. Замещение галогена
- 3.6.1.2. Присоединение-элиминирование
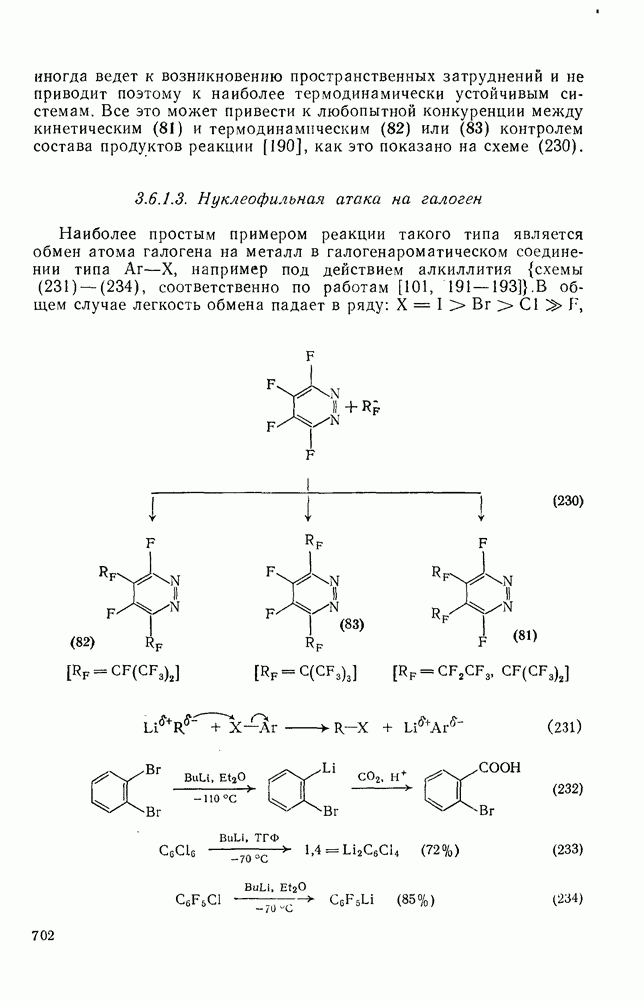
- 3.6.1.3. Нуклеофильная атака на галоген
- 3.6.1.4. Перенос электрона
- 3.6.2. Перегруппировки
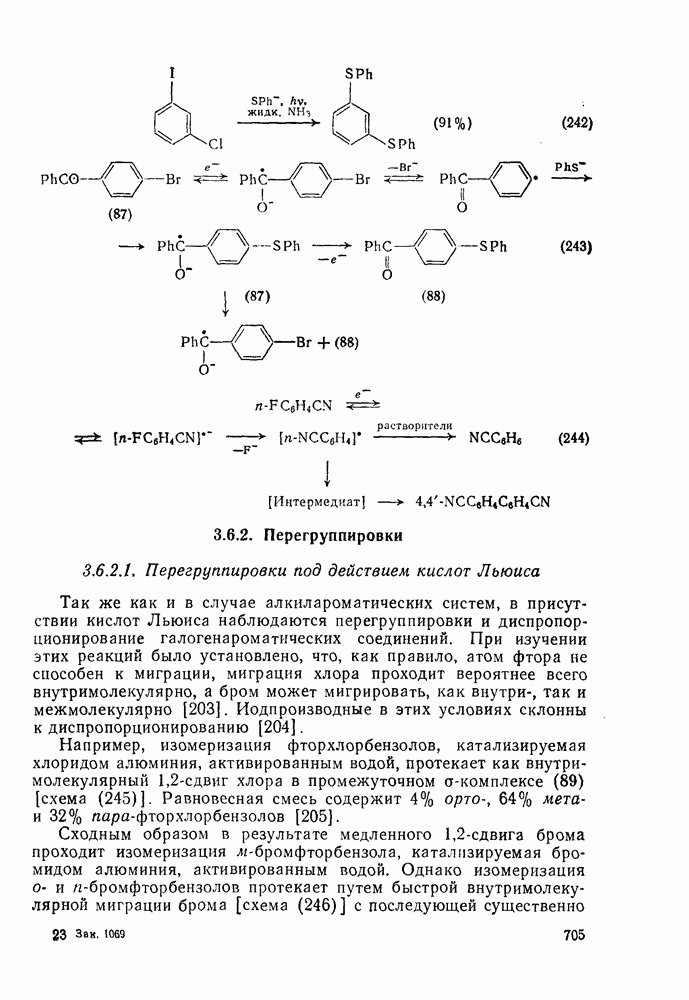
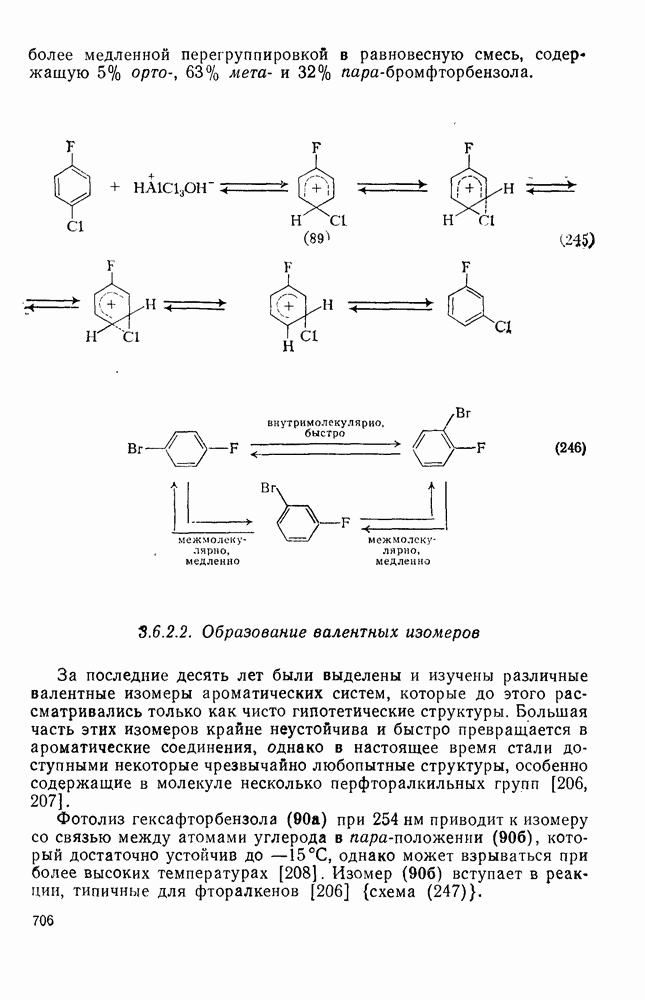
- 3.6.2.1. Перегруппировки под действием кислот Льюиса
- 3.6.2.2. Образование валентных изомеров