| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
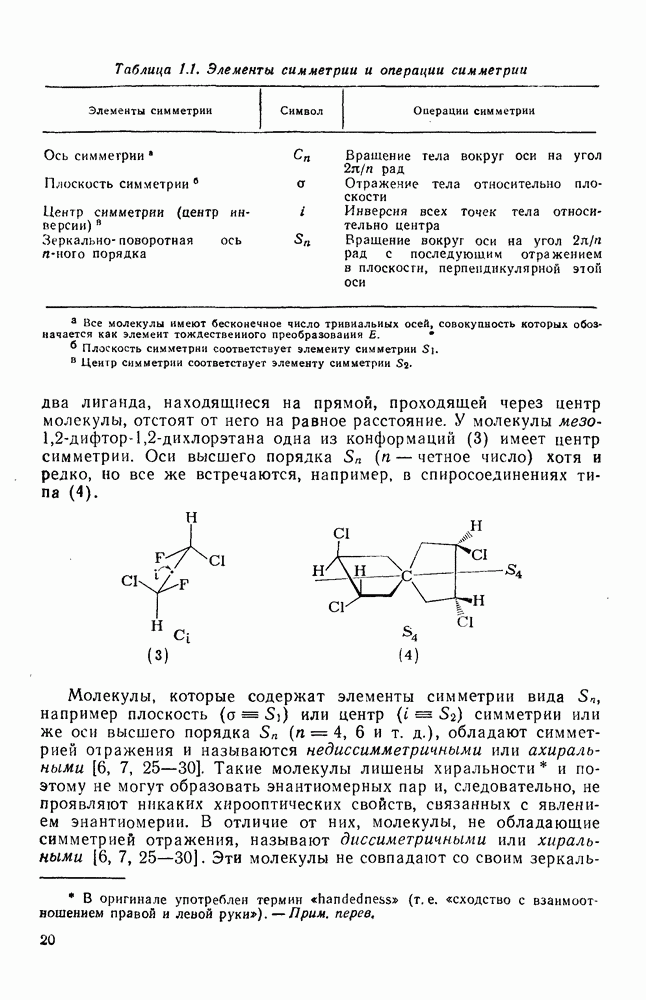
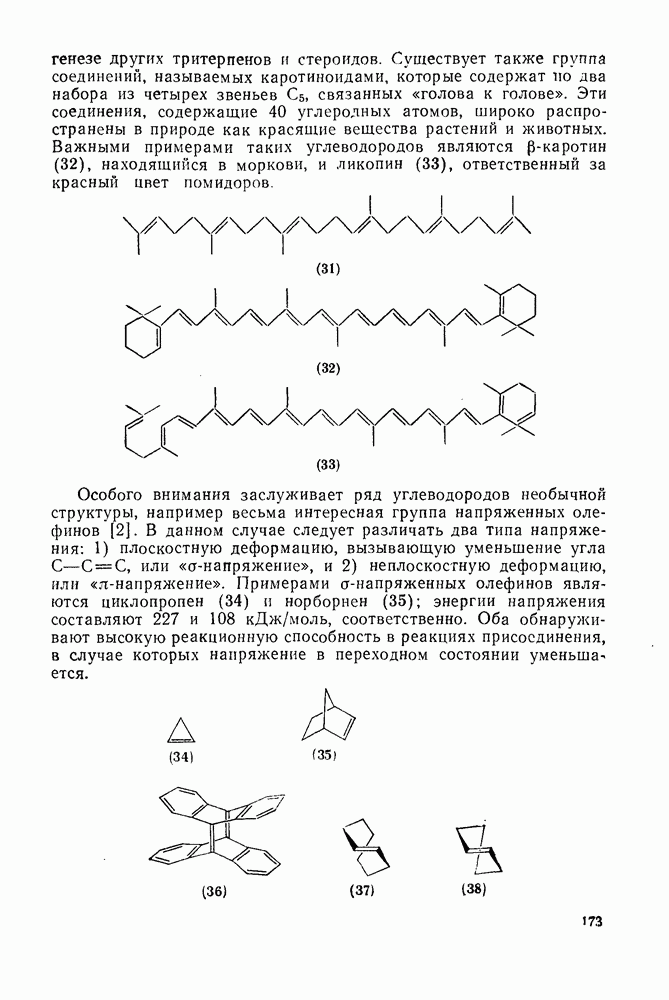
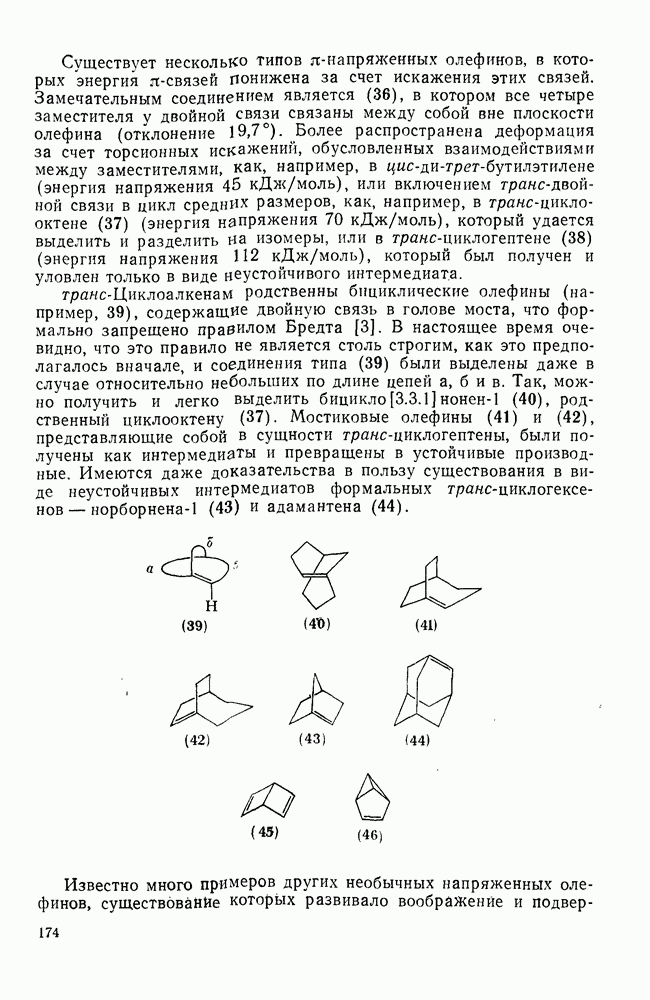
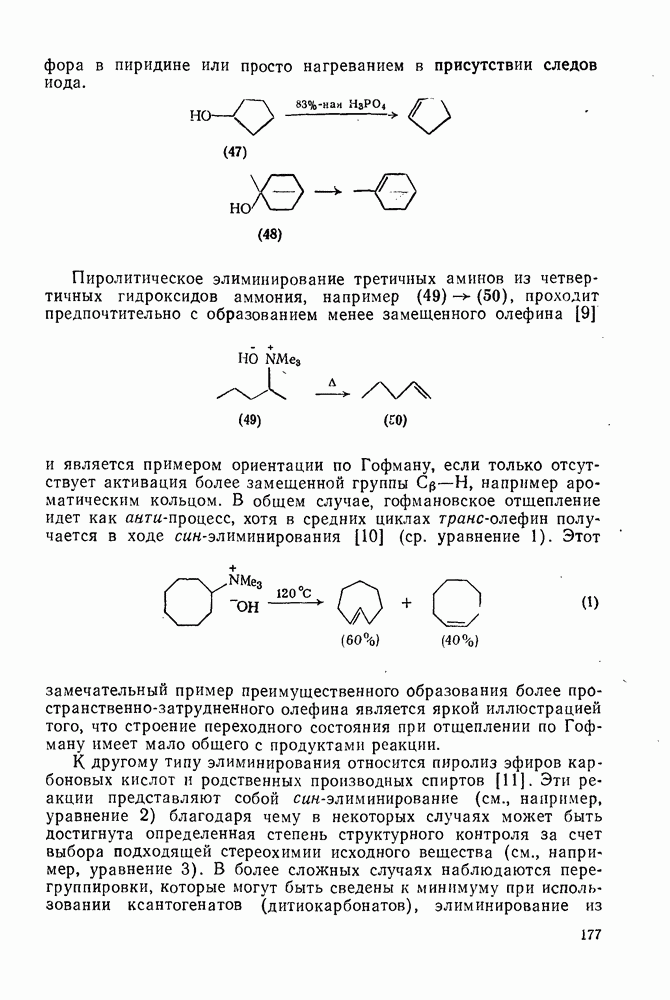
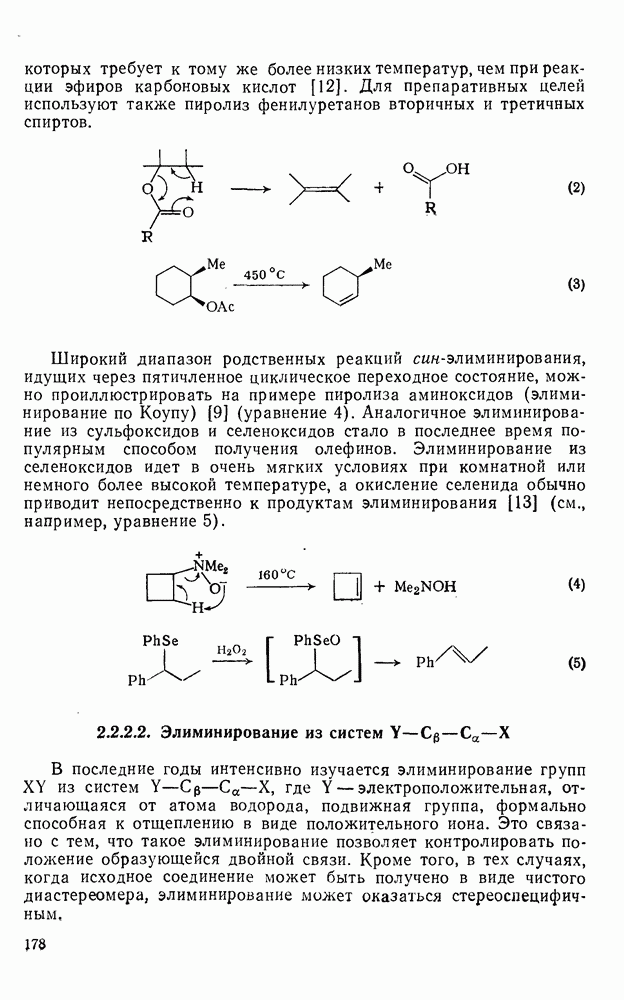
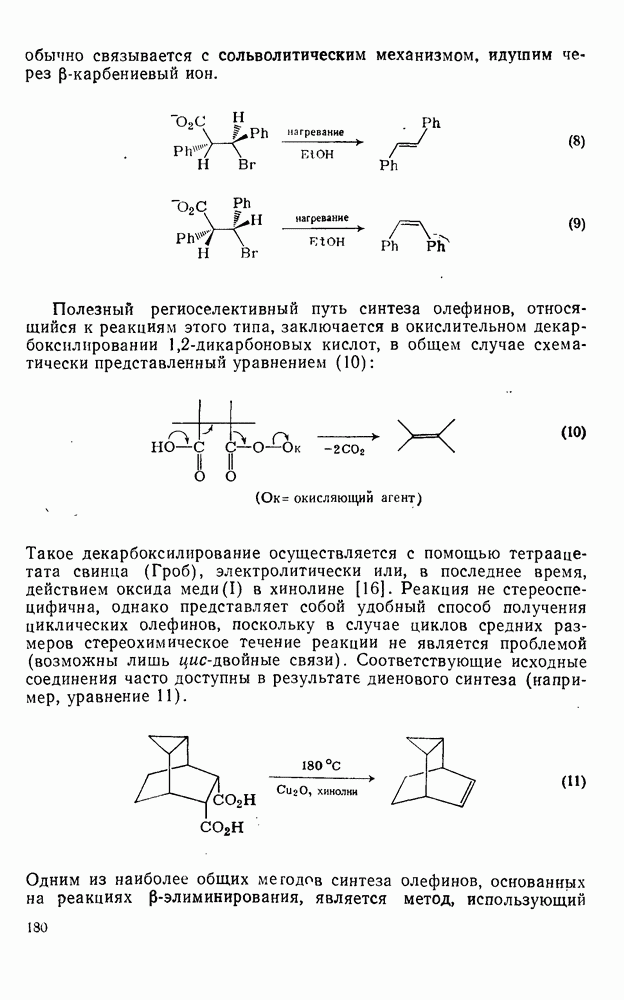
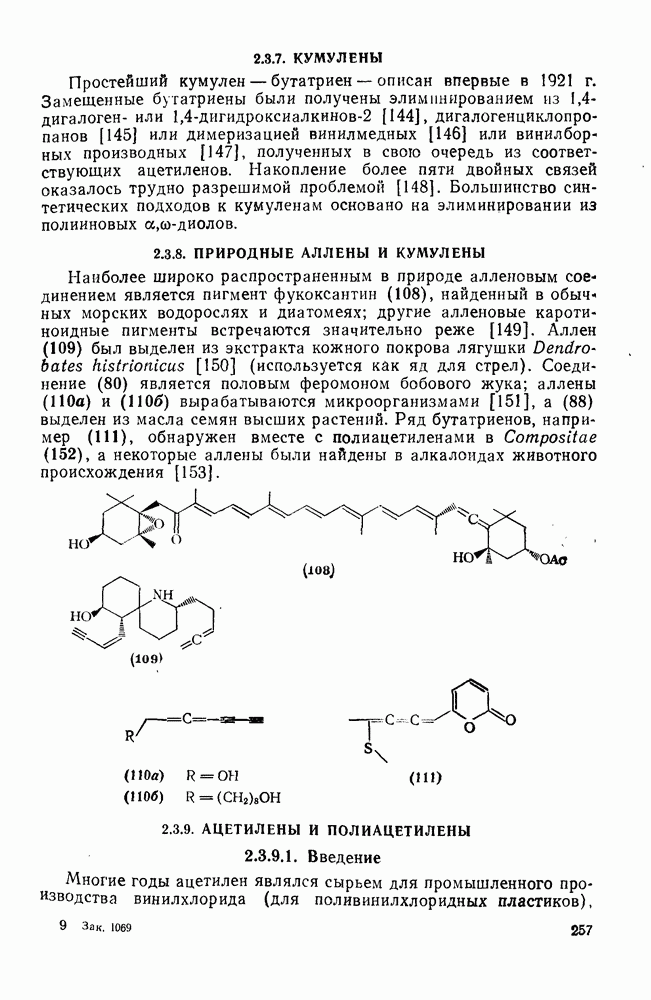
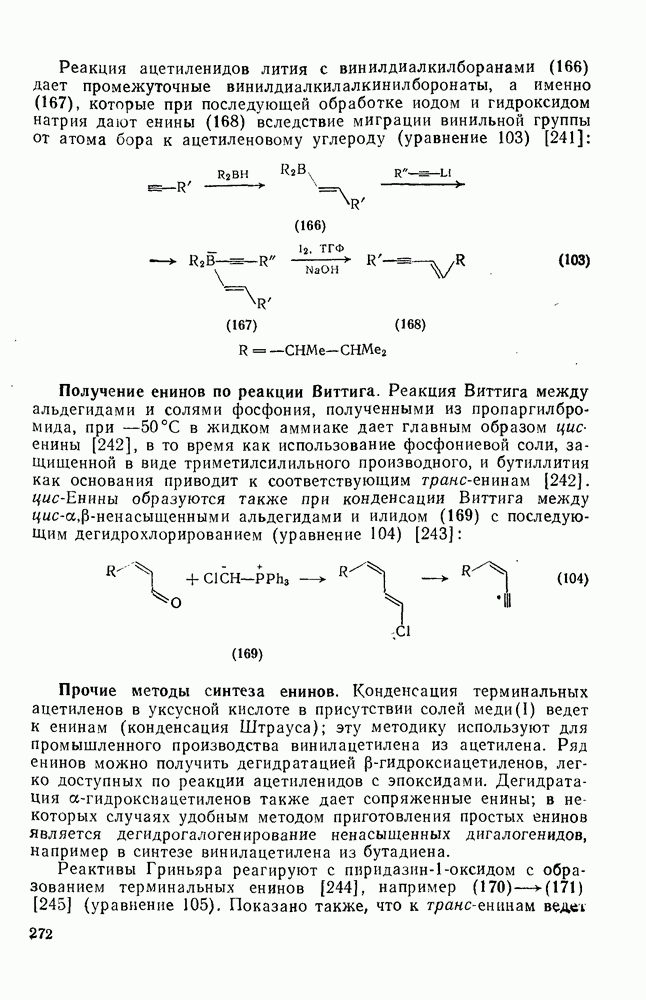
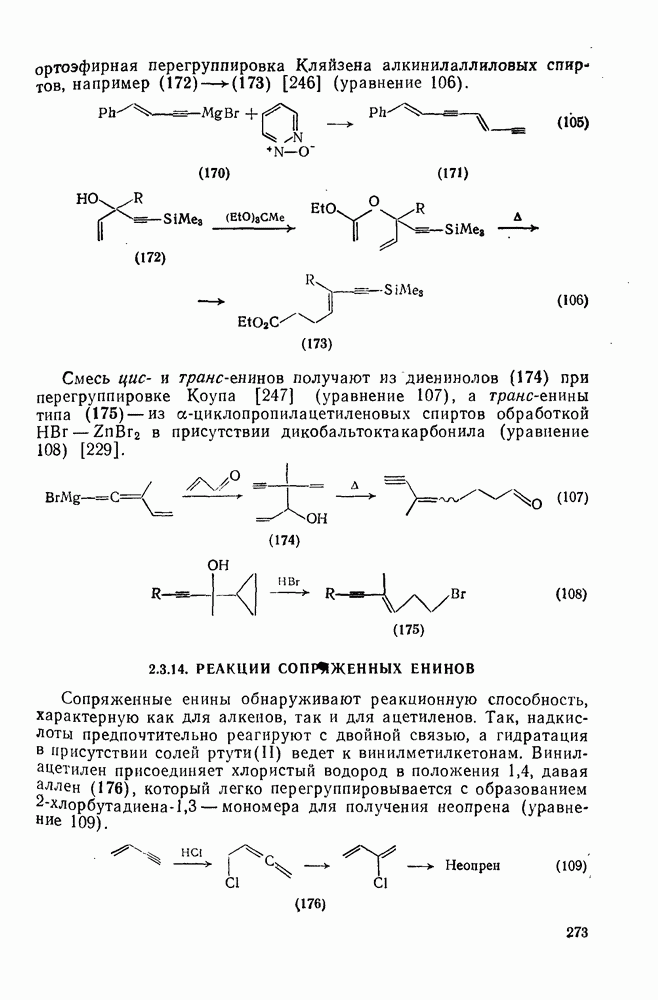
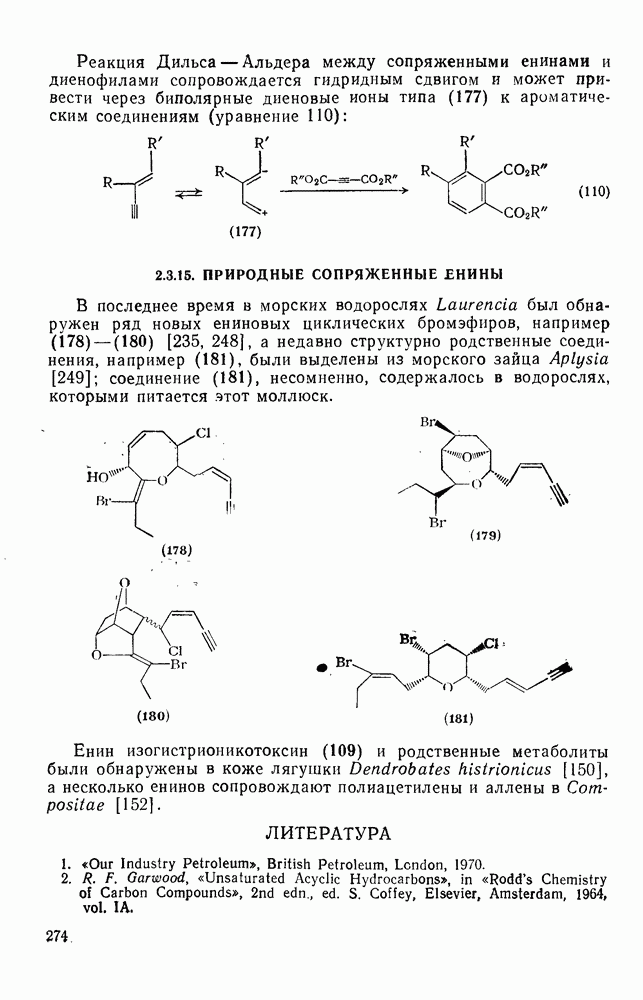
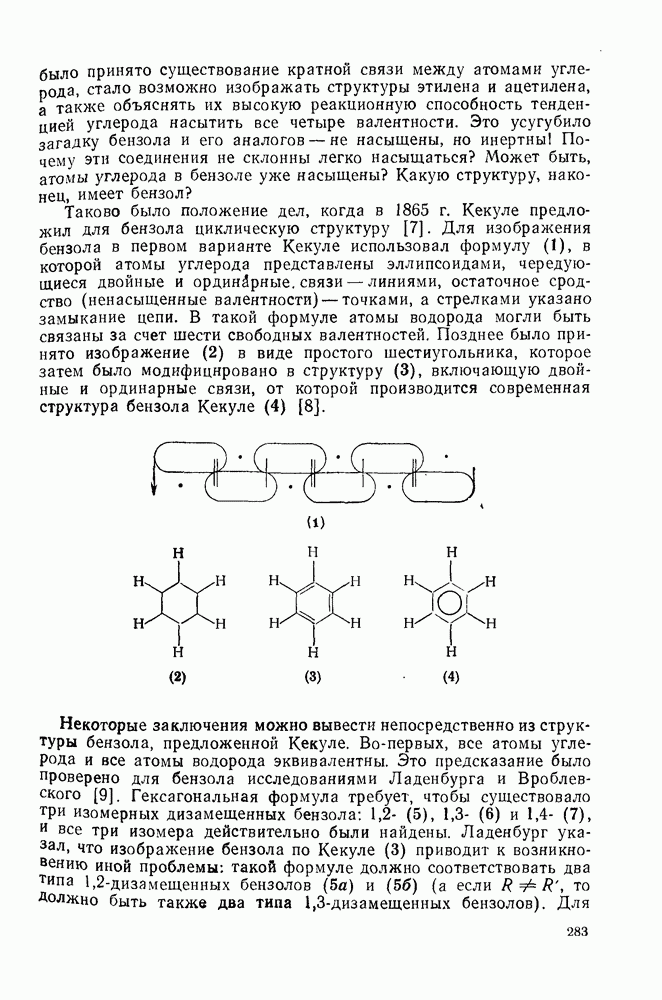
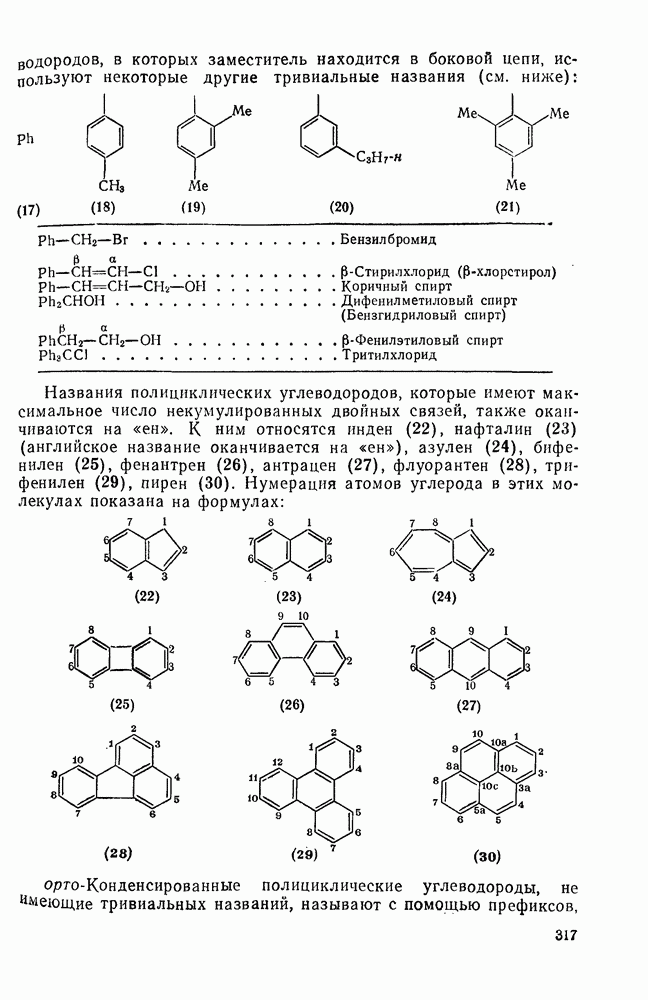
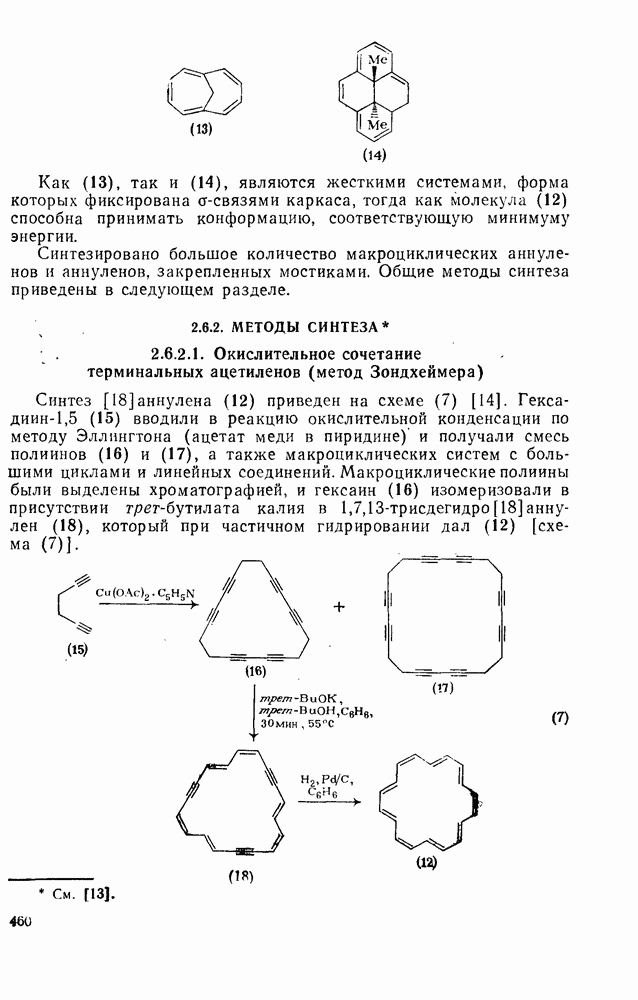
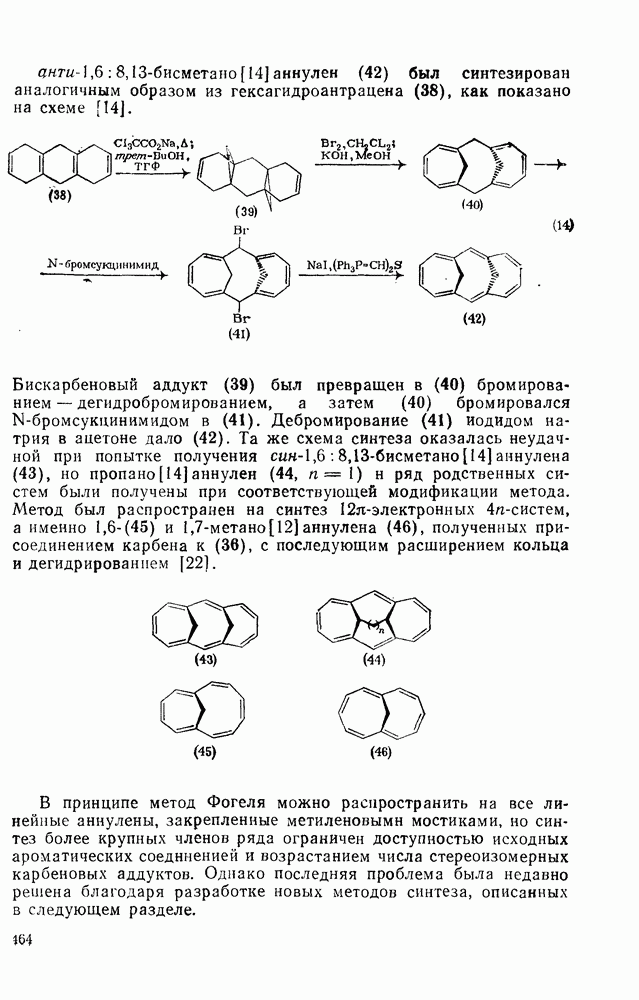
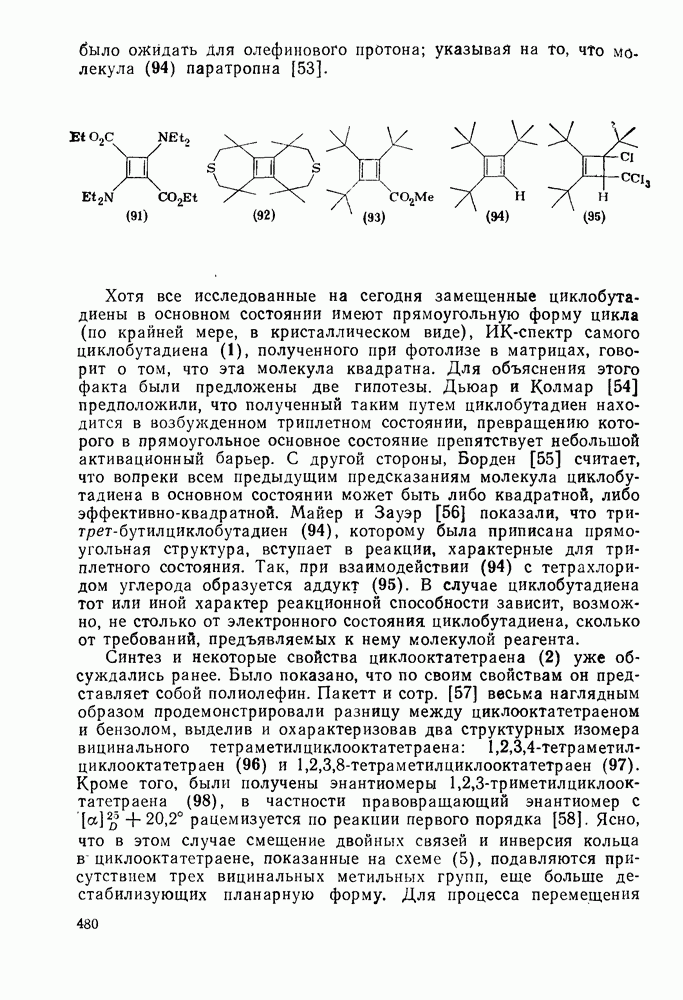
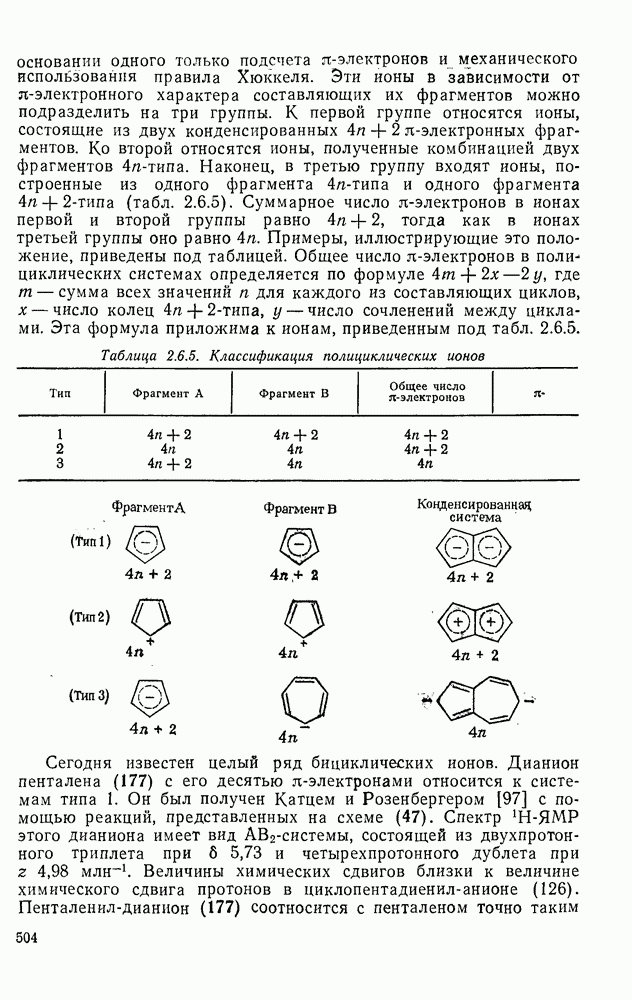
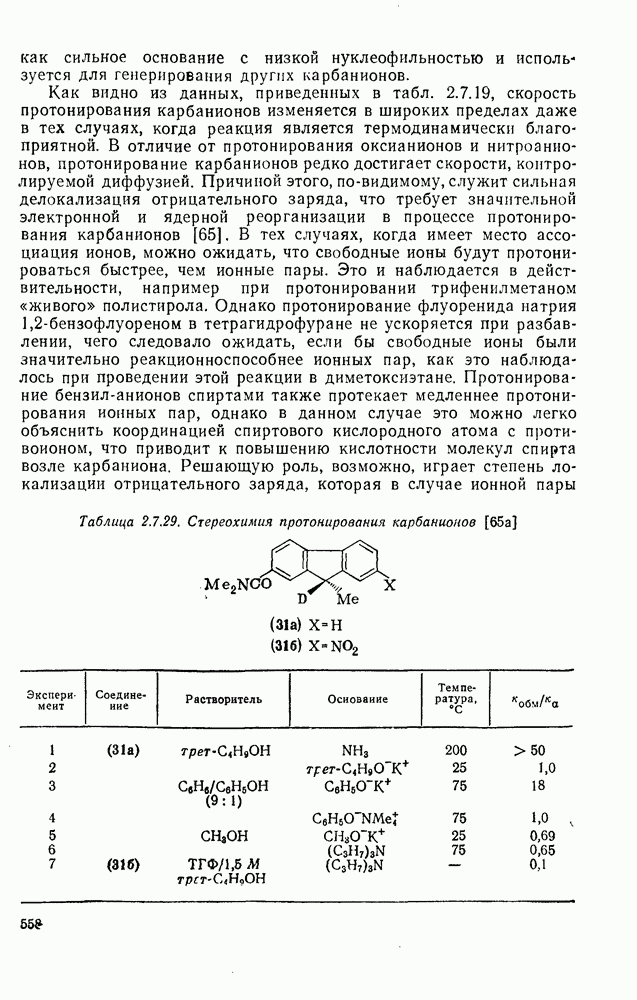
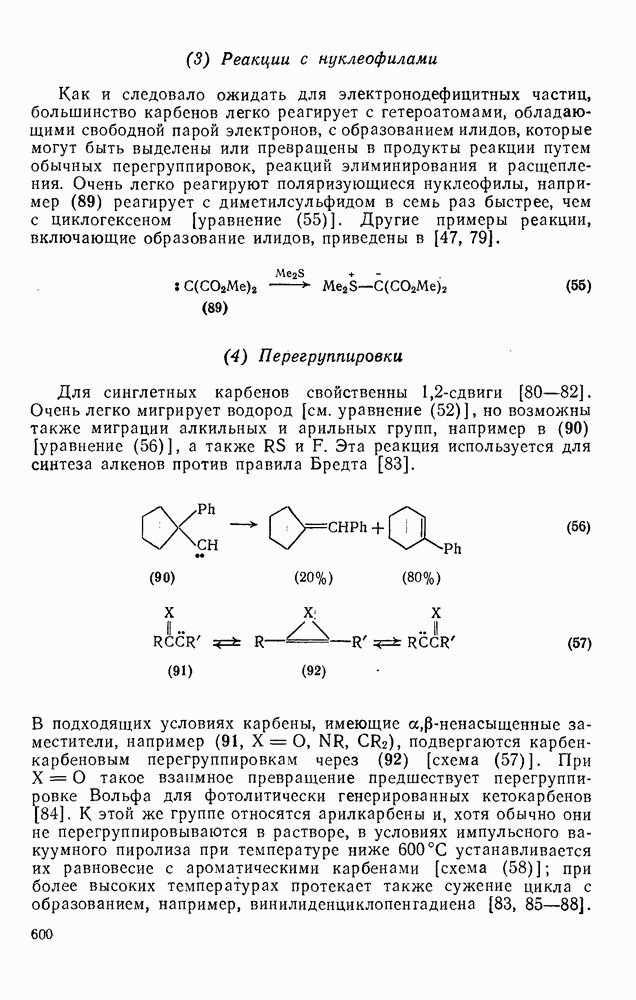
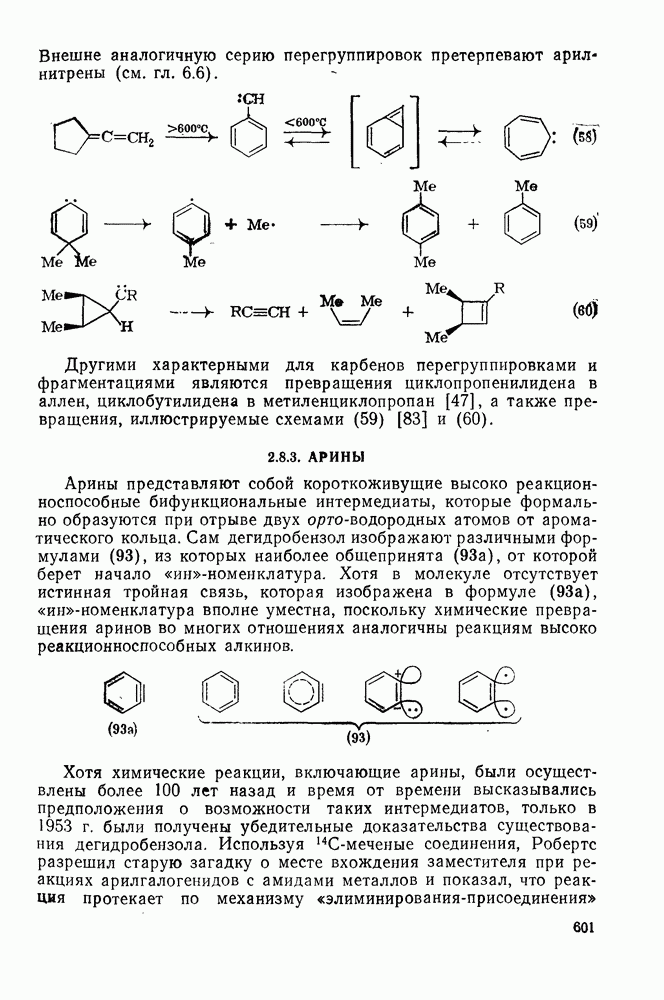
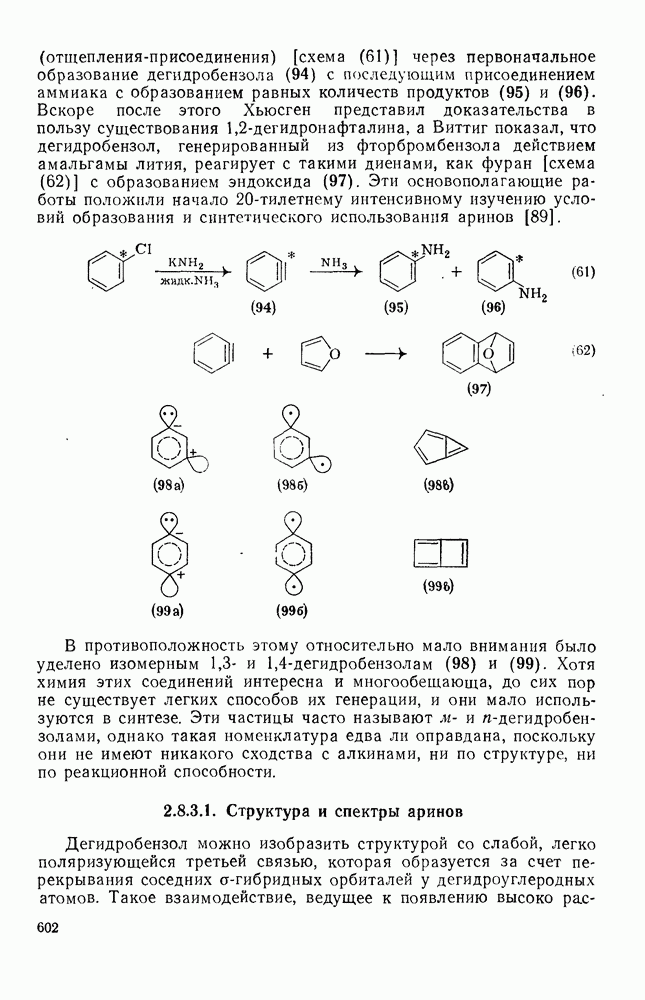
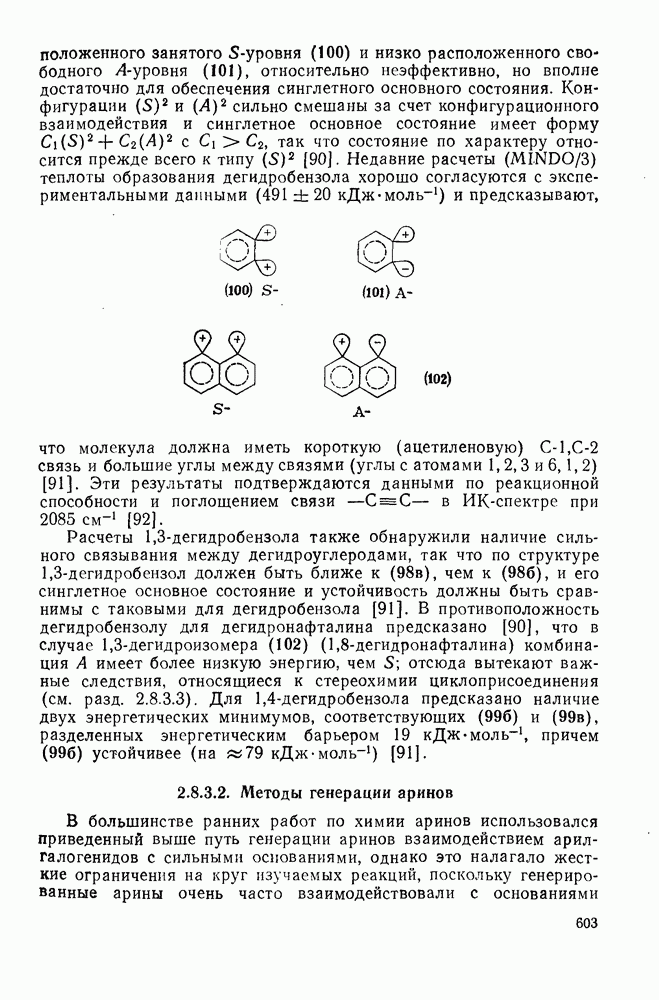
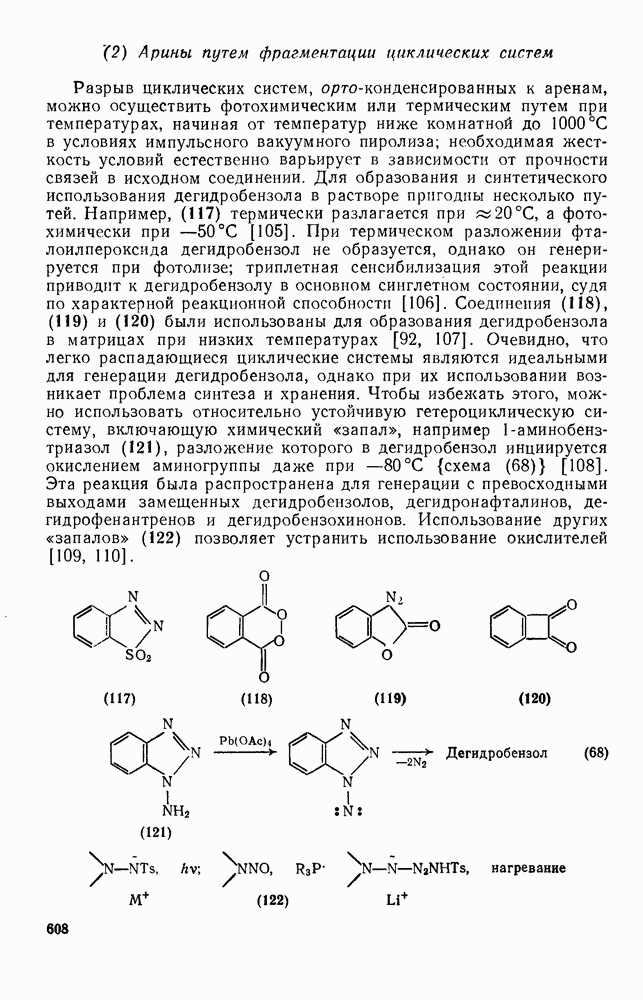
2.6.6. АННЕЛИРОВАННЫЕ АННУЛЕНЫ
Как в подгруппе с  , так и в подгруппе с 4n+2
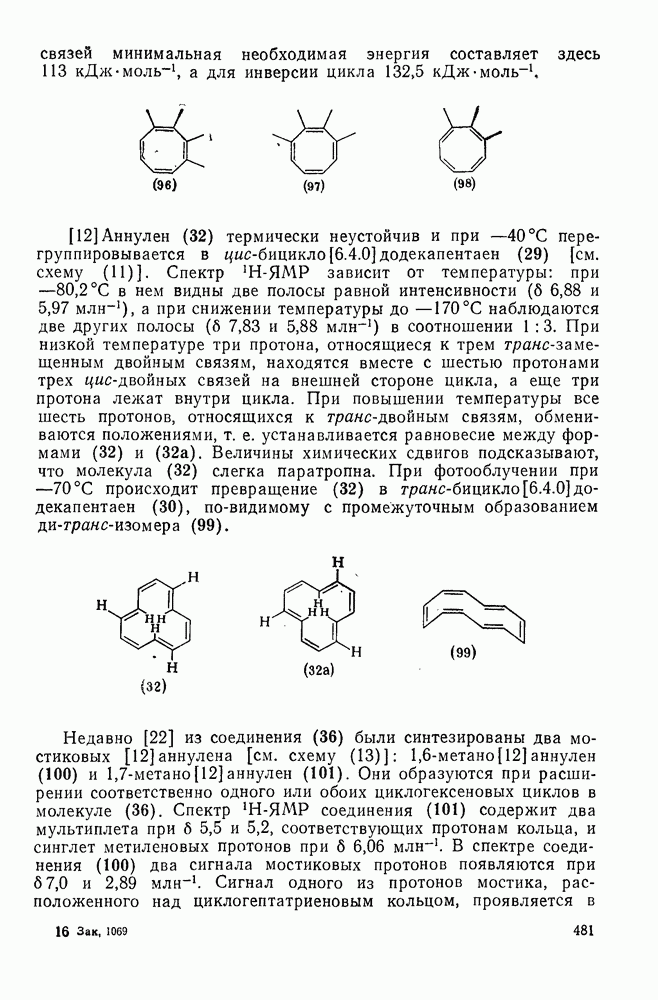
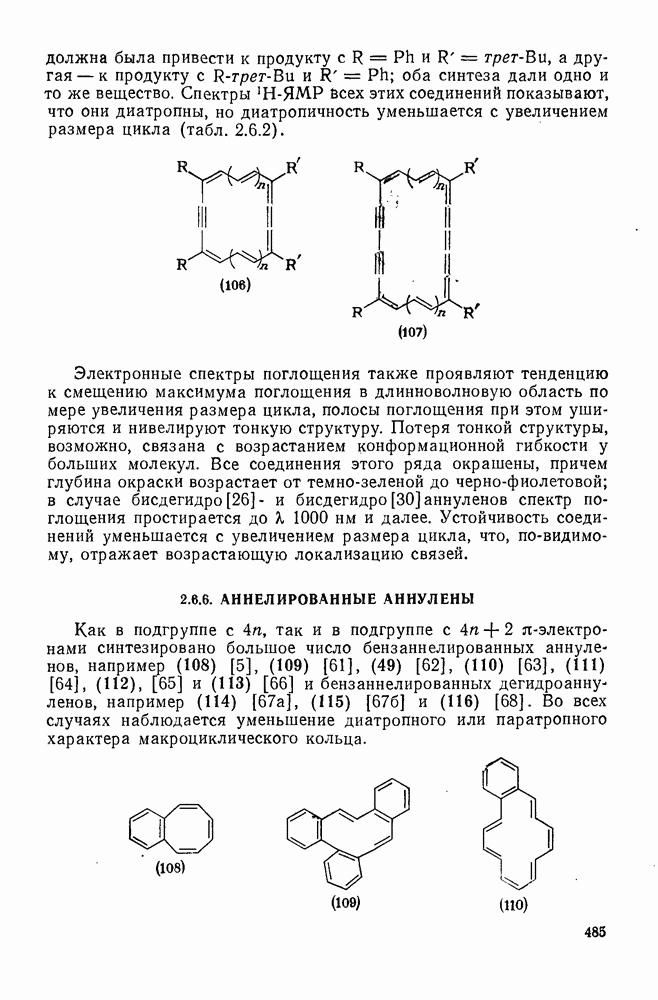
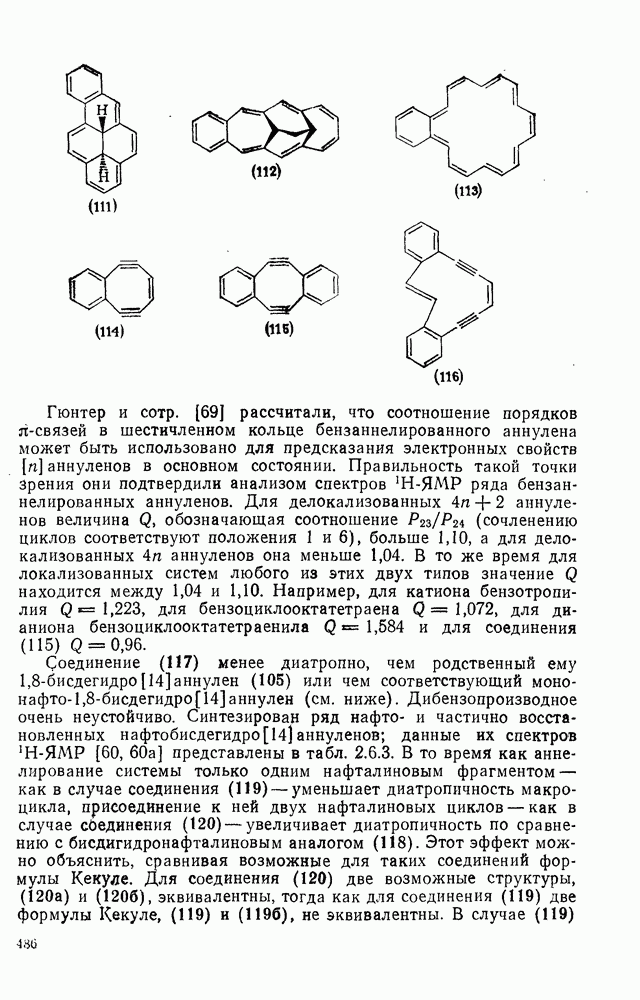
, так и в подгруппе с 4n+2  -электронами синтезировано большое число бензаннелированных аннуленов, например (108) [5], (109) [61], (49) [62], (110) [63], (111) [64], (112), [65] и (113) [66] и бензаннелированных дегидроанну-ленов, например (114) [67а], (115) [676] и (116) [68]. Во всех случаях наблюдается уменьшение диатропного или паратропного характера макроциклического кольца.
-электронами синтезировано большое число бензаннелированных аннуленов, например (108) [5], (109) [61], (49) [62], (110) [63], (111) [64], (112), [65] и (113) [66] и бензаннелированных дегидроанну-ленов, например (114) [67а], (115) [676] и (116) [68]. Во всех случаях наблюдается уменьшение диатропного или паратропного характера макроциклического кольца.


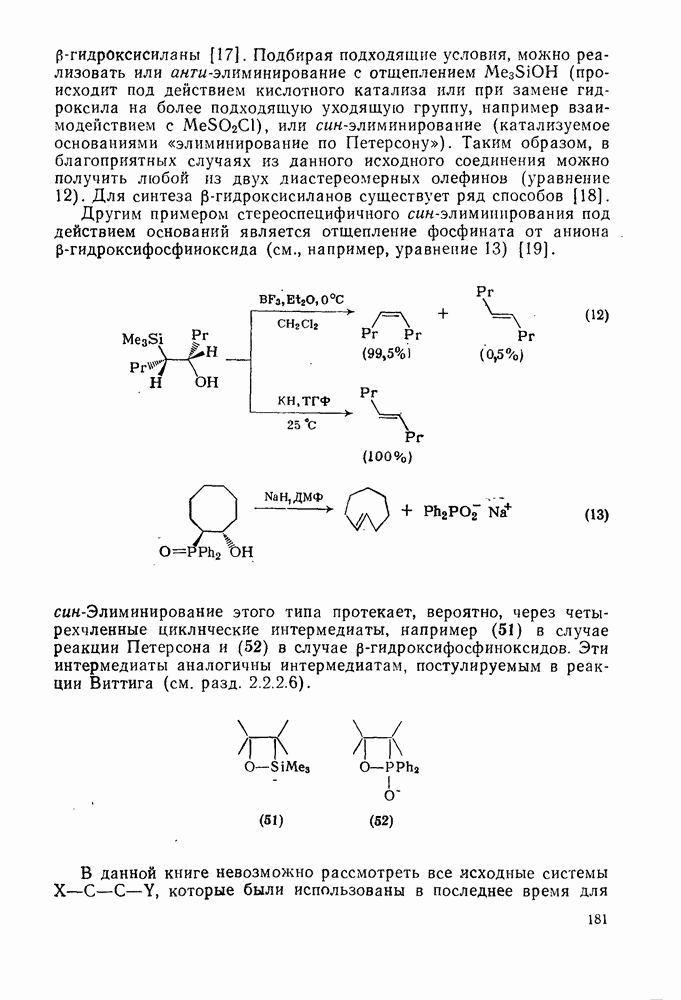
Гюнтер и сотр. [69] рассчитали, что соотношение порядков  -связей в шестичленном кольце бензаннелированного аннулена может быть использовано для предсказания электронных свойств
-связей в шестичленном кольце бензаннелированного аннулена может быть использовано для предсказания электронных свойств  в основном состоянии. Правильность такой точки Зрения они подтвердили анализом спектров
в основном состоянии. Правильность такой точки Зрения они подтвердили анализом спектров  -ЯМР ряда бензаннелированных аннуленов. Для делокализованных
-ЯМР ряда бензаннелированных аннуленов. Для делокализованных  аннуленов величина Q, обозначающая соотношение
аннуленов величина Q, обозначающая соотношение  (сочленению циклов соответствуют положения 1 и 6), больше 1,10, а для делокализованных
(сочленению циклов соответствуют положения 1 и 6), больше 1,10, а для делокализованных  аннуленов она меньше 1,04. В то же время для локализованных систем любого из этих двух типов значение Q находится между 1,04 и 1,10. Например, для катиона бензотропилия 1,223, для бензоциклооктатетраена
аннуленов она меньше 1,04. В то же время для локализованных систем любого из этих двух типов значение Q находится между 1,04 и 1,10. Например, для катиона бензотропилия 1,223, для бензоциклооктатетраена  для дианиона бензоциклооктатетраенила
для дианиона бензоциклооктатетраенила  и для соединения
и для соединения 
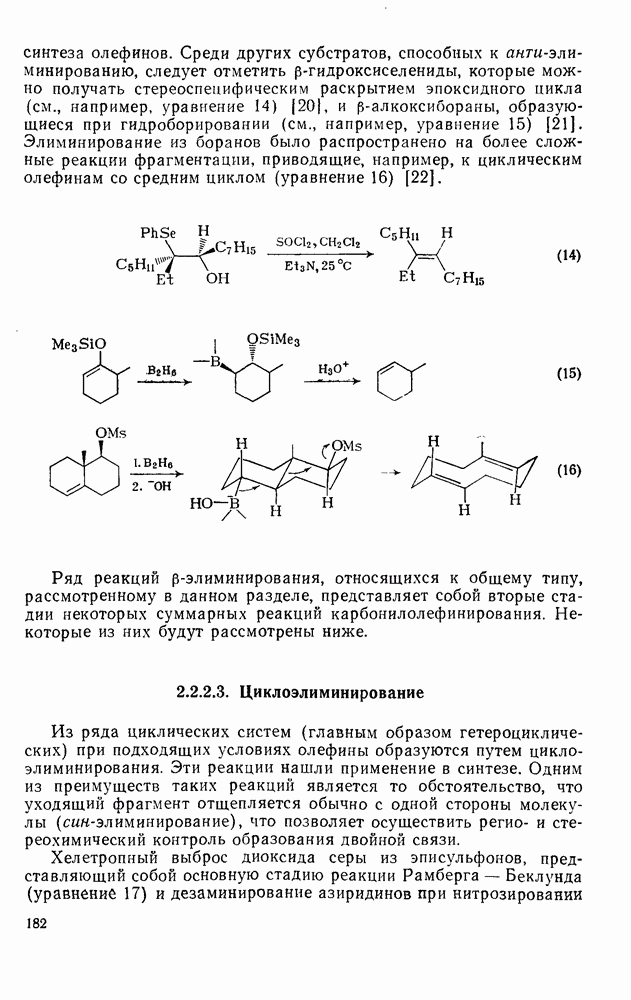
Соединение (117) менее диатропно, чем родственный ему  -бисдегидро
-бисдегидро  или чем соответствующий
или чем соответствующий  (см. ниже). Дибензопроизводное очень неустойчиво. Синтезирован ряд нафто- и частично восстановленных
(см. ниже). Дибензопроизводное очень неустойчиво. Синтезирован ряд нафто- и частично восстановленных  аннуленов; данные их спектров
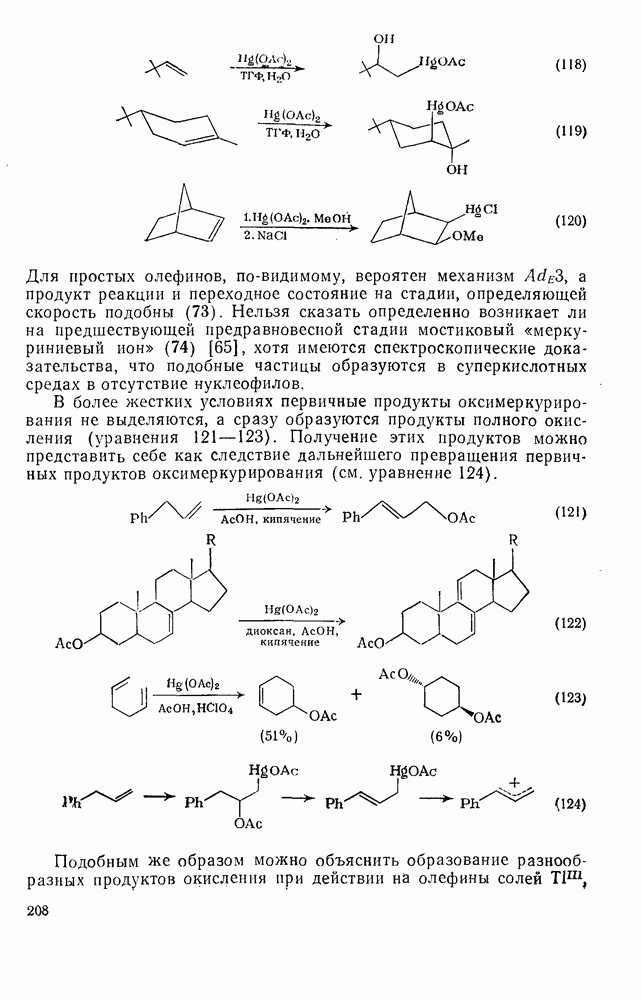
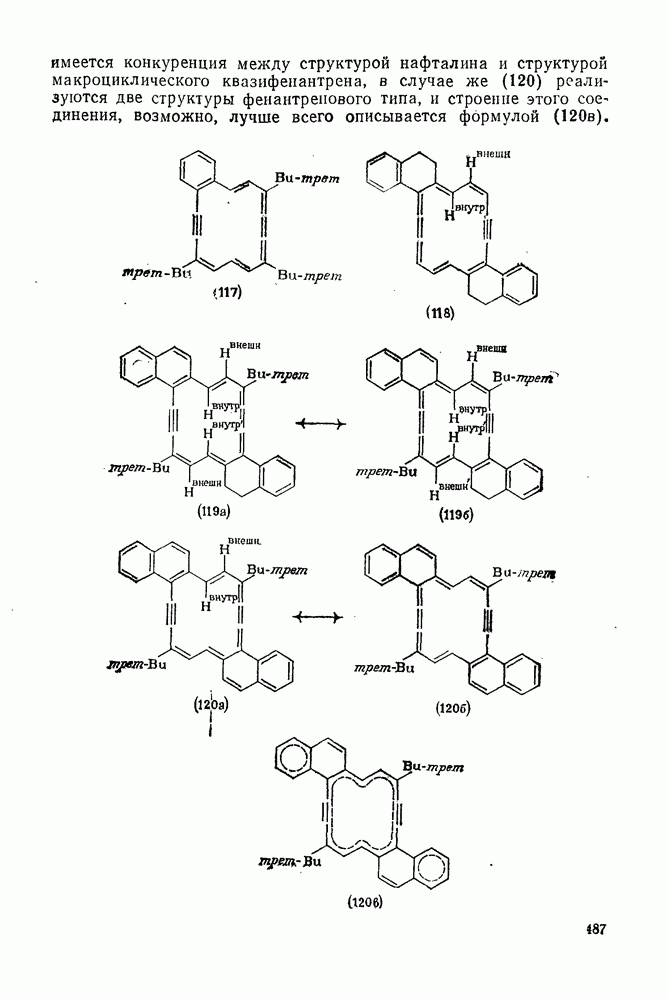
аннуленов; данные их спектров  -ЯМР [60, 60а] представлены в табл. 2.6.3. В то время как анне-лирование системы только одним нафталиновым фрагментом — как в случае соединения (119) — уменьшает диатропичность макроцикла, присоединение к ней двух нафталиновых циклов — как в случае соединения (120) — увеличивает диатропичность по сравнению с бисдигидронафталиновым аналогом (118). Этот эффект можно объяснить, сравнивая возможные для таких соединений формулы Кекуле. Для соединения (120) две возможные структуры, (120а) и (1206), эквивалентны, тогда как для соединения (119) две формулы Кекуле, (119) и (1196), не эквивалентны.
-ЯМР [60, 60а] представлены в табл. 2.6.3. В то время как анне-лирование системы только одним нафталиновым фрагментом — как в случае соединения (119) — уменьшает диатропичность макроцикла, присоединение к ней двух нафталиновых циклов — как в случае соединения (120) — увеличивает диатропичность по сравнению с бисдигидронафталиновым аналогом (118). Этот эффект можно объяснить, сравнивая возможные для таких соединений формулы Кекуле. Для соединения (120) две возможные структуры, (120а) и (1206), эквивалентны, тогда как для соединения (119) две формулы Кекуле, (119) и (1196), не эквивалентны.
В случае (119) имеется конкуренция между структурой нафталина и структурой макроциклического квазифенантрена, в случае же (120) реализуются две структуры фенантрепового типа, и строение этого соединения, возможно, лучше всего описывается формулой (120в).

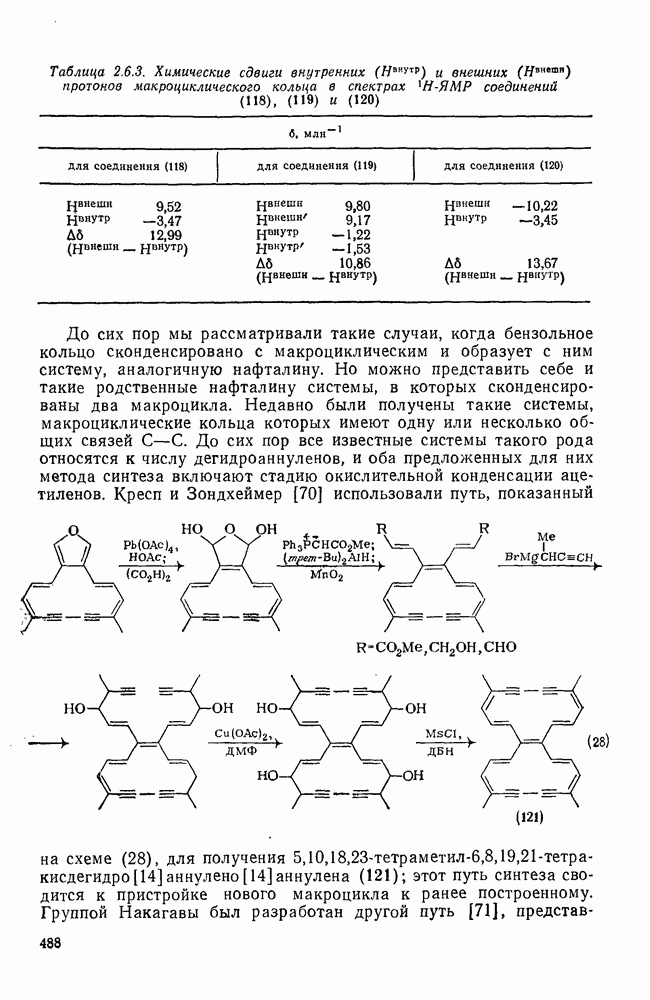
Таблица 2.6.3. Химические сдвиги внутренних ( ) и внешних
) и внешних  протонов макроциклического кольца в спектрах
протонов макроциклического кольца в спектрах  -ЯМР соединений (118), (119) и (120)
-ЯМР соединений (118), (119) и (120)

До сих пор мы рассматривали такие случаи, когда бензольное кольцо сконденсировано с макроциклическим и образует с ним систему, аналогичную нафталину. Но можно представить себе и такие родственные нафталину системы, в которых сконденсированы два макроцикла. Недавно были получены такие системы, макроциклические кольца которых имеют одну или несколько общих связей  . До сих пор все известные системы такого рода относятся к числу дегидроаннуленов, и оба предложенных для них метода синтеза включают стадию окислительной конденсации ацетиленов.
. До сих пор все известные системы такого рода относятся к числу дегидроаннуленов, и оба предложенных для них метода синтеза включают стадию окислительной конденсации ацетиленов.

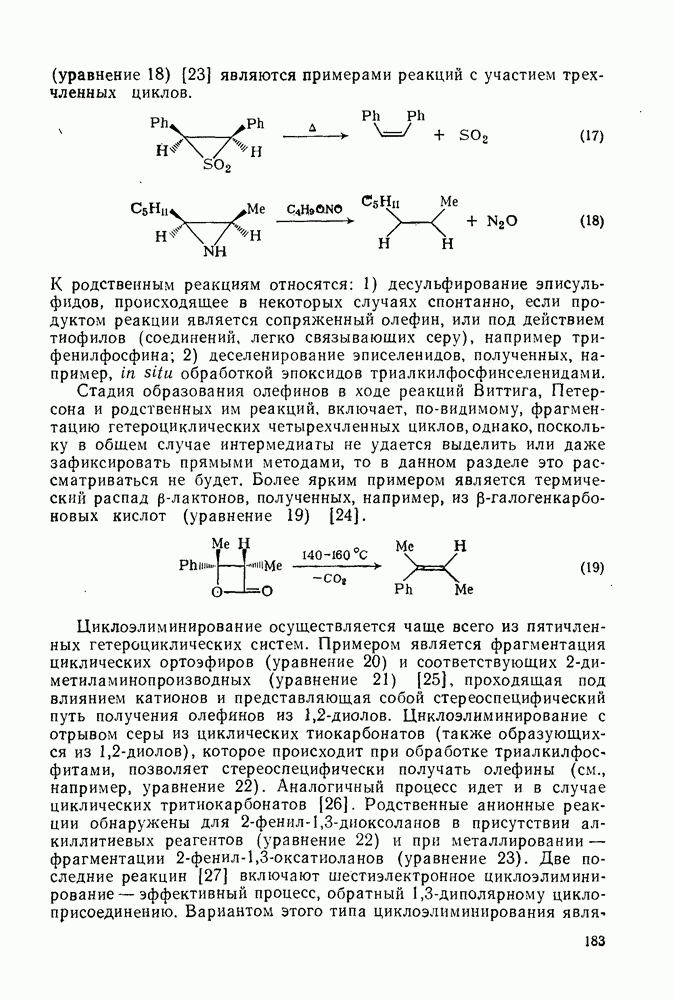
Кресп и Зондхеймер [70] использовали путь, показанный на схеме (28), для получения  (121); этот путь синтеза сводится к пристройке нового макроцикла к ранее построенному. Группой Накагавы был разработан другой путь [71], представленный на схеме (29).
(121); этот путь синтеза сводится к пристройке нового макроцикла к ранее построенному. Группой Накагавы был разработан другой путь [71], представленный на схеме (29).
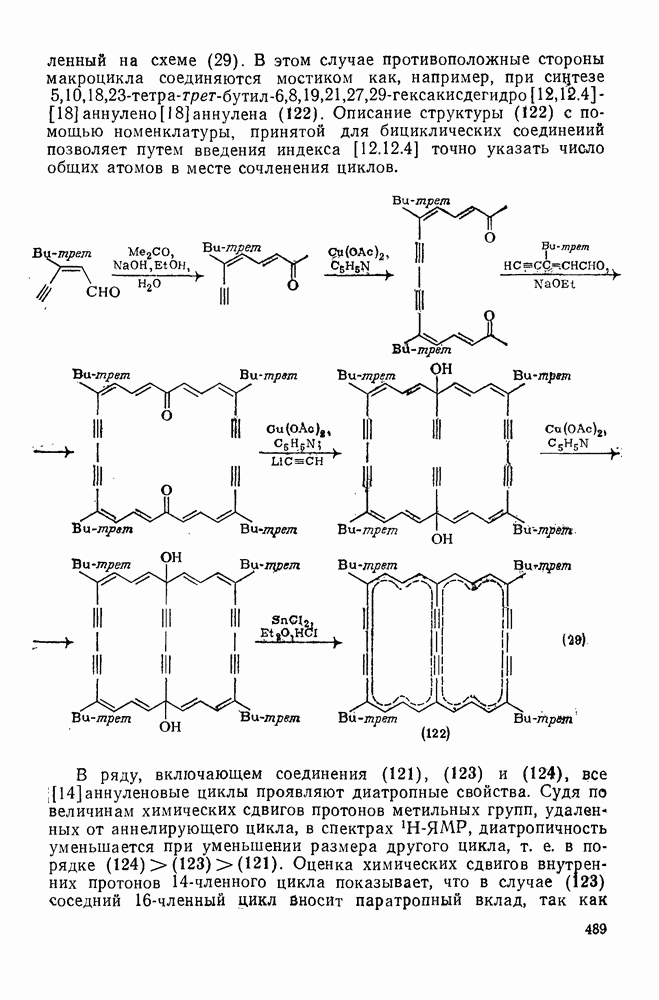
В этом случае противоположные стороны макроцикла соединяются мостиком как, например, при синтезе  (122). Описание структуры (122) с помощью номенклатуры, принятой для бициклических соединений позволяет путем введения индекса [12.12.4] точно указать число общих атомов в месте сочленения циклов.
(122). Описание структуры (122) с помощью номенклатуры, принятой для бициклических соединений позволяет путем введения индекса [12.12.4] точно указать число общих атомов в месте сочленения циклов.

В ряду, включающем соединения (121), (123) и (124), все  циклы проявляют диатропные свойства. Судя по величинам химических сдвигов протонов метальных групп, удаленных от аннелирующего цикла, в спектрах
циклы проявляют диатропные свойства. Судя по величинам химических сдвигов протонов метальных групп, удаленных от аннелирующего цикла, в спектрах  -ЯМР, диатропичность уменьшается при уменьшении размера другого цикла, т. е. в порядке
-ЯМР, диатропичность уменьшается при уменьшении размера другого цикла, т. е. в порядке  (121). Оценка химических сдвигов внутренних протонов
(121). Оценка химических сдвигов внутренних протонов  -членного цикла показывает, что в случае (123) соседний
-членного цикла показывает, что в случае (123) соседний  -членный цикл Вносит паратропный вклад, так как внутренние протоны резонируют в более сильном поле, чем в случае соединений (121) и (124), где аннелирующие циклы вносят диатропный вклад.
-членный цикл Вносит паратропный вклад, так как внутренние протоны резонируют в более сильном поле, чем в случае соединений (121) и (124), где аннелирующие циклы вносят диатропный вклад.

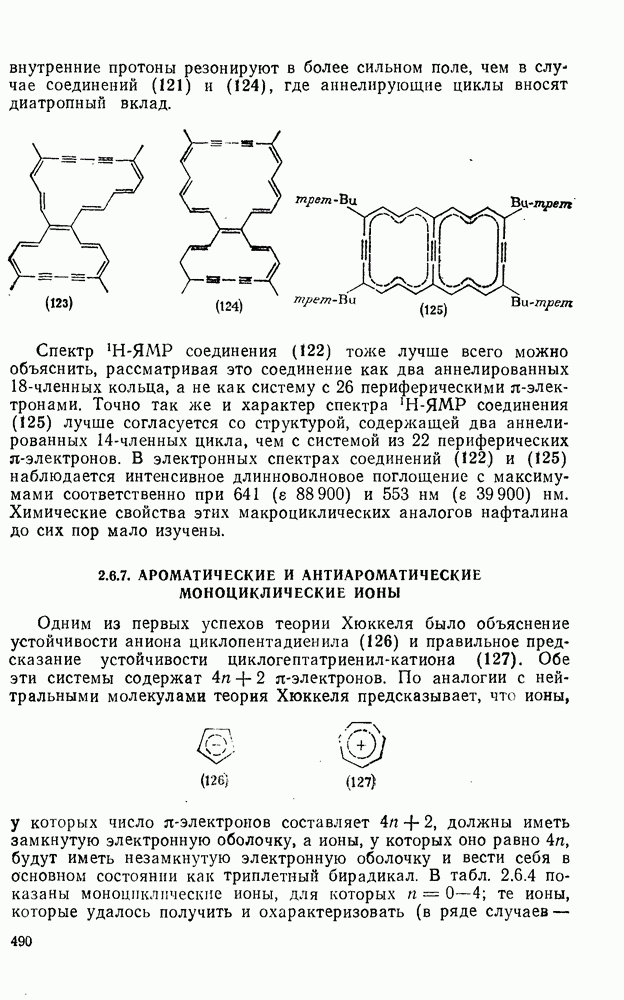
Спектр  -ЯМР соединения (122) тоже лучше всего можно объяснить, рассматривая это соединение как два аннелированных
-ЯМР соединения (122) тоже лучше всего можно объяснить, рассматривая это соединение как два аннелированных  -членных кольца, а не как систему с 26 периферическими
-членных кольца, а не как систему с 26 периферическими  -электронами. Точно так же и характер спектра
-электронами. Точно так же и характер спектра  -ЯМР соединения (125) лучше согласуется со структурой, содержащей два аннелированных
-ЯМР соединения (125) лучше согласуется со структурой, содержащей два аннелированных  -членных цикла, чем с системой из 22 периферических я-электронов. В электронных спектрах соединений (122) и (125) наблюдается интенсивное длинноволновое поглощение с максимумами соответственно при 641 (
-членных цикла, чем с системой из 22 периферических я-электронов. В электронных спектрах соединений (122) и (125) наблюдается интенсивное длинноволновое поглощение с максимумами соответственно при 641 ( 88 900) и 553 нм (
88 900) и 553 нм ( 39 900) нм. Химические свойства этих макроциклических аналогов нафталина до сих пор мало изучены.
39 900) нм. Химические свойства этих макроциклических аналогов нафталина до сих пор мало изучены.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- ПРЕДИСЛОВИЕ
- ИЗ ПРЕДИСЛОВИЯ К ТОМУ 1 АНГЛИЙСКОГО ИЗДАНИЯ
- ЧАСТЬ I. НОМЕНКЛАТУРА И СТЕРЕОХИМИЯ
- 1.1. ВВЕДЕНИЕ И СТЕРЕОХИМИЯ
- 1.1.2. СИММЕТРИЯ И ХИРАЛЬНОСТЬ
- 1.1.3. ХИМИЧЕСКАЯ ТОПОЛОГИЯ
- 1.1.4. ИЗОМЕРИЯ
- 1.1.4.2. Строение
- 1.1.4.3. Абсолютная конфигурация
- 1.1.4.4. Относительная конфигурация
- 1.1.4.5. Конформация
- 1.1.4.6. Концепция изомерии
- 1.1.5. ТОПИЗМ
- 1.1.5.2. Прохиральность
- 1.1.5.3. Псевдоасимметрия (псевдохиральность)
- 1.1.6. ТОПОМЕРИЯ
- 1.1.7. ДИНАМИЧЕСКАЯ СТЕРЕОХИМИЯ. КРАТКИЕ СВЕДЕНИЯ
- ЧАСТЬ 2. УГЛЕВОДОРОДЫ
- 2.1. НАСЫЩЕННЫЕ УГЛЕВОДОРОДЫ
- 2.1.2. Строение и номенклатура
- 2.1.2.1. Номенклатура IUPAC
- 2.1.2.2. Алициклические алканы
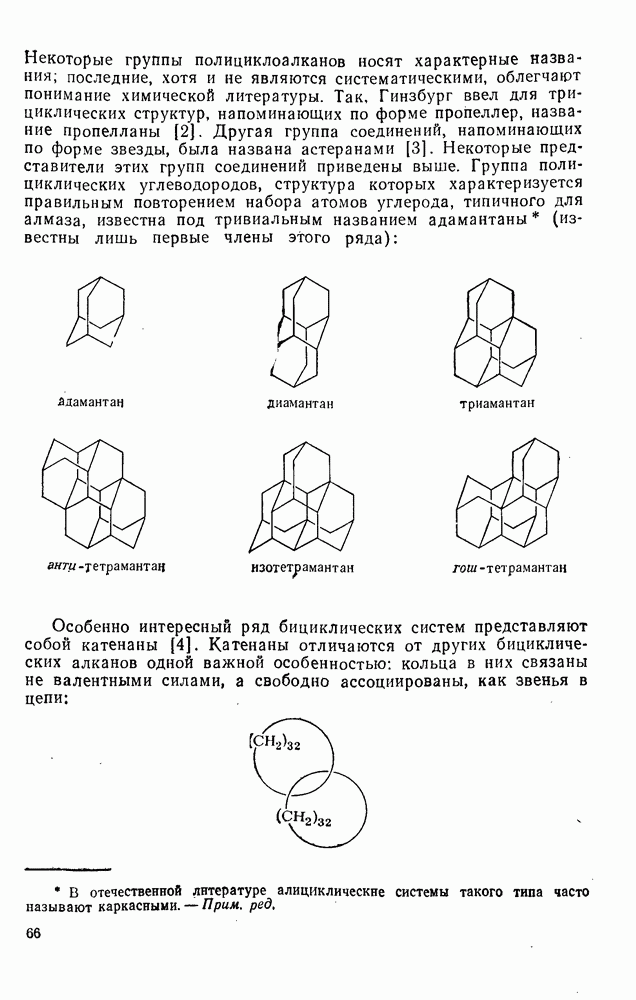
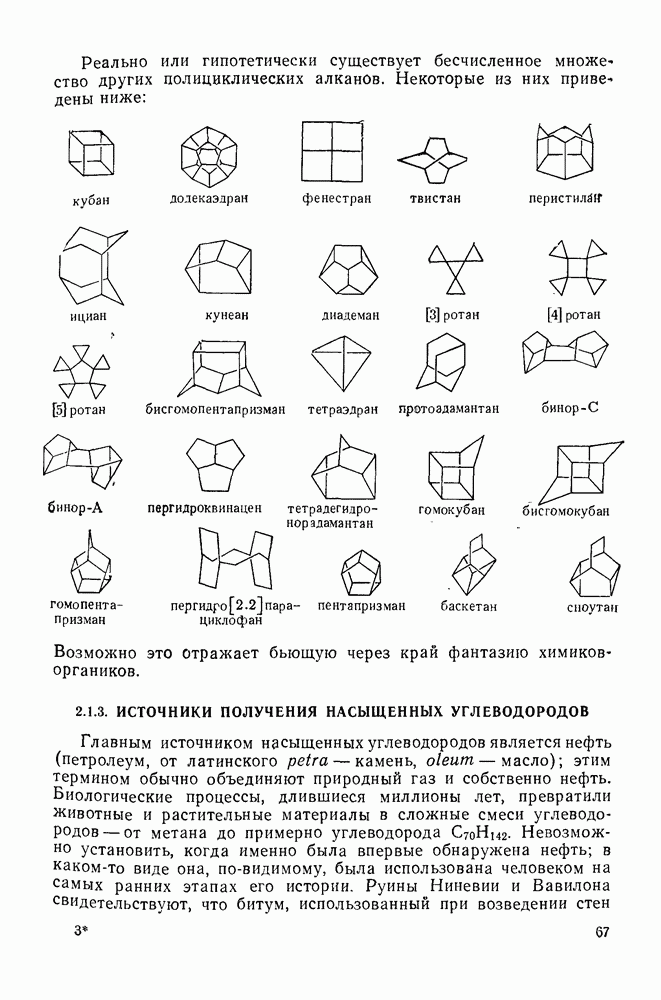
- 2.1.2.3. Полициклоалканы
- 2.1.3. ИСТОЧНИКИ ПОЛУЧЕНИЯ НАСЫЩЕННЫХ УГЛЕВОДОРОДОВ
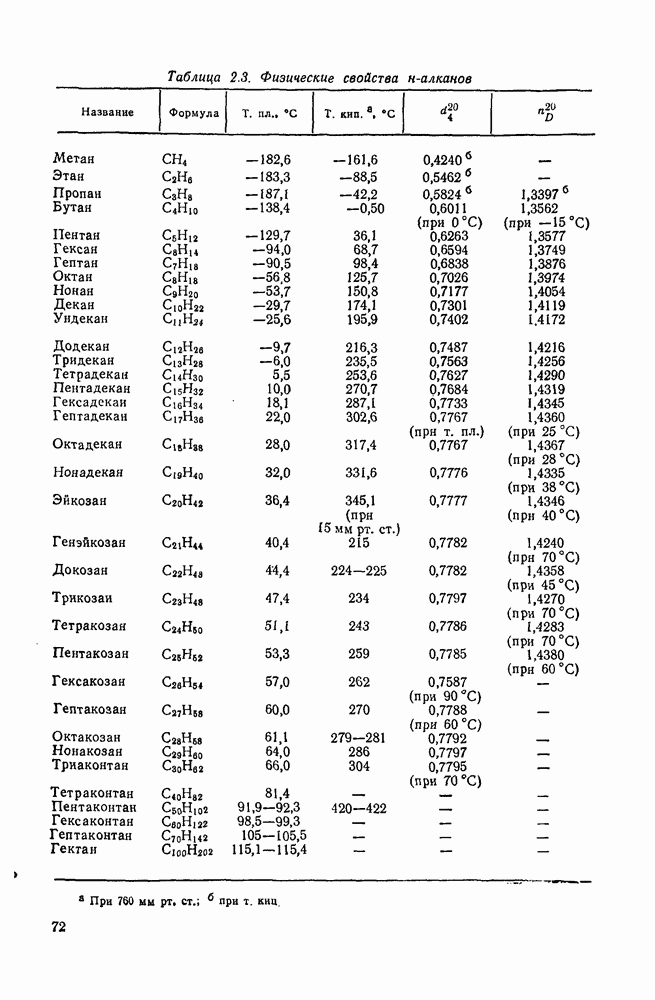
- 2.1.4. ФИЗИЧЕСКИЕ СВОЙСТВА
- 2.1.4.1. Ациклические алканы
- 2.1.4.2. Моно- и полициклоалканы
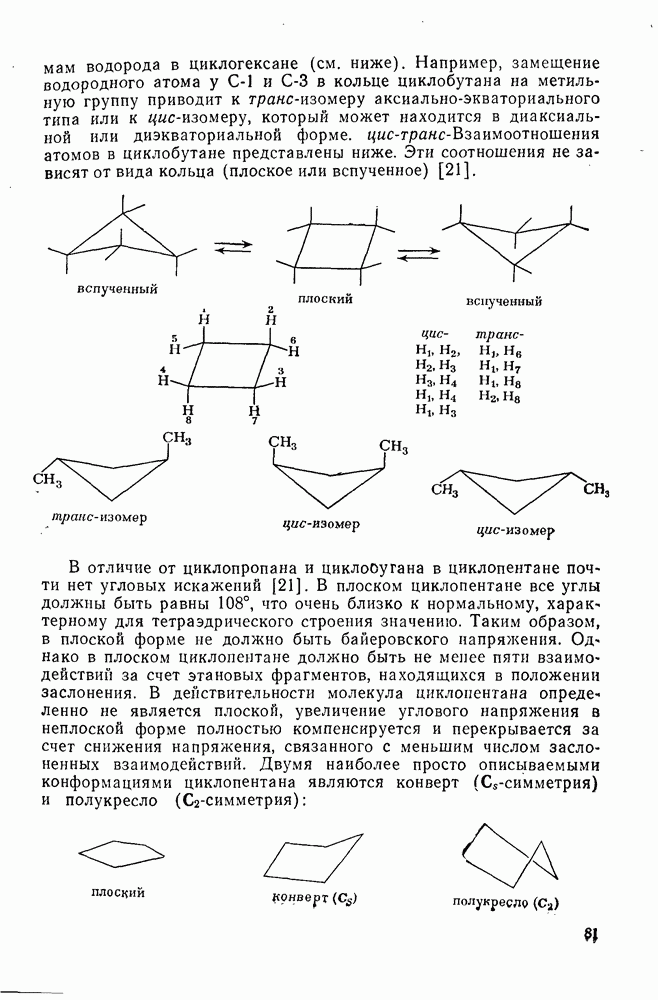
- 2.1.5. СТЕРЕОХИМИЯ И КОНФОРМАЦИОННЫЙ АНАЛИЗ
- 2.1.5.1. Углы и длины связей
- 2.1.5.2. Алкил- и полиалкилциклогексаны
- 2.1.5.3. Конформация карбоциклических колец, больших, чем циклогексан
- 2.1.6. ТЕРМОХИМИЧЕСКИЕ СВОЙСТВА
- 2.1.6.1. Горение. Алканы и циклоалканы как топливо
- 2.1.6.2. Определение теплот сгорания и термохимические свойства
- 2.1.6.3. Эмпирические методы оценки теплот образования алканов
- 2.1.6.4. Оценка теплот образования алканов на основе энергии связей
- 2.1.6.5. Оценка теплот образования алканов на основе инкрементов групп
- 2.1.6.6. Оценка теплот образования циклических, полициклических и мостиковых алканов на основе инкрементов «скошенных разобщенных» групп и «единственных» наиболее устойчивых конформаций
- 2.1.6.7. Молекулярно-механические расчеты теплот образования и энергии напряжения
- 2.1.6.8. Моно- и полициклоалкаиы
- 2.1.7. ПОЛУЧЕНИЕ АЦИКЛИЧЕСКИХ АЛКАНОВ
- 2.1.7.1. Получение алканов восстановлением олефинов
- 2.1.7.2. Получение алканов из альдегидов и кетонов
- 2.1.7.3. Получение алканов из спиртов и алкилгалогенидов
- 2.1.7.4. Получение алканов из карбоновых кислот
- 2.1.8. СИНТЕЗ МОНО- И ПОЛИЦИКЛОАЛКАНОВ
- 2.1.9. РЕАКЦИИ АЦИКЛИЧЕСКИХ АЛКАНОВ
- 2.1.9.1. Галогенирование
- 2.1.9.2. Нитрование
- 2.1.9.3. Окисление
- 2.1.9.4. Каталитическая изомеризация алканов
- 2.1.9.5. Каталитическое алкилирование алканов
- 2.1.9.6. Реакции крекинга алканов
- 2.1.9.7. Термический крекинг
- 2.1.9.8. Каталитический крекинг
- 2.1.9.9. Каталитический риформинг и дегидроциклизация алканов
- 2.1.10. РЕАКЦИИ ЦИКЛОАЛКАНОВ И ПОЛИЦИКЛОАЛКАНОВ
- 2.2. ОЛЕФИНОВЫЕ И АЦЕТИЛЕНОВЫЕ УГЛЕВОДОРОДЫ
- 2.2.2. ПОЛУЧЕНИЕ ОЛЕФИНОВ
- 2.2.2.1. Элиминирование в системах
- 2.2.2.2. Элиминирование из систем
- 2.2.2.3. Циклоэлиминирование
- 2.2.2.4. Частичное восстановление
- 2.2.2.5. Элиминирование сульфонилгидразонов
- 2.2.2.6. Реакция Виттига и родственные ей реакции
- 2.2.2.7. Различные реакции конденсации
- 2.2.2.8. Электроциклические реакции
- 2.2.2.9. Циклоолигомеризация
- 2.2.2.11. Реакции винильных производных
- 2.2.3. РЕАКЦИИ ОЛЕФИНОВ
- 2.2.3.1. Электрофильное присоединение
- 2.2.3.2. Нуклеофильное присоединение
- 2.2.3.3. Радикальное присоединение
- 2.2.3.4. Циклоприсоединение и родственные реакции
- 2.2.3.5. Окисление
- 2.2.3.6. Восстановление
- 2.2.3.7. Перегруппировки
- 2.2.3.8. Фотохимические реакции
- 2.2.3.9. Прочие реакции
- 2.3. ДИЕНЫ, ПОЛНЕНЫ И АЦЕТИЛЕНОВЫЕ УГЛЕВОДОРОДЫ
- 2.3.1. СОПРЯЖЕННЫЕ ДИЕНЫ И ПОЛНЕНЫ
- 2.3.1.2. Получение сопряженных диенов
- 2.3.2. РЕАКЦИИ СОПРЯЖЕННЫХ ДИЕНОВ
- 2.3.2.2. Восстановление
- 2.3.2.3. Гидроборирование
- 2.3.2.4. Реакция Дильса — Альдера
- 2.3.2.5. Комплексы с карбонилами железа
- 2.3.2.6. Фотохимические термические реакции
- 2.3.2.7. Прочие реакции
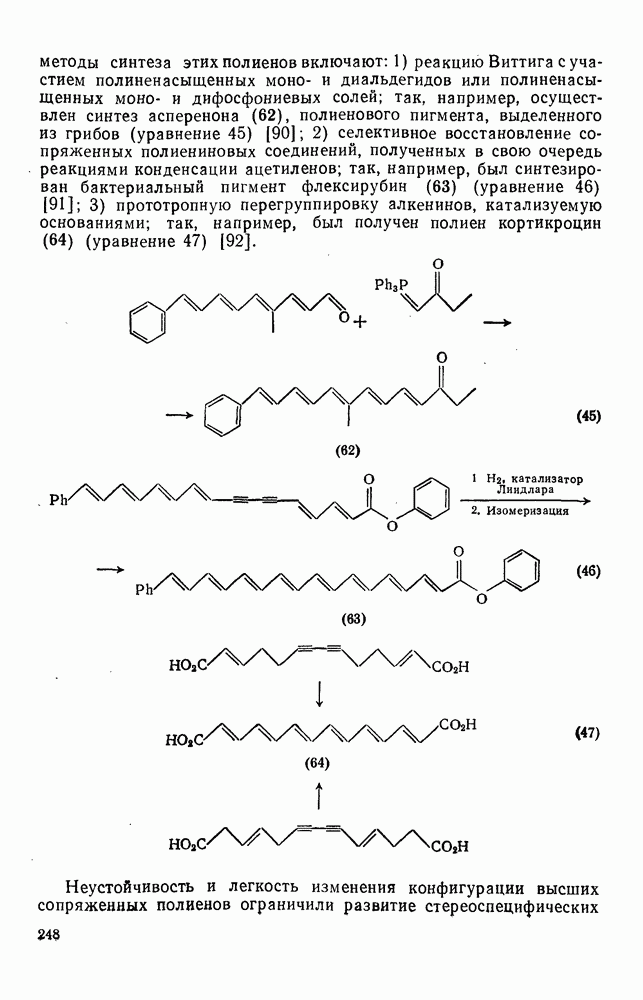
- 2.3.3. СОПРЯЖЕННЫЕ ПОЛИЕНЫ
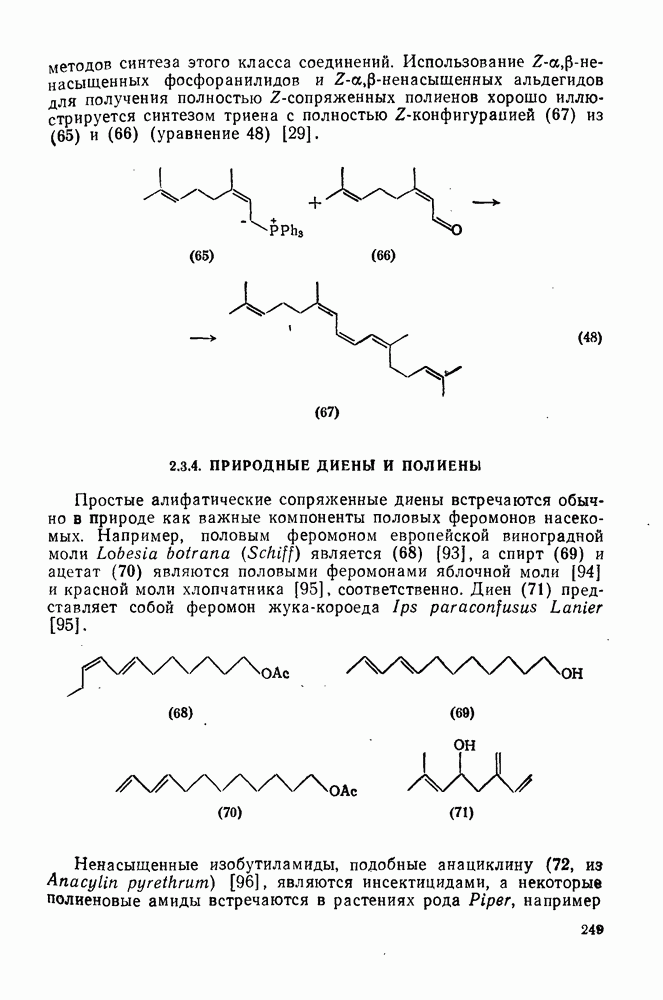
- 2.3.4. ПРИРОДНЫЕ ДИЕНЫ И ПОЛНЕНЫ
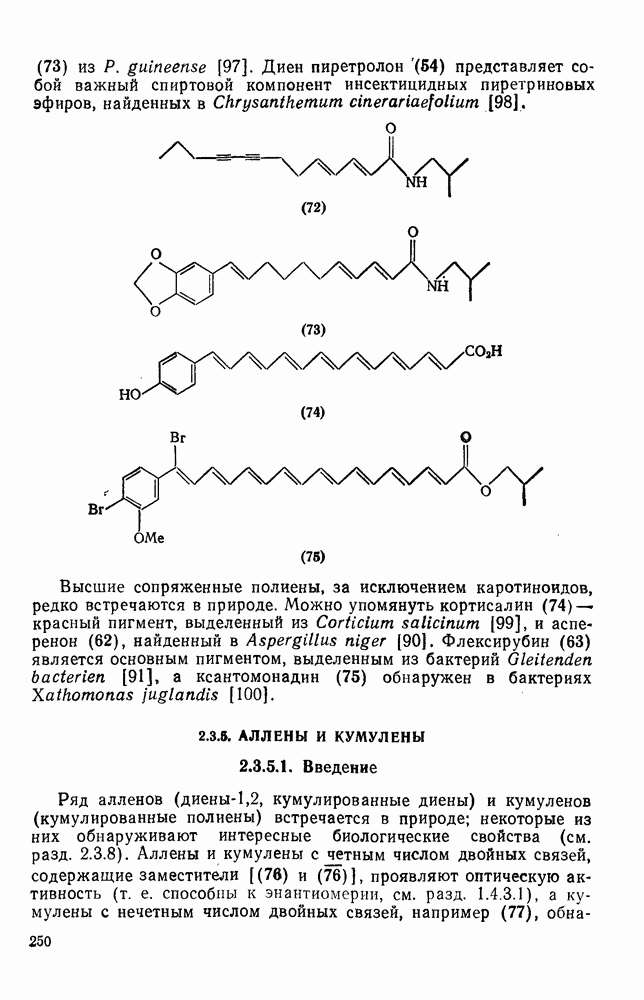
- 2.3.5. АЛЛЕНЫ И КУМУЛЕНЫ
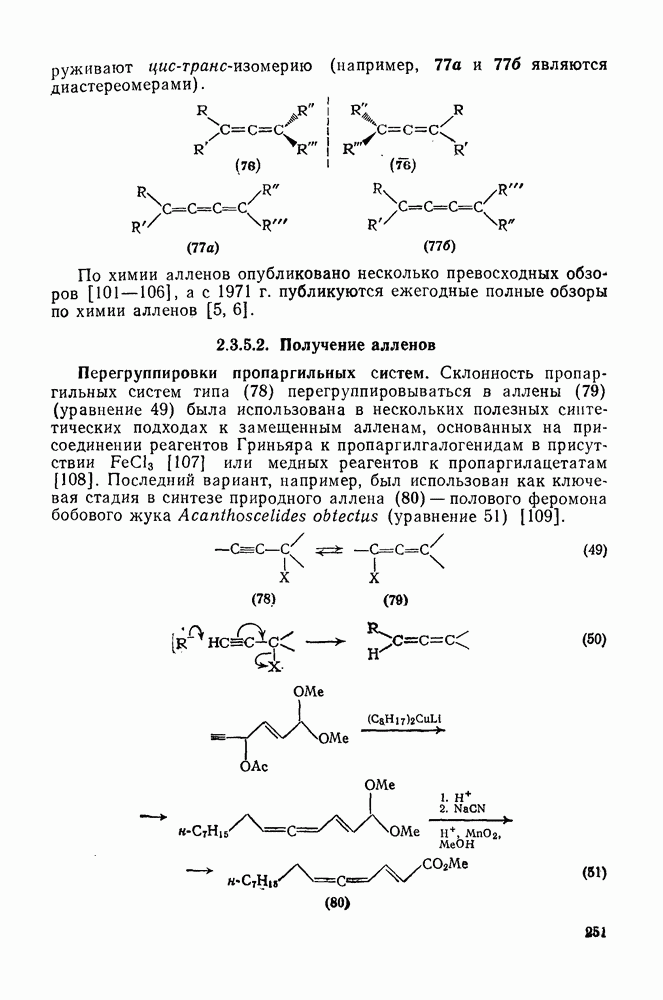
- 2.3.5.2. Получение алленов
- 2.3.6. РЕАКЦИИ АЛЛЕНОВ
- 2.3.6.2. Гидрирование
- 2.3.6.3. Реакции алленов в присутствии комплексов металлов
- 2.3.7. КУМУЛЕНЫ
- 2.3.8. ПРИРОДНЫЕ АЛЛЕНЫ И КУМУЛЕНЫ
- 2.3.9. АЦЕТИЛЕНЫ И ПОЛИАЦЕТИЛЕНЫ
- 2.3.9.2. Получение ацетиленов
- 2.3.10. РЕАКЦИИ АЦЕТИЛЕНОВ
- 2.3.10.2. Изомеризация
- 2.3.10.3. Пропаргильные перегруппировки
- 2.3.10.4. Реакции присоединения
- 2.3.10.5. Гидроборирование и гидроалюминирование
- 2.3.10.6. Реакции замещения
- 2.3.10.7. Восстановление
- 2.3.10.8. Окисление
- 2.3.10.9. Циклоприсоединение
- 2.3.10.10. Реакции катализуемые металлами
- 2.3.11. ПОЛИАЦЕТИЛЕНЫ
- 2.3.12. ПРИРОДНЫЕ АЦЕТИЛЕНЫ И ПОЛИАЦЕТИЛЕНЫ
- 2.3.13. СОПРЯЖЕННЫЕ ЕНИНЫ
- 2.3.13.1. Получение сопряженных енинов
- 2.3.14. РЕАКЦИИ СОПРЯЖЕННЫХ ЕНИНОВ
- 2.3.15. ПРИРОДНЫЕ СОПРЯЖЕННЫЕ ЕНИНЫ
- 2.4. АРОМАТИЧНОСТЬ
- 2.4.2. ЭЛЕКТРОННЫЕ ТЕОРИИ СТРОЕНИЯ БЕНЗОЛА
- 2.4.3. КРИТЕРИИ АРОМАТИЧНОСТИ
- 2.4.3.1. Термодинамические свойства
- 2.4.3.2. Структурные особенности
- 2.4.3.3. Магнитные свойства
- 2.4.3.4. Прочие критерии
- 2.4.4. АНТИАРОМАТИЧНОСТЬ
- 2.4.4.1. Термодинамические свойства
- 2.4.4.2. Структурные особенности
- 2.4.4.3. Магнитные свойства
- 2.4.4.4. Прочие свойства
- 2.4.5. ТЕОРЕТИЧЕСКИЕ ОПРЕДЕЛЕНИЯ АРОМАТИЧНОСТИ
- 2.4.5.1. Полуэмпирические расчеты и дьюаровская резонансная энергия
- 2.4.5.2. Расчеты по методу валентных пар и применение резонансного метода
- 2.4.5.3. Локализация связей
- 2.4.5.4. Связь энергетических критериев с критериями локализации связей
- 2.4.6. АРОМАТИЧЕСКИЕ ПЕРЕХОДНЫЕ СОСТОЯНИЯ
- 2.5. АРЕНЫ И ИХ РЕАКЦИИ
- 2.5.2. НОМЕНКЛАТУРА
- 2.5.3. ФИЗИЧЕСКИЕ СВОЙСТВА АРЕНОВ
- 2.5.4. ПРОМЫШЛЕННОЕ ПРОИЗВОДСТВО АРЕНОВ
- 2.5.5. ЦИКЛОТРИМЕРИЗАЦИЯ АЦЕТИЛЕНОВ
- 2.5.6. РЕАКЦИИ ЭЛЕКТРОФИЛЬНОГО ПРИСОЕДИНЕНИЯ — ЭЛИМИНИРОВАНИЯ АРЕНОВ
- 2.5.6.1. Механизм ароматического нитрования [15]
- 2.5.6.2. Кинетические изотопные эффекты [21]
- 2.5.6.3. Реакции, включающие ипсо-протонирование
- 2.5.6.4. Металлирование
- 2.5.6.5. Электрофилы IV группы
- 2.5.6.6. Электрофилы V группы
- 2.5.6.7. Электрофилы VI группы [18, 56]
- 2.5.6.8. Электрофилы VII группы [18, 25а, 56]
- 2.5.7. ОРИЕНТАЦИЯ В РЕАКЦИЯХ ЭЛЕКТРОФИЛЬНОГО ПРИСОЕДИНЕНИЯ — ЭЛИМИНИРОВАНИЯ
- 2.5.8. РАДИКАЛЬНОЕ ГАЛОГЕНИРОВАНИЕ АРЕНОВ В БОКОВУЮ ЦЕПЬ [96]
- 2.5.9. РЕАКЦИИ ПРИСОЕДИНЕНИЯ К АРЕНАМ
- 2.5.9.1. Восстановление аренов
- 2.5.9.2. Термическое циклоприсоединение к аренам
- 2.5.9.3. Фотоциклоприсоединение к моноциклическим аренам [126]
- 2.5.9.4. Фотохимические реакции полициклических аренов
- 2.6.10. ФОТОИЗОМЕРИЗАЦИЯ АРЕНОВ [126б]
- 2.5.11. ОКИСЛЕНИЕ АРЕНОВ [153]
- 2.5.12. РЕАКЦИИ АРЕНОВ С СИНГЛЕТНЫМ КИСЛОРОДОМ [162]
- 2.5.13. ПРИГОТОВЛЕНИЕ БИ- И ПОЛИАРИЛОВ
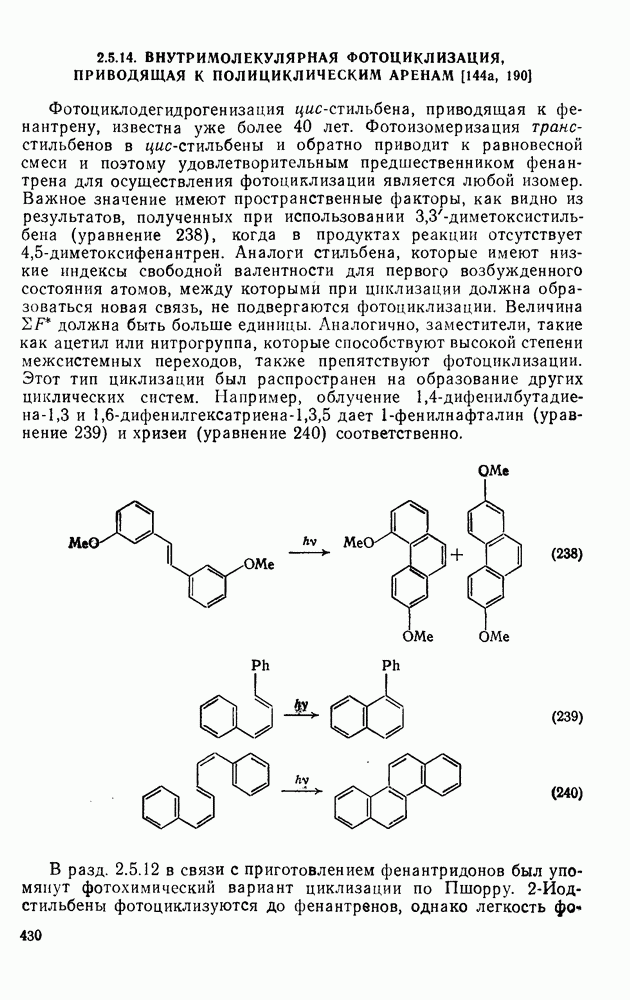
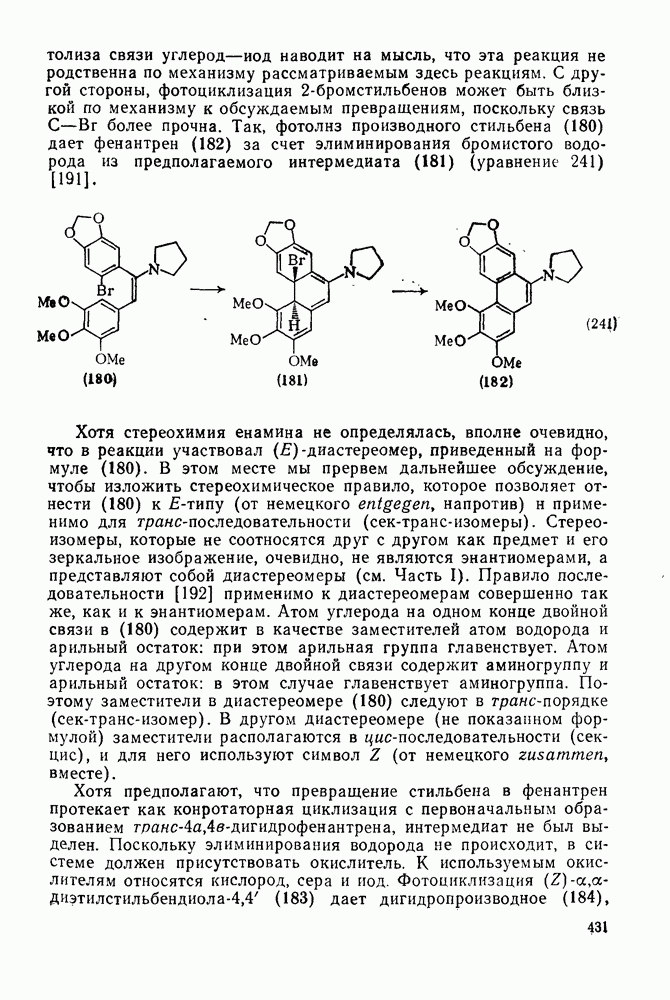
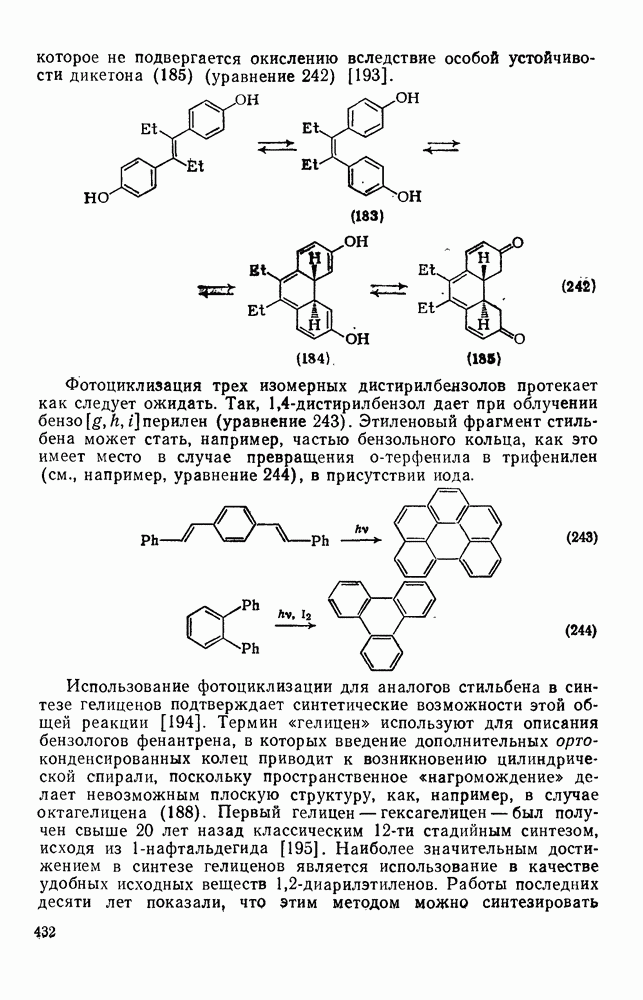
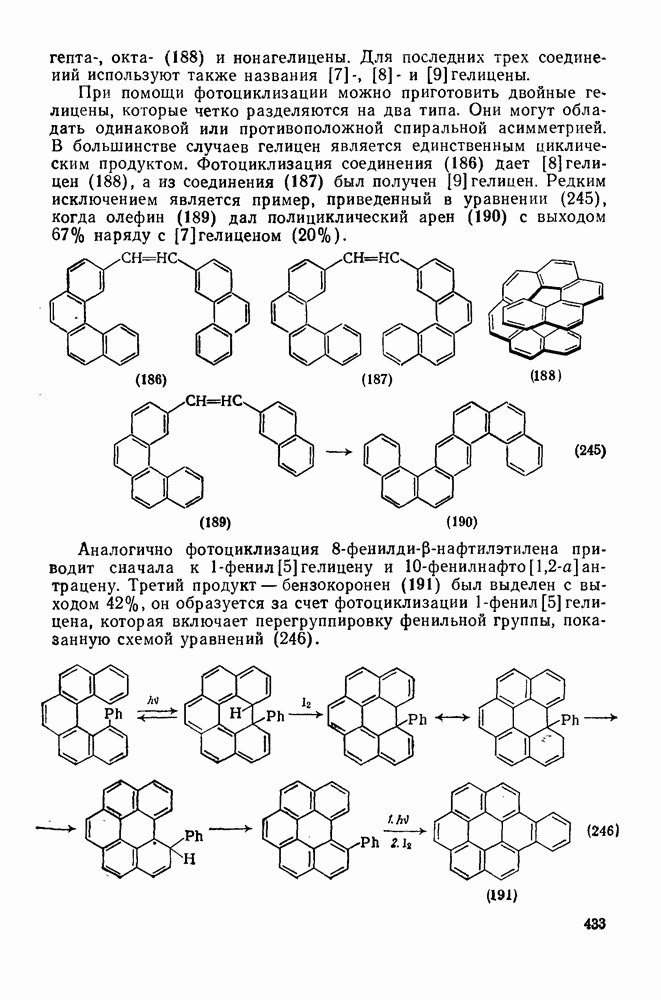
- 2.5.14. ВНУТРИМОЛЕКУЛЯРНАЯ ФОТОЦИКЛИЗАЦИЯ, ПРИВОДЯЩАЯ К ПОЛИЦИКЛИЧЕСКИМ АРЕНАМ
- 2.5.15. ВНУТРИМОЛЕКУЛЯРНАЯ ЦИКЛИЗАЦИЯ ДИЗАМЕЩЕННЫХ АРЕНОВ
- 2.5.16. ЦИКЛОФАНЫ
- 2.5.17. КОНФОРМАЦИЯ И ХИРАЛЬНОСТЬ АРЕНОВ
- 2.5.18. АЗУЛЕНЫ И НЕБЕНЗОИДНЫЕ АРЕНЫ
- 2.6. АННУЛЕНЫ И РОДСТВЕННЫЕ СИСТЕМЫ
- 2.6.2. МЕТОДЫ СИНТЕЗА
- 2.6.2.1. Окислительное сочетание терминальных ацетиленов (метод Зондхеймера)
- 2.6.2.2. Фотооблучение полициклических валентных таутомеров
- 2.6.2.3. Валентная таутомерия типа норкарадиен — циклогептатриен (метод Фогеля)
- 2.6.2.4. Прочие методы
- 2.6.3. СВОЙСТВА АННУЛЕНОВ
- 2.6.4. СВОЙСТВА 4n-АННУЛЕНОВ
- 2.6.5. ДЕГИДРОАННУЛЕНЫ
- 2.6.6. АННЕЛИРОВАННЫЕ АННУЛЕНЫ
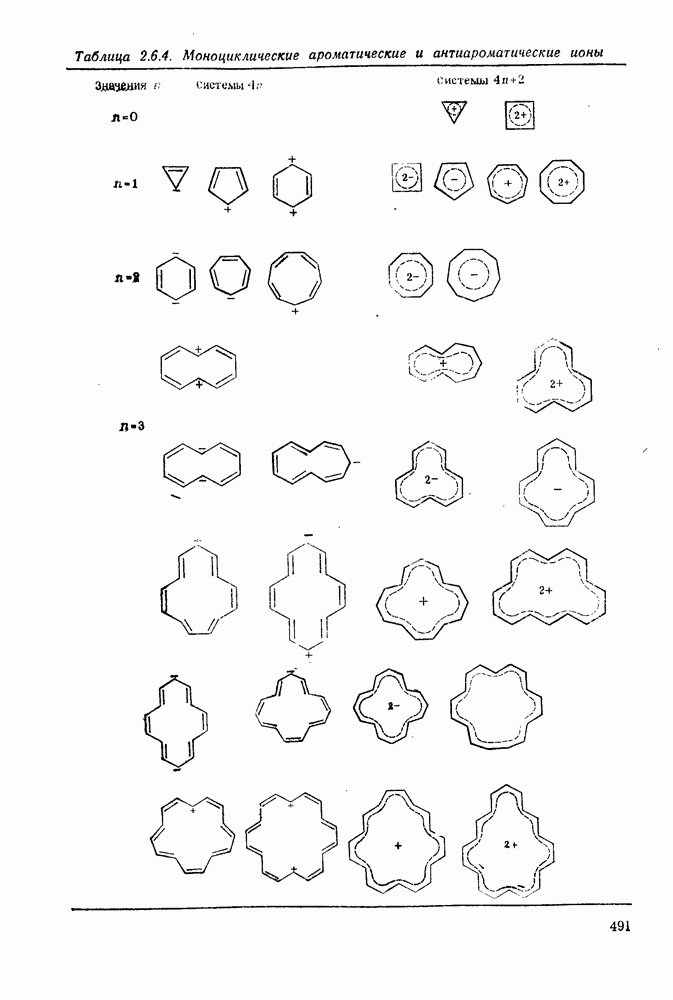
- 2.6.7. АРОМАТИЧЕСКИЕ И АНТИАРОМАТИЧЕСКИЕ МОНОЦИКЛИЧЕСКИЕ ИОНЫ
- 2.6.8. АРОМАТИЧЕСКИЕ И АНТИАРОМАТИЧЕСКИЕ ПОЛИЦИКЛИЧЕСКИЕ ИОНЫ
- 2.6.9. ГОМОАРОМАТИЧЕСКИЕ СИСТЕМЫ
- 2.7. КАРБОКАТИОНЫ И КАРБАНИОНЫ
- 2.7.1.2. Краткий исторический очерк развития химии карбокатионов
- 2.7.1.3. Методы генерации карбокатионов
- 2.7.1.4. Типы карбокатионов
- 2.7.1.5. Изучение карбокатионов: методы и результаты
- 2.7.1.6. Реакции карбокатионов
- 2.7.2. КАРБАНИОНЫ
- 2.7.2.2. Методы генерации карбанионов
- 2.7.2.3. Типы карбанионов
- 2.7.2.4. Физические свойства карбанионов
- 2.7.5.2. Реакции карбанионов
- 2.8. РАДИКАЛЫ, КАРБЕНЫ, АРИНЫ
- 2.8.1. РАДИКАЛЫ
- 2.8.1.1. Структура, устойчивость и реакционная способность радикалов
- 2.8.1.2. Методы генерации и реакции радикалов
- 2.8.2. КАРБЕНЫ
- 2.8.2.1. Методы генерации карбенов и карбеноидов
- 2.8.2.2. Реакции карбенов
- 2.8.3. АРИНЫ
- 2.8.3.1. Структура и спектры аринов
- 2.8.3.2. Методы генерации аринов
- 2.8.3.3. Реакции аринов
- ЧАСТЬ 3. ГАЛОГЕНСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
- 3.2. МЕТОДЫ ГАЛОГЕНИРОВАНИЯ
- 3.2.1. Гомолитическое замещение водорода
- 3.2.1.2. Использование галогенпроизводных в качестве реагентов
- 3.2.2. Гомолитическое замещение функциональных групп
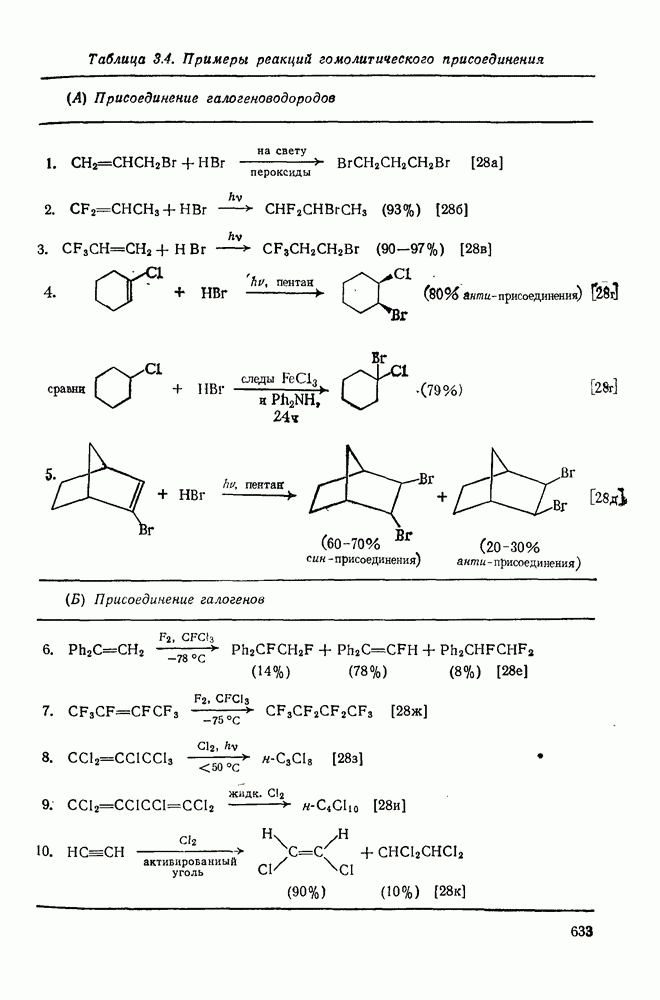
- 3.2.3. Гомолитическое присоединение к ненасыщенным системам
- 3.2.3.1. Присоединение галогеноводородов
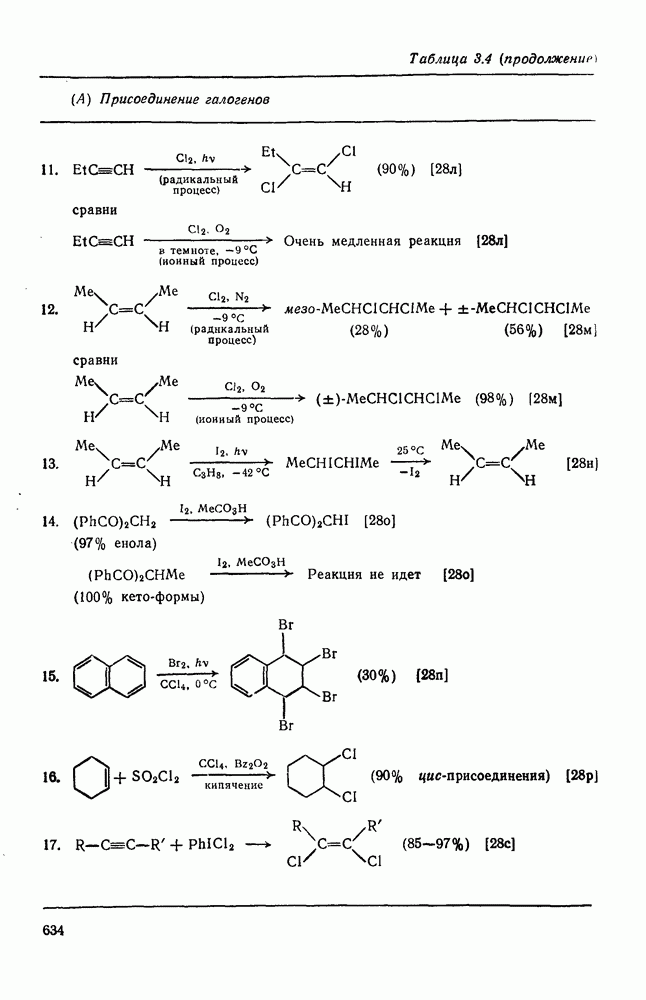
- 3.2.3.2. Присоединение галогенов
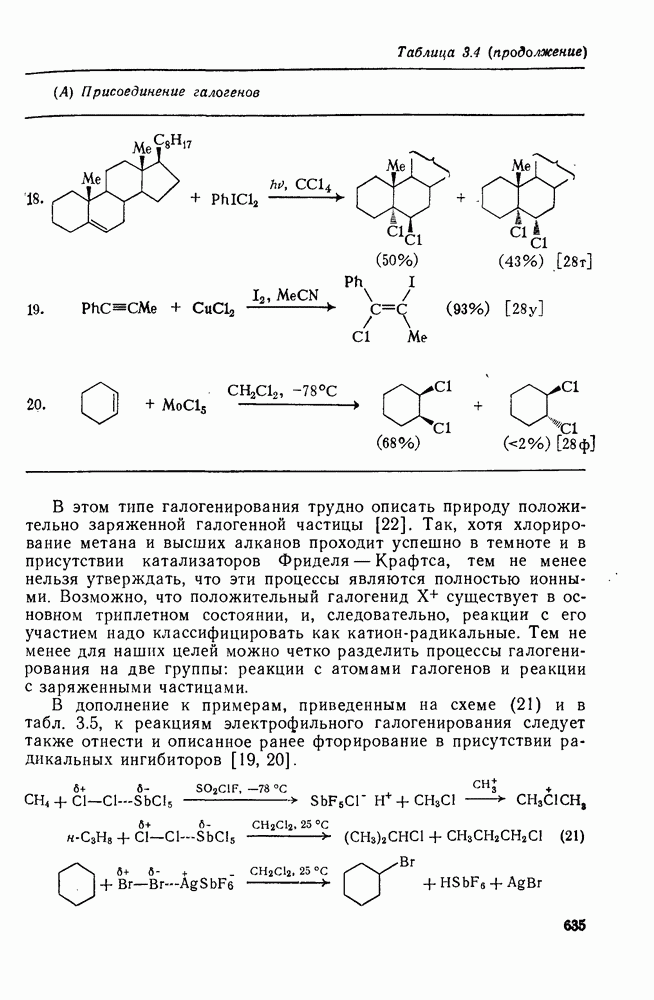
- 3.2.4. Электрофильное галогенирование
- 3.2.4.1. Замещение у насыщенной связи С-Н
- 3.2.4.2. Реакции с ненасыщенными системами
- 3.2.4.3. Реакции с карбанионами
- 3.2.5. Нуклеофильное галогенирование
- 3.2.5.1. Галогенирование с замещением функциональной группы
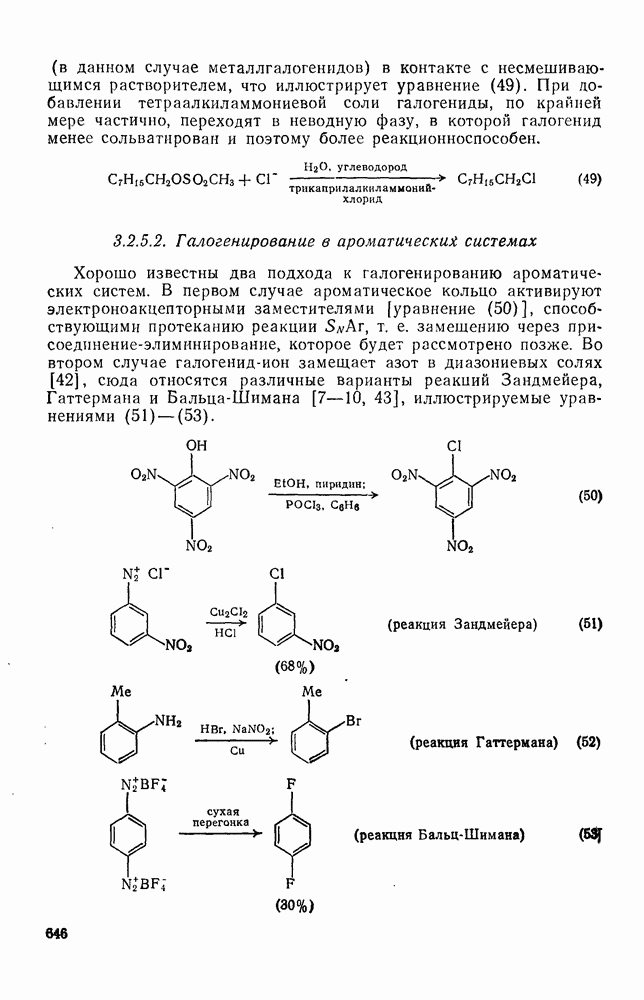
- 3.2.5.2. Галогенирование в ароматических системах
- 3.2.5.3. Галогенирование путем обмена галогенов
- 3.2.6. Синтез полигалогенированных соединений
- 3.2.6.1. Синтез полифторированных соединений
- 3.2.6.2. Синтез других полигалогенированных соединений
- 3.3. ГАЛОГЕНАЛКАНЫ
- 3.3.1. Характеристика связей углерод-галоген
- 3.3.2. Промышленное применение
- 3.3.3. Нуклеофильное замещение галогена
- 3.3.3.1. Реакции SN2 и родственные процессы
- 3.3.3.2. Соучастие соседних групп
- 3.3.3.3. Реакции SN1 и относительно долгоживущие карбениевые ионы
- 3.3.3.4. Галогенониевые ионы
- 3.3.3.5. Галогенсодержащие карбениевые ионы
- 3.3.3.6. Механизм замещения с переносом электрона
- 3.3.4. Восстановление
- 3.3.5. Замещение на металлы
- 3.3.6. Элиминирование
- 3.3.6.1. b-Элиминирование
- 3.3.6.2. Галогенкарбанионы
- 3.3.6.3. Элиминирование через карбанионы
- 3.3.6.4. b-Элиминирование из металлорганических соединений
- 3.3.6.5. a-Элиминирование (генерирование карбенов)
- 3.4. ГАЛОГЕНАЛКЕНЫ
- 3.4.1. Синтез галогеналкенов
- 3.4.2. Нуклеофильная атака
- 3.4.2.1. Реакции, индуцируемые фторид-ионом
- 3.4.2.2. Другие реакции замещения
- 3.4.3. Радикальное присоединение
- 3.4.4. Электрофильное присоединение
- 3.4.5. Циклоприсоединение
- 3.4.5.1. [2+2]-Циклоприсоединение
- 3.4.5.2. [4+2]-Циклоприсоединение
- 3.5. ГАЛОГЕНАЛКИНЫ
- 3.6. ГАЛОГЕНАРЕНЫ
- 3.6.1. Замещение галогена
- 3.6.1.2. Присоединение-элиминирование
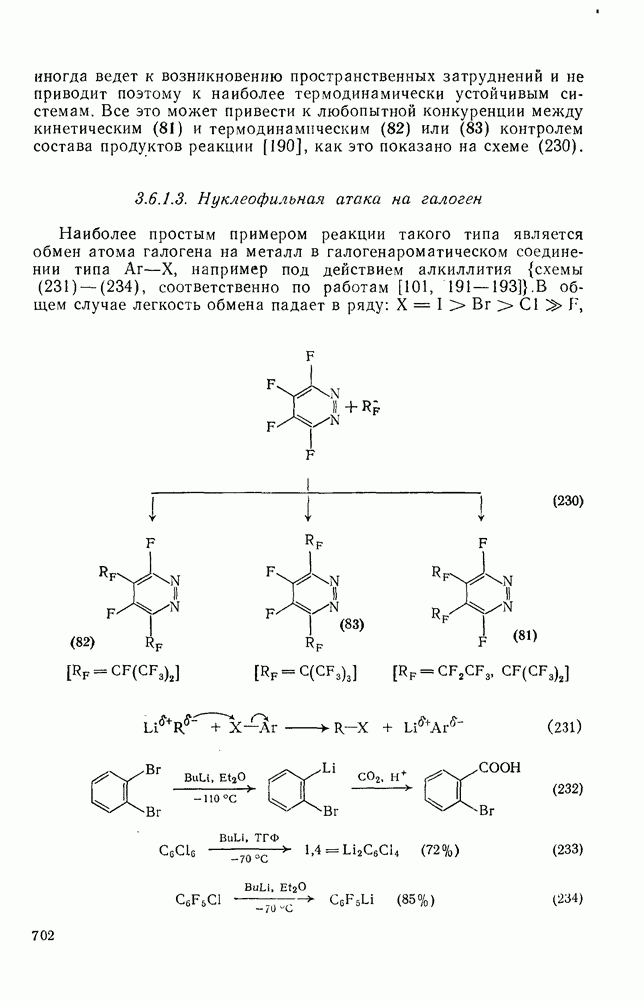
- 3.6.1.3. Нуклеофильная атака на галоген
- 3.6.1.4. Перенос электрона
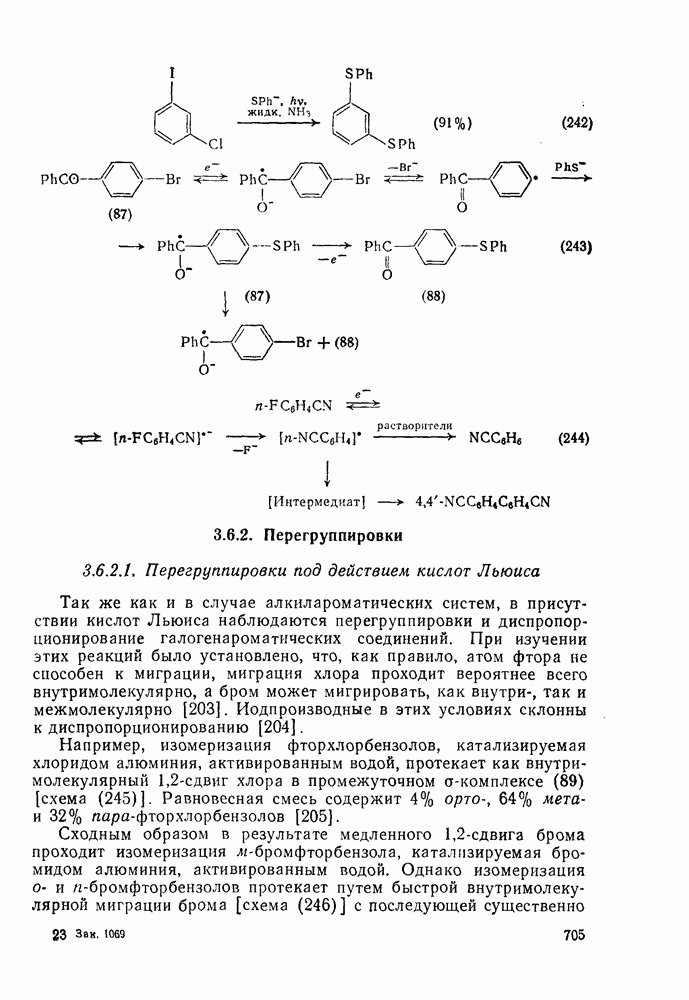
- 3.6.2. Перегруппировки
- 3.6.2.1. Перегруппировки под действием кислот Льюиса
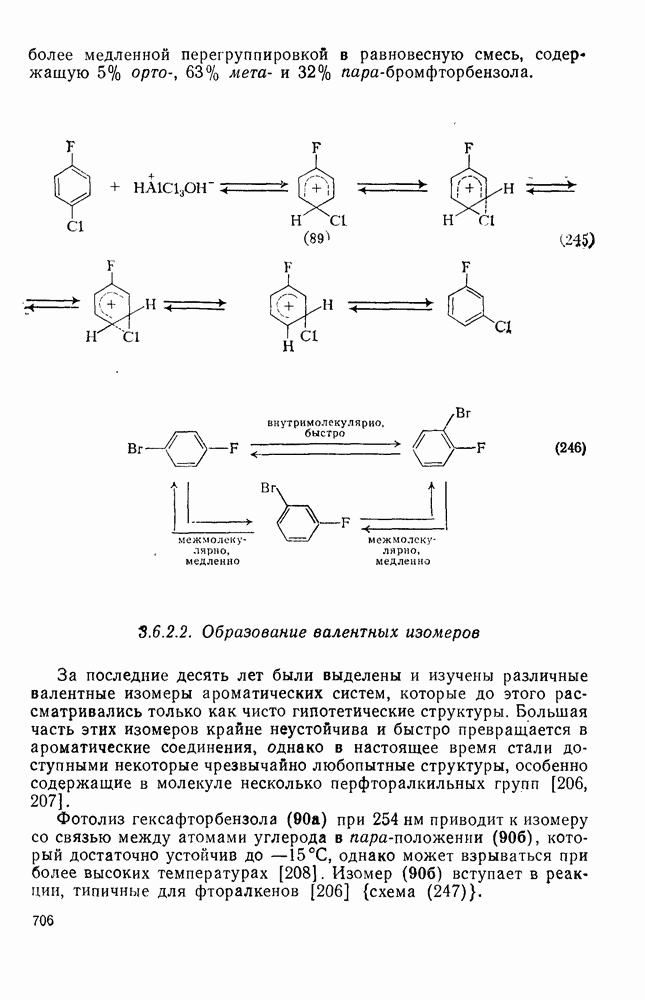
- 3.6.2.2. Образование валентных изомеров