| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
2.1.10. РЕАКЦИИ ЦИКЛОАЛКАНОВ И ПОЛИЦИКЛОАЛКАНОВ
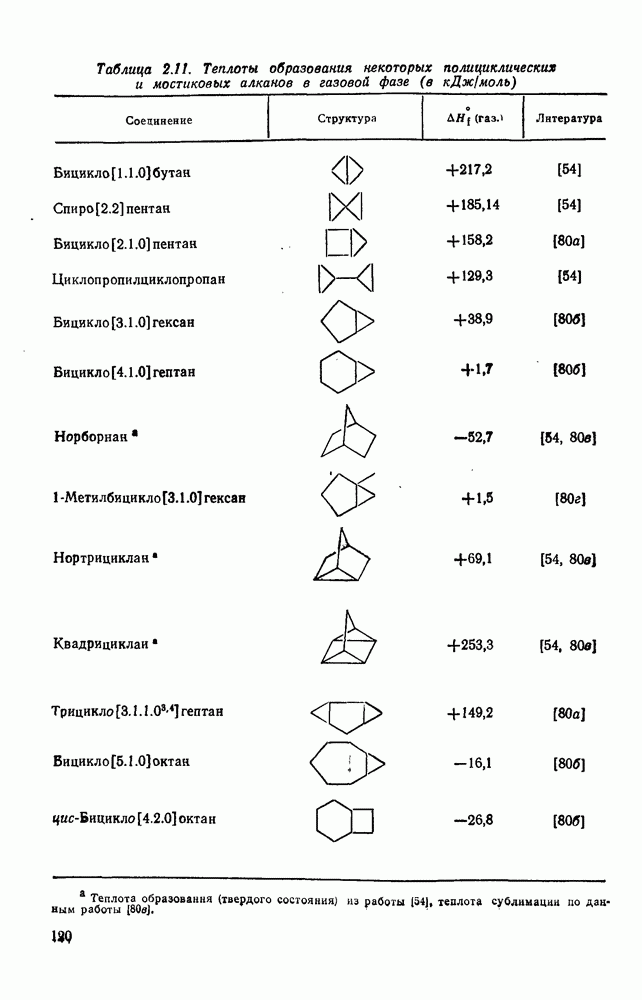
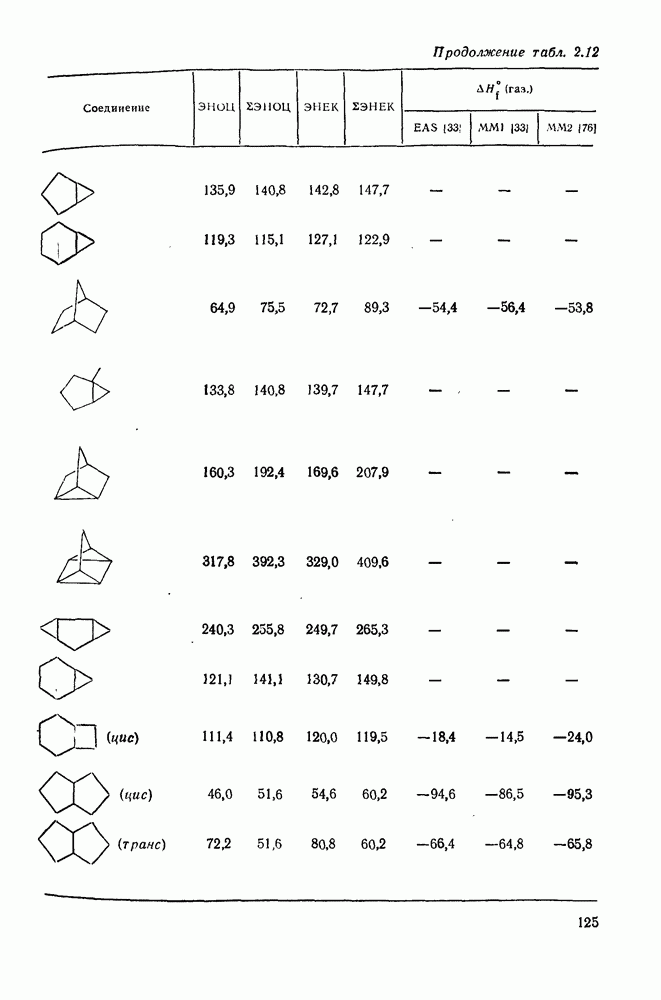
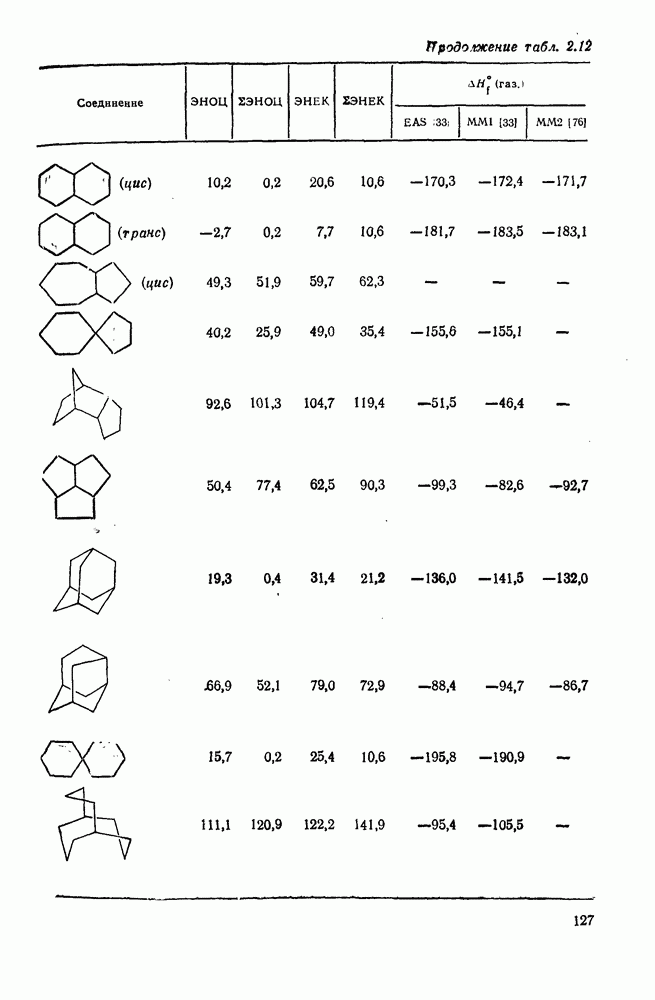
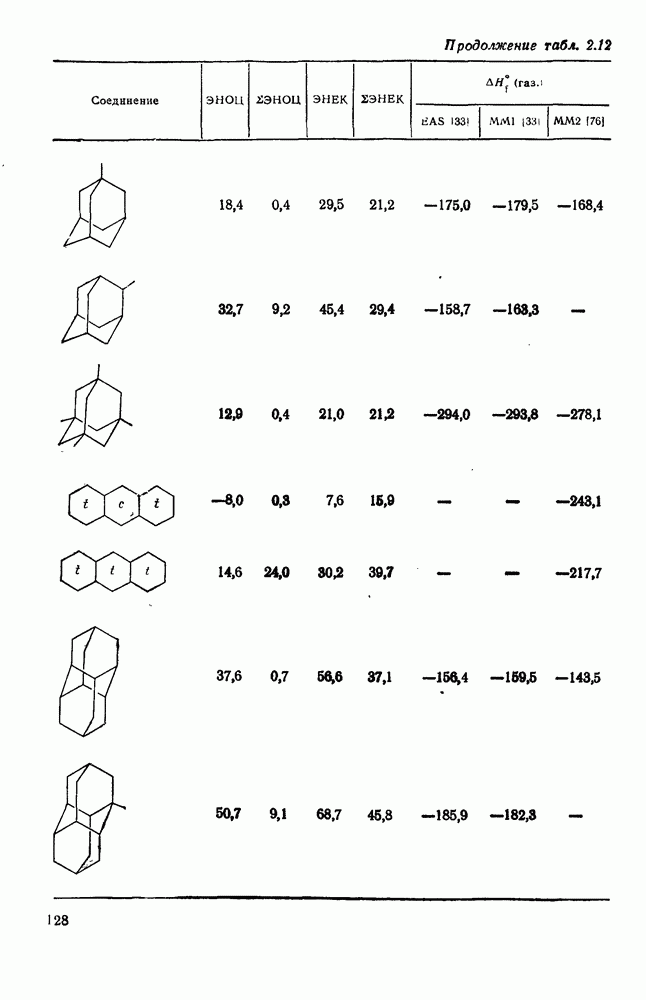
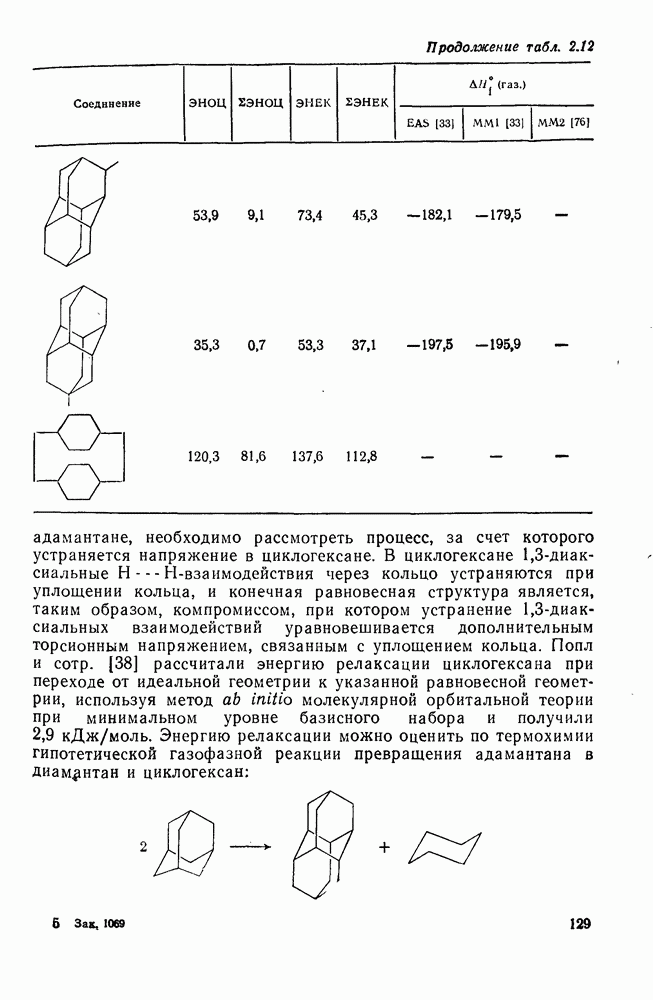
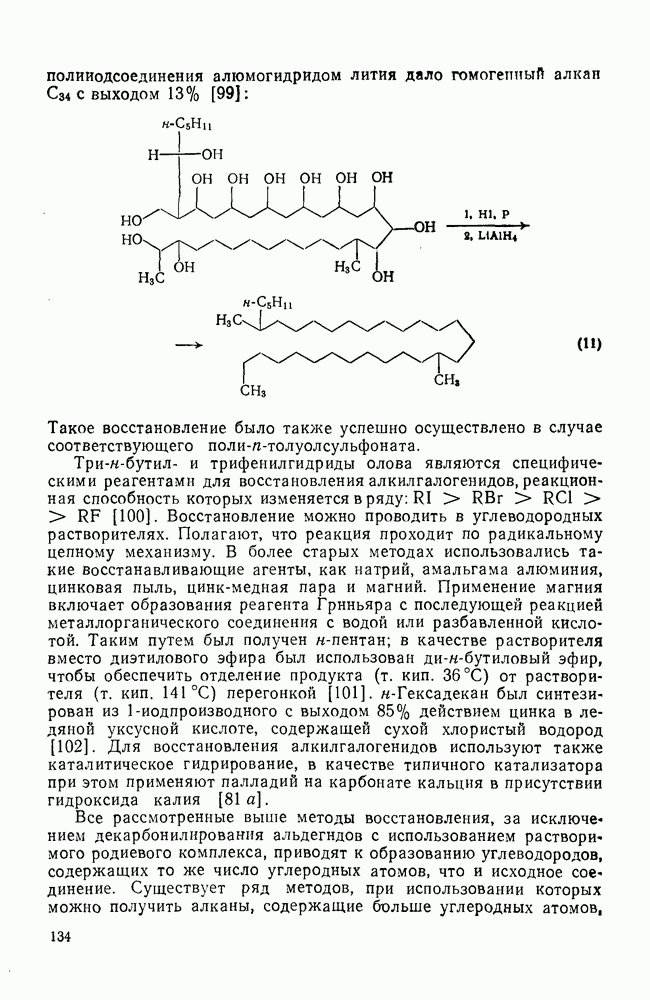
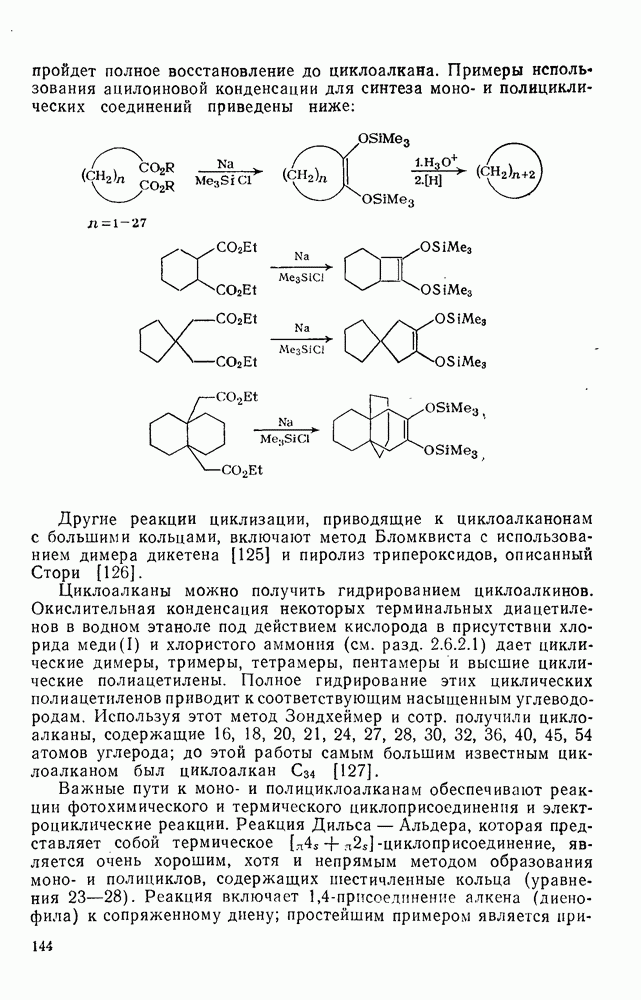
Многие из реакций ациклических насыщенных углеводородов, рассмотренных выше, применимы также для циклоалканов и полициклоалканов. Так, многие циклоалканы вступают в реакции ионного и свободнорадикального галогенирования, окисления и нитрования без изменения скелета или разрыва углерод-углеродной связи. Различия в химическом поведении часто обусловлены наличием в некоторых циклических структурах избыточного углового напряжения. Как отмечалось в разделах, посвященных стереохимии и термохимии, угловое напряжение характерно для малых циклов, что отражается на значениях их теплот сгорания и энергиях циклизации (см. табл. 2.10). Следует ожидать, что наличие сильного углового напряжения должно отразиться и на некоторых химических свойствах. Циклопропан гораздо более реакционноспособен, чем другие циклоалканы, благодаря освобождению энергии напряжения при раскрытии цикла. Так, одной из наиболее легко проходящих реакций изомеризации является превращение циклопропана в пропен. Эта реакция может быть осуществлена термически или каталитически в присутствии платины, палладия, железа, никеля, родия или оксида алюминия при значительно более низких температурах. Циклобутан менее реакционноспособен, чем циклопропан, а циклоалканы с большими циклами реагируют в большинстве случаев аналогично соответствующим ациклическим соединениям. Хорошей иллюстрацией является поведение циклоалканов при каталитическом гидрогенолизе [81]. Каталитический гидрогенолиз ординарной углерод-углеродной связи в ациклических алканах проходит только при высоких температурах  и в конечном итоге ведет к метану. Однако гидрогенолиз циклопропана и многих алкилциклопропанов на платине идет легко при комнатной температуре. Для гидрогенолиза циклобутана в н-бутан требуется более высокая температура.
и в конечном итоге ведет к метану. Однако гидрогенолиз циклопропана и многих алкилциклопропанов на платине идет легко при комнатной температуре. Для гидрогенолиза циклобутана в н-бутан требуется более высокая температура.
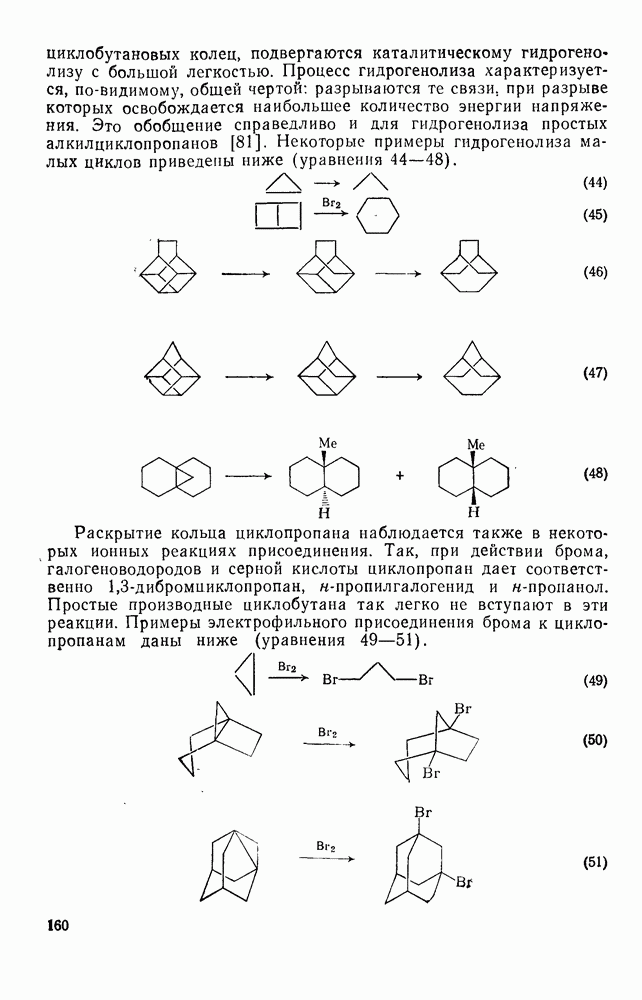
Очень напряженные полициклоалканы, состоящие из нескольких конденсированных циклопропановых или циклобутановых колец, подвергаются каталитическому гидрогенолизу с большой легкостью. Процесс гидрогенолиза характеризуется, по-видимому, обшей чертой: разрываются те связи, при разрыве которых освобождается наибольшее количество энергии напряжения. Это обобщение справедливо и для гидрогенолиза простых алкилциклопропанов [81]. Некоторые примеры гидрогенолиза малых циклов приведены ниже (уравнения 44—48).

Раскрытие кольца циклопропана наблюдается также в некоторых ионных реакциях присоединения. Так, при действии брома, галогеноводородов и серной кислоты циклопропан дает соответственно  -дибромииклопропан, н-пропилгалогенид и н-пропанол. Простые производные циклобутана так легко не вступают в эти реакции. Примеры электрофильного присоединения брома к циклопропанам даны ниже (уравнения 49—51).
-дибромииклопропан, н-пропилгалогенид и н-пропанол. Простые производные циклобутана так легко не вступают в эти реакции. Примеры электрофильного присоединения брома к циклопропанам даны ниже (уравнения 49—51).

Однако не все реакции циклопропанов приводят к ациклическим продуктам. Свободнорадикальное хлорирование циклопропана в мягких условиях приводит к хлор- и  -дихлорциклопропанам. Аналогично идет свободнорадикальное галогенирование высших циклоалканов. Некоторые полициклоалканы очень легко подвергаются ионному бромированию по атому углерода, находящемуся в голове мостика. Так, адамантан, диамантан, триамантан и их алкильные производные селективно реагируют с жидким бромом, давая соответствующие бромиды [134]. Однако в присутствии кислот Льюиса образуются полибромпроизводные. Циклоалканы и полициклоалканы селективно окисляются озоном, адсорбированным на силикагеле [144]. Алкилциклопропаны реагируют по
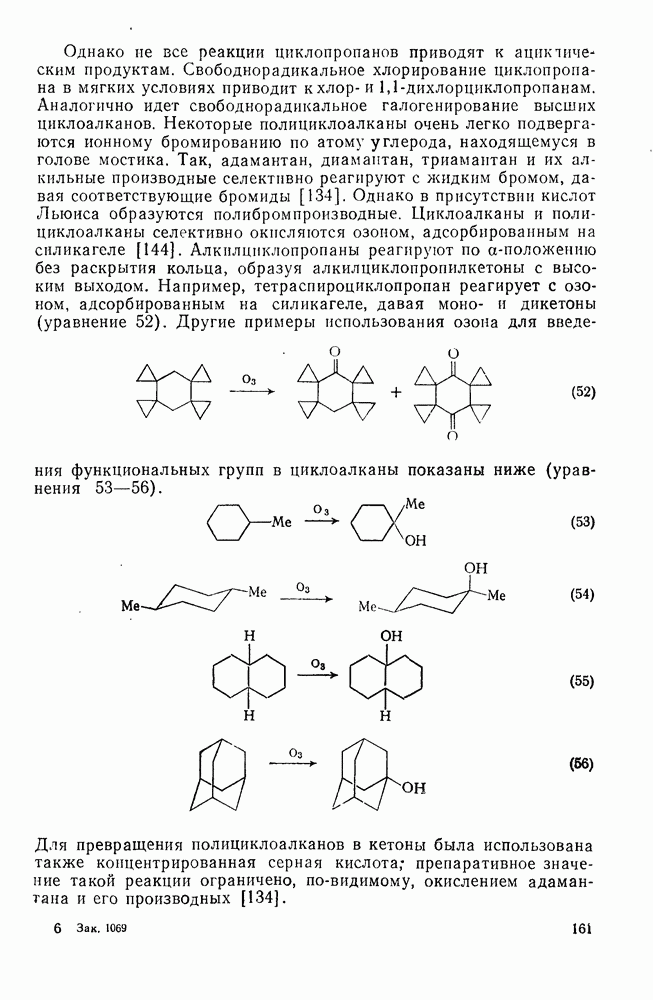
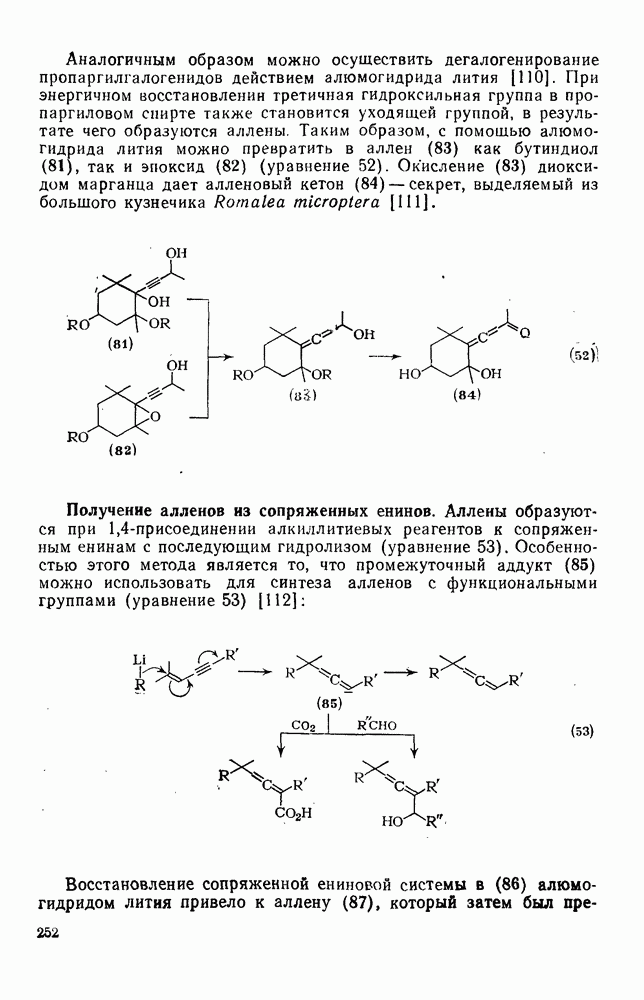
-дихлорциклопропанам. Аналогично идет свободнорадикальное галогенирование высших циклоалканов. Некоторые полициклоалканы очень легко подвергаются ионному бромированию по атому углерода, находящемуся в голове мостика. Так, адамантан, диамантан, триамантан и их алкильные производные селективно реагируют с жидким бромом, давая соответствующие бромиды [134]. Однако в присутствии кислот Льюиса образуются полибромпроизводные. Циклоалканы и полициклоалканы селективно окисляются озоном, адсорбированным на силикагеле [144]. Алкилциклопропаны реагируют по  -положению без раскрытия кольца, образуя алкилциклопропилкетоны с высоким выходом. Например, тетраспироциклопропан реагирует с озоном, адсорбированным на силикагеле, давая моно- и дикетоны (уравнение 52). Другие примеры использования озона для введе-
-положению без раскрытия кольца, образуя алкилциклопропилкетоны с высоким выходом. Например, тетраспироциклопропан реагирует с озоном, адсорбированным на силикагеле, давая моно- и дикетоны (уравнение 52). Другие примеры использования озона для введе-

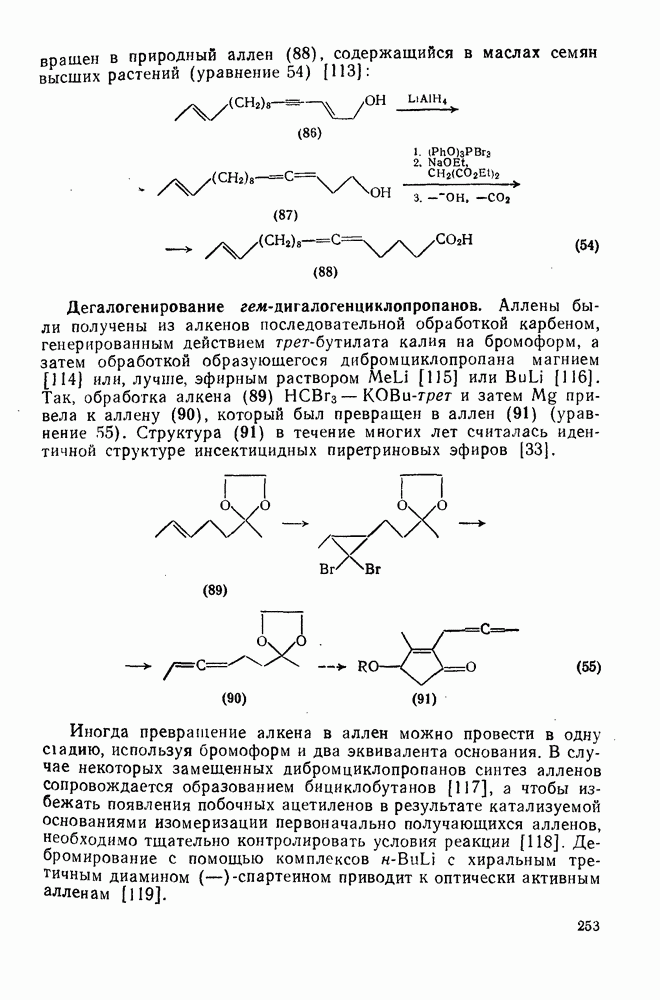
ния функциональных групп в циклоалканы показаны ниже (уравнения 53—56).

Для превращения полициклоалканов в кетоны была использована также концентрированная серная кислота; препаративное значение такой реакции ограничено, по-видимому, окислением адамантана и его производных [134].
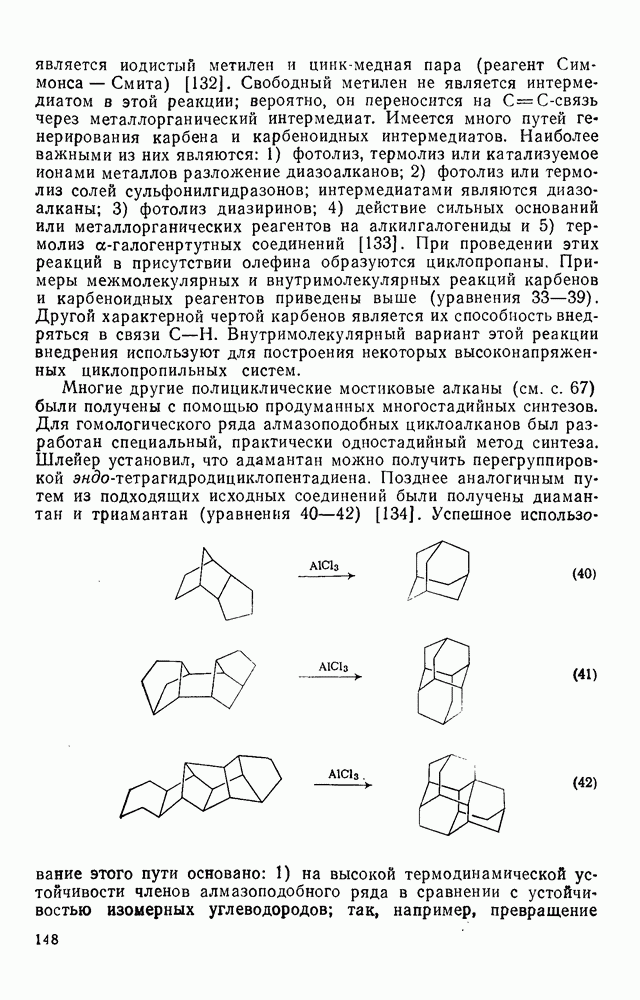
Как и в случае ациклических алканов, имеется большое число примеров реакций изомеризации и перегруппировки моно- и полициклоалканов [141, 142]. Кислоты Льюиса как катализаторы вызывают реакции сужения и расширения циклов, проходящие через карбениевые ионы, по типу, рассмотренному для изомеризации н-бутана в изобутан. В равновесной смеси циклоалканов обычно преобладают пяти- и шестичленные циклы. Трех-, четырех-, семи- и более высокочленные циклы обычно отсутствуют в равновесных смесях, что находится в согласии с общими соображениями относительно энергии напряжения этих циклов. Так, циклопентан не образует циклопропанов или метилциклобутана, а циклогептан изо-меризуется в метилциклогексан. При обычной температуре в равновесной смеси пяти- и шестичленных циклов преобладают изомеры с большим циклом. Так, в присутствии алюминийгалогенидов при  метилциклопентан и циклогексан образуют равновесную смесь, содержащую 88% циклогексана. Перегруппировка полициклоалканов, проходящая через карбениевые ионы, может иметь синтетическое значение; особенно большой интерес представляет синтез адамантанов из напряженных полициклов, катализуемый кислотами Льюиса (см. уравнения 40—42). Хотя такие перегруппировки проходят по сложному механизму, высокая термодинамическая устойчивость продуктов обеспечивает протекание реакции [145].
метилциклопентан и циклогексан образуют равновесную смесь, содержащую 88% циклогексана. Перегруппировка полициклоалканов, проходящая через карбениевые ионы, может иметь синтетическое значение; особенно большой интерес представляет синтез адамантанов из напряженных полициклов, катализуемый кислотами Льюиса (см. уравнения 40—42). Хотя такие перегруппировки проходят по сложному механизму, высокая термодинамическая устойчивость продуктов обеспечивает протекание реакции [145].
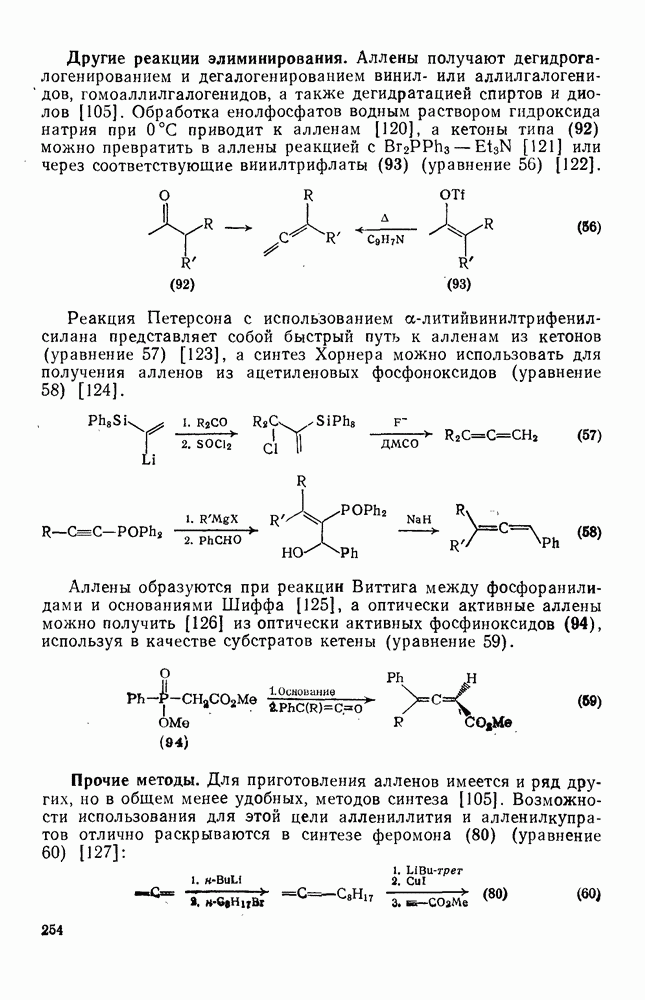
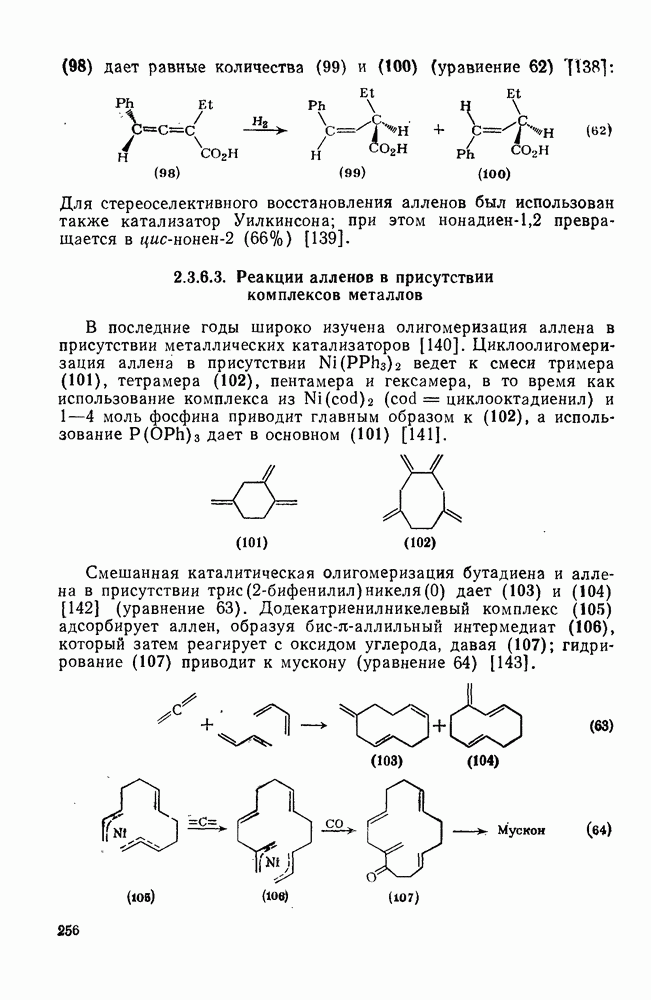
Высокое угловое напряжение в полициклах, включающих малые кольца, обеспечивает протекание недавно обнаруженных перегруппировок и реакций изомеризации под влиянием ионов металлов и комплексов металлов. Некоторые примеры таких реакций приведены ниже (уравнения 57—64).

 (64)
(64)
Иногда тип изомеризации или перегруппировки зависит от природы катализатора. Например, в присутствии комплексов родия (I) кубан дает кунеан, а в присутствии ионов серебра — трициклооктадиен. Предполагают, что в этих реакциях принимают участие металлорганические интермедиаты, однако истинный механизм реакций все еще недостаточно понятен. Для объяснения механизма реакции были предположены: образование металлокарбениевых ионов, комплексов металлокарбена и окислительное присоединение металла к напряженной ординарной углерод-углеродной связи [146].
ЛИТЕРАТУРА

Литература (продолжение)
Литература (продолжение)
Литература (продолжение)
Литература (продолжение)
Литература (продолжение)
Литература (окончание)
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- ПРЕДИСЛОВИЕ
- ИЗ ПРЕДИСЛОВИЯ К ТОМУ 1 АНГЛИЙСКОГО ИЗДАНИЯ
- ЧАСТЬ I. НОМЕНКЛАТУРА И СТЕРЕОХИМИЯ
- 1.1. ВВЕДЕНИЕ И СТЕРЕОХИМИЯ
- 1.1.2. СИММЕТРИЯ И ХИРАЛЬНОСТЬ
- 1.1.3. ХИМИЧЕСКАЯ ТОПОЛОГИЯ
- 1.1.4. ИЗОМЕРИЯ
- 1.1.4.2. Строение
- 1.1.4.3. Абсолютная конфигурация
- 1.1.4.4. Относительная конфигурация
- 1.1.4.5. Конформация
- 1.1.4.6. Концепция изомерии
- 1.1.5. ТОПИЗМ
- 1.1.5.2. Прохиральность
- 1.1.5.3. Псевдоасимметрия (псевдохиральность)
- 1.1.6. ТОПОМЕРИЯ
- 1.1.7. ДИНАМИЧЕСКАЯ СТЕРЕОХИМИЯ. КРАТКИЕ СВЕДЕНИЯ
- ЧАСТЬ 2. УГЛЕВОДОРОДЫ
- 2.1. НАСЫЩЕННЫЕ УГЛЕВОДОРОДЫ
- 2.1.2. Строение и номенклатура
- 2.1.2.1. Номенклатура IUPAC
- 2.1.2.2. Алициклические алканы
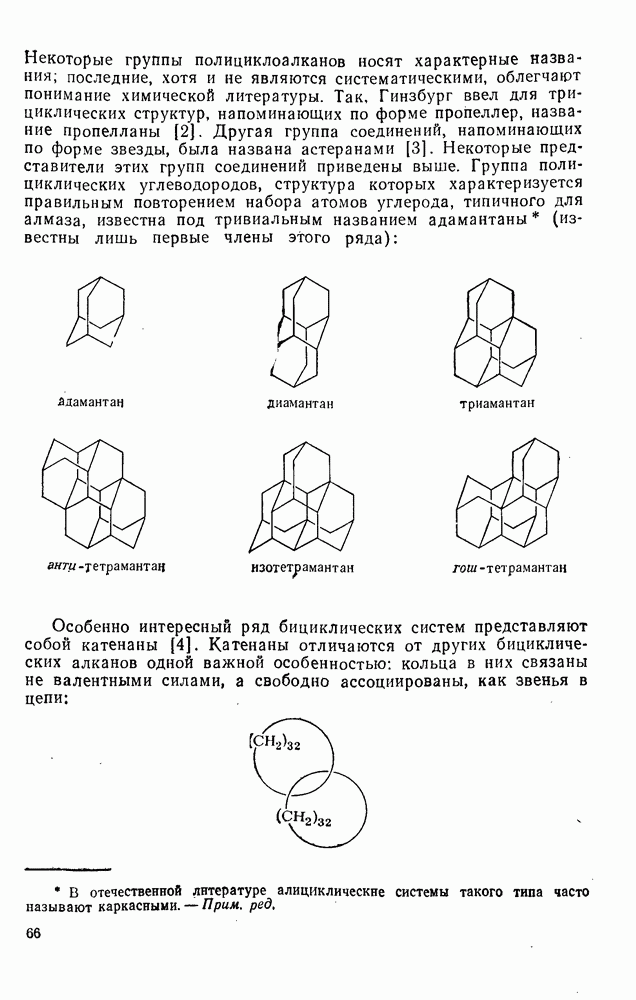
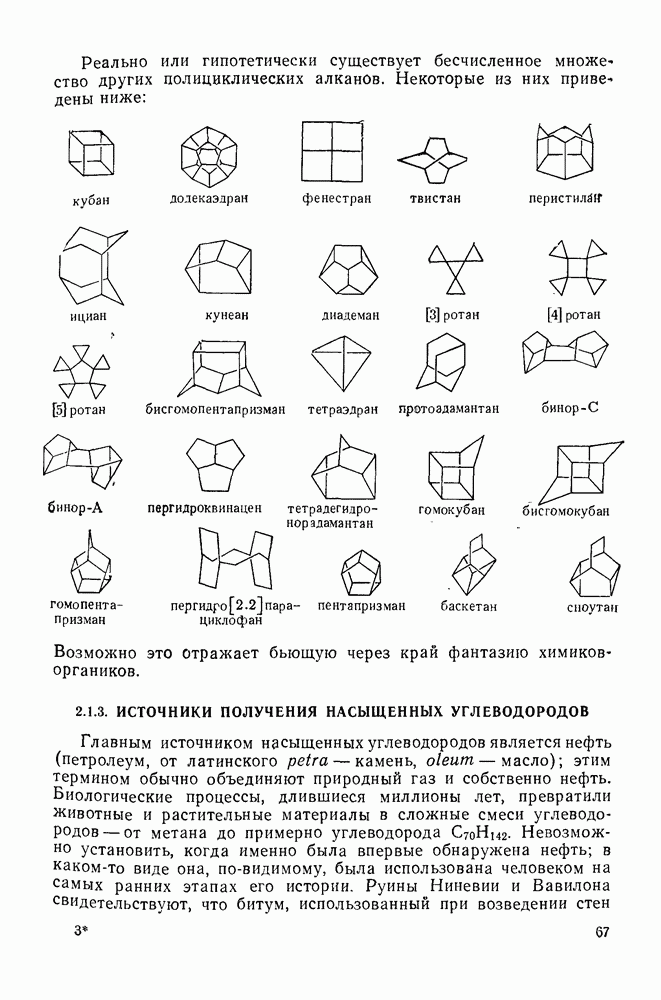
- 2.1.2.3. Полициклоалканы
- 2.1.3. ИСТОЧНИКИ ПОЛУЧЕНИЯ НАСЫЩЕННЫХ УГЛЕВОДОРОДОВ
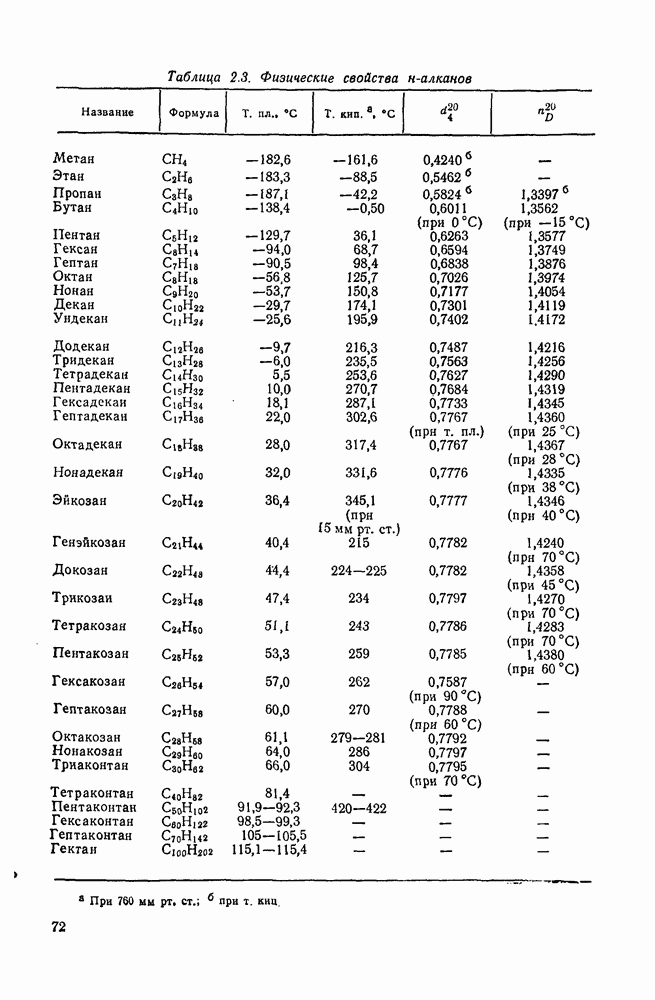
- 2.1.4. ФИЗИЧЕСКИЕ СВОЙСТВА
- 2.1.4.1. Ациклические алканы
- 2.1.4.2. Моно- и полициклоалканы
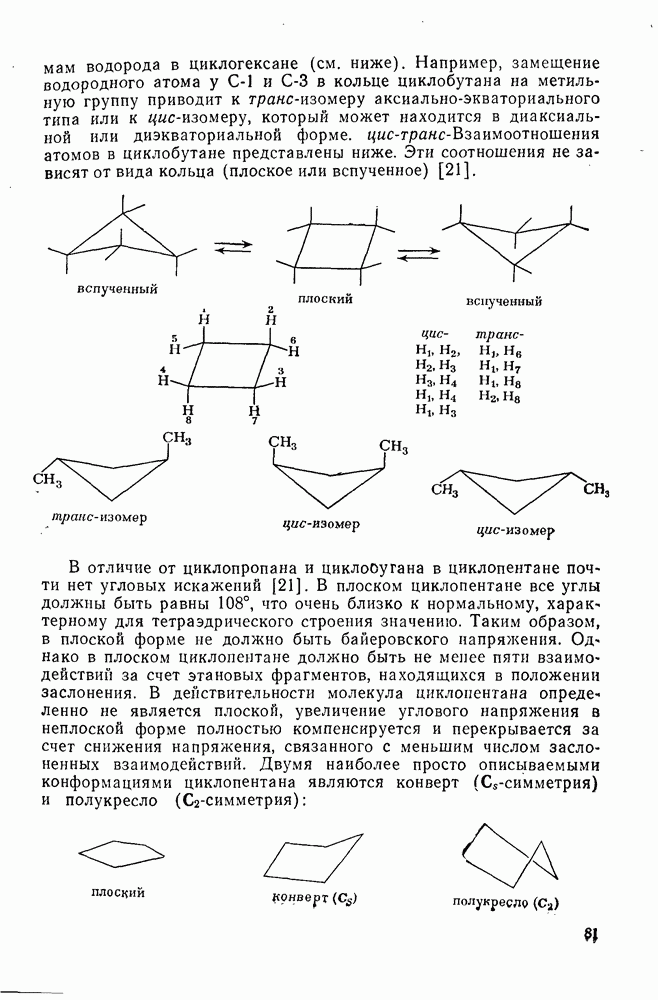
- 2.1.5. СТЕРЕОХИМИЯ И КОНФОРМАЦИОННЫЙ АНАЛИЗ
- 2.1.5.1. Углы и длины связей
- 2.1.5.2. Алкил- и полиалкилциклогексаны
- 2.1.5.3. Конформация карбоциклических колец, больших, чем циклогексан
- 2.1.6. ТЕРМОХИМИЧЕСКИЕ СВОЙСТВА
- 2.1.6.1. Горение. Алканы и циклоалканы как топливо
- 2.1.6.2. Определение теплот сгорания и термохимические свойства
- 2.1.6.3. Эмпирические методы оценки теплот образования алканов
- 2.1.6.4. Оценка теплот образования алканов на основе энергии связей
- 2.1.6.5. Оценка теплот образования алканов на основе инкрементов групп
- 2.1.6.6. Оценка теплот образования циклических, полициклических и мостиковых алканов на основе инкрементов «скошенных разобщенных» групп и «единственных» наиболее устойчивых конформаций
- 2.1.6.7. Молекулярно-механические расчеты теплот образования и энергии напряжения
- 2.1.6.8. Моно- и полициклоалкаиы
- 2.1.7. ПОЛУЧЕНИЕ АЦИКЛИЧЕСКИХ АЛКАНОВ
- 2.1.7.1. Получение алканов восстановлением олефинов
- 2.1.7.2. Получение алканов из альдегидов и кетонов
- 2.1.7.3. Получение алканов из спиртов и алкилгалогенидов
- 2.1.7.4. Получение алканов из карбоновых кислот
- 2.1.8. СИНТЕЗ МОНО- И ПОЛИЦИКЛОАЛКАНОВ
- 2.1.9. РЕАКЦИИ АЦИКЛИЧЕСКИХ АЛКАНОВ
- 2.1.9.1. Галогенирование
- 2.1.9.2. Нитрование
- 2.1.9.3. Окисление
- 2.1.9.4. Каталитическая изомеризация алканов
- 2.1.9.5. Каталитическое алкилирование алканов
- 2.1.9.6. Реакции крекинга алканов
- 2.1.9.7. Термический крекинг
- 2.1.9.8. Каталитический крекинг
- 2.1.9.9. Каталитический риформинг и дегидроциклизация алканов
- 2.1.10. РЕАКЦИИ ЦИКЛОАЛКАНОВ И ПОЛИЦИКЛОАЛКАНОВ
- 2.2. ОЛЕФИНОВЫЕ И АЦЕТИЛЕНОВЫЕ УГЛЕВОДОРОДЫ
- 2.2.2. ПОЛУЧЕНИЕ ОЛЕФИНОВ
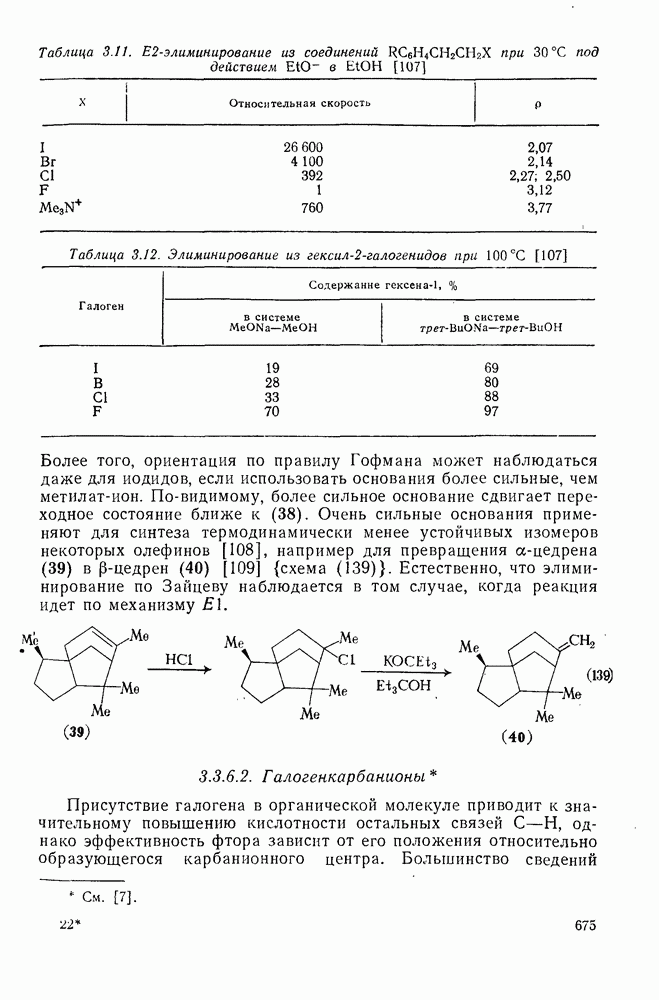
- 2.2.2.1. Элиминирование в системах
- 2.2.2.2. Элиминирование из систем
- 2.2.2.3. Циклоэлиминирование
- 2.2.2.4. Частичное восстановление
- 2.2.2.5. Элиминирование сульфонилгидразонов
- 2.2.2.6. Реакция Виттига и родственные ей реакции
- 2.2.2.7. Различные реакции конденсации
- 2.2.2.8. Электроциклические реакции
- 2.2.2.9. Циклоолигомеризация
- 2.2.2.11. Реакции винильных производных
- 2.2.3. РЕАКЦИИ ОЛЕФИНОВ
- 2.2.3.1. Электрофильное присоединение
- 2.2.3.2. Нуклеофильное присоединение
- 2.2.3.3. Радикальное присоединение
- 2.2.3.4. Циклоприсоединение и родственные реакции
- 2.2.3.5. Окисление
- 2.2.3.6. Восстановление
- 2.2.3.7. Перегруппировки
- 2.2.3.8. Фотохимические реакции
- 2.2.3.9. Прочие реакции
- 2.3. ДИЕНЫ, ПОЛНЕНЫ И АЦЕТИЛЕНОВЫЕ УГЛЕВОДОРОДЫ
- 2.3.1. СОПРЯЖЕННЫЕ ДИЕНЫ И ПОЛНЕНЫ
- 2.3.1.2. Получение сопряженных диенов
- 2.3.2. РЕАКЦИИ СОПРЯЖЕННЫХ ДИЕНОВ
- 2.3.2.2. Восстановление
- 2.3.2.3. Гидроборирование
- 2.3.2.4. Реакция Дильса — Альдера
- 2.3.2.5. Комплексы с карбонилами железа
- 2.3.2.6. Фотохимические термические реакции
- 2.3.2.7. Прочие реакции
- 2.3.3. СОПРЯЖЕННЫЕ ПОЛИЕНЫ
- 2.3.4. ПРИРОДНЫЕ ДИЕНЫ И ПОЛНЕНЫ
- 2.3.5. АЛЛЕНЫ И КУМУЛЕНЫ
- 2.3.5.2. Получение алленов
- 2.3.6. РЕАКЦИИ АЛЛЕНОВ
- 2.3.6.2. Гидрирование
- 2.3.6.3. Реакции алленов в присутствии комплексов металлов
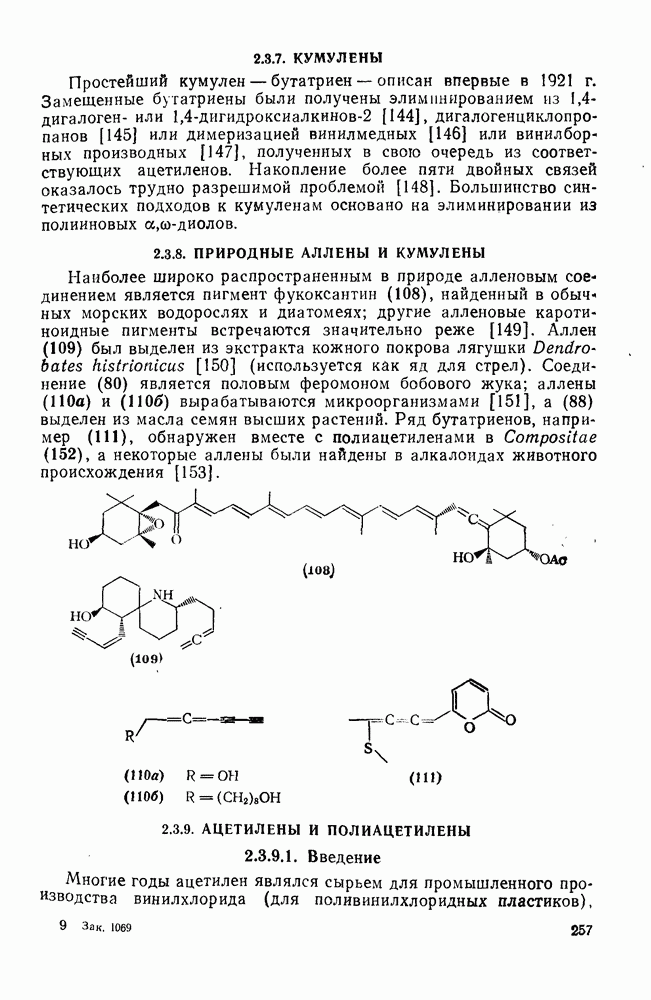
- 2.3.7. КУМУЛЕНЫ
- 2.3.8. ПРИРОДНЫЕ АЛЛЕНЫ И КУМУЛЕНЫ
- 2.3.9. АЦЕТИЛЕНЫ И ПОЛИАЦЕТИЛЕНЫ
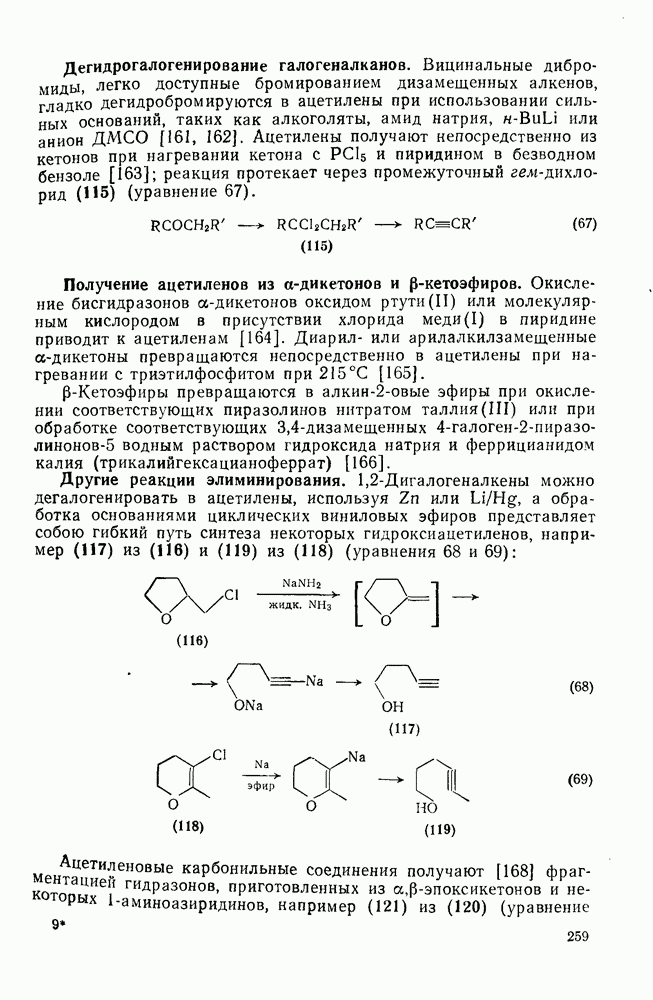
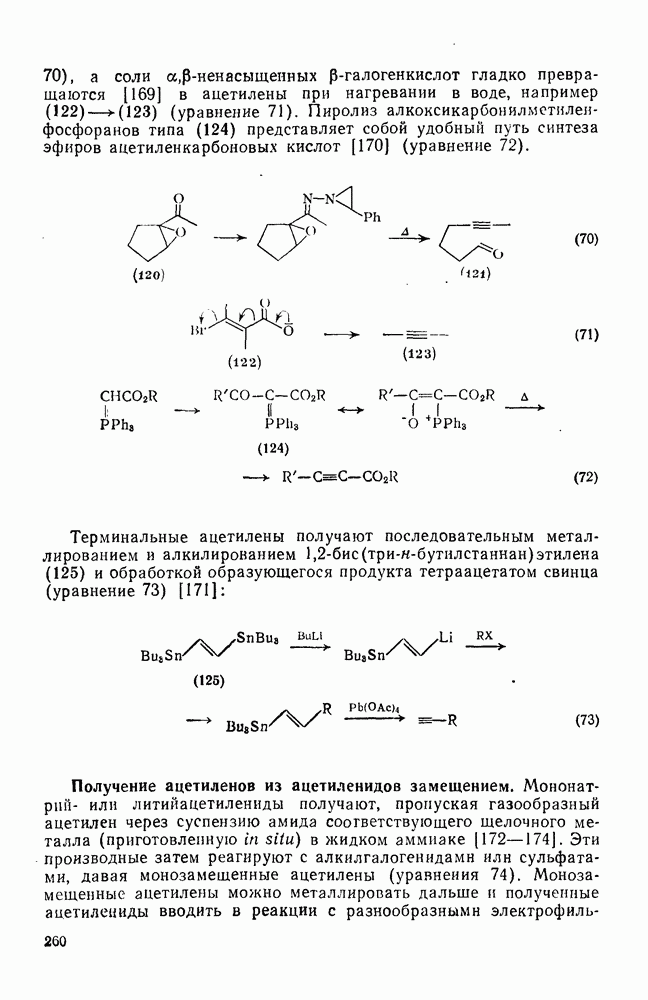
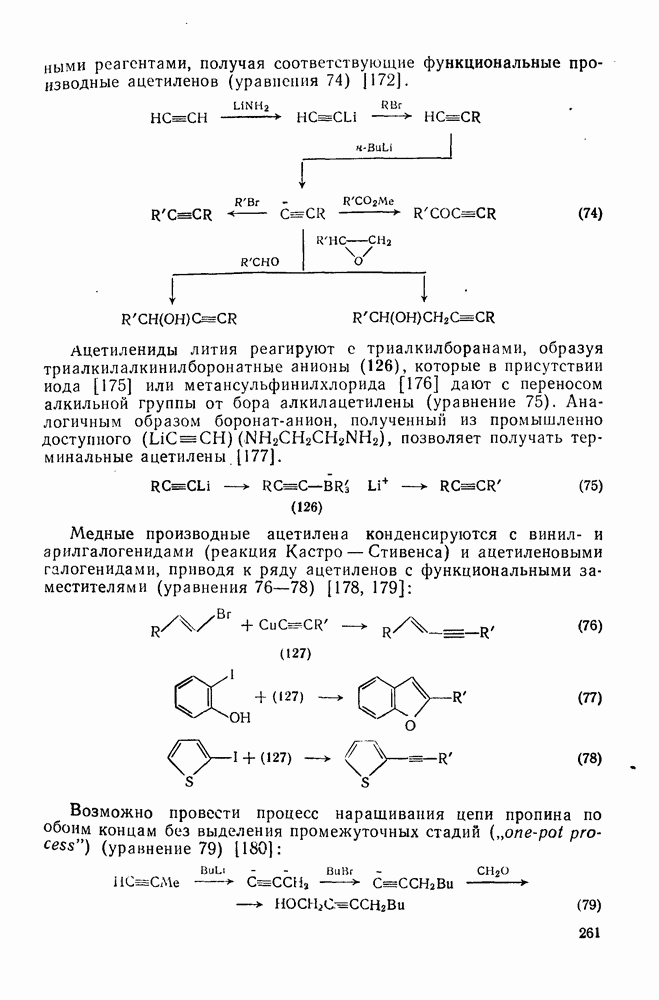
- 2.3.9.2. Получение ацетиленов
- 2.3.10. РЕАКЦИИ АЦЕТИЛЕНОВ
- 2.3.10.2. Изомеризация
- 2.3.10.3. Пропаргильные перегруппировки
- 2.3.10.4. Реакции присоединения
- 2.3.10.5. Гидроборирование и гидроалюминирование
- 2.3.10.6. Реакции замещения
- 2.3.10.7. Восстановление
- 2.3.10.8. Окисление
- 2.3.10.9. Циклоприсоединение
- 2.3.10.10. Реакции катализуемые металлами
- 2.3.11. ПОЛИАЦЕТИЛЕНЫ
- 2.3.12. ПРИРОДНЫЕ АЦЕТИЛЕНЫ И ПОЛИАЦЕТИЛЕНЫ
- 2.3.13. СОПРЯЖЕННЫЕ ЕНИНЫ
- 2.3.13.1. Получение сопряженных енинов
- 2.3.14. РЕАКЦИИ СОПРЯЖЕННЫХ ЕНИНОВ
- 2.3.15. ПРИРОДНЫЕ СОПРЯЖЕННЫЕ ЕНИНЫ
- 2.4. АРОМАТИЧНОСТЬ
- 2.4.2. ЭЛЕКТРОННЫЕ ТЕОРИИ СТРОЕНИЯ БЕНЗОЛА
- 2.4.3. КРИТЕРИИ АРОМАТИЧНОСТИ
- 2.4.3.1. Термодинамические свойства
- 2.4.3.2. Структурные особенности
- 2.4.3.3. Магнитные свойства
- 2.4.3.4. Прочие критерии
- 2.4.4. АНТИАРОМАТИЧНОСТЬ
- 2.4.4.1. Термодинамические свойства
- 2.4.4.2. Структурные особенности
- 2.4.4.3. Магнитные свойства
- 2.4.4.4. Прочие свойства
- 2.4.5. ТЕОРЕТИЧЕСКИЕ ОПРЕДЕЛЕНИЯ АРОМАТИЧНОСТИ
- 2.4.5.1. Полуэмпирические расчеты и дьюаровская резонансная энергия
- 2.4.5.2. Расчеты по методу валентных пар и применение резонансного метода
- 2.4.5.3. Локализация связей
- 2.4.5.4. Связь энергетических критериев с критериями локализации связей
- 2.4.6. АРОМАТИЧЕСКИЕ ПЕРЕХОДНЫЕ СОСТОЯНИЯ
- 2.5. АРЕНЫ И ИХ РЕАКЦИИ
- 2.5.2. НОМЕНКЛАТУРА
- 2.5.3. ФИЗИЧЕСКИЕ СВОЙСТВА АРЕНОВ
- 2.5.4. ПРОМЫШЛЕННОЕ ПРОИЗВОДСТВО АРЕНОВ
- 2.5.5. ЦИКЛОТРИМЕРИЗАЦИЯ АЦЕТИЛЕНОВ
- 2.5.6. РЕАКЦИИ ЭЛЕКТРОФИЛЬНОГО ПРИСОЕДИНЕНИЯ — ЭЛИМИНИРОВАНИЯ АРЕНОВ
- 2.5.6.1. Механизм ароматического нитрования [15]
- 2.5.6.2. Кинетические изотопные эффекты [21]
- 2.5.6.3. Реакции, включающие ипсо-протонирование
- 2.5.6.4. Металлирование
- 2.5.6.5. Электрофилы IV группы
- 2.5.6.6. Электрофилы V группы
- 2.5.6.7. Электрофилы VI группы [18, 56]
- 2.5.6.8. Электрофилы VII группы [18, 25а, 56]
- 2.5.7. ОРИЕНТАЦИЯ В РЕАКЦИЯХ ЭЛЕКТРОФИЛЬНОГО ПРИСОЕДИНЕНИЯ — ЭЛИМИНИРОВАНИЯ
- 2.5.8. РАДИКАЛЬНОЕ ГАЛОГЕНИРОВАНИЕ АРЕНОВ В БОКОВУЮ ЦЕПЬ [96]
- 2.5.9. РЕАКЦИИ ПРИСОЕДИНЕНИЯ К АРЕНАМ
- 2.5.9.1. Восстановление аренов
- 2.5.9.2. Термическое циклоприсоединение к аренам
- 2.5.9.3. Фотоциклоприсоединение к моноциклическим аренам [126]
- 2.5.9.4. Фотохимические реакции полициклических аренов
- 2.6.10. ФОТОИЗОМЕРИЗАЦИЯ АРЕНОВ [126б]
- 2.5.11. ОКИСЛЕНИЕ АРЕНОВ [153]
- 2.5.12. РЕАКЦИИ АРЕНОВ С СИНГЛЕТНЫМ КИСЛОРОДОМ [162]
- 2.5.13. ПРИГОТОВЛЕНИЕ БИ- И ПОЛИАРИЛОВ
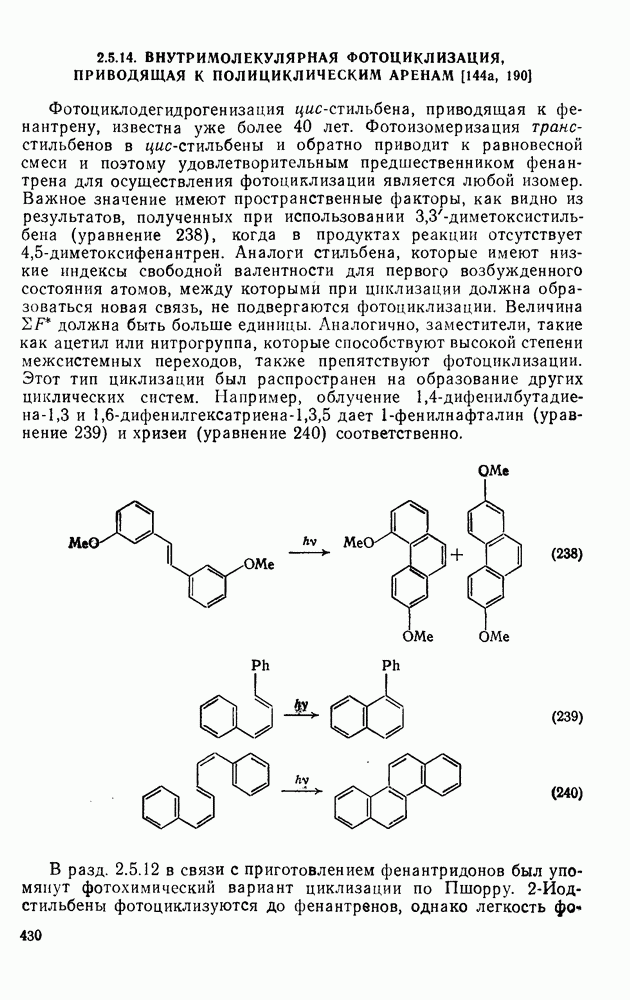
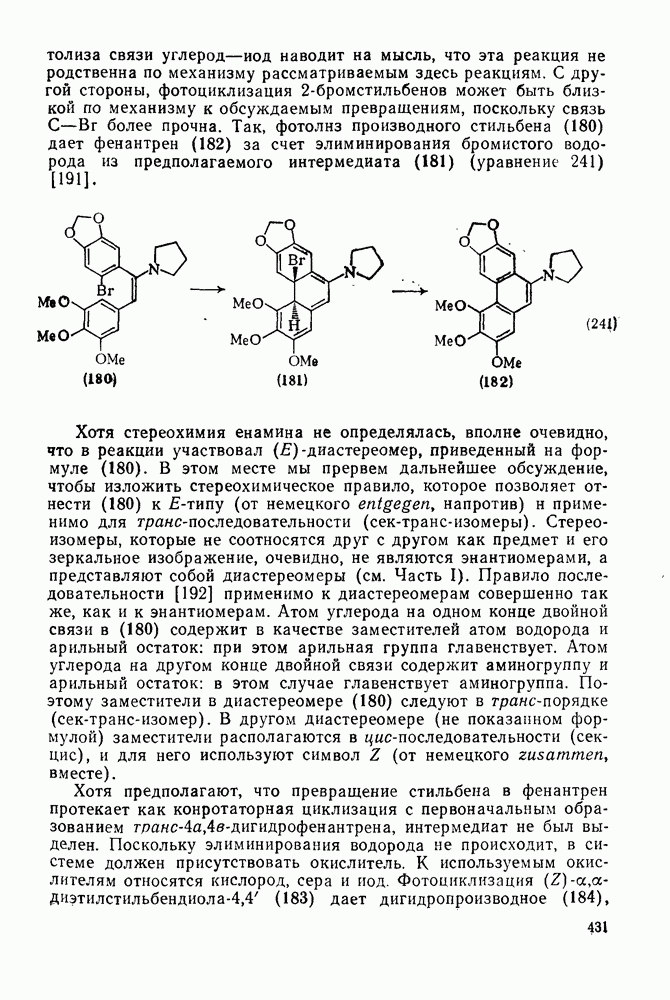
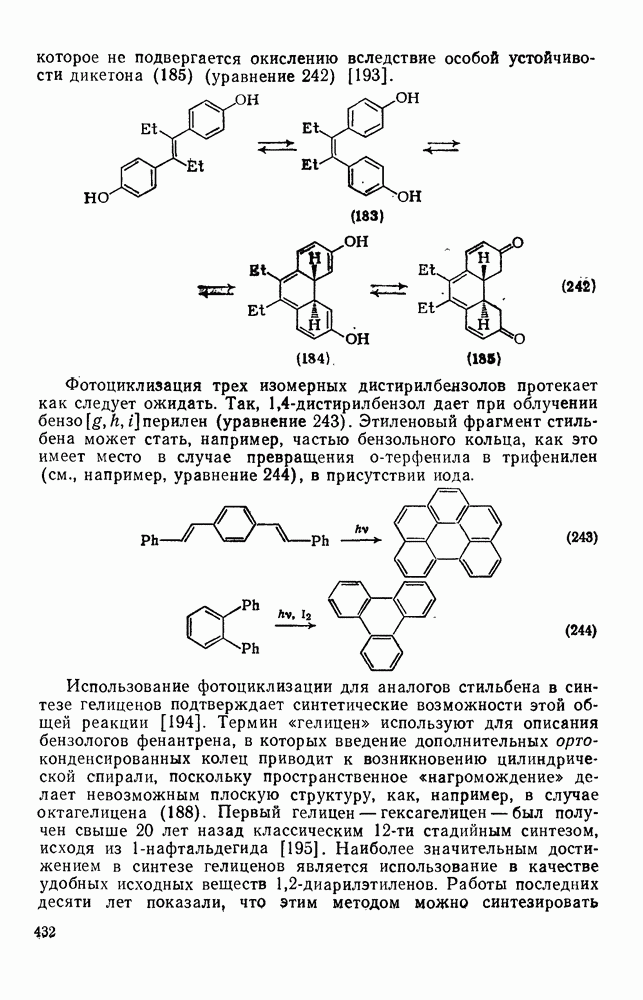
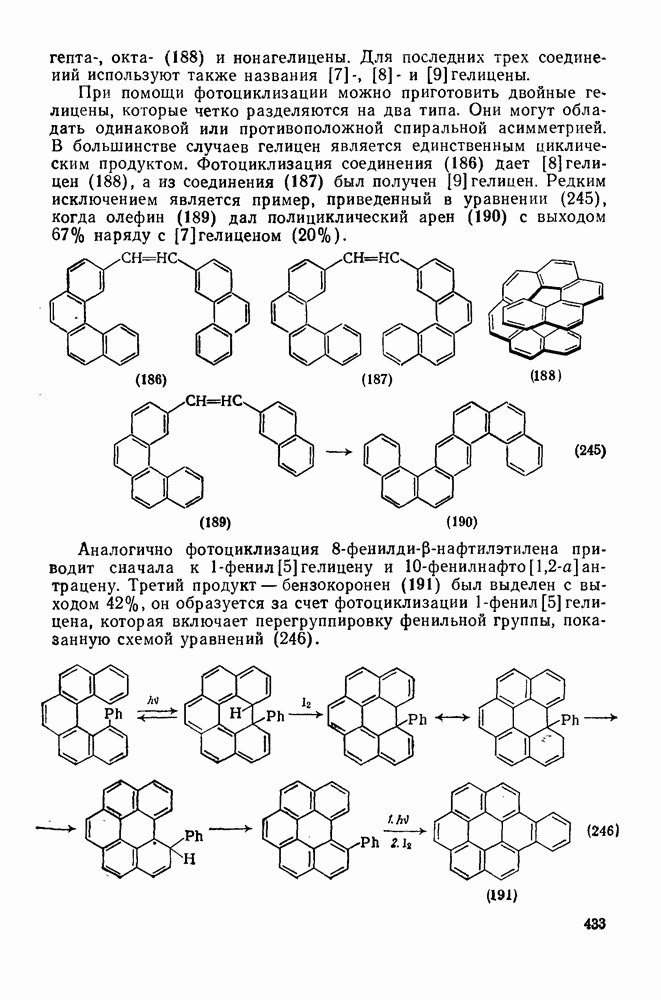
- 2.5.14. ВНУТРИМОЛЕКУЛЯРНАЯ ФОТОЦИКЛИЗАЦИЯ, ПРИВОДЯЩАЯ К ПОЛИЦИКЛИЧЕСКИМ АРЕНАМ
- 2.5.15. ВНУТРИМОЛЕКУЛЯРНАЯ ЦИКЛИЗАЦИЯ ДИЗАМЕЩЕННЫХ АРЕНОВ
- 2.5.16. ЦИКЛОФАНЫ
- 2.5.17. КОНФОРМАЦИЯ И ХИРАЛЬНОСТЬ АРЕНОВ
- 2.5.18. АЗУЛЕНЫ И НЕБЕНЗОИДНЫЕ АРЕНЫ
- 2.6. АННУЛЕНЫ И РОДСТВЕННЫЕ СИСТЕМЫ
- 2.6.2. МЕТОДЫ СИНТЕЗА
- 2.6.2.1. Окислительное сочетание терминальных ацетиленов (метод Зондхеймера)
- 2.6.2.2. Фотооблучение полициклических валентных таутомеров
- 2.6.2.3. Валентная таутомерия типа норкарадиен — циклогептатриен (метод Фогеля)
- 2.6.2.4. Прочие методы
- 2.6.3. СВОЙСТВА АННУЛЕНОВ
- 2.6.4. СВОЙСТВА 4n-АННУЛЕНОВ
- 2.6.5. ДЕГИДРОАННУЛЕНЫ
- 2.6.6. АННЕЛИРОВАННЫЕ АННУЛЕНЫ
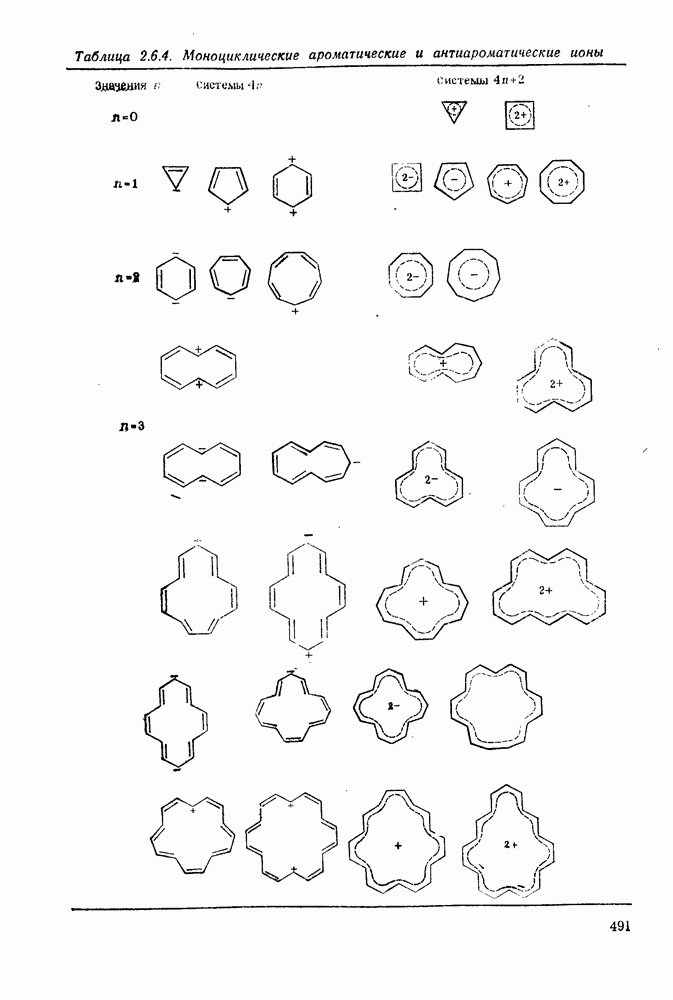
- 2.6.7. АРОМАТИЧЕСКИЕ И АНТИАРОМАТИЧЕСКИЕ МОНОЦИКЛИЧЕСКИЕ ИОНЫ
- 2.6.8. АРОМАТИЧЕСКИЕ И АНТИАРОМАТИЧЕСКИЕ ПОЛИЦИКЛИЧЕСКИЕ ИОНЫ
- 2.6.9. ГОМОАРОМАТИЧЕСКИЕ СИСТЕМЫ
- 2.7. КАРБОКАТИОНЫ И КАРБАНИОНЫ
- 2.7.1.2. Краткий исторический очерк развития химии карбокатионов
- 2.7.1.3. Методы генерации карбокатионов
- 2.7.1.4. Типы карбокатионов
- 2.7.1.5. Изучение карбокатионов: методы и результаты
- 2.7.1.6. Реакции карбокатионов
- 2.7.2. КАРБАНИОНЫ
- 2.7.2.2. Методы генерации карбанионов
- 2.7.2.3. Типы карбанионов
- 2.7.2.4. Физические свойства карбанионов
- 2.7.5.2. Реакции карбанионов
- 2.8. РАДИКАЛЫ, КАРБЕНЫ, АРИНЫ
- 2.8.1. РАДИКАЛЫ
- 2.8.1.1. Структура, устойчивость и реакционная способность радикалов
- 2.8.1.2. Методы генерации и реакции радикалов
- 2.8.2. КАРБЕНЫ
- 2.8.2.1. Методы генерации карбенов и карбеноидов
- 2.8.2.2. Реакции карбенов
- 2.8.3. АРИНЫ
- 2.8.3.1. Структура и спектры аринов
- 2.8.3.2. Методы генерации аринов
- 2.8.3.3. Реакции аринов
- ЧАСТЬ 3. ГАЛОГЕНСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
- 3.2. МЕТОДЫ ГАЛОГЕНИРОВАНИЯ
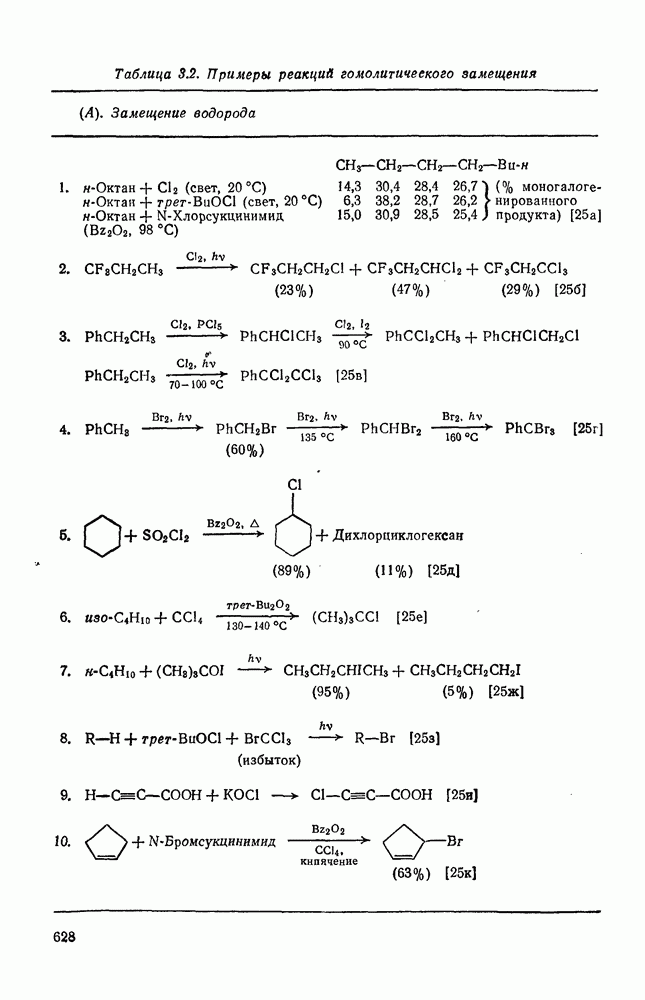
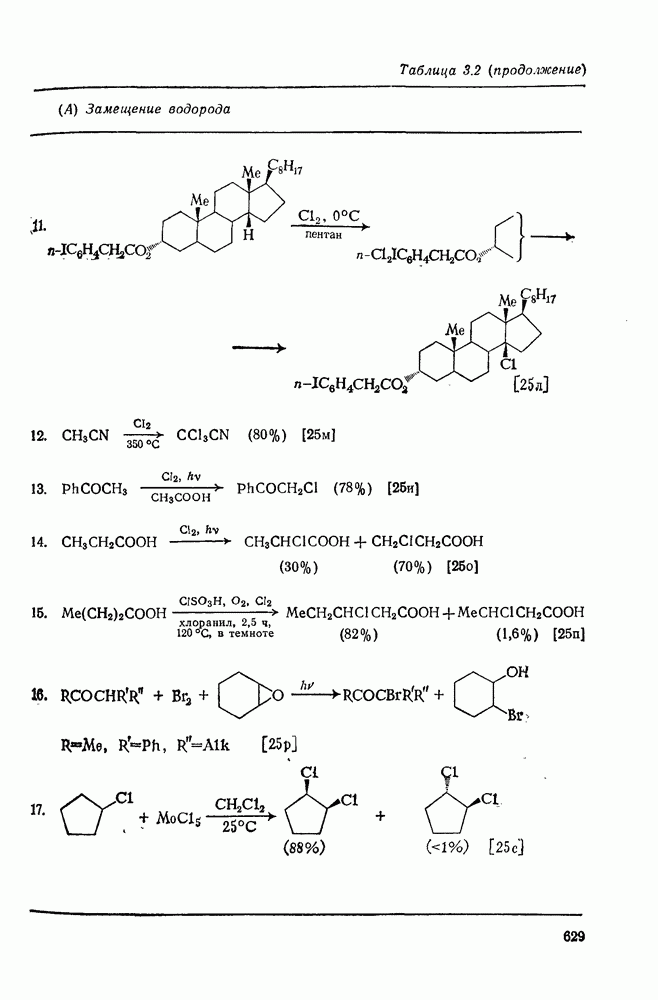
- 3.2.1. Гомолитическое замещение водорода
- 3.2.1.2. Использование галогенпроизводных в качестве реагентов
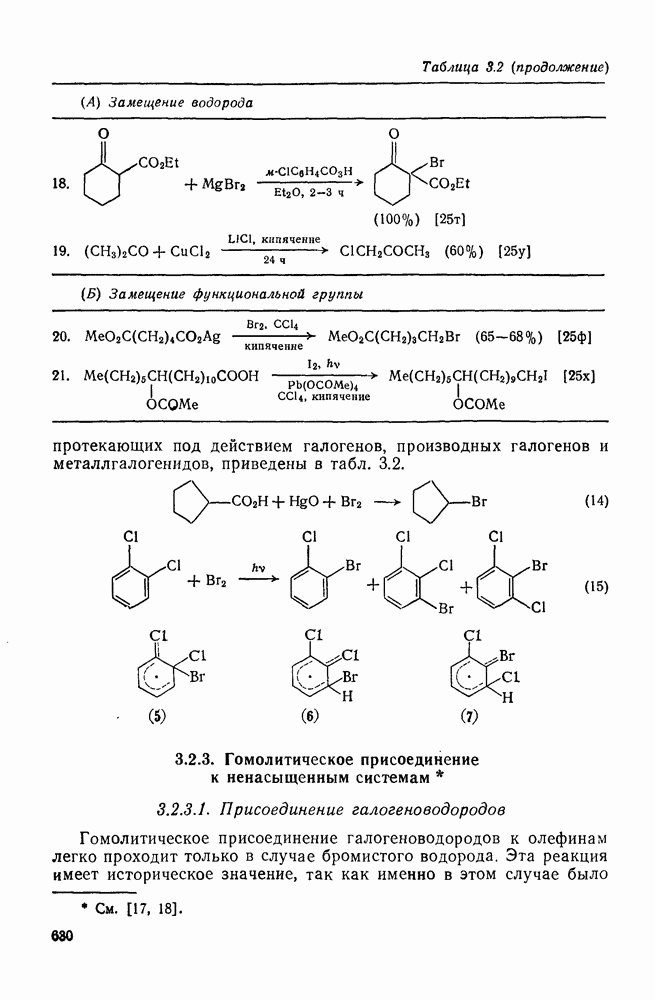
- 3.2.2. Гомолитическое замещение функциональных групп
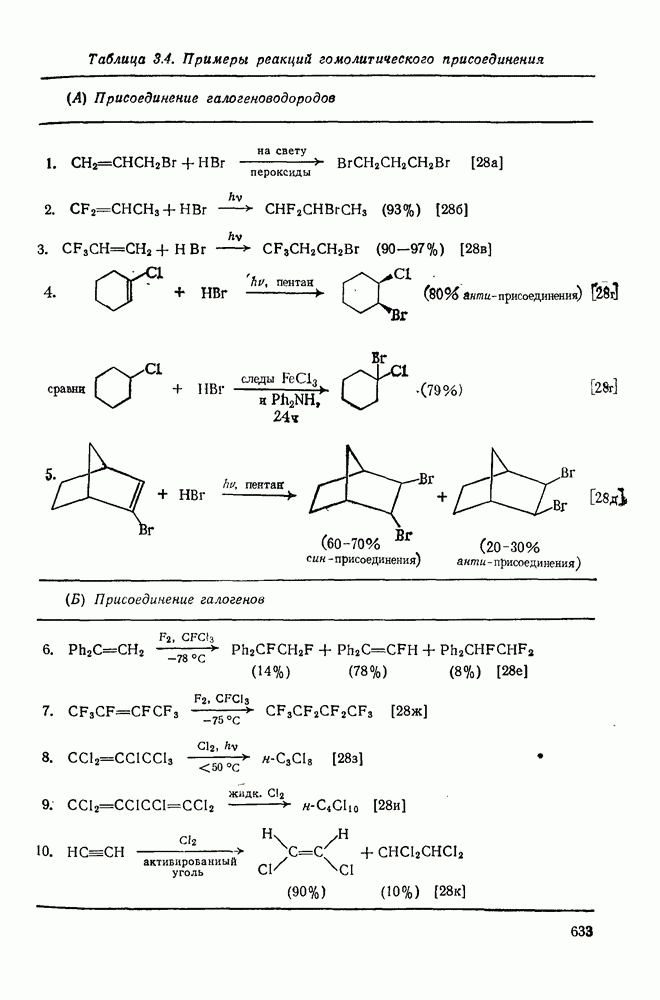
- 3.2.3. Гомолитическое присоединение к ненасыщенным системам
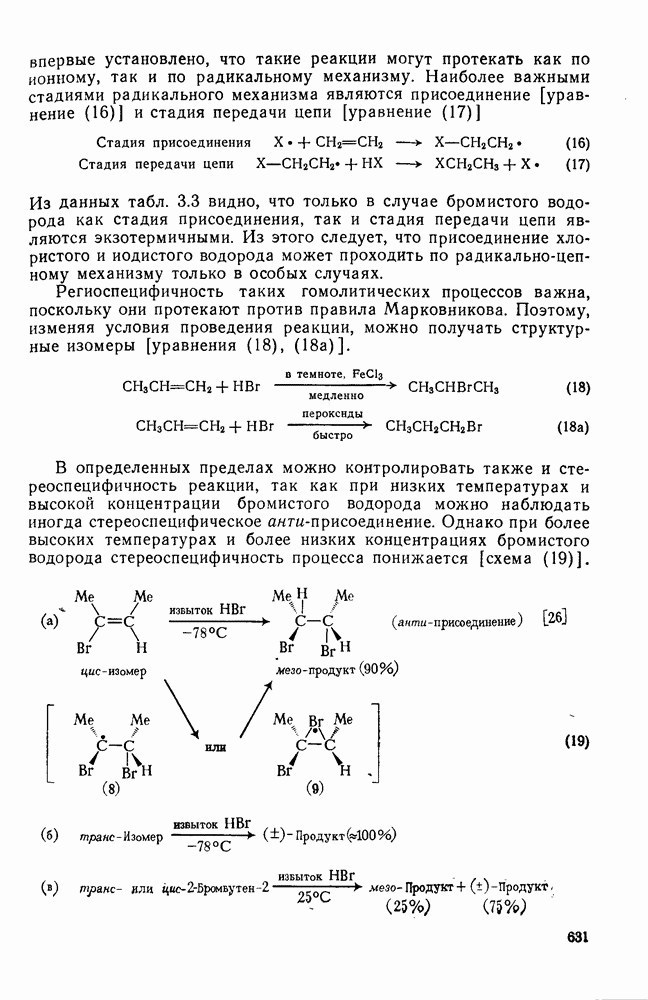
- 3.2.3.1. Присоединение галогеноводородов
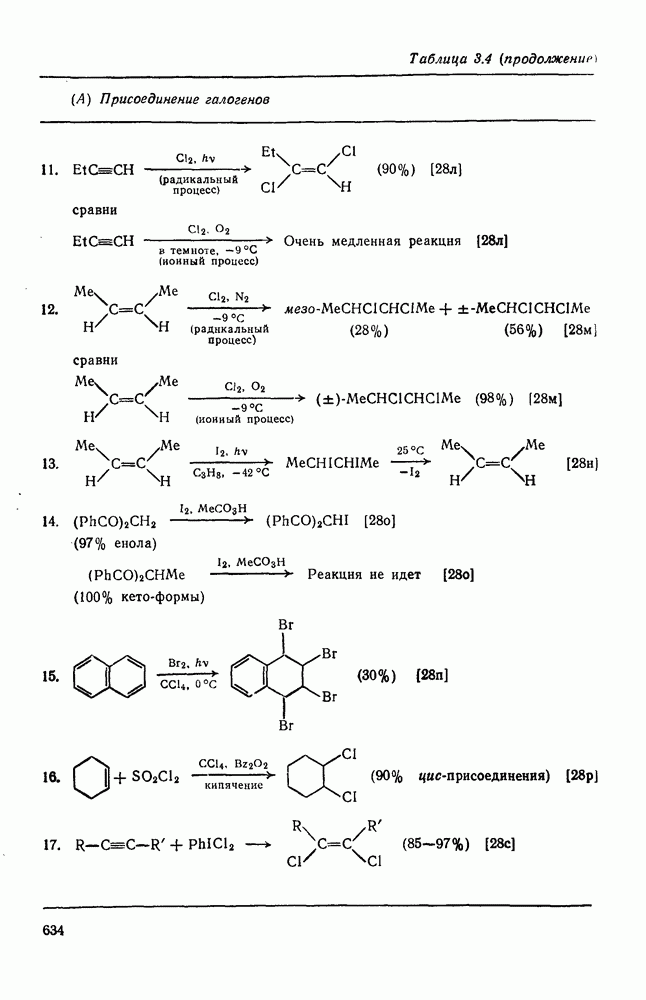
- 3.2.3.2. Присоединение галогенов
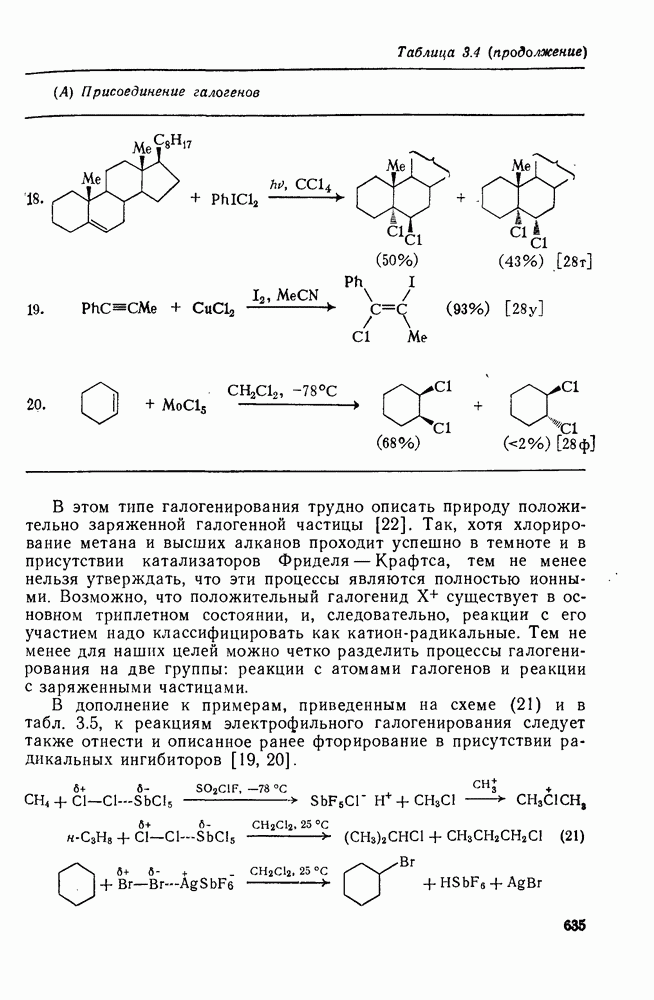
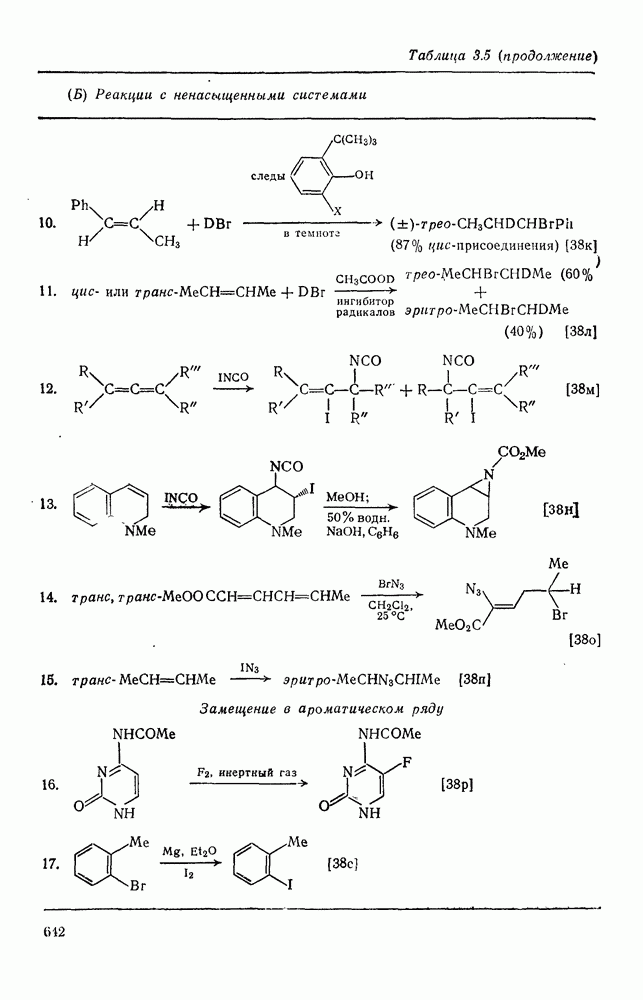
- 3.2.4. Электрофильное галогенирование
- 3.2.4.1. Замещение у насыщенной связи С-Н
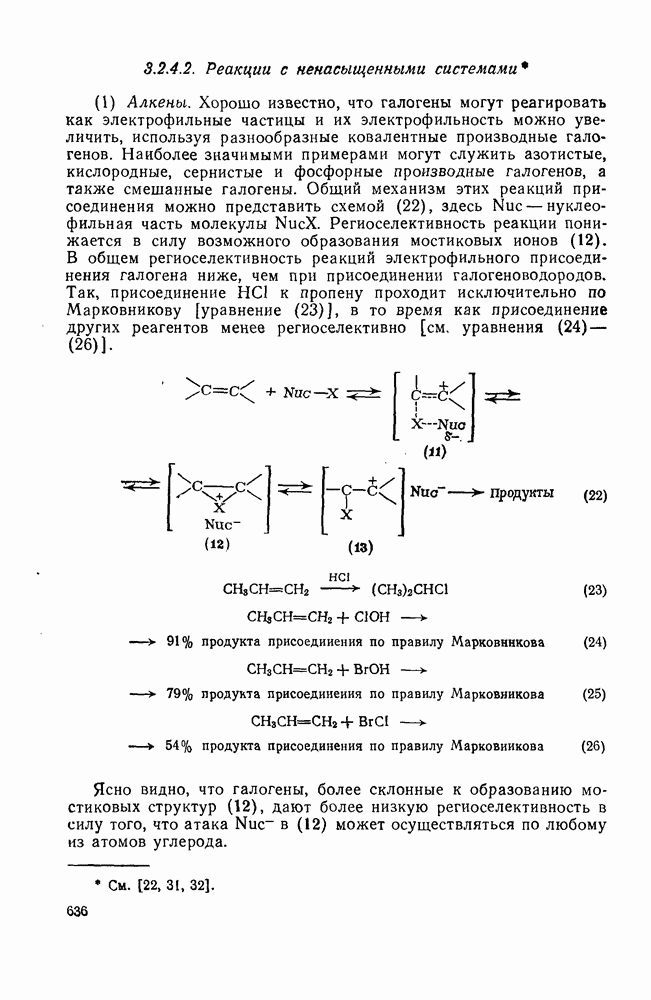
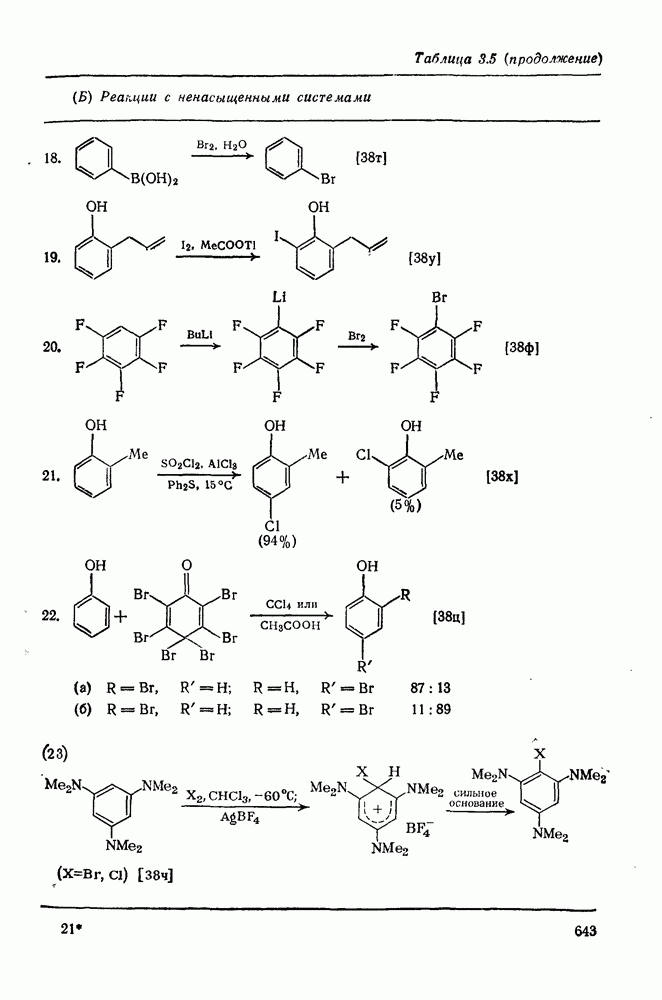
- 3.2.4.2. Реакции с ненасыщенными системами
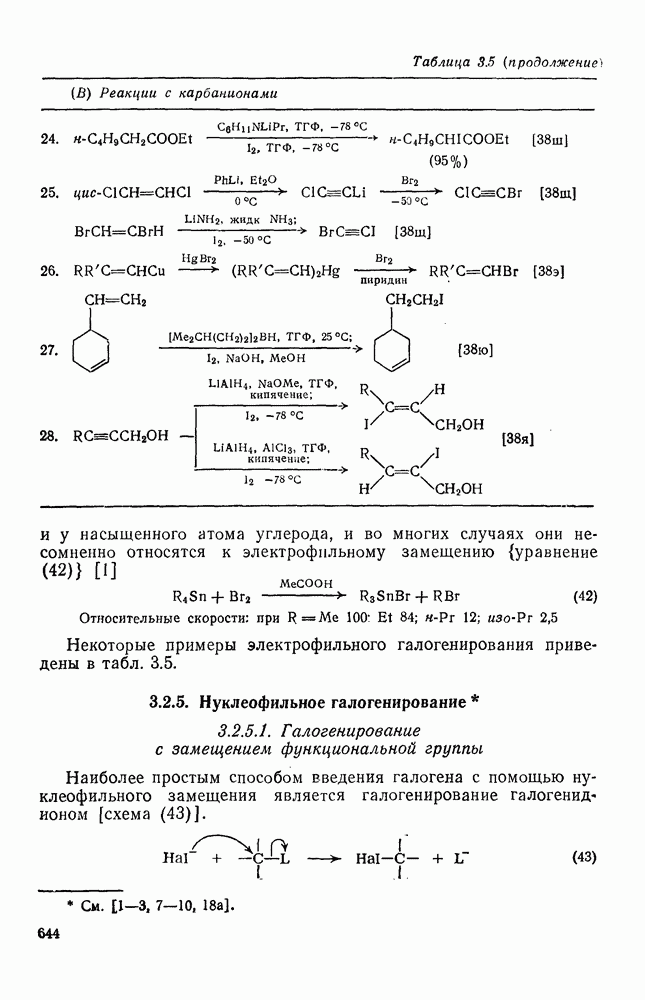
- 3.2.4.3. Реакции с карбанионами
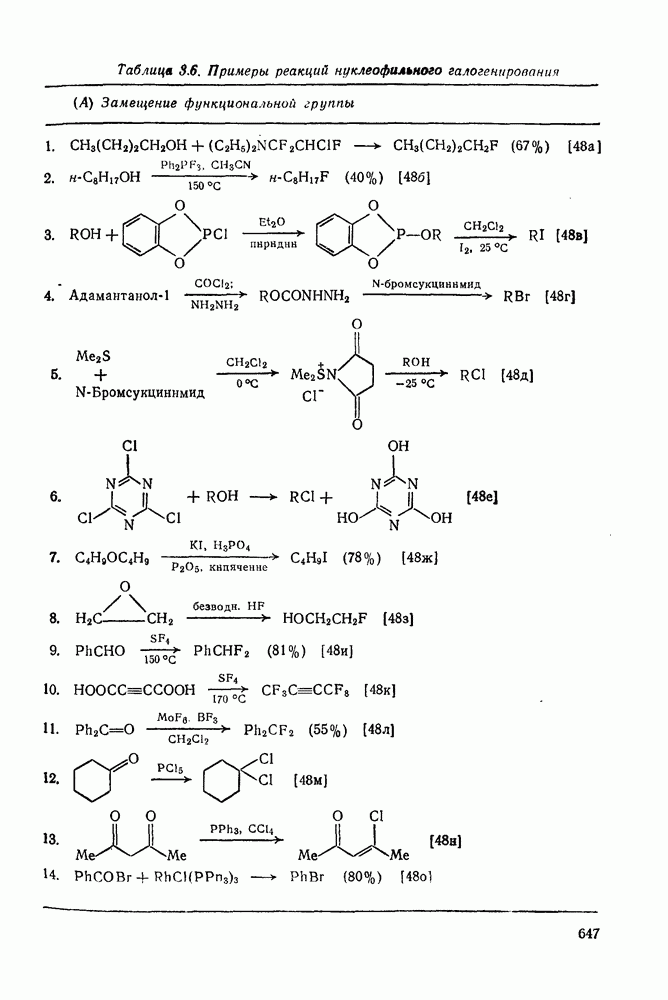
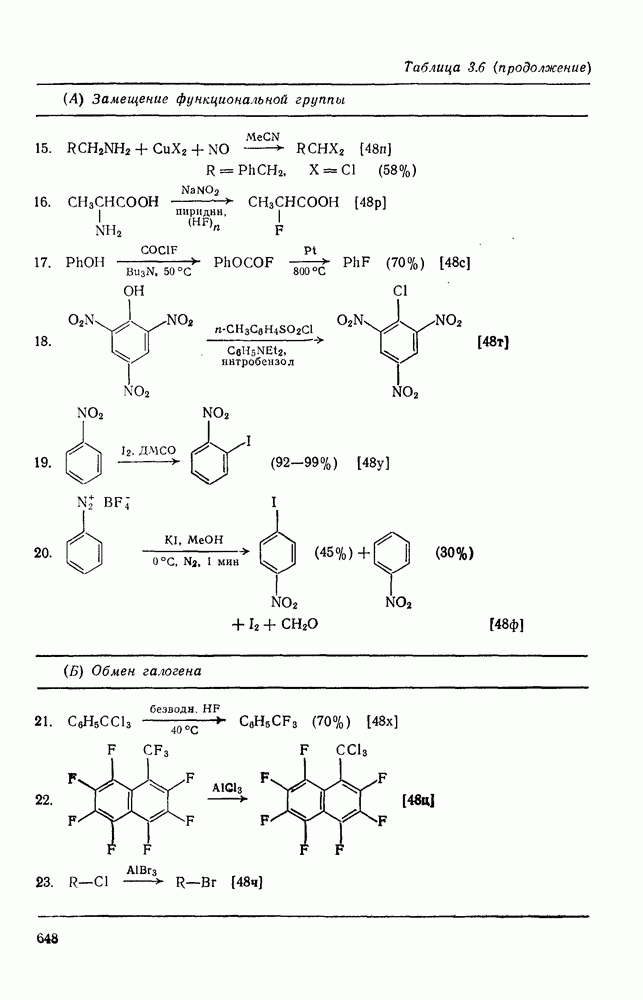
- 3.2.5. Нуклеофильное галогенирование
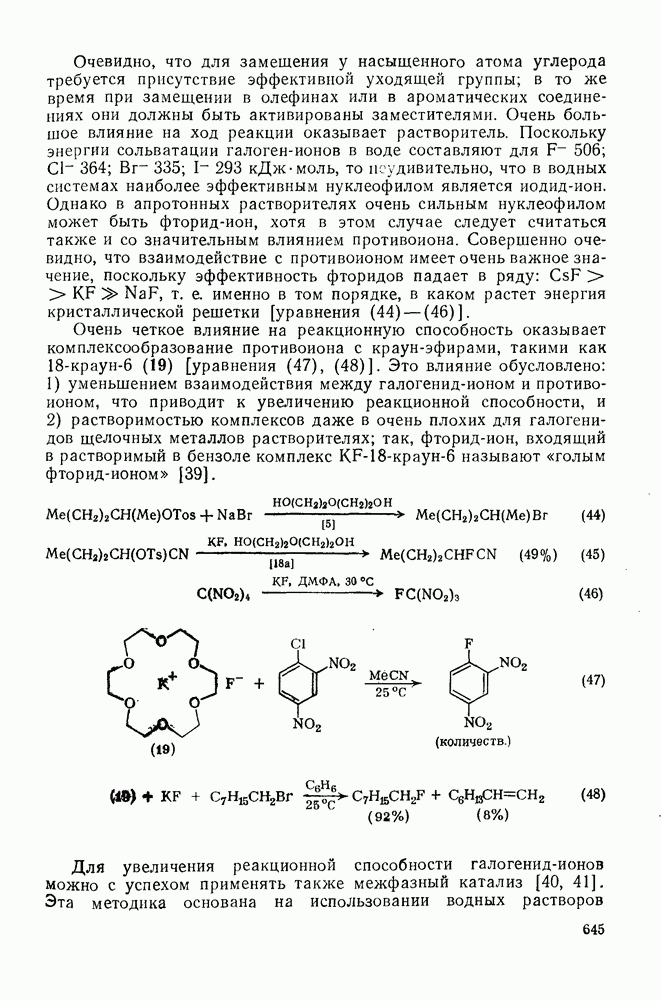
- 3.2.5.1. Галогенирование с замещением функциональной группы
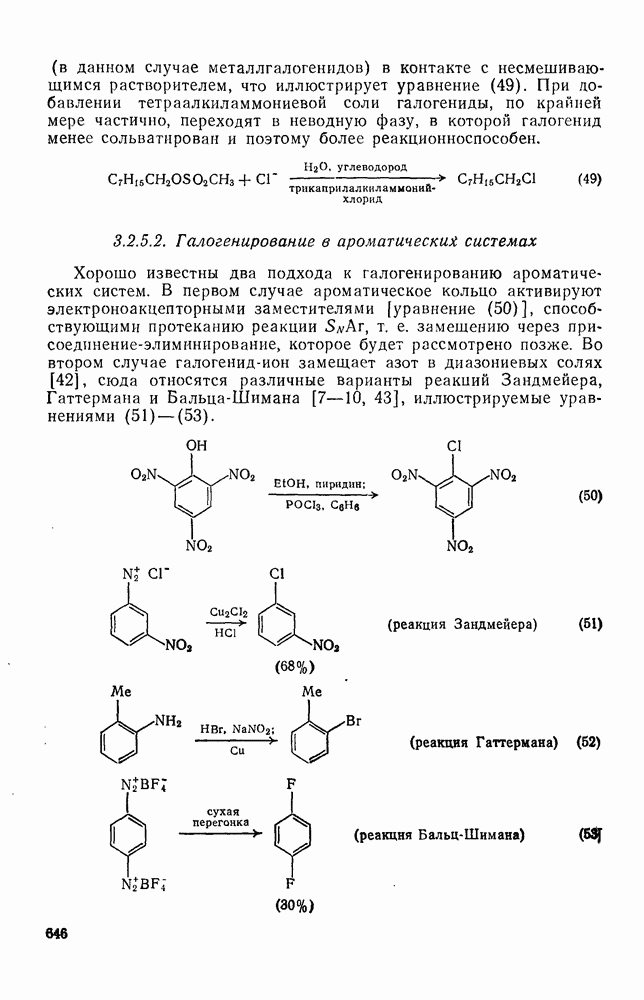
- 3.2.5.2. Галогенирование в ароматических системах
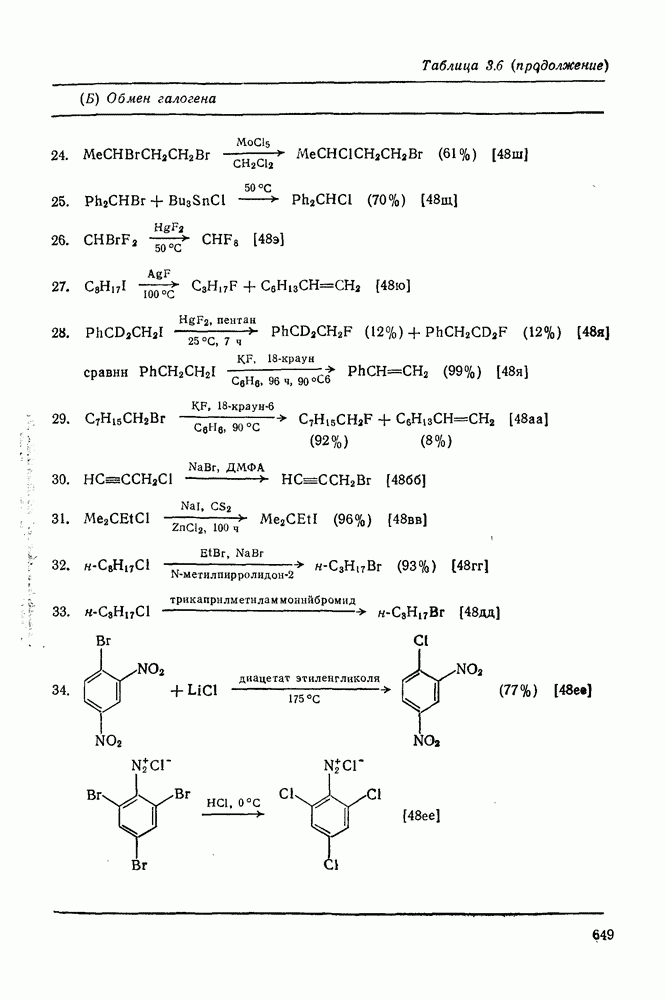
- 3.2.5.3. Галогенирование путем обмена галогенов
- 3.2.6. Синтез полигалогенированных соединений
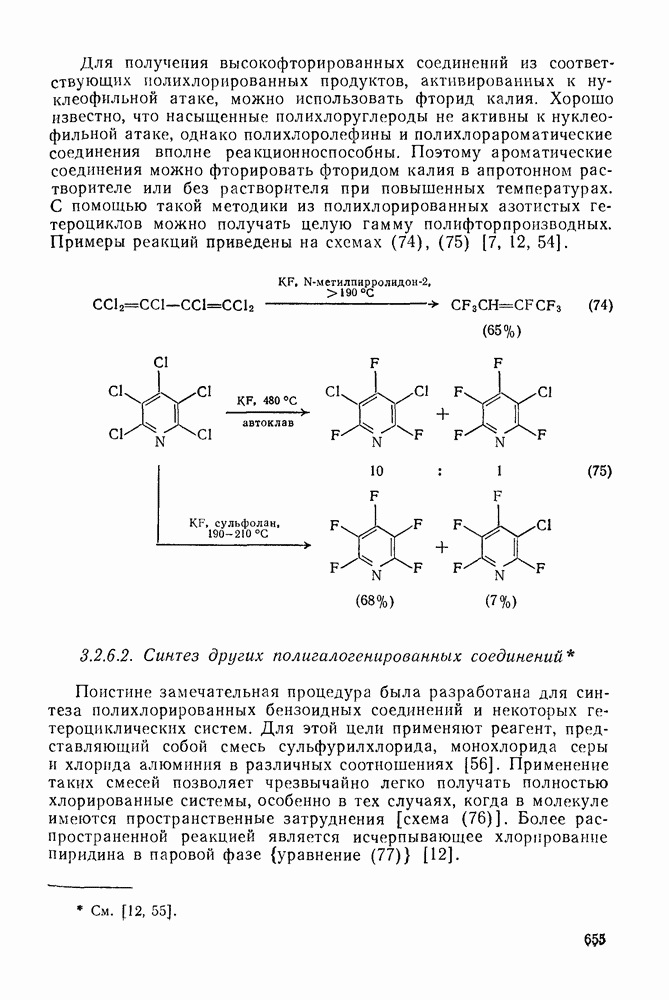
- 3.2.6.1. Синтез полифторированных соединений
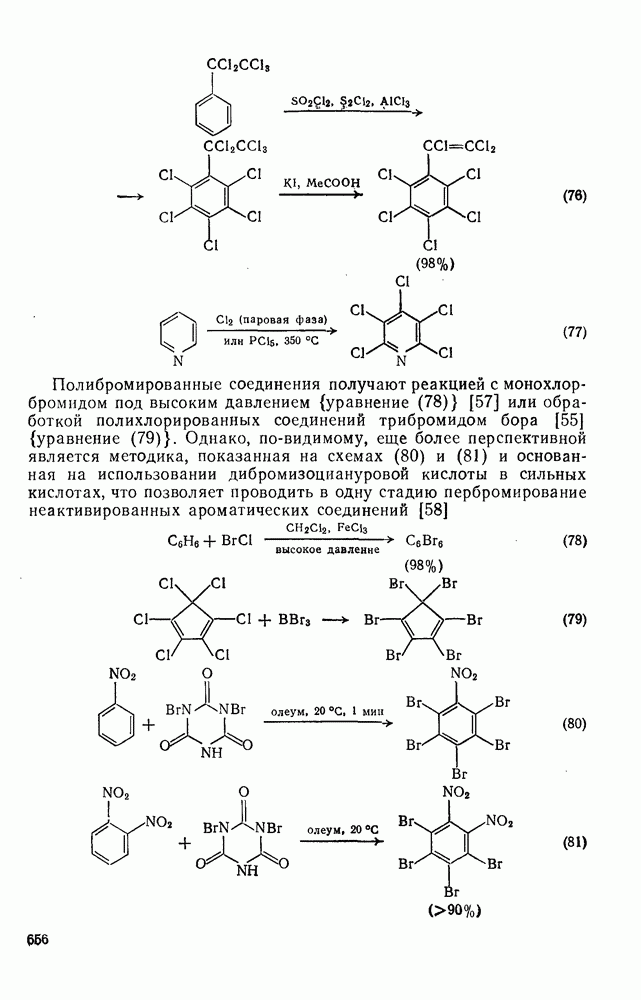
- 3.2.6.2. Синтез других полигалогенированных соединений
- 3.3. ГАЛОГЕНАЛКАНЫ
- 3.3.1. Характеристика связей углерод-галоген
- 3.3.2. Промышленное применение
- 3.3.3. Нуклеофильное замещение галогена
- 3.3.3.1. Реакции SN2 и родственные процессы
- 3.3.3.2. Соучастие соседних групп
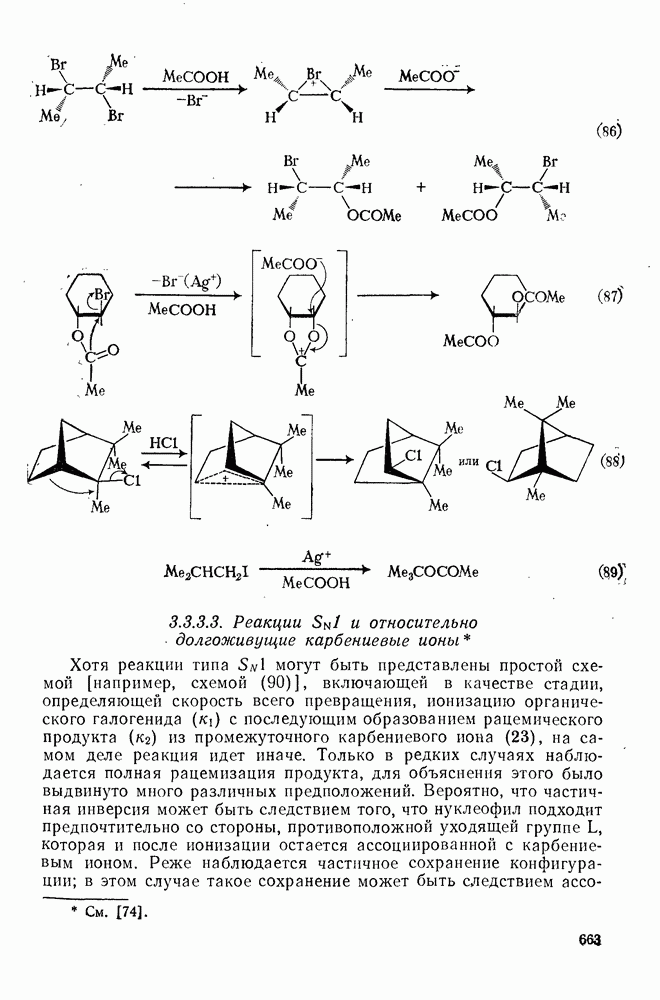
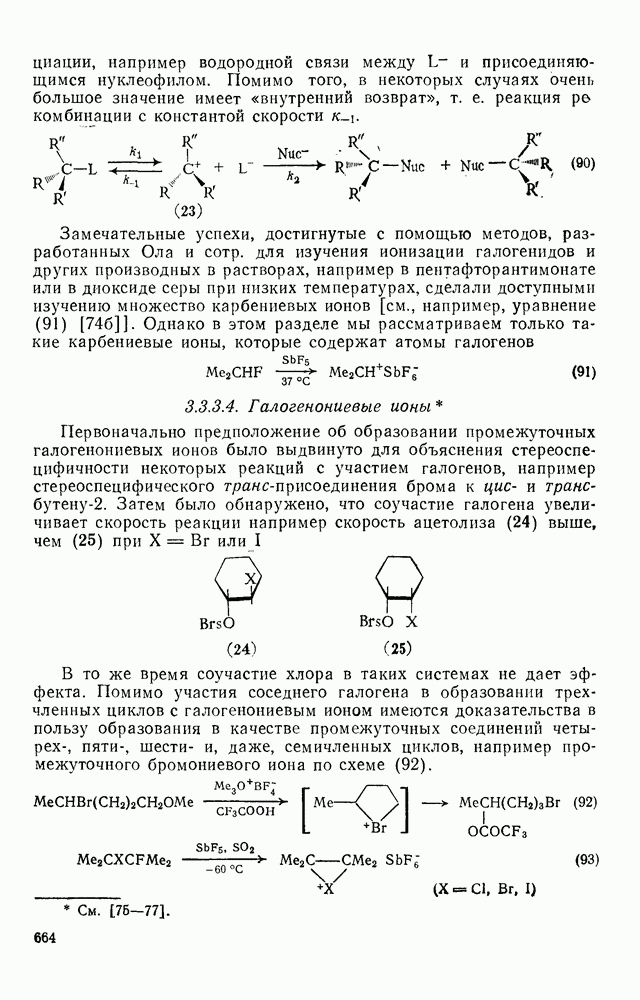
- 3.3.3.3. Реакции SN1 и относительно долгоживущие карбениевые ионы
- 3.3.3.4. Галогенониевые ионы
- 3.3.3.5. Галогенсодержащие карбениевые ионы
- 3.3.3.6. Механизм замещения с переносом электрона
- 3.3.4. Восстановление
- 3.3.5. Замещение на металлы
- 3.3.6. Элиминирование
- 3.3.6.1. b-Элиминирование
- 3.3.6.2. Галогенкарбанионы
- 3.3.6.3. Элиминирование через карбанионы
- 3.3.6.4. b-Элиминирование из металлорганических соединений
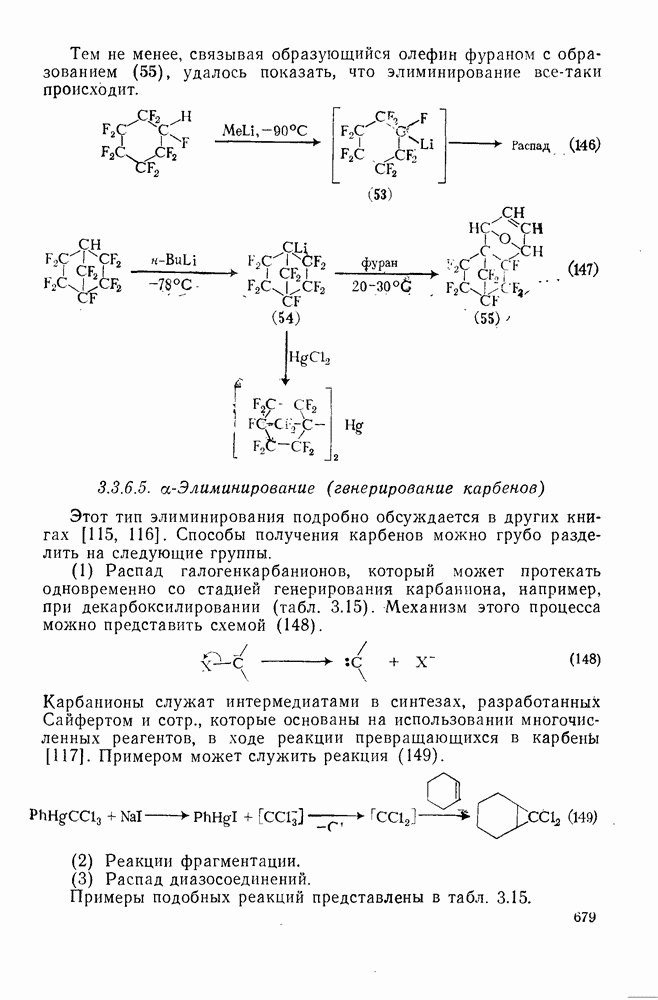
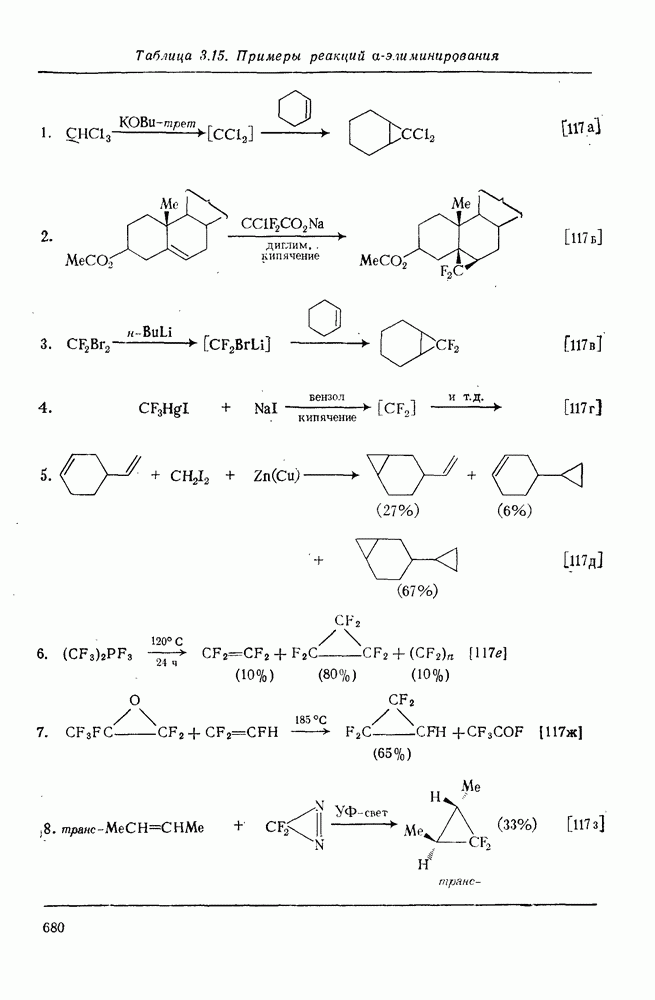
- 3.3.6.5. a-Элиминирование (генерирование карбенов)
- 3.4. ГАЛОГЕНАЛКЕНЫ
- 3.4.1. Синтез галогеналкенов
- 3.4.2. Нуклеофильная атака
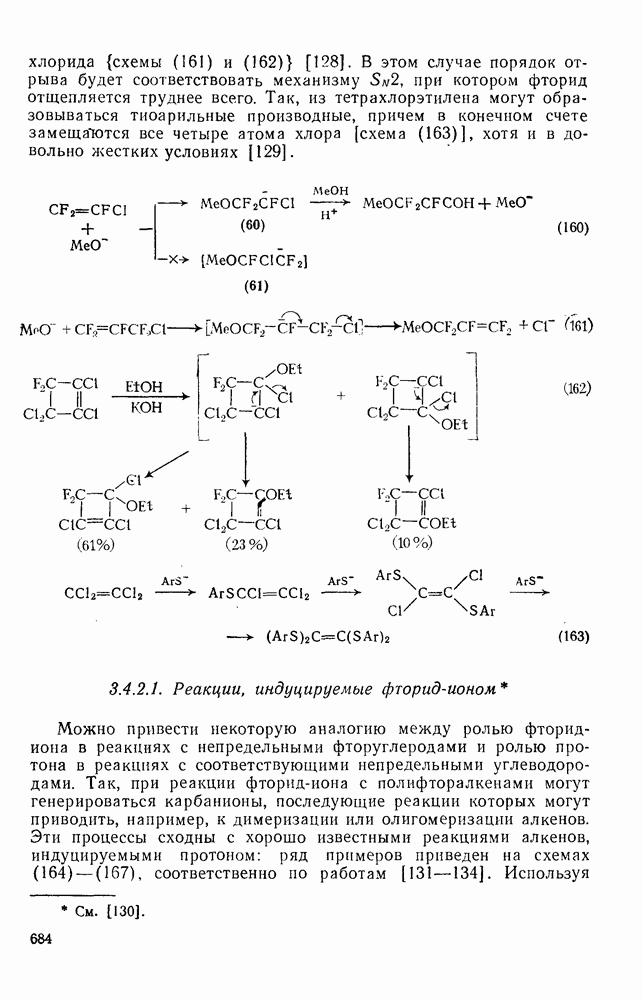
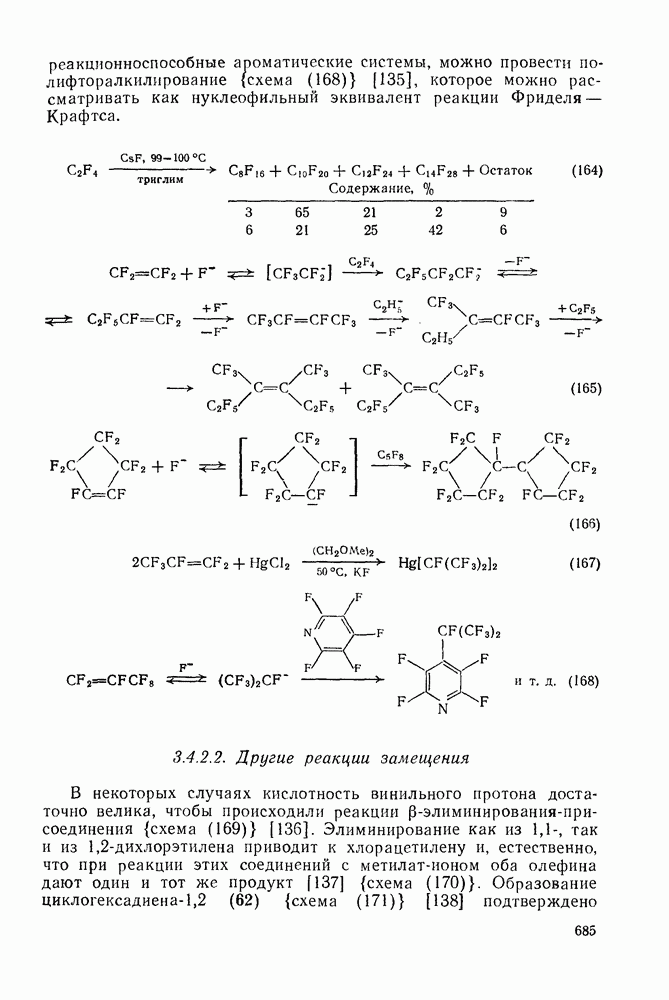
- 3.4.2.1. Реакции, индуцируемые фторид-ионом
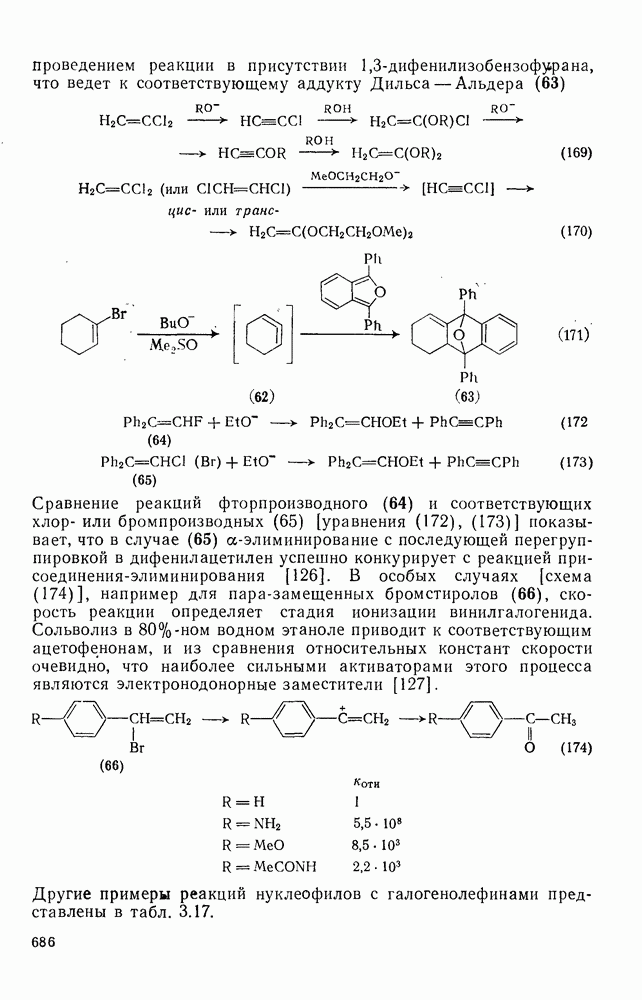
- 3.4.2.2. Другие реакции замещения
- 3.4.3. Радикальное присоединение
- 3.4.4. Электрофильное присоединение
- 3.4.5. Циклоприсоединение
- 3.4.5.1. [2+2]-Циклоприсоединение
- 3.4.5.2. [4+2]-Циклоприсоединение
- 3.5. ГАЛОГЕНАЛКИНЫ
- 3.6. ГАЛОГЕНАРЕНЫ
- 3.6.1. Замещение галогена
- 3.6.1.2. Присоединение-элиминирование
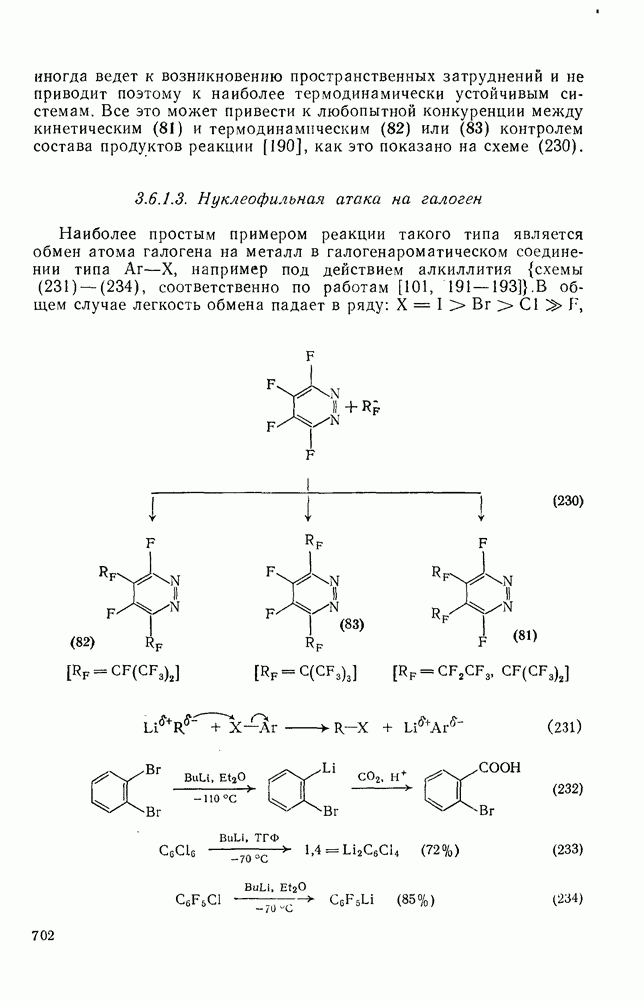
- 3.6.1.3. Нуклеофильная атака на галоген
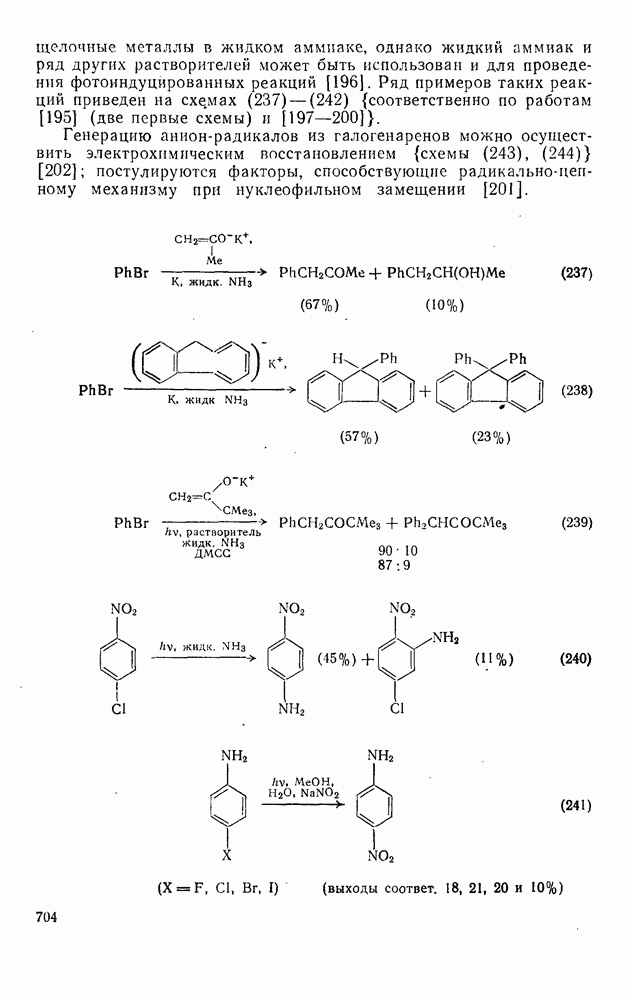
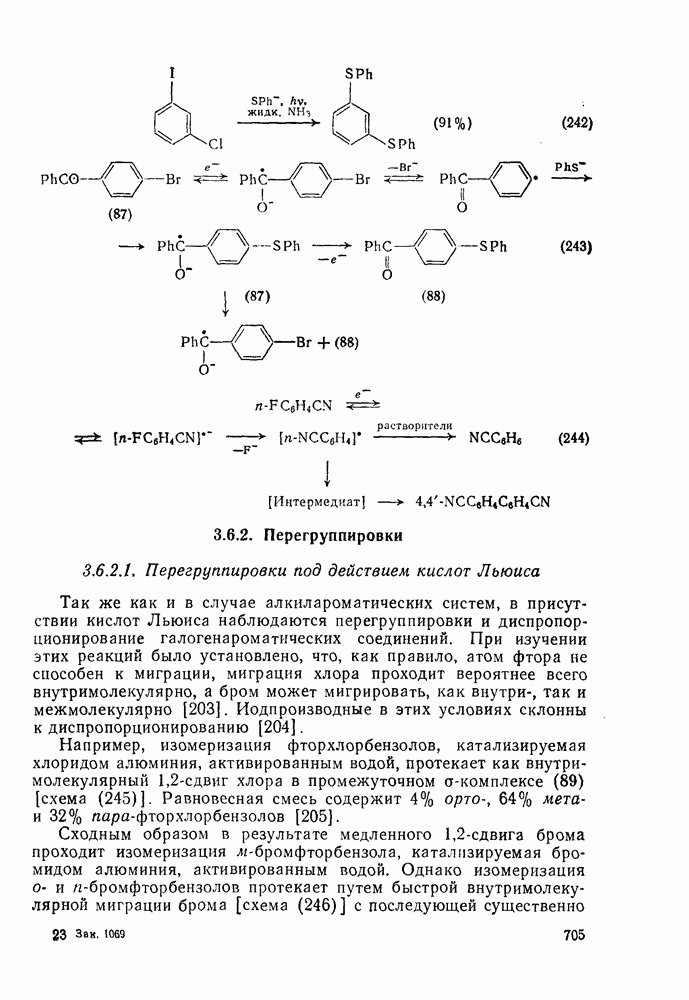
- 3.6.1.4. Перенос электрона
- 3.6.2. Перегруппировки
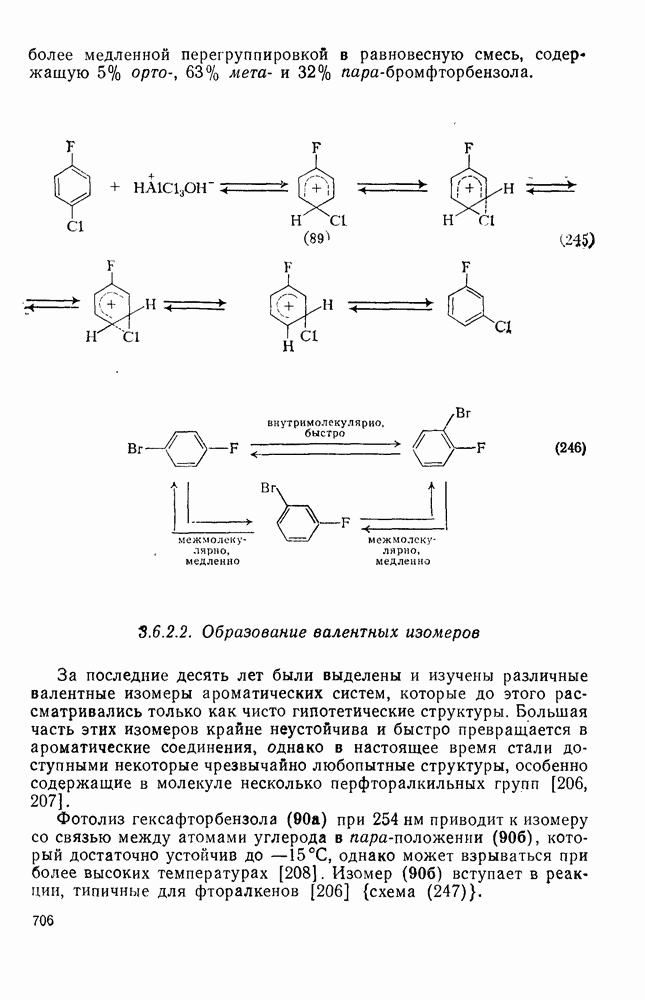
- 3.6.2.1. Перегруппировки под действием кислот Льюиса
- 3.6.2.2. Образование валентных изомеров