| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ГЛАВА XI. ДВУХАТОМНАЯ МОЛЕКУЛА
§ 78. Электронные термы двухатомной молекулы
В теория молекул основную роль играет тот факт, что массы ядер атомов очень велики по сравнению с массой электронов. Благодаря такой разнице в массах скорости движения ядер в молекуле малы по сравнению со скоростями электронов. Это дает возможность рассматривать электронное движение при неподвижных ядрах, расположенных на заданных расстояниях друг от друга. Определяя уровни энергии  такой системы, мы найдем, как говорят, электронные термы молекулы. В противоположность атомам, где энергетические уровни представляли собой определенные числа, здесь электронные термы являются не числами, а функциями от параметров — расстояний между ядрами в молекуле. В энергию
такой системы, мы найдем, как говорят, электронные термы молекулы. В противоположность атомам, где энергетические уровни представляли собой определенные числа, здесь электронные термы являются не числами, а функциями от параметров — расстояний между ядрами в молекуле. В энергию  включается также и электростатическая энергия взаимодействия ядер друг с другом, так что
включается также и электростатическая энергия взаимодействия ядер друг с другом, так что  представляет собой по существу полную энергию молекулы при заданном расположении неподвижных ядер.
представляет собой по существу полную энергию молекулы при заданном расположении неподвижных ядер.
Мы начнем изучение молекул с наиболее простого типа — двухатомных молекул, допускающего наиболее полное теоретическое исследование. Электронные термы двухатомной молекулы являются функциями всего одного параметра — расстояния  между ядрами.
между ядрами.
Одним из основных принципов классификации атомных термов была классификация по значениям полного орбитального момента L. В молекулах же вообще не имеет места закон сохранения полного орбитального момента электронов, поскольку электрическое поле нескольких ядер не обладает центральной симметрией.
В двухатомных молекулах, однако, поле обладает аксиальной симметрией относительно оси, проходящей через оба ядра. Поэтому здесь сохраняется проекция орбитального момента на эту ось, и мы можем классифицировать электронные термы молекул по значениям этой проекции. Абсолютную величину проекции орбитального момента на ось молекулы принято обозначать буквой  ; она пробегает значения
; она пробегает значения  Термы с различными значениями
Термы с различными значениями  обозначают большими греческими буквами, соответствующими латинским символам атомных термов с различными
обозначают большими греческими буквами, соответствующими латинским символам атомных термов с различными 
Так, при  говорят соответственно о
говорят соответственно о  -термах; большие
-термах; большие  обычно не приходится рассматривать.
обычно не приходится рассматривать.
Далее, каждое электронное состояние молекулы характеризуется полным спином s всех электронов в молекуле. При отличном от нуля s имеет место вырождение по направлениям полного спина кратности  . Число
. Число  как и в атомах, называется мулътиплетностью терма и пишется вверху слева от символа терма; так,
как и в атомах, называется мулътиплетностью терма и пишется вверху слева от символа терма; так,  обозначает терм с
обозначает терм с  .
.
Наряду с поворотами на произвольный угол вокруг оси, симметрия молекулы допускает также и отражение в любой плоскости, проходящей через эту ось. Если произвести такое отражение, то энергия молекулы останется неизменной. Получающееся же в результате состояние не будет, однако, вполне тождественным с исходным. Именно, при отражении в плоскости, проходящей через ось молекулы, изменится знак момента (аксиальный вектор!) относительно этой оси. Таким образом, мы приходим к результату, что все электронные термы с отличным от нуля значением  двукратно вырождены — каждому значению энергии соответствуют два состояния, отличающиеся направлением проекции орбитального момента на ось молекулы. Что же касается случая
двукратно вырождены — каждому значению энергии соответствуют два состояния, отличающиеся направлением проекции орбитального момента на ось молекулы. Что же касается случая  то здесь при отражении состояние молекулы вообще не меняется, так что
то здесь при отражении состояние молекулы вообще не меняется, так что  -термы не вырождены. Волновая функция
-термы не вырождены. Волновая функция  -терма в результате отражения может лишь умножиться на постоянную. Поскольку двукратное отражение в одной и той же плоскости сводится к тождественному преобразованию, то эта постоянная равна ±1. Таким образом, надо различать
-терма в результате отражения может лишь умножиться на постоянную. Поскольку двукратное отражение в одной и той же плоскости сводится к тождественному преобразованию, то эта постоянная равна ±1. Таким образом, надо различать  -термы, волновая функция которых не меняется вовсе при отражении, и термы, волновая функция которых меняет знак. Первые обозначаются посредством
-термы, волновая функция которых не меняется вовсе при отражении, и термы, волновая функция которых меняет знак. Первые обозначаются посредством  а вторые — как
а вторые — как 
Если молекула состоит из двух одинаковых атомов, то появляется новая симметрия, а с нею и дополнительная характеристика электронных термов. Именно, двухатомная молекула с одинаковыми ядрами обладает еще и центром симметрии относительно точки, делящей пополам линию, соединяющую ядра (начало координат выбираем в этой точке). Поэтому гамильтониан инвариантен относительно одновременного изменения знака координат всех электронов в молекуле (при неизменных координатах ядер).
Поскольку оператор этого преобразования коммутативен также и с оператором орбитального момента, то мы получаем возможность классифицировать термы с определенными значениями  еще и по их четности: волновая функция четных
еще и по их четности: волновая функция четных  состояний не меняется при изменении знака координат электронов, а нечетных
состояний не меняется при изменении знака координат электронов, а нечетных  — меняет знак. Индексы
— меняет знак. Индексы  , указывающие четность, принято писать внизу при символе терма:
, указывающие четность, принято писать внизу при символе терма:  и т. п.
и т. п.
Эмпирически известно, что у подавляющего большинства химически устойчивых двухатомных молекул нормальное электронное состояние обладает полной симметрией — электронная волновая функция инвариантна по отношению ко всем преобразованиям симметрии молекулы. В подавляющем большинстве случаев в нормальном состоянии также равен нулю полный спин S. Другими словами, основной терм молекулы есть  а если молекула состоит из одинаковых атомов, то
а если молекула состоит из одинаковых атомов, то  Известными исключениями из этих правил являются молекулы
Известными исключениями из этих правил являются молекулы  (нормальный терм
(нормальный терм  )
)  (нормальный терм
(нормальный терм  ).
).
Задача
Произвести разделение переменных в уравнении Шредингера для электронных термов иона  , воспользовавшись эллиптическими координатами.
, воспользовавшись эллиптическими координатами.
Решение. Уравнение Шредингера для электрона в поле двух неподвижных протонов:

(пользуемся атомными единицами). Эллиптические координаты  определяются как
определяются как

а третья координата  есть угол поворота вокруг оси, проходящей через два ядра, находящихся на расстоянии R друг от друга (см. I, § 48). Оператор Лапласа в этих координатах
есть угол поворота вокруг оси, проходящей через два ядра, находящихся на расстоянии R друг от друга (см. I, § 48). Оператор Лапласа в этих координатах

Полагая

получим для X и  следующие уравнения:
следующие уравнения:

где А — параметр разделения. Каждый электронный терм Е (R) характеризуется тремя квантовыми числами: А и двумя «эллиптическими квантовыми числами»  определяющими число нулей функций
определяющими число нулей функций 
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА К ЧЕТВЕРТОМУ ИЗДАНИЮ
- НЕКОТОРЫЕ ОБОЗНАЧЕНИЯ
- ГЛАВА I. ОСНОВНЫЕ ПОНЯТИЯ КВАНТОВОЙ МЕХАНИКИ
- § 1. Принцип неопределенности
- § 2. Принцип суперпозиции
- § 3. Операторы
- § 4. Сложение и умножение операторов
- § 5. Непрерывный спектр
- § 6. Предельный переход
- § 7. Волновая функция и измерения
- ГЛАВА II. ЭНЕРГИЯ И ИМПУЛЬС
- § 8. Гамильтониан
- § 9. Дифференцирование операторов по времени
- § 10. Стационарные состояния
- § 11. Матрицы
- § 12. Преобразование матриц
- § 13. Гейзенберговское представление операторов
- § 14. Матрица плотности
- § 15. Импульс
- § 16. Соотношения неопределенности
- ГЛАВА III. УРАВНЕНИЕ ШРЕДИНГЕРА
- § 17. Уравнение Шредингера
- § 18. Основные свойства уравнения Шредингера
- § 19. Плотность потока
- § 20. Вариационный принцип
- § 21. Общие свойства одномерного движения
- § 22. Потенциальная яма
- § 23. Линейный осциллятор
- § 24. Движение в однородном поле
- § 25. Коэффициент прохождения
- ГЛАВА IV. МОМЕНТ ИМПУЛЬСА
- § 26. Момент импульса
- § 27. Собственные значения момента
- § 28. Собственные функции момента
- § 29. Матричные элементы секторов
- § 30. Четность состояния
- § 31. Сложение моментов
- ГЛАВА V. ДВИЖЕНИЕ В ЦЕНТРАЛЬНО-СИММЕТРИЧНОМ ПОЛЕ
- § 32. Движение в центрально-симметричном поле
- § 33. Сферические волны
- § 34. Разложение плоской волны
- § 35. Падение частицы на центр
- § 36. Движение в кулоновом поле (сферические координаты)
- § 37. Движение в кулоновом поле (параболические координаты)
- ГЛАВА VI. ТЕОРИЯ ВОЗМУЩЕНИЙ
- § 38. Возмущения, не зависящие от времени
- § 39. Секулярное уравнение
- § 40. Возмущения, зависящие от времени
- § 41. Переходы под влиянием возмущения, действующего в течение конечного времени
- § 42. Переходы под влиянием периодического возмущения
- § 43. Переходы в непрерывном спектре
- § 44. Соотношение неопределенности для энергии
- § 45. Потенциальная энергия как возмущение
- ГЛАВА VII. КВАЗИКЛАССИЧЕСКИЙ СЛУЧАЙ
- § 46. Волновая функция в квазиклассическом случае
- § 47. Граничные условия в квазиклассическом случае
- § 48. Правило квантования Бора — Зоммерфельда
- § 49. Квазиклассическое движение в центрально-симметричном
- § 50. Прохождение через потенциальный барьер
- § 51. Вычисление квазиклассических матричных элементов
- § 52. Вероятность перехода в квазиклассическом случае
- § 53. Переходы под влиянием адиабатических возмущений
- ГЛАВА Vlll. СПИН
- § 54. Спин
- § 55. Оператор сиина
- § 56. Спиноры
- § 57. Волновые функции частиц с произвольным спином
- § 58. Оператор конечных вращений
- § 59. Частичная поляризация частиц
- § 60. Обращение времени и теорема Крамерса
- ГЛАВА IX. ТОЖДЕСТВЕННОСТЬ ЧАСТИЦ
- § 61. Принцип неразличимости одинаковых частиц
- § 62. Обменное взаимодействие
- § 63. Симметрия по отношению к перестановкам
- § 64. Вторичное квантование. Случай статистики Бозе
- § 65. Вторичное квантование. Случай статистики Ферми
- ГЛАВА X. АТОМ
- § 66. Атомные уровни энергии
- § 67. Состояния электронов в атоме
- § 68. Водородоподобные уровни энергии
- § 69. Самосогласованное поле
- § 70. Уравнение Томаса — Ферми
- § 71. Волновые функции внешних электронов вблизи ядра
- § 72. Тонкая структура атомных уровней
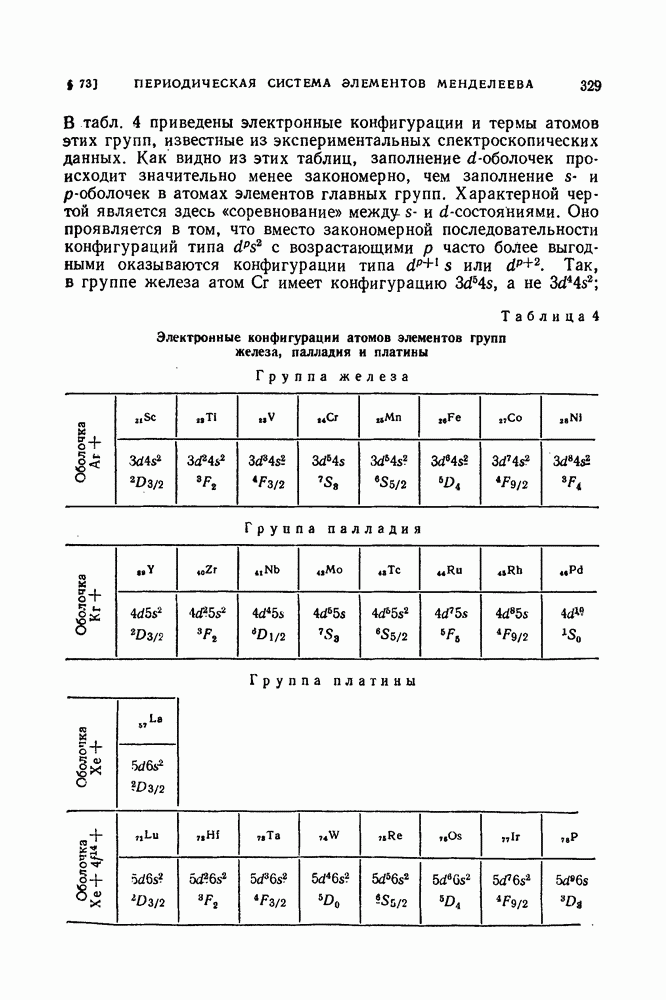
- § 73. Периодическая система элементов Менделеева
- § 74. Рентгеновские термы
- § 75. Мультипольные моменты
- § 76. Атом в электрическом поле
- § 77. Атом водорода в электрическом поле
- ГЛАВА XI. ДВУХАТОМНАЯ МОЛЕКУЛА
- § 78. Электронные термы двухатомной молекулы
- § 79. Пересечение электронных термов
- § 80. Связь молекулярных термов с атомными
- § 81. Валентность
- § 82. Колебательная и вращательная структуры синглетных термов двухатомной молекулы
- § 83. Мультиплетные термы. Случай а
- § 84. Мультиплетные термы. Случай b
- § 85. Мультиплетные термы. Случаи c и d
- § 86. Симметрия молекулярных термов
- § 87. Матричные элементы для двухатомной молекулы
- § 88. Л-удвоение
- § 89. Взаимодействие атомов на далеких расстояниях
- § 90. Предиссоциация
- ГЛАВА XII. ТЕОРИЯ СИММЕТРИИ
- § 91. Преобразования симметрии
- § 92. Группы преобразований
- § 93. Точечные группы
- § 94. Представления групп
- § 95. Неприводимые представления точечных групп
- § 96. Неприводимые представления и классификация термов
- § 97. Правила отбора для матричных элементов
- § 98. Непрерывные группы
- § 99. Двузначные представления конечных точечных групп
- ГЛАВА XIII. МНОГОАТОМНЫЕ МОЛЕКУЛЫ
- § 100. Классификация молекулярных колебаний
- § 101. Колебательные уровни энергии
- § 102. Устойчивость симметричных конфигураций молекулы
- § 103. Квантование вращения волчка
- § 104. Взаимодействие колебаний и вращения молекулы
- § 105. Классификация молекулярных термов
- ГЛАВА XIV. СЛОЖЕНИЕ МОМЕНТОВ
- § 106. 3j-символы
- § 107. Матричные элементы тензоров
- § 108. 6j-символы
- § 109. Матричные элементы при сложении моментов
- § 110. Матричные элементы для аксиально-симметричных систем
- ГЛАВА XV. ДВИЖЕНИЕ В МАГНИТНОМ ПОЛЕ
- § 111. Уравнение Шредингера в магнитном поле
- § 112. Движение в однородном магнитном поле
- § 113. Атом в магнитном поле
- § 114. Спин в переменном магнитном поле
- § 115. Плотность тока в магнитном поле
- ГЛАВА XVI. СТРУКТУРА АТОМНОГО ЯДРА
- § 116. Изотопическая инвариантность
- § 117. Ядерные силы
- § 118. Модель оболочек
- § 119. Несферические ядра
- § 120. Изотопическое смещение
- § 121. Сверхтонкая структура атомных уровней
- § 122. Сверхтонкая структура молекулярных уровней
- ГЛАВА XVII. УПРУГИЕ СТОЛКНОВЕНИЯ
- § 123. Общая теория рассеяния
- § 124. Исследование общей формулы
- § 125. Условие унитарности для рассеяния
- § 126. Формула Борна
- § 127. Квазиклассический случай
- § 128. Аналитические свойства амплитуды рассеяния
- § 129. Дисперсионное соотношение
- § 130. Амплитуда рассеяния в импульсном представлении
- § 131. Рассеяние при больших энергиях
- § 132. Рассеяние медленных частиц
- § 133. Резонансное рассеяние при малых энергиях
- § 134. Резонанс на квазидискретном уровне
- § 135. Формула Резерфорда
- § 136. Система волновых функций непрерывного спектра
- § 137. Столкновения одинаковых частиц
- § 138. Резонансное рассеяние заряженных частиц
- § 139. Упругие столкновения быстрых электронов с атомами
- § 140. Рассеяние при спин-орбитальном взаимодействии
- § 141. Полюсы Редже
- ГЛАВА XVIII. НЕУПРУГИЕ СТОЛКНОВЕНИЯ
- § 142. Упругое рассеяние при наличии неупругнх процессов
- § 143. Неупругое рассеяние медленных частиц
- § 144. Матрица рассеяния при наличии реакций
- § 145. Формулы Брейта и Вигнера
- § 146. Взаимодействие в конечном состоянии при реакциях
- § 147. Поведение сечений вблизи порога реакции
- § 148. Неупругие столкновения быстрых электронов с атомами
- § 149. Эффективное торможение
- § 150. Неупругие столкновения тяжелых частиц с атомами
- § 151. Рассеяние нейтронов
- § 152. Неупругое рассеяние при больших энергиях
- МАТЕМАТИЧЕСКИЕ ДОПОЛНЕНИЯ
- § а. Полиномы Эрмита
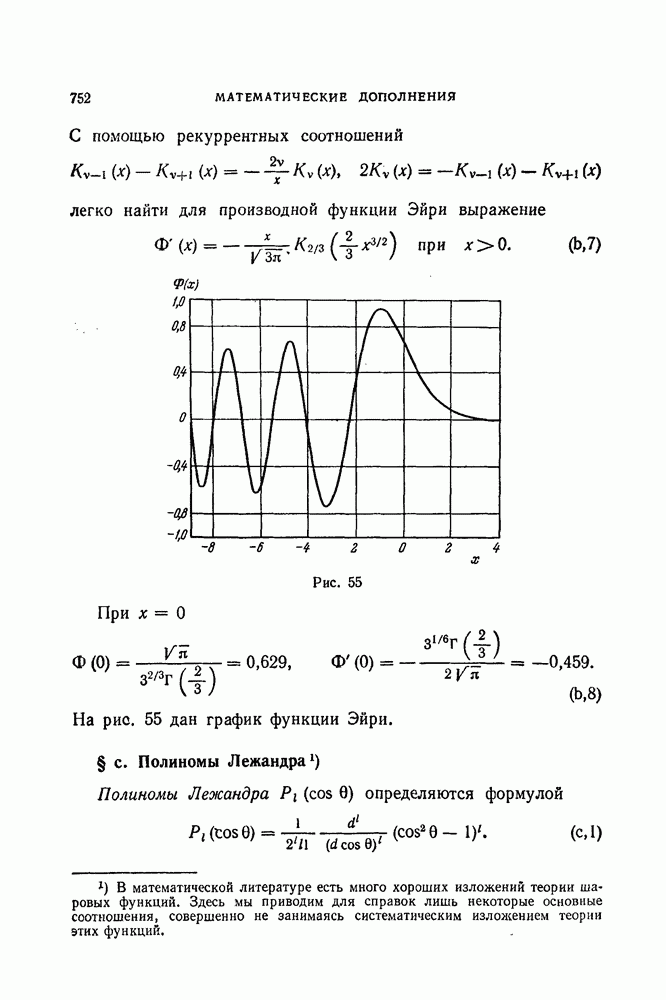
- § b. Функция Эйри
- § с. Полиномы Лежандра
- § d. Вырожденная гипергеометрическая функция
- § е. Гипергеометрическая функция
- § f. Вычисление интегралов с вырожденными гипергеометрическими функциями