| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ 67. Состояния электронов в атоме
Атом с более чем одним электроном представляет собой сложную систему взаимодействующих друг с другом электронов, движущихся в поле ядра. Для такой системы можно, строго говоря, рассматривать только состояния системы в целом. Тем не менее оказывается, что в атоме можно, с хорошей точностью, ввести понятие о состояниях каждого электрона в отдельности, как о стационарных состояниях движения электрона в некотором эффективном центрально-симметричном поле, созданном ядром вместе со всеми остальными электронами. Для различных электронов в атоме эти поля, вообще говоря, различны, причем определяться они должны одновременно все, поскольку каждое из них зависит от состояний всех остальных электронов. Такое поле называется самосогласованным.
Поскольку самосогласованное поле центрально-симметрично, то каждое состояние электрона характеризуется определенным значением его орбитального момента l, Состояния отдельного электрона при заданном l нумеруются (в порядке возрастания их энергии) с помощью главного квантового числа  , пробегающего значения
, пробегающего значения  такой выбор порядка нумерации устанавливают в соответствии с тем, который принят для атома водорода. Но последовательность возрастания уровней энергии с различными l в сложных атомах, вообще говоря, отличается от имеющей место у атома водорода. В последнем энергия вообще не зависит от l, так что состояния с большими
такой выбор порядка нумерации устанавливают в соответствии с тем, который принят для атома водорода. Но последовательность возрастания уровней энергии с различными l в сложных атомах, вообще говоря, отличается от имеющей место у атома водорода. В последнем энергия вообще не зависит от l, так что состояния с большими  всегда обладают большей энергией. В сложных же атомах уровень, например, с
всегда обладают большей энергией. В сложных же атомах уровень, например, с  оказывается лежащим ниже уровня с
оказывается лежащим ниже уровня с  (см. об этом подробнее в § 73).
(см. об этом подробнее в § 73).
Состояния отдельных электронов с различными  и l принято обозначать символом, состоящим из цифры, указывающей значение главного квантового числа, и буквы, указывающей значение l. Так,
и l принято обозначать символом, состоящим из цифры, указывающей значение главного квантового числа, и буквы, указывающей значение l. Так,  обозначает состояние с
обозначает состояние с  Полное описание состояния атома требует, наряду с указанием значений полных L, S, J, также и перечисления состояний всех электронов. Так, символ
Полное описание состояния атома требует, наряду с указанием значений полных L, S, J, также и перечисления состояний всех электронов. Так, символ  обозначает состояние атома гелия, в котором
обозначает состояние атома гелия, в котором  а два электрона находятся в состояниях
а два электрона находятся в состояниях  Если несколько электронов находится в состояниях с одинаковыми
Если несколько электронов находится в состояниях с одинаковыми  и
и  , то это принято обозначать для краткости в виде показателя степени; так,
, то это принято обозначать для краткости в виде показателя степени; так,  обозначает два электрона в состояниях
обозначает два электрона в состояниях  . О распределении электронов в атоме по состояниям с различными
. О распределении электронов в атоме по состояниям с различными  говорят, как об электронной конфигурации.
говорят, как об электронной конфигурации.
При заданных значениях  электрон может обладать различными значениями проекций орбитального момента
электрон может обладать различными значениями проекций орбитального момента  и спина
и спина  на ось
на ось  . При заданном I число
. При заданном I число  пробегает
пробегает  значений; число же а ограничено всего двумя значениями ±1/2. Поэтому всего имеется (
значений; число же а ограничено всего двумя значениями ±1/2. Поэтому всего имеется ( ) различных состояний с одинаковыми
) различных состояний с одинаковыми  такие состояния называют эквивалентными. В каждом из них может находиться, согласно принципу Паули, по одному электрону. Таким образом, в атоме может одновременно иметь одинаковые
такие состояния называют эквивалентными. В каждом из них может находиться, согласно принципу Паули, по одному электрону. Таким образом, в атоме может одновременно иметь одинаковые  не более (
не более ( ) электронов. О совокупности электронов, заполняющих все состояния с данными
) электронов. О совокупности электронов, заполняющих все состояния с данными  , говорят как о замкнутой оболочке данного типа.
, говорят как о замкнутой оболочке данного типа.
Различие в энергии атомных уровней, обладающих различными L, S при одинаковой электронной конфигурации 1), связано с электростатическим взаимодействием электронов. Обычно разности этих энергий сравнительно малы — в несколько раз меньше расстояний между уровнями с различными конфигурациями. По поводу взаимного расположения уровней с одинаковой конфигурацией, но различными L, S существует следующее эмпирически установленное правило Хунда (F. Hund, 1925):
Наименьшей энергией обладает терм с наибольшим возможным при данной электронной конфигурации значением S и наибольшим (возможным при этом S) значением 
Покажем, каким образом можно найти возможные для данной электронной конфигурации атомные термы. Если электроны не эквивалентны, то определение возможных значений L, 5 производится непосредственно по правилу сложения моментов. Так, при конфигурации  (с различными
(с различными  ) суммарный момент L может иметь значения 2, 1, 0, а суммарный спин
) суммарный момент L может иметь значения 2, 1, 0, а суммарный спин  ; комбинируя их друг с другом, получим термы
; комбинируя их друг с другом, получим термы 
Если же мы имеем дело с эквивалентными электронами, то появляются ограничения, налагаемые принципом Паули. Рассмотрим, например, конфигурацию из трех эквивалентных  -электронов.
-электронов.
При  (
( -состояние) проекция
-состояние) проекция  орбитального момента может иметь значения
орбитального момента может иметь значения  , так что возможны шесть состояний со следующими парами чисел
, так что возможны шесть состояний со следующими парами чисел 

Три электрона можно расположить по одному в трех любых из этих состояний. В результате получим состояния атома со следующими значениями проекций  а полного орбитального момента и спина:
а полного орбитального момента и спина:

(состояний с отрицательными значениями  можно не выписывать, так как они не дают ничего нового). Наличие состояния с
можно не выписывать, так как они не дают ничего нового). Наличие состояния с  показывает, что должен иметься терм
показывает, что должен иметься терм  этому терму должны соответствовать еще и по одному состоянию (1, 1/2), (0, 1/2). Далее, остается еще одно состояние с (1, 1/2), так что должен иметься терм
этому терму должны соответствовать еще и по одному состоянию (1, 1/2), (0, 1/2). Далее, остается еще одно состояние с (1, 1/2), так что должен иметься терм  ему отвечает также и одно из состояний с (0, 1/2). Наконец, остаются еще состояния (0, 3/2) и (0, 1/2), которые соответствуют терму 45. Таким образом, для конфигурации из трех эквивалентных
ему отвечает также и одно из состояний с (0, 1/2). Наконец, остаются еще состояния (0, 3/2) и (0, 1/2), которые соответствуют терму 45. Таким образом, для конфигурации из трех эквивалентных  -электронов возможны лишь по одному терму типов
-электронов возможны лишь по одному терму типов 
Таблица 1. Возможные термы для конфигураций из эквивалентных электронов

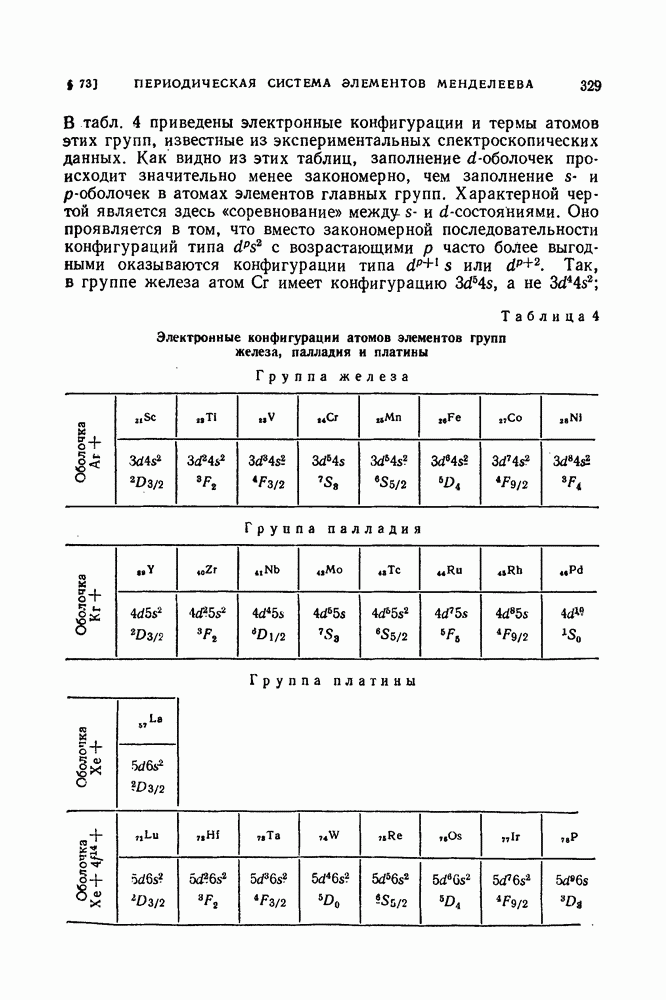
В табл. 1 перечислены возможные термы для различных конфигураций из эквивалентных  и
и  -электронов. Числа под символами термов указывают число термов данного типа, имеющихся для данной конфигурации, если это число превышает единицу. Для конфигурации из наибольшего возможного числа эквивалентных электронов
-электронов. Числа под символами термов указывают число термов данного типа, имеющихся для данной конфигурации, если это число превышает единицу. Для конфигурации из наибольшего возможного числа эквивалентных электронов  терм есть всегда
терм есть всегда  .
.
Обратим внимание на совпадение характера термов, отвечающих конфигурациям, из которых одна имеет столько электронов, сколько не хватает другой для заполнения оболочки. Это является очевидным результатом того, что отсутствие электрона в оболочке можно рассматривать как дырку, состояние которой определяется теми же квантовыми числами, что и состояние отсутствующего электрона.
При применении правила Хунда для определения нормального терма атома по известной электронной конфигурации надо рассматривать только незаполненную оболочку, поскольку моменты электронов в заполненных оболочках взаимно компенсируются. Пусть, например, вне замкнутых оболочек в атоме имеется четыре  -электрона. Магнитное квантовое число
-электрона. Магнитное квантовое число  -электрона может принимать пять значений: 0, ±1, ±2. Поэтому все четыре электрона могут иметь одинаковую проекцию спина
-электрона может принимать пять значений: 0, ±1, ±2. Поэтому все четыре электрона могут иметь одинаковую проекцию спина  так что максимальный возможный полный спин есть
так что максимальный возможный полный спин есть  После этого мы должны приписать электронам различные значения числа
После этого мы должны приписать электронам различные значения числа  , которые дали бы наибольшее значение
, которые дали бы наибольшее значение  это 2, 1,0, — 1, так что
это 2, 1,0, — 1, так что  . Это значит, что и наибольшее возможное при
. Это значит, что и наибольшее возможное при  значение L равно 2 (терм
значение L равно 2 (терм  ).
).
Задача
Найти орбитальные волновые функции возможных состояний системы трех эквивалентных  -электронов.
-электронов.
Решение. В состоянии S проекции спинов а всех электронов одинаковы, а потому значения  различны. Волновая функция дается определителем вида (61,5), составленным из функций
различны. Волновая функция дается определителем вида (61,5), составленным из функций  (индекс указывает значение
(индекс указывает значение  ).
).
Для терма  рассмотрим состояние с наибольшим возможным значением
рассмотрим состояние с наибольшим возможным значением  При этом две из проекций
При этом две из проекций  должны быть равны 1, а одна 0. Пусть электроны 2, 3 имеют
должны быть равны 1, а одна 0. Пусть электроны 2, 3 имеют  а электрон
а электрон  (в соответствии с полным спином
(в соответствии с полным спином  Соответствующая орбитальная волновая функция, обладающая требуемым свойством симметрии, есть
Соответствующая орбитальная волновая функция, обладающая требуемым свойством симметрии, есть

(цифра в аргументе функции указывает номер электрона, к которому она относится).
Для терма  рассматриваем состояние с
рассматриваем состояние с  и теми же, что и выше, значениями проекций спина электронов. Это состояние можно осуществить с двумя различными наборами значений
и теми же, что и выше, значениями проекций спина электронов. Это состояние можно осуществить с двумя различными наборами значений  , так что орбитальная волновая функция дается линейной комбинацией
, так что орбитальная волновая функция дается линейной комбинацией

Для определения коэффициентов воспользуемся соотношением

которому должна удовлетворять волновая функция с  (см. (27,8)).
(см. (27,8)).
С помощью матричных элементов (27,12) найдем, что

и затем

Отсюда  ; учитывая также условие нормировки, имеем
; учитывая также условие нормировки, имеем 
Волновые функции состояний с  получаются из найденных нами функций воздействием на них оператора
получаются из найденных нами функций воздействием на них оператора  .
.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА К ЧЕТВЕРТОМУ ИЗДАНИЮ
- НЕКОТОРЫЕ ОБОЗНАЧЕНИЯ
- ГЛАВА I. ОСНОВНЫЕ ПОНЯТИЯ КВАНТОВОЙ МЕХАНИКИ
- § 1. Принцип неопределенности
- § 2. Принцип суперпозиции
- § 3. Операторы
- § 4. Сложение и умножение операторов
- § 5. Непрерывный спектр
- § 6. Предельный переход
- § 7. Волновая функция и измерения
- ГЛАВА II. ЭНЕРГИЯ И ИМПУЛЬС
- § 8. Гамильтониан
- § 9. Дифференцирование операторов по времени
- § 10. Стационарные состояния
- § 11. Матрицы
- § 12. Преобразование матриц
- § 13. Гейзенберговское представление операторов
- § 14. Матрица плотности
- § 15. Импульс
- § 16. Соотношения неопределенности
- ГЛАВА III. УРАВНЕНИЕ ШРЕДИНГЕРА
- § 17. Уравнение Шредингера
- § 18. Основные свойства уравнения Шредингера
- § 19. Плотность потока
- § 20. Вариационный принцип
- § 21. Общие свойства одномерного движения
- § 22. Потенциальная яма
- § 23. Линейный осциллятор
- § 24. Движение в однородном поле
- § 25. Коэффициент прохождения
- ГЛАВА IV. МОМЕНТ ИМПУЛЬСА
- § 26. Момент импульса
- § 27. Собственные значения момента
- § 28. Собственные функции момента
- § 29. Матричные элементы секторов
- § 30. Четность состояния
- § 31. Сложение моментов
- ГЛАВА V. ДВИЖЕНИЕ В ЦЕНТРАЛЬНО-СИММЕТРИЧНОМ ПОЛЕ
- § 32. Движение в центрально-симметричном поле
- § 33. Сферические волны
- § 34. Разложение плоской волны
- § 35. Падение частицы на центр
- § 36. Движение в кулоновом поле (сферические координаты)
- § 37. Движение в кулоновом поле (параболические координаты)
- ГЛАВА VI. ТЕОРИЯ ВОЗМУЩЕНИЙ
- § 38. Возмущения, не зависящие от времени
- § 39. Секулярное уравнение
- § 40. Возмущения, зависящие от времени
- § 41. Переходы под влиянием возмущения, действующего в течение конечного времени
- § 42. Переходы под влиянием периодического возмущения
- § 43. Переходы в непрерывном спектре
- § 44. Соотношение неопределенности для энергии
- § 45. Потенциальная энергия как возмущение
- ГЛАВА VII. КВАЗИКЛАССИЧЕСКИЙ СЛУЧАЙ
- § 46. Волновая функция в квазиклассическом случае
- § 47. Граничные условия в квазиклассическом случае
- § 48. Правило квантования Бора — Зоммерфельда
- § 49. Квазиклассическое движение в центрально-симметричном
- § 50. Прохождение через потенциальный барьер
- § 51. Вычисление квазиклассических матричных элементов
- § 52. Вероятность перехода в квазиклассическом случае
- § 53. Переходы под влиянием адиабатических возмущений
- ГЛАВА Vlll. СПИН
- § 54. Спин
- § 55. Оператор сиина
- § 56. Спиноры
- § 57. Волновые функции частиц с произвольным спином
- § 58. Оператор конечных вращений
- § 59. Частичная поляризация частиц
- § 60. Обращение времени и теорема Крамерса
- ГЛАВА IX. ТОЖДЕСТВЕННОСТЬ ЧАСТИЦ
- § 61. Принцип неразличимости одинаковых частиц
- § 62. Обменное взаимодействие
- § 63. Симметрия по отношению к перестановкам
- § 64. Вторичное квантование. Случай статистики Бозе
- § 65. Вторичное квантование. Случай статистики Ферми
- ГЛАВА X. АТОМ
- § 66. Атомные уровни энергии
- § 67. Состояния электронов в атоме
- § 68. Водородоподобные уровни энергии
- § 69. Самосогласованное поле
- § 70. Уравнение Томаса — Ферми
- § 71. Волновые функции внешних электронов вблизи ядра
- § 72. Тонкая структура атомных уровней
- § 73. Периодическая система элементов Менделеева
- § 74. Рентгеновские термы
- § 75. Мультипольные моменты
- § 76. Атом в электрическом поле
- § 77. Атом водорода в электрическом поле
- ГЛАВА XI. ДВУХАТОМНАЯ МОЛЕКУЛА
- § 78. Электронные термы двухатомной молекулы
- § 79. Пересечение электронных термов
- § 80. Связь молекулярных термов с атомными
- § 81. Валентность
- § 82. Колебательная и вращательная структуры синглетных термов двухатомной молекулы
- § 83. Мультиплетные термы. Случай а
- § 84. Мультиплетные термы. Случай b
- § 85. Мультиплетные термы. Случаи c и d
- § 86. Симметрия молекулярных термов
- § 87. Матричные элементы для двухатомной молекулы
- § 88. Л-удвоение
- § 89. Взаимодействие атомов на далеких расстояниях
- § 90. Предиссоциация
- ГЛАВА XII. ТЕОРИЯ СИММЕТРИИ
- § 91. Преобразования симметрии
- § 92. Группы преобразований
- § 93. Точечные группы
- § 94. Представления групп
- § 95. Неприводимые представления точечных групп
- § 96. Неприводимые представления и классификация термов
- § 97. Правила отбора для матричных элементов
- § 98. Непрерывные группы
- § 99. Двузначные представления конечных точечных групп
- ГЛАВА XIII. МНОГОАТОМНЫЕ МОЛЕКУЛЫ
- § 100. Классификация молекулярных колебаний
- § 101. Колебательные уровни энергии
- § 102. Устойчивость симметричных конфигураций молекулы
- § 103. Квантование вращения волчка
- § 104. Взаимодействие колебаний и вращения молекулы
- § 105. Классификация молекулярных термов
- ГЛАВА XIV. СЛОЖЕНИЕ МОМЕНТОВ
- § 106. 3j-символы
- § 107. Матричные элементы тензоров
- § 108. 6j-символы
- § 109. Матричные элементы при сложении моментов
- § 110. Матричные элементы для аксиально-симметричных систем
- ГЛАВА XV. ДВИЖЕНИЕ В МАГНИТНОМ ПОЛЕ
- § 111. Уравнение Шредингера в магнитном поле
- § 112. Движение в однородном магнитном поле
- § 113. Атом в магнитном поле
- § 114. Спин в переменном магнитном поле
- § 115. Плотность тока в магнитном поле
- ГЛАВА XVI. СТРУКТУРА АТОМНОГО ЯДРА
- § 116. Изотопическая инвариантность
- § 117. Ядерные силы
- § 118. Модель оболочек
- § 119. Несферические ядра
- § 120. Изотопическое смещение
- § 121. Сверхтонкая структура атомных уровней
- § 122. Сверхтонкая структура молекулярных уровней
- ГЛАВА XVII. УПРУГИЕ СТОЛКНОВЕНИЯ
- § 123. Общая теория рассеяния
- § 124. Исследование общей формулы
- § 125. Условие унитарности для рассеяния
- § 126. Формула Борна
- § 127. Квазиклассический случай
- § 128. Аналитические свойства амплитуды рассеяния
- § 129. Дисперсионное соотношение
- § 130. Амплитуда рассеяния в импульсном представлении
- § 131. Рассеяние при больших энергиях
- § 132. Рассеяние медленных частиц
- § 133. Резонансное рассеяние при малых энергиях
- § 134. Резонанс на квазидискретном уровне
- § 135. Формула Резерфорда
- § 136. Система волновых функций непрерывного спектра
- § 137. Столкновения одинаковых частиц
- § 138. Резонансное рассеяние заряженных частиц
- § 139. Упругие столкновения быстрых электронов с атомами
- § 140. Рассеяние при спин-орбитальном взаимодействии
- § 141. Полюсы Редже
- ГЛАВА XVIII. НЕУПРУГИЕ СТОЛКНОВЕНИЯ
- § 142. Упругое рассеяние при наличии неупругнх процессов
- § 143. Неупругое рассеяние медленных частиц
- § 144. Матрица рассеяния при наличии реакций
- § 145. Формулы Брейта и Вигнера
- § 146. Взаимодействие в конечном состоянии при реакциях
- § 147. Поведение сечений вблизи порога реакции
- § 148. Неупругие столкновения быстрых электронов с атомами
- § 149. Эффективное торможение
- § 150. Неупругие столкновения тяжелых частиц с атомами
- § 151. Рассеяние нейтронов
- § 152. Неупругое рассеяние при больших энергиях
- МАТЕМАТИЧЕСКИЕ ДОПОЛНЕНИЯ
- § а. Полиномы Эрмита
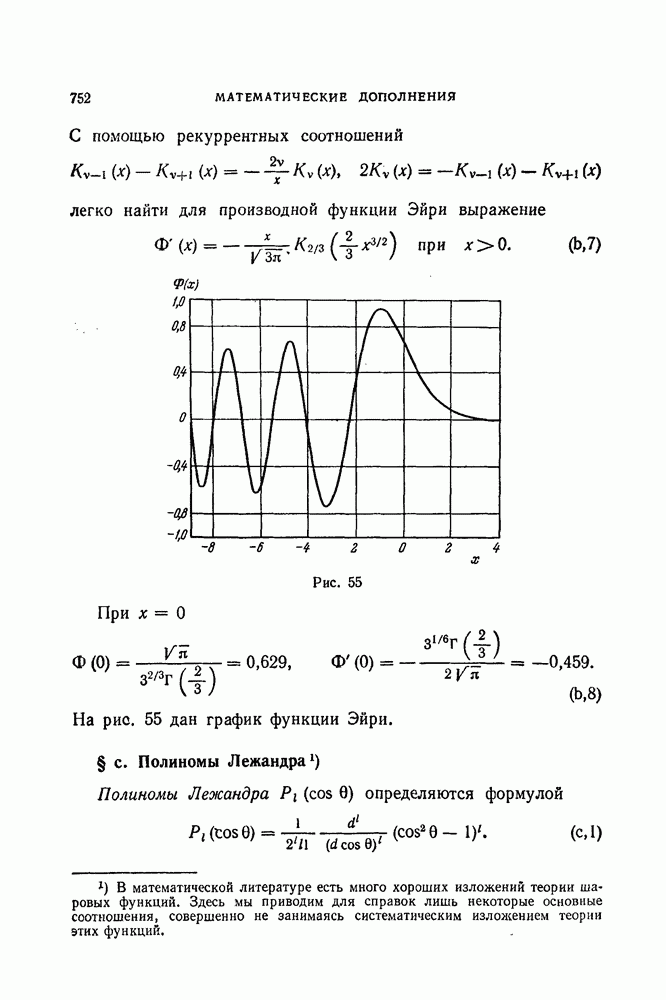
- § b. Функция Эйри
- § с. Полиномы Лежандра
- § d. Вырожденная гипергеометрическая функция
- § е. Гипергеометрическая функция
- § f. Вычисление интегралов с вырожденными гипергеометрическими функциями