| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
2.7. Равновесие фаз. Фазовые переходы
Условия равновесия фаз. Фазой называется часть системы, однородная по физическим и химическим свойствам. Одно и то же по химическому составу вещество может находиться в разных фазах. Примерами двухфазной системы являются: (жидкость+насыщенный пар), (твердое тело+жидкость) и (твердое тело+пар).
Условия равновесия фаз: 1) равенство давлений — механическое равновесие; 2) равенство температур — тепловое равновесие; 3) равенство химических потенциалов (или удельных потенциалов Гиббса) — равновесие по отношению переходу вещества из одной фазы в другую. Последнее условие соответствует минимуму термодинамического потенциала Гиббса  (см. разд. 2.4) по отношению к числу частиц в одной из фаз
(см. разд. 2.4) по отношению к числу частиц в одной из фаз  Условие
Условие  дает (для простой системы) уравнение для кривой сосуществования фаз
дает (для простой системы) уравнение для кривой сосуществования фаз  двухфазная простая система имеет только одну степень свободы. Так, давление насыщенного пара (положение горизонтального участка изотермы, см. разд. 2.6) является однозначной функцией температуры; то же самое относится к зависимости температуры плавления от внешнего давления (кривая плавления) и к зависимости от температуры давления пара над твердой поверхностью (кривая возгонки).
двухфазная простая система имеет только одну степень свободы. Так, давление насыщенного пара (положение горизонтального участка изотермы, см. разд. 2.6) является однозначной функцией температуры; то же самое относится к зависимости температуры плавления от внешнего давления (кривая плавления) и к зависимости от температуры давления пара над твердой поверхностью (кривая возгонки).
На рис. 20 приведены все три кривые (существования, плавления и возгонки) для воды. Точка пересечения этих кривых называется тройной точкой (для воды 
Для существования трехфазной системы должны выполняться сразу два условия:  которые однозначно определяют ее" давление и температуру.
которые однозначно определяют ее" давление и температуру.

Рис. 20.
Фазовый переход первого рода. Теплота и энтропия перехода. Чтобы в двухфазной системе перевести часть вещества массой  из одной фазы в другую, не меняя при этом давления и температуры, надо сообщить системе теплоту
из одной фазы в другую, не меняя при этом давления и температуры, надо сообщить системе теплоту  которую называют (скрытой) теплотой фазового перехода
которую называют (скрытой) теплотой фазового перехода  — удельная теплота перехода). При переходе вещества в новую фазу ее энтропия изменилась на
— удельная теплота перехода). При переходе вещества в новую фазу ее энтропия изменилась на  а внутренняя энергия на
а внутренняя энергия на  удельный объем). Величину
удельный объем). Величину  называют удельной энтропией перехода, а Ди
называют удельной энтропией перехода, а Ди  — изменением удельной энергии при переходе. Переход вещества между фазами двухфазной системы, связанный с поглощением (выделением) теплоты перехода и сопровождающийся скачкообразным изменением внутренней энергии, энтропии, плотности (объема) и др., называется фазовым переходом первого рода.
— изменением удельной энергии при переходе. Переход вещества между фазами двухфазной системы, связанный с поглощением (выделением) теплоты перехода и сопровождающийся скачкообразным изменением внутренней энергии, энтропии, плотности (объема) и др., называется фазовым переходом первого рода.
Уравнение Клапейрона — Клаузиуса. Если изменить температуру двухфазной системы, то ее давление изменится таким образом, что химические потенциалы (или удельные потенциалы Гиббса) фаз останутся равными:  или —
или —  (см. разд. 2.4). Получаем, что наклон кривой фазового равновесия равен
(см. разд. 2.4). Получаем, что наклон кривой фазового равновесия равен

(уравнение Клапейрона — Клаузиуса). Например, для перехода лед — вода при атмосферном давлении температура плавления равна  и мы
и мы  получим
получим  Знак минус объясняется аномальным
Знак минус объясняется аномальным  свойством воды: при плавлении (таянии) ее плотность увеличивается.
свойством воды: при плавлении (таянии) ее плотность увеличивается.
Пример 1. Если непрерывно подводить к жидкости теплоту, то в тот момент, когда ее температура достигает значения, при котором давление насыщенного пара равно внешнему давлению, наступает интенсивное парообразование во всем объеме жидкости, которое называют кипением. Уравнение (49) определяет зависимость температуры кипения от внешнего давления. Пренебрегая удельным объемом жидкости и выражая удельный объем пара из уравнения состояния
идеального газа:  получим приближенное уравнение Например, для воды
получим приближенное уравнение Например, для воды  при атмосферном давлении
при атмосферном давлении  Па температура кипения равна
Па температура кипения равна  удельная теплота
удельная теплота  и мы получим
и мы получим 
Фазовый переход второго рода. При фазовом переходе второго рода (точка Кюри перехода в ферромагнитное состояние, точка перехода жидкого гелия в сверхтекучее состояние и др.) плотность, внутренняя энергия, энтропия изменяются непрерывно, а различного вида производные этих термодинамических функций (восприимчивости) — теплоемкость, сжимаемость, диэлектрическая или магнитная проницаемость и т.д. — изменяются скачком или проявляют критическое поведение (стремятся к бесконечности при приближении к точке перехода). Фазовый переход второго рода происходит сразу во всем объеме. В результате перехода происходит качественное изменение внутреннего строения — появляется (или исчезает) дополнительная симметрия.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ
- 1. Аналитическая геометрия на плоскости
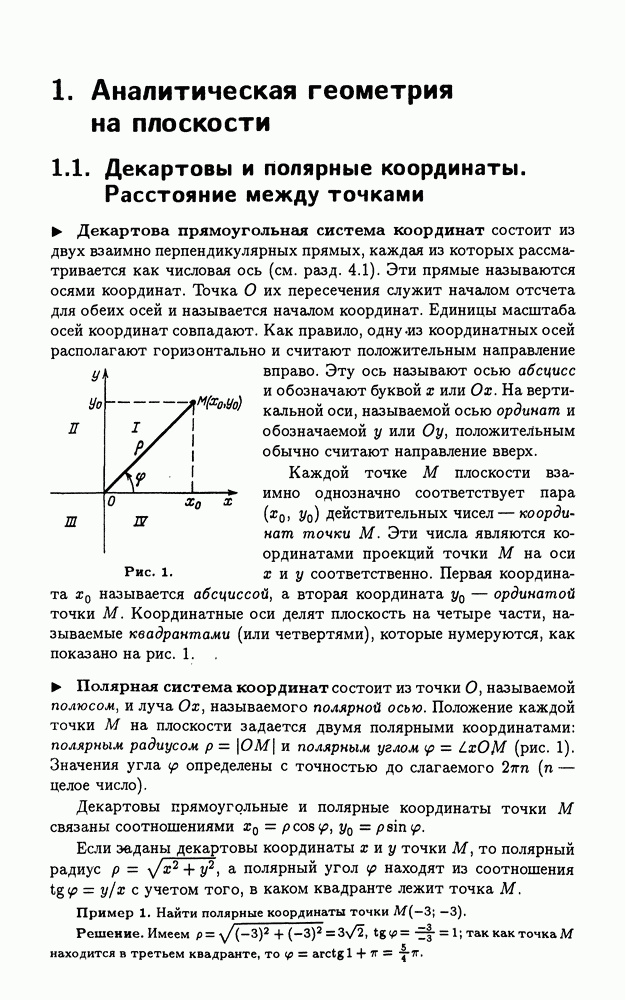
- 1.1. Декартовы и полярные координаты. Расстояние между точками
- 1.2. Деление отрезка в данном отношении. Площадь многоугольника
- 1.3. Различные виды уравнения прямой
- 1.4. Угол между прямыми. Расстояние от точки до прямой
- 1.5. Окружность, эллипс, гипербола и парабола
- 1.6. Приведение общего уравнения кривой второго порядка к каноническому виду
- 2. Аналитическая геометрия в пространстве
- 2.2. Векторы
- 2.3. Действия над векторами. Скалярное произведение
- 2.4. Векторное и смешанное произведения
- 2.5. Плоскость в пространстве
- 2.6. Прямая в пространстве
- 2.7. Прямая и плоскость в пространстве
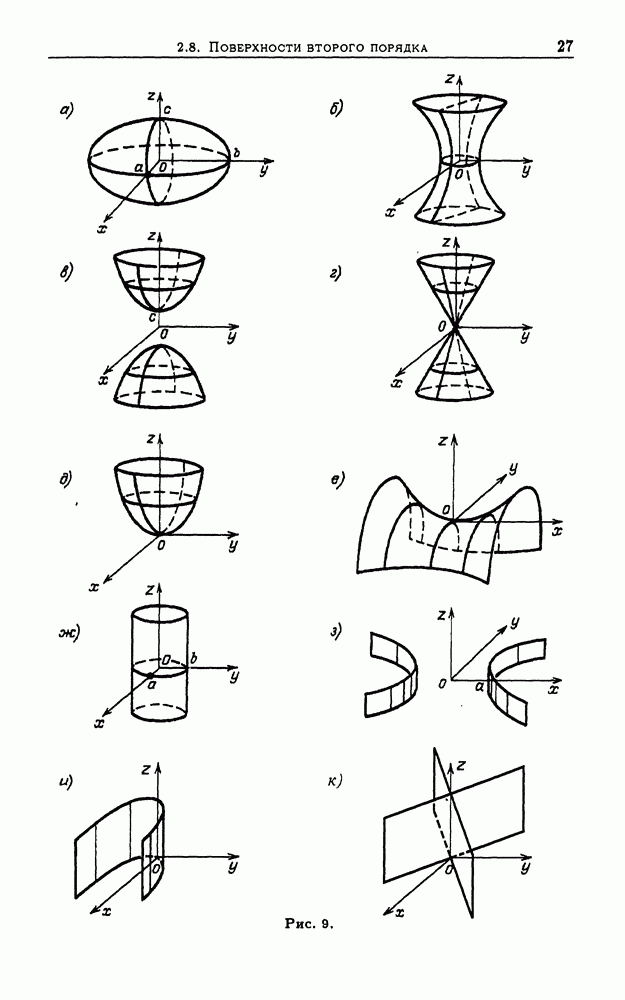
- 2.8. Поверхности второго порядка
- 3. Линейная алгебра
- 3.2. Матрицы
- 3.3. Системы линейных уравнений
- 3.4. Системы n-мерных векторов. Собственные значения и собственные векторы матрицы
- 4. Основные понятия математического анализа
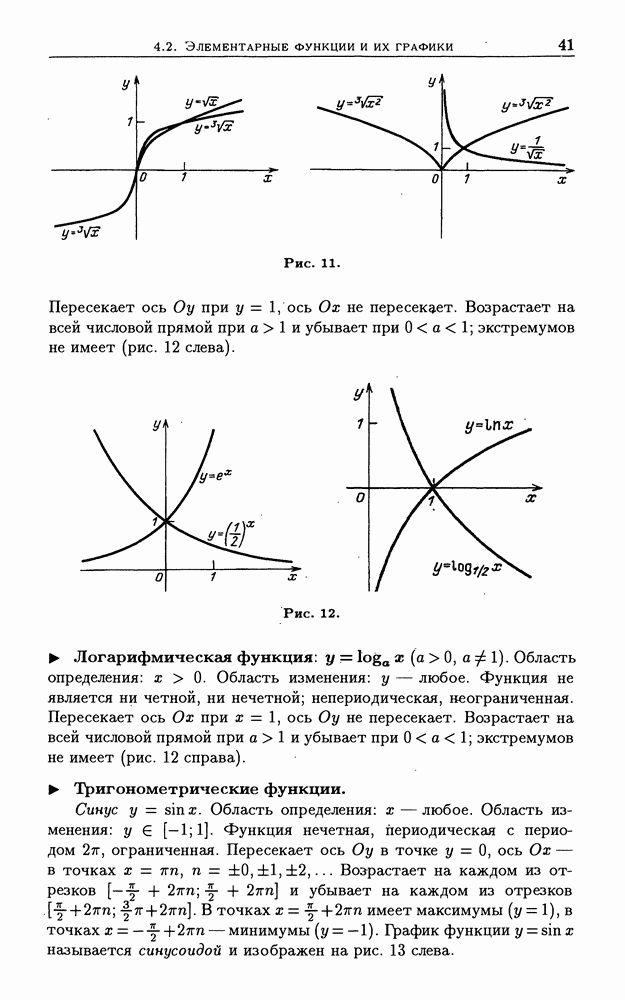
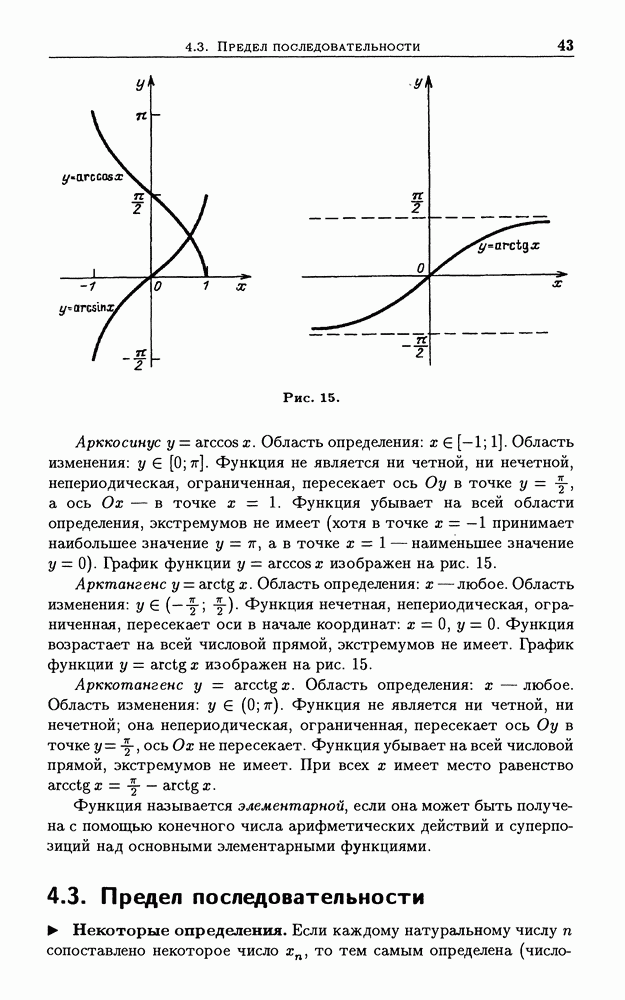
- 4.2. Элементарные функции и их графики
- 4.3. Предел последовательности
- 4.4. Предел функции
- 4.5. Бесконечно малые и бесконечно большие функции
- 4.6. Непрерывность
- 4.7. Асимптоты графика функции
- 5. Дифференциальное исчисление функций одной переменной
- 5.2. Таблица производных и правила дифференцирования
- 5.3. Теоремы о дифференцируемых функциях. Правило Лопиталя
- 5.4. Производные и дифференциалы высших порядков. Формула Тейлора
- 5.5. Экстремумы. Точки перегиба
- 5.6. Общая схема исследования функции и построение графика
- 6. Функции нескольких переменных
- 6.1. Точечные множества. Функции. Предел и непрерывность
- 6.2. Дифференцирование функций нескольких переменных
- 6.3. Производная по направлению. Геометрические приложения
- 6.4. Экстремумы функций нескольких переменных
- 7. Неопределенный интеграл
- 7.1. Первообразная. Неопределенный интеграл и его свойства
- 7.2. Таблица основных интегралов. Примеры интегрирования
- 7.3. Интегрирование по частям. Метод замены переменной
- 7.4. Интегрирование рациональных функций
- 7.5. Интегрирование иррациональных функций
- 7.6. Интегрирование показательных и тригонометрических функций
- 8. Определенный интеграл
- 8.1. Основные определения. Геометрический смысл определенного интеграла
- 8.2. Свойства определенного интеграла
- 8.3. Геометрические и физические приложения определенного интеграла
- 8.4. Несобственные интегралы
- 9. Двойные и тройные интегралы
- 9.1. Определение и свойства двойного интеграла
- 9.2. Вычисление двойного интеграла
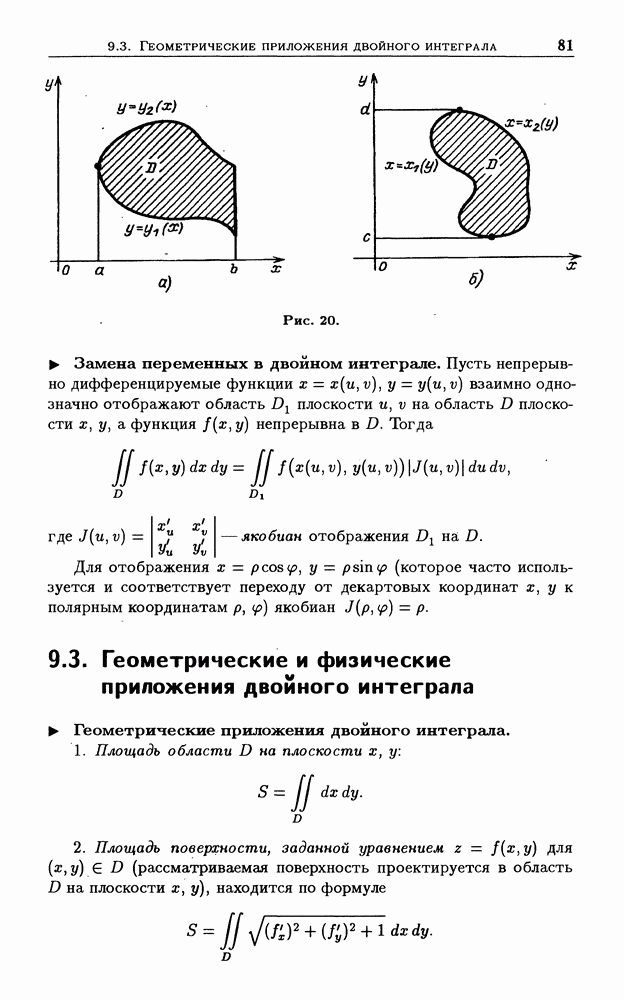
- 9.3. Геометрические и физические приложения двойного интеграла
- 9.4. Определение и свойства тройного интеграла
- 9.5. Вычисление тройного интеграла. Некоторые приложения
- 10. Криволинейные и поверхностные интегралы
- 10.2. Криволинейный интеграл второго рода
- 10.3. Поверхностный интеграл первого рода
- 10.4. Поверхностный интеграл второго рода
- 10.5. Дифференциальные операции и интегральные формулы теории поля
- 11. Ряды
- 11.1. Числовые ряды
- 11.2. Функциональные ряды
- 11.3. Степенные ряды
- 11.4. Ряд Фурье
- 11.5. Интеграл Фурье. Преобразование Фурье
- 12. Обыкновенные дифференциальные уравнения
- 12.2. Дифференциальные уравнения высших порядков
- 12.3. Линейные уравнения n-го порядка
- 12.4. Решение линейных однородных уравнений n-го порядка с постоянными коэффициентами
- 12.5. Линейные неоднородные уравнения n-го порядка
- 12.6. Системы обыкновенных дифференциальных уравнений
- 13. Приближенные вычисления
- 13.1. Метод наименьших квадратов
- 13.2. Приближенное решение алгебраических уравнений
- 13.3. Вычисление определенного интеграла
- 13.4. Численное интегрирование дифференциальных уравнений
- 14. Теория вероятностей
- 14.1. Правила и формулы комбинаторики
- 14.2. Основные понятия теории вероятностей
- 14.3. Условная вероятность. Теоремы и формулы теории вероятностей
- 14.4. Математическое ожидание и дисперсия
- 14.5. Закон больших чисел
- 1. Физические основы механики
- 1.1. Кинематика точки
- 1.2. Кинематика твердого тела
- 1.3. Динамика
- 1.4. Закон сохранения импульса
- 1.5. Закон сохранения энергии
- 1.6. Закон сохранения момента импульса
- 1.7. Задана двух тел и движение в центральном поле
- 1.8. Поле тяготения
- 1.9. Неинерциальные системы отсчета
- 1.10. Динамика твердого тела
- 1.11. Специальная теория относительности
- 2. Молекулярная физика и термодинамика
- 2.2. Первое начало термодинамики
- 2.3. Второе начало термодинамики
- 2.4. Энтропия. Свободная энергия
- 2.5. Кинетическая теория идеального газа
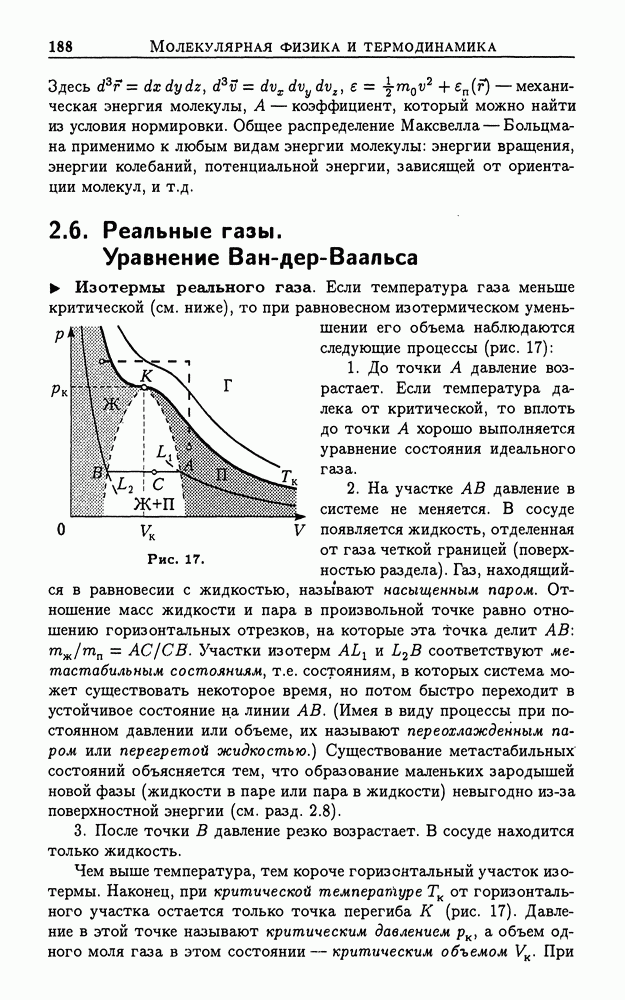
- 2.6. Реальные газы. Уравнение Ван-дер-Ваальса
- 2.7. Равновесие фаз. Фазовые переходы
- 2.8. Поверхностное натяжение
- 2.9. Явления переноса в газах
- 3. Электродинамика
- 3.1. Электрический заряд. Закон Кулона
- 3.2. Электрическое поле. Напряженность поля
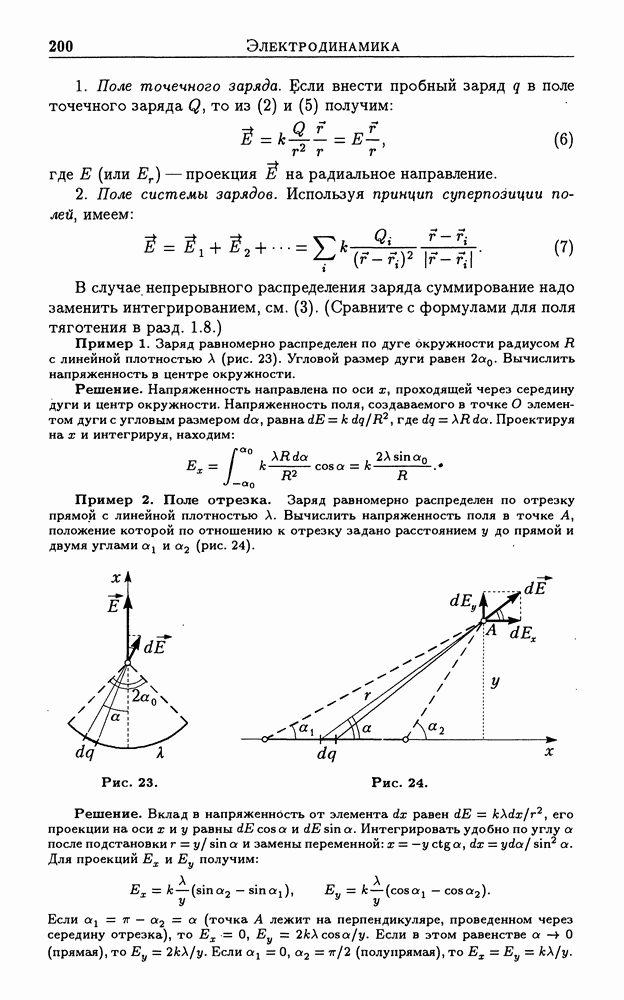
- 3.3. Электростатическое поле. Принцип суперпозиции для напряженности и потенциала
- 3.4. Теорема Гаусса
- 3.5. Электростатика проводников
- 3.6. Электростатика диэлектриков
- 3.7. Конденсаторы
- 3.8. Энергия электростатического поля
- 3.9. Постоянный ток
- 3.10. Магнитное поле. Сила Лоренца и закон Ампера
- 3.11. Вычисление магнитной индукции
- 3.12. Циркуляция и поток вектора магнитной индукции
- 3.13. Магнитное поле в веществе
- 3.14. Электромагнитная индукция
- 3.15. Уравнения Максвелла
- 4. Колебания и волны
- 4.1. Гармонические колебания. Сложение колебаний
- 4.2. Свободные незатухающие колебания
- 4.3. Затухающие и вынужденные колебания
- 4.4. Упругие волны
- 4.5. Электромагнитные волны
- 5. Оптика
- 5.1. Геометрическая оптика. Фотометрия
- 5.2. Интерференция света
- 5.3. Дифракция
- 5.4. Поляризация света. Формулы Френеля
- 5.5. Дисперсия и поглощение света
- 5.6. Тепловое излучение
- 5.7. Световые кванты
- Список литературы
- 1. Кинематика
- 1.1. Кинематика точки
- 1.2. Кинематика твердого тела
- 1.3. Плоскопараллельное движение твердого тела
- 1.4. Произвольное движение твердого тела
- 1.5. Сложное движение точки
- 2. Основные понятия и аксиомы механики
- 2.2. Аксиомы механики
- 3. Статика
- 3.2. Условия уравновешенности систем сил, приложенных к твердому телу
- 3.3. Решение задан статики
- 3.4. Центр параллельных сил. Центр тяжести твердого тела
- 3.5. Распределенные силы
- 3.6. Законы трения (законы Кулона)
- 4. Динамика материальной точки
- 4.2. Первая и вторая задачи динамики
- 5. Общие теоремы динамики механической системы
- 5.2. Теорема о движении центра масс
- 5.3. Теорема об изменении количества движения
- 5.4. Теорема об изменении кинетического момента
- 5.5. Теорема об изменении кинетической энергии
- 6. Принцип Даламбера. Элементы аналитической механики
- 6.2. Классификация механических связей. Обобщенные координаты
- 6.3. Принцип возможных перемещений
- 6.4. Общее уравнение динамики (принцип Даламбера — Лагранжа)
- 6.5. Уравнения Лагранжа второго рода
- 1. Основные понятия
- 1.1. Введение. Внешние и внутренние силы
- 1.2. Напряжения и деформации в точке
- 1.3. Основные понятия и допущения
- 2. Напряженно-деформированное состояние в точке
- 2.2. Одноосное растяжение и сжатие
- 2.3. Чистый сдвиг
- 3. Центральное растяжение и сжатие
- 3.2. Напряжения и деформации при растяжении или сжатии
- 3.3. Расчеты на прочность при растяжении и сжатии
- 4. Кручение
- 4.2. Напряжения и деформации при кручении
- 4.3. Расчеты на прочность при кручении
- 5. Прямой изгиб
- 5.2. Напряжения и деформации при прямом чистом изгибе
- 5.3. Напряжения и деформации при прямом поперечном изгибе
- 5.4. Расчет на прочность при прямом изгибе
- 6. Сложное сопротивление
- 6.2. Внецентренное растяжение или сжатие
- 6.3. Изгиб с кручением
- 7. Устойчивость сжатых стержней
- 7.2. Формула Эйлера
- 7.3. Влияние способов закрепления концов стержня на величину критической силы
- 7.4. Пределы применимости формулы Эйлера
- 7.5. Расчеты сжатых стержней на устойчивость
- ПРИЛОЖЕНИЯ
- 1. Элементарные функции и их свойства
- 2. Таблица неопределенных интегралов
- 3. Решения обыкновенных дифференциальных уравнений
- 4. Ортогональные криволинейные системы координат
- 5. Некоторые физические постоянные